DE60315542T2 - Verfahren zur Stabilisierung von vinylaromatischen Monomeren mit Verwendung von ausgewählten Polymerisierungsinhibitoren sowie daraus hergestellte Polymere - Google Patents
Verfahren zur Stabilisierung von vinylaromatischen Monomeren mit Verwendung von ausgewählten Polymerisierungsinhibitoren sowie daraus hergestellte Polymere Download PDFInfo
- Publication number
- DE60315542T2 DE60315542T2 DE60315542T DE60315542T DE60315542T2 DE 60315542 T2 DE60315542 T2 DE 60315542T2 DE 60315542 T DE60315542 T DE 60315542T DE 60315542 T DE60315542 T DE 60315542T DE 60315542 T2 DE60315542 T2 DE 60315542T2
- Authority
- DE
- Germany
- Prior art keywords
- vinyl aromatic
- tert
- monomer
- aromatic monomer
- butylcatechol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 239000000178 monomer Substances 0.000 title claims abstract description 69
- 238000000034 method Methods 0.000 title claims abstract description 48
- 238000006116 polymerization reaction Methods 0.000 title claims abstract description 43
- 239000003112 inhibitor Substances 0.000 title description 29
- 229920000642 polymer Polymers 0.000 title description 22
- 230000006641 stabilisation Effects 0.000 title description 4
- 238000011105 stabilization Methods 0.000 title description 4
- 229920002554 vinyl polymer Polymers 0.000 claims abstract description 49
- XESZUVZBAMCAEJ-UHFFFAOYSA-N 4-tert-butylcatechol Chemical compound CC(C)(C)C1=CC=C(O)C(O)=C1 XESZUVZBAMCAEJ-UHFFFAOYSA-N 0.000 claims abstract description 44
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical group C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 claims abstract description 15
- 238000004821 distillation Methods 0.000 claims description 20
- LGRLWUINFJPLSH-UHFFFAOYSA-N methanide Chemical compound [CH3-] LGRLWUINFJPLSH-UHFFFAOYSA-N 0.000 claims description 14
- 239000000463 material Substances 0.000 claims description 12
- 238000002360 preparation method Methods 0.000 claims description 8
- 230000008021 deposition Effects 0.000 claims description 4
- 238000010438 heat treatment Methods 0.000 claims description 4
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 claims description 3
- 238000004064 recycling Methods 0.000 claims 2
- 125000003011 styrenyl group Chemical group [H]\C(*)=C(/[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 claims 1
- 238000004519 manufacturing process Methods 0.000 abstract description 14
- 150000001875 compounds Chemical class 0.000 abstract description 6
- 238000003860 storage Methods 0.000 abstract description 6
- 230000003993 interaction Effects 0.000 abstract description 4
- 230000002411 adverse Effects 0.000 abstract 1
- 239000000047 product Substances 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 10
- AZQWKYJCGOJGHM-UHFFFAOYSA-N para-benzoquinone Natural products O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 10
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 8
- 229910052760 oxygen Inorganic materials 0.000 description 8
- 239000001301 oxygen Substances 0.000 description 8
- -1 vinyl aromatic compounds Chemical class 0.000 description 8
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 7
- OWZPCEFYPSAJFR-UHFFFAOYSA-N 2-(butan-2-yl)-4,6-dinitrophenol Chemical compound CCC(C)C1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1O OWZPCEFYPSAJFR-UHFFFAOYSA-N 0.000 description 5
- 125000005525 methide group Chemical group 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- HOYRZHJJAHRMLL-UHFFFAOYSA-N 2,6-dinitro-p-cresol Chemical compound CC1=CC([N+]([O-])=O)=C(O)C([N+]([O-])=O)=C1 HOYRZHJJAHRMLL-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 229910052736 halogen Inorganic materials 0.000 description 3
- 150000002367 halogens Chemical class 0.000 description 3
- 230000000379 polymerizing effect Effects 0.000 description 3
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 2
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 2
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 239000012535 impurity Substances 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 229950000688 phenothiazine Drugs 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- HEMHJVSKTPXQMS-UHFFFAOYSA-M sodium hydroxide Inorganic materials [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 2
- VETPHHXZEJAYOB-UHFFFAOYSA-N 1-n,4-n-dinaphthalen-2-ylbenzene-1,4-diamine Chemical compound C1=CC=CC2=CC(NC=3C=CC(NC=4C=C5C=CC=CC5=CC=4)=CC=3)=CC=C21 VETPHHXZEJAYOB-UHFFFAOYSA-N 0.000 description 1
- GBPNAALUHSMCQE-UHFFFAOYSA-N 3-[hydroxy(3-hydroxypropyl)amino]propan-1-ol Chemical compound OCCCN(O)CCCO GBPNAALUHSMCQE-UHFFFAOYSA-N 0.000 description 1
- ZZMVLMVFYMGSMY-UHFFFAOYSA-N 4-n-(4-methylpentan-2-yl)-1-n-phenylbenzene-1,4-diamine Chemical compound C1=CC(NC(C)CC(C)C)=CC=C1NC1=CC=CC=C1 ZZMVLMVFYMGSMY-UHFFFAOYSA-N 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- UTGQNNCQYDRXCH-UHFFFAOYSA-N N,N'-diphenyl-1,4-phenylenediamine Chemical compound C=1C=C(NC=2C=CC=CC=2)C=CC=1NC1=CC=CC=C1 UTGQNNCQYDRXCH-UHFFFAOYSA-N 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 238000005137 deposition process Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000000446 fuel Substances 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- NWVVVBRKAWDGAB-UHFFFAOYSA-N p-methoxyphenol Chemical compound COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 description 1
- 150000002989 phenols Chemical class 0.000 description 1
- 150000004986 phenylenediamines Chemical class 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 230000002028 premature Effects 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 238000007711 solidification Methods 0.000 description 1
- 230000008023 solidification Effects 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C4/00—Preparation of hydrocarbons from hydrocarbons containing a larger number of carbon atoms
- C07C4/08—Preparation of hydrocarbons from hydrocarbons containing a larger number of carbon atoms by splitting-off an aliphatic or cycloaliphatic part from the molecule
- C07C4/12—Preparation of hydrocarbons from hydrocarbons containing a larger number of carbon atoms by splitting-off an aliphatic or cycloaliphatic part from the molecule from hydrocarbons containing a six-membered aromatic ring, e.g. propyltoluene to vinyltoluene
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C7/00—Purification; Separation; Use of additives
- C07C7/20—Use of additives, e.g. for stabilisation
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F112/00—Homopolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F112/02—Monomers containing only one unsaturated aliphatic radical
- C08F112/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F112/06—Hydrocarbons
- C08F112/08—Styrene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2/00—Processes of polymerisation
- C08F2/38—Polymerisation using regulators, e.g. chain terminating agents, e.g. telomerisation
- C08F2/40—Polymerisation using regulators, e.g. chain terminating agents, e.g. telomerisation using retarding agents
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Polymers & Plastics (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Engineering & Computer Science (AREA)
- Water Supply & Treatment (AREA)
- Analytical Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Polymerisation Methods In General (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
- HINTERGRUND DER ERFINDUNG
- 1. Gebiet der Erfindung
- Die vorliegende Erfindung betrifft ein Verfahren zur Stabilisierung vinylaromatischer Monomere unter Verwendung ausgewählter Polymerisationsinhibitoren sowie daraus hergestellte Polymere. Die vorliegende Erfindung betrifft insbesondere ein Verfahren zur Stabilisierung von Styrolmonomer sowie daraus hergestellte Polystyrolpolymere.
- 2. Technischer Hintergrund
- Es ist geläufig, dass vinylaromatische Verbindungen, wie etwa monomeres Styrol, Alpha-Methylstyrol und dergleichen, gut polymerisieren und dass die Rate einer solchen Polymerisation bei steigenden Temperaturen steigt. Moderne Produktionsverfahren für diese und andere vinylaromatische Verbindungen umfassen Abscheide- und Reinigungsverfahren. Solche Abscheidung und Reinigung wird oft durch Destillation vollzogen.
- Es sind verschiedene Typen von Polymerisationsinhibitoren eingesetzt worden, um die Polymerisation während der Produktion und Lagerung vinylaromatischer Verbindungen zu verhindern. Beispielsweise offenbart das
US-Patent 4,466,904 an Watson et al., dass Inhibitoren, die zur Polymerisation vinylaromatischer Verbindungen nützlich sind, 4-tert-Butylcatechol (TBC), Phenothiazin und 2,6-Dinitro-p-cresol umfassen. Insbesondere TBC ist ein bevorzugter Polymerisationsinhibitor für Lagerungsanwendungen, da es eine gute Effizienz bei der Verhinderung vorzeitiger Polymerisation und keinen Stickstoff und/oder Halide aufweist, die besondere Sorgfalt während der Abfallentsorgung erfordern können. Solche Verwendung von Polymerisationsinhibitoren zur Verhinderung der Polymerisation vinylaromatischer Monomere wird oft als Stabilisation bezeichnet, und ein Monomer, bei dem eine wirksame Menge eines Polymerisationsinhibitors vorliegt, wird als Monomer bezeichnet, das stabilisiert wird. - Manche Polymerisationsinhibitoren funktionieren gut in Abwesenheit von Sauerstoff. 2,6-Dinitro-p-cresol funktioniert gut als Polymerisationsinhibitor in einem sauerstofffreien Verfahren. Andere tun dies nicht. Eine andere Chemikalienklasse, die als Polymerisationsinhibitoren bei der Produktion vinylaromatischer Monomere gebrauchsgeeignet ist, sind die Phenylendiamine. Gewisse Polymerisationsinhibitoren, wie etwa Phenylendiamin und TBC, erfordern die Gegenwart von Sauerstoff, um die Polymerisation vinylaromatischer Monomere zu inhibieren.
- Eine als 7-substituierte Chinonmethide beschriebene rezentere Klasse von Inhibitoren ist in dem
US-Patent 5,760,765 an Nesvadba et al., und demUS-Patent 6,024,895 an Arhancet et al. offenbart. In Nesvadba wird offenbart, dass diese Polymerisationsinhibitoren aktiver sind als früher beschriebene Methide. In Arhancet werden die 7-substituierten Chinonmethide als besonders nützlich, wenn sie in Kombination mit N,N- bis (Hydroxypropyl)hydroxylamin verwendet werden, offenbart. - Die Verwendung solcher Polymerisationsinhibitoren im allgemeinen und von TBC insbesondere ist nicht ohne Probleme. Beispielsweise muss für viele Anwendungen TBC vor der Polymerisation vinylaromatischer Monomere entfernt werden. Ein Verfahren zum Entfernen von TBC aus vinylaromatischen Monomeren ist Filtrieren durch Aluminiumoxid. Ein anderes Verfahren des Entfernens von TBC aus vinylaromatischen Monomeren wird durchgeführt, indem die vinylaromatischen Monomere mit wässrigem Natrium- oder Kaliumhydroxid gewaschen werden.
- ZUSAMMENFASSUNG DER ERFINDUNG
- Die vorliegende Erfindung ist ein Verfahren zur Herstellung eines vinylaromatischen Monomers. Das Verfahren umfasst das Erhitzen eines Zuschlags des vinylaromatischen Monomers und eines 7-Arylchinonmethids, wobei das 7-Arylchinonmethid in einer Konzentration vorliegt, die ausreicht, um das vinylaromatische Monomer am Polymerisieren zu hindern; Abscheiden des vinylaromatischen Monomers und 7-Arylchinonmethids zur Herstellung eines vinylaromatischen Monomer-Kopfdestillats und eines Sumpfproduktmaterials; und Einbringen von 4-tert-Butylcatechol in das Destillat auf einer Konzentration, die ausreicht, um das vinylaromatische Monomer am Polymerisieren zu hindern; wobei das 4-tert-Butylcatechol so in das Destillat eingebracht wird, dass im Wesentlichen kein 4-tert-Butylcatechol in das Sumpfproduktmaterial eintritt.
- DETAILLIERTE BESCHREIBUNG DER BEVORZUGTEN AUSFÜHRUNGSFORMEN
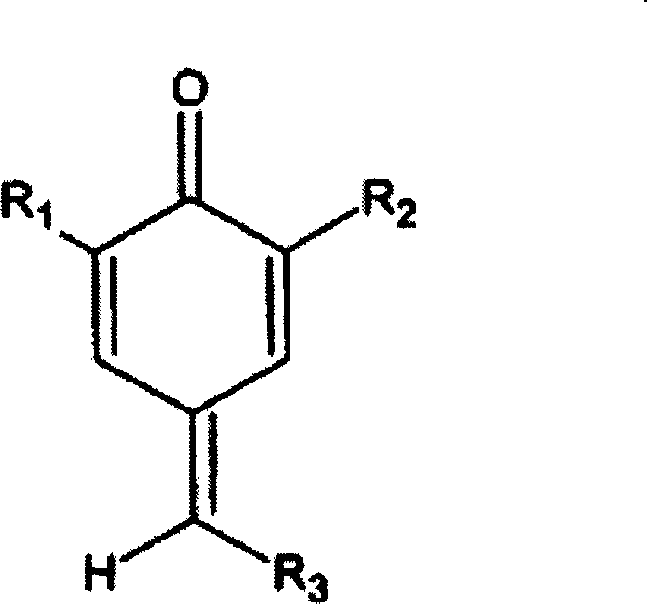
- In einem Aspekt ist die vorliegende Erfindung eine Verfahrensverbesserung in einem Verfahren zur Herstellung eines vinylaromatischen Monomers, wobei ein 7-Arylchinonmethid in dem Verfahren in einer Menge verwendet wird, die wirksam ist, um die Polymerisierung vinylaromatischer Monomere zu inhibieren. Für die Zwecke der vorliegenden Erfindung sind die 7-Arylchinonmethide als diejenigen Verbindungen definiert, welche die allgemeine Formel haben: wobei R1 und R2 unabhängig H, C4- bis C18-Alkyl; C5- bis C12-Cycloalkyl; oder C7- bis C15-Phenylalkyl sind. Bevorzugt sind R1 und R2 tert-Butyl, tert-Amyl, tert-Octyl, Cyclohexyl, α-Methylbenzyl der α,α-Dimethylbenzyl. R3 ist bevorzugt Aryl, oder mit C1- bis C6-Alkyl, Alkoxy, Hydroxy, Nitro, Amino, Carboxy oder Mischungen davon substituiertes Aryl. Verfahren zur Herstellung dieser Verbindungen sind in dem
US-Patent 4,032,547 zu finden. Bevorzugt ist das 7-Arylchinonmethid 2,6-Di-tert-butyl-4-benzyliden-cyclo-2,5-dienon. - Ein wichtiger Aspekt der vorliegenden Erfindung ist die Entdeckung der Tatsache, dass die zwei Polymerisationsinhibitoren, die 7-Arylchinonmethide und TBC, wenn sie in Kombination verwendet werden, die Polymerisation nicht in demselben Umfang verhindern, wie jedes es tun würde, wenn es getrennt verwendet würde. Anders gesagt, es ist ein Phänomen beobachtet worden, dass, wenn diese zwei Verbindungen zusammen verwendet werden, sie einander großenteils unfähig machen können, Polymerisation in einem vinylaromatischen Monomer zu inhibieren.
- In Verfahren zur Herstellung vinylaromatischer Monomere wird üblicherweise praktiziert, Polymerisationsinhibitoren in dem Verfahren anzuwenden, um das Monomer zu stabilisieren, wenn es produziert wird. An gewissen kritischen Stellen des Verfahrens wird ein Zwischenmaterial, das Monomer, Verunreinigungen und einen Polymerisationsinhibitor enthält, Erhitzung unterworfen, um das vergleichsweise niedrigsiedende Monomer zu destillieren, unter Produktion eines Destillats, das in erster Linie Monomer ist, und eines Sumpfproduktmaterials, das Monomer, polymerisiertes Monomer und Nebenprodukt-Verunreinigungen enthält. An diesem Punkt ist es üblich, dem Monomerdestillat TBC zuzusetzen, typischerweise an einer Stelle in der Destillationseinheit, um Polymerbildung zu verhindern.
- Eine vergleichsweise geringe Menge TBC kann eine vergleichsweise große Menge 7-Arylchinonmethid unwirksam bei der Verhinderung von Polymerisierung machen. Wenn ein Verfahren zur Produktion vinylaromatischen Monomers ein 7-Arylchinonmethid als Verfahrensinhibitor verwendet wird und TBC in diesem Verfahren einer Destillationseinheit an einer solchen Stelle zugesetzt wird, dass zugelassen wird, dass etwas von dem TBC wieder in das Verfahren eintritt und sich in dem Sumpfproduktmaterial sammelt, dann kann das Sumpfproduktmaterial beginnen, zu polymerisieren und kann seine Viskosität rasch ansteigen. Diese Sumpfproduktmaterialien werden üblicherweise entsorgt, oft durch Verbrennen. Wenn das Sumpfproduktmaterial bis zur Verfestigung an Viskosität ansteigt, oder sogar gerade bis zu dem Punkt, dass es nicht mehr leicht gepumpt oder anderweitig zur Entsorgung entfernt werden kann, dann können Verfahrensunterbrechungen oder sogar Stillegungen von Einheiten auftreten. Die Kosten für ein unerwartetes Stillegen einer Produktionsanlage aufgrund eines derartigen Problems kann leicht 1.000.000,00 $ an Reinigungskosten und Produktionsverlust überschreiten.
- In der Technik der Produktion vinylaromatischer Monomere wäre es wünschenswert, teure Stillegungen aufgrund unerwünschter Wechselwirkungen zwischen 7-Arylchinonmethiden und TBC zu vermeiden. Daher ist in einem Aspekt die vorliegende Erfindung eine Verfahrensverbesserung in einem Verfahren zur Herstellung eines vinylaromatischen Monomers, wobei ein 7-Arylchinonmethid in dem Verfahren in einer Menge verwendet wird, die wirksam ist, um erhitztes vinylaromatisches Monomer am Polymerisieren zu hindern, und TBC einem vinylaromatischen Monomerdestillat in einer Menge zugesetzt wird, die wirksam ist, um Polymerisation des vinylaromatischen Monomerdestillats zu verhindern, wobei die Verbesserung das Verhindern des Eintretens von TBC in das Verfahren an gleich welchem Punkt umfasst, an dem das vinylaromatische Monomer durch das 7-Arylchinonmethid stabilisiert wird. Es ist anzumerken, dass die Erhitzungsschritte und die Destillationsschritte des Verfahrens der vorliegenden Erfindung in dem gleichen oder verschiedenen Teilen des Verfahrens stattfinden können.
- In einer Ausführungsform der vorliegenden Erfindung, wo das Verfahren zur Herstellung eines vinylaromatischen Monomers eine Destillationskolonne umfasst, würde TBC dem vinylaromatischen Monomerdestillat nicht zugesetzt werden, bis das vinylaromatische Monomerdestillat die Destillationskolonne verlassen hätte. Ein Vorteil dieser Ausführungsform ist, dass TBC im Wesentlichen vom Rest des Verfahrens ausgeschlossen werden kann, jedoch könnte ein Hinauszögern des Zusetzens des TBC bis an diesem Punkt in dem Verfahren zu übermäßiger Polymerbildung führen.
- In einer anderen Ausführungsform der vorliegenden Erfindung, wo das Verfahren zur Herstellung eines vinylaromatischen Monomers eine Destillationskolonne umfasst, wird TBC innerhalb der Kolonne, jedoch in Produktflussrichtung einem getrennten Rückführsystem nachgeschaltet zugesetzt, was im Wesentlichen das gesamte TBC am Erreichen des Destillationssumpfs hindern würde. Ein Vorteil dieser Ausführungsform wäre niedrigere Polymerproduktion, da das Monomer weniger Zeit unvermischt mit einem Polymerisationsinhibitor verbringen würde. Ein Nachteil für ein solches System wären höhere Investierungskosten.
- In einem Verfahren der vorliegenden Erfindung, wobei TBC so in ein vinylaromatisches Destillat eingebracht wird, dass im Wesentlichen kein TBC in den Destillationssumpf eintritt, beträgt die TBC-Konzentration in dem Destillationssumpf weniger als 10 ppm, bevorzugt weniger als 5 ppm, und höchstbevorzugt weniger als 1 ppm. Jedes Verfahren, das den Fachleuten in der Technik der Herstellung vinylaromatischer Monomere zum Zusetzen einer wirksamen Menge TBC zu einem aromatischen Monomerdestillat vor der Bildung unerwünschter Mengen von Polymer, jedoch auch ohne dazu zu führen, dass TBC in den Destillationssumpf eintritt, als gebrauchsgeeignet bekannt ist, kann bei dem Verfahren der vorliegenden Erfindung verwendet werden.
- Jegliches Verfahren, das gebrauchsgeeignet ist, um TBC aus einem vinylaromatischen Monomer zu entfernen, das den Fachleuten in der Technik der Herstellung solcher vinylaromatischer Monomere bekannt ist, kann bei der vorliegenden Erfindung angewendet werden. Beispielsweise kann Waschen mit einer wässrigen Base angewendet werden, wie auch Filtrieren durch Aluminiumoxid.
- Ein anderes Verfahren, das verwendet werden kann, um das Stillegen einer Produktionsanlage für vinylaromatisches Monomer aufgrund einer unerwünschten Wechselwirkung von TBC und einem 7-Arylchinonmethid zu vermeiden, wäre die Verwendung mindestens eines zusätzlichen Polymerisationsinhibitors in dem Verfahren in einer solchen Konzentration, dass der zusätzliche Inhibitor in dem Destillationssumpf in einer Menge vorhanden wäre, die ausreichen würde, um die rasche Polymerisation von Sumpfproduktmaterialien zu verhindern. Eine solche Lösung würde den raschen Ansteig der Sumpfproduktviskosität und Polymerbildung in Monomer verhindern, die eine Stillegung verursachen würden, würde jedoch auch den Verzicht auf mindestens einige der Nutzen der Verwendung eines 7-Arylchinonmethids allein erfordern.
- Die Abwesenheit oder das geringe Vorkommen von Heteroatomen, wie etwa Stickstoff und Halogenen, in den bevorzugten 7-Arylchinonmethiden könnte aus einer Perspektive der Entsorgung der Sumpfproduktmaterialien wünschenswert sein. Insbesondere, wenn das gewünschte Entsorgungsverfahren Verbrennen für Kraftstoff ist, können die Notwendigkeit des Reduzierens der Abfuhr von Verbindungen wie etwa NOx und dergleichen die Kosten solcher Entsorgungspraktiken stark erhöhen. Die Verwendung gering stickstoff- und halogenhaltiger oder stickstoff- und halogenfreier Polymerisationsinhibitoren verringert oder eliminiert diese Kosten.
- Zusätzliche Polymerisationsinhibitoren, die bei dem Verfahren der vorliegenden Erfindung verwendet werden können, umfassen: Phenothiazin, 2,6-Dinitro-p-cresol, 2-sec-Butyl-4,6-dinitrophenol und andere Phenole und Polyhydroxyaromaten, wie etwa Hydrochinon und Hydrochinonmonomethylether; aromatische Amine wie etwa N,N'-Di-2-naphthyl-p-phenylendiamin, N-Phenyl-N'-(1,3-dimethylbutyl)-p-phenylendiamin und N,N'-Diphenyl-p-phenylendiamin. Auch gebrauchsgeeignet sind N-Oxyl-Verbindungen, wie etwa die in dem
US-Patent 6,348,598 offenbarten. Jegliche Zusammensetzung, die als Polymerisationsinhibitor zur Verwendung bei vinylaromatischen Monomeren geeignet ist, außer wie hier anderweitig angedeutet, kann bei dem Verfahren der vorliegenden Erfindung verwendet werden. - Es ist beabsichtigt, dass die vorliegende Erfindung bei der Produktion und Lagerung gleich welcher vinylaromatischer Monomere angewendet werden kann. Beispiele solcher Monomere sind monomeres Styrol und Alpha-Methylstyrol. Die vorliegende Erfindung richtet sich speziell auf Styrolproduktion und -lagerung.
- BEISPIELE
- Die folgenden Beispiele werden zur Veranschaulichung der vorliegenden Erfindung angeführt. Es ist nicht beabsichtigt, dass die Beispiele die Reichweite der vorliegenden Erfindung einschränken, und sie sollten nicht so interpretiert werden. Mengenangaben sind in Gewichtsteilen oder Gewichtsprozentsätzen, wenn nicht anders angegeben.
- Beispiel 1
- Ein Kolbentest der Wirksamkeit von 2,6-Di-tert-butyl-4-benzyliden-cyclo-2,5-dienon wird durch Zumischen von 100 ppm pro Gewicht von 2,6-Di-tert-butyl-4-benzyliden cyclo-2,5-dienon mit Styrolmonomer auf einer Temperatur von etwa 122°C in Abwesenheit von Sauerstoff durchgeführt. Nach 90 Minuten wird eine Probe des Styrolmonomers unter Verwendung von Methanolausfällung auf den Polymergehalt getestet. Es wird ermittelt, dass der Polymergehalt 2,5 Prozent beträgt.
- Beispiel 2
- Beispiel 1 wird wiederholt und im Wesentlichen identisch getestet, außer dass der Zuschlag von 2,6-Di-tert-butyl-4-benzyliden-cyclo-2,5-dienon und Styrolmonomer zusätzlich 15 ppm 4-tert-Butylcatechol enthält. Es wird ermittelt, dass der Polymergehalt 10 Prozent beträgt.
- Beispiel 3
- Beispiel 1 wird wiederholt und im Wesentlichen identisch getestet, außer dass dem Monomer zusätzlich 100 ppm Phenylendiamin zugesetzt werden. Es ist anzumerken, dass das Fehlen von Sauerstoff verhindert, dass das Phenylendiamin als Polymerisationsinhibitor wirkt. Es wird ermittelt, dass der Polymergehalt 2 Prozent beträgt.
- Beispiel 4
- Ein Kolbentest wird unter Verwendung eines Styrolmonomers durchgeführt, das 15 ppm 4-tert-Butylcatechol enthält, dem 100 ppm Phenylendiamin und 100 ppm 2-sec-Butyl-4,6-dinitrophenol beigemischt sind. Der Monomerzuschlag wird in Abwesenheit von Sauerstoff 2 Stunden lang auf 122°C erhitzt. Eine Probe des Zuschlags wird genommen und auf den Polymergehalt geprüft. Es ist anzumerken, dass das Fehlen von Sauerstoff verhindert, dass das Phenylendiamin als Polymerisationsinhibitor wirkt. Es wird ermittelt, dass der Polymergehalt etwa 2 Prozent beträgt.
- Beispiel 5
- Ein Kolbentest wird durchgeführt und im Wesentlichen identisch zu Beispiel 4 getestet, außer dass 2,6-Di-tert-butyl-4-benzyliden-cyclo-2,5-dienon anstelle von 2-sec-Butyl-4,6-dinitrophenol verwendet wird. Es wird ermittelt, dass der Polymergehalt etwa 6 Prozent beträgt.
- Beispiel 6
- Ein Kolbentest wird durchgeführt und im Wesentlichen identisch zu Beispiel 4 getestet, außer dass kein Polymerisationsinhibitor verwendet wird. Es wird ermittelt, dass der Polymergehalt etwa 13 Prozent beträgt.
- Beispiel 1 zeigt den Umfang der Polymerbildung in einem 2,6-Di-tert-butyl-4-benzyliden-cyclo-2,5-dienoninhibierten Monomer. Beispiel 2 zeigt, dass der Zusatz von 4-tert-Butylcatechol zu demselben Monomer die Polymerbildung erhöht. Beispiel 3 zeigt, dass der Zusatz von Phenylendiamin zu einem 2,6-Di-tert-butyl-4-benzyliden-cyclo-2,5-dienon-inhibierten Monomer keinen Anstieg der Polymerbildung verursacht, selbst in Abwesenheit von Sauerstoff, der von dem Phenylendiamin benötigt wird, um als Polymerisationsinhibitor zu wirken. Beispiel 4 zeigt, dass die Wirkung des Zusetzens von sowohl 4-tert-Butylcatechol als auch Phenyldiamin, die beide Sauerstoff benötigen, um als Polymerisationsinhibitoren zu wirken, zu 2-sec-Butyl-4,6-dinitrophenol die Polymerbildung nicht erhöht. Beispiel 5 zeigt, dass Wiederholung von Beispiel 4, wobei 2,6-Di-tert-butyl-4-benzyliden-cyclo-2,5-dienon anstelle von 2-sec-Butyl-4,6-dinitrophenol verwendet wird, zu erhöhter Polymerbildung führt. Beispiel 6 zeigt den Umfang der Polymerbildung in einem nicht inhibierten System.
Claims (9)
- Verfahren zur Herstellung eines vinylaromatischen Monomers, ausgewählt unter Styrol und Alpha-Methylstyrol, umfassend: Erhitzen einer Beimischung des vinylaromatischen Monomers und eines 7-Arylchinonmethids, wobei das 7-Arylchinonmethid auf einer Konzentration vorliegt, die ausreicht, um das vinylaromatische Monomer am Polymerisieren zu hindern; Abscheiden des vinylaromatischen Monomers und 7-Arylchinonmethids zur Herstellung eines vinylaromatischen Monomer-Kopfdestillats und eines Sumpfproduktmaterials; und Einbringen von 4-tert-Butylcatechol in das Destillat auf einer Konzentration, die ausreicht, um das vinylaromatische Monomer am Polymerisieren zu hindern; wobei das 4-tert-Butylcatechol so in das Destillat eingebracht wird, dass kein 4-tert-Butylcatechol in das Sumpfprodukt eintritt.
- Verfahren von Anspruch 1, wobei das vinylaromatische Monomer Styrol ist.
- Verfahren von Anspruch 2, wobei das 7-Arylchinonmethid 2,6-di-tert-Butyl-4-benzylidencyclohexy-2,5-dienon ist.
- Verfahren von Anspruch 3, wobei die Abscheidung durch Destillation durchgeführt wird, unter Verwendung einer Destillationskolonne, die das Styrolmonomerdestillat und ein Destillationssumpfprodukt produziert.
- Verfahren von Anspruch 4, wobei das 4-tert-Butylcatechol an einem Punkt in das vinylaromatische Monomerdestillat eingebracht wird, nachdem das vinylaromatische Monomerdestillat die Destillationskolonne verlassen hat.
- Verfahren von Anspruch 4, wobei die Destillationskolonne ein Kolonnenrückführsystem aufweist, das das gesamte, zu dem Destillationskolonnensumpfprodukt rückgeführte Material sammelt.
- Verfahren von Anspruch 6, wobei das 4-tert-Butylcatechol an einem Punkt stromabwärts von dem Kolonnenrückführsystem in das vinylaromatische Monomerdestillat eingebracht wird.
- Verfahren von Anspruch 4, wobei das Destillationssumpfprodukt einen 4-tert-Butylcatecholgehalt von weniger als 10 ppm hat.
- Verfahren von Anspruch 4, wobei das Destillationssumpfprodukt einen 4-tert-Butylcatecholgehalt von weniger als 1 ppm hat.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/139,524 US6960279B2 (en) | 2002-05-06 | 2002-05-06 | Method for stabilizing vinyl aromatic monomers using selected polymerization inhibitors and polymers prepared therewith |
| US139524 | 2002-05-06 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| DE60315542D1 DE60315542D1 (de) | 2007-09-27 |
| DE60315542T2 true DE60315542T2 (de) | 2008-05-15 |
Family
ID=29269562
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60328839T Expired - Fee Related DE60328839D1 (de) | 2002-05-06 | 2003-04-22 | Verfahren zur Stabilisierung von vinylaromatischen Monomeren mit Verwendung von ausgewählten Polymerisierungsinhibitoren sowie daraus hergestellte Polymere |
| DE60315542T Expired - Fee Related DE60315542T2 (de) | 2002-05-06 | 2003-04-22 | Verfahren zur Stabilisierung von vinylaromatischen Monomeren mit Verwendung von ausgewählten Polymerisierungsinhibitoren sowie daraus hergestellte Polymere |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DE60328839T Expired - Fee Related DE60328839D1 (de) | 2002-05-06 | 2003-04-22 | Verfahren zur Stabilisierung von vinylaromatischen Monomeren mit Verwendung von ausgewählten Polymerisierungsinhibitoren sowie daraus hergestellte Polymere |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US6960279B2 (de) |
| EP (2) | EP1837322B1 (de) |
| JP (2) | JP4418641B2 (de) |
| KR (1) | KR20030086928A (de) |
| CN (2) | CN1326816C (de) |
| AT (2) | ATE439384T1 (de) |
| CA (1) | CA2423209A1 (de) |
| DE (2) | DE60328839D1 (de) |
| ES (2) | ES2330799T3 (de) |
| TW (2) | TW200710101A (de) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102007052891A1 (de) | 2007-11-02 | 2009-05-07 | Evonik Degussa Gmbh | Verfahren zur Stabilisierung von olefinisch ungesättigten Monomeren |
| US8187346B2 (en) * | 2008-12-29 | 2012-05-29 | Fina Technology, Inc. | Stabilization of pygas for storage |
| US7651635B1 (en) * | 2009-02-05 | 2010-01-26 | Nalco Company | Polymer inhibition of vinyl aromatic monomers using a quinone methide/alkyl hydroxylamine combination |
| US8298440B2 (en) * | 2010-06-03 | 2012-10-30 | General Electric Company | Methods and compositions for inhibiting vinyl aromatic monomer polymerization |
| JP5833652B2 (ja) * | 2010-08-02 | 2015-12-16 | ダウ グローバル テクノロジーズ エルエルシー | ビニルアリールモノマーの重合抑制組成物及び抑制方法 |
| US9090526B2 (en) * | 2011-06-13 | 2015-07-28 | Nalco Company | Synergistic combination for inhibiting polymerization of vinyl monomers |
| FR2979348B1 (fr) * | 2011-08-25 | 2013-08-09 | Rhodia Operations | Procede de preparation d'une composition inhibitrice comprenant un compose a base d'au moins deux solides inhibiteurs de polymerisation |
| KR101812624B1 (ko) * | 2011-08-26 | 2017-12-27 | 도르프 케탈 케미칼즈 (인디아) 프라이비트 리미티드 | 스타이렌의 중합화의 제어 및 억제를 위한 첨가제 조성물, 및 그의 제조와 사용 방법 |
| US9206268B2 (en) * | 2011-09-16 | 2015-12-08 | General Electric Company | Methods and compositions for inhibiting polystyrene formation during styrene production |
| US8901362B2 (en) * | 2012-02-02 | 2014-12-02 | General Electric Company | Methods and compositions for styrene inhibition via in situ generation of quinone methides |
| DE102013204950A1 (de) | 2013-03-20 | 2014-09-25 | Evonik Industries Ag | Verfahren und Zusammensetzung zur Inhibierung der Polymerisation von Cyclopentadienverbindungen |
| US11180578B2 (en) | 2018-07-13 | 2021-11-23 | Ecolab Usa Inc. | Polymerization inhibitor and retarder compositions with amine stabilizer |
| TWI826485B (zh) | 2018-07-13 | 2023-12-21 | 美商藝康美國公司 | 作為乙烯系單體之防垢劑之含氧胺及醌甲基化物之組合物 |
| JP7247630B2 (ja) * | 2019-02-13 | 2023-03-29 | 栗田工業株式会社 | 不飽和芳香族単量体の重合を抑制する方法 |
| CN114163290B (zh) * | 2021-12-06 | 2024-02-27 | 万华化学集团股份有限公司 | 一种碱洗塔黄油抑制剂及其制备方法 |
| CN116553996A (zh) * | 2023-07-07 | 2023-08-08 | 吉林金海化工新材料有限公司 | 一种阻聚剂及其应用 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4003800A (en) * | 1976-01-02 | 1977-01-18 | Gulf Research & Development Company | Styrene purification process |
| US4032547A (en) | 1976-02-23 | 1977-06-28 | Gulf Research & Development Company | Quinone alkide synthesis system |
| US4434307A (en) * | 1982-12-27 | 1984-02-28 | Atlantic Richfield Company | Inhibiting polymerization of vinyl aromatic monomers |
| US4466904A (en) | 1983-01-10 | 1984-08-21 | Cosden Technology, Inc. | Polymerization co-inhibitors for vinyl aromatic compounds |
| US4616774A (en) * | 1984-03-01 | 1986-10-14 | Plus Corporation | Stapler |
| US5254760A (en) * | 1992-07-29 | 1993-10-19 | Ciba-Geigy Corporation | Inhibiting polymerization of vinyl aromatic monomers |
| SG49028A1 (en) * | 1994-01-25 | 1998-05-18 | Sumitomo Chemical Co | A method fo inhibiting polymerization of vinyl compound and polymerization inhibitor used therein |
| US5583247A (en) | 1995-04-14 | 1996-12-10 | Ciba-Geigy Corporation | 7-substituted quinone methides as inhibitors for unsaturated monomers |
| US5616774A (en) | 1995-04-14 | 1997-04-01 | Ciba-Geigy Corporation | Inhibition of unsaturated monomers with 7-aryl quinone methides |
| DE19882797T1 (de) | 1997-11-12 | 2001-02-22 | Mitsubishi Rayon Co | N-Oxyl-Verbindungen, Verfahren zu ihrer Herstellung und Methode zur Inhibierung der Polymerisation von Vinyl-Monomeren durch Verwendung von N-Oxyl-Verbindungen |
| US6024894A (en) | 1998-03-25 | 2000-02-15 | Betzdearborn Inc. | Compositions and methods for inhibiting vinyl aromatic monomer polymerization |
| US6685823B2 (en) * | 2000-10-16 | 2004-02-03 | Uniroyal Chemical Company, Inc. | C-nitrosoaniline compounds and their blends as polymerization inhibitors |
| KR100812038B1 (ko) * | 2000-10-16 | 2008-03-10 | 유니로얄 캐미칼 캄파니, 인크. | 중합 억제제로서 퀴논 알키드와 니트록실 화합물의 블렌드물 |
| US20040034247A1 (en) * | 2002-08-16 | 2004-02-19 | Sherif Eldin | Compositions and methods for inhibiting vinyl aromatic monomer polymerization |
-
2002
- 2002-05-06 US US10/139,524 patent/US6960279B2/en not_active Expired - Fee Related
-
2003
- 2003-03-18 TW TW095143757A patent/TW200710101A/zh unknown
- 2003-03-18 TW TW092105927A patent/TWI278338B/zh not_active IP Right Cessation
- 2003-03-24 CA CA002423209A patent/CA2423209A1/en not_active Abandoned
- 2003-04-22 EP EP07112448A patent/EP1837322B1/de not_active Revoked
- 2003-04-22 AT AT07112448T patent/ATE439384T1/de not_active IP Right Cessation
- 2003-04-22 AT AT03076188T patent/ATE370110T1/de not_active IP Right Cessation
- 2003-04-22 DE DE60328839T patent/DE60328839D1/de not_active Expired - Fee Related
- 2003-04-22 EP EP03076188A patent/EP1362838B1/de not_active Expired - Lifetime
- 2003-04-22 ES ES07112448T patent/ES2330799T3/es not_active Expired - Lifetime
- 2003-04-22 ES ES03076188T patent/ES2291589T3/es not_active Expired - Lifetime
- 2003-04-22 DE DE60315542T patent/DE60315542T2/de not_active Expired - Fee Related
- 2003-04-28 JP JP2003123487A patent/JP4418641B2/ja not_active Expired - Fee Related
- 2003-04-29 CN CNB031241557A patent/CN1326816C/zh not_active Expired - Fee Related
- 2003-04-29 CN CNA200710106321XA patent/CN101054335A/zh active Pending
- 2003-05-02 KR KR10-2003-0028326A patent/KR20030086928A/ko not_active Ceased
-
2005
- 2005-08-29 US US11/214,109 patent/US20060020089A1/en not_active Abandoned
-
2009
- 2009-10-19 JP JP2009240496A patent/JP2010013483A/ja not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| ATE439384T1 (de) | 2009-08-15 |
| ES2330799T3 (es) | 2009-12-15 |
| EP1362838A2 (de) | 2003-11-19 |
| EP1837322B1 (de) | 2009-08-12 |
| JP2003321401A (ja) | 2003-11-11 |
| TWI278338B (en) | 2007-04-11 |
| CN101054335A (zh) | 2007-10-17 |
| TW200402318A (en) | 2004-02-16 |
| TW200710101A (en) | 2007-03-16 |
| ES2291589T3 (es) | 2008-03-01 |
| KR20030086928A (ko) | 2003-11-12 |
| DE60328839D1 (de) | 2009-09-24 |
| US20030205452A1 (en) | 2003-11-06 |
| JP4418641B2 (ja) | 2010-02-17 |
| US6960279B2 (en) | 2005-11-01 |
| CN1326816C (zh) | 2007-07-18 |
| EP1837322A3 (de) | 2008-04-30 |
| DE60315542D1 (de) | 2007-09-27 |
| JP2010013483A (ja) | 2010-01-21 |
| CN1456542A (zh) | 2003-11-19 |
| ATE370110T1 (de) | 2007-09-15 |
| EP1837322A2 (de) | 2007-09-26 |
| CA2423209A1 (en) | 2003-11-06 |
| US20060020089A1 (en) | 2006-01-26 |
| EP1362838B1 (de) | 2007-08-15 |
| EP1362838A3 (de) | 2004-03-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DE60315542T2 (de) | Verfahren zur Stabilisierung von vinylaromatischen Monomeren mit Verwendung von ausgewählten Polymerisierungsinhibitoren sowie daraus hergestellte Polymere | |
| DE3879550T2 (de) | Stabilisierte vinylaromatische Zusammensetzung. | |
| DE2804449C2 (de) | Verfahren zum Inhibieren der Polymerisation einer leicht polymerisierbaren aromatischen Vinylverbindung | |
| DE69933558T2 (de) | Zusammensetzung und verfahren zur vermeidung der polymerisation von aromatischen vinylpolymeren | |
| DE60116894T2 (de) | C-nitrosoanilinverbindungen und deren mischungen als polymerisationsinhibitoren | |
| DE69617962T2 (de) | Methoden zur verhinderung der polymerisation von aromatischen vinylmonomeren | |
| DE19820200A1 (de) | Bimetallkomplex-Katalysatorsystem, Verfahren zu dessen Herstellung sowie Verwendung des Katalysatorsystems zur Hydrierung von ungesättigten Kopolymeren | |
| DE69710163T2 (de) | Hemmung der Polymerisation von vinylaromatischen Monomeren | |
| DE69507253T2 (de) | Verfahren zur Herstellung von 4'-Bromomethyl-2-cyanobiphenyl | |
| DE69724432T2 (de) | Polymerisationsinhibitor | |
| DE2149670A1 (de) | Verfahren zur Gewinnung von Acrylnitril | |
| DE2540328C2 (de) | Verfahren zur Reinigung von Reaktoren für die Polymerisation und die Mischpolymerisation von Vinylchlorid | |
| DE1595046A1 (de) | Verfahren zur Herstellung von Polyarylenaethern | |
| DE60125067T2 (de) | Verhinderung des popcorn-effekts während des polymerwachstums | |
| EP0072575A1 (de) | N,N'-Diphenyl-p-phenylendiamine, Verfahren zu ihrer Herstellung und ihre Verwendung als Stabilisatoren für organische Materialien | |
| DE69605923T2 (de) | Behandlungen zur inhibierung der polymerisation von vinylaromatischen monomeren | |
| DE69314549T2 (de) | Kompressor-Verstoffungsschutz in Vinylacetat-Produktionseinheiten | |
| DE2539430C2 (de) | Verfahren zum Abstoppen der Polymerisation von Vinylchlorid in wäßriger Emulsion oder Suspension | |
| DE1951879C3 (de) | Verfahren zum Herstellen niedermolekularer, wachsartiger Polyäthylene | |
| DE69702247T2 (de) | Zusammensetzung zur inhibierung der polymerisierung | |
| DE2410248C3 (de) | Stabilisierung eines aromatischen Chlorkohlenwasserstoffs | |
| DE1545098C3 (de) | Verfahren zur Polymerisation von Äthylen | |
| EP0652196A1 (de) | Verfahren zur Herstellung von hochchlorierten Parraffinen | |
| EP0133504A2 (de) | Verfahren zur Reinigung von Methacrylamidopropyltrimethylammoniumchlorid und verwandten Verbindungen | |
| AT203716B (de) | Verfahren zur vorzugsweise kontinuierlichen Herstellung von Polyäthylen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 8364 | No opposition during term of opposition | ||
| 8339 | Ceased/non-payment of the annual fee |