-
Die
vorliegende Erfindung betrifft Verbesserungen an härtbaren
Zusammensetzungen, bei denen die Härtung durch Vernetzung von
Polyisocyanaten, gefolgt von einer Wärmezersetzung eines blockierten
Polyisocyanats, bewirkt wird. Insbesondere richtet sich die Erfindung
auf die Verwendung von gemischt-blockierten Polyisocyanaten, die
wärmeaktive
Blockierungsgruppen und 1,3-Dicarbonyl-Blockierungsgruppen enthalten. Härtbare Beschichtungszusammensetzungen,
die auf solchen gemischtblockierten Polyisocyanaten basieren, weisen
eine gute Kratzfestigkeit auf und bieten eine gute Zwischenschichthaftung,
wie weiter unten erläutert werden
wird.
-
Bei
bestimmten gemischt-blockierten Polyisocyanate kann ein gewisser
Grad an Inkompatibilität
mit anderen Inhaltsstoffen vorliegen, die häufig in härtbaren Beschichtungszusammensetzungen
verwendet werden, doch kann dies durch Verwendung Hybid-blockierter
Polyisocyanate vermieden werden. Bei letzteren, die einen speziellen
Aspekt der vorliegenden Erfindung darstellen, tragen einzelne Polyisocyanat-Moleküle wenigstens
eine wärmeaktive
Blockierungsgruppe und wenigstens eine 1,3-Dicarbonyl-Blockierungsgruppe.
-
Die
vorliegende Erfindung betrifft daher die Verwendung gemischt-blockierter
Polyisocyanate in einer härtbaren
Zusammensetzung, um der gehärteten
Zusammensetzung Kratzfestigkeit und gute Zwischenschichthaftung,
wenn eine weitere Überzugsschicht
aufgebracht wird, zu verleihen.
-
Die
vorliegende Erfindung betrifft außerdem neuartige Hybrid-blockierte
Polyisocyanate, Verfahren zur Herstellung derselben, Zusammensetzungen,
die diese enthal ten, und Verfahren zur Ablagerung der Beschichtungszusammensetzungen
auf einem Substrat, als auch deren Verwendung in härtbaren
Zusammensetzungen.
-
Blockierte
Polyisocyanate werden herkömmlicherweise
in Zusammensetzungen verwendet, die außerdem aktiven Wasserstoff
enthaltene Verbindungen, z.B. Amine und Alkohole, enthalten. Diese
Zusammensetzungen können,
zum Beispiel bei Ablagerung auf einem zu beschichtenden Gegenstand,
durch Erhitzung gehärtet
werden, was oftmals als Ofentrocknung bezeichnet wird. Während der
Ofentrocknung zerfallen die blockierten Polyisocyanate, sodass die
Isocyanatgruppen zur Reaktion mit den aktiven Wasserstoff enthaltenden
Verbindungen verfügbar
werden, was zur Vernetzung und Härtung
der Beschichtung führt.
-
Im
Fachgebiet ist die Blockierung von Polyisocyanaten mit einer Vielfalt
von Blockierungsmitteln, wie etwa Phenolen und auch Pyrazolen wie
3,5-Dimethylpyrazol (DMP), bekannt. Das Blockierungsmittel soll
die Isocyanatgruppen am Reagieren mit Verbindungen hindern, die
aktive Wasserstoffatome enthalten (z.B. Härter oder Härtungsmittel), außer bei
Erhitzung. Es ist daher möglich,
blockierte Isocyanate bei Raumtemperatur mit aktiven Wasserstoffverbindungen
zu mischen und die Gemische zu behandeln und für einen bestimmten Zeitraum
zu lagern. Um eine vollständige
Härtung
zu bewirken, werden die Gemische auf eine Temperatur erhitzt, bei
der die blockierten Polyisocyanate mit den aktiven Wasserstoffverbindungen
reagieren. Viele Arten von Verbindungen sind bereits als geeignete
Reaktionspartner beschrieben worden, einschließlich Polyalkoholen, Polyaminen,
Polythiolen, Polycarboxylsäuren,
Tri- oder Diamiden, Urethanen oder Wasser.
-
Die
Verwendung von Malonatestern als Blockierungsmitteln ist bekannt.
Es wird allgemein vorausgesetzt, dass Malonatester-blockierte Polyisocyanate
durch eine Transveresterungsreaktion vernetzen und so die fertig
gestellten gehärteten
Zusammensetzungen bilden. Dies steht im Gegensatz zur Freisetzung
der wiederhergestellten Blockierungsmittel, die beim Entblockieren
der Polyisocyanate, die wärmeaktive
Blockierungsgruppen tragen, auftritt. Allerdings zeigen mit solchen
Estern blockierte Isocyanate oftmals Inkompatibilitäten bei
Mischung mit Polyolen, indem diese Gemische häufig einer Gelbildung bei Raumtemperatur
oder etwa 23°C
unterliegen. Dies ist ungünstig,
da Polyole häufig
in blockierte Polyisocyanate enthaltenden Zusammensetzungen, gewöhnlich als
Härter,
vorhanden sind. Es wird angenommen, dass die Inkompatibilität mit Polyolen
auf eine gewisse Transveresterung zurückzuführen ist, die bei Raumtemperatur
stattfindet und eine Phasentrennung oder teilweise Härtung bewirkt.
Obschon das Mischen der blockierten Isocyanate mit einem Hydroxyfunktionellen
Lösungsmittel,
wie etwa einem monofunktionellen Alkohol, die Inkompatibilität vermindern
kann, kann es diese nicht vollständig
beseitigen.
-
Malonester-blockierte
Polyisocyanate können
auch an Stabilitätsproblemen
leiden, die zum Beispiel zu einer Verfestigung führen können. Wird zum Beispiel Hexamethylendiisocyanatisocyanurat
(HDI-Trimer) mit Diethylmalonat blockiert, so neigt das blockierte
Isocyanat zur Kristallisation oder Verfestigung. Im Gegensatz dazu
bleibt ein stabil blockiertes Isocyanat flüssig (bei 23°C).
-
Überraschenderweise
ist festgestellt worden, dass dann, wenn ein Polyisocyanat mit einer
1,3-Dicarbonyl-Verbindung teilweise blockiert wird, ausgewählt aus
Diethylmalonat, Dimethylmalonat, Meldrumsäure und Ethylacetoacetat, und
außerdem
mit einem wärmeaktiven
Blockierungsmittel blockiert wird, welches eine Pyrazol-basierte
Verbindung ist, die Inkompatibilitäten, die Polyisocyanate, die
lediglich mit einem Malonester blockiert sind, zeigen, ausgeschaltet
werden.
-
Ein
Vorteil der vorliegenden Erfindung liegt in der Tatsache, dass diese
Hybridblockierten Polyisocyanate Moleküle enthalten, von denen jedes
mit mindestens einer 1,3-Dicarbonyl-Verbindung und mit mindestens
einer wärmeaktiven
Blockierungsgruppe blockiert ist. [Oftmals werden sie außerdem Moleküle enthalten, die
lediglich mit einer der Blockierungsgruppen blockiert sind, und
andere Moleküle,
die lediglich mit einer anderen der Blockierungsgruppen blockiert
sind.] Auf diese Weise verfestigt sich ein physikalisches Gemisch
aus (i) einem vollständig
DMP-blockierten HDI-Trimer mit (ii) einem vollständig Diethylmalonat (DEM)-blockierten HDI-Trimer
bei 23°C,
wohingegen das äquivalente
Hybrid-blockierte Polyisocyanat klar und als einer einzelnen Phase
verbleibt.
-
Blockierte
Polyisocyanate werden oftmals zur Bildung von Überzugsschichten verwendet,
zum Beispiel bei Spulenbeschichtungen, Pulverbeschichtungen und
in der Automobilindustrie, wo sie besonders nützlich zur Herstellung von
Klarschichten als der Endbeschichtung sind und daher so formuliert
sind, dass sie einen guten Schutz gegen Stoffe aus der Umwelt bieten.
-
Diese
Klarschichten sind typischerweise einer Kratzerbildung während der
Lebensdauer des Vehikels ausgesetzt. Kratzer sind ästhetisch
unerwünscht
und können
zur Korrosion des Substrats führen,
wenn dieses durch den Kratzer oder durch eine nach und nach erfolgende
Entfernung der unteren Beschichtungslagen in der Folge eines Kratzers
in der äußersten
Schicht freigelegt wird. Daher besteht eine Aufgabe der vorliegenden Erfindung
in der Bereitstellung von Beschichtungen, die eine gute Kratzfestigkeit
aufweisen.
-
Bei
OEM-Beschichtungen für
Automobile beispielsweise bestehen die Schichten, die typischerweise die
Beschichtung ausmachen, aus einer Grundierung, dann einer Grundfarbschicht
und schließlich
der Klarschicht. Diese werden in dieser Reihenfolge auf das Substrat
aufgebracht.
-
Liegt
ein Makel in der Beschichtung oder in einer der Unterschichten vor,
wie etwa der Grundfarbschicht oder der Grundierung, der während der
grundlegenden Beschichtungsverfahren in der Fabrik oder später erfolgen
kann, zum Beispiel durch Kratzen, so werden weitere Überzugsschichten
aufgebracht. Dies führt zur
Aufbringung zum Beispiel einer Grundfarbschicht über die bestehende ausgehärtete Klarschicht,
die aus dem blockierten Polyisocyanat hergestellt ist. Aufgrund
der gehärteten
Beschaffenheit der Klarschicht ist die Haftung einer weiteren Beschichtung
erschwert, was zu weiteren Defekten führt. Diese schlechte Haftung
zwischen der zuvorigen Oberfläche
und der neuen Überschichtung
ist im Industriezweig als Fehlen von Zwischenschichthaftung bekannt.
-
Insbesondere
DMP ist als ein Blockierungsmittel in Polyisocyanat-basierten Produkten,
wie etwa Automobil-Klarschichten, breit eingesetzt worden, wo seine
Kombination aus Stabilität
und leichter Entblockierung, seine Festigkeit gegenüber Gelbfär bung beim Überbrennen
und seine Säureätzfestigkeit
in dieser sehr anspruchsvollen Rolle sehr geschätzt worden sind. Allerdings
wäre ein
höherer
Grad an Kratzfestigkeit insbesondere für die Automobilindustrie von
Vorteil. In ähnlicher
Weise ist eine verbesserte Zwischenschichthaftung, insbesondere
dort, wo wahrscheinlich eine Reparatur erforderlich sein wird, eine
Zielsetzung in Verbindung mit Pyrazol-blockierten Polyisocyanat-Beschichtungszusammensetzungen.
-
Überraschenderweise
ist festgestellt worden, dass dann, wenn ein gemischtblockiertes
Polyisocyanat, das 1,3-Dicarbonyl-Blockierungsgruppen enthält, die
von Diethylmalonat, Dimethylmalonat, Meldrumsäure und/oder Ethylacetoacetat
abgeleitet sind, und wärmeaktive
Pyrazol-Blockierungsgruppen zum Erhalt einer Beschichtung, wie etwa
einer Klarschicht, verwendet werden, die Kratzfestigkeit der Beschichtung
verbessert ist. Außerdem
ist die Zwischenschichthaftung einer später aufgebrachten Beschichtung,
wie etwa einer Grundfarbschicht, im Vergleich zur Zwischenschichthaftung
an beispielsweise eine Beschichtung, die aus einem DMP-blockierten
Polyisocyanat hergestellt ist, stark verbessert. In der Tat kann
die Zwischenschichthaftung ebenso hoch sein wie bei der ursprünglichen
Aufbringung der Klarschicht auf die Grundfarbschicht. Dies wird erreicht,
ohne dabei die Stabilitätsprobleme
in Verbindung mit Malonatester-Blockierungsmitteln zu bewirken.
-
Demgemäß stellt
die vorliegende Erfindung die Verwendung eines gemischtblockierten
Polyisocyanatprodukts in einer härtbaren
Zusammensetzung bereit, wobei das gemischt-blockierte Polyisocyanatprodukt durch
Blockieren eines oder mehrerer Polyisocyanate mit wenigstens einem
1,3-Dicarbonyl-Blockierungsmittel, ausgewählt aus Diethylmalonat, Dimethylmalonat,
Meldrumsäure
und Ethylacetoacetat, und wenigstens einem wärmeaktiven Blockierungsmittel,
ausgewählt
aus Pyrazolen, wobei das molare Verhältnis von 1,3-Dicarbonyl-Blockierungsgruppen
zu wärmeaktiven
Blockierungsgruppen in dem gemischt-blockierten Polyisocyanat im
Bereich von 4:1 bis 1:99 liegt, erhältlich ist. Das gemischt-blockierte
Polyisocyanat kann irgendein blockiertes Polyisocyanat sein, das
das erforderliche Gemisch an Blockierungsgruppen aufweist. Die härtbare Zusammensetzung
ist als eine Beschichtungszusammensetzung geeignet. Das gemischt-blockierte
Polyisocyanatprodukt kann in fester oder flüssiger Form (bezeichnet als „100% Feststoffe" im Fachgebiet) in
Abhängigkeit von der
Natur der Komponenten des gemischt-blockierten Polyisocyanats, oder
in Form einer Dispersion in Wasser oder eines Flüssigträgers oder einer Lösung in
einem organischen Lösungsmittel
oder Wasser, vorliegen.
-
Bei
einer Ausführungsform
ist das gemischt-blockierte Polyisocyanatprodukt ein Hybrid-blockiertes Polyisocyanatprodukt,
worin zumindest ein Anteil der Moleküle sowohl mit einer 1,3-Dicarbonyl-Blockierungsgruppe,
die von Diethylmalonat, Dimethylmalonat, Meldrumsäure oder
Ethylacetoacetat abgeleitet ist, als auch einer wärmeaktiven
Blockierungsgruppe, die von einem Pyrazol abgeleitet ist, so blockiert
ist, dass das molare Verhältnis
von 1,3-Dicarbonyl-Blockierungsgruppen zu wärmeaktiven Blockierungsgruppen
im Hybrid-blockierten Polyisocyanatprodukt im Bereich von 4:1 bis
1:99 liegt.
-
Das
Hybrid-blockierte Polyisocyanatprodukt weist eine gemischte Population
von vollständig
blockierten Polyisocyanat-Molekülen
auf. Typischerweise sind einige Moleküle vollständig mit einem der Blockierungsmittel
(z.B. dem wärmeaktiven
Blockierungsmittel) blockiert und andere Moleküle mit einem anderen Blockierungsmittel
(z.B. einem 1,3-Dicarbonyl-Blockierungsmittel) blockiert. Allgemein
ist die Verwendung solcher Mengen mindestens zweier Blockierungsmittel
bevorzugt, dass etwa 10 mol-% oder mehr der Polyisocyanat-Moleküle durch
mindestens eine 1,3-Dicarbonyl-Blockierungsgruppe
und durch mindestens eine wärmeaktive
Blockierungsgruppe blockiert sind, vorzugsweise mindestens 20%,
zum Beispiel mindestens 30%, 40%, 50%, 60% oder 70%.
-
In
einer weiteren Ausführungsform
ist das gemischt-blockierte Polyisocyanatprodukt ein Gemisch, das ein
Polyisocyanat, das mit mindestens einer 1,3-Dicarbonyl-Blockierungsgruppe,
abgeleitet von Diethylmalonat, Dimethylmalonat, Meldrumsäure und/oder
Ethylacetoacetat, blockiert ist, und dasselbe oder ein unterschiedliches
Polyisocyanat umfasst, das mit mindestens einer wärmeaktiven
Blockierungsgruppe, abgeleitet von einem Pyrazol, blockiert ist,
wobei das molare Verhältnis
der 1,3-Dicarbonyl-Blockierungsgruppen
zu den wärmeaktiven
Blockierungsgruppen im blockierten Polyisocyanatprodukt-Gemisch
im Bereich von 4:1 bis 1:99 liegt. Das ge mischt-blockierte Polyisocyanat
kann mehr als ein Polyisocyanat enthalten, das mit beiden Arten von
Blockierungsgruppe blockiert ist.
-
Bei
einer anderen Ausführungsform
ist das gemischt-blockierte Polyisocyanatprodukt ein Gemisch aus
zwei oder mehreren blockierten Polyisocyanaten, von denen eines
oder mehrere ein Hybrid-blockiertes Polyisocyanat sind, wobei das
Gemisch ein molare Verhältnis
von 1,3-Dicarbonyl-Blockierungsgruppen zu wärmeaktiven Blockierungsgruppen
im Bereich von 4:1 bis 1:99 ist. Die Hybrid-blockierten Polyisocyanate können jeweils
unabhängig
ein molares Verhältnis
von Blockierungsgruppen aufweisen, das außerhalb dieses Bereichs fällt, solange
das Gemisch ein molares Verhältnis
von 1,3-Dicarbonyl-Blockierungsgruppen zu wärmeaktiven Blockierungsgruppen
von 4:1 bis 1:99 aufweist.
-
Bei
einer besonderen Ausführungsform
ist das gemischt-blockierte Polyisocyanatprodukt ein Gemisch, umfassend
(a) ein Hybrid-blockiertes Polyisocyanat und wenigstens eines von
(b) einem Polyisocyanat, das mit wenigstens einer 1,3-Dicarbonylgruppe,
abgeleitet von Diethylmalonat, Dimethylmalonat, Meldrumsäure und/oder
Ethylacetoacetat, blockiert ist, und (c) einem Polyisocyanat, das
mit wenigstens einer wärmeaktiven
Gruppe, abgeleitet von einem Pyrazol, blockiert ist, wobei wobei
das molare Verhältnis
der 1,3-Dicarbonyl-Blockierungsgruppen zu den wärmeaktiven Blockierungsgruppen
im Gemisch im Bereich von 4:1 bis 1:99 liegt. Das Hybridblockierte
Polyisocyanat weist wahlweise ein molares Verhältnis der 1,3-Dicarbonyl-Blockierungsgruppen
zu den wärmeaktiven
Blockierungsgruppen im Bereich von 4:1 bis 1:99 auf. Allerdings
kann ein Hybrid-blockiertes Polyisocyanat mit einem molaren Verhältnis der
1,3-Dicarbonyl-Blockierungsgruppen zu den wärmeaktiven Blockierungsgruppen
außerhalb
des Bereichs von 4:1 bis 1:99 verwendet werden, solange das gemischt-blockierte
Polyisocyanatprodukt ein molares Verhältnis der 1,3-Dicarbonyl-Blockierungsgruppen zu
den wärmeaktiven
Blockierungsgruppen im Bereich von 4:1 bis 1:99 aufweist.
-
Das
Polyisocyanat kann jegliches organische Polyisocyanat sein, das
für vernetzende
Verbindungen, die aktiven Wasserstoff enthalten, z.B. aliphatische
oder cycloaliphatische, aromatische, heterocyclische und gemischt
aliphatisch-aromatische Polyi socyanate, die 2, 3 oder mehr Isocyanatgruppen
enthalten, von denen viele im Fachgebiet wohl bekannt sind, geeignet
ist. Eine Substitution des Polyisocyanats z.B. durch Alkoxygruppen
ist möglich.
-
Die
Polyisocyanat-Verbindung kann zum Beispiel, ohne darauf beschränkt zu sein,
Ethylendiisocyanat, Propylendiisocyanat, Tetramethylendiisocyanat,
Hexamethylendiisocyanat (HDI), Decamethylendiisocyanat, Dodecamethylendiisocyanat,
2,4,4-Trimethylhexamethylen-1,6-diisocyanat,
Phenylendiisocyanat, 2,4-Diisocyanatotoluol, 2,6-Diisocyanatotoluol,
Naphthylendiisocyanat, Dianisidindiisocyanat, 4,4'-Methylen-bis(phenylisocyanat), 2,4'-Methylen-bis(phenylisocyanat),
4,4'-Ethylenbis(phenylisocyanat), ω,ω'-Diisocyanato-1,3-dimethylbenzol,
Cyclohexandi-iso-cyanat, ω,ω'-Diisocyanato-1,4-dimethylcyclohexan, ω,ω'-Diisocyanato-1,4-dimethylbenzol, ω,ω'-Diisocyanato-1,3-dimethylcyclohexan,
1-Methyl-2,4-diisocyanatocyclohexan, 4,4'-Methylen-bis(cyclohexylisocyanat),
3-Isocyanatomethyl-3,5,5-trimethylcyclohexylisocyanat (Isophorondiisocyanat,
IPDI), Dimersäure-Diisocyanat, ω,ω'-Diisocyanatodiethylbenzol, ω,ω'-Diisocyanatodimethyltoluol, ω,ω'-Diisocyanatodiethyltoluol,
Fumarsäure-bis(2-isocyanatoethyl)ester
bis Triphenylmethantrüsocyanat, 1,4-Bis-(2-isocyanato-prop-2yl)benzol,
1,3-Bis-(2-isocyanat-prop-2-yl)benzol sein. Bei einer Ausführungsform der
Erfindung ist das Polyisocyanat vorzugsweise frei von Isocyanatgruppen,
die direkt an die aromatischen Kerne gebunden sind. Bei einer anderen
Ausführungsform
kann das Polyisocyanat Isocyanat-gruppen enthalten, die direkt an
aromatische Kerne geknüpft
sind.
-
Das
Polyisocyanat kann auch ein Polyisocyanat sein, das durch Reaktion
einer Überschussmenge des
Isocyanats mit a) Wasser, b) einem niedermolekularen Polyol (z.B.
MG ≤ 300)
oder c) einem Polyol mit mittleren Molekulargewicht, z.B. ein Polyol
mit einem MG von größer 300
oder kleiner 8000, z.B. Sucrose, oder durch die Reaktion des Isocyanats
mit sich selbst zum Erhalt eines Isocyanurats erhalten wird.
-
Das
niedermolekulare Polyol umfasst zum Beispiel Ethylenglykol, Propylenglykol,
1,3-Butylenglykol, Neopentylglykol, 2,2,4-Trimethyl-1,3-pentandiol,
Hexamethylenglykol, Cyclohexandimethanol, hydriertes Eisphenol-A,
Trimethylolpropan, Trimethylolethan, 1,2,6-Hexantriol, Glycerin,
Sorbitol oder Pentaerythritol.
-
Das
durch die obige Reaktion erhaltene Polyisocyanat kann eine Biuret-Struktur
aufweisen oder eine Allophanatgruppe enthalten.
-
Ebenfalls
nützlich
für die
Erfindung sind die Trimere von Di- oder höheren Polyisocyanaten, d.h.
Materialien, die eine Isocyanuratgruppe enthalten.
-
Zu
bevorzugten Polyisocyanaten zählen
HDI-Timer, HDI-Biuret und IPDI-Trimer.
-
Polyisocyanat-Vorpolymere,
die durchschnittlich mehr als eine Isocyanatgruppe pro Molekül enthalten,
sind ebenfalls zur Verwendung bei der vorliegenden Erfindung geeignet.
Die Vorpolymere werden durch Vorreagieren einer molaren Überschussmenge
eines der oben benannten Polyisocyanate mit einem organischen Material
erhalten, das mindestens zwei aktive Wasserstoffatome pro Molekül enthält, zum
Beispiel in Form von Hydroxylgruppen, wie bei Polyalkylenglykolen.
-
Die
1,3-Dicarbonyl-Blockierungsgruppe ist von einer 1,3-Dicarbonyl-Verbindung
abgeleitet, welches eine Verbindung ist, die eine in Formel (I)
gezeigte Komponente enthält
worin die Gruppe Z Wasserstoff,
Methyl oder Ethyl ist.
-
Wie
hierin verwendet, wird eine 1,3-Dicarbonyl-Verbindung ausgewählt aus
Diethylmalonat, Dimethylmalonat, Meldrumsäure und Ethylacetoacetat, wobei
Diethylmalonat am bevorzugtesten ist.
-
Die
wärmeaktive
Blockierungsgruppe ist jegliche Gruppe, die ein blockiertes Polyisocyanat
bereitstellt, welches bei Raumtemperatur, wie etwa 20 bis 25°C, zum Beispiel etwa
23°C, stabil
bleibt, doch die bei Erhitzung, zum Beispiel bei Erhitzung auf eine
Temperatur oberhalb von 80°C,
vorzugsweise bis zu etwa 130°C, zum
Beispiel bis zu 120, 115 oder 110°C,
unter praktikablen Bedingungen entblockiert, wie etwa bei Beschichtungszusammensetzungen
in Anwesenheit einer aktiven Wasserstoffverbindung. Die Entblockierungstemperatur
kann auch unter experimentellen Bedingungen in Abwesenheit der aktiven
Wasserstoffverbindungen mittels IR-spektroskopischer Techniken bestimmt
werden, und beträgt
unter solchen Bedingungen geeigneterweise mehr als 60°C, zum Beispiel
mehr als 70 oder 80°C,
und kann bis zu 110°C,
bevorzugter bis zu 105 oder 100°C
betragen. Folglich wird eine wärmeaktive
Blockierungsgruppe Isocyanate bei Erhitzung freisetzen, selbst wenn
kein Härtungsmittel
vorhanden ist.
-
Die
wärmeaktive
Blockierungsgruppe ist von einem wärmeaktiven Mittel abgeleitet,
ausgewählt
aus Pyrazolen wie 3,5-Dimethylpyrazol, 3,5-Diethylpyrazol, 3-Methylpyrazol,
Pyrazol and 3-iso-Butyl-5-terf-butylpyrazol, 3-iso-Butyl-5-methylpyrazol
und 3,5-Di-terf-butylpyrazol.
-
Zur
Vermeidung eines Missverständnisses
sollte zur Kenntnis genommen werden, dass der Begriff „wärmeaktive
Blockierungsgruppe",
wie hierin verwendet, keine Gruppen umfassen soll, die bei Erhitzung,
um die Entblockierung zu bewirken, eine Restgruppe in Bindung an
die Isocyanatgruppe zurücklassen.
Blockierungsgruppen, die aktive Methylengruppen umfassen, wie etwa
die Acetoacetonate (z.B. Ethylacetoacetonat) werden daher nicht
als „wärmeaktive
Blockierungsgruppen" betrachtet
und sind davon ausgeschlossen.
-
Die
Pyrazole können
gewählt
werden aus den Pyrazolen der Formel (II)
worin n 0, 1, 2 oder 3 ist,
die Gruppen R
1 jeweils gerad- oder verzweigtkettiges
Alkyl, Alkenyl, Aralkyl, N-substituiertes Carbamyl, Phenyl sind
oder
worin R
2 eine
C
1-C
4-Alkylgruppe
ist und dann, wenn n 2 oder 3 ist, die Gruppen R
1 gleich
oder verschieden sein können.
Vorzugsweise ist n = 2.
-
Vorzugsweise
ist die Pyrazolgruppe in den 3- und 5-Positionen substituiert. Bevorzugter
sind beide R1-Gruppen Alkylgruppen mit 1
bis 6 Kohlenstoffatomen, wie etwa Methyl oder Ethyl, oder ist mindestens
ein R1 eine verzweigte Alkylgruppe mit 3
bis 6 Kohlenstoffatomen.
-
Zu
geeigneten verzweigten Alkylgruppen zählen Isopropyl, Isobutyl, sec-Butyl
und tert-Butyl. Besonders bevorzugte verzweigte Alkylpyrazole sind
3-Methyl-5-iso-propylpyrazol,
3-iso-Butyl-5-methylpyrazol, 3-sec-Butyl-5-methylpyrazol, 3-tert-Butyl-5-methylpyrazol,
3-Ethyl-5-iso-propylpyrazol, 3-iso-Butyl-5-ethylpyrazol, 3-sec-Butyl-5-ethylpyrazol, 3-tert-Butyl-5-ethylpyrazol,
3-iso-Propyl-5-n-propylpyrazol, 3-iso-Butyl-5-n-propylpyrazol, 3-sec-Butyl-5-n-propylpyrazol,
3-tert-Butyl-5-n-propylpyrazol, 3-n-Butyl-5-iso-propylpyrazol, 3-iso-Butyl-5-n-butylpyrazol,
3-n-Butyl-5-sec-butylpyrazol, 3-n-Butyl-5-tert-butylpyrazol, 3,5-Di-iso-propylpyrazol,
3-iso-Butyl-5-iso-propylpyrazol, 3-sec-Butyl-5-iso-propylpyrazol,
3-tert-Butyl-5-iso-propylpyrazol, 3,5-Di-iso-butylpyrazol, 3-iso-Butyl-5-sec-butylpyrazol,
3-iso-Butyl-5-tert-butylpyrazol, 3,5-Di-sec-butylpyrazol, 3-sec-Butyl-5-terf-butylpyrazol
und 3,5-Di-terf-butylpyrazol.
-
Substituierte
Pyrazole, einschließlich
verzweigter Alkylpyrazole, können
mittels herkömmlicher
Methoden unter Einbeziehung der Bildung eines Diketons aus einem
Methylketon und eines Esters und Umsetzen des Diketons mit Hydrazin
erzeugt werden. Etwa 1 mol der Base ist erforderlich, um die Reaktion
zwischen 1 mol des Methylketons und 1 mol des Esters zu bewirken.
Dies ist nachstehend ausführlicher
beschrieben.
-
Bei
einer bevorzugten Ausführungsform
ist das wärmeaktive
Agenz eine Pyrazol-Verbindung,
bevorzugter 3,5-Dimethylpyrazol oder 3,5-Di-tert-butylpyrazol, und
am bevorzugtesten 3,5-Dimethylpyrazol Bei einer Ausführungsform
ist das wärmeaktive
Agenz ein verzweigtes Alkylpyrazol. Von diesen ist 3,5-Di-tert-butylpyrazol
aufgrund seiner besonders niedrigen Entblokkierungstemperatur besonders
bevorzugt, ebenso wie für seine
Stabilität
und Fähigkeit,
die Entblockierungstemperaturen bei Verwendung in einem gemischtblockierten Polyisocyanat
allgemein zu senken.
-
Bei
einer Ausführungsform
der vorliegenden Erfindung weist das gemischt-blockierte Polyisocyanat eine
1,3-Dicarbonyl-Blockierungsgruppe auf, die von Diethylmalonat, Dimethylmalonat,
Meldrumsäure
oder Ethylacetoacetat abgeleitet ist, und eine wärmeaktive Blockierungsgruppe,
die von einem Pyrazol abgeleitet ist. Bei einer bevorzugten Ausführungsform
der vorliegenden Erfindung ist das gemischt-blockierte Polyisocyanatprodukt
durch Blockieren eines Polyisocyanats mit Diethylmalonat oder Dimethylmalonat
und 3,5-Dimethylpyrazol oder 3,5-Di-tert-butylpyrazol erhältlich.
Bei einer besonders bevorzugten Ausführungsform ist das gemischt-blockierte
Polyisocyanatprodukt durch Blockieren mit zumindest Dimethylmalonat
und 3,5-Dimethylpyrazol erhältlich.
Bei einer besonders bevorzugten Ausführungsform ist das gemischt-blockierte
Polyisocyanat durch Blockieren lediglich mit Ethylmalonat und 3,5-Dimethylpyrazol erhältlich.
-
Das
molare Verhältnis
von 1,3-Dicarbonyl-Blockierungsgruppen zu wärmeaktiven Blockierungsgruppen
im gemischt-blockierten Polyisocyanat beträgt von 4:1 bis 1:99, vorzugsweise
4:1 bis 2:98, bevorzugt 3:1 bis 5:95, bevorzugter 2:1 bis 1:9, und
am bevorzugtesten 1:1. Ein besonders bevorzugtes Verhältnis für Diethylmalonat
und 3,5-Dimethylpyrazol beträgt
1:1.
-
Bei
einer bevorzugten Ausführungsform
ist das gemischt-blockierte Polyisocyanat ein Hybrid-blockiertes
Polyisocyanat, das durch Blockieren mit Diethylmalonat oder Dimethylmalonat
und 3,5-Dimethylpyrazol oder 3,5-Di-tert-butylpyrazol erhältlich ist.
-
Bei
einer anderen bevorzugten Ausführungsform
ist das gemischt-blockierte Polyisocyanat ein Gemisch aus einem
blockierten Polyisocyanat, das durch Blockieren mit Diethylmalonat
oder Dimethylmalonat erhältlich
ist, und einem blockierten Polyiso cyanat, das durch Blockieren mit
3,5-Dimethylpyrazol oder 3,5-Di-tert-butylpyrazol erhältlich ist.
Bevorzugter enthält
das Gemisch ein Diethylmalonat-blockiertes Polyisocyanat und ein
3,5-Dimethylpyrazol-blockiertes Polyisocyanat.
-
Ein
Hybrid-blockiertes Polyisocyanat wird typischerweise mittels eines
Verfahrens hergestellt, welches das Umsetzen einer oder mehrerer
Polyisocyanate mit wenigstens einer 1,3-Dicarbonyl-Verbindung und
wenigstens einem wärmeaktiven
Mittel umfasst. Dies ist nachstehend ausführlich beschrieben.
-
Für die Herstellung
von Gemischen werden zwei oder mehrere blockierte Polyisocyanate
miteinander vermengt. Polyisocyanate, die mit Gruppen blockiert
sind, die von einer 1,3-Dicarbonyl-Verbindung abgeleitet sind, oder
mit Gruppen blockiert sind, die von einer wärmeaktiven Verbindung abgeleitet
sind, können
mittels im Fachgebiet bekannter Methoden erzeugt werden.
-
Ein
Gemisch aus Polyisocyanaten wird allgemein durch Mischen des/r blockierten
Polyisocyanats/e und/oder Hybrid-blockierten Polyisocyanate erhalten.
Das Mischen wird fortgesetzt, bis ein homogenes Gemisch erhalten
ist.
-
Typischerweise
werden das Polyisocyanat und das Blockierungsmittel erhitzt, damit
die Blockierungsreaktion stattfinden kann. Das Reaktionsgemisch
wird auf eine geeignete Temperatur für den Ablauf der Reaktion erhitzt.
Allgemein wird das Reaktionsgemisch auf über 50°C, vorzugsweise über 60°C erhitzt.
Wo allerdings geeignet, kann die anfängliche Erhitzung des Reaktionsgemischs
bei einer niedrigeren Temperatur erfolgen. So wird beispielsweise
HDI-Trimer mit 3,5-Dimethylpyrazol reagieren, wenn anfänglich auf
30 bis 40°C erhitzt.
Nach dem Einleiten der Reaktion kann eine Abkühlung erforderlich sein, um
das Exotherm zu kontrollieren, das beispielsweise durch Pyrazol-Blockierungsmittel
erzeugt wird.
-
Die
vorliegende Erfindung stellt auch ein Verfahren zum Überziehen
einer gehärteten
Beschichtung, die aus einer Zusammensetzung hergestellt ist, umfassend
ein gemischt-blockiertes Polyisocyanatprodukt, das durch Blockieren
eines Polyisocyanats mit mindestens einem 1,3-Dicarbonyl-Blockierungsmittel,
ausgewählt
aus Diethylma lonat, Dimethylmalonat, Meldrumsäure und Ethylacetoacetat, und
mindestens einem wärmeaktiven
Blockierungsmittel, ausgewählt
aus Pyrazolen, erhalten wird, sodass das molare Verhältnis von 1,3-Dicarbonyl-Blockierungsgruppen
zu wärmeaktiven
Blockierungsgruppen im gemischt-blockierten Polyisocyanat im Bereich
von 4:1 bis 1:99 liegt, und eine aktiven Wasserstoff enthaltende
Verbindung, welches Verfahren das Aufbringen einer weiteren Schicht über die
gehärtete
Beschichtung und das Härten
umfasst. Dieses Verfahren kann zum Beispiel zur Reparatur eines
Gegenstands, der während
der Verwendung beschädigt
worden ist, oder eines Defekts, der während des anfänglichen
Herstellungsverfahrens eines beschichteten Gegenstands festgestellt
worden ist, angewendet werden. Bei einer besonderen Ausführungsform
ist die weitere Schicht eine Grundfarbschicht. Das Verfahren kann
außerdem
das Aufbringen einer oder mehrerer zusätzlicher Beschichtungen, wie
etwa einer Klarschicht, die ein gemischt-blockiertes Polyisocyanat
umfasst, beinhalten.
-
Die
vorliegende Erfindung stellt auch eine Beschichtungszusammensetzung
bereit, umfassend eine aktiven Wasserstoff enthaltende Verbindung
und ein gemischtblockiertes Polyisocyanatprodukt, das durch Blockieren
eines Polyisocyanats mit mindestens einem 1,3-Dicarbonyl-Blockierungsmittel,
ausgewählt
aus Diethylmalonat, Dimethylmalonat, Meldrumsäure und Ethylacetoacetat, und
mindestens einem wärmeaktiven Blockierungsmittel,
ausgewählt
aus Pyrazolen, sodass das molare Verhältnis von 1,3-Dicarbonyl-Blockierungsgruppen
zu wärmeaktiven
Blockierungsgruppen im gemischt-blockierten Polyisocyanat von 4:1
bis 1:99 beträgt,
erhalten wird. Bei einer Ausführungsform
wird das gemischt-blockierte Polyisocyanatprodukt mit Pyrazolen
als dem/n wärmeaktiven
Blockierungsmittel(n) blockiert, sodass mindestens 70% der Blockierungsgruppen
von Pyrazolen abgeleitet sind. Bei einer weiteren Ausführungsform
weist das gemischt-blockierte Polyisocyanatprodukt 1 bis 20%, bevorzugt
1 bis 10% an Blockierungsgruppen auf, die 1,3-Dicarbonyl-Blockierungsgruppen,
vorzugsweise Diethylmalonat, sind.
-
Die
vorliegende Erfindung stellt ein industrielles Verfahren bereit,
welches umfasst:
- i) Beschichten von Gegenständen mit
einer Endbeschichtung aus einer Zusammensetzung, umfassend ein gemischt-blockiertes
Polyisocyanatprodukt, das durch Blockieren eines Polyisocyanats
mit wenigstens einem 1,3-Dicarbonyl- Blockierungsmittel, ausgewählt aus
Diethylmalonat, Dimethylmalonat, Meldrumsäure und Ethylacetoacetat, und
wenigstens einem wärmeaktiven
Blockierungsmittel, ausgewählt
aus Pyrazolen, wobei das molare Verhältnis von 1,3-Dicarbonyl-Blockierungsgruppen
zu wärmeaktiven
Blockierungsgruppen in dem gemischtblockierten Polyisocyanat im
Bereich von 4:1 bis 1:99 liegt, erhältlich ist, und eine Verbindung,
die aktiven Wasserstoff enthält,
- ii) Härten
der Beschichtung,
- iii) Untersuchen der Gegenstände
auf Fehler, und
- iv) teilweises oder vollständiges
Neubeschichten von fehlerhaften Gegenständen. Vorzugsweise beinhaltet der
Neubeschichtungsschritt das Beschichten mit einer oder mehreren
Schichten und dann das Überziehen mit
einer Beschichtungszusammensetzung, die eine aktiven Wasserstoff
enthaltende Verbindung und ein gemischt-blockiertes Polyisocyanatprodukt,
wie oben beschrieben, enthält,
und dann das Härten.
-
Die
vorliegende Erfindung umfasst außerdem ein Hybrid-blockiertes
Polyisocyanat mit wenigstens einer 1,3-Dicarbonyl-Blockierungsgruppe,
die von Diethylmalonat, Dimethylmalonat, Meldrumsäure oder
Ethylacetoacetat abgeleitet ist, und wenigstens einer wärmeaktiven
Blockierungsgruppe, die von einem Pyrazol abgeleitet ist, wobei
das molare Verhältnis
von 1,3-Dicarbonyl-Blockierungsgruppen zu wärmeaktiven Blockierungsgruppen
in dem Hybrid-blockierten Polyisocyanat im Bereich von 4:1 bis 1:9
liegt. Bei einer Ausführungsform
beträgt
das molare Verhältnis
von 1,3-Dicarbonyl-Blockierungsgruppen
zu wärmeaktiven
Blockierungsgruppen etwa 1:9.
-
Bei
einer besonders bevorzugten Ausführungsform
besteht das Hybrid-blockierte Polyisocyanat aus einem Polyisocyanat,
das vollständig
mit lediglich einem 1,3-Dicarbonyl-Blockierungsmittel
und mit lediglich einem wärmeaktiven
Blockierungsmittel blockiert ist.
-
Das
Hybrid-blockierte Polyisocyanat enthält eine ausreichende Menge
der wärmeaktiven
Blockierungsgruppen, um die Inkompatibilitäten zu beseitigen, die sich
gezeigt haben, wenn lediglich 1,3-Dicarbonyl-Blockierungsgruppen
verwendet wurden (doch wenigstens 20 mol-%, bezogen auf die insgesamt
vorhandenen Blockierungsgrup pen), wobei bis zu 90% der Blockierungsgruppen
die wärmeaktive
Blockierungsgruppe sind. Bei einer bevorzugten Ausführungsform
sind im Hybrid-blockierten Polyisocyanat 20 bis 65 mol-% der Blockierungsgruppen
wärmeaktive
Blockierungsgruppen.
-
Wird
das Polyisocyanat mit einem ersten Blockierungsmittel umgesetzt,
so werden einige der Polyisocyanat-Moleküle vollständig mit dem Blockierungsmittel
blockiert, einige Moleküle
(vorzugsweise der Großteil) teilweise
blockiert und verbleiben einige unblockiert. Wird das teilweise
blockierte Polyisocyanat mit einem zweiten (und wahlweise weiteren)
Blockierungsmittel umgesetzt, so werden alle der unblockierten funktionellen
Gruppen zu blockierten Gruppen. Das Ergebnis ist eine Mischpopulation
von vollständig
blockierten Polyisocyanat-Molekülen.
Allgemein ist die Verwendung von solchen Mengen der beiden Blockierungsmittel
bevorzugt, dass etwa 10 mol-% oder mehr der Polyisocyanat-Moleküle durch
mindestens eine 1,3-Dicarbonyl-Blockierungsgruppe
und durch mindestens eine wärmeaktive
Blockierungsgruppe, vorzugsweise zu mindestens 20%, zum Beispiel
zu wenigstens 30%, 40%, 50%, 60% oder 70%, blockiert sind.
-
Das
Polyisocyanat kann jegliches organische Polyisocyanat sein, einschließlich Biurets,
Allophanaten, Trimeren (Isocyanurate) und Vorpolymeren, die oben
als geeignet für
vernetzende Verbindungen, die aktiven Wasserstoff enthalten, beschrieben
sind. Die oben angegebenen Präferenzen
gelten gleichermaßen
für die Hybridblockierten
Polyisocyanate. HDI-Trimer ist besonders bevorzugt.
-
Die
1,3-Dicarbonyl-Blockierungsgruppe ist von einer oben beschriebenen
1,3-Dicarbonyl-Verbindung abgeleitet.
Die oben angegebenen Präferenzen
gelten gleichermaßen
für die
Hybrid-blockierten Polyisocyanate. HDI-Trimer ist besonders bevorzugt.
-
Die
wärmeaktive
Blockierungsgruppe ist jegliche Pyrazolgruppe, die bei Raumtemperatur
stabil bleibt, doch die bei Erhitzung entblockiert, zum Beispiel
bei Erhitzung auf eine Temperatur von über 80°C unter praktikablen Bedingungen
(siehe oben). Die wärmeaktive
Blockierungsgruppe ist von einem wärmeaktiven Agenz abgeleitet,
wie oben beschrieben. Die oben angegebenen Präferenzen gelten gleichermaßen für die Hybrid-blockierten
Polyisocyanate. HDI-Trimer ist besonders bevorzugt.
-
Das
Hybrid-blockierte Polyisocyanat weist eine 1,3-Dicarbonyl-Blockierungsgruppe
auf, die von Diethylmalonat, Dimethylmalonat, Meldrumsäure oder
Ethylacetoacetat abgeleitet ist, und eine wärmeaktive Blockierungsgruppe,
die von einem Pyrazol abgeleitet ist. Bei einer bevorzugten Ausführungsform
der vorliegenden Erfindung weist das Hybrid-blockierte Polyisocyanat
eine 1,3-Dicarbonyl-Blockierungsgruppe auf, die von Diethylmalonat
oder Dimethylmalonat abgeleitet ist, und eine wärmeaktive Blockierungsgruppe,
die von 3,5-Dimethylpyrazol oder 3,5-Di-tert-butylpyrazol abgeleitet
ist. Bei einer besonders bevorzugten Ausführungsform weist das Hybrid-blockierte
Polyisocyanat eine 1,3-Dicarbonyl-Blockierungsgruppe auf, die von
Diethylmalonat abgeleitet ist, und eine wärmeaktive Blockierungsgruppe,
die von 3,5-Dimethylpyrazol abgeleitet ist. Bei einer besonders
bevorzugten Ausführungsform
weist das Hybrid-blockierte Polyisocyanat eine 1,3-Dicarbonyl-Blockierungsgruppe
auf, die von Diethylmalonat abgeleitet ist, und eine wärmeaktive
Blockierungsgruppe, die von 3,5-Dimethylpyrazol
abgeleitet ist, wobei keine weiteren Blockierungsgruppen vorhanden
sind.
-
Das
molare Verhältnis
der 1,3-Dicarbonyl-Blockierungsgruppen zu wärmeaktiven Blockierungsgruppen
im Hybrid-blockierten Polyisocyanat ist wie oben beschrieben, zum
Beispiel 4:1 bis 1:9, bevorzugt 3:1 bis 1:8, bevorzugter 2:1 bis
1:6, noch bevorzugter 2:1 bis 1:4, sogar noch bevorzugter 2:1 bis
1:2 und am bevorzugtesten 1:1. Ein besonders bevorzugtes Verhältnis für Diethylmalonat
und 3,5-Dimethylpyrazol beträgt
1:1.
-
Die
vorliegende Erfindung stellt auch ein Verfahren zur Herstellung
eines Hybridblockierten Polyisocyanats der vorliegenden Erfindung
bereit, welches Verfahren das Umsetzen eines oder mehrerer Polyisocyanate
mit wenigstens einer 1,3-Dicarbonyl-Verbindung, ausgewählt aus Diethylmalonat, Dimethylmalonat,
Meldrumsäure
und Ethylacetoacetat, und wenigstens einem wärmeaktiven Agenz, ausgewählt aus
Pyrazolen, umfasst, wobei die Mengen an 1,3-Dicarbonyl-Verbindung
und wärmeaktivem
Agenz so sind, dass das molare Verhältnis von 1,3-Dicarbonyl-Blockierungs gruppen
zu wärmeaktiven
Blockierungsgruppen im Hybrid-blockierten Polyisocyanat im Bereich
von 4:1 bis 1:99, bevorzugt 4:1 bis 1:9 liegt. Das/die Polyisocyanat(e)
werden mit den Blockierungsmitteln gleichzeitig oder in einer beliebigen
Reihenfolge umgesetzt.
-
Werden
lediglich zwei Blockierungsmittel verwendet, so kann das Polyisocyanat
mit beiden zusammen umgesetzt werden, oder mit dem wärmeaktiven
Blockierungsmittel zuerst, gefolgt vom Umsetzen mit der 1,3-Dicarbonyl-Verbindung,
oder zuerst mit der 1,3-Dicarbonyl-Verbindung, gefolgt vom Umsetzen
mit dem wärmeaktiven
Blockierungsmittel. Vorzugsweise wird die 1,3-Dicarbonyl-Verbindung
zuerst verwendet.
-
Werden
mehr als zwei Blockierungsmittel verwendet, so kann das Polyisocyanat
mit den Blockierungsmitteln in jeglicher Reihenfolge oder Kombination
umgesetzt werden.
-
Bei
einer speziellen Ausführungsform
stellt die vorliegende Erfindung außerdem ein Verfahren zur Herstellung
eines Hybrid-blockierten Polyisocyanats bereit, welches Verfahren
das Umsetzen eines oder mehrerer Polyisocyanate mit einem Gemisch
von zwei oder mehr Blockierungsmitteln umfasst, wobei zumindest eines
der Blockierungsmittel eine 1,3-Dicarbonyl-Verbindung ist, ausgewählt aus
Diethylmalonat, Dimethylmalonat, Meldrumsäure und Ethylacetoacetat, wobei
zumindest eines der Blockierungsmittel ein wärmeaktives Agenz ist, ausgewählt aus
Pyrazolen, und wobei das molare Verhältnis von 1,3-Dicarbonyl-Blockierungsmitteln zu
wärmeaktiven
Blockierungsmitteln im Hybrid-blockierten Polyisocyanat im Bereich
von 4:1 bis 1:99, vorzugsweise 4:1 bis 1:19, noch bevorzugter 4:1
bis 1:9 liegt.
-
Typischerweise
werden das Polyisocyanat und das Blockierungsmittel erhitzt, damit
die Blockierungsreaktion erfolgen kann. Das Reaktionsgemisch wird
auf eine geeignete Temperatur für
das Erfolgen der Reaktion erhitzt. Allgemein wird das Reaktionsgemisch
auf über
50°C, vorzugsweise über 60°C erhitzt.
Wo geeignet, kann die anfängliche
Erhitzung des Reaktionsgemischs jedoch auf eine niedrigere Temperatur
erfolgen. Zum Beispiel wird HDI-Trimer mit 3,5-Dimethylpyrazol bei
anfänglicher
Erhitzung auf 30–40°C umgesetzt. Nach
Einleitung der Reaktion kann eine Abkühlung erforderlich sein, um
das Exotherm zu kontrollieren, das zum Beispiel durch die Pyrazol-Blockierungsmittel
erzeugt wird.
-
Die
Hybrid-blockierten Polyisocyanate der vorliegenden Erfindung werden
in Klarschichten, Anstrichfarben, Elastomeren, Klebstoffen, Zusammensetzungen
zum Formen oder zur Oberflächenbehandlung,
zum Beispiel für
Fasern oder Gewebe, verwendet. Die Produkte können in Abhängigkeit von den individuellen
Komponenten in fester oder flüssiger
Form (selbst in Abwesenheit von Lösungsmitteln, bezeichnet als „100% Feststoffe" im Fachgebiet) oder
in Form einer Dispersion in Wasser oder einem Flüssigträger oder einer Lösung in einem
organischen Lösungsmittel
oder Wasser vorliegen. Hybrid-blockierte Polyisocyanate, die mit
aktiven Wasserstoff enthaltenden Verbindungen reagieren, können durch
Kettenverlängerung
oder Vernetzung gehärtet
werden und werden außerdem
zur Vernetzung von Acrylharzen für
die Grundierung und Deckschicht bei Automobilen, Formulieren von
Elastomeren und Oberflächenbeschichtungen
in einer Packung, die das Hybrid-blockierte Isocyanat enthalten,
und als ein Kettenverlängerer
in einer einzigen lagerstabilen Verpackung verwendet werden, die
nach dem Formen durch Anwendung von Temperaturen oberhalb der Entblockier-ungstemperatur
gehärtet
werden können.
Die Hybridblockierten Polyisocyanate der Erfindung sind besonders nützlich in
Polyurethan-Beschichtungszusammensetz-ungen.
-
Die
vorliegende Erfindung stellt auch eine Zusammensetzung bereit, die
ein Hybridblockiertes Polyisocyanat der Erfindung und mindestens
eine monofunktionelle oder bifunktionelle oder polyfunktionelle
Verbindung umfasst, die aktiven Wasserstoff enthält. Die Zusammensetzung kann
außerdem
jegliche weiteren Komponenten umfassen, die im Bereich der Anwendung
der Zusammensetzung bekannt sind. Zum Beispiel kann eine Anstrichfarben-Zusammensetzung,
die ein Hybrid-blockiertes Polyisocyanat der vorliegenden Erfindung
umfasst, außerdem
ein Pigment umfassen. Die Anstrichfarbe kann unter Anwendung jegliches
im Fachgebiet bekannten Verfahrens aufgebracht werden, einschließlich der
elektrophoretischen Ablagerung.
-
Im
Zusammenhang mit der vorliegenden Erfindung sollte zur Kenntnis
genommen werden, dass das Entblockieren von wärmeaktiven Blockierungsmitteln
jener Vor gang ist, der stattfindet, wenn ein blockiertes Polyisocyanat,
das solch ein Blockierungsmittel enthält, bis zu dem Punkt erhitzt
wird, bei dem es zerfällt
und das Isocyanat freigesetzt wird. Die Entblockierungsreaktion
verläuft
getrennt von der Härtungsreaktion.
Bei der Entblockierungsreaktion werden freie Isocyanatgruppen wiederhergestellt,
die dann zur Reaktion mit anderen Komponenten der Härtungszusammensetzung
in der Lage sind. Die Entblockierungsreaktion ist natürlich ein umkehrbarer
Vorgang (die umgekehrte Reaktion wird zum Blockieren des Isocyanats
ausgenützt)
und unterliegt daher in verschiedenen Weisen einer Kontrolle. Zum
Beispiel begünstigt
eine erhöhte
Temperatur die Entblockierungsreaktion, und folglich sind blockierte
Polyisocyanate wärmelabil.
Die Entblockierungsreaktion wird auch durch die Konzentrationen
der verschiedenen Reagenzien kontrolliert. Zu Beginn einer Entblockierungsreaktion,
wenn alle Isocyanatgruppen blockiert sind, herrscht natürlich die
Entblockierungsreaktion vor. Wird das Blockierungsmittel entfernt
(zum Beispiel kann ein flüchtiges
Blockierungsmittel aus einer Beschichtung verdampfen), so wird die
Reaktion in Richtung der Entstehung von entblockierten Isocyanaten
vorangetrieben. Entsprechend wird dann, wenn das entblockierte Isocyanat
entfernt wird (gewöhnlich
erfolgt dies durch Reaktion mit den anderen Komponenten der Härtungszusammensetzung),
die Reaktion ebenfalls in Richtung der Entstehung des entblockierten
Materials vorangetrieben. Liegt jedoch ein Überschuss an Blockierungsmittel vor,
so kann die umgekehrte Reaktion im Vordergrund stehen. Diese Faktoren
tragen alle zur Gesamtrate der Entblockierungsreaktion bei.
-
Im
Gegensatz dazu ist die Härtungsreaktion
im Wesentlichen irreversibel. Freie Isocyanatgruppen reagieren schnell
mit den aktiven Wasserstoff enthaltenden Komponenten der Härtungszusammensetzungen und
erzeugen die gewünschten
Polyurethanpolymere, die die Grundlage eines vernetzten Produkts
bilden. Die Rate der Härtungsreaktion
wird von der Natur der Polyisocyanate, der Natur der aktiven Wasserstoff
enthaltenden Komponenten, ihren jeweiligen Konzentrationen, der
Temperatur und der Bewegungsfreiheit einzelner Moleküle innerhalb
der Zusammensetzung, wenn sich die Härtungsreaktion ihrem Abschluss
nähert
und das Medium visköser
wird, abhängen.
Die Rate der Härtungsreaktion
kann durch Katalyse erhöht
werden. Sie kann auch durch die Blockierungsreaktion nachteilig
beeinflusst werden, was wiederum die Menge an freiem Isocyanat in
dem Fall reduziert (wie mit DMP), bei dem ein relativ nicht-flüchtiges
Blockierungsmittel in zunehmendem Überschuss vorliegt, da gegen
das Ende der Härtungsreaktion
zu die Menge an freiem Isocyanat gegen Null abnimmt.
-
Es
besteht daher ein Unterschied zwischen (a) der Temperatur, bei der
die Entblockierung bei einer praktikablen Rate zur Härtung der
Zusammensetzung erfolgt, und (b) der Rate, bei der die Härtungsreaktion selbst
abläuft.
Nonrmalerweise ist die Härtungsreaktion
schnell und wird die Härtung
daher durch die Entblockierungstemperatur kontrolliert.
-
Im
Gegensatz dazu wird von den 1,3-Dicarbonyl-Blockierungsgruppen angenommen,
dass sie über eine
Transveresterungsreaktion reagieren (Wicks, Zeno W., et al., Organic
Coatings: Science and Technology, 2. Aufl., J. Wiley & Sons, 1999, ISBN
0-471-24507-0, Seite 200). Bei der Reaktion wird die Blockierungsgruppe durch
eine Hydroxyl-funktionelle Verbindung angegriffen, was die Hydroxy-funktionellen
Verbindungen vernetzt, und woraufhin das alkoholische Nebenprodukt
abgeht.
-
In
der Praxis können
Beschichtungszusammensetzungen auf der Basis der gemischt- und Hybrid-blockierten
Polyisocyanate der Erfindung bei jeglicher Temperatur oberhalb der
Entblockierungstemperatur gehärtet
werden, vorausgesetzt, dass sie in geeigneter Weise formuliert sind,
was die Blockierungsmittel betrifft, um eine schnellere Härtung zu
erreichen. Beispielsweise zeigen 3,5-DMP-blockierte Polyisocyanate
einen nachweisbaren NCO-Peak im IR-Spektrum bei 95°C, wohingegen
in einer praktischen Situation typische Härtungsbedingungen in Gegenwart
eines Polyols als einer aktiven Wasserstoffverbindung und einer
geeigneten Menge an Katalysator bei etwa 120°C für etwa 45 Minuten oder etwa
140°C für 30 Minuten
liegen würden.
-
Mit
der vorliegenden Erfindung werden die Inkompatibilitäts-Probleme
vermieden, die manchmal mit bekannten Polyisocyanaten entstehen.
Die Kompatibilität
zweier oder mehrerer Substanzen wird durch Untersuchen beurteilt,
ob die Substanzen in Mischung ein stabiles homogenes Gemisch bilden;
Substanzen, bei denen dies nicht der Fall ist, sind inkompatibel.
-
Beim
Entblockieren/Härten
reagieren die Isocyanatgruppen und bilden dabei ein Polymer. Die
aus den Polyisocyanaten der vorliegenden Erfindung gebildeten Polymere
umfassen Einheiten, die aus der Transveresterung stammen, angrenzend
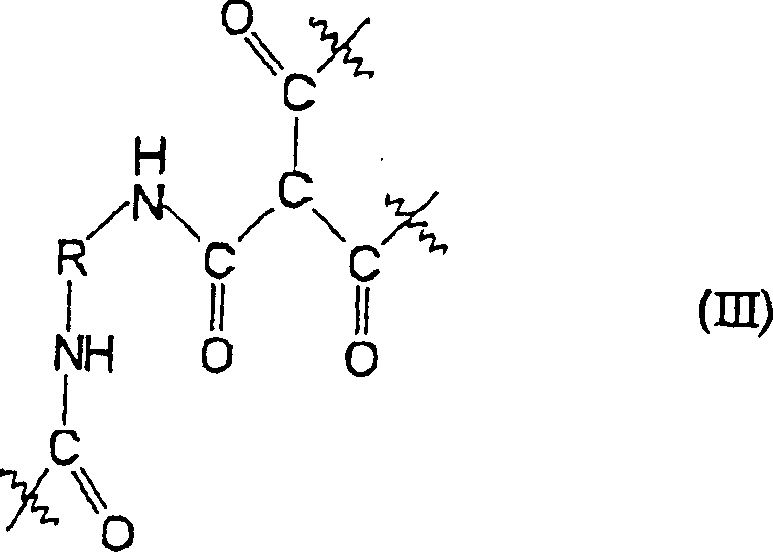
an Urethaneinheiten. Solche Polymere umfassen als einer Wiederholungseinheit
die Komponente der Formel (III)
worin die Komponente
-
-
von
einem Di- oder höheren
Isocyanat abgeleitet ist, wie etwa den oben genannten Isocyanaten.
-
Die
vorliegende Erfindung stellt weiterhin gehärtete Zusammensetzungen bereit,
umfassend ein Polymer, das als eine Wiederholungseinheit die Komponente
der Formel (II), wie oben definiert, umfasst, wobei die Beschichtungen
jene sind, die durch Härten
einer Beschichtungszusammensetzung, wie oben definiert, erhältlich sind.
Wo die wärmeaktiven
Pyrazol-Blockierungsgruppen bei thermischer Entblockierung ein relativ nicht-flüchtiges
Blockierungsmittel erzeugen, werden solche gehärteten Beschichtungen zusätzlich zum
Polymer, das die Wiederholungseinheiten der Formel (II) umfasst,
ein freigesetztes Pyrazol-Blockierungsmittel umfassen. Die Erfindung
stellt außerdem
ein Verfahren bereit, umfassend das Härten einer Beschichtungszusammensetzung,
wie oben definiert, durch Erhitzung zum Entblockieren des Polyiso cyanats
und Bewirken einer Vernetzungsreaktion. Die Erfindung stellt außerdem eine
Beschichtung bereit, die durch solch ein Verfahren erhältlich ist,
eine Beschichtung, umfassend ein Polymer, das als Wiederholungseinheit
eine Komponente der Formel (II), wie oben definiert, und freies
Pyrazol-Blockierungsmittel umfasst. Am bevorzugtesten ist das Pyrazol
3,5-Dimethylpyrazol, 3-iso-Butyl-5-tert-butylpyrazol oder 3-iso-Butyl-5-methylpyrazol.
-
Im
Anschluss an diese Arbeit hat der Anmelder außerdem eine Reihe von Pyrazol-Blockierungsmitteln identifiziert,
die besonders geeignet zur Verwendung bei der Herstellung Hybrid-blockierter
Polyisocyanate sind, doch auch alleine nützlich sein können. Dieses
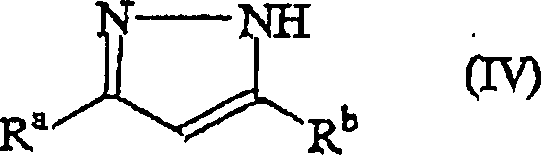
sind die verzweigten Alkylpyrazole der Formel (IV)
worin R
a Alkyl
mit 1 bis 6 Kohlenstoffatomen ist und R
b ein
verzweigtes Alkyl mit 3 bis 6 Kohlenstoffatomen ist. Vorzugsweise
ist R
a Methyl, Ethyl, n-Propyl, n-Butyl
oder verzweigtes Alkyl mit 3 bis 6 Kohlenstoffatomen. Sind R
a und R
b beide verzweigtes
Alkyl, so können
sie das selbe oder verschiedene sein.
-
Zu
geeigneten verzweigten Alkylgruppen zählen Isopropyl, Isobutyl, sec-Butyl
und tert-Butyl. Die vorliegende Erfindung stellt die folgenden,
besonders bevorzugten, verzweigten Alkylpyrazole bereit:
3-Methyl-5-iso-propylpyrazol,
3-iso-Butyl-5-methylpyrazol,
3-sec-Butyl-5-methylpyrazol,
3-Ethyl-5-iso-propylpyrazol,
3-iso-Butyl-5-ethylpyrazol,
3-sec-Butyl-5-ethylpyrazol,
3-tert-Butyl-5-ethylpyrazol,
3-iso-Propyl-5-n-propylpyrazol,
3-iso-Butyl-5-n-propylpyrazol,
3-sec-Butyl-5-n-propylpyrazol,
3-tert-Butyl-5-n-propylpyrazol,
3-n-Butyl-5-iso-propylpyrazol,
3-iso-Butyl-5-n-butylpyrazol,
3-n-Butyl-5-sec-butylpyrazol,
3-n-Butyl-5-tert-butylpyrazol,
3,5-Di-iso-propylpyrazol,
3-iso-Butyl-5-iso-propylpyrazol,
3-sec-Butyl-5-iso-propylpyrazol,
3,5-Di-iso-butylpyrazol,
3-iso-Butyl-5-sec-butylpyrazol,
3-iso-Butyl-5-tert-butylpyrazol,
3,5-Di-sec-butylpyrazol
und 3-sec-Butyl-5-tert-butylpyrazol.
-
3-tert-Butyl-5-methylpyrazol,
3-tert-Butyl-5-iso-propylpyrazol und 3,5-Di-tert-butylpyrazol können ebenfalls verwendet werden.
-
Von
diesen sind 3-iso-Butyl-5-terf-butylpyrazol, 5-iso-Butyl-3-methylpyrazol
und 3,5-Di-terf-butylpyrazol
bevorzugt und ist 3,5-Di-tert-butylpyrazol aufgrund seiner besonders
niedrigen Entblockierungstemperatur bei alleiniger Verwendung und
aufgrund seiner Stabilität
und Kapazität
zur generellen Senkung der Entblockierungstemperaturen, wenn in
einem Hybrid-blockierten Polyisocyanat verwendet, wie oben beschrieben,
besonders bevorzugt.
-
Solche
verzweigten Alkylpyrazole können
mittels herkömmlicher
Methoden hergestellt werden, welche die Bildung eines Diketons aus
einem Methylketon und einem Ester und das Umsetzen des Diketons
mit Hydrazin einbeziehen. Etwa 1 mol der Base ist erforderlich,
um die Reaktion zwischen 1 mol des Methylketons und 1 mol des Esters
zu bewirken. Für
die Synthese von asymmetrisch substituierten Pyrazolen liefert einer der
Vorläufer
die Gruppe R
a und liefert der andere die
Gruppe R
b:
wenn R
a und R
b wie oben
definiert sind und R
e-O- eine Ester-bildende
Gruppe ist, so ist R
e vorzugsweise eine Alkylgruppe,
wie z.B. Methyl.
-
Diese
Reaktionen sind sehr gut bekannt und die Ausgangsmaterialien ohne
Weiteres kommerziell verfügbar
oder mittels bekannter Methoden leicht herstellbar.
-
Eine
weitere Ausführungsform
der vorliegenden Erfindung ist ein blockiertes Polyisocyanat, bei
dem das Blockierungsmittel ein verzweigtes Alkylpyrazol ist, wie
oben beschrieben, vorzugsweise 3,5-Di-tert-butylpyrazol. Ein verzweigtes
Alkylpyrazolblockiertes Polyisocyanat wird durch Erhitzen des verzweigten
Alkylpyrazols mit einem Polyisocyanat in herkömmlicher Weise hergestellt.
Die Blockierungsmittel sind von Vorteil, wenn einzeln verwendet
oder wenn in Kombination mit 1,3-Dicarbonyl-Blockierungsmittel verwendet, da sie
eine niedrige Entblockierungstemperatur und eine gute Stabilität aufweisen
und nützliche
Grade an Stabilisierung bei Verwendung in Kombination mit 1,3-Dicarbonyl-Blockierungsmitteln
verleihen.
-
Die
Erfindung wird nun anhand der folgenden nicht-beschränkenden
Beispiele veranschaulicht werden.
-
BEISPIELE
-
Referenzbeispiel 1: Herstellung
von mit Diethylmalonat blockiertem HDI-Trimer
-
HDI-Trimer
(Desmodur N3300) (530,4 g); Diethylmalonat (933,0 g) und Natriummethoxid
(3,2 g) wurden in einen Laborreaktor eingespeist und bei 70–80°C erhitzt,
bis der NCO-Gehalt (mittels Titration bestimmt) weniger als 0,5%
betrug. Eine weitere Einspeisung von HDI-Trimer (530,4 g) und Diethylmalonat
(3,2 g) wurde vorgenommen und die Reaktion fortgesetzt, bis der
NCO-Gehalt weniger als 0,1% betrug.
-
Referenzbeispiel 2: Herstellung
von mit 3,5-DMP blockiertem HDI-Trimer
-
HDI-Trimer
(Desmodur N3300) (661,1 g) wurde in einen Laborreaktor eingespeist
und auf 35–40°C erhitzt.
DMP (338,9 g) wurde langsam zugesetzt, wobei die Temperatur unter
90°C gehalten
wurde. Die Reaktionstemperatur wurde bei etwa 90°C gehalten, bis der NCO-Gehalt
weniger als 0,1 % betrug.
-
Beispiel 1: Herstellung
von mit DMP/Diethvlmalonat (molares Verhältnis 1:1) blockiertem HDI-Trimer
-
HDI-Trimer
(Desmodur N3300) (1195,4 g), Diethylmalonat (501,3 g) und Natriummethoxid
(2,9 g) wurden in einen Laborreaktor eingespeist und bei 6–70°C erhitzt,
bis der mittels Titration bestimmte NCO-Gehalt 7,5% betrug. Die
Reaktion wurde auf 56°C
abgekühlt,
und DMP (300,4 g) wurde zugesetzt. Die Reaktion wurde bei etwa 70°C erhitzt,
bis der NCO-Gehalt weniger als 0,1 % betrug.
-
Beispiel 2: Vergleich
von DMP/DEM-blockiertem HDI-Trimer mit einem Gemisch von DEM-blockierten
und DMP-blockierten Isocyanaten
-
Die
folgenden Produkte wurden hergestellt:
- a) Ein
gemäß Referenzbeispiel
1 hergestelltes und in verschiedenen Lösungsmitteln gelöstes Produkt,
wie in nachstehender Tabelle 1 detailliert angegeben (3 Teile Lösungsmittel
zu 7 Teilen blockiertem Isocyanat).
- b) Ein gemäß Referenzbeispiel
2 hergestelltes und in verschiedenen Lösungsmitteln gelöstes Produkt,
wie in nachstehender Tabelle 1 detailliert angegeben (3 Teile Lösungsmittel
zu 7 Teilen blockiertem Isocyanat).
- c) Ein gemäß Beispiel
1 hergestelltes und in verschiedenen Lösungsmitteln gelöstes Produkt,
wie in nachstehender Tabelle 1 detailliert angegeben (3 Teile Lösungsmittel
zu 7 Teilen blockiertem Isocyanat).
- d) Ein Produkt, das durch Mischen des bei a) hergestellten Produkts
mit dem bei b) hergestellten Produkt wie oben in gleichen Anteilen
hergestellt wurde.
-
Das
Aussehen jeder Probe wurde über
einen gewissen Zeitraum bei 23°C
beobachtet; die Ergebnisse sind in Tabelle 1 gezeigt:
-
-
Die
Analyse des physikalischen Gemischs d) und Hybrid c) im Methoxypropanol-Lösungsmittel mittels GPC zeigt
eine engere Molekulargewichtsverteilung und ein niedrigeres Peak-Molekulargewicht
für das
Hybrid-Polyisocyanat c).
-
Beispiel 3: Herstellung
von mit DMP:Diethylmalonat (molares Verhältnis 1:9) blockiertem HDI-Trimer
-
HDI-Trimer
(Desmodur N3300) (387,8 g), Diethylmalonat (292,7 g) und Natriummethoxid
(1,0 g) wurden in einen Laborreaktor eingespeist und bei 65–70°C erhitzt,
bis der mittels Titration bestimmte NCO-Gehalt 1,25% betrug. DMP
(19,5 g) wurde zugegeben und die Reaktion bei etwa 70°C gehalten,
bis der NCO-Gehalt weniger als 0,1 % betrug. Methoxypropanol (300,0
g) wurde zugesetzt und das Produkt entnommen. Nach 10 Tagen war
das Produkt nach wie vor flüssig.
-
Beispiel 4: Vergleich
der Eigenschaften von DEM-, DMP- und DEM/DMP-blockiertem Isocyanat
-
Das
Aussehen des in Beispiel 3 erzeugten blockierten Isocyanats wurde überwacht,
und die Ergebnisse wurden mit entsprechenden Isocyanaten verglichen,
die mit dem einen oder dem anderen von DEM und DMP und mit einem
Gemisch dieser beiden blockierten Isocyanate blockiert waren. Die
gezeigten Ergebnisse in nachstehender Tabelle 2 bestätigen, dass
die sogenannten Hybridprodukte eine verminderte Neigung zur Kristallisation
zeigen.
-
-
Die „kristallisierten" Produkte verfestigten
sich alle, obschon in einigen Fällen „kristallisierte" Produkte klar blieben.
-
Beispiel 5
-
Aus
dem blockierten Isocyanat des Beispiels 3, bzw. aus den im obigen
Beispiel 4 genannten Vergleichsmaterialien, und einem Acrylpolyol
(Crodaplast AC589BN) wurden unter Verwendung eines DBTL-Katalysators
(0,8 Gew-% an Gesamtfeststoffen) Beschichtungen erzeugt. Die Formulierungen
wurden auf grundierte Stahlplatten aufgestrichen und bei 90, 100
oder 120°C
für 45
min gehärtet.
Die Tg des resultierenden Films, die MEK-Beständigkeit (Doppelreibungen)
und die Bleistifthärte
wurden bestimmt. Das Verhältnis
von OH:NCO der Beschichtungszusammensetzungen wurde mit 1,6:1 für das DEM-blockierte
Isocyanat gewählt (nach
Vortests bei 1,3:1 und 1,6:1 zeigte letzteres eine bessere Härtung),
1:1 für
DMP-blockiertes Isocyanat und 1,3:1 für das Hybrid-DEM/DMP-blockierte
Isocyanat. Die Ergebnisse für
die optimierten Formulierungen sind in den nachstehenden Tabellen
3, 4 und 5 gezeigt:
-
-
Tabelle
4 MEK-Doppelreibungen
-
-
Die
Ergebnisse zeigen, dass die Härtung
mit steigender Temperatur verbessert wird. Die Ergebnisse zeigen
auch, dass bei 100°C
DEM die stärkere
Härtung
ergibt, und dass bei 120°C
das Hybrid verbesserte Ergebnisse gegenüber einem DMP-blockierten Isocyanat
ergibt. Dieser Unterschied lässt
sich den beiden unterschiedlichen Reaktionswegen, die befolgt werden,
zuschreiben. Findet zum Beispiel die Transveresterung bei einer
geringeren Temperatur als der Wärmezersetzungstemperatur
statt, so wird eine nur „teilweise
Härtung" bewirkt, wenn das
Hybrid bei 100°C
verwendet wird, da die Wärmezersetzung
der DMP-blockierten Isocyanatgruppen im Zeitraum des Experiments
nicht vollständig
stattgefunden hat.
-
Die
geringfügigen
Unterschiede zwischen der bei 120°C
erreichten Härtung
können
einer unvollständigen
Reaktion des DMP-blockierten Isocyanats in der Reaktionszeit oder
chemischen Verschiedenheiten bei der vernetzten Beschichtung (Carbamat-
gg. Nicht-Carbamat-Vernetzungen) zugeschrieben werden.
-
Kurz
gesagt ist die Härtung
eines Hybrid-blockierten Isocyanats ähnlich oder etwas besser als
bei einem rein DMP-blockierten Isocyanat bei 120°C.
-
Beispiel 6: Herstellung
von 3,5-Di-t-butylpyrazol (DTP)
-
2,2,6,6-Tetramethyl-3,5-heptandion
(25 g) wurde in Dichlormethan (100 ml) gelöst. 100% Hydrazinhydrat (7,12
g) wurde unter Rühren
bei Raumtemperatur zugetropft. Das Gemisch wurde bei Raumtemperatur (25°C) über Nacht
gerührt.
Ein weiteres Aliquot des Dichlormethans (50 ml) wurde zugesetzt
und die organische Phase von der wässrigen Phase getrennt. Das
Lösungsmittel
wurde durch Verdampfung ent fernt und der resultierende Feststoff
aus Aceton rekristallisiert, was einen weißen kristallinen Feststoff
ergab. Schmp. 191–193°C.
-
Beispiel 7: Herstellung
von mit Di-t-butylpvrazol blockiertem Isocyanat
-
HDI-Trimer
(Desmodur N3300) (21,41 g) wurde mit Methoxypropanol (18 g) gemischt.
3,5-Di-t-butylpyrazol (21,41 g) wurde portionsweise über 15 Minuten
zugegeben. Das Reaktionsgemisch wurde auf 60°C erhitzt und für 1,5 Std.
gerührt.
Zwei weitere Aliquots (0,5 g) an Di-t-butylpyrazol wurden zugegeben
und die Reaktion gerührt,
bis die Infrarotanalyse die Abwesenheit der Isocyanatgruppen anzeigte.
-
Beispiel 8: Herstellung
von sowohl mit Diethylmalonat als auch 3,5-Di-tert-butylgyrazol blockiertem
HDI-Trimer
-
HDI-Trimer
(Desmodur N3300) (73,4 g) und Diethylmalonat (31,34 g) wurden gemeinsam
bei Raumtemperatur gerührt.
Natriummethoxidlösung
(0,2 g einer 27% Lösung
in Methanol) wurde zugetropft. Die Reaktionstemperatur wurde auf
65°C erhöht und durch
Titration überwacht,
bis der NCO-Gehalt 7,6% betrug. Methoxypropanol (60,0 g) wurde zugesetzt,
gefolgt von 3,5-Di-tert-butylpyrazol (35,26 g). Die Reaktionstemperatur
wurde auf 65°C
gehalten und die Reaktion durch Titration überwacht. Als der NCO-Gehalt
etwa 0,53% betrug, wurde ein weiterer Anteil an 3,5-Di-tert-butylpyrazol (3,0
g) zugesetzt. Die IR-Analyse zeigte, dass im Wesentlichen alle NCO-Gruppen
reagiert hatten.
-
Beispiel 9: Beschichtungen
auf der Basis von mit 3,5-Di-terf-butylpvrazol blockierten Polyisocyanaten
-
Beschichtungen
wurden analog dem Beispiel 5 hergestellt, außer, dass das DMP-blockierte Isocyanat durch
ein entsprechend dem Beispiel 7 hergestelltes Material ersetzt wurde
und das Hybrid-DEM/DMP-blockierte Isocyanat durch ein blockiertes
Isocyanat ersetzt wurde, dass gemäß Beispiel 8 hergestellt worden
war. Das Verhältnis
von OH:NCO betrug 1,6:1 für
DEM-blockiertes Isocyanat und 1:1 für Pyrazolblockiertes Isocyanat.
Für die
Formulierung, die das Hybrid-DEM/DTP-blockierte Iso cyanat enthielt,
wurde ein Verhältnis
von 1,3:1 angelegt. Die Formulierungen wurden auf grundierte Stahlplatten
aufgestrichen und bei der angegebenen Temperatur für 45 min
gehärtet;
die MEK-Beständigkeit
(Doppelreibungen) und die Bleistifthärte wurden alle wie oben beschrieben
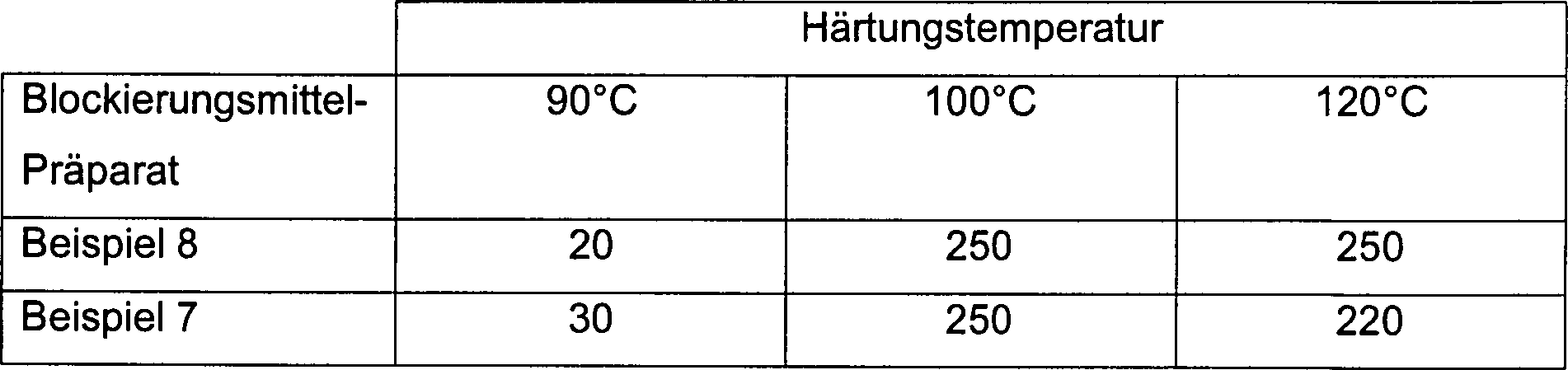
bestimmt. Die Ergebnisse sind in Tabellen 6 und 7 gezeigt.
-
Tabelle
6 MEK-Doppelreibungen
-
-
Die
Ergebnisse wurden mit denen in Tabellen 3 und 4 verglichen. Die
Bleistifthärte
ist von der selben Größenordnung,
wobei der Wert für
das Hybrid bei 120°C
niedriger und bei 100°C
höher ist.
Signifikanter ist der enorme Unterschied beim MEK-Reibungstest, bei
dem 250 MEK-Doppelreibungen sowohl für das Hybrid-DEM/Di-t-butylpyrazol als
auch das Di-t-butylpyrazol alleine erreicht wurden.
-
Beispiel 10: Beschichtungen
aus DEM/DMP-Hybrid und einem DMP-blockierten Isocyanat
-
Im
folgenden Beispiel ist das DEM/DMP-Hybrid-blockierte Isocyanat ein
blockiertes HDI-Trimer, das gemäß Beispiel
1 hergestellt und in Methoxypropanol so gelöst wurde, dass der abschließende Feststoffgehalt 70%
betrug. Das DMP-blockierte Isocya nat wird gemäß dem Referenzbeispiel 2 hergestellt
und in Methoxypropanol gelöst,
sodass der abschließende
Feststoffgehalt 70% beträgt.
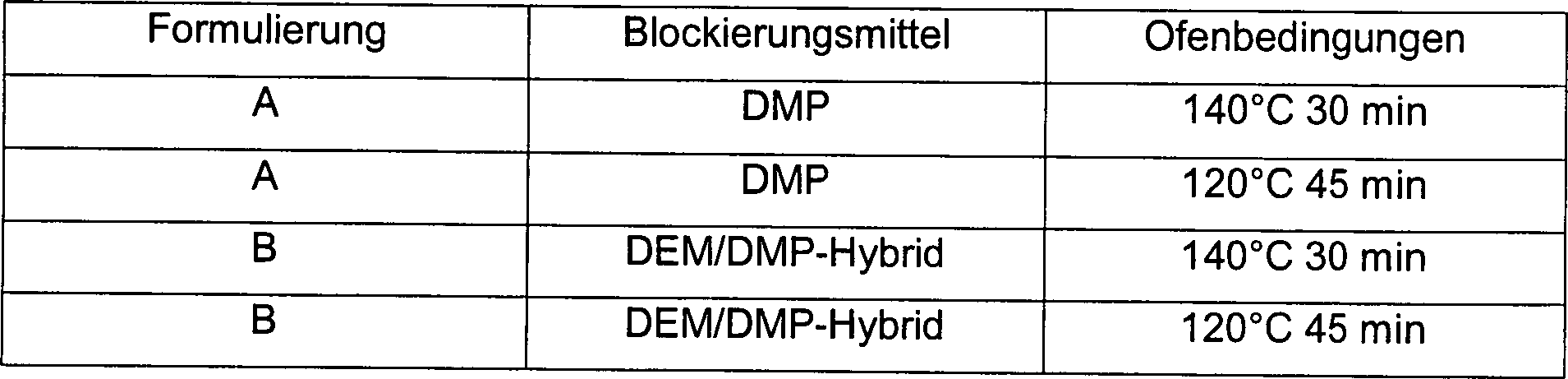
Beschichtungsformulierungen wurden gemäß der folgenden Tabelle hergestellt,
auf weiße
grundierte Stahlplatten bei 150 μm
Nassfilmdicke aufgetragen und entweder bei 120°C für 45 min oder 140°C für 30 min
ofengetrocknet. Die Formulierungen sind in Tabelle 8 und 9 gezeigt.
Die Härtungsbedingungen
sind in Tabelle 9 gezeigt.
-
-
-
Beispiel 11
-
Herstellung
eines Hybrid-blockierten Isocyanats, blockiert mit 3,5-Dimethylpyrazol:
Diethylmalonat in einem Verhältnis
von 90:10 bei 70% Feststoffkonzentration.
-
HDI-Trimer
(Desmodur N3300) (455,5 g), Diethylmalonat (38,2 g) und Natriummethoxid
(0,2 g) wurden in einen Reaktor eingespeist, gemischt und Temperatur
auf 65 bis 70°C
angehoben. Die Reaktion wurde fortgesetzt, bis der Isocyanatgehalt
18,20% betrug. 3,5-Dimethylpyrazol (206,1 g) wurde zugesetzt, wobei
die Temperatur auf unter 85°C
gehalten wurde, gefolgt von der Zugabe von Methoxypropanol (300
g). Kein Isocyanat-Peak war mittels Infrarotanalyse nachweisbar.
-
Beispiel 12
-
Herstellung
eines Hybrid-blockierten Isocyanats, blockiert mit 3,5-Dimethylpyrazol
und Diethylmalonat in einem Verhältnis
von 95:5 bei 70% Feststoffkonzentration.
-
HDI-Trimer
(Desmodur N3300) (460,6 g), Diethylmalonat (19,3 g) und Natriummethoxid
(0,2 g) wurden in einen Reaktor eingespeist, gemischt und die Temperatur
auf 65 bis 70°C
angehoben. Die Reaktion wurde fortgesetzt, bis der Isocyanatgehalt
19,7% betrug. 3,5-Dimethylpyrazol (219,9 g) wurde zugesetzt, wobei
die Temperatur auf unter 85°C
gehalten wurde, gefolgt von der Zugabe von Methoxypropanol (300
g). Kein Isocyanat-Peak war mittels Infrarotanalyse nachweisbar.
-
Herstellungsbeispiel 1
-
Herstellung
eines mit 3,5-Dimethylpyrazol bei 70% Feststoffkonzentration blockierten
Isocyanats.
-
HDI-Trimer
(Desmodur N3300) (925,6 g) wurde in einen Reaktor eingespeist, gemischt
und die Temperatur auf 40°C
erhöht.
3,5-Dimethylpyrazol (474,4 g) wurde zugesetzt, wobei die Temperatur
auf unterhalb 90°C
gehalten wurde, gefolgt von der Zugabe von Methoxypropanol (300
g). Kein Isocyanat-Peak war mittels Infrarotanalyse nachweisbar.
-
Herstellungsbeispiel 2
-
Herstellung
eines mit Diethylmalonat bei 76% Feststoffkonzentration blockierten
Isocyanats.
-
HDI-Trimer
(Desmodur N3300) (1007,5 g), Diethylmalonat (1773.0 g) und Natriummethoxid
(6,0 g) wurden in einen Reaktor eingespeist, gemischt und die Temperatur
auf 65 bis 70°C
angehoben. Die Reaktion wurde fortgesetzt, bis der Isocyanatgehalt
weniger als 0,1 % betrug. Eine weitere Menge an HDI-Trimer (1007,6
g) und Natriumethoxid (6,0 g) wurde zugesetzt, wobei die Temperatur
auf unter 70°C
gehalten wurde. Als der Isocyanatgehalt unter 0,1 % betrug, wurde
Methoxypropanol (1200 g) zugegeben. Kein Isocyanat-Peak war mittels
Infrarotanalyse nachweisbar.
-
Beispiele 13 bis 22
-
Herstellung von Klarschichten.
-
Alle
Klarschichten wurden durch Vermengen der geeigneten Menge an blockiertem/n
Isocyanat(en) (siehe nachstehende Tabelle 10) mit der geeigneten
Menge an Acrylharz (Crodaplast AC589) (siehe Tabelle 10) hergestellt.
Die folgenden Mengen der anderen Reagenzien wurden zugesetzt: Dibutylzinndilaurat
(0,1 %); Fließadditiv
(Tego 450) (verdünnt
auf 50% in Butylacetat, 0,19%); Ultraviolett-Stabilisator (Tinuvin
400) (0,97%); Ultraviolett-Stabilisator (Tinuvin 123) (0,48%), Methylethylketon
(13,64%) und Methoxypropylacetat (geeignete Menge zum Auffüllen auf
100%).
-
Bestimmung der Zwischenschichthaftung.
-
Phosphat-behandelte
Platten wurden durch Beschichten mit einer anmeldereigenen Grundierungsformulierung
(aufgebracht zu 100 μm
Nassfilmdichte) grundiert, gefolgt von Härten bei 140°C für 30 Minuten.
Eine anmeldereigene Grundschicht wurde zu 90 um Nassfilmdichte aufgetragen,
bei 50°C
für 15
Minuten getrocknet, gefolgt von der Aufbringung einer Klarschichtformulierung,
die gemäß Tabelle
10 zusammengesetzt war, zu 120 μm
Nassfilmdicke. Die beschichteten Platten wurden dann bei 140°C für 30 Minuten
gehärtet.
Die gehärteten
Beschichtungen wurden dann mit der selben anmeldereigenen Grundschicht überschichtet,
die zu einer Nassfilmdicke von 90 μm aufgetragen wurde, bei 50°C für 50 Minuten
getrocknet, gefolgt von der Aufbringung der selben Klarschicht,
aufgetragen zu 120 μm
Nassfilmdicke. Die überschichteten
Platten wurden dann bei 140°C
für 30
Minuten gehärtet.
Querschnitts-Hafttests
wurden unter Anwendung von BS3900 Teil E6 (1992) durchgeführt. Die
Ergebnisse sind in Tabelle 10 gezeigt. Eine Punktbewertung von 5
ist sehr schlecht und eine Punktbewertung von 0 die beste (es wurde
kein Versagen der Haftung beobachtet). Wo ein Versagen der Haftung
auftrat, so lag dies zwischen der ersten Klarschicht und der zweiten
Grundschicht vor.
-
Beispiel 23: Bestimmung
der Entblockierungstemperatur in Abwesenheit aktiver Wasserstoffverbindungen
-
Eine
Art und Weise, die Entblockierungstemperatur von wärmeaktiven
Blockierungsmitteln zu bestimmen, besteht im Überwachen des Auftretens des
freien Isocyanats bei erhöhter
Temperatur mittels Infrarotspektroskopie.
-
Ein
Rundbodenkolben (2 Liter), ausgestattet mit einem Rührer und
einer Temperaturaufzeichnung, wurde in einen Isomantel eingebracht.
Die Infrarotsonde eines Mettler Toledo React IR 4000 wurde in den
Kolben zur Aufzeichnung des Infrarotspektrums während der Reaktion, insbesondere
der Absorptionsbande bei 2270 cm–1 (die
Bande entsprechend der Absorption einer Isocyanatgruppe (-NCO))
eingebracht. Propylenglykolmonomethyletheracetat (Dowanol PMA, 1500
g) wurde eingespeist, gefolgt von HDI-Biuret (20,0 g). Die Temperatur
wurde auf 60°C
angehoben, und 3,5-Di-tert-butylpyrazol (DBTP, 19,23 g) zugesetzt.
Die Intensität der
Bande bei 2270 cm–1 wurde überwacht.
Nach dem Umsetzen bei 60°C
für eine
Stunde und Abkühlen
auf 25°C über Nacht
(ca. 18 Stunden) war keine Absorbanz bei 2270 cm–1 nachweisbar,
was anzeigte, dass die NCO-Gruppen vollständig mit dem DBTP reagiert
hatten. Beim Erhitzen des Produkts auf 60°C tauchte der Peak bei 2270
cm–1 wieder
auf, was die Wiederherstellung der Isocyanat-Funktionalität aufzeigte.
-
Ein ähnliches
Experiment, das unter Verwendung von 3,5-Dimethylpyrazol (DMP) anstelle
von DTBP durchgeführt
wurde, zeigte das Wiederauftreten der NCO-Bande bis 95°C nicht an.
Dies weist die niedrigere Entblockierungstemperatur von DTBP im
Vergleich zu DMP nach.
-