-
Gebiet der
Erfindung
-
Diese Erfindung betrifft Elektroden
zur Verwendung in elektrochemischen Zellen.
-
Hintergrund
der Erfindung
-
Elektrochemische Zellen sind für verschiedene
Anwendungen, insbesondere zum Betrieb als Brennstoffzellen erwünscht. Brennstoffzellen
sind für
viele Anwendungen einschließlich
elektrischer Fahrzeugantriebsanlagen als Ersatz für Verbrennungsmotoren
vorgeschlagen worden. Eine Brennstoffzellenkonstruktion verwendet
eine Festpolymerelektrolytmembran (SPE-Membran) oder Protonenaustauschmembran
(PEM), um einen Ionenaustausch zwischen der Kathode und der Anode
vorzusehen. Mit Brennstoffzellen sind sowohl gasförmige als
auch flüssige
Brennstoffe verwendbar. Beispiele umfassen Wasserstoff und Methanol,
wobei Wasserstoff bevorzugt ist. Wasserstoff wird an die Anode der
Brennstoffzelle geliefert. Sauerstoff (als Luft) ist das Zellen-Oxidationsmittel
und wird an die Kathode der Zelle geliefert. Die Elektroden sind
aus porösen
leitfähigen
Materialien hergestellt, wie beispielsweise Graphitgewebe (Carbon
Cloth), mit Graphit versehene Tafeln oder Kohlenstoffpapier (Carbon
Paper), um zu ermöglichen,
dass der Brennstoff über
die Oberfläche
der Membran, die zu der Brennstofflieferelektrode weist, verteilt
wird. Eine typische Brennstoffzelle ist in der
US 5,272,017 und der
US 5,316,871 (Swathirajan et al.)
beschrieben.
-
Wichtige Aspekte einer Brennstoffzelle
umfassen Reaktionsoberflächen,
an denen elektrochemische Reaktionen stattfinden, Katalysatoren,
die eine derartige Reaktion katalysieren, Ionen leitende bzw. durchlassende
Medien sowie Stofftransportmedien. Die Kosten des Stroms, der durch
eine Brennstoffzelle erzeugt wird, sind teilweise abhängig von
den Kosten des Katalysators. Die Kosten des Stroms, der durch eine
Brennstoffzelle erzeugt wird, sind erheblich höher als bei konkurrierenden
Stromerzeugungsalternativen, was sich teilweise auf eine relativ
schlechte Verwendung von Edelmetallkatalysatoren in herkömmlichen
Elektroden zurückführen lässt. Jedoch
besteht ein großer
Bedarf für
von auf Wasserstoff basierenden Brennstoffzellen erzeugten Strom,
da Wasserstoff vom Umweltschutz her gesehen akzeptabel ist und Wasserstoff-Brennstoffzellen
zudem wirtschaftlich und effizient arbeiten. Daher ist es erwünscht, den
Katalysatorgebrauch in Brennstoffzellenanordnungen zu verbessern,
um Brennstoffzellen zur Stromerzeugung attraktiver zu machen. Es
ist auch erwünscht,
eine Reaktandengasdiffusion sowie auch eine Bewegung von Produktwasser
in der Brennstoffzelle zu verbessern.
-
Das Patent Abstracts of Japan Band
007, Nr. 076 (E-167),
JP
58 004270 A offenbart eine Gaselektrode, die aus einer
katalytischen Schicht besteht, die derart ausgebildet ist, dass
ihre eine Seite in Kontakt mit einer porösen Basis steht und ein Kollektor
in der Schicht auf der anderen Seite integriert ist. Die katalytische Schicht
besitzt eine doppellagige Struktur. Die Konzentration der katalytischen
Substanz ist in der Nähe
der porösen
Basis, die bei einer Gasionisierungsreaktion betroffen ist, erhöht, während in
der katalytischen Schicht auf der Kollektorseite ein Konzentrationsmangel
durch eine erhöhte
Zugaberate eines Bindemittels ergänzt ist, um sowohl die Klebfestigkeit
zu steigern als auch die Elektrodenleistungsfähigkeit zu verbessern.
-
Die Abhandlung "Effects of Nafion impregnation on performance
of PEMFC electrodes",
Electrochimica Acta, Band 43, Seiten 3693 bis 3701 von Lee, S. J.
et al., offenbart eine zweilagige Elektrode bestehend aus einem
Kohlenstoffgewebesubstrat, das mit einer Katalysatorschicht beschichtet
ist.
-
Die EP-A-0 872 906 offenbart eine
Elektrode, die zur Anwendung in Brennstoffzellen mit Festpolymerelektrolyt
geeignet ist und ein dünnes
poröses
planares leitendes Substrat umfasst, von dem eine Seite mit einer
Vorschicht beschichtet ist, die aus leitfähigem Kohlenstoff mit einer
geringen Oberfläche
gemischt mit einem ersten hydrophoben Mittel besteht, auf die eine
katalytische Schicht aufgebracht ist, die aus Platin, das auf leitfähigem Kohlenstoff
mit hoher Oberfläche
getragen ist, gemischt mit einem zweiten hydrophoben Mittel besteht.
Der Hydrophobie-Grad der aufgebrachten Schichten ist geeignet eingestellt,
um die beste Ausnutzung des Katalysators zu erhalten und das Wassergleichgewicht
des Verfahrens zu verbessern.
-
Die EP-A-0 569 062 offenbart eine
kombinierte einheitliche Membran- und Elektrodenanordnung mit einer
Festpolymerelektrolytmembran und ersten und zweiten Elektroden,
die zumindest teilweise in gegenüberliegenden
Flächen
der Membran eingebettet sind. Die Elektroden umfassen jeweils eine
jeweilige Gruppe von fein geteilten Kohlenstoffpartikeln, sehr fein
geteilten katalytischen Partikeln, die auf Innen- und Außenflächen der
Kohlenstoffpartikel getragen sind, und ein protonenleitendes Material,
das mit den katalytischen Partikeln und Kohlenstoffpartikeln vermischt ist.
Eine erste Gruppe aus fein geteilten Kohlenstoffpartikeln, die die erste
Elektrode bildet, besitzt größere Wasseranziehungs-
und Wasserrückhalteeigenschaften
und ist relativ stärker
hydrophil und weniger hydrophob als eine zweite Gruppe von fein
geteilten Kohlenstoffpartikeln, die die zweite Elektrode bildet.
-
Die US-A-4 362 790 offenbart eine
poröse
Elektrode mit zumindest einer porösen katalytischen Schicht,
die ein katalytisch aktives Edelmetall, Kohlenstoff und einen Polymerbinder
umfasst. Ein poröser
Metallkollektor ist an der Elektrolytseite dieser Schicht angeordnet.
Die katalytische Schicht besitzt eine Dicke von weniger als 80 μm, und die
Edelmetallpartikel in der Schicht sind auf der Oberfläche und/oder
in den Poren von Teilen der Kohlenstoffpartikel angeordnet, während der
Rest der Kohlenstoffpartikel keine Edelmetallpartikel umfasst.
-
Die Abhandlung "Influence of PTFE content in the diffusion
layer of low PT loading electrodes for polymer electrolyte fuel
cells", Electrochimica
Acta, Band 43, Seiten 3675 bis 3680 von Griorgi, L. et al. offenbart eine
Elektrodenanordnung mit einem Kohlenstoffpapiersubstrat, einer Diffusionsschicht,
die aus Kohlenstoffpartikeln und Polytetrafluorethylen (PTFE) besteht,
und einer Katalysatorschicht, die durch einen Katalysator, bei dem
Platin auf Kohlenstoff abgeschieden ist, und Nafion (Perfluorsulfonsäurepolymer)
gebildet ist.
-
Zusammenfassung
der Erfindung
-
Gemäß einer Ausführungsform
ist eine Elektrodenanordnung vorgesehen mit:
- (a)
einer Stromkollektortafel, die ein poröses Substrat und ein Tetrafluorethylenpolymer
umfasst;
- (b) einer Barrierenschicht, die ein protonenleitendes Material
und Kohlenstoffpartikel umfasst; und
- (c) einer Katalysatorschicht, die ein protonenleitendes Material
und Kohlenstoffpartikel umfasst;
wobei - (i)
die Barrierenschicht zwischen der Stromkollektortafel und der Katalysatorschicht
angeordnet ist,
- (ii) die Barrierenschicht keinen Katalysator besitzt oder mit
einem Katalysator in Form katalytischer Partikel versehen ist,
- (iii) die Katalysatorschicht mit einem Katalysator in Form katalytischer
Partikel versehen ist, und
- (iv) die Barrierenschicht unter der Voraussetzung, dass die
Barrierenschicht mit einem Katalysator versehen ist, eine Katalysatorbeladung
von bis zu 0,02 mg/cm2 aufweist, was auf der Basis von 100 Gewichtsteilen
von Katalysator und Kohlenstoffpartikeln 5 Gewichtsteilen
katalytischen Partikeln und 95 Gewichtsteilen Kohlenstoffpartikeln
entspricht.
-
Somit umfasst die Elektrodenanordnung
eine Stromkollektortafel, eine erste Elektrodenschicht und eine
zweite Elektrodenschicht. Die erste Elektrodenschicht ist zwischen
der Stromkollektortafel und der zweiten Elektrodenschicht angeordnet.
Die erste Schicht umfasst eine kleine Gruppe von Kohlenstoffpartikeln,
und die zweite Schicht umfasst eine zweite Gruppe von Kohlenstoffpartikeln.
Die erste Schicht besitzt keinen Katalysator oder ist mit einem
Katalysator in der Form einer ersten Gruppe von sehr fein geteilten
katalytischen Partikeln versehen. Die zweite Schicht ist mit einem
Katalysator in Form einer zweiten Gruppe von sehr fein geteilten
katalytischen Partikeln versehen. Das Gewichtsverhältnis von
katalytischen Partikeln zu Kohlenstoffpartikeln der ersten Schicht
ist kleiner als das der zweiten Schicht.
-
Jede der Kohlenstoffpartikelgruppen
kann eine Vielzahl der Kohlenstoffpartikel umfassen, wobei Innen-
und Außenflächen eine
Vielzahl von Poren innerhalb und zwischen den Kohlenstoffpartikeln
definieren. Die sehr fein geteilten katalytischen Partikel sind
auf den Innen- und den Außenflächen der
Kohlenstoffpartikel getragen.
-
Die erste Schicht muss keinen Katalysator
besitzen, und die zweite Schicht umfasst die Kohlenstoffpartikel
mit sehr fein geteilten katalytischen Partikeln, die auf den Innen-
und den Außenflächen der
Kohlenstoffpartikel getragen sind.
-
Bevorzugt ist die erste Gruppe von
Kohlenstoffpartikeln durch eine Dichte von 0,1 g pro Kubikzentimeter
oder weniger gekennzeichnet, die einem Volumen pro Gramm von zumindest
10 Kubikzentimeter pro Gramm entspricht. Geeigneterweise ist die
zweite Gruppe von Kohlenstoffpartikeln durch einen pH gekennzeichnet,
der im Bereich von etwa 6 bis etwa 9 liegt. Bevorzugt ist jede der
Kohlenstoffpartikelgruppen durch einen pH gekennzeichnet, der im
Bereich von etwa 6 bis etwa 9 liegt. Geeigneterweise ist die zweite
Gruppe von Kohlenstoffpartikeln durch einen durchschnittlichen Porenradius
gekennzeichnet, der größer als
5 Nanometer ist. Jede der Schichten umfasst ferner ein protonenleitendes
Material, das mit den Kohlenstoffpartikeln und den katalytischen
Partikeln gemischt ist.
-
Geeigneterweise ist die Beladung
der zweiten Schicht mit katalytischen Partikeln kleiner als etwa
0,30 mg pro cm2 der Elektrodenoberfläche. Die
katalytische Beladung der ersten Schicht ist kleiner als diejenige
der zweiten Schicht und liegt geeigneterweise in der Größenordnung
von bis zu etwa 0,15 mg/cm2 und liegt bevorzugt
in der Größenordnung
von bis zu etwa 0,02 mg/cm2.
-
Bei einem Aspekt umfasst die zweite
Schicht katalytische Partikel und Kohlenstoffpartikel in einem Gewichtsverhältnis von
etwa 20 : 80. Das protonenleitende Material bildet etwa 30 bis etwa
35 Gewichtsprozent der zweiten Schicht, und die katalytischen Partikel
und Kohlenstoffpartikel bilden den Rest.
-
Bei einem Verfahren zur Herstellung
einer verbesserten Elektrodenanordnung, die oben beschrieben ist,
zur Verwendung in einer elektrochemischen Zelle wird die erste Schicht
der Elektrode dadurch hergestellt, dass eine Mischung bestehend
aus protonenleitendem Material, einer ersten Gruppe von Kohlenstoffpartikeln und
optimalerweise katalytischen Partikeln gebildet wird. Die Mischung
wird auf eine Stromkollektortafel aufgetragen, um einen Film zu
bilden. Die zweite Schicht der Elektrode wird durch Formen einer
zweiten Schicht über
der ersten Schicht hergestellt, wobei die zweite Schicht ein protonenleitendes
Material, eine zweite Gruppe von Kohlenstoffpartikeln und katalytische
Partikel umfasst. Die Gewichtsmenge der katalytischen Partikel relativ
zu den Kohlenstoffpartikeln der zweiten Schicht ist größer als
die der ersten Schicht. Dieses Verfahren erzeugt eine Elektrode
mit einer erheblich gesteigerten Katalysatorverwendung und einer
erheblichen Verringerung der Katalysatorbeladung, wo durch die Elektrode
daher weniger teuer herzustellen ist, als Elektroden, die nach Verfahren
nach dem Stand der Technik hergestellt werden.
-
Es ist auch ein Verfahren zur Herstellung
einer kombinierten Elektrolyt- und
Elektrodenanordnung für eine
elektrochemische Zelle vorgesehen, die eine Elektrolytmembran aus
protonenleitendem Festpolymermaterial und erste und zweite Elektroden
aufweist, die auf jeder Seite der Elektrolytmembran angeordnet sind. Zumindest
eine der Elektroden wird durch das Verfahren der Erfindung, das
oben beschrieben ist, ausgebildet. Die bei diesem Verfahren hergestellte
Elektrode wird anschließend
auf einer ersten Fläche
der Elektrolytmembran angeordnet, so dass die zweite Schicht zu
der Membran weist. Eine zweite Elektrode wird auf der gegenüberliegenden
Fläche
der Membran angeordnet, und die resultierende Anordnung wird erhitzt
und gepresst, um die Elektroden an der Membran anzuhaften. Bei einer
bevorzugten Ausführungsform
des erfindungsgemäßen Verfahrens
werden die Elektroden an der Membran angehaftet, indem die Anordnung
einer Drucklast und einer erhöhten
Temperatur ausgesetzt wird, was zur Folge hat, dass einige der Partikel
zumindest teilweise in der Membran eingebettet werden, wodurch ein
kontinuierlicherer Weg für
Protonen zu dem Katalysatorort vorgesehen wird, an dem die Reaktion
erfolgt.
-
Die ersten und zweiten Gruppen von
Kohlenstoffpartikeln sind gleich oder unterschiedlich. D.h. sie können dieselben
Eigenschaften besitzen oder sich in zumindest einer Eigenschaft
unterscheiden. In dem Fall, wenn beide Schichten mit Katalysatoren
versehen sind, können
die Katalysatoren der jeweiligen Schichten gleich oder verschieden
sein.
-
Wie aus der Beschreibung der Elektrode,
der Membranelektrodenanordnung und dem Brennstoffzellensystem, wie
oben beschrieben ist, offensichtlich ist, sieht die Erfindung eine
verbesserte Katalysatorverwendung sowie ein verbessertes Wassermanagement
vor.
-
Es ist eine Aufgabe der Erfindung,
neue Elektroden und neue Membranelektrodenanordnungen vorzusehen.
Eine andere Aufgabe besteht darin, ein Verfahren zur Herstellung
der Elektroden und Anordnungen, die die verbesserten Elektroden
umfassen, vorzusehen. Vorteilhafterweise sieht die Membran/Elektrodenanordnung
der Erfindung einen relativ hohen Stromausgang mit einer unerwartet
niedrigen Katalysatorbeladung vor.
-
Diese und andere Aufgaben, Merkmale
und Vorteile werden aus der folgenden Beschreibung der bevorzugten
Ausführungsformen,
Ansprüche
und begleitenden Zeichnungen offensichtlich.
-
Zeichnungskurzbeschreibung
-
1 ist
eine schematische Ansicht einer noch nicht zusammengebauten elektrochemischen
Brennstoffzelle mit einer Elektrode und einer kombinierten Membran-
und Elektrodenanordnung gemäß der Erfindung.
-
2 ist
eine bildliche Darstellung eines Querschnittes einer Membranelektrodenanordnung
gemäß der Erfindung.
-
3 ist
eine bildliche Darstellung eines anderen Querschnitts einer Membranelektrodenanordnung mit
Graphittafeln.
-
4 ist
eine vergrößerte Darstellung,
die ein katalytische Partikel tragendes Kohlenstoffpartikel vermischt
mit protonenleitendem Material zeigt.
-
5 zeigt
die Wirkung des Teflongehaltes des Stromkollektors auf eine PEM-Brennstoffzelle,
die mit den folgenden Parametern betrieben wurde: 80°C, Luft/H2, Stöchiometrie
3/1,2, 207 kPa (30 psig), 20 Gewichtsprozent PtVu, 10 mil SC, 0,5
g/cc, Nafionll2-Membran, Pt-Beladung
= 0,28 mg/cm2/Elektrode.
-
6 zeigt
die Wirkung der Verwendung einer Primär-Kohlenstoff/ Katalysatorschicht auf
die Leistungsfähigkeit
einer PEM-Brennstoffzelle, wobei 20 Gewichtsprozent PtVu und 5 Gewichtsprozent
Pt/AB, jeweils für
die Haupt- und Primärschichten
verwendet wurden. Nafion-112-Membran;
Pt-Beladung : 0,35 mg/cm2/Elektrode; Luft/H2, 80°C,
207 kPa (30 psig), Stöchiometrie
3/1,2.
-
7 zeigt
die Wirkung der Stromkollektordichte auf die Leistungsfähigkeit
einer PEM-Brennstoffzelle, die mit den folgende Parametern betrieben
wurde: 80°C,
Luft/H2, Stöchiometrie 3/1,4 und 207 kPa
(30 psig), 20 Gewichtsprozent PtVu, Nafion-112-Membran, Pt-Beladung = 0,3 mg/cm2/Elektrode.
-
8 zeigt
die Wirkung das Nafion-Gehaltes einer Kathode auf die Leistungsfähigkeit
der PEM-Brennstoffzelle, wenn sie mit den folgenden Parametern betrieben
wurde: 80°C,
Luft/H2, Stöchiometrie 3/1,5, 55 / 207
kPa (30 psig), 20 Gewichtsprozent PtVu, 10 mil SC, 0,42 g/cc, 19
Gewichtsprozent Teflon, Dowmembran, Pt-Beladung = 0,45 mg/cm2/Zelle.
-
9 zeigt
das Volumen von einem Gramm von 10 Gewichtsprozent auf Kohlenstoff
getragenem Pt-Katalysator.
-
10 zeigt
die Wirkung des Kohlenstofftyps auf die Leistungsfähigkeit
der PEM-Brennstoffzelle, wenn sie mit den folgenden Parametern betrieben
wurde: 0,5 V, 80°C,
Luft/H2, 207 kPa (30 psig), Stöchiometrie
3/1,5, 10 Gewichtsprozent Pt/Kohlenstoff, 10 mil SC, 0,42 g/cc,
25 Gewichtsprozent Teflon, Dowmembran, Pt = 0,11 ± 0,02
mg/cm2/Elektrode.
-
11 zeigt
die Auswirkung einer Behandlung mit Vulcan XC-72R auf die Leistungsfähigkeit
der PEM-Brennstoffzelle, - wenn sie mit den folgenden Parametern
betrieben wurde: 80°C,
Luft/H2, 207 kPa (30 psig), Stöchiometrie
3/1,5, 10 Gewichtsprozent PtVu, 10 mil SC, 0,42 g/cc, 24 Gewichtsprozent
Teflon, Dowmembran, Pt = 0,23 mg/cm2/Zelle.
-
12 zeigt
die Auswirkung des Kohlenstofftyps auf die elektrochemische Oberfläche von
Platin.
-
13 zeigt
den Ausdruck einer Zellenstromdichte bei 0,5 Volt in Abhängigkeit
des pH der Kohlenstoffaufschlämmung,
die dazu verwendet wird, den Pt-Katalysator zu verteilen. Die experimentellen
Bedingungen sind gleich zu 10.
-
14 zeigt
den Ausdruck einer Zellenstromdichte bei 0,5 Volt in Abhängigkeit
des durchschnittlichen Porenradius des Kathodenkohlenstoffträgers. Die
experimentellen Bedingungen sind gleich wie in 10.
-
Detaillierte
Beschreibung der bevorzugten Ausführungsformen
-
Bei einer Ausführungsform ist eine Elektrodenanordnung
vorgesehen, die eine Stromkollektortafel und erste und zweite Schichten
aus Elektrodenmaterial umfasst. Gemeinsam verbessern die Schichten
eine Katalysatorverwendung sowie ein Wassermanagement. Diese Schichtenanordnung
ist insbesondere als eine Kathode nützlich. Vor der weiteren Beschreibung
der Elektrodenanordnung wird nun zunächst die Zelle, die die Elektrode
umfasst, beschrieben.
-
In 1 ist
eine elektrochemische Zelle 10 mit einer kombinierten Membranelektrolyt-
und Elektrodenanordnung (MEA) 12, die darin eingeschlossen
ist, in einer nicht zusammengebauten Form dargestellt. Die elektrochemische
Zelle 10 ist als eine Brennstoffzelle aufgebaut. Jedoch
ist die hier beschriebene Erfindung ebenfalls auf elektrochemische
Zellen allgemein anwendbar. Die elektrochemische Zelle 10 umfasst
Endplatten 14, 16 aus rostfreiem Stahl, Graphitblöcke 18, 20 mit Öffnungen 22, 24,
um eine Gasverteilung zu erleichtern, Dichtungen 26, 28,
Stromkollektoren 30, 32 aus Kohlenstofftafeln
mit jeweiligen Verbindungen 31 und 33 sowie die
Membranelektrolyt- und Elektrodenanordnung (MEA) 12. Die
beiden Sätze
von Graphitblöcken, Dichtungen
und Stromkollektoren, nämlich 18, 26, 30 und 20, 28, 32 werden
jeweils als jeweilige Gas- und Stromtransportmittel 36, 38 bezeichnet.
Die Anodenverbindung 31 und Kathodenverbindung 33 werden
dazu verwendet, eine Verbindung mit einer externen Schaltung herzustellen,
die andere Brennstoffzellen umfassen kann.
-
Die elektrochemische Brennstoffzelle 10 arbeitet
mit gasförmigen
Reaktanden, von denen einer ein Brennstoff, der von einer Brennstoffquelle 37 geliefert
wird, und der andere ein Oxidationsmittel ist, das von einer Quelle 39 geliefert
wird. Die Gase von den Quellen 37, 39 diffundieren
durch jeweilige Gas- und Stromtransportmittel 36 und 38 auf
gegenüberliegenden
Seiten der MEA 12.
-
2 zeigt
eine schematische Darstellung der Anordnung 12 gemäß der vorliegenden
Erfindung. Wie in 2 gezeigt
ist, bilden poröse
Elektroden 40 eine Anode 42 auf der Brennstoffseite
und ein Kathode 44 auf der Sauerstoffseite. Die Anode 42 ist
von der Kathode 44 durch eine Festpolymerelektrolytmembran (SPE-Membran) 46 getrennt.
Die SPE-Membran
46 sorgt für einen Innentransport, um
Reaktionen in der Brennstoffzelle 10 zu erleichtern. Bei
einer Anordnung sehen die Elektroden der Erfindung eine wirksamere Protonenübertragung
durch engen Kontakt mit der Elektrode und der Ionomermembran vor,
um einen im Wesentlichen kontinuierlichen Polymerkontakt für eine derartige
Protonenübertragung
vorzusehen. Bevorzugt ist die Elektrode in die Membran eingesetzt
oder zumindest teilweise in dieser eingebettet. Demgemäß besitzt
die MEA 12 der Zelle 10 eine Membran 46 mit
beabstandeten ersten und zweiten gegenüberliegenden Flächen 50, 52,
eine Dicke oder ein Zwischenmembranbereich 53 zwischen
den Flächen 50, 52.
Jeweilige Elektroden 40, nämlich die Anode 42 und
die Kathode 44 sind mit der Membran 46 an einer
entsprechenden der Flächen 50, 52 gut
verklebt.
-
Bei einer Ausführungsform umfassen jeweilige
Elektroden 40 (Anode 42, Kathode 44)
ferner jeweilige erste und zweite teflonierte (mit Polytetrafluorethylen
beschichtete, imprägnierte)
Graphittafeln 80, 82 an jeweiligen Stellen der
Membran 46. (3)
Das aktive Anodenmaterial ist zwischen der ersten Fläche 50 der
Membran und der ersten Tafel 80 angeordnet. Das aktive
Kathodenmaterial ist zwischen der zweiten Fläche 52 und der zweiten
Tafel 82 angeordnet.
-
SPE-Membran
-
Die Festpolymerlektrolytmembran (SPE-Membran) 46 der
vorliegenden Erfindung ist in der Technik als ein innenleitendes
Material gut bekannt. Derartige SPE-Membrane werden auch als Polymerelektrolytmembrane
(PEM) bezeichnet. Typische SPE-Membrane sind in den U.S.-Patenten
Nrn. 4,272,353, 3,134,697 und 5,211,984 beschrieben.
-
Die SPE-Membrane oder -Tafeln sind
Ionentauscherharzmembrane. Die Harze umfassen Innengruppen in ihrer
polymeren Struktur, wobei eine Ionenkomponente durch die Polymermatrix
fixiert oder gehalten ist und zumindest eine andere Ionenkomponente
ein mobiles austauschbares Ion ist, das elektrostatisch mit der fixierten
Komponente verbunden ist. Die Fähigkeit
des mobilen Ions, unter geeigneten Umständen gegen andere Ionen ausgetauscht
werden zu können,
verleiht diesen Materialien eine Ionentauschereigenschaft.
-
Die Ionentauscherharze können durch
Polymerisieren einer Mischung von Bestandteilen hergestellt werden,
von denen eines einen ionischen Bestandteil umfasst. Das sogenannte
Sulfonsäure-Kationentauscherharz
stellt eine breite Klasse von Kationen tauschenden protonenleitenden
Harzen dar. Bei den Sulfonsäuremembranen
sind die Kationen-Ionentauschergruppen
hydrierte Sulfonsäureradikale,
die durch Sulfonierung an der Polymerhauptkette angebracht sind.
-
Die Bildung dieser Ionentauscherharze
in Membrane oder Tafeln ist in der Technik ebenfalls gut bekannt.
Der bevorzugte Typ ist ein Polymerelektrolyt mit perfluorierter
Sulfonsäure,
bei dem die gesamte Membranstruktur Ionentauschereigenschaften besitzt.
Diese Membrane sind kommerziell erhältlich. Ein typisches Beispiel
einer kommerziell erhältlichen
sulfonierten protonenleitenden Perfluorcarbonmembran wird durch
E.I. Dupont de Nemours & Co.
mit dem Markennamen Nafion® vertrieben. Andere wurden
von Dow Chemical entwickelt. Derartige protonenleitende Membrane
können
durch Monomere der Strukturen: CF2=CFOCF2CF2SO3H,
CF2=CFOCF2CF(CF3)OCF2SO3H
und -CF2CF2CF(ORX)CF2CF2- gekenn zeichnet sein,
wobei x So3H oder CO2H
ist. Nafion® ist
ein Fluoropolymer und genauer ein Copolymer, das monomere Einheiten
perfluorierter Carbon- oder Sulfonsäure umfasst. Nafion®-Polymer
und Polymermembrane sind Nafion®-Polymere,
die aus Copolymeren aus Tetrafluorethen und perfluorierten Monomeren
hergestellt sind, die Sulfon- oder Carbonsäuregruppen umfassen. Das perfluorierte
Sulfoncopolymer ist für
die Erfindung bevorzugt.
-
Bei der in dieser Erfindung beispielhaft
dargestellten elektrochemischen Brennstoffzelle 10 ist
die Membran 46 eine für
Kationen permeable, protonenleitende Membran mit H+-Ionen
als dem mobilen Ion. Das Brennstoffgas ist Wasserstoff (oder Reformat),
und das Oxidationsmittel ist Sauerstoff oder Luft. Die Gesamtzellenreaktion
ist die Oxidation von Wasserstoff zu Wasser, und die jeweiligen
Reaktionen an der Anode 42 und Kathode 44 sind
H2 = 2H+ + 2e (Anode)
und ½ O2 + 2H+ + 2e = H2O (Kathode).
-
Da Wasserstoff als das Brennstoffgas
verwendet wird, ist das Produkt der Gesamtzellenreaktion Wasser.
Typischerweise wird das Produktwasser an der Kathode 44 abgegeben,
die die Elektrode 40 auf der Sauerstoffseite ist. Typischerweise
entweicht das Wasser dann durch einfache Strömung oder durch Verdampfung.
Jedoch kann ggf. ein Mittel vorgesehen sein, um das Wasser zu sammeln,
wenn es gebildet wird, und dieses von der Zelle wegzutragen. Ein
Wassermanagement in der Zelle ist für einen erfolgreichen Langzeitbetrieb
der elektrochemischen Brennstoffzelle wichtig. Wassermanagementtechniken
und Zellenkonstruktionen, die damit in Verbindung stehen, sind in
den U.S.-Patenten Nrn. 5,272,017 ('017) und 5,316,871 ('871) beschrieben. Die vorliegende Erfindung
verbessert das Wassermanagement während des Brennstoffzellenbetriebs weiter
und ist auch auf andere Merkmale, wie beispielsweise eine effektive
Elektrodenverwendung, eine effektive Protonenübertragung zwischen Elektroden
und der Membran und einer guten Gasdiffusion gerichtet. Diese Merkmale
werden durch die verbesserte Elektrodenkonstruktion der vorliegenden
Erfindung zumindest teilweise verbessert.
-
Elektroden
-
Die Elektroden der Erfindung umfassen
einen Stromkollektor sowie ein aktives Elektrodenmaterial, das in
Zellenreaktionen eingreift. Elektrochemische Reaktionen in einer
Brennstoffzelle erfolgen an einem Schnittstellenbereich zwischen
dem protonenleitenden Ionomer, dem Katalysator, A dem
elektronenleitenden Kohlenstoff sowie dem gasförmigen Reaktanden. Somit sollte
für eine
gute Katalysatorverwendung der Elektrode so aufgebaut sein, dass
die Katalysatorstellen in engem Kontakt mit der Protonenaustauschmembran, dem
gasförmigen
Reaktanden sowie dem elektronenleitenden Kohlenstoff stehen.
-
Eine herkömmliche Elektrode kann durch
Verfahren hergestellt werden, die in den U.S.-Patenten Nr. 5,272,017
und 5,316,871 beschrieben sind. Dies wird durch die Anode der 2 und 3 beispielhaft dargestellt. Bei einer
derartigen Anordnung werden die mit Katalysator versehenen Kohlenstoffpartikel
vorbereitet und dann mit dem protonenleitenden Bindemittel in Lösung mit
einem Gusslösungsmittel
kombiniert. Die Lösung wird
auf eine teflonierte Graphittafel 30 aufgebracht, das Gusslösungsmittel
wird verdampft und die verbleibende Schicht, die mit Katalysatoren
versehene Kohlenstoffpartikel und Binder umfasst, wird dann in Kontakt mit der
Membran gebracht und mit dieser heißverpresst. Hierbei stehen
die mit Katalysator versehenen Kohlenstoffpartikel 60 in
engem Kontakt mit der Membran 46 und sind daran angehaftet.
Wie hier beschrieben ist, wird bevorzugt ein gewisser Anteil der
mit Katalysatoren versehenen Kohlenstoffpartikel zumindest teilweise in
der Membran 46 eingebettet.
-
4 ist
eine bildliche Darstellung, die die vergrößerte Ansicht eines mit Katalysator
versehenen Kohlenstoffpartikels 60 zeigt, wobei darauf
sehr fein geteilte katalytische Partikel 62 getragen sind.
Mit den Partikeln ist ein protonenleitendes Material 64 vermischt.
-
Der neue Aufbau der Elektrode der
Erfindung ist hier zur Verwendung als eine Kathode beschrieben, ist
jedoch nicht darauf beschränkt.
Es wird davon ausgegangen, dass sie sowohl als Anode als auch als
Kathode verwendbar ist, wobei hier jedoch gezeigt wird, dass es
besonders vorteilhaft ist, wenn sie als eine Kathode verwendet wird.
Die Elektrode der vorliegenden Erfindung umfasst eine Stromkollektortafel 82,
eine erste Elektrodenschicht 70 und eine zweite Elektrodenschicht 72.
Die erste Elektrodenschicht 70 liegt zwischen der Stromkollektortafel 82 und
der zweiten Schicht 72. Die erste Elektrodenschicht umfasst
eine erste Gruppe von Kohlenstoffpartikeln 60, und die
zweite Schicht umfasst eine zweite Gruppe von Kohlenstoffpartikeln 60. Die
Kohlenstoffpartikel der ersten und zweiten Gruppe können vom
selben Typ an Kohlenstoffpartikeln sein und können dieselben physikalischen
Eigenschaften besitzen, wie in den Tabellen gezeigt sind. Bei einer
anderen Ausführungsform
sind die Kohlenstoffpartikel der ersten und zweiten Gruppe unterschiedliche
Typen von Kohlenstoffpartikeln und besitzen unterschiedliche Eigenschaften.
Die Eigenschaften sind in Tabelle 2 definiert.
-
Bei einer Ausführungsform besitzen die Kohlenstoffpartikel
der ersten Gruppe keinen Katalysator (3).
Bei einer weiteren Ausführungsform
sind die Kohlenstoffpartikel der ersten Gruppe, die die erste Schicht
bildet, mit einem Katalysator versehen (2). Der Katalysator 62 liegt
in der Form von sehr fein geteilten katalytischen Partikeln vor
und besteht typischerweise aus Metallpartikeln, wie nachfolgend
weiter beschrieben ist. Bei beiden Ausführungsformen ist die zweite
Schicht 72 mit einem Katalysator in Form fein geteilter
katalytischer Partikel 62 versehen. Der relative Gehalt
von katalytischen Partikeln 62 und Kohlenstoffpartikeln 60 der
ersten und zweiten Schichten ist so gewählt, dass das Gewichtsverhältnis der
katalytischen Partikel zu Kohlenstoffpartikeln der ersten Schicht 70 kleiner
als das der zweiten Schicht 72 ist. Es ist offensichtlich,
dass, wenn die erste Schicht keine katalytischen Partikel umfasst,
aber die zweite Schicht mit einem Katalysator versehen ist, diese
Bedingung erfüllt
ist. Bei der Ausführungsform,
wenn katalytische Partikel in beiden Schichten enthalten sind, ist
das Gewichtsverhältnis
von katalytischen Partikeln zu Kohlenstoffpartikeln in der zweiten
Schicht größer als
das der ersten.
-
Bei einer Ausführungsform umfassen die Kohlenstoffpartikel
der ersten Schicht eine Vielzahl von inneren und äußeren Flächen, die
eine Vielzahl von Poren definieren. Die sehr fein geteilten katalytischen
Partikel sind auf den inneren und äußeren Flächen der Kohlenstoffpartikel
getragen (4). Bevorzugt
werden die Kohlenstoffpartikel 60 mit einem Katalysator
in der Form der katalytischen Partikel 62 versehen, bevor
sie mit einem protonenleitenden Material 64 gemischt werden,
um die erste Schicht zu formen.
-
Bei einer Ausführungsform wird die zweite
Schicht auf im Wesentlichen dieselbe Art und Weise wie die erste
Schicht ausgebildet. Dies bedeutet, dass die Kohlenstoffpartikel
mit einem Katalysator in Form der katalytischen Partikel versehen
werden und anschließend
die mit Katalysator versehenen Kohlenstoffpartikel mit dem protonenleitenden
Material gemischt werden. Diese Mischung wird dann auf die erste
Schicht aufgebracht, um die zweite Schicht zu bilden.
-
Die katalytischen Partikel sind bevorzugt
metallisch, Metalle oder Legierungen. Am Bevorzugtesten werden Edelmetallkatalysatoren
verwendet, wie beispielsweise Platin (Pt) und Palladium (Pd). Zusätzlich können andere,
relativ stabile Metalle verwendet werden, einschließlich der
Legierungsbildung. Beispiele sind Titan, Ruthenium, Rhodium, Wolfram,
Zinn oder Molybdän.
-
Die Erfindung sieht ein Verfahren
zum Formen der mehrlagigen Elektrode vor, die zumindest erste und zweite
Schichten aufweist. Die erste Schicht wird auch als Primärschicht
und die zweite Schicht als Hauptschicht bezeichnet. Das Verfahren
zum Herstellen einer Elektrodenstruktur umfasst die Schritte, dass:
(a) eine Stromkollektortafel 82 vorgesehen wird; (b) eine
erste Schicht 70 auf der Tafel gebildet wird, die protonenleitendes
Material 64, eine erste Gruppe von Kohlenstoffpartikeln 60 und
optional katalytische Partikel 62 umfasst; und (c) eine
zweite Schicht 72 über
der ersten Schicht geformt wird, wobei die zweite Schicht protonenleitendes
Material 64, eine zweite Gruppe von Kohlenstoffpartikeln 60 und
katalytische Partikel 62 umfasst. Die Gewichtsmenge katalytischer
Partikel relativ zu Kohlenstoffpartikeln der zweiten Schicht ist
größer als
diejenige der ersten Schicht. Bei einer Ausführungsform wird wie bei dem
vorher erwähnten
Verfahren Schritt (a) ausgeführt,
indem eine erste Mischung eines protonenleitenden Materials, eine
erste Gruppe von Kohlenstoffpartikeln und eine erste Gruppe von
fein geteilten katalytischen Partikeln, die auf und in den Kohlenstoffpartikeln getragen
sind, gebildet wird; und die erste Mischung auf die Oberfläche des
Stromkollektors aufgebracht und ein erster Film aus der Mischung
gebildet wird.
-
Bei einer Ausführungsform wird Schritt (c)
ausgeführt,
in dem eine zweite Mischung aus protonenleitendem Material, eine
zweite Gruppe von Kohlenstoffpartikeln und eine zweite Gruppe von
fein geteilten katalytischen Partikeln, die auf und in den Kohlenstoffpartikeln
getragen sind, gebildet wird; und die zweite Mischung auf die erste
Schicht aufgebracht wird.
-
Die Membranelektrodenanordnung wird
hergestellt, indem die mehrlagige Elektrode und eine Gegenelektrode
auf eine jeweilige Oberfläche
der Membran aufgebracht und dann bei einer Temperatur und Drucklast
heißgepresst
wird, die ausreichend sind, um die Elektroden an die Membran anzuhaften.
Bevorzugt wird zumindest ein Anteil der Partikel der Elektroden
zumindest teilweise in der Membran eingebettet, die während des
Heißpressens
bei hoher Temperatur aufgeweicht wird.
-
Genauer wird das aktive Material
der Anode 42 auf eine teflonierte Graphittafel 80 aufgebracht.
Dann wird die Seite des aktiven Anodenmaterials, das von der Tafel 80 getragen
wird, mit der ersten Fläche 50 der Membran 46 in
Kontakt gebracht. Das mehrlagige aktive Material der Kathode 44 auf
Tafel 82 wird mit der zweiten Fläche 52 der Membran 46 in
Kontakt gebracht. Die beschichteten Tafeln 80, 82 werden
mit der Membran heißverpresst,
während
sie für
eine ausreichende Zeitdauer und bei einer Temperatur und Drucklast
erhitzt wird, die ausreichend sind, um die Membran 46 aufzuweichen
und zumindest einen Anteil der Partikel in der Membran zumindest
teilweise einzubetten, wodurch die ersten und zweiten Elektroden 42, 44 geformt
werden. Die eingebetteten oder eingesetzten Partikel sind zumindest
teilweise in jeweilige Oberflächen
der Membran eingesetzt, obwohl sie von der Membran nicht vollständig umgeben
oder unterhalb ihrer Oberfläche
angeordnet sind.
-
Der Schritt zum Erhitzen beim Pressen
wird bei etwa 17 bar bis etwa 69 bar (250 bis 1000 Pfund pro Quadratzoll)
Drucklast für
eine bis etwa fünf
Minuten bei einer Temperatur von etwa 280°F (130°C) bis etwa 320°F (160°C) ausgeführt. Es
hat sich herausgestellt, dass eine Drucklast von , etwa 34,5 bar
(500 Pfund pro Quadratzoll) für
etwa ein bis etwa zwei Minuten bei einer Temperatur von etwa 300°F (etwa 150°C) effektiv
ist.
-
Die Drucklast kann mit der Zeit variieren.
Dies bedeutet, dass eine geringere Last und längere Zeitdauer verwendet werden
können,
wobei umgekehrt das gleiche gilt.
-
Das Einbetten von Elektroden in die
Membran unter Druck sorgt für
einen kontinuierlichen Weg von protonenleitendem Material von einer
Seite der Membranelektrodenanordnung zu der anderen. Die enge Vermischung
des protonenleitenden Materials mit Katalysator und Kohlenstoffpartikeln
sieht einen kontinuierlichen Weg für Protonen zu dem Katalysatorort
vor, an dem die Reaktion erfolgt. Das Verfahren erzielt auch eine relativ
optimale Verwendung der katalytischen Partikel einschließlich benachbart
der Membran an der Elektrode.
-
Das protonenleitende Material und
die katalytischen Partikel sowie Kohlenstoffpartikel, die die Hauptschicht
(zweite Schicht) der Anode und Kathode bilden, sind in einem auf
100 Teilen basierenden Gewichtsverhältnis mit etwa 30 bis etwa
70 Teile protonenleitendem Material und dem Rest katalytischen Partikeln
und Kohlenstoffpartikeln vorhanden. Die katalytischen Partikel und
Kohlenstoffpartikel sind in einem auf 100 Gewichtsteilen basierenden
Verhältnis
mit bis zu etwa 20 Teilen katalytischen Partikeln und dem Rest Kohlenstoffpartikeln
vorhanden. Die Kathodenprimärschicht
(erste Schicht) besitzt keinen Katalysator oder umfasst einen geringeren
Prozentsatz an katalytischen Partikeln. Die Menge liegt in der Größenordnung
von 0,02 mg/cm2 katalytischen Partikeln. Dies entspricht etwa 5
Gewichtsteilen katalytischen Partikeln und 95 Gewichtsteilen Kohlenstoffpartikeln.
-
Bei einer Ausführungsform umfasst die Kathode
eine erste Schicht, die Kohlenstoffpartikel umfasst, die mit protonenleitendem
Material vermischt sind. Alternativ dazu umfasst die erste Schicht
Kohlenstoffpartikel, die mit einem Katalysator in Form einer geringen
Menge an Platin in der Größenordnung
von 0,02 mg/cm2 (5 Gewichtsprozent Platin) versehen sind, und als
Rest Kohlenstoff. Diese Schicht umfasst allgemein 40 Gewichtsprozent
protonenleitendes Material (Nafion) und als Rest den Kohlenstoff
oder mit Katalysator versehenen Kohlenstoff in der Größenordnung
von 60 Gewichtsprozent. Diese Schicht besitzt typischerweise eine
Dicke von etwa 10 bis etwa 13 Mikron. Die zweite Schicht umfasst
Kohlenstoffpartikel, die mit einem Katalysator in Form von 20 Gewichtsprozent
Platin versehen sind. Das Gewichtsverhältnis von Nafion zu mit Katalysator versehenem
Kohlenstoff in der Hauptschicht liegt im Bereich von 30 bis 35 Gewichtsprozent
Nafion (protonenleitendes Material) und 65 bis 70 Gewichtspro zent
mit Katalysator versehenem Kohlenstoff. Es ist erwünscht, dass
der Kohlenstoff einen pH in einer durch den Kohlenstoff und das
Wasser gebildeten Aufschlämmung
von etwa 6 bis 9 aufweist. Bevorzugt ist der pH größer als
6,5 und liegt bei etwa 6,5 bis etwa 9. Es ist bevorzugt, dass die
durchschnittliche Porengröße einem
Radius von größer als
5 Nanometern entspricht. Dies stellt die durchschnittliche Porengröße von sowohl
Mesoporen als auch Mikroporen dar. Es ist bevorzugt, dass der Stromkollektor,
der die Primärschicht
(erste Schicht) und Hauptschicht (zweite Schicht) trägt, eine
Dichte in der Größenordnung
von 0,3–0,35
gν/cm2 aufweist.
-
Beispiel
-
Bei diesem Beispiel wurde eine Membranelektrodenanordnung
(MEA) 12 hergestellt. Die Anode wurde durch herkömmliche
Mittel hergestellt und die Kathodenelektrode wurde durch das verbesserte
Verfahren der Erfindung hergestellt. In beiden Fällen wurde Kohlenstoffpapier
für den
Stromkollektor verwendet, das die Komponenten des aktiven Materials
der Elektrode trug. Bei diesem Beispiel wurden sowohl Nafion® als
auch Teflon® verwendet.
Die Membran aus Nafion® und Lösung aus Nafion® wurde
von DuPont bzw. Solution Technology erhalten. Nafion® ist
ein registriertes Markenzeichen von DuPont. Teflon® ist
ebenfalls ein Markenzeichen von DuPont.
-
Behandlung
der Kohlenstofftafel
-
Es wurden Kohlenstofftafeln aus SpectraCarb(SC)
für den
Stromkollektor von der Spectra Corp. Lawrence, MA in dem Dickenbereich
von 8–11
Mils und einer Dichte erhalten, die von 0,26 g/cc bis 0,7 g/cc variierte.
Das Kohlenstoffpapier wurde mit Teflon beschichtet, indem dieses
horizontal an einem Gestell angeordnet wurde und dann das Papier
und das Gestell in eine gut gerührte
Mischung aus Teflon und Wasser für
2 Minuten eingetaucht wurde. Die Teflonsuspension wurde hergestellt,
indem ein Volumenteil einer Lösung
aus Teflon 30 B von DuPont mit 24 Volumenteilen aus deionisiertem
Wasser gemischt wurde. Nach dem Trocknen der Tafel bei 120°C für 15–20 Minuten
wurde das Papier bei 320°C
für 15
Minuten und 380°C
für 30–60 Minuten in
einem Muffelofen gesintert. Der Teflongehalt der Tafel wurde berechnet,
indem die Tafel vor und nach der Teflonbehandlung gewogen wurde.
Die Verteilung von Teflon in der Kohlenstofftafel wurde unter Verwendung einer
Elektronenmikrosondenanalyse gemessen. Es wurde beobachtet, dass
der obere Anteil der Tafel einen höheren Teflongehalt aufwies,
als die untere Seite.
-
Herstellung
der MEA
-
Nach der Beschichtung der Kohlenstofftafel
mit Teflon wurde die Seite mit dem höheren Teflongehalt zur Beschichtung
einer doppellagigen Elektrodenstruktur ausgewählt. Die Primärschicht
bestand aus einer Barrierenschicht, um das Eindringen der Katalysatoraufschlämmung in
die Kohlenstofftafel zu verhindern. Die Aufschlämmung für die Primärkohlenstoff/Barrierenschicht
wurde hergestellt, indem 1 g Acetylen- Schwarz (AB) mit 5 Gewichtsprozent
Pt, 10 g deionisiertem Wasser und 13,4 g Nafion-Lösung
(5 % Lösung,
Solution Technology) in einem Ultraschallbad für 2 bis 3 Minuten gemischt
wurde, um eine dicke Aufschlämmung
zu bilden. Nach Aufbringen einer Schicht der AB-Aufschlämmung auf
die obere Seite einer teflonierten Kohlenstofftafel unter Verwendung
einer Bürste,
einer Rakel bzw. einem Streichmesser oder einer Sprühpistole
wurde die Tafel unter einer Wärmelampe
für 15
Minuten bei 100°C
getrocknet. Der trockene Film besaß eine Katalysatorbeladung
von 0,02 mg/cm2, eine Nafion-Beladung von 40 Gewichtsprozent und
eine Kohleschwarz-Beladung von 60 Gewichtsprozent. TEM-Studien zeigten,
dass die Dicke der Primärschicht
zwischen 10 bis 13 μm
lag.
-
Um den Kathodenkatalysator in der
Hauptkatalysatorschicht (zweiten Schicht) zu tragen, wurden neun Kohlenstoffträger mit
unterschiedlichen Eigenschaften bewertet. Der Anodenkatalysatorträger war
Vulcan XC-72R, der durch herkömmliche
Mittel hergestellt wurde. Kohlenstoffe, die für den Kathodenkatalysator verwendet
wurden, wurden sowohl in wie gelieferter als auch wärmebehandelter
Form verwendet. Die Wärmebehandlung
wurde bei 1000°C
für 1 Stunde
in Argon ausgeführt.
Die Kohlenstoffe waren mit einem Katalysator in Form eines Platinkatalysators
(Pt-Katalysators)
versehen. Der Katalysator wurde hergestellt, indem eine wässrige Lösung aus
Hexachlorplatinsäure
(Johnson Matthey) zu einer Kohlenstoff/Wasser-Mischung zugesetzt
wurde und dies anschließend
für 1 Stunde
gerührt
wurde. Das Pt (IV) wurde dann durch Zusatz von Natriumborhydrid
im Überschuss
auf den metallischen Zustand reduziert, das tropfenweise zu der
Kohlenstoffaufschlämmung
hinzugesetzt wurde. Nach einem Rühren
der Mischung für
eine weitere Stunde wurde der pH der Lösung auf ca. 7,0 eingestellt,
indem 1 M Schwefelsäure
zugesetzt wurde. Schließlich
wurde die mit Platin beladene Kohlenstoffmischung gefiltert, vollständig mit
Wasser gewaschen und in Luft bei 100°C über Nacht getrocknet. Anschließend wurde
eine Aufschlämmung
vorbereitet, in dem der mit Platin versehene Kohlenstoff mit 5 Gewichtsprozent
Nafion-Lösung (Solution
Technology, Inc., Mendenhall, Pennsylvania) eingehend gemischt wurde.
Die Katalysatoraufschlämmung
wurde auf die Kohlenstofftafel aufgebracht, die bereits mit der Primärschicht
(ersten Schicht) beschichtet worden ist. Die Katalysatoraufschlämmung wurde
durch Bürsten aufgebracht
und die Elektroden wurden bei 100°C
für eine
Stunde getrocknet. Die Pt-Beladungen wurden durch Wiegen der eingehend
getrockneten Kohlenstofftafeln vor und nach dem Aufbringen jeder
Schicht berechnet. Um die MEA vorzubereiten, wurde eine Dow-Experimentalmembran
oder eine Membran mit Nafion 112 zwischen den beiden Elektroden
schichtartig angeordnet, und die MEA wurde bei etwa 34,5 bar bis
etwa 69 bar (500 bis 1000 Pfund pro Quadratzoll) für 1,5–2,0 Minuten
bei etwa 150 °C
(300°F)
heißgepresst.
-
MEA-Bewertung
-
Die Membranelektronanordnung mit
einer aktiven Elektrodenfläche
von 25 cm2 wurde in der aus Graphit bestehenden Untersuchungsspanneinrichtung
für einzelne
Zellen (Elektrochem, Inc.) positioniert. Die einzelne Zelle wurde
durch eine Brennstoffzellenuntersuchungsstation von Globe-Tech betrieben, die
das Zellenpotential oder den Zellenstrom, die Temperatur, den Druck,
den Mengendurchfluss von Gasen sowie die Befeuchtung der Reaktandengase
unter Verwendung eines auf einem IBM-PC basierenden Datenaufnahme-
und Steuersystems steuerte. Um die MEA zu konditionieren, wurde
die Zelle für
24 Stunden bei 1 A/cm2 mit Wasserstoff und
Sauerstoff als Reaktanden bei 80°C
und 207 kpa (30 psig) Druck betrieben. Es wurde eine Strom-Spannung=Kurve
mit H2/Luft als Reaktanden bei 80°C sowie verschiedenen
Gasdrücken
aufgezeichnet. Die Stöchiometrie
der Reaktanden betrug 2,5–3
für Luft
und 1,2–1,5
für H2. An dem Ende jeder Untersuchung wurden
zyklische Voltammogramme (CV) (Stromspannungskurven) der MEA aufgezeichnet,
um die elektrochemisch aktive Oberfläche des Pt-Katalysators an
der Kathode zu bestimmen, wie vorher beschrieben wurde.
-
Experimentelle
Erlebnisse Wirkungen der Behandlung des Stromkollektors
-
Graphittafeln wurden als Stromkollektor
und Gasdiffusor nach einer Beladung derselben mit einem feuchtebeständigen Mittel
verwendet, wie beispielsweise Teflon®. Zusätzlich zur Änderung
der Teflonbeladung in der Kohlenstofftafel wurde auch die Dichte
der Kohlenstofftafel variiert. 20 Gewichtsprozent Pt (getragen auf Vulcan
XC-72R Kohlenstoff) wurden als der Katalysator verwendet, und die
MEA wurde mit einer Membran aus Nafion 112 sowie einer
Pt-Beladung von 0,28 mg/cm2/Elektrode hergestellt. 5 zeigt die Auswirkung der Abänderung
des Teflongehalts des Stromkollektors auf die Leistungsfähigkeit
der Brennstoffzelle. Wenn die Teflonbeladung erhöht wird, fällt die Leistungsfähigkeit
der Zelle bei geringeren Stromdichten ab. Eine Zunahme des spezifischen
Widerstandes der Elektrode infolge eines höheren Gehaltes an nichtleitendem
Teflon-Polymer in
der Matrix wird ebenfalls als ein Nebeneffekt beobachtet. Da Teflon
hinzugesetzt wird, um die Hydrophobie der Elektrode zu steigern,
scheint es, dass eine Zunahme in der Hydrophobie zu Schwierigkeiten bei
der Entfernung von Wasser von den Reaktionsorten führt. Dies
führt zu
einer Überflutung
der Elektrode; die den scharfen Abfall des Stromes bei verschiedenen
Spannungen zur Folge hat, wenn der Teflongehalt erhöht wird.
Die höchste
Leistungsfähigkeit
der Brennstoffzelle (820 mA/Cm2 bei 0,6V)
in dieser Serie von Experimenten wurde bei dem geringsten Teflon gehalt
für das
Graphitpapier von 4 Gewichtsprozent erhalten. Dies bedeutet, 4 Gewichtsprozent
Teflon und 96 Gewichtsprozent Graphitpapier.
-
Die Auswirkung des Auftragens einer
Primärkohlenstoffschicht
auf die Graphittafel vor Beschichtung der Hauptkatalysatorschicht
ist in 6 gezeigt. Die
Primärschicht
hilft, die Leistungsfähigkeit
der Brennstoffzelle zu verbessern, indem die Hauptkatalysatorschicht
in der Nähe
der Membrangrenzfläche
verdichtet ist. Die Katalysatoraufschlämmung dringt nun nicht mehr
in die Graphittafel ein, und daher hat die Primärkohlenstoffschicht (erste
Schicht) einen wichtigen Anteil daran, die Verwendung von Kohlenstofftafeln
mit geringer Dichte zu ermöglichen,
die wie nachfolgend beschrieben ist eine überlegene Leistungsfähigkeit
zeigen.
-
Es wurde die Auswirkung der Dichte
des Stromkollektors der Kohlenstofftafel in dem Bereich von 0,26 g/cc
bis 0,7 g/cc auf die Leistungsfähigkeit
der PEM-Brennstoffzelle studiert. Die Ergebnisse sind in 7 gezeigt. Die Dichte des
Papiers bestimmt deutlich die Stromdichte, bei der die Spannung
infolge von Stoffportbegrenzungen abrupt abfiel. Tafeln mit geringerer
Dichte sind poröser,
und die Makroporosität
hilft bei einer leichten Entfernung des Wassers sogar bei hohen
Stromdichten. Wenn die Papierdichte von 0,7 auf 0,26 g/cc verringert
wurde, wurden zwei Auswirkungen beobachtet. Zunächst stieg die Stromdichte
bei 0,6 V von 0,62 A/cm2 auf ein Maximum
von 1 A/cm2 bei 0,33 g/cc vor Verringerung auf 0,26 g/cc an. Diese
Verbesserung der Zellenleistungsfähigkeit wurde trotz der Zunahme
des Teflongehaltes von dem optimalen Niveau von 4 Gewichtsprozent
auf 8 Gewichtsprozent bei einer Dichte von 0,33 g/cc beobachtet.
Wenn die Papierdichte verringert wurde, stieg der Teflongehalt von
4 auf 11,7 Gewichtsprozent infolge der höheren Teflonauufnahme bei geringeren Dichten
von einer Aufschlämmung,
die eine konstante Teflonkonzentration in Lösung besaß. Diese Zunahme des Teflongehaltes
bewirkte möglicherweise
das Maximum in der Stromdichte bei 0,6 V bei einer Papierdichte
von 0,33 g/cc. Zweitens stieg die maximale Stromdichte in dem linearen
Bereich der Strom-Spannungs-Kurve (vor dem scharfen Abfall) von
0,6 A/cm2 auf einen Wert von 1,8 A/cm2 bei der geringsten Dichte von
0,26 g/cc. Somit erscheint eine Stromkollektordichte von 0,3 bis
0,35 g/cc für
Kathodenanwendungen optimal zu sein.
-
Auswirkung
des Nafion-Gehaltes in der Hauptkatalysatorschicht
-
Die Katalysatorschicht benötigt das
protonenleitende Nafionpolymer in seiner Matrix] um einen guten Kontakt
aller Katalysatorpartikel mit dem Elektrolyt sicherzustellen. Jedoch
muss die Menge an Nafion optimiert werden, da jeder Überschuss
zu einer Wasserzurückhaltung
und der folgenden Überflutung
von Katalysatororten führen
kann. 8 zeigt die Auswirkung
des Kathoden-Nafion-Gehaltes auf die Leistungsfähigkeit der PEM-Brennstoffzelle.
Diese Serie von Experimenten verwendete 20 Gewichtsprozent Pt/Vulcan
XC-72R Katalysator, der im Haus hergestellt wurde, Graphitpapier
(10 mil, 0,42 g/cc) von SpectraCorp mit einem Teflon-Gehalt von
19 Gewichtsprozent. Eine Erhöhung
des Nafion-Gehaltes
von 20 Gewichtsprozent auf 30 Gewichtsprozent ergab eine erhebliche
Verbesserung der Leistungsfähigkeit
der Brennstoffzelle, während
weitere Erhöhungen
zu einer Verminderung der Leistungsfähigkeit der Zelle führten.
-
Um die Auswirkung der Nafion-Beladung
zu interpretieren, wurde die echte Oberfläche des Platinkatalysators
durch das elektrochemische Wasserstoffadsorptionsverfahren bestimmt,
wobei die Ergebnisse in Tabelle 1 gezeigt sind. Bei einer Nafion-Beladung
von weniger als 30 Gewichtsprozent hat jede Erhöhung des Nafion-Gehaltes zur
Folge, dass die echte Pt-Oberfläche
zunimmt. Infolgedessen erhöht
dies die Erreichbarkeit der Katalysatororte für den protonenleitenden Elektrolyt.
Um Unterschiede in der tatsächlichen
Pt-Beladung zu berücksichtigen,
wurde die Pt-Oberfläche unter
Verwendung der Gesamt-Pt-Beladung, der geometrischen Oberfläche und
des absoluten elektrochemischen Bereiches normalisiert. Aus Tabelle
1 ist zu sehen, dass eine Erhöhung
des Nafion-Gehaltes
von 20 auf 30 Gewichtsprozent in einer Zunahme der normalisierten Oberfläche von
57 % resultierte, was die starke Erhöhung der Leistungsfähigkeit
der Brennstoffzelle erklärt. Erhöhungen der
Nafion-Beladung über 30 Gewichtsprozent
führt nur
zu kleinen Erhöhungen
in der echten Fläche,
die infolge nachteiliger Auswirkungen von überschüssigem Naflon auf das Elektrodenwassermanagement der
Leistungsfähigkeit
der Brennstoffzelle nicht nützt.
-
Es wurde bestimmt, dass eine höhere Nafion-Beladung
in der Primärschicht
(erste Schicht) erforderlich ist, da Nafion ein Bindemittel ist
und zwischen der Haupt- oder Katalysatorschicht (zweiten Schicht)
und der Kohlenstofftafel eine gute Bindung erforderlich ist. Wenn
die Nafion-Beladung
in der Primärschicht
auf 30 bis 35 % verringert wurde, wurde ein Brechen der Haupt- oder
Katalysatorschicht (zweiten Schicht) beobachtet. Die Leistungsfähigkeit
der Brennstoffzelle war auch bei einem Experiment, das mit 30 %
Nafion in der Primärschicht
durchgeführt
wurde, geringer.
-
Auswirkung des Kohlenstoffträgers in
der Hauptkatalysatorschicht
-
Physikalisch-chemische Eigenschaften
der Kohlenstoffträger,
die dazu verwendet werden, die Katalysatoren der Brennstoffzelle
zu verteilen, spielen in Verbindung mit dem Wassermanagement der
Zelle und insbesondere an der Luftkathode eine entscheidende Rolle.
In den U.S. Patenten Nrn. 5,272,017 und 5,316,817 erzielten unter
Umgebungsbedingungen kugelgemahlenes Vulcan XC-72R für die Anode
und Ketjen-Black, das im gelieferten Zustand verwendet wurde, für die Kathode
eine überlegene
Leistungsfähigkeit.
Es ist bestimmt worden, dass physikalische Eigenschaften, wie beispielsweise
die Gesamtoberfläche,
Porenverteilung, Porenvolumen und durchschnittliche Porengröße den Grad
der Dispersion des Pt-Katalysators und das Ausmaß einer Überflutung in den Poren, die
durch Kapillarkräfte
betrieben wird, bestimmen. Chemische Eigenschaften, wie beispielsweise
die chemische Zusammensetzung der Oberfläche, die durch den pH der Aufschlämmung gemessen
wird, bestimmen den Grad an Hydrophobie der Porenwände. Halbhydrophobe
Bereiche stellen eine Abweisung von Wasser von der Elektrodenmatrix
sicher und ermöglichen
einen leichten Transport von Reaktandengasen zu den Katalysatororten.
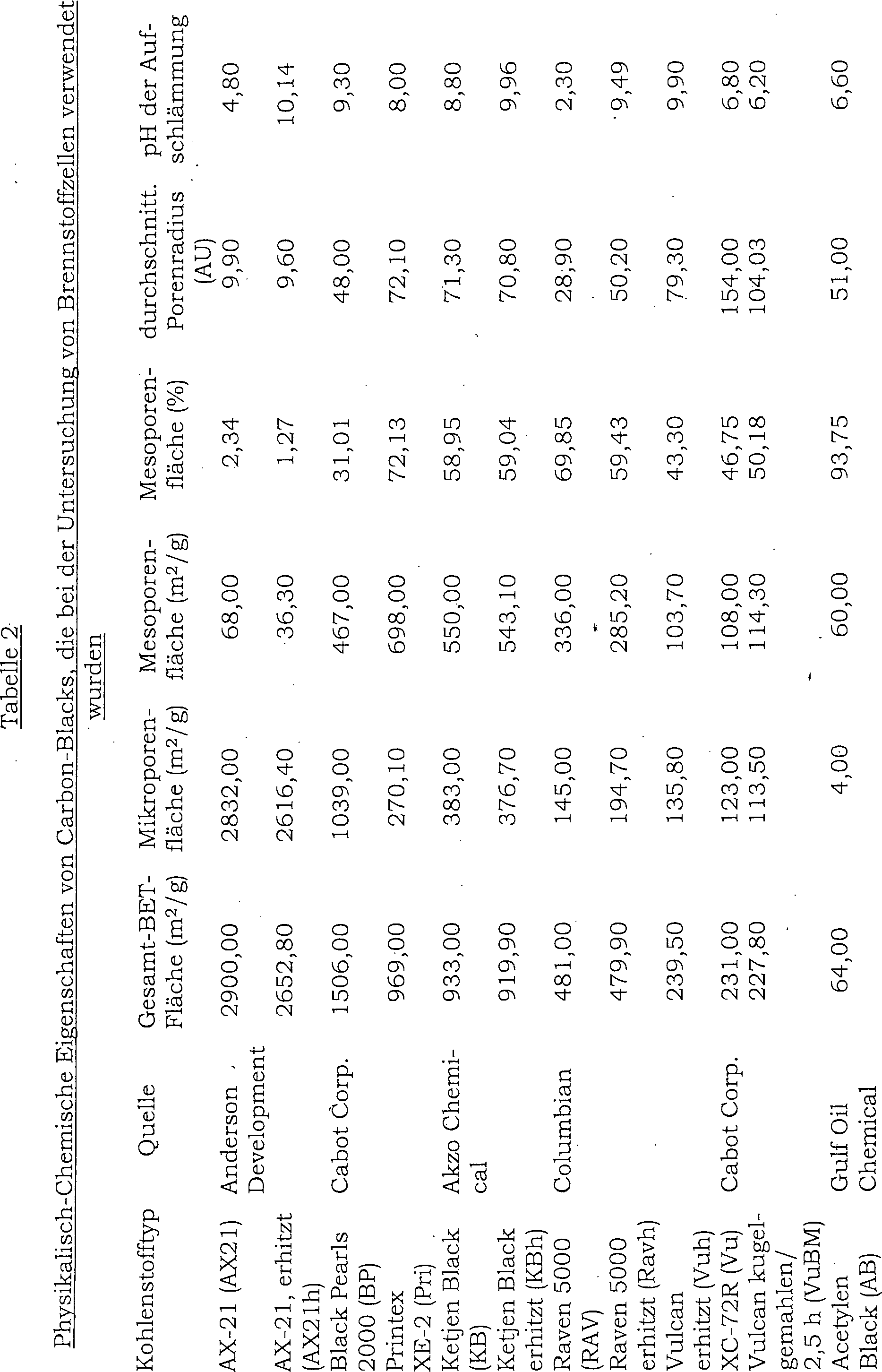
Tabelle 2 listet verschiedene physikalisch – chemische Eigenschaften von
mehreren Arten von Kohle-Schwarz auf, die für die Leistungsfähigkeit
der Brennstoffzellenelektrode von Interesse sind. Mikroporen in
Kohlenstoffen besitzen Porengrößen mit
einem Durchmesser von kleiner als 2 nm, während Mesoporen Porendurchmesser
im Bereich von 2 bis 50 nm besitzen. Acetylen-Schwarz besitzt den
höchsten
Prozentsatz an Mesoporenfläche,
und AX-21 den geringsten. Kohlenstoffe besitzen sowohl einen sauren
als auch alkalischen pH in der gelieferten Form, aber eine Wärmebehandlung macht
sie alle alkalisch. Ketjen-Black- und Black-Pearls- 2000-Kohlenstoffe
besitzen den höchsten
pH und Raven 5000 besitzt den geringsten pH in gelieferter
Form. Bei der Elektrodenherstellung ist ebenfalls die Dichte von
Kohlenstoffpartikeln sowie das Porenvolumen, das für die Gasdiffusion
verfügbar
ist, von Interesse. Diese kann von dem Volumen von 1 Gramm Kohleschwarz,
das mit 10 Gewichtsprozent Pt beladen ist, bewertet werden, was
in 9 gezeigt ist. Acetylen-Black
und Raven 5000 besaßen
die höchsten
bzw. geringsten Kohlenstoffvolumen. Vulcan XC-72R, Ketjen-Black,
Printex und Black-Pearls 2000 besaßen ähnliche Porenvolumen.
-
10 zeigt
die Leistungsfähigkeit
der Brennstoffzelle für
die verschiedenen Carbon-Blacks im gelieferten bzw. wärmebehandelten
Zustand. Obwohl diese Experimente nicht mit der optimalen Stromkollektordicke
oder Teflonbeladung durchgeführt
wurden, zeigen sie eine wichtige Tendenz in den Ergebnissen, die
mit der Hydrophobie der Träger
korreliert werden kann. Anders als in dem vorliegenden Fall, bei
dem KB sich als das deutlich beste herausgestellt hat, zeigen die
Hochtemperatur- und Hochdruckexperimente, dass Acetylen-Black, Ketjen-Black
und Vulcan XC-72R ähnliche
Leistungsfähigkeiten
besitzen. Eine Wärmebehandlung von
Acetylen-Black, Ketjen-Black, Printex und Vulcan XC-72R resultierte
in einer Verringerung der Zellenleistungsfähigkeit im Vergleich zu den
Kohlenstoffen im gelieferten Zustand. Wärmebehandeltes Raven 5000 und Black
Pearls 2000 zeigte eine erhebliche Zunahme der Zellenleistungsfähigkeit
von 88% bzw. 43%. Vulcan XC-72R wurde verschiedenen physikalischen
Behandlungen unterzogen, wie beispielsweise Kugelmahlen, Wärmebehandlung
sowie einer Kombination aus Kugelmahlen und Wärmebehandlung, wobei die Ergebnisse in 11 gezeigt sind. Ein Kugelmahlen
von Vulcan XC-72R oder die Kombination aus Kugelmahlen/ Erwärmung resultierte
in einem Abfall der Leistungsfähigkeit
der Zelle von 40%. Eine mögliche
Erklärung
könnte
in der Verringerung des Kohlenstoffvolumens (um 60 %) und des durchschnittlichen
Porenradius (um 30%) infolge des Kugelmahlens sein, was zu Stofftransportbeschränkungen
geführt
haben kann.
-
Eine weitere Kenntnis darüber, warum
eine Wärmebehandlung
die Leistungsfähigkeit
verschiedener Kohlenstoffe verschlechtert, während die Leistungsfähigkeit
von anderen erheblich verbessert wird, wurde durch Messung der wirklichen
Platinoberfläche
des an verschiedenen Kohlenstoffen dispergierten Pt-Katalysators
erhalten. 12 zeigt die
Auswirkung des Kohlenstofftyps auf die echte Platinoberfläche, wobei
Ketjen-Black und
AX-21 die höchste
Platinoberfläche
von 84 m2/gm zeigten, jedoch AX-21 die geringste
Leistungsfähigkeit
der Zelle zeigte. Dies betont erneut die Rolle der physikalisch-chemischen
Eigenschaften des Kohlenstoffes bei der Verbesserung der Verwendung
des dispergierten Platinkatalysators. Es ist von Interesse, dass
die echte Pt-Fläche
des Katalysators, der auf Ketjen-Black und Printex dispergiert ist,
infolge der Wärmebehandlung
einen Abfall von 50% hinsichtlich der Platinoberfläche zeigte.
Dies zeigt, dass ein stark hydrophober Träger nicht zu einer guten Verteilung
des Platinkatalysators führt,
da die Platinlösung
während
der Abscheidung in die Kohlenstoffporen eindringen muss. Dies erläutert, warum
das KB, AB und Vulcan im Lieferzustand im Vergleich zu ihren wärmebehandelten
Versionen eine überlegene
Leistungsfähigkeit
aufwiesen. Es wird daraus geschlossen, dass Carbon-Blacks mit einem
pH der Aufschlämmung
in dem neutralen Bereich von 6 bis 9, insbesondere in den gelieferten
Formen, und einem durchschnittlichen Porenradius von größer als
5 nm (9 und 10) am besten für die Dispergierung
des Pt- Katalysators
für Kathodenanwendungen
für PEM-Brennstoffzellen
geeignet sind. Der pH der Aufschlämmung ist ein Maß des pH
der Kohlenstoffaufschlämmung
in Wasser.
-
Der pH der Primärkohlenstoffschicht (erste
Schicht) wurde nicht variiert, da Acetylen-Black (AB) einen optimalen
pH für
einen halbhydrophoben Träger
besaß.
Ebenfalls ist es unwahrscheinlich, dass der optimale pH-Bereich für die Primärschicht
(erste Schicht) von der Haupt- oder Katalysatorschicht (zweiten
Schicht) stark verschieden ist.
-
Der optimale Porenradius für die Primärschicht
(erste Schicht) kann ähnlich
der Katalysatorschicht und braucht nicht von dieser verschieden
sein. Jedoch wird angenommen, dass das Kohlenstoffvolumen pro Masseneinheit
wichtig ist. AB besitzt die geringste Dichte und daher das höchste Volumen
pro Gramm (9). Somit
stellt AB die mechanische Blockierung von Poren in der Kohlenstofftafel
sicher, ohne dass ein Gastransport durch die Poren in der Primärschicht
merklich beeinträchtigt
wird. Aufgrund dessen ist es bevorzugt, dass diese Kohlenstoffpartikel
durch ein Volumen pro Gramm von zumindest etwa 10 cm3/gm
gekennzeichnet sind. Dies entspricht einer Dichte von etwa 0,1 gm/cm3 oder weniger für die Kohlenstoffpartikel der
Primärschicht.
-
Obwohl optional dazu Katalysatoren
auch in der Primärschicht
(ersten Schicht) enthalten sein können, ist dies nicht notwendig,
da es unwahrscheinlich ist, dass sich die Reaktionszone über die
Haupt- oder Katalysatorschicht (zweite Schicht) hinaus erstreckt.
Jedoch verbessert der Zusatz von Spurenmengen von Katalysatoren
(Platin) die Leitfähigkeit
der Matrix und erleichtert somit die Zellenleistungsfähigkeit.
Da eine äußerst geringe Beladung
von 0,02 mg/cm
2 ausreichend war, um diesen
Vorteil zu erzielen, ist eine Menge dieser Größe angemessen, und es erscheint
im Moment nicht nützlich,
die Beladung weiter zu erhöhen.
Es wird davon ausgegangen, dass ein Bereich in der Größenordnung
von 0 bis etwa 0,15 mg/cm
2 angemessen ist.
-
Zusammenfassend verbessert die vorliegende
Erfindung eine essentielle Komponente der PEM-Brennstoffzelle, die
die Membranelektrodenanordnung (MEA) umfasst, die eine Membran umfasst,
die zwischen zwei Stromkollektoren aus Kohlenstofftafeln schichtartig
angeordnet ist, die Katalysatorschichten für die Reaktionen in der Brennstoffzelle
tragen. Die hier beschriebenen Merkmale verbessern eine Entfernung von
Produktwasser und steigern die Rate des Sauerstofftransportes an
die Reaktionsstellen an der Grenzfläche zwischen Membran und Elektrode.
Dies wird durch vorsichtige Optimierung der Konstruktion und Struktur der
Luftelektrode (Kathode) erreicht: die Graphitpapierdichte und ihr
Teflongehalt, die Nafion-Beladung in der Reaktionsschicht und die
Porenverteilung sowie der pH der Aufschlämmung des Kohlenstoffträgers, der
dazu verwendet wird, die Katalysatoren zu dispergieren. Diese Merkmale
verbes- , sern die Katalysatordispergierung, den Gastransport zu
der Katalysatorschicht sowie das Wassermanagement.
-
Nafion in der Elektrode wirkt als
ein Bindemittel wie auch als der protonenleitende Elektrolyt in
der Katalysatorschicht. Kohlenstoffträger wurden früher für Zellen,
die bei Raumtemperatur und im Bereich von atmosphärischem
Druck betrieben wurden, untersucht. Ketjen-Black an der Kathode
sowie kugelgemahlenes Vulcan XC-72R an der Anode haben sich als
die besten Carbon-Black-Träger
zur Dispergierung von Platinkatalysator und für optimales Wassermanagement
herausgestellt (U.S. Patente Nrn. 5,272,017 und 5,316,817).
-
Vor den Verbesserungen, die in den
US-Patenten Nr. 5,272,017 und 5,316,817 beschrieben sind, betraf
das Verfahren zur Herstellung der Membranelektrodenanordnung (MEA)
die Beschichtung der Membran mit mit Platin versehener Kohlenstoffaufschlämmung und
anschließend
die Anbringung einer Kohlenstofftafel als Stromkollektor an der
Membran. Dies besaß den
Nachteil, dass dies hauptsächlich
für dicke
Membrane mit hohem Äquivalentgewicht
geeignet war, wie beispielsweise Nafion 117. Das Verfahren der U.S.
Patente Nrn. 5,272,017 und 5,316,817 betrifft das direkte Auftragen
der mit Katalysator versehenen Kohlenstoffaufschlämmung auf
die Kohlenstofftafel und im Anschluss daran das Heißverpressen
der Elektroden mit einer Membran. Die vorliegende Methode verwendet
eine mehrlagige Elektrodenstruktur, die leicht zur Massenproduktion
verwendet wie auch für
einen beliebigen Typ von Protonenaustauschmembran oder Kohlenstofftafel
für die
Gasdiffusionsverstärkung
verwendet werden kann.
-
Die mehrlagige Kathodenstruktur bestand
aus einer Primärschicht
aus Carbon-Black mit sehr geringen Mengen an Pt (0,02 mg/cm2) und
einer Hauptprimärkatalysatorschicht
aus einem geeignet behandelten Carbon-Black, das mit 20 Gewichtsprozent Pt
beladen ist. Die Primärschicht
verbesserte die Beschichtbarkeit der Hauptkatalysatorschicht und
half, die Zellenleistungsfähigkeit
zu verbessern, indem die Schicht näher an der Membrangrenzfläche angeordnet
wurde. Die Leistungsfähigkeit
der Hauptkatalysatorschicht wurde mit Kohlenstoffträgern optimiert,
die eine angemessene Hydrophobie aufwiesen, um Wasser von der Elektrodenmatrix
abzustoßen,
die jedoch eine ausreichende Hydrophobie besaßen, um den Pt-Katalysator
für eine
optimierte Katalysatorverwendung zu verteilen. Die Beladung mit
Nafionpolymer in der Hauptkatalysatorschicht und Teflonpolymer in
dem Stromkollektor der Kohlenstofftafel wurden ebenfalls zur besseren
Gasverteilung und Katalysatorverwendung optimiert. Kohlenstofftafeln
mit Dichten im Bereich von 0,3 bis 0,35 g/cc und einem Teflon-Gehalt
von weniger als 5 Gewichtsprozent haben sich für den Stromkollektor als optimal
herausgestellt. Der Kathoden-Nafion-Gehalt von 30 bis 35 Gewichtsprozent
erzielte eine akzeptable Pt-Verwendung, während eine Elektrodenüberflutung
auf einem Minimum gehalten wird. Unter den verschiedenen Kohlenstoffmaterialien
mit einem breiten Spektrum von Eigenschaften, die als Kathodenkatalysatorträger bewertet
wurden, sind Kohlenstoffe mit durchschnittlichen Porenradien, die
größer als
5 nm sind, und einem pH der Aufschlämmung im neutralen Bereich
von 6 bis 9 für
Kathodenanwendung am besten geeignet.
-
Eine verbesserte Leistungsfähigkeit
der Wasserstoff/Luft-Zelle, die hier demonstriert wurde, wurde durch
verschiedene Vorbereitungs- und Zusammensetzungsparameter erreicht,
wie beispielsweise den Nafion-Gehalt der Kathode, den Teflongehalt
sowie die Dichte der Kohlenstofftafel als auch die physikalisch – chemischen
Eigenschaften von Kohlenstoffträgern,
die zur Verteilung des Katalysators verwendet wurden, wobei all
diese optimiert wurden. Die Wirksamkeit wurde durch die hier beschriebenen
Untersuchungsergebnisse deutlich gezeigt.
-
Während
diese Erfindung in Bezug auf bestimmte Ausführungsformen beschrieben worden
ist, ist es nicht beabsichtigt, dass diese auf die obige Beschreibung
begrenzt, sondern vielmehr nur durch den in den folgenden Ansprüchen angegebenen
Schutzumfang beschränkt
ist.
-
Die Ausführungsformen der Erfindung,
in denen ein exklusives geistiges Eigentum oder Privileg beansprucht
ist, sind in den folgenden Ansprüchen
definiert.