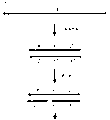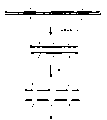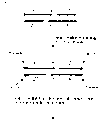CN1388831A - 基因的检测方法 - Google Patents
基因的检测方法 Download PDFInfo
- Publication number
- CN1388831A CN1388831A CN01802491A CN01802491A CN1388831A CN 1388831 A CN1388831 A CN 1388831A CN 01802491 A CN01802491 A CN 01802491A CN 01802491 A CN01802491 A CN 01802491A CN 1388831 A CN1388831 A CN 1388831A
- Authority
- CN
- China
- Prior art keywords
- probe
- target gene
- cut
- zone
- ligation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
- C12Q1/682—Signal amplification
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Immunology (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Analytical Chemistry (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Abstract
本发明提供一种基因的检测方法,通过利用PALSAR法,不需要捕获连接的低聚核苷酸和洗涤多余的低聚核苷酸的操作,能够通过聚合物的形成检测基因。使用复数对由n(n≥3)个互补碱基序列区域构成的成对探针,预先切断上述成对探针与目标基因互补区域的单侧或两侧的一个部位或数个部位,通过控制温度,使之进行杂交反应、连接反应和解离反应,使上述切断的探针连接,形成完全探针,使用探针聚合物的制备方法形成双链聚合物,检测出上述目标基因。
Description
技术领域
本发明涉及采用探针聚合物制备方法检测基因的方法,所述探针聚合物的制备方法是使用复数对由n(n≥3)个互补碱基序列区域构成的成对探针(以下,有时称为HoneyComb Probe:HCP),使之杂交达到相互交错的状态,从而形成双链聚合物的方法(USP6261846、特开2000-201687号以及特愿2000-98797号,以下,称为PALSAR(Probe alternationlink self-assembly reaction)法)。
背景技术
已开发出通过进行杂交使之与目标基因或单核苷酸多态性互补的二个低聚核苷酸邻接从而连接二个低聚核苷酸的连接反应,检测目标基因或单核苷酸多态性的方法。
上述连接反应大致分为使用连接酶(Ligase)的方法和不使用酶而使用特殊低聚核苷酸的方法。
使用连接酶(Ligase)的方法中包括一般基因操作中使用的T4DNA连接酶或LCR(Ligase chain reaction)法中使用的耐热性DNA连接酶(Thermus thermophilus DNA ligase)(USP5792607和USP5494810)。另外,不使用酶的自动连接反应(Autoligation reaction)法(Yanzheng Xu andEric T.Kool.(1999)Nucleic Acids Res.,27.875-881),是预先使硫代磷酸(phosphorothioate)结合在相邻的二个低聚核苷酸的3’末端,并使碘代胸腺嘧啶核甙(iodo thymidine)结合在5’末端,进行5’-桥连硫代磷酸连接(5’-bridging phosphorothioate linkage),从而连接二个低聚核苷酸的方法。
如上所述,连接二个低聚核苷酸的方法有各种各样的方法,但用于检测连接后的低聚核苷酸的方法如LCRTM所代表的那样,通过特殊的装置仅仅捕获连接的低聚核苷酸,如果不通过采用洗涤的B/F分离操作除去多余的低聚核苷酸,则不能进行基因检测。
另外,通过分离猝灭剂使能够通过猝灭剂抑制荧光的荧光物质发出荧光的方法中,包括TaqMan PCR法和转化法,Taqman PCR法是通过利用Taq DNA聚合酶的5’核酸酶活性,切断结合有荧光物质的探针,分离猝灭剂使之发出荧光的方法,另外,转化法是通过使用具有识别DNA的结构进行切割的特殊内切核酸酶活性的酶(cleavase),切断结合有荧光物质的探针,分离猝灭剂使之发出荧光的方法,两种方法均为需要特殊酶的方法。
另一方面,本发明人发明了不使用酶或分支DNA但能够有效进行探针聚合的划时代的方法,即PALSAR法,并已经提出申请(参见USP6261846、特开2000-201687号以及特愿2000-98797号)。
发明内容
鉴于上述已有技术的现状,本发明人为了创造出采用上述PALSAR法的新型基因检测方法,反复悉心研究后发现如下述试验例1所示,不切断图25所示PALSAR法中使用的成对探针与目标基因互补的区域时,如图27中箭头所示,依赖于杂交反应温度形成聚合物,但是另一方面,切断图26所示PALSAR法中使用的成对探针与目标基因互补的区域时,如图28所示在任意的杂交反应温度下均不会形成聚合物。
发现通过利用这种PALSAR法中使用的成对探针的性质,不用分离与目标基因连接的低聚核苷酸和未反应的多余的低聚核苷酸,仅在目标基因存在的场合就可以获得形成聚合物的探针,能够简单地检测出基因,从而完成了本发明。
本发明的目的在于提供一种基因的检测方法,通过利用PALSAR法,不需要捕获连接的低聚核苷酸和洗涤多余的低聚核苷酸的操作,能够通过聚合物的形成检测基因,另外通过在PALSAR法中使用的成对探针的5’末端标记荧光物质,并使猝灭剂结合在3’末端,不需要特殊的酶,采用PALSAR法形成双链聚合物时,能够根据荧光由于猝灭剂消失来检测基因。
为了解决上述课题,本发明的基因检测方法的第1种方式是一种采用通过使用复数对由n(n≥3)个互补碱基序列区域构成的成对探针,使之杂交达到相互交错的状态,从而形成双链聚合物的探针聚合物制备方法的基因检测方法,其特征在于,使上述成对的探针中任意一个探针的一个以上互补区域成为具有与目标基因的一部分互补的碱基序列的区域,预先切断上述成对探针与目标基因互补区域的单侧或两侧的一个部位或数个部位,通过控制温度,使之进行杂交反应、连接反应和解离反应,使上述切断的探针连接,形成完全探针,通过上述探针聚合物的制备方法形成双链聚合物,检测出上述目标基因。
而且,具体而言,具有与目标基因互补的区域并切断了这一部位的探针,在存在目标基因时,与目标基因杂交后,通过连接反应连接,之后通过热使双链解离。其次,尚未切断的探针与目标基因或连接的探针进行杂交后,通过连接反应进行连接,通过热使双链解离。通过控制温度,反复进行上述杂交反应→连接反应→解离反应,使探针连接,形成完全探针。连接的探针通过PALSAR法形成双链聚合物。不存在目标基因时,切断的探针不连接,切断的探针不形成聚合物。因此,根据聚合物的形成,能够检测出目标基因。
优选采用DNA连接酶、耐热性DNA连接酶或不使用酶的自动连接法进行上述连接反应。
上述目标基因可以使用单链DNA或RNA。
上述目标基因可以使用双链DNA或RNA。
优选设计成上述预选切断的探针部分与单核苷酸多态性(singlenucleotide polymorphisms:以下称为SNPs)互补。
上述方法中,最好使用控制反应温度的仪器。
优选使猝灭剂(Quencher:使荧光消失的物质)和荧光物质(Fluorophore)结合在上述使用的成对探针的单侧或两侧的末端,通过荧光的消失确认形成的双链聚合物。
附图说明
图1是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测单链目标基因的一个实例的示意图,(a)表示单链目标基因,(b)表示具有与目标基因的Y区域互补的区域的一对探针,而且(c)表示将与目标基因互补的区域切断1处后的一对探针。
图2是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测单链目标基因的一个实例的示意图,(d)表示与目标基因互补的Y区域被切断1处后的探针,(e)表示单链目标基因,(f)表示切断的探针与目标基因的杂交反应,而且(g)表示切断的探针的连接反应。
图3是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测单链目标基因的一个实例的示意图,(h)表示连接的探针,(i)表示成对的HCP的另一个探针,(j)表示复数对连接的成对探针,而且(k)表示根据PALSAR法的原理形成聚合物。
图4是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(a)表示双链目标基因,(b)表示具有与双链目标基因的Y区域和Y’区域互补的区域的一对探针,而且(c)表示将与双链目标基因互补的区域切断1处后的一对探针。
图5是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(d)表示与目标基因互补的Y区域和Y’区域被切断1处后的探针,(e)表示双链解离的目标基因,(f)表示切断的探针与解离的目标基因的杂交反应,而且(g)表示切断的探针的连接反应。
图6是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(h)表示连接的探针,(i)表示切断的探针,而且(j)表示连接的探针与切断的探针的杂交反应。
图7是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(k)表示复数对连接的成对探针,而且(l)表示根据PALSAR法的原理形成聚合物。
图8是表示通过3个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(a)表示双链目标基因,(b)表示具有与双链目标基因上的X区域和X’区域、Y区域和Y’区域、Z区域和Z’区域互补的区域的一对探针,而且(c)表示将与目标基因互补的3个区域分别切断1处(共计3处)后的一对探针。
图9是表示通过3个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(d)表示目标基因的Y区域与切断的探针的Y’区域的杂交反应,(e)表示目标基因的X区域与切断的探针的X’区域的杂交反应,而且(f)表示目标基因的Z区域与切断的探针的Z’区域的杂交反应。
图10是表示通过3个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(g)表示连接的一对探针,(h)表示切断的探针,(i)表示连接的探针的Z区域与切断的探针的Z’区域以及连接的探针的X’区域与切断的探针的X区域的杂交反应,(j)表示连接的探针的Y区域与切断的探针的Y’区域的杂交反应,以及连接的探针的Y’区域与切断的探针的Y区域的杂交反应,(k)表示连接的探针的X区域与切断的探针的X’区域的杂交反应,以及连接的探针的Z’区域与切断的探针的Z区域的杂交反应。
图11是表示通过3个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图,(l)表示复数对连接的成对探针,而且(m)表示根据PALSAR法的原理形成聚合物。
图12是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测SNPs的一个实例的示意图,(a)表示具有与包含SNPs的目标基因互补的区域(Y区域),并将这一区域切断1处后的一对探针,(b1)表示使包含SNPs的目标基因的SNPs与切断了1处的探针的连接部分完全一致(Complete match)进行杂交时的杂交反应和连接反应,而且(b2)表示包含SNPs的目标基因的SNPs与切断了1处的探针的连接部分不匹配(Mismatch)时的杂交反应和连接反应。
图13是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测SNPs的一个实例的示意图,(c)表示与连接反应无关的探针通过碱性磷酸酶脱磷酸化,(d)表示连接的探针,(e)表示一对HCP中未切断的另一个探针,而且(f)表示根据PALSAR法的原理形成聚合物。
图14是表示Sephide公司的I-CORETM(Smart CyclerTM)的原理的说明图,(a)表示反复通过侧面大致呈五角形状的容器以及侧壁冷却和加热,另外(b)表示确认有无荧光物质存在的方法。
图15是表示使用Sephide公司的I-CORETM(Smart CyclerTM)通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因时的示意图,(a)表示双链目标基因,(b)表示将具有与双链目标基因的Y区域和Y’区域互补的区域的一对探针的互补区域切断1处后的探针,而且(c)表示使用Sephide公司的I-CORETM(Smart CyclerTM)的连接反应。
图16是表示使用Sephide公司的I-CORETM(Smart CyclerTM)通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因时的示意图,(d)表示双链目标基因,(e)表示双链解离后的目标基因,(f)表示目标基因与切断的探针的杂交反应,而且(g)表示切断的探针的连接反应。
图17是表示使用Sephide公司的I-CORETM(Smart CyclerTM)通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因时的示意图,(h)表示连接的一对探针,(i)表示切断的一对探针,而且(j)表示连接的探针与切断的探针的杂交反应。
图18是表示使用Sephide公司的I-CORETM(Smart CyclerTM)通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因时的示意图,(k)表示复数对连接的成对探针,而且(l)表示根据PALSAR法的原理形成聚合物。
图19是表示使用Sephide公司的I-CORETM(Smart CyclerTM)通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因时的示意图,(m)表示根据PALSAR法的原理形成的聚合物,而且(n)表示使用Sephide公司的I-CORETM(Smart CyclerTM)通过荧光检测聚合物的方法。
图20是通过分子标记(Molecular Beacons)检测按PALSAR法形成的聚合物时(不一致)的示意图,(a)表示将PALSAR法中使用的探针与目标基因互补的区域(Y区域)切断后的一对HCP,而且(b)表示在HCP的5’末端标记荧光物质,并使猝灭剂结合在3’末端的一对切断的探针。
图21是通过分子标记检测按PALSAR法形成的聚合物时(完全一致)的示意图,(a)表示将PALSAR法中使用的探针与目标基因互补的区域(Y区域)切断后的一对HCP,而且(b)表示在HCP的5’末端标记荧光物质,并使猝灭剂结合在3’末端的一对切断的探针。
图22是通过分子标记检测按PALSAR法形成的聚合物时(完全一致)的示意图,(c)表示通过连接反应连接的一对探针,而且(d)表示根据PALSAR法的原理形成的聚合物引起的荧光消失。
图23是表示实施例1、比较例1、比较例2、比较例4和比较例5的结果的照片,(a)表示PAGE的结果,而且(b)表示琼脂糖凝胶电泳法的结果。
图24是表示实施例2~实施例4以及比较例3~比较例5的结果的照片,(a)表示PAGE的结果,而且(b)表示琼脂糖凝胶电泳法的结果。
图25是表示试验例1中所使用的未将PALSAR法中使用的成对探针与目标基因互补的区域切断时的DNA探针的示意图。
图26是表示试验例1中所使用的将PALSAR法中使用的成对探针与目标基因互补的区域切断时的DNA探针的示意图。
图27是表示未将PALSAR法中使用的成对探针与目标基因互补的区域切断时的试验例1的结果的琼脂糖凝胶电泳法照片。
图28是表示将PALSAR法中使用的成对探针与目标基因互补的区域切断时的试验例1的结果的琼脂糖凝胶电泳法照片。
具体实施方式
以下结合附图说明本发明的实施方式,但是这些实施方式是示例性的,当然只要不脱离本发明的技术思想,能够进行各种变形。
另外,以下所示的实施方式中使用的连接反应并不限定于使用连接酶(Ligase)的方法和不使用酶而使用特殊低聚核苷酸的方法中的任意一种。
图1~图3是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测单链目标基因的一个实例的示意图。
如图1(a)(b)所示,由单链目标基因制作具有与目标基因互补的区域(Y’区域)的HCP及其对的HCP〔图1(b)〕,如图1(c)所示,预先将具有与目标基因的Y区域互补的区域的探针〔图1(b)〕的Y’区域的一处切断。切断的探针〔图2(d)〕如图2(f)所示,与目标基因杂交后,如图2(g)所示,通过连接反应连接。
其次,该连接的探针〔图3(h)〕和切断的探针〔图2(d)〕通过将温度控制在94℃~25℃的范围内反复进行解离、杂交和连接反应后〔图2(f)、图2(g)、图3(h)〕,连接的探针〔图3(h)〕与另外加入的对的另一个HCP〔图3(i)(j)〕反应,如图3(k)所示,根据PALSAR法的原理形成聚合物。
这里形成的聚合物能够通过一般的琼脂糖凝胶电泳法或下述检测方法(图20~图22)简单地确认。
另外,也可以使用同时在互补区域将成对探针切断的探针。
图4~图7是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图。
如图4(a)(b)所示,由双链目标基因制作具有与目标基因互补的区域的一对HCP,如图4(c)所示,预先将具有与图4(a)所示双链目标基因上的Y区域和Y’区域互补的区域的探针〔图4(b)〕的Y’区域和Y区域的一处切断。切断的探针〔图5(d)〕如图5(f)所示与双链解离的目标基因〔图5(e)〕杂交后,如图5(g)所示,通过连接反应连接。其次,该连接的探针〔图6(h)〕和图6(i)的切断的探针杂交后,如图6(j)所示,通过连接反应连接。
连接的的探针〔图6(h)〕和切断的探针〔图5(d)〕通过将温度控制在94℃~25℃的范围内反复进行解离、杂交和连接反应后〔图6(j)、图7(k)〕,如图7(l)所示,根据PALSAR法的原理形成聚合物。
这里形成的聚合物能够通过一般的琼脂糖凝胶电泳法或下述检测方法(图20~图22)简单地确认。
图8~图11是表示通过3个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因的一个实例的示意图。
如图8(a)(b)所示,由双链目标基因制作具有与目标基因3处互补的区域的一对HCP,如图8(c)所示,预先分别将具有与图8(a)所示双链目标基因上的X区域和X’区域、Y区域和Y’区域、Z区域和Z’区域互补的区域的探针〔图8(b)〕的各区域的一处(共计3处)切断。切断的探针〔图8(c)〕如图9(d)(e)(f)所示,与解离的目标基因杂交后,通过连接反应连接。
其次,该连接的探针〔图10(g)〕和预先将3处切断的探针〔图10(h)〕通过将温度控制在94℃~25℃的范围内反复进行解离、杂交和连接反应后〔图10(i)(j)(k)、图11(1)〕,如图11(m)所示,根据PALSAR法的原理形成聚合物。
这里形成的聚合物能够通过一般的琼脂糖凝胶电泳法或下述检测方法(图20~图22)简单地确认。
图12~图13是表示通过1个部位被切断的PALSAR法中使用的成对探针的连接反应检测SNPs的一个实例的示意图。
图12(a)表示将PALSAR法中使用的一对探针中与包含SNPs的目标基因互补的区域(Y)切断1处后的探针。
如图12(b1)所示,使包含SNPs的目标基因的SNPs与切断了1处的探针的连接部分完全一致(Complete match)进行杂交时,切断的探针通过连接反应连接,而包含SNPs的目标基因的SNPs与切断了1处的探针的连接部分不匹配(Mismatch)时,即使进行杂交反应,也不能进行连接反应,因此探针仍然断开〔图12(b2)〕。
之后,与连接反应无关的探针如图13(c)所示通过碱性磷酸酶进行脱磷酸化,能够形成对连接反应不能应答的形态。
连接的探针〔图13(d)〕与另外加入的对的另一个HCP〔图13(e)〕反应,如图13(f)所示,根据PALSAR法的原理形成聚合物。
这里形成的聚合物能够通过一般的琼脂糖凝胶电泳法或下述检测方法(图20~图22)简单地确认。
图14是表示本发明方法中优选使用的控制反应温度的仪器的说明图。该图表示Sephide公司的I-CORETM(Smart CyclerTM),该反应温度控制仪器具有侧面大致呈五角形状的容器主体,该容器主体具备具有高热传导性的一对侧壁以及互相倾斜接合的倾斜底板。因此,如图14(a)所示,能够通过侧壁反复进行冷却和加热。另外,如图14(b)所示,为了确认有无荧光物质的存在,能够通过由一侧的倾斜底板投射激发光,由另一侧的倾斜底板观察发光状态进行。
图15~图19是表示使用Sephide公司的I-CORETM(Smart CyclerTM)通过上述1个部位被切断的PALSAR法中使用的成对探针的连接反应检测双链目标基因时的示意图。
向图15(c)的反应池中加入目标基因〔图15(a)〕和1处被切断的PALSAR法中使用的成对探针〔图15(b)〕。
只有在能够控制温度的反应池中存在检测的目标基因〔图16(d)〕时,解离的目标基因〔图16(e)〕和切断的聚合物发生杂交反应〔图16(f)〕,探针通过连接反应连接〔图16(g)〕。连接的探针〔图17(h)〕和切断的探针〔图17(i)〕通过将温度控制在94℃~25℃的范围内反复进行解离、杂交和连接反应后〔图17(j)、图18(k)〕,如图18(l)所示,根据PALSAR法的原理形成聚合物。
形成的聚合物〔图19(m)〕可以通过添加插入到低聚核苷酸的双链中发出荧光的色素,使用Sephide公司的I-CORETM(Smart CyclerTM),观察荧光的发光状态进行检测〔图19(n)〕。
这里形成的聚合物能够通过一般的琼脂糖凝胶电泳法或下述检测方法(图20~图22)简单地确认。
图20~图22是通过分子标记(Molecular Beacons)检测按PALSAR法形成的聚合物时的示意图。
它是将图20(a)和图21(a)所示的PALSAR法中使用的探针与目标基因互补的区域(Y区域和Y’区域)切断,在其HCP的5’末端标记荧光物质,并使猝灭剂结合在3’末端〔图20(b)、图21(b)〕,从而与目标基因互补的区域(Y区域和Y’区域)不匹配时〔图20(b)〕,不能通过PALSAR法形成聚合物,保持发出荧光的状态,而与目标基因互补的区域(Y区域和Y’区域)完全一致时〔图21(b)〕,能够通过连接反应获得HCP〔图22(c)〕,如图22(d)所示,通过PALSAR法形成聚合物,而且5’末端和3’末端邻接,从而根据荧光由于猝灭剂消失能够检测基因的方法。另外,也可以采用用增强子代替猝灭剂的方法。
另外,图中,前端锐角部分表示3’末端,起始端黑圆圈表示5’末端。实施例
以下结合本发明的实施例进行说明,但是本发明当然并不限于这些实施例。
实施例1~4和比较例1~5中使用的DNA探针和目标基因a)探针1(INT-1):(5’-X’-
Y’-Z’-3’)5’-ACGCAGAAAGCGTCTAGC-
CGCTCACAGTTAA CGTGAGATTTCAC-GTACTGCCTGATAGGGTG-3’b)探针2(INT-2):(5’-X-
Y-Z-3’)5’-GCTAGACGCTTTCTGCGT-
GTGAAATCTCACG TTAACTGTGAGCG-CACCCTATCAGGCAGTAC-3’c)探针3(INT-1-A):(5’-X’-
Y’(切断)-3’)5’-ACGCAGAAAGCGTCTAGC-
CGCTCACAGTTAA -3’d)探针4(INT-1-B):(5’-
Y’(切断)-Z’-3’)5’(磷酸化)-
CGTGAGATTTCAC-GTACTGCCTGATAGGGTG-3’e)探针5(INT-2-C):(5’-X-
Y(切断)-3’)5’-GCTAGACGCTTTCTGCGT-
GTGAAATCTCACG -3’f)探针6(INT-2-D):(5’-
Y(切断)-Z-3’)5’(磷酸化)-
TTAACTGTGAGCG-CACCCTATCAGGCAGTAC-3’g)目标基因(INT-①):(5’--
Y--3’)5’-GGTTTGTCGCGTTGTTC-
GTGAAATCTCACG TTAACT GTGAGCG-TGCGGGCGATACGGG-3’h)目标基因(INT-①S1):(5’--
Y--3’)5’-GGTTTGTCGCGTTGTTC-
GTGAAATCTCACG C TTAACT GTGAGCG-TGCGGGCGATACGGG-3’i)目标基因(INT-①S2):(5’--
Y--3’)5’-GGTTTGTCGCGTTGTTC-
GTGAAATCTCACG G TTAACTGTGAGCG-TGCGGGCGATACGGG-3’j)目标基因(INT-①R):(5’--
Y’--3’)5’-CCCGTATCGCCCGCA-
CGCTCACAGTTAAG CCGTGAGATTTCAC-GAACAACGCGACAAACC-3’
(实施例1、比较例1和比较例2)HCP中的连接反应(目标基因:双链)
1、目的
尝试通过1处被切断的HCP的连接反应检测双链目标基因。
2、材料
1)关于目标基因,制作源于Mycobacterium intracellulare 16s rRNA基因的60个碱基的合成低聚核苷酸(以下称为INT-①)以及与目标基因INT-①互补序列的合成低聚核苷酸(以下称为INT-①R),使两者形成双链,进行以下的实验。
2)制作由具有与目标基因INT-①的Y区域互补的区域的探针1(以下称为INT-1)以及各区域与该探针1互补的探针2(以下称为INT-2)构成的成对HCP。并且准备分别将其1处切断后得到的探针(以下分别称为INT-1-A、INT-1-B、INT-2-C、INT-2-D)。
3)作为耐热性DNA连接酶,使用将Tsc DNA ligase,thermostable(Roche Molecular Biochemicals)添加到培养缓冲液(Incubation buffer)中的物质。
4)作为缓冲液使用20×SSC(3M-NaCl,0.3M-C6H5O7Na3·2H2O,pH7.0)。
3、方法
a)反应液的配制
将分别配制成100pmol/μL的INT-1-A、INT-1-B、INT-2-C以及INT-2-D 0.5μL分别加入0.2mL的灭菌后的微管中,加入连接酶1μL、培养缓冲液2μL,加入配制成100pmol/μL的由INT-①和INT-①R构成双链的目标基因1μL,通过DW2制成20μL的反应液(实施例1)。另外,作为对照,制作相对于上述反应液未添加目标基因的反应液(比较例1),以及连接酶和目标基因均未添加的反应液(比较例2)。
b)连接反应
之后,使用热循环装置(Parkinermar公司制),使上述各种反应液在94℃下反应2分钟,然后循环进行〔94℃/30秒→50℃/2分钟→55℃/5分钟〕的反应30次,使之分别进行连接反应。之后,通过99℃/10分钟,进行用于使连接酶惰化的反应。
c)通过聚丙烯酰胺凝胶电泳(PAGE)确认连接
在连接反应之后,对各反应液进行PAGE。使用反应液5μL,用16%PAGE(30% Acrylamide/Bis Solution 29∶1,10% Ammonium Persulfate,TEMED,Bio-Rad Laboratories,10%TBE,H2O)在90分钟、130V的条件下进行电泳。作为对照使用INT-①、INT-①R、以及INT-①和INT-①R构成的双链目标基因。作为分子尺寸标记使用10bpDNA梯(DNALadder,GIBCO BRL公司制)。电泳90分钟后,用溴化乙锭(EtBr Solution,株式会社NIPPON GEN制)将凝胶染色。
d)聚合物形成反应
分别向0.2mL微管中的上述连接反应后的反应液10μL中加入20×SSC 10μL,使用热循环装置(Parkinermar公司制),使之在66℃反应16小时。
e)通过琼脂糖凝胶电泳法确认聚合物
对于聚合物形成反应后的反应液8μL,用2%Nusieve 3∶1琼脂糖凝胶(Bio Whittaker Molecular Applications公司制)在100V电泳30分钟。作为分子尺寸标记使用1kbDNA延伸梯(DNA Extension Ladder,GIBCOBRL公司制)。琼脂糖凝胶电泳后,用溴化乙锭将凝胶染色。
4、结果
结果如图23(a)和(b)所示。根据图23(a)的用于确认连接的PAGE的结果,添加目标基因时(实施例1、泳道1)检测出对照(比较例2、泳道2)中未见到的用箭头表示的较高位置的条带。认为该条带是连接反应的结果得到的已连接探针的条带。另外,在图中没有显示,比较例1也得到了与比较例2同样的结果。
如图23(b)所示,通过琼脂糖凝胶电泳法确认聚合物形成时,仅在添加了目标基因的场合(实施例1、泳道1)中能够观察到聚合物的形成,比较例1(泳道2)和比较例2(泳道3)中观察不到聚合物。上述内容表明,切断的HCP通过双链目标基因连接,连接的HCP形成聚合物,从而能够检测出双链目标基因。
(实施例2~4以及比较例3)通过HCP的连接反应检测SNPs
1、目的
讨论通过1处被切断的HCP的连接反应是否能够检测单链目标基因和SNPs。
2、材料
除实施例1中使用的探针、连接酶、连接缓冲液、缓冲液以及目标基因INT-①之外,重新制作INT-①的Y区域仅1个碱基不同的目标基因INT-①S1(与切断HCP的Y区域5’末端互补的部分的1个碱基不同)和INT-①S2(与切断HCP的Y区域3’末端互补的部分的1个碱基不同)。
3、方法
a)反应液的配制
将分别配制成100pmol/μL的INT-1-A、INT-1-B、INT-2-C以及INT-2-D 0.5μL分别加入0.2mL的灭菌后的微管中,加入连接酶1μL、培养缓冲液2μL,加入配制成100pmol/μL的目标基因0.5μL,通过DW2分别制成20μL的反应液。作为目标基因,在实施例2中选择INT-①,在实施例3中选择INT-①S1,在实施例4中选择INT-①S2。另外,作为对照,制作相对于上述反应液未添加目标基因(INT-①、INT-①S1和INT-①S2)的反应液(比较例3)。
b)连接反应
之后,使用热循环装置(Parkinermar公司制),对于上述各种反应液,循环进行〔94℃/30秒→50℃/90秒→55℃/3分钟〕的反应30次,使之分别进行连接反应。之后,通过99℃/10分钟,进行用于使连接酶惰化的反应。
c)通过聚丙烯酰胺凝胶电泳(PAGE)的确认
采用与实施例1同样的步骤和条件,对于各反应液通过PAGE进行确认。作为对照,使用INT-①、INT-①S1和INT-①S2。作为分子尺寸标记,除10bpDNA梯以外,还使用50bpDNA梯(DNA Ladder,GIBCOBRL公司制)。
d)聚合物形成反应
采用与实施例1同样的步骤和条件,对上述连接反应后的反应液进行聚合物形成反应。
e)通过琼脂糖凝胶电泳法确认聚合物
采用与实施例1同样的步骤和条件,对于聚合物形成反应后的反应液进行琼脂糖凝胶电泳。
4、结果
结果如图24(a)和(b)所示。根据图24(a)的用于确认连接的PAGE的结果,添加了INT-①的实例(实施例2、泳道1)中,由于目标基因和切断探针的Y区域的序列完全匹配,因此进行连接反应,在高于约350bp的位置可见用箭头表示的浓条带。与此相对,添加了SNPs即INT-①S1(实施例3、泳道2)和INT-①S2(实施例4、泳道3)的实例中,由于目标基因和切断探针的Y区域的序列有1个碱基不同(不匹配),因此不发生连接反应,确认没有泳道1中看见的条带。另一方面,仅有连接酶而未添加目标基因的泳道3(比较例3)中,仅可以确认切断的4根探针连结成环状得到的浓条带。
如图24(b)所示,通过琼脂糖凝胶电泳法确认聚合物形成时,也只有添加了目标基因和切断探针的Y区域的序列完全匹配的INT-①的实例(实施例2、泳道1)形成了聚合物,实施例3(泳道2)和实施例4(泳道3)没有观察到聚合物。另外,图中没有显示,比较例3也与实施例3和4同样没有观察到聚合物。以上内容表明,切断的HCP通过序列完全匹配的单链目标基因连接,连接的HCP形成聚合物,从而能够检测出单链目标基因。而且,SNPs的场合,切断的HCP不能连接,也不能形成聚合物,因此能够通过1处被切断的HCP的连接反应检测出SNPs。
(比较例4和比较例5)
1、目的
比较切断HCP的场合和不切断HCP的场合下通过PALSAR法形成聚合物的反应。
2、材料
1)作为比较例4的探针,使用INT-1和INT-2,作为比较例5的探针,使用INT-1-A、INT-1-B、INT-2-C和INT-2-D。
2)作为缓冲液使用20×SSC(3M-NaCl,0.3M-C6H5O7Na3·2H2O,pH7.0)。
3、方法
a)反应液的配制
分别在0.2mL的灭菌后的微管中加入20×SSC 20μL、分别配制成100pmol/μL的探针0.5μL,通过DW2分别制成20μL的反应液。作为探针,在比较例4中选择INT-1和INT-2,在比较例5中选择INT-1-A、INT-1-B、INT-2-C和INT-2-D。
b)聚合物形成反应
使用热循环装置(Parkinermar公司制),使各反应液在94℃下反应30秒后,在66反应16小时。
c)通过琼脂糖凝胶电泳法确认聚合物
采用与实施例1同样的步骤和条件,对反应后的反应液进行琼脂糖凝胶电泳。
4、结果
如图23(b)和图24(b)所示,使用未切断的探针的比较例4中,观察到聚合物的形成,使用切断的探针的比较例5中,没有观察到聚合物的形成。
(试验例1)通过PALSAR法使用HCP的形成聚合物的反应
1、目的
比较在将PALSAR法中使用的成对探针切断1处的场合以及未切断的场合温度变化时的聚合物的形成反应。
2、材料
1)聚合时使用以下的成对HCP(探针7、探针8)以及将探针7切断1处得到的探针,即探针9、探针10。a)探针7(HCP-1)5’-GAATAAGTCATAGCTCATA-
AAGGACTGG TCGCTCGAC-ATCGTCCTAGGGAGATTCG-3’b)探针8(HCP-2)5’-TATGAGCTATGACTTATTC-GTCGAGCGACCAGTCCTT-CGAATCTCCCTAGGACGAT-3’c)探针9(HCP-1-1)5’-GAATAAGTCATAGCTCATA-
AAGGACTGG-3’d)探针10(HCP-1-2)5’(磷酸化)-
TCGCTCGAC-ATCGTCCTAGGGAGATTCG-3’
2)作为缓冲液使用20×SSC(3M-NaCl,0.3M-C6H5O7Na3·2H2O,pH7.0)。
3、方法
分别向0.2mL的灭菌后的微管中加入配制成1013拷贝/μL的探针7和探针8,或者探针9、探针10和探针85μL,加入40μL的20×SSC,加盖后,在94℃下煮沸30秒,在52℃、54℃、56℃、58℃、60℃、62℃、64℃、66℃、68℃、70℃下分别加热30分钟。
加热后,使用0.5%的琼脂糖凝胶进行电泳,通过溴化乙锭染色,确认聚合的效果。
4、结果
图27和图28用照片表示使用0.5%的琼脂糖凝胶进行100V、30分钟的电泳得到的试验例1的结果。
图27是表示未将PALSAR法中使用的成对探针切断时的结果的照片。如图27中箭头所示,未切断的HCP依赖于杂交温度形成双链聚合物。
图28是表示将PALSAR法中使用的成对探针切断1处时的结果的照片。如图28所示,在任何杂交温度下均不形成聚合物。
工业实用性
如上所述,按照本发明的基因检测方法,通过利用PALSAR法,不需要捕获连接的低聚核苷酸和洗涤多余的低聚核苷酸的操作,能够通过聚合物的形成检测基因,另外通过在PALSAR法中使用的成对探针的5’末端标记荧光物质,并使猝灭剂结合在3’末端,从而不需要特殊的酶,采用PALSAR法形成双链聚合物时,能够根据荧光由于猝灭剂消失来检测基因,产生了显著的效果。
序列表<110>Sanko Junyaku Co.,Ltd.<120>Gene detecting method<130>76014-PCT-CN<140>PCT/JP01/07020<141>2001-08-14<150>JP 2000-261687<151>2000-08-30<160>14<210>1<211>66<212>DNA<213>人工序列<220><223>人工序列的描述:探针1<400>1acgcagaaag cgtctagccg ctcacagtta agccgtgaga tttcacgtac tgcctgatag 60ggtg 64<210>2<211>64<212>DNA<213>人工序列<220><223>人工序列的描述:探针2<400>2gctagacgct ttctgcgtgt gaaatctcac ggcttaactg tgagcgcacc ctatcaggca 60gtac 64<210>3<211>32<212>DNA<213>人工序列<220><223>人工序列的描述:探针3<400>3acgcagaaag cgtctagccg ctcacagtta ag 32<210>4<211>32<212>DNA<213>人工序列<220><221>misc feature<222>(1)<223>连接在5′末端的磷酸<220><223>人工序列的描述:探针4<400>4ccgtgagatt tcacgtactg cctgataggg tg 32<210>5<211>32<212>DNA<213>人工序列<220><223>人工序列的描述:探针5<400>5gctagacgct ttctgcgtgt gaaatctcac gg 32<210>6<211>32<212>DNA<213>人工序列<220><221>misc feature<222>(1)<223>连接在5′末端的磷酸<220><223>人工序列的描述:探针6<400>6cttaactgtg agcgcaccct atcaggcagt ac 32<210>7<211>60<212>DNA<213>人工序列<220><223>人工序列的描述:目标基因-1<400>7ggtttgtcgc gttgttcgtg aaatctcacg gcttaactgt gagcgtgcgg gcgatacggg 60<210>8<211>60<212>DNA<213>人工序列<220><223>人工序列的描述:目标基因-S1<400>8ggtttgtcgc gttgttcgtg aaatctcacg tcttaactgt gagcgtgcgg gcgatacggg 60<210>9<211>60<212>DNA<213>人工序列<220><223>人工序列的描述:目标基因-S2<400>9ggtttgtcgc gttgttcgtg aaatctcacg ggttaactgt gagcgtgcgg gcgatacggg 60<210>10<211>54<212>DNA<213>人工序列<220><223>人工序列的描述:目标基因-1R<400>10cccgtatcgc ccgcacgctc acagttaag ccgtgagattt cacgaacaac gcgacaaacc 60<210>11<211>54<212>DNA<213>人工序列<220><223>人工序列的描述:探针7<400>11gaataagtca tagctcataa aggactggtc gctcgacatc gtcctaggga gattcg 56<210>12<211>56<212>DNA<213>人工序列<220><223>人工序列的描述:探针8<400>12tatgagctat gacttattcg tcgagcgacc agtccttcga atctccctag gacgat 56<210>13<211>28<212>DNA<213>人工序列<220><223>人工序列的描述:探针9<400>13gaataagtca tagctcataa aggactgg 28<210>14<211>28<212>DNA<213>人工序列<220><221>misc feature<222>(1)<223>连接在5′末端的磷酸<220><223>人工序列的描述:探针10<400>14tcgctcgaca tcgtcctagg gagattcg 28
Claims (7)
1、一种基因检测方法,它是采用通过使用复数对由n(n≥3)个互补碱基序列区域构成的成对探针,使之杂交达到相互交错的状态,从而形成双链聚合物的探针聚合物制备方法的基因检测方法,其特征在于,使上述成对的探针中任意一个探针的一个以上的互补区域成为具有与目标基因的一部分互补的碱基序列的区域,预先切断上述成对探针与目标基因互补区域的单侧或两侧的一个部位或数个部位,通过控制温度,使之进行杂交反应、连接反应和解离反应,使上述切断的探针连接,形成完全探针,通过上述探针聚合物的制备方法形成双链聚合物,检测出上述目标基因。
2、如权利要求1所述的方法,其特征在于,采用DNA连接酶、耐热性DNA连接酶或不使用酶的自动连接法进行上述连接反应。
3、如权利要求1或2所述的方法,其特征在于,上述目标基因使用单链DNA或RNA。
4、如权利要求1或2所述的方法,其特征在于,上述目标基因使用双链DNA或RNA。
5、如权利要求1~4中任意一项所述的方法,其特征在于,设计成上述预选切断的探针部分与SNPs互补。
6、如权利要求1~5中任意一项所述的方法,其特征在于,使用控制反应温度的仪器。
7、如权利要求1~6中任意一项所述的方法,其特征在于,使猝灭剂和荧光物质结合在上述使用的成对探针的单侧或两侧的末端,通过荧光的消失确认形成的双链聚合物。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2000261687 | 2000-08-30 | ||
| JP261687/00 | 2000-08-30 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1388831A true CN1388831A (zh) | 2003-01-01 |
Family
ID=18749488
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN01802491A Pending CN1388831A (zh) | 2000-08-30 | 2001-08-14 | 基因的检测方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20030175689A1 (zh) |
| EP (1) | EP1229131A1 (zh) |
| KR (1) | KR20020065471A (zh) |
| CN (1) | CN1388831A (zh) |
| AU (1) | AU7873001A (zh) |
| CA (1) | CA2389310A1 (zh) |
| WO (1) | WO2002018642A1 (zh) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7632639B2 (en) | 2003-02-21 | 2009-12-15 | Eisai R&D Management Co., Ltd. | Signal amplification method for detecting mutated gene |
| CN102703584A (zh) * | 2012-04-20 | 2012-10-03 | 中国人民解放军第四军医大学 | 自组装聚合分支dna探针的制备方法 |
| CN102046788B (zh) * | 2008-05-28 | 2013-07-10 | 和光纯药工业株式会社 | 胞内分枝杆菌检测用引物和探针、以及使用该引物和探针检测胞内分枝杆菌的方法 |
| CN104271768A (zh) * | 2012-02-14 | 2015-01-07 | 约翰霍普金斯大学 | miRNA分析方法 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20040041529A (ko) * | 2001-09-28 | 2004-05-17 | 산코 준야쿠 가부시키가이샤 | Dna 칩의 시그널 증폭방법 |
| AU2004212083B2 (en) * | 2003-02-14 | 2009-01-29 | Eisai R&D Management Co., Ltd. | Signal amplification method for detecting expressed gene |
| WO2005106031A1 (ja) * | 2004-04-28 | 2005-11-10 | Eisai R & D Management Co., Ltd. | ハイブリダイゼーション方法 |
| WO2007037282A1 (ja) * | 2005-09-27 | 2007-04-05 | Eisai R & D Management Co., Ltd. | 微小粒子に自己集合体を形成させる方法及び標的分析物の検出方法 |
| EP1997908A4 (en) | 2006-03-15 | 2010-09-29 | Eisai R&D Man Co Ltd | METHOD FOR FORMING A SIGNAL CONDUCTOR POLYMER |
| KR20100085923A (ko) * | 2007-10-24 | 2010-07-29 | 에자이 알앤드디 매니지먼트 가부시키가이샤 | 핵산프로브 및 프로브폴리머의 형성방법 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| HU218095B (hu) * | 1990-05-01 | 2000-05-28 | Amgen Inc. | Eljárás átvitt szennyeződések csökkentésére, amplifikációs eljárásokban |
| JPH08505531A (ja) * | 1993-01-15 | 1996-06-18 | ザ パブリック ヘルス リサーチ インスティチュート オブ ザ シティー オブ ニューヨーク インク | Rnaバイナリ・プローブとリボザイムリガーゼを用いたrna検定法 |
| DE69531542T2 (de) * | 1994-02-07 | 2004-06-24 | Beckman Coulter, Inc., Fullerton | Ligase/polymerase-vermittelte analyse genetischer elemente von einzelnukleotid-polymorphismen und ihre verwendung in der genetischen analyse |
| US6287766B1 (en) * | 1997-10-28 | 2001-09-11 | The Regents Of The University Of California | DNA polymorphism identity determination using flow cytometry |
| US6277578B1 (en) * | 1998-03-13 | 2001-08-21 | Promega Corporation | Deploymerization method for nucleic acid detection of an amplified nucleic acid target |
| JP3267576B2 (ja) * | 1998-11-09 | 2002-03-18 | 三光純薬株式会社 | プローブ高分子の形成方法 |
| DK1188841T3 (da) * | 2000-03-31 | 2009-04-20 | Sanko Junyaku Kk | Probe til fremstilling af en polymerprobe, fremgangsmåde til fremstilling af en polymerprobe samt anvendelse af polymerproben |
| EP1304386B1 (en) * | 2000-10-11 | 2006-10-04 | Sanko Junyaku Co., Ltd. | Method of constructing self-assembly probes and method of detecting the same |
-
2001
- 2001-08-14 US US10/111,817 patent/US20030175689A1/en not_active Abandoned
- 2001-08-14 KR KR1020027002719A patent/KR20020065471A/ko not_active Application Discontinuation
- 2001-08-14 EP EP01956887A patent/EP1229131A1/en not_active Withdrawn
- 2001-08-14 AU AU78730/01A patent/AU7873001A/en not_active Abandoned
- 2001-08-14 WO PCT/JP2001/007020 patent/WO2002018642A1/ja not_active Application Discontinuation
- 2001-08-14 CN CN01802491A patent/CN1388831A/zh active Pending
- 2001-08-14 CA CA002389310A patent/CA2389310A1/en not_active Abandoned
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7632639B2 (en) | 2003-02-21 | 2009-12-15 | Eisai R&D Management Co., Ltd. | Signal amplification method for detecting mutated gene |
| CN102046788B (zh) * | 2008-05-28 | 2013-07-10 | 和光纯药工业株式会社 | 胞内分枝杆菌检测用引物和探针、以及使用该引物和探针检测胞内分枝杆菌的方法 |
| CN104271768A (zh) * | 2012-02-14 | 2015-01-07 | 约翰霍普金斯大学 | miRNA分析方法 |
| CN102703584A (zh) * | 2012-04-20 | 2012-10-03 | 中国人民解放军第四军医大学 | 自组装聚合分支dna探针的制备方法 |
| CN102703584B (zh) * | 2012-04-20 | 2013-08-21 | 中国人民解放军第四军医大学 | 自组装聚合分支dna探针的制备方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20020065471A (ko) | 2002-08-13 |
| US20030175689A1 (en) | 2003-09-18 |
| WO2002018642A1 (en) | 2002-03-07 |
| AU7873001A (en) | 2002-03-13 |
| CA2389310A1 (en) | 2002-03-07 |
| EP1229131A1 (en) | 2002-08-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10597653B2 (en) | Methods for selecting and amplifying polynucleotides | |
| US9944924B2 (en) | Polynucleotide modification on solid support | |
| CN1473201A (zh) | 扩增和任选表征核酸的方法 | |
| CN1697882A (zh) | 多重pcr | |
| US20130045872A1 (en) | Methods of targeted sequencing | |
| US20090226975A1 (en) | Constant cluster seeding | |
| CN1185181A (zh) | 扩增特异核酸序列的方法 | |
| CN1489632A (zh) | 固相支持物上的核酸等温扩增 | |
| CN1293204C (zh) | 等位基因的测定方法 | |
| WO2009132860A1 (en) | Substances and methods for a dna based profiling assay | |
| CN1304596C (zh) | 检测系统 | |
| CN1388831A (zh) | 基因的检测方法 | |
| CN101076606A (zh) | 识别靶多核苷酸 | |
| CN1650029A (zh) | Headloop DNA扩增 | |
| CN1948508A (zh) | 多重固相核酸扩增测定 | |
| CN1650028A (zh) | 解链温度依赖性dna扩增 | |
| CN102741402A (zh) | Mpl基因多态性检测用探针及其用途 | |
| CN101050472A (zh) | 用两性离子化合物提高核酸杂交特异性的方法 | |
| Shammas et al. | ThalassoChip, an array mutation and single nucleotide polymorphism detection tool for the diagnosis of β-thalassaemia | |
| US12060554B2 (en) | Method for selecting and amplifying polynucleotides | |
| CN1858244A (zh) | 具有增强的结合特异性的多核苷酸探针,其上固定有该探针的微阵列及设计该探针的方法 | |
| KR20240037181A (ko) | 핵산 농축 및 검출 | |
| CN1186456C (zh) | 通用模板核酸检测方法和试剂盒 | |
| CN101065483A (zh) | 碱基多态性的鉴定方法 | |
| CN1860241A (zh) | 部分双链型核酸分子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |