CN1268549C - 具有金红石样结晶相的纳米粒子及其制备方法 - Google Patents
具有金红石样结晶相的纳米粒子及其制备方法 Download PDFInfo
- Publication number
- CN1268549C CN1268549C CNB028228545A CN02822854A CN1268549C CN 1268549 C CN1268549 C CN 1268549C CN B028228545 A CNB028228545 A CN B028228545A CN 02822854 A CN02822854 A CN 02822854A CN 1268549 C CN1268549 C CN 1268549C
- Authority
- CN
- China
- Prior art keywords
- mixed oxide
- oxide nanoparticle
- particle
- nanoparticle particle
- precursor
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G23/00—Compounds of titanium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B82—NANOTECHNOLOGY
- B82Y—SPECIFIC USES OR APPLICATIONS OF NANOSTRUCTURES; MEASUREMENT OR ANALYSIS OF NANOSTRUCTURES; MANUFACTURE OR TREATMENT OF NANOSTRUCTURES
- B82Y30/00—Nanotechnology for materials or surface science, e.g. nanocomposites
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G23/00—Compounds of titanium
- C01G23/04—Oxides; Hydroxides
- C01G23/047—Titanium dioxide
- C01G23/053—Producing by wet processes, e.g. hydrolysing titanium salts
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G30/00—Compounds of antimony
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/20—Oxides; Hydroxides
- C08K3/22—Oxides; Hydroxides of metals
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/30—Three-dimensional structures
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/50—Solid solutions
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/50—Agglomerated particles
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/62—Submicrometer sized, i.e. from 0.1-1 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/64—Nanometer sized, i.e. from 1-100 nanometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/80—Particles consisting of a mixture of two or more inorganic phases
- C01P2004/82—Particles consisting of a mixture of two or more inorganic phases two phases having the same anion, e.g. both oxidic phases
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K2201/00—Specific properties of additives
- C08K2201/011—Nanostructured additives
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/29—Coated or structually defined flake, particle, cell, strand, strand portion, rod, filament, macroscopic fiber or mass thereof
- Y10T428/2982—Particulate matter [e.g., sphere, flake, etc.]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/29—Coated or structually defined flake, particle, cell, strand, strand portion, rod, filament, macroscopic fiber or mass thereof
- Y10T428/2982—Particulate matter [e.g., sphere, flake, etc.]
- Y10T428/2991—Coated
Abstract
纳米大小的粒子包含钛和锑的混合氧化物,其特征为金红石一样结晶相。通过热液加工容易制备所述粒子,并可将其用作胶体,或者以各种组合物和制件形式使用。
Description
本发明涉及一种纳米大小的粒子,它包含钛和锑的氧化物,尤其涉及制造这种粒子的方法以及包含它的组合物或制件。
纳米复合材料,即在有机粘合剂中均匀分散有无机纳米粒子的材料已经用作用于各种应用的保护性透明涂层。相比其中没有分散无机纳米粒子的相应有机粘合剂涂层而言,这种材料具有高耐磨性和/或光学性质(例如折射率)。
已经描述了包含各种无机纳米粒子如氧化钛(即二氧化钛)纳米粒子的纳米复合材料。二氧化钛以至少三种结晶形式存在:锐钛矿、板钛矿和金红石。这当中,所述金红石形式的密度、硬度和折射率最大。
制备二氧化钛溶胶,尤其是具有金红石结晶相的二氧化钛溶胶的主要问题包括:工艺时间长、需要使用额外的稳定抗衡离子(例如,氯离子、硝酸根等,在用于如有机保护膜之前必费地除去)、极端的pH值和/或有限的稳定性。
最好有一种能快速且容易地制备包含钛的无机粒子的稳定胶态分散体的方法,其中,所述粒子具有至少和二氧化钛的金红石形式相当的性质。还最好均匀地将这种粒子加入有机粘合剂中,形成折射率高的耐磨涂层。
一方面,本发明提供一种组合物,它以水性胶态分散体形式包含许多的Ti/Sb混合氧化物纳米粒子,其中,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相。
在一些实施方式中,所述纳米粒子具有至少一个连接到所述纳米粒子表面上的有机部分。
另一方面,本发明提供一种制备Ti/Sb混合氧化物纳米粒子的水性胶态分散体的方法,所述方法包括如下步骤:
a)提供一种二氧化钛水性前体;
b)提供一种氧化锑水性前体;
c)将两种水性前体混合;
d)热液加工所述混合物;
其中,钛和锑的重量比为0.14-11.3。
在一些实施方式中,所述方法还包括对所述纳米粒子表面改性的步骤。
本发明制备的胶态分散体通常很稳定。
另一方面,本发明提供一种组合物,它包含团聚的纳米粒子,其中,所述团聚的纳米粒子包含Ti/Sb混合氧化物纳米粒子,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相。
在一些实施方式中,所述团聚的纳米粒子再次分散到液体载体中。
另一方面,本发明提供一种纳米复合物前体,它包含许多均匀分散在有机粘合剂前体中的纳米粒子,其中,所述纳米粒子包含Ti/Sb混合氧化物纳米粒子,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相。
另一方面,本发明提供一种纳米复合物,它包含许多分散在有机粘合剂中的纳米粒子,其中,所述纳米粒子包含Ti/Sb混合氧化物纳米粒子,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相。
在一些实施方式中,所述纳米粒子具有至少一个连接到所述纳米粒子表面上的有机部分。
在一些实施方式中,本发明纳米复合物可以载于基材上。
本发明纳米复合物很适合用作保护涂层,并且具有高折射率。
如本文所述,以下定义适用:
“水性二氧化钛前体”是指包含钛的水性组合物,通过加热、蒸发、沉淀、pH调节以及它们组合中的一种或多种方式,它可以转化成二氧化钛;
“水性氧化锑前体”是指包含锑的水性组合物,通过加热、蒸发、沉淀、pH调节以及它们组合中的一种或多种方式,它可以转化成氧化锑;
“热液加工”是指在密闭容器中,在水性介质中加热至水标准沸点以上的温度;
“纳米粒子”是指最大粒径小于500纳米的粒子;
“金红石样”是指具有四方晶体结构,且空间群为P42/mnm(#136);
“有机部分”是指有机基团、离子或者分子;
“混合氧化物”是指钛和锑的氧化物的均质混合物。
图1是本发明复合制件的横截面图。
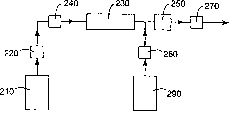
图2是用于制备本发明Ti/Sb混合氧化物纳米粒子的反应系统的示意图。
图3是实施本发明所用脉冲阻尼器的一个实施方式的横截面图。
在各种情况下,本发明涉及纳米粒子,它包含钛和锑的混合氧化物(下文简称为Ti/Sb混合氧化物),其中,至少一部分Ti/Sb混合氧化物具有金红石样结晶相。
本发明纳米粒子包含Ti/Sb混合氧化物。通常,在纳米粒子中钛和锑的重量比为0.14-11.30,较好是0.22-5.02,更好是0.42-2.93。
本发明Ti/Sb混合氧化物纳米粒子较好包含金红石样结晶相。在各个Ti/Sb混合氧化物纳米粒子中,所述金红石样结晶相可以和其它结晶相共存。各个纳米粒子可以包含至多100重量%的金红石样结晶相。Ti/Sb混合氧化物纳米粒子总体(即,作为整体的所有Ti/Sb混合氧化物纳米粒子)通常包含具有各种大小、元素组成和结晶相的纳米粒子。本文所用的术语“总体平均”是指就所述整个总体而言参数的平均值。因此,所述术语是指整体性质,并不一定反映所述总体中单独组分的性质。
以所述Ti/Sb的总重量计,所述Ti/Sb混合氧化物纳米粒子中金红石样结晶相的总体平均含量较好至少为20重量%,更好是至少40重量%,更好是至少60重量%,尤其更好是至少80重量%。
在一些应用中,最好基本上所有的Ti/Sb混合氧化物纳米粒子包含金红石样结晶相。
对于本发明的Ti/Sb混合氧化物纳米粒子,如X-射线衍射分析(即下文所述的XRD)所测量的,金红石样结晶相比锐钛矿的总体平均相对强度宜大于1∶10。此外,由XRD所观察的任意锐钛矿或氧化锑相对强度的最大值还宜具有小于1%,更好是小于0.1%的相对强度,此时,所述金红石样相的最大衍射相对强度最大值定义为100%。
通常,所述Ti/Sb混合氧化物纳米粒子不含额外的金属元素,虽然对一些具体应用来说,最好加入其它元素(包括硅)。若存在其它金属元素,在总体平均的Ti/Sb混合氧化物纳米粒子中存在的每摩尔钛中,其量较好小于0.1摩尔%。其它金属元素的例子包括稀土元素。
本发明Ti/Sb混合氧化物纳米粒子,其总体平均粒度一般小于500纳米,较好是小于100纳米,更好是小于40纳米,尤其是当纳米粒子加入透明涂层中时。
在一些实施方式中,Ti/Sb混合氧化物纳米粒子可以和具有不同元素组成(例如,二氧化硅、氧化锆、氧化铝、二氧化钛、五氧化二锑)的其它纳米粒子混合。若存在的话,这种其它纳米粒子的平均粒度较好和所述Ti/Sb混合氧化物纳米粒子的相当。这种纳米粒子可以是市售的,例如从Nalco ChemicalCo.(Naperville,IL)或Nyacol Nano Technologies,Inc.(Ashland,MA)获得。在美国专利No.5,037,579和6,261,700中也描述了其它纳米粒子的例子。
在本发明一些实施方式中,选择所述纳米粒子,使胶体和纳米复合物没有粒子团聚或者凝结,它们会影响所需的组合物的性质。较好将各个未缔合(即未团聚和未凝结)的粒子分散在整个组合物中。在这些实施方式中,所述粒子较好不会相互不可逆缔合(例如,通过共价键合和/或氢键键合)。
在其它实施方式中,例如在制备薄膜时,最好所述纳米粒子不可逆地团聚,尤其是在没有分散介质(例如,液体载体或粘合剂)的条件下使用时。
在本发明胶态分散体中存在最多30%或以上的纳米粒子。其量可以随纳米粒子的密度和表面性质改变。所述纳米粒子较好占所述胶态分散体的1-25重量%,更好是10-20重量%。
根据所述应用,本发明胶态分散体的pH可以是任何值,但是通常为4-9,较好是5-8。
本发明胶态分散体通常制成纳米粒子在水性载体中的分散体。所述水性载体包括水(通常作为主要组分),并且可以包含有机溶剂(尤其是可以在二氧化钛或氧化锑前体中存在的溶剂)。溶剂可以在热液加工前加入,或者更好是在之后加入。有机溶剂的例子包括具有4-12个碳原子的醇、醚和/或酮。这种较好溶剂中的一种就是1-甲氧基-2-丙醇。
溶剂若存在的话,取决于它加入的时刻,可根据其挥发性以及它和水性二氧化钛和二氧化锑前体、粘合剂前体和/或粘合剂的相容性选择本发明所用溶剂。
本发明纳米粒子可以加入粘合剂中,形成纳米复合物。所述纳米粒子可以直接掺合到粘合剂中,或者掺合到随后固化形成粘合剂的粘合剂前体中。以所述纳米粒子的总重量计,纳米复合物中纳米粒子的量宜至少为30重量%。
无机纳米粒子和有机粘合剂的相容性通常通过用偶合剂适当处理无机粒子来实现。
在掺入粘合剂或粘合剂前体之前,本发明所用纳米粒子通常进行表面改性,这可以通过使表面改性剂连接到粒子表面上来实现。连接到所述粒子表面上的表面改性剂可以改变粒子的表面性质,得到各种性质,包括例如提高所述粒子和所述组合物中组分的相容性、便于所述粒子分散在组合物中(以游离形式或者胶体形式)、以及提高所述组合物及其混合物的光学透明度。也可以对所述粒子表面改性,使之包含能和组合物中其它组分结合的表面基团。例如,当所述组合物聚合时,所述表面基团可以和组合物中至少一种组分结合,成为聚合物网状结构部分。所述表面基团较好能够和第一单体、第二单体或者它们的混合物结合。较好对所述粒子进行表面改性,使之包含能使所述组合物具有所需分散性、透明度、粘合性以及流变性的表面基团组合。
表面改性剂可以由通式A-B示意性地表示,其中,A基团能连接到粒子的表面上,B基团是相容基团,它可以和组合物的组分反应,或者不反应。为所述粒子提供极性的相同基团B包括例如聚醚。为所述粒子提供非极性的相容基团B包括例如烃。
合适的表面改性剂包括例如羧酸、磺酸、磷酸、硅烷、磷酸酯以及它们的混合物。有用的羧酸包括例如长链脂肪酸如辛酸、油酸以及它们混合物。具有羧酸官能团的极性改性剂的代表例子包括CH3O(CH2CH2O)2CH2CO2H、2-(2-甲氧基乙氧基乙酸以及琥珀酸单(聚乙二醇)酯。具有羧酸官能团的非极性表面改性剂的代表例子包括辛酸、十二烷酸以及油酸。
有用的硅烷例子包括有机硅烷,例如辛基二甲氧基硅烷、3-甲基丙烯酰氧基丙基三甲氧基硅烷、3-巯基丙基三甲氧基硅烷、正辛基三乙氧基硅烷、苯基三乙氧基硅烷、对甲苯基三乙氧基硅烷、乙烯基三甲氧基硅烷以及它们的混合物。
能和组合物中有机组分结合的非硅烷表面改性剂的例子包括丙烯酸、甲基丙烯酸、丙烯酸β-羧基乙酯、琥珀酸单-2-(甲基丙烯酰氧基乙基)酯以及它们的混合物。提供极性以及对所述粒子的反应性的有用表面改性剂是琥珀酸单-(甲基丙烯酰氧基聚乙二醇)酯。
纳米粒子可以使用各种方法来进行表面改性,包括例如将表面改性剂加入纳米粒子(例如以粉末或水溶胶形式)中,并使所述表面改性剂和所述纳米粒子反应。可将助溶剂加入到组合物中,提高表面改性剂和/或表面改性粒子与水性混合物的相容性(例如,溶解性或混溶性)。
所述表面改性纳米粒子可以在固化前和可固化的粘合剂前体均匀混合,随后进行加工。所述粘合剂前体的选择并不是关键性的,只要它在环境条件下不会和表面改性纳米粒子反应即可。粘合剂前体的例子包括但不限于可聚合的材料,如可自由基聚合的单体和低聚物,如丙烯酸酯、甲基丙烯酸酯、烯丙基化合物、乙烯醚、乙烯酯等,环氧树脂,醇酸树脂、酚醛树脂、氰酸酯、蜜胺以及蜜胺-甲醛树脂、聚氨酯树脂以及它们的混合物。粘合剂前体较好包含丙烯酸酯和/或甲基丙烯酸酯。
所述粘合剂前体可以包括催化剂或其它固化剂,以便于固化。这种催化剂和其它固化剂取决于所述粘合剂前体的性质,可以包括在固化技术领域中熟知的那些,例如,自由基热引发剂,如过氧化物和偶氮化合物、光引发剂、光催化剂、胺硬化剂、硫醇等。
通过施加能量如热量或光辐射(例如,紫外光和电子束辐射)或者通过加入催化剂或固化剂,所述粘合剂前体可以固化形成粘合剂。在可自由基聚合的粘合剂前体情况下,在所述粘合剂前体中较好存在光引发剂,所述混合物较好在惰性气氛如氮气中用来自灯的紫外光照射。在选择保护基的条件下,使用光辐射固化所述粘合剂前体,获得很高的柔性。
当使用时,用于固化的光辐射能量取决于许多因素,如所用反应物的量和类型、能源、卷材速度、离能源的距离、要固化的材料厚度。作为一般准则,光辐射通常包括0.1-10焦/平方厘米的总能量曝光,电子束辐射通常包括小于1兆拉德到100兆拉德或以上,较好是1-10兆拉德的总能量曝光。曝光时间可以从小于1秒到10分钟或以上。
适用于本发明的市售产生自由基光引发剂包括但不限于二苯甲酮、苯偶姻醚以及酰基膦光引发剂,如以商品名IRGACURE和DAROCUR从Ciba-Geigy Corp.(Ardsley,NY)购得的光引发剂。以所述粘合剂前体的总重量计,光引发剂的用量通常在0.1-15重量%,较好在0.5-7重量%之间变化。
可以加入共引发剂(Co-initiator)和胺增效剂,以提高固化速度。其例子包括异丙基噻吨酮、4-(二甲基氨基)苯甲酸乙酯、二甲基氨基苯甲酸2-乙基己酯以及甲基丙烯酸二甲基氨基乙酯。
表面改性纳米粒子和粘合剂前体的体积比为1∶99到最多70∶30,较好是5∶95到最多55∶45,更好是10∶90到最多40∶60。
对透明度很重要的应用来说,在粘合剂前体和/或粘合剂中存在的纳米粒子宜具有小粒度(例如,<40nm),以将光散射效应减至最小。
本领域那些技术人员也会理解到,根据所述应用,所述粘合剂及其前体可以包含其它任选助剂,如表面活性剂、抗静电剂(例如,导电聚合物)、流平剂、热引发剂、光敏剂、UV吸收剂、稳定剂、抗氧化剂、填料、润滑剂、颜料、染料、增塑剂、悬浮剂等。
如图1所示,复合制件100可以包括纳米复合层10,它包含分散在粘合剂40中的Ti/Sb混合氧化物纳米粒子30,并载于基材20上,其中,至少一部分Ti/Sb混合氧化物纳米粒子包含金红石样结晶相。
实际上,所述基材可以是任何固体材料。这种基材的非限制性例子包括玻璃(包括电子显示器)、石英、透明或半透明陶瓷、木材、金属、上漆表面(包括上漆的金属)、以及热固性和热塑性材料如丙烯酸类聚合物(例如聚甲基丙烯酸甲酯)、聚碳酸酯、聚氨酯、聚苯乙烯、苯乙烯共聚物如丙烯腈-丁二烯-苯乙烯共聚物和丙烯腈-苯乙烯共聚物、纤维素酯(例如,乙酸纤维素、二乙酸纤维素、三乙酸纤维素和乙酸丁酸纤维素共聚物)、聚氯乙烯、聚烯烃(例如,聚乙烯和聚丙烯)、聚酰胺、聚酰亚胺、酚醛树脂、环氧树脂、聚苯醚和聚酯(例如,聚对苯二甲酸乙二酯)。热塑性材料可以包含填料和其它助剂。
所述基材较好是玻璃或热塑性聚合物膜。根据所述应用,基材可以是不透明的或透明的。
纳米复合层10可以通过将组合物涂布到基材20上并固化所述粘合剂前体来制备,所述组合物包含纳米粒子30和粘合剂前体。涂布可以通过任何已知的涂布方式来进行,这种方式不会在化学或物理上改变所述粘合剂前体的性质。涂布方式的例子包括例如旋涂、刮涂、线材涂布、流涂、搓涂、喷涂、挤出、浸渍、辊涂、发泡技术等。
所涂布的粘合剂前体和纳米粒子混合物层的厚度取决于具体的主基材和应用。对保护性涂层而言,所得固化的纳米复合层厚度较好为1纳米-50微米或以上,更好是0.5-10微米,更好是3-6微米。更厚纳米复合层会导致经过一段时间后出现裂纹或其它缺陷,但是,更薄的层则往往不能提供足以耐划伤的表面材料。
当作为透明或半透明基材上的涂层时,较好选择纳米复合层中的成份,使之具有和基材接近的折射率。这有助于降低Moire图案或其它可见干涉条纹产生的可能性。
通过将二氧化钛水性前体和氧化锑水性前体混合来制备Ti/Sb混合氧化物纳米粒子。
由于很希望均匀混合晶格中的钛原子和锑原子,故氧化锑水性前体较好是分子形式(即,具有单个锑原子的形式),或者松结合的形式(在反应条件下会分离)。可以使用任何符合这一要求的二氧化钛或氧化锑前体。
二氧化钛水性前体的例子包括钛的醇盐和过氧化氢的反应产物。醇盐例子包括1-丁醇盐、2-乙基己醇盐、2-甲氧基-1-乙醇盐、直链和支链醇盐(例如乙醇盐、1-丙醇盐、2-丙醇盐、2-丁醇盐、异丁醇盐、叔丁醇盐、己醇盐等)。可以将两个或多个相同或不同的有机配位体连接到钛上。所述二氧化钛水性前体较好是钛的醇盐和过氧化氢的反应产物。
氧化锑水性前体的例子包括锑的醇盐和过氧化氢的反应产物及HSb(OH)6。醇盐的例子包括1-丁醇盐、2-乙基己醇盐、2-甲氧基-1-乙醇盐、直链和支链醇盐(例如乙醇盐、1-丙醇盐、2-丙醇盐、2-丁醇盐、异丁醇盐、叔丁醇盐、己醇盐等)。可以将两个或多个相同或不同的有机配位体连接到锑上。
在搅拌条件下混合所述二氧化钛和氧化锑的水性前体,并且同时或按顺序置于使它们形成混合氧化物的条件下。根据制备本发明Ti/Sb混合氧化物纳米粒子所需的化学计量确定各前体的用量。此外若需要的话,可以将金属氧化物水性前体和氧化锑及氧化锑的水性前体混合。
在混合所述二氧化钛和氧化锑水性前体之后,通常对所述混合物加热加压。在一些实施方式中,这可以通过压力容器如从Parr Instruments Co.(Moline,IL)购得的搅拌或不搅拌的压力反应器来完成。所述容器应能够承受所述压力,并且能够密封。将所述包含混合物的容器密封,并将所述溶液加热至很好进行反应物水解和缩合的温度下。通常,以5℃/分钟的速度加热所述容器,直到达到所需的温度。通过温度以及用于加热反应混合物的容器控制合适的压力。通常,所需温度大于120℃,但低于300℃。所述温度较好为150-200℃。在密闭容器中加热所述溶液会形成压力。容器中的压力通常为18-40大气压。虽然反应时间较短更有效,但是一般加热所述溶液高达5小时,以确保完全水解。由使整体达到所需温度的时间来确定加热时间的长短。一旦达到这一温度,所述反应通常瞬间完成。在这一温度下再放一段时间通常会增大微晶的大小,这往往会降低纳米粒子的胶体稳定性。所述Ti/Sb混合氧化物纳米粒子的总体平均金红石样微晶大小较好小于20纳米,更好是小于15纳米。
在加热以及随后冷却至室温之后,一般观察到所述混合金属氧化物粒子在水性载体中通常为固体沉淀的浆液(即,团聚的Ti/Sb混合氧化物纳米粒子)。通过将所述浆液转移到离心瓶中,离心分离所述浆液并轻轻倒出上层清液,将所述粒子从液体中分离出来。从反应混合物分离所述混合金属氧化物粒子的其它方法可以是如过滤、沉降或者冲洗。
或者,可通过蒸发或选择性蒸馏除去所述反应混合物中任何不想要的组分。这时,可以任选地干燥所述金属氧化物粒子。
也可以使用搅拌管式反应器(即STR)来制备Ti/Sb混合氧化物纳米粒子。搅拌管式反应器通常具有电动机驱动的轴,它沿加热管的长度方向共轴定位。所述轴具有许多安装在其上的叶桨,用于反应混合物的混合及传热。搅拌管式反应器在本领域中为人熟知。一种具体的STR装置如实施例15中有说明。
在图2中简略说明了使用STR制备本发明Ti/Sb混合氧化物纳米粒子的胶态分散体的方法的一个实施方式。贮器210包含固体含量为1-2重量%的二氧化钛前体和氧化锑前体的水性混合物。泵220将水性混合物泵入加热至约180-220℃的STR230中,以提供开始形成纳米粒子的热液反应所需的热量。泵220较好能保持基本上均匀的流速(例如,隔膜泵)。在美国专利No.5,644,007(Davidson等),5,814,278(Maistrovich等),4,770,777(Steadly)和PCT申请No.WO 01/5896(于2001年8月16日公开)中说明了搅拌管式反应器的例子。
为了避免因泵产生的会导致粒度分布变宽的脉冲,以及有助于将表面官能化剂添加到纳米粒子上,宜在泵220和STR230之间设置脉冲阻尼器240。在本领域中熟知的是液压脉冲阻尼器。脉冲阻尼器的例子包括封端管,在美国专利No.5,816,291和2,504,424中有说明。所述脉冲阻尼器较好包括封端竖管。
图3中画出脉冲阻尼器的一个特别有用的实施方式。脉冲阻尼器300包含增压流体315,并且由一定长度的管310(在所述管的最上端具有端盖320和空腔325)、在管最下端的增压流体进口330组成。传送管340和管310垂直相接。传送管340连接到背压阀370上,背压阀具有出口管380。管310、340和380相互连接,使流体从进口管向出口管传送,而不会损失原料。当在本发明的该实施方式中使用时,增压流体从出口管380流出,进入STR。因此,在隔膜泵向前冲程时,其将液体推入增压流体进口330中,由于空气压缩,使空腔325的体积收缩。在其返回冲程时,当隔膜泵为下一次传送再次充满时,所述压缩空气起到微型压缩进料室的作用,使液体返回到流体流中。泵的运行时,所述循环反复进行,由此使所泵入流体的压力脉冲变平稳。
所述水性混合物在STR230中典型的停留时间为10-20分钟。在离开STR230之后,所述加热的混合物流经热交换器250,在收集前使所述混合物冷却。任选地,第二泵260可以将贮器290中的表面官能化剂加入就要进入热交换器之前的加热混合物中以处理所述粒子的表面防止团聚。在热交换器之后设置了背压调节阀270,用于控制STR230的压力,确保水仍旧为液态。STR中的一般压力约为250-350磅/平方英寸(1.7-2.4兆帕)。所述STR提供内混合,这有助于高效地传热。此外,STR的混合在反应器中形成活塞流状态。
在热液加工之后,所述Ti/Sb混合氧化物纳米粒子的胶态分散体可以包含极端(即,过大)的粒子。因此,从STR流出的水性胶态分散体不可能是光学透明的。这些极端粒子可以通过离心分离来除去,由此提高所述胶体分散体的透明度,并使粒度分布变窄。
所述胶态分散体可以以该形式使用,或使用有机溶剂或包含有机溶剂和分散助剂的溶液来代替溶剂(例如,水),使用本领域已知的方法形成浆液。本发明使用的溶剂可以根据挥发性以及它和粘合剂前体的相容性进行选择,所述粘合剂前体可以和所述纳米粒子混合使用。典型的有机溶剂包括C6-C12脂族化合物、芳族化合物、醇、醚、酯和/或酮。脂族溶剂的例子包括环己烷、庚烷、甲苯、二甲苯、2-丁酮或4-甲基-2-戊酮、1-甲氧基-2-丙醇等。尤其较好是1-甲氧基-2-丙醇。
本发明Ti/Sb混合氧化物纳米粒子宜和至少一种分散助剂混合,所述助剂将有机部分,较好是通过至少一个共价键连接到金属氧化物粒子的表面上。典型的分散助剂包括烷氧基硅烷如烷基三烷氧基硅烷,有机酸如羧酸,醇,聚乙二醇、脂肪酸的单酯或二酯,聚环氧乙烷和聚环氧丙烷、烷氧基化磷酸及其酯,以及它们的混合物。
分散助剂较好包括烷氧基硅烷,较好是辛基三乙氧基硅烷、十八烷基三甲氧基硅烷、十六烷基三甲氧基硅烷、羧酸以及它们的混合物。
其它合适的分散助剂包括硬脂酸、油酸和KEN-REACT偶合剂KR TTS(从Kenrich Petrochemicals(Bayonne,NJ)购得)。可以使用为偶合剂的分散助剂。偶合剂是具有两个官能团的分散助剂。合适的偶合剂包括甲基丙烯酸、甘氨酸、乙醇酸、巯基乙酸、乙酰乙酸甲基丙烯酰氧基乙酯、乙酰乙酸烯丙酯、3-丙烯酰氧基丙基三甲氧基硅烷、3-氨基丙基三乙氧基硅烷、3-巯基丙基三甲氧基硅烷、3-环氧丙氧基丙基三甲氧基硅烷、7-辛烯-1-基三甲氧基硅烷以及烯丙基三乙氧基硅烷。
在加入所述分散助剂之后,所述胶态分散体的固体含量通常为1-2重量%,虽然也可以使用更高和更低的固体含量。然后,搅拌所述胶态分散体,较好是在大于60℃且小于95℃温度下加热的条件下进行,直到所述胶体状分散的粒子表面基本上涂布分散助剂,和/或与分散助剂反应。所述胶态分散体可以浓缩形成固体含量为2-20重量%,较好是5-10重量%的胶态分散体。所述胶态分散体中,分散剂和金属氧化物的比例为0.1-6.0毫摩尔/克,较好是0.2-2.0毫摩尔/克。
然后,加入足量的水(中性、酸性或碱性),除去残留的可水解的基团,并将分散剂进一步浓缩到粒子表面上。对于本发明,发现碱性水解对烷氧基有机硅烷的水解以及浓缩到粒子表面上尤其有利。
任选的步骤包括除去稳定胶态分散体中高沸点的副产物,由此通过加热或真空干燥将稳定胶态分散体浓缩成浆。若所述稳定胶态分散体包括极性液体,通过加入非极性液体,所述结晶纳米粒子出现弱的絮凝。若所述稳定的胶态分散体包含非极性液体,通过加入极性液体,所述结晶纳米粒子出现弱的絮凝。通常,通过离心分离将絮凝的纳米粒子分离,然后通过在一种絮凝液中再次悬浮进行洗涤,并离心分离。所述沉淀物可以干燥形成粉末,或者将沉淀物分散在有机液体或溶剂中,形成胶体。
通过以2500rpm离心分离所述胶体样品10分钟来测量,本发明的胶体是稳定的分散体。若离心分离之后基本上不含沉降物的话,胶体(或溶胶)认为是稳定的分散体。
现在。通过以下实施例进一步说明本发明。
实施例
除非另有说明,以下实施例中使用的原料可以普通工业化学品供应商如Aldrich Chemical Co.(Milwaukee,WI)处购得。
实施例中使用的测试方法
粒度
使用从Coulter Corp.(Miami,FL)购得的Coulter N4亚微粒子分析器,通过光子相关谱分析法确定粒度。
结晶相
使用X射线衍射分析(即,XRD)来确定所述结晶相。使用Philips垂直衍射仪(从Philips Electronic Instruments Co.(Mahwah,NJ)购得)收集数据。所述衍射仪装有可变入口狭缝、固定的0.2°接受狭缝、石墨衍射束单色器和用于散射辐射的记录的比例检测器。以45kV和35mA的发生器设定使用一密封的铜靶X-射线源。在玻璃基材上制备作为乙醇浆液的各样品。使用0.04°步距和4秒计数时间在5-80°(2θ)之间进行全阶步扫描。通过将所观察的衍射最大值和International Centre for Diffraction Data powder data file中的图案(International Centre for Diffraction Data,12 Campus Boulevard,Newton Square,PA)进行比较(如H.P.Klug和L.E.Alexander在“X-RayDiffraction Procedures for Polycrystalline and Amorphous Materials”John Wiley& Sons,New York(1954)中所述的)来鉴定存在的结晶相。
实施例中使用的中间体
过钛酸
用848g去离子水、85g 30重量%过氧化氢(从Fisher Scientific(Pittsburgh,PA)购得)以及32g 0.33M的氢氧化铵水溶液加入2升的烧瓶中。在冷水浴中将所述烧瓶中搅拌的物质冷却至10℃,并在3分钟内缓慢地加入35.6g四异丙醇钛(从Gelest,Inc.(Tullytown,PA)购得),形成橙黄色沉淀物,并缓慢地放出气体。在6小时内将所述浆液缓慢升至室温,在这期间,所述沉淀物完全溶解,形成黄色的可倾倒的液体,它由溶于水中的过钛酸组成(理论产率为1重量%TiO2)。
氢过氧化锑溶液
将469g去离子水和21g 30重量%过氧化氢加入1升烧瓶中。在冰浴中将所述搅拌的物质冷却至5℃,并在3分钟内缓慢加入10.5g三正丁醇锑,形成白色沉淀物。在6小时内将所述浆液缓慢升至室温,在这期间,所述沉积物完全溶解,形成无色透明溶液(理论产率为1重量%Sb2O5)。
制备胶体HSb(OH)6
将297g去离子水、20g AMBERLITE IR-120(+)离子交换树脂和4.9g六羟基锑酸钾加入0.5升烧瓶中。将所得浆液搅拌14小时,之后在1小时内加热至65℃,形成稳定的白色溶胶。将所述溶胶冷却至室温,并在C-级玻璃烧结物上过滤,形成HSb(OH)6的白色水性胶体,其pH测得为3(理论产率为1重量%Sb2O5)
实施例1-13和对比例A-C
根据以下一般步骤,制备实施例1-13和对比例A-C,其成份的量按表1所示进行修改,说明了包含Ti/Sb混合氧化物纳米粒子的水性胶体的制备方法,所述纳米粒子具有金红石样结晶相。
将约1200g过钛酸和胶体HSb(OH)6(重量比如表1所示)的混合物加入2升压力反应器(从Pressure Products Industries,Inc.(Warminster,PA)购得)中。将所述反应器加热至180℃,并保持3小时。在12小时内将所述反应器缓慢冷却至室温。通过GF/B过滤器(玻璃纤维过滤器,1.0微米孔径,从Whatman,Inc.(Clifton,NJ)购得)过滤所得透明的胶体。
结果显示制得了具有金红石样相的纳米粒子,其Ti/Sb混合氧化物的组成具有大于10重量%,但小于100重量%的Sb2O5理论含量。
表1
| 实施例 | 重量%Sb2O5 | Sb/Ti重量比 | 粉末X-射线衍射 | 粉末X-射线衍射 | 晶格参数 | 动态光 | |||||||
| 相对强度 | 微晶大小(nm) | 锐钛矿 | 金红石 | 散射a | |||||||||
| 锐钛矿 | 金红石 | Sb2O5·4H2O | 锐钛矿 | 金红石 | Sb2O5·4H2O | a | c | a | c | 溶液粒度(nm) | |||
| 对比例A | 0 | 0.00 | 100 | 2 | 0 | 19.5* | 0.0 | 0.0 | 3.796 | 9.528 | - | - | 1000 |
| 对比例B | 5 | 0.07 | 100 | 1 | 0 | 24.5 | 0.0 | 0.0 | 3.802 | 9.541 | - | - | 278 |
| 1 | 10 | 0.14 | 100 | 14 | 0 | 19.0 | 14.0 | 0.0 | 3.800 | 9.522 | 4.610 | 2.974 | 233 |
| 2 | 15 | 0.22 | 19 | 100 | 0 | 13.0 | 13.5 | 0.0 | 3.797 | 9.562 | 4.623 | 2.987 | 173 |
| 3 | 20 | 0.31 | 3 | 100 | 0 | <5 | 12* | 0.0 | - | - | 4.628 | 2.990 | 42* |
| 4 | 25 | 0.42 | 0 | 100 | 0 | 0.0 | 10.5 | 0.0 | - | - | 4.633 | 2.997 | 51* |
| 5 | 30 | 0.54 | 0 | 100 | 0 | 0.0 | 10.0 | 0.0 | - | - | 4.639 | 2.998 | 6 |
| 6 | 35 | 0.68 | 0 | 100 | 0 | 0.0 | 9.0 | 0.0 | - | - | 4.638 | 3.010 | 32 |
| 7 | 40 | 0.84 | 0 | 100 | 0 | 0.0 | 9.8* | 0.0 | - | - | 4.649 | 2.997 | 30 |
| 8 | 45 | 1.03 | 0 | 100 | 0 | 0.0 | 10.0 | 0.0 | - | - | 4.657 | 3.012 | 3 |
| 9 | 50 | 1.26 | 0 | 100 | 0 | 0.0 | 10.3* | 0.0 | - | - | 4.657 | 3.001 | 28 |
| 10 | 60 | 1.88 | 0 | 100 | 0 | 0.0 | 11.5 | 0.0 | - | - | 4.659 | 3.017 | 47 |
| 11 | 70 | 2.93 | 0 | 100 | 0 | 0.0 | 12.5 | 0.0 | - | - | 4.664 | 3.006 | 166 |
| 12 | 80 | 5.02 | 0 | 71 | 100 | 0.0 | 11.5 | 20.0 | - | - | 4.666 | 3.025 | 6 |
| 13 | 90 | 11.30 | 0 | 12 | 100 | 0.0 | 12.0 | 17.5 | - | - | 4.658 | 3.018 | 105 |
| 对比例C | 100 | N/a | 0 | 0 | 100 | 0.0 | 0.0 | 18.5 | - | - | - | - | 30 |
在表1中,“*”表示该值是两种独立测量的数字平均。
实施例14
本实施例说明了具有金红石样结晶相的Ti/Sb混合氧化物纳米粒子的水性胶体的制备方法。
将约1369g过钛酸和342g胶体HSb(OH)6(重量比为80份二氧化钛比20份氧化锑)加入2升压力反应器中。将所述反应器加热至180℃,并保持2小时。反应器中的压力达到300磅/平方英寸(2.07兆帕)。通过用干冰包裹所述反应器的外壁,将所述反应器迅速冷却至75℃。所述反应生成淡蓝色的透明胶体,所测粒度为31.9nm,标准偏差为6.4纳米。在100℃炉子中干燥一部分(即,5ml)胶体,通过XRD分析所得粉末,显示了微晶大小为20.5nm的100%相对强度的金红石样峰,以及微晶大小为15.0nm的49%相对强度锐钛矿峰。没有任何证据表明存在单独的氧化锑峰,而是所观察的金红石样相的衍射最大值稍稍偏离本身的金红石,这表明锑原子分布在整个晶格结构中。
实施例15
本实施例说明根据本发明的一个实施方式使用搅拌管式反应器制备Ti/Sb的方法。
将胶体HSb(OH)6加入过钛酸中,使TiO2和Sb2O5的计算重量比为80/20。往所述混合物中加入充分浓缩的氢氧化铵,将pH升至约7,使前体稳定,并防止胶凝。所述混合物形成中间过氧化复合物,并在3小时内溶解形成混合金属过氧化复合物的透明橙色溶液(1重量% TiO2/Sb2O5)。
将所述混合物注入316不锈钢2升管式反应器中,它在204℃的加热温度下操作,停留时间为11.1分钟。STR的长度为60英寸,内径为2英寸,其L/D比为30。其生产量为180g/分钟,所述搅拌电动机的速度为120转/分钟。所述系统压力为300磅/平方英寸(2.1兆帕)。在反应器出口的温度为190℃。
使用隔膜泵(No.EK-1型,从American Lewa,Inc.(Holliston,MA)购得,它具有由10英寸1/2″OD不锈钢管的封端长度制成的空腔以及如图3所示设置的处于所述泵和STR进口之间的背压阀组成的脉冲阻尼器)将所述混合物泵入反应器中。来自STR的出口混合物立即流经热交换器,迅速将所述混合物冷却至约75-80℃。使用从Matec Applied Sciences,Inc.(Northborough,MA)购得的CHDF2000粒子分析器测定所得胶态分散体的粒度。所述重均粒度为123纳米。
使用从Kendro Laboratory Products(Franklin,MA)购得的CARRPOWERFUGE PILOT重力离心机以10的设定速度(相当于20,308的G-Force)离心分离这一分散体,形成Ti/Sb混合氧化物纳米粒子的透明胶态分散体,其显示出金红石样结晶相,重均粒度为64纳米,且粒度分布窄。
实施例16
本实施例显示了使用具有金红石样结晶相的胶体表面改性的Ti/Sb混合氧化物纳米粒子制备复合制件的方法。
将100g掺杂锑的二氧化钛胶体(如实施例3中制备的)和600毫克SILQUESTA1230(从Witco Corp.of Endicott,NY购得的硅烷偶合剂)加入8-盎司(237毫升)玻璃瓶中。将所述透明的胶体置于80℃的炉子中16小时,然后冷却至室温。将所述胶体转移到烧瓶中,并使用旋转蒸发器降至3g。往所述胶体中加入1-甲氧基-2-丙醇(18g,从Aldrich of Milwaukee,WI购得),并使用旋转蒸发器将所述混合物降至7g。往所述胶体中加入1-甲氧基-2-丙醇(12g),并使用旋转蒸发器减少所述混合物,制得具有8.1重量%金属氧化物的最终胶体。
将这一胶体和1.85g 30重量%SR 295(季戊四醇四丙烯酸酯的商品名)、30重量%SR 506(丙烯酸异冰片酯的商品名)和40重量%SR 238(1,6-己二醇二丙烯酸酯的商品名)(以上均从Sartomer Company,Inc.(Exton PA)购得)的混合物混合。往所述混合物中加入三(N-亚硝基-N-苯基羟基-氨基(aminato))铵(2毫克,从First Chemical Corp.(Pascagoula,MS)购得),然后使用旋转蒸发器将其降至3.83g。所述树脂的热重分析隙显示所述树脂中有22.65%无机固体。
往所述树脂中加入1%的2,4,6-三甲基苯甲酰基-二苯基-氧化膦液体光引发剂(从BASF Corp.(Mount Olive,NJ)购得,商品名为LUCIRIN LR8893),然后以0.5密耳的厚度用棒将其涂布在0.125英寸的聚甲基丙烯酸甲酯片上。
通过使所述涂布的样品经过Fusion UV Systems的UV处理机(VPS-6电源,EPIQ 6000辐照器,从Fusion UV Systems,Corp.(Rockville,MD)购得),固化所述涂布的样品,所述处理机装有全功率(600W/英寸)的“D”泡,并在40英尺/分钟(12.2米/分钟)的线速度下操作。
所得固化涂布膜的折射率测得为1.569。
Claims (10)
1.一种组合物,它以水性胶态分散体形式包含许多Ti/Sb混合氧化物纳米粒子,其中,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相,在所述Ti/Sb混合氧化物纳米粒子中,锑与钛之重量比从至少为O.42到最多等于2.93;
所述Ti/Sb混合氧化物纳米粒子中金红石样结晶相的总体平均含量至少为20重量%。
2.一种组合物,它包含团聚的纳米粒子,其中,所述团聚的纳米粒子包含Ti/Sb混合氧化物纳米粒子,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相,在所述Ti/Sb混合氧化物纳米粒子中,锑与钛之重量比从至少为0.42到最多等于2.93;
所述Ti/Sb混合氧化物纳米粒子中金红石样结晶相的总体平均含量至少为20重量%。
3.一种纳米复合物前体,它包含许多均匀分散在有机粘合剂前体中的纳米粒子,其中,所述纳米粒子包含Ti/Sb混合氧化物纳米粒子,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相,在所述Ti/Sb混合氧化物纳米粒子中,锑与钛之重量比从至少为0.42到最多等于2.93;
所述Ti/Sb混合氧化物纳米粒子中金红石样结晶相的总体平均含量至少为20重量%。
4.权利要求3所述的纳米复合物前体,其特征在于,所述粘合剂前体包含可聚合的材料。
5.一种纳米复合物,它包含许多分散在有机粘合剂中的纳米粒子,其中,所述纳米粒子包含Ti/Sb混合氧化物纳米粒子,所述Ti/Sb混合氧化物纳米粒子包含金红石样结晶相,在所述Ti/Sb混合氧化物纳米粒子中,锑与钛之重量比从至少为0.42到最多等于2.93;
所述Ti/Sb混合氧化物纳米粒子中金红石样结晶相的总体平均含量至少为20重量%。
6.权利要求1或2所述的组合物、权利要求3所述的纳米复合物前体或者权利要求5所述的纳米复合物,其特征在于,所述Ti/Sb混合氧化物纳米粒子中金红石样结晶相的总体平均含量至少为40重量%。
7.权利要求1或2所述的组合物、权利要求4所述的纳米复合物前体或者权利要求5所述的纳米复合物,其特征在于,所述Ti/Sb混合氧化物纳米粒子中金红石样结晶相的总体平均含量至少为40重量%。
8.一种制备Ti/Sb混合氧化物纳米粒子的水性胶态分散体的方法,所述方法包括如下步骤:
a)提供一种二氧化钛水性前体;
b)提供一种氧化锑水性前体;
c)将两种水性前体混合;
d)热液加工所述混合物;
其中,锑与钛的重量比从至少为0.42到最多等于2.93。
9.权利要求8所述的方法,其特征在于,热液加工包括使所述混合物流经搅拌管式反应器。
10.权利要求8所述的方法,还包括离心分离所述热液加工混合物的步骤。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US09/990,604 | 2001-11-21 | ||
| US09/990,604 US6962946B2 (en) | 2001-11-21 | 2001-11-21 | Nanoparticles having a rutile-like crystalline phase and method of preparing same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1589237A CN1589237A (zh) | 2005-03-02 |
| CN1268549C true CN1268549C (zh) | 2006-08-09 |
Family
ID=25536321
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB028228545A Expired - Fee Related CN1268549C (zh) | 2001-11-21 | 2002-09-16 | 具有金红石样结晶相的纳米粒子及其制备方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (3) | US6962946B2 (zh) |
| EP (1) | EP1451108B1 (zh) |
| JP (1) | JP4276077B2 (zh) |
| CN (1) | CN1268549C (zh) |
| AT (1) | ATE365701T1 (zh) |
| AU (1) | AU2002326930A1 (zh) |
| DE (1) | DE60220941T2 (zh) |
| WO (1) | WO2003045846A1 (zh) |
Families Citing this family (58)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7683098B2 (en) * | 1996-09-03 | 2010-03-23 | Ppg Industries Ohio, Inc. | Manufacturing methods for nanomaterial dispersions and products thereof |
| US6962946B2 (en) * | 2001-11-21 | 2005-11-08 | 3M Innovative Properties Company | Nanoparticles having a rutile-like crystalline phase and method of preparing same |
| WO2004026783A1 (en) * | 2002-09-17 | 2004-04-01 | 3M Innovative Properties Company | Porous surfactant mediated metal oxide films |
| US7521039B2 (en) * | 2002-11-08 | 2009-04-21 | Millennium Inorganic Chemicals, Inc. | Photocatalytic rutile titanium dioxide |
| US7282272B2 (en) * | 2003-09-12 | 2007-10-16 | 3M Innovative Properties Company | Polymerizable compositions comprising nanoparticles |
| KR20060121919A (ko) * | 2003-09-12 | 2006-11-29 | 쓰리엠 이노베이티브 프로퍼티즈 컴파니 | 내구성 광학 요소 |
| US7074463B2 (en) * | 2003-09-12 | 2006-07-11 | 3M Innovative Properties Company | Durable optical element |
| DE10349061A1 (de) * | 2003-10-22 | 2005-05-25 | Studiengesellschaft Kohle Mbh | Verfahren zur Herstellung von Füllstoffe enthaltenden Kunststoffen |
| US7641940B1 (en) * | 2003-12-23 | 2010-01-05 | University Of Central Florida Research Foundation, Inc. | Method of applying photocatalysts to thermoplastic surfaces |
| WO2005083163A1 (ja) * | 2004-03-02 | 2005-09-09 | Asahi Kasei Fibers Corporation | ポリウレタン弾性繊維及びその製造方法 |
| DE102004010504B4 (de) * | 2004-03-04 | 2006-05-04 | Degussa Ag | Hochtransparente lasermarkierbare und laserschweißbare Kunststoffmaterialien, deren Verwendung und Herstellung sowie Verwendung von Metallmischoxiden und Verfahren zur Kennzeichnung von Produktionsgütern |
| BRPI0508433B1 (pt) * | 2004-03-04 | 2012-12-25 | materiais plÁsticos tingidos por corantes de modo transparente, translécido ou opaco, uso de partÍculas em nanoescala e processos para produÇço e solda do mesmo. | |
| KR100627621B1 (ko) * | 2004-11-19 | 2006-09-25 | 한국화학연구원 | 루타일형 티타니아 나노 졸의 제조방법 |
| CN1325577C (zh) * | 2004-12-03 | 2007-07-11 | 中国科学院长春应用化学研究所 | 合成有机包覆剂包覆的二氧化钛纳米粒子的方法 |
| US7241437B2 (en) * | 2004-12-30 | 2007-07-10 | 3M Innovative Properties Company | Zirconia particles |
| US7326448B2 (en) | 2005-02-17 | 2008-02-05 | 3M Innovative Properties Company | Polymerizable oligomeric urethane compositions comprising nanoparticles |
| JP2008530346A (ja) * | 2005-02-17 | 2008-08-07 | スリーエム イノベイティブ プロパティズ カンパニー | 低ガラス転移温度を有する重合有機相を含む輝度向上フィルム |
| US7274458B2 (en) * | 2005-03-07 | 2007-09-25 | 3M Innovative Properties Company | Thermoplastic film having metallic nanoparticle coating |
| US7704586B2 (en) * | 2005-03-09 | 2010-04-27 | Degussa Ag | Plastic molded bodies having two-dimensional and three-dimensional image structures produced through laser subsurface engraving |
| WO2006099168A2 (en) * | 2005-03-11 | 2006-09-21 | 3M Innovative Properties Company | Polymerizable compositions comprising nanoparticles |
| US20060204745A1 (en) * | 2005-03-14 | 2006-09-14 | Jones Clint L | Light management films with zirconia particles |
| EP1869509A2 (en) * | 2005-03-11 | 2007-12-26 | 3M Innovative Properties Company | Light management films with zirconia particles |
| US20060204676A1 (en) * | 2005-03-11 | 2006-09-14 | Jones Clinton L | Polymerizable composition comprising low molecular weight organic component |
| US7666494B2 (en) * | 2005-05-04 | 2010-02-23 | 3M Innovative Properties Company | Microporous article having metallic nanoparticle coating |
| US7400445B2 (en) * | 2005-05-31 | 2008-07-15 | 3M Innovative Properties Company | Optical filters for accelerated weathering devices |
| US7935540B2 (en) * | 2005-07-14 | 2011-05-03 | 3M Innovative Properties Company | Water-soluble polymeric substrate having metallic nanoparticle coating |
| US7547467B2 (en) | 2005-11-15 | 2009-06-16 | 3M Innovative Properties Company | Brightness enhancing film and methods of surface treating inorganic nanoparticles |
| JP2009520077A (ja) * | 2005-12-15 | 2009-05-21 | キャボット コーポレイション | 透明ポリマー複合材料 |
| MX2008009032A (es) | 2006-01-12 | 2008-09-26 | Univ Arkansas | Composiciones de nanoparticulas y metodos para fabricarlas y utilizarlas. |
| US10100266B2 (en) | 2006-01-12 | 2018-10-16 | The Board Of Trustees Of The University Of Arkansas | Dielectric nanolubricant compositions |
| AU2007217870B2 (en) * | 2006-02-16 | 2011-07-21 | Brigham Young University | Preparation of uniform nanoparticles of ultra-high purity metal oxides, mixed metal oxides, metals, and metal alloys |
| US8226878B2 (en) * | 2006-07-07 | 2012-07-24 | University Of Central Florida Research Foundation, Inc. | Laser processing of metal nanoparticle/polymer composites |
| US7470974B2 (en) * | 2006-07-14 | 2008-12-30 | Cabot Corporation | Substantially transparent material for use with light-emitting device |
| DE102007021199B4 (de) * | 2006-07-17 | 2016-02-11 | Evonik Degussa Gmbh | Zusammensetzungen aus organischem Polymer als Matrix und anorganischen Partikeln als Füllstoff, Verfahren zu deren Herstellung sowie deren Verwendung und damit hergestellte Formkörper |
| DE102006058200A1 (de) * | 2006-12-11 | 2008-06-12 | Merck Patent Gmbh | Redispergierbare oberflächenmodifizierte Partikel |
| EP2104654A2 (en) | 2006-12-29 | 2009-09-30 | 3M Innovative Properties Company | Zirconia body and methods |
| US20080234149A1 (en) * | 2007-01-12 | 2008-09-25 | Malshe Ajay P | Nanoparticulate based lubricants |
| US9358502B2 (en) * | 2007-08-31 | 2016-06-07 | Cristal Usa Inc. | Photocatalytic coating |
| EP2227319A2 (en) * | 2007-11-14 | 2010-09-15 | Advanced Technology Materials, Inc. | Solvent-free synthesis of soluble nanocrystals |
| US20090162560A1 (en) * | 2007-12-21 | 2009-06-25 | Envont L.L.C. | Hybrid vehicle systems |
| US20090163647A1 (en) * | 2007-12-21 | 2009-06-25 | Envont Llc | Hybrid metal oxides |
| US20090163656A1 (en) | 2007-12-21 | 2009-06-25 | Envont Llc | Hybrid vehicle systems |
| US20090253072A1 (en) * | 2008-04-01 | 2009-10-08 | Petruska Melissa A | Nanoparticle reversible contrast enhancement material and method |
| US7981986B2 (en) * | 2008-04-29 | 2011-07-19 | 3M Innovative Properties Company | Optical films comprising fluorenol (meth)acrylate monomer |
| US20090275720A1 (en) * | 2008-04-30 | 2009-11-05 | 3M Innovative Properties Company | Ortho-benzylphenol mono(meth)acrylate monomers suitable for microstructured optical films |
| DE102008048874A1 (de) * | 2008-09-25 | 2010-04-08 | Siemens Aktiengesellschaft | Beschichtungen für elektronische Schaltungen |
| US20110111147A1 (en) * | 2009-11-06 | 2011-05-12 | Ajjer Llc | Variable emissivity coatings and their applications |
| GB201011091D0 (en) * | 2010-07-01 | 2010-08-18 | Lucite Int Uk Ltd | A catalyst and a process for the production of ethylenically unsaturated carboxylic acids or esters |
| CN102515268B (zh) * | 2011-11-04 | 2013-11-06 | 中国科学院金属研究所 | 一种高分散纳米二氧化钛粉体的制备方法 |
| US9114378B2 (en) | 2012-03-26 | 2015-08-25 | Brigham Young University | Iron and cobalt based fischer-tropsch pre-catalysts and catalysts |
| US9079164B2 (en) | 2012-03-26 | 2015-07-14 | Brigham Young University | Single reaction synthesis of texturized catalysts |
| US8476206B1 (en) | 2012-07-02 | 2013-07-02 | Ajay P. Malshe | Nanoparticle macro-compositions |
| US8486870B1 (en) | 2012-07-02 | 2013-07-16 | Ajay P. Malshe | Textured surfaces to enhance nano-lubrication |
| US9289750B2 (en) | 2013-03-09 | 2016-03-22 | Brigham Young University | Method of making highly porous, stable aluminum oxides doped with silicon |
| CN109148689B (zh) * | 2018-08-08 | 2022-04-19 | 广东工业大学 | 醇分散的锐钛矿二氧化钛及其制备方法和聚合物太阳能电池 |
| CN109251648B (zh) * | 2018-08-13 | 2020-07-03 | 山东农业大学 | 含有半纤维素的纳米纤维素化学改性水性木器漆的方法 |
| US11599106B2 (en) | 2019-01-25 | 2023-03-07 | Carrier Corporation | Container monitoring and control by unmanned aerial vehicle |
| CN111573726B (zh) * | 2020-05-29 | 2023-04-25 | 安徽金星钛白(集团)有限公司 | 一种粉末涂料专用金红石型钛白粉及其制备方法 |
Family Cites Families (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2220966A (en) | 1938-07-16 | 1940-11-12 | Du Pont | Titanium oxide suspensions |
| US2504424A (en) * | 1948-08-30 | 1950-04-18 | Kraak Abraham | Liquid shock absorber |
| US3676362A (en) | 1970-11-30 | 1972-07-11 | Du Pont | Method for making metal oxide sols in polar organic solvents |
| GB1580882A (en) | 1976-07-28 | 1980-12-10 | Laporte Industries Ltd | Inorganic oxide pigments |
| AU526110B2 (en) | 1978-12-21 | 1982-12-16 | Tioxide Group Ltd. | Titanium dioxide pigment |
| EP0107284B1 (en) | 1982-08-13 | 1988-11-23 | United Kingdom Atomic Energy Authority | Process for the preparation of dispersions and gels |
| US4612138A (en) | 1983-08-04 | 1986-09-16 | Nalco Chemical Company | Stable acidic and alkaline metal oxide sols |
| EP0261560B1 (en) | 1986-09-22 | 1992-04-01 | Ishihara Sangyo Kaisha, Ltd. | Titania sol and process for producing same |
| US4770777A (en) * | 1987-01-29 | 1988-09-13 | Parker Hannifin Corporation | Microporous asymmetric polyamide membranes |
| FR2617151B1 (fr) | 1987-06-29 | 1990-10-12 | Solvay | Procede pour la fabrication d'une poudre d'oxydes metalliques mixtes, et poudres d'oxydes metalliques mixtes |
| US5403513A (en) * | 1987-10-07 | 1995-04-04 | Catalyst & Chemical Industries, Co., Ltd. | Titanium oxide sol and process for preparation thereof |
| US5104929A (en) | 1988-04-11 | 1992-04-14 | Minnesota Mining And Manufacturing Company | Abrasion resistant coatings comprising silicon dioxide dispersions |
| US5579256A (en) * | 1988-11-01 | 1996-11-26 | Hitachi, Ltd. | Semiconductor memory device and defect remedying method thereof |
| US5037579A (en) * | 1990-02-12 | 1991-08-06 | Nalco Chemical Company | Hydrothermal process for producing zirconia sol |
| US5652192A (en) | 1992-07-10 | 1997-07-29 | Battelle Memorial Institute | Catalyst material and method of making |
| DE4222905A1 (de) | 1992-07-11 | 1994-01-13 | Kronos Titan Gmbh | Subpigmentäres Titandioxid mit verbesserter Photostabilität |
| US5873931A (en) | 1992-10-06 | 1999-02-23 | Minnesota Mining And Manufacturing Company | Coating composition having anti-reflective and anti-fogging properties |
| JPH06329988A (ja) | 1993-05-21 | 1994-11-29 | Nikon Corp | コーティング組成物及びプラスチック基材 |
| CA2175680C (en) | 1993-11-12 | 2008-01-08 | Larry D. Monroe | Abrasive grain and method for making the same |
| AU675477B2 (en) | 1993-12-13 | 1997-02-06 | Ishihara Sangyo Kaisha Ltd. | Ultrafine iron-containing rutile titanium dioxide particle and process for producing the same |
| US5391210A (en) | 1993-12-16 | 1995-02-21 | Minnesota Mining And Manufacturing Company | Abrasive article |
| SE501748C2 (sv) * | 1994-05-20 | 1995-05-08 | Lj Oljeledningar Ab | Anordning för tryckstötsdämpning |
| FR2729651A1 (fr) | 1995-01-24 | 1996-07-26 | Rhone Poulenc Chimie | Catalyseurs d'ammoxydation et leur procede de preparation |
| WO1997015526A1 (en) | 1995-10-27 | 1997-05-01 | E.I. Du Pont De Nemours And Company | Hydrothermal process for making ultrafine metal oxide powders |
| US5644007A (en) | 1996-04-26 | 1997-07-01 | Minnesota Mining And Manufacturing Company | Continuous process for the production of poly(1-alkenes) |
| US5814278A (en) * | 1996-04-26 | 1998-09-29 | Minnesota Mining And Manufacturing Company | Shrouded reaction vessel |
| US5759256A (en) * | 1996-05-24 | 1998-06-02 | Kerr-Mcgee Chemical Corp. | Method for making a rutile mixed metal oxide pigment |
| AU725545B2 (en) | 1996-06-17 | 2000-10-12 | Corning Incorporated | Process for forming a titania-containing preform silica glass blank |
| JP4184487B2 (ja) * | 1997-08-15 | 2008-11-19 | 昭和電工株式会社 | 二酸化チタン微粒子の製造方法 |
| US6607794B1 (en) | 1998-04-16 | 2003-08-19 | Alliedsignal Inc. | Light-reflecting molded articles and methods of making the same |
| CN1202015C (zh) | 1998-07-30 | 2005-05-18 | 美国3M公司 | 钛基氧化物粒子,含该粒子的胶体、组合物,及陶瓷体制品 |
| US6261700B1 (en) * | 1998-12-30 | 2001-07-17 | 3M Innovative Properties Co | Ceramer containing a brominated polymer and inorganic oxide particles |
| US6601046B1 (en) | 1999-03-25 | 2003-07-29 | Koninklijke Philips Electronics N.V. | Usage dependent ticket to protect copy-protected material |
| WO2000064813A1 (en) * | 1999-04-26 | 2000-11-02 | Ferro Corporation | Continuous calcination of mixed metal oxides |
| US6448353B1 (en) * | 2000-02-08 | 2002-09-10 | 3M Innovative Properties Company | Continuous process for the production of controlled architecture materials |
| US6962946B2 (en) * | 2001-11-21 | 2005-11-08 | 3M Innovative Properties Company | Nanoparticles having a rutile-like crystalline phase and method of preparing same |
-
2001
- 2001-11-21 US US09/990,604 patent/US6962946B2/en not_active Expired - Fee Related
-
2002
- 2002-09-16 JP JP2003547308A patent/JP4276077B2/ja not_active Expired - Fee Related
- 2002-09-16 DE DE60220941T patent/DE60220941T2/de not_active Expired - Lifetime
- 2002-09-16 AT AT02761684T patent/ATE365701T1/de not_active IP Right Cessation
- 2002-09-16 CN CNB028228545A patent/CN1268549C/zh not_active Expired - Fee Related
- 2002-09-16 WO PCT/US2002/029392 patent/WO2003045846A1/en active IP Right Grant
- 2002-09-16 EP EP02761684A patent/EP1451108B1/en not_active Expired - Lifetime
- 2002-09-16 AU AU2002326930A patent/AU2002326930A1/en not_active Abandoned
-
2004
- 2004-08-10 US US10/915,308 patent/US7250118B2/en not_active Expired - Fee Related
- 2004-08-10 US US10/915,295 patent/US7304106B2/en not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2005510438A (ja) | 2005-04-21 |
| ATE365701T1 (de) | 2007-07-15 |
| US20050065222A1 (en) | 2005-03-24 |
| US20050063897A1 (en) | 2005-03-24 |
| EP1451108B1 (en) | 2007-06-27 |
| WO2003045846A1 (en) | 2003-06-05 |
| EP1451108A1 (en) | 2004-09-01 |
| DE60220941D1 (de) | 2007-08-09 |
| JP4276077B2 (ja) | 2009-06-10 |
| US6962946B2 (en) | 2005-11-08 |
| CN1589237A (zh) | 2005-03-02 |
| AU2002326930A1 (en) | 2003-06-10 |
| US20030165680A1 (en) | 2003-09-04 |
| US7304106B2 (en) | 2007-12-04 |
| US7250118B2 (en) | 2007-07-31 |
| DE60220941T2 (de) | 2008-03-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1268549C (zh) | 具有金红石样结晶相的纳米粒子及其制备方法 | |
| JP5030694B2 (ja) | 酸化ジルコニウムナノ粒子 | |
| US10753012B2 (en) | Synthesis, capping and dispersion of nanocrystals | |
| JP4279465B2 (ja) | 透明な金属酸化物のコロイド及びセラマーを製造するためのナノサイズ金属酸化物の粒子 | |
| TWI481563B (zh) | Magnesium oxide particles, a method for producing the same, a heat-dissipating filler, a resin composition, a heat-dissipating grease, and a heat-dissipating paint composition | |
| US9617657B2 (en) | Synthesis, capping and dispersion of nanocrystals | |
| US7232556B2 (en) | Titanium comprising nanoparticles and related nanotechnology | |
| JP2821357B2 (ja) | 酸化亜鉛微粒子の製法 | |
| US9359689B2 (en) | Synthesis, capping and dispersion of nanocrystals | |
| WO2007108217A1 (ja) | ナノ粒子分散液の製造方法、ナノ粒子分散液及びナノ粒子分散液製造装置 | |
| US20100324191A1 (en) | Composites of polymers and metal/metalloid oxide nanoparticles and methods for forming these composites | |
| CN102015913A (zh) | 粒子表面改性的方法 | |
| WO2008041729A1 (fr) | Procédé de fabrication d'une dispersion de fines particules de composé métallique et la dispersion correspondante | |
| JP2009024068A (ja) | 酸化ジルコニウムナノ粒子を含む樹脂粒子の製造方法および樹脂粒子 | |
| WO2009152404A1 (en) | Methods of compounding nanoparticles with a resin | |
| JP2012206886A (ja) | 無機粉体混合物及びフィラー含有組成物 | |
| JP2018030752A (ja) | 窒化ホウ素粒子凝集体、その製造方法、組成物及び樹脂シート | |
| JP2008169233A (ja) | ナノ粒子分散液の製造方法、ナノ粒子分散液、ナノコンポジット材の製造方法、ナノコンポジット材及び透明容器又は透明フィルム | |
| JP5606274B2 (ja) | 微粒子分散液の製造方法 | |
| JP2016079050A (ja) | 有機酸含有ジルコニア微粒子分散液、表面修飾ジルコニア微粒子分散液及びその製造方法、樹脂複合組成物 | |
| Nguyen et al. | Transparent nanocomposites of high refractive index based on epoxy resin and TiO2 nanoparticle | |
| JP2004091763A (ja) | 膜形成剤および膜 | |
| JP2014196215A (ja) | 改質金属酸化物微粒子粉末およびその製造方法 | |
| CN116997528A (zh) | 具有金红石型晶体结构的粒子及其制造方法以及粒子的分散液、涂布液、带膜基材的制造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C19 | Lapse of patent right due to non-payment of the annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |