CN111051348A - 结合psma的治疗分子 - Google Patents
结合psma的治疗分子 Download PDFInfo
- Publication number
- CN111051348A CN111051348A CN201880055554.8A CN201880055554A CN111051348A CN 111051348 A CN111051348 A CN 111051348A CN 201880055554 A CN201880055554 A CN 201880055554A CN 111051348 A CN111051348 A CN 111051348A
- Authority
- CN
- China
- Prior art keywords
- seq
- binding molecule
- psma
- sequence
- binding
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
- C07K16/3069—Reproductive system, e.g. ovaria, uterus, testes, prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
- A61K47/6817—Toxins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6851—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell
- A61K47/6869—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting a determinant of a tumour cell the tumour determinant being from a cell of the reproductive system: ovaria, uterus, testes, prostate
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
- G01N33/57434—Specifically defined cancers of prostate
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
- G01N33/57492—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites involving compounds localized on the membrane of tumor or cancer cells
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/569—Single domain, e.g. dAb, sdAb, VHH, VNAR or nanobody®
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- Cell Biology (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Biomedical Technology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Biochemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Oncology (AREA)
- Organic Chemistry (AREA)
- Reproductive Health (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- Hospice & Palliative Care (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Biotechnology (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Pregnancy & Childbirth (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Gynecology & Obstetrics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Toxicology (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
本发明涉及改进的特异性结合前列腺特异性膜抗原(PSMA)的结合分子,特别是,单人可变重链结构域抗体以及用于治疗癌症的相关方法。
Description
发明领域
本发明涉及前列腺特异性膜抗原(PSMA)结合分子,以及这类结合分子在治疗疾病中的用途。
介绍
前列腺癌是发达国家男性中最常见的非皮肤相关性恶性肿瘤。据估计,六分之一的男性被诊断患有前列腺癌。
目前用于前列腺癌的治疗包括手术、放疗和辅助激素疗法。虽然这些疗法在疾病的早期阶段相对有效,但最初诊断为局限性前列腺癌的大多数患者最终复发。虽然化疗是对抗晚期前列腺癌最广泛使用的方法之一,但由于缺乏特异性和相关毒性,其疗效通常不足。缺乏针对前列腺癌细胞的靶向递送是实现可行治疗效果的主要障碍之一。因此,对于增加抗前列腺癌剂的选择性的策略仍然存在迫切的需求(Barve等,J Control Release.2014年8月10日;0:118-132)。
在使用基于血清的标志物例如前列腺特异性抗原(PSA)之后,前列腺癌的诊断已经大大改善。此外,前列腺肿瘤相关抗原为肿瘤成像、诊断和靶向治疗提供了靶标。前列腺特异性膜抗原(PSMA)(是一种前列腺肿瘤相关标志物)就是这样一种靶标。
PSMA是一种高度限制于前列腺分泌上皮细胞膜的750个残基的II型跨膜糖蛋白。它在前列腺癌细胞和非前列腺实体瘤新血管系统中高度表达,并在其他组织(包括健康的前列腺,肾,肝,小肠和脑)中表达较低。PSMA表达随着前列腺疾病进展和转移而增加,其表达水平因此与肿瘤侵袭性相关。各种免疫组织学研究已经证实,与良性前列腺上皮细胞中的PSMA水平相比,几乎所有前列腺癌病例中的PSMA水平均增加。在疾病的所有阶段均可发现强烈的PSMA染色,包括前列腺上皮内瘤变,晚期雄激素非依赖性前列腺癌和局限于淋巴结、骨、软组织和肺的继发性前列腺肿瘤。因此PSMA被广泛用作前列腺癌细胞的生物标志物。
PSMA具有3部分结构:19个氨基酸的内部部分,24个氨基酸的跨膜部分和707个氨基酸的外部部分。它基于其处理神经肽N-乙酰天冬氨酰谷氨酸盐和谷氨酸缀合的叶酸衍生物的能力而形成具有谷氨酸羧肽酶活性的非共价同二聚体。PSMA通过胞吞途径快速有效地内化,并迅速再循环到膜。
基于抗体的疗法已经成为针对在诸如肿瘤、炎症和传染病等领域中越来越多的人类恶性肿瘤的治疗方法的的重要组分。在大多数情况下,治疗功能的基础是基于抗体的药物对其靶抗原具有的高度的特异性和亲和力。用药物、毒素或放射性核素结合单克隆抗体(mAb)是单克隆抗体可能诱导治疗效果的另一种策略。通过将抗体的靶向特异性与毒性效应分子的肿瘤杀伤力相结合,免疫缀合物允许靶标与正常组织之间的敏感区分,从而导致比大多数常规化学治疗药物更少的副作用。
然而,由于它们的大小和其他物理性质,单克隆抗体必须静脉内(iv)或皮下(sc)施用,因此具有较高的全身暴露量。因此,它们的递送途径通常可能不是最理想的,导致抗体在非疾病部位与靶抗原结合(可能损害正常、非疾病组织的健康功能)或导致次优PK/PD特征。由于次优的施用途径,任何一种结果都可能导致功效丧失和/或安全性受损。
第一种被报道的PSMA特异性mAb,即鼠mAb 7E11,作为肿瘤成像的诊断剂(ProstaScint,Cytogen,Princeton,N.J.)被随后开发并商业化。然而,该抗体识别细胞死亡后暴露的PSMA的细胞内表位,这限制了其作为用于检测PSMA的显像剂的用途。最近,鉴定了识别PSMA的细胞外部分的mAb,如J591。
本发明的目的是解决用于治疗前列腺癌的替代性的基于抗体的治疗的需要。
发明内容
在一个方面,本发明涉及能够结合人PSMA的结合分子,其包含选自下列之一的单人可变重链结构域(VH)抗体:单VH结构域抗体,其包含含有SEQ ID NO.1的CDR1序列、含有SEQ ID NO.2的CDR2序列和含有SEQ ID NO.3的CDR3序列;单VH结构域抗体,其包含含有SEQID NO.5的CDR1序列、含有SEQ ID NO.6的CDR2序列和含有SEQ ID NO.7的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.9的CDR1序列、含有SEQ ID NO.10的CDR2序列和含有SEQID NO.11的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.13的CDR1序列、含有SEQ IDNO.14的CDR2序列和含有SEQ ID NO.15的CDR3序列;单VH结构域抗体,其包含含有SEQ IDNO.17的CDR1序列、含有SEQ ID NO.18的CDR2序列和含有SEQ ID NO.19的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.21的CDR1序列、含有SEQ ID NO.22的CDR2序列和含有SEQID NO.23的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.25的CDR1序列、含有SEQ IDNO.26的CDR2序列和含有SEQ ID NO.27的CDR3序列;单VH结构域抗体,其包含含有SEQ IDNO.29的CDR1序列、含有SEQ ID NO.30的CDR2序列和含有SEQ ID NO.31的CDR3序列;单结构域VH结构域抗体,其包含含有SEQ ID NO.33的CDR1序列、含有SEQ ID NO.34的CDR2序列和含有SEQ ID NO.35的CDR3序列,或单VH结构域抗体,其包含含有SEQ ID NO.37的CDR1序列、含有SEQ ID NO.38的CDR2序列和含有SEQ ID NO.39的CDR3序列。
在一个实施方案中,所述CDR1序列包含SEQ ID NO.25,所述CDR2序列包含SEQ IDNO.26,并且所述CDR3序列包含VH结构域抗体1.27(SEQ ID NO.28)或由其组成。在一个实施方案中,所述单结构域VH结构域抗体包含选自SEQ ID NO 4、8、12、16、20、24、28、32、36或40的序列或由其组成。在一个实施方案中,所述单结构域VH结构域抗体包含SEQ ID NO 28或由其组成。
在一个实施方案中,所述结合分子包含如上所述的能够结合人PSMA的第一单人重链可变免疫球蛋白(VH)结构域抗体和能够结合人PSMA的第二单VH结构域抗体。
在一个方面,本发明涉及包含如上所述的结合分子的药物组合物。
在一个方面,本发明涉及包含如上所述的结合分子的免疫缀合物。
在一个方面,本发明涉及治疗前列腺癌或前列腺病症的方法,其包括施用治疗有效量的如上所述的结合分子、免疫缀合物或药物组合物。
在一个方面,本发明涉及如上所述的结合分子、免疫缀合物或药物组合物,其用作药物。
在一个方面,本发明涉及如上所述的结合分子、免疫缀合物或药物,其用于治疗前列腺癌或前列腺病症。
在一个方面,本发明涉及如上所述的结合分子、免疫缀合物或药物组合物在制备用于治疗前列腺癌或前列腺病症的药物中的用途。
在一个方面,本发明涉及用于降低人PSMA活性的体内或体外方法,其包括使人PSMA与上述结合分子接触。
在一个方面,本发明涉及通过免疫测定确定测试样品中PSMA存在的方法,其包括使所述样品与如上所述的结合分子和至少一种可检测标记接触。
在一个方面,本发明涉及分离的核酸分子,其包含编码如上所述的结合分子的核苷酸序列。
在一个方面,本发明涉及包含如上所述的结合分子的免疫缀合物。
在一个方面,本发明涉及式A-(L-D)n的免疫缀合物,其中A是抗原结合部分,其包含如上定义的能够特异性结合人PSMA的第一人单VH结构域抗体,任选地包含能够特异性结合人PSMA的第二人单VH结构域抗体,并且任选地包含第三人单VH结构域抗体,L是接头,D是澳瑞他汀(auristatin)或其衍生物,并且n是1、2、3、4、5、6、7、8、9或10。
附图说明
本发明在以下非限制性的附图中进一步说明。
图1.纯化的抗PSMA VH在FMAT Mirrorball测定中的结合。1a●1.1,·3.1,▲2.10,1b●2.1,▲2.13,◇2.15,○2.12Δ2.22 1c如从上至下由以下符号表示的测试的单结构域抗体●1.8,·1.10,▲1.11,1.13,○1.14,1.16,Δ1.17,1.18。
图2.纯化的抗PSMA单结构域抗体通过Octet REDD 384与rhPSMA的结合,A.2.1,B.1.1,C.3.1。
图4.用抗PSMA单结构域抗体A.VH2.1B.VH1.1杀伤食蟹猴PSMA和人PSMACHO。
图5.用抗PSMA单结构域抗体杀伤LNCap。使用的sDAb(图例中的符号从上到下):VH1.1、2.1、7.1、3.1、12.1、4.1。
图6.加热至40℃后抗PSMA单结构域抗体与食蟹猴PSMA CHO的结合,A.VH 2.1B.VH1.1。
图7.抗PSMA亲本单结构域抗体A.VH 2.1B.VH 1.1.C.VH 3.1在37℃的血清稳定性。
图8.各种抗PSMA变体单结构域抗体在37℃的血清稳定性。
图9.体内成像。成像5min至24h a)基准mAb,b)VH 2.1,c)VH 2.1-MSA,d)VH1.1,e)阴性对照。
图10.体内成像24h射线照片a)基准mAb,b)VH 2.1,c)VH 2.1-MSA,d)VH1.1,e)阴性对照。
图11.PSMA+肿瘤、PSMA-肿瘤和血液生物分布在5min至24h的比较。a)VH 1.1b)VH2.1c)半衰期延长的VH2.1d)基准mAb e)HEL4对照。
图12.PSMA+肿瘤、膀胱和肾脏生物分布在5min至24h的比较。a)VH 1.1b)VH 2.1c)半衰期延长的VH 2.1d)基准mAb e)HEL4对照。
图13.肺、心脏、肝、肌肉和表达PSMA(PSMA+)的肿瘤生物分布在5min至24h的比较。a)VH 1.1b)VH 2.1c)半衰期延长的VH 2.1d)基准mAb e)HEL4对照。
图14.PSMA+肿瘤与PSMA-肿瘤,血液或肌肉比率在5min至24h的比较。a)VH 1.1b)VH2.1c)半衰期延长的VH 2.1d)基准mAb e)HEL4对照。
图15.从5min到24h全身活性的比较。
图16.显示单体MMAE缀合的VH(A和B),二价VH(C和D)和双互补位VH(E和F)对稳定表达人PSMA蛋白的人细胞和匹配的亲本细胞(PSMA阴性)在48小时的温育时间点的体外细胞毒性。
图17.显示MMAE缀合的VH对稳定表达人PSMA蛋白的人细胞在72小时温育时间点的体外细胞毒性。
图18.显示用于制备HumabodyTM药物缀合物(HDC)的HiPEGTM val-cit-PAB-MMAE试剂(MW=2805g/mol)。
图19.显示用于产生Pro_006对照抗体药物缀合物(ADC)的马来酰亚胺己酰基(maleimidocaproyl)-缬氨酸-瓜氨酸-对-氨基苯甲酰基氧基羰基-单甲基澳瑞他汀E(mc-val-cit-PAB-MMAE)缀合试剂(MW=1317g/mol)。
发明详述
现在将进一步描述本发明。在下面的段落中,更详细地定义了本发明的不同方面。除非有明确的相反指示,否则如此定义的每个方面可以与任何其他的一个或多个方面组合。特别地,被指示为优选或有利的任何特征可以与被指示为优选或有利的任何其他一个或多个特征组合。
通常,与细胞和组织培养,病理学,肿瘤学,分子生物学,免疫学,微生物学,遗传学和蛋白质以及核酸化学和杂交有关的术语以及技术是本领域众所周知和常用的。除非另有说明,否则本公开的方法和技术通常根据本领域众所周知的常规方法进行,并如在本说明书全文中引用和讨论的各种通用和更具体的参考文献中所述。参见例如Sambrook等,Molecular Cloning:A Laboratory Manual(第二版,Cold Spring Harbor LaboratoryPress,Cold Spring Harbor,N.Y.(1989))。根据制造商的说明书进行酶促反应和纯化技术,如本领域通常完成的或如本文所述。与本文所述的分析化学,合成有机化学以及药物和药学化学有关的术语以及实验室程序和技术是本领域中众所周知和常用的。标准技术用于化学合成,化学分析,药物制剂,配制品和递送以及患者的治疗。
本发明提供结合人PSMA的分离的PSMA结合分子,特别是包含至少一个单VH结构域抗体的那些,提供包含这类结合分子的药物组合物,以及分离的核酸、重组表达载体和分离的宿主细胞,用于制备这类结合蛋白和片段。还提供使用本文公开的结合蛋白检测人PSMA,以在体外或体内抑制人PSMA的方法,和治疗疾病的方法。本发明的一个方面提供分离的人抗人PSMA结合分子,特别是包含以高亲和力缓慢解离速率结合人PSMA的单VH结构域抗体或由其组成的那些。
本发明的PSMA结合分子结合野生型人PSMA(登录号Q04609)。单体的序列如下所示(SEQ ID NO.250)。
在一个实施方案中,本发明的PSMA结合分子结合野生型人PSMA和/或食蟹猴PSMA。如本文所用,术语“PSMA结合分子”,“PSMA结合蛋白”,“抗PSMA单结构域抗体”或“抗PSMA抗体”都是指能够结合人PSMA抗原的分子。术语“PSMA结合分子”包括PSMA结合蛋白。可以通过标准方法(定性测定)显示结合反应,所述方法包括例如结合测定,竞争测定或用于确定PSMA与其受体结合的抑制的生物测定或任何种类的结合测定,参照其中具有不相关特异性的抗体的阴性对照试验。合适的测定显示在实施例中。
本发明的抗体或结合分子(包括本文所述的单结构域抗体和多价或多特异性结合物)“结合”或“能够结合”感兴趣的抗原,例如,PSMA是以足够的亲和力结合(即靶向)PSMA抗原,使其可用于靶向表达抗原的细胞或组织的治疗中。
本发明的结合分子(包括本文所述的单结构域抗体和多价或多特异性结合物)特异性结合人PSMA。换句话说,与PSMA抗原的结合明显不同于非特异性相互作用。优选地,本发明的单结构域抗体结合人PSMA并且还结合食蟹猴PSMA。本文使用的针对特定多肽或特定多肽靶标上的表位的术语“特异性结合”或“特异性结合至”或“是特异性的”可以例如通过分子对所述靶标具有以下KD来展示:至少约10-4M、备选地至少约10-5M、备选地至少约10-6M、备选地至少约10-7M、备选地至少约10-8M、备选地至少约10-9M、备选地至少约10-10M、备选地至少约10-11M、备选地至少约10-12M或更多。在一个实施方案中,术语“特异性结合”指分子结合特定多肽或特定多肽上的表位而基本上不与任何其他多肽或多肽表位结合。
术语“表位”或“抗原决定簇”指抗原(例如PSMA)的表面上免疫球蛋白、抗体或抗体片段(包括VH单结构域抗体)特异性结合的位点。通常,抗原具有几个或许多不同的表位,并与许多不同的抗体反应。该术语特别包括线性表位和构象表位。蛋白质抗原内的表位可以由连续氨基酸(通常是线性表位)或通过蛋白质的三级折叠并置的非连续氨基酸(通常是构象表位)形成。由连续氨基酸形成的表位通常但不总是在暴露于变性溶剂时保留,而由三级折叠形成的表位通常在用变性溶剂处理时丧失。表位通常包括独特空间构象中的至少3、4、5、6、7、8、9、10、11、12、13、14或15个氨基酸。用于确定什么表位被给定抗体或抗体片段结合(即表位作图)的方法是本领域公知的,并且包括例如免疫印迹和免疫沉淀测定,其中测试重叠或连续肽与给定抗体或抗体片段的反应性。当两个抗体识别相同或空间上重叠的表位时,抗体与参考抗体结合“基本上相同的表位”。用于确定两个表位是否结合相同或空间上重叠的表位的最广泛使用和快速的方法是竞争测定,其可以使用标记的抗原或标记的抗体以不同的格式配置。
本发明提供结合人PSMA的分离的PSMA结合分子,包含此类结合分子的药物组合物和制剂,以及编码此类结合分子的分离的核酸,包含此类核酸的重组表达载体和宿主细胞,用以制备此类结合分子。本发明还提供使用本文公开的结合分子检测人PSMA,以在体外或体内抑制人PSMA的方法和治疗疾病的方法。本发明的一个优选方面提供分离的人抗人PSMA结合分子,特别是包含以高亲和力、缓慢解离速率结合人PSMA的至少一个单人VH结构域抗体或由其组成的那些。
在一个方面,本发明涉及分离的单可变结构域抗体,分离的可变单结构域或分离的免疫球蛋白单可变结构域,其中所述分离的单结构域抗体,分离的可变单结构域或分离的免疫球蛋白单可变结构域结合人PSMA。包含至少一个单结构域抗体、可变单结构域或免疫球蛋白单可变结构域的结合分子也在本发明的范围内。与人PSMA结合的单结构域抗体、可变单结构域或免疫球蛋白单可变结构域的片段也在本发明的范围内。
术语“单结构域抗体,可变单结构域或免疫球蛋白单可变结构域(ISV)”在本领域中都是公知的,并描述了与靶抗原结合的抗体的单可变片段。这些术语在本文中可互换使用。单重链可变结构域抗体(VH)不包含免疫球蛋白轻链。如下所述,本发明各方面的优选实施方案涉及在不存在轻链的情况下结合PSMA抗原的单重链可变结构域抗体/免疫球蛋白重链单可变结构域。人重链单可变(VH)结构域抗体是特别优选的。人重链单可变VH通常缩写为VH结构域。单VH结构域抗体在本文中也称为 是CrescendoBiologics Ltd.的注册商标。
因此,在一些优选的实施方案中,本发明的分离的结合物/分子包含至少一个单结构域抗体或者由其组成,其中所述结构域优选为人重链可变结构域。因此,在一个方面,本发明的结合物包含至少一个人免疫球蛋白单可变重链结构域或者由其组成;它们没有VL结构域。
每个单VH结构域抗体包含三个CDR和四个FR,按照以下顺序从氨基末端到羧基末端排列:FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4。因此,在本发明的一个实施方案中,该结构域是具有下式FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4的人可变重链(VH)结构域。在本发明的一个实施方案中,结合分子包括其抗原结合片段。
术语“分离的”单结构域抗体是指基本上不含其他具有不同抗原特异性的单结构域抗体、抗体或抗体片段的单结构域抗体。此外,分离的单结构域抗体可以基本上不含其他细胞材料和/或化学物质。
“同源性″通常是指在比对序列之后以及在一些实施方案中在引入缺口(如果需要)以获得最大百分比同源性之后,候选序列中与其比较的多肽的残基相同的氨基酸残基的百分比,并且不考虑作为序列同一性的一部分的任何保守置换。因此,两个氨基酸序列之间的百分比同源性等同于两个序列之间的百分比同一性。N-或C-端延伸、标签或插入都不应被解释为降低同一性或同源性。用于比对的方法和计算机程序是众所周知的。
术语“抗体”,广泛地指包含四个多肽链(两个重链(H)和两个轻链(L)或其任何功能片段,突变体、变体或衍生物)的任何免疫球蛋白(Ig)分子或其抗原结合部分(其保留了Ig分子的基本表位结合特征)。此类突变体、变体或衍生物抗体格式是本领域已知的。在全长抗体中,每个重链包含重链可变区(在本文中缩写为HCVR或VH)和重链恒定区。重链恒定区包含三个结构域CH1,CH2和CH3。每个轻链包含轻链可变区(本文缩写为LCVR或VL)和轻链恒定区。轻链恒定区包含一个结构域CL。VH和VL区能够进一步细分成称为互补决定区(CDR)的高变区,其散布于称为构架区(FR)的更保守的区域。每个VH和VL包含三个CDR和四个FR,按照以下顺序从氨基末端到羧基末端排列:FR1,CDR1,FR2,CDR2,FR3,CDR3,FR4。免疫球蛋白分子可以是任何类型(例如,IgG,IgE,IgM,IgD,IgA和IgY),类别(例如,IgG1,IgG2,IgG3,IgG4,IgA1和IgA2)或亚类。
抗体片段是抗体的一部分,例如F(ab′)2,Fab,Fv,sFv等。全长抗体的功能片段保留全长抗体的靶特异性。因此,重组功能性抗体片段如Fab(片段,抗体),scFv(单链可变链片段)和单结构域抗体(dAb)已被用于开发治疗剂作为基于mAb的治疗剂的备选方案。scFv片段(~25kDa)由两个可变结构域VH和VL组成。自然地,VH和VL结构域通过疏水相互作用非共价结合并倾向于解离。然而,通过将结构域与亲水性柔性接头连接以产生单链Fv(scFv),可以构建稳定的片段。最小的抗原结合片段是单可变片段,即VH或VL结构域。靶标结合不需要分别与轻链/重链配偶体结合。这种片段用于单结构域抗体。单结构域抗体(~12至15kDa)因此具有VH或VL结构域。
在某些实施方案中,本发明的分离的结合分子包含至少一个单结构域抗体或由其组成,其中所述结构域是VH结构域。因此,在一个方面,本发明的结合分子包含至少一个具有VH结构域但没有VL结构域的免疫球蛋白单可变重链结构域抗体(sVD,sdAb或ISV)或由其组成。如本文进一步所述,结合分子可以包含两个或更多个单VH结构域抗体。这类结合分子可以是单特异性的或多特异性的,单价的或多价的,如下面进一步详细解释。因此,在本发明的一些优选实施方案中,结合分子不包含轻链。在一些实施方案中,结合分子不包含重链结构域CH2和CH3。在一些实施方案中,结合分子不包含铰链区和重链结构域CH2和CH3。在一些实施方案中,结合分子不包含重链结构域CH1、CH2和CH3。在一些实施方案中,结合分子不包含重链结构域CH1、铰链区重链结构域CH2和重链结构域CH3。在一些实施方案中,结合分子不包含轻链、重链结构域CH1、铰链区重链结构域CH2和重链结构域CH3。
每个VH结构域包含三个CDR和四个FR,按照以下顺序从氨基末端到羧基末端排列:FRi,CDR1,FR2,CDR2,FR3,CDR3,FR4。可以对VH构架进行修饰以改善结合性质。例如,VH结构域可以包含C或N端延伸。在一个实施方案中,VH结构域包含1至10,例如1、2、3、4、5、6、7、8、9或10个另外氨基酸的C端延伸。在一个实施方案中,VH结构域包含1至12个氨基酸残基的C端延伸,例如CH1结构域的1、2、3、4、5、6、7、8、9或10个另外的氨基酸。在一个实施方案中,所述延伸包含至少1个丙氨酸残基,例如单个丙氨酸残基,一对丙氨酸残基或三联丙氨酸残基。这种延伸的VH结构域在本发明的范围内。同样在本发明的范围内的是包含另外的C或N末端残基,例如接头残基和/或His标签,例如六-His(SEQ ID NO.251)或myc标签的VH结构域。例如,除了标签之外,也可以存在载体的另外残基。使用的结合分子可以具有另外的残基(SEQID NO.252)。
根据本发明的各个方面和实施方案,本发明的单结构域抗体的可变结构域优选为人可变结构域(VH)。如本文所用,人VH结构域包括完全人或基本完全人VH结构域。如本文所用,术语人VH结构域还包括从仅有重链的抗体分离的VH结构域,所述抗体由表达完全人免疫球蛋白重链基因座的转基因小鼠特别是应答于用感兴趣的抗原进行的免疫(例如如WO2016/062990和实施例中所描述的)而制备。在一个实施方案中,人VH结构域还能够包括源自或基于编码这种VH结构域的人VH结构域氨基酸或核酸序列的VH结构域。因此,该术语包括源自人种系免疫球蛋白序列或由其编码的可变重链区。基本上人VH结构域或源自或基于人VH结构域的VH结构域可以包括不由人种系免疫球蛋白序列编码的氨基酸残基(例如体外引入的突变,例如通过随机或位点特异性诱变,或通过体内体细胞突变引入的)。因此术语“人VH结构域”还包括其中一个或更多个氨基酸残基已被修饰的基本上人VH结构域。例如,与完全人序列相比,基本上人VH结构域的VH结构域可以包括多达10个,例如1、2、3、4或5个氨基酸修饰。然而,如本文所用,术语“人VH结构域”或“基本上人VH结构域”不意图包括其中来源于另一种哺乳动物物种如小鼠的种系的CDR序列已被移植到人构架序列上的抗体。优选地,本文所用的术语“人VH结构域”也不意图包括骆驼源化VH结构域,即,已经例如通过以下在体外特异性修饰的人VH结构域:利用常规诱变方法以选择VH结构域序列中的预定位置并在预定位置引入一个或更多个点突变以将一个或更多个预定残基改变为可在骆驼VHH结构域中发现的特定残基。
如本文所用,术语VH或“可变结构域”指由Kabat等,Sequences of ImmunologicalInterest,第5版,U.S.Dept.Health&Human Services,Washington,D.C.(1991)定义的免疫球蛋白可变结构域。CDR氨基酸残基在可变结构域内的编号和定位符合公知的Kabat编号惯例。
更特别地,本发明提供单VH结构域抗体或包含一个或更多个单VH结构域抗体的结合分子,其中所述单VH结构域抗体以在本文特别是在实施例中进一步描述的亲和力,Kon-速率,Koff速率,KD和/或KA,EC50和IC50值与人PSMA结合。实施例中还显示了适用于测量这些值的测定。
本发明的结合分子,特别是单VH结构域抗体,包含氨基酸序列及其优选的序列和/或部分(如CDR)或由其组成,如本文所限定的。
术语“CDR”指抗体可变序列内的互补决定区。在重链和轻链的每个可变区中有三个CDR,对于每个可变区,其被命名为CDR1,CDR2和CDR3。术语“CDR组”指出现在能够结合抗原的单可变区中的一组三个CDR。根据不同的系统对这些CDR的确切边界进行了不同的定义。本文使用由Kabat描述的系统。术语“Kabat编号”,“Kabat定义”和“Kabat标记”在此可互换使用。本领域公认的这些术语是指编号氨基酸残基的系统,这些氨基酸序列比抗体或其抗原结合部分的重链和轻链可变区中的其他氨基酸残基更易变(即高变)(Kabat等,(1971)Ann.NY Acad.Sci.190:382-391和Kabat,等,(1991)Sequences of Proteins ofImmunological Interest,第5版,U.S.Department of Health and Human Services,NIHPublication NO.91-3242)。
如实验部分中更详细描述的,基于CDR3序列中的序列同源性,可以将单VH结构域抗体分离并分为家族。通过优化过程,还产生了一组具有衍生自亲本CDR序列的CDR序列的变体单VH结构域抗体,以与亲本分子相比改善对PSMA的亲和力和/或改善效力。
在一个方面,本发明涉及能够结合人PSMA的结合分子,其包含单VH结构域抗体,或者由单VH结构域抗体组成,或其中PSMA结合部分包含单VH结构域抗体或由其组成,其中所述单VH结构域抗体包含表1a中所示的家族1成员或家族-1样序列,其中所述家族-1样序列是如本文所定义的表1a中所示的家族1的变体。在一个实施方案中,所述结合分子包含至少一种能够结合PSMA,优选人PSMA的单VH结构域抗体或由其组成,所述单VH结构域抗体包含如表1a中所示的家族1单VH结构域抗体或如本文定义的表1a中所示的家族1的变体。因此,本发明涉及能够结合PSMA,优选人PSMA的单VH结构域抗体,其中所述单VH结构域抗体如表1a中所示或者是如本文所定义的表1a中所示家族1的变体。单VH结构域抗体可包括CDR1、CDR2和CDR3序列,如下所示。家族1a中的CDR序列和全长VH序列根据如下所示的表1a编号。
表1a.其显示了在本发明范围内的单VH结构域抗体的序列。
表1b其显示与表1a中列出的那些家族成员共享或具有相似CDR3序列的其它家族1成员。
在一个实施方案中,所述单VH结构域抗体包含如下所示的CDR1、2和3序列。因此,根据本发明,所述单VH结构域抗体可选自下列之一:单VH结构域抗体,其包含含有SEQ IDNO.1的CDR1序列、含有SEQ ID NO.2的CDR2序列和含有SEQ ID NO.3的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.5的CDR1序列、含有SEQ ID NO.6的CDR2序列和含有SEQ IDNO.7的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.9的CDR1序列、含有SEQ IDNO.10的CDR2序列和含有SEQ ID NO.11的CDR3序列;单VH结构域抗体,其包含含有SEQ IDNO.13的CDR1序列、含有SEQ ID NO.14的CDR2序列和含有SEQ ID NO.15的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.17的CDR1序列、含有SEQ ID NO.18的CDR2序列和含有SEQID NO.19的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.21的CDR1序列、含有SEQ IDNO.22的CDR2序列和含有SEQ ID NO.23的CDR3序列;单VH结构域抗体,其包含含有SEQ IDNO.25的CDR1序列、含有SEQ ID NO.26的CDR2序列和含有SEQ ID NO.27的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.29的CDR1序列、含有SEQ ID NO.30的CDR2序列和含有SEQID NO.31的CDR3序列;单结构域VH结构域抗体,其包含含有SEQ ID NO.33的CDR1序列、含有SEQ ID NO.34的CDR2序列和含有SEQ ID NO.35的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.37的CDR1序列、含有SEQ ID NO.38的CDR2序列和含有SEQ ID NO.39的CDR3序列。在一个实施方案中,本发明的单VH结构域抗体包含含有SEQ ID NO.25的CDR1序列、含有SEQ ID NO.26的CDR2序列和含有SEQ ID NO.27的CDR3序列。
一个实施方案中,所述单VH结构域抗体包含选自SEQ ID NO.4、8、12、16、20、24、28、32、36或40的序列或由其组成。在一个实施方案中,所述单VH结构域抗体包含选自SEQID NO.4、8、12、16、20、24、28、32、36或40的序列或与其具有至少75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%同源性但其中CDR2没有发生变化的序列,或由其组成。在一个实施方案中,所述单VH结构域抗体包含如SEQ ID NO.2、6、10、14、18、22、26、30、34或38中任一项所标识的CDR2。在一个实施方案中,所述CDR2是SEQ ID NO.26。在一个实施方案中,所述修饰在FR1、CDR1、FR2、CDR3、FR4中。在一个实施方案中,所述单VH结构域抗体具有包含SEQ ID NO.4、8、12、16、20、24、28、32、36或40或由其组成的VH结构域。在一个实施方案中,所述结合分子选自VH单结构域抗体1.21、1.22、1.23、1.24、1.25、1.26、1.27、1.28、1.29或1.30。在一个实施方案中,所述单VH结构域抗体具有包含SEQ ID NO.28或由其组成的VH结构域。
因此,在一些实施方案中,本发明还提供了变体VH单结构域抗体,其是如表1a中所示的亲本分子1.21至1.30的变体,其中这些变体在CDR2序列中不具有修饰。这样的变体具有一个或更多个氨基酸置换、缺失、插入或其他修饰,并且其保留亲本单结构域抗体的生物学功能。因此,变体VH单结构域抗体保留对人PSMA的结合。亲本单结构域抗体可被序列改造以获得变体。修饰可包括编码单结构域抗体或多肽的一个或更多个密码子的一个或更多个置换、缺失或插入,其导致与天然序列VH单结构域抗体或多肽相比的氨基酸序列的改变。氨基酸置换可以是将一个氨基酸用具有相似结构和/或化学性质的另一个氨基酸置换的结果,例如亮氨酸被丝氨酸置换,即保守氨基酸置换。插入或缺失可以任选地在约1至5个氨基酸的范围内。所允许的变化可以通过系统地在序列中进行氨基酸插入、缺失或置换并测试所得变体的全长或成熟天然序列所显示的活性来确定。如本文所用的VH单结构域抗体的变体通常与非变体分子具有至少75%、76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的序列同源性,优选至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的序列同源性。表1a所示的VH单结构域抗体的变体优选在CDR2区中没有任何修饰。
在一个实施方案中,本发明涵盖如SEQ ID No.41或48中所定义的VH单结构域抗体,所述抗体在位置62和63处具有修饰,但在位置55和56处没有修饰。位置62和63的残基DS可以例如修饰为AT、DF、DN、DA、AD、DV、AF、DT、DA、AS或AY。
在一个实施方案中,变体中的修饰是保守序列修饰。如本文所用,术语“保守序列修饰”意指不显著影响或改变含有该氨基酸序列的抗体的结合特征的氨基酸修饰。这种保守修饰包括氨基酸置换、添加和缺失。可以通过本领域已知的标准技术将修饰引入本发明的抗体,例如定点诱变和PCR介导的诱变。保守氨基酸置换是其中氨基酸残基被具有相似侧链的氨基酸残基取代的置换。本领域已经定义了具有相似侧链的氨基酸残基家族。这些家族包括具有以下侧链的氨基酸:碱性侧链(例如赖氨酸,精氨酸,组氨酸),酸性侧链(例如天冬氨酸,谷氨酸),不带电荷的极性侧链(例如甘氨酸,天冬酰胺,谷氨酰胺,丝氨酸,苏氨酸,酪氨酸,半胱氨酸,色氨酸),非极性侧链(例如丙氨酸,缬氨酸,亮氨酸,异亮氨酸,脯氨酸,苯丙氨酸,甲硫氨酸),β-分支侧链(例如苏氨酸,缬氨酸,异亮氨酸)和芳族侧链(例如酪氨酸,苯丙氨酸,色氨酸,组氨酸)。因此,本发明的单结构域抗体的CDR区内的一个或更多个氨基酸残基可被来自相同侧链家族的其他氨基酸残基置换,并且能够使用本文所述的功能测定测试改变的抗体的保留功能(即,以上(c)至(1)所述的功能)。
在一些实施方案中,单结构域抗体的变体选自表1a中所示的那些,其包含一个或更多个序列修饰并且与未修饰的单结构域抗体相比,具有例如结合亲和力、特异性、热稳定性、表达水平、效应子功能、糖基化、降低的免疫原性或溶解性等一种或更多种性质的改善。
技术人员将知道,有不同的方式来鉴定、获得和优化如本文所述的抗原结合分子,包括体外和体内表达文库。这在实施例中进一步描述。可使用本领域已知的优化技术,例如展示(例如,核糖体和/或噬菌体展示)和/或诱变(例如易错诱变)。因此本发明还包含本文所述的单结构域抗体的序列优化的变体。
在一个实施方案中,能够进行修饰以降低单结构域抗体的免疫原性。例如,一种方法是将一个或更多个构架残基恢复到相应的人种系序列。更具体而言,已经经历体细胞突变的单结构域抗体可含有不同于单结构域抗体所源自的种系序列的构架残基。这些残基能够通过将单结构域抗体构架序列与单结构域抗体所源自的种系序列进行比较来鉴定。为了使构架区序列中的一个或更多个氨基酸残基返回至其种系构型,体细胞突变能够通过例如定点诱变或PCR介导的诱变被“回复突变”为种系序列。
另一种类型的构架修饰包括突变构架区内或甚至一个或更多个CDR区内的一个或更多个残基以除去T细胞表位,从而降低抗体的潜在免疫原性。在又一个实施方案中,抗体的糖基化被修改。例如,能够制备非糖基化抗体(即,抗体缺乏糖基化)。能够改变糖基化以例如增加抗体对抗原的亲和力。这种碳水化合物修饰能够通过例如改变抗体序列内的一个或更多个糖基化位点来完成。例如,能够进行一个或更多个氨基酸置换,其导致消除一个或更多个可变区构架糖基化位点,从而消除该位点的糖基化。这种糖基化可增加抗体对抗原的亲和力。
家族1或变体(家族1样)结合分子优选具有如本文进一步描述和如实施例中所示的KD,Koff,KA,Kd,EC50和IC50值。术语“KD”如本申请中所用,是指“平衡解离常数”并且是指在平衡时的滴定测量中获得的值,或者通过将解离速率常数(Koff)除以结合速率常数(Kon)得到的值。本申请中使用的“KA”是指亲和常数。结合速率常数、解离速率常数和平衡解离常数用于表示抗体对抗原的结合亲和力。确定结合和解离速率常数的方法在本领域中是公知的。使用基于荧光的技术提供高灵敏度和在平衡状态下检查生理缓冲液中样品的能力。其他实验方法和仪器如(生物分子相互作用分析)测定和实施例中描述的测定可用于测试本发明的结合分子。
在一个方面,本发明还涉及分离的核酸序列,所述分离的核酸序列包含选自SEQID NO.61至70的序列或由其组成,所述序列编码VH结构域1.21至1.30。在一个实施方案中,所述序列是SEQ ID No.67。
核酸可以包括DNA和/或RNA。在一个方面,本发明提供了编码如上定义的本发明的CDR或CDR组或VH结构域的核酸。根据本发明的核酸可包含DNA或RNA,并且可以是完全或部分合成的或重组产生的。除非上下文另有要求,否则本文所提及的苷酸序列包括具有特定序列的DNA分子,并包括具有其中U取代T的特定序列的RNA分子。
此外,本发明涉及包含至少一种如上所定义的核酸的核酸构建体。构建体可以是质粒、载体、转录或表达盒的形式。本发明还涉及包含一种或更多种如上所述的核酸构建体的分离的重组宿主细胞。宿主细胞可以是细菌、酵母、病毒、哺乳动物或其它合适的宿主细胞。在一个实施方案中,细胞是大肠杆菌细胞。在另一个实施方案中,细胞是酵母细胞。在另一个实施方案中,细胞是中国仓鼠卵巢(CHO)细胞。
本文所述的结合分子可以作为与一个或更多个另外的蛋白质部分的融合蛋白提供。例如,本文所述的单结构域抗体(第一部分)可以作为与第二部分的融合物提供。
第二部分可包含对人PSMA也是特异性的VH结构域,从而提供二价结合分子。在一个实施方案中,结合分子是双互补位的。双互补位结合分子包含结合不同表位的抗原结合部分。本发明的双互补位结合分子能够使用已知技术的方法构建。
例如,为了产生二价结合分子,本发明的两个单结构域抗体可以连接,两个结合分子可以来自本发明的相同家族或不同家族的结合分子。例如,如上所述和例如表1中所示的家族1单VH结构域抗体或其变体可以连接至家族2至15或家族2样至15样单VH结构域抗体。家族样单VH结构域抗体指如本文其它地方所定义的变体。在本发明的一个实施方案中,将如针对单VH结构域抗体1.27(SEQ ID NO.28)所定义的VH与另一个选自家族2或家族3的单VH结构域抗体连接,例如连接至如针对克隆2.1所定义的单VH结构域抗体。两个或更多个单VH结构域抗体可以通过接头连接,例如多肽接头。合适的接头,例如包含包括GS残基的接头,GS残基诸如(Gly4Ser)n,其中n=1至10,例如1,2,3,4,5,6,7,8,9或10。
| 名称 | V<sub>H</sub>全长序列 |
| 2.1-2.25 | SEQ ID NO.71-95 |
表2.家族2单VH结构域抗体
| 名称 | VH全长序列 |
| 3.1-3.24 | SEQ ID NO.96-119 |
表3家族3成员
| 名称 | V<sub>H</sub>全长序列 |
| 4.1-4.4 | SEQ ID NO.120-123 |
表4.家族4成员
| 名称 | V<sub>H</sub>全长序列 |
| 5.1-5.2 | SEQ ID NO.124-125 |
表5.家族5成员
| 名称 | VH全长序列 |
| 6.1-6.7 | SEQ ID NO.126-132 |
表6.家族6成员
| 名称 | V<sub>H</sub>全长序列 |
| 7.1-7.8 | SEQ ID NO.133-140 |
表7.家族7成员
| 名称 | V<sub>H</sub>全长序列 |
| 8.1 | SEQ ID NO.141 |
表8.家族8成员
| 名称 | V<sub>H</sub>全长序列 |
| 9.1 | SEQ ID NO.142 |
表9.家族9成员
| 名称 | V<sub>H</sub>全长序列 |
| 10.1 | SEQ ID NO.143 |
表10.家族10成员
| 名称 | V<sub>H</sub>全长序列 |
| 11.1 | SEQ ID NO.144 |
表11.家族11成员
| 名称 | V<sub>H</sub>全长序列 |
| 12.1 | SEQ ID NO.145 |
表12.家族12成员
| 名称 | V<sub>H</sub>全长序列 |
| 13.1 | SEQ ID NO.146 |
表13.家族13成员
| 名称 | V<sub>H</sub>全长序列 |
| 14.1 | SEQ ID NO.147 |
表14.家族14成员
| 名称 | V<sub>H</sub>全长序列 |
| 15.1 | SEQ ID NO.148 |
表15.冢族15成员
因此,在另一个方面,本发明涉及一种结合分子,所述结合分子包含能够结合人PSMA的第一单VH结构域抗体和能够结合人PSMA的第二单VH结构域抗体,所述第一单VH结构域抗体具有表1a所示的针对VH 1.21至1.30中任一个所示的CDR1、2或3序列或其变体(所述变体优选保留表1a中所示的CDR2序列之一)。在一个实施方案中,所述单第一结构域VH结构域抗体包含选自SEQ ID NO.4、8、12、16、20、24、28、32、36或40的序列。
在一个实施方案中,第二VH结构域结合与第一VH结构域相同的PSMA表位、部分、结构域、亚基或构象。例如,第二VH结构域可选自家族1、5、6、12或13或家族1、5、6、12或13样序列。在一个实施方案中,第一VH结构域包含SEQ ID No:28或由其组成。
在一个实施方式中,第二VH结构域结合与第一VH结构域不同的PSMA表位、部分、结构域、亚基或构象。因此,该分子是双互补位的。第二VH结构域可选自家族2、3、4、7、9、10、11或14或家族2、3、4、7、9、10、11或14样序列。在一个实施方案中,所述第二VH结构域抗体选自表2。在一个实施方案中,第一VH结构域包含SEQ ID No:28,并且所述第二VH结构域包含SEQID NO:71。在一个实施方案中,所述第二VH结构域抗体选自表2。
在一个实施方案中,所述第一单VH结构域抗体位于C或N末端。在一个实施方案中,所述第一和第二VH结构域通过肽共价连接。在一个实施方案中,所述肽的长度为3至50个氨基酸。在一个实施方案中,接头包含甘氨酸和丝氨酸氨基酸残基。在一个实施方案中,肽接头由式(Gly4Ser)n组成,其中n=1-10。
编码家族2-15家族成员的核酸(即SEQ ID No.149-226)可与选自SEQ ID No.61-70中任一的核酸一起用于表达二价结合分子的构建体中。
在另一个实施方案中,第二部分可包含对不同抗原具有特异性的VH结构域或另一抗体片段以提供双特异性结合分子。如本文所用,术语“双特异性结合分子”因此是指多肽,所述多肽包含如本文所述的结合分子(其具有对PSMA具有结合特异性的结合位点)以及第二多肽结构域(其具有对第二靶标具有结合特异性的结合位点),即双特异性结合分子具有对两个靶标的特异性。第一靶标和第二靶标不相同,即是不同的靶标,例如蛋白质;两者都可能存在于细胞表面。因此,如本文所述的双特异性结合分子能够选择性且特异性地结合表达第一靶标和第二靶标(或展示在其细胞表面上)的细胞。在另一个实施方案中,结合分子包含多于两个抗原结合部分。
如本文所用,术语第一和第二并不表示分子的取向,即第一VH可位于C或N末端。
在另一个实施方案中,超过两个部分连接在一起提供多特异性结合分子。如本文所述的多特异性多肽试剂除了能够结合PSMA之外还能够结合一个或更多个另外的靶标,即多特异性多肽能够结合至少两个,至少三个,至少四个,至少五个,至少六个或更多个靶标,其中多特异性多肽试剂分别具有至少两个,至少三个,至少四个,至少五个,至少六个或更多个靶结合位点。
如本文所使用的,术语“靶标”指具有结合位点的多肽结构域能够选择性结合的生物分子(例如,抗原,肽,多肽,蛋白质,脂质,碳水化合物)。靶标可以是例如细胞内靶标(例如细胞内蛋白质靶标)或细胞表面靶标(如膜蛋白,例如受体蛋白)。优选地,靶标是细胞表面靶标,例如细胞表面蛋白质。优选地,第一细胞表面靶标和第二细胞表面靶标都存在于细胞上。在一个实施方案中,靶标是免疫肿瘤学靶标。
本发明的多特异性抗体能够使用已知技术的方法构建。如果需要,双特异性或多特异性结合分子能够与包含CH2和CH3结构域中的一个或两个以及任选的铰链区的抗体Fc区或其片段连接。例如,编码作为单个核苷酸序列连接到Fc区或其片段的双特异性或多特异性结合分子的载体可用于制备这样的多肽。
在一个实施方案中,第二部分可用于延长结合分子的半衰期。第二部分可以包含结合血清白蛋白例如人血清白蛋白(HSA)或小鼠血清白蛋白(MSA)的蛋白质,例如抗体或其部分。第二部分可以包含结合血清白蛋白(例如人血清白蛋白(HSA)或小鼠血清白蛋白(MSA))的VH结构域。
第二部分可以包含血清白蛋白,例如人血清白蛋白(HSA)或其变体如HSA C34S。还提供了如本文所述的包含VH结构域和Fc结构域的结合分子,例如,其中VH结构域与Fc结构域融合。还提供了结合分子,其包含特异性结合第二抗原的第二可变结构域,其中所述第二抗原是除人PSMA之外的抗原。第二抗原可以是分化簇(CD)分子或主要组织相容性复合体(MHC)II类分子。
在一个实施方案中,本发明的结合分子用可检测性或功能性标记进行标记。标记可以是产生或可被诱导产生信号的任何分子,包括但不限于荧光剂,放射性标记,酶,化学发光剂,核磁共振活性标记或光敏剂。因此,该结合可以通过检测荧光或发光,放射性,酶活性或光吸收来检测和/或测量。
在其他实施方案中,本发明的结合分子偶联至少一种治疗部分,如药物,酶或毒素。在一个实施方案中,所述治疗部分是毒素,例如细胞毒性放射性核素,化学毒素或蛋白质毒素。例如,本发明的PSMA结合分子可以与放射性同位素例如α-,β-或γ-发射体,或β-和γ-发射体偶联。
本发明不同方面和实施方案中使用的毒素可以选自加利车霉素,埃斯佩拉霉素(esperamicin),甲氨蝶呤,多柔比星,美法仑,苯丁酸氮芥,ARA-C,长春地辛,丝裂霉素C,顺铂,依托泊苷,博来霉素,5-氟尿嘧啶,雌莫司汀,长春新碱,依托泊苷,多柔比星,紫杉醇,多西他赛,多拉司他汀(dolastatin)10,澳瑞他汀E和澳瑞他汀PHE。在其他实施方案中,所述治疗部分是免疫刺激剂或免疫调节剂。
一方面,本发明因此提供了包含本文所述单VH结构域抗体的免疫缀合物。
在一个方面,本发明涉及式A-(L-D)n的免疫缀合物,其中A是抗原结合部分,所述抗原结合部分包含能够特异性结合如本文所述的人PSMA的第一人单重链可变免疫球蛋白(VH)结构域抗体,任选地包含能够特异性结合人PSMA的第二人单重链可变免疫球蛋白(VH)结构域抗体,并且任选地包含第三人单重链可变免疫球蛋白(VH)结构域抗体,L是接头,D是澳瑞他汀或其衍生物,并且n是1、2、3、4、5、6、7、8、9或10。
因此,包含如本文所述的CDR1、CDR2和CDR3序列的单VH结构域抗体可用于如上所述的免疫缀合物中。所述单结构域VH结构域抗体包含选自SEQ ID NO.4、8、12、16、20、24、28、32、36或40的序列。在一个实施方案中,所述序列是SEQ ID No.28,并且VH是VH1.27。在一个实施方案中,所述第二单结构域VH结构域抗体选自家族2。
在一个实施方案中,D是MMAE、MMAF或其衍生物。在一个实施方案中,D是MMAE或其衍生物,其通过缬氨酸-瓜氨酸(vc)接头(vc-MMAE)与抗原结合部分缀合。在一个实施方案中,D是MMAF或其衍生物,其通过马来酰亚胺己酰基接头(mc-MMAF)与抗原结合部分缀合。在一个实施方案中,L-D是Vedotin或Mafodotin。
本发明的免疫缀合物优选具有式A-(L-D)n,其中A是澳瑞他汀或其衍生物。在一个实施方案中,D是MMAE、MMAF或其衍生物。
澳瑞他汀是抗肿瘤天然产物多拉斯他丁的合成类似物。澳瑞他汀通过阻断微管蛋白的聚合来抑制细胞分裂,并在抗体-药物缀合物中用作毒性有效负载。澳瑞他汀家族包括单甲基澳瑞他汀E(MMAE)和单甲基澳瑞他汀F(MMAF)。在临床前模型中,已发现澳瑞他汀的效力是传统使用的化疗药物的100至1,000倍高。
MMAE和Vedotin
单甲基澳瑞他汀E(MMAE,去甲基澳瑞他汀E)是一种合成的抗有丝分裂抗肿瘤剂,MMAE的IUPAC名称是(S)-N-((3R,4S,5S)-1-((S)-2-((1R,2R)-3-(((1S,2R)-1-羟基-1-苯基丙-2-基)氨基)-1-甲氧基-2-甲基-3-氧丙基)吡咯烷-1-基)-3-甲氧基-5-甲基-1-氧代庚-4-基)-N,3-二甲基-2-((S)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺。
单甲基澳瑞他汀E或MMAE的效力是多柔比星的100-1000倍高,但其毒性使得不能用作药物本身。然而,它已经被用作抗体-药物偶联物或ADC的一部分,其中MMAE与单克隆抗体(mAb)连接,所述单克隆抗体识别在癌细胞中表达的特异性标志物并将MMAE导向癌细胞。
由于MMAE是有毒的,因此只有当与单克隆抗体(mAb)缀合以将MMAE靶向癌细胞时,它才被用作治疗剂。在MMAE-mAb缀合物的国际非专有名称中,名称″vedotin″表示MMAE加上其与抗体的连接结构。连接靶向mAb至MMAE的结构可以包括附接基团(马来酰亚胺(mal)和己酸(cap))、间隔子(对氨基苯甲酸)和组织蛋白酶可切割的接头(氨基酸缬氨酸(Val)和瓜氨酸(Cit))。
连接MMAE与单克隆抗体的系链在细胞外液中稳定,但一旦抗体-药物-缀合物已结合至靶向的癌细胞抗原并进入癌细胞,该系链则被组织蛋白酶切割,之后ADC释放有毒的MMAE并激活有效的抗有丝分裂机制。抗体-药物缀合物增强抗体的抗肿瘤作用并降低高效细胞毒性剂的不利的全身性作用。
MMAF和mafodotin
单甲基澳瑞他汀F(MMAF,去甲基澳瑞他汀F)是一种合成的抗肿瘤剂。MMAF的IUPAC名称是(S)-2-((2R,3R)-3-((S)-1-((3R,4S,5S)-4-((S)-N,3-二甲基-2-((S)-3-甲基-2-(甲基氨基)丁酰胺基)丁酰胺基-3-甲氧基-5-甲基庚酰基)吡咯烷-2-基)-3-甲氧基-2-甲基丙酰胺基)-3-苯基丙酸。
MMAF是用于一些实验性抗癌抗体-药物缀合物如voresetuzumab mafodotin和SGN-CD19A的毒性有效载荷。在MMAF-抗体-缀合物的国际非专有名称中,名称mafodotin是指MMAF加上其与抗体的附接结构。附接基团可以由马来酰亚胺和己酸组成。
Maderna和Leverett在“Recent Advances in the Development of NewAuristatins:Structural Modifications and Application in Antibody DrugConjugates”;Mol.Pharmaceutics,2015,12(6),pp 1798-1812中对澳瑞他汀及其作为ADC组分的用途进行了综述。Mendelsohn等人,“Investigation of Hydrophilic AuristatinDerivatives for Use in Antibody Drug Conjugates”.Bioconjugate Chem.,ArticleASAP DOI:10.1021/acs.bioconjchem.6b00530,出版日期(Web):2017年1月6日中描述了含有吡啶和其它碱性胺的天然产物多拉司他汀10的衍生物,对其进行了检验以评估亲水性更强的澳瑞他汀衍生物将足够有效用于ADC。吡啶衍生物,单甲基澳瑞他汀PYE,当在体内测试时显示最大效力。
本发明的免疫缀合物、组合物和方法的特征可在于一种澳瑞他汀,所述澳瑞他汀为单甲基澳瑞他汀E(MMAE)或单甲基澳瑞他汀F(MMAF)或其衍生物。
MMAE可以通过缬氨酸-瓜氨酸(vc)接头(vc-MMAE)缀合到抗原结合部分。使用HiPEGTM技术,通过马来酰亚氨基己酰基接头(mc-MMAF)将MMAF缀合至抗原结合部分(WO2009/047500;Cong等人,(2012)Bioconjugate Chem.2012,23,248-263。
因此,在一个实施方案中,D是MMAE或其衍生物,所述MMAE或其衍生物通过缬氨酸-瓜氨酸(vc)接头(vc-MMAE)与抗原结合部分缀合。在另一个实施方案中,D是MMAF或其衍生物,所述MMAF或其衍生物通过马来酰亚胺己酰基接头(me-MMAF)与抗原结合部分缀合。在另一个实施方案中,L-D是vedotin或mafodotin。L-D也可以包含一个或更多个连接A和L-D的H氨基酸。
免疫缀合物可以包含另外的毒性部分、标记、半衰期延长或其他部分。
本发明范围内还包括治疗方法,所述治疗方法包括将所述免疫缀合物施用至需要其的受试者。此外,免疫偶联物可用于制备用于治疗与PSMA表达相关的癌症、前列腺癌或前列腺病症的药物。本发明还涉及如上所述的免疫缀合物,其用于治疗如本文所述的疾病。
本发明的PSMA结合分子的毒素缀合形式优选在皮摩尔浓度下介导对表达PSMA的细胞的特异性细胞杀伤。
另一方面,本发明的PSMA结合分子是被修饰的以增加半衰期,例如通过化学修饰,特别是通过聚乙二醇化,或通过掺入脂质体或使用血清白蛋白蛋白质。
在一个实施方案中,本发明的结合分子是共价修饰的。术语“共价修饰的/共价修饰”包括根据本发明的结合分子的修饰,例如本文指定序列的修饰;用有机蛋白质的或非蛋白质的衍生剂修饰,与异源多肽序列的融合以及翻译后修饰。(例如特定序列的)共价修饰的多肽仍具有本文所述的功能特性,例如结合人PSMA的能力,或共价修饰通常通过使靶向的氨基酸残基与有机衍生剂(其能够与选定的侧链或末端残基反应)反应来引入,或通过利用在选择的重组宿主细胞中发挥功能的翻译后修饰机制来引入。某些翻译后修饰是重组宿主细胞对表达的多肽作用的结果。谷氨酰胺酰和天冬酰胺酰残基经常在翻译后脱氨基成相应的谷氨酰和天冬氨酰残基。或者,这些残基在弱酸性条件下被脱氨基。其他翻译后修饰包括脯氨酸和赖氨酸的羟基化,丝氨酰、酪氨酸或苏氨酰残基的羟基的磷酸化,赖氨酸、精氨酸和组氨酸侧链的[α]-氨基的甲基化。共价修饰,例如,包括包含根据本发明的例如具有特定序列及其氨基酸序列变体的PSMA结合分子(如免疫粘附素)的融合蛋白,以及与异源信号序列的N端融合物。
如下面进一步描述的,本发明的结合分子具有某些功能特性。本发明的结合分子的这些和其他药理学活性可以用例如本领域所述的标准测试方法来证明。
本发明的结合分子可以与前列腺特异性膜抗原一起内化到细胞中。本发明的结合分子特异性结合人PSMA的细胞外结构域上的表位。在一个实施方案中,本发明的结合分子特异性结合二聚体形式的PSMA。本发明的结合分子可以与毒性部分缀合并用于消融或杀死表达PSMA的前列腺或癌细胞。
如实施例(参见实施例7b和表18和19)中所示,本发明的结合分子能够结合活细胞,例如肿瘤细胞或前列腺细胞,例如表达人PSMA的CHO细胞,LNCaP细胞。另一方面,本发明提供以如下EC50值结合PSMA的单结构域抗体:100nM至100pM,如平均EC50值为100nM或更低,甚至更优选地平均EC50值为90nM或更低,如低于80、70、60、50、40、30、20、10、5nM或甚至更低,如低于4、3、2、或1nM或甚至更低,如低于500、400、300、200、100pM或甚至更低,如低于4pM,优选地如在FMAT结合测定中所测量的。具体而言,EC50值显示在表19中。在一个实施方案中,本发明的结合分子能够特异性结合人PSMA和食蟹猴PSMA。
除非另有说明,效价通常以IC50值表示,单位为nM。在功能测定中,IC50是将生物学应答降低其最大值的50%的结合成员的浓度。可以通过绘制作为结合成员浓度的对数函数的最大生物学应答的百分比并使用软件程序将数据拟合成S形函数来产生IC50值来计算IC50。用于测量IC50的方法是本领域已知的。例如,为了确定IC50,可以采用HIS ZAP细胞杀伤测定来确定IC50。ECs0表示半数最大有效浓度。
另一方面,本发明涉及包含至少一个针对PSMA(优选人PSMA)的免疫球蛋白单结构域抗体或由其组成的结合分子,其中所述结构域是人VH结构域并且当如实施例中所描述的进行测试时具有约0.2至约1000nM或更多,例如0.2至900,0.2至800,0.2至700,0.2至600,0.2至500,0.2至400,0.2至300,0.2至200,0.2至100,0.2至50,0.2至40,0.2至30,0.2至20,0.2至10,0.2至9,0.2至8,0.2至7,0.2至6,0.2至5,0.2至4,0.2至3,0.2至2或0.2至1的IC50。
此外,本发明的PSMA结合分子结合PSMA的结合动力学和亲和力(表示为平衡解离常数KD)可以例如使用表面等离子体共振如或Octet来确定,或者KD可以从pA2分析来估计。特别地,本发明的分子是非常有效的(即,例如在实验部分中所测量的EC50值在pM范围内)。
另一方面,本发明提供了如本文所述的单结构域抗体,其中所述sdAb以如下平均KD值结合所述PSMA:100nM至10pM,如平均KD值是90nM或更低,甚至更优选平均KD值是80nM或更低,如低于70、60、50、40、30、20、10、5nM或甚至更低,如低于4、3、2、或1nM,如低于500、400、300、200、100、90、80、70、60、50、40、30、20pM或更低,如低于10pM。优选地,如实施例(实施例8b)中所示确定KD。
在一个实施方案中,根据本发明的结合分子对PSMA具有至少约107M-1,优选约109M-1,更优选约1010M-1至1011M-1或更高的亲和力常数的结合亲和力。在一个实施方案中,根据本发明的结合分子具有1.00E+04至1.00E+6(1/Ms)的Kon。在一个实施方案中,根据本发明的结合分子具有1.00E-03至1.00E-05(1/s)的Koff。
本发明的结合分子显示出优异的稳定性,包括热和血清稳定性(参见实施例)。此外,如实施例中所示,本发明的结合分子显示出快速的肿瘤靶向。此外,本发明的结合分子还显示对人PSMA的高度特异性和非靶组织中的低摄取(参见实施例)。
在一个实施方案中,本发明的结合分子显示快速血液清除。在一个实施方案中,本发明的结合分子显示低的肾滞留。在一个实施方案中,结合分子能够抑制(例如竞争性抑制)另一抗体(例如J591)与人PSMA的结合。
在一个实施方案中,如本文所定义的本发明的结合分子可具有选自以下非限制性列表的一种或更多种性质:
a)对肿瘤细胞表面上存在的天然形式的人和/或食蟹猴前列腺特异性膜抗原的高亲和力结合,
b)被肿瘤细胞内化,
c)非靶组织中的低摄取,
d)快速的肿瘤靶向,
e)与LNCaP细胞强烈结合,但不与或仅最低限度地与缺乏前列腺特异性膜抗原表达的细胞结合和/或
f)与PSMA上的独特表位结合。
使用体外表达文库用于制备或产生本文所述的多肽,核酸,宿主细胞,产品和组合物的方法可以包括以下步骤:
a)提供编码氨基酸序列的核酸序列的合集,集合或文库;和
b)筛选所述合集,集合或文库,以获得能够结合PSMA/对其具有亲和力的氨基酸序列,和
c)分离能够结合PSMA/对其有亲和力的氨基酸序列。
在上述方法中,氨基酸序列的合集,集合或文库可以展示在噬菌体,噬菌粒,核糖体或合适的微生物(如酵母)上,例如以便于筛选。用于展示和筛选氨基酸序列(的合集,集合或文库)的合适方法,技术和宿主生物体对于本领域技术人员而言是清楚的(参见例如Phage Display of Peptides and Proteins:A Laboratory Manual,Academic Press;第一版(October 28,1996)Brian K.Kay,Jill Winter,John McCafferty)。
本文所述的结合分子,包括具有VH结构域的重链抗体,能够在转基因啮齿动物(例如小鼠)中表达。转基因啮齿动物,例如小鼠,可具有降低的表达内源性抗体基因的能力。因此,在一个实施方案中,啮齿动物具有降低的表达内源性轻链和/或重链抗体基因的能力。啮齿动物因此可以包含修饰以破坏内源性轻链和/或重链抗体基因的表达,从而不产生功能性的轻链和/或重链。
在本发明的另一方面,提供了包含根据本发明的PSMA结合分子和任选的药学上可接受的载体的药物组合物。本发明的结合分子或组合物可以通过任何便利的途径施用。化合物可以可以通过任何途径施用,包括口服和胃肠外施用。肠胃外施用包括例如静脉内,肌内,动脉内,腹膜内,鼻内,直肠,膀胱内,皮内,局部或皮下施用。组合物可以采取一个或更多个剂量单位的形式。
本发明的组合物可以是液体形式,例如溶液,乳液或悬浮液。该液体可用于通过注射,输注(例如IV输注)或皮下递送。本发明的液体组合物,无论它们是溶液,悬浮液还是其他类似形式,还可以包括以下一种或更多种:无菌稀释剂,例如水,盐水溶液,优选生理盐水,林格溶液(Ringer′s solution),等渗氯化钠,不挥发油如合成的甘油单酯或甘油二酯,聚乙二醇,甘油或其它溶剂;抗菌剂如苯甲醇或对羟基苯甲酸甲酯;和张力调节剂例如氯化钠或右旋糖。组合物可以封装在安瓿,一次性注射器或由玻璃、塑料或其他材料制成的多剂量小瓶中。
在具体的实施方案中,可希望的是将本发明的一种或更多种结合分子或组合物局部施用于需要治疗的区域,或通过静脉内注射或输注。
在治疗特定病症或病况中有效/有活性的本发明结合分子的量将取决于该病症或病况的性质,并且可以通过标准临床技术来确定。此外,可以任选地采用体外或体内测定来帮助确定最佳用量范围。组合物中使用的精确用量还取决于施用途径和疾病或病症的严重程度,并应根据医师的判断和每位患者的情况来决定。
本发明的组合物包含有效量的本发明的结合分子,从而将获得合适的剂量。化合物的正确用量将根据特定的配方,应用模式以及其特定部位,宿主和正在治疗的疾病而变化。应考虑年龄,体重,性别,饮食,施用时间,排泄率,宿主病况,药物组合,反应敏感性和疾病严重程度等其他因素。可以在最大耐受剂量内连续或定期进行施用。
典型地,该量为按组合物重量算至少约0.01%的本发明的结合分子。
制备本发明的优选组合物,使得肠胃外剂量单位含有约0.01重量%至约2重量%的本发明的结合分子。
对于静脉内施用,组合物可以包含约通常约0.1mg/kg至约250mg/kg动物体重,优选约0.1mg/kg至约20mg/kg动物体重,以及更多优选约1mg/kg至约10mg/kg动物体重。
本发明的组合物可以采用合适的载体的形式,例如气溶胶,喷雾剂,悬浮液或适合使用的任何其他形式。合适的药物载体的其他实例由E.W.Martin描述于“Remington′sPharmaceutical Sciences”。
药物组合物可以使用制药领域公知的方法制备。例如,可通过将本发明的结合分子与水组合以形成溶液来制备意欲通过注射施用的组合物。可加入表面活性剂以促进形成均匀溶液或悬浮液。
本发明还涉及用于预防和/或治疗癌症特别是前列腺癌的方法,其包括向患者施用本发明的结合分子,所述方法包括向有需要的受试者施用药物活性量的本发明的结合分子和/或药物组合物。特别地,本发明涉及用于预防和/或治疗癌症特别是前列腺癌的方法,所述方法包括向有需要的受试者施用药物活性量的本发明的结合分子或药物组合物。
本发明还涉及本发明的结合分子,其用于治疗疾病。本发明还涉及本发明的结合分子,其用于治疗癌症特别是前列腺癌或前列腺病症。“前列腺癌”指由前列腺组织产生的所有阶段和所有形式的癌症。本发明还涉及治疗以PSMA异常表达为特征的疾病。
另一方面,本发明涉及本发明的结合分子在治疗疾病中的用途。另一方面,本发明涉及本发明的结合分子在制备用于治疗癌症特别是前列腺癌或前列腺病症的药物中的用途。
本发明的结合分子也可用于治疗,预防或改善癌症特别是前列腺癌或前列腺病症。前列腺病症是指任何折磨男性生殖系统中的前列腺的疾病。前列腺依赖于睾丸的激素分泌。在其他癌症中已经检测到PSMA的表达,更具体地在与这些癌症相关的新血管系统中检测到PSMA的表达。发现了包括常规(透明细胞)肾细胞,膀胱移行细胞,睾丸-胚胎的,神经内分泌的,结肠和乳房以及不同类型的恶性肿瘤在内的多种癌症在其新血管系统中一致且强烈表达PSMA。
本发明的结合分子可以作为唯一活性成分或与一种或更多种其他治疗和/或细胞毒性部分组合施用。在一个实施方案中,结合分子可以与毒性部分缀合。
在前列腺病症例如前列腺癌的治疗中,抗PSMA结合分子能够与现有的治疗方法组合使用。在一个实施方案中,单结构域抗体与现有的治疗或治疗剂(例如抗癌疗法)组合使用。因此,在另一方面,本发明还涉及包括施用本发明的单结构域抗体或药物组合物和抗癌疗法的组合疗法。抗癌疗法可以包括治疗剂或放射疗法,并且包括基因疗法,病毒疗法,RNA疗法骨髓移植,纳米疗法,靶向抗癌疗法或溶瘤药物。其他治疗剂的实例包括其他检查点抑制剂,抗肿瘤剂,免疫原性试剂,减毒癌细胞,肿瘤抗原,抗原递呈细胞例如用肿瘤衍生抗原或核酸脉冲的树突细胞,免疫刺激细胞因子(例如IL-2,IFNα2,GM-CSF),靶向小分子和生物分子(例如信号转导途径的组分,例如酪氨酸激酶的调节剂和受体酪氨酸激酶的抑制剂,以及与肿瘤特异性抗原结合的试剂,包括EGFR拮抗剂),抗炎剂,细胞毒性剂,放射性毒剂,或免疫抑制剂和用编码免疫刺激性细胞因子(例如GM-CSF)的基因转染的细胞,化学疗法。在一个实施方案中,单结构域抗体与手术组合使用。本发明的结合分子可与其他治疗同时或在不同时间施用,例如同时,分开或顺序施用。
在另一方面,本发明提供了包含本发明的结合分子的用于检测前列腺癌的试剂盒,用于诊断,治疗,预后或监测。试剂盒还可以包含使用说明。试剂盒可以包括如上所述的本发明的标记的结合分子和一种或更多种用于检测所述标记的化合物。本发明另一方面提供了以冻干形式包装或包装在水性介质中的本发明的结合分子。
本发明还涉及使用本发明的结合分子的检测方法。考虑到它们结合人PSMA的能力,本文公开的人PSMA结合分子可以用于使用常规免疫测定(例如酶联免疫吸附测定(ELISA),放射免疫测定(RIA)或组织免疫组织化学)检测PSMA(例如,在生物样品例如血清或血浆中)。特别地,本发明还涉及用于诊断或监测癌症特别是前列腺癌的进展的体外或体内方法。体外方法包括检测测试样品中PSMA蛋白的存在并将其与正常受试者的对照样品或正常受试者的标准值或标准值范围进行比较。样品可以选自血液,血浆,血清,精液,尿液或组织活检。
该方法可以包括:(a)使样品(和任选地,参照物,例如阳性和/或阴性对照样品)与本发明的PSMA结合分子接触,和(b)检测样品中与PSMA结合的结合分子或未结合的结合分子,从而检测生物样品中的PSMA。结合分子可以用可检测物质直接或间接标记,以便于检测结合或未结合的抗体。合适的可检测物质包括各种酶,辅基,荧光材料,发光材料和放射性材料。
体内方法可包括检测体内PSMA的存在,例如通过在受试者中成像。在该方法中,标记本发明的PSMA结合分子以检测结合。
作为标记本发明的结合分子的替代方法,可以通过竞争免疫测定在生物流体中测定人PSMA,所述竞争免疫测定利用标记有可检测物质的PSMA标准品和未标记的人PSMA结合分子。在该测定中,组合生物样品,标记的PSMA标准品和人PSMA结合分子,并确定与未标记的结合分子结合的标记的PSMA标准品的量。生物样品中人PSMA的量与结合至PSMA结合分子的标记的PSMA标准品的量成反比。类似地,还可以通过竞争免疫测定在生物流体中测定人PSMA,所述竞争免疫测定利用标记有可检测物质的PSMA标准品和未标记的人PSMA结合分子。
本文公开的结合分子可以用于抑制例如在含有PSMA的细胞培养物中的、在具有与本文公开的结合分子交叉反应的PSMA的人受试者中或其他哺乳动物受试者中的PSMA活性。在一个实施方案中,提供抑制或增加PSMA活性的方法,包括将PSMA与本文公开的结合分子接触,使得PSMA活性被抑制或增加。例如,在含有或怀疑含有PSMA的细胞培养物中,可以将本文公开的结合分子加入到培养基中以抑制培养物中的PSMA活性。
因此,在一个实施方案中,本发明还涉及消融或杀死表达PSMA的细胞(例如癌性或非癌性前列腺细胞)的方法。本发明的方法包括使细胞与足以消融或杀死细胞的量的本发明的PSMA结合分子接触。这些方法可用于(例如体外或离体)培养中的细胞。
除非本文另外定义,否则与本公开相关使用的科学和技术术语应具有本领域普通技术人员通常理解的含义。虽然前述公开内容提供了涵盖在本发明的范围内的主题的一般描述,包括制造和使用本发明的方法及其最佳模式,提供以下实施例以进一步使得本领域技术人员实施本发明的技术并提供其完整的书面描述。然而,本领域技术人员将理解,这些实施例的细节不应被理解为对本发明的限制,其范围应该从本公开所附的权利要求书及其等同物中理解。鉴于本公开,本发明的各种其他方面和实施例对于本领域技术人员来说将是显而易见的。
本说明书中提及的所有文献均通过引用以其整体并入本文,包括对基因登录号的参考。
本文中使用的术语“和/或”被认为是两个特定特征或部件在具有或不具有另一的情况下每一个的具体公开。例如“A和/或B”应被视为(i)A,(ii)B和(iii)A和B中每一个的具体公开,就像每个在此单独列出一样。除非上下文另有规定,否则上述特征的描述和定义不限于本发明的任何特定方面或实施方案,并且同样适用于所描述的所有方面和实施方案。
序列表
本申请含有序列表,其已经以ASCII格式电子提交,并在此通过引用以其全文并入。
在非限制性实施例中进一步描述了本发明。
实施例
实施例1.Tg/TKO小鼠的构建
在针对内源重链和轻链抗体表达被沉默(三重敲除,或TKO)的背景中携带种系构型中的重链抗体转基因基因座的小鼠如先前所述(WO2004/076618和WO2003/000737,Ren等,Genomics,84,686,2004;Zou等,J.Immunol.,170,1354,2003,WO2016/062990)产生。简言之,用酵母人工染色体(YAC)原核显微注射新鲜受精的卵母细胞之后产生转基因小鼠,所述酵母人工染色体包含与缺乏CH1结构域的小鼠免疫球蛋白恒定区基因、小鼠增强子和调控区组合的过量的人VH,D和J基因。
实施例2.用于免疫的抗原
免疫使用了重组纯化蛋白或人细胞系LNCap。重组人PMSA购自R&D(cat.no.4234-ZN),而LNCap细胞来自Sigma Aldrich(cat.no.89110211-1VL)。
实施例3.免疫方案
简而言之,8-12周龄的Tg/TKO小鼠各自接受总共50μg的重组纯化的人PSMA蛋白(在完全弗氏佐剂(Complete Freund’s Adjuvant)中乳化并皮下递送),或者腹膜内递送的在PBS中的1000万个LNCap细胞,接着用1-10μg的重组蛋白(在不完全弗氏佐剂中乳化,也在皮下施用,在初次引发后以不同的间隔施用)加强。最终剂量的纯化的重组人PSMA蛋白抗原在没有佐剂的情况下,在磷酸盐缓冲盐水中腹膜内施用。也可以采用替代的免疫途径和程序。例如,可以使用不同的佐剂或免疫加强程序来代替弗氏佐剂。DNA免疫通常是肌内递送或通过基因枪递送。来自这些细胞的转染细胞或膜制剂通常(虽然不是唯一的)经腹膜内施用。
实施例4.血清ELISA
免疫期间和之后,从小鼠收集血清并通过ELISA检查是否存在对免疫原的重链抗体应答。Nunc Maxisorp板(Nunc cat.no.443404)在4℃用50μl/孔的1μg重组抗原/ml PBS溶液包被过夜。倾析抗原溶液后,使用补充有0.05%(v/v)20(Sigma P1379)的PBS(制备自PBS Tablets,Oxoid cat.no.BR0014G)洗涤平板,随后用未添加Tween 20的PBS洗涤。为了阻断非特异性蛋白质相互作用,向孔中加入在PBS中的3%(w/v)脱脂奶粉溶液并将板在室温下温育至少1小时。在聚丙烯管或板中制备在3%MarvelTM/PBS中的血清稀释液并在室温下温育至少1小时,然后转移至封闭的ELISA板中,在此进一步温育至少1小时。然后用PBS/Tween20并且随后用PBS重复洗涤使得未结合的蛋白质被洗涤掉。然后将在PBS/3%Marvel中制备的生物素缀合的山羊抗小鼠IgG,Fcγ亚类1特异性抗体(Jackson cat.no.115-065-205)的溶液加入到每个孔中并在室温进一步温育至少一小时。通过使用PBS/Tween20和PBS重复洗涤除去未结合的检测抗体。然后将在3%Marvel/PBS中的Neutravidin-HRP溶液(Pierce cat.no.31030)加入到ELISA板中并使其结合至少30分钟。进一步洗涤后,使用TMB底物(Sigma cat.no.T0440)显色ELISA,并且10分钟后通过添加0.5M H2SO4溶液(Sigma cat.no.320501)停止反应。通过在450nm的光密度读数来确定吸光度。备选的测定,例如ELISPOT测定,也可用于检查免疫诱导的重链抗体应答。
实施例5.从免疫的小鼠生成文库
a)处理组织,RNA提取和cDNA制备
将来自每只免疫动物的脾脏,腹股沟和臂部淋巴结收集到中。对于每只动物,分别处理1/2个脾和4个淋巴结。首先,将组织匀化;随后将组织转移至裂解基质D珠管(MP Bio.Cat.no.116983001),加入600μl的含有β-巯基乙醇的RLT缓冲液(来自Qiagenkit cat.no.74104),之后在MP Bio Fastprep96匀浆器(cat#116010500)中以1600rpm匀浆60秒。将含有均化组织的试管转移至冰中,并通过以1200rpm离心5分钟使碎片沉淀。取出400μl上清液样品用于RT-PCR。首先,使用Qiagen试剂盒(cat.no.74104)按照生产商的方案提取RNA。然后使用Superscript III RT-PCR高保真试剂盒(Invitrogen cat.no.12574-035)将每种RNA样品用于制备cDNA。对于每个脾脏和淋巴结RNA样品,进行5次RT-PCR反应,每个反应都利用与VH1,VH2,VH3,VH4或VH6家族的引物组合的VH_J/F(长)引物。引物的细节如下。
表16.V10的引物
粗体残基与pUCG3具有同源性
表17.V23的引物
粗体残基与pUCG3具有同源性
用于简并引物的核苷酸的选择的密码为:R:A,G.Y:C,T。M:A,C。K:G,T。S:C,G。W:A,T。B:C,G,T。V:A,C,G。D:A,G,T。N:A,C,G,T
制备主混合物(Mastermix)用于RT-PCR反应。通过凝胶电泳证实370bp范围内的产物。
a)克隆入噬菌粒载体
这些研究中使用了噬菌粒载体pUCG3。使用基于PCR的方法从扩增的VH序列构建VH噬菌粒文库。使用以下程序:使用PCR产生线性化的pUCG3版本;用以下引物:pUCG3-pHENAPmut4 SEQ ID No.247pUCG3-pHENAPmut5mycHis SEQ ID No.248
具有GC缓冲液的Phusion高保真PCR主混合物和(cat.no.F532L,NEB)用于PCR反应。使用Fermentas GeneJet Gel纯化试剂盒(cat.no.K0691)根据制造商的说明书将PCR产物(3152bp)凝胶纯化,最后洗脱在40μl的洗脱缓冲液中。纯化的VH RT-PCR产物作为大引物与线性化的pUCG3一起用于产生用于转化和文库生成的噬菌粒产物。
实施例6.分离PSMA结合物的选择策略
根据公开的方法(Antibody Engineering,由Benny Lo编,第8章,p161-176,2004)进行文库噬菌体原液的制备和噬菌体展示选择。在大多数情况下,将与淘选方法组合的噬菌体展示用于分离结合VH结构域。然而,本领域已经很好地描述了各种不同的选择方法,包括在压力(stress)(例如热)下进行的可溶性的一个或更多个选择。还利用单价和多价噬菌体进行了促进内化抗PSMA VH的选择(专利US2009170792(A1)-2009-07-02)。简而言之,将冰冷的细胞培养基中的封闭噬菌体加入到4ml的含有2.5×106LnCAP细胞的冰冷的细胞培养基中。将噬菌体和细胞在冰上温育2小时,偶尔混合以防止细胞结块。通过在冰冷的PBS中洗涤5次除去未结合的或弱结合的噬菌体。然后通过在37℃在培养基中温育细胞使噬菌体内化,之后在4℃在低pH细胞剥离缓冲液中用5分钟的洗涤步骤去除结合于细胞外部的噬菌体。然后使用三甲胺裂解细胞以收获内化的噬菌体。在用于感染大肠杆菌之前,用Tris缓冲液中和经剥离和内化的级分。如上所述分析噬菌体输出,以对重组蛋白进行淘选选择。
实施例7.测定靶标结合
在一个或更多个以下测定中筛选来自不同选择的VH,以鉴定能够结合PMSA的特定VH。
a)结合ELISA
选择文库后,按照公布的方法(Antibody Engineering,Benny Lo编,第8章,p161-176,2004)通过噬菌体ELISA鉴定特异性VH抗体。噬菌体ELISA是针对靶蛋白和作为对照的无关抗原进行的。在一些情况下,通过ELISA而不是使用噬菌体ELISA来分析VH结构域的纯化提取物或粗提取物。在这些情况下,使用细菌周质提取物或纯化的VH。
b)FMAT直接细胞结合测定
针对PSMA-结合-His-标记的VH的产生,使用荧光微量测定技术(FMAT)筛选来自大肠杆菌的周质提取物,荧光微量测定技术(FMAT)是一种基于荧光的平台,其检测定位于微孔底部的珠子或细胞上的荧光(Dietz等,Cytometry23:177-186(1996),Miraglia等,J.Biomol.Screening4:193-204(1999)。使用标准程序使用全长人和食蟹猴PSMA在内部生成CHO TREX人和食蟹猴细胞系。LnCAP细胞购自Sigma Aldrich。
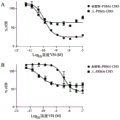
在FMAT直接结合测定中,通过单点筛选测试针对特异性结合CHO人PSMA,CHO食蟹猴PSMA和LnCAP细胞但不结合CHO亲本细胞的VH的存在测试Peripreps。对于滴定,通过末端His标签纯化的VH在FMAT测定缓冲液中连续稀释,然后如上所述测量结合(图1)。改进的变体显示与亲本VH相似的性质(图1b和1c)。
表18抗PSMAVH与表达PSMA的细胞系的结合的EC50值。数值在皮摩尔范围(制备自纯化的VH)
a)
b)抗PSMAVH与人PSMA-CHO结合的EC50值。所用接头长度为6GS(即(G4S)6)。
测序
如上鉴定的每个单独的VH克隆从噬菌粒测序,并基于VH种系和CDR3氨基酸相似性分组为单独的家族。代表性克隆进一步被表征。通过亲本克隆例如1.1和2.1的标准方法产生变体,包括种系变体。表1显示了家族1中克隆家族的序列。克隆1.8-1.30是1.1的变体。克隆1.21到1.30是改进的序列优化的变体,在CDR2序列中具有倾向校正。
实施例8-VH的表征
a)抗PMSA的特异性
按照实施例7(a)中所述的方法,通过ELISA确认单独VH对靶抗原的特异性。测试VH与PMSA的结合并显示不与无关蛋白质交叉反应。
b)使用Octet测量结合动力学
在ForteBio Octet RED 384仪器上测量纯化的抗PSMA VH抗体的结合动力学。将重组PMSA在pH 5的乙酸钠缓冲液(ForteBio,cat.no.18-1069)中稀释至20μg/ml并使用胺偶联化学(NHS-EDC胺偶联,ForteBio cat.no.18-1067和18-1033)偶联至ARG2G生物传感器(ForteBio cat.no.18-5092),随后在乙醇胺中淬灭(ForteBio cat.no.18-1071)。然后通过以下确定抗PSMA VH抗体的结合动力学:制备每种VH抗体的稀释系列(通常以VH的最高浓度15μg/ml开始的1∶2稀释系列),并且然后测量不同VH浓度的与PSMA偶联的生物传感器的结合。然后使用1∶1结合模型和ForteBio Octet DataAnalysis软件从(空白扣除的)传感图迹线确定VH结合动力学。检测了1-150nM和亚纳摩尔范围内的结合亲和力,并且Octet特征曲线的实例显示在图2中和在下表19中的其结合参数中。
表19
另外的家族成员,特别是亲本分子的变体,也如下使用从0.375μg/ml开始的1∶2稀释系列进行测试。如表20和21所示检测了低纳摩尔至皮摩尔范围的结合亲和力。
表20
| 克隆 | KD(nM) | Kdis(1/s) |
| 1.8 | 1.95 | 1.04E-03 |
| 1.10 | 0.67 | 4.18E-04 |
| 1.11 | 0.80 | 4.95E-04 |
| 1.12 | 0.55 | 4.28E-04 |
| 1.14 | 0.46 | 3.35E-04 |
| 1.16 | 0.44 | 3.65E-04 |
| 1.17 | 0.61 | 5.51E-04 |
| 1.18 | 0.59 | 5.72E-04 |
表21
| 克隆 | KD(nM) | Kdis(1/s) |
| 2.1 | 0.32 | 2.28E-04 |
| 2.13 | 0.99 | 7.43E-04 |
| 2.17 | 0.76 | 7.26E-04 |
| 2.15 | 4.72 | 3.44E-03 |
| 2.12 | 1.56 | 1.57E-03 |
| 2.22 | 2.62 | 2.44E-03 |
a)
| 克隆 | KD(nM) | Kdis(1/s) |
| 1.8 | 0.85 | 6.80E-04 |
| 1.17 | 0.58 | 3.92E-04 |
| 1.27 | 0.49 | 6.45E-04 |
b)
| 克隆 | KD(nM) | Kdis(1/s) |
| 1.8 | 1.95 | 1.04E-03 |
| 1.17 | 0.61 | 5.51E-04 |
| 1.27 | 0.49 | 6.45E-04 |
c)
还测试了使用Ni-NTA色谱法(通过C-末端His-标签)从周质提取物纯化的单结构域抗体。结果显示在下表中。如表22中所示检测了1-150nM和在低纳摩尔范围内的结合亲和力。
表22
c)使用荧光微量测定技术测量食蟹猴PSMA结合VH的内化
使用pH敏感性荧光染料green测量纯化的VH的内化。根据制造商的说明书用Green STP酯(Molecular Probes cat.no.P35369)标记抗His抗体(Millipore cat.no.05-949)。所有样品和试剂均在含有PBS和0.1%牛血清白蛋白的内化缓冲液(pH 7.4)中制备。将表达食蟹猴PSMA的CHO细胞以0.1×106个细胞/ml重新悬浮并将120nM DRAQ5加入到细胞悬液中。将VH(10μl)转移到384-孔黑色透明底板测定板(Costarcat.no.3655)中,加入10μl 40nMgreen标记的抗His抗体,接着加入20μl DRAQ5染色的细胞。平板在37℃温育2小时,然后平衡至室温。在488nm和640nm激发后,在TTPMirrorball读板仪上测量FL2(502nm-537nm)和FL5(677-800nm)通道中的荧光发射。数据在FL5周界和峰强度上被门控,使用门控数据的FL2中值平均荧光强度测定VH内化(图3)。
使用如上所述的pH敏感性荧光染料green来测量单结构域抗体1.1和1.2的变体的内化,不同之处在于将系列稀释的VH与green标记的抗His抗体在室温预温育30分钟,之后加入DRAQ5染色的CHO人PSMA克隆1A10细胞(20μl)。将平板在室温下温育2小时,然后测量荧光发射。测定中VH的活性显示在下表23中。
表23
a)
b)
d)使用His-ZAP测定测量结合PSMA的VH的内化
使用缀合至皂草素毒素的抗His抗体(His-ZAP Advanced targeting Systemscat.No.IT52)评估His标记的结合PSMA的VH的内化。His-ZAP试剂与VH结合并通过VH与细胞表面上的PSMA相互作用而内化。皂草素毒素从内体中的复合物释放并使核糖体失活,最终导致细胞死亡。
将表达人或食蟹猴PSMA的CHO细胞(30μl体积中的400个细胞/孔)接种到384孔黑色透明底组织培养物处理的测定板(Costar cat.no.3712)中的Hams F12培养基(Sigmacat.no.N6658)中并在37℃在CO2培养箱中温育过夜,所述Hams F12培养基含有10%胎牛血清,2mM L-谷氨酰胺,10μg/ml杀稻瘟菌素,300μg/ml博来霉素,青霉素/链霉素,1μg/ml四环素。将纯化的VH在培养基中连续稀释,然后加入等体积的40nM His-ZAP。在37℃温育30分钟后,将VH/His-ZAP样品(10μl)转移至细胞测定板中,并在37℃在CO2培养箱中温育72或48小时。在每个平板上设置His-ZAP对照孔(具有His-ZAP试剂的细胞)和背景对照(仅培养基)用于数据归一化。根据制造商的说明书,使用Cell Titer-Glo细胞生存力测定(Promegacat.no.G7571)在72或48小时温育后测定细胞生存力。使用BMG PHERAstar读板仪测量相对发光信号(RLU)。通过减去在不存在细胞时获得的RLU信号并表达为His-ZAP对照孔的背景校正信号的百分比将数据归一化。实例在图4A&B中给出。
对于LnCAP测定,将细胞(每孔2000个,100μl体积)接种到96孔TC-处理的板(Costar cat.No.3340)中的RPMI 1640培养基中,所述RPMI1640含有10%胎牛血清,2mM L-谷氨酰胺和青霉素/链霉素。纯化的VH在培养基中连续稀释,然后加入等体积的60nM His-ZAP。在37℃温育30分钟后,将VH/His-ZAP样品(100μl)转移至细胞测定板中,并在37℃在CO2培养箱中温育96小时。使用Cell Titer-Glo细胞生存力测定测量细胞生存力并如上所述分析数据。实例如图5所示。
确定单结构域抗体1.1和2.1的变体与结合的皂草素缀合的抗His抗体内化导致毒素介导的细胞死亡的能力。如上所述进行测定,不同之处在于CHO人PSMA克隆1A10细胞用于人PSMA测定,并且在测量细胞生存力之前将平板在37℃在CO2培养箱中温育72小时。测定中测试的单结构域抗体的活性显示在下表24中。
表24
a)
b)
测试了双互补位分子并显示了以下EC50值。
c)
实施例9-VH的稳定性
测试来自不同CDR3家族的VH的可显影性特征。
a)热稳定性:HPLC尺寸排阻色谱
将纯化的VH进行尺寸排阻色谱。简而言之,将纯化的VH在4℃或40℃下在PBS缓冲液中储存0-14天,然后使用含有PDA检测器(在280nm处检测)的Waters H-Class Bio UPLC在不同时间点进行分析,其中在Waters ACQUITY BEH SEC柱上进行分离。样品以10μl体积注射,并以0.4ml/分钟的流速在含有200mM NaCl,100mM磷酸钠,pH 7.4+5%丙-1-醇的流动相中运行。收集数据6分钟,并计算储存后与开始时(T=0)存在的单体相比的剩余单体的百分比。亲本分子显示出高稳定性。变体也进行了测试。
样品浓度变化:单价1.1变体:5.0mg/ml
单价2.1变体:3.5mg/ml
结果显示在下表中。
表25
表26
a)
b)
还测试了长达35天的长期稳定性并显示出良好的特征。
b)热稳定性:Mirror ball
将纯化的VH样品在40℃下温育0-8天,然后使用如实施例7(b)中详述的FMAT直接结合测定来测试与表达食蟹猴PSMA的CHO细胞的结合(图6A&B)。
c)使用均相时间分辨荧光(HTRF)测定评估VH血清稳定性。
将纯化的VH与食蟹猴血清混合并在37℃温育0-7天。然后使用HTRF测定评估样品与PSMA的结合。简言之,使用Pierce EZ-Link Micro-Sulfo-NHS-LC-生物素化试剂盒(Thermo Scientificcat.no.21935)对PSMA(R&D Systems cat.no.4234-ZN)进行生物素化。对于HTRF结合测定,所有样品和试剂均在含有PBS,0.1%(w/v)BSA和0.4M氟化钾的HTRF测定缓冲液中制备。在黑色384-浅孔板(Costar cat.no.3676)中以10μl的总测定体积,将VH(经C末端His-Myc标记)与3nM生物素化的PSMA,1.5nM链霉亲和素穴状化合物(Cisbiocat.no.610SAKLA)和10nM Anti-Myc-Alexa Fluor-647(AbD Seroteccat.n0.MCA2200AF647)在室温下温育至少3小时。在BMG PHERAstar读板仪上在337nm激发后测量620nm和665nm处的时间分辨荧光发射并且获得的数据显示在图7A,B和C中。
在另一个实验中,将纯化的VH与人血清在37℃混合0-7天,然后如实施例7(b)FMAT直接细胞结合测定中所述评估与huPSMA CHO 1A10细胞的结合。获得的数据显示在图8中并且EC50值显示在下面的表27和28中。
表27
| VH | EC50 |
| 2.1第0天 | 2.49E-10 |
| 2.1第1天 | 2.54E-10 |
| 2.1第4天 | 2.60E-10 |
| 2.1第7天 | 3.01E-10 |
| 2.17第0天 | 2.30E-10 |
| 2.17第1天 | 2.10E-10 |
| 2.17第4天 | 2.28E-10 |
| 2.17第7天 | 2.38E-10 |
| 2.15第0天 | 2.66E-10 |
| 2.15第1天 | 4.97E-10 |
| 2.15第4天 | 3.93E-10 |
| 2.15第7天 | 3.76E-10 |
| 2.22第0天 | 3.05E-10 |
| 2.22第1天 | 2.91E-10 |
| 2.22第4天 | 3.40E-10 |
| 2.22第7天 | 3.28E-10 |
表28
a)
| VH | EC50 |
| 1.8第0天 | 1.7E-10 |
| 1.8第1天 | 2.2E-10 |
| 1.8第4天 | 2.5E-10 |
| 1.8第7天 | 2.7E-10 |
| 1.17第0天 | 1.6E-10 |
| 1.17第1天 | 1.6E-10 |
| 1.17第4天 | 1.8E-10 |
| 1.17第7天 | 1.5E-10 |
| 1.27第0天 | 1.3E-10 |
| 1.27第1天 | 1.1E-10 |
| 1.27第4天 | 1.2E-10 |
| 1.27第7天 | 1.1E-10 |
b)
c)为了评估不同双互补位组合的血清稳定性,将纯化的双互补位VH与人血清在37℃下混合0-7天,然后如实施例7(b)FMAT直接细胞结合测定中所述评估与huPSMA CHO细胞的结合。获得EC50值。
d)评估VH热稳定性
使用MicroCal VP-Capillary DSC(Malvern)进行差示扫描量热法(DSC)。在10和90℃之间使用60℃/分钟的扫描速率运行300μl在PBS中的0.25mg/ml的蛋白质。使用MicroCal软件分析数据。
结果显示在下表29中。
表29
a)
b)
实施例10小鼠中的成像研究
将VH(VH1.1,VH2.1和具有延长的半衰期的VH2.1)注射入小鼠。小鼠含有PSMA阳性(+)和PSMA阴性(-)肿瘤。研究进行如下:
·每只小鼠~100MBq的Tc-99m注射活性
·在5min、30min、60min、3hr、6hr&24hr的SPECT/CT。
·不同时间点显示的图像
·成像后离体生物分布和放射自显影
·阴性对照VH(αHEL4)
半衰期延长的VH包含具有以下序列的抗小鼠血清白蛋白(抗MSA)VH:SEQ ID NO:249。
特别是与对照单克隆IgG抗PSMA抗体相比,这些实验显示出高水平的特异性肿瘤靶向,更快的渗透和注射剂量对表达PSMA的(PSMA+)肿瘤的更大累积。这可以通过延长VH的半衰期来进一步改善。此外,数据显示裸VH的快速清除。结果显示在图9至15中。
实施例11表位作图
在串联表位中,使用Octet RED 384进行针对彼此的PSMA结合VH的作图。然后使用1∶1结合模型和ForteBio Octet DataAnalysis软件,从(减去参考传感器的)传感图迹线确定VH结合。也参见实施例8b。表30中显示了表位分箱结果。一些克隆显示了部分封闭。
表30
在进一步的实验中,进一步表征单结构域抗体1.1和2.1之间的表位竞争。使用胺偶联第二代试剂盒(ForteBio)将PSMA偶联到AR2G生物传感器上,然后将其用于使用OctetRED384进行的表位分箱实验。在这些实验中,将每个VH稀释至4μg/ml的浓度。生物传感器不负载VH或负载2.1或1.1直到与PSMA的结合达到饱和水平。然后在进行第二结合步骤之前,将这些传感器短暂地浸入PBS/Tween中。第二结合步骤包括将生物传感器浸入仅含有相同VH或含有2.1和1.1两者的孔中。第一VH在后一种组合中的存在确保其继续饱和其PSMA结合位点。然后使用ForteBio分析软件研究结合特征曲线。获得的这些数据证明单结构域抗体2.1和1.2结合PSMA上不同的表位。
实施例12成像研究
在这些研究中测试了以下构建体:
VH 2.1.
VH 2.1.-HIS,1.2mg/ml
SEQ ID NO.253
VH 1.1
VH 1.1-HIS
SEQ ID NO.254
VH 1.1-Hel4
HEL-4-HIS
SEQ ID NO.255
VH 2.1-VH 2.1
VH 2.1-6GS-VH 2.1SEQ ID NO.256
VH
2.1-VH 1.1
VH 2.1-6GS-VH 1.1SEQ ID NO.257
本研究中使用的所有VH结构域都在大肠杆菌中表达。如实施例7a所述,使用镍亲和层析和尺寸排阻层析(SEC)从过滤的上清液中纯化蛋白质。在缓冲液交换到储存缓冲液中之后,使用旋转浓缩器浓缩一些蛋白质。使用SDS-PAGE和分析型SEC分析蛋白质纯度。使用重组蛋白和/或表达PSMA的细胞来检查与PSMA的结合。通过将蛋白质加热至40℃持续延长的时间段(从过夜至4周)并测量蛋白质降解程度来检查稳定性。将蛋白质的等分试样贮存在-80℃直至使用。
共焦荧光显微镜方法,用于测试表达PSMA的细胞系中的感兴趣的VH(以单价、二价和双互补位格式)与内吞作用LAMP-1的标志物(染色溶酶体)和EEA-1的标志物(染色早期核内体)之间共定位的发生。使用结合PSMA的IgG基准抗体作为阳性对照。结果证明二价和双互补位VH构建体的内化得到改善。
实验方案
所用细胞系是CHO T-Rex huPSMA细胞系。
1)在实验前一天用四环素诱导CHO T-Rex huPSMA细胞用于PSMA表达,并铺在盖玻片上。
2)在第二天,将细胞与包含500nM的测试VH(以其单价、二价或双互补位格式)的培养基或与阳性对照一起温育。
3)首先将样品在冰上温育30分钟以阻断胞吞作用,然后在RT下用4%PFA固定10分钟,接着在PBS中洗涤3次。将一式两份的样品进一步在37℃温育2小时以触发胞吞作用,然后固定。
4)固定样品后,用缓冲液渗透。
5)使用在0.5%BSA/PBS+0.05%Tween中以1∶2000稀释的抗人488抗体,将与阳性对照一起温育的细胞染色1小时,随后在PBS+0.05%Tween中洗涤三次(每次5分钟)。
6)使用第一抗HIS抗体(小鼠),将与单价或二价/双互补位测试VH一起温育的细胞染色1小时,然后洗涤,然后用第二抗小鼠488抗体温育1小时,然后洗涤。
7)使用针对早期核内体抗原1(EEA-1)或溶酶体膜抗原1(LAMP-1)(都是兔)的一抗将溶酶体和核内体染色1小时。细胞进一步与抗兔-647二抗RT温育1小时,然后洗涤。
8)所有样品也用HOECHST 1∶1000(0.5μg/ml)染色5分钟,然后洗涤。
9)将盖玻片装入到磨砂端载玻片中,并使用NIKON A1R共焦系统成像。
使用程序NIS-ELEMENTS AR拍摄照片。
使用的激光线是:407.7nm(HOECHST)、487.7nm(VH/单克隆基准)、639.7(LAMP-1、EEA-1)
目标:Apo60x油λS DIC N2
对于共焦模式:针孔尺寸(μm):39.6、Z步骤:0.49μm。
使用表达人PSMA的CHO细胞(15000/孔)进行进一步的成像研究,将其接种到HamsF12(Sigma N6658)培养基中的96孔Poly-L-赖氨酸(Sigma P4707)包被的平板(PerkinElmer 6005550)上,所述Hams F12培养基含有10%胎牛血清、2mM L-谷氨酰胺、10μg/ml杀稻瘟菌素、300μg/ml博来霉素、青霉素/链霉素、1μg/ml四环素,并在CO2培养箱中于37℃温育过夜。将VH加入到平板中,并在4℃温育30分钟,随后在37℃温育2小时。用PBS洗涤平板三次,然后将细胞在4%多聚甲醛中固定,并用0.5%皂苷透化。通过用抗His(Millipore05-949)和抗小鼠AF488(Jackson ImmunoResearch 115-545-098)染色来检测内化的VH。用LAMP-1(Abcam Ab24170)和抗兔AF647(Jackson ImmunoResearch111-605-008)对溶酶体进行染色。使用Hoescht染色剂(Life Technologies H3570)将细胞核染色。使用IN CellAnalyzer 6000使平板成像,并使用ImageJ软件处理图像。
实施例13与免疫缀合物缀合的MMAE毒素的体外效力
使用体外细胞毒性测定确定缀合MMAE毒素的VH内化至表达PSMA的细胞中从而导致细胞杀伤的能力。将稳定表达人PSMA的人细胞(DU-145,ATCC HTB-81)或匹配的PSMA阴性细胞以每孔3000个细胞接种到384孔黑色透明底组织培养物处理的测定板中的RPMI 1640培养基中并在37℃的CO2培养箱中温育过夜,所述培养基含有10%胎牛血清,2mM L-谷氨酰胺,1X青霉素/链霉素。然后将细胞与连续稀释的缀合MMAE毒素的VH温育48或72小时。未处理的对照孔(不存在缀合毒素的VH的细胞)和背景对照孔(仅培养基)设置于每个平板上用于数据归一化。根据制造商的说明书,使用Cell Titer-Glo细胞生存力测定(PromegaG7571)在温育后确定细胞杀伤。使用BMG PHERAstar读板仪测量相对发光信号(RLU)。通过减去背景对照孔中获得的RLU信号将数据归一化,然后表示为未处理对照孔的%(%存活率)。图16说明在代表性实验(48小时温育)中使用表达人PSMA的人细胞系和匹配的亲本(即未转染的)PSMA阴性细胞系获得的剂量应答曲线。表31总结了针对缀合MMAE的构建体获得的IC50值和最大%细胞杀伤。使用HiPEGTM技术(WO 2009/047500;Cong等,(2012)Bioconjugate Chem.2012,23,248-263)将Crescendo的VH缀合至MMAE;使用ThioBridgeTM技术(WO 2016063006;WO 2005/007197;Balan等,(2007)BioconjugateChem.,18,61-76)产生阳性ADC对照。抗PSMA-MMAE缀合的VH特异性杀伤PSMA阳性细胞,对于PSMA阴性对照细胞系观察到最小的细胞杀伤。由靶向PSMA不同表位的两个VH组成的双互补位比单价或二价PSMA VH构建体更有效。DU145测定用48小时和72小时HDC温育进行。这对测量的IC50值和%最大杀伤有影响,但预期不会影响不同HDC格式的排名。对于筛选,48小时温育对于更高通量是优选的。使用48小时温育,没有任何测试的构建体达到100%细胞杀伤(即使在测试的最高浓度下)。最大的应答在约70-85%趋平(见表31)。表31显示了IC50值,图17显示了使用72小时温育时间观察到的更高的最大%细胞杀伤(n=1数据)。
表31.48小时温育后用表达人PSMA的人细胞系获得的体外细胞毒性数据总结。
表32:72小时温育后用表达人PSMA的人细胞系获得的体外细胞毒性数据总结。
观察到的单价构建体的效力顺序为VH2.1>VH1.1>VH3.1。
制备HumabodyTM药物缀合物(HDC)的程序
在进行缀合反应之前,在MeCN中制备缀合试剂HiPEGTM val-cit-PAB-MMAE(图18)的储备溶液。将HumabodyTM(在PBS中0.9mg/mL;20mM EDTA,pH7.5)的溶液与HiPEGTM val-cit-PAB-MMAE试剂(1.5当量/HumabodyTM;5%(v/v)最终MeCN浓度)轻轻混合并在22℃温育19小时。19小时后,将缀合反应物与等体积的pH 7.5的600mM磷酸钠缓冲液(150mM NaCl;20mM EDTA)混合并冷却至4℃。在0.1M NaOH中制备1mg/mL NaBH4溶液的储备溶液。将NaBH4溶液的两份等分试样(每个试剂10当量)加入到冷却的缀合反应中,加入之间间隔30分钟。再过30分钟间隔后,通过使用TOSOH ToyoPearl Pheny1-650S柱的疏水相互作用色谱(HIC)纯化粗混合物。将样品结合在柱上并使用50mM磷酸钠(2M NaCl),pH 7(缓冲液A)洗涤,并使用pH 7的50mM磷酸钠(20%v/v异丙醇)(缓冲液B)梯度洗脱。将含有单加载产物的级分合并并使用配有5kDa MWCO PES膜的Vivaspin20浓缩器进行浓缩。使用PD10柱将浓缩级分缓冲液交换到DPBS中,并且使用0.2μm PVDF注射器过滤单元无菌过滤缓冲液交换材料。
HiPEG val-cit-PAB-MMAE部分通过VH上的C端His6标签附接。每个“有效载荷”毒素分子的附接需要两个组氨酸。Humabody VH,DAR=1的那些被纯化用于细胞毒性研究,在某些情况下未达到精确的DAR 1(见下表)。在本文的实施例中,单个MMAE部分被附接,但多个有效载荷是可能的(DAR>1)。
药物:抗体比率(DAR)为3.5的对照ADC的制备程序
阳性对照抗体Pro_006是由US8470330内所述的重链和轻链序列组成的抗PSMA抗体,并且示例为抗体006。
缀合1:将在反应缓冲液(20mM磷酸钠,150mM NaCl;20mM EDTA,pH 7.5)中的mAbPro_006(5.07mg/mL)的溶液加热至40℃ 15分钟。将TCEP(5mM,2当量/mAb)加入mAb溶液中,轻轻混合并在40℃温育1小时。以2.8mM在DMF中制备缀合试剂mc-val-cit-PAB-MMAE(图19)的储备溶液。将还原的mAb冷却至22℃,用反应缓冲液稀释至4.2mg/mL,并加入mc-val-cit-PAB-MMAE(5.25当量/mAb)。缀合混合物在22℃温育2小时。在22℃下用50mM N-乙酰基-L-半胱氨酸(20当量,超过试剂)处理粗缀合混合物30分钟。使用装有30kDa MWCO PES膜的Vivaspin20浓缩器将反应混合物针对DPBS进行渗滤。使用Centripure P50柱将渗滤的ADC溶液缓冲液交换到DPBS中。样品的DAR通过HIC评估(平均DAR=3.21)。
缀合2:将在反应缓冲液(20mM磷酸钠150mM NaCl;20mM EDTA)pH 7.5中的mAbPro_006(5.07mg/mL)溶液加热至40℃ 15分钟。将TCEP(5mM,2.75当量/mAb)加入mAb溶液中,轻轻混合并在40℃温育1小时。以4.0mM在DMF中制备缀合试剂mc-val-cit-PAB-MMAE(图19)的储备溶液。将还原的mAb冷却至22℃,用反应缓冲液稀释至4.2mg/mL,并加入mc-val-cit-PAB-MMAE(7当量/mAb)。缀合混合物在22℃温育2小时。在22℃下用50mM N-乙酰基-L-半胱氨酸(20当量,超过试剂)处理粗缀合混合物30分钟。使用装有30kDa MWCO PES膜的Vivaspin20浓缩器将反应混合物针对DPBS进行渗滤。使用Centripure P50柱将渗滤的ADC溶液缓冲液交换到DPBS中。样品的DAR通过HIC评估(平均DAR=4.52)。
产生平均DAR 3.5ADC:ADC 1(DAR 3.21)和ADC 2(DAR 4.52)以4∶1摩尔比混合,以制备具有中间DAR的ADC。所得样品使用0.2μm PVDF注射器过滤单元进行无菌过滤。样品的DAR通过HIC评估(平均DAR=3.45)。
半衰期延长的HDC的体外效价
使用DU145细胞杀伤测定(72小时)评价半衰期延长的HDC的体外效价。
产生表34中描述的这种材料以测试向HDC中添加半衰期延长部分的效果。使用结合MSA的VH(SEQ ID No.528)产生半衰期延长的版本(HLE)。使用DU145细胞杀伤测定(72小时)评价体外效价。
表34 PSMA-DU145细胞毒性测定(72小时)的IC50值:
Claims (29)
1.能够结合人PSMA的结合分子,其包含选自下列之一的单人可变重链结构域(VH)抗体:单VH结构域抗体,其包含含有SEQ ID NO.1的CDR1序列、含有SEQ ID NO.2的CDR2序列和含有SEQ ID NO.3的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.5的CDR1序列、含有SEQ ID NO.6的CDR2序列和含有SEQ ID NO.7的CDR3序列;单VH结构域抗体,其包含含有SEQID NO.9的CDR1序列、含有SEQ ID NO.10的CDR2序列和含有SEQ ID NO.11的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.13的CDR1序列、含有SEQ ID NO.14的CDR2序列和含有SEQ ID NO.15的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.17的CDR1序列、含有SEQ ID NO.18的CDR2序列和含有SEQ ID NO.19的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.21的CDR1序列、含有SEQ ID NO.22的CDR2序列和含有SEQ ID NO.23的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.25的CDR1序列、含有SEQ ID NO.26的CDR2序列和含有SEQ ID NO.27的CDR3序列;单VH结构域抗体,其包含含有SEQ ID NO.29的CDR1序列、含有SEQ ID NO.30的CDR2序列和含有SEQ ID NO.31的CDR3序列;单结构域VH结构域抗体,其包含含有SEQ ID NO.33的CDR1序列、含有SEQ ID NO.34的CDR2序列和含有SEQ ID NO.35的CDR3序列;或单VH结构域抗体,包含含有SEQ ID NO.37的CDR1序列、含有SEQ ID NO.38的CDR2序列和含有SEQ ID NO.39的CDR3序列。
2.根据权利要求1所述的结合分子,其中所述单结构域VH结构域抗体包含选自SEQ IDNO 4、8、12、16、20、24、28、32、36或40的序列。
3.结合分子,其包含根据权利要求1或2所述的能够结合人PSMA的第一单人重链可变免疫球蛋白(VH)结构域抗体和能够结合人PSMA的第二单VH结构域抗体。
4.根据权利要求3所述的结合分子,其中所述第一VH结构域和所述第二VH结构域结合人PSMA上的相同表位。
5.根据权利要求3所述的结合分子,其中所述第一单VH结构域抗体结合PSMA上的第一表位,且所述第二单VH结构域抗体结合PSMA上的第二表位,其中所述第一和所述第二表位不相同。
6.根据权利要求5所述的结合分子,其中所述第二VH结构域抗体选自表2。
7.根据权利要求3-5中任一项所述的结合分子,其中所述第一单VH结构域抗体位于C或N末端。
8.根据权利要求3-6中任一项所述的结合分子,其中所述第一和第二VH结构域通过肽共价连接。
9.根据权利要求8所述的结合分子,其中所述肽的长度为3至50个氨基酸。
10.根据权利要求8或8所述的结合分子,其中所述接头包含甘氨酸和丝氨酸氨基酸残基。
11.根据权利要求8-10中任一项所述的结合分子,其中所述肽接头由式(Gly4Ser)n组成,其中n=1-10。
12.根据前述权利要求所述的结合分子,其中所述结合分子与毒素,酶,放射性同位素或其他化学部分缀合。
13.根据前述权利要求所述的结合分子,其获自或能够获自不产生任何功能性内源轻链或重链的小鼠。
14.药物组合物,其包含根据前述权利要求中任一项所述的结合分子和药物载体。
15.治疗前列腺癌或前列腺病症的方法,其包括施用治疗有效量的根据权利要求1至13中任一项所述的结合分子或根据权利要求14所述的药物组合物。
16.根据权利要求1至13中任一项所述的结合分子或根据权利要求14所述的药物组合物,其用作药物。
17.根据权利要求1至13中任一项所述的结合分子或根据权利要求14所述的药物组合物,其用于治疗前列腺癌或前列腺病症。
18.根据权利要求1至13中任一项所述的结合分子或根据权利要求14所述的药物组合物在制备用于治疗前列腺癌或前列腺病症的药物中的用途。
19.用于降低人PSMA活性的体内或体外方法,其包括使人PSMA与根据权利要求1至13中任一项所述的结合分子接触。
20.通过免疫测定确定测试样品中PSMA存在的方法,其包括使所述样品与根据权利要求1至13中任一项所述的结合分子和至少一种可检测标记接触。
21.根据权利要求13所述的方法,其中所述方法包括诊断或评估患者的预防性或治疗性治疗的功效。
22.分离的核酸分子,其包含编码根据权利要求1至13中任一项所述的结合分子的核苷酸序列。
23.构建体,其包含根据权利要求21所述的核酸。
24.宿主细胞,其包含根据权利要求21所述的核酸或根据权利要求23所述的构建体。
25.产生根据权利要求1至13中任一项所述的结合分子的方法,其包括在宿主细胞中表达编码所述结合分子的核酸并从宿主细胞培养物中分离所述结合分子。
26.试剂盒,其包含根据权利要求1至13中任一项所述的结合分子或根据权利要求14所述的药物组合物。
27.多特异性结合分子,其包含根据权利要求1至13中任一项所述的单VH结构域抗体。
28.根据权利要求1至13中任一项所述的结合分子,其中所述结合分子能够被细胞内化。
29.免疫缀合物,其包含根据权利要求1至13中任一项所述的单VH结构域抗体。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1711068.5 | 2017-07-10 | ||
| GBGB1711068.5A GB201711068D0 (en) | 2017-07-10 | 2017-07-10 | Therapeutic molecules binding PSMA |
| PCT/GB2018/051941 WO2019012260A1 (en) | 2017-07-10 | 2018-07-09 | THERAPEUTIC MOLECULES BINDING TO PSMA |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN111051348A true CN111051348A (zh) | 2020-04-21 |
Family
ID=59676551
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201880055554.8A Pending CN111051348A (zh) | 2017-07-10 | 2018-07-09 | 结合psma的治疗分子 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US11401342B2 (zh) |
| EP (1) | EP3652213A1 (zh) |
| JP (1) | JP7346378B2 (zh) |
| CN (1) | CN111051348A (zh) |
| GB (1) | GB201711068D0 (zh) |
| WO (1) | WO2019012260A1 (zh) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11236174B2 (en) | 2016-01-12 | 2022-02-01 | Crescendo Biologics Limited | Therapeutic molecules |
| GB201607968D0 (en) | 2016-05-06 | 2016-06-22 | Crescendo Biolog Ltd | Chimeric antigen receptor |
| EP3565840A1 (en) | 2017-01-06 | 2019-11-13 | Crescendo Biologics Limited | Single domain antibodies to programmed cell death (pd-1) |
| GB201802573D0 (en) | 2018-02-16 | 2018-04-04 | Crescendo Biologics Ltd | Therapeutic molecules that bind to LAG3 |
| IL279062B2 (en) | 2018-06-01 | 2024-02-01 | Eisai R&D Man Co Ltd | Antibody drug conjugates of splicing modulators and methods of use |
| AU2019397062A1 (en) | 2018-12-13 | 2021-05-06 | Eisai R&D Management Co., Ltd. | Herboxidiene antibody-drug conjugates and methods of use |
| MX2021012205A (es) * | 2019-04-05 | 2022-02-21 | Teneobio Inc | Anticuerpos de cadena pesada que se unen al psma. |
| AU2020275926A1 (en) * | 2019-05-15 | 2021-11-18 | Crescendo Biologics Limited | Binding molecules |
| WO2023199069A1 (en) | 2022-04-14 | 2023-10-19 | Crescendo Biologics Limited | Chimeric antigen receptor that binds mesothelin |
| GB202205589D0 (en) | 2022-04-14 | 2022-06-01 | Crescendo Biologics Ltd | Mesothelin binders |
Family Cites Families (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0115256D0 (en) | 2001-06-21 | 2001-08-15 | Babraham Inst | Mouse light chain locus |
| CA2464239C (en) | 2001-10-23 | 2016-07-12 | Psma Development Company, L.L.C. | Psma antibodies and protein multimers |
| US20050215472A1 (en) | 2001-10-23 | 2005-09-29 | Psma Development Company, Llc | PSMA formulations and uses thereof |
| GB2398784B (en) | 2003-02-26 | 2005-07-27 | Babraham Inst | Removal and modification of the immunoglobulin constant region gene cluster of a non-human mammal |
| GB0313132D0 (en) | 2003-06-06 | 2003-07-09 | Ich Productions Ltd | Peptide ligands |
| GB0316294D0 (en) | 2003-07-11 | 2003-08-13 | Polytherics Ltd | Conjugated biological molecules and their preparation |
| CN101124249B (zh) | 2005-02-18 | 2011-06-29 | 米德列斯公司 | 抗前列腺特异性膜抗原(psma)的人单克隆抗体 |
| AU2006341615A1 (en) | 2005-08-03 | 2007-10-18 | Fraunhofer Usa, Inc. | Compositions and methods for production of immunoglobulins |
| CN101820920B (zh) | 2007-10-09 | 2014-08-06 | 宝力泰锐克斯有限公司 | 新的缀合蛋白质和肽 |
| US20100122358A1 (en) | 2008-06-06 | 2010-05-13 | Crescendo Biologics Limited | H-Chain-only antibodies |
| KR20140127816A (ko) | 2012-02-22 | 2014-11-04 | 더 트러스티스 오브 더 유니버시티 오브 펜실바니아 | 암의 치료에 유용한 t 세포의 지속성 집단을 생성시키기 위한 조성물 및 방법 |
| CN103087171B (zh) | 2012-12-24 | 2015-01-14 | 中国人民解放军第四军医大学 | 一种用于前列腺癌早期诊断和治疗的抗psma/fitc双特异性抗体及其制备方法 |
| WO2014141192A1 (en) | 2013-03-15 | 2014-09-18 | Erasmus University Medical Center | Generation of heavy chain-only antibodies |
| CN103333249A (zh) | 2013-06-14 | 2013-10-02 | 广州康合生物科技有限公司 | 一种抗前列腺特异性膜抗原(psma)的单克隆抗体及其应用 |
| US20170335281A1 (en) | 2014-03-15 | 2017-11-23 | Novartis Ag | Treatment of cancer using chimeric antigen receptor |
| TWI701042B (zh) | 2014-03-19 | 2020-08-11 | 美商再生元醫藥公司 | 用於腫瘤治療之方法及抗體組成物 |
| US10851149B2 (en) | 2014-08-14 | 2020-12-01 | The Trustees Of The University Of Pennsylvania | Treatment of cancer using GFR α-4 chimeric antigen receptor |
| CN114774466A (zh) | 2014-10-22 | 2022-07-22 | 克雷森多生物制剂有限公司 | 转基因小鼠 |
| EP3220956B1 (en) | 2014-10-24 | 2023-08-09 | Abzena (UK) Limited | Conjugates and conjugating reagents |
| CN105384825B (zh) | 2015-08-11 | 2018-06-01 | 南京传奇生物科技有限公司 | 一种基于单域抗体的双特异性嵌合抗原受体及其应用 |
| US11236174B2 (en) | 2016-01-12 | 2022-02-01 | Crescendo Biologics Limited | Therapeutic molecules |
| CN105968205B (zh) | 2016-02-03 | 2019-04-26 | 中国人民解放军第三军医大学第三附属医院 | 一种抗前列腺特异性膜抗原的纳米抗体 |
| CN105968204B (zh) | 2016-02-03 | 2020-01-21 | 中国人民解放军第三军医大学第一附属医院 | 一种抗前列腺特异性膜抗原的单域重链抗体 |
| CN105968203A (zh) | 2016-02-03 | 2016-09-28 | 南昌大学 | 一种抗前列腺特异性膜抗原胞外区的单域重链抗体 |
| GB201607968D0 (en) | 2016-05-06 | 2016-06-22 | Crescendo Biolog Ltd | Chimeric antigen receptor |
| EP3710477A1 (en) * | 2017-11-13 | 2020-09-23 | Crescendo Biologics Limited | Single domain antibodies that bind to cd137 |
-
2017
- 2017-07-10 GB GBGB1711068.5A patent/GB201711068D0/en not_active Ceased
-
2018
- 2018-07-09 EP EP18749051.1A patent/EP3652213A1/en active Pending
- 2018-07-09 WO PCT/GB2018/051941 patent/WO2019012260A1/en unknown
- 2018-07-09 CN CN201880055554.8A patent/CN111051348A/zh active Pending
- 2018-07-09 JP JP2020500832A patent/JP7346378B2/ja active Active
- 2018-07-09 US US16/627,968 patent/US11401342B2/en active Active
Non-Patent Citations (2)
| Title |
|---|
| HAMED ZARE等: "Production of nanobodies against prostate-specific membrane antigen (PSMA) recognizing LnCaP cells" * |
| MEHDI EVAZALIPOUR: "Camel Heavy Chain Antibodies Against Prostate-Specific Membrane Antigen" * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP7346378B2 (ja) | 2023-09-19 |
| JP2020530285A (ja) | 2020-10-22 |
| GB201711068D0 (en) | 2017-08-23 |
| US11401342B2 (en) | 2022-08-02 |
| WO2019012260A1 (en) | 2019-01-17 |
| US20200131274A1 (en) | 2020-04-30 |
| EP3652213A1 (en) | 2020-05-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108473589B (zh) | 结合前列腺特异性膜抗原(psma)的分子 | |
| JP7346378B2 (ja) | 治療的psma結合分子 | |
| ES2932777T3 (es) | Sustratos de matriptasa y activador del plasminógeno-u y otros motivos escindibles y métodos de uso de los mismos | |
| CN107135654B (zh) | 巨胞饮人类抗cd46抗体和靶向癌症疗法 | |
| CN110740754B (zh) | 一种抗间皮素抗体及其抗体药物缀合物 | |
| JP6541236B2 (ja) | インスリン様成長因子1受容体特異的抗体及びそれらの使用 | |
| Nováková et al. | Novel monoclonal antibodies recognizing human prostate‐specific membrane antigen (PSMA) as research and theranostic tools | |
| JP7458686B2 (ja) | 抗ネクチン-4抗体、それを含むコンジュゲート、及びその適用 | |
| US20240101706A1 (en) | Development of new monoclonal antibodies recognizing human prostate-specific membrane antigen (psma) | |
| ES2528718T3 (es) | Diana para linfocitos B | |
| US20240174763A1 (en) | Anti-human cd73 antibody and use thereof | |
| WO2023025243A1 (zh) | 抗Nectin-4抗体、药物缀合物及其制备方法和用途 | |
| ES2831651T3 (es) | Uso de anticuerpos y antagonistas dirigidos contra Lrg1 en un tratamiento | |
| US20230391852A1 (en) | Single domain antibodies targeting sars coronavirus spike protein and uses thereof | |
| CN116271079A (zh) | 一种抗dll3抗体及其制备方法、其药物偶联物和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination |