CN103257070A - 用于平衡同位素稀释质谱样品的方法 - Google Patents
用于平衡同位素稀释质谱样品的方法 Download PDFInfo
- Publication number
- CN103257070A CN103257070A CN2013100318147A CN201310031814A CN103257070A CN 103257070 A CN103257070 A CN 103257070A CN 2013100318147 A CN2013100318147 A CN 2013100318147A CN 201310031814 A CN201310031814 A CN 201310031814A CN 103257070 A CN103257070 A CN 103257070A
- Authority
- CN
- China
- Prior art keywords
- sample
- isotope
- species
- balance
- analyte
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N1/00—Sampling; Preparing specimens for investigation
- G01N1/28—Preparing specimens for investigation including physical details of (bio-)chemical methods covered elsewhere, e.g. G01N33/50, C12Q
- G01N1/44—Sample treatment involving radiation, e.g. heat
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N1/00—Sampling; Preparing specimens for investigation
- G01N1/28—Preparing specimens for investigation including physical details of (bio-)chemical methods covered elsewhere, e.g. G01N33/50, C12Q
- G01N1/40—Concentrating samples
- G01N1/405—Concentrating samples by adsorption or absorption
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/14—Heterocyclic carbon compound [i.e., O, S, N, Se, Te, as only ring hetero atom]
- Y10T436/141111—Diverse hetero atoms in same or different rings [e.g., alkaloids, opiates, etc.]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/14—Heterocyclic carbon compound [i.e., O, S, N, Se, Te, as only ring hetero atom]
- Y10T436/142222—Hetero-O [e.g., ascorbic acid, etc.]
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/19—Halogen containing
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/20—Oxygen containing
- Y10T436/200833—Carbonyl, ether, aldehyde or ketone containing
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/20—Oxygen containing
- Y10T436/203332—Hydroxyl containing
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/21—Hydrocarbon
- Y10T436/212—Aromatic
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/24—Nuclear magnetic resonance, electron spin resonance or other spin effects or mass spectrometry
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/25—Chemistry: analytical and immunological testing including sample preparation
- Y10T436/25375—Liberation or purification of sample or separation of material from a sample [e.g., filtering, centrifuging, etc.]
- Y10T436/255—Liberation or purification of sample or separation of material from a sample [e.g., filtering, centrifuging, etc.] including use of a solid sorbent, semipermeable membrane, or liquid extraction
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/25—Chemistry: analytical and immunological testing including sample preparation
- Y10T436/25625—Dilution
Abstract
本发明涉及一种用于平衡同位素稀释质谱样品的方法,包括以下步骤:a)向溶液中添加一定量或浓度的同位素标记分析物类似物以产生预标记微波介质;b)向所述预标记微波介质中添加包含或被怀疑包含与所述同位素标记分析物类似物对应的兴趣分析物的样品,以产生可微波溶液;c)通过将所述可微波溶液培养1秒至1小时而平衡所述兴趣分析物,以产生平衡样品;以及d)对所述平衡样品进行质谱分析。该方法利用通过同时平衡相较于液相和气相具有很多优势的固相来促进平衡,并实现本领域已知的同位素稀释质谱法和物种化同位素稀释质谱法分析的自动化。
Description
本申请是申请号为200780050971.5,申请日为2007年12月7日,发明名称为“固相及催化实现的自动同位素稀释和物种化同位素稀释质谱法”的中国专利申请的分案申请。
相关申请的交叉引用
本申请主张2006年12月7日申请的、名为Equilibration Methods UsingMicrowave Radiation的美国临时专利申请No.60/873,383的权利,该案的内容以引用的方式并入本文。
背景技术
技术领域
本发明涉及一种促进浓缩同位素和标记物种与天然同位素物种的平衡的方法,其使用同位素浓缩物种的固相固定(immobilize)以及分析兴趣所在的天然物种和标记物种的同位素在固相上的平衡和同时萃取、分离和/或选择,还涉及提高IDMS和SIDMS的便携性的方法以及其他提高效率及平衡和自动化的方法。
相关技术的说明
IDMS和SIDMS基于浓缩同位素与待测的严格物种分析物的平衡。本文引用了下列描述同位素稀释质谱法(IDMS)和物种化同位素稀释质谱法(SIDMS)的专利以及平衡解决方案和这些专利的使用——参见U.S.Pat.No.5,414,259和U.S.Pat.No.6,790,673Bl和U.S.Pat.No.6,974,951Bl、以及Pat.No.5,883,349、以及Pat.No.5,830,417和7,005,635B2、以及U.S.Pat.7,220,383B2、Pat.pending No.US2002/0198230Al,其公开了为了测量来制备样品的方法以及测量样品中存在的化学物种的方法,不仅测量其整体化学浓度,而且基于这些方法以提高的灵敏度、精度和效率进行在线自动化测量。这些专利的公开以引用的方式明确并入本文。
发明内容
本发明公开了一种用于在使用固相同位素比平衡和测量的质谱分析之前催化浓缩同位素物种与天然同位素物种的平衡的方法。本发明的基础是用于兴趣分析物的最终的定量和定性分析的分子、元素和物种化、以及定量和定性的样品制备。该方法利用通过同时平衡相较于液相和气相具有很多优势的固相来促进平衡,并实现本领域已知的IDMS和SIDMS分析的自动化。这一创新使用固相和固定的浓缩同位素试剂、同位素浓缩分子制造试剂以及固相与固定相的平衡过程。使用算法来数学确定浓度并直接校正物种位移,无需对质谱数据应用校准曲线。与常规的液/热平衡和分离协议相比,通过固相样品制备,平衡和分离分析物所需的时间显著降低。为固相同位素增量(spiking)及平衡所制的试剂和产品在较长时间内是稳定的,因此可以进行现场样品制备,以及改进保存和保存或装运过程中与试剂和/或样品的降解关联的一系列保管问题。对于现场工作者和实验分析人员来说,通过去掉几个样品制备及操作步骤,固相同位素增量和平衡使得易反应和有毒物质的处理以现场增量和平衡形式进行比作为整体试剂溶液更加安全。样品分析物和同位素浓缩和平衡试剂标示或者在液相和/或气相被洗脱(elude off)以用于分析,或者被表面电离到质谱仪中直接在固相进行分析。固相同位素增量和高速平衡提高了设计包括高度自动化和小型化的子系统的低成本、高吞吐量、可靠的样品制备及分析系统的能力,从而可以设计高度便携、现场实用的、精确、低故障的积极分析及检测系统。这种现场实用的系统对于环境法医学、国土安全和国防、工业合规、生物科学和临床研究和临床诊断将非常有用。一些国防和国土安全应用包括监测易挥发试剂(fugitive agent)的多点饮用水网络和战场上用于保护武装部队的空气/水/表面分析。在增长中的环境卫生领域,这些系统对于评估接触环境和食品中的工业毒素引起人类某些疾病的风险也将是有用的。最后,这种系统可能成为帮助预测某些疾病的发生或减缓这些疾病的发展的工具,如孤独症、某些类型的癌症、以及免疫退化性疾病,如阿尔茨海默氏症,帕金森症和糖尿病。下文将使用上述两个概念进行明确研究。
根据本发明的一方面,提供了一种用于平衡同位素稀释质谱样品的方法,包括以下步骤:a)向溶液中添加一定量或浓度的同位素标记分析物类似物以产生预标记微波介质;b)向所述预标记微波介质中添加包含或被怀疑包含与所述同位素标记分析物类似物对应的兴趣分析物的样品,以产生可微波溶液;c)通过将所述可微波溶液培养1秒至1小时而平衡所述兴趣分析物,以产生平衡样品;以及d)对所述平衡样品进行质谱分析。
附图说明
图1:通过GCMS描述和分析的SPI-SPE平衡和分离含氧化合物的结果。
图2:通过GC-MS描述和分析在PAG-5柱上增量指示含氧化合物并在柱上进行平衡和分离的结果。
图3:血清中的吗啡,采用6ml、0.5g安捷伦Evidex,吗啡IDMS同位素预增量C-13,在PSI-SPE柱上与样品吗啡平衡。
图4:使用同位素浓缩PSI-SPE并在柱上与天然同位素平衡的1,4-二氧六环和1,4二氯乙烷。
图5:生物降解对监测水井样品的影响。浓度以ppb表示,所示误差表示为90%置信区间,n=3。
图6:校准标准样对比校准盒(cartridge)。试剂水增量到2ppm,误差表示为95%置信区间,n=4。
图7:校准标准样对比校准盒。
图8:RF(响应因子)比较。校准RF对比RF=1。
图9:微量滴定板(俯视图),8×12(96孔)格式制备的质谱(IDMS和/或SIDMS)ELISA(酶联免疫吸附测定),具有两种不同类型的浓缩同位素修饰结合抗原的交替行。
图10:微量滴定板或表面修饰固相载体(侧视图),具有两种不同类型的浓缩同位素结合抗原的交替、分立的行。在用天然同位素样品执行ELISA法之前制备一同位素浓缩抗原作为固体表面的一部分。或者,固相上不存在同位素预装抗原,并且在ELISA过程中,当结合到抗体时浓缩和和非浓缩抗原两者迅速平衡。
图11:微量滴定板或表面修饰固相载体(侧视图),有某一百分比的抗体事先已与同位素浓缩抗原结合。通过测量样品中存在的同位素浓缩抗原的结合水平实现ELISA测量,其中所述结合水平是这两组抗原之比的函数。
图12:微量滴定板或表面修饰固相载体(侧视图),使用夹心系统、以及使用同位素浓缩抗原并测量两种浓缩同位素稀释剂之比的双抗体和抗原分析。
图13:具有排列成两个分立行的天然丰度生物标记和同位素浓缩生物标记的微量滴定板或表面修饰SELDI(表面增强激光解吸电离)板(侧视图)。
图14:用于SELDI或ELISA的8孔带的俯视图。
图15:固相表面修饰板,其具有16排交替的浓缩和天然的结合蛋白质生物标记或核酸探针,设置成高密度的微阵列格式。通过使用同位素浓缩和天然多元生物标记或核苷酸并运用IDMS和/或SIDMS直接比率算法来进行定量。
图16:质谱读出表明血液的同位素浓缩特异性物种增量:甲基汞,乙基汞,无机汞和金属汞。
图17:通过正模式ESI-TOF-MS,质谱读出显示含20ppm的NaN3和20ppm的NaNN15N的水。
图18:通过负模式ESI-TOF-MS,质谱读出显示含20ppm的NaN3和20ppm的NaNN15N的水样。
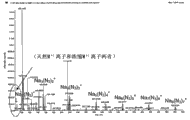
图19:以正离子模式增量20ppm NaNN15N的20ppm NaN3的叠氮化钠离子其中之一的质谱特写,所有天然峰在m/z88,所有同位素峰在m/z89。
图20:以负模式增量20ppm NaNN15N的20ppm NaN3的第一叠氮化钠离子的质谱特写,所有天然峰在107,混合峰在108,所有同位素峰在109并具有1:2或1:3的用于定量的比率。
图21:质谱读出显示该组分子物种中的很多同时比率和定量需要用于定量的多个公式和多个比率。这些采集到的图形是在负模式下的DI H2O中的20ppm的NaN3和20ppm的NaNN15N。每个图形具有一个或多个叠氮化物峰。
图22:质谱读出显示天然叠氮化物Na3(N3)4-(最左边的峰)和叠氮化物Na3(N3)4的三个相应的同位素浓缩标记类似物-(具有不同数目的N15同位素和比率)之间的新的比率关系和多个峰。该图示是负模式下增量了20ppm的NaNN15N的20ppm的NaN3的第三叠氮化钠离子的特写,所有天然峰在237,混合峰在238、239和240,(2×15N)同位素峰在241。
图23:负模式下增量20ppm的NaNN15N的20ppm的NaN3的第四叠氮化钠离子的质谱特写,所有天然峰在302,混合峰在303、304、305和306,所有同位素峰在307。
图24:在正模式下增量了100ppm的K13C15N的100ppm(μg/g)的KCN的第四氰化钾物种离子的纳米ESI-TOF-MS的质谱突出增强视图,所有天然峰在299,同位素浓缩氰化钾峰是在301、303和305的峰,所有同位素峰在307,每一个都用其同位素和天然碳和氮的混合物注释。
图25:显示固相增量和平衡的流程图。
图26:显示浓缩同位素增量和平衡方法的流程图。
图27:甲基汞的同位素理论叠加和测量谱,其采用ESI-TOF
-MS位于m/z338(通过ESI-TOF的甲基汞和巯基丙氨酸)。
具体实施方式
在本文的使用中,“物种(species)”的使用与包含将被定量分析的物种的样品有关,“物种”应指任意的化学物种、离子物种、分子物种、以有机物种、有机金属物种为例的合成物物种、以包含蛋白质的金属以及异质和同质碳物种为例的合成物物种、以及适合于本发明的化学定性和定量物种化分析的其他物种。
问题与方案描述:
问题与方案讨论:
目前,必须在测量之前进行样品制备。为了使用任意形式的IDMS和/或SIDMS(包括特定物种同位素稀释质谱法-SSIDMS),首先需要使物种分析物的浓缩同位素物种与天然同位素达到平衡。如果该步骤需要用几天或者几个小时的时间而仪器分析和自动化只需几秒钟的时间,则存在一时间差,其妨碍了IDMS和/或SIDMS的自动化应用。如果样品必须进行萃取、分离或处理,则需要一种在进行萃取和/或分离的同时还加速平衡的自动化方法。尚未具体确定这种通过加速平衡和IDMS/SIDMS自动化实现效率优化、可重现性和时间节省的方法。本发明在此解决该问题,并实现稳定和安全的毒素处理,这对于国防和国土安全领域、环境和环境法医学、生命科学和工业管控一致性测量方面的应用尤为重要。
同位素稀释(ID)和物种化同位素稀释(SID)的使用需要天然和稳定浓缩同位素物种类似物(以及放射性同位素物种类似物)的平衡,以建立通过质谱仪测量的同位素比。ID和SID的使用允许直接定性和定量质谱法产生对分析兴趣所在的物种极其准确的分析定量分析。因此,在应用通过质谱仪的ID和SID方法之前,精确和不变的同位素浓缩物种和天然同位素物种的平衡是绝对必要的。目前实现的平衡使用标准样的热处理方法,可能需要几小时或几天的时间。下文将提供这些老方法的一些示例。可以稀释浓缩同位素溶液,使其不稳定或使溶液中的多个物种可与浓缩同位素在使用前反应。稳定浓度下浓缩同位素在运输时不一定是安全的。在本发明之前,只有具有很高的教育水平、技能和经验的人员才能把SIDMS和IDMS方法当成工具来使用。经验不足和缺乏技术的人员可能不知道如何正确萃取物种,然后增量、平衡以实现定量。运输、储存、装卸、实地使用、实验室使用、定量转移、样品的平衡、分析物的萃取、分析物或基体的分离、以及分析物浓度计算对于缺乏经验的分析人员来说都是难以解决的。本发明描述的方法提高了浓缩同位素稀释剂的稳定性、分析兴趣所在的增量物种、易用性、关键步骤的可靠性,其包括平衡和自动化,从而使得IDMS和SIDMS的实现和应用为最低技能人员所通用,并解决常需要快速、可靠地分析大量样品的商业实验室的高吞吐量需求。
自从现代色谱法在19世纪中期发展起来,利用固相吸附剂从基质分离出分析物已为人们所熟悉。然而尚未实现如本文所公开的,利用固相吸附剂来平衡浓缩稳定同位素物种以及分离基质与分析物,从而提高IDMS和SIDMS的适用性和可用性。在本发明中,利用具有各种不同性质的固相物质来保存浓缩同位素物种,然后出于样品制备、样品储存或安全目的,将它们提供到实验室或实地现场,从而稀释剂已在固相中而不是在需要处理的试剂溶液中。用于保存浓缩同位素物种的同一固相也可以用来萃取分析物物种。
这里采用的固相选自于离子交换、吸附介质、固相萃取树脂、树脂胶合固相(resin bonded solid phase)、表面修饰过滤器、固定液体萃取(ILE)中使用的二态液体、以及纤维的群组,如固相微萃取(SPME)。将同位素浓缩分子或离子物种化学或物理地稳定或捕捉或保持在固相、层析或萃取物质上。然后向含有分析兴趣所在的物种的样品中添加天然样品物质兴趣物种,其通过能将该物种保持在该介质上的该介质的适当机制保持。该过程可以逆转,可在平衡关系中洗脱浓缩物种和天然物种。其结果是,该物种将取得平衡,并且当从固定相或固相萃取或层析介质洗脱兴趣物种时,样品混合物是平衡的同位素浓缩物质和天然同位素物质的组合,已为ID和SID质谱法做好准备。在这些情况下,电离方法将专用于溶液或气相,例如电喷雾电离(ESI)或纳米电喷雾(Nano-ESI)、或大气压化学电离(APCI)或电子轰击(EI)或电感耦合等离子体(ICP)或微波诱导等离子体(MIP)及其他电离方法。本发明消除可能延长或抑制或阻止平衡的基体,并将其置于固相介质上的两个分析物上,由于两个物种具有相同的化学组成和亲和力,是同样的分子,但具有不同的同位素比,因此两个分析物产生平衡状态以同时洗脱,从而加速洗脱过的液体溶液中的平衡。一实施例允许实地或就近使用,甚至另外用于太稀无法装运或者没有固相载体物质就不稳定的小数量和低浓度。另一实施例能够将现已在固相上平衡的样品物种装运或运输到分析地点,作为形成在固相载体物质上的浓缩同位素和天然平衡分析物。现已平衡的浓缩和中性分析物将在未来某个时间被洗脱或储存,以便后续作为存档进行分析。该实施例产生可被装运、储存或存档的稳定存档平衡的稀释剂和天然样品。
另一实施例利用具有平衡分析物的固相并通过表面电离感兴趣的浓缩分析物和天然分析物来直接诱导电离。用于表面电离的电离方法是下列的一些方法,例如基体辅助激光解吸电离(MALDI)或解吸电喷雾电离(DESI)或激光烧蚀(LA)或酶联免疫吸附测定(ELISA)或免疫化学分析(ICA)或表面增强激光解吸电离(SELDI)。
在固相分离和高吞吐量自动化之前加速溶液中物种的平衡的方法是通过微波增强化学方法而不是热传导和对流方法来进行微波平衡加速。选自例如2450MHz微波波段的微波能量产生分子转动和所有离子的离子电导和永久偶极子,其能够促成更快地从表面解吸,并增强必要的样品制备步骤(如萃取和分解)中进行的天然物种和同位素浓缩物种的类似物的离子和分子平衡。这些结合的样品制备过程使得物种同时达到均匀平衡,并大大缩短了分析周期(样品制备、操作和分析)。该同时萃取和平衡可与(上文所述的)固相萃取中的平衡步骤结合,以同时增强这两个过程。在某些情况下,分析周期可从24小时降至低于600秒。这一结合的同时萃取和平衡步骤可以实现超快速反应,这是医院、临床和商业实验室中的高吞吐量自动化应用以及国土安全和国防设置中的近实时应用的先决技术条件。
通过这里公开的多个示例实现了这些新的增强。
这里公开的主要方法是浓缩同位素标记的预吸附固相固定、快速用于平衡分析兴趣所在的物种的同位素浓缩物种类似物和天然丰度物种类似物、以及通过微波增强化学作用明显加快的溶液中的同位素物种或气体形式的同位素物种的平衡。
固相分离方法和微波增强化学方法是众所周知的,但并未用于提高IDMS和SIDMS的平衡效率、稳定性、现场使用、自动化以及平衡物种的储存和提供。
IDMS和SIDMS方法依赖于同位素比的测量,因此不存在与校准曲线、仪器稳定性和探测器信号漂移关联的问题。因此,这两个同位素稀释过程中的关键步骤是同位素浓缩稀释剂与样品中存在的分析物的平衡。由于只测量同位素比而无须外部校准,因此当达到平衡时,增量(同位素标记或浓缩物种类似物)物质作为理想标准样。这确保了目标分析物的始终精确、可重现的测量。增量物质作为IDMS和SIDMS的理想标准样这一角色也消除了与质谱检测过程中的仪器漂移和基质效应相关联的问题,因为这些效应对物种所有同位素的作用相同。参见RuizEncinar,J.;Rodriguez-Gonzalez,P.;Garcia-Alonso,J.I.;Sanz-Medel,A.Trenes inAnalytical Chemistry,2003,22(2),108-114。
如果稀释剂未与样品完全平衡,则稀释剂的不同的萃取效率将导致测量中产生误差。对于液体样品,通过微微搅拌应能达到充分平衡,而对于固体样品,平衡则是成问题的,因为分析物既能被吸附到样品基质的表面上,又能被包含到样品基质的晶格内。当兴趣物种存在于固体样品中并且被添加的稀释剂是在溶液里时,确保同位素平衡的方式是将原始物种从固体定量萃取到适当的溶剂中,原始物种与液体稀释剂在所述溶剂中的平衡是简单明了的。参见Rodriguez-Gonzalez,P.;Marchante-Gayon,J.M.;Garcia-Alonso,J.I.;Sanz-Medel,A.Spectrochimica Acta,PartB,2005,60,151-207。
Clough,R.等人对两种认证标准样物质中的总汞和甲基汞研究了时间对稀释剂与样品分析物的平衡的影响。他们在研究过程中观察到,如果将稀释剂添加到样品中,并在室温(25℃)下与浓硝酸或50:50的水:甲醇(v/v)和0.01%的2-巯基乙醇一起搅拌多达3000分钟,平衡过程从未达到100%。另一方面,将混合物在家用微波炉中以650W加热2分钟,即可达到平衡。但是,在这种情况下,将增量的样品在室温下保持24小时,以允许微波消解/萃取前的平衡。参见Clough,R.;Belt,S.T.;Evans,E.H.;Fairman,B.;Catterick,T.Anal.Chim.Acta,2003,500,155-170。
Yang,Lu等人发现铬物种通过热对流或传导平衡要用超过6小时,将分析步骤延迟了一天。作者所采用的95℃碱性条件与EPA(美国环保署)方法3060A萃取方法化学相同。
精确的同位素稀释分析需要稀释剂与兴趣分析物之间的同位素平衡。为了使稀释剂和分析物,有机锡和一甲基汞,更快地溶解和稳定并且更快地平衡,对生物样品应用开放聚焦的微波辅助萃取过程。70℃下在5分钟之内达到完全溶解和稳定。然后在GC-MS毛细管色谱柱上完成9分钟分离。参见Monperrus,M.;Rodriguez Martin-Doimeadios,R.C.;Scancar,J.;Amouroux,D.;Donard,O.F.X.Anal.Chem.2003,75,4095-4102;Moreno,MJ.;Arjona,J.P.;Rodríguez-Gonzalez,P.;Homme,H.P.;Amouroux,D.;Donard,O.F.X.J.Mass Spectrom.2006,41,1491-1497。
Rodriguez-Gonzalez,P.等人研究了不同的萃取方法,例如微波辅助萃取、机械震荡、用四甲基氢氧化氨(TMAH)碱解、以及对生物物质中的丁基锡化合物进行酶消化。他们观察到物种大范围降解、以及与TMAH平衡不足和酶消化不足。据称,使用醋酸-甲醇混合物的微波辅助萃取在低降解和快速同位素平衡以及定量回收方面产生最佳结果。他们还在研究中提出,只有当天然存在的有机锡化合物完全从固态基质释放到溶液之后方达到所需要的完全的同位素平衡。参见Rodriguez-Gonzalez,P.;Garcia Alonso,JJ;Sanz-Medel,A.J.Anal.Atom.Spectrom.2004,19,767-772。
结合三种丁基锡化合物的特定物种同位素稀释分析执行贻贝组织的体外胃肠消化。但为了避免内源(endogenous)物种与同位素浓缩稀释剂物种之间的同位素平衡不足所造成的任何问题,在消化过程完成之后才增量同位素。参见Rodriguez-Gonzalez,P.;Encinar,J.R.;Garcia Alonso,J.I.;Sanz-Medel,A.Anal.Bioanal.Chem.2005,381,380-387。
Kawano等人在生物样品中的硒的测定过程中研究了稀释剂平衡的不同加热参数。他们在热解步骤即将开始时使用原位熔化(in situ fusion),以便平衡稀释剂与样品分析物。参见Kawano,T.;Nishide,A.;Okutsu,K.;Minami,H.;Zhang,Q.;Inoue,S.;Atsuya,I.Spectrochim.Acta,2005,60B,327-331。
Valkiers等人在比率测量过程中研究了质谱仪中的气相二氧化碳气体中的碳同位素和氧同位素的同位素平衡程度。参见Valkiers,S.;Varlam,M.;Rube,K.;Berglund,M.;Taylor,P.;Wang,J.;Milton,M.;De Bievre,P.International Journal ofMass Spectrometry,2007,263,195-203。
Chen,Z和同事研究了时间和酸浓度对人血清中的钙同位素平衡的影响。该科学论文指出,对于已知样品,在1小时内平衡需要至少0.22mol/HNO3,对于未知样品,则推荐至少6小时的时间。参见Chen,Z.;Griffin,I.J.;Kriseman,Y.L.;Liang,L.K.;Abrams,S.A.Clinical Chemistry,2003,49(12),2050-2055。
Hunkeler,D.和Aravena,R.研究了使用直接固相微萃取(dSPME)和顶空固相微萃取(headspace solid-pase microextraction,hSPME)的,甲烷氯化物、乙烷、及含水试样中的乙烷中的碳同位素比的萃取和平衡,并且论证出dSPME和hSPME使水相中和SMPE纤维上的碳同位素至少偏差0.4。另一方面,对于顶空平衡,在13C中气相分子较水相分子浓缩达1.46。参见Hunkeler,D.;Aravena,R.Environ.Sci.Technol.2000,34(13),2839-2844。
Crowther,JohnR.将ELISA方法汇编到ELISA Guidebook一书中,其论述了如何通过例如荧光的光学方法将ELISA固定相用于识别蛋白质、抗原和抗体,并与标准样质谱得到的结果进行比较。这本书不包括通过同位素质谱测量分析物的ELISA方法。在文献中未将ELISA的IDMS和SIDMS用于定量,而是其中普遍将ELISA与传统质谱进行比较。参见JohnR.Crowther所著的The ELISAGuidebook,由Humana Press New Jersey于2001年出版。
发明内容
本发明公开了一种用于在使用固相同位素比平衡和测量的质谱分析之前的浓缩同位素物种和天然同位素物种的催化平衡的方法。本发明的基础是分子、元素和物种化、以及用于兴趣分析物的最终定量和定性分析中的定量和定性的样品制备。该方法利用在同时平衡、以及实现本领域已知的IDMS和SIDMS分析的自动化方面相较于液相和气相具有很多优势的固相来促进平衡。这一创新运用了固相和固定的浓缩同位素试剂、同位素浓缩分子制造试剂(manufactured reagents)以及固相与固定相的平衡过程。利用算法来数学确定浓度并直接校正物种位移(species shift),不对质谱数据运用校准曲线。与常规的液/热平衡和分离协议(protocol)相比,通过固相样品制备,平衡和分离分析物所需的时间显著降低。为固相同位素增量及平衡所制的试剂和产品在较长时间内是稳定的,因此可以进行现场样品制备,并且改善储存或装运过程中与试剂和/或样品的降解相关的储存和保管链问题。对于现场工作者和实验分析人员来说,通过去掉几个样品制备及操作步骤,固相同位素增量和平衡将使易反应和有毒物质的处理以现场增量和平衡形式进行,比作为整体试剂溶液更加安全。样品分析物和同位素浓缩和平衡试剂标记要么在液相和/或气相被洗脱以用于分析,要么被表面电离到质谱仪中直接在固相进行分析。固相同位素增量和高速平衡提高了设计包括高度自动化和小型化的子系统的低成本、高吞吐量、可靠的样品制备及分析系统的能力,从而可以设计高度便携、现场使用的、精确、低故障的积极分析及检测系统。这种现场使用的系统对于环境法医学、国土安全和国防、工业合规、生物科学和临床研究和临床诊断有非常大的用处。一些国防和国土安全应用包括监测易挥发试剂(fugitiveagent)的多点饮用水网络和战场上用于保护武装部队的空气/水/表面分析。在增长中的环境卫生领域,这些系统对于评估接触环境和食品中的工业毒素引起人类某些疾病的风险也将是有用的。最后,这种系统可能成为帮助预测某些疾病的发生或减缓这些疾病的发展的工具,如孤独症、某些类型的癌症、以及免疫退化性疾病,如阿尔茨海默氏症、帕金森症和糖尿病。下文将描述使用上述两个概念的明确研究。
具体实施方式
该问题近来在Lu等人的论文中得到了说明,文中指出,酵母中的Cr(VI)和Cr(III)的同位素平衡长达12小时。这一数据证明了该问题的直接解决方案。该论文还指出,本领域技术人员不理解使用微波方法和标准样热方法来平衡同位素和天然物种的不同。该论文讨论了EPA方法6800的应用和成绩,我们在当前的工作中正对其深入研究。
所述的另一应用是可基于更短时帧和快速反应将微波实现加入到微流体设计中,以加速有更快反应需求的反应。下面显示了安捷伦芯片立方微流体设计,其具有例如对该设备的某部分的同轴微波发射,以提高例如反应速度、萃取和/或平衡。本发明包含了使用柱上预吸附增量和微波增强和/或同时使用以上两者的微流体。
在取样、储存、校准和测量过程中,元素和分子物种经历转化并形成其他物种,或是兴趣物种降解为其它物种。在许多这样的情况下,无法进行传统的校准。此外,定量分析的准确度和精度取决于使用的校准协议的类型,例如内标准样化,标准样加入和同位素稀释,使用不同的校准技术会引入误差,如固定误差和随机误差。如果以下假设成立,则得到使用外部校准曲线的准确结果:校准标准样和样品具有相同的基质;校准是线性的;分析人员在限定的误差范围内准确制定校准标准样;无论标准样是如何制定的或是何人制定的,标准样的稳定性都是已知的,并且仅在这些限定的时间、基质、浓度、温度/湿度、容器材料的范围内使用;未知的测量只会比校准的不确定度差;不存在谱干扰和/或质量干扰;为分析制备的样品不涉及任何正的或负的污染误差或取样误差;以及内部标准样表现与样品分析物完全相同。参见Gonzalez-Gago A等人,J.Anal.At.Spectrom.,2007,DOI:10.1039/b705035f; BrownR.J.C.,et al,Anal.Chimica Acta,2007,587(21),158-163。
在5%至10%范围内,ICP-MS生成最高精度的结果(即复杂基质)。与外部校准有关的主要问题是:溶液中的分析物的稳定性;样品制备的准确性;校准标准样的纯度;内部标准样的选择;不正确的仪器安装;总的溶解固体;非谱干扰;基质匹配;标准样加入;进样;色谱分离;随时间的仪器漂移;雾化效率;雾滴尺寸;溶液的物理性质;溶液中的酸含量;分析人员欠缺知识/培训;背景校正;质量偏歧;死时间;同重多原子干扰。参见Vicki,B.Preparation of Calibration Curves:Aguide to best practice,LGC,2003年9月。
为了有效地校正样品和标准样中由于基体效应引起的信号强度的时间变化和分析信号的系统变化,内部标准样的物理性质必须与运用它们的同位素的物理性质小心匹配。参见Hsiung Chiung-Sheng,等人,Clinical Chemistry,1997,43(12),2303-2311;Entwisle,J.American Laboratory,March2004,11-14;Eickhorst,T.;Seubert,A.J.Chromatogr.A,2004,1050,103-109。
当基质相当易变时和/或当无法找到校正等离子体相关影响的内部标准样时,使用标准样加入(addition)技术。虽然标准样加入技术对通过等离子体相关影响的基体干扰提供了更好的可能解决办法,但它要求线性响应。因此,在每个分析物的线性范围内工作是非常重要的。参见Bonnefoy,C.等人,Anal.Bianal.Chem.2005,383,167-173;Melaku,S.等人,Can.J.Anal.Sic.Spectres.,2004,49(6),374-384;Panayot,K.等人,Spectrochim.Acta,Part B,2006,61,50-57。
蛋白质生物标记在研究中对人类疾病特别是癌症的临床管理产生巨大的影响。蛋白质组学和基因组学在蛋白质生物标记发现中的应用使得单一发现工作已能识别数百种生物标记。然而,由于缺乏定量和临床验证,这些发现工具的保证尚未达成。可使用性能良好的高吞吐量酶联免疫吸附测定(ELISA)以超高灵敏度和特异性对目标分析物进行定量。目前的ELISA是基于比色法和荧光读出器来进行定量,并与色谱法和质谱进行比较,但并未进行结合。参见Whiteaker,J.R.;Zhao,Lei;Zhang,H.Y.;Feng,L.C.;Piening,B.D.;Anderson,L.;Paulovich,A.G. AnalyticalBiochemistry,2007,362,44-54。
Martens-Lobenhoffer,J.等人对采用液相色谱质谱法(LC-MS)的人体血浆和血清样品中的非对称二甲基精氨酸(ADMA)的浓度测量进行了评价,并将结果与通过标准样比色ELISA方法得到的结果进行比较。文中指出ELISA比LC-MS产生的值高,并推断出ELISA是依赖于基质的。他们还认为ELISA将血浆中的ADMA浓度高估了2倍。参见Martens-Lobenhoffer,J.;Westphal,S.;Awiszus,F.;Bode-Boger,S.M.;Luley,C.Clinical Chemistry,2005,51,2188-2189。
Charissou,A.等人还评价了对食物样品中的羧甲基赖氨酸(CML)进行定量的ELISA法,并将结果与气相色谱质谱法(GC-MS)的结果进行比较。在这项研究中,他们采用了常规的内部标准样和同位素稀释内部标准样两者进行GC-MS定量,以与标准样ELISA进行比较。他们指出,当使用粉末样品时,与GC-MS相比,ELISA是检出限较低的快速低成本方法。但对液体和水解婴儿配方奶粉(hydrolyzed infant formulas)之类的复杂基质使用两种检测方法则会发现ELISA法受到缺乏特异性和高风险的基体干扰的影响。相反,这两种方法对奶粉样品产生相似的结果。他们还指出,ELISA法高估了某些脂肪含量高的样品中的CML浓度,如肉类产品,以及油炸食品,而通过GC-MS或HPLC(高效液相色谱)法在这些样品中检测不到CML或只能检测到低水平的CML。脂质基质可能对ELISA存在特异性干扰。参见Charissou,A.;Ait-Ameur,L.;Birlouez-Aragon,I.J.Chromatogr.A,2007,1140,189-194。Scholl,P.F.等人在通过同位素稀释质谱法和常规ELISA测定人体中的黄曲霉毒素B1血清白蛋白加合物时也有类似的发现。他们指出,在2mg白蛋白中通过ELISA测量的黄曲霉毒素-白蛋白加合物的浓度和通过IDMS测量的黄曲霉毒素B1-赖氨酸的浓度有很好的相关性;但是,通过ELISA测量的黄曲霉毒素-白蛋白加合物的浓度比黄曲霉毒素B1-赖氨酸加合物的浓度平均高2.6倍。作者在文中推测,ELISA除测量了黄曲霉毒素B1-赖氨酸之外,还测量了其他的黄曲霉毒素加合物。参见Scholl,P.F.;Turner,P.C.;Sutcliffe,A.E;Sylla,A.;Diallo,M.S.;Friesen,M.D.;Groopman,J.D.;Wild,C.P.Cancer EpidemiolBiomarkers Prev.2006,15(4),823-826。
Wolthers,B.G.等人评价了测定人体尿液中的变肾上腺素(MA)和去甲变肾上腺素(NMA)的ELISA法,并将结果与由使用内部标准样和校准曲线但将GC-MS内部标准样称为IDMS分析的GC-MS获得的结果进行比较。他们得出结论,ELISA法能够对尿MA进行定量,从而能够成功用于确诊嗜铬细胞瘤,并还建议可在任意临床实验室执行这个简单的ELISA法,并希望很快可以取代目前实际上更为复杂的色谱方法。参见Wolthers,B.G.;Kema,I.P.;Volmer,M.;Wesemann,R.;Westermann,J.;Manz,B.Clinical Chemistry,1997,43(1),114-120。
从示例文献可以看出,研究人员研究了使用ELISA的不同样品,并将结果与包括许多质谱形式的其他检测方法进行比较,例如GC-MS、HPLC或IDMS,但将ELISA转化为质谱过程尚未得到发展。
在第三部分中描述可用于国防和国土安全和或环境法医学的完全集成的现场和/或实验室系统的示例,其中第三部分是描述所有这些部件如何结合的独立部分。
固相平衡、萃取和分离方法
结合到SCF柱上的浓缩物种
发明者之一在EPA方法3200的制备过程中进行了研究,其涉及在添加来自国际原子能机构(IAEA-085)的人发中汞物种的认证标准样物质样品之前吸附或化学附着到巯基棉纤维(SCF)固相柱上的甲基汞的同位素浓缩物种。这项研究的数据表明本发明和新的固相增量及平衡方法的有效性。将结果与传统的IDMS和SIDMS方法的结果进行了比较,传统的IDMS和SIDMS方法是在不同的汞物种与巯基发生SCF固相共价结合之前,在溶液中进行平衡。样品通过微波能量进行萃取和增量-平衡,然后与预吸附固相物种同位素增量进行比较,发现两者都提供准确的数据。这里描述的示例涉及两组作为相同样品的IAEA-085参考物质人发的处理。表1数据出自常规EPA方法6800—SIDMS的实施,该方法在用微波能量萃取前对样品增量同位素浓缩甲基汞。表2是出自相同的标准样样品(IAEA-085),并服从于新方法,该新方法首先不进行增量,而是采用EPA微波萃取法(EPA方法3200)萃取甲基汞,然后将甲基汞添加到SCF柱,稀释剂在SCF柱的固相中平衡,固相被填充作为柱中而不是溶液中的流通介质床(bed of flow-through medium),如同目前最先进的化学过程所进行的。
表1:IAEA-085,毛发分析:毛发样品经预增量,但SCF柱未经增量
| 子样品复制品 | 无机汞(μg/g) | 甲基汞(μg/g) | 总汞(μg/g) |
| 标准样值 | 21.9-23.9 | 22.4-24.0 | |
| IAEA-085-1 | 1.644±0.152 | 21.155±2.986 | 22.799±2.990 |
| IAEA-085-2 | 1.442±0.073 | 21.006±2.367 | 22.448±2.368 |
| IAEA-085-3 | 1.767±0.109 | 22.933±0.496 | 24.700±0.509 |
| 均值 | 1.617±0.104 | 21.698±0.990 | 23.315±0.995 |
不确定度在95%置信区间,n=4
在运用高效液相色谱-电感耦合等离子体质谱联用法(HPLC-ICP-MS)进行分析并进行数据比较之后,可以看出在与IAEA-085标准样参考物质的标准样值比较的基础上,两个过程都产生100%的回收率并达到相同的准确度。这些数据表明,本发明的优点是有助于显著加快下列关键步骤:提供浓缩同位素稀释剂或浓缩物种类似物,以及将其与兴趣物种平衡以用于IDMS和/或SIDMS。汞物种的平衡可以在柱上或在洗脱过程中和/或在萃取步骤中进行。通过微波进行的平衡产生同样准确的结果。
表2:毛发分析:SCF柱预增量了同位素浓缩汞物种,但样品未经增量
| 样品复制品 | 无机汞(μg/g) | 甲基汞(μg/g) | 总汞(μg/g) |
| 标准样值 | 21.9-23.9 | 22.4-24.0 | |
| IAEA-085-1 | 1.259±0.027 | 24.339±1.289 | 25.598±1.289 |
| IAEA-085-2 | 1.354±0.030 | 21.224±3.935 | 22.578±3.935 |
| IAEA-085-3 | 1.588±0.015 | 22.736±2.325 | 24.324±2.325 |
| 均值 | 1.400±0.092 | 22.766±1.301 | 24.166±1.304 |
不确定度在95%置信区间,n=4
萃取后,萃取物通过SCF柱(未增量),以将无机汞与甲基汞分离,这表明本发明的还涉及用于物种分离的固相物质的两用能力。然后通过HPLC-ICP-MS对两种洗脱液(用于甲基汞的洗脱液1和用于无机汞的洗脱液2,EPA方法3200协议)进行分析。测定经过死时间和质量偏置校正的同位素比,并用它来通过传统的IDMS公式计算无机汞和甲基汞的浓度。从表1和表2的结果可以观察到,在采用这两种对照方法的这些研究中,标准样值和实测值之间不存在显著差异。
从表2的结果可以观察到,在该研究中得到在统计上无法区分的数据,该结果与标准样值在表1的95%置信区间重叠。此外,这两项研究的结果彼此之间以及与标准样值之间在统计上都是无法区分的。因此可以得出结论:天然丰度的汞物种与同位素浓缩汞物种在柱上的平衡是可实现的,并已付诸实施。这种技术产生无偏置的和准确的结果,等效于科学文献所述的传统IDMS和SIDMS。然而,当浓度低于溶液的稳定并因为浓度低,物质被限制向现场、从现场或向远距离实验室或原处运输时,将预增量的固相物质或浓缩物种类似物结合到固相物质上是实现IDMS和SIDMS的有效方法。
作为执行现场IDMS的靶分子的烷基分子在GC-MS中的固相增量和平衡
采用GC-MS分析的现场IDMS中的固相稳定同位素示例
分析过程的某些方面没有跟上现有的先进检测技术的发展。主要的方面是现场取样(样品采集)、保管链(样品封装、运输和存储,尽量减少或消除分析物损失)和实验室分析(样品制备)。分析化学研究进展导致检出限低至万亿分之一(onepart per trillion)的仪器的发展,万亿分之一这一值远低于水标准样品的稳定度。尽管许多色谱仪器技术已经成熟并已自动化,但样品制备仍是缓慢、劳动密集型、常要串行执行的实验室过程之一。目前为每个分析取得和处理大量的样品的做法对于快速运输和高吞吐量分析来说是费力、费时、昂贵和难以实施的。本发明在固相浓缩稀释剂的提供方面的应用减少了步骤数量,改进了水、空气、药物、食品、农业工业样品以及生物和临床标本的现场取样。
固相萃取(SPE)柱体(cartridge)用预吸附在固相物质上的稳定的同位素标记物种类似物填充。修饰的SPE柱体是为现场萃取设计的,并专门为特定分析物组制备的。建立具有适当的吸附剂、床深度、经校准的贮器容量、同位素标记类似物的准备的萃取柱。现场萃取的实现和简化要求最低限度的样品处理。在现场萃取之后,将固相萃取柱体运往实验室,在实验室用有机溶剂通过洗脱使同位素标准样和兴趣分析物解吸。通过该方法,将分析物和同位素标准样固定在固相介质上,而运输和储存时没有基质,分析物和同位素标准样不太容易修饰和降解。通过使用常规的内部标准样定量或同位素稀释定量的GC-MS进行分析。取样和萃取协议的简单性使高效的环境分析方法成为可能,增强了现场取样和分析的稳定性并提高了其精度、准确度和方法效能。整个过程中的质量保证和质量控制的水平得到了提高。
现场SPE是一种可由经验较少的人员在现场和在实验室中执行的萃取方法。通过提供具有同位素浓缩物种的萃取和/或固相,可以不进行大规模培训,采用价廉的、相对简单的、使用预增量的SPE柱体的手动或自动萃取执行该方法。例如,现场人员不是将待分析的水样置于容器内运往分析实验室,而是将水样置于经校准的、与固相萃取柱体相连的样品贮器中,并于现场在固相柱体上进行同位素平衡。加入样品后,通过正压或真空使样品通过SPE介质。在该萃取过程中,由于吸附剂介质与有机分子之间的分子间引力相对较强,有机分析物和兴趣物种被从水中除去。基本脱去有机分析物和同位素标准样的水通过SPE柱体。在进行SPE之后,分析物和同位素标准样被固定在没有水基质的固相介质上,因此比较不易改变和降解,而这种改变和降解在水样被运往实验室期间或存储过程中是可能发生的。
通过现场SPE大大节省了时间和资源且适于自动化,现通过若干示例进行实证。为了表明固相树脂上的现场萃取和平衡的样品保持稳定,在进行现场萃取并且样品在柱体中的固相物质上平衡之后,邮寄柱体以测试该方法。当收到包括柱体和经过萃取、柱上平衡与固定的样品的试剂盒时,分析实验室可以轻松地从柱体洗脱掉结合的样品。可通过任意的质谱仪进行分析。在实证中采用GC-MS分析方法。本发明是一种简化和高效的样品制备方法,其去掉了几个阶段的操作,避免了由于分析物的损失、不完整的化学操作步骤和偏置等操作中可能引入的误差。此外,本发明节省了时间和金钱,并实现了自动化。
固相C-18柱体中预吸附的浓缩同位素上的水萃取示例
下面在图1中给出了在GC-MS之前进行的预增量稳定同位素固相萃取(PSI-SPE),演示了几种类型的分子物种结果。对下列化合物类别进行PSI-SPE:含氧化合物、PAG-5、以及吗啡、1,4-二氧六环和1,2-二氯乙烷这些化合物。这些化合物类别对环境法医学、环境卫生和毒理学测量来说是典型的。使用PSI的所有结果被发现与使用常规实验室SPE获得的结果在在统计上是无法区分的,一定在EPA方法规定可接受的范围内。
含氧化合物示例
含氧化合物是经常在汽油中发现的小极性化合物的列表,作为“抗爆”剂加到馏出物中促进燃烧过程。化合物列表包括:叔丁醇(TBA)、甲基叔丁醚(MTBE)、乙基叔丁醚(ETBE)、二异丙醚(DIIPE)以及叔戊基甲基醚(TAME)。MTBE已与可能是环境造成的健康问题联系起来。这些化合物特别成问题,因为它们是高度混水的。如果发生例如成品汽油的油气泄漏,非极性的石油馏分汽油到达水体表面,可被去除或者至少被追踪,大城市中沿江的饮用水抽水站暂时关闭,直到汽油烟缕经过。完全溶于水的含氧化合物的情况并非如此。含氧化合物可以很容易进入地下水,无法轻易被去除。此外,由于水样萃取中涉及的种种困难,确定含氧化合物污染的浓度的水样分析是成问题的。通过常规手段不易从水样中萃取高极性含氧化合物。为了提高萃取效率,往往要加热样品。已证实这会将MTBE降解为TBA,导致无SIDMS的不准确的结果。此外,已证实MTBE在运送过程中降解为TBA。这会影响含氧化合物萃取过程中的萃取效率和降解。已通过PSI-SPE方法克服了这一问题。如图2所示,增量含氧化合物的水样的萃取得到非常好的结果。
分析物的PAG-5列表是许多环境执行机构在关闭或监测汽油污染场所时必须分析的一组毒素和污染物。该复杂列表包含含氧化合物MTBE、挥发性单环芳烃苯、乙苯和二甲苯、以及三种半挥发性分析物:萘、芴和菲。当采用传统的方法分析该化合物列表时,必须使用两种不同的测试方法:用于挥发性成分的EPA方法8260以及用于半挥发性成分的EPA方法8270。使用PSI-SPE完成分析物的PAG-5列表,用作在单一分析中测量的单一组。这大大减少了测试成本。分析物的PAG-5的PSI-SPE结果参见图6(PAG-5使用PSI-SPE。SPE Supelco公司的苯乙烯-二乙烯基苯/100mg。试剂水增量20ppb的PAG-5;误差表示为95%置信区间,n=5)。
吗啡
吗啡是非常常见的滥用药物。与前面讨论的挥发性化合物不同,吗啡测定中的兴趣样品基质不单单是水,而是非常复杂的有机基质。用于通过GC-MS测定吗啡的传统萃取方法是非常繁琐的。将PSI-SPE用于同位素标记吗啡,作为加快萃取与分析过程以及提供更为常规的可重现的萃取方法的一种手段。如图3所示,SPE结果非常理想(SPE Agilent Evidex,6ml,0.5g;误差表示为95%置信区间,n=4)。成功地从增量过的水和牛血清中萃取了吗啡。
二氧六环和二氯乙烷
小极性分子的另一示例是1,4-二氧六环。这种化合物常用作消毒剂。虽然其未被证实在萃取或分析过程中降解,但同含氧化合物一样,也很难用常规手段从水中萃取。然而,可以使用类似于含氧化合物分析方式的SPE,并取得非常好的结果。(图4:1,4-二氧六环和1,4-二氯乙烷。试剂水增量2ppb的1,4-二氧六环和20ppb的1,4-二氯乙烷。误差表示为90%置信区间,n=3)。
多年来,化合物四氯乙烷(TTCE)已成为非常常见的脱脂溶剂。它的用途的一个示例是用于制造不锈钢管材。在制造过程中用中度碳氢化合物润滑管材。常使用TTCE去除该润滑剂。TTCE一旦进入环境中,会降解为比TTCE的挥发性和水溶性高得多的1,2-二氯乙烷(1,2-DCA)。在地下水中发现的污染物通常是1,2-DCA,而不是母体TTCE。1,2-DCA与非极性芳烃苯系物(BTEX)或高极性含氧化合物和二氧六环的结构有很大的不同。1,2-DCA具有中间极性,为卤代化合物(见图4)。在与上述分析物萃取条件相同的SPE条件下,对1,2-DCA也能获得良好的结果。
使用传统的取样和分析方法时会出现的问题是在运输过程中微生物或化学降解导致化合物的损失。很多微生物能够消耗污染物作为食物来源。如果在样品运输过程中存在这种情况,则无法确定分析物的损失,并损害到测量的准确度。已进行研究来评估样品被萃取并在树脂上平衡之后SPE柱体上是否会发生降解。天然水样取自经分析发现含有一些污染物的监测水井。在第0天通过SPE和PSI-SPE对样品进行萃取和分析(第0天表示在取样活动和萃取/分析之间经过了0天)。允许同一样品的一部分在密封瓶中室温下保留14天,以观察是否有由生物降解造成的损失发生。该样品的一部分也在第0天萃取,但直到第14天才从SPE柱体中洗脱,以观察一旦将分析物和微生物从其水环境中被去除并隔离在柱体上,是否会在柱体上发生与密封瓶中发生的降解相似的降解。图5显示了该研究的结果。(生物降解对监测水井样品的影响。所有浓度以ppb为单位,误差表示为90%置信区间,n=3)。
如图5所示,使用SPE或PSI-SPE在第0天萃取和分析的污染物的初始浓度很好的吻合。让样品在密封瓶内保留14天后所进行的分析显示MTBE以外的所有分析物都完全降解。可令MTBE降解的微生物类型相对较少,在该样品集中未预计MTBE的降解。在对在第0天萃取但直到第14天才从柱体洗脱的样品所进行的分析中没有发现兴趣化合物的降解。该研究表明,在样品基质中进行取样并在没有任何其他步骤的情况下存放时,含有污染物的水样将会降解,而在SPE柱体上进行分离并储存时,含有污染物的水样不会降解。这是现场PSI-SPE的功用的另一示例。
通过固相预增量的同位素进行校准和比较
在传统的环境分析中,对于挥发性有机分析物(VOA)和半挥发性有机分析物(SVOA)来说,SVOA分析(EPA方法8260和8270)基于由校准标准样产生的响应因子进行定量。该标准样使用已知浓度的分析物,该浓度是使用内部标准样和被测分析物建立的。用于该标准样的溶剂与洗脱溶剂相同。在使用校准标准样的方法中,如果样品混合物中兴趣分析物的萃取效率在100%以下,并且未用内部标准样校正,则在定量中会出现误差。由于校准标准样本身并没有经历萃取过程,因此相对于未萃取的校准标准样,分析物萃取效率低下将导致信号减弱。在PSI方法中,当柱上预吸附的内部标准样为以下任一种情形时,误差可以是复合的:1)与萃取介质的结合不如萃取分析物时紧密(穿透),导致错误地升高的浓度,或2)与萃取介质的结合比萃取化合物时紧密(保持),导致错误地降低的浓度。这两种类型的误差都可以通过使用校准柱体来消除。校准柱体是用与样品柱体相同的方式制备的SPE柱体,内部标准样预吸附在固相物质上。为了产生校准柱体,将纯净的试剂水增量一定量的校准化合物。这由分析人员在样品萃取时进行的,方法是破开校准溶液的密封玻璃安瓿(ampoule),将校准溶液添加到纯净的试剂水中。现已用与样品同样的方式,使用PSI-SPE萃取该校准样品。当洗脱该柱体时,将萃取物作为校准标准样。由于这种类型的校准标准样已经历与兴趣样品相同的萃取过程,因此对于小于100%的萃取效率,其产生的响应现在已经得到校正,从而得到优良的数据。图6和图7显示了使用常规校准标准样和校准柱体进行定量的比较结果。
响应因子的比较
响应因子(Response Factor)是给定浓度下化合物的面积与同位素标记类似物的面积之比。如果这两种分析物的响应是相同的,则在整个萃取与分析过程中,面积计数应该是相同的,因此响应因子等于1。然而实际上,化合物与其同位素修饰的类似物的反应会略有不同,主要是由于制备标准样时的不完美的质量测量,因此在实际中,响应因子非常接近于1.0。如果化合物的响应因子是一,或足够近似可假定为值1.0,则定量乃至于分析都容易得多。事实上,如果总可以假定响应因子为1.0,则不再需要制备和操作校准标准样。如果是这种情况,将从根本上改变分析进行的方式。在图8中可以看到,对一半挥发性化合物萘和一挥发性化合物苯,比较了使用响应因子定量与假定响应因子为1.0来定量的经增量的水样的值的接近程度(RF比较。校准RF对比RF=1。SPE Supelco公司的苯乙烯-二乙烯基苯/100mg。试剂水增量20ppb的PAG-5;误差表示为95%置信区间,n=5。RF萘=1.036,RF菲=0.999)。比较的结果非常好,充分表明应进行更大量的研究。
自动化的潜力
将PSI-SPE用作自动化手段的潜力是有吸引力的目标,其将影响到未来仪器系统设计中自动化特性的设计。下面是一些可通过PSI-SPE来使用这样或那样形式的自动化的区域的取样。对于环境法医学和环境卫生监测,有许多机会来应用该技术。由于这些固相预增量物质的长期稳定性,监测被确定为污染地区的饮用水、淡水或水井,或通过常规取样连续监测污染,都是取样自动化的机会。可在装有制备的柱体的多功能系统中使用和/或重复PSI-SPE。通过使用电磁铁和开关阀以及标准样自动化装置,可在预定的时间定期进行取样。可使取样流的流动转向通过柱体达适当的时间量,然后用干燥的空气流替代样品的流动,以在PSI-SPE取样组分之后去除残留的水。萃取完成后,样品在很长一段时间内是稳定的,或者可以立即被除去,样品柱体可被现场分析或运送或甚至邮寄到分析实验室。可将重复样品分配给各种MS分析并归档用于长期质量控制(QA)和验证。
食品、饮料和消费品分析
食品与药物管理局(FDA)和几个独立的组织已在一些软饮料和果汁饮料中鉴定出低水平的苯。研究表明,在低pH值下,用作防腐剂的苯甲酸离子与抗坏血酸(补充的维生素C)反应,形成苯。苯是已知的致癌物质,并受到EPA的管理。废水中5ppb以上的任何浓度的苯都被认为是危险的。发明人对现有产品的调查显示,一些饮料中的苯浓度超过5ppb。尽管形成机理尚未完全已知,但是热、光和某些微量金属以及抗坏血酸似乎有助于苯甲酸离子转化成苯。FDA提出,苯的形成可能是瓶装饮料到达商店后的保质期和温度条件的函数。这是PSI-SPE和额定的(duterated)苯甲酸浓缩同位素标准样的浓度过低在液态标准样形式下不稳定、但被预吸附到固相上将是稳定的情况的示例。FDA或国土安全部需要分析的其他药物和毒素也可以在浓缩同位素形式下被预吸附,并且成为定性和定量分析中有价值的新分析工具。因此,重要的是找到一种方法来对水、饮料、食品、药品和其他样品流中的污染物和毒素进行快速、廉价、常规的监测,类似于这个在生产、质量控制和在国土安全和国防情形下适时地使用苯的示例。通过使用作为完全集成的自动分析测量系统的单独设备或前端模块的自动化多功能系统,可以经济有效地进行PSI-SPE。
SPI-SPE与标准样分析方法的对比研究
进行了时间研究,以提供使用预增量稳定同位素固相萃取(PSI-SPE)可实现的时间节省的示例。该研究主要针对一组10个水样,采用EPA方法8270作为测定方法、EPA方法3510作为萃取方法,对水样进行半挥发性分析物的分析。结果列于表3。
表3.一组10个水样的时间研究
| 过程 | 常规(小时) | 被测(小时) |
| 取样 | 0.67 | 0.33 |
| 装运 | 0.50 | 0.08 |
| 注册 | 0.33 | 0.08 |
| 萃取 | 0.83 | 0.25 |
| 萃取物制备 | 0.33 | 0.00 |
| 分析 | 1.33 | 1.00 |
| 数据处理 | 1.5 | 0.58 |
| 表格/报告 | 1.00 | 0.08 |
| 总计 | 6.49 | 2.41 |
PSI-SPE大大节省了时间。从现场到完成结果所用的样品处理时间是常规方法的37%。数据质量明显优于通过常规协议取得的数据。
经济评价
进行了成本研究,以获得对使用PSI-SPE可实现的成本节省的基本了解。本研究主要针对一组10个水样,采用EPA方法8270作为测定方法、EPA方法3510作为萃取方法,对水样进行半挥发性分析物的分析。结果列于表4。
表4.一组10个水样的成本研究
| 过程 | 常规($) | PSI-SPE($) |
| 取样 | 6.70 | 3.33 |
| 装运 | 5.00 | 0.83 |
| 注册 | 3.33 | 0.83 |
| 萃取 | 9.96 | 2.50 |
| 萃取物制备 | 5.28 | 0.00 |
| 分析 | 21.28 | 16.00 |
| 数据处理 | 24.00 | 9.28 |
| 表格/报告 | 12.00 | 1.33 |
| 总计 | $87.55 | $34.10 |
上述QCS利用现场PSI-SPE,大大节省了成本。从现场到完成结果所需的处理成本比常规方法低39%。当大批量生产和销售根据本发明的产品和设备时,通过规模经济将实现更多的费用节省。
为比较而被分开的样品的比较
获得一组真实世界的样品,并在外部实验室将其分开以比较结果。4个样品是从处于被补救汽油污染物的过程中的污染地点取得。样品被送往商业实验室进行常规分析,并使用现场PSI-SPE进行处理。结果列于表5。
表5.在商业环境实验室分开的监测水井样品
| 商业 | PSI-SPE | 商业 | PSI-SPE | 商业 | PSI-SPE | 商业 | PSI-SPE | |
| 样品名称 | MW-9 | MW-9 | MW-10 | MW-10 | MW-16 | MW-16 | MW-19 | MW-19 |
| 苯 | 54 | 45 | <5 | <5 | 7 | 8 | 58 | 45 |
| 甲苯 | <5 | <15 | <5 | <5 | <5 | <10 | <5 | <10 |
| 乙苯 | 76 | 59 | <5 | <5 | <5 | <5 | <5 | <5 |
| 二甲苯 | <10 | <50 | <10 | <10 | <10 | <10 | <10 | <10 |
| 萘 | 6 | 6 | <5 | <5 | <5 | <10 | <5 | <10 |
在9号监测水井(MW-9)、16号监测水井(MW-16)、以及19号水(MW-19)中检测兴趣分析物。两种方法的分析物的鉴定以及测定值都非常一致。
预吸附稳定同位素固相实证结论
实践表明,预吸附稳定同位素-固相萃取是一种有效的样品萃取和平衡方法。PSI-SPE将消除目前实验室萃取方法中的很多固有误差来源,并成为自动化的基础,从而能够设计出新颖、高效、可靠、快速的样品制备设备和系统。
固相ELISA和SELDI同位素稀释与物种化同位素稀释质谱
ELISA-最普遍的免疫测定法
哺乳动物的免疫反应开始于特定的特殊细胞群(B细胞)对免疫系统无法识别的化合物(抗原)的识别。然后,免疫系统开始产生抗原特异性B细胞,其能产生具有与抗原结合的特性的特定的蛋白质(抗体)。一旦与抗原结合,B细胞就促进一系列力求尽快消灭抗原的反应。免疫诊断法(免疫测定法)用该宿主防御蛋白质(抗体)直接在人的血液中检测外来物质,如病毒抗原。免疫测定法是一组利用抗体的抗原识别特性的高特异性蛋白结合测定法。现今采用的最普遍的免疫测定法为ELISA(酶联免疫吸附测定)法。所有ELISA系统的关键是抗体的使用。动物在抗原的刺激下产生抗体。抗体是特异性生物化学品,其与抗原结合,用于检测特定的抗原,用于生产。因此,如果结合可被证明,则可将抗体用于检测特定抗原。相反,可通过使用确定的抗原来测量特异性抗体,这在免疫化学研究和诊断生物学领域中构成许多测定法的基础。
定量的基础在于酶产生的信号,其与抗原浓度成正比或成线性关系。ELISA的优点是简单、易读(通过肉眼或设备)、快速、灵敏、商业供应的试剂、试剂盒和仪器、适应性强、分析人员和实验室的安全性、安全处置、相对容易的标准样化和定量。
利用激光电离,将同位素掺入固相表面修饰物质,进行直接和定量的固相IDMS和SIDMS质谱测量,从而当基体辅助激光解吸电离(MALDI)或激光烧蚀(LA)将表面和或基体都去除时,进行分析物直接浓缩同位素比分析。在这一点,通过另外一个之前不存在的的自由度为定量增加了另一维度。这个最后的自由度允许表面固态平衡系统用比率代替定量去除,以赋予IDMS和SIDMS数学优势。一个关键的优点是,不必为了实现定量和可重现性而去除整个修饰固相表面/基质(含浓缩同位素标记)和分析物。在IDMS和/或SIDMS情况下,修饰固相表面/基质(含浓缩同位素标记)的任何部分都允许基于同位素比而不是校准曲线来定量。无需校准曲线来实现定量是IDMS和SIDMS所独有的,其他形式的MALDI或LA需要定量和可重现的表面去除以产生校准曲线。这里,平衡表面的任何部分都产生准确定量,并排除通常与质谱定量和ELISA定量两者有关的误差。一旦平衡,基质吸附和清除效率的变化不再是定量中的因素。消除了IDMS和SIDMS方法的定量中传送离子通过质谱仪的质谱仪效率和信号漂移这些方面的误差来源。固相增量(标记)使上述IDMS和SIDMS中不适用于ELISA和或质谱领域的直接数学定量成为可能。
采用荧光定量的ELISA近来开始应用于环境卫生和环境法医学领域。ELISA已应用于三嗪、磺脲类药物、有机磷酸酯、多氯联苯(PCB)、环戊二烯类杀虫剂(cyclodienes)、和BTX(苯,甲苯,二甲苯)及其他毒素的化学分析,用于由美国EPA和环境订约人所作的废弃场所的生物分析和鉴定。限制ELISA在环境领域广泛使用的难点在于检出限、校准曲线误差和基质干扰。这些问题和多种误差来源削弱了ELISA生成的数据在环境卫生和法医领域中的法律辩护性,在这些领域中,专家常在法律程序中评估分析数据。由于使用固相平衡质谱和最终直接算法定量的最终的定量方法,通过IDMS和/或SIDMS的固相平衡和不采用校准曲线的直接定量在法律辩护性方面得到明显改善。由于采用了平衡同位素比,不完全和部分回收的基质和分析物、电离中的波动、仪器效率低下、性能下降和其他样品操作或仪器导向偏差对准确性而言是无关紧要的。因此,这些常见偏差都同时减少或消除,从而使数据辩护在法庭上处于更有利的地位。
ELISA可在各种不同的形状和包装的固体载体物质上以几种不同的格式进行。到目前为止,最普遍的ELISA使用8×12孔格式的塑料微量滴定板作为固相。因此,可在微孔板的92个个体孔的每一个中进行ELISA测试(见图9)。
为了创建有效的ELISA,必须满足三个条件:
稀释线性:这与下一个步骤—回收率密切相关。当在x-y图上绘制信号(表示为峰面积、峰面积或强度)-稀释因子曲线时,其必须生成直线。
回收率:这是当已知数量的有关物质被加入测定反应时,在测定之后观察到的有关物质的百分比。临床日常工作中的回收率应在10%以内。
百分比回收率={(估计值)-(净增值)}/(净增值)×100
批内和批间变异:通常是在不同的日期进行的,在一块ELISA板中的批内平均值,以及不同板间的批间平均值。
ELISA类型和系统
从根本上讲,有两种类型的ELISA:竞争(C-ELISA)或抑制(I-ELISA)。术语“竞争”和“抑制”描述测定,所述测定中的测量涉及通过对建立的预滴定系统的干扰能力来定量物质。该系统也可用于抗体或抗原的测量。
从方法论的角度,有三种基本的ELISA系统,是所有的ELISA测试(包括C型和I型;直接或间接)的基础:
直接ELISA。抗原通过被动吸附附着在固相上。清洗之后,加入酶标记抗体。经过潜伏期和清洗之后加入底物系统,允许颜色逐渐显示。
间接ELISA。来自特定生物物种的抗体与附着在固相上的抗原反应。通过添加异种(antispecies)酶标记抗血清来检测任何结合抗体。这广泛应用于临床诊断。
夹心ELISA。该系统涉及抗体或附着在固相物质上的捕捉抗原。
直接夹心ELISA。如果系统是直接夹心测定,则用酶标记检测抗体。利用抗原的血清特异性来检测抗原。用酶标记检测抗体。捕捉抗体和检测抗体可以是相同的血清,或者是来自同种的不同动物的血清,或是来自不同种动物的血清。用于直接夹心测定的抗原必须具有至少两个抗原基。
间接夹心ELISA。如果系统是间接夹心测定,则通过固相结合抗体来捕捉抗原。然后使用来自其他物种的抗体来检测抗原。其依次被异种结合物(antispeciesconjugate)结合。因此,用于涂层和检测抗体的血清物种必须不同;异种结合物不能与涂层抗体反应。
最常用的酶是辣根过氧化物酶(HRP)和碱性磷酸酶(AP)。也使用其他酶,例如β-半乳糖苷酶、乙酰胆碱酯酶和过氧化氢酶,但这些酶限制了底物选择,还限制其广泛应用。检测酶可直接与第一抗体联结,或通过识别第一抗体的第二抗体引入检测酶。如果第一抗体是生物素标记的,其也可以与例如抗生蛋白链菌素等蛋白质联结。底物的选择取决于检测的必要灵敏度水平和检测可用的仪表(分光光度计、荧光计或照度计)。在所有的蛋白标记和可视化技术中,由于标记和谱测量的简单性以及抗生物素蛋白(在蛋清和鸟类、爬行动物和两栖纲的组织中发现的糖蛋白)的高特异性和对生物素这种小维生素的选择性,人们所透彻了解的生物素化是最流行的。在用于检测和目标生物分析物的测定系统中,抗生物素蛋白-生物素反应是最有用的工具。抗生物素蛋白对生物素特别的亲和力允许复杂混合物中的含生物素的分子与抗生物素蛋白结合物离散地结合。
使用IDMS和/或SIDMS的质谱ELISA微阵列芯片
由于固有的高灵敏度和明显较低的干扰,质谱仪和同位素测量技术作为潜在的免疫检测系统是非常可取的,但是由于一些阻碍,它们没有成功地用作ELISA的最终定量探测器。主要原因是质谱仪的高成本、质谱探测器信号的不稳定、生物科学家缺乏同位素分析方面的专业知识以及质谱仪在生物分析测量领域相对新近的普及。
对于ELISA型测定,当肽位于被设置成微阵列板中的结合抗原或固定抗体行的离散取样点上时,使用浓缩同位素标记或同位素浓缩合成肽来模仿抗原基或抗体是可行的。然后对微阵列板进行处理,并将其引入质谱仪进行液体/或气体电离和最后的定量质谱分析。
当可固定在固相基质上的细胞被固定并作为抗原晶格时,在发酵过程中通过介质中的养分或通过化学同位素标记过程掺入同位素标记的所有细胞都可被使用,不管是活的还是减弱的。这些细胞包含在专门设计的多阵列芯片中,离散取样进行地点有能力保持细胞的结合在质谱仪的分析周期时长内保持存活。
将利用IDMS和/或SIDMS原理的同位素分析方法和本文所述的发明用于通过固定配体对其他生物分子的亲和力捕捉和分析生物分子,固定配体例如是凝集素、多糖、核苷酸、生物分子和/或可以脱离天然源或合成为功能类似物的化学毒素。浓缩同位素可用于固定在基因芯片微阵列上的数以千计的核苷酸探针中的每一个探针的可视化。
图10、11、12显示了根据本发明的实施例的表面修饰固相物质上的浓缩同位素标记抗原。
采用IDMS和/或SIDMS的质谱SELDI分析
质谱技术在临床诊断中的新近的一个应用涉及SELDI(表面增强激光解吸电离)芯片,其具有用于蛋白质表达谱(profiling)的蛋白质和多肽固定的各种不同的功能表面。这些芯片利用来自细胞样品源的固定生物标记,这些生物标记在细胞样品源中根据病情具有独特的响应表达。由于迄今为止的工作都采用直接蛋白组学分析,其到目前为止不涉及任何以最终的定量为目的的分子标记,这是由于整个生物标记分析和蛋白质表达谱领域被缺乏最终直接定量和可重现性所累。浓缩同位素标记通过提供在SELDI蛋白质芯片上测量同位素标记生物标记比的手段,克服了这些局限性,通过IDMS和/或SIDMS定量大大改善了定量和可重现性。见图13、14和15。
使用IDMS和/或SIDMS的直接组织谱
新的分子表达谱技术有助于通过微创活检获得的小病理样品的分析,涉及预后、治疗反应、以及创新的靶标确认相关的病理解剖分析可以发现关键的生物标记。因此健康和病理设置中的组织学水平的蛋白质组学分析是临床蛋白质组学领域中的重要问题。直接组织蛋白质组学分析(DTPA)是SELDI-MS技术的最初应用,可作为对病理解剖诊断的补充来扩展临床蛋白质组学的应用。DPTA方法提供了独特的高吞吐量特点,这可用于发现大量患者组中的生物标记。
DPTA方法已用于肺癌和脑肿瘤等疾病的分类,从而改进病理解剖诊断技术。DPTA是最近开发的快速、灵敏的技术,开启了通向临床蛋白质组学新观点的大门。通过使用浓缩同位素标记及应用引入作为固相表面修饰或非修饰介质的IDMS和/或SIDMS原理,获得了该领域目前需要的明确定量、重现性和灵敏度的发展。
直接数学反卷积是必要的,因为在环境法医学、环境卫生和国土安全测量的实践中只有直接数学求解才允许分析物的定量-实例
如刚刚通过人体组织中的汞物种所例证的,由于校准曲线导致80%以上的误差,因此不能用于定量。只有SIDMS直接浓缩同位素计算才既能进行定量又能校正物种转化中的物种转变。已发现,IDMS和SIDMS都必须通过数学算法直接计算而不应使用校准曲线来避免分析实验室中常见的误差,在国土安全,环境卫生和工业测量等关键测量中,这些误差是关键的、费时的、且不可接受的。
兴趣分析物的浓缩同位素类似物是从原始的浓缩同位素生成的,或是购买的或在实验室中合成的。本发明包含将IDMS和SIDMS与各种电离方法联用,如ESI、纳升电喷雾(nanoESI)、纳米芯片电喷雾(nanochipESI)、DESI、MALDI、LA、SELDI、APCI、ICP、GC-ICP、GC-MS。为实证目的,显示了GC-ICP-MS和纳升电喷雾飞行时间质谱。用GC-ICP-MS和通过nanochipESI与飞行时间质谱联用的电离(nanochipESI飞行时间质谱)平台的示例来例证适合国土安全、环境法医学、环境卫生、工业抽样测量情形的示例。附上汞物种、叠氮化钠和氰化钾的毒素数据的例证。
利用IDMS(同位素稀释质谱)和SIDMS(物种化的同位素稀释质谱)的增量对目标分析物物种进行定量测定需要的数学算法与传统的方法(和数学方法的新应用)不同,因为它们只需通过直接数学求解来完成。由纯标准样获得的校准曲线在单一测量中是不可能的或者可能根本无法采用。发展了这些相对实际情况的简化,并将其应用于多种类型的浓缩同位素样品制备,例如直接溶液电离和表面吸附、结合、离子交换、固相萃取测量及诸多其他方法。
不能通过标准样曲线定量且必须通过SIDMS测量完成的测量的第一示例是具有甲基汞和无机汞并增量了乙基汞的血液样品。样品在与独立的同位素类似物无机汞、乙基汞和甲基汞平衡后被分离和电离。在该示例中,无机汞Hg+2增量了98%的浓缩无机汞Hg+2-199,甲基汞(CH3Hg+)增量了甲基汞CH3Hg+-202,乙基汞(C2H5Hg+)增量了C2H5Hg+-201,金属汞物种(Hg0)未存在于原样品中,是在用于分离三个汞物种的GC柱中通过热分解产生的。下图16表明,使用校准曲线即使不是不可能,也是非常困难的,因为人体血液或尿液中的不同数量的无机汞、甲基汞和/或乙基汞会以不同的比例产生不同数量的四种物种(无机汞,甲基汞,乙基汞和金属汞),而对未知的个体样品是无法建立校准曲线的。只有通过SIDMS法的数学反卷积才能在这种情况下进行定量。与上文所述的人发和6种分离转化的示例相同,在该示例中,须进行定值和校正的至少有4种以上,因为这里不仅形成了第四物种金属汞,而且无机汞、甲基汞和乙基汞也促使了该第四物种的转化。
这些情况比过去更加普遍,且常见于多种类型的反应物种分析,如芥子气、农药和农药代谢物、可卡因及其在体内的代谢产物吗啡。这些分子位移很多都需要定量,但是如果用于定量的方法是校准曲线,则不服从于准确或快速的定量。
IDMS、SIDMS和直接物种算法取决于产生的物种,只有为了IDMS和SIDMS分析而新产生的直接数学算法才能用于动态系统的定量。
浓缩稳定同位素稀释剂(“稀释剂”,spike)与样品之间必须具有不同的同位素组成,但具有相同的兴趣分析物的化学形态和化学性质。实际样品的基质组成与正常标准样很少相同,与其他元素成分的任何差异导致在ESI、nanoESI、nanochipESL、MALDI、SELDI和APCI等软电离方法中表达不同的同位素类似物。因此,没有任何校准曲线能够准确代表样品。在此给出叠氮化钠和氰化钾的示例。
稀释剂是在水和/或酸中和/或有机溶剂溶液中制备的,或者通过吸附、离子交换或结合固定在表面。在软电离方法中,如喷雾(ESI)、nanoESI、DESI、MALDI和SELDI,或者在硬电离方法中,如上述汞物种示例中的ICP-MS,不能通过建立校准曲线的完成校准。在软电离方法中,被测量和定量的离子依赖于实际样品中的基质与分析物,无法通过标准样或者甚至于通过试图与基质匹配的标准样来模拟。离子同时是基质相互作用的产物。分析物可以有许多质谱仪中代表的代表性的分子离子和离子物种。将以叠氮为例显示几个基于基质和样品条件的表示法。每个表示法需要直接使用IDMS和SIDMS的不同数学定量。软电离不会独立于基质产生分子离子,但是把基质与环境结合以改变表示分子离子和同位素浓度类似物离子的浓度。举例如下。校准曲线和标准样IDMS和SIDMS公式的使用不能用于定量,而只有对来自软电离的这些同位素物种采用新的数学算法协议,定量才是可能的。可以看出,标准样IDMS公式不能说明用于定量的多种表达和同时和不同的同位素比。
将IDMS中用于同位素比定量测定的通用数学公式表示为式1,用于确定未知样品浓度的数学求解的直接算法是该公式的重排,显示为式2。该直接数学求解的各个组成部分在下面的式2中表示。
其中,
Wx=样品重量
Ws=同位素稀释剂的重量
Cs=稀释剂中的物种浓度(浓缩)
Cx=样品中的物种浓度(未知)
As=稀释剂中的改变的同位素A的原子分数(浓缩)
Ax=样品中的同位素A的原子分数(天然)
Bs=稀释剂中的改变的同位素B的原子分数(浓缩)
Bx=样品中的同位素B的原子分数(天然)
Mx=样品中的物种的平均原子质量
Ms=稀释剂中的物种的平均原子质量
Rm=同位素A与同位素B的测量同位素比(浓缩/天然)
校准曲线的使用也受到过筛物种浓度的限制,其中过筛(sifting)物种浓度取决于动态物种浓度和无法通过分别进行的标准样校准方案来重复的样品的基质。例如ESI、nanoESI、MALDI、APCI和EI等软电离方法是这些分子软电离源中的一些示例,这些软电离源最容易受到无法在不用基质的标准样溶液中复制的复杂分子离子的影响。动态物种和使用软电离方法通过样品基质本身确定的物种需要与硬电离方法十分不同的数学处理,例如ICP-MS的硬电离方法使所有物种变为元素离子,并且可以使用校准曲线,因为严格的(harsh)电离消除了基质效应和分子信息。
该应用不足以定量软电离和复杂电离的分子离子的各种表达。在该示例中,叠氮化物以正离子模式和负离子模式使用。该纯溶液中含有钠(Na)离子,Na是作为正离子影响添加的,正离子模式下物种之一的1:1的比率和负离子模式下的1:2或1:3的比率同时表达。任何可用和主要(dominant)的离子例如K都可以用只存在于具有上述样品的基质条件的实际样品中的分子离子代表。校准溶液的基质匹配不能准确或完全解释真实样品中的基质离子的浓度和实际条件的复杂性。还存在其他离子模式,如图17至24所示。在所述第一组示例中,只有多算法才能考虑到定量叠氮化物所必须的多种离子表达。在正离子模式中,发现一组物种离子,在负离子模式中,观察到明显不同比值的另一组物种离子(见图17至20)。
当物种是源自相同的母体物种的不同子物种时,在通过质谱仪根据质量分离的同位素浓缩和天然毒素的多种物种的准确定量中,没有偏置的直接校准是IDMS和SIDMS的扩展。这些情况下的反卷积不是正在转变的多种物种的反卷积,而是从溶液或固相的相同的物种产生并以独特的比率和图式表达的多种物种的反卷积。数学上,定量必须准确地考虑到几个物种和他们的不同比来定量毒素。图21表示荷质比(m/z)质谱的多个部分,该质谱在通过具有Na的该基质产生的不同物种中提供超过一打的确认比值,并且都在K和其他离子之间分裂,如果样品中含有K,将产生Na和K离子。在这种情况下,Na4(N3)5-离子也将具有Na3K、Na2K2和NaK3和K4类似物。这些中的每一个都是独特的,且与基于纯标准样进行的校准不同。只有通过对现场产生的实际同位素标记的真实物种应用直接数学求解才是定量的真实的样品。只能使用直接数学同位素比,因为没有基质和实际存在的样品,无法表达通过样品表达的实际分析物物种及其同位素类似物的准确表现。使用同位素比时准确浓度可达2和3位有效数字,但多数情况下在复杂基质中由模拟校准标准样能产生小于1位有效数字,这些这些不能作为工作的基础。
这些从天然和浓缩同位素物种产生的多个相关物种普遍存在于例如nanoESI和MALDI的软电离中,而由于离子的稳定性,这些物种在较硬的电离中消失。另一示例是氰化钾毒素,例如图24中所示。
在任何其他剂量的基质或混合物或阴离子螯合物将表达的金属离子成分(例如K或任何会被CN-螯合物螯合的金属离子)的基质中,谱中的Fe、Cu、Ni、Cd、Hg将被修饰,并会完全不同,在目前无法理论预测。例如,实际样品将具有例如对于Hg2+、Cd2+具有倍增的数学稳定性的形成常数和分阶形成常数,对于K1、K1K2、K1K2K3、K1K2K3K4为5.5、5.1、4.6、3.6,对于Hg和Cd离子分别与氰化物负离子的Ks(底物常数)的对数,为10.0、16.7、3.8和3.0。这些全部在竞争,无法计算,必须进行测量,并且建立校准曲线来定量无法预测的真实样品。在这些复杂软离子分子定量中,只有不校准的直接数学求解是可能的。在水溶液中可能表达超过80阶乘的离子可能组合。
术语的正常上下文中的传统的校准曲线的使用是不适用的。校准曲线的使用、采用校准曲线的内部标准样的使用或者基于这些离子的校准曲线是适当的,并能够由纯校准标准样以定量真实样品的未知基质的浓度的方式建立。如果存在钾和钠和其他离子,则表达钾和钠和其他金属加合离子,以及产生与母体毒素相关但在基于样品基质的质谱中却表达为新的物种的复杂物种,样品制备和离子环境将是独特的。如果同位素类似物的存在允许已知的一对物种也被定性识别为M+1和M+2类似物,识别也将更加确定。
在萃取之前和/或过程中添加到样品中的和/或在固相中平衡以进行所需的必要校准步骤的已知剂量的同位素浓缩物种,在这里通过样品中的非定量分析物表达。当传统意义上的校准不适用时,直接数学计算是既能识别又能定量分析物的唯一的可靠方式。当由添加到样品中的母体物种产生新的物种并且需要新的算法来直接定性和定量处理分析物时,这是SIDMS和IDMS的扩展。
微波增强平衡
使用IDMS和SIDMS方法时平衡时间对物种的影响:传统加热、超声萃取和微波增强平衡的比较
在该说明中,在通过SIDMS和IDMS技术的汞物种形成中使用NIST标准样参考物质(河流泥沙标准样参考物质(SRM)2704和土壤标准样参考物质(SRM)2711)和欧洲IAEA认证标准样物质(CRM)(人发IAEA-085)。两种标准样参考物质(2704和2711)增量已知量的同位素浓缩无机汞(199Hg2+)。该研究中评价的样品制备方法是EPA方法3052、EPA草拟方法3200(微波辅助萃取,MAE)和EPA方法3200(超声辅助萃取,UAE)。为实施EPA方法3052和方法3200(MAE),对样品进行增量,并立刻根据该方法萃取或消解。但是对于方法3200(UAE)这一选择,对样品进行增量,并用不同时间量(1小时、3小时、6小时、12小时、24小时和48小时)进行平衡,然后根据该方法萃取。
表6:平衡时间对总汞的IDMS分析的影响
不确定度在95%置信区间,n=4。
N/A-不适用,对样品进行增量并立刻消解/萃取。
由于EPA方法3052和3200(MAE)是非常高效的,因此实现从两个被研究标准样参考物质总汞的100%回收(表6)。在这种情况下,增量的同位素与样品同位素在萃取过程/消解中在小于10分钟之内平衡。
由于EPA方法3200(UAE)在无机汞的萃取和平衡中效率较低,因此回收百分比随着不同的研究标准样参考物质和时间而不同。标准样参考物质2704的回收百分比在24小时内上升到大约100%,而标准样参考物质2711即使在48小时之后也未获得定量回收。从方法3200(UAE)的回收百分比数据显示,无论稀释剂与样品的平衡花费1小时还是48小时,当使用UAE时,回收都取决于样品基质。该实践研究最后显示,用于水样IDMS分析的“稀释剂同位素与样品同位素的平衡”不是对所有类型的萃取协议下的复杂或固态样品都适用的。在前面提到的(LuYang等人)酵母的铬物种分析中,同一时间依赖萃取经历12小时来进行组织样品的热对流和热传导。对于固态样品,在质谱之前,高效萃取和平衡方法对于兴趣物种是必要的。低效的固相样品萃取和/或消解和平衡方法会导致不准确的IDMS或SIDMS分析。
SIDMS需要多种物种同时平衡并鉴别物种转变,以便校正每个物种的最终浓度。使用人发中的汞物种作为只包含甲基汞和无机汞物种的良好模型的示例,比较EPA方法3200中的两种可选方法,用MAE和UAE萃取这些物种。从表7的比较可以看出,UAE未获得正确的标准样结果,因为该步骤中结合的天然和浓缩同位素物种的萃取和平衡不发生,或者不够完全因此无法获得正确的答案。MAE与之形成对比,MAE采用微波来同时萃取两个物种和平衡浓缩的同位素物种。MAE在比UAE示例的一半时间更少的时间内获得统计学有效度内的标准样值。
表7.通过EPA方法6800的毛发样品(IAEA-085)中汞物种的浓度和百分比变化的反卷积,SIDMS使用浓缩的同位素试剂和反卷积算法
不确定度在95%置信区间,n=4
MAE-微波辅助萃取,共10分钟
UAE—超声辅助萃取,共28分钟
*括号中的值代表回收百分比
多物种转变和直接数学确定是必要的,优于校准曲线
有必要评价多物种转变和多物种的转化,以证明本发明所述的萃取和平衡方法的耐用性。目前没有三种汞物种的认证组织样品,因此将之前的认证标准样参考物质(CRM)(人发认证参考标准样物质,IAEA-085)增量第三汞物种乙基汞。这是一种合理的选择,因为文献表明乙基汞是人体从疫苗中的汞防腐剂硫柳汞代谢的汞物种。由于这三种物种的存在,必须计算六种物种转化。为这一特殊目的发展了数学算法,用于样品制备过程中的三种物种和它们之间的转化的SIDMS测量。表8中揭示了80%以上的乙基汞转化,该乙基汞转化主要是由于乙基汞转化为无机汞以及乙基汞转化为甲基汞。甲基汞的转化也值得注意,并特定的从乙基汞转化得到的甲基汞单独测量。如果没有统一地同时萃取和平衡所有汞物种,该测量无法进行。
表8:对总汞和甲基汞认证的人发认证标准样参考物质(IAEA-085),增量浓度22μg/g的天然乙基汞。使用微波萃取和HPLC-ICP-MS分析,对三种物种应用EPA方法6800,对物种的全部六种转化应用校正。显示了该实践研究中得到的多个复制品及分析空白试验值
这些数据是三个物种的第一应用,采用微波萃取(EPA方法3200)与IDMS/SIDMS(EPA方法6800)联用技术同时校正全部三个物种的转变和互变物种,说明即使可以转变或破坏80%以上的乙基汞,也只能通过应用SIDMS技术得到准确快速的同步测量。对这些测量进行证明和实践,准确度保持在4%以下。
根据物种和同位素浓缩物种的表达,IDMS和SIDMS中的算法容易手动或动态可调。然而,校准曲线是不可调的。必须每次产生它们,例行公事并且相对频繁。校准曲线不是对多物种分析的数学可行的替代,因为即使当发生最微小的基质样品变化时,误差和位移也会妨碍其使用。因此,进行用于定量的同位素浓缩类似物的IDMS和SIDMS测量的唯一的数学准确的方法。这对于国土安全和国防应用以及必须得到和确保最低的第一类误差(false positive)和第二类误差(falsenegative)的质量保证测量而言是关键的。本文通过实例进一步描述了IDMS和SIDMS的这些方面。
第三部分—描述了现场应用的完全自动化系统中的集成:
例如用于国防和国土安全,说明如下:
随着恐怖主义的威胁和食物、空气和饮用水的针对性污染的潜在可能,产生了以最准确的可能方式(第一类误差最低或不存在)对易挥发试剂快速检测大量的相对少见但高毒性的化合物的需要。由于最危险的试剂是非常有效的,因此强烈要求毒素探测器能够准确可靠地检测到最低浓度水平。鉴于工作的任务的关键性和时间紧迫性,依赖性地在不同的情况和环境下能够保持其准确度和灵敏度的耐用的现场使用系统中,周期(取样、样品制备/样品操作和分析)必须快速结束。
如果使用标准样,优选的是不处理标准样(典型为高毒性物质的化学类似物),以便这些标准样固定在固相过滤器、充满珠子的柱、柱体和其他相对安全的小型固相设备中,这些固相设备的运输远比液体更为安全,并且可在对液体而言会不稳定且需要频繁更换的浓度下来运输。如果需要将在现场或远处取得的样品运输到实验室,将样品放入固相容器内的能力,可能以在整个保管链(从源中去除样品与运往通常是专门的实验室的分析地之间的步骤)中稳定(将保持其化学形式)和安全地处理的形式固定。
现今可用的大多数灵敏和有用的检测系统在分析样品时都使用标准样校准方法来建立有用的探测器信号范围,并依赖于校准范围作为计算探测器产生的探测器信号的参考。任何在实验室工作的化学家将非常熟悉校准曲线的使用。不幸的是,校准曲线受到许多的潜在误差源的影响,并且需要频繁中断样品分析周期来重新校准。基质(在其中发现兴趣分析物的物质)变化、分析物萃取过程中的变化都在基于校准曲线的测量中引入误差。此外,质谱仪是能够检测到“万亿(trillion)分之一”水平的分子的最灵敏的探测器,其产生使最终建立的校准曲线无效的信号漂移。为质谱仪建立新的校准曲线意味着分析人员要进行大量的手动、繁重、耗时的样品制备和分析步骤。所有这些与校准曲线有关的潜在误差源排除了现有的质谱仪为了国土安全和国防目的自动化的可能性。
本文前面所引用的关于IDMS和SIDMS的现有发明和专利以及本文所描述的发明解决了这些问题。浓缩同位素标记和浓缩标准样类似物的使用提供了在核子范围而不是化学范围进行测量的能力,该技术基于所有流行的发色、荧光、化学发光和其他可视化技术。其依次消除了许多干扰和稳定性问题。IDMS和SIDMS利用数学求解来产生最终数据,这消除了校准曲线的需要,消除或最小化了与基质变化和萃取步骤之后的分析物回收有关的问题。通过IDMS和/或SIDMS协议下的质谱法产生的分析数据是校准的和高度准确的结果。在应用该专利的时候,IDMS和SIDMS协议已被美国环保署(EPA)所接受,作为国家方法,指定为“方法6800”,该方法已被EPA和英国标准样协会(BSI)在发表的意见和文件中认可,作为能够产生用于物种化的元素分析的法律辩护数据的唯一方法。
目前,分析前(前期过程)的样品制备要求从现场去除样品、兴趣分析物萃取、分析物分离、用浓缩同位素进行增量(或标记),其包括高度熟练的分析人员进行的一系列的手动步骤。该过程将花费几小时到数天均有可能。前期的时间的显著缩短和手动步骤的消除是在IDMS和SIDMS能够自动化之前势在必行的。本发明精确实现了这些前期性能改进来实现完全的、交付使用的自动化。
在应用本发明的时候,发明人正处于代表美国政府开发被称为“集成工业方法系统(IIMS)”的五阶段程序,目标是创建武装部队和紧急出动人员能够实地使用的化学和生物测量系统。将自校准、实地使用构思为包括本发明所述的所有自动化特征的质量分析器。
无论是通过恐怖分子还是工业过程引入到环境中,毒剂都以物种化和复杂的化学形式存在,这常常使得可以通过现有的实验室分析自动检测和测量它们。通常,必须使用长期、繁琐的样品制备和校准步骤和多种检测方法。这些方法完全不适合IIMS类型的应用。
自动化需要和安全和检测性能问题的大多数或所有方面已付诸实施。例如,应用同位素技术(AIT)公司发售的IDMS和SIDMS产品已向环境实验室、研究实验室、工业实验室和疾病控制中心出售,用于测量水、土壤、毛发、组织、血液和尿液,以及天然和工业来源的有毒化学制品的分析。AIT产品已作为IDMS和SIDMS试剂盒出售,包括同位素稀释剂、浓缩标准样类似物和用于最终的数学反卷积和计算的软件。AIT的产品已用于不同类型的质谱仪,例如飞行时间(TOF)和电感耦合等离子体(ICP)、与高效液相色谱(HPLC)和气相色谱(GC)联用,采用电喷射电离(液体到液体喷雾)和气体电离(液体到气体)的形式。其他发明,如用于快速增量和平衡、同时萃取、增量和平衡的固相介质保持同位素标记或浓缩标准样类似物,已付诸实施。
Claims (8)
1.一种用于平衡同位素稀释质谱样品的方法,包括以下步骤:
a)向溶液中添加一定量或浓度的同位素标记分析物类似物以产生预标记微波介质;
b)向所述预标记微波介质中添加包含或被怀疑包含与所述同位素标记分析物类似物对应的兴趣分析物的样品,以产生可微波溶液;
c)通过将所述可微波溶液培养1秒至1小时而平衡所述兴趣分析物,以产生平衡样品;以及
d)对所述平衡样品进行质谱分析。
2.根据权利要求1所述的方法,其中分析物选自包括含有任意天然存在同位素变化的元素的化合物或成分的组。
3.根据权利要求1所述的方法,其中微波所述可微波溶液的步骤在1010至1013赫兹范围内进行。
4.根据权利要求3所述的方法,其中微波所述可微波溶液的步骤在2450兆赫兹处进行。
5.根据权利要求1所述的方法,其中分析物选自包括含有汞、叔丁醇、甲基叔丁醚、乙基叔丁醚、二异丙醚、叔戊基甲基醚、吗啡、二氧六环、二氯乙烷、四氯乙烷、萘和菲的单质和化合物的组。
6.根据权利要求2所述的方法,其中基于存在的全体分析物与同位素标记分析物类似物之比来计算样品中的分析物的浓度,其中所述全体分析物是通过质谱测定的。
7.根据权利要求2所述的方法,其中基于物种的同位素比使用浓度和/或降解调整的数学计算来直接计算分析物的浓度,而不使用校准曲线。
8.根据权利要求2所述的方法,其中所述平衡步骤用于自动化的IDMS或SIDMS质谱。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US87338306P | 2006-12-07 | 2006-12-07 | |
| US60/873,383 | 2006-12-07 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2007800509715A Division CN101600954B (zh) | 2006-12-07 | 2007-12-07 | 固相及催化实现的自动同位素稀释和物种化同位素稀释质谱法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103257070A true CN103257070A (zh) | 2013-08-21 |
Family
ID=39734950
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2013100318147A Pending CN103257070A (zh) | 2006-12-07 | 2007-12-07 | 用于平衡同位素稀释质谱样品的方法 |
| CN2007800509715A Active CN101600954B (zh) | 2006-12-07 | 2007-12-07 | 固相及催化实现的自动同位素稀释和物种化同位素稀释质谱法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2007800509715A Active CN101600954B (zh) | 2006-12-07 | 2007-12-07 | 固相及催化实现的自动同位素稀释和物种化同位素稀释质谱法 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US8383420B2 (zh) |
| EP (1) | EP2108111B1 (zh) |
| JP (1) | JP5412288B2 (zh) |
| CN (2) | CN103257070A (zh) |
| AU (1) | AU2007349186B2 (zh) |
| CA (1) | CA2671859C (zh) |
| DK (1) | DK2108111T3 (zh) |
| HK (1) | HK1138908A1 (zh) |
| WO (1) | WO2008112032A2 (zh) |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103837593A (zh) * | 2014-03-18 | 2014-06-04 | 中国计量科学研究院 | 一种人血清蛋白质电泳后同位素稀释质谱定量方法 |
| CN103913534A (zh) * | 2014-02-11 | 2014-07-09 | 中国科学院地质与地球物理研究所兰州油气资源研究中心 | 一种天然气中系列烃类化合物碳同位素分析方法 |
| CN104006993A (zh) * | 2014-05-26 | 2014-08-27 | 中国兵器工业集团第五三研究所 | Id-icp-ms法燃油中硫含量的测试样品制备方法 |
| CN108780064A (zh) * | 2016-03-07 | 2018-11-09 | 株式会社日立高新技术 | 分析装置 |
| CN109073658A (zh) * | 2016-04-14 | 2018-12-21 | 豪夫迈·罗氏有限公司 | 用于测定体液样品中的靶分析物的浓度的方法 |
| CN110243919A (zh) * | 2019-05-14 | 2019-09-17 | 中国石油天然气股份有限公司 | 一种利用钒同位素对油气成因与来源进行分析的方法 |
| CN113167802A (zh) * | 2018-12-04 | 2021-07-23 | 百时美施贵宝公司 | 通过多同位素体反应监测使用样品内校准曲线的分析方法 |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2771467A1 (en) | 2009-08-19 | 2011-02-24 | Mcgill University | Methods and systems for the quantitative chemical speciation of heavy metals and other toxic pollutants |
| US9443708B2 (en) * | 2014-09-10 | 2016-09-13 | Battelle Memorial Institute | Ion implantation system and process for ultrasensitive determination of target isotopes |
| CN104897766B (zh) * | 2015-04-27 | 2017-08-08 | 北京市医疗器械检验所 | 一种用同位素稀释质谱法测定样品中痕量元素的校正方法 |
| US11099165B1 (en) | 2016-03-08 | 2021-08-24 | United States Of America As Represented By The Secretary Of The Air Force | Focusing agents and methods of using same |
| CN107576748B (zh) * | 2016-09-29 | 2019-07-12 | 宁波大学 | 一种应用超声辅助-顶空-固相微萃取技术测定土壤中七种多氯联苯的方法 |
| USD827309S1 (en) | 2017-03-07 | 2018-09-04 | Paris Presents Incorporated | Makeup brush |
| USD827308S1 (en) | 2017-03-07 | 2018-09-04 | Paris Presents Incorporated | Makeup brush |
| CN108624516B (zh) * | 2017-03-20 | 2022-08-26 | 华东理工大学 | 一种提高发酵细胞中的代谢产物量及制备idms标准品的方法 |
| CN108303457B (zh) * | 2018-02-11 | 2023-12-29 | 中国科学院地质与地球物理研究所 | 一种用于电离层H、He同位素测量的仪器和方法 |
| EP3576129B1 (en) * | 2018-06-01 | 2023-05-03 | Thermo Fisher Scientific (Bremen) GmbH | Method for detecting the isotopic labelling state of unknown species of molecules |
| CN111089969B (zh) * | 2018-10-24 | 2023-08-22 | 复旦大学 | 一种n-糖链快速酶解释放和固相富集并质谱分析的方法 |
| US11022593B2 (en) | 2018-10-25 | 2021-06-01 | Savannah River Nuclear Solutions, Llc | Solid phase sampling device and methods for point-source sampling of polar organic analytes |
| CN111257098A (zh) * | 2018-11-30 | 2020-06-09 | 中国科学院大连化学物理研究所 | 一种催化剂重积碳物种结构的定性检测方法 |
| CN112683986B (zh) * | 2021-03-18 | 2021-06-15 | 裕菁科技(上海)有限公司 | 一种用于定量样品中目标分析物的天然同位素校准曲线法 |
| CN115060808A (zh) * | 2022-02-24 | 2022-09-16 | 上海大学 | 固相萃取结合气相色谱-质谱同时检测水环境介质中多种有机磷酸酯的方法 |
| CN115859632B (zh) * | 2022-12-07 | 2023-05-26 | 中科三清科技有限公司 | 在线源解析模型不确定度调节方法、装置与可读存储介质 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5414259A (en) * | 1994-01-05 | 1995-05-09 | Duquesne University Of The Holy Ghost | Method of speciated isotope dilution mass spectrometry |
| CN1292090A (zh) * | 1998-01-29 | 2001-04-18 | 霍利戈斯特杜肯大学 | 活性物质的物种化同位素稀释质谱法及相关方法 |
| EP1256370A2 (en) * | 1996-03-15 | 2002-11-13 | British Nuclear Fuels PLC | Separation of isotopes by ionisation for processing of nuclear fuel materials |
| CN1575195A (zh) * | 2001-01-29 | 2005-02-02 | 美塔莱公司 | 自动在过程同位素和质谱分析 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6113153A (ja) * | 1984-06-29 | 1986-01-21 | Hitachi Ltd | 自動滴定装置 |
| AU6689401A (en) * | 2000-06-12 | 2001-12-24 | Univ Washington | Selective labeling and isolation of phosphopeptides and applications to proteomeanalysis |
| JP4833498B2 (ja) * | 2000-10-03 | 2011-12-07 | ミラリ バイオサイエンシズ,インコーポレーテッド | 指向性マイクロ波化学のための方法および組成物 |
| US7348182B2 (en) * | 2000-10-03 | 2008-03-25 | Mirari Biosciences, Inc. | Directed microwave chemistry |
| JP4062514B2 (ja) * | 2001-01-02 | 2008-03-19 | ザ・クリーブランド・クリニック・ファンデーション | ミエロペルオキシダーゼ、心臓血管疾患についての危険性指示因子 |
| US7183116B2 (en) * | 2001-05-14 | 2007-02-27 | The Institute For Systems Biology | Methods for isolation and labeling of sample molecules |
| US7220383B2 (en) * | 2001-07-13 | 2007-05-22 | Metara, Inc. | Method and instrument for automated analysis of fluid-based processing systems |
| US7531134B1 (en) * | 2002-03-08 | 2009-05-12 | Metara, Inc. | Method and apparatus for automated analysis and characterization of chemical constituents of process solutions |
| FR2883977B1 (fr) * | 2005-04-05 | 2007-06-22 | Centre Nat Rech Scient | Machine laser d'analyse directe |
-
2007
- 2007-12-07 WO PCT/US2007/086795 patent/WO2008112032A2/en active Application Filing
- 2007-12-07 JP JP2009540500A patent/JP5412288B2/ja active Active
- 2007-12-07 EP EP07873961.2A patent/EP2108111B1/en active Active
- 2007-12-07 CN CN2013100318147A patent/CN103257070A/zh active Pending
- 2007-12-07 CN CN2007800509715A patent/CN101600954B/zh active Active
- 2007-12-07 US US11/952,471 patent/US8383420B2/en active Active
- 2007-12-07 CA CA2671859A patent/CA2671859C/en active Active
- 2007-12-07 DK DK07873961.2T patent/DK2108111T3/da active
- 2007-12-07 AU AU2007349186A patent/AU2007349186B2/en active Active
-
2010
- 2010-06-08 HK HK10105610.7A patent/HK1138908A1/xx unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5414259A (en) * | 1994-01-05 | 1995-05-09 | Duquesne University Of The Holy Ghost | Method of speciated isotope dilution mass spectrometry |
| EP1256370A2 (en) * | 1996-03-15 | 2002-11-13 | British Nuclear Fuels PLC | Separation of isotopes by ionisation for processing of nuclear fuel materials |
| CN1292090A (zh) * | 1998-01-29 | 2001-04-18 | 霍利戈斯特杜肯大学 | 活性物质的物种化同位素稀释质谱法及相关方法 |
| CN1575195A (zh) * | 2001-01-29 | 2005-02-02 | 美塔莱公司 | 自动在过程同位素和质谱分析 |
Non-Patent Citations (1)
| Title |
|---|
| ROBERT CLOUGH等: "Investigation of equilibration and uncertainty contributions for the determination of inorganic mercury and methylmercury by isotope dilution inductively coupled plasma mass spectrometry", 《ANALYTICA CHIMICA ACTA》 * |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103913534A (zh) * | 2014-02-11 | 2014-07-09 | 中国科学院地质与地球物理研究所兰州油气资源研究中心 | 一种天然气中系列烃类化合物碳同位素分析方法 |
| CN103913534B (zh) * | 2014-02-11 | 2016-08-17 | 中国科学院地质与地球物理研究所兰州油气资源研究中心 | 一种天然气中系列烃类化合物碳同位素分析方法 |
| CN103837593A (zh) * | 2014-03-18 | 2014-06-04 | 中国计量科学研究院 | 一种人血清蛋白质电泳后同位素稀释质谱定量方法 |
| CN103837593B (zh) * | 2014-03-18 | 2016-11-23 | 中国计量科学研究院 | 一种人血清蛋白质电泳后同位素稀释质谱定量方法 |
| CN104006993A (zh) * | 2014-05-26 | 2014-08-27 | 中国兵器工业集团第五三研究所 | Id-icp-ms法燃油中硫含量的测试样品制备方法 |
| CN104006993B (zh) * | 2014-05-26 | 2016-08-24 | 中国兵器工业集团第五三研究所 | Id-icp-ms法燃油中硫含量的测试样品制备方法 |
| CN108780064A (zh) * | 2016-03-07 | 2018-11-09 | 株式会社日立高新技术 | 分析装置 |
| CN109073658A (zh) * | 2016-04-14 | 2018-12-21 | 豪夫迈·罗氏有限公司 | 用于测定体液样品中的靶分析物的浓度的方法 |
| CN109073658B (zh) * | 2016-04-14 | 2021-07-09 | 豪夫迈·罗氏有限公司 | 用于测定体液样品中的靶分析物的浓度的方法 |
| CN113167802A (zh) * | 2018-12-04 | 2021-07-23 | 百时美施贵宝公司 | 通过多同位素体反应监测使用样品内校准曲线的分析方法 |
| CN110243919A (zh) * | 2019-05-14 | 2019-09-17 | 中国石油天然气股份有限公司 | 一种利用钒同位素对油气成因与来源进行分析的方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2671859C (en) | 2016-07-12 |
| CN101600954A (zh) | 2009-12-09 |
| WO2008112032A2 (en) | 2008-09-18 |
| DK2108111T3 (da) | 2019-07-15 |
| JP2010512515A (ja) | 2010-04-22 |
| US8383420B2 (en) | 2013-02-26 |
| US20120142545A1 (en) | 2012-06-07 |
| HK1138908A1 (en) | 2010-09-03 |
| JP5412288B2 (ja) | 2014-02-12 |
| EP2108111A2 (en) | 2009-10-14 |
| AU2007349186B2 (en) | 2014-03-06 |
| CN101600954B (zh) | 2013-03-13 |
| AU2007349186A1 (en) | 2008-09-18 |
| CA2671859A1 (en) | 2008-09-18 |
| WO2008112032A3 (en) | 2008-12-31 |
| EP2108111B1 (en) | 2019-04-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101600954B (zh) | 固相及催化实现的自动同位素稀释和物种化同位素稀释质谱法 | |
| Ammann | Inductively coupled plasma mass spectrometry (ICP MS): a versatile tool | |
| Cigić et al. | An overview of conventional and emerging analytical methods for the determination of mycotoxins | |
| Rahmani et al. | Qualitative and quantitative analysis of mycotoxins | |
| B’hymer et al. | Selenium speciation analysis using inductively coupled plasma-mass spectrometry | |
| Benson et al. | Forensic applications of isotope ratio mass spectrometry—a review | |
| Maggira et al. | Determination of aflatoxin m1 in raw milk using an hplc-fl method in comparison with commercial elisa kits—Application in raw milk samples from various regions of greece | |
| Xue et al. | Towards mass spectrometry-based chemical exposome: current approaches, challenges, and future directions | |
| Sieper et al. | A measuring system for the fast simultaneous isotope ratio and elemental analysis of carbon, hydrogen, nitrogen and sulfur in food commodities and other biological material | |
| Samy et al. | An advanced LC-MS (Q-TOF) technique for the detection of amino acids in atmospheric aerosols | |
| López-Ruiz et al. | Metabolomics approaches for the determination of multiple contaminants in food | |
| Namieśnik et al. | Role of reference materials in analysis of environmental pollutants | |
| Pan et al. | Automatic supported liquid extraction (SLE) coupled with HILIC-MS/MS: an application to method development and validation of erlotinib in human plasma | |
| Pereira et al. | An Automated Methodology for Non-targeted Compositional Analysis of Small Molecules in High Complexity Environmental Matrices Using Coupled Ultra Performance Liquid Chromatography Orbitrap Mass Spectrometry | |
| Birbeck et al. | Dhb microcystins discovered in USA using an online concentration LC–MS/MS platform | |
| Gharibi et al. | Proteomics-Compatible Fourier Transform Isotopic Ratio Mass Spectrometry of Polypeptides | |
| Wahlen et al. | Simultaneous co‐extraction of organometallic species of different elements by accelerated solvent extraction and analysis by inductively coupled plasma mass spectrometry coupled to liquid and gas chromatography | |
| Waddell et al. | Inductively coupled plasma mass spectrometry for elemental speciation: Applications in the new millennium | |
| Centineo et al. | Isotope dilution SPME GC/MS for the determination of methylmercury in tuna fish samples | |
| Ismail et al. | Validation and measurement uncertainty of rapid and simultaneous determination of 19 elements in drinking water using ICP-MS | |
| Morabito et al. | Towards a new certified reference material for butyltins, methylmercury and arsenobetaine in oyster tissue | |
| Baeyens et al. | Investigation of headspace and solvent extraction methods for the determination of dimethyl-and monomethylmercury in environmental matrices | |
| Grocholska et al. | Qualitative and Quantitative Mass Spectrometry in Salivary Metabolomics and Proteomics | |
| Yip et al. | Commonly used methodologies for inorganic analysis in international key comparisons | |
| Groh et al. | Mass spectrometry in environmental toxicology |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20130821 |