CN102787355A - 一种α-Bi2O3单晶微米棒的制备方法 - Google Patents
一种α-Bi2O3单晶微米棒的制备方法 Download PDFInfo
- Publication number
- CN102787355A CN102787355A CN2012103270056A CN201210327005A CN102787355A CN 102787355 A CN102787355 A CN 102787355A CN 2012103270056 A CN2012103270056 A CN 2012103270056A CN 201210327005 A CN201210327005 A CN 201210327005A CN 102787355 A CN102787355 A CN 102787355A
- Authority
- CN
- China
- Prior art keywords
- preparation
- biobr
- bi2o3
- nabr
- monocrystalline
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Inorganic Compounds Of Heavy Metals (AREA)
Abstract
本发明涉及一种生产α-Bi2O3单晶微米棒的方法。其方法是以溴化钠(NaBr)和硝酸铋(Bi(NO3)3•5H2O)为原料,首先合成α-Bi2O3的前驱体BiOBr,然后将生成的BiOBr放入马弗炉中以10℃/分钟的升温速率从室温升温至750~900℃后,保温2~4小时后,随炉温冷却至室温,使BiOBr在焙烧过程中失去溴元素的同时发生晶格转变,生成直径为5~10μm、长度为10~50μm的α-Bi2O3单晶微米棒。所制备的α-Bi2O3单晶结晶度高、晶粒形貌、大小均匀,晶体纯度高。本发明制备工艺简单,且原料要求低,有利于工业化生产,具有良好的工业化运用前景。
Description
技术领域
本发明为微米级α-Bi2O3单晶微米棒的生产技术,尤其涉及一种通过焙烧使BiOBr失去溴元素的同时发生晶格转变生产α-Bi2O3单晶微米棒材料的方法。
背景技术
Bi2O3是一种先进的半导体功能材料。由于其具有特殊的能带、电子结构和独特的晶体形态,因而被广泛应用于电子陶瓷材料、特种玻璃、电解质材料、光电材料、传感器,微电子元件,微电子元件、高温超导材料、催化剂、铁电材料等各领域中, 同时还用于化学试剂、铋盐、防火材料、高折光率玻璃、核工程玻璃制造和核反应堆燃料等方面( 吴绍华,刘进,兰尧中. Bi2O3 制备方法的研究现状及发展趋势[J]. 湿法冶金, 2005,24(3)121-127)。例如, Bi2O3可作为高效光催化剂降解水体有机污染物(刘红, 梅光军, 周国华. Bi2O3催化氧化法处理选矿废水试验研究 [J], 金属矿山, 2011,(417)151-153),Bi2O3可给α-H 提供氧原子形成对称的烯丙基中间体,因此它可用作丙烯的选择性氧化制丙烯醛及丙烯氨氧化的高效催化剂;当它作为检测NO气体的半导体传感材料时,其选择性比常用的SnO2 高得多;Bi2O3 用作固体电解质材料添加剂时,其传导性优于ZrO2和CeO2;在氧化锌压敏电阻器的生产中,加入一定量的Bi2O3, 能大幅度提高其压敏电阻性能。氧化铋薄膜还常用于光学涂层、光电子器件、透明陶瓷玻璃的生产等。目前随着工业技术的发展和研究的深入,Bi2O3 的应用领域仍在不断扩大。因此,探索生产过程简单、产品纯度高、结晶性能好、具有特殊形貌的纳米或微米级的Bi2O3的制备方法具有重要意义。铋还是我国重要的有色金属之一,其资源丰富,我国铋年产量居世界第一,但目前由于产品科技含量较低,大部分以金属铋锭形式出口,在国际市场竞争力不强,因而开发具有自主知识产全的具有高附加值的铋精细化学品产品具有重要的经济和社会价值。
作为先进半导体功能材料的Bi2O3,其功能强烈取决于其晶型、晶体形貌、结晶度等微观结构。如具有介孔形貌的β-Bi2O3薄膜的光催化活性远优于非孔结构的β-Bi2O3薄膜的光催化活性(K. Brezesinski, R. Ostermann, P. Hartmann, J. Perlich, T. Brezesinski, Exceptional photocatalytic activity of ordered mesoporous β-Bi2O3 thin films and electrospun nanofiber mats [J], Chemistry Materials, 2010, 22 (10) 3079–3085);而在α-, β-, γ-, δ-和 ω-Bi2O3五种晶型中,ω-Bi2O3或δ-Bi2O3的离子导电性最好(H. W. Kim, Synthesis and characterization of crystalline β- Bi2O3 nanobelts [J], Thin Solid Films, 2008, (516) 3665–3668)。颗粒尺寸在几个纳米的Bi2O3颗粒通常具有大比表面积和表面能,易表现出纳米材料独特的表面效应、量子尺寸效应等,通常具有很高的催化活性;而型貌为一维、二维或三维的Bi2O3纳米/微米线、带和棒等通常具有更优异的离子导电性和气敏性,特别是当尺寸达到微米级的Bi2O3单晶具有更实际的使用价值。因此,寻找能合成具有特定晶型、特定形貌的Bi2O3的方法极为重要。
目前,Bi2O3的主要制备方法有化学沉淀法、溶胶-凝胶法、水热法、化学气相沉积法、固相室温法、等离子体法等。化学沉淀法是首先制得铋盐溶液,然后加入碱、碳酸根等沉淀剂和一定的分散剂或络合剂,制得沉淀,再经过过滤、洗涤、焙烧等处理制取Bi2O3粉体。 该法过程简单,易操作,易于实现规模化生产,是目前常用的制备Bi2O3纳米粉体的主要方法之一。但该法不能制备尺寸达到微米级别且有固定晶体形貌的一维、二维或三维的Bi2O3纳米棒、线和带等,且该法制备的Bi2O3晶型通常比较复杂,常有α-, β-, γ-, δ-和 ω晶相共存,很难制得单一晶型,颗粒尺寸均匀具有特殊形貌的Bi2O3晶体。溶胶-凝胶法是制备Bi2O3粉体材料的另一方法。它是通过金属的有机或无机化合的盐溶液水解得到溶胶,在溶胶中加入螯合剂,催化剂或分散剂等形成水凝胶,然后经干燥蒸发溶剂形成凝胶后进行焙烧处理,得到纳米材料。该法生产的Bi2O3具有纯度高,均匀性好,颗粒尺寸小等优点。但在反应条件的控制、转化剂的选择和实际操作方面,仍具有很多局限性,且制备成本较高,同样无法制备尺寸达到微米级别且有固定形貌的二维纳米棒、线和带等。如Pan采用聚丙烯酰氨溶胶法制备了颗粒尺寸为30 ~ 50 nm Bi2O3纳米粒子(C. Y. Pan, X. H. Li , F.R. Wang, L. F. Wang. Synthesis of bismuth oxide nanoparticles by the polyacrylamide gel route [J], Ceramics International, 2008, (34) 439–441)。该法比较适合少量薄膜和复合氧化物的生产。微乳液法是利用两种互不相溶的溶剂在表面活性剂的作用下形成乳液,在微泡中经成核、聚集、团聚,再经过过滤、洗涤、干燥和焙烧制取纳米粉体材料的一种方法,其特点是微粒的分散性和界面性好,但在反应条件的控制,表面活性剂的选择和实际操作和成本方面具有很多局限性,同样无法制备尺寸达到微米级别且有固定形貌的二维纳米棒、线和带等。如丁鹏等以十二烷基苯磺酸钠为表面活性剂,采用微乳法制备了25.16~ 35.11 nm Bi2O3 纳米粒子(丁鹏, 杜尧国, 徐自力, 微乳法制备的纳米Bi2O3对苯系物光催化活性, 吉林大学学报, 2004,(42)451-454)。室温固相法是一种通过固相到固相的变化来制备纳米粉体的一种方法。在室温下,通过机械力的作用使反应的粒子间剧烈碰撞、变形、融合,首先在反应离子的界面上发生塑性变形,随粒子剪切力的增加,反应粒子连续破裂,成为次粒子,次粒子不断破裂变小,表面能不断升高,克服能垒后,聚集成核得到产物微粒。在反应中,控制晶核的进一步聚集,可得到超细纳米粒子。固相反应法工艺比较简单,且在室温下就可以实现,因而在Bi2O3纳米粉体制备研究具有一定优势,但从原理和工艺过程可以看出。固相反应相当于机械合金化过程,在研磨过程中容易带入杂质,对制备高纯度的功能材料有一定的局限性,同时对研磨设备有比较高的要求。该法同样无法生产且有固定晶体形貌的一维、二维或三维的Bi2O3纳米棒、线和带等。水热合成法是利用高温高压条件下,在水溶液介质中制备纳米材料的一种软化学合成方法。与前面几种方法相比,水热合成制备的Bi2O3具有纯度高、分散性好、结晶度高、且易实现对Bi2O3晶体形貌的控制,可生长出具有特定形貌的Bi2O3晶体。如Xiong等以油酸和EDTA为形貌控制剂,采用水热法制备了颗粒尺寸为 500 nm 的具有手掌形貌的α-Bi2O3晶体 (Y. Xiong , M. Z. Wu , J. Ye , Q.W. Chen. Synthesis and luminescence properties of hand-like α-Bi2O3 microcrystals [J], Materials Letters, 2008, (62)1165–1168);杨保群等(杨保群,李永祥,殷庆瑞. Bi2O3晶须的水热合成研究[J]. 无机材料学报,2002,(1795) 979-984)用水热法制备了Bi2O3晶须,他们采用Bi(NO3)3·5H2O和Bi(OH)3为原料,以分析纯的KOH为矿化剂,在120~220℃水热条件下反应10小时,制得具有单斜结构的α-Bi2O3晶须。但是水热合成方法制备的Bi2O3的产量小,效率低,且需要能耐高温、高压的水热反应釜装置。化学气相沉积法,是将Bi2O3的前驱体,如金属铋、铋的金属有机化合物等在高温下进行气化成蒸汽,在高温下蒸汽与氧反应生成Bi2O3。如 Kim等以三甲基铋和氧为原料,采取复杂的金属有机化学气相沉积法制备了长度为40~400 nm的β-Bi2O3纳米带(H. W. Kim. Synthesis and characterization of crystalline β-Bi2O3 nanobelts [J], Thin Solid Films, 2008,(516)3665–3668);Shen等采用常压化学气相沉积法(atmospheric pressure chemical vapor deposition, APCVD), 以复杂的Bi(S2CNEt2)3前驱体为原料制备了直径为50~100 nm,长度达到微米级的β-Bi2O3纳米线(X. P. Shen, S. K.Wu, H. Zhao, Q. Liu. Synthesis of single-crystalline Bi2O3 nanowires by atmospheric pressure chemical vapor deposition approach [J],Physica E, 2007, (39) 133–136)。化学气相沉积法通常首先要合成复杂的金属有机化合物,工艺复杂,对设备要求极高,操作条件非常苛刻,因而面临生产成本高,产量小,能耗大等问题。等离子体法是在真空容器中充入定压气体,利用高温热源或直流电弧产生等离子体将微米级Bi2O3粉加热、熔化、蒸发,与等离子体发生物理、化学反应,使Bi2O3蒸汽经循环泵输送到集粉器中冷凝、沉积,即可获得纳米级Bi2O3粉体。用该法生产纳米级Bi2O3粉体,具有生产效率和纯度高,方法比较简单等优点,但缺点是设备投资高,成本高。如高跃生等采用100 kW高频等离子体装置,频率为2~3MHz,以高频等离子体为热源,以普通微米级氧化铋粉体为原料制备高纯氧化铋纳米粉末(高跃生,黎明,张瑜,王翔,许发玲,郭军高频等离子体法制备纳米氧化铋, 兵器材料科学与工程,2011,(34),90-92);Wang 等以金属铋粉为原料,采用等离子体热处理方法制备了长度在30 nm至600nm的Bi2O3纳米棒(L. Wang, Z. L. Cui, Z. K.Zhang. Bi nanoparticles and Bi2O3 nanorods formed by thermal plasma and heat treatment [J], Surface & Coatings Technology, 2007, (201) 5330–5332)。最近CN102140688B公开了一种多晶Bi2O3粉体生产方法。该方法将Bi2O3,SiO2混合均匀形成配合料,在高温下将配合料加入刚玉坩埚中熔制,然后,将熔制均匀的氧化铋高温玻璃熔体倒入耐热钢模具中,退火后自然冷却至室温得到氧化铋玻璃熔体;将制备的均匀氧化铋玻璃熔体放入马弗炉中,以5℃/分钟速率升温至550~600℃,保温3~8小时,随炉冷却至室温后,将试样破碎成粒度小于50目的颗粒,然后将破碎的颗粒试样放入浓度为15~20%的氢氟酸溶液,浸泡1~3小时,除去试样中非晶相SiO2,过滤既得到多晶Bi2O3。该法具有一定的工业化运用前景,但该法不能制备有特殊形貌的,颗粒尺寸达到微米级别的Bi2O3单晶。
综上所述,在现有Bi2O3的制备方法中,化学沉淀法、溶胶-凝胶法、固相室温法通常只适合制备无固定形貌的Bi2O3纳米粉体材料,无法生产尺寸达到微米级别的一维、二维或三维的Bi2O3纳米线,带或棒。水热法和化学化学气相沉积法在生产纳米Bi2O3粉体材料的同时,也可以用来生产尺寸达到微米级别的一维、二维或三维的Bi2O3。但是水热合成方法制备的-Bi2O3的产量小,效率低,且需要特别的水热反应釜。化学气相沉积法则通常首先要合成复杂的金属有机化合物,工艺复杂,对设备要求极高,操作条件非常苛刻,因而面临生产成本高,产量小,能耗大等问题。
发明内容
本发明的目的是在于克服上述现有技术的缺点,提供了一种制备高质量,晶体尺寸达到几个或几十个微米的α-Bi2O3单晶微米棒的制备方法。按照本发明制备方法制得的α-Bi2O3单晶微米棒结晶度高,纯度高,晶粒形貌、大小均匀。本发明制备工艺简单,且原料要求低,有利于工业化生产,具有良好的工业化运用前景。
为达到上述目的,本发明采用的技术方案是:
第一步:BiOBr前驱体的制备
首先,将 0.01摩尔 Bi(NO3)3·5H2O溶解到7毫升的冰醋酸中,制成Bi(NO3)3的醋酸溶液。然后将0.01摩尔NaBr溶解到10 毫升去离子水中得到NaBr水溶液。在搅拌的同时,把Bi(NO3)3的醋酸溶液快速倒入到NaBr水溶液中,并用磁力搅拌器5~13小时左右,然后过滤,用去离子水洗涤3~6次,在100℃下烘干12 小时。得到BiOBr前驱体。
第二步:α-Bi2O3单晶微米棒的制备
将第一步制备的BiOBr放入马弗炉中以10℃/分钟的升温速率自室温升温至750~900℃,并保温2~4小时后,随炉温冷却至室温,即得到α-Bi2O3单晶微米棒。
本发明的Bi(NO3)3的醋酸溶液中NaBr的浓度为1~2mol/L,NaBr水溶液中NaBr浓度为1~2mol/L。
本发明的Br-离子还可以通过溴化氢、溴化钾引入,Bi3+ 离子还可以通过氯化铋引入。
本发明的BiOBr放入马弗炉中的升温速率为3~15℃/分钟,煅烧温度为750~900℃,保温时间为2~4小时。
本发明利用BiOBr的热稳定性差的特点,通过控制焙少温度和时间,让BiOBr在逐步释放溴元素的同时,使晶格发生改变,生长α-Bi2O3单晶微米棒。
本发明在BiOBr发生相转变生成α-Bi2O3单晶微米棒时未加入任何成核剂,所制备的α-Bi2O3具有独特的形貌, 为长度为10~50 μm,宽度为5~1 0μm的α-Bi2O3单晶微米棒。且微米棒大小均匀,结晶度高,杂相及少,且原料要求低,价格低廉,来源丰富,制备工艺简单,有利于工业化生产。生产的α-Bi2O3具有独特的形貌,可在导电性和气敏性材料得到广泛运用。因而具有可观的经济和社会效益,应用前景十分广阔。
附图说明
图1本是按照本发明制备方法制得的α-Bi2O3单晶微米棒的扫描电镜照片。表明本发明方法制得的α-Bi2O3为长度为10~50 μm,宽度为5~10 μm的α-Bi2O3单晶微米棒。
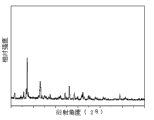
图2本是按照本发明制备方法制得的α-Bi2O3单晶微米棒的X射线衍射图。说明按照本发明方法制得的Bi2O3的晶型为α型,且具有很好的结晶性能。
具体实施方式
实施例1
第一步:BiOBr前驱体的制备
首先,将 0.01摩尔 Bi(NO3)3·5H2O溶解到7毫升的冰醋酸中,制成Bi(NO3)3的醋酸溶液。然后将0.01摩尔NaBr溶解到10 毫升去离子水中得到NaBr水溶液。在搅拌的同时,把Bi(NO3)3的醋酸溶液快速倒入到NaBr水溶液中,并用磁力搅拌器6小时左右,然后过滤,用去离子水洗涤4次,在100℃下烘干12 小时。得到BiOBr前驱体。
第二步:α-Bi2O3单晶微米棒的制备
将第一步制备的BiOBr放入马弗炉中以10℃/分钟的升温速率自室温升温至800℃,并保温2.5小时后,随炉温冷却至室温,即得到α-Bi2O3单晶微米棒。
实施例2
第一步:BiOBr前驱体的制备
首先,将 0.01摩尔 Bi(NO3)3·5H2O溶解到7毫升的冰醋酸中,制成Bi(NO3)3的醋酸溶液。然后将0.01摩尔NaBr溶解到10 毫升去离子水中得到NaBr水溶液。在搅拌的同时,把Bi(NO3)3的醋酸溶液快速倒入到NaBr水溶液中,并用磁力搅拌器6小时左右,然后过滤,用去离子水洗涤4次,在100℃下烘干12 小时。得到BiOBr前驱体。
第二步:α-Bi2O3单晶微米棒的制备
将第一步制备的BiOBr放入马弗炉中以10℃/分钟的升温速率自室温升温至850℃,并保温2.5小时后,随炉温冷却至室温,即得到α-Bi2O3单晶微米棒。
实施例3
第一步:BiOBr前驱体的制备
首先,将 0.01摩尔 Bi(NO3)3·5H2O溶解到7毫升的冰醋酸中,制成Bi(NO3)3的醋酸溶液。然后将0.01摩尔NaBr溶解到10 毫升去离子水中得到NaBr水溶液。在搅拌的同时,把Bi(NO3)3的醋酸溶液快速倒入到NaBr水溶液中,并用磁力搅拌器6小时左右,然后过滤,用去离子水洗涤4次,在100℃下烘干12 小时。得到BiOBr前驱体。
第二步:α-Bi2O3单晶微米棒的制备
将第一步制备的BiOBr放入马弗炉中以10℃/分钟的升温速率自室温升温至800℃,并保温3小时后,随炉温冷却至室温,即得到α-Bi2O3单晶微米棒。
实施例4
第一步:BiOBr前驱体的制备
首先,将 0.02摩尔 Bi(NO3)3·5H2O溶解到7毫升的冰醋酸中,制成Bi(NO3)3的醋酸溶液。然后将0.02摩尔NaBr溶解到10 毫升去离子水中得到NaBr水溶液。在搅拌的同时,把Bi(NO3)3的醋酸溶液快速倒入到NaBr水溶液中,并用磁力搅拌器6小时左右,然后过滤,用去离子水洗涤4次,在100℃下烘干12 小时。得到BiOBr前驱体。
第二步:α-Bi2O3单晶微米棒的制备
将第一步制备的BiOBr放入马弗炉中以10℃/分钟的升温速率自室温升温至800℃,并保温4小时后,随炉温冷却至室温,即得到α-Bi2O3单晶微米棒。
Claims (2)
1.一种α-Bi2O3单晶微米棒的制备方法,其特征在于:
第一步:BiOBr前驱体的制备
首先,将 0.01摩尔 Bi(NO3)3·5H2O溶解到7毫升冰醋酸中,制成Bi(NO3)3的醋酸溶液,然后将0.01摩尔NaBr溶解到10毫升去离子水中得到NaBr水溶液,在搅拌的同时,把Bi(NO3)3的醋酸溶液快速倒入到NaBr水溶液中,并用磁力搅拌器搅拌5~13小时,然后过滤,用去离子水洗涤3~6次,在100℃下烘干12 小时,得到α-Bi2O3的前驱体BiOBr;
第二步:α-Bi2O3单晶微米棒的制备
将第一步制备的BiOBr放入马弗炉中以10℃/分钟的升温速率自室温升温至750~900℃,并保温2~4小时后,随炉温冷却至室温,即得到α-Bi2O3单晶微米棒。
2.根据权利要求1所述的α-Bi2O3单晶微米棒的制备方法,其特征在于:Bi(NO3)3的醋酸溶液中NaBr的浓度为1~2mol/L,NaBr水溶液中NaBr浓度为1~2mol/L;Br-离子还可以通过溴化氢、溴化钾引入,Bi3+ 离子还可以通过氯化铋引入;BiOBr放入马弗炉中的升温速率为3~15℃/分钟,焙烧温度为750~900℃,保温时间为2~4小时;生成的α-Bi2O3单晶微米棒的直径为5~10 μm、长度为10~50μm。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2012103270056A CN102787355A (zh) | 2012-09-07 | 2012-09-07 | 一种α-Bi2O3单晶微米棒的制备方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2012103270056A CN102787355A (zh) | 2012-09-07 | 2012-09-07 | 一种α-Bi2O3单晶微米棒的制备方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102787355A true CN102787355A (zh) | 2012-11-21 |
Family
ID=47152935
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2012103270056A Pending CN102787355A (zh) | 2012-09-07 | 2012-09-07 | 一种α-Bi2O3单晶微米棒的制备方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN102787355A (zh) |
Cited By (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103193267A (zh) * | 2013-04-27 | 2013-07-10 | 哈尔滨理工大学 | 一种高纯度氧氯化铋的制备方法 |
| CN103708424A (zh) * | 2013-12-18 | 2014-04-09 | 江苏大学 | {001}晶面暴露的BiOBr方形纳米片的制备方法 |
| CN103721701A (zh) * | 2014-01-21 | 2014-04-16 | 南京信息工程大学 | 一种新型巢状氧化铋光催化剂及其制备方法 |
| CN104667951A (zh) * | 2015-02-11 | 2015-06-03 | 太原理工大学 | 一种溴氧铋高光催化剂的制备及应用方法 |
| CN106378125A (zh) * | 2016-10-08 | 2017-02-08 | 合肥工业大学 | 一种具有微纳结构的棒状Bi2O3光催化材料及其制备方法 |
| CN106379938A (zh) * | 2016-09-10 | 2017-02-08 | 河南师范大学 | 一种制备黑色α‑Bi2O3粉末材料的方法 |
| CN107552038A (zh) * | 2017-09-05 | 2018-01-09 | 云南大学 | 一种纳米线状氧化铋的制法和用途 |
| CN109702186A (zh) * | 2019-01-28 | 2019-05-03 | 合肥学院 | 一种金属铋纳米壳材料及其制备方法 |
| CN114789058A (zh) * | 2022-04-27 | 2022-07-26 | 东南大学 | 一种非均相微波响应芬顿催化剂及其制法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101850263A (zh) * | 2010-06-17 | 2010-10-06 | 江西理工大学 | 一种Ag掺杂的BiOBr催化材料及其制备方法与应用 |
| WO2012066545A2 (en) * | 2010-11-16 | 2012-05-24 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Bismuth oxyhalide compounds useful as photocatalysts |
-
2012
- 2012-09-07 CN CN2012103270056A patent/CN102787355A/zh active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN101850263A (zh) * | 2010-06-17 | 2010-10-06 | 江西理工大学 | 一种Ag掺杂的BiOBr催化材料及其制备方法与应用 |
| WO2012066545A2 (en) * | 2010-11-16 | 2012-05-24 | Yissum Research Development Company Of The Hebrew University Of Jerusalem Ltd. | Bismuth oxyhalide compounds useful as photocatalysts |
Non-Patent Citations (2)
| Title |
|---|
| YU CHANGLIN 等: "Thermal stability, microstructure and photocatalytic activity of the bismuth oxybromide photocatalyst", 《CHINESE JOURNAL OF CHEMISTRY》 * |
| 王云燕 等: "硝酸铋转化水解法制备片状BiOCl粉末的研究", 《湖南冶金》 * |
Cited By (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103193267A (zh) * | 2013-04-27 | 2013-07-10 | 哈尔滨理工大学 | 一种高纯度氧氯化铋的制备方法 |
| CN103708424A (zh) * | 2013-12-18 | 2014-04-09 | 江苏大学 | {001}晶面暴露的BiOBr方形纳米片的制备方法 |
| CN103708424B (zh) * | 2013-12-18 | 2015-10-28 | 江苏大学 | {001}晶面暴露的BiOBr方形纳米片的制备方法 |
| CN103721701A (zh) * | 2014-01-21 | 2014-04-16 | 南京信息工程大学 | 一种新型巢状氧化铋光催化剂及其制备方法 |
| CN103721701B (zh) * | 2014-01-21 | 2015-12-02 | 南京信息工程大学 | 一种新型巢状氧化铋光催化剂及其制备方法 |
| CN104667951A (zh) * | 2015-02-11 | 2015-06-03 | 太原理工大学 | 一种溴氧铋高光催化剂的制备及应用方法 |
| CN106379938A (zh) * | 2016-09-10 | 2017-02-08 | 河南师范大学 | 一种制备黑色α‑Bi2O3粉末材料的方法 |
| CN106379938B (zh) * | 2016-09-10 | 2017-11-21 | 河南师范大学 | 一种制备黑色α‑Bi2O3粉末材料的方法 |
| CN106378125A (zh) * | 2016-10-08 | 2017-02-08 | 合肥工业大学 | 一种具有微纳结构的棒状Bi2O3光催化材料及其制备方法 |
| CN107552038A (zh) * | 2017-09-05 | 2018-01-09 | 云南大学 | 一种纳米线状氧化铋的制法和用途 |
| CN109702186A (zh) * | 2019-01-28 | 2019-05-03 | 合肥学院 | 一种金属铋纳米壳材料及其制备方法 |
| CN114789058A (zh) * | 2022-04-27 | 2022-07-26 | 东南大学 | 一种非均相微波响应芬顿催化剂及其制法 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102787355A (zh) | 一种α-Bi2O3单晶微米棒的制备方法 | |
| CN110668452B (zh) | 一种由粉煤灰制备SiO2-Al2O3复合气凝胶材料的方法 | |
| CN101234750B (zh) | 一种超细微粒和纳米颗粒的制备方法 | |
| CN101319381B (zh) | 低温条件制备高定向生长的纳米片状Bi2Fe4O9 | |
| CN106542586B (zh) | 一种钨酸钴纳米棒的制备方法 | |
| CN102336431B (zh) | 一种SnO2花状结构纳米材料及其水热制备方法 | |
| CN105645959B (zh) | Y2o3基透明陶瓷粉体的喷射共沉淀制备方法 | |
| CN104894636B (zh) | 八钛酸钾晶须的制备方法 | |
| CN101857430B (zh) | 一种钛酸盐系列电子陶瓷纳米晶体材料的合成方法 | |
| CN103570068A (zh) | 一种铌铁矿结构ZnNb2O6纤维及其制备方法 | |
| CN110629288A (zh) | 一种水热技术制备晶须状铝酸钆粉体材料的方法 | |
| CN110451953A (zh) | 一种取向性钛酸钡锶纳米多晶的可控制备方法 | |
| CN103265291A (zh) | 一种纳米六硼化钙粉末的制备方法 | |
| CN105883910A (zh) | 一种钙钛矿SrTiO3多孔纳米颗粒的制备方法及产物 | |
| CN108609652B (zh) | 一种利用熔盐制备二氧化锆纳米粉体的方法 | |
| CN101177268A (zh) | 一种低温制备立方碳化硅纳米线的方法 | |
| CN100577571C (zh) | 一种氧化铝纳米粉体的制备方法 | |
| CN109437296B (zh) | 一种熔盐法制备四方相氧化锆纳米棒的方法 | |
| CN105129834A (zh) | 一种纳米级稀土氧化物粉体的制备方法 | |
| CN102716701A (zh) | 一种超声喷雾制备镍掺杂硅酸铋微米球的方法 | |
| CN103274460A (zh) | 一种选择性解胶制备金红石相二氧化钛亚微米球的方法 | |
| CN113277558B (zh) | 一种α′-AgVO3纳米材料的制备方法 | |
| CN114162869A (zh) | 一种具有微纳米棒状结构Li2Zn2Mo3O12材料及制备方法 | |
| CN102140688A (zh) | 一种Bi2O3多晶的制备方法 | |
| CN103603050B (zh) | 一种液相制备ZnO纳米晶须的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20121121 |