CN102753707A - 用随机引物和特异性引物的混合物等温扩增核酸 - Google Patents
用随机引物和特异性引物的混合物等温扩增核酸 Download PDFInfo
- Publication number
- CN102753707A CN102753707A CN2011800087156A CN201180008715A CN102753707A CN 102753707 A CN102753707 A CN 102753707A CN 2011800087156 A CN2011800087156 A CN 2011800087156A CN 201180008715 A CN201180008715 A CN 201180008715A CN 102753707 A CN102753707 A CN 102753707A
- Authority
- CN
- China
- Prior art keywords
- nucleic acid
- amplification
- primer
- dna
- sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/26—Preparation of nitrogen-containing carbohydrates
- C12P19/28—N-glycosides
- C12P19/30—Nucleotides
- C12P19/34—Polynucleotides, e.g. nucleic acids, oligoribonucleotides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/6853—Nucleic acid amplification reactions using modified primers or templates
Abstract
本发明提供用于在等温条件下扩增核酸以形成扩增的核酸序列的方法和试剂盒。所述方法和试剂盒包括提供核酸模板、DNA聚合酶、脱氧核糖核苷三磷酸、包含随机序列的引物和特异性引物,以及扩增所述核酸模板。
Description
相关申请的交叉引用
本申请要求保护于2010年2月9日提交的美国专利申请号12/702,884的优先权,其公开内容通过引用以其整体并入本文。
关于联邦政府资助研究与开发的声明
本发明在政府资助下进行,合同号为由国防威胁降低局授予的HDTRA1-07-C-0097。政府拥有本发明某些权利。
发明领域
本发明通常涉及用于等温链置换核酸扩增的方法和试剂盒。所述方法具体涉及用随机引物和特异性引物的混合物等温扩增核酸。
发明背景
目前许多技术用于扩增核酸,甚至从几个分子的起始核酸模板开始扩增。这些技术包括聚合酶链式反应(PCR)、连接酶链式反应(LCP)、自动维续序列扩增(3SR)、基于核酸序列的扩增(NASBA)、链置换扩增(SDA)、多重置换扩增(MDA)或滚环扩增(RCA)。
核酸扩增技术经常用于基于核酸的测定,其用于分析物检测、传感、法医和诊断应用、基因组测序、全基因组扩增等。所述应用常常要求扩增技术具有高特异性、灵敏度、准确性和稳健性。当可用的起始模板核酸为极小量时,核酸扩增尤其重要。然而,大多数目前可利用的核酸扩增技术受到通过产生不需要的/假的扩增产物的非特异性扩增反应而产生的高本底信号的影响。
用等温扩增条件可以以更高的准确性和容易性实现自生物样品的核酸扩增和分析。等温扩增方法相对于热循环方法(例如PCR)的主要优势是通过避开对热循环仪的需要而用最少仪器实施反应的能力。用于等温扩增的仪器可以利用受控的加热块或水浴,使得所述技术更易获得、更方便和更经济。此外,许多等温扩增技术,例如滚环扩增、全基因组扩增或环介导的等温扩增(LAMP),可以不需要事先纯化靶标核酸,直接用含有靶标核酸的粗生物材料来实施。然而,在某些特定应用中,例如全基因组扩增中,当采用现有扩增方法时,一些特定的目的基因座可在扩增过程中丢失。因此,需要开发设计为保存模板核酸中存在的所有必需序列的更好的等温扩增方法。
简述
本发明的一个或多个实施方案提供了用于有效扩增核酸的方法和试剂盒。在一些实施方案中,提供了在等温条件下利用特异性引物和包含随机序列的引物的核酸扩增方法。
在一个实施方案中,提供了用于核酸扩增的方法。所述方法包括提供核酸模板、DNA聚合酶、脱氧核糖核苷三磷酸、包含随机序列的引物和特异性引物。所述方法包括在等温条件下扩增核酸模板以形成扩增的核酸序列。
在用于核酸扩增的方法的另一实施方案中,所述方法包括提供核酸模板、DNA聚合酶、脱氧核糖核苷三磷酸、包含随机序列的引物和特异性引物。所述方法包括在等温条件下扩增核酸模板以形成与表面连接的扩增的核酸序列。
在另一实施方案中,提供了用于核酸扩增的试剂盒。所述试剂盒包括Phi29
DNA聚合酶、至少一种包含随机序列的引物和至少一种特异性引物。
附图
当参考附图阅读以下详述时,本发明这些和其它特征、方面和优势将变得更好理解,附图中相似符号在全部附图中代表相似部分,其中:
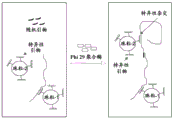
图1是滚环扩增反应、通过珠粒结合的特异性引物对扩增的脱氧核糖核酸(DNA)的捕获和捕获的DNA的进一步扩增的示意图。
图2是在珠粒上的等温滚环DNA扩增反应示意图,其显示了用随机引物让DNA从一个珠粒转移到另一个珠粒。
图3是显示珠粒结合的DNA与表面结合的引物杂交和表面结合的引物的进一步延伸以在表面捕获DNA拷贝的图。
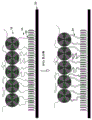
图4A是用扩增的DNA和捕获的DNA包被的单个珠粒的图像。图4B显示没有任何扩增DNA包被的单个珠粒。
图5是阐明与阴性和阳性对照(泳道3和4)相比的通过珠粒结合的特异性引物捕获的扩增pUC 18 DNA的EcoRI限制性酶消化产物(泳道2)的琼脂糖凝胶图像。
图6是阐明在不同条件下通过珠粒结合的特异性引物捕获的扩增DNA的EcoRI限制性酶消化产物的琼脂糖凝胶图像。
图7是在珠粒上捕获的扩增的DNA (SEQ ID NO:
2)的测序数据图。
详述
包括单分子DNA扩增或全基因组扩增的基于核酸的测定,需要就序列覆盖率而言具有高收率、高保真度和小偏倚的高效核酸扩增方法。采用包含随机序列的引物的诸如滚环扩增(RCA)或多重置换扩增(MDA)等等温核酸扩增反应,对于所述应用比温度依赖性核酸扩增反应(如PCR)更合适。
本发明一个或多个实施方案涉及用于有效等温扩增核酸的方法和试剂盒。在一些实施方案中,所述方法包括采用两种类型的引物的核酸模板体外扩增,所述两种类型的引物为包含随机序列的一种引物和特异性引物。在一些实施方案中,所述方法包括采用包含随机序列的引物和特异性引物体外扩增核酸模板,所述随机序列包含核苷酸类似物。所述方法部分地提高核酸扩增反应的效率。所述方法进一步包括用与基质或捕获剂(或者术语“捕获剂”在本文中用作“捕捉剂”)连接的特异性引物捕获扩增的核酸序列。
为了更清晰和简明地描述和指出所要求保护的发明的主题,为用于以下说明和附加权利要求中的特定术语提供以下定义。在整个说明书中,特定术语的例证应该被视为非限制性实例。
除非上下文中另外明确指出,否则单数形式“一个”、“一种”和“该”包括复数所指物。如本文整个说明书和权利要求中所用,近似措词可以用于修饰在不引起改变与其相关的基本功能的情况下可允许改变的任何定量性表述。因此,由术语例如“约”修饰的值不限于规定的精确值。在一些情况中,近似表措词可相当于检测值的仪器的准确值。相似地,“不含(free)”可以与术语联合使用,可包括少量或痕量,而仍认为不含所修饰术语。在必要时提供了范围,那些范围包含了它们之间的所有子范围。
本文所用术语“核苷”指葡基胺化合物,其中核酸碱基(核碱基)与糖部分连接。核酸碱基可以是天然核碱基或修饰的/合成的核碱基。核酸碱基可以包括但不限于嘌呤碱基(例如腺嘌呤或鸟嘌呤)、嘧啶(例如胞嘧啶、尿嘧啶或胸腺嘧啶)或脱氮杂嘌呤碱基。核酸碱基可以连接至戊糖(例如核糖或脱氧核糖)糖部分的1’位置或等同位置。所述糖部分可以包括但不限于天然糖、糖取代物(例如碳环部分或无环部分)、取代糖或修饰糖(例如在锁定核酸(LNA)核苷酸中的双环呋喃糖单元)。核苷可以含有2’-羟基、2’-脱氧或2’,3’-双脱氧形式的糖部分。
本文所用术语“核苷酸”或“核苷酸碱基”指核苷磷酸。所述术语包括但不限于天然核苷酸、合成核苷酸、修饰核苷酸或代替物取代部分(例如肌苷)。核苷磷酸可以是核苷单磷酸、核苷双磷酸或核苷三磷酸。核苷磷酸中的糖部分可以是戊糖,如核糖,并且磷酸酯化位点可对应于与核苷戊糖C-5位置连接的羟基。核苷酸可以是但不限于脱氧核糖核苷三磷酸(dNTP)或核糖核苷三磷酸(NTP)。可以用英文字母(字母命名)表示核苷酸,如表1所示。例如,A表示腺苷(即含有腺嘌呤核碱基的核苷酸),C表示胞嘧啶,G表示鸟苷,T表示胸苷。W表示A或T/U,而S表示G或C。N代表随机核苷酸(即N可以是A、C、G或T/U中的任一个)。字母命名前的加号(+)标记表示该字母命名的核苷酸是LNA核苷酸。例如,+A代表腺苷LNA核苷酸,+N代表随机的锁定核苷酸(随机LNA核苷酸)。字母命名前的星号(*)标记表示由该字母命名的核苷酸是硫代磷酸酯修饰的核苷酸。例如,*N代表硫代磷酸酯修饰的随机核苷酸。
表1:不同核苷酸的字母命名
| 字母符号 | 由字母符号代表的核苷酸 |
| G | G |
| A | A |
| T | T |
| C | C |
| U | U |
| R | G或A |
| Y | T/U或C |
| M | A或C |
| K | G或T/U |
| S | G或C |
| W | A或T/U |
| H | A或C或T/U |
| B | G或T/U或C |
| V | G或C或A |
| D | G或A或T/U |
| N | G或A或T/U或C |
本文所用术语“核苷酸类似物”指与天然核苷酸结构上相似(类似物)的化合物。核苷酸类似物可以具有改变的磷酸酯骨架、糖部分、核碱基或其组合。通常具有改变的核碱基的核苷酸类似物尤其赋予不同的碱基配对和碱基堆积特性。具有改变的磷酸酯-糖骨架的核苷酸类似物(例如肽核酸(PNA)、锁定核酸(LNA))通常尤其改变链特性,例如二级结构形成。
本文所用术语“LNA (锁定核酸)核苷酸”指核苷酸类似物,其中核苷酸的糖部分包含锁定于模拟核糖核酸(RNA)的糖构象中的双环呋喃糖单元。从化学角度看,自脱氧核糖核苷酸(或核糖核苷酸)到LNA核苷酸的结构改变受到限制,即在2’位和4’位碳原子之间引入另外的键(例如2’-C,4’-C-氧亚甲基键)。LNA核苷酸中呋喃糖单元的2’和4’位可以由O-亚甲基(例如氧-LNA:2’-O,4’-C-亚甲基-β-D-呋喃核糖核苷酸)、S-亚甲基部分(硫代-LNA)或NH-亚甲基(氨基-LNA)等等连接。所述键限制了呋喃糖环的构象自由。LNA寡核苷酸表现出对互补单链RNA和互补的单链或双链DNA增强的杂交亲和力。LNA寡核苷酸可诱导A型(RNA样)双链体构象。
本文所用术语“寡核苷酸”指核苷酸或其衍生物的寡聚体。本文所用术语“核酸”指核苷酸或其衍生物的聚合物。本文所用术语“序列”指寡核苷酸或核酸的核苷酸序列。在整个说明书中,无论何时寡核苷酸/核酸由字母序列表示时,核苷酸从左到右是5'→3'次序。例如,由字母序列(W)x(N)y(S)z代表的寡核苷酸(其中x=2、y=3和z=1),代表寡核苷酸序列WWNNNS,其中W是5'末端核苷酸,S是3’末端核苷酸。寡核苷酸/核酸可以是DNA、RNA或其类似物(例如硫代磷酸酯类似物)。寡核苷酸或核酸也可以包括修饰的碱基和/或骨架(例如修饰的磷酸酯键或修饰的糖部分)。赋予核酸稳定性和/或其它优势的合成骨架的非限制性实例可以包括硫代磷酸酯键、肽核酸、锁定核酸、木糖核酸或其类似物。
本文所用术语“引物”或“引物序列”指与靶标核酸序列(例如待扩增的DNA模板)杂交以引发核酸合成反应的短的线性寡核苷酸。引物可以是RNA寡核苷酸、DNA寡核苷酸或嵌合序列。引物可以含有天然的、合成的或修饰的核苷酸。引物长度的上限和下限均凭经验确定。引物长度的下限是在核酸扩增反应条件下与靶标核酸杂交时形成稳定双链体所需的最小长度。非常短的引物(通常少于3-4个核苷酸长度)在所述杂交条件下不能与靶标核酸形成热力学稳定的双链体。上限通常决定于在靶标核酸的非预定核酸序列的区域中形成双链体的概率。适合的引物长度范围通常为约4-约40个核苷酸长度。
本文所用术语“包含随机序列的引物”指引物序列的混合物,所述序列通过以使得给定位置可由任何可能的核苷酸或其类似物组成的方式(完全随机化)随机化寡核苷酸序列任何给定位置的核苷酸来产生。在一个实例中,引物可为“随机引物”或“完全随机引物”或“嵌合随机引物”。因此,随机引物是由序列中每一种可能的核苷酸组合组成的寡核苷酸序列的随机混合物。例如,六聚体随机引物可以由序列NNNNNN或(N)6表示。六聚体随机DNA引物由4种DNA核苷酸A、C、G和T的每一种可能的六聚体组合组成,这导致产生包含46 (4,096)种独特六聚体DNA寡核苷酸序列的随机混合物。当靶标核酸序列未知时,可将随机引物有效地用于引发核酸合成反应。
本文所用术语“部分受限的引物”指引物序列的混合物,所述序列通过使寡核苷酸序列的一些核苷酸完全随机化(即所述核苷酸可以是A、T/U、C、G或其类似物中的任一种),同时限制一些其它核苷酸的完全随机化(即在某些位置的核苷酸随机化程度低于可能的A、T/U、C、G或其类似物的组合)来产生。例如,由WNNNNN代表的部分受限的DNA六聚体引物,代表了其中混合物中所有序列的5’末端核苷酸是A或T的引物序列混合物。与完全随机DNA引物(NNNNNN)的最多4种可能的组合(A、T、G或C)相比,此处的5’末端核苷酸限制于两种可能的组合(A或T)。部分受限引物的合适引物长度可在约4个核苷酸-约40个核苷酸的范围内。完全随机引物可含有完全随机的序列,例如,十二聚体完全随机引物可以由序列NNNNNNNNNNNN或(N)12来代表。嵌合随机引物可含有与特异性序列组合的随机序列。例如,十二聚体嵌合随机引物可以由序列WWWWNNNNNNNN代表。与完全随机DNA引物在3’末端的最多4种可能组合(A、T、G或C)相比,5’末端的4个核苷酸限制于两种可能组合(A或T)。
本文所用术语“质粒”指与染色体核酸分离的染色体外核酸。质粒DNA在细胞内可能能够独立于染色体核酸(染色体DNA)复制。质粒DNA常为环状双链的。
本文所用术语“扩增”或“核酸扩增”指产生核酸模板的多个拷贝,或产生与核酸模板互补的多个核酸序列拷贝。
本文所用术语“靶标核酸”指需要在核酸扩增反应中扩增的核酸。例如,靶标核酸包含核酸模板。
本文所用术语“DNA聚合酶”指利用核酸链作为模板从头合成DNA链的酶。DNA聚合酶利用已有的DNA或RNA作为模板合成DNA,并且催化脱氧核糖核苷酸沿其读取的模板链聚合。新合成的DNA链与模板链互补。DNA聚合酶仅可向新形成链的3’-羟基末端添加游离核苷酸。它通过从脱氧核糖核苷三磷酸(dNTP)转移核苷单磷酸至成长的寡核苷酸链的3’-羟基来合成寡核苷酸。这导致新链以5’→3’方向延伸。因为DNA聚合酶仅可在预先已有的3’-OH基团添加核苷酸以开始DNA合成反应,所以DNA聚合酶需要其可添加第一个核苷酸的引物。适合的引物包括RNA或DNA的寡核苷酸。DNA聚合酶可以是天然存在的DNA聚合酶或具有上述活性的天然酶的变体。例如,它可以包括具有链置换活性的DNA聚合酶、缺乏5’→3’外切核酸酶活性的DNA聚合酶、具有逆转录酶活性的DNA聚合酶或具有外切核酸酶活性的DNA聚合酶。
本文所用的“链置换核酸聚合酶”指除其核酸合成活性之外还有链置换活性的核酸聚合酶。就是说,链置换核酸聚合酶可在核酸模板链序列的基础上继续合成核酸(即读取模板链),同时置换已与模板链退火的互补链。
本文所用术语“互补的”当用于相对于第二条核酸/寡核苷酸序列描述第一条核酸/寡核苷酸序列时,指包含第一条核酸/寡核苷酸序列的多核苷酸或寡核苷酸在一定杂交条件下与包含第二条核酸/寡核苷酸序列的寡核苷酸或多核苷酸杂交(例如形成双链体结构)的能力。杂交通过核苷酸(互补核苷酸)的碱基配对来进行。核苷酸的碱基配对可经由沃森-克里克碱基配对、非沃森-克里克碱基配对或通过非天然的/修饰的核苷酸形成的碱基配对来进行。
本文所用术语“高严格杂交条件”,指对于寡核苷酸杂交事件赋予比可用于核酸扩增反应的条件所提供的严格性更高严格性的条件。可需要较高严格性杂交条件以防止可在得到的杂交双链体中含有错配碱基的寡核苷酸杂交事件。例如,在核酸扩增反应中,可以通过增加反应温度或通过降低盐浓度或通过在缓冲液中包括诸如甘油或乙二醇等变性剂来实现高严格杂交条件。核酸扩增反应有时在约75 mM盐浓度下进行。相反,如果核酸扩增反应在15 mM盐浓度下进行成,这可提供高严格杂交条件。可通过增加反应温度到高于30℃的典型反应温度,将高严格杂交条件用于体外等温核酸扩增反应。例如,等温核酸扩增反应可以在约35℃-约45℃进行。
本文所用术语“滚环扩增 (RCA)”,指经由滚环机制扩增环状核酸模板(例如单链DNA环)的核酸扩增反应。滚环扩增反应可由引物与环状(通常为单链)核酸模板杂交引发。然后核酸聚合酶通过在环状核酸模板周围连续前进来延伸与环状核酸模板杂交的引物,以反复复制核酸模板序列(滚环机制)。滚环扩增通常产生包含环状核酸模板序列的串联重复单元的多联体。滚环扩增可为显示线性扩增动力学的线性RCA
(LRCA) (例如用单一特异性引物的RCA),或可为显示指数扩增动力学的指数RCA
(ERCA)。滚环扩增也可以用多引物进行(多重引发的滚环扩增或MPRCA),这导致超分支多联体。例如,在双引发的RCA中,如在LRCA中一样,一种引物可与环状核酸模板互补,然而另一引物可与RCA产物的串联重复单元核酸序列互补。因此,双引发的RCA可以以具有指数(几何)扩增动力学的链式反应进行,其特征为涉及两种引物的多重杂交、引物延伸和链置换事件的分支级联。这通常产生多连环双链核酸扩增产物的离散集合。滚环扩增可以在等温条件下用适合的核酸聚合酶例如Phi29 DNA聚合酶在体外实施。
本文所用术语“多重置换扩增”(MDA)指核酸扩增方法,其中扩增包括使引物与变性核酸退火,接着链置换核酸合成。随着通过链置换取代所述核酸,出现逐渐增加的引发事件数目,形成超分支核酸结构的网络。MDA尤其可用于用于自少量基因组DNA样品产生具有有限序列偏崎的高分子量DNA的全基因组扩增中。可将诸如Phi29 DNA聚合酶或大片段Bst
DNA聚合酶等链置换核酸聚合酶用于多重置换扩增。MDA经常在等温反应条件下进行,随机引物用于所述反应以达到具有有限序列偏崎的扩增。
本文所用术语“反应混合物”指用于实施化学分析或生物学测定的试剂或试剂溶液的组合。
一个或多个实施方案涉及用于使用包含随机序列的引物和特异性引物的等温核酸扩增反应的方法和试剂盒。这些扩增方法比现在使用的扩增技术更可靠,因此更适于以下应用:例如其中靶标核酸可以较少量获得的稀有序列的扩增(例如检测野生型序列群内的稀有突变序列),或全基因组扩增反应。
本发明一个或多个实施方案包含使用包含随机序列的引物和特异性引物用于扩增模板核酸序列的等温扩增反应。一个或多个实施方案也包含在等温扩增反应期间使用特异性引物捕获扩增的核酸序列。包含随机序列的引物和特异性引物二者均存在于同一反应混合物中,以用于同时扩增、捕获和捕获的核酸序列的后续扩增。可让特异性引物与基质连接。所述方法的一个实例可用于产生用核酸包被的基质。
在一个或多个实施方案中,包含随机序列的引物可以包含至少一个经修饰的核酸碱基。当使用时所述引物通常需要高盐或低温条件以与模板核酸序列有效杂交,从而开始扩增反应。在一种或多种方法中使用的引物中存在的修饰核酸碱基,能够提高引物(其具有随机序列)的解链温度(Tm)。
在一些实施方案中,包含随机序列的引物是部分受限的引物。部分受限引物的适合长度可以在约4-约10个核苷酸的范围内。也可使用具有不同引物长度的部分受限的引物的组合。包含随机序列的引物(例如部分受限的引物)可以包含提高引物Tm的修饰核酸碱基。可将通过随机引物和特异性引物的扩增以及通过在相同条件下在相同反应混合物中特异性引物的随后捕获,用于进一步提高扩增效率。
通过让核酸模板与DNA聚合酶和脱氧核糖核苷三磷酸接触,并在适合核酸扩增的条件下孵育反应混合物,来扩增核酸。可在等温条件下进行核酸模板的扩增。在一些实施方案中,通过RCA方法利用等温核酸扩增来扩增核酸模板。
在一个或多个实施方案中,包含随机序列的引物可包含完全随机DNA引物(NNNNNN)。在一个或多个其它实施方案中,引物可以包含部分受限的引物,其中寡核苷酸序列中的一些核苷酸是随机的(WWWNNN)。在一个或多个实施方案中,引物可在5’末端包含特异性序列并且在3’末端包含随机序列。
如所提及,随机引物的合适长度可在4个核苷酸-10个核苷酸长度范围内。在一些实施方案中,随机引物的长度是5-6个核苷酸。在一些包含部分受限引物的实施方案中,引物为约5-约7个核苷酸长度。短随机引物的一个潜在缺点是具有随机序列的短引物具有低的解链温度。通过将修饰的核酸碱基引入到短随机引物中,可提高引物解链温度。适合的修饰核酸碱基包括但不限于可以是锁定核酸碱基、肽核酸碱基或核糖核酸碱基。
在一些实施方案中,包含随机序列的引物可以是部分受限的引物。部分受限的引物在适合位置包含核酸类似物(例如锁定核酸(LNA)核苷酸),所述核酸类似物比天然核苷酸具有更高的互补特异性。核苷酸类似物在部分受限的引物中的位置,可以以使得其在核酸扩增反应条件下与模板核酸序列中存在的互补序列特异性杂交的方式来选择。当将包含LNA核苷酸的部分受限引物用于核酸扩增反应时,所述扩增反应可以在更严格的杂交条件下进行。更严格的条件可以有益于DNA聚合酶。扩增反应可在较高温度(例如等温核酸扩增的高于30℃)下进行,温度上限是用于反应的DNA聚合酶在该温度下可变成无功能的温度。也可以在较正常使用浓度(例如约75 μM盐浓度)低的盐浓度(例如约10 μM-约25 μM 盐浓度)下进行。由于较高的互补特异性,包含LNA核苷酸的部分受限引物与靶标核酸的杂交可基本不受高严格杂交条件的影响。因此,也可基本不影响所需的靶标核酸的扩增。
杂交的严格条件是有意义的,因为短随机引物通常需要高盐或低温条件以有效杂交从而开始DNA扩增。然而,所述条件不适合于单链扩增的产物DNA与特异性引物正确杂交。通常期望特异性引物更长,因此需要高严格杂交条件以为杂交提供正确的特异性。在这种情况下,使用受限的随机引物连同修饰的核苷酸可以是在高严格条件下具有扩增的解决方法。因为受限的随机引物的Tm高,因此即使在高严格条件下具有随机序列的引物也能够与模板DNA杂交以进行扩增反应。
可以通过使寡核苷酸序列的一个或多个核苷酸完全随机化(即核苷酸碱基可以是A、T/U、C、G或其类似物中的任一种),同时限制一些其它核苷酸的完全随机化(即在某些位置核苷酸碱基的随机化程度低于四种可能组合A、T/U、C、G),来产生部分受限的引物。在一些实施方案中,部分受限的引物中两个核苷酸的随机化受到限制。在一些实施方案中,部分受限的引物中不止两个核苷酸(例如3个、4个或5个核苷酸)的随机化受到限制。随机化的程度可基于扩增反应要求和反应条件凭经验确定。
在一些实施方案中,部分受限的引物可在适当位置包含核苷酸类似物。在一些实施方案中,可以使用具有比天然核苷酸高的互补特异性的核苷酸类似物。可掺入部分受限引物的合适的核酸类似物的非限制性实例包括肽核酸(PNA)、2’-氟代N3-P5’-氨基磷酸酯、1’,5’-脱水己糖醇核酸(HNA)、核糖核酸(RNA)或锁定核酸(LNA)核苷酸。由于核苷酸类似物的较高互补特异性,使用包含核苷酸类似物的部分受限引物的核酸扩增反应可以在更严格的条件下实施(例如在更高温度或更低盐浓度下实施反应)。具有核苷酸类似物的部分受限引物对靶标具有更高的互补特异性(例如,当部分受限引物包含核苷酸类似物时靶标核酸-引物复合物的Tm可以更高)。由于所述引物即使在更高温度/更低盐浓度下也与靶标核酸杂交,在严格杂交条件下不会实质上影响所期需靶标核酸的扩增。
在一些实施方案中,部分受限引物在适合的位置包含LNA核苷酸。适合的LNA核苷酸包括但不限于氧-LNA (2’-O,4’-C-亚甲基-β-D-呋喃核糖核苷酸)、硫代-LNA (2’-S,4’-C-亚甲基-β-D-呋喃核糖核苷酸)或氨基-LNA (2’-NH,4’-C-亚甲基-β-D-呋喃核糖核苷酸)核苷酸。LNA核苷酸可以定位于部分受限引物序列的5’末端。在一些实施方案中,部分受限引物包含两个LNA核苷酸。例如,部分受限引物可以在5’末端位置具有LNA核苷酸,亦可在邻近5’末端位置的位置具有LNA核苷酸。在其它实例中,部分受限引物的5’末端核苷酸可以是天然核苷酸,而邻近5’末端核苷酸的接下来的两个核苷酸可以是LNA核苷酸。当LNA核苷酸定位于离引物3'末端多于1或2个碱基的区域时,聚合酶效率好于LNA核苷酸定位于离引物3'末端不多于1或2个碱基(最后或倒数第二个碱基)的情况。
在一个或多个实施方案中,反应混合物中存在的特异性引物也参与反应。用于扩增反应的特异性引物是长引物,例如10-20个核苷酸序列或15-20个核苷酸序列。长特异性引物的解链温度普遍高,在一些实施方案中它们仅可在诸如低盐和高温条件等更严格条件下杂交。往反应混合物中添加引物的顺序无关紧要,因为在特异性引物和包含随机序列的引物同时存在时,扩增反应才开始。在同一反应中具有两种引物的一个优势是同时扩增存在于模板核酸序列中的不同基因座。在一些实施方案中,特异性引物可以对特定基因座具有高特异性,例如,对可存在于模板中的5个基因座中的基因座2具有高特异性。通过包含随机序列的引物和通过特异性引物的同时扩增可导致产生具有全部5个基因座的扩增核酸序列(通过包含随机序列的引物),亦产生仅具有基因座2的扩增核酸序列(通过特异性引物)。在一些实施方案中,包含随机序列的引物可以不能有效支持一些可被特异性引物扩增的基因座的扩增。例如,包含随机序列的引物不能扩增基因座2、3和4,而特异性引物能够扩增这些基因座,这就导致产生包含基因座1和5及高表达的基因座2、3和4的扩增核酸序列群。在所述实施方案中,存在于模板核酸序列中的特定基因座的丢失率降低。一个或多个实施方案亦通过用随机引物和特异性引物二者增加不同基因座的扩增和表达率。
所述方法的一个或多个实例包括提供多种特异性引物,其中所述多种特异性引物包含第一特异性引物、第二特异性引物、第三特异性引物和第四特异性引物。在一个实施方案中,模板DNA包含多个基因座,例如基因座1、2、3和4。第一、第二、第三和第四特异性引物分别与模板DNA上存在的基因座1、2、3和4杂交,并扩增基因座1、2、3和4形成第一、第二、第三和第四扩增核酸序列。因此,使用随机引物降低了扩增期间每个基因座扩增不足(under-amplification)的可能性。
使用随机引物和基质结合(例如珠粒-1-结合)的特异性引物二者的扩增方法的一个实例见图1。扩增反应代表在Phi 29 DNA聚合酶存在时利用作为模板的环状DNA和随机引物的滚环扩增。珠粒-1-结合的特异性引物与扩增的DNA杂交,随后从特异性引物末端延伸。
通过用phi29 DNA聚合酶随机引发的模板DNA的扩增来产生链置换的单链DNA。单链DNA可与作为反应中存在的特异性引物的额外引物杂交,其中所述引物与基质连接(如图1图解所示)。所述方法包括通过与连接于第一基质(珠粒-1,如图1所描述)的特异性引物杂交来捕获所扩增的核酸序列,以形成第一基质结合的核酸序列。所述方法进一步包括利用第一基质结合(珠粒-1-结合)的核酸序列作为模板,自特异性引物的杂交位点延伸核酸序列。
所述方法又一实例进一步包括通过包含随机序列的引物扩增第一基质结合的核酸序列(如图2所示的珠粒-1结合的核酸)。扩增产生第二扩增核酸序列。所述方法进一步包括通过第二基质(珠粒-2,如图2所示)来捕获第二扩增核酸序列,其通过第二扩增核酸与连接于第二基质(珠粒-2)的特异性引物杂交来实现(如图2图解所示)。本文称为“第一扩增核酸序列”的扩增核酸序列与第一基质结合(珠粒-1-结合)的特异性引物连接,可以进一步通过随机引物扩增以形成被第二基质(珠粒-2)结合的特异性引物捕获的“第二扩增核酸序列”,如图2中图解所示。第二扩增核酸序列可进一步在杂交后通过第二基质结合的特异性引物扩增,以形成第三扩增核酸序列。因此,将第一基质结合的单链核酸序列通过随机引物扩增,并通过与第二基质连接的特异性引物捕获,并转移到第二基质。
在一个实例中,在通过第二基质(22)结合的特异性引物(20)捕获第一基质(例如珠粒)(16)结合的扩增核酸序列(18)之后,核酸序列自所述引物末端的延伸产生与第二基质结合的双链核酸序列(24),其图解阐述于图3。
扩增反应是等温的,不像温度循环反应。可以使用的适合的等温核酸扩增反应的非限制实例包括但不限于滚环扩增(RCA)或多重置换扩增(MDA)。所述方法可以用于例如环状核酸模板或线性核酸模板的扩增。即使当待扩增的核酸模板的量极少时,所述方法也可以有效地使用。所述方法可以用于例如全基因组扩增或单核酸扩增反应。
等温核酸扩增方法的非限制性实例包括LCR、自动维持序列扩增(SSR)、NASBA、LAMP、利用Qb-复制酶的扩增等等。在一些实施方案中,用SDA扩增核酸模板。在一些实施方案中,用MDA扩增核酸模板。在一个实施方案中,用RCA法扩增核酸模板。RCA可以作为LRCA使用,或可以是ERCA。在另一实施方案中,采用MPRCA来扩增核酸模板。
用于扩增的核酸聚合酶可以是校正或非校正核酸聚合酶。在一些实施方案中,使用的核酸聚合酶是链置换核酸聚合酶。核酸聚合酶可以是嗜热的或嗜温的核酸聚合酶。适合于使用的DNA聚合酶的实例包括但不限于:Phi29
DNA聚合酶、高保真度融合DNA聚合酶(例如具有持续合成能力增强结构域的热球菌属(Pyrococcus)样酶,New England Biolabs,MA)、来自激烈热球菌(Pyrococcus furiosus)的Pfu DNA聚合酶(Strategene,Lajolla,CA)、来自嗜热脂肪芽孢杆菌(Bacillus stearothermophilus)的Bst DNA聚合酶(New England
Biolabs,MA)、T7
DNA聚合酶的Sequenase™变体、exo(-)
VentR TM DNA聚合酶(New
England Biolabs,MA)、来自大肠杆菌(E. coli)的DNA聚合酶I的Klenow片段、T7 DNA聚合酶、T4 DNA聚合酶、来自热球菌GB-D的DNA聚合酶(New England Biolabs,MA)或来自Thermococcus litoralis的DNA聚合酶(New England Biolabs,MA)。
在一些实施方案中,所述方法可采用高度持续的链置换聚合酶以在用于高保真度碱基掺入的条件下扩增核酸模板。高保真度DNA聚合酶指这样的DNA聚合酶,其在适合条件下具有的错误掺入率等于或低于与常用的耐热PCR聚合酶例如Vent DNA聚合酶或T7 DNA聚合酶相关的错误掺入率(从约1.5 x 10-5-约5.7 x 10-5)。扩增反应混合物中可包括另外的酶以使错误掺入事件最小化。例如,可以加入蛋白介导的差错校正酶,例如MutS,以提高在聚合酶反应之中或之后的聚合酶保真度。
在一些实施方案中,扩增反应采用扩增后产生单链扩增DNA的DNA聚合酶。该DNA聚合酶能够进行链置换DNA合成。该聚合酶能够产生单链DNA,随后合成新链以形成双链DNA。在一个实施方案中,一旦引物结合到模板核酸,则DNA聚合酶以3’到5’方向开始核酸聚合,同时通过以5’到3’方向将任何封闭链(blocking
strand)置换来置换任何封闭链。
在一些实施方案中,可以使用Phi29 DNA聚合酶或Phi29样聚合酶来扩增DNA模板。在一些实施方案中,可使用Phi29 DNA聚合酶和另一种DNA聚合酶的组合。
核酸模板可以是单链核酸模板,或它可以是双链核酸模板。它可以是环状核酸模板、带切口的核酸模板或线性核酸模板。核酸模板可以包含DNA和/或RNA或DNA-RNA嵌合模板。在一些实施方案中,核酸模板可以是DNA模板。DNA模板可以是cDNA或基因组DNA。环状核酸模板可以是合成模板(例如通过酶促/化学反应环化的线性或带切口的DNA),或其可以是质粒DNA。核酸模板可以是合成核酸或天然核酸。其也可以包含修饰核苷酸。在一个实施方案实例中,核酸模板是环状DNA模板。
例如,模板DNA可以采集自患者或供体。在一个实例中,从患者采集模板DNA,接着扩增所述DNA,然后在基质上捕获所述DNA用于测序和分析。扩增的模板DNA用于检测特定基因座、单核苷酸多态性(SNP)或限制性片段长度多态性(RFLP)。模板DNA可例如从毛根、红细胞、上皮细胞、唾液或病理样本回收,扩增的DNA可经历法医分析或分子诊断。
核酸模板可以包含重组位点。重组位点包含有利于重组的核酸序列。在一个实施方案中,可将核酸模板进行工程改造以包含重组位点,扩增工程改造的核酸模板产生包含重组位点的扩增核酸。可以通过本领域已知的任何基因工程或分子生物学技术来实现核酸模板的工程改造,所述技术为例如但不限于克隆。在一些实施方案中,重组位点可以是位点特异性重组位点。位点特异性重组位点指包含被特异性重组蛋白识别的特异性序列的重组位点。
可以在适合于进行核酸扩增反应的溶液中扩增核酸模板以产生扩增的核酸。在一些实施方案中,环状DNA模板可以通过滚环扩增进行扩增。在一些其它的实施方案中,线性DNA模板可以利用多重置换核酸扩增进行扩增。
可预处理用于核酸扩增反应的每种试剂以去除任何污染核酸序列。试剂的预处理可以包括但不限于在紫外辐射存在下孵育试剂。例如,试剂也可以通过在核酸酶及其辅因子(例如金属离子)存在下孵育试剂来净化。合适的核酸酶包括但不限制于外切核酸酶,例如外切核酸酶I或外切核酸酶III。可用于DNA扩增反应的校正DNA聚合酶可以例如通过与二价金属离子(例如镁或锰)孵育来净化。用于核酸模板扩增的游离核苷酸可以包括但不限于天然核苷酸(例如dATP、dGTP、dCTP或dTTP)或其经修饰类似物。也可以添加诸如缓冲液、盐等其它组分。
在DNA模板扩增后,可通过采用基质结合的特异性引物来捕获扩增的DNA,所述特异性引物与扩增DNA的至少某一部分同源。基质结合的特异性引物可以捕获扩增的核酸序列(例如通过杂交),产生基质结合的扩增DNA。此外,在同一反应中,可在后续的DNA扩增反应中进一步通过DNA聚合酶延伸基质结合的引物,以产生额外量的基质上捕获的DNA。
在一些实施方案中,可让特异性引物与基质或捕获剂连接。基质可以是第一基质、第二基质、第三基质等。例如,基质可以是珠粒。例如,基质材料可选自聚合物、玻璃或金属。在一个实施方案中,基质材料是聚合物。捕获剂可以是亲和标签。特异性引物可以通过不同的相互作用与基质或捕获剂连接。例如,特异性引物可以经由核酸杂交、共价键、静电相互作用、范德瓦尔斯相互作用、疏水相互作用或这些相互作用的组合与捕获剂连接。例如,特异性引物可以与由聚合物制成的基质共价连接。在DNA扩增反应后,可以例如通过由聚合物制成的基质来捕获扩增的DNA。扩增反应可以包含不同的特异性引物,其中它们中的每一种均可多连接到不同类型的捕获剂。一系列的特异性引物也可以连接到第一基质、第二基质、第三基质等。第一或第二或第三基质可以包含例如珠粒、试管、多孔板、载玻片和eppendorfs。
如所提及,核酸模板的扩增拷贝可以与捕获珠粒连接。作为非限制性实例,这些连接可以由与珠粒表面结合的化学基团或寡核苷酸介导。核酸模板的扩增拷贝可以以本领域已知的任何合适方式与固相支持体连接,所述固相支持体为例如但不限于捕获珠粒或其它合适表面。例如核酸模板的扩增拷贝可以通过杂交与基质结合的特异性引物连接。
特异性引物可以直接或经由接头与基质(或第一基质)或捕获剂连接。可将经由接头与基质连接的特异性引物,用于纯化具有与特异性引物互补的序列的核酸。第一基质选自珠粒或表面。捕获剂选自亲和标签或聚合物。在一个非限制性实施方案中,接头可以是聚合物,例如丙烯酰胺、葡聚糖或聚乙二醇(PEG)。在至少一个实施方案中,接头的一端可以包含与待固定化的特异性引物形成共价键的反应基团(例如酰胺基)。特异性引物可以通过共价键例如螯合作用与DNA捕获剂例如亲和标签结合。亲和标签可以包括但不限于组氨酸(His-标签)或生物素。
例如,可以通过与亲和标签连接的特异性引物来捕获扩增的核酸以形成亲和标签结合的扩增核酸序列。然后可通过用于特异性标签的适合基质来随后捕获亲和标签结合的扩增核酸序列。例如,通过生物素化的特异性引物捕获的扩增核酸,可以进一步通过形成生物素-链霉亲和素复合物而被链霉亲和素捕获。可以选择亲和标签以使其可用不涉及核酸杂交的方法来捕获。例如,亲和标签可通过共价键、静电相互作用、范德瓦尔斯相互作用、疏水相互作用或这些相互作用的组合来捕获。亲和标签可以用于例如从扩增反应中纯化不同种类的扩增核酸。
珠粒可具有任何适合的大小,可由选自但不限于无机物、天然聚合物或合成聚合物的材料制备。这些材料的具体实例包括但不限于纤维素、纤维素衍生物、丙烯酸树脂、玻璃、硅胶、聚苯乙烯、明胶、聚乙烯吡咯烷酮、乙烯和丙烯酰胺的共聚物、与二乙烯苯交联的聚苯乙烯、葡聚糖、聚丙烯酰胺、交联葡聚糖(例如SephadexTM)、琼脂糖凝胶(SepharoseTM)或其它本领域已知的固相支持体。例如,捕获珠粒可以具有约1-400 μm的直径。
在一个或多个实施方案中,特异性引物序列与珠粒的共价化学连接可以通过用标准偶联剂来完成。例如,水溶性碳二亚胺可用于通过氨基磷酸酯键连接特异性引物序列的5’-磷酸与胺包被的捕获珠粒。可以用于连接寡核苷酸与珠粒的其它键合化学物包括但不限于N-羟基丁二酰胺(NHS)及其衍生物。
在一个或多个实施方案中,可将捕获剂例如捕获珠粒设计为具有多种特异性引物,所述特异性引物识别核酸模板的一部分及该模板的扩增拷贝或与其互补。例如,为了获得模板的克隆扩增,可将独特的核酸种类用于与任何一种捕获珠粒连接。可将一种或多种扩增方法用于产生DNA包被的珠粒,其例如可以用于模拟细菌菌落中存在的质粒。例如,所述方法也可以用于产生多种不同的DNA序列,所述序列可用于下游目的例如DNA测序或DNA检测。
在一个实施方案中,扩增可以在乳液中实施。可以在乳化之前或形成乳液之后将模板捕获到珠粒。在另一实施方案中,表面结合的特异性引物可以定位于在乳液液滴中的珠粒上,以允许产生不同的DNA包被的珠粒。例如,可产生这样的乳液,其中每个液滴可包含单独的或除其它DNA分子之外的单个目的DNA分子。如果每个珠粒存在于每个乳液液滴中,则捕获后可随后洗涤具有扩增产物DNA的珠粒,以移除未结合的DNA。然后可将洗涤的珠粒用于另外的扩增反应。如果单个DNA分子最初已隔离到乳液液滴中,则可将具有扩增核酸的洗涤珠粒用于产生“DNA文库”。可自群体中分离单个珠粒以通过珠粒结合的DNA的后续DNA扩增在溶液中产生“DNA克隆”。可将珠粒结合的扩增DNA用于许多不同类型的分析(例如蛋白表达或克隆)。也可将珠粒用于产生“DNA阵列”。通过形成可与表面连接的珠粒单层,可形成非重叠的随机珠粒阵列,其中每个珠粒均与产物DNA连接。
也可将乳液中的珠粒用作模板用于通过链置换合成的另外DNA扩增和通过杂交捕获产物。可以在将珠粒加到扩增溶液中后产生乳液。可将有或没有连接核酸模板的捕获剂例如捕获珠粒,悬浮在热稳定的水包油乳液中。可存在带有珠粒但没有任何核酸或者带有核酸但没有任何珠粒或者没有任何核酸或没有任何珠粒的微滴。可存在具有多于一个拷贝的核酸的微滴。可以通过任何适合的方法形成乳液或微滴,所述方法包括但不限于佐剂法、反向流动法、错流方法、转鼓法和膜法。
可在化学或热变性条件下处理乳液中的珠粒以产生具有单链DNA的珠粒。通过在扩增反应期间延伸与单链产物杂交的连接引物来产生单链DNA。可将具有扩增核酸的珠粒用于需要单链DNA的下游方法,所述下游方法为例如通过杂交进行的测序或通过连接进行的测序或通过合成进行的测序。
在用于扩增核酸的试剂盒的一些实施方案中,所述试剂盒包括Phi29
DNA聚合酶、包含随机序列的引物和特异性引物。可将特异性引物与基质或捕获剂连接。试剂盒可进一步包括本领域已知的可用于核酸扩增的其它试剂。试剂盒也可包括核酸聚合酶和部分受限的引物。核酸聚合酶和部分受限的引物可包装在单个容器中,或它们可包装在分开的容器中。
在一个实施方案中,试剂盒包括Phi29 DNA聚合酶和部分受限的引物。试剂盒中的部分受限引物可以包含核苷酸类似物,例如LNA核苷酸。在一些实施方案中,部分受限的引物是DNA-LNA嵌合引物。试剂盒中的部分受限引物可以是抗核酸酶引物,例如抗外切核酸酶的引物。试剂盒中的这些抗外切核酸酶引物可以在核苷酸间含有一个或多个硫代磷酸酯键。
试剂盒可进一步包括进行核酸扩增反应所需要的试剂或试剂溶液。其可以进一步包括说明手册,其详述试剂盒中包括的具体组分或在核酸扩增反应中使用所述组分的方法,或两者都有。
实施例
1
扩增前反应混合物的净化
在使用用于核酸扩增反应的试剂和试剂溶液之前,让其在不含核酸的通风柜里净化以去除任何污染核酸。诸如Phi29
DNA聚合酶、外切核酸酶I、外切核酸酶III和SSB蛋白等试剂,保存于50 mM Tris-HCl
(pH 7.2)、200 mM NaCl、10 mM DTT、1 mM EDTA、0.01% (v/v) Tween-20和50 %
(v/v)甘油中。通过让引物-核苷酸混合物与外切核酸酶I、外切核酸酶III和单链DNA结合蛋白(SSB蛋白)的组合孵育,来净化包含引物和核苷酸(dNTP)的引物-核苷酸溶液(引物-核苷酸混合物)。通过在二价阳离子(例如Mg2+)存在下与外切核酸酶孵育来净化包含DNA聚合酶的酶混合物。用净化的酶混合物和引物-核苷酸混合物实施任何靶标核酸扩增反应。
如表2所示,让含有200 ng Phi29 DNA聚合酶的酶混合物,在含有15 mM KCl、20 mM
MgCl2、0.01%(v/v)
Tween-20和1 mM 三(2-羧乙基)膦(TCEP)的50 mM HEPES缓冲液(pH=8.0)中与0.1单位外切核酸酶III孵育。孵育在30℃下进行约60分钟或在4℃下进行12小时。然后将孵育的酶混合物转移至冰浴,用于DNA扩增反应,因此外切核酸酶III不会有任何失活。如果在完成后立即处理完成的扩增反应物以使外切核酸酶失活,那么该少量的外切核酸酶III对扩增反应没有实质影响。
为净化引物-核苷酸混合物,让其与表2中所示的外切核酸酶I、外切核酸酶III和SSB蛋白的组合孵育。孵育在含有15 mM KCl、20 mM MgCl2、0.01%
(v/v) Tween-20和1 mM TCEP的 50
mM HEPES缓冲液(pH=8.0)中于37℃进行约60分钟(总反应体积为5 μL)。在该实施例中使用大肠杆菌SSB蛋白作为适合的单链结合蛋白。在引物-核苷酸混合物净化后,通过让引物-核苷酸混合物在85℃孵育约15分钟接着在95℃孵育约5分钟-约10分钟,来热灭活外切核酸酶。
表2:酶混合物和引物-核苷酸混合溶液的净化
| 引物-核苷酸混合物(每个反应) | DNA聚合酶(酶)混合物(每个反应) | |
| 2X反应缓冲液(反应缓冲液是 50 mM HEPES缓冲液(pH=8.0)、15mM KCl、20 mM MgCl2、0.01% Tween-20和1 mM TCEP) | 2.6 μL | 2.5 μL |
| 蒸馏水 | - | 2.2 μL |
| 10 mM dNTP混合物 | 0.4 μL | - |
| 1 mM引物 | 0.4 μL | - |
| 外切核酸酶I (20单位/μL) | 0.5 μL | - |
| 外切核酸酶III (10单位/μL) | 0.1 μL | - |
| 外切核酸酶III (1单位/μL) | - | 0.1 μL |
| SSB蛋白(100 ng/μL) | 1 μL | - |
| Phi29 DNA聚合酶(1mg/ml) | - | 0.2 μL |
| 总反应体积 | 5 μL | 5 μL |
实施例
2
无模板对照扩增
通过实施不加任何模板DNA的DNA扩增反应(无模板对照(NTC)扩增),来评估在核酸扩增反应期间的非特异性扩增反应。反应采用或者完全随机引物或者包含LNA核苷酸的部分受限引物。这两种引物均为抗外切核酸酶引物,在接近(towards)序列3'末端的核苷酸之间有硫代磷酸酯键。
来自未添加靶标DNA模板的DNA扩增反应(NTC)的扩增产物产生于非特异性扩增反应(假扩增或背景扩增)。非特异性扩增可以是由于扩增污染DNA分子或扩增通过珠粒结合的特异性引物而被珠粒捕获的背景DNA分子而产生。为避免任何源自于污染DNA的非特异性扩增反应,用实施例1中所述方法净化用于扩增反应的任何试剂或试剂溶液(酶混合物和引物-核苷酸),以去除任何污染DNA。
为评估非特异性DNA扩增反应,通过让净化的引物-核苷酸混合物和净化的酶混合物在不添加任何DNA模板时于30℃孵育约400分钟,来进行DNA扩增反应。扩增反应混合物由以下物质组成:40 μM引物(随机引物或序列W+W+NN*S的部分受限引物,其中W表示A或T/U,S表示G或C,N代表随机核苷酸(即N可以是A、C、G或T/U中的任一种),字母命名前面的加号(+)标记表示该字母命名的核苷酸是LNA核苷酸,字母前面的星号(*)标记表示该字母命名的核苷酸是硫代磷酸酯修饰核苷酸。);400 μM dNTP (dATP、dCTP、dGTP、dTTP各自的等量混合物)和200 ng phi29 DNA聚合酶(200
ng/10 μL反应物)。反应混合物在含有15 mM KCl、20 mM MgCl2、0.01% (v/v) Tween-20、1 mM
TCEP的50 mM HEPES缓冲液(pH=8.0)中孵育。
实施例
3
扩增反应
对于核酸扩增反应,让引物-核苷酸混合物和酶混合物净化后与模板核酸混合在一起,以形成扩增反应,然后在约30℃下孵育。在Phi 29 DNA聚合酶以及随机引物、珠粒结合的特异性引物和pUC18质粒DNA存在下实施等温扩增反应。
为评估DNA扩增反应,通过让净化的引物-核苷酸混合物和净化的酶混合物与pUC18质粒DNA模板在30℃孵育约400分钟,来实施DNA扩增反应。扩增反应混合物由以下物质组成:40 μM引物(随机引物或具有序列W+WNN*S的部分受限引物,其中W表示A或T/U,S表示G或C,N代表随机核苷酸(即N可以是A、C、G或T/U中的任一种),字母命名前面的加号(+)标记表示该字母命名的核苷酸是LNA核苷酸,字母前面的星号(*)标记表示该字母命名的核苷酸是硫代磷酸酯修饰核苷酸。);1 μL特异性引物缀合的珠粒(每微升大约70,000个珠粒,其中特异性引物与珠粒共价连接);400 μM dNTP (dATP、dCTP、dGTP、dTTP各自400 μM);1 pg pUC 18质粒DNA和200 ng phi29 DNA 聚合酶(200
ng/10 μL反应物)。反应混合物在含有15 mM KCl、20 mM MgCl2、0.01% (v/v) Tween-20、1 mM
TCEP的50 mM HEPES缓冲液中孵育。
实施例
4
捕获珠粒合成
其中特异性引物与珠粒连接的DNA捕获珠粒如下合成。将N-羟基琥珀酰亚胺酯(NHS)激活的Sepharose (NHS HP SpinTrapTM, GE Healthcare,
Piscataway, N.J.)珠粒用于合成DNA捕获珠粒。然后利用产品说明书所述方案(GE Healthcare NHS HP SpinTrapTM方案)用寡核苷酸官能化珠粒。自IDT Technologies
(Coralville, Iowa, USA)市购与-40通用捕获引物5'末端连接的胺标记的HEG (六聚乙二醇(hexaethyleneglycol))接头(5'-胺-3 HEG间隔基/5AmMC6/GTTTTCCCAGTCACGACGTTG*T*A-3';
SEQ ID NO:1),所述通用引物与pUC 18质粒DNA一条链(待扩增的模板)的一部分互补,其中5AmMC6表示通过六聚乙二醇接头与寡核苷酸5'末端连接的伯胺基团。让捕获引物溶入pH 8.0的TE缓冲液以达到最终浓度为1 mM。让3皮摩尔的引物与各1 μL珠粒结合,1 μL引物缀合的珠粒的填充浆液含有50,000-70,000个单独珠粒,其中珠粒具有的直径约为30微米。这会导致产生大约3皮摩尔的与60,000个珠粒连接的引物,或1.5×108引物/珠粒(如果连接反应达到100%完成)。
实施例
5
珠粒上捕获扩增的
DNA
捕获珠粒包含特异性引物序列或与珠粒连接的序列。将DNA捕获珠粒(珠粒-间隔基- Seq. ID No. 1或珠粒-间隔基- Seq. ID No. 2)如下用于捕获扩增DNA分子。通过让净化的引物-核苷酸混合物和净化的酶混合物,在30℃与pUC18质粒DNA模板在确保珠粒在反应期间保持悬浮的旋转器平台上孵育约400分钟,来实施DNA扩增反应。扩增反应混合物由以下物质组成:40 μM引物(具有序列W+WNN*S的部分受限引物,其中W表示A或T/U,S表示G或C,N代表随机核苷酸(即N可以是A、C、G或T/U中的任一种),字母命名前面的加号(+)标记表示该字母命名的核苷酸是LNA核苷酸,字母前面的星号(*)标记表示该字母命名的核苷酸是硫代磷酸酯修饰核苷酸。);3 μL特异性引物(每微升大约70,000个珠粒,特异性引物与珠粒共价连接);400 μM dNTP (dATP、dCTP、dGTP、dTTP各自400 μM);2 ng pUC 18质粒DNA和200 ng phi29 DNA聚合酶(200
ng/10 μL反应物)。在含有15 mM KCl、20 mM MgCl2、0.01% (v/v) Tween-20、1 mM
TCEP的50 mM HEPES缓冲液(pH = 8.0)中实施孵育。反应后允许珠粒沉降。从反应管中移除含有未结合DNA扩增产物的反应上清液,将其保存用于后续分析。然后通过加入TE,短时间漩涡振荡和用microfuge短时间离心,来用200 μL TE洗涤剩余的珠粒沉淀。移除该步骤的TE上清液,再重复两次洗涤步骤。将洗涤的沉淀悬浮于97 μL TE中。将来自如上所述扩增反应的15 μL TE洗涤的捕获珠粒转移到培养皿。让珠粒浆液沉降,通过显微操作分离单个珠粒。
用随机引物和特异性引物捕获珠粒扩增pUC 18 DNA,产生珠粒结合的DNA。如图4A所示,包被有连接的特异性引物的单个珠粒上存在的捕获DNA的扩增,产生被扩增DNA完全包被的珠粒。图4B显示了从含有许多这种珠粒的混合物中分离的相同珠粒,这证明可从这类混合物中分离单个珠粒。
实施例
6
限制性消化
在如上所述的特异性引物包被的珠粒上捕获来自NTC的扩增产物和来自pUC18质粒DNA的扩增产物。用TE洗涤珠粒3次,然后进行EcoRI限制性酶消化。单独对pUC18 DNA (作为阳性对照)进行限制性酶消化。通过加入10单位EcoRI、1 μL 10X酶缓冲液、1 μL TE洗涤的珠粒和7 μL水至10 μL总反应体积,来消化DNA,让反应混合物在37℃水浴孵育1小时。
如图5所示,将限制性酶消化产物上样至琼脂糖凝胶以分析消化产物相对于标准分子量标记(泳道1)的分子量。通过珠粒来捕获扩增的pUC18 DNA,接着用EcoRI限制性酶消化,将消化产物上样至琼脂糖凝胶泳道2 (如图5所示)。用EcoRI消化纯化的pUC18质粒DNA,并作为对照上样至泳道4,其显示纯pUC 18限制性酶消化产物DNA和限制性酶消化后的扩增的珠粒结合的pUC 18 DNA具有相同的分子量。将NTC扩增DNA的限制性酶消化产物上样至泳道3,其显示不存在被珠粒捕获的背景扩增产物。这证明用上述方法同时扩增和捕获靶标DNA没有背景扩增。
实施例
7 DNA
从一个珠粒到其它珠粒的转移
为评估DNA扩增、捕获和DNA从一个珠粒到另一珠粒的转移,实施以下方法。通过让净化的引物-核苷酸混合物、净化的酶混合物与引物包被的捕获珠粒并与pUC18质粒DNA模板在30℃于管中孵育约400分钟,来启动DNA扩增反应。扩增反应混合物与上述相同。在存在于管中的珠粒上捕获扩增DNA。
如上所述将具有捕获DNA的5个单独分离的珠粒各自转移到单独的反应管。从每个管中移除过量TE,向每个珠粒加入10 μL扩增反应混合物。扩增反应混合物由以下物质组成:40 μM引物(具有序列+W+WNN*S的部分受限引物,其中W表示A或T/U,S表示G或C,N代表随机核苷酸(即N可以是A、C、G或T/U中的任一种),字母命名前面的加号(+)标记表示该字母命名的核苷酸是LNA核苷酸,字母前面的星号(*)标记表示该字母命名的核苷酸是硫代磷酸酯修饰核苷酸。);400 μM dNTP (dATP、dCTP、dGTP、dTTP各自400 μM);和200 ng phi29 DNA聚合酶(200 ng/10 μL反应物)。在含有15 mM KCl、20 mM MgCl2、0.01%
(v/v) Tween-20、1 mM TCEP的50 mM
HEPES缓冲液(pH = 8.0)中实施孵育。允许反应在30℃孵育约400分钟。在已捕获在这些单独珠粒上的DNA扩增后,移出1 μL扩增反应混合物上清液,留珠粒在管中。用限制酶EcoRI消化珠粒结合的DNA。将不同管的EcoRI消化产物上样于如图6所示的琼脂糖凝胶泳道2、4、6、8和10 (分离5个单独珠粒,扩增与其结的DNA);而将未消化的相同样品上样于如图6所示的琼脂糖凝胶泳道3、5、7、9和11。可以在每个泳道中清楚地看到2.7 KB的pUC18扩增产物。这证明在最初扩增反应期间被加到扩增反应中的每个单独珠粒的确捕获了pUC18扩增产物。这显示了可如何将该方法用于扩增和捕获DNA的非限制性实例。
在另一个反应中,将具有捕获的扩增DNA的一个珠粒转移至已经含有新鲜扩增反应混合物及另外的特异性引物包被珠粒的管中。扩增反应混合物由以下物质组成:40 μM引物(具有序列+W+WNN*S的部分受限引物,其中W表示A或T/U,S表示G或C,N代表随机核苷酸(即N可以是A、C、G或T/U中的任一种),字母命名前面的加号(+)标记表示该字母命名的核苷酸是LNA核苷酸,字母命名前面的星号(*)标记表示该字母命名的核苷酸是硫代磷酸酯修饰核苷酸。);3 μL特异性引物(每微升约70,000个珠粒,特异性引物共价连接至珠粒);400 μM dNTP ( dATP、dCTP、dGTP和dTTP各400 μM);和200 ng Phi29 DNA聚合酶(200
ng/10 μL反应物)。在含有15 mM KCl、20 mM MgCl2、0.01% (v/v) Tween-20和1 mM
TCEP的50 mM HEPES缓冲液(pH = 8.0)中实施孵育。此处扩增反应包括从如上所述的先前扩增反应管中转移的单个珠粒上捕获的DNA。来自单个珠粒的扩增DNA在该反应中进一步扩增,并且在反应期间被转移到其它珠粒。如上所述通过TE洗涤在另外珠粒上捕获的扩增的DNA 3次,然后用EcoRI限制性酶消化。取出1 μL所得的经洗涤的珠粒,如实例6所述用EcoRI消化。将EcoRI消化产物上样至如图6所示的琼脂糖凝胶泳道12,未消化产物上样至泳道13。上述实施例清晰地证明,在第一次扩增反应中最初扩增并在珠粒上捕获的DNA,随后在后续扩增反应中于该单个珠粒上扩增,并在新的捕获珠粒群上被捕获。在本实施例中,通过该方法使用单个pUC18包被的珠粒以产生大约150,000个另外的pUC18包被的珠粒。这显示该方法可如何用于从一个位置或表面转移DNA到另一个位置或表面的非限制性实例
实施例
8
序列分析
作为上述珠粒含有扩增的模板的进一步证明,自所述珠粒获得DNA序列信息。如以上实施例5所述,在珠粒上捕获扩增的DNA。在扩增和捕获后,将TE洗涤的珠粒用作DNA测序反应的模板,以证明珠粒含有与表面连接的扩增的DNA。取出1 μL所得的经洗涤的珠粒(50,000个珠粒),将3.2皮摩尔(1 μL) M13反向测序引物、4 μL Big Dye DNA测序预混物、2 μL测序缓冲液和12 μL水混合物加至所述珠粒。按制造商建议实施DNA循环测序,通过沉淀来纯化测序产物,在ABI
3730 x l测序仪(Applied Biosystem)中解析。序列数据(SEQ ID NO. 2)示于图7。自这些珠粒获得的序列具有与用约200 ng pUC18模板DNA正常获得的序列相同的信号强度。这表明每个珠粒可具有约10皮克连接的扩增的pUC18 DNA。获得的序列与获自pUC18 DNA的序列准确匹配,这表明与珠粒连接的DNA是扩增的pUC18
DNA。
尽管本文仅阐明和阐述了本发明的某些特点,但本领域技术人员可想到许多修改和改变。因此,应该理解,附加权利要求意欲涵盖落入本发明真正精神之内的全部这类修改和改变。
Claims (23)
1. 一种用于扩增核酸的方法,所述方法包括:
提供核酸模板、DNA聚合酶、脱氧核糖核苷三磷酸、包含随机序列的引物和特异性引物;和
在等温条件下扩增所述核酸模板以形成扩增的核酸序列。
2. 权利要求1的方法,其中所述随机引物包含至少一个经修饰的核酸碱基。
3. 权利要求2的方法,其中所述经修饰的核酸碱基增加所述包含随机序列的引物的解链温度。
4. 权利要求2的方法,其中所述经修饰的核酸碱基选自锁定核酸碱基、肽核酸碱基或核糖核酸碱基。
5. 权利要求1的方法,其中所述特异性引物与第一基质连接。
6. 权利要求5的方法,其中所述第一基质选自珠粒、试管、多孔板或载玻片。
7. 权利要求5的方法,其中所述第一基质的材料选自聚合物、玻璃或金属。
8. 权利要求5的方法,其进一步包括通过所述扩增的核酸序列与特异性引物的杂交以形成第一基质结合的核酸序列,来捕获所述扩增的核酸序列。
9. 权利要求8的方法,其进一步包括用所述第一基质结合的核酸序列作为模板从所述特异性引物的杂交位点延伸核酸序列。
10. 权利要求8的方法,其进一步包括通过包含随机序列的引物扩增所述第一基质结合的核酸序列以形成第二扩增的核酸序列。
11. 权利要求10的方法,其进一步包括通过所述第二扩增的核酸与连接于第二基质的特异性引物的杂交,来用所述第二基质捕获所述第二扩增的核酸序列。
12. 权利要求1的方法,其中所述特异性引物与捕获剂连接。
13. 权利要求12的方法,其中所述捕获剂包含亲和标签。
14. 权利要求1的方法,其中所述扩增在乳液中实施。
15. 权利要求1的方法,其中所述扩增包括滚环扩增或多重置换扩增。
16. 权利要求1的方法,其中所述扩增的核酸序列是串联重复核酸序列。
17. 权利要求1的方法,其中所述核酸模板是环状核酸。
18. 权利要求1的方法,其中所述核酸模板包含重组位点。
19. 权利要求1的方法,其中所述核酸模板是DNA。
20. 权利要求1的方法,其中所述DNA聚合酶是Phi 29 DNA聚合酶。
21. 权利要求1的方法,其中所述随机引物包含至少5个核苷酸。
22. 一种用于扩增核酸的试剂盒,其包括:
Phi29 DNA聚合酶;
至少一种包含随机序列的引物;和
至少一种特异性引物。
23. 权利要求22的试剂盒,其中所述特异性引物与基质或捕获剂连接。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/702,884 | 2010-02-09 | ||
| US12/702,884 US20110195457A1 (en) | 2010-02-09 | 2010-02-09 | Isothermal amplification of nucleic acid using primers comprising a randomized sequence and specific primers and uses thereof |
| PCT/US2011/023996 WO2011142861A2 (en) | 2010-02-09 | 2011-02-08 | Isothermal amplification of nucleic acid using primers comprising a randomized sequence and specific primers and uses thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102753707A true CN102753707A (zh) | 2012-10-24 |
Family
ID=44354018
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2011800087156A Pending CN102753707A (zh) | 2010-02-09 | 2011-02-08 | 用随机引物和特异性引物的混合物等温扩增核酸 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US20110195457A1 (zh) |
| EP (1) | EP2534268A4 (zh) |
| JP (1) | JP2013518598A (zh) |
| CN (1) | CN102753707A (zh) |
| AU (1) | AU2011253427B2 (zh) |
| BR (1) | BR112012019396A2 (zh) |
| CA (1) | CA2788821A1 (zh) |
| IN (1) | IN2012DN06299A (zh) |
| WO (1) | WO2011142861A2 (zh) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105992815A (zh) * | 2013-10-28 | 2016-10-05 | 韩国科学技术研究院 | 多孔结构及其制造方法 |
| CN106460040A (zh) * | 2014-03-26 | 2017-02-22 | 通用电气公司 | 在低盐条件下的等温扩增 |
| CN108350492A (zh) * | 2015-11-05 | 2018-07-31 | 通用电气公司 | 连接酶辅助的核酸环化和扩增 |
| CN110195056A (zh) * | 2019-05-31 | 2019-09-03 | 汪雪 | 一种双引物及其应用 |
| CN111334562A (zh) * | 2018-12-19 | 2020-06-26 | 合肥铼科生物科技有限公司 | 一种含有修饰引物的核酸扩增方法和试剂盒 |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2012050393A (ja) * | 2010-09-02 | 2012-03-15 | Sony Corp | 核酸等温増幅方法 |
| WO2013117595A2 (en) * | 2012-02-07 | 2013-08-15 | Illumina Cambridge Limited | Targeted enrichment and amplification of nucleic acids on a support |
| US9353393B2 (en) | 2012-02-15 | 2016-05-31 | General Electric Company | Methods and kits for reducing non-specific nucleic acid amplification |
| US9777319B2 (en) | 2012-06-29 | 2017-10-03 | General Electric Company | Method for isothermal DNA amplification starting from an RNA template |
| EP3428290B1 (en) * | 2012-07-26 | 2022-04-06 | Illumina, Inc. | Compositions and methods for the amplification of nucleic acids |
| JP6366896B2 (ja) * | 2013-03-07 | 2018-08-01 | 国立研究開発法人農業・食品産業技術総合研究機構 | Dna親和性物質含有組成物、dna親和性物質の精製方法、dna親和性物質含有組成物の製造方法およびdna親和性物質を精製するためのキット |
| US9422535B2 (en) | 2013-04-25 | 2016-08-23 | Thermo Fisher Scientific Baltics Uab | phi29 DNA polymerase mutants having increased thermostability and processivity |
| US9938568B2 (en) | 2013-07-26 | 2018-04-10 | General Electric Company | Ligase-assisted nucleic acid circularization and amplification |
| US9644232B2 (en) * | 2013-07-26 | 2017-05-09 | General Electric Company | Method and device for collection and amplification of circulating nucleic acids |
| US9410172B2 (en) * | 2013-09-16 | 2016-08-09 | General Electric Company | Isothermal amplification using oligocation-conjugated primer sequences |
| WO2015084802A1 (en) * | 2013-12-02 | 2015-06-11 | Regents Of The University Of Minnesota | Rna amplification and oligonucleotide library preparation |
| AU2015273480A1 (en) | 2014-06-11 | 2016-12-08 | Samplix S.A.R.L. | Nucleotide sequence exclusion enrichment by droplet sorting (needls) |
| US11220705B2 (en) | 2015-04-24 | 2022-01-11 | Qiagen Gmbh | Method for immobilizing a nucleic acid molecule on solid support |
| US11085073B2 (en) | 2015-04-24 | 2021-08-10 | Qiagen Gmbh | Method for immobilizing a nucleic acid molecule on a solid support |
| JP7056012B2 (ja) * | 2017-05-19 | 2022-04-19 | トヨタ自動車株式会社 | ランダムプライマーセット、及びこれを用いたdnaライブラリーの作製方法 |
| EP3643788A4 (en) * | 2017-06-20 | 2021-01-06 | MGI Tech Co., Ltd. | PAIR OF PRIMERS FOR PCR AND RELATED APPLICATION |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030207267A1 (en) * | 2000-06-28 | 2003-11-06 | Lasken Roger S. | Multiply-primed amplification of nucleic acid sequences |
| US20040209298A1 (en) * | 2003-03-07 | 2004-10-21 | Emmanuel Kamberov | Amplification and analysis of whole genome and whole transcriptome libraries generated by a DNA polymerization process |
| EP1482059A1 (en) * | 2003-05-28 | 2004-12-01 | Agilent Technologies, Inc. | Comparative genomic hybridization assays using immobilized oligonucleotide targets |
| US20040248105A1 (en) * | 2003-06-06 | 2004-12-09 | Gyanendra Kumar | Method of whole genome amplification with reduced artifact production |
| US20080128298A1 (en) * | 2001-10-15 | 2008-06-05 | Carole Bornarth | Nucleic acid amplification |
| WO2008118679A1 (en) * | 2007-03-23 | 2008-10-02 | Ge Healthcare Bio-Sciences Corp. | Multiply-primed amplification of circular nucleic acid sequences |
| US20090035279A1 (en) * | 2007-06-13 | 2009-02-05 | Decode Genetics Efh | Genetic variants on chr 15q24 as markers for use in diagnosis, prognosis and treatment of exfoliation syndrome and glaucoma |
| US20090203085A1 (en) * | 2008-02-12 | 2009-08-13 | Nurith Kurn | Isothermal Nucleic Acid Amplification Methods and Compositions |
| US20100022412A1 (en) * | 2008-07-02 | 2010-01-28 | Roberto Rigatti | Using populations of beads for the fabrication of arrays on surfaces |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1999002939A1 (en) * | 1997-07-14 | 1999-01-21 | Spectral Dimensions, Inc. | Methods and devices for very rapid scan interferometry |
| US6620597B1 (en) * | 1998-01-09 | 2003-09-16 | University Of Utah Research Foundation | Method for in vitro amplification of circular DNA |
| US7601497B2 (en) * | 2000-06-15 | 2009-10-13 | Qiagen Gaithersburg, Inc. | Detection of nucleic acids by target-specific hybrid capture method |
| US20040121338A1 (en) * | 2002-12-19 | 2004-06-24 | Alsmadi Osama A. | Real-time detection of rolling circle amplification products |
| JP2007525151A (ja) * | 2003-01-29 | 2007-09-06 | 454 コーポレーション | 一本鎖dnaライブラリーの調製方法 |
| CA2521520A1 (en) * | 2003-04-29 | 2004-11-11 | Amersham Biosciences Corp | Multiply-primed amplification of nucleic acid sequences |
| AU2005216549A1 (en) * | 2004-02-27 | 2005-09-09 | President And Fellows Of Harvard College | Polony fluorescent in situ sequencing beads |
| US9139849B2 (en) * | 2005-04-08 | 2015-09-22 | The United States of America as Represented by the Government of the Department of Health and Human Services | Rapid generation of long synthetic centromeric tandem repeats for mammalian artificial chromosome formation |
| CN101213311B (zh) * | 2005-04-29 | 2013-02-13 | 合成基因组股份有限公司 | 利用滚环扩增扩增和克隆单个dna分子 |
| US20100008939A1 (en) * | 2008-07-09 | 2010-01-14 | General Electric Company | Unprocessed rolling circle amplification product |
-
2010
- 2010-02-09 US US12/702,884 patent/US20110195457A1/en not_active Abandoned
-
2011
- 2011-02-08 AU AU2011253427A patent/AU2011253427B2/en not_active Ceased
- 2011-02-08 CN CN2011800087156A patent/CN102753707A/zh active Pending
- 2011-02-08 CA CA2788821A patent/CA2788821A1/en not_active Abandoned
- 2011-02-08 EP EP11780952.5A patent/EP2534268A4/en not_active Withdrawn
- 2011-02-08 JP JP2012552146A patent/JP2013518598A/ja not_active Ceased
- 2011-02-08 IN IN6299DEN2012 patent/IN2012DN06299A/en unknown
- 2011-02-08 WO PCT/US2011/023996 patent/WO2011142861A2/en active Application Filing
- 2011-02-08 BR BR112012019396A patent/BR112012019396A2/pt not_active IP Right Cessation
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030207267A1 (en) * | 2000-06-28 | 2003-11-06 | Lasken Roger S. | Multiply-primed amplification of nucleic acid sequences |
| US20080128298A1 (en) * | 2001-10-15 | 2008-06-05 | Carole Bornarth | Nucleic acid amplification |
| US20040209298A1 (en) * | 2003-03-07 | 2004-10-21 | Emmanuel Kamberov | Amplification and analysis of whole genome and whole transcriptome libraries generated by a DNA polymerization process |
| EP1482059A1 (en) * | 2003-05-28 | 2004-12-01 | Agilent Technologies, Inc. | Comparative genomic hybridization assays using immobilized oligonucleotide targets |
| US20040248105A1 (en) * | 2003-06-06 | 2004-12-09 | Gyanendra Kumar | Method of whole genome amplification with reduced artifact production |
| WO2008118679A1 (en) * | 2007-03-23 | 2008-10-02 | Ge Healthcare Bio-Sciences Corp. | Multiply-primed amplification of circular nucleic acid sequences |
| US20090035279A1 (en) * | 2007-06-13 | 2009-02-05 | Decode Genetics Efh | Genetic variants on chr 15q24 as markers for use in diagnosis, prognosis and treatment of exfoliation syndrome and glaucoma |
| US20090203085A1 (en) * | 2008-02-12 | 2009-08-13 | Nurith Kurn | Isothermal Nucleic Acid Amplification Methods and Compositions |
| US20100022412A1 (en) * | 2008-07-02 | 2010-01-28 | Roberto Rigatti | Using populations of beads for the fabrication of arrays on surfaces |
Non-Patent Citations (2)
| Title |
|---|
| DEAN ET AL: "Rapid amplication of plasmid and phage DNA using phi29 DNA polymerase and multiply-primed rolling circle amplification", 《GENOME RESEARCH》 * |
| ZHANG ET AL: "Ramification Amplification: A Novel Isothermal DNA Amplification Method", 《MOLECULAR DIAGNOSIS》 * |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105992815A (zh) * | 2013-10-28 | 2016-10-05 | 韩国科学技术研究院 | 多孔结构及其制造方法 |
| CN106460040A (zh) * | 2014-03-26 | 2017-02-22 | 通用电气公司 | 在低盐条件下的等温扩增 |
| CN106460040B (zh) * | 2014-03-26 | 2021-01-08 | 通用电气公司 | 在低盐条件下的等温扩增 |
| CN108350492A (zh) * | 2015-11-05 | 2018-07-31 | 通用电气公司 | 连接酶辅助的核酸环化和扩增 |
| CN111334562A (zh) * | 2018-12-19 | 2020-06-26 | 合肥铼科生物科技有限公司 | 一种含有修饰引物的核酸扩增方法和试剂盒 |
| CN110195056A (zh) * | 2019-05-31 | 2019-09-03 | 汪雪 | 一种双引物及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2011253427A1 (en) | 2012-08-23 |
| CA2788821A1 (en) | 2011-11-17 |
| US20110195457A1 (en) | 2011-08-11 |
| EP2534268A4 (en) | 2013-09-04 |
| WO2011142861A9 (en) | 2012-03-15 |
| WO2011142861A2 (en) | 2011-11-17 |
| WO2011142861A3 (en) | 2012-02-02 |
| IN2012DN06299A (zh) | 2015-09-25 |
| BR112012019396A2 (pt) | 2017-06-06 |
| AU2011253427B2 (en) | 2015-06-25 |
| EP2534268A2 (en) | 2012-12-19 |
| JP2013518598A (ja) | 2013-05-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102753707A (zh) | 用随机引物和特异性引物的混合物等温扩增核酸 | |
| AU2013203624B2 (en) | Isothermal amplification of nucleic acid using a mixture of randomized primers and specific primers | |
| US8673567B2 (en) | Method and kit for nucleic acid sequence detection | |
| JP3085409B2 (ja) | 標的核酸配列の検出方法およびそのための試薬キット | |
| Karami et al. | A review of the current isothermal amplification techniques: applications, advantages and disadvantages | |
| EP1167524A1 (en) | Method for amplifying nucleic acid sequence | |
| CA2877368C (en) | Kit for isothermal dna amplification starting from an rna template | |
| CN105392901A (zh) | 连接酶-辅助的核酸环化和扩增 | |
| US20100273159A1 (en) | Nested Multiplex Amplification Method for Identification of Multiple Biological Entities | |
| JPH0723800A (ja) | 核酸の検出方法 | |
| CN104350159B (zh) | 制备在利用核酸聚合酶来检测核酸时使用的高精度核酸的方法 | |
| JP7420850B2 (ja) | 熱安定性ポリメラーゼ阻害剤組成物及び方法 | |
| US20170096694A1 (en) | Strand-invasion based dna amplification method | |
| CN114174535A (zh) | Crispr多靶标检测方法及其试剂盒 | |
| CN108350492A (zh) | 连接酶辅助的核酸环化和扩增 | |
| US11608522B2 (en) | Method of detecting target nucleic acid using rolling circle amplification and composition for detecting target nucleic acid | |
| WO2014081511A1 (en) | Method for preventing carry-over contamination in nucleic acid amplification reactions | |
| US20190203269A1 (en) | Tri-nucleotide rolling circle amplification | |
| CN108291252B (zh) | 稳定特定rna的通用方法 | |
| US9074248B1 (en) | Primers for helicase dependent amplification and their methods of use | |
| JP2004141105A (ja) | Dna合成反応を促進する方法、およびそのための組成物 | |
| AU2004205118B2 (en) | Method for amplifying nucleic acid sequence | |
| JP3145169B2 (ja) | 核酸検出法及びキット | |
| JP2011055787A (ja) | プライマー固定化基板による標的核酸の特異的検出法 | |
| KR20140073214A (ko) | 표적 핵산을 증폭 또는 분석하는 방법 및 표적 핵산을 증폭하기 위한 키트 또는 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C12 | Rejection of a patent application after its publication | ||
| RJ01 | Rejection of invention patent application after publication |
Application publication date: 20121024 |