CN1026231C - 从精馏馏出物中回收苯酚的方法 - Google Patents
从精馏馏出物中回收苯酚的方法 Download PDFInfo
- Publication number
- CN1026231C CN1026231C CN89107635A CN89107635A CN1026231C CN 1026231 C CN1026231 C CN 1026231C CN 89107635 A CN89107635 A CN 89107635A CN 89107635 A CN89107635 A CN 89107635A CN 1026231 C CN1026231 C CN 1026231C
- Authority
- CN
- China
- Prior art keywords
- phenol
- extraction
- weight
- referring
- phase
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C37/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom of a six-membered aromatic ring
- C07C37/68—Purification; separation; Use of additives, e.g. for stabilisation
- C07C37/70—Purification; separation; Use of additives, e.g. for stabilisation by physical treatment
- C07C37/72—Purification; separation; Use of additives, e.g. for stabilisation by physical treatment by liquid-liquid treatment
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
本发明涉及从含有各种有机夹杂物的精馏馏出物中回收苯酚的方法,该方法包括将所述馏出物经过萃取操作,使用的萃取溶剂是碱金属酚盐的水溶液。
Description
本发明涉及从含有各种有机夹杂物的精馏馏出物中回收苯酚的方法。
众所周知,分离氢过氧化枯烯制备苯酚时得到粗制苯酚,它必须用加氢蒸馏方法或萃取蒸馏法精馏,在这两种精馏方法中都使用了两个蒸馏塔。在第一个塔的顶部,分离夹杂物,它主要是纯苯酚中作为杂质存在的由异亚丙基丙酮,羟基丙酮、枯烯,α-甲基苯乙烯,2-甲基-苯并呋喃及其它有机物质组成的轻馏分;第二个塔中蒸馏出纯苯酚。由第一蒸馏塔顶得到的馏出物含有苯酚,其浓度(按重量)为20-90%一般为50-80%。所述馏出物中含的苯酚,众所周知,可用强碱(例如氢氧化钠)成盐的方法回收;形成的苯酚钠溶解并留在水相中。然后有H2SO4,H2CO3或其它的酸进行酸化,从而再次获得游离苯酚。为了使苯酚以盐的形式完全(或几乎完全)转移到水相,则需要在碱过量的情况下操作,并且使用的碱应是NaOH,过剩量一般是转化成苯酚钠的最高极限量的1%-30%范围内,因而碱的消耗量是相当大的。
欧洲专利申请NO.28522建议了另一方案,即用蒸汽蒸馏的方法从所述馏出物中回收苯酚,但在这种情况下同样涉及使用蒸汽的成本问题是不可忽视的。
原则上说,可以用水萃取方法来回收苯酚,这种方法可以避免消耗NaOH或蒸汽。但是,苯酚在水相和有机馏出物之间的分配系数需要往装置添加大量的水,这将导致增加能量和试剂的消耗因而成本增高,甚至比用NaOH进行成盐的方法回收的成本更高。
本申请人发现了一种用非常简单的方式从所述精馏的馏出物中回收苯酚的方法,并且其回收量与用NaOH成盐或蒸汽蒸馏法的回收量相当,但却完全避免NaOH或蒸汽的消耗。
概括说来,本发明涉及从含有(按重量)20-90%苯酚,其它还含各种夹杂物(具体说由异亚丙基丙酮,羟基丙酮,枯烯、α-甲基苯乙烯、2-甲基-苯并呋喃构成的杂质)的精馏馏出物中回收苯酚的方法,该方法包括使所述馏出物经受萃取操作,用作萃取溶剂的是碱金属酚盐,例如苯酚钠(C6H5ONa)的水溶液。
众所周知,通过分离氢过氧化枯烯合成苯酚的工厂中,有各种苯酚钠的水溶液,其总量远远大于待处理的馏出物;本申请人意外地发现上述苯酚钠溶液的萃取作用与用纯碱的普通萃取同样有效,因而可以特别便宜地进行上述苯酚回收。换句话说,本发明的优点在于有碱金属酚盐存在而导致水相与有机相之间苯酚的分配系数意想不到地增加,从而促进了苯酚在无机相中的溶解。
本方法中使用的苯酚钠水溶液除含所述苯酚盐外还含有少量的游离NaOH,在这种情况下将会发生少量的苯酚成盐作用,当然,还不会减少本发明的效益。
本发明可以各种方式完成,例如按以下方式进行特别有利。
-水溶剂中含有(按重量)1~15%,最好是5~15%的苯酚钠;
-萃取温度范围为室温~90℃,最好是40°~80℃;
-萃取溶剂量的范围是相对于每一份馏出物为1~15份,最好是5~15(按重量);
-连续进行萃取,反应剂为逆流形式装入由二个或更多的混合器以及二个或更多的滗析器所组成的装置,或可以得到许多萃取段而无需分离两种流体的装置中,最好保持有机相是连续相而水相是分散相;
-所述装置最好是管型并且可以用填充物,最好是不锈钢或其它能被有机相润湿的金属做成的填充物填满。
-所述填充物是RASCHIG环或PALL环。
以下实施例用于说明本发明,但并不限制本发明。
实施例1
“A”部分(萃取蒸馏)
按照图1,将滴定率为95%(按重量)左右且由分离氢过氧化枯烯(已经分离出丙酮,大部分枯烯以及高沸点杂质)所得到的粗制苯酚(1)装入萃取柱(C1),该萃取柱还供入来自柱C2底部的二甘醇(DEG)和苯酚(2)的混合物,几乎所有的杂质(3)(具体地说是α-甲基苯乙烯和其它烃类,羟基丙酮,异亚丙基丙酮,2-甲基苯并呋喃等)在柱C1的顶部被分离出,而同时由所述柱C1的底部得到苯酚和DEG的混合物(4),它被送入柱C2。由柱C2的顶部得到纯苯酚(5),同时从底部获得苯酚/DEG混合物,它被再循环至柱C1。两个柱的回流(图中未示出)由他们各自的端冷凝来完成。
“B”部分(从馏出物中回收苯酚)
柱C1的头馏产物(3)100g(按重量它含有60%苯酚,1%水和39%有机杂质)装入容积约为1000cm3,设有加热喷嘴,挡板和旋转式搅拌器(500r、p、m)的萃取槽(R)中。所述杂质主要包括异亚丙基丙酮,羟基丙酮、α-甲基苯乙烯和2-甲基-苯并呋喃。将来自另一苯酚合成厂区的含有15%(按重量)苯酚钠的水溶液(6)500g送入同一装置。温度升至50℃,搅拌15分钟,然后全部保持静止(一直保持在50℃)60分钟。得到有机相(较高)(7)和水相(较低)(8),结果示于表1,示出苯酚显著地转移到水相。
实施例2
使用含有10%(按重量)苯酚钠的水溶液作为萃取剂,重复实施例1。数据与结果示于表1。
实施例3
使用含有5%(按重量)苯酚钠的水溶液作为萃取剂,重复实施例1。
数据与结果示于表1。(表见文后)
实施例4(对比例)
用500g纯(去离子)水代替苯酚钠加入,重复实施例1。由表1可看出,转移到水相中的苯酚,与添加苯酚钠时所得到的数值相比较是很低的。
实施例5-6
改变萃取温度(分别为70°和90℃),重复实施例3,结果示于表2,表明即使温度稍微升高也
会大大地增加萃取率。(表见文后)
实施例7
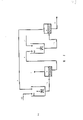
用图2示出的装置系统进行萃取,重复实施例3,所述系统包括两个混合槽(M1和M2)和两个滗析槽(D1和D2)。按照图2,将具有实施例1所述成分的柱C1头馏产物(3)100g/小时,与滗析槽(D1)中分离出来的水相(9)一起连续供入混合槽(M2)中。来自M2的溢流(10)送入滗析槽D2,在此处将含有全部萃取苯酚的水相流(8)和有机相流(11)分离,最后有机流(11)与含有5%(按重量)苯酚钠的水溶液(12)500g/小时加入混合槽M1中。从M1流出的液体(13)被送至分离槽D1,在该槽将水相流(9)和有机相流(7)分离,将分离出的水相流(9)送至混合槽M2。表2示出数据和结果,它清楚地表明,萃取结束时,留在39.5%有机相中的苯酚仅有9.7g,这意味着83.8%的起始苯酚被回收到水相中。
实施例8
在设有加热喷嘴且外直径为75mm、长度为9m(分成每一段为3m的三段)的管型萃取装置中装填陶瓷马鞍形填料,填料大小为3/8″(9.5mm)。向萃取槽底部连续供入51/小时实施例3的精馏馏出物,与501/小时(比率=10∶1)含苯酚钠(按重量)为5%的萃取水溶液逆流而行,通过热水循环将温度保持在50℃。水相流形成连续相,而有机相流形成分散相。数据与结果示于表3,由此表明,萃取结果时仅有5.1%(按重量)的苯酚留在有机相中,而96.4%的起始苯酚被回收在水相中。(表见文后)
实施例9
用大小为3/8″(9.5mm)的不锈钢(AISI316)RASCHIG环代替陶瓷马鞍形填料,重复实施例8。与实施例8相反,有机相形成连续相,而水相形成分散相。数据与结果示于表3,由此表明,萃取结束时仅有0.20%(按重量)苯酚留在有机相中,而99.9%的起始苯酚被回收在水相中。上述残余在杂质中的苯酚百分比(0.20%)低于普通技术在完成处理之后保留的苯酚量(0.30%),普通技术是指在设有旋转搅拌器的反应器中有30%(按重量)NaOH的溶液,成盐后剩余的NaOH量等于水相的0.6%(按重量)。意外地发现,在毫不消耗苛性钠的情况下得到十分好的效果。
实施例10
“A”部分(加氢蒸馏)
按照图3,将粗制苯酚(14)供入柱C3。夹杂物(15)的分离实际上在柱C3的顶部进行,同时在底部获得含有极少量高沸点杂质和水的苯酚流(16),并将它送至第二个柱C4,从这个柱的侧馏出物中得到纯酚(17),同时从其底部得到苯酚和高沸点产物(18)的混合物,它被再循环至柱C3的上游进行处理。由柱C4的顶部得到少量的酚馏出物和水(19),再将它送入柱C3。使第1个柱C3头馏产物(15)流到回流罐D,在此处杂质作为有机相(20)离开回流罐D,而水相(21)作为回流,与为补偿有机相(20)中损失而另外补充的水(22)一起再循环至上述柱C3的顶部。然后所述有机相(20)与苯酚钠溶液(23)接触,详细情况在“B”部分叙述。
“B”部分(从馏出物中回收苯酚)
从来自分离槽(D)并含有(按重量)60%苯酚、10%水30%有机夹杂物的有机相(20)100g装入类似于实施例1装置(R)的萃取装置中。所述夹杂物主要组成为异亚丙基丙酮,羟基丙酮、α-甲基苯乙烯、2-甲基-苯并呋喃。按实施例1操作,得到表4所示结果,示出苯酚明显地转移到水相。
实施例11
使用含(按重量)10%苯酚钠的水溶液作为萃取剂,重复实施例10。数据和结果示于表4。(表见文后)
实施例12
使用含(按重量)5%苯酚钠的水溶液作为萃取剂,重复实施例10。使用含(按重量)10%苯酚钠的水溶液作为萃取剂,重复实施例10。数据和结果示于表4。
实施例13-14
改变萃取温度(分别为70°和90°)重复实施例12,结果示于表5。(表见文后)
实施例15
用图2所示装置进行萃取,重复实施例12,该系统,如实施例7中所述包括2个混合槽(M1和M2)以及两个滗析槽(D1和D2)。数据与结果
示于表5。由此表明,结束萃取时,31g的有机相中仅留有0.8g苯酚,这意味着98.7%的起始苯酚被回收在水相中。
实施例16
在实施例8的管型萃取器的底部,连续装入51/小时实施例12的加氢蒸馏馏出物,与251/小时(体积比5∶1)含有(按重量)5%苯酚钠的萃取水溶液逆流而行,通过热水循环使温度保持在50℃。水相是连续相而有机相是分散相。数据与结果示于表6,由此表明,结束萃取时有机相中仅留下0.32%(重量)苯酚,99.8%的起始苯酚被回收在水相中。(表见文后)
实施例17
改用不锈钢(AISI316)RASCHIG环(3/8″)重复实施例16。与实施例16相反,有机相是连续相而水相是分散相。数据与结果示于表6,由此表明,结束反应时,留下的有机相少于(按重量)0.05%而大于99.97%的起始苯酚被回收在水相中。所述剩余的苯酚(在杂质物中低于0.05%)远远低于按普通技术(即在装有旋转搅拌器的萃取器中使用有30%(重量)NaOH的溶液,其量为成盐作用之后,NaOH的剩余量等于水相的0.6%(按重量)得到的数值。在不消耗苛性钠的情况下意外的获得了极好的结果。
实施例18和19
用PALL环代替RASCHIG环重复实施例9和17,获得类似的结果。
表1(重量%)
实施例 1 2 3 4(*)
温度(℃) 50 参看例1 参看例1 参看例1
精馏馏出物
数量(g) 100 参看例1 参看例1 参看例1
数 苯酚(%) 60 参看例1 参看例1 参看例1
据 H2O(%) 1 参看例1 参看例1 参看例1
其它(%) 39 参看例1 参看例1 参看例1
萃取溶液
数量(g) 500 参看例1 参看例1 参看例1
苯酚钠(%) 15 10 5 0
有机相:
数量(g) 44.0 48.0 55.0 61.2
苯酚(%) 29.6 35.6 41.8 47.7
H2O(%) 3.0 3.5 3.5 5.0
结 其它(%) 67.4 60.9 53.7 47.3
果 无机相
数量(g) 556.0 551.1 545.0 538.8
苯酚钠(%) 13.5 9.2 4.6 -
游离苯酚(%) 8.45 7.7 6.8 5.7
萃取率(%) 78.3 70.7 61.8 51.2
注(*)对比例
表2(重量%)
实施例 5 6 7
温度(℃) 70 90 50
精馏馏出物
数量(g) 100 参看例5 参看例5
数 苯酚(%) 60 参看例1 参看例1
据 H2O(%) 1 参看例5 参看例5
其它(%) 39 参看例5 参看例5
萃取溶液
数量(g) 500 参看例5 参看例5
苯酚钠(%) 5 参看例5 参看例5
有机相:
数量(g) 41.4 36.2 39.5
苯酚(%) 26.4 17.2 24.6
H2O(%) 2.6 1.5 2.0
结 其它(%) 71.0 81.3 73.4
果 无机相
数量(g) 558.6 563.8 560.5
苯酚钠(%) 4.5 4.4 4.5
游离苯酚(%) 8.8 9.5 9.0
萃取率(%) 81.9 89.3 83.8
表3(重量%)
实施例 8 9
温度(℃) 50 50
精馏馏出物
数量(/1小时) 5 参看例8
苯酚(%) 60 参看例8
数 H2O(%) 1 参看例8
据 其它(%) 39 参看例8
萃取溶液
数量(1/小时) 50 参看例8
苯酚钠(%) 5 参看例8
有机相:
数量(1/小时) 2.4 2.2
苯酚(%) 5.1 0.20
H2O(%) 1.0 1.0
结 其它(%) 93.9 98.8
果 无机相
数量(1/小时) 52.6 52.7
苯酚钠(%) 4.75 4.7
游离苯酚(%) 5.40 5.6
萃取率(%) 96.4 99.9
表4(重量%)
实施例 10 11 12
温度(℃) 50 参看例10 参看例10
精馏馏出物
数量(g) 100 参看例10 参看例10
苯酚(%) 60 参看例10 参看例10
数 H2O(%) 10 参看例10 参看例10
据 其它(%) 30 参看例10 参看例10
萃取溶液
数量(g) 500 参看例10 参看例10
苯酚钠(%) 15 10 5
有机相:
数量(g) 35.3 34.6 37.0
苯酚(%) 14.9 16.8 18.8
H2O(%) 1.5 1.5 2.0
结 其它(%) 83.6 81.7 79.2
果 无机相
数量(g) 564.7 565.4 563.0
苯酚钠(%) 13.3 8.8 4.4
游离苯酚(%) 9.7 9.6 9.4
萃取率(%) 91.3 90.5 88.2
表5(重量%)
实施例 13 14 15
79 90 93
温F))(g)
苯酚(%) 100 参看例13 参看例13
数 H2O(%) 60 参看例13 参看例13
据 其它(%) 10 参看例13 参看例13
萃取溶液 30 参看例13 参看例13
数量(g)
苯酚钠(%) 500 参看例13 参看例13
5 参看例13 参看例13
有机相:
数量(g) 33.2 31.6 31.0
苯酚(%) 9.5 5.1 2.6
H2O(%) 1.0 0.5 0.6
结 其它(%) 89.5 94.4 96.8
果 无机相
数量(g) 556.8 568.4 569.0
苯酚钠(%) 4.4 4.4 4.4
游离苯酚(%) 10.0 10.3 10.4
萃取率(%) 92.8 97.6 98.7
表6(重量%)
实施例 16 17
温度(℃) 90 50
精馏馏出物
数量(/1小时) 5 参看例16
数 苯酚(%) 60 参看例16
据 H2O(%) 10 参看例16
其它(%) 30 参看例16
萃取溶液
数量(1/小时) 25 参看例16
苯酚钠(%) 5 参看例16
数量(1/小时) 1.7 1.7
苯酚(%) 0.32 <0.05
H2O(%) 1.0 1.0
结 其它(%) 98.7 99.0
果 无机相
数量(1/小时) 28.2 28.2
苯酚钠(%) 4.4 4.4
游离苯酚(%) 10.4 10.4
萃取率(%) 99.8 99.97
Claims (18)
1、从含有20-90%(重量)苯酚及其它各种有机夹杂物的精馏馏出物中回收苯酚的方法,该方法包括使上述馏出物经过萃取操作,使用的萃取剂是碱金属酚盐的水溶液。
2、根据权利要求1所述之方法,其中所述酚盐是苯酚钠。
3、根据权利要求2所述之方法,其中所述水溶液是含1-15%(按重量)的苯酚钠。
4、根据权利要求3的方法,其中所述的水溶液是含5-15%(按重量)的苯酚钠。
5、根据权利要求1所述之方法,其中萃取温度范围为室温至90℃。
6、根据权利要求5的方法,其中萃取温度范围为40-80℃。
7、根据权利要求1所述之方法,其中萃取溶剂量的范围为1~15份(按每份馏出物的重量)。
8、根据权利要求7的方法,其中萃取溶剂量的范围为5-15份(按每份馏出物的重量)。
9、根据权利要求1-8所述之方法,其中萃取作用是连续进行,料流是逆向装入由两个或更多个混合槽以及两个或更多个滗析槽所组成的装置系统中。
10、根据权利要求1-8所述之方法,其中是在可以获得许多萃取段的装置中进行连续逆流萃取,无需两相流的物理分离。
11、根据权利要求10所述之方法,其中有机相是连续相,而水相是分散相。
12、根据权利要求10所述之方法,其中萃取作用是在装有填充材料的管型装置中进行。
13、根据权利要求12所述之方法,其中填充材料是不锈钢或其它最好被有机相润湿的材料。
14、从含有20-90%(按重量)苯酚及其它主要为异亚丙基丙酮,羟基丙酮,枯烯,α-甲基苯乙烯和2-甲基-苯并呋喃的挥发性有机夹杂物的精馏馏出物中回收苯酚的方法,其特征在于,将所述馏出物经受与5-15%(按重量)的苯酚钠水溶液,在操作温度为40-80℃的萃取作用,其特征还在于,a)水溶液的量相对于每一份馏出物为5-10份(按重量);
b)有机相是连续相,而水相是分散相;
c)萃取作用是在装有不锈钢填充体的管型装置中连续且逆流进行。
15、根据权利要求14的方法,其中精馏馏出物中含的苯酚钠为50-80%(按重量)。
16、根据权利要求13所述之方法,其中所述填充体是Raschig环或Pall环。
17、根据权利要求2所述之方法,其中所述溶液除含酚钠外,还含有游离苛性钠(NaOH),游离苛性钠的量低于全部苯酚成盐所需的量。
18、根据权利要点17的方法,其中游离苛性钠的量为低于全部苯酚成盐所需量的50%。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IT8822823A IT1227668B (it) | 1988-12-02 | 1988-12-02 | Processo per il recupero del fenolo da uno spurgo di rettifica |
| IT22823A/88 | 1988-12-02 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1043119A CN1043119A (zh) | 1990-06-20 |
| CN1026231C true CN1026231C (zh) | 1994-10-19 |
Family
ID=11200858
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN89107635A Expired - Fee Related CN1026231C (zh) | 1988-12-02 | 1989-09-29 | 从精馏馏出物中回收苯酚的方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US4973766A (zh) |
| EP (1) | EP0372685B1 (zh) |
| CN (1) | CN1026231C (zh) |
| AT (1) | ATE123750T1 (zh) |
| AU (1) | AU617527B2 (zh) |
| BR (1) | BR8904729A (zh) |
| CA (1) | CA1322763C (zh) |
| DE (1) | DE68923068T2 (zh) |
| ES (1) | ES2074467T3 (zh) |
| IT (1) | IT1227668B (zh) |
| ZA (1) | ZA896790B (zh) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5338453A (en) * | 1992-07-27 | 1994-08-16 | The Dow Chemical Company | Recovery of phenols from hydrocarbon mixtures |
| IT1271279B (it) | 1994-12-15 | 1997-05-27 | Enichem Spa | Processo per il recupero di fenolo da un flusso acquoso contenente na2 so4 |
| ITMI980864A1 (it) * | 1998-04-23 | 1999-10-23 | Enichem Spa | Processo per l'estrazione dei sali contenuti nel prodotto scisso neutralizzato ottenuto nella preparazione di fenolo via ossidazione |
| US6066767A (en) * | 1999-02-10 | 2000-05-23 | Illa International, Llc | Method of purifying cumene hydroperoxide decomposition products from hydroxyacetone and from other carbonyls |
| US6965056B1 (en) * | 1999-05-03 | 2005-11-15 | Shell Oil Company | Removal of salts in the manufacture of phenolic compound |
| US6667178B2 (en) | 2001-05-07 | 2003-12-23 | Sunoco, Inc. (R&M) | Optimization of caustic usage |
| US6576798B1 (en) | 2001-11-29 | 2003-06-10 | General Electric Company | Method and system for purifying cumene hydroperoxide cleavage products |
| US6573408B1 (en) | 2001-11-29 | 2003-06-03 | General Electric Company | System and method for purifying cumene hydroperoxide cleavage products |
| JP2005526718A (ja) * | 2002-02-08 | 2005-09-08 | ゼネラル・エレクトリック・カンパニイ | フェノールの精製方法及び触媒 |
| RU2217409C2 (ru) * | 2002-02-08 | 2003-11-27 | Общество с ограниченной ответственностью "Петрофенол" | Способ и катализатор получения паракумилфенола |
| RU2217408C2 (ru) * | 2002-02-08 | 2003-11-27 | Общество с ограниченной ответственностью "Петрофенол" | Способ и катализатор очистки фенола |
| JP3931714B2 (ja) * | 2002-03-27 | 2007-06-20 | 住友化学株式会社 | タールの処理方法 |
| WO2008140948A1 (en) * | 2007-05-09 | 2008-11-20 | Stone & Webster, Inc. | Bpa process improvement |
| CN105669388B (zh) * | 2016-03-08 | 2018-09-28 | 江苏常青树新材料科技有限公司 | 一种亚磷酸一苯二异辛酯生产装置上苯酚与异辛醇混合物的分离回收工艺 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2200370A (en) * | 1937-07-26 | 1940-05-14 | Koppers Co Inc | Process for the recovery of pure phenols or phenolates from gas liquor or the like |
| GB674754A (en) * | 1948-08-11 | 1952-07-02 | Carbide & Carbon Chem Corp | Process for recovery of tar acids and bases from hydrocarbon oils |
| DE1094758B (de) * | 1957-07-24 | 1960-12-15 | Metallgesellschaft Ag | Verfahren zur Gewinnung von neutraloelfreien und lichtbestaendigen Phenolen aus phenolhaltigen OElen oder Rohphenolen |
| DE1101435B (de) * | 1959-04-02 | 1961-03-09 | Metallgesellschaft Ag | Verfahren zur Gewinnung von neutraloelfreien und lichtbestaendigen Phenolen |
| US4262150A (en) * | 1979-12-31 | 1981-04-14 | Uop Inc. | Process for the recovery of phenol from a reaction mixture resulting from the acid cleavage of cumene hydroperoxide |
| US4262151A (en) * | 1979-12-31 | 1981-04-14 | Uop Inc. | Process for the recovery of phenol from a reaction mixture resulting from the acid cleavage of cumene hydroperoxide |
-
1988
- 1988-12-02 IT IT8822823A patent/IT1227668B/it active
-
1989
- 1989-09-05 ZA ZA896790A patent/ZA896790B/xx unknown
- 1989-09-11 DE DE68923068T patent/DE68923068T2/de not_active Expired - Lifetime
- 1989-09-11 AT AT89309183T patent/ATE123750T1/de not_active IP Right Cessation
- 1989-09-11 EP EP89309183A patent/EP0372685B1/en not_active Expired - Lifetime
- 1989-09-11 ES ES89309183T patent/ES2074467T3/es not_active Expired - Lifetime
- 1989-09-14 CA CA000611490A patent/CA1322763C/en not_active Expired - Fee Related
- 1989-09-15 AU AU41438/89A patent/AU617527B2/en not_active Ceased
- 1989-09-20 BR BR898904729A patent/BR8904729A/pt not_active IP Right Cessation
- 1989-09-29 CN CN89107635A patent/CN1026231C/zh not_active Expired - Fee Related
- 1989-10-23 US US07/425,106 patent/US4973766A/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| CA1322763C (en) | 1993-10-05 |
| EP0372685A2 (en) | 1990-06-13 |
| IT1227668B (it) | 1991-04-23 |
| BR8904729A (pt) | 1991-03-26 |
| US4973766A (en) | 1990-11-27 |
| EP0372685B1 (en) | 1995-06-14 |
| DE68923068T2 (de) | 1995-10-19 |
| AU4143889A (en) | 1990-06-07 |
| IT8822823A0 (it) | 1988-12-02 |
| ES2074467T3 (es) | 1995-09-16 |
| EP0372685A3 (en) | 1991-09-25 |
| ZA896790B (en) | 1990-06-27 |
| DE68923068D1 (de) | 1995-07-20 |
| CN1043119A (zh) | 1990-06-20 |
| ATE123750T1 (de) | 1995-06-15 |
| AU617527B2 (en) | 1991-11-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1026231C (zh) | 从精馏馏出物中回收苯酚的方法 | |
| CN1022560C (zh) | 高纯度双酚a的制造方法 | |
| CN1974511A (zh) | 用于生产有机化合物的方法 | |
| CN1150155C (zh) | 高纯乙酸的生产方法 | |
| CN1230410C (zh) | 生产和提纯(甲基)丙烯酸的连续法 | |
| CN1993308A (zh) | 在金属盐存在下由多羟基脂肪烃和/或其酯用于生产氯代醇的方法 | |
| CN1413178A (zh) | 从聚酯废料中分离和回收对苯二甲酸二甲酯和乙二醇的方法 | |
| CN1061222A (zh) | 由乳酸水料脱水生产丙交酯 | |
| CN1128986A (zh) | D-手性肌醇的制造方法 | |
| CN1025327C (zh) | 芳香羟基羧酸的制备方法 | |
| CN1519225A (zh) | 高纯度三链烷醇胺的制备方法 | |
| CN1553889A (zh) | (甲基)丙烯酸酯的制备方法 | |
| CN1263725C (zh) | (甲基)丙烯酸的精制方法 | |
| CN1837220A (zh) | 环硼氮烷化合物的制备方法 | |
| CN1240417A (zh) | 由异丙苯制备苯酚和丙酮的改良方法 | |
| CN1235867C (zh) | 芳香族化合物的制备方法 | |
| CN1622930A (zh) | (甲基)丙烯酸类的制造方法 | |
| CN1185201C (zh) | 氧化丙烯和/或丙烯醛所得到的丙烯酸的纯化方法 | |
| CN101033194A (zh) | 高纯度三链烷醇胺的制备方法 | |
| CN100349854C (zh) | (甲基)丙烯酸酯的制备方法 | |
| CN1249002C (zh) | 苯酚与苯酚衍生物工业中二元酚的分离和提纯方法及装置 | |
| CN1145620C (zh) | 制备γ丁内酯和四氢呋喃的方法 | |
| CN100338006C (zh) | α-、β-或γ-取代的羧酸的提纯方法 | |
| CN1532179A (zh) | 丙烯酸类的精制装置和方法 | |
| CN1305832C (zh) | (甲基)丙烯酸的提纯方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C06 | Publication | ||
| PB01 | Publication | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C15 | Extension of patent right duration from 15 to 20 years for appl. with date before 31.12.1992 and still valid on 11.12.2001 (patent law change 1993) | ||
| OR01 | Other related matters | ||
| C19 | Lapse of patent right due to non-payment of the annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |