CN100522184C - 具有抗肿瘤和抗毒活性的提取物 - Google Patents
具有抗肿瘤和抗毒活性的提取物 Download PDFInfo
- Publication number
- CN100522184C CN100522184C CNB2003801031172A CN200380103117A CN100522184C CN 100522184 C CN100522184 C CN 100522184C CN B2003801031172 A CNB2003801031172 A CN B2003801031172A CN 200380103117 A CN200380103117 A CN 200380103117A CN 100522184 C CN100522184 C CN 100522184C
- Authority
- CN
- China
- Prior art keywords
- extract
- present
- cell
- filtrate
- therapeutic compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/185—Magnoliopsida (dicotyledons)
- A61K36/27—Asclepiadaceae (Milkweed family), e.g. hoya
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/02—Antidotes
Abstract
本发明涉及从植物白花牛角瓜中提取的具有药理活性、特别是具有抗毒活性的提取物以及从中分离的活性化合物。另外,本发明还涉及获得所述提取物的方法。本发明还涉及用于肿瘤治疗的药物组合物或产品,该组合物或产品含有有效量的所述提取物或其活性化合物、治疗性化合物,还可以选择添加药学上可接受的载体。
Description
发明领域
本发明涉及医学领域。本发明的第一方面涉及从植物白花牛角瓜(Calotropisprocera)中提取的具有药理活性的、特别是具有抗肿瘤活性和/或抗毒活性的提取物以及从中分离的活性化合物。本发明的第二方面涉及获得所述提取物的方法。本发明的第三方面还涉及用于癌症治疗的药物组合物,该组合物包含有效量的所述提取物或其活性化合物。本发明的第四方面涉及所述提取物或其活性化合物作为药物的应用以及所述提取物或其活性化合物在制备抗癌药中的应用。
发明背景
当某些组织发生基因组突变干扰了细胞周期动力学使细胞增殖过度或细胞死亡减少时就会产生肿瘤。这种干扰可导致发生基因组突变的细胞群出现无限制地生长。这种突变细胞群中的某些细胞可转化成具有血管形成表型的细胞,这些细胞可作为健康组织内内皮细胞的补充,导致恶性肿瘤组织持续生长。随后,某些细胞从恶性肿瘤组织内迁移出来并增殖成新的组织,其迁移的途径主要依靠血管或淋巴管。这一过程也被称为转移过程。
目前在医院中用于治疗癌症病人的大多数药物对癌细胞动力学特性,即对细胞增殖的直接靶向性或高或低。这种抗肿瘤药物的作用机制基本上都是通过作用于细胞动力学来破坏肿瘤细胞的增殖。这些药物包括烷化剂、嵌入剂、抗代谢药物等,其中大多数是靶向于DNA或调节DNA复制和延伸过程的酶。这些药物可攻击DNA。
这些药物的一个主要缺点是没有选择性,即这些药物不能区分正常细胞和恶性细胞。其作用原理基于这样一个事实:快速增殖的细胞如癌细胞与增殖速度慢的细胞如正常细胞相比,其DNA对这类药物更敏感。但是,快速生长的肿瘤并不总是具有高水平细胞增殖的肿瘤。快速生长的肿瘤也可能包括细胞增殖水平比其来源的正常细胞群增殖水平还低的肿瘤,对于这些类型的快速生长的肿瘤来说,上述药物是无效的。
另外,通过改变细胞动力学方式治疗肿瘤的绝大多数药物都具有毒性,甚至毒性还很高,即对正常细胞、组织和器官有许多有害的副作用,这就使其用于临床时给每个患者使用的剂量相对较低。另外,为了达到显著的抗癌疗效就需要联合使用几种这样的化合物进行联合化疗。显然,这种抗癌药联合化疗会增加治疗的毒性效应,也限制了其使用的范围。
现在发现某些天然来源的抗癌药,如微管蛋白抑制剂化合物,其作用机制不是作用于细胞动力学。这些药物的目的在于阻止癌细胞的迁移,这些癌细胞从原发肿瘤中逃逸出来首先侵入到临近组织形成转移瘤。但是,到目前为止,已知这种类型的化合物也具有很大的毒副作用,因此也限制了其用于长期治疗。
因此,在本领域中急需找到至少能克服上述药物的某些缺点的抗癌药。因此,本发明的一个主要目的就是提供这样的抗癌药。具体来说,本发明的目的就在于提供副作用很低的抗癌药。
发明概述
本发明的一个实施方案是白花牛角瓜植物的提取物,其特征在于,所述提取物具有药理活性,特别是抗毒活性。
本发明的另外一个实施方案是利用提取方法获得上述提取物,该方法包括如下步骤:
a)在脂肪族醇中提取所述白花牛角瓜植物的起始原料,所述起始原料选自果实、地上部分、地下部分或其混合物,利用所述醇溶解起始原料获得所述原料的脂肪族醇悬液,搅拌所述悬液,用多孔玻璃过滤所述悬液从而得到第一滤液和第一固体组分;
b)用脂肪族醇提取所述第一固体组分从而得到第二滤液和第二固体组分;
c)混合所述第一滤液和第二滤液得到混合滤液,在真空下蒸发所述混合滤液从而得到所述提取物。
本发明的另外一个实施方案是利用提取方法获得上述提取物,该方法包括如下步骤:
a)研磨白花牛角瓜的叶片、茎、皮和根获得植物精粉,
b)在索氏抽提器中用二氯甲烷提取步骤a)的粉末至少6、12、18小时,优选24小时,
c)倾析步骤b)的二氯甲烷,过滤后蒸发滤液,得到胶状物。
本发明的另外一个实施方案是利用提取方法获得上述提取物,该方法包括如下步骤:
a)研磨白花牛角瓜的叶片、茎、皮和根获得植物精粉,
b)在索氏抽提器中用二氯甲烷提取步骤a)的粉末至少6、12、18小时,优选24小时,
c)倾析步骤b)的二氯甲烷,过滤后蒸发滤液,得到胶状物,
d)在索氏抽提器中用甲醇提取步骤c)的残留物至少6、12、18小时,优选24小时,
e)倾析步骤d)的甲醇,过滤后蒸发滤液,得到胶状物,
f)以二氯甲烷-甲醇为溶剂利用快速硅胶柱层析处理步骤e)的胶状物,以及
g)收集第一组分,蒸发所述组分得到含有生物活性组分的胶状物。
本发明的另外一个实施方案是利用提取方法获得上述提取物,该方法包括如下步骤:
a)研磨白花牛角瓜的叶片、茎、皮和根获得植物精粉,
b)在索氏抽提器中用二氯甲烷提取步骤a)的粉末至少6、12、18小时,优选24小时,
c)倾析步骤b)的二氯甲烷,过滤后蒸发滤液,得到胶状物,
d)在索氏抽提器中用甲醇提取步骤c)的残留物至少6、12、18小时,优选24小时,
e)倾析步骤d)的甲醇,过滤后蒸发滤液,得到胶状物,
f)以二氯甲烷-甲醇为溶剂利用快速硅胶柱层析处理步骤e)的胶状物,
g)收集含有生物活性组分的第一组分,
h)以己烷-丙酮为溶剂用快速硅胶柱层析处理步骤g)的浓缩组分得到两个组分,以及
i)步骤h)后用甲醇洗涤层析柱以得到含有生物活性成分的第三组分。
本发明的另外一个实施方案是一种组合物,其中包含:
—上述白花牛角瓜提取物,和
—至少一种治疗性化合物和/或物理疗法,其中的化合物和/或物理疗法对正常的非癌细胞、组织或器官的具有一定毒副作用。
本发明的另外一个实施方案是一种产品,其中包含:
—上述白花牛角瓜提取物,和
—至少一种治疗性化合物和/或物理疗法的产品,其中的化合物和/或物理疗法对正常的非癌细胞、组织或器官具有一定毒副作用,
组合物二者可同时、分别或依次给予患者。
本发明的另外一个实施方案是上述的组合物或上述的产品,其中,所述提取物含有至少两种选自如下一组的活性化合物:马利筋苷、异牛角瓜甙(calactin)、弗汝沙林(vorusharin)、牛角瓜苷、牛角瓜苷元、乌沙苷元、卡洛托星(calotoxin)、乌沙林(usharin)和乌沙利定(usharidin)。
本发明的另外一个实施方案是上述的组合物或上述的产品,其中,所述提取物至少还含有表1中所列的一种化合物。
本发明的另外一个实施方案是上述的组合物或上述的产品,其中的提取物:治疗性化合物的重量比为0.001:1-1000:1。
本发明的另外一个实施方案是上述组合物或上述产品作为药物的应用。
本发明的另外一个实施方案是上述组合物或上述产品作为肿瘤治疗药物的应用。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述肿瘤选自:乳腺癌、淋巴瘤、肉瘤、胰腺癌、黑色素瘤、结肠癌、胶质瘤、非小细胞肺癌、小细胞肺癌、皮肤癌、骨癌、卵巢癌、CNS癌、膀胱癌、头颈癌、前列腺癌、肝癌、血癌。
本发明的另外一个实施方案是上述组合物或上述产品,其中还包含一种或多种其他的治疗性化合物。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述治疗性化合物是抗癌药。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述治疗性化合物选自:阿霉素、爱克兰(alkeran)、阿糖胞嘧啶、博来霉素、biCNU(卡氮芥)、白消安、CCNU(环已亚硝脲)、卡铂、顺铂、环磷酰胺、癌得星(cytoxan)、柔红霉素、DTIC(达卡巴嗪)、5-FU(5-氟尿嘧啶)、氟达拉滨、吉西他滨(注射用盐酸吉西他滨)、赫赛汀(herceptin)、六甲密胺、羟脲、伊达比星、异环磷酰胺、依立替康(盐酸伊立替康和山梨醇注射剂,CPT-11)、克拉立平、氨甲蝶呤、光辉霉素、丝裂霉素、二羟基蒽酮、武活龙、诺维本、氮芥、奥沙利铂、美罗华(rituxan)、STI-571(甲磺酸伊马替尼)、链脲菌素、紫杉醇、泰索帝、托泊替康(盐酸托泊替康针剂)、硫酸长春碱、长春新碱、VP-16(依托泊甙)、希罗达(卡培他滨)或泽娃灵(zevelin)。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述治疗性化合物选自:阿霉酮(adriamycine)、长春新碱、喜树碱和奥沙利铂。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述治疗性化合物是细胞毒性抗体或其片段。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述治疗性化合物是细胞毒性激素或其片段。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述治疗性化合物是细胞毒性肽或其片段。
本发明的另外一个实施方案是上述组合物,该组合物还包含药学上可接受的载体,或者上述产品,其中,组合物和/或治疗性化合物还包含药学上可接受的载体。
本发明的另外一个实施方案是上述白花牛角瓜提取物在制备减轻一种或多种治疗性化合物的副作用的药物中的应用。
本发明的另外一个实施方案是上述白花牛角瓜提取物在制备增加一种或多种治疗性化合物使用剂量的药物中的应用。
本发明的另外一个实施方案是上述提取物的用途,其中,所述治疗性化合物具有抗癌活性。
本发明的另外一个实施方案是上述提取物的用途,其中,所述治疗性化合物选自::阿霉素、爱克兰、阿糖胞嘧啶、博来霉素、biCNU、白消安、CCNU、卡铂、顺铂、环磷酰胺、癌得星、柔红霉素、DTIC、5-FU、氟达拉滨、吉西他滨(注射用盐酸吉西他滨)、赫赛汀、六甲密胺、羟脲、伊达比星、异环磷酰胺、依立替康(盐酸伊立替康和山梨醇注射剂,CPT-11)、克拉立平、氨甲蝶呤、光辉霉素、丝裂霉素、二羟基蒽酮、武活龙、诺维本、氮芥、奥沙利铂、美罗华、STI-571、链脲菌素、紫杉醇、泰索帝、托泊替康(盐酸托泊替康针剂)、硫酸长春碱、长春新碱、VP-16、希罗达(卡培他滨)或泽娃灵。
本发明的另外一个实施方案是上述提取物的用途,其中,所述治疗性化合物选自:阿霉酮、长春新碱、喜树碱和奥沙利铂。
本发明的另外一个实施方案是上述提取物的用途,其中,所述治疗性化合物是细胞毒性抗体或其片段。
本发明的另外一个实施方案是上述提取物的用途,其中,所述治疗性化合物是细胞毒性激素或其片段。
本发明的另外一个实施方案是上述提取物的用途,其中,所述治疗性化合物是细胞毒性肽或其片段。
本发明的另外一个实施方案是上述提取物的用途,其中,所述治疗性化合物是治疗性辐射。
本发明的另外一个实施方案是上述提取物的用途,其中,所述提取物含有至少两种选自如下一组的活性化合物:马利筋苷、异牛角瓜甙、弗汝沙林、牛角瓜苷、牛角瓜苷元、乌沙苷元、卡洛托星、乌沙林和乌沙利定。
本发明的另外一个实施方案是上述提取物的用途,其中,所述提取物至少还含有表1中所列的一种化合物。
本发明的另外一个实施方案是上述提取物的用途,其中,所述提取物在给予所述治疗性化合物前给药。
本发明的另外一个实施方案是上述提取物的用途,其中,所述提取物在给予所述治疗性化合物后给药。
本发明的另外一个实施方案是上述提取物的用途,其中,所述提取物在给予所述治疗性化合物的同时给药。
本发明的另外一个实施方案是上述提取物的用途,其中的提取物:治疗性化合物的重量比为0.001:1-1000:1。
本发明的另外一个实施方案是获得含有生物活性成分的提取物的提取方法,该方法包括如下步骤:
a)在脂肪族醇中提取所述白花牛角瓜植物的起始原料,所述起始原料选自果实、地上部分、地下部分或其混合物,利用所述醇溶解起始原料获得所述原料的脂肪族醇悬液,搅拌所述悬液;用多孔玻璃过滤所述悬液从而得到第一滤液和第一固体组分;
b)用脂肪族醇提取所述第一固体组分从而得到第二滤液和第二固体组分;
c)混合所述第一滤液和第二滤液得到混合滤液;以及
d)在真空下蒸发所述混合滤液从而得到所述提取物。
本发明的另外一个实施方案是获得含有生物活性成分的提取物的提取方法,其中的活性成分存在于白花牛角瓜的叶片、茎、皮和根内,该方法包括如下步骤:
a)研磨起始原料白花牛角瓜的叶片、茎、皮和根获得植物精粉,
b)在索氏抽提器中用二氯甲烷提取步骤a)的粉末至少6、12、18小时,优选24小时,
c)倾析步骤b)的二氯甲烷,过滤后蒸发滤液,得到胶状物。
本发明的另外一个实施方案是上面所述的提取方法,该方法还包括如下步骤:
d)在索氏抽提器中用甲醇提取步骤c)的残留物至少6、12、18小时,优选24小时,
e)倾析步骤d)的甲醇,过滤后蒸发滤液,得到胶状物,
f)以二氯甲烷-甲醇为溶剂利用快速硅胶柱层析处理步骤e)的胶状物,以及
g)收集含有生物活性成分的第一组分,蒸发洗脱液得到所述提取物。
本发明的另外一个实施方案是上面所述的提取方法,该方法还包括如下步骤:
h)以己烷-丙酮为溶剂用快速硅胶柱层析处理步骤g)的组分得到两个组分,
i)步骤h)后用甲醇洗涤层析柱以得到含有生物活性成分的第三组分。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤b)在20-80℃下进行。
本发明的另外一个实施方案是上面所述的提取方法,其中,所述步骤b)重复1-5次。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤b)的持续时间为4-48小时。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤d)的固相是硅胶。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤d)的洗脱液是二元洗脱液,洗脱液中两种组分的比例在100:0到0:100之间。
本发明的另外一个实施方案是上面所述的提取方法,其中,所述二元洗脱液的组分包含一种醇溶剂和一种非极性溶剂。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤e)在20-50℃下进行。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤f)的固相是硅胶。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤f)的洗脱液是二元洗脱液,洗脱液中两种组分的比例在100:0到0:100之间。
本发明的另外一个实施方案是上面所述的提取方法,其中,所述二元洗脱液的组分包含一种醇溶剂和一种非极性溶剂。
本发明的另外一个实施方案是上面所述的提取方法,其中二元洗脱液两种组分—非极性组分:极性组分之比为50:50到100:0。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤h)的溶剂是甲醇。
本发明的另外一个实施方案是上面所述的提取方法,其中,步骤e)在20-50℃下进行。
本发明的另外一个实施方案是通过上述提取方法所分离的活性提取物。
本发明的另外一个实施方案是上述活性提取物作为药物的应用。
本发明的另外一个实施方案是上述活性提取物作为肿瘤治疗药物的应用。
本发明的另外一个实施方案是一种治疗肿瘤的方法,该方法包括给予需要这种治疗的患者以上面所述的药物组合物或上面所述的产品。
本发明的另外一个实施方案是上述的方法,其中,所述肿瘤选自:乳腺癌、淋巴瘤、肉瘤、胰腺癌、黑色素瘤、结肠癌、胶质瘤、非小细胞肺癌、小细胞肺癌、皮肤癌、骨癌、卵巢癌、CNS癌、肾癌、膀胱癌、头颈癌、前列腺癌、肝癌、血癌。
本发明的另外一个实施方案是上述组合物或上述产品,其中,所述治疗性化合物是辐射。
本发明的另外一个实施方案是试剂盒,该试剂盒包括上述白花牛角瓜提取物以及装有治疗性化合物的容器。
发明详述
本发明涉及白花牛角瓜植物的提取物。在第一实施方案中,本发明涉及植物白花牛角瓜的具有药理活性的提取物,特别是具有抗肿瘤活性和/或抗毒活性的提取物。令人惊喜的是,本发明的提取物中至少有一个既有抗肿瘤活性,又有抗毒活性。
本发明所用的术语“抗肿瘤活性”是指至少一种提取物或从提取物中分离的化合物所具有的体外及体内抗肿瘤效应。抗肿瘤效应主要包括而不限于细胞生长的急剧下降及促凋亡效应。更重要的是,本发明的提取物对多种类型的肿瘤都具有抗肿瘤活性,如乳腺癌、黑色素瘤或淋巴瘤以及其他肿瘤。
本发明的提取物的另外一个特征是其抗毒活性。术语“抗毒活性”是指本发明的提取物或从提取物中分离的化合物所具有的减弱或反转治疗性化合物或治疗方案的效应的能力。本文所用的术语“治疗性化合物”是指对正常的(即非癌)细胞、组织或器官能产生一定毒副作用的化合物。因此术语治疗性化合物也包括用于治疗特定疾病但是具有一定毒副作用的化合物、药物、物理疗法或治疗方案。这种副作用是本领域技术人员所熟知的,包括而不限于疲倦、恶心、呕吐、褥疮、口疮、干性皮肤、皮肤过敏、脱发、红细胞和白细胞数降低。这种治疗性化合物包括而不限于化疗药、辐射、抗体和激素。
本发明可用的治疗性化合物包括用于化疗的或具有细胞毒性的那些化合物,其中包括而不限于阿霉素、爱克兰、阿糖胞嘧啶、博来霉素、biCNU、白消安、CCNU、卡铂、顺铂、环磷酰胺、癌得星、柔红霉素、DTIC、5-FU、氟达拉滨、吉西他滨(注射用盐酸吉西他滨)、赫赛汀、六甲密胺、羟脲、伊达比星、异环磷酰胺、依立替康(盐酸伊立替康和山梨醇注射剂,CPT-11)、克拉立平、氨甲蝶呤、光辉霉素、丝裂霉素、二羟基蒽酮、武活龙、诺维本、氮芥、奥沙利铂、美罗华、STI-571、链脲菌素、紫杉醇、泰索帝、托泊替康(盐酸托泊替康针剂)、硫酸长春碱、长春新碱、VP-16、希罗达(卡培他滨)或泽娃灵。
在本发明的另外一个方面,治疗性药物包含一种或多种来源于本发明的提取物的抗癌药。本发明中具有潜在抗癌活性的化合物是指从白花牛角瓜中提取的任何化合物,如马利筋苷、异牛角瓜甙、弗汝沙林、牛角瓜苷、牛角瓜苷元、乌沙苷元、卡洛托星、乌沙林和乌沙利定。
在本发明的另外一个实施方案中,抗癌化合物是指从白花牛角瓜中提取的任何化合物,如表2中所示的2"-氧-弗汝沙林(2"oxo-voruscharin)及其衍生物。
在本发明的另外一个方面,治疗性药物是本发明的提取物。所述提取物可能是与具有抗毒活性的提取物一样的提取物。另外,所述提取物可能是与具有抗毒活性的提取物一样的提取物,但是每种提取物中都不包含一种或多种活性化合物。另外,所述提取物可能是与具有抗毒活性的提取物一样的提取物,但是每种提取物中都包含一种或多种活性化合物。另外,所述提取物可能是与具有抗毒活性的提取物一样的提取物,但是每种提取物中的一种或多种活性化合物的浓度不同。
在本发明的另外一个方面,治疗性化合物是物理治疗,如辐射。所述辐射是指任何可用于治疗的辐射。例如,辐射可以是用于抑制肿瘤生长、作为骨髓移植手术一部分的全身辐射等。辐射也可以是用于诊断的辐射,如X射线或放射性标记物。
在本发明的另外一个方面,治疗性化合物是抗体或其片段。所述抗体具有细胞毒活性。治疗性抗体的例子包括而不限于赫赛汀R(HerceptinR)、Prostascint、利妥昔单抗(Rituximab)和曲妥单抗(Trastuzumab)。
在本发明的另外一个方面,治疗性化合物是激素或其片段。所述激素具有细胞毒活性。治疗性激素的例子包括而不限于布舍瑞林、氟羟甲基睾丸素、氟他胺、福美斯坦、诺乙雄龙、炔诺酮、氢化泼尼松、泼尼松和tamoxifene。
在本发明的另外一个方面,治疗性化合物是肽或其片段。所述肽具有细胞毒活性。
抗体、激素或肽的片段是指包含抗体、激素或肽的一部分并且能识别完整抗体、激素或肽的靶位的肽。片段还能识别完整抗体、激素或肽的靶位。这一部分可以包括不改变该部分的靶位识别能力的氨基酸替代、缺失或插入。替代、缺失或插入的氨基酸数目可以是少于2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、40、45、50、55、60、65、70、75、80、85、90、95、100、200、300、400或500。
在本发明的另外一个方面,由于提取物的抗毒活性使治疗性化合物可以较高的剂量给药。通过给予较高剂量的治疗性化合物可以使肿瘤得到更快速有效地治疗。接受较高剂量治疗性化合物和本发明提取物的患者可得益于治疗性化合物毒副作用的降低。
在本发明的另外一个方面,由于提取物的抗毒活性使治疗性化合物可以联合给药。联合治疗可同时针对肿瘤的不同方面,从而使治疗更有效。通过与本发明的提取物联合,患者发生副作用的程度将降低,从而得益于联合治疗的效果。
在另外一个实施方案中,本发明涉及从提取物中分离的活性化合物。术语提取物的“活性化合物”或“活性成分”用于本文中意义相同,是指存在于提取物中的、与提取物上述活性的至少一个活性一样的化合物。
在另外一个实施方案中,本发明涉及获得植物白花牛角瓜提取物的方法。
由于本发明中至少有一个提取物具有抗肿瘤活性,因此本发明的提取物特别适用于治疗如肿瘤一样的疾病。因此,在另一方面,本发明涉及含有上述的一种提取物或提取物中的至少一种活性化合物的药物组合物。
此外,由于本发明的提取物还具有抗毒活性,因此,本发明的提取物也特别适用于和其他具有一定毒副作用的治疗性化合物如其他药物联合使用。因而在另外一个实施方案中本发明涉及含有上述的一种提取物或提取物中的至少一种活性化合物以及第二种具有一定毒副作用的药理活性化合物的药物组合物。
此外,本发明涉及一种所述提取物和/或提取物中的至少一种活性化合物作为药物的应用。本发明还涉及一种所述提取物和/或提取物中的至少一种活性化合物在制备疾病治疗药物、特别是肿瘤治疗药物中的应用。
在另外一个实施方案中,本发明还涉及治疗肿瘤的方法。
通过说明书的详细描述并参考附图可以很清楚地理解本发明的其他目的及优点。
附图
图1描述的是本发明不同浓度的提取物对不同类型的肿瘤总体生长状况的影响。
图2-11显示的是本发明的提取物在体外对不同类型的人源癌细胞系的影响。图2显示的是乳腺癌细胞系,图3显示的是肉瘤细胞系,图4显示的是胰腺癌细胞系,图5显示的是黑色素瘤细胞系,图6显示的是结肠癌细胞系,图7显示的是胶质瘤细胞系,图8显示的是肺癌细胞系,图9显示的是膀胱癌细胞系,图10显示的是前列腺癌细胞系,图11显示的是头颈癌细胞系。
图12-16描述的是本发明的提取物在体外对5种不同的人源细胞系,HCT-15(图12)、RPMI(图13)、A172(图14)、J82(图15)和Hs683(图16)细胞周期动力学的影响。图的上部显示的是加入不同剂量的提取物时细胞的总体生长状况,以活的癌细胞对对照细胞的百分数表示。图的中间部分和下部显示的是不同浓度的所述提取物在加入24和72小时后对细胞周期动力学的影响。用斯氏测验分析统计学差异,其中*表示p≤0.05;**表示p≤0.01;***表示p≤0.001。
图17-20显示的是本发明的提取物对四种不同人源细胞系,HCT-15(图17)、A172(图18)、J82(图19)和Hs683(图20)细胞的体外凋亡诱导效应和坏死诱导效应。图的上半部分显示的是不同剂量的所述提取物在加入24小时后所产生的凋亡诱导效应和坏死诱导效应,图的下半部分显示的是加入72小时后的效应。
图21显示的是本发明的提取物对体内淋巴瘤模型的效应。所述提取物通过腹腔内注射,注射给P388淋巴瘤荷瘤小鼠的提取物的剂量分别为2.5mg/kg;5mg/kg和10mg/kg。图21A显示的是所述提取物对对照鼠(未处理)和治疗鼠体重的影响。图21B显示的是所述提取物对对照鼠和治疗鼠体内肿瘤生长的影响。
图22显示的是本发明的提取物对体内淋巴瘤模型的效应。所述提取物通过腹腔内注射,注射给P388淋巴瘤荷瘤小鼠的提取物的剂量分别为0.63mg/kg;1.25mg/kg和2.5mg/kg。图22A显示的是所述提取物对对照鼠(未处理)和治疗鼠体重的影响。图22B显示的是所述提取物对对照鼠和治疗鼠体内肿瘤生长的影响。
图23显示的是本发明的提取物对体内黑色素瘤模型的效应。所述提取物通过腹腔内注射,注射给B16黑色素瘤荷瘤小鼠的提取物的剂量分别为2.5mg/kg;1.25mg/kg和0.63mg/kg。图23A显示的是所述提取物对对照鼠(未处理)和治疗鼠体重的影响。图23B显示的是所述提取物对对照鼠和治疗鼠体内肿瘤生长的影响。
图24显示的是本发明的提取物对体内黑色素瘤模型的效应。所述提取物通过口服给药,给予B16黑色素瘤荷瘤小鼠的提取物的剂量分别为0.63mg/kg;1.255mg/kg和2.5mg/kg。图24A显示的是所述提取物对对照鼠(未处理)和治疗鼠体重的影响。图24B显示的是所述提取物对对照鼠和治疗鼠体内肿瘤生长的影响。
图25显示的是本发明的提取物对体内乳腺癌模型的效应。所述提取物通过腹腔内注射,注射给MXT-HI乳腺癌荷瘤小鼠的提取物的剂量分别为2.5mg/kg;5mg/kg和10mg/kg。图25A显示的是所述提取物对对照鼠(未处理)和治疗鼠体重的影响。图25B显示的是所述提取物对对照鼠和治疗鼠体内肿瘤生长的影响。
图26显示的是试验组小鼠(腹腔分别注射2.5mg/kg;5mg/kg和10mg/kg的提取物)和对照组小鼠存活率的统计图(Kaplan-Meier统计学分析)。
图27显示的是给小鼠腹腔注射5mg/kg和1.25mg/kg本发明的提取物后3天与对照组相比对白细胞数、红细胞数、血红蛋白浓度和血球比容值的影响(在图中“白柱”表示的提取物剂量为1.25mg/kg)
图28-35显示的本发明的提取物与抗肿瘤化合物阿霉酮、长春新碱、喜树碱或奥沙利铂联合使用时的抗毒性效应。
提取物的特性
白花牛角瓜属萝摩科植物,是一种生长在非洲和亚洲的植物。这种植物被用于传统医药中,经研究发现还有多种用途,如解热、抗疟、止泻(anti-diarroeal)、止痛、治疗胃炎、保护粘膜以及杀虫、镇咳、抗菌、愈合创伤、松弛肌肉。已知白花牛角瓜的茎、花和叶都含有某种被称为强心甾的化合物。最近,实验证明这些强心甾具有心脏毒性,已被开发成治疗人心功能不全的药物。
出乎意料的是,本发明至少提供了一种具有另一类活性、特别是“抗肿瘤活性”的白花牛角瓜提取物。另外,还证明本发明的提取物中至少有一种在体外和体内都具有抗肿瘤活性。本发明的所述提取物可诱导肿瘤生长的显著抑制,具有促凋亡活性。这些特性在实施例3和4中进行了进一步的说明。另外,发明者通过体内实验证明本发明的所述提取物中至少有一种提取物对几种类型的肿瘤都有较高的抑制活性。如下面实施例中所描述的,本发明的所述提取物在几种肿瘤实验模型中都产生了显著的抗肿瘤效应,这些模型代表了一个较宽组织学类型的肿瘤,其中包括乳腺癌、淋巴瘤、黑色素瘤。这些模型是与临床相关的,因为它们模拟了人肿瘤的特殊临床阶段。
令人吃惊的是,本发明所述的提取物在相对低的剂量时也具有较高的活性。所述提取物在0.4到2.2mg/kg的低剂量时也具有抗肿瘤活性,优选的剂量范围是0.5到2mg/kg。低剂量也有较高的抗肿瘤活性说明所述提取物活性很高。当阅读下面的实施例时可以惊奇地发现,本发明所述的提取物在进行长期低剂量,即0.6mg/kg到1.25mg/kg治疗时所达到的抗肿瘤效应比进行高剂量,即5mg/kg到10mg/kg治疗时所达到的效果还要好。本发明所述的提取物的最大耐受剂量(MTD)指数是20mg/kg,这个指数是指一次可以给予健康动物的所述提取物的最大剂量。这个数值说明本发明所述的提取物具有较宽的治疗窗口。
术语“毒性”或“毒性效应”是指化合物对正常细胞、组织或器官可能的有害效应。本发明的提取物的其他重要特性包括其毒性水平较低。试验证明所述提取物在体内不会导致血液学指标的改变和体重的下降,对不同类型的器官和组织的副作用都很小。事实上,本发明所述提取物的毒性水平是非常低的。本发明所述提取物结合了如下一些基本特征:较高的抗肿瘤活性、较低的毒性以及很少产生毒副作用。
另外,本发明的植物白花牛角瓜提取物还具有“抗毒活性”。如上所述,术语“抗毒活性”用在本文中是指本发明的提取物降低或反转化合物毒副作用的能力。发明者吃惊地发现本发明的提取物与具有一定毒副作用的化合物联合使用可使治疗性化合物的副作用降低。例如,实施例8说明本发明的提取物与大家所熟知的抗癌药如长春新碱、阿霉酮、喜树碱或奥沙利铂联合使用可降低这些抗癌药由于对正常细胞的毒性而产生的某些副作用。
当本发明的至少一种提取物在给予治疗性化合物前给药时,即化合物与提取物先后给药时可观察到其具有抗毒活性。在给予治疗性化合物前任意时间点给予提取物是本发明的一个方面。本发明的其他方面涉及在给予治疗性化合物前不超过336、312、288、264、240、216、192、168、144、120、96、72、48、24、20、16、12、8、4、2、1或0.5小时给予提取物。
当本发明的至少一种提取物在给予治疗性化合物的同时,即化合物与提取物作为一种组合物或者同时单独给药时也可以观察到其具有抗毒活性。
当本发明的至少一种提取物在给予治疗性化合物后给药时,即提取物与化合物先后给药时也可以观察到其具有抗毒活性。在给予治疗性化合物后任意时间点给予提取物是本发明的一个方面。本发明的其他方面涉及在给予治疗性化合物后0.5、1、2、4、8、12、16、20、24、48、72、96、120、144、168、192、216、240、264、288、312或366小时内给予提取物。
在先后给药时,所述组合物可在给予治疗性化合物前和/或后以各种剂量给药一次或多次。先后给药还可以结合同时给药或先后给药。
提取物的组合物
本发明的提取物包含一种或几种活性化合物,即存在于本发明提取物中的、具有与本发明提取物上述的至少一种活性一样活性的化合物。至少一种提取物的主要活性是抗肿瘤活性和抗毒活性。本领域的技术人员可以理解存在于所述提取物中的活性化合物可以只具有这些特性中的一种,或者两种。
在另外一个实施方案中,本发明的至少一种提取物含有至少两种选自如下一组的活性化合物:马利筋苷、异牛角瓜甙、弗汝沙林、牛角瓜苷、牛角瓜苷元、乌沙苷元、卡洛托星、乌沙林和乌沙利定、2″-氧-弗汝沙林。
还可以理解的是,本发明的提取物还可以含有一种或多种不属于强心甾类的活性化合物及其他化合物。在另外一个实施方案中,提取物至少含有表1中的一种化合物。
表1 包含在本发明的至少一种提取物中的某些化合物
| 存在于本发明的提取物中的化合物 | 3-O-乙酰-牛角瓜苷,α-香树精、α-香树精-苯甲酸盐、α-牛角瓜醇、α-山莴苣醇、α-山莴苣酰-乙酸盐、α-山莴苣酰-异戊酸盐、阿拉伯糖、ASH、苯甲酰异厚果酮、苯甲酰厚果酮、β-香树精、β-香树精-苯甲酸盐、β-牛角瓜醇、β-谷固醇、弹性橡皮、粉绿小冠花苷元、副冠毒苷元、D-氨基葡萄糖、弗如糖苷、GIGANTEOL、大曲茵素(GIGANTIN)、葡萄糖、组胺、ISOGIGANTEOL、异山莴苣醇、异厚果酮、月桂烷厚果酮、月桂酸、亚油酸、蜂醇、牛角瓜皮苦素、油酸、软脂酸、高牛角瓜苷、伪牛角瓜苷元、鼠李糖豆固醇、西里奥苷元蒲公英甾醇、蒲公英甾醇苯甲酸盐、胰蛋白酶。 |
在另外的实施方案中,本发明涉及从本发明的提取物中分离出的活性化合物。
在本发明的另外一个实施方案中提取物中的活性化合物是2″-氧-弗汝沙林。本发明的一个方面是表2中所列的所述化合物(化合物A)及其衍生物(化合物B到H)的抗癌活性和/或抗毒活性。
表2:2″-氧-弗汝沙林(化合物A)及其衍生物(化合物B到H)的化学结构
*是指式I的含氮杂环的N原子和C原子之间的双键。
提取方法
根据另外一个实施方案,本发明的提取物可通过醇提取、特别是甲醇提取获得。
在另一个实施方案中,本发明涉及提取本发明的提取物的方法,该方法包括:
a)在脂肪族醇中提取所述白花牛角瓜植物的起始原料,所述起始原料选自果实、地上部分、地下部分或其混合物,利用所述醇溶解起始原料获得所述原料的脂肪族醇悬液,搅拌所述悬液;用多孔玻璃过滤所述悬液从而得到第一滤液和第一固体组分;
b)用脂肪族醇提取所述第一固体组分从而得到第二滤液和第二固体组分;
c)混合所述第一滤液和第二滤液得到混合滤液;以及
d)在真空下蒸发所述混合滤液从而得到油性残留物。
在一个优选实施方案中,所述白花牛角瓜植物的起始原料取自植物的地下部分,特别是植物的根。
在另一个实施方案中,用于提取本发明的起始原料的脂肪族醇是乙醇。在另外一个实施方案中,提取过程中获得的残留物用溶剂收集,特别是药用溶剂。
在另一个实施方案中,本发明涉及提取本发明的提取物的方法,该方法包括:
a)研磨白花牛角瓜的叶片、茎、皮和根获得植物精粉,
b)在索氏抽提器中用二氯甲烷提取步骤a)的粉末至少6、12、18小时,优选24小时,
c)倾析步骤b)的二氯甲烷,过滤后蒸发滤液,得到胶状物,
d)在索氏抽提器中用甲醇提取步骤c)的残留物至少6、12、18小时,优选24小时,
e)倾析步骤d)的甲醇,过滤后蒸发滤液,得到胶状物,
f)以二氯甲烷-甲醇为溶剂利用快速硅胶柱层析处理步骤e)的胶状物,
g)收集含有生物活性组分的第一组分,
h)以己烷-丙酮为溶剂用快速硅胶柱层析处理步骤g)的浓缩组分得到两个组分,以及
i)步骤h)后用甲醇洗涤层析柱以得到含有生物活性成分的第三组分。
本发明的提取物包括从步骤c)、g)和i)中获得的那些提取物。
本发明的一个方面是以利于保持提取物中生物活性化合物完整性的方式进行的提取方法。这些需要注意的地方是本领域技术人员所熟知的。
提取物的应用
由于本文所述的提取物中至少有一种提取物具有一些优越的特性,特别是其抗肿瘤活性、抗毒活性、低毒性和/或其在低剂量时也具有高活性的特征,因此本发明的提取物或提取物中的活性化合物特别适用于作为治疗疾病,尤其是治疗肿瘤的药物。
在另一个实施方案中,本发明涉及本发明的提取物或其中的活性化合物作为药物的应用。
在另外一个实施方案中,本发明还涉及至少一种本发明的提取物或其中的活性化合物在制备肿瘤治疗药物中的应用。更具体地说,本发明所述提取物或其中的活性化合物可用于制备肿瘤治疗药物。可用本发明的提取物治疗的肿瘤包括而不限于乳腺癌、淋巴瘤、肉瘤、胰腺癌、黑色素瘤、结肠癌、胶质瘤、非小细胞肺癌、小细胞肺癌、皮肤癌、骨癌、卵巢癌、CNS癌、膀胱癌、头颈癌、前列腺癌、肝癌、血癌。
如上所述,本发明的提取物还具有抗毒活性。发明者已经发现本发明的提取物或其中的活性化合物与具有一定毒副作用的第二化合物联合使用可使第二化合物的毒性降低,但是其治疗活性却没有减弱。因此,本发明的白花牛角瓜提取物还可以与其他化合物、特别是其他抗肿瘤化合物联合使用。
包含提取物的药物组合物
在另一个实施方案中,本发明涉及治疗肿瘤的药物组合物,该组合物包含治疗有效量的本发明的白花牛角瓜提取物或其中的活性化合物以及药学上可接受的载体。
在另外一个实施方案中,本发明涉及治疗肿瘤的药物组合物,该组合物包含
-治疗有效量的本发明的白花牛角瓜提取物或其中的活性化合物,
-治疗有效量的治疗性化合物,以及
-药学上可接受的载体。
本文所用的术语“治疗有效量”是指研究者、兽医、医生或其他临床医师认为至少有一种提取物或其中的活性化合物、或药物的量能够在组织、系统、动物或人体内激发生物反应或医学反应,其中包括被治疗疾病症状的缓解。
药物组合物可以本领域技术人员熟知的方法制备。为此,本发明的提取物和/或其中的任何活性化合物、一种或多种固体或液体药学上可接受的载体以及其他药理活性化合物要被制成适宜的给药形式或剂型,作为药物用于治疗人或动物的疾病。
药物组合物的特定形式可以是溶液、悬液、乳化液、乳膏、片剂、胶囊、鼻喷剂、脂质体或微储装置(micro-reservoir),尤其是口服可吸收的组合物或无菌注射剂,如无菌注射水悬液或油悬液,或者栓剂。本发明优选的剂型是干燥固体形式,其中包括胶囊、颗粒、片剂、丸剂、药团和粉末。固体载体可包含一种或多种载体,乳糖、填料、分散剂、粘合剂,如纤维素、羧甲基纤维素、淀粉或防止片剂粘附到压片机上的抗粘剂,如硬脂酸镁。片剂、丸剂和药团的形式可以使药物快速分解,或者使活性成分缓慢释放。
另外,由于本发明的提取物或其中的活性化合物具有抗毒活性,因此也特别适于和具有一定毒副作用的其他药理活性化合物联合使用,如具有一定毒副作用的其他药物。
“具有一定毒副作用的药理活性化合物”包括任何用于治疗疾病但是又能诱导一些不需要的毒性效应的化合物。这种化合物优选用于治疗肿瘤的化合物。例如,本发明的提取物或其中的活性化合物可与具有抗肿瘤活性的一种或多种其他化合物联合使用。由于两种或多种具有抗肿瘤活性的化合物联合使用,因此其抗肿瘤效应可以得到提高。另外,这种联合用药可以降低一种或几种抗肿瘤化合物所诱导的毒副作用。
本发明的提取物或其中的活性化合物与其他治疗性化合物联合用药方案包括所述提取物或其中的活性化合物与其他治疗性化合物分别用药。特别是在给予其他治疗性化合物前(预处理)、同时或之后(治疗后)给予本发明的提取物或其中的活性化合物。
另外,提取物或其中的活性化合物与其他治疗性化合物联合用药方案还可以包括两种药物的混合物。因此,在一个优选实施方案中,本发明涉及包含第一组分和第二组分的药物组合物,其中,所述第一组分是上面所述的提取物或其中的至少一种活性化合物,所述第二组分包含具有一定毒副作用的药理活性化合物。
产品
本发明的一个方面是含有白花牛角瓜提取物和治疗性化合物的产品,其中提取物与治疗性化合物同时、分别或依次给予患者。可用于本发明的产品是本发明的一个方面。
同时给药是指两种组分同时给予患者。例如,两种组分的混合物。其中包括而不限于静脉注射的溶液、片剂、液体、局部用的乳膏等,其中每种剂型都包含两种组分。
分别给药是指两种组分同时或者在同一个时间内先后给予患者,但是两种组分分别存在于独立的制剂中。例如,两种组分分别存在于两种片剂中。片剂可同时服用,或者先后服用。
先后给药是指分别存在于两种独立的制剂中的两种组分先后给予患者。两次服药之间可有一段间隔时间。例如,一种组分可在服用另一种组分后336、312、288、264、240、216、192、168、144、120、96、72、48、24、20、16、12、8、4、2、1或0.5小时服用。
先后用药时提取物可在给予治疗性化合物前和/或后以各种剂量给予一次或多次。先后给药可结合同时给药或先后给药。
试剂盒
本发明的另一个方面是试剂盒,其中包括装有白花牛角瓜提取物的容器和装有治疗性化合物的容器。本发明的提取物和治疗性化合物见上面的描述。
在提及由装白花牛角瓜提取物的容器和装治疗性化合物的容器组成的试剂盒时,应当清楚试剂盒可以包含单次剂量或多次剂量,这些药物可以装在两个单独的容器里,每个容器内都装有多次剂量的药物,试剂盒内还可以包括多个容器,每个容器装有一种单次剂量的药物。还应当清楚试剂盒也可以包含不止一种治疗性化合物,每种化合物都用单独的容器盛装,或者将治疗性化合物的混合物装在一个容器内。
容器可以是医学领域所熟知的任何容器,如小玻璃瓶、发泡包装、注射器、可再封的瓶子、配药瓶、吸气器、滴瓶、膏药、涂药器、栓剂。
将提取物和治疗性化合物分别包装便于这两种药物同时、分别或依次给药。
治疗方法
由于本发明至少有一种提取物具有优越的抗肿瘤活性,因此所述提取物特别适用于治疗肿瘤患者。在另一个实施方案中,本发明还涉及治疗肿瘤的方法,该方法是给予需要治疗的患者以本发明的药物组合物。由于所述提取物的毒性和副作用都很小,因此利用包含一种所述提取物的药物组合物治疗肿瘤时所产生的副作用是很小的。因此,本发明的提取物可用于肿瘤的长期治疗。
在一个优选实施方案中,本发明特别提供了一种治疗肿瘤的方法,其中的肿瘤选自:乳腺癌、淋巴瘤、肉瘤、胰腺癌、黑色素瘤、结肠癌、胶质瘤、非小细胞肺癌、小细胞肺癌、皮肤癌、骨癌、卵巢癌、CNS癌、肾癌、膀胱癌、头颈癌、前列腺癌、肝癌和血癌。
为了达到治疗的目的,本发明的药物组合物可以口服给药、胃肠外途径给药,其中包括皮下注射、静脉注射、肌肉注射、动脉内注射或融合技术,或者通过鼻内喷雾或直肠内给药,单位剂量的剂型内含有常规的非毒性药学上可接受的载体、佐剂或运载体。
根据本发明的方法,所述药物组合物可在治疗过程中在不同的时间分别给药,或者以分开的剂型或混合剂型同时给药。因此,本发明可以被理解为包括了所有的同时给药方案或替代治疗方案,术语“给药”因而得以被阐释。
治疗实体瘤的主要方法包括手术、放疗和化疗,这些方法可单独使用,也可以联合使用。本发明的提取物适于与这些治疗方法联合使用。本发明的提取物可用于提高肿瘤细胞对放疗时辐射的敏感性,也可用于提高化疗药对肿瘤的渗透或杀伤活性。本发明的提取物还可用于致敏多药耐药肿瘤细胞。本发明的提取物与其他DNA损伤性治疗性化合物联合使用时是一种有效的治疗性化合物,例如在与放疗联合使用时可增强放疗的疗效。应当清楚的是,本发明的药物组合物可以特定的剂量、特定的给药频率用于人体内,剂量大小及给药频率的选择要根据病人的具体情况而定,其中包括患者的年龄、体重、一般健康状况、性别、饮食、给药途径及给药时间、排泄速率、联合用药、患者疾病的严重程度。
下面的实施例是用于说明本发明。这些实施例不应该被理解为限制本发明的范围。第一个实施例说明了从植物白花牛角瓜中提取本发明的提取物的方法。实施例2-4描述了本发明的提取物在体外的抗肿瘤活性特征。实施例5到7描述了本发明的提取物在体内的抗肿瘤活性特征。实施例8描述的是本发明的提取物的抗毒性效应。
实施例
实施例1从植物白花牛角瓜中提取本发明的提取物的方法
本发明的提取物(提取物A)是用甲醇从白花牛角瓜植物(萝摩科)的根中提取的。所述提取物还被称为提取物A(编号)。将10克植物放入含150ml甲醇的三角烧瓶中,用磁力搅拌12小时,然后用多孔玻璃过滤。固体残留物用甲醇再提取2小时。将两次的滤液混合,然后用旋转蒸发器在真空下蒸发。含甲醇提取物的残留物被命名为提取物A。
通过分析提取物A发现其中含有几种类型的化合物。在所述提取物A中有一组特殊的化合物是由强心甾类化合物组成的,如马利筋苷、异牛角瓜甙、弗汝沙林、牛角瓜苷、牛角瓜苷元、乌沙苷元、卡洛托星、乌沙林和乌沙利定。另外,提取物A中包含的其他化合物包括而不限于3-O-乙酰-牛角瓜苷,α-香树精、α-香树精-苯甲酸盐、α-牛角瓜醇、α-山莴苣醇、α-山莴苣酰-乙酸盐、α-山莴苣酰-异戊酸盐、阿拉伯糖、ASH、苯甲酰异厚果酮、苯甲酰厚果酮、β-香树精、β-香树精-苯甲酸盐、β-牛角瓜醇、β-谷固醇、弹性橡皮、粉绿小冠花苷元、副冠毒苷元、D-氨基葡萄糖、弗如糖苷、GIGANTEOL、大曲茵素、葡萄糖、组胺、ISOGIGANTEOL、异山莴苣醇、异厚果酮、月桂烷厚果酮、月桂酸、亚油酸、蜂醇、牛角瓜皮苦素、油酸、软脂酸、高牛角瓜苷、伪牛角瓜苷元、鼠李糖豆固醇、西里奥苷元蒲公英甾醇、蒲公英甾醇苯甲酸盐、胰蛋白酶。
本发明的其他提取物是通过如下方法提取的,该方法包括:
a)研磨白花牛角瓜的叶片、茎、皮和根获得植物精粉,
b)在索氏抽提器中用二氯甲烷提取步骤a)的粉末24小时,
c)倾析步骤b)的二氯甲烷,过滤后蒸发滤液,得到胶状物,
d)在索氏抽提器中用甲醇提取步骤c)的残留物24小时,
e)倾析步骤d)的甲醇,过滤后蒸发滤液,得到胶状物,
f)以二氯甲烷-甲醇为溶剂利用快速硅胶柱层析处理步骤e)的胶状物,
g)收集含有生物活性组分的第一组分,
h)以己烷-丙酮为溶剂用快速硅胶柱层析处理步骤g)的浓缩组分得到两个组分,以及
i)步骤h)后用甲醇洗涤层析柱以得到第三组分。
在步骤c)中所分离的提取物在下文中被称为提取物B。在步骤g)中所分离的提取物在下文中被称为提取物C。在步骤i)中所分离的提取物在下文中被称为提取物D。
实施例2本发明的提取物对细胞系细胞整体生长状况的影响
本实施例说明了本发明的提取物A对不同类型肿瘤的抗肿瘤活性。为了确定提取物A的体外活性特征,进行了提取物A的MTT试验。MTT试验是本领域所熟知的间接检测方法,可以快速地、即在5天内测定给定产品对细胞系整体生长状况的影响。该试验可检测具有代谢活性的活细胞数,因为活细胞可通过线粒体还原反应将黄色的MTT产品(3-(4,5-二甲基噻唑-2-基)-2,5二苯基四唑嗅化物)转化成蓝色的产品甲,这种转化只有活细胞才可以产生。试验结束时甲形成的量通过分光光度计测定,其数值与活细胞数成正比。
表2所述的48株人源肿瘤细胞系用提取物A处理。这些细胞系涵盖了10个组织学类型,分别是胰腺癌、肉瘤、乳腺癌、黑色素瘤、结肠癌、胶质瘤、肺癌、膀胱癌、前列腺癌和头颈癌。细胞在平底96孔培养板中培养,每孔100μl细胞悬液,根据细胞类型的不同细胞数在每孔3000到5000之间。每株细胞都用其特定的培养基培养,见表2。
表2 MTT试验中所用的人源癌细胞系及其所用的培养基
| 细胞系 | ATCC编号 | 组织 | 培乔基 |
| BxPC-3 | CRL-1687 | 胰腺 | RPMI 10%血清 |
| MiaPACA-2 | CRL-1420 | 胰腺 | DMEM葡萄糖 10% |
| PANC-1 | CRL-1469 | 胰腺 | OPTIMEM 5% |
| CAPAN-1 | HTB-79 | 胰腺 | RPMI 10%血清 |
| CFPAC-1 | CRL-1918 | 胰腺 | Iscove′s 10%血清 |
| Hs766T | HTB-134 | 胰腺 | OPTIMEM 5% |
| SU.86.86 | CRL-1837 | 胰腺 | RPMI 10%血清 |
| SK-LMS-1 | HTB-88 | 肉瘤 | MEM 10%血清 |
| SK-UT-1B | HTB-115 | 肉瘤 | MEM 10%血清AA |
| HT-1080 | CCL-121 | 肉瘤 | MEM 5%血清 |
| Hs729 | HTB-153 | 肉瘤 | MEM 10%血清AA |
| MES-SA | CRL-1976 | 肉瘤 | MEM 5%血清 |
| RD | CCL-136 | 肉瘤 | MEM 5%血清 |
| A204 | HTB-82 | 肉瘤 | MEM 5%血清 |
| MCF-7 | HTB-22 | 乳腺 | MEM 5%血清 |
| T-47D | HTB-133 | 乳腺 | MEM 5%血清 |
| MDA-MB-231 | HTB-26 | 乳腺 | DMEM Nut mix 10%血清 |
| ZR-75-1 | CRL-1500 | 乳腺 | MEM 5%血清 |
| Hs578T | HTB-126 | 乳腺 | MEM 5%血清 |
| SK-MEL-28 | HTB-72 | 黑色素瘤 | RPMI 10%血清 |
| HT-144 | HTB-63 | 黑色素瘤 | MEM 10%血清AA |
| C-32 | CRL-1585 | 黑色素瘤 | MEM 5%血清 |
| Malme-3M | HTB-64 | 黑色素瘤 | MEM 5%血清 |
| G-361 | CRL-1424 | 黑色素瘤 | OPTIMEM 5%血清 |
| HCT-15 | CCL-225 | 结肠 | MEM 5%血清 |
| LoVo | CCL-229 | 结肠 | MEM 5%血清 |
| DLD-1 | CCL-221 | 结肠 | MEM 10%血清AA |
| Ls-174T | CL-188 | 结肠 | MEM 10%血清AA |
| HT29 | HTB-38 | 结肠 | MEM 10%血清AA |
| WiDR | CCL-218 | 结肠 | MEM 10%血清AA |
| SW948 | CCL-237 | 结肠 | OPTMEM 5%血清 |
| A172 | CRL-1620 | 胶质瘤 | MEM 5%血清 |
| H4 | HTB-148 | 胶质瘤 | MEM 5%血清 |
| Hs683 | HTB-138 | 胶质瘤 | MEM 5%血清 |
| SW1088 | HTB-12 | 胶质瘤 | MEM 5%血清 |
| U-118MG | HTB-15 | 胶质瘤 | MEM 5%血清 |
| U-87MG | HTB-14 | 胶质瘤 | MEM 5%血清 |
| U-373MG | HTB-17 | 胶质瘤 | MEM 5%血清 |
| A427 | HTB-53 | 肺 | MEM 5%血清 |
| A549 | CCL-185 | 肺 | MEM 5%血清 |
| J82 | HTB-1 | 膀胱 | MEM 5%血清 |
| T24 | HTB-4 | 膀胱 | MEM 5%血清 |
| PC3 | CRL-1435 | 前列腺 | MEM 5%血清 |
| Detroit | CCL-138 | 头颈 | MEM 10%血清AA |
| RPMI | CCL-30 | 头颈 | MEM 10%血清AA |
| FaDu | HTB-43 | 头颈 | MEM 10%血清AA |
| SCC9 | CRL-1629 | 头颈 | MEM 10%血清AA |
| SCC25 | CRL-1628 | 头颈 | MEM 10%血清AA |
其中AA代表“氨基酸”
细胞在37℃孵育24小时后,用100μl新鲜培养基换液,培养基中含有不同浓度的提取物A,浓度分别为0.01μg/ml、0.05μg/ml、0.1μg/ml、0.5μg/ml、1μg/ml、5μg/ml、10μg/ml、50μg/ml和100μg/ml。每个试验条件设6个复孔。
与含药物的培养基(试验条件)或不含药物的培养基(对照)孵育72小时后用100μl含1mg/ml MTT的RPMI培养基换液。将微孔板置于37℃孵育3小时后400g离心10分钟。然后去掉MTT,形成的甲结晶用100μl DMSO溶解。震荡微孔板5分钟,然后用分光光度计测定吸光度值,使用两种波长,其中一个为甲的最大吸收波长570nm,另一个是背景噪声波长630nm。
计算每种试验条件下所测得的6个孔的平均吸光度值及其标准误差(SEM)。计算剩余活细胞与对照组相比所占的百分率。试验结果见图1-11。
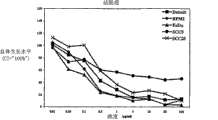
图1显示的是10种不同组织类型的细胞的总体结果。如图所示,提取物A对所检测的所有组织类型的细胞都具有抗肿瘤活性。膀胱组织来源的人肿瘤细胞系对提取物A的敏感性比其他9种类型的细胞系低。测定了能杀死细胞总数的50%时所需要的植物提取物的量,这个数值被称为IC50。提取物A对乳腺组织来源的细胞系和胰腺癌细胞系的IC50在0.5μg/ml到1μg/ml之间。提取物A对肉瘤、黑色素瘤、胶质瘤、肺癌、头颈癌和结肠癌细胞系的抗肿瘤活性更强,其IC50在0.5-0.1μg/ml之间。PC3前列腺癌细胞系的敏感性最显著,其IC50在0.01-0.05μg/ml之间。
如图1所示,5种乳腺癌细胞系的IC50在0.5μg/ml到1μg/ml之间。在图2中进一步描述了T-47D、MDA-MB-231、ZR-75-1、MCF-7和Hs578T这5种乳腺癌细胞系的整体生长情况。其中T-47D、MDA-MB-231、ZR-75-1和Hs578T对提取物A的敏感性一致,而MCF-7细胞整体生长状况下降的速度比其他4种乳腺癌细胞都要快。
如图1所述,7种肉瘤细胞系(见表2)的IC50在0.5μg/ml到0.1μg/ml之间。在图3中进一步描述了各个细胞系的整体生长情况。提取物A对A204细胞系的抗肿瘤活性最高,其IC50在0.1μg/ml到0.05μg/ml之间。Hs729细胞系被认为是7株肉瘤细胞系中最不敏感的,因为其IC50在1μg/ml到5μg/ml之间。
如图1所述,7株胰腺癌细胞系(见表2)的平均IC50在0.5μg/ml到0.1μg/ml之间。进一步观察了7株胰腺癌细胞系中6株胰腺癌细胞系的整体生长状况(图4)。在这7株细胞系中,Panc-1对提取物A的敏感性最高,Hs766T的敏感性最低。这两株细胞系的IC50分别为0.1μg/ml-0.5μg/ml和1μg/ml-5μg/ml。
如图1所述,5株黑色素瘤癌细胞系(见表2)的平均IC50在0.5μg/ml到0.1μg/ml之间。在大于或等于5μg/ml的浓度时,本发明的提取物对所有黑色素瘤细胞系总体生长水平的抑制超过60%。所有的黑色素瘤细胞系的总体生长状况相似,其IC50在0.1μg/ml到0.5μg/ml之间。
如图1所述,7株结肠癌细胞系(见表2)的平均IC50在0.5μg/ml到0.1μg/ml之间。在所有被检测的结肠癌细胞系中(图6),LoVo细胞系的IC50约为0.1μg/ml,被认为是最敏感的结肠癌细胞系。SW948肿瘤细胞系被认为是最不敏感的,其IC50在0.5μg/ml到1μg/ml之间。
如图1所述,7株胶质瘤癌细胞系(见表2)的平均IC50在0.5μg/ml到0.1μg/ml之间。Hs683是对提取物最敏感的细胞系,其IC50接近0.05μg/ml。即使是0.01μg/ml到10μg/ml的提取物A对A172细胞的生长也没有影响,其IC50在10μg/ml到50μg/ml之间。
如图1所述,2株人非小细胞肺癌细胞系(NSCLC)的平均IC50在0.1μg/ml到0.5μg/ml之间。图8表明两株细胞系对提取物A都敏感。
如图1所述,2株人膀胱癌细胞系(见表2)的平均IC50在50μg/ml到100μg/ml之间。这两株细胞系对提取物A的敏感性明显不同(图9)。事实上,5μg/ml的提取物A就可以使T24细胞系的总体生长水平下降80%以上,而100μg/ml的提取物A也只能使J82细胞系的总体生长水平下降32%。J82细胞系对提取物A的敏感性极低。
1株前列腺癌细胞系(PC3细胞系)用提取物A处理后通过MTT试验分析其总体生长状况。0.5μg/ml-100μg/ml的提取物A可使该细胞系的总体生长水平被抑制约90%,其IC50约为0.1μg/ml(图10)。
如图1所述,5株头颈癌细胞系的平均IC50在0.1μg/ml到0.5μg/ml之间。5株头颈癌细胞系中有4株的总体生长水平相似(图11)。在所有的5株细胞系中,SCC9好像是最不敏感的,其对提取物A的IC50约为5μg/ml。
总之,本发明的提取物A对上述试验所分析的48株人源癌细胞系中的46株都是具有较高的抗肿瘤活性的。这种抗肿瘤活性表现为可使这些人源肿瘤模型的总体生长水平显著下降,这些人源肿瘤模型所代表的组织学类型的范围很宽。
实施例3 本发明的提取物对细胞动力学的影响
本实施例说明了本发明的提取物A的细胞增殖抑制效应。从实施例2所述的MTT比色分析结果中可以清楚的看到提取物A可明显抑制MTT试验所分析的48株人源癌细胞系中大部分细胞系的总体生长水平。在下面的实施例中要分析提取物对细胞生长的抑制效应是由于细胞周期动力学的改变引起的(实施例3),还是由于诱导凋亡引起的(实施例4),还是两种因素都存在。
细胞周期一般分为以下几个期:G0/G1、S和G2/M期。调控细胞增殖和/或细胞死亡的蛋白所发生的改变是提取物A中的活性化合物的靶位。细胞周期动力学的改变可用不同的荧光物质通过流式细胞术测定,如碘化丙啶、吖啶橙和溴乙啶等。流式细胞术可以确定每个癌细胞所处的细胞周期(可测定数千个细胞)。因此可通过DNA直方图模式的变化确定各种治疗性化合物的作用机制。用图或数学模型处理流式细胞术所得到的数据以估计处于G1、S和G2/M期的细胞比例。大多数的数学计算都是根据某个模型和假设。
将细胞接种到含7ml培养基的培养瓶(面积为25cm2)内。37℃孵育48小时后用含提取物A的新鲜培养基换液,提取物A的浓度分别为可以杀死50%(IC50)、30%(IC30)和10%(IC10)细胞的浓度。加入提取物后24或72小时收获悬液中的细胞,用4℃的磷酸盐缓冲液(PBS)洗涤,然后用70%的乙醇(4℃)固定,置于-20℃过夜。细胞用PBS洗涤后用碘化丙啶溶液(80μg/ml)在37℃孵育30分钟,然后置于4℃过夜。加入核糖核酸酶A(3%V/V)以使双链DNA断裂。绘制每个样品的细胞周期图。用流式细胞仪内的特殊软件确定处于不同细胞周期的准确细胞百分率。每个细胞周期相以峰面积表示,计算百分率。整个细胞周期的表面积为100%。每个试验进行3次。计算每个相的平均百分率及其标准差。给定条件下的每个细胞周期所占有的百分数与对照细胞、即未处理细胞中每个细胞周期所占的百分数进行比较。
提取物A具有很高的抗人源肿瘤细胞活性。流式细胞术试验中所选择的浓度参考了MTT试验的结果(实施例2)。一共检测了Hs683(胶质瘤)、J82(膀胱癌)、A172(胶质瘤)、RPMI(头颈癌)和HCT-15(结肠癌)这5株人源细胞系,确定了杀死10%、30%和50%的这些细胞所需要的提取物A的剂量(表3),以分析浓度不断增加的提取物A是否可以在处理24或72小时后促进处于某一细胞周期相的细胞积聚。
表3 在5株细胞系内本发明的提取物A杀死10%、30%和50%的细胞所需要的剂量
| 细胞系 | IC<sub>50</sub> | IC<sub>30</sub> | IC<sub>10</sub> |
| HCT-15 | 0.25μg/ml | 0.1μg/ml | 0.05μg/ml |
| RPMI | 0.25μg/ml | 0.1μg/ml | 0.05μg/ml |
| A172 | 25μg/ml | --- | 10μg/ml |
| J82 | --- | 50μg/ml | 10μg/ml |
| Hs683 | 0.05μg/ml | --- | 0.025μg/ml |
HCT-15细胞周期分析(图12)结果表明所有浓度的提取物A处理后24小时处于不同细胞周期的细胞分布情况与对照组都一样。但是用0.25μg/ml的提取物处理72小时后处于S期的细胞群明显增多。对照组处于S期的细胞占21%,而0.25μg/ml提取物处理72小时后的细胞处于S期的占59%。在S期细胞数增加的同时G0/G1期的细胞数减少。处于G0/G1期的细胞从71%下降到29%。
RPMI细胞周期分析(图13)结果表明0.05μg/ml的提取物A处理后24小时处于不同细胞周期的细胞分布情况与对照组一样,而0.1μg/ml和0.25μg/ml组在处理后24小时处于S期的细胞数略微升高。但是,当RPMI细胞与3种浓度的提取物A共孵育72小时后处于S期的细胞数明显增多。0.05μg/ml、0.1μg/ml和0.25μg/ml组处于S期的细胞百分数分别为71%、69%和62%。相应的,处于G0/G1期的细胞百分数明显下降,处于G2/M期的细胞百分数轻微升高,达到细胞总数的29%。
A172细胞用10μg/ml和25μg/ml的提取物A处理,这两个浓度分别等于IC10和IC50。结果(图14)表明两种浓度的提取物A都可以在处理后24小时使处于G0/G1期的细胞数增加。对照组处于G0/G1期的细胞数占39%,而提取物A处理组处于G0/G1期的细胞数达到60%。随着处于G0/G1期的细胞增多,最大浓度组处于G2/M期的细胞也有轻微增多。处理后24小时所观察到的结果在处理后72小时消失。处于不同细胞周期的细胞百分数确实没有明显的改变。
J82细胞对提取物基本不敏感(cfr.MTT试验)。流式细胞术所用的浓度相当于IC10和IC30(图15)。在两种检测浓度下,处理24小时后处于G0/G1的细胞出现轻微积聚。但是用50μg/ml和100μg/ml的提取物A处理细胞72小时后处于S期的细胞分别占到30%和47%,而对照组只有18%。100μg/ml时也可以观察到G2/M期细胞的积聚。
用0.05μg/ml的提取物A处理Hs683细胞后24小时可观察到处于G0/G1期细胞的积聚,约占细胞总数的70%,而对照组为58%(图16)。相应的,处于S期的细胞数减少。同样,在两种浓度下,处理72小时后大多数细胞处于G0/G1期。有60%以上的细胞处于这一周期,而对照组处于这一周期的细胞占细胞总数的46%。
总之,提取物A主要诱导G0/G1期细胞的积聚,说明提取物A具有细胞增殖抑制效应。
实施例4本发明提取物的促凋亡效应
本实施例说明了本发明提取物的促凋亡效应。
细胞死亡以两种途径发生,一种是意外发生的,一种是受遗传程序控制的。细胞的意外死亡也被称为坏死,这是物理损伤或生物损伤的结果。凋亡是指遗传程序控制的细胞死亡,正常生理条件下就会发生。凋亡被诱导以后,细胞内会发生一系列事件,如细胞死亡受体的活化、一系列细胞溶解蛋白酶的活化、凋亡小体的形成、DNA的片段化。
用4株人源细胞系检测提取物A对凋亡通路的影响:Hs683(胶质瘤)、J82(膀胱癌)、A172(胶质瘤)和HCT-15(结肠癌)。
将细胞接种到含7ml培养基的培养瓶(面积为25cm2)内。37℃孵育48小时后用含提取物A的新鲜培养基换液,提取物A的浓度分别为可以杀死50%细胞和30%细胞的浓度。加入提取物后24或72小时收获悬液中的细胞并计数。4℃、1700rpm离心10分钟收获250,000个细胞。沉淀下来的细胞团用4℃的PBS洗涤,然后在黑暗处与4℃的膜联蛋白V-FITC和碘化丙啶溶液孵育15分钟。每个样品计数约10,000个细胞,所得到的数值用对数值记录。用流式细胞仪附带的软件精确分析发生凋亡和/或坏死的细胞所占的百分数以及正常细胞所占的百分数。每个试验重复两次,计算发生凋亡及坏死的细胞百分数的平均值及其标准差。每个处理组都与对照组,即未处理的细胞相比较。
与对照细胞相比,用0.25μg/ml的提取物A处理24小时后,发生凋亡的HCT-15细胞增加40倍(图17)。用25μg/ml的提取物A处理24小时后,A172细胞系也会发生凋亡和坏死(图18)。这种趋势可以维持到处理后72小时。提取物A可以浓度依赖的方式诱导J82细胞的凋亡,在处理后72小时特别明显(图19)。两种浓度的药物处理72小时后可以观察到坏死细胞所占的百分数也有提高。用0.025μg/ml的提取物A处理24小时后,发生凋亡的Hs683细胞所占百分数增加2.5倍(图20)。处理后72小时凋亡细胞百分数是以剂量依赖的方式增加的。
总之,提取物A主要是使凋亡细胞所占的比例增加。在某些条件下可以观察到提取物A对坏死通路的影响。
实施例5本发明提取物的最大耐受剂量
在本实施例中确定了本发明提取物A的MTD指数。某种药物的最大耐受剂量(MTD)被定义为所能给健康动物,如未移植肿瘤的动物,腹腔、静脉、皮下注射或口服一次药物的最大剂量。
确定提取物A的MTD指数所需要的试验条件如下。记录未移植肿瘤小鼠的存活期到注射后14天。用6种不同剂量的提取物A确定其MTD指数。给予荷瘤小鼠的最大剂量为160mg/kg。其他剂量有5mg/kg、10mg/kg、20mg/kg、40mg/kg和80mg/kg。每个确定MTD指数的试验组包括两只小鼠。下面的表4给出了计算提取物A的MTD指数所需要的数据。
表4 确定本发明提取物A的MTD指数
| 提取物A的给药剂量(mg/kg) | 给药后1天 | 给药后14天 |
| 1×5 | -- | -- |
| 1×10 | -- | -- |
| 1×20 | -- | -- |
| 1×40 | x | |
| 1×80 | xx | |
| 1×160 | xx |
其中“x”代表一只死亡小鼠,“--”代表小鼠全部存活
根据上面的定义,提取物A给小鼠单次注射的MTD指数是20mg/kg。因此,提取物A的最大耐受剂量(MTD),即所能给健康动物注射的最大剂量,为20mg/kg提取物。这个数值说明提取物A的治疗窗口很大。
实施例6在3种肿瘤模型内评价本发明提取物的体内效应
本实施例说明了本发明的提取物A在3种肿瘤模型内的体内效应。
在移植了不同类型肿瘤的小鼠体内研究提取物A的体内效应,这些肿瘤包括淋巴瘤、黑色素瘤和乳腺癌。用3类参数来评价体内效应:
-累积毒性,通过记录荷瘤小鼠在治疗期间体重的变化来评价
-对肿瘤生长的实际影响水平,通过用卡钳每周3次测定肿瘤的大小来评价。肿瘤的实际生长水平用两个最大垂直直径相乘所得到的面积(mm2)来表示。
-处理小鼠的存活时间,用T/C指数来计算。这个指数是指处理组小鼠平均存活时间(T)与对照组小鼠平均存活时间(C)的比值。如果T/C值在130%以上,则提取物被认为是有活性的(P<0.05);如果T/C值在150%以上,则认为提取物的活性很高(P<0.01),如果T/C值在70%以下,则提取物被认为是有毒性的。
提取物A对淋巴瘤模型的体内效应
用攻击性P388淋巴瘤模型评价提取物A。第一次试验设3个剂量组,10mg/kg、5mg/kg和2.5mg/kg,分别与对照组比较。在D0天时小鼠皮下接种106 P388细胞,在随后的3周内共治疗9次,分别在移植后的D5天、D7天、D9天、D12天、D14天、D16天、D19天、D21天和D23天。每个试验组包括9只小鼠。
图21A说明提取物A对小鼠的体重没有影响。图21B说明提取物A可明显抑制P388淋巴瘤的生长。7×10mg/kg注射方案所得到的T/C为111%,6×5mg/kg注射方案所得到的T/C为100%,8×2.5mg/kg注射方案所得到的T/C为121%。总之,这些结果说明给予提取物A可抑制P388淋巴瘤的生长,但是各试验浓度的提取物A都不能明显延长PW88淋巴瘤荷瘤小鼠的生存期。
在第二组试验中,给药的次数从9次增加到16次,但是每次给药的剂量相应减少。皮下注射给药的剂量分别为2.5mg/kg、1.25mg/kg和0.63mg/kg。每日注射提取物A,每周注射5天,连续注射5周(5×5=25)。
图22说明0.63mg/kg和1.25mg/kg的活性提取物A对小鼠的毒性效应很小,因为P388淋巴瘤荷瘤小鼠在治疗期间体重没有减轻。图22A说明0.63mg/kg和1.25mg/kg的提取物A可明显抑制P33淋巴瘤的生长。另外,15×2.5mg/kg注射方案所得到的T/C为137%,15×1.25mg/kg注射方案所得到的T/C为137%,13×0.63mg/kg注射方案所得到的T/C为116%。因此,注射15次2.5mg/kg的提取物A及注射15次1.25mg/kg的提取物A可以使P388淋巴瘤荷瘤小鼠的生存期延长37%。说明用2.5mg/kg和1.25mg/kg的提取物A治疗可延长P388淋巴瘤荷瘤小鼠的生存期。
总之,本发明的提取物A对攻击性的P388淋巴瘤模型具有明显的抗肿瘤效应,并且不会导致被处理动物体重的下降。另外,意外地发现,本发明的提取物A用长期低剂量、即约1.25到0.63mg/kg,比用高剂量,即10到5mg/kg治疗具有更高的抗肿瘤活性。
提取物A对黑色素瘤模型的体内效应
用攻击性B16黑色素瘤模型评价提取物A。提取物A皮下注射给小鼠,剂量分别为10mg/kg、5mg/kg和2.5mg/kg。每日注射提取物A,每周注射5天,连续5周。
图23A说明该剂量的提取物A对小鼠的毒性效应很小,因为B16黑色素瘤荷瘤小鼠在治疗期间体重没有减轻。图23B说明2.5mg/kg或和1.25mg/kg的提取物A都可以明显抑制B16黑色素瘤的生长。另外,20×2.5mg/kg注射方案所得到的T/C为117%,20×1.25mg/kg注射方案所得到的T/C为117%,25×0.63mg/kg注射方案所得到的T/C为140%。因此,提取物A可抑制B16黑色素瘤的生长,显著延长B16黑色素瘤荷瘤小鼠的生存期,特别是注射提取物A25×0.63mg/kg时,所达到的水平具有统计学差异。
在第二组试验中,提取物A通过口服(per os)给药。
图24A说明该剂量的提取物A对小鼠的毒性效应很小,因为B16黑色素瘤荷瘤小鼠在治疗期间体重没有减轻。图24B说明口服2.5或1.25mg/kg的提取物A可明显抑制B16黑色素瘤的生长,抑制效应可持续到移植后25天。另外,19×2.5mg/kg给药方案所得到的T/C为114%,15×1.25mg/kg给药方案所得到的T/C为100%,16×0.63mg/kg给药方案所得到的T/C为104%。因此,2.5mg/kg的提取物A可抑制B16黑色素瘤的生长,稍微延长B16黑色素瘤荷瘤小鼠的生存期。
总之,两组试验的结果说明本发明的提取物A不论采取何种给药途径对B16黑色素瘤都具有明显的抗肿瘤效应。
提取物A对乳腺癌的体内效应
在MXT-HI乳腺癌模型上评价提取物A的效应,该模型是对激素不敏感的乳腺癌突变株。MXT-HI模型相当于具有肝脏高转移能力的未分化癌,因此相当于人的晚期乳腺癌。MXT-HI代表了一种高攻击性的肿瘤模型。
B6D2F1小鼠腹部皮下注射MXT肿瘤碎块在小鼠体内诱导MXT-HI乳腺癌模型。如果不加以治疗,接种后4到7周小鼠就会死亡。提取物A的给药剂量为10mg/kg、5mg/kg和2.5mg/kg,给药9次,即每周3次,连续3周。
图25A说明试验中所用的各种剂量的提取物A对小鼠都没有产生大的毒性效应,因为MXT-HI荷瘤小鼠没有出现体重的显著下降。图25B说明2.5mg/kg的提取物A给药9次可显著抑制MXT-HI肿瘤的生长。9×10mg/kg给药方案所得到的T/C为103%,9×5mg/kg给药方案所得到的T/C为103%,9×2.5mg/kg给药方案所得到的T/C为119%。因此,2.5mg/kg的提取物A可以延长MXT-HI荷瘤小鼠的生存期。
图26给出了对照组(未处理组)和试验组(用提取物处理)内MXT-HI乳腺癌荷瘤小鼠在试验期间死亡的数目。用Kaplan-Meier统计学分析计算每组中9只小鼠的死亡率。统计数值表明了试验组小鼠和对照组小鼠存活率的一般情况。
总之,上述试验的结果表明提取物A对MXT-HI乳腺癌具有明显的抗肿瘤效应。
实施例6的结论
本发明的提取物A对各种试验肿瘤模型都具有明显的抗肿瘤效应。这些模型代表了多个组织学类型的肿瘤,其中包括乳腺癌、淋巴瘤和黑色素瘤。这些模型是与临床相关的,因为它们模拟了人肿瘤的特殊临床阶段。除此之外,它们还具有生物攻击性和浸润性,因为其中的两个模型可以快速地转移到肝脏。
虽然本发明的提取物A具有很高的抗肿瘤活性,但是其毒性很小,因为在治疗期间荷瘤小鼠的体重都没有明显下降。因此,半纯化的提取物除了包含具有本文所述的各种抗肿瘤活性的抗肿瘤化合物以外,还包含“解毒剂”。
令人惊喜的是,本发明的提取物A用长期低剂量、即约1.25到0.63mg/kg,比用高剂量,即10到5mg/kg治疗具有更高的抗肿瘤活性。
实施例7本发明提取物的体内毒理学效应
本实施例说明了本发明提取物A的体内毒理学效应,特别是其在体内的血液毒性和一般毒性。
血液毒性
通过检测每个动物样品的造血系统指标来评价提取物的血液毒性。特别需要注意的是血小板、红细胞和白细胞的数量。通过给小鼠的腹腔内注射5mg/kg和1.25mg/kg的提取物A来评价其毒性效应。给药方案是每周5次,连续5周,共注射25次。最后一次注射后3天处死动物。每组10只动物。
与对照组相比,用提取物A处理后造血系统指标没有出现具有统计学意义的变化(图27)。红细胞的平均细胞体积、血球血红蛋白的平均体积、血球血红蛋白的平均浓度以及血小板的数量在治疗后没有出现明显变化。
一般毒性
通过小鼠的组织学检测来评价提取物A的一般毒性,制作不同类型的器官和组织的组织学切片,HE染色后进行常规的组织病理学分析。小鼠腹腔注射5mg/kg和1.25mg/kg的提取物A。给药方案是每周5次,连续5周,共注射25次。最后一次注射后3天处死动物。收集动物的脑、心、肝脏、胰腺、胃、小肠和卵巢。每组10只动物。
通过检测所收集的器官发现对照组(未处理组)小鼠的器官未出现任何特殊的变化。处理组小鼠的脑、心脏、肝脏、胰腺、胃、小肠和卵巢也未受5mg/kg或1.25mg/kg提取物A处理的影响,说明提取物A不产生一般毒性效应。
实施例8本发明提取物的抗毒性效应
本实施例说明了本发明提取物的抗毒性效应。给4到5周龄的雌性小鼠注射2倍或4倍最大耐受剂量的两种临床上常用的抗肿瘤药物阿霉酮(MTD×4)和长春新碱(MTD×2)。在第0天,给小鼠腹腔单次注射40mg/kg的阿霉酮或20mg/kg的长春新碱。图28中的Lot 1代表了注射MTD×2长春新碱或MTD×4阿霉酮的小鼠的存活曲线。
在注射抗肿瘤药物前给小鼠腹腔注射10mg/kg的本发明的提取物A。给药方案如下:
-在注射治疗性化合物阿霉酮或长春新碱的同一天(即第0天)但是是在注射前4小时注射提取物A。这种治疗方案所得到的结果由图28的lot 2代表。
-在注射治疗性化合物阿霉酮或长春新碱前注射提取物A,每天注射一次,共注射8天。这种治疗方案所得到的结果由图28的lot 3代表。
-在注射治疗性化合物阿霉酮或长春新碱前注射提取物A,每天注射一次,共注射8天,然后再于注射抗肿瘤药物后注射提取物A,每天注射一次,共注射7天。这种治疗方案所得到的结果由图28的lot 4代表。
如图28所示,提取物A与治疗性化合物联合用药的所有方案与只注射治疗性化合物的给药方案相比都可以显著延长小鼠的生存期。
第二个例子说明了提取物A用其他给药方法时的抗毒性效应。在第0天时给小鼠腹腔单次注射20mg/kg的长春新碱。图29中的Lot 1代表了注射长春新碱的小鼠的存活曲线。
在注射抗肿瘤药物前或同时给小鼠腹腔注射10mg/kg的本发明的提取物A。给药方案如下:
-在注射治疗性化合物长春新碱的同一天(即第0天)但是是在注射前6小时注射提取物A。这种治疗方案所得到的结果由图29的lot 2代表。
-在注射治疗性化合物长春新碱的同一天(即第0天)但是是在注射前4小时注射提取物A。这种治疗方案所得到的结果由图29的lot 3代表。
-在注射治疗性化合物长春新碱的同一天(即第0天)但是是在注射前2小时注射提取物A。这种治疗方案所得到的结果由图29的lot 4代表。
-在注射治疗性化合物长春新碱的同一天(即第0天)并且是同时注射提取物A。这种治疗方案所得到的结果由图29的lot 5代表。
确定提取物A对抗肿瘤药物的毒性效应的保护作用,即抗毒性效应的参数是“生存期的延长时间”。用Kaplan-Meier统计学方法进行统计学分析。显著差异的水平定义为p<0.05。
如图29所示,与只注射治疗性化合物的给药方案相比,注射长春新碱前3小时注射提取物A的给药方案(lot 3)可显著延长小鼠的生存期。
因此可以得出结论:提取物A能够明显保护小鼠不受一些致死剂量的常用抗肿瘤药物如阿霉酮或长春新碱的毒性效应的影响。因此本发明的提取物A具有抗毒性效应,通过其抗毒性效应可以降低已知的抗肿瘤化合物的毒性效应。
第三个例子说明了提取物B的抗毒性效应。给4到5周龄的雌性小鼠注射四种临床上常用的抗肿瘤化合物:阿霉酮、长春新碱、奥沙利铂和喜树碱。在第0天时,给小鼠腹腔单次注射20mg/kg的阿霉酮、20mg/kgd的长春新碱、40mg/kg的奥沙利铂或20mg/kg的喜树碱。
图30、31、32、33中的lot 1代表了注射阿霉酮、长春新碱、奥沙利铂或喜树碱的小鼠的存活曲线。
图30到33中的lot 2代表了注射10mg/kg提取物B的小鼠的“存活时间点”。
图30到33中的lot 3代表了在注射治疗性化合物的同一天(即第0天)但是是在注射前4小时注射10mg/kg提取物B的小鼠的存活曲线。从图30到33中可以看出,与只注射治疗性化合物相比,提取物B与治疗性化合物联合使用可显著延长小鼠的生存期。用Kaplan-Meier统计学方法进行统计学分析。每一组提取物B和治疗性化合物联合用药的统计学差异水平都是p<0.05。
因此可以得出结论:提取物B能够明显保护小鼠不受一些致死剂量的常用抗肿瘤药物的毒性效应的影响。因此本发明的提取物B具有抗毒性效应,通过其抗毒性效应可以降低已知的抗肿瘤药物的毒性效应。与提取物A一样,提取物B也具有抗毒活性。
第四个例子说明了提取物C的抗毒性效应。提取物C与20mg/kg的阿霉酮联合使用。
图34中的lot 1代表了注射20mg/kg阿霉酮的小鼠的存活曲线。
图34中的lot 2代表了在注射治疗性化合物的同一天(即第0天)但是是在注射前4小时注射10mg/kg提取物C的小鼠的存活曲线。
从图34中可以看出,与只注射治疗性化合物相比,注射提取物C可明显延长小鼠的生存期。因此可以得出结论:提取物C与上述的提取物B一样具有抗毒活性。
第五个例子说明了提取物D的抗毒性效应。给4到5周龄的雌性小鼠注射阿霉酮。在第0天给小鼠腹腔单次注射20mg/kg的阿霉酮(图35中的Lot 1)。图35中的Lot 2代表了在注射治疗性化合物阿霉酮的同一天(即第0天)但是是在注射前4小时注射5mg/kg提取物D的小鼠的存活曲线。
如图35所示,与只注射治疗性化合物相比,注射提取物D可明显延长小鼠的生存期。因此可以得出结论:提取物D与上述的提取物C一样具有抗毒活性。
总之,这些试验说明了与只注射治疗性化合物相比,本发明的纯化提取物可显著延长小鼠的生存期。提取物D是最纯的提取物,对抗肿瘤药物的毒性效应具有抗毒活性。
Claims (14)
1.一种包含白花牛角瓜提取物和至少一种治疗性化合物的组合物在制备癌症治疗药物中的应用,其中,所述治疗性化合物和/或物理治疗措施对正常的非癌细胞、组织或器官具有一定毒副作用。
2.如权利要求1所述的组合物的应用,其中,所述提取物是通过包括如下步骤的提取方法获得的:
a)在脂肪族醇中提取所述白花牛角瓜植物的起始原料,所述起始原料选自果实、地上部分、地下部分或其混合物,利用所述醇溶解起始原料获得所述原料的脂肪族醇悬液,搅拌所述悬液,用多孔玻璃过滤所述悬液从而得到第一滤液和第一固体组分;
b)用脂肪族醇提取所述第一固体组分从而得到第二滤液和第二固体组分;
c)混合所述第一滤液和第二滤液得到混合滤液,在真空下蒸发所述混合滤液从而得到所述提取物。
3.如权利要求1或2所述组合物的应用,其中,所述提取物含有至少两种选自如下一组的活性化合物:马利筋苷、异牛角瓜甙、弗汝沙林、牛角瓜苷、牛角瓜苷元、乌沙苷元、卡洛托星、乌沙林、乌沙利定和2"-氧-弗汝沙林。
4.如权利要求1所述的组合物的应用,其中,所述提取物:治疗性化合物的重量比为0.001:1-1000:1。
5.如权利要求1所述的组合物的应用,其中,所述肿瘤选自:乳腺癌、淋巴瘤、肉瘤、胰腺癌、黑色素瘤、结肠癌、胶质瘤、非小细胞肺癌、小细胞肺癌、皮肤癌、骨癌、卵巢癌、CNS癌、肾癌、膀胱癌、头颈癌、前列腺癌、肝癌、血癌。
6.如权利要求1所述的组合物的应用,其中,所述治疗性化合物是抗癌药。
7.如权利要求6所述的组合物的应用,其中,所述治疗性化合物选自:阿霉素、爱克兰、阿糖胞嘧啶、博来霉素、卡氮芥、白消安、环已亚硝脲、卡铂、顺铂、环磷酰胺、癌得星、柔红霉素、达卡巴嗪、5-氟尿嘧啶、氟达拉滨、吉西他滨、赫赛汀、六甲密胺、羟脲、伊达比星、异环磷酰胺、依立替康、克拉立平、氨甲蝶呤、光辉霉素、丝裂霉素、二羟基蒽酮、武活龙、诺维本、氮芥、奥沙利铂、美罗华、甲磺酸伊马替尼、链脲菌素、紫杉醇、泰索帝、托泊替康、硫酸长春碱、长春新碱、依托泊甙、希罗达或泽娃灵。
8.如权利要求1所述的组合物的应用,其中,所述治疗性化合物是细胞毒性抗体或其片段。
9.如权利要求1所述的组合物的应用,其中,所述治疗性化合物是细胞毒性激素或其片段。
10.如权利要求1所述的组合物的应用,其中,所述治疗性化合物是细胞毒性肽或其片段。
11.如权利要求1所述的组合物的应用,其中,所述提取物和所述治疗性化合物分别包装。
12.一种获得包含生物活性成分的提取物的提取方法,其特征在于,所述方法包括以下步骤:
a)在脂肪族醇中提取所述白花牛角瓜植物的起始原料,所述起始原料选自果实、地上部分、地下部分或其混合物,利用所述醇溶解起始原料获得所述原料的脂肪族醇悬液,搅拌所述悬液;用多孔玻璃过滤所述悬液从而得到第一滤液和第一固体组分;
b)用脂肪族醇提取所述第一固体组分从而得到第二滤液和第二固体组分;
c)混合所述第一滤液和第二滤液得到混合滤液;以及
d)在真空下蒸发所述混合滤液从而得到所述提取物。
13.用权利要求12所述方法分离的活性提取物。
14.一种试剂盒,其特征在于,所述试剂盒包括一个装有如权利要求1-11中任一项所述的白花牛角瓜提取物的容器和一个装有治疗性化合物的容器。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/EP2002/011310 WO2004032947A1 (en) | 2002-10-09 | 2002-10-09 | Extract with anti-tumor and anti-poisonous activity |
| EPPCT/EP02/11310 | 2002-10-09 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1711099A CN1711099A (zh) | 2005-12-21 |
| CN100522184C true CN100522184C (zh) | 2009-08-05 |
Family
ID=32087933
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB2003801031172A Expired - Fee Related CN100522184C (zh) | 2002-10-09 | 2003-10-09 | 具有抗肿瘤和抗毒活性的提取物 |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US20060057237A1 (zh) |
| EP (1) | EP1549329B1 (zh) |
| JP (1) | JP4944380B2 (zh) |
| CN (1) | CN100522184C (zh) |
| AT (1) | ATE349221T1 (zh) |
| AU (2) | AU2002342808A1 (zh) |
| CA (1) | CA2501240A1 (zh) |
| DE (1) | DE60310742T2 (zh) |
| DK (1) | DK1549329T3 (zh) |
| ES (1) | ES2279157T3 (zh) |
| HK (1) | HK1082663A1 (zh) |
| MX (1) | MXPA05003634A (zh) |
| PT (1) | PT1549329E (zh) |
| WO (2) | WO2004032947A1 (zh) |
| ZA (1) | ZA200502790B (zh) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20080280995A1 (en) * | 2004-04-10 | 2008-11-13 | All India Institute Of Medical Sciences | Extracts of Latex of Calotropis Procera and to a Method of Preparation Thereof |
| CN101647790B (zh) * | 2006-11-23 | 2011-10-26 | 樊献俄 | 三十烷醇在制备抗癌药物中的应用 |
| CN101190210B (zh) * | 2006-11-23 | 2010-05-12 | 樊献俄 | 三十烷醇在制备抗癌药物中的应用 |
| CN101391998B (zh) * | 2008-09-25 | 2012-07-04 | 成都普思生物科技有限公司 | 一种喜树碱的高效分离纯化方法 |
| MY179036A (en) * | 2012-12-13 | 2020-10-26 | Malaysian Palm Oil Board | Anti-proliferative effects of palm vegetation liquor and extracts thereof in preventing pancreatic cancer |
| CN104398532B (zh) * | 2013-04-11 | 2017-02-22 | 中国热带农业科学院热带作物品种资源研究所 | 一种强心苷化合物的用途 |
| US9533019B1 (en) * | 2016-03-02 | 2017-01-03 | King Saud University | Calotropis procera extracts as anti-ulcerative colitis agents |
| IL256648A (en) | 2017-12-28 | 2018-02-28 | Ahava Dead Sea Laboratories Ltd | Cosmetic preparations containing Sodom apple extract |
| US10111918B1 (en) | 2018-03-02 | 2018-10-30 | King Saud University | Method of preparing biologically active derivatives from Calotropis gigantea flowers |
| CN111214478B (zh) * | 2020-02-24 | 2023-08-08 | 海南医学院 | 弗如糖苷在制备治疗和/或预防滑膜相关疾病的药物中的用途 |
| CN112194703B (zh) * | 2020-09-03 | 2021-08-03 | 澳门科技大学 | 一种强心苷类化合物及其合成方法与应用 |
| CN114831997A (zh) * | 2022-06-07 | 2022-08-02 | 南昌大学第一附属医院 | 抑制结直肠癌细胞增殖药物及蒲公英甾醇的应用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4904697A (en) * | 1987-04-09 | 1990-02-27 | Merrell Dow Pharmaceuticals Inc. | Controlling the growth of certain tumor tissue with chalcone derivatives |
| CA2136091A1 (en) * | 1992-05-20 | 1993-11-25 | Daniel S. Martin | Chemotherapeutic drug combinations |
| US5916596A (en) * | 1993-02-22 | 1999-06-29 | Vivorx Pharmaceuticals, Inc. | Protein stabilized pharmacologically active agents, methods for the preparation thereof and methods for the use thereof |
| GB9710698D0 (en) * | 1997-05-24 | 1997-07-16 | Verkaik Margaretha S E | Composition |
| US8029561B1 (en) * | 2000-05-12 | 2011-10-04 | Cordis Corporation | Drug combination useful for prevention of restenosis |
| AU2002246827B2 (en) * | 2000-12-22 | 2008-02-21 | Bristol-Myers Squibb Company | Methods for modulating tumor growth and metastasis |
-
2002
- 2002-10-09 WO PCT/EP2002/011310 patent/WO2004032947A1/en not_active Application Discontinuation
- 2002-10-09 AU AU2002342808A patent/AU2002342808A1/en not_active Abandoned
-
2003
- 2003-10-09 AT AT03757940T patent/ATE349221T1/de active
- 2003-10-09 US US10/530,905 patent/US20060057237A1/en not_active Abandoned
- 2003-10-09 WO PCT/EP2003/011192 patent/WO2004032948A1/en active IP Right Grant
- 2003-10-09 DK DK03757940T patent/DK1549329T3/da active
- 2003-10-09 AU AU2003273973A patent/AU2003273973B2/en not_active Ceased
- 2003-10-09 PT PT03757940T patent/PT1549329E/pt unknown
- 2003-10-09 DE DE60310742T patent/DE60310742T2/de not_active Expired - Lifetime
- 2003-10-09 CA CA002501240A patent/CA2501240A1/en not_active Abandoned
- 2003-10-09 CN CNB2003801031172A patent/CN100522184C/zh not_active Expired - Fee Related
- 2003-10-09 EP EP03757940A patent/EP1549329B1/en not_active Expired - Lifetime
- 2003-10-09 MX MXPA05003634A patent/MXPA05003634A/es active IP Right Grant
- 2003-10-09 JP JP2004542473A patent/JP4944380B2/ja not_active Expired - Fee Related
- 2003-10-09 ES ES03757940T patent/ES2279157T3/es not_active Expired - Lifetime
-
2005
- 2005-04-06 ZA ZA200502790A patent/ZA200502790B/xx unknown
-
2006
- 2006-01-06 HK HK06100309A patent/HK1082663A1/xx not_active IP Right Cessation
Non-Patent Citations (2)
| Title |
|---|
| 白花牛角瓜根氯仿提取物抗胃溃疡作用的实验研究. 杜海燕.国外医学.中医中药分册,第20卷第3期. 1998 |
| 白花牛角瓜根氯仿提取物抗胃溃疡作用的实验研究. 杜海燕.国外医学.中医中药分册,第20卷第3期. 1998 * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP1549329B1 (en) | 2006-12-27 |
| DK1549329T3 (da) | 2007-05-07 |
| MXPA05003634A (es) | 2005-12-14 |
| CN1711099A (zh) | 2005-12-21 |
| JP4944380B2 (ja) | 2012-05-30 |
| AU2002342808A1 (en) | 2004-05-04 |
| ZA200502790B (en) | 2006-02-22 |
| WO2004032947A1 (en) | 2004-04-22 |
| AU2003273973A1 (en) | 2004-05-04 |
| PT1549329E (pt) | 2007-03-30 |
| WO2004032948A1 (en) | 2004-04-22 |
| DE60310742T2 (de) | 2007-10-11 |
| HK1082663A1 (en) | 2006-06-16 |
| ATE349221T1 (de) | 2007-01-15 |
| US20060057237A1 (en) | 2006-03-16 |
| DE60310742D1 (de) | 2007-02-08 |
| AU2003273973B2 (en) | 2008-11-20 |
| JP2006503872A (ja) | 2006-02-02 |
| CA2501240A1 (en) | 2004-04-22 |
| ES2279157T3 (es) | 2007-08-16 |
| EP1549329A1 (en) | 2005-07-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN100522184C (zh) | 具有抗肿瘤和抗毒活性的提取物 | |
| US9005678B1 (en) | Pharmaceutical composition for treating cancer and use thereof | |
| CN101485655A (zh) | 二氢杨梅素在制备防治肿瘤放化疗不良反应的药物的应用 | |
| CN102488682A (zh) | 绿原酸的抗癌新用途 | |
| CN109320570A (zh) | 一种淫羊藿次苷ⅰ类化合物、衍生物、可药用盐及应用 | |
| CN108498497A (zh) | 用于治疗肾癌的药物组合物及其应用 | |
| KR20190124197A (ko) | 종양 치료용 한약 조성물 및 그 제조방법 및 응용 | |
| CN104013636A (zh) | 瓦草五环三萜皂苷类化合物抗肿瘤的药物用途 | |
| CN108310080A (zh) | 黑果腺肋花楸花色苷在制备抗肝纤维化药品或保健品中的应用 | |
| CN106309758B (zh) | 一种抗胃肠癌的药物组合物 | |
| CN115300624A (zh) | 人参皂苷联合pd-1阻断剂在制备抗头颈鳞癌药物中的应用 | |
| CN108703979A (zh) | 一种基于无柄灵芝提取物的乳腺癌肿瘤治疗用药 | |
| CN111249274B (zh) | 银杏内酯b在制备胶质瘤细胞活性抑制剂中的应用 | |
| CN1824184A (zh) | 一种治疗肺癌的药物 | |
| CN110279862B (zh) | 一种抗癌组合物及其在制备治疗骨肉瘤的药物中的应用 | |
| CN104688722B (zh) | 淫羊藿苷元在制备预防或治疗骨髓抑制药物中的用途 | |
| CN107708728A (zh) | 一种用于治疗胃癌的肿瘤疫苗及其制备方法 | |
| CN102579419B (zh) | 绿原酸的抗癌用途 | |
| CN105030798B (zh) | 一种抗肿瘤的药物组合物及其制备方法和应用 | |
| CN109820879A (zh) | 牛樟芝萃取物、牛樟芝组合物的制备方法及医药组合物 | |
| CN1331468C (zh) | 一种用于治疗癌症的植物提取物 | |
| CN101156841A (zh) | 一种联苯乙酸及其盐的抗肿瘤新用途 | |
| CN106974902A (zh) | 洛铂在制备治疗恶性胸膜间皮瘤药物中的应用 | |
| CN104840463B (zh) | 一种促进肺癌细胞凋亡的药物组合物以及检测方法 | |
| CN104116778B (zh) | 一种中药组合物、其提取物及应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20090805 Termination date: 20131009 |