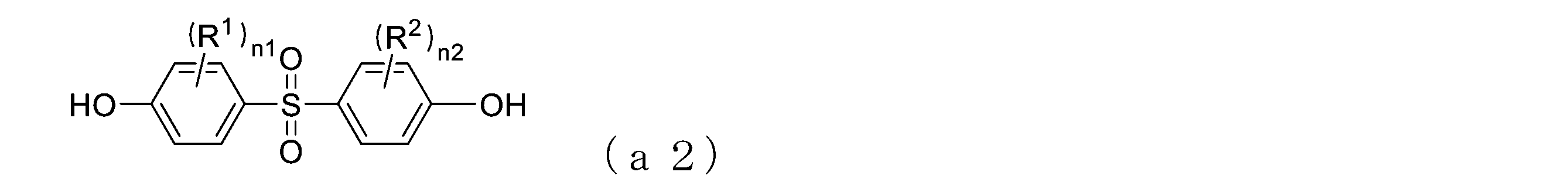WO2023033164A1 - ブロックコポリマー - Google Patents
ブロックコポリマー Download PDFInfo
- Publication number
- WO2023033164A1 WO2023033164A1 PCT/JP2022/033206 JP2022033206W WO2023033164A1 WO 2023033164 A1 WO2023033164 A1 WO 2023033164A1 JP 2022033206 W JP2022033206 W JP 2022033206W WO 2023033164 A1 WO2023033164 A1 WO 2023033164A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- block
- block copolymer
- aromatic polysulfone
- polyoxyalkylene
- group
- Prior art date
Links
- 229920001400 block copolymer Polymers 0.000 title claims abstract description 160
- 125000003118 aryl group Chemical group 0.000 claims abstract description 152
- 229920002492 poly(sulfone) Polymers 0.000 claims abstract description 140
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 78
- 238000005259 measurement Methods 0.000 claims abstract description 34
- 238000005160 1H NMR spectroscopy Methods 0.000 claims abstract description 24
- 238000001228 spectrum Methods 0.000 claims abstract description 14
- 125000004432 carbon atom Chemical group C* 0.000 claims description 25
- 229920000642 polymer Polymers 0.000 claims description 21
- 125000002947 alkylene group Chemical group 0.000 claims description 9
- 125000000217 alkyl group Chemical group 0.000 claims description 8
- 229920000428 triblock copolymer Polymers 0.000 claims description 8
- 229920000359 diblock copolymer Polymers 0.000 claims description 7
- 125000005843 halogen group Chemical group 0.000 claims description 7
- 239000012528 membrane Substances 0.000 description 57
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 48
- 150000001875 compounds Chemical class 0.000 description 28
- 239000002904 solvent Substances 0.000 description 27
- 238000000926 separation method Methods 0.000 description 26
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 25
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 25
- 238000006243 chemical reaction Methods 0.000 description 20
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 20
- 239000000243 solution Substances 0.000 description 20
- 239000004695 Polyether sulfone Substances 0.000 description 18
- 229920006393 polyether sulfone Polymers 0.000 description 18
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 18
- 238000012360 testing method Methods 0.000 description 17
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- 238000004519 manufacturing process Methods 0.000 description 15
- 238000001914 filtration Methods 0.000 description 12
- -1 2-ethylhexyl group Chemical group 0.000 description 11
- 238000009835 boiling Methods 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- 239000000203 mixture Substances 0.000 description 9
- 229910000027 potassium carbonate Inorganic materials 0.000 description 9
- 235000011181 potassium carbonates Nutrition 0.000 description 9
- 125000001309 chloro group Chemical group Cl* 0.000 description 8
- 238000005227 gel permeation chromatography Methods 0.000 description 8
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 8
- 239000002798 polar solvent Substances 0.000 description 8
- 239000003513 alkali Substances 0.000 description 7
- 229910052783 alkali metal Inorganic materials 0.000 description 7
- 238000004364 calculation method Methods 0.000 description 7
- 230000000052 comparative effect Effects 0.000 description 7
- 239000003960 organic solvent Substances 0.000 description 7
- 229920001223 polyethylene glycol Polymers 0.000 description 7
- 238000011084 recovery Methods 0.000 description 7
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 6
- 239000002202 Polyethylene glycol Substances 0.000 description 6
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 6
- 229940098773 bovine serum albumin Drugs 0.000 description 6
- 239000012778 molding material Substances 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- 239000002244 precipitate Substances 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 5
- 229910052799 carbon Inorganic materials 0.000 description 5
- 238000000034 method Methods 0.000 description 5
- 238000000465 moulding Methods 0.000 description 5
- 239000002994 raw material Substances 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 125000001424 substituent group Chemical group 0.000 description 5
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 238000000149 argon plasma sintering Methods 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 239000003480 eluent Substances 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 230000035699 permeability Effects 0.000 description 4
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 3
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 239000006227 byproduct Substances 0.000 description 3
- 229960001760 dimethyl sulfoxide Drugs 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 238000006068 polycondensation reaction Methods 0.000 description 3
- 239000001103 potassium chloride Substances 0.000 description 3
- 235000011164 potassium chloride Nutrition 0.000 description 3
- 239000011342 resin composition Substances 0.000 description 3
- 125000001140 1,4-phenylene group Chemical group [H]C1=C([H])C([*:2])=C([H])C([H])=C1[*:1] 0.000 description 2
- ZNQVEEAIQZEUHB-UHFFFAOYSA-N 2-ethoxyethanol Chemical compound CCOCCO ZNQVEEAIQZEUHB-UHFFFAOYSA-N 0.000 description 2
- XLLIQLLCWZCATF-UHFFFAOYSA-N 2-methoxyethyl acetate Chemical compound COCCOC(C)=O XLLIQLLCWZCATF-UHFFFAOYSA-N 0.000 description 2
- GPAPPPVRLPGFEQ-UHFFFAOYSA-N 4,4'-dichlorodiphenyl sulfone Chemical compound C1=CC(Cl)=CC=C1S(=O)(=O)C1=CC=C(Cl)C=C1 GPAPPPVRLPGFEQ-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- YNQLUTRBYVCPMQ-UHFFFAOYSA-N Ethylbenzene Chemical compound CCC1=CC=CC=C1 YNQLUTRBYVCPMQ-UHFFFAOYSA-N 0.000 description 2
- 230000005526 G1 to G0 transition Effects 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- 239000004353 Polyethylene glycol 8000 Substances 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- 229910000288 alkali metal carbonate Inorganic materials 0.000 description 2
- 150000008041 alkali metal carbonates Chemical class 0.000 description 2
- 125000000732 arylene group Chemical group 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 229940057838 polyethylene glycol 4000 Drugs 0.000 description 2
- 229940085678 polyethylene glycol 8000 Drugs 0.000 description 2
- 235000019446 polyethylene glycol 8000 Nutrition 0.000 description 2
- 229910000028 potassium bicarbonate Inorganic materials 0.000 description 2
- 235000015497 potassium bicarbonate Nutrition 0.000 description 2
- 239000011736 potassium bicarbonate Substances 0.000 description 2
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 2
- 239000008213 purified water Substances 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 238000009987 spinning Methods 0.000 description 2
- 230000003068 static effect Effects 0.000 description 2
- HHVIBTZHLRERCL-UHFFFAOYSA-N sulfonyldimethane Chemical compound CS(C)(=O)=O HHVIBTZHLRERCL-UHFFFAOYSA-N 0.000 description 2
- JXTGICXCHWMCPM-UHFFFAOYSA-N (methylsulfinyl)benzene Chemical compound CS(=O)C1=CC=CC=C1 JXTGICXCHWMCPM-UHFFFAOYSA-N 0.000 description 1
- 125000002030 1,2-phenylene group Chemical group [H]C1=C([H])C([*:1])=C([*:2])C([H])=C1[H] 0.000 description 1
- CYSGHNMQYZDMIA-UHFFFAOYSA-N 1,3-Dimethyl-2-imidazolidinon Chemical compound CN1CCN(C)C1=O CYSGHNMQYZDMIA-UHFFFAOYSA-N 0.000 description 1
- 125000001989 1,3-phenylene group Chemical group [H]C1=C([H])C([*:1])=C([H])C([*:2])=C1[H] 0.000 description 1
- ZFPGARUNNKGOBB-UHFFFAOYSA-N 1-Ethyl-2-pyrrolidinone Chemical compound CCN1CCCC1=O ZFPGARUNNKGOBB-UHFFFAOYSA-N 0.000 description 1
- MBDUIEKYVPVZJH-UHFFFAOYSA-N 1-ethylsulfonylethane Chemical compound CCS(=O)(=O)CC MBDUIEKYVPVZJH-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- SVONRAPFKPVNKG-UHFFFAOYSA-N 2-ethoxyethyl acetate Chemical compound CCOCCOC(C)=O SVONRAPFKPVNKG-UHFFFAOYSA-N 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- VPWNQTHUCYMVMZ-UHFFFAOYSA-N 4,4'-sulfonyldiphenol Chemical compound C1=CC(O)=CC=C1S(=O)(=O)C1=CC=C(O)C=C1 VPWNQTHUCYMVMZ-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- 101100062433 Arabidopsis thaliana DHDPS1 gene Proteins 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 1
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 1
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 1
- SUAKHGWARZSWIH-UHFFFAOYSA-N N,N‐diethylformamide Chemical compound CCN(CC)C=O SUAKHGWARZSWIH-UHFFFAOYSA-N 0.000 description 1
- ZWXPDGCFMMFNRW-UHFFFAOYSA-N N-methylcaprolactam Chemical compound CN1CCCCCC1=O ZWXPDGCFMMFNRW-UHFFFAOYSA-N 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 238000000071 blow moulding Methods 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 238000005266 casting Methods 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 229920000547 conjugated polymer Polymers 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 238000001125 extrusion Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 238000001879 gelation Methods 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 125000004836 hexamethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 238000001746 injection moulding Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 150000002596 lactones Chemical class 0.000 description 1
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- AJFDBNQQDYLMJN-UHFFFAOYSA-N n,n-diethylacetamide Chemical compound CCN(CC)C(C)=O AJFDBNQQDYLMJN-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- NEVPGZLSKXATIM-UHFFFAOYSA-N n-dimethoxyphosphoryl-n-methylmethanamine Chemical compound COP(=O)(OC)N(C)C NEVPGZLSKXATIM-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- QJQAMHYHNCADNR-UHFFFAOYSA-N n-methylpropanamide Chemical compound CCC(=O)NC QJQAMHYHNCADNR-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 125000003261 o-tolyl group Chemical group [H]C1=C([H])C(*)=C(C([H])=C1[H])C([H])([H])[H] 0.000 description 1
- 125000005702 oxyalkylene group Chemical group 0.000 description 1
- 125000001037 p-tolyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- 239000012466 permeate Substances 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 229940086066 potassium hydrogencarbonate Drugs 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 150000003457 sulfones Chemical class 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- 125000003258 trimethylene group Chemical group [H]C([H])([*:2])C([H])([H])C([H])([H])[*:1] 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/34—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from hydroxy compounds or their metallic derivatives
- C08G65/38—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from hydroxy compounds or their metallic derivatives derived from phenols
- C08G65/40—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from hydroxy compounds or their metallic derivatives derived from phenols from phenols (I) and other compounds (II), e.g. OH-Ar-OH + X-Ar-X, where X is halogen atom, i.e. leaving group
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G81/00—Macromolecular compounds obtained by interreacting polymers in the absence of monomers, e.g. block polymers
Definitions
- the present invention relates to block copolymers. This application claims priority based on Japanese Patent Application No. 2021-144891 filed in Japan on September 6, 2021, the content of which is incorporated herein.
- Aromatic polysulfone is used for various purposes due to its excellent heat resistance and chemical resistance. Depending on the application, a hydrophilized aromatic polysulfone may be required.
- block copolymers having aromatic polysulfone as a polymer chain have been produced.
- a block copolymer containing an aromatic polysulfone block and a polyoxyalkylene block tends to have excellent hydrophilicity.
- US Pat. No. 6,200,008 discloses a method for making polyarylethersulfone-polyalkyleneoxide-block copolymers.
- Aromatic polysulfone is sometimes used as a molding material for separation membranes, and it is desirable that the resulting separation membranes are less prone to fouling.
- the present invention has been made to solve the above problems, and is a block copolymer containing an aromatic polysulfone block and a polyoxyalkylene block, which is suitable as a separation membrane molding material having excellent fouling resistance. It is an object of the present invention to provide a block copolymer having a
- a block copolymer containing an aromatic polysulfone block and a polyoxyalkylene block and having at least one terminal OH group at the main chain end has 1 H-NMR measurement.
- the fouling resistance of the separation membrane obtained by setting the number of terminal OH groups per 100 structural units constituting the aromatic polysulfone block to a specific range, calculated from the peak area of the spectrum obtained by can be improved, and have completed the present invention. That is, the present invention has the following aspects.
- a block copolymer comprising an aromatic polysulfone block (A) and a polyoxyalkylene block (B),
- the block copolymer has at least one terminal OH group at the main chain end,
- the number of terminal OH groups per 100 structural units constituting the aromatic polysulfone block (A), calculated from the peak area of the spectrum obtained by 1 H-NMR measurement, is 0.43 or more.
- a block copolymer that is ⁇ 2> The polyoxyalkylene block (B) per 100 structural units constituting the aromatic polysulfone block (A) calculated from the peak area of the spectrum obtained by 1 H-NMR measurement
- the aromatic polysulfone block (A) comprises a polymer chain having a structural unit represented by the following general formula (1): copolymer.
- R 1 and R 2 each independently represent an alkyl group having 1 to 10 carbon atoms, an aryl group having 6 to 20 carbon atoms or a halogen atom; n1 and n2 are each independently an integer of 0 to 4, A plurality of R 1 and R 2 in the aromatic polysulfone block (A) when n1 or n2 is 2 or more may be the same or different.
- the polyoxyalkylene block (B) consists of a polymer chain having a structural unit represented by the following general formula (2), The block copolymer according to any one of ⁇ 1> to ⁇ 4>, wherein the polyoxyalkylene block (B) has a terminal unit represented by the following general formula (2e).
- R 3 represents an alkylene group having 2 to 6 carbon atoms.
- R 3 represents an alkylene group having 2 to 6 carbon atoms. * represents a bond.
- the polyoxyalkylene block (B) consists of a polymer chain having a structural unit represented by the following formula (2-1), The block copolymer according to ⁇ 5> above, wherein the polyoxyalkylene block (B) has a terminal unit represented by the following formula (2-1e). [In formula (2-1e), * represents a bond. ] ⁇ 7> The block copolymer according to any one of ⁇ 1> to ⁇ 6>, which has a weight average molecular weight of 20,000 to 150,000.
- the ratio of the aromatic polysulfone block (A) and the polyoxyalkylene block (B) in the total mass (100% by mass) of the block copolymer is 80% by mass or more and 100% by mass or less,
- a block copolymer containing an aromatic polysulfone block and a polyoxyalkylene block and suitable as a molding material for a separation membrane having excellent fouling resistance.
- Embodiments of the block copolymer of the present invention are described below.
- An embodiment block copolymer is a block copolymer comprising an aromatic polysulfone block (A) and a polyoxyalkylene block (B), said block copolymer having at least one terminal OH group at the main chain end ,
- the number of terminal OH groups per 100 structural units constituting the aromatic polysulfone block (A), calculated from the peak area of the spectrum obtained by H-NMR measurement, is 0.43 or more and 2 or less. is.
- a separation membrane formed from the block copolymer has excellent fouling resistance.
- fouling means an irreversible deterioration of membrane performance, for example, clogging (clogging) of a separation membrane.
- the fouling resistance of the membrane can be evaluated from the recovery rate of the water permeation rate measured under the following conditions for the separation membrane formed from the block copolymer of the embodiment. It means that the higher the recovery rate of the water permeation rate, the higher the fouling resistance of the separation membrane.
- a separation membrane is cut into a circular shape so as to be attached to the pressure cell to prepare a test membrane.
- a test membrane is attached to the pressure cell, and pure water is filtered against the test membrane at 23 ° C. and a pressure of 0.2 bar (20 kPa), and between 9 minutes and 30 seconds and 10 minutes after the start of filtration.
- the water permeation rate (J 0 ) is determined by measuring the amount of pure water permeating through the test membrane (30 seconds).
- the test membrane is then used to filter an aqueous bovine serum albumin solution (100 ppm) at 23° C. and the same pressure of 0.2 bar (20 kPa) for 1 hour.
- the test membrane is turned inside out and purified water is filtered for 2 minutes at 23° C. and a pressure of 0.1 bar (10 kPa) to wash the membrane. Again, the test membrane is turned over, and the pure water is filtered at 23 ° C. and a pressure of 0.2 bar (20 kPa), and permeates the test membrane between 9 minutes and 30 seconds and 10 minutes (30 seconds) after the start of filtration.
- the water permeation rate (J) is obtained by measuring the amount of purified water. From the obtained water permeation rate (J 0 ) and water permeation rate (J), the recovery rate (%) of the water permeation rate of the test membrane is calculated by the following formula.
- Permeability rate recovery rate (%) (J/J 0 ) x 100
- J 0 water permeation rate before bovine serum albumin filtration (L/m 2 /h/10 5 Pa)
- J Permeation rate after bovine serum albumin filtration (L/m 2 /h/10 5 Pa)
- the aromatic polysulfone block (A) has a structural unit containing at least a structure in which a sulfonyl group ( --SO.sub.2-- ), an arylene group (--Ar--) and an ether bond (--O--) are bonded in this order.
- a block consisting of a polymer chain can be mentioned.
- the arylene group may have a substituent, and typical examples of the substituent include an alkyl group, an aryl group and a halogen atom.
- the aromatic polysulfone block (A) preferably has a structural unit containing a structure represented by general formula (S-1) below. -ph 1 -SO 2 -ph 2 -O- (S-1) [In the formula (S-1), ph 1 and ph 2 are each independently a phenylene group optionally having a substituent. ]
- the phenylene group in ph 1 and ph 2 may be a p-phenylene group, an m-phenylene group, or an o-phenylene group, provided that it is a p-phenylene group. is preferred.
- Examples of the substituent that the phenylene group may have include an alkyl group, an aryl group, and a halogen atom.
- the alkyl group is preferably an alkyl group having 1 to 10 carbon atoms, and specific examples include methyl group, ethyl group, n-propyl group, isopropyl group, n-butyl group, isobutyl group, s-butyl group, Preferable examples include t-butyl group, n-hexyl group, 2-ethylhexyl group, n-octyl group, n-decyl group and the like.
- the aryl group is preferably an aryl group having 6 to 20 carbon atoms, and specific examples thereof include phenyl, o-tolyl, m-tolyl, p-tolyl, 1-naphthyl and 2-naphthyl groups. etc. are preferably exemplified.
- the halogen atom includes fluorine atom, chlorine atom, bromine atom, iodine atom and the like.
- the aromatic polysulfone block (A) preferably has a structural unit represented by the following general formula (1).
- R 1 and R 2 each independently represent an alkyl group having 1 to 10 carbon atoms, an aryl group having 6 to 20 carbon atoms or a halogen atom; n1 and n2 are each independently an integer of 0 to 4, A plurality of R 1 and R 2 in the aromatic polysulfone block (A) when n1 or n2 is 2 or more may be the same or different.
- n1 and n2 are each independently an integer of 0 to 4, preferably 0 to 2, more preferably 0 to 1, and even more preferably 0.
- the aromatic polysulfone block (A) may be a block composed of structural units represented by the general formula (1).
- the polyoxyalkylene block (B) includes a block composed of a polymer chain having an oxyalkylene group as a structural unit.
- the polyoxyalkylene block (B) preferably has a structural unit represented by general formula (2) below.
- R 3 represents an alkylene group having 2 to 6 carbon atoms.
- At least one terminal OH group that the block copolymer of the present embodiment has at the end of the main chain is preferably bonded to the polyoxyalkylene block (B). That is, the block copolymer of the present embodiment can contain polyoxyalkylene blocks (B) having terminal OH groups at both ends or one end of the main chain of the block copolymer.
- the polyoxyalkylene block (B) is composed of a polymer chain having a structural unit represented by the general formula (2), and the polyoxyalkylene block (B) is represented by the following general formula It preferably has a terminal unit represented by (2e).
- the OH group in general formula (2e) corresponds to the terminal OH group of the block copolymer of the embodiment.
- R 3 represents an alkylene group having 2 to 6 carbon atoms. * represents a bond.
- the alkylene group having 2 to 6 carbon atoms in R 3 includes an ethylene group, a trimethylene group, —CH(CH 3 )CH 2 —, a tetramethylene group, —CH 2 CH 2 CH(CH 3 )—, and hexamethylene. and the like.
- the polyoxyalkylene block (B) may be a block composed of structural units represented by the general formula (2).
- the polyoxyalkylene block (B) preferably has a structural unit represented by the following formula (2-1).
- the polyoxyalkylene block (B) consists of a polymer chain having a structural unit represented by the formula (2-1), and the polyoxyalkylene block (B) is represented by the following formula It preferably has a terminal unit represented by (2-1e).
- the OH group in formula (2-1e) corresponds to the terminal OH group of the block copolymer of the embodiment.
- the structural unit represented by the above formula (2-1) is contained at 80 mol% or more and 100 mol% or less with respect to 100 mol% of the total amount of all structural units constituting the polyoxyalkylene block (B). 90 mol % or more and 100 mol % or less, or 98 mol % or more and 100 mol % or less.
- the polyoxyalkylene block (B) may be a block composed of structural units represented by the above formula (2-1).
- the number of aromatic polysulfone blocks (A) and polyoxyalkylene blocks (B) contained in the block copolymer of the embodiment is not particularly limited.
- the block copolymers of the embodiments have at least one terminal OH group at the main chain end, and at least the above linear block copolymers having three blocks; and linear block copolymers having at least said two blocks of a polyoxyalkylene block (B) and an aromatic polysulfone block (A).
- the block copolymers of the embodiments have at least one terminal OH group at the main chain end, and at least the above At least one selected from the group consisting of a linear block copolymer having three blocks, and a linear block copolymer having at least the above two blocks of a polyoxyalkylene block (B) and an aromatic polysulfone block (A) It may contain block copolymers.
- linear as used herein may mean that the block copolymer does not have a branched structure (branched chain).
- branched chain branched chain
- conjugated polymers for example, the end of the main chain of the polymer chain of the aromatic polysulfone block (A) and the end of the main chain of the polymer chain of the polyoxyalkylene block (B) are directly Included are conjugated polymers.
- the block copolymers of the embodiments have at least one terminal OH group at the end of the main chain, and the polyoxyalkylene block (B), the aromatic polysulfone block (A), and the polyoxyalkylene block (B), in that order, the above three linear triblock copolymers having two blocks; and linear diblock copolymers having said two blocks, a polyoxyalkylene block (B) and an aromatic polysulfone block (A).
- the block copolymers of the embodiments have at least one terminal OH group at the end of the main chain, and the polyoxyalkylene block (B), the aromatic polysulfone block (A), and the polyoxyalkylene block (B), in that order, the above three At least one selected from the group consisting of a linear triblock copolymer having two blocks, and a linear diblock copolymer having the above two blocks of a polyoxyalkylene block (B) and an aromatic polysulfone block (A) It may contain block copolymers.
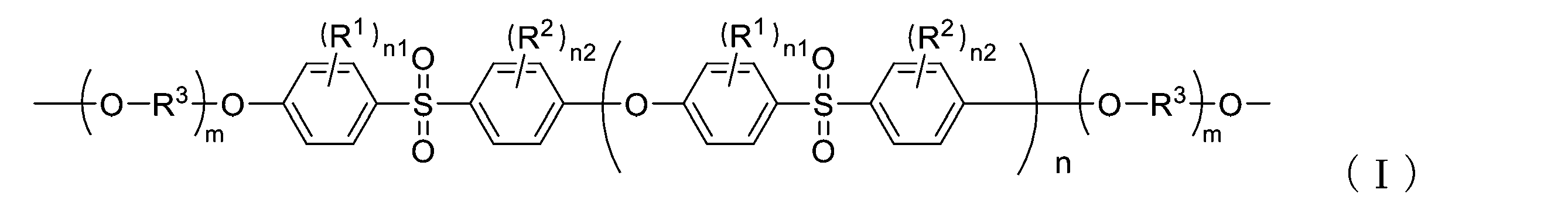
- the aromatic polysulfone block (A) consists of a polymer chain having a structural unit represented by the general formula (1)
- the polyoxyalkylene block (B) is represented by the general formula (2).
- An example of the case of a polymer chain having a structural unit is illustrated.
- R 1 , R 2 , R 3 , n1 and n2 have the same meanings as in formulas (1) and (2) above.
- n is an integer of 0 or more
- m is an integer of 1 or more
- multiple R 3 may be the same or different
- multiple m may be the same or different.
- n is the number of repeating structural units of the aromatic polysulfone block (A) in the formula (I).
- m is the number of repeating structural units of the polyoxyalkylene block (B) in the formula (I).
- the block copolymer of the embodiment has at least one terminal OH group at the main chain end, and has the polyoxyalkylene block (B) having the terminal OH group, the aromatic polysulfone block (A), and the terminal OH group.
- a linear block copolymer having, in order of the polyoxyalkylene block (B), at least the above three blocks, and at least the above two of the polyoxyalkylene block (B) having a terminal OH group and the aromatic polysulfone block (A) linear block copolymers having blocks.
- the block copolymer of the embodiment has at least one terminal OH group at the main chain end, and has the polyoxyalkylene block (B) having the terminal OH group, the aromatic polysulfone block (A), and the terminal OH group.
- a linear block copolymer having, in order of the polyoxyalkylene block (B), at least the above three blocks, and at least the above two of the polyoxyalkylene block (B) having a terminal OH group and the aromatic polysulfone block (A) At least one block copolymer selected from the group consisting of linear block copolymers having blocks.
- the block copolymer of the embodiment has at least one terminal OH group at the main chain end, and has the polyoxyalkylene block (B) having the terminal OH group, the aromatic polysulfone block (A), and the terminal OH group.
- a linear triblock copolymer having said three blocks, in order of polyoxyalkylene block (B), and said two blocks of said polyoxyalkylene block (B) having terminal OH groups and said aromatic polysulfone block (A) a linear diblock copolymer having
- the block copolymer of the embodiment has at least one terminal OH group at the main chain end, and has the polyoxyalkylene block (B) having the terminal OH group, the aromatic polysulfone block (A), and the terminal OH group.
- An example of the copolymer is a polymer represented by general formula (I-1) below.
- the aromatic polysulfone block (A) consists of a polymer chain having a structural unit represented by the general formula (1)
- the polyoxyalkylene block (B) is represented by the general formula (2).
- An example of the case where the polyoxyalkylene block (B) has a terminal unit represented by the general formula (2e) is illustrated below.
- the ratio of the aromatic polysulfone block (A) and the polyoxyalkylene block (B) to the total mass (100% by mass) of the block copolymer of the embodiment is 80% by mass or more and 100% by mass or less. may be 90% by mass or more and 100% by mass or less, may be 98% by mass or more and 100% by mass or less, or may be 100% by mass.
- a block copolymer of embodiments is a block copolymer comprising an aromatic polysulfone block (A) and a polyoxyalkylene block (B), said block copolymer having at least one terminal OH group at the main chain end, Number of terminal OH groups per 100 structural units constituting the aromatic polysulfone block (A ) (terminal OH group/block 100 structural units of (A)) is 0.43 or more and 2 or less.
- the value of the above ratio is in the range of 0.43 to 2, preferably 1.5 or less, and 1 or less. more preferred.
- the numerical range of the above ratio is 0.43 or more and 2 or less, and for example, 0.43 or more and 1 0.5 or less is preferable, and 0.43 or more and 1 or less is more preferable.
- a block copolymer of embodiments is a block copolymer comprising an aromatic polysulfone block (A) and a polyoxyalkylene block (B), said block copolymer having at least one terminal OH group at the main chain end, Bonded to the polyoxyalkylene block (B) per 100 structural units constituting the aromatic polysulfone block (A), calculated from the peak area of the spectrum obtained by 1 H-NMR measurement
- the number of terminal OH groups present is preferably 0.43 or more and 2 or less, more preferably 0.43 or more and 1.5 or less, and even more preferably 0.43 or more and 1 or less.
- a block copolymer of embodiments is a block copolymer comprising an aromatic polysulfone block (A) and a polyoxyalkylene block (B), said block copolymer having at least one terminal OH group at the main chain end,
- the aromatic polysulfone block (A) is a polymer chain composed of a structural unit represented by the general formula (1)
- the polyoxyalkylene block (B) is a structural unit represented by the general formula (2).
- the number of terminal OH groups present is preferably 0.43 or more and 2 or less, more preferably 0.43 or more and 1.5 or less, and even more preferably 0.43 or more and 1 or less.
- the separation membrane obtained from the block copolymer has improved fouling resistance. do.
- the improvement in the fouling resistance of the separation membrane is compared with a separation membrane obtained from a block copolymer having an equivalent structural unit that can be comparatively evaluated, and the above ratio value is not within the above range. I can confirm.
- the number of terminal OH groups per 100 structural units constituting the aromatic polysulfone block (A) is calculated based on the peak area of the spectrum obtained by 1 H-NMR measurement of the block copolymer. A specific calculation method will be described below, taking as an example the case where the terminal OH group is bonded to the polyoxyalkylene block (B).
- the peak area Xp 01 attributed to the hydrogen atoms bonded to the aromatic ring whose number of hydrogen atoms is already known is measured by 1 H-NMR. demand.
- the number of structural units can be calculated by dividing the peak area Xp 01 by the number of hydrogen atoms bonded to the aromatic ring (for example, the peak area Xp 01 is the aromatic Divide by 4 if it is the peak area attributed to the four hydrogen atoms attached to the aromatic rings of the polysulfone block (A)).
- a peak area Yp 01 assigned to the hydrogen atoms of the OH groups bonded to the alkylene chains in the polyoxyalkylene block (B) is determined by 1 H-NMR measurement.
- the number of terminal OH groups can be calculated by dividing the peak area Yp 01 by the number of hydrogen atoms in the OH group (one).
- the number of terminal OH groups determined in (iv) is divided by the number of structural units (number of units) determined in (ii), and further multiplied by 100 (100 units) to obtain an aromatic polysulfone block (A) It is possible to calculate the number of terminal OH groups per 100 structural units constituting As Xp 01 , an integrated value of 7.25 to 7.27 ppm can be used. Also, as Yp 01 , an integrated value of 4.53 to 4.60 ppm can be used.
- any solvent can be used as long as the 1 H-NMR measurement is possible and the block copolymer to be measured can be dissolved, and deuterated dimethyl sulfoxide is suitable.
- 1 H-NMR measurement conditions when deuterated dimethyl sulfoxide is used as the measurement solvent include the following conditions.
- the ratio represented by the weight of the polyoxyalkylene block (B)/the weight of the aromatic polysulfone block (A) in the block copolymer of the embodiment is 0.05 or more.
- the ratio represented by the weight of the polyoxyalkylene block (B)/the weight of the aromatic polysulfone block (A) is preferably 0.2 or less, more preferably 0.18 or less.
- the numerical range of the ratio represented by the weight of the polyoxyalkylene block (B)/the weight of the aromatic polysulfone block (A) is more preferably 0.05 or more and 0.2 or less, and more preferably 0.05. 0.18 or less is more preferable.
- the resulting separation membrane when the value of the above ratio (ratio of the weight of the polyoxyalkylene block (B)/the weight of the aromatic polysulfone block (A)) is at least the above lower limit, the resulting separation membrane It is preferable because the fouling resistance is improved.
- the above ratio (ratio of the weight of the polyoxyalkylene block (B)/the weight of the aromatic polysulfone block (A)) is equal to or less than the above upper limit, gelation of the block copolymer is suppressed to produce a separation membrane. It is preferable because it facilitates the separation, and it is preferable because the resulting separation membrane tends to have improved fouling resistance.
- the weight of the aromatic polysulfone block (A) in the block copolymer of the embodiment is the sum of the weights of the aromatic polysulfone blocks (A) contained in the block copolymer of the embodiment.
- the weight of the polyoxyalkylene block (B) in the block copolymer of the embodiment is the sum of the weights of the polyoxyalkylene blocks (B) contained in the block copolymer of the embodiment.
- the weight of the polyoxyalkylene block (B)/the weight of the aromatic polysulfone block (A) is the peak area ratio of the spectrum obtained by 1 H-NMR measurement of the block copolymer. calculated based on A specific calculation method is as follows. ⁇ i> In the structural unit of the aromatic polysulfone block (A), the peak area Xp 01 attributed to the hydrogen atoms bonded to the aromatic ring whose number of hydrogen atoms is already known is measured by 1 H-NMR. demand.
- the peak area Zp 01 attributed to the hydrogen atoms bonded to the alkylene chain whose number of hydrogen atoms is already known is measured by 1 H-NMR. demand.
- ⁇ iii> The value obtained by multiplying the peak area Zp 01 obtained in ⁇ ii> by the molecular weight of the structural unit of the polyoxyalkylene block (B) is obtained by adding the peak area Xp 01 obtained in ⁇ i> to the aromatic polysulfone block (A).
- the weight of the polyoxyalkylene block (B)/the weight of the aromatic polysulfone block (A) can be calculated by dividing by the value obtained by multiplying the molecular weight of the structural unit.
- Xp 01 an integrated value of 7.25 to 7.27 ppm can be used.
- Zp 01 an integrated value of 3.4 to 3.6 ppm can be used.
- the weight average molecular weight (Mw) of the block copolymer of the embodiment may be, for example, 20,000 or more, 30,000 or more, or 40,500 or more.
- the weight average molecular weight (Mw) of the block copolymer of the embodiment may be, for example, 150,000 or less, 130,000 or less, or 100,000 or less.
- the numerical range of the weight average molecular weight (Mw) of the block copolymer of the embodiment may be, for example, 20,000 to 150,000, 30,000 to 130,000, or 40,500 to 100,000.
- the weight average molecular weight is the weight average molecular weight measured by gel permeation chromatography (GPC), and is determined under the following measurement conditions.
- GPC gel permeation chromatography
- the block copolymers of the embodiments unintended decomposition progresses, unreacted raw materials remain, etc., and the polymer that does not contain the aromatic polysulfone block (A) and the polyoxyalkylene block (B) is It is also assumed that a very small amount is mixed.
- the above-described block copolymer specifications e.g., the number of terminal OH groups, the content ratio of a predetermined structural unit, the weight ratio of block (B)/weight of block (A), the weight average molecular weight
- the above-described block copolymer specifications may be determined for a resin composition containing the block copolymer of the embodiment.
- the resin composition contains a block copolymer containing an aromatic polysulfone block (A) and a polyoxyalkylene block (B) in an amount of 95% by mass or more and 100% by mass or less with respect to the total mass of the resin composition. It may be contained in an amount of 98% by mass or more and 100% by mass or less.
- the block copolymer of the embodiment is suitable as a material for forming a separation membrane, and the separation membrane formed from the block copolymer is resistant to fouling and has excellent properties as a separation membrane.
- Shaped bodies of embodiments comprise block copolymers of embodiments.
- a molded article of the embodiment is molded from the block copolymer of the embodiment.
- the molded article of the embodiment can be produced using the block copolymer of the embodiment as a molding material.
- the content of the block copolymer of the embodiment relative to the total mass of the molded article of the embodiment may be, for example, 50 to 100% by mass, 80 to 99.5% by mass, or 90 to 99% by mass. It's okay.
- Examples of the method for producing a molded product include a method having a step of molding the block copolymer of the embodiment into a desired shape.
- Examples of the molding method include a method of molding a material containing the block copolymer of the embodiment by solution casting, extrusion molding, T-die molding, blow molding, injection molding, and the like.
- the block copolymers of the embodiments can be molded into various shapes by selecting a molding method according to the desired shape of the molded article.
- a film containing the block copolymer of the embodiment can be exemplified as an example of the molded article of the embodiment.
- the film is preferably a porous membrane.
- the film is preferably a porous membrane that has water permeability and can be provided as a separation membrane or a semipermeable membrane.
- the molded article of the embodiment can be used as a water permeable separation membrane or semipermeable membrane.
- the molded article of the embodiment is water-permeable and can be used as a separation membrane or a semi-permeable membrane that allows a protein-containing fluid to pass through.
- the thickness of the film of the embodiment is not particularly limited, but may be, for example, 5 to 200 ⁇ m, 7 to 100 ⁇ m, or 10 to 50 ⁇ m.
- the method for producing the block copolymer of the embodiment is not particularly limited, but the following method for producing the block copolymer can be exemplified as one embodiment.
- the block copolymer production method of the embodiment comprises a step of reacting an aromatic polysulfone (a) having at least one terminal Cl atom with a polyoxyalkylene compound (b) having a terminal hydroxy group (block copolymer production step).
- the block copolymer production method of the embodiment is intended to react a prepolymerized aromatic polysulfone (a) with a polyoxyalkylene compound (b), and includes a step of preparing the aromatic polysulfone (a) in advance. It may contain further.
- a method for producing a block copolymer of an embodiment comprises the steps of preparing in advance an aromatic polysulfone (a) having at least one terminal Cl atom; A step of reacting the aromatic polysulfone (a) with a polyoxyalkylene compound (b) having a terminal hydroxy group (block copolymer production step) may be included.
- the step of preliminarily preparing the aromatic polysulfone (a) only requires that the aromatic polysulfone (a) is available, and includes simply preparing a commercially available aromatic polysulfone (a).
- the block copolymer production method of the embodiment may further include a step of producing aromatic polysulfone (a) (aromatic polysulfone production step).
- a method for producing a block copolymer comprises a step of obtaining an aromatic polysulfone (a) having at least one terminal Cl atom by a polycondensation reaction; A step of reacting the aromatic polysulfone (a) with a polyoxyalkylene compound (b) having a terminal hydroxy group (block copolymer production step) may be included.
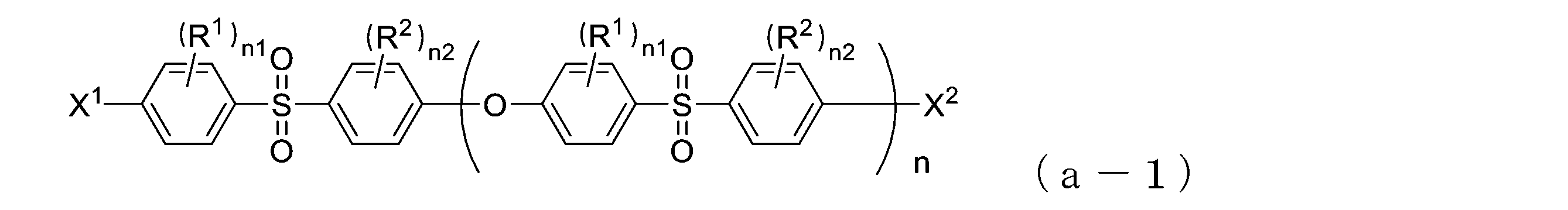
- aromatic polysulfone (a) for example, a compound represented by the following general formula (a1) and a compound represented by the following general formula (a2) are subjected to a polycondensation reaction to give the following general formula (a-1 ) can be obtained.
- aromatic polysulfone (a) obtained by the above polycondensation reaction examples include compounds represented by the following general formula (a-1).
- R 1 , R 2 , n1, n2 and n have the same meanings as in formula (I) above.
- -X 1 and -X 2 are each independently -OH or -Cl, and at least one of -X 1 and -X 2 is -Cl.
- n is the number of repetitions of the structural unit of the aromatic polysulfone (a-1).
- aromatic polysulfone (a) In the reaction between the aromatic polysulfone (a) and the polyoxyalkylene compound (b), examples of the aromatic polysulfone (a) include those described above.
- the value of the weight-average molecular weight of the aromatic polysulfone (a) used as a raw material may be appropriately determined according to the weight-average molecular weight of the block copolymer to be produced.
- the weight-average molecular weight of the above aromatic polysulfone (a) used as a raw material, measured by gel permeation chromatography in a DMF solvent, may be 20,000 or more, 20,000 or more and 70,000 or less, or 20,000. It may be greater than or equal to 65000 or less.
- Examples of the polyoxyalkylene compound (b) include compounds represented by the following general formula (b-1).
- the value of the weight-average molecular weight of the polyoxyalkylene compound (b) used as a raw material may be appropriately determined.
- the weight average molecular weight of the polyoxyalkylene compound (b) used as a raw material may be 2,000 or more, 2,000 or more and 20,000 or less, or 2,000 or more and 10,000 or less.
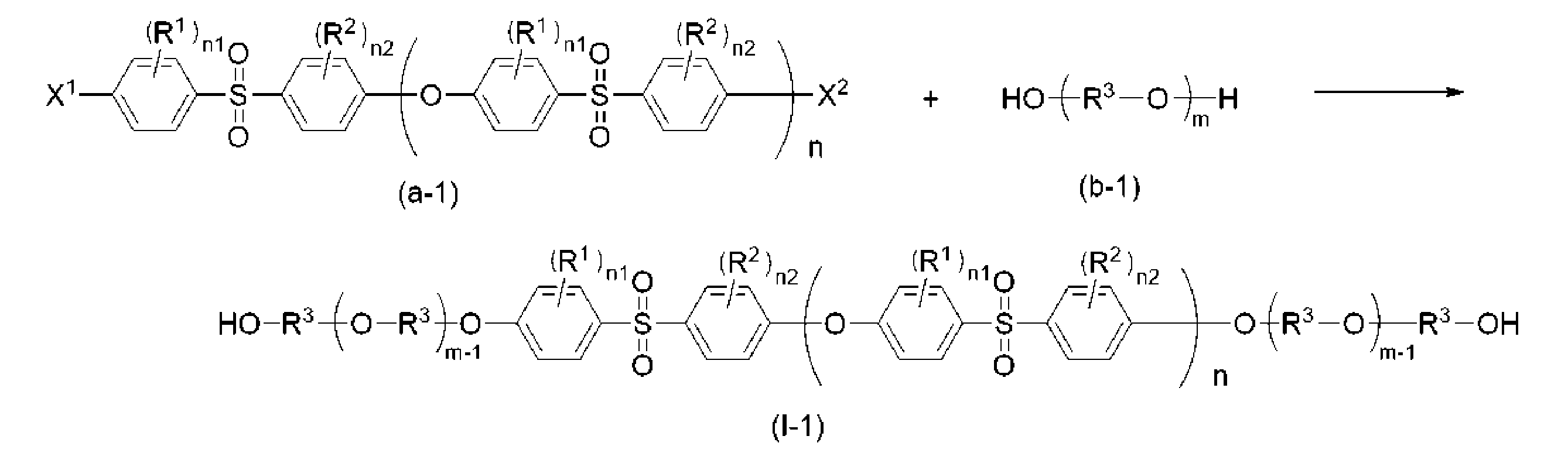
- a compound represented by the general formula (a-1) and a compound represented by the general formula (b-1) can be exemplified.
- the reaction can be represented by the following reaction formula.
- a block copolymer represented by general formula (I-1) is obtained as an example.
- R 1 , R 2 , R 3 , n1, n2, n, m, X 1 and X 2 are the above formula (a-1), formula (b-1) and formula (I-1) has the same meaning as in ]
- the aromatic polysulfone (a) may be used alone or in combination of two or more.
- the polyoxyalkylene compound (b) may be used alone or in combination of two or more.
- the amount of the polyoxyalkylene compound (b) having a terminal hydroxy group is preferably 1 mol or more per 1 mol of the aromatic polysulfone (a) having at least one terminal Cl atom. ⁇ 2.5 mol is more preferred, and 1-2 mol is even more preferred.
- the aromatic polysulfone (a) having at least one terminal Cl atom is preferably a compound represented by the general formula (a-1).
- a compound represented by the general formula (b-1) is preferred.
- the reaction between the aromatic polysulfone (a) and the polyoxyalkylene compound (b) is preferably carried out using an alkali metal carbonate and/or an alkali metal bicarbonate as the base of the catalyst.
- the reaction is preferably carried out in an organic solvent as the solvent, more preferably using an alkali metal salt of carbonic acid as the base and in an organic solvent.
- the alkali metal salt of carbonic acid may be a normal salt of alkali carbonate (alkali metal carbonate) or an acid salt of alkali bicarbonate (alkali hydrogen carbonate, alkali metal hydrogen carbonate). Alternatively, it may be a mixture of these (alkali carbonate and alkali bicarbonate).
- alkali carbonates include sodium carbonate, potassium carbonate and the like.
- preferred alkali bicarbonate include sodium bicarbonate (sodium hydrogen carbonate) and potassium bicarbonate (potassium hydrogen carbonate).
- the mixing ratio of the alkali metal salt of carbonate is preferably 0.90 mol or more and 1.30 mol or less, preferably 0.95 mol or more and 1.30 mol or less as an alkali metal per 1 mol of the polyoxyalkylene compound (b). It is more preferably 0.20 mol or less.
- the organic solvent examples include aprotic polar solvents, and the boiling point of the aprotic polar solvent under 1 atmosphere is preferably 250°C or less.
- the reaction can proceed while removing by-products by refluxing the aprotic polar solvent at a relatively low temperature.
- the boiling point of the aprotic polar solvent is preferably 250° C. or lower, may be 230° C. or lower, or may be 210° C. or lower.
- the boiling point of the aprotic polar solvent may be 120° C. or higher, 140° C. or higher, or 150° C. or higher.
- An example of the numerical range of the boiling point of the aprotic polar solvent may be 120° C. or higher and 230° C. or lower, 140° C. or higher and 210° C. or lower, or 150° C. or higher and 210° C. or lower. good too.
- aprotic polar solvents having a boiling point of 250° C. or less examples include sulfone solvents such as dimethylsulfone and diethylsulfone, N,N-dimethylacetamide, N-methyl-pyrrolidone, N-ethyl-pyrrolidone, N-methylcaprolactam, N, N-dimethylformamide, N,N-diethylformamide, N,N-diethylacetamide, N-methylpropionamide, amide solvents such as dimethylimidazolidinone, lactone solvents such as ⁇ -butyl lactone and ⁇ -butyl lactone, Examples include sulfoxide solvents such as methyl sulfoxide and methylphenyl sulfoxide, cellosolve solvents such as tetramethylphosphoricamide and hexamethylphosphoricamide, and cellosolve solvents such as ethyl cellosolve acetate and methyl cellosolve acetate
- water may be produced as a by-product. ” may be added.
- an azeotropic mixture is formed with water with respect to the total amount of solvent used in the reaction.
- the proportion of the solvent used in the reaction is preferably 0 to 20% by mass, more preferably 0 to 10% by mass, even more preferably 0 to 3% by mass, and the solvent used in the reaction is water. It is particularly preferred to be substantially free of solvents that form an azeotrope with.
- the molecular weight of the produced block copolymer can be increased. be.
- the boiling point of the solvent that forms an azeotropic mixture with water is preferably 250° C. or lower, may be 230° C. or lower, or may be 210° C. or lower.
- the boiling point of the solvent that forms an azeotropic mixture with water may be 40° C. or higher, 80° C. or higher, or 100° C. or higher.
- An example of the numerical range of the boiling point of the solvent that forms an azeotropic mixture with water may be 40° C. or higher and 250° C. or lower, 80° C. or higher and 230° C. or lower, or 100° C. or higher and 210° C. It may be below.
- solvents having a boiling point of 250°C or lower and forming an azeotropic mixture with water include benzene, chlorobenzene, toluene, xylene, ethylbenzene, methyl isobutyl ketone, hexane, and cyclohexane.
- the reaction between the aromatic polysulfone (a) and the polyoxyalkylene compound (b) is preferably carried out at 250°C or lower. By conducting the reaction at a relatively low temperature of 250° C. or less, the energy load can be kept low.
- the reaction temperature is preferably 250° C. or lower, may be 230° C. or lower, or may be 210° C. or lower.
- the lower limit of the reaction temperature is not limited, but may be 100° C. or higher, 120° C. or higher, or 140° C. or higher.
- An example of the numerical range of the reaction temperature between the aromatic polysulfone (a) and the polyoxyalkylene compound (b) may be 100° C. or higher and 250° C. or lower, or 120° C. or higher and 230° C. or lower. may be 140° C. or higher and 210° C. or lower.
- the block copolymer can be separated from the reaction mixture by filtering, extracting, centrifuging, or the like, removing the alkalinity), and the organic solvent.
- the organic solvent may be removed by distilling off the organic solvent directly from the solution, or the solution may be mixed with a poor solvent for the block copolymer to precipitate the block copolymer, followed by filtration, centrifugation, or the like. You may carry out by separating. A predetermined amount of the organic solvent may remain.
- poor solvents for block copolymers include methanol, ethanol, 2-propanol, acetone, hexane, heptane and water, preferably water and methanol due to their low cost.
- the poor solvent for the block copolymer may be used singly or in combination of two or more.
- the two hydrogen atoms each bonded to the two carbon atoms adjacent to the ph 1 carbon atom bonded to S, and the two carbon atoms adjacent to the ph 2 carbon atom bonded to S The peak area (Xp 01 ) attributed to two hydrogen atoms (four hydrogen atoms in total) bonded one by one, and the hydrogen atom of the OH group bonded to the polyoxyalkylene block (B) It was calculated based on the following formula (m1) using the peak area (Yp 01 ).
- Xp 01 an integrated value of 7.25 to 7.27 ppm was used.
- Yp 01 an integrated value of 4.53 to 4.60 ppm was used.
- Example 1 69.5 g of polyethylene glycol 8000 (manufactured by Tokyo Kasei Kogyo Co., Ltd., weight average molecular weight 9100) (per mol of PES about 2 molar equivalents), 0.92 g of potassium carbonate and 150 g of N-methyl-2-pyrrolidone (NMP) were mixed, heated to 100 ° C., and polyethersulfone (manufactured by Sumitomo Chemical Co., Ltd., Sumika Excel PES 3600P , weight average molecular weight greater than 20,000 as determined by gel permeation chromatography in DMF solvent) was added.
- NMP N-methyl-2-pyrrolidone
- Example 2 The above example except that the polyethylene glycol used in Example 1 was replaced with 17.4 g of polyethylene glycol 4000 (manufactured by Tokyo Chemical Industry Co., Ltd., weight average molecular weight 3000) (about 1 molar equivalent with respect to 1 mol of PES).
- An aromatic polysulfone block copolymer of Example 2 was obtained in the same manner as in Example 1.
- Example 3 The polyethylene glycol used in Example 1 was replaced with polyethylene glycol 4000 (manufactured by Tokyo Chemical Industry Co., Ltd., weight average molecular weight 3000) 11.0 g (about 2 molar equivalents per 1 mol of PES), and the amount of potassium carbonate used was 0.
- Polyethersulfone (Sumitomo Chemical Co., Ltd., Sumika Excel PES 5900P, weight average molecular weight of 30000 or more as measured in DMF solvent by gel permeation chromatography) was replaced with 100 g of polyethersulfone instead of .46 g.
- An aromatic polysulfone block copolymer of Example 3 was obtained in the same manner as in Example 1.
- Example 4 The polyethylene glycol used in Example 1 was replaced with 10.4 g of polyethylene glycol 2000 (manufactured by Tokyo Chemical Industry Co., Ltd., weight average molecular weight 2100) (about 2 molar equivalents per 1 mol of PES), and the amount of potassium carbonate used was 0.
- Polyethersulfone (Sumitomo Chemical Co., Ltd., Sumika Excel PES 4800P, weight average molecular weight of 25000 or more as measured in DMF solvent by gel permeation chromatography) was replaced with 100 g of polyethersulfone instead of .46 g.
- An aromatic polysulfone block copolymer of Example 4 was obtained in the same manner as in Example 1.
- the resulting reaction mixture solution was then diluted with NMP and cooled to room temperature to precipitate unreacted potassium carbonate and by-produced potassium chloride.
- the above solution was dropped into water to precipitate aromatic polysulfone, and unnecessary NMP was removed by filtration to obtain a precipitate.
- the resulting precipitate was carefully washed repeatedly with methanol and water and dried by heating at 100° C. to obtain an aromatic polysulfone block copolymer of Comparative Example 2.
- Table 1 shows the above measurement results for the aromatic polysulfone block copolymer of each example.
- the test membrane of each example was turned inside out and pure water was filtered for 2 minutes at 23° C. and a pressure of 0.1 bar (10 kPa) to wash the membrane. Again, the test membrane of each example was turned over, and the pure water was filtered at 23° C. and a pressure of 0.2 bar (20 kPa).
- the water permeation rate (J) was obtained by measuring the amount of pure water that permeated the test membrane of each example. From the obtained water permeation rate (J 0 ) and water permeation rate (J), the recovery rate (%) of the water permeation rate of the test membrane of each example was calculated by the following formula.
- Permeability rate recovery rate (%) (J/J 0 ) x 100
- J 0 water permeation rate before bovine serum albumin filtration (L/m 2 /h/10 5 Pa)
- J Permeation rate after bovine serum albumin filtration (L/m 2 /h/10 5 Pa)
- the number of terminal OH groups bonded to the polyoxyalkylene block (B) per 100 structural units constituting the aromatic polysulfone block (A) is 0.43 or more.
- the porous membranes produced by using the aromatic polysulfone block copolymers of Examples 1 to 4, which are 2 or less, as molding materials are produced by using the aromatic polysulfone block copolymers of Comparative Examples 1 to 2, which do not satisfy the numerical range, as molding materials.
- the fouling resistance was improved compared to the porous membrane. From this, it was shown that the aromatic polysulfone block copolymer to which the present invention is applied is useful as a material for forming separation membranes.
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Other Resins Obtained By Reactions Not Involving Carbon-To-Carbon Unsaturated Bonds (AREA)
Abstract
Description
本願は、2021年9月6日に、日本に出願された特願2021-144891号に基づき優先権を主張し、その内容をここに援用する。
例えば、特許文献1には、ポリアリールエーテルスルホン-ポリアルキレンオキシド-ブロックコポリマーの製造方法が開示されている。
すなわち、本発明は以下の態様を有する。
前記ブロックコポリマーは、主鎖末端に少なくとも1つの末端OH基を有し、
1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの前記末端OH基の数が、0.43以上2以下である、ブロックコポリマー。
<2> 1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの、前記ポリオキシアルキレンブロック(B)に結合している前記末端OH基の数が、0.43以上2以下である、前記<1>に記載のブロックコポリマー。
<3> 前記ポリオキシアルキレンブロック(B)の重量/前記芳香族ポリスルホンブロック(A)の重量で表される比が0.05以上である、前記<1>又は<2>に記載のブロックコポリマー。
<4> 前記芳香族ポリスルホンブロック(A)が、下記一般式(1)で表される構造単位を有する高分子鎖からなる、前記<1>~<3>のいずれか一つに記載のブロックコポリマー。
R1及びR2は、それぞれ独立に、炭素数1~10のアルキル基、炭素数6~20のアリール基又はハロゲン原子を表し、
n1及びn2は、それぞれ独立に、0~4の整数であり、
n1又はn2が2以上である場合の前記芳香族ポリスルホンブロック(A)が有する、複数個のR1及びR2は互いに同一でも異なっていてもよい。]
<5> 前記ポリオキシアルキレンブロック(B)が、下記一般式(2)で表される構造単位を有する高分子鎖からなり、
前記ポリオキシアルキレンブロック(B)が、下記一般式(2e)で表される末端単位を有する、前記<1>~<4>のいずれか一つに記載のブロックコポリマー。
<6> 前記ポリオキシアルキレンブロック(B)が、下記式(2-1)で表される構造単位を有する高分子鎖からなり、
前記ポリオキシアルキレンブロック(B)が、下記式(2-1e)で表される末端単位を有する、前記<5>に記載のブロックコポリマー。
<7> 重量平均分子量が20000~150000である、前記<1>~<6>のいずれか一つに記載のブロックコポリマー。
<8> 前記末端OH基を有する前記ポリオキシアルキレンブロック(B)、前記芳香族ポリスルホンブロック(A)、及び前記末端OH基を有する前記ポリオキシアルキレンブロック(B)の順に、前記3つのブロックを有する直鎖状トリブロックコポリマー、並びに
前記末端OH基を有する前記ポリオキシアルキレンブロック(B)及び前記芳香族ポリスルホンブロック(A)の前記2つのブロックを有する直鎖状ジブロックコポリマー、からなる群から選ばれる少なくとも一種のブロックコポリマーである、前記<1>~<7>のいずれか一つに記載のブロックコポリマー。
<9> 前記ブロックコポリマーの総質量(100質量%)に占める、前記芳香族ポリスルホンブロック(A)及び前記ポリオキシアルキレンブロック(B)の割合が、80質量%以上100質量%以下である、前記<1>~<8>のいずれか一つに記載のブロックコポリマー。
実施形態のブロックコポリマーは、芳香族ポリスルホンブロック(A)及びポリオキシアルキレンブロック(B)を含むブロックコポリマーであって、前記ブロックコポリマーは、主鎖末端に少なくとも1つの末端OH基を有し、1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの前記末端OH基の数が、0.43以上2以下である。
直径47mmの圧力セルを用い、該圧力セルに装着できるように分離膜を円形に切り出し、試験膜を作製する。試験膜を該圧力セルに装着し、試験膜に対して、23℃、0.2バール(20kPa)の圧力で、純水をろ過し、ろ過開始から9分30秒経過時から10分経過時の間(30秒間)に試験膜を透過した純水の量を測定して、透水速度(J0)を求める。
次に、試験膜を用いて、ウシ血清アルブミン水溶液(100ppm)を、23℃、同じ圧力0.2バール(20kPa)で1時間ろ過する。その後、試験膜を裏返し、23℃、0.1バール(10kPa)の圧力で、純水を2分間ろ過し、膜の洗浄を行う。再度、試験膜を裏返し、23℃、0.2バール(20kPa)の圧力で、純水をろ過し、ろ過開始から9分30秒経過時から10分経過時の間(30秒間)に試験膜を透過した純水の量を測定して透水速度(J)を求める。
得られた透水速度(J0)及び透水速度(J)から、以下の式によって試験膜の透水速度の回復率(%)を算出する。
透水速度の回復率(%)=(J/J0)×100
J0:ウシ血清アルブミンろ過前の透水速度(L/m2/h/105Pa)
J:ウシ血清アルブミンろ過後の透水速度(L/m2/h/105Pa)
芳香族ポリスルホンブロック(A)としては、スルホニル基(-SO2-)とアリーレン基(-Ar-)とエーテル結合(-O-)とがこの順で結合した構造を少なくとも含む構造単位、を有する高分子鎖からなるブロックが挙げられる。
前記アリーレン基は置換基を有していてもよく、該置換基の典型例としては、アルキル基、アリール基又はハロゲン原子が挙げられる。
-ph1-SO2-ph2-O- ・・・(S-1)
[式(S-1)中、ph1及びph2は、それぞれ独立に、置換基を有してもよいフェニレン基である。]
該アルキル基としては、炭素原子数1~10のアルキル基が好ましく、具体的には、メチル基、エチル基、n-プロピル基、イソプロピル基、n-ブチル基、イソブチル基、s-ブチル基、t-ブチル基、n-ヘキシル基、2-エチルヘキシル基、n-オクチル基、n-デシル基等が好適に挙げられる。
該アリール基としては、炭素原子数6~20のアリール基が好ましく、具体的には、フェニル基、o-トリル基、m-トリル基、p-トリル基、1-ナフチル基、2-ナフチル基等が好適に挙げられる。
該ハロゲン原子としては、フッ素原子、塩素原子、臭素原子、ヨウ素原子等が挙げられる。
R1及びR2は、それぞれ独立に、炭素数1~10のアルキル基、炭素数6~20のアリール基又はハロゲン原子を表し、
n1及びn2は、それぞれ独立に、0~4の整数であり、
n1又はn2が2以上である場合の前記芳香族ポリスルホンブロック(A)が有する、複数個のR1及びR2は互いに同一でも異なっていてもよい。]
n1及びn2は、それぞれ独立に、0~4の整数であり、0~2が好ましく、0~1がより好ましく、0がさらに好ましい。
ポリオキシアルキレンブロック(B)としては、オキシアルキレン基を構造単位として有する高分子鎖からなるブロックが挙げられる。ポリオキシアルキレンブロック(B)は、下記一般式(2)で表される構造単位を有することが好ましい。
即ち、本実施形態のブロックコポリマーは、末端OH基を有するポリオキシアルキレンブロック(B)を、ブロックコポリマーの主鎖の両末端又は片末端に含むことができる。
ポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の少なくとも上記2つのブロックを有する直鎖状ブロックコポリマー、の少なくとも一方を含んでよい。
ポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の少なくとも上記2つのブロックを有する直鎖状ブロックコポリマー、からなる群から選ばれる少なくとも一種のブロックコポリマーを含んでよい。
ポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の上記2つのブロックを有する直鎖状ジブロックコポリマー、の少なくとも一方を含んでよい。
ポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の上記2つのブロックを有する直鎖状ジブロックコポリマー、からなる群から選ばれる少なくとも一種のブロックコポリマーを含んでよい。
ここでは、前記芳香族ポリスルホンブロック(A)が、前記一般式(1)で表される構造単位を有する高分子鎖からなり、ポリオキシアルキレンブロック(B)が前記一般式(2)で表される構造単位を有する高分子鎖からなる場合の一例を例示している。
R1、R2、R3、n1及びn2は、上記式(1)及び式(2)におけるものと同一の意味を表す。
nは0以上の整数であり、mは1以上の整数であり、複数存在するR3は、互いに同一でも異なっていてもよく、複数存在するmは、互いに同一でも異なっていてもよい。]
mは、上記式(I)における、ポリオキシアルキレンブロック(B)の有する上記構造単位の繰り返し数である。
前記末端OH基を有するポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の少なくとも上記2つのブロックを有する直鎖状ブロックコポリマー、の少なくとも一方を含んでよい。
前記末端OH基を有するポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の少なくとも上記2つのブロックを有する直鎖状ブロックコポリマー、からなる群から選ばれる少なくとも一種のブロックコポリマーを含んでよい。
前記末端OH基を有するポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の上記2つのブロックを有する直鎖状ジブロックコポリマー、の少なくとも一方を含んでよい。
前記末端OH基を有するポリオキシアルキレンブロック(B)及び芳香族ポリスルホンブロック(A)の上記2つのブロックを有する直鎖状ジブロックコポリマー、からなる群から選ばれる少なくとも一種のブロックコポリマーを含んでよい。
ここでは、前記芳香族ポリスルホンブロック(A)が、前記一般式(1)で表される構造単位を有する高分子鎖からなり、ポリオキシアルキレンブロック(B)が前記一般式(2)で表される構造単位を有する高分子鎖からなり、前記ポリオキシアルキレンブロック(B)が前記一般式(2e)で表される末端単位を有する場合の一例を例示する。
1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの、前記末端OH基の数(末端OH基/ブロック(A)の構造単位100ユニット)の比が、0.43以上2以下である。
1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの、前記ポリオキシアルキレンブロック(B)に結合している前記末端OH基の数が、0.43以上2以下であることが好ましく、0.43以上1.5以下がより好ましく、0.43以上1以下がさらに好ましい。
前記芳香族ポリスルホンブロック(A)が、前記一般式(1)で表される構造単位からなる高分子鎖であり、ポリオキシアルキレンブロック(B)が前記一般式(2)で表される構造単位からなる高分子鎖であり、
1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの、前記ポリオキシアルキレンブロック(B)に結合している前記末端OH基の数が、0.43以上2以下であることが好ましく、0.43以上1.5以下がより好ましく、0.43以上1以下がさらに好ましい。
一方で、後述の実施例においても確認されるように、当該末端OH基の量が多すぎても、ファウリング耐性が低下する。この理由については明らかではないが、当該末端OH基とブロックコポリマーの周囲にある水分子との水和状態の変化が関係していると考えられる。
(i)芳香族ポリスルホンブロック(A)の構造単位において、既に水素原子の数が分かっている芳香環に結合している水素原子に帰属されるピーク面積Xp01を、1H-NMRの測定で求める。
(ii)ピーク面積Xp01を、前記芳香環に結合している水素原子の数で割ることにより、構造単位数(ユニット数)を算出することができる(例えば、ピーク面積Xp01が、芳香族ポリスルホンブロック(A)の芳香環に結合している4つの水素原子に帰属されるピーク面積である場合は、4で割る)。
(iii)ポリオキシアルキレンブロック(B)におけるアルキレン鎖に結合しているOH基の水素原子に帰属されるピーク面積Yp01を、1H-NMRの測定で求める。
(iv)ピーク面積Yp01を、前記OH基の水素原子の数(1つ)で割ることにより、前記末端OH基の数を算出することができる。
(v)(iv)で求めた末端OH基の数を、(ii)で求めた構造単位数(ユニット数)で割り、さらに100(100ユニット)を掛けることにより、芳香族ポリスルホンブロック(A)を構成している構造単位100ユニット当たりの末端OH基の数を算出することができる。
なお、Xp01としては、7.25~7.27ppmの積分値を採用することができる。また、Yp01としては、4.53~4.60ppmの積分値を採用することができる。
測定溶媒として重ジメチルスルホキシドを用いた場合の1H-NMRの測定条件としては、以下の条件が挙げられる。
測定装置:ECZ400S(JEOL社製)
静磁場強度:9.4テスラ(共鳴周波数:400MHz(1H))
スピニング:15Hz
繰り返し時間:7.2s
積算回数:64回
温度:23℃
化学シフト標準物質:ジメチルスルホキシド
実施形態のブロックコポリマーの、ポリオキシアルキレンブロック(B)の重量/芳香族ポリスルホンブロック(A)の重量で表される比は、0.2以下が好ましく、0.18以下がより好ましい
実施形態のブロックコポリマーの、ポリオキシアルキレンブロック(B)の重量/芳香族ポリスルホンブロック(A)の重量で表される比の上記数値範囲としては、0.05以上0.2以下がより好ましく、0.05以上0.18以下がさらに好ましい。
後述の実施例においても確認されるように、同等のPEG/PES重量比であっても、ファウリング耐性に差がみられる。このことから、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの前記末端OH基の量のほうが、上記のブロック(B)の重量/ブロック(A)の重量比よりも、ファウリング耐性の向上に対し、より寄与の大きい要因であると考えられる。
同じく、実施形態のブロックコポリマーにおける、上記のポリオキシアルキレンブロック(B)の重量は、実施形態のブロックコポリマーに含まれるポリオキシアルキレンブロック(B)の重量の総和である。
<i>芳香族ポリスルホンブロック(A)の構造単位において、既に水素原子の数が分かっている芳香環に結合している水素原子に帰属されるピーク面積Xp01を、1H-NMRの測定で求める。
<ii>ポリオキシアルキレンブロック(B)の構造単位において、既に水素原子の数が分かっているアルキレン鎖に結合している水素原子に帰属されるピーク面積Zp01を、1H-NMRの測定で求める。
<iii><ii>で求めたピーク面積Zp01にポリオキシアルキレンブロック(B)の構造単位の分子量を乗じた値を、<i>で求めたピーク面積Xp01に芳香族ポリスルホンブロック(A)の構造単位の分子量を乗じた値で割ることにより、ポリオキシアルキレンブロック(B)の重量/芳香族ポリスルホンブロック(A)の重量を算出することができる。
なお、Xp01としては、7.25~7.27ppmの積分値を採用することができる。また、Zp01としては、3.4~3.6ppmの積分値を採用することができる。
[測定条件]
試料:10mM臭化リチウム含有N,N-ジメチルホルムアミド溶液1mLに対し、測定対象のブロックコポリマー0.002gを配合
試料注入量:100μL
カラム(固定相):東ソー株式会社製「TSKgel GMHHR-H」
(7.8mmφ×300mm)を2本直列に連結
カラム温度:40℃
溶離液(移動相):10mM臭化リチウム含有N,N-ジメチルホルムアミド
溶離液流量:0.8mL/分
検出器:示差屈折率計(RI)+光散乱光度計(LS)
分子量算出法:光散乱光度計(LS)の測定結果から分子量を算出(試料のdn/dcを0.187とし分子量を算出)
実施形態の成形体は、実施形態のブロックコポリマーを含む。実施形態の成形体は、実施形態のブロックコポリマーより成形されたものである。
実施形態の成形体は、実施形態のブロックコポリマーを成形材料として作製することができる。
実施形態の成形体は、透水性を有する分離膜又は半透膜として利用可能である。実施形態の成形体は、透水性を有し、タンパク質を含む流体を通過させる分離膜又は半透膜として利用可能である。
実施形態のブロックコポリマーの製造方法は、特に限定されるものではないが、一実施形態として、下記のブロックコポリマーの製造方法を例示できる。
前記芳香族ポリスルホン(a)と、末端にヒドロキシ基を有するポリオキシアルキレン化合物(b)と、を反応させる工程(ブロックコポリマー製造工程)を含んでよい。
又は、実施形態のブロックコポリマーの製造方法は、芳香族ポリスルホン(a)を製造する工程(芳香族ポリスルホン製造工程)を、さらに含んでよい。
前記芳香族ポリスルホン(a)と、末端にヒドロキシ基を有するポリオキシアルキレン化合物(b)と、を反応させる工程(ブロックコポリマー製造工程)を含んでよい。
-X1及び-X2は、それぞれ独立に、-OH又は-Clであり、-X1及び-X2の少なくとも一方は、-Clである。]
原料として使用される上記の芳香族ポリスルホン(a)の、ゲル浸透クロマトグラフィーによりDMF溶媒で測定された重量平均分子量は、20000以上であってもよく、20000以上70000以下であってもよく、20000以上65000以下であってもよい。
原料として使用される上記のポリオキシアルキレン化合物(b)の重量平均分子量は、2000以上であってもよく、2000以上20000以下であってもよく、2000以上10000以下であってもよい。
ここで、末端に少なくとも1つのCl原子を有する芳香族ポリスルホン(a)としては、前記一般式(a-1)で表される化合物が好ましい。末端にヒドロキシ基を有するポリオキシアルキレン化合物(b)としては、前記一般式(b-1)で表される化合物が好ましい。
上記の非プロトン性極性溶媒の沸点の数値範囲の一例としては、120℃以上230℃以下であってもよく、140℃以上210℃以下であってもよく、150℃以上210℃以下であってもよい。
芳香族ポリスルホン(a)と、ポリオキシアルキレン化合物(b)と、の反応において、水と共沸混合物を形成する溶媒の使用量を低減することにより、製造されるブロックコポリマーの分子量を向上可能である。
上記の水と共沸混合物を形成する溶媒の沸点の数値範囲の一例としては、40℃以上250℃以下であってもよく、80℃以上230℃以下であってもよく、100℃以上210℃以下であってもよい。
上記の芳香族ポリスルホン(a)と、ポリオキシアルキレン化合物(b)との反応温度の数値範囲の一例としては、100℃以上250℃以下であってもよく、120℃以上230℃以下であってもよく、140℃以上210℃以下であってもよい。
本実施形態において、ブロックコポリマーの貧溶媒は、1種を単独で用いてもよいし、2種以上を併用してもよい。
各ブロックコポリマーにおける、重量平均分子量(Mw)を、GPC測定により求めた。なお、Mwはいずれも2回測定し、その平均値を記載した。
[測定条件]
試料:10mM臭化リチウム含有N,N-ジメチルホルムアミド溶液1mLに対し、測定対象のブロックコポリマー0.002gを配合
試料注入量:100μL
カラム(固定相):東ソー株式会社製「TSKgel GMHHR-H」(7.8mmφ×300mm)を2本直列に連結
カラム温度:40℃
溶離液(移動相):10mM臭化リチウム含有N,N-ジメチルホルムアミド
溶離液流量:0.8mL/分
検出器:示差屈折率計(RI)+光散乱光度計(LS)
分子量算出法:光散乱光度計(LS)の測定結果から分子量を算出(試料のdn/dcを0.187とし分子量を算出した)
溶液1H-NMRの測定には、測定対象のブロックコポリマーの濃度が80mg/mLとなるように、各例のブロックコポリマーを重ジメチルスルホキシドに溶解させた試料を用いた。測定条件は次のとおりである。
[測定条件]
測定装置:ECZ400S(JEOL社製)
静磁場強度:9.4テスラ(共鳴周波数:400MHz(1H))
スピニング:15Hz
繰り返し時間:7.2s
積算回数:64回
温度:23℃
化学シフト標準物質:ジメチルスルホキシド
上記<溶液1H-NMRの測定>で測定されたスペクトルの、芳香族ポリスルホンブロック(A)を構成している構造単位(-ph1-SO2-ph2-O-)において、Sに結合するph1の炭素原子に隣接する2つの炭素原子にそれぞれ1つずつ結合している水素原子、及びSに結合するph2の炭素原子に隣接する2つの炭素原子にそれぞれ1つずつ結合している水素原子(計4つの水素原子)に帰属されるピーク面積(Xp01)と、ポリオキシアルキレンブロック(B)を構成している構造単位(-CH2-CH2-O-)において、炭素原子に結合している水素原子(計4つの水素原子)に帰属されるピーク面積(Zp01)を用いて、それぞれの繰り返し単位の分子量を乗じ、下記式(m2)に基づいて算出した。
ポリオキシアルキレンブロック(B)の重量/芳香族ポリスルホンブロック(A)の重量の算出=(Zp01×44/(Xp01×232)・・・(m2)
なお、Xp01としては、7.25~7.27ppmの積分値を採用した。また、Zp01としては、3.4~3.6ppmの積分値を採用した。
ブロックコポリマーにおいて、芳香族ポリスルホンブロック(A)を構成している構造単位100ユニット当たりの、ポリオキシアルキレンブロック(B)に結合する末端OH基量(A01)は、NMR測定によって算出した。
具体的には、上記<溶液1H-NMRの測定>で測定されたスペクトルの、芳香族ポリスルホンブロック(A)を構成している構造単位(-ph1-SO2-ph2-O-)において、Sに結合するph1の炭素原子に隣接する2つの炭素原子にそれぞれ1つずつ結合している2つの水素原子、及びSに結合するph2の炭素原子に隣接する2つの炭素原子にそれぞれ1つずつ結合している2つの水素原子(計4つの水素原子)に帰属されるピーク面積(Xp01)と、ポリオキシアルキレンブロック(B)に結合するOH基の水素原子に帰属されるピーク面積(Yp01)とを用いて、下記式(m1)に基づいて算出した。
A01=Yp01/(Xp01/4)×100
=Yp01/Xp01×400・・・(m1)
なお、Xp01としては、7.25~7.27ppmの積分値を採用した。また、Yp01としては、4.53~4.60ppmの積分値を採用した。
[実施例1]
撹拌機、窒素導入管、温度計、及び先端に受器を付したコンデンサーを備えた重合槽内で、ポリエチレングリコール 8000(東京化成工業株式会社製、重量平均分子量9100)69.5g(PES1モルに対して約2モル当量)、炭酸カリウム0.92g及びN-メチル-2-ピロリドン(NMP)150gを混合し、100℃に昇温後、ポリエーテルスルホン(住友化学株式会社製、スミカエクセルPES 3600P,ゲル浸透クロマトグラフィーによりDMF溶媒で測定された重量平均分子量20000以上)100gを加えた。ポリエーテルスルホンが溶解した後、200℃で加熱し14時間反応させた。次いで、得られた反応混合溶液を、NMPで希釈し、室温まで冷却して、未反応の炭酸カリウム及び副生した塩化カリウムを析出させた。上述の溶液を水中に滴下し、芳香族ポリスルホンを析出させ、ろ過で不要なNMPを除去することにより、析出物を得た。
得られた析出物を、入念にメタノールおよび水で繰り返し洗浄し、100℃で加熱乾燥させることにより、ポリエチレングリコールブロックを有する、実施例1の芳香族ポリスルホンブロックコポリマーを得た。
実施例1において使用したポリエチレングリコールを、ポリエチレングリコール 4000(東京化成工業株式会社製、重量平均分子量3000)17.4g(PES1モルに対して約1モル当量)に代えた以外は、上記の実施例1と同様にして、実施例2の芳香族ポリスルホンブロックコポリマーを得た。
実施例1において使用したポリエチレングリコールを、ポリエチレングリコール 4000(東京化成工業株式会社製、重量平均分子量3000)11.0g(PES1モルに対して約2モル当量)に代え、炭酸カリウムの使用量を0.46gに代え、ポリエーテルスルホンを、ポリエーテルスルホン(住友化学株式会社製、スミカエクセルPES 5900P,ゲル浸透クロマトグラフィーによりDMF溶媒で測定された重量平均分子量30000以上)100gに代えた以外は、上記の実施例1と同様にして、実施例3の芳香族ポリスルホンブロックコポリマーを得た。
実施例1において使用したポリエチレングリコールを、ポリエチレングリコール 2000(東京化成工業株式会社製、重量平均分子量2100)10.4g(PES1モルに対して約2モル当量)に代え、炭酸カリウムの使用量を0.46gに代え、ポリエーテルスルホンを、ポリエーテルスルホン(住友化学株式会社製、スミカエクセルPES 4800P,ゲル浸透クロマトグラフィーによりDMF溶媒で測定された重量平均分子量25000以上)100gに代えた以外は、上記の実施例1と同様にして、実施例4の芳香族ポリスルホンブロックコポリマーを得た。
撹拌機、窒素導入管、温度計、及び先端に受器を付したコンデンサーを備えた重合槽内で、ポリエチレングリコール8000(東京化成工業株式会社製、重量平均分子量9100)107.6g(PES1モルに対して約3モル当量)、炭酸カリウム1.43g、4,4’-ジクロロジフェニルスルホン(DCDPS)1.4g及びN-メチル-2-ピロリドン(NMP)120gを混合し、100℃に昇温後、ポリエーテルスルホン(住友化学株式会社製、スミカエクセルPES 3600P,ゲル浸透クロマトグラフィーによりDMF溶媒で測定された重量平均分子量20000以上)80gを加えた。ポリエーテルスルホンが溶解した後、200℃で加熱し14時間反応させた。次いで、得られた反応混合溶液を、NMPで希釈し、室温まで冷却して、未反応の炭酸カリウム及び副生した塩化カリウムを析出させた。上述の溶液を水中に滴下し、芳香族ポリスルホンを析出させ、ろ過で不要なNMPを除去することにより、析出物を得た。
得られた析出物を、入念にメタノールおよび水で繰り返し洗浄し、100℃で加熱乾燥させることにより、比較例1の芳香族ポリスルホンブロックコポリマーを得た。
撹拌機、窒素導入管、温度計、及び先端に受器を付したコンデンサーを備えた重合槽内で、4,4’-ジクロロジフェニルスルホン(DCDPS)81.79g、4,4’-ジヒドロキシジフェニルスルホン(DHDPS)67.71g、ポリエチレングリコール 2000(東京化成工業株式会社製、重量平均分子量2100)29.20g及び炭酸カリウム41.34gを、窒素雰囲気下、NMP150mL中に懸濁させた。このバッチを1時間以内で190℃に加熱し、10時間反応させた。次いで、得られた反応混合溶液を、NMPで希釈し、室温まで冷却して、未反応の炭酸カリウム及び副生した塩化カリウムを析出させた。上述の溶液を水中に滴下し、芳香族ポリスルホンを析出させ、ろ過で不要なNMPを除去することにより、析出物を得た。
得られた析出物を、入念にメタノールおよび水で繰り返し洗浄し、100℃で加熱乾燥させることにより、比較例2の芳香族ポリスルホンブロックコポリマーを得た。
加熱容器内で、上述した各実施例の芳香族ポリスルホンブロックコポリマー、又は各比較例の芳香族ポリスルホンブロックコポリマーのいずれか18質量%と、NMP82質量%とをそれぞれ混合し、80℃で2時間撹拌することで、淡黄色の溶液を得た。これらの溶液を、厚さ3mmのガラス板の一面にフィルムアプリケーターを用いてそれぞれ塗布した後、水に浸漬させることで、各実施例又は各比較例の芳香族ポリスルホンブロックコポリマーからなる、膜厚が140~170μmの多孔質膜をそれぞれ形成した。
各例の多孔質膜をガラス板から剥離し、水により複数回洗浄した後、測定開始まで膜を水中で保存した。
直径47mmの圧力セルを用い、該圧力セルに装着できるように各例の多孔質膜をそれぞれ円形に切り出し、各例の試験膜を作製した。各例の試験膜を該圧力セルにそれぞれ装着し、各例の試験膜に対して、23℃、0.2バール(20kPa)の圧力で、純水をろ過し、ろ過開始から9分30秒経過時から10分経過時の間(30秒間)に、各例の試験膜を透過した純水の量を測定して、透水速度(J0)を求めた。
次に、各例の試験膜を用いて、ウシ血清アルブミン水溶液(100ppm)を、23℃、同じ圧力0.2バール(20kPa)でそれぞれ1時間ろ過した。その後、各例の試験膜を裏返し、23℃、0.1バール(10kPa)の圧力で、純水を2分間ろ過し、膜の洗浄を行った。再度、各例の試験膜を裏返し、23℃、0.2バール(20kPa)の圧力で、純水をろ過し、ろ過開始から9分30秒経過時から10分経過時の間(30秒間)に、各例の試験膜をそれぞれ透過した純水の量を測定して透水速度(J)を求めた。
得られた透水速度(J0)及び透水速度(J)から以下の式によって各例の試験膜の透水速度の回復率(%)を算出した。その結果を表1に示した。
なお、透水速度の回復率が高いほど、ファウリング耐性が高いことを意味する。
透水速度の回復率(%)=(J/J0)×100
J0:ウシ血清アルブミンろ過前の透水速度(L/m2/h/105Pa)
J:ウシ血清アルブミンろ過後の透水速度(L/m2/h/105Pa)
Claims (9)
- 芳香族ポリスルホンブロック(A)及びポリオキシアルキレンブロック(B)を含むブロックコポリマーであって、
前記ブロックコポリマーは、主鎖末端に少なくとも1つの末端OH基を有し、
1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの前記末端OH基の数が、0.43以上2以下である、ブロックコポリマー。 - 1H-NMR測定によって取得されたスペクトルのピーク面積から算出された、前記芳香族ポリスルホンブロック(A)を構成している構造単位100ユニットあたりの、前記ポリオキシアルキレンブロック(B)に結合している前記末端OH基の数が、0.43以上2以下である、請求項1に記載のブロックコポリマー。
- 前記ポリオキシアルキレンブロック(B)の重量/前記芳香族ポリスルホンブロック(A)の重量で表される比が0.05以上である、請求項1又は2に記載のブロックコポリマー。
- 重量平均分子量が20000~150000である、請求項1~6のいずれか一項に記載のブロックコポリマー。
- 前記末端OH基を有する前記ポリオキシアルキレンブロック(B)、前記芳香族ポリスルホンブロック(A)、及び前記末端OH基を有する前記ポリオキシアルキレンブロック(B)の順に、前記3つのブロックを有する直鎖状トリブロックコポリマー、並びに
前記末端OH基を有する前記ポリオキシアルキレンブロック(B)及び前記芳香族ポリスルホンブロック(A)の前記2つのブロックを有する直鎖状ジブロックコポリマー、からなる群から選ばれる少なくとも一種のブロックコポリマーである、請求項1~7のいずれか一項に記載のブロックコポリマー。 - 前記ブロックコポリマーの総質量(100質量%)に占める、前記芳香族ポリスルホンブロック(A)及び前記ポリオキシアルキレンブロック(B)の割合が、80質量%以上100質量%以下である、請求項1~8のいずれか一項に記載のブロックコポリマー。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023545706A JPWO2023033164A1 (ja) | 2021-09-06 | 2022-09-05 | |
| CN202280059092.3A CN117881722A (zh) | 2021-09-06 | 2022-09-05 | 嵌段共聚物 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021144891 | 2021-09-06 | ||
| JP2021-144891 | 2021-09-06 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2023033164A1 true WO2023033164A1 (ja) | 2023-03-09 |
Family
ID=85412421
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2022/033206 WO2023033164A1 (ja) | 2021-09-06 | 2022-09-05 | ブロックコポリマー |
Country Status (3)
| Country | Link |
|---|---|
| JP (1) | JPWO2023033164A1 (ja) |
| CN (1) | CN117881722A (ja) |
| WO (1) | WO2023033164A1 (ja) |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5911880A (en) * | 1995-12-15 | 1999-06-15 | Research Corporation Technologies, Inc. | Self-wetting membranes from engineering plastics |
| JP2010058096A (ja) * | 2008-09-08 | 2010-03-18 | Toray Ind Inc | 親水化ポリエーテルスルホン分離膜及びその製造方法 |
| JP2016522849A (ja) * | 2013-05-02 | 2016-08-04 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | ブロックコポリマー |
| WO2021182348A1 (ja) * | 2020-03-09 | 2021-09-16 | 住友化学株式会社 | ブロックコポリマーの製造方法及びブロックコポリマー |
| WO2021182342A1 (ja) * | 2020-03-09 | 2021-09-16 | 住友化学株式会社 | ブロックコポリマー |
| JP2021144891A (ja) | 2020-03-13 | 2021-09-24 | 本田技研工業株式会社 | 金属セパレータ及びセパレータの製造方法 |
-
2022
- 2022-09-05 CN CN202280059092.3A patent/CN117881722A/zh active Pending
- 2022-09-05 WO PCT/JP2022/033206 patent/WO2023033164A1/ja active Application Filing
- 2022-09-05 JP JP2023545706A patent/JPWO2023033164A1/ja active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5911880A (en) * | 1995-12-15 | 1999-06-15 | Research Corporation Technologies, Inc. | Self-wetting membranes from engineering plastics |
| JP2010058096A (ja) * | 2008-09-08 | 2010-03-18 | Toray Ind Inc | 親水化ポリエーテルスルホン分離膜及びその製造方法 |
| JP2016522849A (ja) * | 2013-05-02 | 2016-08-04 | ビーエーエスエフ ソシエタス・ヨーロピアBasf Se | ブロックコポリマー |
| WO2021182348A1 (ja) * | 2020-03-09 | 2021-09-16 | 住友化学株式会社 | ブロックコポリマーの製造方法及びブロックコポリマー |
| WO2021182342A1 (ja) * | 2020-03-09 | 2021-09-16 | 住友化学株式会社 | ブロックコポリマー |
| JP2021144891A (ja) | 2020-03-13 | 2021-09-24 | 本田技研工業株式会社 | 金属セパレータ及びセパレータの製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2023033164A1 (ja) | 2023-03-09 |
| CN117881722A (zh) | 2024-04-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2008507614A (ja) | ポリスルホン−ポリエーテルブロックコポリマー、その合成方法、該コポリマーから製造した膜 | |
| EP3850032B1 (en) | Polyarylene ether | |
| CN112673052A (zh) | 聚亚芳基醚砜 | |
| CN110914336A (zh) | 磺化的聚芳基醚砜及其膜 | |
| JP7254726B2 (ja) | 新規な膜ポリマーおよび膜 | |
| CN110892000A (zh) | 亲水性共聚物和膜 | |
| US20210340332A1 (en) | Method for producing aromatic polyethersulfones containing isohexide | |
| WO2023033164A1 (ja) | ブロックコポリマー | |
| JP2022500528A (ja) | ポリアリーレンエーテルコポリマー | |
| WO2021182348A1 (ja) | ブロックコポリマーの製造方法及びブロックコポリマー | |
| CN110922596A (zh) | 聚醚醚苯亚胺-醚醚砜共聚物、其制备方法和应用、聚醚醚酮-醚醚砜共聚物及其制备方法 | |
| WO2008073532A1 (en) | Polyarylether membranes | |
| WO2021182342A1 (ja) | ブロックコポリマー | |
| JP2010058073A (ja) | 親水化ポリエーテルスルホン分離膜及びその製造方法 | |
| JP2021535246A (ja) | 生物由来のフランジオールを含有する芳香族ポリエーテル | |
| EP1589057A2 (en) | Block copolymer, process to synthesize it, composition and article made therefrom | |
| WO2016050798A1 (en) | (co)polymers including cyclic diamides | |
| JP2023553775A (ja) | ポリフェニレンスルホン | |
| JP2022527265A (ja) | 半芳香族ポリエーテルの合成プロセス | |
| JP2022002839A (ja) | 多孔質膜 | |
| WO2024068442A1 (en) | Graft polyarylether copolymers | |
| WO2024068441A1 (en) | Graft polyarylether copolymers | |
| WO2020200666A1 (en) | Amorphous polymer (p) comprising segments (s1), (s2) and (s3) | |
| WO2023006830A1 (en) | Polyarylether copolymers based on diols sugar alcohols | |
| EP4263668A1 (en) | Bio-based sulfone copolymers free of bpa and bps |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 22864746 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2023545706 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 202280059092.3 Country of ref document: CN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2022864746 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2022864746 Country of ref document: EP Effective date: 20240408 |