WO2021200744A1 - 増殖細胞の生産方法、細胞生産物の生産方法、間葉系幹細胞集団およびその生産方法、幹細胞の培養上清およびその生産方法、並びに治療剤 - Google Patents
増殖細胞の生産方法、細胞生産物の生産方法、間葉系幹細胞集団およびその生産方法、幹細胞の培養上清およびその生産方法、並びに治療剤 Download PDFInfo
- Publication number
- WO2021200744A1 WO2021200744A1 PCT/JP2021/013099 JP2021013099W WO2021200744A1 WO 2021200744 A1 WO2021200744 A1 WO 2021200744A1 JP 2021013099 W JP2021013099 W JP 2021013099W WO 2021200744 A1 WO2021200744 A1 WO 2021200744A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- culture
- cells
- cell
- mesenchymal stem
- laminin
- Prior art date
Links
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 289
- 230000002062 proliferating effect Effects 0.000 title claims abstract description 114
- 210000004027 cell Anatomy 0.000 title claims description 691
- 210000002901 mesenchymal stem cell Anatomy 0.000 title claims description 306
- 239000012228 culture supernatant Substances 0.000 title claims description 278
- 210000000130 stem cell Anatomy 0.000 title claims description 126
- 239000000047 product Substances 0.000 title claims description 70
- 239000003814 drug Substances 0.000 title claims description 55
- 229940124597 therapeutic agent Drugs 0.000 title claims description 50
- 239000012634 fragment Substances 0.000 claims abstract description 280
- 238000000034 method Methods 0.000 claims abstract description 245
- 238000012258 culturing Methods 0.000 claims abstract description 79
- 230000027455 binding Effects 0.000 claims abstract description 70
- 102000006495 integrins Human genes 0.000 claims abstract description 57
- 108010044426 integrins Proteins 0.000 claims abstract description 57
- 239000000758 substrate Substances 0.000 claims abstract description 21
- 239000001963 growth medium Substances 0.000 claims description 182
- 230000012010 growth Effects 0.000 claims description 117
- 102000004127 Cytokines Human genes 0.000 claims description 80
- 108090000695 Cytokines Proteins 0.000 claims description 80
- 210000003954 umbilical cord Anatomy 0.000 claims description 79
- 238000011084 recovery Methods 0.000 claims description 77
- 230000001464 adherent effect Effects 0.000 claims description 53
- 238000004113 cell culture Methods 0.000 claims description 40
- 239000000853 adhesive Substances 0.000 claims description 38
- 230000001070 adhesive effect Effects 0.000 claims description 38
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims description 34
- 108090000623 proteins and genes Proteins 0.000 claims description 29
- 102000004169 proteins and genes Human genes 0.000 claims description 28
- 102100037241 Endoglin Human genes 0.000 claims description 23
- 101000881679 Homo sapiens Endoglin Proteins 0.000 claims description 23
- 239000006228 supernatant Substances 0.000 claims description 22
- 108010067306 Fibronectins Proteins 0.000 claims description 18
- 102000004877 Insulin Human genes 0.000 claims description 17
- 108090001061 Insulin Proteins 0.000 claims description 17
- 229940125396 insulin Drugs 0.000 claims description 17
- 102100021943 C-C motif chemokine 2 Human genes 0.000 claims description 15
- 101710155857 C-C motif chemokine 2 Proteins 0.000 claims description 15
- 102100025222 CD63 antigen Human genes 0.000 claims description 15
- 101000934368 Homo sapiens CD63 antigen Proteins 0.000 claims description 15
- 102000003814 Interleukin-10 Human genes 0.000 claims description 15
- 108090000174 Interleukin-10 Proteins 0.000 claims description 15
- 108090000978 Interleukin-4 Proteins 0.000 claims description 14
- 102000037865 fusion proteins Human genes 0.000 claims description 14
- 108020001507 fusion proteins Proteins 0.000 claims description 14
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims description 10
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims description 10
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 claims description 9
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 claims description 9
- MXNRLFUSFKVQSK-UHFFFAOYSA-N 2-Amino-6-(trimethylazaniumyl)hexanoate Chemical group C[N+](C)(C)CCCCC(N)C([O-])=O MXNRLFUSFKVQSK-UHFFFAOYSA-N 0.000 claims description 7
- 102000009027 Albumins Human genes 0.000 claims description 7
- 108010088751 Albumins Proteins 0.000 claims description 7
- 102000004338 Transferrin Human genes 0.000 claims description 5
- 108090000901 Transferrin Proteins 0.000 claims description 5
- 239000012581 transferrin Substances 0.000 claims description 5
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 claims 1
- 102000016359 Fibronectins Human genes 0.000 claims 1
- 230000035755 proliferation Effects 0.000 abstract description 31
- 108010085895 Laminin Proteins 0.000 description 256
- 239000000243 solution Substances 0.000 description 139
- 239000002609 medium Substances 0.000 description 70
- 210000001808 exosome Anatomy 0.000 description 38
- 238000010899 nucleation Methods 0.000 description 34
- 239000003102 growth factor Substances 0.000 description 30
- 210000003141 lower extremity Anatomy 0.000 description 27
- 210000002744 extracellular matrix Anatomy 0.000 description 23
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 21
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 21
- 102100034221 Growth-regulated alpha protein Human genes 0.000 description 21
- 239000000126 substance Substances 0.000 description 21
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 20
- 108010038862 laminin 10 Proteins 0.000 description 19
- 230000001225 therapeutic effect Effects 0.000 description 19
- 201000002818 limb ischemia Diseases 0.000 description 18
- 102100037362 Fibronectin Human genes 0.000 description 17
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 17
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 17
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 17
- 239000007640 basal medium Substances 0.000 description 16
- 230000017531 blood circulation Effects 0.000 description 16
- 201000010099 disease Diseases 0.000 description 16
- 238000002474 experimental method Methods 0.000 description 16
- 101150093802 CXCL1 gene Proteins 0.000 description 14
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 14
- 229920002971 Heparan sulfate Polymers 0.000 description 14
- 150000001413 amino acids Chemical class 0.000 description 14
- 239000006285 cell suspension Substances 0.000 description 14
- 230000000052 comparative effect Effects 0.000 description 14
- 102000004388 Interleukin-4 Human genes 0.000 description 13
- 108010002586 Interleukin-7 Proteins 0.000 description 13
- 102100021592 Interleukin-7 Human genes 0.000 description 13
- 208000027418 Wounds and injury Diseases 0.000 description 13
- 229940100994 interleukin-7 Drugs 0.000 description 13
- 238000012832 cell culture technique Methods 0.000 description 11
- -1 CD31 Proteins 0.000 description 10
- 210000001185 bone marrow Anatomy 0.000 description 10
- 230000010261 cell growth Effects 0.000 description 10
- 210000004700 fetal blood Anatomy 0.000 description 10
- 210000002826 placenta Anatomy 0.000 description 10
- 238000009331 sowing Methods 0.000 description 10
- LOGFVTREOLYCPF-KXNHARMFSA-N (2s,3r)-2-[[(2r)-1-[(2s)-2,6-diaminohexanoyl]pyrrolidine-2-carbonyl]amino]-3-hydroxybutanoic acid Chemical compound C[C@@H](O)[C@@H](C(O)=O)NC(=O)[C@H]1CCCN1C(=O)[C@@H](N)CCCCN LOGFVTREOLYCPF-KXNHARMFSA-N 0.000 description 9
- 102000003777 Interleukin-1 beta Human genes 0.000 description 9
- 108090000193 Interleukin-1 beta Proteins 0.000 description 9
- 102000004125 Interleukin-1alpha Human genes 0.000 description 9
- 108010082786 Interleukin-1alpha Proteins 0.000 description 9
- 241000700159 Rattus Species 0.000 description 9
- 239000002458 cell surface marker Substances 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 239000003550 marker Substances 0.000 description 9
- 229920001342 Bakelite® Polymers 0.000 description 8
- 206010052428 Wound Diseases 0.000 description 8
- 239000003797 essential amino acid Substances 0.000 description 8
- 235000020776 essential amino acid Nutrition 0.000 description 8
- 208000031104 Arterial Occlusive disease Diseases 0.000 description 7
- 102100032366 C-C motif chemokine 7 Human genes 0.000 description 7
- 108010055124 Chemokine CCL7 Proteins 0.000 description 7
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 7
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 7
- 101001069921 Homo sapiens Growth-regulated alpha protein Proteins 0.000 description 7
- 206010058571 Spinal cord infarction Diseases 0.000 description 7
- 208000021328 arterial occlusion Diseases 0.000 description 7
- 206010008118 cerebral infarction Diseases 0.000 description 7
- 208000026106 cerebrovascular disease Diseases 0.000 description 7
- 230000001684 chronic effect Effects 0.000 description 7
- 230000014509 gene expression Effects 0.000 description 7
- 208000023589 ischemic disease Diseases 0.000 description 7
- 108010028309 kalinin Proteins 0.000 description 7
- 238000001000 micrograph Methods 0.000 description 7
- 208000010125 myocardial infarction Diseases 0.000 description 7
- 102100022464 5'-nucleotidase Human genes 0.000 description 6
- 102100031092 C-C motif chemokine 3 Human genes 0.000 description 6
- 101710155856 C-C motif chemokine 3 Proteins 0.000 description 6
- 238000002965 ELISA Methods 0.000 description 6
- 102100023688 Eotaxin Human genes 0.000 description 6
- 101710139422 Eotaxin Proteins 0.000 description 6
- 108010010803 Gelatin Proteins 0.000 description 6
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 6
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 6
- 101000678236 Homo sapiens 5'-nucleotidase Proteins 0.000 description 6
- 101000800116 Homo sapiens Thy-1 membrane glycoprotein Proteins 0.000 description 6
- 102000003816 Interleukin-13 Human genes 0.000 description 6
- 108090000176 Interleukin-13 Proteins 0.000 description 6
- 102000003812 Interleukin-15 Human genes 0.000 description 6
- 108090000172 Interleukin-15 Proteins 0.000 description 6
- 108090001005 Interleukin-6 Proteins 0.000 description 6
- 102000004889 Interleukin-6 Human genes 0.000 description 6
- 108090001007 Interleukin-8 Proteins 0.000 description 6
- 102000004890 Interleukin-8 Human genes 0.000 description 6
- 102100033523 Thy-1 membrane glycoprotein Human genes 0.000 description 6
- 206010003246 arthritis Diseases 0.000 description 6
- 210000001671 embryonic stem cell Anatomy 0.000 description 6
- 235000012041 food component Nutrition 0.000 description 6
- 229920000159 gelatin Polymers 0.000 description 6
- 239000008273 gelatin Substances 0.000 description 6
- 235000019322 gelatine Nutrition 0.000 description 6
- 235000011852 gelatine desserts Nutrition 0.000 description 6
- 210000004263 induced pluripotent stem cell Anatomy 0.000 description 6
- 208000027866 inflammatory disease Diseases 0.000 description 6
- 230000000302 ischemic effect Effects 0.000 description 6
- 210000001778 pluripotent stem cell Anatomy 0.000 description 6
- 238000002360 preparation method Methods 0.000 description 6
- 208000009329 Graft vs Host Disease Diseases 0.000 description 5
- 108010002335 Interleukin-9 Proteins 0.000 description 5
- 230000002491 angiogenic effect Effects 0.000 description 5
- 230000006378 damage Effects 0.000 description 5
- 208000024908 graft versus host disease Diseases 0.000 description 5
- 210000003897 hepatic stem cell Anatomy 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 208000014674 injury Diseases 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 230000007774 longterm Effects 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 210000001665 muscle stem cell Anatomy 0.000 description 5
- 230000001172 regenerating effect Effects 0.000 description 5
- 210000002966 serum Anatomy 0.000 description 5
- 210000001988 somatic stem cell Anatomy 0.000 description 5
- 208000023275 Autoimmune disease Diseases 0.000 description 4
- 208000027932 Collagen disease Diseases 0.000 description 4
- 206010050685 Cytokine storm Diseases 0.000 description 4
- 206010012438 Dermatitis atopic Diseases 0.000 description 4
- 102400001368 Epidermal growth factor Human genes 0.000 description 4
- 101800003838 Epidermal growth factor Proteins 0.000 description 4
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 description 4
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 4
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 4
- 102000014429 Insulin-like growth factor Human genes 0.000 description 4
- 102000000585 Interleukin-9 Human genes 0.000 description 4
- 206010028980 Neoplasm Diseases 0.000 description 4
- 102000046299 Transforming Growth Factor beta1 Human genes 0.000 description 4
- 101800002279 Transforming growth factor beta-1 Proteins 0.000 description 4
- 201000008937 atopic dermatitis Diseases 0.000 description 4
- 201000011510 cancer Diseases 0.000 description 4
- 239000006143 cell culture medium Substances 0.000 description 4
- 230000004663 cell proliferation Effects 0.000 description 4
- 206010052015 cytokine release syndrome Diseases 0.000 description 4
- 230000003247 decreasing effect Effects 0.000 description 4
- 229940116977 epidermal growth factor Drugs 0.000 description 4
- 230000006698 induction Effects 0.000 description 4
- 206010023332 keratitis Diseases 0.000 description 4
- 201000006417 multiple sclerosis Diseases 0.000 description 4
- 201000008383 nephritis Diseases 0.000 description 4
- 238000011002 quantification Methods 0.000 description 4
- 229940099456 transforming growth factor beta 1 Drugs 0.000 description 4
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 4
- UZOVYGYOLBIAJR-UHFFFAOYSA-N 4-isocyanato-4'-methyldiphenylmethane Chemical compound C1=CC(C)=CC=C1CC1=CC=C(N=C=O)C=C1 UZOVYGYOLBIAJR-UHFFFAOYSA-N 0.000 description 3
- 206010003805 Autism Diseases 0.000 description 3
- 208000020706 Autistic disease Diseases 0.000 description 3
- 102100032912 CD44 antigen Human genes 0.000 description 3
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 description 3
- 102000035195 Peptidases Human genes 0.000 description 3
- 108091005804 Peptidases Proteins 0.000 description 3
- 239000012980 RPMI-1640 medium Substances 0.000 description 3
- 208000013738 Sleep Initiation and Maintenance disease Diseases 0.000 description 3
- 235000010724 Wisteria floribunda Nutrition 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000021164 cell adhesion Effects 0.000 description 3
- 238000005138 cryopreservation Methods 0.000 description 3
- 208000026278 immune system disease Diseases 0.000 description 3
- 238000012744 immunostaining Methods 0.000 description 3
- 206010022437 insomnia Diseases 0.000 description 3
- 208000020016 psychiatric disease Diseases 0.000 description 3
- 238000012453 sprague-dawley rat model Methods 0.000 description 3
- 208000011580 syndromic disease Diseases 0.000 description 3
- 230000002792 vascular Effects 0.000 description 3
- 230000029663 wound healing Effects 0.000 description 3
- 108090000100 Hepatocyte Growth Factor Proteins 0.000 description 2
- 102100021866 Hepatocyte growth factor Human genes 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 102000040739 Secretory proteins Human genes 0.000 description 2
- 108091058545 Secretory proteins Proteins 0.000 description 2
- 108090000992 Transferases Proteins 0.000 description 2
- 102000004357 Transferases Human genes 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 238000004115 adherent culture Methods 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 210000004748 cultured cell Anatomy 0.000 description 2
- 229940088597 hormone Drugs 0.000 description 2
- 239000005556 hormone Substances 0.000 description 2
- 210000005260 human cell Anatomy 0.000 description 2
- 238000003384 imaging method Methods 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 239000002207 metabolite Substances 0.000 description 2
- 210000005036 nerve Anatomy 0.000 description 2
- 210000002569 neuron Anatomy 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000000644 propagated effect Effects 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 239000012679 serum free medium Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 238000010257 thawing Methods 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 210000003462 vein Anatomy 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 108010067225 Cell Adhesion Molecules Proteins 0.000 description 1
- 102000016289 Cell Adhesion Molecules Human genes 0.000 description 1
- 241000725101 Clea Species 0.000 description 1
- 235000005956 Cosmos caudatus Nutrition 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000006354 HLA-DR Antigens Human genes 0.000 description 1
- 108010058597 HLA-DR Antigens Proteins 0.000 description 1
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 description 1
- 206010019909 Hernia Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 description 1
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 108010065805 Interleukin-12 Proteins 0.000 description 1
- 102000013462 Interleukin-12 Human genes 0.000 description 1
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- 108010004729 Phycoerythrin Proteins 0.000 description 1
- 102100024616 Platelet endothelial cell adhesion molecule Human genes 0.000 description 1
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- 230000006052 T cell proliferation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000003444 anaesthetic effect Effects 0.000 description 1
- 210000003423 ankle Anatomy 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 238000011882 arthroplasty Methods 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 238000002659 cell therapy Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000000799 fluorescence microscopy Methods 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 210000003090 iliac artery Anatomy 0.000 description 1
- 210000003111 iliac vein Anatomy 0.000 description 1
- 230000005931 immune cell recruitment Effects 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000007365 immunoregulation Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 229940076144 interleukin-10 Drugs 0.000 description 1
- 229940117681 interleukin-12 Drugs 0.000 description 1
- 229940028885 interleukin-4 Drugs 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 229960002725 isoflurane Drugs 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 210000001178 neural stem cell Anatomy 0.000 description 1
- 230000003959 neuroinflammation Effects 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 230000001131 transforming effect Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 230000006711 vascular endothelial growth factor production Effects 0.000 description 1
- 239000011782 vitamin Substances 0.000 description 1
- 229940088594 vitamin Drugs 0.000 description 1
- 229930003231 vitamin Natural products 0.000 description 1
- 235000013343 vitamin Nutrition 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/28—Bone marrow; Haematopoietic stem cells; Mesenchymal stem cells of any origin, e.g. adipose-derived stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
- C12N5/0665—Blood-borne mesenchymal stem cells, e.g. from umbilical cord blood
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0662—Stem cells
- C12N5/0668—Mesenchymal stem cells from other natural sources
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/12—Hepatocyte growth factor [HGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/15—Transforming growth factor beta (TGF-β)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/21—Chemokines, e.g. MIP-1, MIP-2, RANTES, MCP, PF-4
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2301—Interleukin-1 (IL-1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2304—Interleukin-4 (IL-4)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/231—Interleukin-10 (IL-10)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/25—Tumour necrosing factors [TNF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/599—Cell markers; Cell surface determinants with CD designations not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/50—Proteins
- C12N2533/52—Fibronectin; Laminin
Abstract
Description
更に、本発明は、上述の細胞培養技術に基づいて、新規特徴を有する間葉系幹細胞集団を提供すること、および、上述の細胞培養技術に基づいて、多量のサイトカインなどの細胞生産物を含む、幹細胞の培養上清を提供することを目的とする。また、本発明は、上述の間葉系幹細胞集団または上述の培養上清を含む治療剤を提供することを目的とする。
上述の「増殖細胞の生産方法」に従って細胞を増殖培養液中で培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと
を含む、細胞生産物の生産方法が提供される。
更に別の側面によれば、
上述の「増殖細胞の生産方法」に従って細胞を増殖培養液中で培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返される、細胞生産物の生産方法が提供される。
更に別の側面によれば、HLA-ABC陽性の間葉系幹細胞の比率が70%以下である間葉系幹細胞集団が提供される。
更に別の側面によれば、
幹細胞の培養上清の生産方法であって、
幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返され、前記方法が、前記生産培養液中での前記培養の後に、前記生産培養液の上清を回収することを更に含む、方法が提供される。
更に別の側面によれば、5000pg/mL以上のHGFを含有する、幹細胞の培養上清が提供される。
更に別の側面によれば、50pg/mL以上のCD9/CD63 ECドメイン 融合タンパク質を含有する、幹細胞の培養上清が提供される。
更に別の側面によれば、上述の間葉系幹細胞集団または上述の培養上清を含む治療剤が提供される。
本発明によれば、上述の細胞培養技術に基づいて、新規特徴を有する間葉系幹細胞集団を提供すること、および、多量のサイトカインなどの細胞生産物を含む、幹細胞の培養上清を提供することができる。また、本発明によれば、上述の間葉系幹細胞集団または上述の培養上清を含む治療剤を提供することができる。
1つの側面によれば、0.002~2000細胞/cm2の細胞密度で播種された細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、前記細胞を増殖させることを含む、増殖細胞の生産方法が提供される。
ラミニンフラグメントまたはその改変体を含有する増殖培養液を予め調製し、細胞を、0.002~2000細胞/cm2の播種密度になるように、予め調製された増殖培養液に懸濁し、得られた細胞懸濁液を培養容器に播種することと、
前記細胞を前記増殖培養液中で、接着培養により培養して、前記細胞を増殖させることと
を含むことができる。
細胞を、0.002~2000細胞/cm2の播種密度になるように増殖培養液に懸濁し、得られた細胞懸濁液にラミニンフラグメントまたはその改変体を添加し、これを培養容器に播種することと、
前記細胞を前記増殖培養液中で、接着培養により培養して、前記細胞を増殖させることと
を含むことができる。
細胞を、0.002~2000細胞/cm2の播種密度になるように増殖培養液に懸濁し、得られた細胞懸濁液を培養容器に播種し、播種された細胞懸濁液にラミニンフラグメントまたはその改変体を添加することと、
前記細胞を前記増殖培養液中で、接着培養により培養して、前記細胞を増殖させることと
を含むことができる。
細胞としては、任意の細胞、例えば幹細胞を使用することができる。細胞は、好ましくは、間葉系幹細胞、人工多能性幹細胞(iPS細胞)、または胚性幹細胞(ES細胞)であり、より好ましくは間葉系幹細胞である。細胞は、より好ましくは、臍帯由来間葉系幹細胞、骨髄由来間葉系幹細胞、脂肪由来間葉系幹細胞、胎盤由来間葉系幹細胞、または臍帯血由来間葉系幹細胞であり、更に好ましくは臍帯由来間葉系幹細胞である。
この方法では、細胞を0.002~2000細胞/cm2の細胞密度で増殖培養液に播種する。
0.002~2000細胞/cm2の細胞密度で播種された細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントまたはその改変体の存在下で、接着培養により培養する。
従来、細胞を低い細胞密度で播種すると、細胞の増殖が停止し、コンフルエントの状態になるまで増殖させることができなかったのに対し、上述の方法によれば、低い細胞密度で播種された細胞を高い増殖倍率で増殖させることができる。これにより、培養容器1枚の細胞から、次の代で培養される培養容器の枚数を増やすことができ、増殖細胞や細胞由来成分を効率良く生産することができる。
<2-1.第1実施形態(1回の生産培養工程を行う実施形態)>
別の側面によれば、上述の「増殖細胞の生産方法」に従って細胞を増殖培養液中で培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと
を含む、細胞生産物の生産方法が提供される。
0.002~2000細胞/cm2の細胞密度で播種された細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと
を含む。
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと
を含む、細胞生産物の生産方法が提供される。
増殖培養までの工程は、<1.増殖細胞の生産方法>の欄で説明したとおり行うことができる。これにより、増殖細胞を接着状態で得ることができる。増殖培養を、細胞がコンフルエントの状態に達するまで行えば、増殖細胞をコンフルエントの状態で得ることができる。
増殖培養後、増殖細胞を、接着状態を維持したまま、生産培養液中で培養する。「増殖細胞を、接着状態を維持したまま、生産培養液中で培養する」とは、増殖培養後、培養容器底面に接着している細胞を、培養容器底面から剥がさないで接着状態を維持したまま生産培養を行うことを意味する。
従来、増殖培養の途中で細胞の増殖が停止したり、生産培養の途中で細胞が培養容器から剥離して、細胞の接着状態を維持することができなかったりしたのに対し、上述の方法によれば、低い細胞密度で播種された細胞を高い増殖倍率で増殖させ、その後、得られた増殖細胞の接着状態を維持したまま生産培養を行うことができる。これにより、簡便な手法で多量の細胞生産物を生産することができる。
別の側面によれば、
上述の「増殖細胞の生産方法」に従って細胞を増殖培養液中で培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返される、細胞生産物の生産方法が提供される。
0.002~2000細胞/cm2の細胞密度で播種された細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返される。
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返される、細胞生産物の生産方法が提供される。
増殖培養までの工程は、<1.増殖細胞の生産方法>の欄で説明したとおり行うことができる。これにより、増殖細胞を接着状態で得ることができる。増殖培養を、細胞がコンフルエントの状態に達するまで行えば、増殖細胞をコンフルエントの状態で得ることができる。
生産培養の工程は、<2-1.第1実施形態(1回の生産培養工程を行う実施形態)>の欄で説明したとおり行うことができる。これにより、細胞に細胞生産物を生産させることができる。
生産培養後、増殖細胞を、接着状態を維持したまま、回復培養液中で培養する。「増殖細胞を、接着状態を維持したまま、回復培養液中で培養する」とは、生産培養後、培養容器底面に接着している細胞を、培養容器底面から剥がさないで接着状態を維持したまま回復培養を行うことを意味する。
第2実施形態に係る方法は、第1実施形態に係る方法と同様、低い細胞密度で播種された細胞を高い増殖倍率で増殖させ、その後、得られた増殖細胞の接着状態を維持したまま生産培養を行うことができる。加えて、第2実施形態に係る方法は、生産培養を終えた細胞の接着状態を維持したまま回復培養を行い、細胞が細胞生産物を生産する能力を回復させることができる。これにより、細胞の接着状態を維持したまま複数回の生産培養工程を繰り返し行うことができ、その結果、簡便な手法で多量の細胞生産物を長期にわたって生産することができる。
以下に、本発明の好ましい実施形態をまとめて示す。
[A1] 0.002~2000細胞/cm2の細胞密度で播種された細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、前記細胞を増殖させることを含む、増殖細胞の生産方法。
[A2] 0.002~2000細胞/cm2の細胞密度で播種された細胞を、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質を含有する増殖培養液中で、接着培養により培養して、前記細胞を増殖させることを含む、増殖細胞の生産方法。
[A3] 増殖培養液と、0.002~2000細胞/cm2の播種密度を達成する量の細胞と、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質とを含む細胞懸濁液を培養容器に播種することと、その後、
前記細胞を前記増殖培養液中で、接着培養により培養して、前記細胞を増殖させることと
を含む、増殖細胞の生産方法。
[A4] 増殖培養液と、0.002~2000細胞/cm2の播種密度を達成する量の細胞とを含む細胞懸濁液を培養容器に播種することと、
播種された前記細胞懸濁液に、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質を添加することと、その後、
前記細胞を前記増殖培養液中で、接着培養により培養して、前記細胞を増殖させることと
を含む、増殖細胞の生産方法。
[A5] 前記細胞が幹細胞である[A1]~[A4]の何れか1に記載の方法。
[A7] 前記細胞が間葉系幹細胞である[A1]~[A6]の何れか1に記載の方法。
[A8] 前記細胞が、臍帯由来間葉系幹細胞、骨髄由来間葉系幹細胞、脂肪由来間葉系幹細胞、胎盤由来間葉系幹細胞、または臍帯血由来間葉系幹細胞である[A1]~[A7]の何れか1に記載の方法。
[A9] 前記細胞が臍帯由来間葉系幹細胞である[A1]~[A8]の何れか1に記載の方法。
[A10] 前記細胞がヒト幹細胞である[A1]~[A5]の何れか1に記載の方法。
[A12] 前記細胞がヒト間葉系幹細胞である[A1]~[A7]、[A10]および[A11]の何れか1に記載の方法。
[A13] 前記細胞が、ヒト臍帯由来間葉系幹細胞、ヒト骨髄由来間葉系幹細胞、ヒト脂肪由来間葉系幹細胞、ヒト胎盤由来間葉系幹細胞、またはヒト臍帯血由来間葉系幹細胞である[A1]~[A8]および[A10]~[A12]の何れか1に記載の方法。
[A14] 前記細胞がヒト臍帯由来間葉系幹細胞である[A1]~[A13]の何れか1に記載の方法。
[A15] 前記細胞が凍結細胞である[A1]~[A14]の何れか1に記載の方法。
[A17] 前記細胞が、0.002~1900細胞/cm2、好ましくは0.002~1800細胞/cm2、より好ましくは0.002~1700細胞/cm2、更に好ましくは0.002~1600細胞/cm2、更に好ましくは0.002~1500細胞/cm2、更に好ましくは0.002~1400細胞/cm2、更に好ましくは0.002~1300細胞/cm2、更に好ましくは0.002~1200細胞/cm2、更に好ましくは0.002~1100細胞/cm2、更に好ましくは0.002~1000細胞/cm2、更に好ましくは0.002~900細胞/cm2、更に好ましくは0.002~800細胞/cm2、更に好ましくは0.002~700細胞/cm2、更に好ましくは0.002~600細胞/cm2、更に好ましくは0.002~500細胞/cm2、更に好ましくは0.002~400細胞/cm2、更に好ましくは0.002~300細胞/cm2、更に好ましくは0.002~200細胞/cm2、更に好ましくは0.002~100細胞/cm2の細胞密度で播種される[A1]~[A16]の何れか1に記載の方法。
[A18] 前記細胞が、1~2000細胞/cm2、好ましくは1~1900細胞/cm2、より好ましくは1~1800細胞/cm2、更に好ましくは1~1700細胞/cm2、更に好ましくは1~1600細胞/cm2、更に好ましくは1~1500細胞/cm2、更に好ましくは1~1400細胞/cm2、更に好ましくは1~1300細胞/cm2、更に好ましくは1~1200細胞/cm2、更に好ましくは1~1100細胞/cm2、更に好ましくは1~1000細胞/cm2、更に好ましくは1~900細胞/cm2、更に好ましくは1~800細胞/cm2、更に好ましくは1~700細胞/cm2、更に好ましくは1~600細胞/cm2、更に好ましくは1~500細胞/cm2、更に好ましくは1~400細胞/cm2、更に好ましくは1~300細胞/cm2、更に好ましくは1~200細胞/cm2、更に好ましくは1~100細胞/cm2の細胞密度で播種される[A1]~[A16]の何れか1に記載の方法。
[A19] 前記増殖培養液が、前記細胞の増殖を促進するタンパク質を含む増殖培養液である[A1]~[A18]の何れか1に記載の方法。
[A20] 前記増殖培養液が、増殖因子を追加した細胞培養用基本培地を含む培養液である[A1]~[A19]の何れか1に記載の方法。
[A22] 前記培養が、前記細胞がコンフルエントの状態に達するまで行われる[A1]~[A21]の何れか1に記載の方法。
[A23] 前記培養が、500cm2以上の底面積を有する培養容器で行われる[A1]~[A22]の何れか1に記載の方法。
[A24] 前記培養が、500~10000cm2の底面積を有する培養容器で行われる[A1]~[A23]の何れか1に記載の方法。
[A25] 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントである[A1]~[A24]の何れか1に記載の方法。
[A27] 前記ラミニンフラグメントが、ラミニンE8フラグメントである[A25]または[A26]に記載の方法。
[A28] 前記ラミニンフラグメントが、ラミニン511 E8フラグメント、ラミニン521 E8フラグメント、ラミニン411 E8フラグメント、ラミニン421 E8フラグメント、ラミニン332 E8フラグメント、ラミニン311 E8フラグメント、ラミニン321 E8フラグメント、ラミニン211 E8フラグメント、ラミニン221 E8フラグメント、ラミニン213 E8フラグメント、ラミニン111 E8フラグメント、またはラミニン121 E8フラグメントである[A25]~[A27]の何れか1に記載の方法。
[A29] 前記ラミニンフラグメントが、ラミニン511 E8フラグメントである[A25]~[A28]の何れか1に記載の方法。
[A30] 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントの改変体である[A1]~[A24]の何れか1に記載の方法。
[A32] 前記改変体が、インテグリン結合活性を有するラミニンフラグメントと増殖因子結合分子との複合体である[A30]または[A31]に記載の方法。
[A33] 前記ラミニンフラグメントが、ラミニンE8フラグメントである[A31]または[A32]に記載の方法。
[A34] 前記ラミニンE8フラグメントが、ラミニン511 E8フラグメント、ラミニン521 E8フラグメント、ラミニン411 E8フラグメント、ラミニン421 E8フラグメント、ラミニン332 E8フラグメント、ラミニン311 E8フラグメント、ラミニン321 E8フラグメント、ラミニン211 E8フラグメント、ラミニン221 E8フラグメント、ラミニン213 E8フラグメント、ラミニン111 E8フラグメント、またはラミニン121 E8フラグメントである[A33]に記載の方法。
[A35] 前記ラミニンE8フラグメントが、ラミニン511 E8フラグメントである[A33]または[A34]に記載の方法。
[A36] 前記ラミニンE8フラグメントが、ラミニン421 E8フラグメントである[A33]または[A34]に記載の方法。
[A38] 前記改変体が、ラミニン511 E8フラグメントとヘパラン硫酸との複合体である[A30]~[A37]の何れか1に記載の方法。
[A39] 前記改変体が、ラミニン421 E8フラグメントとヘパラン硫酸との複合体である[A30]~[A37]の何れか1に記載の方法。
[A40] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.005μg~2μgである[A1]~[A39]の何れか1に記載の方法。
[A41] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.01μg~0.5μgである[A1]~[A40]の何れか1に記載の方法。
[A42] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.05μg~0.25μgである[A1]~[A41]の何れか1に記載の方法。
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと
を含む、細胞生産物の生産方法。
[B2] [A1]~[A42]の何れか1に記載の方法に従って細胞を増殖培養液中で培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返される、細胞生産物の生産方法。
[B3] 前記細胞生産物が、アミノ酸、脂質、糖などの細胞代謝物;ホルモン;ペプチド;サイトカイン、細胞外マトリックスなどの分泌タンパク質;またはエクソソームである[B1]または[B2]に記載の方法。
[B4] 前記細胞生産物がサイトカインである[B1]~[B3]の何れか1に記載の方法。
[B5] 前記細胞生産物がエクソソームである[B1]~[B3]の何れか1に記載の方法。
[B7] 前記生産培養液が、サイトカインやインスリンを含まない培養液である[B1]~[B6]の何れか1に記載の方法。
[B8] 前記生産培養液が、タンパク質を含まない培養液である[B1]~[B7]の何れか1に記載の方法。
[B9] 前記生産培養液が、血清を含まない培養液である[B1]~[B8]の何れか1に記載の方法。
[B10] 前記生産培養液中での前記培養の後に、前記生産培養液の上清を回収することを更に含む[B1]~[B9]の何れか1に記載の方法。
[B12] 前記生産培養液が、細胞培養用基本培地であるか、または細胞の栄養成分を追加した細胞培養用基本培地である[B1]~[B11]の何れか1に記載の方法。
[B13] 前記生産培養液が、細胞の栄養成分、好ましくはアミノ酸を追加した細胞培養用基本培地である[B1]~[B12]の何れか1に記載の方法。
[B14] 前記生産培養液が、ラミニンフラグメントまたはその改変体を含まない[B1]~[B13]の何れか1に記載の方法。
[B15] 前記生産培養液中での前記培養が、0.5~10日間、好ましくは2~5日間にわたって行われる[B1]~[B14]の何れか1に記載の方法。
[B17] 前記回復培養液が、前記細胞の増殖を促進するタンパク質を含む培養液である[B2]~[B16]の何れか1に記載の方法。
[B18] 前記回復培養液が、増殖因子を追加した細胞培養用基本培地を含む培養液である[B2]~[B17]の何れか1に記載の方法。
[B19] 前記回復培養液が、増殖因子を追加した細胞培養用基本培地である[B2]~[B18]の何れか1に記載の方法。
[B20] 前記回復培養液が、前記増殖培養液と同じ組成を有する[B2]~[B19]の何れか1に記載の方法。
[B22] 前記回復培養液中での前記培養が、0.5~10日間、好ましくは2~5日間にわたって行われる[B2]~[B21]の何れか1に記載の方法。
[B23] 前記生産培養液中での前記培養と前記回復培養液中での前記培養とのサイクルが、2~10回繰り返される[B2]~[B22]の何れか1に記載の方法。
本発明者らは、<1.増殖細胞の生産方法>の欄で説明した方法に従って、間葉系幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントの存在下において培養すると、間葉系幹細胞の細胞表面マーカーであるHLA-ABCおよびCD105の発現が低下することを新たに見出した(後述の実施例4を参照)。
CD105の陽性率が低い細胞は、TGFb1の発現量が高く、T細胞増殖を抑制するため、炎症疾患への治療効果が期待されている報告がある。
本発明者らは、<2.細胞生産物の生産方法>の欄で説明した方法に従って、間葉系幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントの存在下において培養し、その後、生産培養液中での培養と回復培養液中での培養とを交互に繰り返し、生産培養液の上清を回収すると、生産培養の回数を重ねるにつれて、培養上清中のサイトカイン、細胞外マトリックス、およびエクソソームの量が増加することを新たに見出した(後述の実施例5を参照)。
幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返され、前記方法が、前記生産培養液中での前記培養の後に、前記生産培養液の上清を回収することを更に含む、方法が提供される。この方法において、幹細胞は、例えば間葉系幹細胞である。
本発明者らは、<1.増殖細胞の生産方法>の欄で説明した方法に従って、間葉系幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントの存在下において培養すると、得られた間葉系幹細胞は、下肢虚血モデルのラットの虚血下肢の血流を有意に増加させることができることを新たに見出した(後述の実施例6を参照)。
以下に、本発明の好ましい実施形態をまとめて示す。
<7-1.間葉系幹細胞集団およびその生産方法>
[C1] 間葉系幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において培養して、増殖細胞を得ることを含む、低下したHLA-ABC陽性率を有する間葉系幹細胞集団の生産方法。
[C2] 前記間葉系幹細胞が、臍帯由来間葉系幹細胞、骨髄由来間葉系幹細胞、脂肪由来間葉系幹細胞、胎盤由来間葉系幹細胞、または臍帯血由来間葉系幹細胞である[C1]に記載の方法。
[C3] 前記間葉系幹細胞が、臍帯由来間葉系幹細胞または脂肪由来間葉系幹細胞、好ましくは臍帯由来間葉系幹細胞である[C1]または[C2]に記載の方法。
[C4] 前記間葉系幹細胞がヒト間葉系幹細胞である[C1]に記載の方法。
[C5] 前記間葉系幹細胞が、ヒト臍帯由来間葉系幹細胞、ヒト骨髄由来間葉系幹細胞、ヒト脂肪由来間葉系幹細胞、ヒト胎盤由来間葉系幹細胞、またはヒト臍帯血由来間葉系幹細胞である[C1]または[C2]に記載の方法。
[C7] 前記増殖培養液が、前記幹細胞の増殖を促進するタンパク質を含む増殖培養液である[C1]~[C6]の何れか1に記載の方法。
[C8] 前記増殖培養液が、増殖因子を追加した細胞培養用基本培地を含む培養液である[C1]~[C7]の何れか1に記載の方法。
[C9] 前記増殖培養液が、増殖因子を追加した細胞培養用基本培地である[C1]~[C8]の何れか1に記載の方法。
[C10] 前記培養が、前記細胞がコンフルエントの状態に達するまで行われる[C1]~[C9]の何れか1に記載の方法。
[C12] 前記培養が、500~10000cm2の底面積を有する培養容器で行われる[C1]~[C11]の何れか1に記載の方法。
[C13] 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントである[C1]~[C12]の何れか1に記載の方法。
[C14] 前記ラミニンフラグメントが、ヒト由来のラミニンフラグメントである[C13]に記載の方法。
[C15] 前記ラミニンフラグメントが、ラミニンE8フラグメントである[C13]または[C14]に記載の方法。
[C17] 前記ラミニンフラグメントが、ラミニン511 E8フラグメントである[C13]~[C16]の何れか1に記載の方法。
[C18] 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントの改変体である[C1]~[C12]の何れか1に記載の方法。
[C19] 前記改変体が、インテグリン結合活性を有するラミニンフラグメントと他の機能性分子との複合体である[C18]に記載の方法。
[C20] 前記改変体が、インテグリン結合活性を有するラミニンフラグメントと増殖因子結合分子との複合体である[C18]または[C19]に記載の方法。
[C22] 前記ラミニンE8フラグメントが、ラミニン511 E8フラグメント、ラミニン521 E8フラグメント、ラミニン411 E8フラグメント、ラミニン421 E8フラグメント、ラミニン332 E8フラグメント、ラミニン311 E8フラグメント、ラミニン321 E8フラグメント、ラミニン211 E8フラグメント、ラミニン221 E8フラグメント、ラミニン213 E8フラグメント、ラミニン111 E8フラグメント、またはラミニン121 E8フラグメントである[C21]に記載の方法。
[C23] 前記ラミニンE8フラグメントが、ラミニン511 E8フラグメントである[C21]または[C22]に記載の方法。
[C24] 前記ラミニンE8フラグメントが、ラミニン421 E8フラグメントである[C21]または[C22]に記載の方法。
[C25] 前記増殖因子結合分子が、ヘパラン硫酸である[C20]~[C24]の何れか1に記載の方法。
[C27] 前記改変体が、ラミニン421 E8フラグメントとヘパラン硫酸との複合体である[C18]~[C25]の何れか1に記載の方法。
[C28] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.005μg~2μgである[C1]~[C27]の何れか1に記載の方法。
[C29] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.01μg~0.5μgである[C1]~[C28]の何れか1に記載の方法。
[C30] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.05μg~0.25μgである[C1]~[C29]の何れか1に記載の方法。
[C31] 前記低下したHLA-ABC陽性率が、70%以下、好ましくは60%以下、より好ましくは50%以下、更に好ましくは40%以下、更に好ましくは30%以下、更に好ましくは20%以下、更に好ましくは10%以下である[C1]~[C30]の何れか1に記載の方法。
[D2] HLA-ABC陽性の間葉系幹細胞の前記比率が、60%以下、好ましくは50%以下、より好ましくは40%以下、更に好ましくは30%以下、更に好ましくは20%以下、更に好ましくは10%以下である[D1]に記載の間葉系幹細胞集団。
[D3] 前記間葉系幹細胞集団は、CD105陽性の間葉系幹細胞の比率が50%以下である[D1]または[D2]に記載の間葉系幹細胞集団。
[D4] CD105陽性の間葉系幹細胞の前記比率が、40%以下、好ましくは30%以下、より好ましくは20%以下、更に好ましくは10%以下である[D3]に記載の間葉系幹細胞集団。
[D5] [C1]~[C31]の何れか1に記載の方法によって得られる間葉系幹細胞集団。
[D6] 前記間葉系幹細胞集団が、[C1]~[C31]の何れか1に記載の方法によって得られる[D1]~[D4]の何れか1に記載の間葉系幹細胞集団。
[E1] 幹細胞の培養上清の生産方法であって、
幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返され、前記方法が、前記生産培養液中での前記培養の後に、前記生産培養液の上清を回収することを更に含む、方法。
[E2] 前記生産培養液の上清の回収が、前記生産培養液中での2回目以降の前記培養の後、好ましくは、前記生産培養液中での3回目以降の前記培養の後、に行われる[E1]に記載の方法。
[E3] 前記幹細胞が、間葉系幹細胞、神経幹細胞、皮膚幹細胞、肝幹細胞、筋幹細胞、脂肪幹細胞などの体性幹細胞;または人工多能性幹細胞(iPS細胞)、胚性幹細胞(ES細胞)などの多能性幹細胞である[E1]または[E2]に記載の方法。
[E4] 前記幹細胞が間葉系幹細胞である[E1]~[E3]の何れか1に記載の方法。
[E5] 前記幹細胞が、臍帯由来間葉系幹細胞、骨髄由来間葉系幹細胞、脂肪由来間葉系幹細胞、胎盤由来間葉系幹細胞、または臍帯血由来間葉系幹細胞である[E1]~[E4]の何れか1に記載の方法。
[E7] 前記幹細胞がヒト幹細胞である[E1]または[E2]に記載の方法。
[E8] 前記幹細胞が、ヒト間葉系幹細胞、ヒト神経幹細胞、ヒト皮膚幹細胞、ヒト肝幹細胞、ヒト筋幹細胞、ヒト脂肪幹細胞などのヒト体性幹細胞;またはヒト人工多能性幹細胞(ヒトiPS細胞)、ヒト胚性幹細胞(ヒトES細胞)などのヒト多能性幹細胞である[E1]~[E3]の何れか1に記載の方法。
[E9] 前記幹細胞がヒト間葉系幹細胞である[E1]~[E4]の何れか1に記載の方法。
[E10] 前記幹細胞が、ヒト臍帯由来間葉系幹細胞、ヒト骨髄由来間葉系幹細胞、ヒト脂肪由来間葉系幹細胞、ヒト胎盤由来間葉系幹細胞、またはヒト臍帯血由来間葉系幹細胞である[E1]~[E5]の何れか1に記載の方法。
[E12] 前記増殖培養液が、前記幹細胞の増殖を促進するタンパク質を含む増殖培養液である[E1]~[E11]の何れか1に記載の方法。
[E13] 前記増殖培養液が、増殖因子を追加した細胞培養用基本培地を含む培養液である[E1]~[E12]の何れか1に記載の方法。
[E14] 前記増殖培養液が、増殖因子を追加した細胞培養用基本培地である[E1]~[E13]の何れか1に記載の方法。
[E15] 前記増殖培養液中での前記培養が、前記細胞がコンフルエントの状態に達するまで行われる[E1]~[E14]の何れか1に記載の方法。
[E17] 前記増殖培養液中での前記培養が、500~10000cm2の底面積を有する培養容器で行われる[E1]~[E16]の何れか1に記載の方法。
[E18] 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントである[E1]~[E17]の何れか1に記載の方法。
[E19] 前記ラミニンフラグメントが、ヒト由来のラミニンフラグメントである[E18]に記載の方法。
[E20] 前記ラミニンフラグメントが、ラミニンE8フラグメントである[E18]または[E19]に記載の方法。
[E22] 前記ラミニンフラグメントが、ラミニン511 E8フラグメントである[E18]~[E21]の何れか1に記載の方法。
[E23] 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントの改変体である[E1]~[E17]の何れか1に記載の方法。
[E24] 前記改変体が、インテグリン結合活性を有するラミニンフラグメントと他の機能性分子との複合体である[E23]に記載の方法。
[E25] 前記改変体が、インテグリン結合活性を有するラミニンフラグメントと増殖因子結合分子との複合体である[E23]または[E24]に記載の方法。
[E27] 前記ラミニンE8フラグメントが、ラミニン511 E8フラグメント、ラミニン521 E8フラグメント、ラミニン411 E8フラグメント、ラミニン421 E8フラグメント、ラミニン332 E8フラグメント、ラミニン311 E8フラグメント、ラミニン321 E8フラグメント、ラミニン211 E8フラグメント、ラミニン221 E8フラグメント、ラミニン213 E8フラグメント、ラミニン111 E8フラグメント、またはラミニン121 E8フラグメントである[E26]に記載の方法。
[E28] 前記ラミニンE8フラグメントが、ラミニン511 E8フラグメントである[E26]または[E27]に記載の方法。
[E29] 前記ラミニンE8フラグメントが、ラミニン421 E8フラグメントである[E26]または[E27]に記載の方法。
[E30] 前記増殖因子結合分子が、ヘパラン硫酸である[E25]~[E29]の何れか1に記載の方法。
[E32] 前記改変体が、ラミニン421 E8フラグメントとヘパラン硫酸との複合体である[E23]~[E30]の何れか1に記載の方法。
[E33] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.005μg~2μgである[E1]~[E32]の何れか1に記載の方法。
[E34] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.01μg~0.5μgである[E1]~[E33]の何れか1に記載の方法。
[E35] 前記増殖培養液中の前記ラミニンフラグメントまたはその改変体の濃度が、培養容器の培養面積1cm2あたり0.05μg~0.25μgである[E1]~[E34]の何れか1に記載の方法。
[E37] 前記生産培養液が、サイトカインやインスリンを含まない培養液である[E1]~[E36]の何れか1に記載の方法。
[E38] 前記生産培養液が、タンパク質を含まない培養液である[E1]~[E37]の何れか1に記載の方法。
[E39] 前記生産培養液が、血清を含まない培養液である[E1]~[E38]の何れか1に記載の方法。
[E40] 前記生産培養液が、細胞培養用基本培地を含む培養液であるか、または細胞の栄養成分を追加した細胞培養用基本培地を含む培養液である[E1]~[E39]の何れか1に記載の方法。
[E42] 前記生産培養液が、細胞の栄養成分、好ましくはアミノ酸を追加した細胞培養用基本培地である[E1]~[E41]の何れか1に記載の方法。
[E43] 前記生産培養液が、ラミニンフラグメントまたはその改変体を含まない[E1]~[E42]の何れか1に記載の方法。
[E44] 前記生産培養液中での前記培養が、0.5~10日間、好ましくは2~5日間にわたって行われる[E1]~[E43]の何れか1に記載の方法。
[E45] 前記回復培養液が、前記幹細胞の増殖培養液である[E1]~[E44]の何れか1に記載の方法。
[E47] 前記回復培養液が、増殖因子を追加した細胞培養用基本培地を含む培養液である[E1]~[E46]の何れか1に記載の方法。
[E48] 前記回復培養液が、増殖因子を追加した細胞培養用基本培地である[E1]~[E47]の何れか1に記載の方法。
[E49] 前記回復培養液が、前記増殖培養液と同じ組成を有する[E1]~[E48]の何れか1に記載の方法。
[E50] 前記回復培養液が、ラミニンフラグメントまたはその改変体を含まない[E1]~[E49]の何れか1に記載の方法。
[E51] 前記回復培養液中での前記培養が、0.5~10日間、好ましくは2~5日間にわたって行われる[E1]~[E50]の何れか1に記載の方法。
[E52] 前記生産培養液中での前記培養と前記回復培養液中での前記培養とのサイクルが、2~10回繰り返される[E1]~[E51]の何れか1に記載の方法。
[F2] 前記培養上清が、10000pg/mL以上、好ましくは15000pg/mL以上のHGFを含有する[F1]に記載の培養上清。
[F3] 前記培養上清が、5000~1000000pg/mL、好ましくは10000~1000000pg/mL、より好ましくは15000~1000000pg/mLのHGFを含有する[F1]または[F2]に記載の培養上清。
[F4] 50pg/mL以上のCD9/CD63 ECドメイン 融合タンパク質を含有する、幹細胞の培養上清。
[F5] 前記培養上清が、100pg/mL以上、好ましくは200pg/mL以上のCD9/CD63 ECドメイン 融合タンパク質を含有する[F4]に記載の培養上清。
[F7] 前記培養上清が、50pg/mL以上のCD9/CD63 ECドメイン 融合タンパク質を更に含有する[F1]~[F3]の何れか1に記載の培養上清。
[F8] 前記培養上清が、100pg/mL以上、好ましくは200pg/mL以上のCD9/CD63 ECドメイン 融合タンパク質を更に含有する[F1]~[F3]の何れか1に記載の培養上清。
[F9] 前記培養上清が、50~100000pg/mL、好ましくは100~100000pg/mL、より好ましくは200~100000pg/mLのCD9/CD63 ECドメイン 融合タンパク質を更に含有する[F1]~[F3]の何れか1に記載の培養上清。
[F10] 前記培養上清が、3000pg/mL以上のMCP-1、1000pg/mL以上のGRO、および5μg/mL以上のフィブロネクチンを更に含有する[F1]~[F9]の何れか1に記載の培養上清。
[F12] 前記培養上清が、3000~1000000pg/mL、好ましくは4000~1000000pg/mL、より好ましくは6000~1000000pg/mLのMCP-1;1000~1000000pg/mL、好ましくは2000~1000000pg/mL、より好ましくは4000~1000000pg/mLのGRO;および、5~1000μg/mL、好ましくは6~1000μg/mL、より好ましくは8~1000μg/mLのフィブロネクチンを更に含有する[F1]~[F9]の何れか1に記載の培養上清。
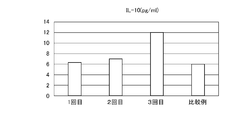
[F13] 前記培養上清が、200pg/mL以上のTGF-1b、5pg/mL以上のIL-4、および8pg/mL以上のIL-10を更に含有する[F1]~[F12]の何れか1に記載の培養上清。
[F14] 前記培養上清が、300pg/mL以上、好ましくは500pg/mL以上のTGF-1b;10pg/mL以上、好ましくは20pg/mL以上のIL-4;および、10pg/mL以上、好ましくは12pg/mL以上のIL-10を更に含有する[F1]~[F12]の何れか1に記載の培養上清。
[F15] 前記培養上清が、200~100000pg/mL、好ましくは300~100000pg/mL、より好ましくは500~100000pg/mLのTGF-1b;5~100000pg/mL、好ましくは10~100000pg/mL、より好ましくは20~100000pg/mLのIL-4;および、8~100000pg/mL、好ましくは10~100000pg/mL、より好ましくは12~100000pg/mLのIL-10を更に含有する[F1]~[F12]の何れか1に記載の培養上清。
[F17] 前記培養上清が、インスリン、トランスフェリン、およびアルブミンのいずれも含まない[F1]~[F16]の何れか1に記載の培養上清。
[F18] 前記培養上清が、組換えタンパク質を含まない[F1]~[F17]の何れか1に記載の培養上清。
[F19] 前記培養上清が、IL-1α、IL-1βおよびTNF-αの少なくとも1つを0~15pg/mLの量で含む[F1]~[F18]の何れか1に記載の培養上清。
[F20] 前記培養上清が、IL-1α、IL-1βおよびTNF-αの各々を0~15pg/mLの量で含む[F1]~[F19]の何れか1に記載の培養上清。
[F22] 前記培養上清が、間葉系幹細胞、神経幹細胞、皮膚幹細胞、肝幹細胞、筋幹細胞、脂肪幹細胞などの体性幹細胞の培養上清;または人工多能性幹細胞(iPS細胞)、胚性幹細胞(ES細胞)などの多能性幹細胞の培養上清である[F1]~[F21]の何れか1に記載の培養上清。
[F23] 前記培養上清が、間葉系幹細胞の培養上清である[F1]~[F22]の何れか1に記載の培養上清。
[F24] 前記培養上清が、臍帯由来間葉系幹細胞の培養上清、骨髄由来間葉系幹細胞の培養上清、脂肪由来間葉系幹細胞の培養上清、胎盤由来間葉系幹細胞の培養上清、または臍帯血由来間葉系幹細胞の培養上清である[F1]~[F23]の何れか1に記載の培養上清。
[F25] 前記培養上清が、臍帯由来間葉系幹細胞の培養上清または脂肪由来間葉系幹細胞の培養上清、好ましくは臍帯由来間葉系幹細胞の培養上清である[F1]~[F24]の何れか1に記載の培養上清。
[F27] 前記培養上清が、ヒト臍帯由来間葉系幹細胞の培養上清、ヒト骨髄由来間葉系幹細胞の培養上清、ヒト脂肪由来間葉系幹細胞の培養上清、ヒト胎盤由来間葉系幹細胞の培養上清、またはヒト臍帯血由来間葉系幹細胞の培養上清である[F1]~[F24]の何れか1に記載の培養上清。
[F28] 前記培養上清が、ヒト臍帯由来間葉系幹細胞の培養上清またはヒト脂肪由来間葉系幹細胞の培養上清、好ましくはヒト臍帯由来間葉系幹細胞の培養上清である[F1]~[F25]の何れか1に記載の培養上清。
[F29] [E1]~[E52]の何れか1に記載の方法によって得られる培養上清。
[F30] 前記培養上清が、[E1]~[E52]の何れか1に記載の方法によって得られる[F1]~[F28]の何れか1に記載の培養上清。
[G1] [D1]~[D6]の何れか1に記載の間葉系幹細胞集団または[F1]~[F30]の何れか1に記載の培養上清を含む治療剤。
[G2] [D1]~[D6]の何れか1に記載の間葉系幹細胞集団を含む治療剤。
[G3] [F1]~[F30]の何れか1に記載の培養上清を含む治療剤。
[G4] 前記治療剤が、下肢虚血、心筋梗塞、脳梗塞、脊髄梗塞、慢性動脈閉塞症などの虚血性疾患;上皮創傷、熱傷などの傷;老化に伴うサルコペニア;リウマチ、椎間板ヘルニア、変形性関節症などの関節炎;腎炎、角膜炎、サイトカインストームなどの炎症性疾患;神経炎症が原因の一つと考えられる自閉症や不眠症などの精神疾患;GVHD(移植片対宿主病)、シェーグレン症候群、アトピー性皮膚炎、膠原病、多発性硬化症、自己免疫性疾患などの免疫疾患;またはがん疾患を治療するためのものである[G1]~[G3]の何れか1に記載の治療剤。
[G5] 前記治療剤が、虚血性疾患;好ましくは、下肢虚血、心筋梗塞、脳梗塞、脊髄梗塞、または慢性動脈閉塞症;より好ましくは下肢虚血を治療するためのものである[G1]~[G4]の何れか1に記載の治療剤。
[G7] [D1]~[D6]の何れか1に記載の間葉系幹細胞集団を被検体に投与することを含む、傷病の治療方法。
[G8] [F1]~[F30]の何れか1に記載の培養上清を被検体に投与することを含む、傷病の治療方法。
[G9] 前記傷病が、下肢虚血、心筋梗塞、脳梗塞、脊髄梗塞、慢性動脈閉塞症などの虚血性疾患;上皮創傷、熱傷などの傷;老化に伴うサルコペニア;リウマチ、椎間板ヘルニア、変形性関節症などの関節炎;サイトカインストーム、腎炎、角膜炎などの炎症性疾患;神経炎症が原因の一つと考えられる自閉症や不眠症などの精神疾患;GVHD(移植片対宿主病)、シェーグレン症候群、アトピー性皮膚炎、膠原病、多発性硬化症、自己免疫性疾患などの免疫疾患;またはがん疾患である[G6]~[G8]の何れか1に記載の方法。
[G10] 前記傷病が、虚血性疾患;好ましくは、下肢虚血、心筋梗塞、脳梗塞、脊髄梗塞、または慢性動脈閉塞症;より好ましくは下肢虚血である[G6]~[G9]の何れか1に記載の治療剤。
[G11] 前記被検体が、哺乳類、好ましくはヒトである[G6]~[G10]の何れか1に記載の方法。
[G13] 治療剤の製造のための[D1]~[D6]の何れか1に記載の間葉系幹細胞集団の使用。
[G14] 治療剤の製造のための[F1]~[F30]の何れか1に記載の培養上清の使用。
[G15] 前記治療剤が、下肢虚血、心筋梗塞、脳梗塞、脊髄梗塞、慢性動脈閉塞症などの虚血性疾患;上皮創傷、熱傷などの傷;老化に伴うサルコペニア;リウマチ、椎間板ヘルニア、変形性関節症などの関節炎;サイトカインストーム、腎炎、角膜炎などの炎症性疾患;神経炎症が原因の一つと考えられる自閉症や不眠症などの精神疾患;GVHD(移植片対宿主病)、シェーグレン症候群、アトピー性皮膚炎、膠原病、多発性硬化症、自己免疫性疾患などの免疫疾患;またはがん疾患を治療するためのものである[G12]~[G14]の何れか1に記載の使用。
[G16] 前記治療剤が、虚血性疾患;好ましくは、下肢虚血、心筋梗塞、脳梗塞、脊髄梗塞、または慢性動脈閉塞症;より好ましくは下肢虚血を治療するためのものである[G12]~[G15]の何れか1に記載の治療剤。
(1)方法
実施例1では、幹細胞の増殖培養を行った。幹細胞として、凍結保存液Stem Cell Banker(ゼノアック)で凍結保存された臍帯由来間葉系幹細胞(UCMSC)を使用した。
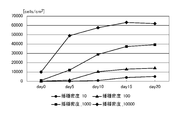
臍帯由来間葉系幹細胞(UCMSC)を、5x10e3の細胞数(播種密度10cells/cm2)、5x10e4の細胞数(播種密度100cells/cm2)、5x10e5の細胞数(播種密度1000cells/cm2)、および5x10e6の細胞数(播種密度10000cells/cm2)で、MSC Expansion XSFM B 培地(富士フイルム和光純薬株式会社)100mlに懸濁し、得られた細胞懸濁液をピールオフT512フラスコ(住友ベークライト株式会社)に播種した。それぞれの条件ごとに、4枚のフラスコに播種した。
臍帯由来間葉系幹細胞(UCMSC)を、5x10e3の細胞数(播種密度10cells/cm2)、5x10e4の細胞数(播種密度100cells/cm2)、5x10e5の細胞数(播種密度1000cells/cm2)、および5x10e6の細胞数(播種密度10000cells/cm2)で、MSC Expansion XSFM B 培地(富士フイルム和光純薬株式会社)100mlに懸濁し、iMatrix-511ラミニンフラグメント(株式会社ニッピ)を50μl/100mlで添加し、得られた細胞懸濁液をピールオフT512フラスコ(住友ベークライト株式会社)に播種した。それぞれの条件ごとに、4枚のフラスコに播種した。
臍帯由来間葉系幹細胞(UCMSC)を、5x10e3の細胞数(播種密度10cells/cm2)、5x10e4の細胞数(播種密度100cells/cm2)、5x10e5の細胞数(播種密度1000cells/cm2)、および5x10e6の細胞数(播種密度10000cells/cm2)で、MSC Expansion XSFM B 培地(富士フイルム和光純薬株式会社)100mlに懸濁し、予めゼラチンコーティングしたピールオフT512フラスコ(住友ベークライト株式会社)に播種した。ゼラチンコーティングは、ゼラチン溶液(StemSure 0.1w/v% Gelatin Solution、富士フイルム和光純薬株式会社)で2時間処理することより行った。
臍帯由来間葉系幹細胞(UCMSC)が増殖してT512フラスコでコンフルエントの状態に達すると、約3×10e7個の細胞(すなわち、約60000cells/cm2)が回収できた。したがって、図1、3および5において、約60000cells/cm2がコンフルエントの状態を表す。
(1)方法
実施例2では、幹細胞の増殖培養を行った後、生産培養を行った。幹細胞として、凍結保存液Stem Cell Banker(ゼノアック)で凍結保存された臍帯由来間葉系幹細胞(UCMSC)を使用した。
臍帯由来間葉系幹細胞(UCMSC)を、5x10e5(播種密度1000cells/cm2)の細胞数で、MSC Expansion XSFM B(富士フイルム和光純薬株式会社)(以下、MSC培地Bともいう)100mlに懸濁し、得られた細胞懸濁液をピールオフT512フラスコ(住友ベークライト株式会社)に播種した。
臍帯由来間葉系幹細胞(UCMSC)を、5x10e5(播種密度1000cells/cm2)の細胞数で、MSC Expansion XSFM B(富士フイルム和光純薬株式会社)(以下、MSC培地Bともいう)100mlに懸濁し、iMatrix-511ラミニンフラグメント(株式会社ニッピ)を50μl/100mlで添加し、得られた細胞懸濁液をピールオフT512フラスコ(住友ベークライト株式会社)に播種した。
図7Aでは、一部の細胞が剥がれて細胞塊になっていた。図7Aにおいて細胞塊が存在する箇所を矢印で示した。図7Bでは、大部分の細胞が剥がれて残っていなかった。一方、図8Aおよび図8Bのどちらの画像においても、細胞は剥がれておらず接着状態を保っていた。
(1)方法
実施例3では、幹細胞の増殖培養を行った後、長期の生産培養を行った。実施例3で行った培養工程を模式的に図9に示す。幹細胞として、凍結保存液Stem Cell Banker(ゼノアック)で凍結保存された臍帯由来間葉系幹細胞(UCMSC)を使用した。
臍帯由来間葉系幹細胞(UCMSC)を、5x10e5の細胞数(播種密度1000cells/cm2)で、MSC Expansion XSFM B(富士フイルム和光純薬株式会社)(以下、MSC培地Bともいう)100mlに懸濁し、iMatrix-511ラミニンフラグメント(株式会社ニッピ)を50μl/100mlで添加し、得られた細胞懸濁液をピールオフT512フラスコ(住友ベークライト株式会社)に播種した。
臍帯由来間葉系幹細胞(UCMSC)を、1.5x10e5の細胞数(播種密度1000cells/cm2)でMSC Expansion XSFM B(富士フイルム和光純薬株式会社)(MSC培地B)20mlに懸濁し、iMatrix-511ラミニンフラグメントを添加しないでT150フラスコ(コーニング)に播種した。ラミニンフラグメントを添加しなかったこと以外は実験3-1と同様の手順で増殖培養を行った。
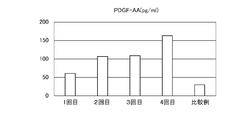
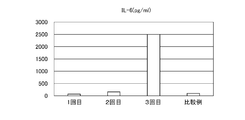
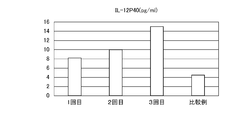
サイトカインの定量結果を図10~12に示す。図10~12のそれぞれのグラフは、左から順に、
本発明の例で1回目の生産培養後に回収された培養上清中のサイトカインの量、
本発明の例で2回目の生産培養後に回収された培養上清中のサイトカインの量、
本発明の例で3回目の生産培養後に回収された培養上清中のサイトカインの量、および
比較例で回収された培養上清中のサイトカインの量
を示す。
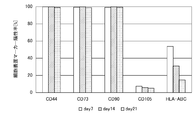
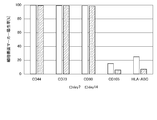
実施例4では、間葉系幹細胞をラミニンフラグメントの存在下で培養し、得られた間葉系幹細胞集団の細胞表面マーカー陽性率を解析した。また、間葉系幹細胞をラミニンフラグメントの存在下で培養し、得られた間葉系幹細胞集団の細胞表面マーカーの発現を免疫染色画像により確認した。
実験4-1(本発明の例)
臍帯由来間葉系幹細胞(UCMSC)または脂肪由来間葉系幹細胞(ADMSC)を、5x10e5の細胞数(播種密度1000cells/cm2)で、MSC Expansion XSFM B 培地(富士フイルム和光純薬株式会社)100mlに懸濁し、iMatrix-511ラミニンフラグメント(株式会社ニッピ)を50μl/100mlで添加し、得られた細胞懸濁液をピールオフT512フラスコ(住友ベークライト株式会社)に播種した。臍帯由来間葉系幹細胞は、1週間、2週間、3週間の期間にわたって培養し、脂肪由来間葉系幹細胞は、1週間、2週間の期間にわたって培養した。
臍帯由来間葉系幹細胞(UCMSC)を、5x10e5の細胞数(播種密度1000cells/cm2)で、MSC Expansion XSFM B 培地(富士フイルム和光純薬株式会社)100mlに懸濁し、iMatrix-511ラミニンフラグメントを添加しないでピールオフT512フラスコ(住友ベークライト株式会社)に播種した。ラミニンフラグメントを添加しなかったこと以外は実験4-1と同様の手順で培養を行った。
ラミニンフラグメントの存在下で培養した場合の臍帯由来間葉系幹細胞の細胞表面マーカーの陽性率を図13に示し、ラミニンフラグメントの存在下で培養した場合の脂肪由来間葉系幹細胞の細胞表面マーカーの陽性率を図14に示し、ラミニンフラグメントの非存在下で培養した場合の臍帯由来間葉系幹細胞の細胞表面マーカーの陽性率を図15に示す。
実施例5では、実施例3に記載の方法に従って、間葉系幹細胞の増殖培養を行った後に複数回の生産培養を行い、各々の生産培養の後に培養上清を回収した。得られた間葉系幹細胞の培養上清に含まれるサイトカイン、細胞外マトリックス、およびエクソソームマーカーの量を解析した。
培養上清に含まれるサイトカインおよび細胞外マトリックスの量を、ELISA解析キット(R&D Systems社)を用いて解析した。サイトカインとして、HGF(肝細胞増殖因子)、MCP-1、GRO/CXCL1、PDGF-AA、VEGF(血管内皮増殖因子)、TGF-1b、IL-4、IL-10、IL-13、IL-7、IL-15、IL-9、IL-1α、IL-1β、TNF-α、IL-8、EOTAXIN、IL-6、G-CSF、GM-CSF、MCP-3、IL-12P40、IP-10、MIP-1αの24種類を解析し、細胞外マトリックスとしてFibronectinを解析した。また、培養上清に含まれるエクソソームの量を、CD9/CD63 ELISAキット(コスモバイオ)を用いて、エクソソームマーカータンパク質(CD9/CD63融合タンパク質)を指標として解析した。本明細書において、サイトカインの量、細胞外マトリックスの量、エクソソームマーカータンパク質の量は、特異的な抗体を用いてELISA法により測定される値を指す。
この実施例においても、実施例3と同様、本発明の例では、ラミニンフラグメントの存在下で増殖培養を行ったのに対し、比較例では、ラミニンフラグメントの非存在下で増殖培養を行った。このため、本発明の例では、複数回の生産培養を繰り返し行うことができたが、比較例では、1回目の生産培養の間に細胞が培養容器から剥がれ始めたため、1回目の生産培養しか行うことができなかった。
実施例6では、本発明の方法に従って得られた間葉系幹細胞を下肢虚血モデルのラットに投与し、治療効果を確認した。
<下肢虚血モデルのラットの準備>
12週齢のSprague Dawley(SD)雄ラット(CLEA Japan(大阪、日本)から購入)を使用した。SDラットを5ml/kgの用量でコンビネーション麻酔薬(M/M/B:0.3/4/5)を腹腔内投与して麻酔した。下肢虚血は、外腸骨動脈と内腸骨静脈、足首直下レベルの伏在動脈と静脈、および全枝を露出させて結紮し、結紮した血管のうち全血管を切除することにより誘導した。
臍帯由来間葉系幹細胞(UCMSC)を、実施例4と同様の方法で、ラミニンフラグメントの存在下および非存在下のそれぞれで培養した。また、脂肪由来間葉系幹細胞(ADMSC)を、実施例4と同様の方法で、ラミニンフラグメントの存在下および非存在下のそれぞれで培養した。得られた間葉系幹細胞(すなわち、ラミニンフラグメントの存在下で培養した臍帯由来間葉系幹細胞、ラミニンフラグメントの非存在下で培養した臍帯由来間葉系幹細胞、ラミニンフラグメントの存在下で培養した脂肪由来間葉系幹細胞、およびラミニンフラグメントの非存在下で培養した脂肪由来間葉系幹細胞)を、1mlのDMEM/F12培地(Sigma)に1.25x10e6の細胞数で懸濁した。
下肢の血流量をMoor LDI 2.0システム(Moor instruments, Devon, UK)を用いて評価した。血流量は、下肢虚血の誘導から14日後に測定した。血流量の測定時には、ラットにイソフルラン吸入麻酔を行った。血流量比(%)は、下記式により相対値で算出した。
血流量比(%)=(左虚血下肢の血流量/右非虚血下肢の血流量)×100
下肢血流量比の結果を図43に示す。図43において、「Control」は、DMEM/F12培地を投与した群、「UCMSC laminin-」は、ラミニンフラグメントの非存在下で培養した臍帯由来間葉系幹細胞を投与した群、「UCMSC laminin+」は、ラミニンフラグメントの存在下で培養した臍帯由来間葉系幹細胞を投与した群、「ADMSC laminin-」は、ラミニンフラグメントの非存在下で培養した脂肪由来間葉系幹細胞を投与した群、「ADMSC laminin+」は、ラミニンフラグメントの存在下で培養した脂肪由来間葉系幹細胞を投与した群を表す。図43において、エラーバーは標準誤差を表す。
Claims (33)
- 0.002~2000細胞/cm2の細胞密度で播種された細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、前記細胞を増殖させることを含む、増殖細胞の生産方法。
- 前記培養が、前記培養基質を含有する増殖培養液中で行われる請求項1に記載の方法。
- 前記細胞が幹細胞である請求項1または2に記載の方法。
- 前記細胞が間葉系幹細胞である請求項1~3の何れか1項に記載の方法。
- 前記細胞が臍帯由来間葉系幹細胞である請求項1~4の何れか1項に記載の方法。
- 前記細胞が凍結細胞である請求項1~5の何れか1項に記載の方法。
- 前記培養が、前記細胞がコンフルエントの状態に達するまで行われる請求項1~6の何れか1項に記載の方法。
- 前記培養が、500cm2以上の底面積を有する培養容器で行われる請求項1~7の何れか1項に記載の方法。
- 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントである請求項1~8の何れか1項に記載の方法。
- 前記培養基質が、インテグリン結合活性を有するラミニンフラグメントの改変体である請求項1~8の何れか1項に記載の方法。
- 請求項1~10の何れか1項に記載の方法に従って細胞を増殖培養液中で培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと
を含む、細胞生産物の生産方法。 - 請求項1~10の何れか1項に記載の方法に従って細胞を増殖培養液中で培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返される、細胞生産物の生産方法。 - 前記生産培養液が、異種由来成分を含まない培養液である請求項11または12に記載の方法。
- 前記生産培養液が、サイトカインやインスリンを含まない培養液である請求項11~13の何れか1項に記載の方法。
- 前記生産培養液が、タンパク質を含まない培養液である請求項11~14の何れか1項に記載の方法。
- 前記生産培養液中での前記培養の後に、前記生産培養液の上清を回収することを更に含む請求項11~15の何れか1項に記載の方法。
- 幹細胞の培養上清の生産方法であって、
幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において、接着培養により培養して、増殖細胞を接着状態で得ることと、
前記増殖細胞を、前記接着状態を維持したまま、生産培養液中で培養して、前記細胞に細胞生産物を生産させることと、
前記生産培養液中での前記培養の後、前記増殖細胞を、前記接着状態を維持したまま、回復培養液中で培養することと
を含み、
前記生産培養液中での前記培養と、前記回復培養液中での前記培養とが、細胞の前記接着状態を維持したまま交互に繰り返され、前記方法が、前記生産培養液中での前記培養の後に、前記生産培養液の上清を回収することを更に含む、方法。 - 前記生産培養液の上清の回収が、前記生産培養液中での2回目以降の前記培養の後に行われる請求項17に記載の方法。
- 前記幹細胞が間葉系幹細胞である請求項17または18に記載の方法。
- 間葉系幹細胞を、増殖培養液中で、インテグリン結合活性を有するラミニンフラグメントおよびその改変体から選ばれる培養基質の存在下において培養して、増殖細胞を得ることを含む、低下したHLA-ABC陽性率を有する間葉系幹細胞集団の生産方法。
- HLA-ABC陽性の間葉系幹細胞の比率が70%以下である間葉系幹細胞集団。
- CD105陽性の間葉系幹細胞の比率が50%以下である請求項21に記載の間葉系幹細胞集団。
- 5000pg/mL以上のHGFを含有する、幹細胞の培養上清。
- 50pg/mL以上のCD9/CD63 ECドメイン 融合タンパク質を含有する、幹細胞の培養上清。
- 3000pg/mL以上のMCP-1、1000pg/mL以上のGRO、および5μg/mL以上のフィブロネクチンを更に含有する請求項23または24に記載の培養上清。
- 200pg/mL以上のTGF-1b、5pg/mL以上のIL-4、および8pg/mL以上のIL-10を更に含有する請求項23~25の何れか1項に記載の培養上清。
- インスリン、トランスフェリン、およびアルブミンの少なくとも1つを含まない請求項23~26の何れか1項に記載の培養上清。
- 組換えタンパク質を含まない請求項23~27の何れか1項に記載の培養上清。
- IL-1α、IL-1βおよびTNF-αの少なくとも1つが0~15pg/mLの量で含まれる、請求項23~28の何れか1項に記載の培養上清。
- 20種類以上のサイトカインを含み、各サイトカインが10pg/mL以上の濃度を有する請求項23~29の何れか1項に記載の培養上清。
- 前記培養上清が、間葉系幹細胞の培養上清である請求項23~30の何れか1項に記載の培養上清。
- 前記培養上清が、臍帯由来間葉系幹細胞の培養上清である請求項23~31の何れか1項に記載の培養上清。
- 請求項21または22に記載の間葉系幹細胞集団または請求項23~32の何れか1項に記載の培養上清を含む治療剤。
Priority Applications (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA3173721A CA3173721A1 (en) | 2020-03-31 | 2021-03-26 | Method of producing proliferated cells, method of producing cell product, mesenchymal stem cell population and method of producing same, culture supernatant of stem cells and method of producing same, and therapeutic agent |
| US17/995,095 US20230172992A1 (en) | 2020-03-31 | 2021-03-26 | Method for producing proliferating cells, method for producing cell product, mesenchymal stem cell population and method for producing same, culture supernatant of stem cells and method for producing same, and therapeutic agent |
| EP21779739.8A EP4130240A4 (en) | 2020-03-31 | 2021-03-26 | METHOD FOR PRODUCING PROLIFERATIVE CELLS, METHOD FOR PRODUCING CELLULAR PRODUCT, POPULATION OF MESENCHYMAL STEM CELLS AND METHOD FOR PRODUCING SAME, SUPERNAtant OF STEM CELL CULTURE AND METHOD FOR PRODUCING SAME, AND THERAPEUTIC AGENT |
| AU2021247879A AU2021247879A1 (en) | 2020-03-31 | 2021-03-26 | Method of producing proliferated cells, method of producing cell product, mesenchymal stem cell population and method of producing same, culture supernatant of stem cells and method of producing same, and therapeutic agent |
| CN202180024893.1A CN115362252A (zh) | 2020-03-31 | 2021-03-26 | 增殖细胞和细胞生产物的生产法、间充质干细胞群和干细胞培养上清及其生产法、治疗剂 |
| CN202310081275.1A CN116179480A (zh) | 2020-03-31 | 2021-03-26 | 增殖细胞和细胞生产物的生产法、间充质干细胞群和干细胞培养上清及其生产法、治疗剂 |
| JP2022512159A JPWO2021200744A1 (ja) | 2020-03-31 | 2021-03-26 | |
| EP22207135.9A EP4155389A3 (en) | 2020-03-31 | 2021-03-26 | Method of producing proliferated cells, method of producing cell product, mesenchymal stem cell population and method of producing same, culture supernatant of stem cells and method of producing same, and therapeutic agent |
| JP2022160399A JP2022181218A (ja) | 2020-03-31 | 2022-10-04 | 増殖細胞の生産方法、細胞生産物の生産方法、間葉系幹細胞集団およびその生産方法、幹細胞の培養上清およびその生産方法、並びに治療剤 |
| AU2022259729A AU2022259729A1 (en) | 2020-03-31 | 2022-10-25 | Method of producing proliferated cells, method of producing cell product, mesenchymal stem cell population and method of producing same, culture supernatant of stem cells and method of producing same, and therapeutic agent |
| JP2023206347A JP2024015245A (ja) | 2020-03-31 | 2023-12-06 | 増殖細胞の生産方法、細胞生産物の生産方法、間葉系幹細胞集団およびその生産方法、幹細胞の培養上清およびその生産方法、並びに治療剤 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020-063408 | 2020-03-31 | ||
| JP2020063408 | 2020-03-31 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021200744A1 true WO2021200744A1 (ja) | 2021-10-07 |
Family
ID=77930052
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2021/013099 WO2021200744A1 (ja) | 2020-03-31 | 2021-03-26 | 増殖細胞の生産方法、細胞生産物の生産方法、間葉系幹細胞集団およびその生産方法、幹細胞の培養上清およびその生産方法、並びに治療剤 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20230172992A1 (ja) |
| EP (2) | EP4155389A3 (ja) |
| JP (3) | JPWO2021200744A1 (ja) |
| CN (2) | CN115362252A (ja) |
| AU (2) | AU2021247879A1 (ja) |
| CA (2) | CA3173721A1 (ja) |
| TW (2) | TW202204605A (ja) |
| WO (1) | WO2021200744A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024019080A1 (ja) * | 2022-07-19 | 2024-01-25 | 国立大学法人 長崎大学 | 血管内皮増殖因子を高発現する臍帯由来間葉系細胞の製造方法、および肺疾患治療用医薬組成物 |
Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05207875A (ja) * | 1992-01-28 | 1993-08-20 | Mitsui Toatsu Chem Inc | 無血清培地 |
| JPH09512165A (ja) * | 1994-04-06 | 1997-12-09 | イミュネックス・コーポレーション | インターロイキン15 |
| JPH10179147A (ja) * | 1996-12-27 | 1998-07-07 | Ishikawajima Harima Heavy Ind Co Ltd | 植物細胞培養方法および二次代謝物高生産性植物細胞 |
| JP2010538681A (ja) * | 2008-10-10 | 2010-12-16 | 深▲セン▼市嘉天源生物科技有限公司 | 人または動物胚から間葉系幹細胞を抽出及びその分泌物を抽出する方法 |
| WO2012137970A1 (ja) | 2011-04-08 | 2012-10-11 | 国立大学法人大阪大学 | 改変ラミニンおよびその利用 |
| WO2014103534A1 (ja) | 2012-12-28 | 2014-07-03 | 国立大学法人大阪大学 | コラーゲン結合性分子を付加した改変ラミニンおよびその利用 |
| WO2014199754A1 (ja) * | 2013-06-12 | 2014-12-18 | 国立大学法人大阪大学 | ラミニンフラグメントが乾燥状態でコーティングされている細胞培養器具 |
| CN104651305A (zh) * | 2015-02-13 | 2015-05-27 | 沈阳澔源生物科技有限公司 | 一种利用脐带间充质干细胞获取生物活性蛋白的方法 |
| WO2016010082A1 (ja) | 2014-07-16 | 2016-01-21 | 国立大学法人大阪大学 | ラミニンフラグメントの細胞培養基質活性増強方法 |
| WO2017082220A1 (ja) * | 2015-11-10 | 2017-05-18 | 国立大学法人京都大学 | ラミニンフラグメント含有培地を用いる細胞培養方法 |
| WO2019245050A1 (ja) * | 2018-06-22 | 2019-12-26 | 株式会社バイオミメティクスシンパシーズ | 中空糸細胞培養装置,細胞培養方法,培養上清の製造方法 |
| JP2020508679A (ja) * | 2017-02-28 | 2020-03-26 | ユニバーシティ デ ロライン | 敗血症の治療のための、ワルトンジェリーから取得された間葉系幹細胞 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5378612A (en) * | 1990-05-11 | 1995-01-03 | Juridical Foundation The Chemo-Sero-Therapeutic Research Institute | Culture medium for production of recombinant protein |
| AU2007294731B2 (en) * | 2006-09-13 | 2014-04-17 | Abbvie Inc. | Cell culture improvements |
| WO2012145682A1 (en) * | 2011-04-21 | 2012-10-26 | Amgen Inc. | A method for culturing mammalian cells to improve recombinant protein production |
| KR102363146B1 (ko) * | 2016-03-09 | 2022-02-14 | 아비타 인터내셔널 리미티드 | 간엽 마커와 뉴런 마커를 발현하는 줄기 세포, 이의 조성물 및 이의 제조 방법 |
-
2021
- 2021-03-26 EP EP22207135.9A patent/EP4155389A3/en active Pending
- 2021-03-26 JP JP2022512159A patent/JPWO2021200744A1/ja active Pending
- 2021-03-26 WO PCT/JP2021/013099 patent/WO2021200744A1/ja unknown
- 2021-03-26 CN CN202180024893.1A patent/CN115362252A/zh active Pending
- 2021-03-26 EP EP21779739.8A patent/EP4130240A4/en active Pending
- 2021-03-26 CN CN202310081275.1A patent/CN116179480A/zh not_active Withdrawn
- 2021-03-26 AU AU2021247879A patent/AU2021247879A1/en active Pending
- 2021-03-26 CA CA3173721A patent/CA3173721A1/en active Pending
- 2021-03-26 CA CA3177567A patent/CA3177567A1/en active Pending
- 2021-03-26 US US17/995,095 patent/US20230172992A1/en active Pending
- 2021-03-30 TW TW110111636A patent/TW202204605A/zh unknown
- 2021-03-30 TW TW111147409A patent/TW202311526A/zh unknown
-
2022
- 2022-10-04 JP JP2022160399A patent/JP2022181218A/ja active Pending
- 2022-10-25 AU AU2022259729A patent/AU2022259729A1/en active Pending
-
2023
- 2023-12-06 JP JP2023206347A patent/JP2024015245A/ja active Pending
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH05207875A (ja) * | 1992-01-28 | 1993-08-20 | Mitsui Toatsu Chem Inc | 無血清培地 |
| JPH09512165A (ja) * | 1994-04-06 | 1997-12-09 | イミュネックス・コーポレーション | インターロイキン15 |
| JPH10179147A (ja) * | 1996-12-27 | 1998-07-07 | Ishikawajima Harima Heavy Ind Co Ltd | 植物細胞培養方法および二次代謝物高生産性植物細胞 |
| JP2010538681A (ja) * | 2008-10-10 | 2010-12-16 | 深▲セン▼市嘉天源生物科技有限公司 | 人または動物胚から間葉系幹細胞を抽出及びその分泌物を抽出する方法 |
| WO2012137970A1 (ja) | 2011-04-08 | 2012-10-11 | 国立大学法人大阪大学 | 改変ラミニンおよびその利用 |
| WO2014103534A1 (ja) | 2012-12-28 | 2014-07-03 | 国立大学法人大阪大学 | コラーゲン結合性分子を付加した改変ラミニンおよびその利用 |
| WO2014199754A1 (ja) * | 2013-06-12 | 2014-12-18 | 国立大学法人大阪大学 | ラミニンフラグメントが乾燥状態でコーティングされている細胞培養器具 |
| WO2016010082A1 (ja) | 2014-07-16 | 2016-01-21 | 国立大学法人大阪大学 | ラミニンフラグメントの細胞培養基質活性増強方法 |
| CN104651305A (zh) * | 2015-02-13 | 2015-05-27 | 沈阳澔源生物科技有限公司 | 一种利用脐带间充质干细胞获取生物活性蛋白的方法 |
| WO2017082220A1 (ja) * | 2015-11-10 | 2017-05-18 | 国立大学法人京都大学 | ラミニンフラグメント含有培地を用いる細胞培養方法 |
| JP2020508679A (ja) * | 2017-02-28 | 2020-03-26 | ユニバーシティ デ ロライン | 敗血症の治療のための、ワルトンジェリーから取得された間葉系幹細胞 |
| WO2019245050A1 (ja) * | 2018-06-22 | 2019-12-26 | 株式会社バイオミメティクスシンパシーズ | 中空糸細胞培養装置,細胞培養方法,培養上清の製造方法 |
Non-Patent Citations (5)
| Title |
|---|
| ANONYMOUS: "CD9XCD63 ELISA Kit for Human-Derived Exosome Quantitation", COSMO BIO NEWS, no. 140, 1 April 2018 (2018-04-01), JP, pages 15, XP009540547 * |
| DE LA GARZA-RODEA ANABEL S., VERWEIJ MARIEKE C., BOERSMA HESTER, VAN DER VELDE-VAN DIJKE IETJE, DE VRIES ANTOINE A. F., HOEBEN ROB: "Exploitation of Herpesvirus Immune Evasion Strategies to Modify the Immunogenicity of Human Mesenchymal Stem Cell Transplants", PLOS ONE, vol. 6, no. 1, 1 January 2011 (2011-01-01), XP055925774, DOI: 10.1371/journal.pone.0014493 * |
| FUJITA, MIYUKI; YANAGAWA, TOSHIHIDE; IMABAYASHI, TSUKASA; TAKAHASHI, EMI; OYANAGI, JUN; MIYAZAKI, KAORU: "2T10p-18 Effects of various laminin isoforms on growth and differentiation of human mesenchymal stem cells", 84TH ANNUAL MEETING OF THE JAPANESE BIOCHEMICAL SOCIETY; KYOTO, JAPAN; SEPTEMBER 21-24, 2011, vol. 84, 30 November 2010 (2010-11-30) - 24 September 2011 (2011-09-24), pages 2T10p-18, XP009541007 * |
| See also references of EP4130240A4 |
| STEPHANOPOULOS A. SAMBANIS ET AL.: "Use of Regulated Secretion in Protein Production from Animal Cells: An Evaluation with the AtT-20 Model Cell Line", BIOTECHNOLOGY AND BIOENGINEERING, vol. 35, 1990, pages 771 - 780, XP000673557, DOI: 10.1002/bit.260350804 * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024019080A1 (ja) * | 2022-07-19 | 2024-01-25 | 国立大学法人 長崎大学 | 血管内皮増殖因子を高発現する臍帯由来間葉系細胞の製造方法、および肺疾患治療用医薬組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2021247879A1 (en) | 2022-11-03 |
| EP4130240A1 (en) | 2023-02-08 |
| CA3173721A1 (en) | 2021-10-07 |
| CN115362252A (zh) | 2022-11-18 |
| TW202204605A (zh) | 2022-02-01 |
| CN116179480A (zh) | 2023-05-30 |
| AU2022259729A1 (en) | 2022-12-01 |
| US20230172992A1 (en) | 2023-06-08 |
| TW202311526A (zh) | 2023-03-16 |
| JPWO2021200744A1 (ja) | 2021-10-07 |
| EP4130240A4 (en) | 2024-05-08 |
| EP4155389A2 (en) | 2023-03-29 |
| EP4155389A3 (en) | 2023-07-12 |
| CA3177567A1 (en) | 2021-10-07 |
| JP2024015245A (ja) | 2024-02-01 |
| JP2022181218A (ja) | 2022-12-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Ichim et al. | Fibroblasts as a practical alternative to mesenchymal stem cells | |
| Das et al. | The role of hypoxia in bone marrow–derived mesenchymal stem cells: considerations for regenerative medicine approaches | |
| EP2171043B1 (en) | Treatment of diseases and disorders using self-renewing colony forming cells cultured and expanded in vitro | |
| WO2017188403A1 (ja) | Cd201、cd46、cd56、cd147及びcd165からなる群より選択される少なくとも1種の細胞表面マーカーを発現する間葉系幹細胞及びその調製方法、並びに上記間葉系幹細胞を含む医薬組成物及びその調製方法 | |
| Calle et al. | Strategies for whole lung tissue engineering | |
| CA2867953C (en) | Regulating stem cells | |
| US20060110825A1 (en) | Process for the preparation of stem cells from human muscle tissue and adipose tissue, and stem cell obtainable by this process | |
| US20210292712A1 (en) | Methods for the long-term expansion of granulocyte-macrophage progenitors and applications thereof | |
| JP2022078044A (ja) | コロニー形成培地及びその使用 | |
| TW200916581A (en) | Paracrine signals from mesenchymal feeder cells and regulating expansion and differentiation of hepatic progenitors using same | |
| JP2024015245A (ja) | 増殖細胞の生産方法、細胞生産物の生産方法、間葉系幹細胞集団およびその生産方法、幹細胞の培養上清およびその生産方法、並びに治療剤 | |
| JP2020072725A (ja) | 向上された臍帯由来付着型幹細胞、その製造方法及びその用途 | |
| Anstee | Production of erythroid cells from human embryonic stem cells (hESC) and human induced pluripotent stem cells (hiPS) | |
| Lei et al. | An effective cytokine combination for ex vivo expansion of porcine muscle stem cells | |
| KR20110097064A (ko) | 무혈청 줄기 세포 배양 조성물, 이를 함유한 조직 재생용 조성물 및 이를 이용한 조직 재생 방법 | |
| Zhu et al. | IL-6 coaxes cellular dedifferentiation as a pro-regenerative intermediate that contributes to pericardial ADSC-induced cardiac repair | |
| WO2003050273A1 (fr) | Milieu de culture pour des cellules humaines et methode de culture | |
| JP6695795B2 (ja) | 造血細胞の増殖ペプチドおよびその用途 | |
| US20240117301A1 (en) | Method for producing proliferating cells, method for producing cell product, mesenchymal stem cell population and method for producing same, culture supernatant of stem cells and method for producing same, and therapeutic agent | |
| NZ793106A (en) | Method of producing proliferated cells, method of producing cell product, mesenchymal stem cell population and method of producing same, culture supernatant of stem cells and method of producing same, and therapeutic agent | |
| US20130266542A1 (en) | Compositions and Methods of Using Living and Non-Living Bioactive Devices with Components Derived From Self-Renewing Colony Forming Cells Cultured and Expanded In Vitro | |
| WO2023286834A1 (ja) | 血管内皮増殖因子(vegf)高発現ペリサイト様細胞 | |
| JP2003235548A (ja) | ヒト細胞の培養用培地および培養方法 | |
| WO2023286832A1 (ja) | 血管内皮増殖因子(vegf)高発現ペリサイト様細胞の製造方法 | |
| Seo et al. | The effect of fibroblast growth factor and periodontal ligament fibroblast-conditioned medium on fibroblast-related gene expression in bone marrow stromal cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 21779739 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 3173721 Country of ref document: CA Ref document number: 2022512159 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2021247879 Country of ref document: AU Date of ref document: 20210326 Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2021779739 Country of ref document: EP Effective date: 20221031 |