WO2020241876A1 - 効率的なpprタンパク質の作製方法及びその利用 - Google Patents
効率的なpprタンパク質の作製方法及びその利用 Download PDFInfo
- Publication number
- WO2020241876A1 WO2020241876A1 PCT/JP2020/021472 JP2020021472W WO2020241876A1 WO 2020241876 A1 WO2020241876 A1 WO 2020241876A1 JP 2020021472 W JP2020021472 W JP 2020021472W WO 2020241876 A1 WO2020241876 A1 WO 2020241876A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- sequence
- amino acid
- ppr
- amino acids
- seq
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/5308—Immunoassay; Biospecific binding assay; Materials therefor for analytes not provided for elsewhere, e.g. nucleic acids, uric acid, worms, mites
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/02—Fusion polypeptide containing a localisation/targetting motif containing a signal sequence
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/09—Fusion polypeptide containing a localisation/targetting motif containing a nuclear localisation signal
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/60—Fusion polypeptide containing spectroscopic/fluorescent detection, e.g. green fluorescent protein [GFP]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/85—Fusion polypeptide containing an RNA binding domain
Abstract
Description
[1] 下記のいずれか1つの、PPRモチーフ:
(A-1)配列番号:9の配列からなるPPRモチーフ、又は配列番号:9の配列において、位置10のアミノ酸のチロシンへの置換、位置15のアミノ酸のリジンへの置換、位置16のアミノ酸のロイシンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置18のアミノ酸のアスパラギン酸への置換、及び位置28のアミノ酸のグルタミン酸への置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ、又は配列番号401の配列からなるPPRモチーフ、又は配列番号401の配列において、位置10のアミノ酸のチロシンへの置換、位置16のアミノ酸のロイシンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置18のアミノ酸のアスパラギン酸への置換、及び位置28のアミノ酸のグルタミン酸への置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
;
(A-2)配列番号:9又は401の配列において、位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~20個を置換、欠失、又は付加した配列からなり、かつアデニン結合性であるPPRモチーフ;
(A-3)配列番号:9又は401の配列と少なくとも42%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつアデニン結合性であるPPRモチーフ;
(C-1)配列番号:10の配列からなるPPRモチーフ、又は配列番号:10の配列において、位置2のアミノ酸のセリンへの置換、位置5のアミノ酸のイソロイシンへの置換、位置7のアミノ酸のロイシンへの置換、位置8のアミノ酸のリジンへの置換、位置10のアミノ酸のフェニルアラニン又はチロシンへの置換、位置15のアミノ酸のアルギニンへの置換、位置22のアミノ酸のバリンへの置換、位置24のアミノ酸のアルギニンへの置換、位置27のアミノ酸のロイシンへの置換、及び位置29のアミノ酸のアルギニンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(C-2)配列番号:10の配列において、位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~25個を置換、欠失、又は付加した配列からなり、かつシトシン結合性であるPPRモチーフ;
(C-3)配列番号:10の配列と少なくとも25%の配列同一性を有し、ただし位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつシトシン結合性であるPPRモチーフ;
(G-1)配列番号:11の配列からなるPPRモチーフ、又は配列番号:11の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置15のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のバリンの置換、位置28のアミノ酸のセリンへの置換、及び位置35のアミノ酸のイソロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(G-2)配列番号:11の配列において、位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~21個を置換、欠失、又は付加した配列からなり、かつグアニン結合性であるPPRモチーフ;
(G-3)配列番号:11の配列と少なくとも40%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつグアニン結合性であるPPRモチーフ;
(U-1)配列番号:12の配列からなるPPRモチーフ、又は配列番号:12の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置13のアミノ酸のセリンへの置換、位置15のアミノ酸のリジンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置20のアミノ酸のロイシンへの置換、位置21のアミノ酸のリジンへの置換、位置23のアミノ酸のフェニルアラニンへの置換、位置24のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のリジンへの置換、位置28のアミノ酸のリジンへの置換、位置29のアミノ酸のアルギニンへの置換、及び位置31のアミノ酸のロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ
(U-2)配列番号:12の配列において、位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~22個を置換、欠失、又は付加した配列からなり、かつウラシル結合性であるPPRモチーフ;
(U-3)配列番号:12の配列と少なくとも37%の配列同一性を有し、ただし位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつウラシル結合性であるPPRモチーフ。
[2] 1に記載のPPRモチーフの、標的RNAが15塩基長以上であるPPRタンパク質の作製のための使用。
[3] 1に記載のPPRモチーフのPPRタンパク質の作製のための使用であって、PPRタンパク質の標的RNAへの結合性能を高めるための使用。
[4] n個の塩基配列からなる標的RNAに結合可能な、n個のPPRモチーフを含むタンパク質であって、
該塩基配列中のアデニンに対するPPRモチーフが、1に定義した(A-1)、(A-2)、又は(A-3)のPPRモチーフであり;
該塩基配列中のシトシンに対するPPRモチーフが、1に定義した(C-1)、(C-2)、又は(c-3)のPPRモチーフであり;
該塩基配列中のグアニンに対するPPRモチーフが、1に定義した(G-1)、(G-2)、又は(G-3)のPPRモチーフであり;
該塩基配列中のウラシルに対するPPRモチーフが、1に定義した(U-1)、(U-2)、又は(U-3)のPPRモチーフである、PPRタンパク質。
[5] nが、15以上である、4に記載のタンパク質。
[6] N末端から1番目のPPRモチーフが下記のいずれか1つである、4又は5に記載のタンパク質:
(1st A-1)配列番号:402の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換したPPRモチーフ;
(1st A-2)(1st A-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつアデニン結合性であるPPRモチーフ;
(1st A-3)(1st A-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつアデニン結合性であるPPRモチーフ;
(1st C-1)配列番号:403の配列からなるPPRモチーフ;
(1st C-2)(1st C-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつシトシン結合性であるPPRモチーフ;
(1st C-3)(1st C-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつシトシン結合性であるPPRモチーフ;
(1st G-1)配列番号:404の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換した配列からなるPPRモチーフ;
(1st G-2)(1st G-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつグアニン結合性であるPPRモチーフ;
(1st G-3)(1st G-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつグアニン結合性であるPPRモチーフ;
(1st U-1)配列番号:405の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換した配列からなるPPRモチーフ;
(1st U-2)(1st U-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつウラシル結合性であるPPRモチーフ;
(1st U-3)(1st U-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつウラシル結合性であるPPRモチーフ。
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がグルタミン酸である組み合わせ
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がグルタミンである組み合わせ
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がリジンである組み合わせ
・位置6のアミノ酸アスパラギン酸であり、かつ位置9アミノ酸がグリシンである組み合わせ
[7] 4~6のいずれか1項に記載のタンパク質を用いることを特徴とする、RNAスプライシングの制御方法。
[8] 4~6のいずれか1項に記載のタンパク質を用いることを特徴とする、RNAの検出方法。
[9] 蛍光タンパク質、核移行シグナルペプチド、及びタグタンパク質からなる群より選択される少なくとも一つと、4~6のいずれか1項に記載のタンパク質との、融合タンパク質。
[10] 1に記載のPPRモチーフ、又は4~6のいずれか1項に記載のタンパク質をコードする核酸。
[11] 10に記載の核酸を含む、ベクター。
[12] 11に記載のベクターを含む、細胞(ヒト個体は除く。)。
[13] 1に記載のPPRモチーフ、4~6のいずれか1項に記載のタンパク質、又は11に記載のベクターを用いる、RNAの操作方法(ヒト個体での実施を除く。)。
[14] 13に記載の操作方法を含む、生物の生産方法。
(A-1)配列番号:9の配列からなるPPRモチーフ、又は配列番号:9の配列において、位置10のアミノ酸のチロシンへの置換、位置15のアミノ酸のリジンへの置換、位置16のアミノ酸のロイシンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置18のアミノ酸のアスパラギン酸への置換、及び位置28のアミノ酸のグルタミン酸への置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(A-2)配列番号:9の配列において、位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~20個を置換、欠失、又は付加した配列からなり、かつアデニン結合性であるPPRモチーフ;
(A-3)配列番号:9の配列と少なくとも42%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつアデニン結合性であるPPRモチーフ;
(C-1)配列番号:10の配列からなるPPRモチーフ、又は配列番号:10の配列において、位置2のアミノ酸のセリンへの置換、位置5のアミノ酸のイソロイシンへの置換、位置7のアミノ酸のロイシンへの置換、位置8のアミノ酸のリジンへの置換、位置10のアミノ酸のフェニルアラニン又はチロシンへの置換、位置15のアミノ酸のアルギニンへの置換、位置22のアミノ酸のバリンへの置換、位置24のアミノ酸のアルギニンへの置換、位置27のアミノ酸のロイシンへの置換、及び位置29のアミノ酸のアルギニンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(C-2)配列番号:10の配列において、位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~25個を置換、欠失、又は付加した配列からなり、かつシトシン結合性であるPPRモチーフ;
(C-3)配列番号:10の配列と少なくとも25%の配列同一性を有し、ただし位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつシトシン結合性であるPPRモチーフ;
(G-1)配列番号:11の配列からなるPPRモチーフ、又は配列番号:11の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置15のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のバリンの置換、位置28のアミノ酸のセリンへの置換、及び位置35のアミノ酸のイソロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(G-2)配列番号:11の配列において、位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~21個を置換、欠失、又は付加した配列からなり、かつグアニン結合性であるPPRモチーフ;
(G-3)配列番号:11の配列と少なくとも40%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつグアニン結合性であるPPRモチーフ;
(U-1)配列番号:12の配列からなるPPRモチーフ、又は配列番号:12の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置13のアミノ酸のセリンへの置換、位置15のアミノ酸のリジンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置20のアミノ酸のロイシンへの置換、位置21のアミノ酸のリジンへの置換、位置23のアミノ酸のフェニルアラニンへの置換、位置24のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のリジンへの置換、位置28のアミノ酸のリジンへの置換、位置29のアミノ酸のアルギニンへの置換、及び位置31のアミノ酸のロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ
(U-2)配列番号:12の配列において、位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~22個を置換、欠失、又は付加した配列からなり、かつウラシル結合性であるPPRモチーフ;
(U-3)配列番号:12の配列と少なくとも37%の配列同一性を有し、ただし位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつウラシル結合性であるPPRモチーフ。
[2] 1に記載のPPRモチーフの、標的RNAが15塩基長以上であるPPRタンパク質の作製のための使用。
[3] 1に記載のPPRモチーフのPPRタンパク質の作製のための使用であって、PPRタンパク質の標的RNAへの結合性能を高めるための使用。
[4] n個の塩基配列からなる標的RNAに結合可能な、n個のPPRモチーフを含むタンパク質であって、
該塩基配列中のアデニンに対するPPRモチーフが、1に定義した(A-1)、(A-2)、又は(A-3)のPPRモチーフであり;
該塩基配列中のシトシンに対するPPRモチーフが、1に定義した(C-1)、(C-2)、又は(c-3)のPPRモチーフであり;
該塩基配列中のグアニンに対するPPRモチーフが、1に定義した(G-1)、(G-2)、又は(G-3)のPPRモチーフであり;
該塩基配列中のウラシルに対するPPRモチーフが、1に定義した(U-1)、(U-2)、又は(U-3)のPPRモチーフである、PPRタンパク質。
[5] nが、15以上である、4に記載のタンパク質。
[6] 4又は5に記載のタンパク質を用いることを特徴とする、RNAスプライシングの制御方法。
[7] 4又は5に記載のタンパク質を用いることを特徴とする、RNAの検出方法。
[8] 蛍光タンパク質、核移行シグナルペプチド、及びタグタンパク質からなる群より選択される少なくとも一つと、4又は5に記載のタンパク質との、融合タンパク質。
[9] 1に記載のPPRモチーフ、又は4又は5に記載のタンパク質をコードする核酸。
[10] 9に記載の核酸を含む、ベクター。
[11] 10に記載のベクターを含む、細胞(ヒト個体は除く。)。
[12] 1に記載のPPRモチーフ、4又は5に記載のタンパク質、又は10に記載のベクターを用いる、RNAの操作方法(ヒト個体での実施を除く。)。
[13] 12に記載の操作方法を含む、生物の生産方法。
[14] 以下の工程を含む、n個の塩基配列からなる標的核酸に結合可能な、n個のPPRモチーフを含むタンパク質をコードする遺伝子の作製方法:
アデニン、シトシン、グアニン、又はウラシルもしくはチミン結合性であるPPRモチーフ各々をコードする4種類、及びPPRモチーフの2個の連結物各々をコードする16種類を含む、少なくとも20種類のポリヌクレオチドが、少なくともm種類の順に連結可能に設計された中間ベクターDest-a...のそれぞれに挿入された、少なくとも20×m種類のPPRパーツのライブラリーから、目的遺伝子を作製するために必要なm個のPPRパーツを選択し;
選択したm種類のPPRパーツを、ベクターパーツとともにGolden Gate反応に供してm個のポリヌクレオチドの連結物が挿入されたベクターを得る(ただしnは、m以上であり、かつm×2以下である。)。
[15] mが10であり、15個以上のPPRモチーフを含むタンパク質をコードする遺伝子を作製するための、14に記載の作製方法。
[16] 下記の工程を含む、n個の塩基配列からなる標的核酸に結合可能な、n個のPPRモチーフを含むタンパク質を検出又は定量する方法:
固相化された標的核酸に、候補タンパク質を含む溶液を供し、標的核酸に結合したタンパク質を検出又は定量する工程。
[17] 候補タンパク質が標識タンパク質と融合されている、16に記載の方法。
(定義)
本発明でPPRモチーフというときは、特に記載した場合を除き、Web上のタンパク質ドメイン検索プログラムでアミノ酸配列を解析した際に、PfamにおいてPF01535、PrositeにおいてPS51375で得られるE値が所定値以下(望ましくはE-03)のアミノ酸配列をもつ30~38アミノ酸で構成されるポリペプチドをいう。本発明で定義するPPRモチーフを構成するアミノ酸の位置番号は、PF01535とほぼ同義である一方で、PS51375のアミノ酸の場所から2引いた数(例;本発明の1番→PS51375の3番)に相当する。ただし、“ii”(-2)番のアミノ酸というときは、PPRモチーフを構成するアミノ酸の後ろ(C末端側)から2番目のアミノ酸、又は次のPPRモチーフの1番アミノ酸に対して2個N末端側、すなわち-2番目のアミノ酸とする。次のPPRモチーフが明確に同定されない場合、次のヘリックス構造の1番目のアミノ酸に対して、2コ前のアミノ酸を“ii”とする。Pfamについてはhttp://pfam.sanger.ac.uk/、Prositeについては、http://www.expasy.org/prosite/を参照することができる。
Xは、存在しないか又は1~9アミノ酸長からなる部分であり;
Helix Bは、11~13アミノ酸長からなる、αヘリックス構造を形成可能な部分であり;
Lは、2~7アミノ酸長の、式3で表される部分であり;
(3-1) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、アスパラギン及びアスパラギン酸の場合、そのPPRモチーフは、Uに強く結合し、次にCに、その次にA又はGに対して結合するという、選択的なRNA塩基結合能を有する。
(3-2) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、トレオニン、アスパラギンの場合、そのPPRモチーフは、Aに強く結合し、次にGに、その次にCに対して結合するが、Uには結合しないという、選択的なRNA塩基結合能を有する。
(3-3) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、アスパラギン、アスパラギンの場合、そのPPRモチーフは、Cに強く結合し、次にA又はUに対して結合するが、Gには結合しないという、選択的なRNA塩基結合能を有する。
(3-4) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、グルタミン酸、グリシン、アスパラギン酸の場合、そのPPRモチーフは、Gに強く結合するが、A、U及びCには結合しないという、選択的なRNA塩基結合能を有する。
(3-5) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、アスパラギン、アスパラギンの場合、そのPPRモチーフは、Cに強く結合し、次にUに、その次にAに対して結合するが、Gには結合しないという、選択的なRNA塩基結合能を有する。
(3-6) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、トレオニン、アスパラギン酸の場合、そのPPRモチーフは、Gに強く結合し、次にUに対して結合するが、AとCには結合しないという、選択的なRNA塩基結合能を有する。
(3-7) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、リジン、トレオニン、アスパラギン酸、の場合、そのPPRモチーフは、Gに強く結合し、次にAに対して結合するが、U及びCには結合しないという、選択的なRNA塩基結合能を有する。
(3-8) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、フェニルアラニン、セリン、アスパラギンの場合、そのPPRモチーフは、Aに強く結合し、次にCに、その次にG及びUに対して結合するという、選択的なRNA塩基結合能を有する。
(3-9) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、アスパラギン、セリンの場合、そのPPRモチーフは、Cに強く結合し、次にUに対して結合するが、A及びGには結合しないという、選択的なRNA塩基結合能を有する。
(3-10) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、フェニルアラニン、トレオニン、アスパラギンの場合、そのPPRモチーフは、Aに強く結合するが、G、U及びCには結合しないという、選択的なRNA塩基結合能を有する。
(3-11) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、アスパラギン、アスパラギン酸の場合、そのPPRモチーフは、Uに強く結合し、次にAに対して結合するが、G及びCには結合しないという、選択的なRNA塩基結合能を有する。
(3-12) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、トレオニン、トレオニン、アスパラギンの場合、そのPPRモチーフは、Aに強く結合するが、G、U及びCには結合しないという、選択的なRNA塩基結合能を有する。
(3-13) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、メチオニン、アスパラギン酸の場合、そのPPRモチーフは、Uに強く結合し、次にCに対して結合するが、A及びGには結合しないという、選択的なRNA塩基結合能を有する。
(3-14) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、フェニルアラニン、プロリン、アスパラギン酸の場合PPR、そのモチーフは、Uに強く結合し、次にCに対して結合するが、A及びGには結合しないという、選択的なRNA塩基結合能を有する。
(3-15) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、チロシン、プロリン、アスパラギン酸の場合、そのPPRモチーフは、Uに強く結合するが、A、G及びCには結合しないという、選択的なRNA塩基結合能を有する。
(3-16) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、ロイシン、トレオニン、アスパラギン酸の場合、そのPPRモチーフは、Gに強く結合するが、A、U及びCには結合しないという、選択的なRNA塩基結合能を有する。
(2-1) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、グリシン、アスパラギン酸であるとき、そのPPRモチーフは、Gに選択的に結合する;
(2-2) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、グルタミン酸、グリシン、アスパラギン酸であるとき、そのPPRモチーフは、Gに選択的に結合する;
(2-3) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、グリシン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-4) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、グルタミン酸、グリシン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-5) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、グリシン、セリンであるとき、そのPPRモチーフは、Aに選択的に結合し、次にCに対して結合する;
(2-6) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、イソロイシン、任意のアミノ酸であるとき、そのPPRモチーフは、T及びCに選択的に結合する;
(2-7) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、イソロイシン、アスパラギンであるとき、そのPPRモチーフは、Tに選択的に結合し、次にCに対して結合する;
(2-8) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、ロイシン、任意のアミノ酸であるとき、そのPPRモチーフは、T及びCに選択的に結合する;
(2-9) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、ロイシン、アスパラギン酸であるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-10) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、ロイシン、リシンであるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-11) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、メチオニン、任意のアミノ酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-12) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、メチオニン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-13) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、メチオニン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合し、次にCに対して結合する;
(2-14) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、アスパラギン、任意のアミノ酸であるとき、そのPPRモチーフは、C及びTに選択的に結合する;
(2-15) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、アスパラギン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-16) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、フェニルアラニン、アスパラギン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-17) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、グリシン、アスパラギン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-18) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、アスパラギン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-19) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、トレオニン、アスパラギン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-20) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、アスパラギン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合し、次にCに対して結合する;
(2-21) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、チロシン、アスパラギン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合し、次にCに対して結合する;
(2-22) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、アスパラギン、アスパラギンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-23) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、アスパラギン、アスパラギンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-24) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、セリン、アスパラギン、アスパラギンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-25) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、アスパラギン、アスパラギンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-26) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、アスパラギン、セリンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-27) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、アスパラギン、セリンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-28) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、アスパラギン、トレオニンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-29) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、アスパラギン、トレオニンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-30) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、アスパラギン、トリプトファンであるとき、そのPPRモチーフは、Cに選択的に結合し、次にTに対して結合する;
(2-31) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、アスパラギン、トリプトファンであるとき、そのPPRモチーフは、Tに選択的に結合し、次にCに対して結合する;
(2-32) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、プロリン、任意のアミノ酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-33) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、プロリン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-34) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、フェニルアラニン、プロリン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-35) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、チロシン、プロリン、アスパラギン酸であるとき、そのPPRモチーフは、Tに選択的に結合する;
(2-36) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、セリン、任意のアミノ酸であるとき、そのPPRモチーフは、A及びGに選択的に結合する;
(2-37) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、セリン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-38) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、フェニルアラニン、セリン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-39) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、セリン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-40) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、トレオニン、任意のアミノ酸であるとき、そのPPRモチーフは、A及びGに選択的に結合する;
(2-41) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、トレオニン、アスパラギン酸であるとき、そのPPRモチーフは、Gに選択的に結合する;
(2-42) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、トレオニン、アスパラギン酸であるとき、そのPPRモチーフは、Gに選択的に結合する;
(2-43) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、トレオニン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-44) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、フェニルアラニン、トレオニン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-45) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、トレオニン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-46) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、バリン、トレオニン、アスパラギンであるとき、そのPPRモチーフは、Aに選択的に結合する;
(2-47) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、バリン、任意のアミノ酸であるとき、そのPPRモチーフは、A、C及びTに結合するが、Gには結合しない;
(2-48) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、イソロイシン、バリン、アスパラギン酸であるとき、そのPPRモチーフは、Cに選択的に結合し、次にAに対して結合する;
(2-49) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、バリン、グリシンであるとき、そのPPRモチーフは、Cに選択的に結合する;
(2-50) A1、A4、及びLiiの3つのアミノ酸の組み合わせが、順に、任意のアミノ酸、バリン、トレオニンであるとき、そのPPRモチーフは、Tに選択的に結合する。
本発明は、新規なPPRモチーフを提供する。本発明により提供される新規なPPRモチーフであって、アデニン結合性であるものは、下記の(A-1)、(A-2)、及び(A-3)である:
(A-1)配列番号:9の配列からなるPPRモチーフ、又は配列番号:9の配列において、位置10のアミノ酸のチロシンへの置換、位置15のアミノ酸のリジンへの置換、位置16のアミノ酸のロイシンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置18のアミノ酸のアスパラギン酸への置換、及び位置28のアミノ酸のグルタミン酸への置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(A-2)配列番号:9の配列において、位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~20個を置換、欠失、又は付加した配列からなり、かつアデニン結合性であるPPRモチーフ;
(A-3)配列番号:9の配列と少なくとも42%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつアデニン結合性であるPPRモチーフ。
好ましくは、位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置5、8、13、21、22、23、25、29、35のアミノ酸以外のアミノ酸の1~11個であり、
より好ましくは、位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置5、8、13、21、22、23、25、29、35のアミノ酸以外のアミノ酸であって、かつ位置20、24、31、及び32のアミノ酸以外のアミノ酸の1~7個であり、
さらに好ましくは、位置10、15、16、17、18、及び28のアミノ酸のいずれかである。
好ましくは、配列番号:9の配列と少なくとも71%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸、及び位置5、8、13、21、22、23、25、29、35のアミノ酸は同一であることであり、
より好ましくは、配列番号:9の配列と少なくとも80%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸、位置5、8、13、21、22、23、25、29、35のアミノ酸、及び位置20、24、31、及び32のアミノ酸は同一であることであり、
さらに好ましくは、配列番号:9の配列と少なくとも82%の配列同一性を有し、ただし同一でないアミノ酸は、位置10、15、16、17、18、及び28のアミノ酸のいずれかである。
(C-1)配列番号:10の配列からなるPPRモチーフ、又は配列番号:10の配列において、位置2のアミノ酸のセリンへの置換、位置5のアミノ酸のイソロイシンへの置換、位置7のアミノ酸のロイシンへの置換、位置8のアミノ酸のリジンへの置換、位置10のアミノ酸のフェニルアラニン又はチロシンへの置換、位置15のアミノ酸のアルギニンへの置換、位置22のアミノ酸のバリンへの置換、位置24のアミノ酸のアルギニンへの置換、位置27のアミノ酸のロイシンへの置換、及び位置29のアミノ酸のアルギニンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(C-2)配列番号:10の配列において、位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~25個を置換、欠失、又は付加した配列からなり、かつシトシン結合性であるPPRモチーフ;
(C-3)配列番号:10の配列と少なくとも25%の配列同一性を有し、ただし位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつシトシン結合性であるPPRモチーフ。
好ましくは、位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置6、9、11、12、17、20、21、23、25、28、及び35のアミノ酸以外のアミノ酸の1~14個であり、
より好ましくは、位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置6、9、11、12、17、20、21、23、25、28、及び35のアミノ酸以外のアミノ酸であって、かつ位置13、16、31、及び32のアミノ酸以外のアミノ酸の1~10個であり、
さらに好ましくは、位置2、5、7、8、10、15、22、24、27、及び29のアミノ酸のいずれかである。
好ましくは、配列番号:10の配列と少なくとも60%の配列同一性を有し、ただし位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸、及び6、9、11、12、17、20、21、23、25、28、及び35のアミノ酸は同一であることであり、
より好ましくは、配列番号:10の配列と少なくとも71%の配列同一性を有し、ただし位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸、位置6、9、11、12、17、20、21、23、25、28、及び35のアミノ酸、及び位置13、16、31、及び32のアミノ酸は同一であることであり、
さらに好ましくは、配列番号:10の配列と少なくとも71%の配列同一性を有し、ただし同一でないアミノ酸は、位置2、5、7、8、10、15、22、24、27、及び29のアミノ酸のいずれかである。
(G-1)配列番号:11の配列からなるPPRモチーフ、又は配列番号:11の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置15のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のバリンの置換、位置28のアミノ酸のセリンへの置換、及び位置35のアミノ酸のイソロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(G-2)配列番号:11の配列において、位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~21個を置換、欠失、又は付加した配列からなり、かつグアニン結合性であるPPRモチーフ;
(G-3)配列番号:11の配列と少なくとも40%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつグアニン結合性であるPPRモチーフ。
好ましくは、位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置5、11、12、17、20、21、22、23、及び25のアミノ酸以外のアミノ酸の1~12個であり、
より好ましくは、位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置5、11、12、17、20、21、22、23、及び25のアミノ酸以外のアミノ酸であって、かつ位置8、13、16、24、29、31、及び32のアミノ酸以外のアミノ酸の1~5個であり、
さらに好ましくは、位置10、15、27、28、及び35のアミノ酸のいずれかである。
好ましくは、配列番号:11の配列と少なくとも65%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸、及び位置5、11、12、17、20、21、22、23、及び25のアミノ酸は同一であることであり、
より好ましくは、配列番号:11の配列と少なくとも85%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸、位置5、11、12、17、20、21、22、23、及び25のアミノ酸、及び位置8、13、16、24、29、31、及び32のアミノ酸は同一であることであり、
さらに好ましくは、配列番号:11の配列と少なくとも85%の配列同一性を有し、ただし同一でないアミノ酸は、位置10、15、27、28、及び35のアミノ酸のいずれかである。
(U-1)配列番号:12の配列からなるPPRモチーフ、又は配列番号:12の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置13のアミノ酸のセリンへの置換、位置15のアミノ酸のリジンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置20のアミノ酸のロイシンへの置換、位置21のアミノ酸のリジンへの置換、位置23のアミノ酸のフェニルアラニンへの置換、位置24のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のリジンへの置換、位置28のアミノ酸のリジンへの置換、位置29のアミノ酸のアルギニンへの置換、及び位置31のアミノ酸のロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(U-2)配列番号:12の配列において、位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~22個を置換、欠失、又は付加した配列からなり、かつウラシル結合性であるPPRモチーフ;
(U-3)配列番号:12の配列と少なくとも37%の配列同一性を有し、ただし位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつウラシル結合性であるPPRモチーフ。
好ましくは、位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置5、7、9、16、18、22、25、及び35のアミノ酸以外のアミノ酸の1~14個であり、
より好ましくは、位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸であって、かつ位置5、7、9、16、18、22、25、及び35のアミノ酸以外のアミノ酸であって、かつ位置8、及び32のアミノ酸以外のアミノ酸の1~12個であり、
さらに好ましくは、位置10、13、15、17、20、21、23、24、27、28、29、及び31のアミノ酸のいずれかである。
好ましくは、配列番号:12の配列と少なくとも60%の配列同一性を有し、ただし位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸、及び位置5、7、9、16、18、22、25、及び35のアミノ酸は同一であることであり、
より好ましくは、配列番号:12の配列と少なくとも65%の配列同一性を有し、ただし位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸、位置5、7、9、16、18、22、25、及び35のアミノ酸、及び位置8、及び32のアミノ酸は同一であることであり、
さらに好ましくは、配列番号:12の配列と少なくとも65%の配列同一性を有し、ただし同一でないアミノ酸は、位置10、13、15、17、20、21、23、24、27、28、29、及び31のアミノ酸のいずれかである。
図1~4には、シロイヌナズナのPPRモチーフ配列のうち、位置1、4、及びiiのアミノ酸の組み合わせがアデニンを認識するPPRモチーフのためにはVTN、シトシンを認識するPPRモチーフのためにはVSN、グアニンを認識するPPRモチーフのためにはVTD、ウラシルを認識するPPRモチーフのためにはVNDであるものを収集し、各位置に出現するアミノ酸の種類及びその数をまとめたものである。新たなPPRモチーフの配列v2 A(SEQ ID NO:9)、v2 C(SEQ ID NO:10)、v2 G(SEQ ID NO:11)、v2 U(SEQ ID NO:12)においては、各位置のアミノ酸は出現頻度が高いものである。図6Aには、これらの新規な配列とともに、dPPRモチーフの配列において、位置1、4、及びiiのアミノ酸の組み合わせをv2と同じにした、v1 A(SEQ ID NO:13)、v1 C(SEQ ID NO:14)、v1 G(SEQ ID NO:15)、v1 U(SEQ ID NO:16)も示した。
本発明は、新規なPPRモチーフを含む新規なPPRタンパク質を提供する。
本発明により提供される新規なPPRタンパク質は、下記のものである。
n個の塩基配列からなる標的RNAに結合可能な、n個のPPRモチーフを含むタンパク質であって、
該塩基配列中のアデニンに対するPPRモチーフが、上述の(A-1)、(A-2)、又は(A-3)のPPRモチーフであり;
該塩基配列中のシトシンに対するPPRモチーフが、上述の(C-1)、(C-2)、又は(c-3)のPPRモチーフであり;
該塩基配列中のグアニンに対するPPRモチーフが、上述の(G-1)、(G-2)、又は(G-3)のPPRモチーフであり;
該塩基配列中のウラシルに対するPPRモチーフが、上述の(U-1)、(U-2)、又は(U-3)のPPRモチーフである、PPRタンパク質。
なお表中、Kd値は、各文献で示されている最も低い値を表記した。
本発明は、新規なPPRモチーフ及びそれを含む新規なPPRタンパク質をコードする核酸を提供する。新規なPPRモチーフをコードする塩基配列は、コドンの縮退により、いくつかのバリエーションがある。
本発明者らは、天然に存在する既存のPPRモチーフのアミノ酸情報から、PPRモチーフの6番目の位置のアミノ酸は疎水性(特にロイシン)、9番目の位置のアミノ酸は非親水性のアミノ酸(特にグリシン)である場合が非常に多いことを見出した。すでに結晶構造が得られているPPRタンパク質の構造(非特許文献6:Coquille et al., 2014 Nat. Commun.; PDB ID: 4PJQ, 4WN4, 4WSL, 4PJR; 非特許文献7:Shen et al., 2015 Nat. Commun., PDB ID: 5I9D, 5I9F, 5I9G, 5I9H)から、1モチーフ目(N末側)のそれら6番目、9番目は外側に露出するため、その露出した疎水性アミノ酸が原因で凝集性を示すと想像した(図6A)。一方で、2モチーフ目以降においては、6番目、9番目のアミノ酸は、タンパク質内に埋もれ、疎水性コアを形成するため、すべてのモチーフの6番目、9番目に親水性残基を入れるとタンパク質構造が崩壊する可能性があると考えた。そこで1モチーフ目のみ、6番目、好ましくは6番目及び9番目のアミノ酸を親水性のアミノ酸(アスパラギン、アスパラギン酸、グルタミン、グルタミン酸、リジン、アルギニン、セリン、トレオニン)にすることでPPRの凝集性を減少させることとした。
特定の塩基配列を有する標的核酸と結合可能なタンパク質において、N末端から1番目のPPRモチーフ(M1)において:
(1)A6アミノ酸を、親水性アミノ酸、好ましくはA6アミノ酸を、アスパラギン又はアスパラギン酸とする。
(2)さらに、A9アミノ酸を、親水性アミノ酸又はグリシン、好ましくはグルタミン、グルタミン酸、リジン、又はグリシンとする。
(3)あるいは、A6アミノ酸及びA9アミノ酸を、下記のいずれかの組み合わせとする。
・A6アミノ酸がアスパラギンであり、かつA9アミノ酸がグルタミン酸である組み合わせ
・A6アミノ酸がアスパラギンであり、かつA9アミノ酸がグルタミンである組み合わせ
・A6アミノ酸がアスパラギンであり、かつA9アミノ酸がリジンである組み合わせ
・A6アミノ酸アスパラギン酸であり、かつA9アミノ酸がグリシンである組み合わせ
(1st A-1)配列番号:402の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換したPPRモチーフ;
(1st A-2)(1st A-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつアデニン結合性であるPPRモチーフ;
(1st A-3)(1st A-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつアデニン結合性であるPPRモチーフ;
(1st C-1)配列番号:403の配列からなるPPRモチーフ;
(1st C-2)(1st C-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつシトシン結合性であるPPRモチーフ;
(1st C-3)(1st C-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつシトシン結合性であるPPRモチーフ;
(1st G-1)配列番号:404の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換した配列からなるPPRモチーフ;
(1st G-2)(1st G-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつグアニン結合性であるPPRモチーフ;
(1st G-3)(1st G-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつグアニン結合性であるPPRモチーフ;
(1st U-1)配列番号:405の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換した配列からなるPPRモチーフ;
(1st U-2)(1st U-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつウラシル結合性であるPPRモチーフ;
(1st U-3)(1st U-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつウラシル結合性であるPPRモチーフ。
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がグルタミン酸である組み合わせ
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がグルタミンである組み合わせ
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がリジンである組み合わせ
・位置6のアミノ酸アスパラギン酸であり、かつ位置9アミノ酸がグリシンである組み合わせ
本発明で塩基配列(ヌクレオチド配列ということもある。)又はアミノ酸配列に関し「同一性」というときは、特に記載した場合を除き、2つの配列を最適の態様で整列させた場合に、2つの配列間で共有する一致した塩基又はアミノ酸の個数の百分率を意味する。すなわち、同一性=(一致した位置の数/位置の全数)×100で算出でき、市販されているアルゴリズムを用いて計算することができる。また、このようなアルゴリズムは、Altschul et al., J.Mol.Biol. 215(1990) 403-410に記載されるNBLAST及びXBLASTプログラム中に組込まれている。より詳細には、塩基配列又はアミノ酸配列の同一性に関する検索・解析は、当業者には周知のアルゴリズム又はプログラム(例えば、BLASTN、BLASTP、BLASTX、ClustalW)により行うことができる。プログラムを用いる場合のパラメーターは、当業者であれば適切に設定することができ、また各プログラムのデフォルトパラメーターを用いてもよい。これらの解析方法の具体的な手法もまた、当業者には周知である。
疎水性(非極性)アミノ酸;アラニン、バリン、グリシン、イソロイシン、ロイシン、フェニルアラニン、プロリン、トリプトファン、チロシン
非疎水性アミノ酸;アルギニン、アスパラギン、アスパラギン酸、グルタミン酸、グルタミン、リジン、セリン、トレオニン、システイン、ヒスチジン、メチオニン;
親水性アミノ酸;アルギニン、アスパラギン、アスパラギン酸、グルタミン酸、グルタミン、リジン、セリン、トレオニン;
酸性アミノ酸:アスパラギン酸、グルタミン酸;
塩基性アミノ酸:リジン、アルギニン、ヒスチジン;
中性アミノ酸:アラニン、アスパラギン、システイン、グルタミン、グリシン、イソロイシン、ロイシン、メチオニン、フェニルアラニン、プロリン、セリン、トレオニン、トリプトファン、チロシン、バリン;
含硫アミノ酸:メチオニン、システイン;
含芳香環アミノ酸:チロシン、トリプトファン、フェニルアラニン。
本発明のPPRモチーフ、それを含むタンパク質、又はそれらをコードする核酸は、当業者であれば、従来技術を利用して調製することができる。
(結合力)
本発明の新規 PPRモチーフ(SEQ ID NOs:9-12)を用いて作製したPPRタンパク質は、比較的長い標的RNAに対するPPRタンパク質の作製に適しているのみならず、同じ標的RNAに対する既存のPPR(SEQ ID NOs:13-16)モチーフを用いて作製したPPRタンパク質よりも高いRNA結合性能を有しうる。
本発明の新規 PPRモチーフを用いて作製したPPRタンパク質は、標的配列に対する特異性において、同じ標的RNAに対する既存のPPRモチーフを用いて作製したPPRタンパク質よりも高い能力を有しうる。
本発明の新規 PPRモチーフを用いて作製したPPRタンパク質は、標的RNAに対し、高い親和性(平衡解離乗数、Kd値)を有しうる。
本発明の新規 PPRモチーフを用いることにより、所望のPPRタンパク質を効率的に構築することができる。構築効率は、既存の方法を用い、高いKd値を有するPPRタンパク質が構築できた割合を求めることにより、算出できる。Kd値の代わりに、上述のようにRPB-ELISAによる発光シグナル値を求め、同様に算出してもよい。
本発明はまた、以下の工程を含む、n個の塩基配列からなる標的核酸に結合可能な、n個のPPRモチーフを含むタンパク質をコードする遺伝子の作製方法を提供する:
アデニン、シトシン、グアニン、又はウラシルもしくはチミン結合性であるPPRモチーフ各々をコードする4種類、及びPPRモチーフの2個の連結物各々をコードする16種類を含む、少なくとも20種類のポリヌクレオチドが、少なくともm種類の順に連結可能に設計された中間ベクターDest-a...のそれぞれに挿入された、少なくとも20×m種類のPPRパーツのライブラリーから、目的遺伝子を作製するために必要なm個のPPRパーツを選択し;
選択したm種類のPPRパーツを、ベクターパーツとともにGolden Gate反応に供してm個のポリヌクレオチドの連結物が挿入されたベクターを得る。nは、m以上であり、かつm×2以下の整数である。nは、例えば10~20とすることができる。
本発明は、下記の工程を含む、n個の塩基配列からなる標的核酸に結合可能な、n個のPPRモチーフを含むタンパク質を検出又は定量する方法を提供する:
固相化された標的核酸に、候補タンパク質を含む溶液を供し、標的核酸に結合したタンパク質を検出又は定量する工程。
この本発明の検出・分析方法は、ハイスループットなPPRタンパク質の結合性能を評価する方法として有用である。
(複合体、融合タンパク質)
本発明により提供されるPPRモチーフ又はPPRタンパク質は、機能性領域を連結し、複合体とすることができる。また、タンパク質性の機能性領域を連結し、融合タンパク質とすることができる。機能性領域とは、生体内又は細胞内で特定の生物学的機能、例えば酵素機能、触媒機能、阻害機能、亢進機能などの機能を有する部分、又は標識としての機能を有する部分をいう。そのような領域は、例えば、タンパク質、ペプチド、核酸、生理活性物質、薬剤からなる。なお、以下では、本発明を、複合体に関し、融合タンパク質を例に説明することがあるが、当業者であれば、その説明に準じて、融合タンパク質以外の複合体の場合についても理解することができる。
本発明は、上述の、PPRモチーフ、PPRタンパク質又は融合タンパク質をコードする核酸、核酸を含むベクター(例えば増幅のためのベクター、発現ベクター)も提供する。増幅のためのベクターは、大腸菌や酵母を宿主として用いうる。本明細書において、発現ベクターとは、例えば上流から、プロモーター配列を有するDNA、所望のタンパク質をコードするDNA、及びターミネーター配列を有するDNAを含むベクターを意味するが、所望の機能を発揮する限り、必ずしもこの順に配列されている必要はない。本発明においては、当業者が通常使用し得る様々なベクターを組み換えて使用することができる。
本発明のPPRタンパク質、又は融合タンパク質は、生体内又は細胞内に、核酸配列特異的に機能性領域をデリバリーし、機能させることができる可能性がある。GFP等の標識部分を連結した複合体は、所望のRNAを生体内で可視化するために用いうる。
・特定の疾患に関連した特定のRNAを認識し、結合するPPRタンパク質を作製する。また、特定のRNAに関し、標的配列を解析し、及び付随するタンパク質を解析する。それらの解析結果は、疾患の治療のための化合物の探索に用いうる。
・農作物、林産物、水産物などにおいて、収量や品質を改善する。
・耐病性の向上、環境耐性の向上、向上された又は新たな機能性を有した生物を育種する。
・微生物、培養細胞、植物体、動物体(例えば昆虫体)を利用した有用物質生産において、DNA、RNAの操作により、タンパク発現量を制御する。これにより、有用物質の生産性を向上することができる。有用物質の例は、抗体、ワクチン、酵素等のタンパク質性の物質のほか、医薬品の中間体、香料、色素等の比較的低分子の化合物である。
(モチーフの設計)
まず、PPRモチーフの設計を行った。これまでに報告された人工PPRタンパク質において用いられているPPRモチーフ配列は、様々な方法で抽出した天然界に存在するPPRモチーフ配列のコンセンサス配列が用いられている。それらの中でもdPPR(前掲非特許文献2、3、及び6)のモチーフ配列を用いて作製されたPPRタンパク質が、Kd値が低い(親和性が高い)。このPPRモチーフ配列を以下v1 PPRモチーフとする。
これら設計したPPRモチーフ配列をシームレスに連結するクローニング方法を構築した(図5)。クローニングは、3つのステップで行われる。STEP1では、各モチーフ配列の設計と作製、STEP2では1つもしくは2つのモチーフがクローニングされたプラスミドライブラリーの作製、STEP3で、必要なモチーフ数を連結することで目的のPPR遺伝子が完成する。
P1aの場合は、ggtctcaatac(SEQ ID NO:18)、gtggtgagacc(SEQ ID NO:19)、
P2aの場合は、ggtctcaatac(前掲SEQ ID NO:18)、gtggtcacatatgagacc(SEQ ID NO:20)、
P2bの場合は、ggtctcacatac(SEQ ID NO:21)、gtggtgagacc(前掲SEQ ID NO:19)
の配列をそれぞれ付加した塩基配列を遺伝子合成技術により作製し、pUC57-amp へクローニングした。
Dest-aは、gaagacataaactccgtggtcacATACagagaccaaggtctcaGTGGtcacatacatgtcttc(SEQ ID NO:1)、
Dest-bは、gaagacatATACagagaccaaggtctcaGTGGtgacataatgtcttc(SEQ ID NO:22)、
Dest-cは、gaagacatcATACagagaccaaggtctcaGTGGttacatatgtcttc(SEQ ID NO:23)、
Dest-dは、gaagacatacATACagagaccaaggtctcaGTGGttacaatgtcttc(SEQ ID NO:24)、
Dest-eは、gaagacattacATACagagaccaaggtctcaGTGGtgacatgtcttc(SEQ ID NO:25)、
Dest-fは、gaagacattgacATACagagaccaaggtctcaGTGGttaatgtcttc(SEQ ID NO:26)、
Dest-gは、gaagacatgttacATACagagaccaaggtctcaGTGGtcatgtcttc(SEQ ID NO:27)、
Dest-hは、gaagacatggtcacATACagagaccaaggtctcaGTGGtatgtcttc(SEQ ID NO:28)、
Dest-iは、gaagacattggttacATACagagaccaaggtctcaGTGGatgtcttc(SEQ ID NO:29)、
Dest-jは、gaagacatgtggtgacATACagagaccaaggtctcaGTGGtcttc(SEQ ID NO:30)
を、遺伝子合成技術により作製し、pUC57-kanへcloningした。
一般的に、核酸結合タンパク質と核酸分子との結合評価は、EMSAやBiacoreを用いた方法によって行われる。EMSA (Electrophoretic Mobility Shift Assay)は、タンパク質と核酸が結合したサンプルを電気泳動した際、核酸分子の移動度が結合していない場合と比較して変化する性質を利用する方法である。この方法は精製タンパク質が必要なこと、操作が煩雑なことや、一度に多くのサンプルを解析できない欠点がある。Biacoreに代表される分子間相互作用解析機器は、反応速度論的解析ができるため、詳細なタンパク質-核酸結合解析が可能であるが、こちらも精製タンパク質が必要であり、また特別な装置が必要である。そこで、スループットが高く、短期間でタンパク質と核酸との結合が評価できる方法を考えた。
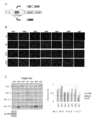
v1又はv2 PPRモチーフを用いて作製したPPRタンパク質のRNA結合性能を評価するため、大腸菌でリコンビナントタンパク質を作製し、RPB-ELISAを用いて結合性能の評価を行った。比較のため5種類の標的配列(T 1、T 2、T 3、T 4、T 5, SEQ ID NOs:46-50)を設定し、それぞれに結合するPPRタンパク質を設計し、それぞれをコードする遺伝子を作製した(v1 PPR1、v1 PPR2、v1 PPR3、v1 PPR4、v1 PPR5、v2 PPR1、v2 PPR2、v2 PPR3、v2 PPR4
v2 PPR5, SEQ ID NOs:35-39, 40-45)。作製したPPR遺伝子のN末側にルシフェラーゼタンパク質遺伝子、C末側にヒスタグ配列を付加し、pET21ベクターへクローニングした(NL v1 PPR1、NL v1 PPR2、NL v1 PPR3、NL v1 PPR4、NL v1 PPR5、NL v2 PPR1、NL v2 PPR2、NL v2 PPR3、NL v2 PPR4、 NL v2 PPR5, SEQ ID NOs:51-60)。PPR発現プラスミドをRosetta(DE3)株へ形質転換した。この大腸菌を、2 mLの100 μg/mLアンピシリン入りLB培地で37℃、12時間培養し、OD600が、0.5から0.8に到達した時に、15℃のインキュベーターに培養液を移し、30分間静置させた。その後、100 μL (終濃度0.1 mM IPTG)を加え、15℃、16時間培養を行った。5,000 x g, 4℃, 10分間遠心によって、大腸菌ペレットを回収し、1.5 mLの溶解バッファー (20 mM Tris-HCl, pH8.0、150 mM NaCl、0.5% NP-40、1 mM MgCl2、2mg/mL リゾチーム、1 mM PMSF、2 μLの10 mg/mL DNase) を加え、-80℃で20分間凍結させた。25℃、30分間浸透しながら細胞の凍結破砕をおこなった。続いて3,700 rpm, 4℃, 15分間遠心操作を行い、可溶性のPPRタンパク質を含む上清(大腸菌ライセート)を回収した。
ことから、v2がv1より親和性も高く、標的に対する特異性が高いことが分かった。
(特異性評価)
v2モチーフを用いて、23種類の標的配列(T 1~3、T 5~T 24, SEQ ID NOs:46-48, 51-69)に対するPPRタンパク質を作製(NL v2 PPR1~3、NL v2 PPR5~24, SEQ ID NOs:56-58, 70-88)し、RPB-ELISAを用いて全ての結合組み合わせを解析した。実験方法は、実施例3と同じである。
さらに、各PPRタンパク質の標的RNAに対する親和性(Kd値)を算出するため、EMSAを行った。先の23種類のうち、10種類のPPRタンパク質をコードする遺伝子配列のN末側にストレプトアビジン結合ペプチド配列、C末側に6xヒスタグ配列を付加し、大腸菌発現プラスミドを構築した(SBP v2 PPR1 HIS, SBP v2 PPR 2 HIS, SBP v2 PPR 3 HIS, SBP v2 PPR6 HIS, SBP v2 PPR9 HIS, SBP v2 PPR12 HIS, SBP v2 PPR15 HIS, SBP v2 PPR16 HIS, SBP v2 PPR20 HIS, SBP v2 PPR24 HIS, SEQ ID NOs:89-97)。Rosetta(DE3)株の大腸菌に形質転換し、2mLの100 μg/mL アンピシリン入りLB培地で37℃一晩培養した。その後,2 mLの培養液を300 mLの100 μg/mL アンピシリン入りLB培地へ移し、OD600が0.5から0.8に達するまで37℃で培養した。培養した培地を15℃に下げた後に、0.1 mMのIPTGを加えさらに12時間培養を行った。5000 x g, 4℃, 10分間、培養液を遠心し菌体を回収し、5 mLの溶解バッファー(20mM Tris-HCl, pH8.0, 150 mM NaCl, 0.5% NP-40, 1mM DTT, and 1 mM EDTA)を加え、Voltexで撹拌したのち、ソニケーションを行い菌体を破砕した。15000 rpm , 4℃, 10分間遠心し、上清を回収した。
さらに、72種類の標的配列(T1~T3、T6~T76, SEQ ID NOs:46-48, 51-69, 117-168)に対するPPRタンパク質をv2モチーフを用いて作製(NL v2 PPR1~3、NL v2 PPR6~76, SEQ ID NOs:56-58, 70-88, 169-220)し、RPB-ELISAを用いて構築成功確率を算出した。標的配列を含むビオチン化RNAプローブ(RNA 1~3,RNA 6~76, SEQ ID NOs:61~63, 98~116, 221~272)と標的しない配列(T 51, SEQ ID NO:143)を含むビオチン化RNAプローブ(RNA51, SEQ ID NO:247)を作製した(Greinar)。実験方法は、実施例3と同じである。その結果を図11に示す。
PPRモチーフ数と標的結合活性に関して解析を行った。13種類の18塩基の標的配列を設定し、その配列の5'側3塩基、6塩基をそれぞれ削り15塩基(T 1a、T 49a、T 3a、T 14a、T 40a、T 12a、T 13a、T 2a、T 38a、T 37a、T 39a、T 56a、T 68a, SEQ ID NOs, 273, 275, 277, 279, 281, 283, 285, 287, 289, 291, 293, 395, 297)、12塩基(T 1b、T 49b、T 3b、T 14b、T 40b、T 12b、T 13b、T 2b、T 38b、T 37b、T 39b、T 56b、T 68b, SEQ ID NOs: 274, 276, 278, 280, 282, 284, 286, 288, 290, 292, 294, 296, 298)の標的配列を設定した。それらに対応するPPRタンパク質(15モチーフは、PPRxa、12モチーフは、PPRxbと名付けた)を作製した(NL v2 PPR1, 1a, 1b; NL v2 PPR49, 49a, 49b; NL v2 PPR3, 3a, 3b; NL v2 PPR14, 14a, 14b; NL v2 PPR40, 40a, 40b; NL v2 PPR12, 12a, 12b; NL v2 PPR13, 13a, 13b; NL v2 PPR2, 2a, 2b; NL v2 PPR38, 38a, 38b; NL v2 PPR37, 37a, 37b; NL v2 PPR39, 39a, 39b; NL v2 PPR56, 56a, 56b; NL v2 PPR68, 68a, 68b; SEQ ID NOs:56, 299-324)。RPB-ELISAによる解析を行うために、標的配列を含むビオチン化RNAプローブ(T 1、T 49、T 3、T 14、T 40、T 12、T 13、T 2、T 38、T 37、T 39、T 56、T 68)と、標的しない配列(T 51, SEQ ID NO:143)を含むビオチン化RNAプローブ(RNA 51, SEQ ID NO:247)を作製し、標的(on target)、非標的(off target)とそれぞれのPPRタンパク質との結合活性をRPB-ELISAで解析した。
PPRタンパク質が細胞内で標的RNA分子に結合し、目的とするRNA操作ができることを示すため、スプライシングレポーターを利用した実験を行った(図13A)。スプライシングレポーター(RG6)は、エクソン1、イントロン1、エクソン2,イントロン2、エクソン3といった遺伝子構造をとっている(Orengo et al., 2006 NAR)。イントロン1、エクソン2及びイントロン2には、チキンcTNTのイントロン4、イントロン5及び、人工的に作製されたオルタナティブエクソン配列が挿入されている。本レポーターは、2つのスプライシングフォームを有しており、エクソン2がスキップしたmRNA、スキップしないmRNAの量比が1:1程度になっている。また、エクソン3には、RFPとGFP遺伝子がコードされているが、エクソン2の存在、非存在により読み枠が変わることで、エクソン2がスキップしたmRNAではRFPが発現し、スキップしないmRNAではGFPが発現する。このレポーターのスプライシングフォームの量は、イントロン1,エクソン2,イントロン2の領域に結合するスプライシング因子により制御されていることが知られている(Orengo et al., 2006 NAR)。そこで、イントロン1,エクソン2,イントロン2の領域の中から18塩基の配列を選択し、それらに結合するPPRタンパク質によって、RG-6レポーターのスプライシングフォームを変化させられるか実験を行った。
V2モチーフを用いたPPRタンパク質(塩基配列はSEQ ID NO:457、アミノ酸配列はSEQ ID NO:458)と、v3.2モチーフを用いたPPRタンパク質(塩基配列はSEQ ID NO:459、アミノ酸配列はSEQ ID NO:460)それぞれを大腸菌発現系で作成し精製し、ゲルろ過クロマトグラフィーで分離した。
目的のPPRタンパク質をコードしたDNA配列を含むpE-SUMOpro Kanプラスミドを用いて、大腸菌Rosetta株を形質転換し、37度で培養後、OD600が0.6に達した時に20度に温度を下げ、終濃度0.5mMになるようにIPTGを加え、目的PPRタンパク質をSUMO融合タンパクつとして、大腸菌内で発現させた。1晩、培養後、菌体を遠心よって集菌し、Lysis Buffer (50mM Tris-HCl pH8.0, 500mM NaCl)で再懸濁した。超音波破砕によって、大腸菌を破砕し、17000g, 30minの遠心後、上清画分をNi-Agaroseカラムに供与し、20mM imidazoleを含むLysis Bufferでカラム洗浄後、400mM imidazoleを含むLysis Bufferで、SUMO融合目的PPRタンパク質を溶出させた。溶出後、Ulp1によるSUMOタンパク質を目的PPRタンパク質から切り離すと同時に、透析により、イオン交換Buffer(50mM Tris-Hcl pH8.0, 200mM NaCl)にタンパク溶液を置換した。その後、SPカラムを用いた陽イオン交換クロマトグラフィーを行った。カラム供与後、NaCl濃度を200mMから1Mまで徐々に上げることによって、タンパク質を溶出させた。目的PPRタンパク質を含む画分をSuperdex200カラムを用いたゲルろ過クロマトグラフィーによって最終精製を行った。 ゲルろ過Buffer(25mM HEPES pH7.5, 200mM NaCl, 0.5mM tris(2-carboxyethyl)phosphine (TCEP))で平衡化したゲルろ過カラムに、イオン交換から溶出した目的PPRタンパク質を供与した。最後に目的PPRタンパク質を含む画分を濃縮し、液体窒素で凍結し、次の分析に使用するまで-80度で保存した。
精製したリコンビナントPPRタンパク質を濃度1mg/mlに調整した。ゲルろ過クロマトグラフィーは、Superdex 200 increase 10/300 GL (GE Helthcare)を用いた。25mM HEPES pH7.5, 200mM NaCl, 0.5mM tris(2-carboxyethyl)phosphine (TCEP)で平衡化したゲルろ過カラムに、調整したタンパク質を供与し、ゲルろ過カラムより溶出してくる溶液を280nmの吸光度を測定することにより、タンパク質の性質を分析した。
結果を図14に示す。溶出画分(Elution vol.)が少ないほど分子サイズが大きい。V2では、8から10mLの溶出画分で溶出された一方で、v3.2では、12から14mLの溶出画分にピークが見られた。このことから、v2では、タンパク質サイズが大きくなっていることから凝集している可能性が示唆され、その凝集はv3.2において改善されていることが分かった。
Claims (14)
- 下記のいずれか1つの、PPRモチーフ:
(A-1)配列番号:9の配列からなるPPRモチーフ、又は配列番号:9の配列において、位置10のアミノ酸のチロシンへの置換、位置15のアミノ酸のリジンへの置換、位置16のアミノ酸のロイシンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置18のアミノ酸のアスパラギン酸への置換、及び位置28のアミノ酸のグルタミン酸への置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ、又は配列番号401の配列からなるPPRモチーフ、又は配列番号401の配列において、位置10のアミノ酸のチロシンへの置換、位置16のアミノ酸のロイシンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置18のアミノ酸のアスパラギン酸への置換、及び位置28のアミノ酸のグルタミン酸への置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
;
(A-2)配列番号:9又は401の配列において、位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~20個を置換、欠失、又は付加した配列からなり、かつアデニン結合性であるPPRモチーフ;
(A-3)配列番号:9又は401の配列と少なくとも42%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつアデニン結合性であるPPRモチーフ;
(C-1)配列番号:10の配列からなるPPRモチーフ、又は配列番号:10の配列において、位置2のアミノ酸のセリンへの置換、位置5のアミノ酸のイソロイシンへの置換、位置7のアミノ酸のロイシンへの置換、位置8のアミノ酸のリジンへの置換、位置10のアミノ酸のフェニルアラニン又はチロシンへの置換、位置15のアミノ酸のアルギニンへの置換、位置22のアミノ酸のバリンへの置換、位置24のアミノ酸のアルギニンへの置換、位置27のアミノ酸のロイシンへの置換、及び位置29のアミノ酸のアルギニンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(C-2)配列番号:10の配列において、位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~25個を置換、欠失、又は付加した配列からなり、かつシトシン結合性であるPPRモチーフ;
(C-3)配列番号:10の配列と少なくとも25%の配列同一性を有し、ただし位置1、3、4、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつシトシン結合性であるPPRモチーフ;
(G-1)配列番号:11の配列からなるPPRモチーフ、又は配列番号:11の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置15のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のバリンの置換、位置28のアミノ酸のセリンへの置換、及び位置35のアミノ酸のイソロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ;
(G-2)配列番号:11の配列において、位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~21個を置換、欠失、又は付加した配列からなり、かつグアニン結合性であるPPRモチーフ;
(G-3)配列番号:11の配列と少なくとも40%の配列同一性を有し、ただし位置1、2、3、4、6、7、9、14、18、19、26、30、33、及び34のアミノ酸は同一であり、かつグアニン結合性であるPPRモチーフ;
(U-1)配列番号:12の配列からなるPPRモチーフ、又は配列番号:12の配列において、位置10のアミノ酸のフェニルアラニンへの置換、位置13のアミノ酸のセリンへの置換、位置15のアミノ酸のリジンへの置換、位置17のアミノ酸のグルタミン酸への置換、位置20のアミノ酸のロイシンへの置換、位置21のアミノ酸のリジンへの置換、位置23のアミノ酸のフェニルアラニンへの置換、位置24のアミノ酸のアスパラギン酸への置換、位置27のアミノ酸のリジンへの置換、位置28のアミノ酸のリジンへの置換、位置29のアミノ酸のアルギニンへの置換、及び位置31のアミノ酸のロイシンへの置換からなる群より選択されるいずれかの置換を行ったアミノ酸配列からなるPPRモチーフ
(U-2)配列番号:12の配列において、位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸以外のアミノ酸の1~22個を置換、欠失、又は付加した配列からなり、かつウラシル結合性であるPPRモチーフ;
(U-3)配列番号:12の配列と少なくとも37%の配列同一性を有し、ただし位置1、2、3、4、6、11、12、14、19、26、30、33、及び34のアミノ酸は同一であり、かつウラシル結合性であるPPRモチーフ。 - 請求項1に記載のPPRモチーフの、標的RNAが15塩基長以上であるPPRタンパク質の作製のための使用。
- 請求項1に記載のPPRモチーフのPPRタンパク質の作製のための使用であって、PPRタンパク質の標的RNAへの結合性能を高めるための使用。
- n個の塩基配列からなる標的RNAに結合可能な、n個のPPRモチーフを含むタンパク質であって、
該塩基配列中のアデニンに対するPPRモチーフが、請求項1に定義した(A-1)、(A-2)、又は(A-3)のPPRモチーフであり;
該塩基配列中のシトシンに対するPPRモチーフが、請求項1に定義した(C-1)、(C-2)、又は(c-3)のPPRモチーフであり;
該塩基配列中のグアニンに対するPPRモチーフが、請求項1に定義した(G-1)、(G-2)、又は(G-3)のPPRモチーフであり;
該塩基配列中のウラシルに対するPPRモチーフが、請求項1に定義した(U-1)、(U-2)、又は(U-3)のPPRモチーフである、PPRタンパク質。 - nが、15以上である、請求項4に記載のタンパク質。
- N末端から1番目のPPRモチーフが下記のいずれか1つである、請求項4又は5に記載のタンパク質:
(1st A-1)配列番号:402の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換したPPRモチーフ;
(1st A-2)(1st A-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつアデニン結合性であるPPRモチーフ;
(1st A-3)(1st A-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつアデニン結合性であるPPRモチーフ;
(1st C-1)配列番号:403の配列からなるPPRモチーフ;
(1st C-2)(1st C-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつシトシン結合性であるPPRモチーフ;
(1st C-3)(1st C-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつシトシン結合性であるPPRモチーフ;
(1st G-1)配列番号:404の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換した配列からなるPPRモチーフ;
(1st G-2)(1st G-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつグアニン結合性であるPPRモチーフ;
(1st G-3)(1st G-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつグアニン結合性であるPPRモチーフ;
(1st U-1)配列番号:405の配列において、位置6及び9のアミノ酸を、下記に定義した組み合わせのいずれか1つを満たすように置換した配列からなるPPRモチーフ;
(1st U-2)(1st U-1)の配列において、位置1、4、6、9、及び34のアミノ酸以外のアミノ酸の1~9個を置換、欠失、又は付加した配列からなり、かつウラシル結合性であるPPRモチーフ;
(1st U-3)(1st U-1)の配列と少なくとも80%の配列同一性を有し、ただし位置1、4、6、9、及び34のアミノ酸は同一であり、かつウラシル結合性であるPPRモチーフ。
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がグルタミン酸である組み合わせ
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がグルタミンである組み合わせ
・位置6のアミノ酸がアスパラギンであり、かつ位置9のアミノ酸がリジンである組み合わせ
・位置6のアミノ酸アスパラギン酸であり、かつ位置9アミノ酸がグリシンである組み合わせ - 請求項4~6のいずれか1項に記載のタンパク質を用いることを特徴とする、RNAスプライシングの制御方法。
- 請求項4~6のいずれか1項に記載のタンパク質を用いることを特徴とする、RNAの検出方法。
- 蛍光タンパク質、核移行シグナルペプチド、及びタグタンパク質からなる群より選択される少なくとも一つと、請求項4~6のいずれか1項に記載のタンパク質との、融合タンパク質。
- 請求項1に記載のPPRモチーフ、又は請求項4~6のいずれか1項に記載のタンパク質をコードする核酸。
- 請求項10に記載の核酸を含む、ベクター。
- 請求項11に記載のベクターを含む、細胞(ヒト個体は除く。)。
- 請求項1に記載のPPRモチーフ、請求項4~6のいずれか1項に記載のタンパク質、又は請求項11に記載のベクターを用いる、RNAの操作方法(ヒト個体での実施を除く。)。
- 請求項13に記載の操作方法を含む、生物の生産方法。
Priority Applications (11)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20815305.6A EP3978513A4 (en) | 2019-05-29 | 2020-05-29 | Efficient ppr protein production method and use thereof |
| CN202080039706.2A CN114729017A (zh) | 2019-05-29 | 2020-05-29 | Ppr蛋白的有效制作方法及其应用 |
| AU2020283177A AU2020283177A1 (en) | 2019-05-29 | 2020-05-29 | Efficient method for preparing ppr protein and use of the same |
| BR112021023878A BR112021023878A2 (pt) | 2019-05-29 | 2020-05-29 | Motivo ppr, uso do motivo, proteína ppr, método para controlar o entrançamento de rna, método para detectar rna, proteína de fusão, ácido nucleico, vetor, célula, método para manipular rna, e, método para produzir um organismo |
| KR1020217040377A KR20220023985A (ko) | 2019-05-29 | 2020-05-29 | 효율적인 피피알 단백질의 작제방법 및 그의 이용 |
| SG11202113055UA SG11202113055UA (en) | 2019-05-29 | 2020-05-29 | Efficient method for preparing ppr protein and use of the same |
| CA3142299A CA3142299A1 (en) | 2019-05-29 | 2020-05-29 | Efficient method for preparing ppr protein and use of the same |
| JP2021521907A JPWO2020241876A1 (ja) | 2019-05-29 | 2020-05-29 | |
| US17/614,231 US20220289795A1 (en) | 2019-05-29 | 2020-05-29 | Efficient method for preparing ppr protein and use of the same |
| IL288426A IL288426A (en) | 2019-05-29 | 2021-11-25 | An effective method for preparing ppr protein and using it |
| JP2023126196A JP2023145672A (ja) | 2019-05-29 | 2023-08-02 | 効率的なpprタンパク質の作製方法及びその利用 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019100551 | 2019-05-29 | ||
| JP2019-100551 | 2019-05-29 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2020241876A1 true WO2020241876A1 (ja) | 2020-12-03 |
Family
ID=73553200
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/021472 WO2020241876A1 (ja) | 2019-05-29 | 2020-05-29 | 効率的なpprタンパク質の作製方法及びその利用 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20220289795A1 (ja) |
| EP (1) | EP3978513A4 (ja) |
| JP (2) | JPWO2020241876A1 (ja) |
| KR (1) | KR20220023985A (ja) |
| CN (1) | CN114729017A (ja) |
| AU (1) | AU2020283177A1 (ja) |
| BR (1) | BR112021023878A2 (ja) |
| CA (1) | CA3142299A1 (ja) |
| IL (1) | IL288426A (ja) |
| SG (1) | SG11202113055UA (ja) |
| WO (1) | WO2020241876A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3142303A1 (en) * | 2019-05-29 | 2020-12-03 | Editforce, Inc. | Ppr protein causing less aggregation and use of the same |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011111829A1 (ja) * | 2010-03-11 | 2011-09-15 | 国立大学法人九州大学 | Pprモチーフを利用したrna結合性蛋白質の改変方法 |
| WO2013058404A1 (ja) | 2011-10-21 | 2013-04-25 | 国立大学法人九州大学 | Pprモチーフを利用したrna結合性蛋白質の設計方法及びその利用 |
| WO2014175284A1 (ja) | 2013-04-22 | 2014-10-30 | 国立大学法人九州大学 | Pprモチーフを利用したdna結合性タンパク質およびその利用 |
| WO2017209122A1 (ja) | 2016-06-03 | 2017-12-07 | 国立大学法人九州大学 | 標的mRNAからのタンパク質発現量を向上させるための融合タンパク質 |
| WO2018030488A1 (ja) * | 2016-08-10 | 2018-02-15 | 和光純薬工業株式会社 | Pprモチーフを利用したdna結合性タンパク質およびその利用 |
| WO2019232588A1 (en) * | 2018-06-06 | 2019-12-12 | The University Of Western Australia | Proteins and their use for nucleotide binding |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003006622A2 (en) * | 2001-07-12 | 2003-01-23 | Mcgill University | Nuclear fertility restorer genes and methods of use in plants |
-
2020
- 2020-05-29 AU AU2020283177A patent/AU2020283177A1/en active Pending
- 2020-05-29 JP JP2021521907A patent/JPWO2020241876A1/ja active Pending
- 2020-05-29 BR BR112021023878A patent/BR112021023878A2/pt unknown
- 2020-05-29 SG SG11202113055UA patent/SG11202113055UA/en unknown
- 2020-05-29 CA CA3142299A patent/CA3142299A1/en active Pending
- 2020-05-29 CN CN202080039706.2A patent/CN114729017A/zh active Pending
- 2020-05-29 KR KR1020217040377A patent/KR20220023985A/ko active Search and Examination
- 2020-05-29 EP EP20815305.6A patent/EP3978513A4/en active Pending
- 2020-05-29 WO PCT/JP2020/021472 patent/WO2020241876A1/ja unknown
- 2020-05-29 US US17/614,231 patent/US20220289795A1/en active Pending
-
2021
- 2021-11-25 IL IL288426A patent/IL288426A/en unknown
-
2023
- 2023-08-02 JP JP2023126196A patent/JP2023145672A/ja active Pending
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011111829A1 (ja) * | 2010-03-11 | 2011-09-15 | 国立大学法人九州大学 | Pprモチーフを利用したrna結合性蛋白質の改変方法 |
| WO2013058404A1 (ja) | 2011-10-21 | 2013-04-25 | 国立大学法人九州大学 | Pprモチーフを利用したrna結合性蛋白質の設計方法及びその利用 |
| WO2014175284A1 (ja) | 2013-04-22 | 2014-10-30 | 国立大学法人九州大学 | Pprモチーフを利用したdna結合性タンパク質およびその利用 |
| WO2017209122A1 (ja) | 2016-06-03 | 2017-12-07 | 国立大学法人九州大学 | 標的mRNAからのタンパク質発現量を向上させるための融合タンパク質 |
| WO2018030488A1 (ja) * | 2016-08-10 | 2018-02-15 | 和光純薬工業株式会社 | Pprモチーフを利用したdna結合性タンパク質およびその利用 |
| WO2019232588A1 (en) * | 2018-06-06 | 2019-12-12 | The University Of Western Australia | Proteins and their use for nucleotide binding |
Non-Patent Citations (15)
| Title |
|---|
| ALTSCHUL ET AL., J. MOL. BIOL., vol. 215, 1990, pages 403 - 410 |
| COQUILLE, S ET AL.: "An artificial PPR scaffold for programmable RNA recognition", NATURE COMMUNICATIONS, vol. 5, 2014 |
| DATABASE UniProt KB UniProt; 10 April 2019 (2019-04-10), "SubName: Full=Uncharacterized protein {ECO:0000313|EMBL:PIA53975.1};", XP055769830, Database accession no. A0A2G5EDW6 * |
| DATABASE UniProtKB UniProt; 10 April 2019 (2019-04-10), "SubName: Full=Pentatricopeptide repeat {ECO:0000313|EMBL:OVA05176.1};", XP055769857, Database accession no. A0A200Q3Y9 * |
| DATABASE UniProtKB UniProt; 10 April 2019 (2019-04-10), "SubName: Full=Uncharacterized protein {ECO:0000313|EMBL:ERN18345.1};", XP055769838, Database accession no. U5D7X0 * |
| DATABASE UniProtKB UniProt; 16 January 2019 (2019-01-16), "SubName: Full=Uncharacterized protein {ECO:0000313|EMBL:OWM76000.1};", XP055769853, Database accession no. A0A218WUG1 * |
| DATABASE UniProtKB UniProt; 16 January 2019 (2019-01-16), "SubName: Full=Uncharacterized protein {ECO:0000313|EnsemblPlants:GSMUA_Achr8P04810_001};", XP055769851, Database accession no. M0TMN4 * |
| DATABASE UniProtKB UniProt; 8 May 2019 (2019-05-08), "SubName: Full=LOW QUALITY PROTEIN: pentatricopeptide repeat-containing protein At5g61990, mitochondrial-like {ECO:0000313|RefSeq:XP_008790694.3};", XP055769847, Database accession no. A0A2H3XYK4 * |
| GULLY, B.S. ET AL.: "The design and structural characterization of a synthetic pentatricopeptide repeat protein", ACTA CRYST., vol. D71, 2015, pages 196 - 208 |
| JUNJIE YAN, YINYING YAO, SIXING HONG, YAN YANG, CUICUI SHEN, QUNXIA ZHANG, DELIN ZHANG, TINGTING ZOU, PING YIN: "Delineation of pentatricopeptide repeat codes for target RNA prediction", NUCLEIC ACIDS RESEARCH, vol. 47, no. 7, 11 February 2019 (2019-02-11), pages 3728 - 3738, XP055769935, DOI: 10.1093/nar/gkz075 * |
| MIRANDA, R.G. ET AL.: "RNA-binding specificity landscapes of designer pentatricopeptide repeat proteins elucidate principles of PPR-RNA interactions", NUCLEIC ACIDS RESEARCH, vol. 46, no. 5, 2018, pages 2613 - 2623 |
| SHEN, C ET AL.: "Specific RNA Recognition by Designer Pentatricopeptide Repeat Protein", MOLECULAR PLANT, vol. 8, 2015, pages 667 - 670 |
| SHEN, C ET AL.: "Structural basis for specific single-stranded RNA recognition by designer pentatricopeptide repeat proteins", NATURE COMMUNICATIONS, vol. 7, 2016, XP055768010 |
| TRINH, T. ET AL.: "An Escherichia coli strain for the stable propagation of retroviral clones and direct repeat sequences", FOCUS, vol. 16, 1994, pages 78 - 80 |
| YAN, J ET AL.: "Delineation of pentatricopeptide repeat codes for target RNA prediction", NUCLEIC ACIDS RESEARCH, 2019, pages gkz075 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2023145672A (ja) | 2023-10-11 |
| BR112021023878A2 (pt) | 2022-01-25 |
| JPWO2020241876A1 (ja) | 2020-12-03 |
| EP3978513A4 (en) | 2023-06-28 |
| US20220289795A1 (en) | 2022-09-15 |
| IL288426A (en) | 2022-01-01 |
| EP3978513A1 (en) | 2022-04-06 |
| KR20220023985A (ko) | 2022-03-03 |
| AU2020283177A1 (en) | 2022-01-06 |
| CA3142299A1 (en) | 2020-12-03 |
| SG11202113055UA (en) | 2021-12-30 |
| CN114729017A (zh) | 2022-07-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4262778B2 (ja) | 生体分子相互作用を検出するためのタンパク質断片相補性アッセイ | |
| JP6889758B2 (ja) | 植物シスタチンに由来する足場タンパク質 | |
| US20130273553A9 (en) | Stabilization of cyclic peptide structures | |
| Ozaki et al. | A replicase clamp-binding dynamin-like protein promotes colocalization of nascent DNA strands and equipartitioning of chromosomes in E. coli | |
| Dubin et al. | A versatile set of tagged expression vectors to monitor protein localisation and function in Dictyostelium | |
| JP2023145672A (ja) | 効率的なpprタンパク質の作製方法及びその利用 | |
| JP2023537158A (ja) | Krab融合抑制因子並びに遺伝子発現を抑制する方法及び組成物 | |
| Oberholzer et al. | Approaches for functional analysis of flagellar proteins in African trypanosomes | |
| JP2023036848A (ja) | 凝集の少ないpprタンパク質及びその利用 | |
| JP5804520B2 (ja) | 核酸構築物、それを用いた複合体の製造方法およびスクリーニング方法 | |
| WO2020045281A1 (ja) | 新規ヌクレアーゼドメインおよびその利用 | |
| Hoepflinger et al. | Molecular analysis and localization of CaARA7 a conventional RAB5 GTPase from characean algae | |
| KR20080113247A (ko) | 단백질 가용화를 위한 단백질 s 융합물의 용도 | |
| US10370776B2 (en) | Antibody like protein | |
| WO2012082069A1 (en) | Protein aptamers based on unstructured scaffold proteins | |
| Wollschläger et al. | Single‐molecule experiments to elucidate the minimal requirement for DNA recognition by transcription factor epitopes | |
| US10870926B2 (en) | Antibody like protein | |
| JP4478772B2 (ja) | c−Fos蛋白質と複合体を形成する蛋白質、及び、それをコードする核酸、ならびに、それらの利用方法 | |
| Valencia‐Burton et al. | Visualization of RNA Using Fluorescence Complementation Triggered by Aptamer‐Protein Interactions (RFAP) in Live Bacterial Cells | |
| Barreto | A genetic screen to isolate “lariat” peptide inhibitors of protein function | |
| WO2012135500A1 (en) | Engineered thioredoxin-like fold proteins | |
| Sander | Protein folding in the cell is modulated by the translating ribosome | |
| JPWO2013046960A1 (ja) | ペプチド抗体のスクリーニングに使用する核酸構築物およびそれを用いたスクリーニング方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20815305 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2021521907 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 3142299 Country of ref document: CA |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112021023878 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 2020283177 Country of ref document: AU Date of ref document: 20200529 Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 112021023878 Country of ref document: BR Kind code of ref document: A2 Effective date: 20211126 |
|
| ENP | Entry into the national phase |
Ref document number: 2020815305 Country of ref document: EP Effective date: 20220103 |