WO2017006932A1 - 損傷末梢神経治療用組成物 - Google Patents
損傷末梢神経治療用組成物 Download PDFInfo
- Publication number
- WO2017006932A1 WO2017006932A1 PCT/JP2016/069900 JP2016069900W WO2017006932A1 WO 2017006932 A1 WO2017006932 A1 WO 2017006932A1 JP 2016069900 W JP2016069900 W JP 2016069900W WO 2017006932 A1 WO2017006932 A1 WO 2017006932A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- nerve
- sugar
- composition
- glca
- glcnac
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7008—Compounds having an amino group directly attached to a carbon atom of the saccharide radical, e.g. D-galactosamine, ranimustine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7012—Compounds having a free or esterified carboxyl group attached, directly or through a carbon chain, to a carbon atom of the saccharide radical, e.g. glucuronic acid, neuraminic acid
Abstract
本発明は、神経損傷時に正常な神経再生を促し、その結果、神経腫の発生自体を抑制することで、続発する難治性の神経障害性疼痛の発生を防止する損傷末梢神経治療用組成物に関する。また、本発明は、脂質が結合していないGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を0.01w/v%以上の濃度で含有し、末梢神経損傷治療に用いられることを特徴とする損傷した末梢神経を治療するための組成物に関する。
Description
本発明は、神経損傷時に局所に作用させることにより、健全な神経再生を促し、その結果、神経腫の発生自体を抑制することで、難治性の神経障害性疼痛の発生を防止し、鈍化または喪失した感覚の回復を促進させる損傷末梢神経治療用組成物に関する。
外傷や手術等により損傷した神経は、その損傷局所が瘢痕化することにより、神経腫の形成を誘導し、その結果難治性の神経障害性疼痛を生じさせることがある。この神経腫は一般的に損傷した神経の修復を阻害し(非特許文献1)、感覚の鈍化または喪失といった病態を形成するだけでなく、神経障害性疼痛を引き起こすことが知られている。そのため、患者の日常運動が大きく阻害されQOLは大幅に低下する。また、本疾患はさまざまな治療は行われているが、未だ有効な方法が認められていないことから、患者は長期間の苦痛を強いられることになる。
下歯槽神経は三叉神経第3枝であり、下顎の歯や歯肉、下口唇やオトガイ部の感覚を支配している。本神経は下顎管という硬い骨皮質で覆われた管腔構造内を走行しているため、一般的には外傷を受けにくい。しかし、一般歯科診療や口腔外科で行われている抜歯や嚢胞摘出術、インプラント埋入術等の口腔外科手術で、損傷されることが少なくない。神経が損傷されると口唇やオトガイ部の感覚は鈍くなり、また異常な痛みや頑固な痺れが発生することがある。その結果、会話、食事など日常生活に支障をきたすため、患者にとっては大きな問題となっている。しかし、現時点では抜歯などの処置時に神経が露出していることを確認できても適切な治療法がない。そのため、術者は損傷にたいして放置するしかなく、その結果多くの症例で術後は損傷し再生しようとする神経は瘢痕化してしまう。結果として神経腫を形成し、回復困難な知覚低下や痺れの後遺症が生じてしまうのが現状である。また、現在多くの歯科医療訴訟はこれらによるものである。
一方、神経腫の形成が難治性の疼痛を誘発するメカニズムは、未だ解明されていない。そのため、この疼痛に対する有効な予防法及び治療法は確立されていない。従って、患者は積極的な治療は勿論のこと、レントゲンなどによる現在に一般的な歯科医療では発見が出来ないことから、医師から病変の存在自体を認められないまま苦しみ続けている場合が少なくない。したがって最も重要なのは予防することである。
非特許文献2によると、従来から外科的に神経腫を切除し、その断端を直接又は採取した自家神経を介して接続することで、損傷した神経を治療する方法が実施されてきた。また、非特許文献3によると、中腔をコラーゲンで満たしたポリグリコール酸線維で作られたチューブ状の人工神経を用いて、外科的に切除した神経腫の切断端を接続することで、損傷した神経を治療する試みが注目されている。
しかしながら、外科的療法の問題点として、神経腫の切除や神経の再生は全身麻酔下で行わなければならず、身体的・経済的負担が大きい。また、神経再生術は術後に再生痛という特殊な痛みが出ることが知られており、感覚はある程度回復するものの長期間を要する。また自家神経採取では採取部位の感覚異常などの合併症のリスクもある。以上より、外科的療法は、患者にとって後戻りのできない選択肢となるため、適応は限定されてしまう課題がある。
以上より多くの症例で、抜歯等の神経が損傷した直後であれば、損傷した部位に直接アプローチすることは容易である。損傷した神経に対し、直接何らかの適切な処置を施すことができれば、神経腫の発生自体を効果的に防止でき、また神経障害性疼痛による患者の負担をなくすことができると考えられる。
Neuroreport. 2006 Aug 21;17(12):1245-9.
新潟歯学会雑誌 44(2):69-81 2014
Pain Clinic, 29;452-458, 2008
本発明は、神経損傷時に正常な神経再生を促し、その結果、神経腫の発生自体を抑制することで、続発する難治性の神経障害性疼痛の発生を防止する、損傷末梢神経治療用組成物を提供することを目的とする。
本発明者らは、N-アセチルグルコサミン(GlcNAc)及び/又はD-グルクロン酸(GlcA)を少なくとも構成糖とする糖又はその塩を用いて、正常な神経再生を促し、その結果、神経腫の発生自体を抑制することで、神経障害性疼痛の発生を防止する損傷末梢神経治療用組成物に関する研究を鋭意行った。下歯槽神経を切断した動物モデルにて神経腫発生抑制効果を評価したところ、対照として生理食塩水を投与した群では神経再生部位には明らかな神経腫の形成を認めた。一方、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を投与した群では驚くべきことに、対照と比較して、神経腫の形成を著明に抑制し、損傷した神経の再生を促進することを初めて見出した。更に驚くべきことに、この神経腫形成抑制効果にはGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の濃度依存性があることを見出した。また、この神経腫形成抑制効果にはGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の粘度平均分子量及び/又は粘度とも高い相関関係を示すことが明らかとなった。この知見を基に、神経損傷時に正常な神経再生を促し、その結果、神経腫の発生自体を抑制することで神経障害性疼痛の発生を防止し、損傷した末梢神経に対する治療効果を飛躍的に向上させた組成物として、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を含有することを特徴とする、損傷末梢神経治療用組成物を見出し、本発明を完成させた。
すなわち、本発明によれば、脂質が結合していないGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を0.01w/v%以上の濃度で含有することを特徴とする、損傷した末梢神経を治療するための組成物が提供される。先行技術と比べ、神経損傷時に正常な神経再生を促し、その結果、神経損傷時に神経腫の発生自体を抑制するため、神経障害性疼痛の発生を防止し、損傷した神経を再生・修復する効果が期待できる。またGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を0.01w/v%以上の濃度で含有することで、神経腫の形成抑制及び神経障害性疼痛の発生防止効果が向上する。また別に、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の粘度平均分子量が100万超とすることでも、神経腫の形成抑制及び神経障害性疼痛の発生防止効果が向上する。更にGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩が、末梢神経損傷に対する治療に用いられることを特徴とする。
以下、本発明の好適な実施の形態について説明する。なお、同様の内容については繰り返しの煩雑さをさけるために、摘示説明を省略している。
本発明の一実施形態は、脂質が結合していないGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を0.01w/v%以上の濃度で含有することを特徴とする、損傷した末梢神経を治療するための組成物である。このような組成物は、神経損傷局部に滴下又は塗布することで、後述する実施例で実証されているように高い治療効果が得られる。
本願明細書において、上記「糖」は、GlcNAcを構成糖とする糖であってもよく、GlcAを構成糖とする糖であってもよく、GlcNAc及びGlcAを構成糖とする糖であってよい。好ましくは、GlcNAc及びGlcAを構成糖とする糖である。構成糖は、互いにグリコシド結合することによって、分子量が100万を超える巨大な分子を構成することが可能になる。GlcNAc及び/又はGlcAを少なくとも構成糖とする糖としては、例えば、ヒアルロン酸を挙げることができる。
本願明細書において、用語「脂質が結合していない」とは、脂質がGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩と共有結合していないことを指す。「脂質」には、ホスファチジルエタノールアミン、ホスファチジルセリン、ホスファチジルトレオニン、エタノールアミンプラスマロゲン、セリンプラスマロゲン、リゾホスファチジルコリン、リゾホスファチジルイノシトール等のリン脂質、モノアシルグリセロール、ジアシルグリセロール等の中性脂質等のグリセロ脂質、長鎖の脂肪酸、長鎖の脂肪族アミン、コレステロール類、スフィンゴシン、セラミドが含まれるが、これらに限定されるものではない。なお、脂質結合は、意図的に実施された脂質結合を意味するものであり、例えば、合成の過程、精製の過程及び/又は他の物質との混合過程(希釈過程を含む)において、意図せずに生じた脂質結合は含まれない。
脂質結合には、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩のカルボキシル基(ラクトンを含む)、ホルミル基もしくは水酸基、又はGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩に別途導入された前記基と、脂質のカルボキシル基、ホルミル基もしくは1級アミノ基、又は脂質に別途導入された前記基との間で形成される酸アミド結合(-CO-NH-)、エステル結合又はアミノアルキル結合(-CH2-NH-)による共有結合が含まれる。
別の実施形態としては、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の粘度平均分子量が100万以上であることを特徴とする、損傷した末梢神経治療するための組成物である。このような組成物は、より高い治療効果を示すことができる。本明細書において、高い治療効果とは、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を投与しない例と比較して、神経の損傷箇所の瘢痕化を防止若しくは抑制すること、神経腫の形成が小さいこと、神経再生が促進されること、難治性の神経障害性疼痛の発生を防止すること、鈍化若しくは喪失した感覚の回復を促進させること、及び/又は、骨を修復させることをいう。
本明細書における損傷した末梢神経を治療するための組成物は、後述の実施例に示すように末梢神経損傷時に正常な神経再生を促し、その結果、神経損傷時に神経腫の発生自体を抑制することができる。本明細書における損傷した末梢神経を治療するための組成物は、社会保険診療報酬支払基金の傷病名マスターに記載の、腋窩神経損傷、オトガイ神経損傷、下肢神経損傷、下歯槽神経損傷、下肢皮膚知覚神経損傷、下腿神経損傷、下腿皮膚知覚神経損傷、滑車神経損傷、下腹神経叢損傷、外傷性滑車神経損傷、外傷性外転神経損傷、外傷性顔面神経損傷、外傷性嗅神経損傷、外傷性三叉神経損傷、外傷性視神経損傷、外傷性聴神経損傷、外傷性動眼神経損傷、外傷性脳神経損傷、外側足底神経損傷、外転神経損傷、顔面神経損傷、嗅神経損傷、胸椎神経根損傷、胸部交感神経損傷、胸部末梢神経損傷、筋皮神経損傷、脛骨神経損傷、頚椎神経根損傷、頚部交感神経損傷、頚部神経損傷、頚部末梢神経損傷、広汎性神経損傷、三叉神経損傷、坐骨神経損傷、視神経管損傷、趾神経損傷、視神経損傷、尺骨神経上腕部損傷、尺骨神経損傷、尺骨神経不全損傷、手指神経損傷、食道神経叢損傷、新生児顔面神経損傷、新生児末梢神経損傷、心臓神経叢損傷、上肢神経損傷、上肢皮膚知覚神経損傷、星状神経節損傷、正中神経上腕部損傷、正中神経損傷、脊髄神経根損傷、仙椎神経根損傷、舌下神経損傷、舌咽神経損傷、前腕多発性神経損傷、前腕皮膚知覚神経損傷、前腕部神経損傷、大腿神経損傷、中枢神経系損傷、聴神経損傷、橈骨神経上腕部損傷、橈骨神経損傷、動眼神経損傷、内耳神経損傷、内側足底神経損傷、内臓神経損傷、脳神経損傷、肺神経叢損傷、腓骨神経損傷、腹腔神経節損傷、腹腔神経叢損傷、副神経損傷、母指神経損傷、腰仙神経叢損傷、腰椎神経根損傷、腕神経叢損傷に好ましく用いることができる。また、本明細書における末梢神経損傷とは、外傷により神経の一部を損なうだけでなく、神経の断裂や切断も含まれ、更には、抜歯や嚢胞摘出術、インプラント埋入術等の口腔外科手術による損傷も含まれる。
別の実施形態としては、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩は、前記末梢神経を治療すると共に骨形成を促進することを特徴とする、損傷した末梢神経を治療するための組成物である。後述の実施例に示すように、本明細書における損傷した末梢神経を治療するための組成物は、骨髄腔の狭小化が観察されたことから、骨修復促進効果も期待できる。
別の実施形態としては、末梢神経は、三叉神経であることを特徴とする、損傷した末梢神経を治療するための組成物である。後述の実施例に示すように、本明細書における損傷した末梢神経を治療するための組成物は、体内で唯一骨内に神経が束となって走行している切断した三叉神経の再生を促進することが観察されたことから、三叉神経に対して高い治療効果が得られる。別の実施形態としては、三叉神経は、下顎神経である。別の実施形態としては、下顎神経は、下歯槽神経である。
本明細書においてGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩とは、ヒアルロン酸であってもよく、ヒアルロン酸ナトリウム、ヒアルロン酸カリウム、ヒアルロン酸亜鉛、ヒアルロン酸カルシウム、ヒアルロン酸マグネシウム、ヒアルロン酸アンモニウム等のヒアルロン酸塩であってもよい。この中でも、所望の粘度が得られ、充分な治療効果が期待できるという観点からは、ヒアルロン酸ナトリウムが好ましい。ヒアルロン酸ナトリウムの化学名は、例えば[→3)-2-acetamido-2-deoxy-β-D-glucopyranosyl-(1→4)-β-D-sodium glucopyranosyluronate-(1→]n(IUPAC)で表すことができる。GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の起源は、動物組織から抽出したものでも、発酵法で製造したものでもその起源を問うことなく使用できるが、不純物による副作用の懸念が小さいという点で、発酵法で製造したものが好ましい。発酵法で製造する場合、使用する菌株は自然界から分離されるストレプトコッカス属等のGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の生産能を有する微生物、又は特開昭63-123392号公報に記載したストレプトコッカス・エクイFM-100(微工研菌寄第9027号)、特開平2-234689号公報に記載したストレプトコッカス・エクイFM-300(微工研菌寄第2319号)のような高収率で安定にGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を生産する変異株が望ましい。上記の変異株を用いて培養、精製されたものが用いられる。GlcNAc及び/又はGlcAを少なくとも構成糖とする糖及び/又はその塩の溶媒は、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩が溶解するものであればどのようなものでもよく、水、水とエタノールの混合液、水とプロピレングリコールの混合液等が挙げられるが、好ましくは水である。溶液には適宜、塩化ナトリウム、リン酸水素ナトリウム水和物、リン酸二水素ナトリウム、L-メチオニン、チオ硫酸ナトリウム、塩化亜鉛、ヨウ化ナトリウム、クエン酸ナトリウム等の、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖との間で共有結合生成を伴う化学反応を起こさない、添加物を含むことができる。なお、本明細書におけるGlcNAc及び/又はGlcAを少なくとも構成糖とする糖及び/又はその塩には、安全性を損なわない範囲で、一部又は全量を架橋又は修飾した物を用いることができるが、好ましくは非架橋かつ非修飾のGlcNAc及び/又はGlcAを少なくとも構成糖とする糖及び/又はその塩が用いられ、より好ましくは非架橋かつ非修飾のヒアルロン酸及び/又はその塩が用いられる。
本明細書で用いる損傷末梢神経治療用組成物は、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩と、水以外に、医薬品として製品化する上で必要とされる種々の有効成分、添加物を含むことができる。例えば有効成分としては、局所麻酔剤(リドカイン、キシロカイン等)、非ステロイド系抗炎症薬(インドメタシン、ジクロフェナク等)、ステロイド系抗炎症薬(プレドニゾロン、デキサメタゾン等)、抗生物質(セフメタゾール、エリスロマイシン等)、筋弛緩剤、造影剤、抗体医薬、核酸医薬等を含むことができる。添加物としては、等張化剤(塩化ナトリウム、塩化カリウム等)、pH調整剤(リン酸水素ナトリウム水和物、リン酸二水素ナトリウム、酢酸、酢酸ナトリウム等)、安定化剤(L-メチオニン、クエン酸ナトリウム、キシリトール、塩化亜鉛、エタノール、グリセリン等)等を含むことができる。損傷末梢神経治療用組成物は溶液状態でも懸濁状態でも良いが、検査が容易という点で、溶液状態が好ましい。損傷末梢神経治療用組成物の調製には、一般に知られている各種の方法を用いることができる。例えば、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖及び/又はその塩以外の成分(水、有効成分、添加物)を混合、溶解した後、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を加えて混合溶解後、バイアルやシリンジ等の容器に充填することができる。無菌の損傷末梢神経治療用組成物とするには、全操作を無菌的に行う方法や、ろ過滅菌する方法、混合溶解後又は充填後に加熱滅菌する方法等を用いることができる。
GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の濃度は0.01w/v%以上であればどのような値でもよいが、薬効をより向上させるため、好ましくは0.8w/v%以上、より好ましくは1.5w/v%以上、さらに好ましくは1.9w/v%以上である。また生産コスト低減という観点からは、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の濃度は3.5w/v%以下であることが好ましく、2.5w/v%以下であることがより好ましく、2.2w/v%以下であることがさらに好ましい。
別の実施形態としては、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩は、0.8w/v%以上3.5w/v%以下の濃度で含有することを特徴とする、損傷した末梢神経治療するための組成物である。上記濃度の範囲には、その上限値又は下限値とその間に含まれる数値との間の範囲も含まれる。例えば、上記濃度の範囲は、0.8、0.9、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2.0、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3.0、3.1、3.2、3.3、3.4及び3.5w/v%からなる群より選択される2つの値の範囲であってもよい。
実施形態の一つに記載のGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の粘度平均分子量は100万超であればどのような値でもよいが、薬効をより向上させるため、好ましくは110万以上、より好ましくは150万以上、さらに好ましくは190万以上である。また生産コスト低減という観点からは、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の粘度平均分子量は350万以下であることが好ましく、250万以下であることがより好ましく、220万以下であることがさらに好ましい。
粘度平均分子量は、第十六改正日本薬局方 一般試験法 粘度測定法 第一法に基づき、ウベローデ型粘度計で測定温度30℃にて測定して得られた極限粘度の値を用いて、下記のLaurentの式により求めることができる。
粘度平均分子量 = ((極限粘度(dL/g))×105/36)1/0.78
粘度平均分子量 = ((極限粘度(dL/g))×105/36)1/0.78
実施形態の一つに記載の25℃、せん断速度0.1s-1における粘度は、1000mPa・s以上であればどのような値でもよいが、薬効をより長期間持続させるという観点からは、10Pa・s以上であることが好ましく、100Pa・s以上であることがより好ましい。またこの粘度は、生産コスト低減という観点からは、3000Pa・s以下であることが好ましく、2500Pa・s以下であることがより好ましく、1500Pa・s以下であることがより好ましい。上記粘度の範囲には、その上限値又は下限値とその間に含まれる数値との間の範囲も含まれる。例えば、上記粘度の範囲は、1000mPa・s、10Pa・s、100Pa・s、500Pa・s、1000Pa・s、1500Pa・s、2000Pa・s、2500Pa・s又は3000Pa・sからなる群より選択される2つの値の範囲であってもよい。
粘度は、市販のレオメーターを用いて以下に示す条件で測定できる。
・レオメーター:回転式(例えばアントン・パール社製MCR300)
・測定治具:コーンプレート型治具(例えばアントン・パール社製CP50-1)
・測定温度:25℃
・剪断速度:0.1(1/s)
・レオメーター:回転式(例えばアントン・パール社製MCR300)
・測定治具:コーンプレート型治具(例えばアントン・パール社製CP50-1)
・測定温度:25℃
・剪断速度:0.1(1/s)
損傷末梢神経治療用組成物を神経損傷局所に滴下する際の液量は、GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩が意図する目的を達成するのに有効な量で含有される薬剤とすることができ、「治療的有効量」又は「薬理学的有効量」は当業者に十分に認識され、薬理学的結果を生じるために有効な薬剤の量をいう。治療的有効量の決定は十分に当業者に知られている。
治療的有効量とは、投与により疾患の状態を軽減する薬剤の量をいう。治療効果及び毒性は、細胞培養又は実験動物における標準的な薬学的手順によって決定され得る。用量は、好ましくは、毒性をほとんど又は全くともなわないLD50を含む循環濃度の範囲内にある。この用量は、使用される投与形態、患者の感受性、及び投与経路に依存してこの範囲内で変化する。一例として、複合体の投与量は、年齢その他の患者の条件、疾患の種類、使用する複合体の種類等により適宜選択される。
以上、本発明の実施形態について述べたが、これらは本発明の例示であり、上記以外の様々な構成を採用することができる。例えば、脂質が結合していないGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を0.01w/v%以上の濃度で含有することを特徴とする、損傷した末梢神経の瘢痕化を防止若しくは抑制するための組成物、損傷した末梢神経における神経種の形成を防止又は抑制させるための組成物、損傷した末梢神経における鈍化若しくは喪失した感覚の回復を促進させる組成物、骨を修復させるための組成物、及び、骨の修復を促進させる足場材を例示することができる。
以下実施例により本発明を説明するが、本発明はこれらに限定されるものではない。
(試料調製例1)
粘度平均分子量190万のヒアルロン酸ナトリウム(電気化学工業社製)を乾燥重量として10.0g採取し、滅菌済の2Lの円筒形プラスチックボトル(コーニング社製)に無菌的に入れた。ここに、無菌的に調製した1Lのリン酸緩衝生理食塩液(pH7.2)を加えて振り混ぜた。これを室温で1日間、攪拌溶解し、「1.0w/v%-Mη190万試料」とした。なおヒアルロン酸ナトリウムの乾燥重量は、湿重量と、第十六改正日本薬局方 医薬品各条 精製ヒアルロン酸ナトリウムの乾燥減量の項で求めた乾燥減量値から求めた。
粘度平均分子量190万のヒアルロン酸ナトリウム(電気化学工業社製)を乾燥重量として10.0g採取し、滅菌済の2Lの円筒形プラスチックボトル(コーニング社製)に無菌的に入れた。ここに、無菌的に調製した1Lのリン酸緩衝生理食塩液(pH7.2)を加えて振り混ぜた。これを室温で1日間、攪拌溶解し、「1.0w/v%-Mη190万試料」とした。なおヒアルロン酸ナトリウムの乾燥重量は、湿重量と、第十六改正日本薬局方 医薬品各条 精製ヒアルロン酸ナトリウムの乾燥減量の項で求めた乾燥減量値から求めた。
(試料調製例2)
粘度平均分子量190万のヒアルロン酸ナトリウム(電気化学工業社製)を乾燥重量として20.0g採取した以外は、試料調製例1と同様に行い、「2.0w/v%-Mη190万試料」とした。
粘度平均分子量190万のヒアルロン酸ナトリウム(電気化学工業社製)を乾燥重量として20.0g採取した以外は、試料調製例1と同様に行い、「2.0w/v%-Mη190万試料」とした。
(試料調製例3)
粘度平均分子量190万のヒアルロン酸ナトリウム(電気化学工業社製)を乾燥重量として30.0g採取した以外は、試料調製例1と同様に行い、「3.0w/v%-Mη190万試料」とした。
粘度平均分子量190万のヒアルロン酸ナトリウム(電気化学工業社製)を乾燥重量として30.0g採取した以外は、試料調製例1と同様に行い、「3.0w/v%-Mη190万試料」とした。
試料調製例1~3の各試料につき、以下のとおり測定及び評価した。
<ヒアルロン酸ナトリウム溶液の粘度測定>
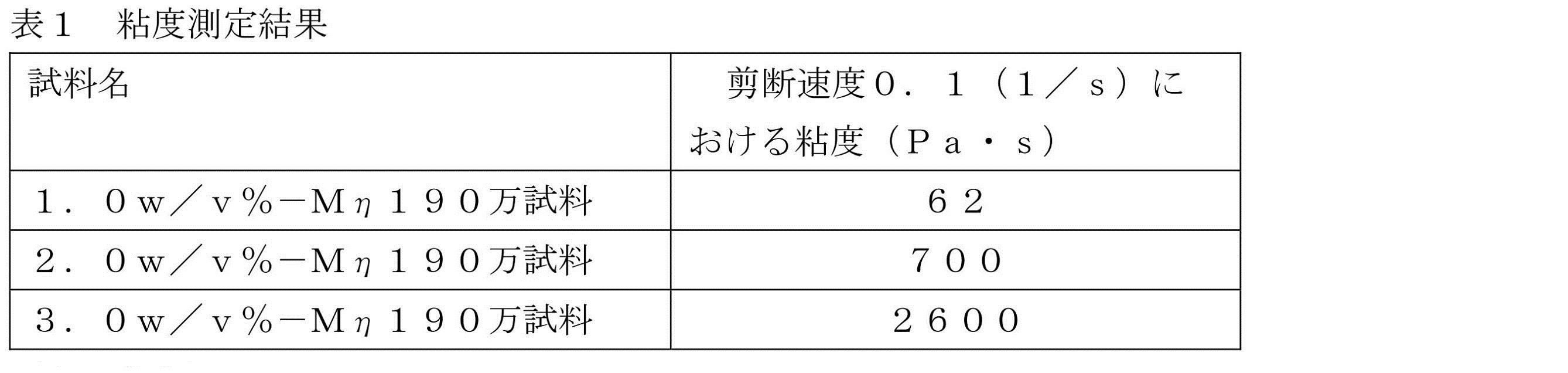
粘度測定装置であるレオメーターとして、MCR300(商品名、アントン・パール製)を使用した。コーンプレートはCP50-1(コーン角1.009°,D=49.938mm)を用い、測定温度25℃、剪断速度:0.01~1000(1/s)(せんだん速度の対数が一定間隔となるよう増加)、測定点数:51点、試料量:0.6mL、測定時間:10秒/点にて測定した。得られたデータのうち、剪断速度0.1(1/s)に最も近く、0.1(1/s)を挟む2点のデータを基に、補間法により剪断速度0.1(1/s)における粘度の値を算出した。表1に粘度の測定結果を示す。
粘度測定装置であるレオメーターとして、MCR300(商品名、アントン・パール製)を使用した。コーンプレートはCP50-1(コーン角1.009°,D=49.938mm)を用い、測定温度25℃、剪断速度:0.01~1000(1/s)(せんだん速度の対数が一定間隔となるよう増加)、測定点数:51点、試料量:0.6mL、測定時間:10秒/点にて測定した。得られたデータのうち、剪断速度0.1(1/s)に最も近く、0.1(1/s)を挟む2点のデータを基に、補間法により剪断速度0.1(1/s)における粘度の値を算出した。表1に粘度の測定結果を示す。
<ヒアルロン酸ナトリウム溶液の粘度平均分子量測定>
第十六改正日本薬局方 医薬品各条 精製ヒアルロン酸ナトリウム の項に準じて、ウベローデ型粘度計で測定した時の流下時間が0.2mol/L塩化ナトリウム試液の2.0~2.4倍となるよう、0.2mol/L塩化ナトリウム試液にて希釈し、この液をさらに4段階に希釈し、第十六改正日本薬局方 一般試験法 粘度測定法 第1法に従いウベローデ型粘度計にて各試料の流下時間を測定、極限粘度を算出した。極限粘度の値からは、下記の式にて粘度平均分子量を算出した。表2に粘度平均分子量の測定結果を示す。
粘度平均分子量 = ((極限粘度(dL/g))×105/36)1/0.78
第十六改正日本薬局方 医薬品各条 精製ヒアルロン酸ナトリウム の項に準じて、ウベローデ型粘度計で測定した時の流下時間が0.2mol/L塩化ナトリウム試液の2.0~2.4倍となるよう、0.2mol/L塩化ナトリウム試液にて希釈し、この液をさらに4段階に希釈し、第十六改正日本薬局方 一般試験法 粘度測定法 第1法に従いウベローデ型粘度計にて各試料の流下時間を測定、極限粘度を算出した。極限粘度の値からは、下記の式にて粘度平均分子量を算出した。表2に粘度平均分子量の測定結果を示す。
粘度平均分子量 = ((極限粘度(dL/g))×105/36)1/0.78
<神経損傷時の神経腫発生に及ぼすヒアルロン酸ナトリウムの効果>
ヒアルロン酸ナトリウムが神経損傷時における神経腫発生に及ぼす作用を、ラット実験的神経損傷モデルを用いて検討した。
ヒアルロン酸ナトリウムが神経損傷時における神経腫発生に及ぼす作用を、ラット実験的神経損傷モデルを用いて検討した。
<下歯槽神経切断モデルの作製とサンプルの投与>
動物としては、6週齢のSDラット(体重230-250g)、雄16匹を用いた。動物は、可動式ラックに装着したブラケット式金属製金網床ケージ(292W×400D×200H mm)にまとめて収容し、温度23±2℃、湿度50±10%、換気回数10~15回/時間、照明時間8:00~20:00(明12時間、暗12時間)の環境下で飼育した。動物を入荷後10日間馴化させた。
動物としては、6週齢のSDラット(体重230-250g)、雄16匹を用いた。動物は、可動式ラックに装着したブラケット式金属製金網床ケージ(292W×400D×200H mm)にまとめて収容し、温度23±2℃、湿度50±10%、換気回数10~15回/時間、照明時間8:00~20:00(明12時間、暗12時間)の環境下で飼育した。動物を入荷後10日間馴化させた。
飼料はステンレス製給餌器により手術前は実験動物用ペレット状、手術後はMF粉末飼料(オリエンタル酵母工業(株)社製)を自由摂取として与え、飲料水はポリプロピレン製給水瓶(先管ステンレス製)により自由に与えた。動物の個体識別は尻尾に識別番号を記載して識別した。
ヒアルロン酸ナトリウム1.0w/v%-Mη190万試料を投与する群、2.0w/v%-Mη190万試料を投与する群、3.0w/v%-Mη190万試料を投与する群と、対照として生理食塩水(大塚生食水、大塚製薬工場(株))を投与する群の合計4群とした。各群4匹ずつのラットを用いた。
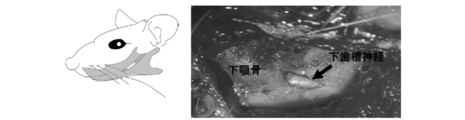
セボフルラン(製品名セボフレン、丸石製薬(株))製)吸引下で、全身麻酔状態とし、更に4%抱水クロラールを体重100gにつき1mLを腹腔投与して手術に適切な麻酔深度とした。その後、左頬部の皮膚切開を入れて咬筋を剥離した後、一部咬筋を切離して下顎骨外側表面を露出させた。下顎骨表面には最後方臼歯と切歯形成端の間に相当する位置に、歯科用ドリルを用いてφ2mm程度の楕円形の小穴を開けて下歯槽神経を完全に露出させた(図1)。露出した下歯槽神経はマイクロ剪刃で完全に切断した後、切断端はそのまま元の位置に戻した。直後に骨削した孔を覆う様に1.0w/v%-Mη190万試料または2.0w/v%-Mη190万試料または3.0w/v%-Mη190万試料または生理食塩水を局所投与した。1.0w/v%-Mη190万試料はシリンジ(製品名テルモシリンジ1ml、18G針付、テルモ社製)を用いて切断局所の神経全体を覆う程度に滴下した。その後咬筋を縫合して閉創した。なお2.0w/v%-Mη190万試料及び3.0w/v%-Mη190万試料は粘度が高くシリンジで吸引不可能であったので、鑷子にて適量を滴下した。
<灌流固定とパラフィン包埋>
術後3週間で全てのラットを灌流固定した。セボフルラン麻酔後、8%抱水クロラール0.5ml/100g とヘパリン1cc投与を腹腔内投与した。開胸して右心房を切開して生理食塩水を左心室に投与した後に4%パラホルムアルデヒドを続けて注射して固定を行った。その後、一晩後固定を行い、PBSで洗浄した。手術部位を含む下顎を摘出し、50%ギ酸と20%クエン酸を等量混和した脱灰液に浸漬して、1週間脱灰を行った。脱水した後にパラフィンで包埋した。
術後3週間で全てのラットを灌流固定した。セボフルラン麻酔後、8%抱水クロラール0.5ml/100g とヘパリン1cc投与を腹腔内投与した。開胸して右心房を切開して生理食塩水を左心室に投与した後に4%パラホルムアルデヒドを続けて注射して固定を行った。その後、一晩後固定を行い、PBSで洗浄した。手術部位を含む下顎を摘出し、50%ギ酸と20%クエン酸を等量混和した脱灰液に浸漬して、1週間脱灰を行った。脱水した後にパラフィンで包埋した。
<アザン染色による形態学的観察>
形態学的観察のためにはアザン染色を用いた。包埋した切片を脱パラフィンした。その後60℃アゾカルミン液、0.1%アニリンアルコール、酢酸アルコールに順次浸漬し、さらに5%リンタングステン酸に浸漬してアニリンブルー・オレンジG液に漬けた。水洗した後、純アルコールで分別し、封入した後に顕微鏡下で切断神経の再生とその周囲の骨変化を観察した。
形態学的観察のためにはアザン染色を用いた。包埋した切片を脱パラフィンした。その後60℃アゾカルミン液、0.1%アニリンアルコール、酢酸アルコールに順次浸漬し、さらに5%リンタングステン酸に浸漬してアニリンブルー・オレンジG液に漬けた。水洗した後、純アルコールで分別し、封入した後に顕微鏡下で切断神経の再生とその周囲の骨変化を観察した。
図2aに示すように、生理食塩水を投与した群では、切断した部位の神経は大きく膨大化し、外傷性神経腫の形成が認められた。この膨大部の内部にはコラーゲンの貯留が多く認められており、周囲の神経には空胞の形成が多く認められ、再生は不良であった。さらに同部位における神経線維の走行には大きな乱れがあった。
一方、ヒアルロン酸ナトリウム投与群(図2b~2d)では、神経腫の形成は認められたが、コントロール群と比較してその大きさは小さい傾向があった。同部におけるコラーゲンの含有は明らかに少なかった。1.0w/v%-Mη190万試料投与群及び3.0w/v%-Mη190万試料投与群では神経腫形成は認められるものの、同部におけるコラーゲン量は明らかに減少していたが軸索の周囲組織への伸長は認められていた(図2b及び2d)。
2.0w/v%-Mη190万試料投与群では神経の膨大すなわち神経腫の形成は小さかった(図2c)。同部位内部のコラーゲン含有は1.0w/v%-Mη190万試料投与群及び3.0w/v%-Mη190万試料投与群に比較しても明らかに少なかった。再生部位における神経の空胞形成も少なく、2.0w/v%-Mη190万試料投与群では軸索は1.0w/v%-Mη190万試料投与群及び3.0w/v%-Mη190万試料投与群に比べて長軸方向に並んでいる線維が多く、周囲への発芽伸長は少ない傾向が認められた。下歯槽神経周囲の骨組織においては、1.0w/v%-Mη190万試料投与群及び3.0w/v%-Mη190万試料投与群より2.0w/v%-Mη190万試料投与群で骨髄腔が狭小化している傾向があり、骨の成熟が進んでいることが推察された。
以上の結果より、いずれのヒアルロン酸ナトリウム投与群においても、対照群と比較して神経腫の形成が減少していた。このことから、ヒアルロン酸ナトリウムには神経腫形成抑制効果があることが示された。また、2.0w/v%-Mη190万試料の場合においては、骨修復効果を有し、損傷部の修復・再生が更に促進していることが示された。
本発明組成物は、正常な神経再生を促すことができ、且つ神経腫の発生自体を抑制することができる。従って本発明組成物は、難治性の神経障害性疼痛の発生を防止し、鈍化または喪失した感覚の回復を促進させることができるため、神経損傷による神経障害性疼痛の根本治療に寄与する。また、本発明組成物を用いた損傷末梢神経に対する処置は、リスクの大きい従来の外科的療法に比べて、より安全かつ確実に行うことができる。従って本発明組成物は、抜歯や嚢胞摘出術、インプラント埋入術等の口腔外科手術を受ける患者の負担やリスクの軽減にもつながり、極めて有用である。
Claims (7)
- 脂質が結合していないGlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩を0.01w/v%以上の濃度で含有することを特徴とする、損傷した末梢神経を治療するための組成物。
- 前記GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の粘度平均分子量が100万超であることを特徴とする、請求項1に記載の組成物。
- 前記GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩は、0.8w/v%以上3.5w/v%以下の濃度で含有することを特徴とする、請求項1又は2に記載の組成物。
- 前記組成物は、前記末梢神経を治療すると共に骨形成を促進することを特徴とする、請求項1から3のいずれかに記載の組成物。
- 前記末梢神経は、三叉神経であることを特徴とする、請求項1から4のいずれかに記載の組成物。
- 前記GlcNAc及び/又はGlcAを少なくとも構成糖とする糖又はその塩の、25℃、せん断速度0.1s-1における粘度が1000mPa・s以上であることを特徴とする、請求項1から5のいずれかに記載の組成物。
- 前記GlcNAc及び/又はGlcAを少なくとも構成糖とする糖は、ヒアルロン酸である、請求項1から6のいずれかに記載の組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017527465A JP6875988B2 (ja) | 2015-07-07 | 2016-07-05 | 損傷末梢神経治療用組成物 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015-136453 | 2015-07-07 | ||
| JP2015136453 | 2015-07-07 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2017006932A1 true WO2017006932A1 (ja) | 2017-01-12 |
Family
ID=57685619
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2016/069900 WO2017006932A1 (ja) | 2015-07-07 | 2016-07-05 | 損傷末梢神経治療用組成物 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP6875988B2 (ja) |
| WO (1) | WO2017006932A1 (ja) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08208706A (ja) * | 1994-10-06 | 1996-08-13 | Genzyme Corp | ポリアニオン性多糖類と疎水性生物吸収ポリマーを含む組成物 |
-
2016
- 2016-07-05 JP JP2017527465A patent/JP6875988B2/ja active Active
- 2016-07-05 WO PCT/JP2016/069900 patent/WO2017006932A1/ja active Application Filing
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08208706A (ja) * | 1994-10-06 | 1996-08-13 | Genzyme Corp | ポリアニオン性多糖類と疎水性生物吸収ポリマーを含む組成物 |
Non-Patent Citations (7)
| Title |
|---|
| AGENOR A ET AL.: "Hyaluronic acid/carboxymethyl cellulose directly applied to transected nerve decreases axonal outgrowth", J BIOMED MATER RES B APPL BIOMATER, ISSN: 1552-4973 * |
| MURRAY RC ET AL.: "Acute effects of perineural administration of sodium hyaluronate on palmer digital neurectomy sites in horses", AM J VET RES, vol. 55, no. 10, 1994, pages 1484 - 1489, ISSN: 0002-9645, [retrieved on 20160727] * |
| OZGENEL GY ET AL.: "Combined application of human amniotic membrane wrapping and hyaluronic acid injection in epineurectomized rat sciatic nerve", J RECONSTR MICROSURG, vol. 20, no. 2, 2004, pages 153 - 157, ISSN: 0743-684X * |
| SECKEL BR ET AL.: "Hyaluronic acid through a new injectable nerve guide delivery system enhances peripheral nerve regeneration in the rat", J NEUROSCI RES, vol. 40, no. 3, 1995, pages 318 - 324, ISSN: 0360-4012 * |
| TETSUYA WATANABE ET AL.: "Effects of application of hyaluronan to rat calvarial defects on bone formation", JOURNAL OF THE JAPANESE SOCIETY OF PERIODONTOLOGY, vol. 49, no. 4, 2007, pages 305 - 315, ISSN: 0385-0110 * |
| WANG, KK ET AL.: "Hyaluronic acid enhances peripheral nerve regeneration in vivo", MICROSURGERY, vol. 18, no. 4, 1998, pages 270 - 275, XP002376338, ISSN: 0738-1085, DOI: doi:10.1002/(SICI)1098-2752(1998)18:4<270::AID-MICR11>3.0.CO;2-V * |
| ZHANG H ET AL.: "Implantation of neural stem cells embedded in hyaluronic acid and collagen composite conduit promotes regeneration in a rabit facial nerve injury model", J TRANSL MED, vol. 6, 2008, pages 67, XP021050733, ISSN: 1479-5876, DOI: doi:10.1186/1479-5876-6-67 * |
Also Published As
| Publication number | Publication date |
|---|---|
| JP6875988B2 (ja) | 2021-05-26 |
| JPWO2017006932A1 (ja) | 2018-04-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2000501740A (ja) | リン脂質とプロピレングリコールによる滑剤 | |
| Luo et al. | Dental-craniofacial manifestation and treatment of rare diseases | |
| US10046082B2 (en) | Collagen sponge containing a drug for promoting fracture healing and method for preparing the same | |
| Dreiseidler et al. | Changes in volume during the four months’ remodelling period of iliac crest grafts in reconstruction of the alveolar ridge | |
| WO2001015743A3 (en) | Viscosity-standardised compositions which facilitate swallowing in dysphagic subjects | |
| JP4990446B2 (ja) | 関節症治療用注入剤 | |
| JP4820024B2 (ja) | 局所麻酔用組成物 | |
| WO2017006932A1 (ja) | 損傷末梢神経治療用組成物 | |
| TWI748090B (zh) | 加速急性創傷性周邊神經損傷復元之複合生物材料及其應用 | |
| Retief et al. | The vervet monkey (Cercopithecus aethiops) as an experimental model for pulpal studies | |
| von Arx et al. | Outcome of first-time surgical closures of oroantral communications due to tooth extractions. A retrospective analysis of 162 cases | |
| RU2582976C1 (ru) | Способ ускорения процесса репаративного остеогенеза | |
| JP6706632B2 (ja) | 半月板変性治療用組成物 | |
| Sahib et al. | Evaluation of healing process of periapical defect filled by platelet rich fibrin using cone beam computed tomography–comparative clinical study | |
| KR20210119453A (ko) | 치주염 치료 및 치간 유두 재생용 조성물 | |
| TWI611805B (zh) | 用於治療坐骨神經損傷之醫藥組合物 | |
| RU2551312C1 (ru) | Способ восстановления тканей зубочелюстной системы | |
| Albrektsson et al. | Failure of Core-Vent implants: A retrieval analysis of 19 hollow basket implants | |
| RU2593817C2 (ru) | Способ ускорения процесса репаративного остеогенеза | |
| Pinho et al. | Accidental Intraoperative Mandibular Fracture in a Third Molar Surgery: When Surgical Skills Are Mandatory in the Face of Empiricism | |
| EP4252762A1 (en) | Method for preparing injectable injection composition derived from animal cartilage, and use thereof | |
| JP2017516852A (ja) | 骨、軟骨、歯、および歯周組織の再生と、腫瘍および嚢胞の処置のための製剤 | |
| TW201739457A (zh) | 組成物在製備治療動物或人的受傷肌腱之藥物的用途與套組 | |
| JP4073986B2 (ja) | 脊髄潅流液 | |
| RU2558988C1 (ru) | Способ восстановления тканей пародонта |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 16821401 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2017527465 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 16821401 Country of ref document: EP Kind code of ref document: A1 |