WO2016010161A1 - 多量体IgA型遺伝子組換え抗体及びその利用 - Google Patents
多量体IgA型遺伝子組換え抗体及びその利用 Download PDFInfo
- Publication number
- WO2016010161A1 WO2016010161A1 PCT/JP2015/070742 JP2015070742W WO2016010161A1 WO 2016010161 A1 WO2016010161 A1 WO 2016010161A1 JP 2015070742 W JP2015070742 W JP 2015070742W WO 2016010161 A1 WO2016010161 A1 WO 2016010161A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- antibody
- iga
- protein
- type
- multimeric
- Prior art date
Links
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 169
- 102000004169 proteins and genes Human genes 0.000 claims abstract description 135
- 102400001107 Secretory component Human genes 0.000 claims abstract description 69
- 101000840258 Homo sapiens Immunoglobulin J chain Proteins 0.000 claims abstract description 64
- 102100029571 Immunoglobulin J chain Human genes 0.000 claims abstract description 63
- 238000000034 method Methods 0.000 claims abstract description 52
- 238000004519 manufacturing process Methods 0.000 claims abstract description 42
- 230000027455 binding Effects 0.000 claims abstract description 39
- 239000000427 antigen Substances 0.000 claims abstract description 35
- 108091007433 antigens Proteins 0.000 claims abstract description 34
- 102000036639 antigens Human genes 0.000 claims abstract description 34
- 239000003814 drug Substances 0.000 claims abstract description 26
- 230000003472 neutralizing effect Effects 0.000 claims abstract description 25
- 239000004480 active ingredient Substances 0.000 claims abstract description 7
- 101150026046 iga gene Proteins 0.000 claims description 227
- 239000013604 expression vector Substances 0.000 claims description 55
- 150000001413 amino acids Chemical class 0.000 claims description 31
- 102100023542 Ribosome-binding protein 1 Human genes 0.000 claims description 24
- 125000000539 amino acid group Chemical group 0.000 claims description 19
- 150000007523 nucleic acids Chemical class 0.000 claims description 17
- 108020004707 nucleic acids Proteins 0.000 claims description 13
- 102000039446 nucleic acids Human genes 0.000 claims description 13
- 101710159080 Aconitate hydratase A Proteins 0.000 claims description 12
- 101710159078 Aconitate hydratase B Proteins 0.000 claims description 12
- 102000044126 RNA-Binding Proteins Human genes 0.000 claims description 12
- 101710105008 RNA-binding protein Proteins 0.000 claims description 12
- 239000002773 nucleotide Substances 0.000 claims description 10
- 125000003729 nucleotide group Chemical group 0.000 claims description 10
- 230000002209 hydrophobic effect Effects 0.000 claims description 7
- 208000035473 Communicable disease Diseases 0.000 claims description 6
- 108091081024 Start codon Proteins 0.000 claims description 5
- 230000002265 prevention Effects 0.000 claims description 5
- 230000006798 recombination Effects 0.000 claims description 5
- 238000011144 upstream manufacturing Methods 0.000 claims description 5
- 230000000295 complement effect Effects 0.000 claims description 4
- 238000005215 recombination Methods 0.000 claims description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 2
- 102100033400 4F2 cell-surface antigen heavy chain Human genes 0.000 abstract 1
- 101000800023 Homo sapiens 4F2 cell-surface antigen heavy chain Proteins 0.000 abstract 1
- 210000004027 cell Anatomy 0.000 description 143
- 235000018102 proteins Nutrition 0.000 description 112
- 125000003275 alpha amino acid group Chemical group 0.000 description 71
- 235000001014 amino acid Nutrition 0.000 description 45
- 241000700605 Viruses Species 0.000 description 43
- 230000000694 effects Effects 0.000 description 41
- 239000000539 dimer Substances 0.000 description 40
- 230000014509 gene expression Effects 0.000 description 38
- 108020004414 DNA Proteins 0.000 description 35
- 238000005516 engineering process Methods 0.000 description 34
- 229940024606 amino acid Drugs 0.000 description 31
- 239000000178 monomer Substances 0.000 description 29
- 239000000243 solution Substances 0.000 description 29
- 238000001890 transfection Methods 0.000 description 26
- 238000006386 neutralization reaction Methods 0.000 description 25
- 241000712461 unidentified influenza virus Species 0.000 description 25
- 238000000746 purification Methods 0.000 description 23
- 239000000047 product Substances 0.000 description 22
- 239000000523 sample Substances 0.000 description 22
- 239000013638 trimer Substances 0.000 description 22
- 230000015572 biosynthetic process Effects 0.000 description 20
- 239000012634 fragment Substances 0.000 description 20
- 239000000203 mixture Substances 0.000 description 20
- 239000013612 plasmid Substances 0.000 description 20
- 230000006870 function Effects 0.000 description 17
- 108091008146 restriction endonucleases Proteins 0.000 description 17
- 238000004458 analytical method Methods 0.000 description 16
- 239000013613 expression plasmid Substances 0.000 description 16
- 150000002500 ions Chemical class 0.000 description 16
- 238000006467 substitution reaction Methods 0.000 description 16
- 238000004113 cell culture Methods 0.000 description 15
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 15
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 14
- 230000010530 Virus Neutralization Effects 0.000 description 14
- 238000000055 blue native polyacrylamide gel electrophoresis Methods 0.000 description 14
- 239000002953 phosphate buffered saline Substances 0.000 description 14
- 238000002360 preparation method Methods 0.000 description 14
- 108090000765 processed proteins & peptides Proteins 0.000 description 14
- 230000001737 promoting effect Effects 0.000 description 14
- 230000001965 increasing effect Effects 0.000 description 13
- 206010022000 influenza Diseases 0.000 description 13
- 108010068327 4-hydroxyphenylpyruvate dioxygenase Proteins 0.000 description 12
- 210000004379 membrane Anatomy 0.000 description 12
- 239000012528 membrane Substances 0.000 description 12
- 101150095279 PIGR gene Proteins 0.000 description 11
- 239000000872 buffer Substances 0.000 description 11
- 210000002729 polyribosome Anatomy 0.000 description 11
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 11
- 239000006228 supernatant Substances 0.000 description 11
- 241001465754 Metazoa Species 0.000 description 10
- 239000012570 Opti-MEM I medium Substances 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 10
- 238000003776 cleavage reaction Methods 0.000 description 10
- 239000003623 enhancer Substances 0.000 description 10
- 230000002708 enhancing effect Effects 0.000 description 10
- 210000004180 plasmocyte Anatomy 0.000 description 10
- 230000007017 scission Effects 0.000 description 10
- 230000003248 secreting effect Effects 0.000 description 10
- 102000003886 Glycoproteins Human genes 0.000 description 9
- 108090000288 Glycoproteins Proteins 0.000 description 9
- 101710154606 Hemagglutinin Proteins 0.000 description 9
- 101710093908 Outer capsid protein VP4 Proteins 0.000 description 9
- 101710135467 Outer capsid protein sigma-1 Proteins 0.000 description 9
- 101710176177 Protein A56 Proteins 0.000 description 9
- 238000002474 experimental method Methods 0.000 description 9
- 238000012163 sequencing technique Methods 0.000 description 9
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 8
- 101150071100 CBY2 gene Proteins 0.000 description 8
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 8
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 8
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 8
- 239000012228 culture supernatant Substances 0.000 description 8
- 229940079593 drug Drugs 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 7
- 238000010367 cloning Methods 0.000 description 7
- 239000002299 complementary DNA Substances 0.000 description 7
- 210000002919 epithelial cell Anatomy 0.000 description 7
- 239000002609 medium Substances 0.000 description 7
- 239000011780 sodium chloride Substances 0.000 description 7
- 239000013598 vector Substances 0.000 description 7
- 230000003612 virological effect Effects 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- 108060003951 Immunoglobulin Proteins 0.000 description 6
- 101800000695 MLL cleavage product C180 Proteins 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 239000006285 cell suspension Substances 0.000 description 6
- 239000003153 chemical reaction reagent Substances 0.000 description 6
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 6
- 102000018358 immunoglobulin Human genes 0.000 description 6
- 229960003971 influenza vaccine Drugs 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 238000001638 lipofection Methods 0.000 description 6
- 239000011159 matrix material Substances 0.000 description 6
- 108020004999 messenger RNA Proteins 0.000 description 6
- 230000028327 secretion Effects 0.000 description 6
- 238000001542 size-exclusion chromatography Methods 0.000 description 6
- 229960005486 vaccine Drugs 0.000 description 6
- 238000001262 western blot Methods 0.000 description 6
- 241000282412 Homo Species 0.000 description 5
- 108700005078 Synthetic Genes Proteins 0.000 description 5
- 108090000631 Trypsin Proteins 0.000 description 5
- 102000004142 Trypsin Human genes 0.000 description 5
- 238000005119 centrifugation Methods 0.000 description 5
- 239000007795 chemical reaction product Substances 0.000 description 5
- 238000012790 confirmation Methods 0.000 description 5
- 230000002068 genetic effect Effects 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 208000015181 infectious disease Diseases 0.000 description 5
- 238000004949 mass spectrometry Methods 0.000 description 5
- 230000035772 mutation Effects 0.000 description 5
- 238000001426 native polyacrylamide gel electrophoresis Methods 0.000 description 5
- 229920000642 polymer Polymers 0.000 description 5
- 238000011160 research Methods 0.000 description 5
- 230000004083 survival effect Effects 0.000 description 5
- 239000012588 trypsin Substances 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- IVLXQGJVBGMLRR-UHFFFAOYSA-N 2-aminoacetic acid;hydron;chloride Chemical compound Cl.NCC(O)=O IVLXQGJVBGMLRR-UHFFFAOYSA-N 0.000 description 4
- 241000271566 Aves Species 0.000 description 4
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 4
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 4
- 241000283984 Rodentia Species 0.000 description 4
- 230000003321 amplification Effects 0.000 description 4
- 229940125644 antibody drug Drugs 0.000 description 4
- 238000004422 calculation algorithm Methods 0.000 description 4
- 238000010276 construction Methods 0.000 description 4
- 238000011067 equilibration Methods 0.000 description 4
- 238000001641 gel filtration chromatography Methods 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 239000000185 hemagglutinin Substances 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 210000004962 mammalian cell Anatomy 0.000 description 4
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 4
- 210000004400 mucous membrane Anatomy 0.000 description 4
- 210000002850 nasal mucosa Anatomy 0.000 description 4
- 238000003199 nucleic acid amplification method Methods 0.000 description 4
- 239000008363 phosphate buffer Substances 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 102000004196 processed proteins & peptides Human genes 0.000 description 4
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 4
- 238000013207 serial dilution Methods 0.000 description 4
- 230000010473 stable expression Effects 0.000 description 4
- 238000002255 vaccination Methods 0.000 description 4
- WURBVZBTWMNKQT-UHFFFAOYSA-N 1-(4-chlorophenoxy)-3,3-dimethyl-1-(1,2,4-triazol-1-yl)butan-2-one Chemical compound C1=NC=NN1C(C(=O)C(C)(C)C)OC1=CC=C(Cl)C=C1 WURBVZBTWMNKQT-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 241000283707 Capra Species 0.000 description 3
- 108020004705 Codon Proteins 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 3
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 3
- 206010065764 Mucosal infection Diseases 0.000 description 3
- 238000012300 Sequence Analysis Methods 0.000 description 3
- 108090000190 Thrombin Proteins 0.000 description 3
- 108010084455 Zeocin Proteins 0.000 description 3
- 238000002835 absorbance Methods 0.000 description 3
- 210000004899 c-terminal region Anatomy 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000012258 culturing Methods 0.000 description 3
- 230000001086 cytosolic effect Effects 0.000 description 3
- 238000000605 extraction Methods 0.000 description 3
- 239000012091 fetal bovine serum Substances 0.000 description 3
- 238000007852 inverse PCR Methods 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 229960000310 isoleucine Drugs 0.000 description 3
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 3
- 230000004807 localization Effects 0.000 description 3
- 239000011259 mixed solution Substances 0.000 description 3
- 210000003097 mucus Anatomy 0.000 description 3
- CWCMIVBLVUHDHK-ZSNHEYEWSA-N phleomycin D1 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC[C@@H](N=1)C=1SC=C(N=1)C(=O)NCCCCNC(N)=N)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C CWCMIVBLVUHDHK-ZSNHEYEWSA-N 0.000 description 3
- 230000000069 prophylactic effect Effects 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 239000001488 sodium phosphate Substances 0.000 description 3
- 229910000162 sodium phosphate Inorganic materials 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 239000007921 spray Substances 0.000 description 3
- 238000005507 spraying Methods 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 229960004072 thrombin Drugs 0.000 description 3
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 3
- 230000009385 viral infection Effects 0.000 description 3
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 2
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 2
- 208000030507 AIDS Diseases 0.000 description 2
- 108010011170 Ala-Trp-Arg-His-Pro-Gln-Phe-Gly-Gly Proteins 0.000 description 2
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 2
- 239000005695 Ammonium acetate Substances 0.000 description 2
- 108091026890 Coding region Proteins 0.000 description 2
- 102000008186 Collagen Human genes 0.000 description 2
- 108010035532 Collagen Proteins 0.000 description 2
- 208000001528 Coronaviridae Infections Diseases 0.000 description 2
- 239000004971 Cross linker Substances 0.000 description 2
- 102000012410 DNA Ligases Human genes 0.000 description 2
- 108010061982 DNA Ligases Proteins 0.000 description 2
- 101100291267 Drosophila melanogaster Miga gene Proteins 0.000 description 2
- 239000012591 Dulbecco’s Phosphate Buffered Saline Substances 0.000 description 2
- 241000588724 Escherichia coli Species 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- 241000238631 Hexapoda Species 0.000 description 2
- 125000000998 L-alanino group Chemical group [H]N([*])[C@](C([H])([H])[H])([H])C(=O)O[H] 0.000 description 2
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 2
- 125000000510 L-tryptophano group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C(C([H])([H])[C@@]([H])(C(O[H])=O)N([H])[*])C2=C1[H] 0.000 description 2
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 2
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 108091027974 Mature messenger RNA Proteins 0.000 description 2
- 208000025370 Middle East respiratory syndrome Diseases 0.000 description 2
- 208000034578 Multiple myelomas Diseases 0.000 description 2
- 239000002033 PVDF binder Substances 0.000 description 2
- 102000003992 Peroxidases Human genes 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 108010046644 Polymeric Immunoglobulin Receptors Proteins 0.000 description 2
- 108010021757 Polynucleotide 5'-Hydroxyl-Kinase Proteins 0.000 description 2
- 102000008422 Polynucleotide 5'-hydroxyl-kinase Human genes 0.000 description 2
- 201000003176 Severe Acute Respiratory Syndrome Diseases 0.000 description 2
- 102000039471 Small Nuclear RNA Human genes 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 108091005906 Type I transmembrane proteins Proteins 0.000 description 2
- 229940043376 ammonium acetate Drugs 0.000 description 2
- 235000019257 ammonium acetate Nutrition 0.000 description 2
- 210000000628 antibody-producing cell Anatomy 0.000 description 2
- -1 aromatic amino acids Chemical class 0.000 description 2
- 210000002469 basement membrane Anatomy 0.000 description 2
- OWMVSZAMULFTJU-UHFFFAOYSA-N bis-tris Chemical compound OCCN(CCO)C(CO)(CO)CO OWMVSZAMULFTJU-UHFFFAOYSA-N 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 238000004364 calculation method Methods 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 230000004186 co-expression Effects 0.000 description 2
- 229920001436 collagen Polymers 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 230000000120 cytopathologic effect Effects 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 230000008260 defense mechanism Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- UQLDLKMNUJERMK-UHFFFAOYSA-L di(octadecanoyloxy)lead Chemical compound [Pb+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O UQLDLKMNUJERMK-UHFFFAOYSA-L 0.000 description 2
- 239000000032 diagnostic agent Substances 0.000 description 2
- 229940039227 diagnostic agent Drugs 0.000 description 2
- 238000010586 diagram Methods 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 210000000981 epithelium Anatomy 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 238000009396 hybridization Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 230000010365 information processing Effects 0.000 description 2
- 238000011081 inoculation Methods 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 210000004877 mucosa Anatomy 0.000 description 2
- 210000001331 nose Anatomy 0.000 description 2
- 210000005259 peripheral blood Anatomy 0.000 description 2
- 239000011886 peripheral blood Substances 0.000 description 2
- 210000005105 peripheral blood lymphocyte Anatomy 0.000 description 2
- 108040007629 peroxidase activity proteins Proteins 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 2
- 229950010131 puromycin Drugs 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 230000009257 reactivity Effects 0.000 description 2
- 210000002345 respiratory system Anatomy 0.000 description 2
- 239000012898 sample dilution Substances 0.000 description 2
- 108091029842 small nuclear ribonucleic acid Proteins 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 210000001324 spliceosome Anatomy 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 238000004114 suspension culture Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 230000032258 transport Effects 0.000 description 2
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 2
- 238000011179 visual inspection Methods 0.000 description 2
- AUTOLBMXDDTRRT-JGVFFNPUSA-N (4R,5S)-dethiobiotin Chemical compound C[C@@H]1NC(=O)N[C@@H]1CCCCCC(O)=O AUTOLBMXDDTRRT-JGVFFNPUSA-N 0.000 description 1
- 102100031585 ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Human genes 0.000 description 1
- 108700028369 Alleles Proteins 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 1
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 102100027207 CD27 antigen Human genes 0.000 description 1
- 101100172879 Caenorhabditis elegans sec-5 gene Proteins 0.000 description 1
- 241000282465 Canis Species 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 108091035707 Consensus sequence Proteins 0.000 description 1
- 235000005956 Cosmos caudatus Nutrition 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- YQYJSBFKSSDGFO-UHFFFAOYSA-N Epihygromycin Natural products OC1C(O)C(C(=O)C)OC1OC(C(=C1)O)=CC=C1C=C(C)C(=O)NC1C(O)C(O)C2OCOC2C1O YQYJSBFKSSDGFO-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000701533 Escherichia virus T4 Species 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 102000009123 Fibrin Human genes 0.000 description 1
- 108010073385 Fibrin Proteins 0.000 description 1
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 241000282575 Gorilla Species 0.000 description 1
- 101000777636 Homo sapiens ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Proteins 0.000 description 1
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 1
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 1
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 1
- 101500027203 Homo sapiens MLL cleavage product C180 Proteins 0.000 description 1
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 1
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 1
- 108050006430 Immunoglobulin-like domains Proteins 0.000 description 1
- 102000016844 Immunoglobulin-like domains Human genes 0.000 description 1
- 229940124873 Influenza virus vaccine Drugs 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 125000000393 L-methionino group Chemical group [H]OC(=O)[C@@]([H])(N([H])[*])C([H])([H])C(SC([H])([H])[H])([H])[H] 0.000 description 1
- 125000000174 L-prolyl group Chemical group [H]N1C([H])([H])C([H])([H])C([H])([H])[C@@]1([H])C(*)=O 0.000 description 1
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 1
- 108091026898 Leader sequence (mRNA) Proteins 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 241000282567 Macaca fascicularis Species 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- BACYUWVYYTXETD-UHFFFAOYSA-N N-Lauroylsarcosine Chemical compound CCCCCCCCCCCC(=O)N(C)CC(O)=O BACYUWVYYTXETD-UHFFFAOYSA-N 0.000 description 1
- 102000003729 Neprilysin Human genes 0.000 description 1
- 108090000028 Neprilysin Proteins 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 101710131079 Polymeric immunoglobulin receptor Proteins 0.000 description 1
- 102100035187 Polymeric immunoglobulin receptor Human genes 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 102000029797 Prion Human genes 0.000 description 1
- 108091000054 Prion Proteins 0.000 description 1
- 101710186352 Probable membrane antigen 3 Proteins 0.000 description 1
- 101710181078 Probable membrane antigen 75 Proteins 0.000 description 1
- 101710199886 Protein 0.5 Proteins 0.000 description 1
- 108010026552 Proteome Proteins 0.000 description 1
- 230000004570 RNA-binding Effects 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 241000725643 Respiratory syncytial virus Species 0.000 description 1
- 206010039085 Rhinitis allergic Diseases 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 102000004598 Small Nuclear Ribonucleoproteins Human genes 0.000 description 1
- 108010003165 Small Nuclear Ribonucleoproteins Proteins 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- 101710178472 Tegument protein Proteins 0.000 description 1
- 108010028230 Trp-Ser- His-Pro-Gln-Phe-Glu-Lys Proteins 0.000 description 1
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 1
- 102000006986 U2 Small Nuclear Ribonucleoprotein Human genes 0.000 description 1
- 108010072724 U2 Small Nuclear Ribonucleoprotein Proteins 0.000 description 1
- 101150004685 UL48 gene Proteins 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 238000011481 absorbance measurement Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 238000001261 affinity purification Methods 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 201000010105 allergic rhinitis Diseases 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 230000005875 antibody response Effects 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- LFYJSSARVMHQJB-QIXNEVBVSA-N bakuchiol Chemical compound CC(C)=CCC[C@@](C)(C=C)\C=C\C1=CC=C(O)C=C1 LFYJSSARVMHQJB-QIXNEVBVSA-N 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 210000003022 colostrum Anatomy 0.000 description 1
- 235000021277 colostrum Nutrition 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- KAKKHKRHCKCAGH-UHFFFAOYSA-L disodium;(4-nitrophenyl) phosphate;hexahydrate Chemical compound O.O.O.O.O.O.[Na+].[Na+].[O-][N+](=O)C1=CC=C(OP([O-])([O-])=O)C=C1 KAKKHKRHCKCAGH-UHFFFAOYSA-L 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 229950003499 fibrin Drugs 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 238000010230 functional analysis Methods 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 125000000404 glutamine group Chemical group N[C@@H](CCC(N)=O)C(=O)* 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 238000003317 immunochromatography Methods 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- VBCVPMMZEGZULK-NRFANRHFSA-N indoxacarb Chemical compound C([C@@]1(OC2)C(=O)OC)C3=CC(Cl)=CC=C3C1=NN2C(=O)N(C(=O)OC)C1=CC=C(OC(F)(F)F)C=C1 VBCVPMMZEGZULK-NRFANRHFSA-N 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- PGLTVOMIXTUURA-UHFFFAOYSA-N iodoacetamide Chemical compound NC(=O)CI PGLTVOMIXTUURA-UHFFFAOYSA-N 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 238000000464 low-speed centrifugation Methods 0.000 description 1
- 238000007403 mPCR Methods 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 238000001840 matrix-assisted laser desorption--ionisation time-of-flight mass spectrometry Methods 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000007923 nasal drop Substances 0.000 description 1
- 229940100662 nasal drops Drugs 0.000 description 1
- 239000006199 nebulizer Substances 0.000 description 1
- 238000007899 nucleic acid hybridization Methods 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 238000012946 outsourcing Methods 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 239000012521 purified sample Substances 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000000241 respiratory effect Effects 0.000 description 1
- 210000001533 respiratory mucosa Anatomy 0.000 description 1
- 210000003705 ribosome Anatomy 0.000 description 1
- 102200065564 rs6318 Human genes 0.000 description 1
- 210000003296 saliva Anatomy 0.000 description 1
- 108700004121 sarkosyl Proteins 0.000 description 1
- 238000002864 sequence alignment Methods 0.000 description 1
- YEENEYXBHNNNGV-XEHWZWQGSA-M sodium;3-acetamido-5-[acetyl(methyl)amino]-2,4,6-triiodobenzoate;(2r,3r,4s,5s,6r)-2-[(2r,3s,4s,5r)-3,4-dihydroxy-2,5-bis(hydroxymethyl)oxolan-2-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound [Na+].CC(=O)N(C)C1=C(I)C(NC(C)=O)=C(I)C(C([O-])=O)=C1I.O[C@H]1[C@H](O)[C@@H](CO)O[C@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 YEENEYXBHNNNGV-XEHWZWQGSA-M 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 125000001493 tyrosinyl group Chemical group [H]OC1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 238000012795 verification Methods 0.000 description 1
- 239000011534 wash buffer Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/06—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies from serum
- C07K16/065—Purification, fragmentation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/01—Preparation of mutants without inserting foreign genetic material therein; Screening processes therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/10—Processes for the isolation, preparation or purification of DNA or RNA
- C12N15/1034—Isolating an individual clone by screening libraries
- C12N15/1086—Preparation or screening of expression libraries, e.g. reporter assays
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/66—General methods for inserting a gene into a vector to form a recombinant vector using cleavage and ligation; Use of non-functional linkers or adaptors, e.g. linkers containing the sequence for a restriction endonuclease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
- A61K2039/507—Comprising a combination of two or more separate antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
- C07K16/1002—Coronaviridae
Abstract
Description
(1)多量体IgA型遺伝子組換え抗体。
(2)重鎖定常領域の第458番目のアミノ酸残基が疎水性アミノ酸に由来するアミノ酸残基である、(1)に記載の多量体IgA型遺伝子組換え抗体。
(3)四量体の含有量が全IgAの20モル%以上である、(1)又は(2)に記載の多量体IgA型遺伝子組換え抗体。
(4)(1)~(3)のいずれか一項に記載の多量体IgA型遺伝子組換え抗体を有効成分として含有する医薬。
(5)感染症の治療又は予防用である、(4)に記載の医薬。
(6)IgA型抗体重鎖タンパク質、抗体軽鎖タンパク質、抗体J鎖タンパク質及び分泌成分タンパク質を1つの細胞内で共発現させる工程を含む、多量体IgA型抗体の製造方法。
(7)前記IgA型抗体重鎖タンパク質は、遺伝子組換えによりIgG型からIgA型に変換されたものである、(6)に記載の製造方法。
(8)前記工程において、更にp180タンパク質及びSF3b4タンパク質を前記細胞内で共発現させる、(6)又は(7)に記載の製造方法。
(9)前記細胞がCHO YA7細胞株(受託番号NITE BP-01535)である、(6)~(8)のいずれかに記載の製造方法。
(10)前記工程は、IgA型抗体重鎖タンパク質、抗体軽鎖タンパク質、抗体J鎖タンパク質及び分泌成分タンパク質を発現するための発現ベクターを前記細胞内に導入することにより行われ、前記発現ベクターは、プロモーターの下流で、かつ、IgA型抗体重鎖タンパク質、抗体軽鎖タンパク質、抗体J鎖タンパク質又は分泌成分タンパク質をコードする核酸の開始コドンの上流に、RNA結合タンパク質が認識、結合又は相互作用するcis-エレメントを有する、(6)~(9)のいずれかに記載の製造方法。
(11)前記cis-エレメントが、配列モチーフGAN1-(X)n-ACN2(nは3~6の整数であり、N1及びN2は、それぞれ独立して、A、T、G、Cのいずれかである。)からなる塩基配列を1~数個含む、(10)に記載の製造方法。
(12)前記cis-エレメントが、
配列番号21~23のいずれかに示される塩基配列、
配列番号21~23のいずれかに示される塩基配列において、1~数個の塩基が欠失、置換又は付加されている塩基配列からなり、かつRNA結合タンパク質が認識、結合若しくは相互作用する塩基配列、
配列番号21~23のいずれかに示される塩基配列と同一性が80%以上である塩基配列からなり、かつ、RNA結合タンパク質が認識、結合若しくは相互作用する塩基配列、又は、
配列番号21~23のいずれかに示される塩基配列からなる核酸と相補的な塩基配列からなる核酸とストリンジェントな条件下でハイブリダイズすることができる塩基配列からなり、かつRNA結合タンパク質が認識、結合若しくは相互作用する塩基配列からなる、(10)又は(11)に記載の製造方法。
(13)抗体を多量体IgA型化する工程を含む、前記抗体の抗原結合活性又は中和活性を向上させる方法。
(14)前記抗体は、IgG型抗体である、(13)に記載の方法。
(15)前記工程が、前記抗体の重鎖可変領域を有するIgA型抗体重鎖タンパク質、前記抗体の軽鎖タンパク質、抗体J鎖タンパク質及び分泌成分タンパク質を1つの細胞内で共発現させる工程を含む、(13)又は(14)に記載の方法。
IgA型抗体に関連して、従来用いられている用語について以下に説明する。
IgAは、血清中では、主に単量体IgAとして分子量17万前後で存在しており、IgA1が主要構成要素である。
二量体IgAとは、粘膜固有層に存在する形質細胞が産生する二量体IgAであって、重鎖:軽鎖:J鎖の割合が4:4:1である分子を指す。IgA2が約半分程度存在する。
従来、ポリメリックIg受容体により認識される二量体以上のIgAを総称して、多量体IgAという場合が多い。すなわち、重鎖:軽鎖:J鎖の構成比が4:4:1の複合体である二量体IgAが主成分で、抗体J鎖タンパク質(Joining chain)によりIgA二分子が結合し、分泌成分タンパク質(secretory component、SCタンパク質)を含む場合と含まない場合の両方について「多量体IgA」という用語が使用されている。
粘膜上皮細胞の基底膜側の細胞膜上に発現しているpIgRは、免疫グロブリンスーパーファミリーに属するI型の膜貫通型蛋白質で、細胞外ドメイン部分、膜貫通部、細胞質内領域からなる。pIgRは粘膜固有層に存在する形質細胞が産生したJ鎖を含む二量体/多量体型Ig分子を特異的に認識して結合し、上皮細胞中への取り込み後も結合したままアピカル側へ輸送される。上皮細胞内から粘膜面への放出には、pIgRの細胞外ドメイン部分と膜貫通部との間で切断が必要で、上皮細胞のタンパク質分解酵素による切断後に内腔側粘膜層へS-IgAとして分泌される。このpIgRの細胞外ドメイン部分がIgA複合体の構成成分となる事実に由来して、分泌成分タンパク質(secretory component、SCタンパク質)とも呼ばれている。pIgRは五量体IgMの取り込みにも同様にして機能している。
粘膜上皮細胞より分泌され、SCタンパク質を含んだ二量体以上のIgA複合体を指し、Secretory dimeric IgA(S-dIgA)の場合は重鎖:軽鎖:J鎖:SCの構成比が4:4:1:1である。
粘膜固有層に存在する形質細胞が産生する多量体IgAの分子量等の性状解析は技術的に困難なため、分泌型多量体IgA形成の詳細な分子形成過程は不明である。すなわち、生体内で形質細胞が産生する主要な分泌型多量体IgAは、二量体、三量体、四量体等の多量体のうちどれが主であるか、多量体化は上皮細胞内で起こっているかどうか、粘膜部で生体防御に中心的役割を果たしているのがどの型かも不明である。生体内IgA及び組換え体でも二量体(440kDa付近)より大きいIgAも微量検出されているが、凝集体との鑑別はなされていない。
本明細書においては、分泌成分タンパク質(SC)を分子内に有する多量体抗体を分泌型抗体という。また、次のように表記する場合がある。
・単量体抗体=mIgA
・二量体抗体=dIgA
・分泌型二量体抗体=S-dIgA
・分泌型三量体抗体=S-tIgA
・分泌型四量体抗体=S-qIgA
・四量体以上の分泌型多量体抗体=S-pIgA
・組換え単量体抗体=rmIgA
・組換え二量体抗体=rdIgA
・組換え分泌型二量体抗体=recombinant S-dIgA(rS-dIgA)
・組換え分泌型三量体抗体=recombinant S-tIgA(rS-tIgA)
・組換え分泌型四量体抗体=recombinant S-qIgA(rS-qIgA)
・四量体以上の組換え分泌型多量体抗体=recombinant S-pIgA(rS-pIgA)
ここでは、分泌成分タンパク質(SC)を分子内に有する場合に「S-」を分子名の頭に付記する。分子内にSCを有さない抗体は「S-」を付記しない。また、分子の会合状態を、IgAの前に略称を付記することにより表記する。単量体は「m」、二量体は「d」、三量体は「t」、四量体は「q」、四量体以上の多量体は「p」を付記する。また、単量体抗体と組換え単量体抗体を特に区別なく「monomer」と表記する場合がある。また、二量体抗体と分泌型二量体抗体、組換え二量体抗体、組換え分泌型二量体抗体を特に区別なく「dimer」と表記する場合がある。また、分泌型三量体抗体と組換え分泌型三量体抗体を特に区別なく「trimer」と表記する場合がある。また、分泌型四量体抗体と組換え分泌型四量体抗体を特に区別なく「tetramer」と表記する場合がある。また、四量体以上の分泌型抗体と四量体以上の組換え分泌型多量体抗体を特に区別なく「polymer」と表記する場合がある。
1実施形態において、本発明は、多量体IgA型遺伝子組換え抗体を提供する。本実施形態の多量体IgA型遺伝子組換え抗体は、本来非IgA型であった抗体を遺伝子組換えによりIgA型に変換し、更に多量体化したものであってもよい。非IgA型抗体としては、特に制限されず、例えば、非IgA型の、ヒト抗体、非ヒト哺乳動物由来の抗体、げっ歯類由来の抗体、鳥類由来の抗体等が挙げられる。また、抗体のクラスも特に制限されず、例えば、IgG型、IgM型、IgE型、IgD型、IgY型抗体等が挙げられる。
1実施形態において、本発明は、多量体IgA型遺伝子組換え抗体を有効成分として含有する医薬を提供する。本実施形態の医薬は、感染症の治療又は予防用であることが好ましい。感染症としては、寄生虫、細菌、真菌、ウイルス、異常プリオン等の病原体によるものが挙げられる。
1実施形態において、本発明は、IgA型抗体重鎖タンパク質、抗体軽鎖タンパク質、抗体J鎖タンパク質及び分泌成分タンパク質を1つの細胞内で共発現させる工程を含む、多量体IgA型抗体の製造方法を提供する。多量体IgA型抗体は、遺伝子組換え抗体であってもよい。
1実施形態において、本発明は、抗体を多量体IgA型化する工程を含む、前記抗体の抗原結合活性又は中和活性を向上させる方法を提供する。
(ワクチン接種と末梢血リンパ球の回収)
高病原性トリインフルエンザウイルスA/H5N1の不活化全粒子ワクチンを健康成人へ3週間隔で2回経鼻接種(片鼻250μL、計500μL)した。ワクチンとしては、45μgのヘマグルチニン(HA)を含有する不活化全粒子ワクチンを使用した。2回目のワクチン接種から7日後に末梢血を回収し、血球分離溶液Lymphoprep(商標)(AXIS-SHIELD社)を用いて末梢血リンパ球を回収した。
経鼻ワクチン接種により末梢血中に誘導された抗体産生形質細胞の単離は、FACS Aria (BD Bioscience社)を用いて実施した。細胞表面マーカーCD2-、CD3-、CD4-、CD10-、CD20-、IgD-、CD19low、CD27highかつCD38highの細胞集団を抗体産生形質細胞とし、単一細胞として分離・回収した。単一抗体産生形質細胞は、各ウェルに45ngのキャリアRNAを含む滅菌水9μLを分注した96穴プレートに回収した。cDNA調製は、T. Tillerら(J Immunol Methods, 329, 112-24, 2008)の報告に則り実施した。具体的には、細胞を回収した各ウェルにSuperscript III RT(ライフテクノロジーズ社)、Randam Hexamer(ライフテクノロジーズ社)、RNaseOUT(ライフテクノロジーズ社)、dNTP mix(キアゲン社)を含む6μLの混合液を添加し、50℃50分、85℃5分の反応を行うことでcDNAを調製した。
調製したcDNAを2μL用いて、各ウェルに単離された抗体重鎖のアイソタイプをReal-time PCRにより決定した。IgG、IgAおよびIgMの各定常領域に対してTaqManプローブとプライマーを準備した。IgG、IgAおよびIgMに対するTaqManプローブは、それぞれFAM、HEXおよびCy5による標識とした。QuantiTect Multiplex PCR NoROX Master Mix(キアゲン社)を使用し、LightCycler480(ロシュ社)を用いて解析を行った。
抗体可変領域遺伝子の増幅は、T. Tillerら(J Immunol Methods, 329, 112-24, 2008)の報告に則り実施した。具体的には、調製したcDNA1μLに対して11.5μLのHotStarTaq DNA polymerase(キアゲン社)、dNTP mix及び各抗体可変領域遺伝子を増幅するプライマーセットの混合液を添加し、1回目のPCR反応を行った。更にこのPCR産物1μLに含まれる各遺伝子に対して更に内側に設計したプライマーセットを用いて2回目のPCR反応を行った。いずれのPCR反応においても、95℃15分、(94℃30秒、58℃20秒、72℃60秒)×43サイクル、72℃2分の条件で増幅を行った。また、PCR産物の塩基配列解析(シークエンス)を常法により行った。
抗体可変領域遺伝子のPCRはPrimeSTAR(登録商標)MAX DNA Polymerase(TaKaRa社)を使用して、説明書にしたがって実施した。鋳型として上述の1回目のPCR産物を使用し、プライマーとしては、上述の2回目のPCR産物のシークエンスの結果に基づいて、増幅する遺伝子座に適切なペアを選択した。PCR条件は98℃10秒、55℃5秒、72℃10秒で25サイクルとした。PCR産物の精製はMonoFas(登録商標)DNA精製キットI(ジーエルサイエンス社)を使用して、説明書にしたがって実施し、30μLのBuffer Cに溶出した。
遺伝子組換え抗体の作製にはExpi293(商標)Expression System(ライフテクノロジーズ社)を説明書にしたがって用いた。30mLの系を以下に例示する。
細胞のデブリを1000×g、10分間の遠心分離により取り除いた後、Millex-HV Filter Unit (ミリポア社)で上清の濾過を行った。遺伝子組換え抗体の精製はCaptureSelect(商標)human Fc affinity matrix(ライフテクノロジーズ社)を用いて、説明書にしたがって実施した。具体的には、カラムは10カラム容量のリン酸緩衝液(PBS)で平衡化し、サンプルをロードし、10カラム容量のPBSで洗浄し、5カラム容量の0.1M Glycine-HCl(pH3.0)により抗体を溶出し、1M Tris-HCl(pH9.0)で溶出液を中和した。カラムは10カラム容量のPBSで再平衡化した。抗体の濃度はNanoDrop(Thermo Scientific社)で測定した。抗体の濃縮はAmicon(登録商標)Ultra Centrifugal Filter Devices(ミリポア社)を用いて、説明書にしたがって実施した。Zeba Desalt Spin Columns(Thermo Scientific社)で、説明書にしたがってPB(pH7.4)にバッファー交換した。バッファー交換後の濃度はNanoDropで測定した。
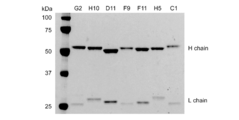
精製した抗体の確認はNuPAGE(登録商標)Bis-Tris Gel(ライフテクノロジーズ社)を用いて、説明書にしたがってSDSポリアクリルアミドゲル電気泳動(SDS-PAGE)を実施した。図1はSDS-PAGEの結果を示す写真である。抗体クローンG2、H10、D11、F9、F11、H5及びC1が、IgG1型化されたことが確認された。抗体クローンG2、H10、D11、F9、F11、H5及びC1が、IgG1型化されたことが確認された。クローンによって発現量にばらつきが見られた。40mL培養系において、クローンB12は約40mg、クローンD11は約4mg、クローンF9は約1.5mg、クローンF11は約2.1mg、クローンH5は約1mgの抗体を作製することができた。
IgA型遺伝子組換え抗体を以下の方法により作製した。実験例1で作製したIgG1抗体に限らず、配列が既知の抗体は全て以下の方法でIgA型化することができる。
IgA1抗体定常領域遺伝子を含む発現ベクターα1 HCを作製した。IgA1抗体定常領域遺伝子のPCRは、PrimeSTAR(登録商標)MAX DNA Polymerase(TaKaRa社)を使用して、説明書にしたがって実施した。
抗体可変領域遺伝子のPCRはPrimeSTAR(登録商標)MAX DNA Polymerase(TaKaRa社)を使用して、説明書にしたがって実施した。γ1 HC発現ベクターへクローニングした抗体遺伝子を鋳型として、リバースプライマーをα1 HC発現ベクター用のものに変更し、PCR条件は98℃10秒、55℃5秒、72℃5秒で25サイクルとした。
遺伝子組換え抗体の作製にはExpi293(商標)Expression System(ライフテクノロジーズ社)を説明書にしたがって用いた。30mLの系を以下に例示する。
細胞のデブリを1000×g、10分間の遠心分離により取り除いた後、Millex-HV Filter Unit (ミリポア社)で上清の濾過を行った。遺伝子組換え抗体の精製はCaptureSelect(商標)human IgA affinity matrix(ライフテクノロジーズ社)を用いて、説明書にしたがって実施した。具体的には、カラムは10カラム容量のリン酸緩衝液(PBS)で平衡化し、サンプルをロードし、10カラム容量のPBSで洗浄し、5カラム容量の0.1M Glycine-HCl(pH3.0)により抗体を溶出し、1M Tris-HCl(pH9.0)で溶出液を中和した。カラムは10カラム容量のPBSで再平衡化した。抗体の濃度はNanoDrop(Thermo Scientific社)で測定した。抗体の濃縮はAmicon(登録商標)Ultra Centrifugal Filter Devices(ミリポア社)を用いて、説明書にしたがって実施した。Zeba Desalt Spin Columns(Thermo Scientific社)で、説明書にしたがってPB(pH7.4)にバッファー交換した。バッファー交換後の濃度はNanoDropで測定した。
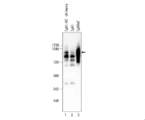
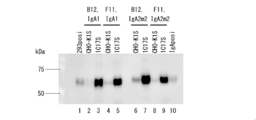
精製した抗体の確認はNuPAGE(登録商標)Bis-Tris Gel(ライフテクノロジーズ社)を用いて、説明書にしたがってSDSポリアクリルアミドゲル電気泳動(SDS-PAGE)を実施した。図2はSDS-PAGEの結果を示す写真である。抗体クローンB12、D11、F9、F11及びH5が、IgA1型化されたことが確認された。
実験例2において作製したIgA1抗体発現コンストラクトを用いて、二量体IgA1型抗体を作製した。
抗体J鎖は人工遺伝子合成サービス(オペロン バイオテクノロジー)を利用して、J鎖(GenBank accession no.NM_144646)のコード領域(CDS)の5’側にXhoI切断サイト及びKozak配列を付加し、3’側にNotI切断サイトを付加した人工遺伝子(配列番号24)を合成した。J鎖遺伝子をXhoI及びNotI-HF(以上、NEB社)を用いて、適切な条件で制限酵素処理した。同一の制限酵素で処理したpCXSNベクター(CMVプロモーターとSV40 polyAから構成される哺乳類細胞発現用ベクター)にクロ-ニングし、抗体J鎖の発現プラスミドであるpCXSN-hJCを得た。
二量体IgA1型抗体の作製にはExpi293(商標)Expression System(ライフテクノロジーズ社)を説明書にしたがって用いた。30mLの系を以下に例示する。
細胞のデブリを1000×g、10分間の遠心分離により取り除いた後、Millex-HV Filter Unit (ミリポア社)で上清の濾過を行った。遺伝子組換え抗体の精製はCaptureSelect(商標)human IgA affinity matrix(ライフテクノロジーズ社)を用いて、説明書にしたがって実施した。具体的には、カラムは10カラム容量のリン酸緩衝液(PBS)で平衡化し、サンプルをロードし、10カラム容量のPBSで洗浄し、5カラム容量の0.1M Glycine-HCl(pH3.0)により抗体を溶出し、1M Tris-HCl(pH9.0)で溶出液を中和した。カラムは10カラム容量のPBSで再平衡化した。抗体の濃度はNanoDrop(Thermo Scientific社)で測定した。抗体の濃縮はAmicon(登録商標)Ultra Centrifugal Filter Devices(ミリポア社)を用いて、説明書にしたがって実施した。Zeba Desalt Spin Columns(Thermo Scientific社)で、説明書にしたがってPB(pH7.4)にバッファー交換した。バッファー交換後の濃度はNanoDropで測定した。
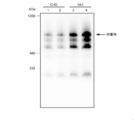
精製した抗体の確認は、未変性ポリアクリルアミドゲル電気泳動法(BN-PAGE、3-13%、Invitrogen社)により行った。図3はBN-PAGEの結果を示す写真である。J鎖非発現群(-J)では、単量体IgA型遺伝子組換え抗体のバンドが確認されたのに対し、J鎖発現群(+J)では、単量体のバンドに加えて、二量体IgA型遺伝子組換え抗体のバンドが確認された。
実験例2において作製したIgA1抗体発現コンストラクトを用いて、多量体IgA1型抗体を作製した。
GeneArt(登録商標)Strings(商標)DNA Fragments(ライフテクノロジーズ社)を利用して、polymeric immunoglobulin receptor(GenBank accession no. NM_002644)の185~2005残基の5’側にXhoI切断サイト及びKozak配列を付加し、3’側にHindIII切断サイト、thrombin切断サイト、ヒスチジンタグ及びNotI切断サイトを付加した人工DNAフラグメントを、中央付近で重複するように5’側フラグメントと3’側フラグメントの2本合成した。合成した2本のDNAフラグメントを鋳型に用いてPrimeSTAR(登録商標)MAX DNA Polymerase(TaKaRa社)を使用したoverlap PCRを行い、分泌成分(SC)をコードする遺伝子断片を増幅し(配列番号25)、XhoI及びNotIで制限酵素処理し、pCXSNベクターにクローニングし、分泌成分の発現プラスミドであるpCXSN-hSC-HisTagを得た。また、pCXSN-hSC-HisTagを鋳型としてインバースPCRを行い、3’側に付与したHindIII切断サイト、thrombin切断サイト、ヒスチジンタグを除去した分泌成分のみを発現するpCXSN-hSCを作製した。分泌成分としてどちらのプラスミドを用いても多量体抗体を作製することができた。
多量体IgA1型抗体の作製にはExpi293(商標)Expression System(ライフテクノロジーズ社)を説明書にしたがって用いた。30mLの系を以下に例示する。
細胞のデブリを1000×g、10分間の遠心分離により取り除いた後、Millex-HV Filter Unit (ミリポア社)で上清の濾過を行った。遺伝子組換え抗体の精製はCaptureSelect(商標)human IgA affinity matrix(ライフテクノロジーズ社)を用いて、説明書にしたがって実施した。具体的には、カラムは10カラム容量のリン酸緩衝液(PBS)で平衡化し、サンプルをロードし、10カラム容量のPBSで洗浄し、5カラム容量の0.1M Glycine-HCl(pH3.0)により抗体を溶出し、1M Tris-HCl(pH9.0)で溶出液を中和した。カラムは10カラム容量のPBSで再平衡化した。抗体の濃度はNanoDrop(Thermo Scientific社)で測定した。抗体の濃縮はAmicon(登録商標)Ultra Centrifugal Filter Devices(ミリポア社)を用いて、説明書にしたがって実施した。Zeba Desalt Spin Columns(Thermo Scientific社)で、説明書にしたがってPB(pH7.4)にバッファー交換した。バッファー交換後の濃度はNanoDropで測定した。
濃縮した多量体IgA1型抗体を、AKTA explorer10(GEヘルスケア社)を用いて、ゲル濾過クロマトグラフィーにより分画した。カラムには、Superose6 10/300 GL (GEヘルスケア社)を用いた。DPBS(Dulbecco’s Phosphate Buffered Saline)を以下のプロトコールで流した。流速0.5mL/分、カラム平衡化1.5カラム容量、溶出0.5mL(計1.5カラム容量)。
実験例1において、インフルエンザウイルスに対するヒトIgG1抗体を作製し、実験例2において、当該IgG1抗体と同一の可変領域を有するIgA1抗体を作製した。また、実験例3及び4において多量体IgA1型抗体を作製した。これらの抗体を用いて、インフルエンザウイルス中和活性を検討した。
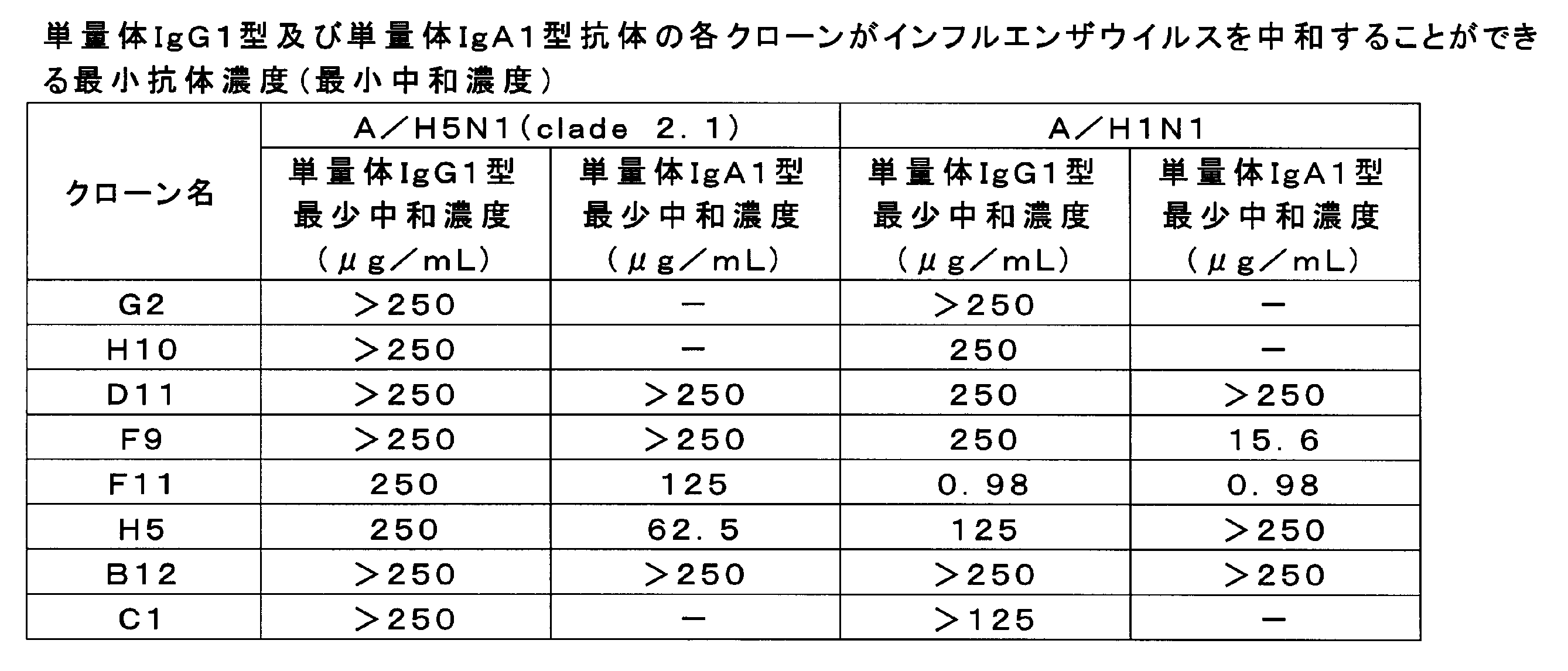
抗体クローンG2、H10、D11、F9、F11、H5、B12及びC1の単量体IgG1型抗体及び単量体IgA1型抗体を用いて、インフルエンザウイルス中和活性を測定した。ウイルスにはA/H5N1株(clade 2.1)及びA/H1N1株を使用した。
抗体クローンD11、F9、F11、H5及びB12の単量体IgA1型抗体及び二量体IgA1型抗体を用いて、上記と同様にしてインフルエンザウイルス中和活性を測定した。ウイルスにはA/H5N1株(clade 2.1)及びA/H1N1株を使用した。
抗体クローンF9、F11及びH5の単量体IgA1型抗体、二量体IgA1型抗体及び四量体IgA1型抗体を用いて、上記と同様にしてインフルエンザウイルス中和活性を測定した。ウイルスにはA/H5N1株(clade 2.1)を使用した。表3に結果を示す。最少中和濃度が低いほどウイルス中和活性が高いことを示す。
抗体クローンF11及びH5について、単量体IgG1型抗体、単量体IgA1型抗体、二量体IgA1型抗体及び四量体IgA1型抗体の中和能の活性比較のため、図5A及び図5Bに単量体IgG1型抗体のウイルス中和活性を1とした場合における、単量体IgA1型抗体、二量体IgA1型抗体及び四量体IgA1型抗体の中和活性比を示した。ウイルスにはA/H5N1株(clade 2.1)を使用した。
抗体クローンF11及びH5について、重鎖及び軽鎖の塩基配列及びアミノ酸配列をIGBLAST(http://www.ncbi.nlm.nih.gov/igblast/)にて解析した。また、相補性決定領域(complementarity determining region、CDR)をAndrew C.R. Martin博士らの方法(http://www.bioinf.org.uk/abs/)により決定した。配列表の配列番号と、各塩基配列及びアミノ酸配列との対応を表4に示す。クローンF11の軽鎖はκ鎖であった。また、クローンH5の軽鎖はλ鎖であった。
遺伝子組換えウイルス糖タンパク質発現ベクターの作製、遺伝子組換えウイルス糖タンパク質の発現と精製は後述する実験例9と同様の方法により行った。抗体クローンB12及びF11について、単量体IgA1型抗体、二量体IgA1型抗体及び四量体IgA1型抗体を用いて、インフルエンザウイルスHAタンパク質に対する抗原結合活性を検討した。
上述した抗体J鎖タンパク質の発現プラスミドであるpCXSN-hJCのプロモーターの下流かつJ鎖タンパク質の開始コドンの上流に、配列番号22に示すcis-エレメント#1を導入し、pCXSN-cis#1-hJCを得た。遺伝子配列解析によりcis-エレメントの向きが正しい挿入方向であることを確認した。
(抗RSウイルスFタンパク質抗体の作製)
公共データベースであるRCSB PDBに登録されている抗RSウイルスFタンパク質抗体のアミノ酸配列(PDB ID:2HWZ)の重鎖及び軽鎖可変領域のアミノ酸配列をヒト用にコドン最適化したアミノ酸配列をコードするDNA断片をそれぞれ人工合成した。合成した重鎖可変領域をコードするDNA断片を上述したα1 HCに、軽鎖 可変領域をコードするDNA断片を上述したκ LCにクローニングした。続いて、実験例4と同様にして抗RSウイルスFタンパク質抗体の多量体の発現及び精製を行った。
インフルエンザウイルスのHAタンパク質及びRSウイルスのFタンパク質ΔFP(アミノ酸配列137-146番の欠失変異体、McLellan J. S., et al., Structure of respiratory syncytial virus fusion glycoprotein in the postfusion conformation reveals preservation of neutralizing epitopes., J. Virol. 85(15), 7788-7796, 2011 を参照)の細胞外領域をコードするアミノ酸配列のC末端側に三量体形成配列及び精製用タグのコード配列(バクテリオファージT4フィブリチン三量体形成フォールドン配列、トロンビン切断部位(RSRSLVPRGSPGSGYIPEAPRDGQAYVRKDGEWVLLSTFL、配列番号26)、タンパク質精製用のStrep-tag(登録商標)II配列(WSHPQFEK、配列番号27)及び6×His tag配列(Stevens J. et al., Structure of the uncleaved human H1 hemagglutinin from the extinct 1918 influenza virus., Science 303, 1866-1870, 2004 を参照))を融合したアミノ酸配列をコードするDNA断片を合成し、哺乳類細胞発現用のベクターpCXSNにクローニングした。
遺伝子組換えウイルス糖タンパク質の作製にはExpi293(商標)Expression System(ライフテクノロジーズ社)を説明書にしたがって用いた。30mL系を以下に例示する。
まず、回収した上清中の細胞のデブリを1000×g、10分間の遠心分離により取り除いた。続いて、Millex-HV Filter Unit(ミリポア社)を使用して上清をろ過した。続いて、AKTA explorer10(GEヘルスケア社)を用いたアフィニティー精製によりウイルス糖タンパク質を精製した。カラムにはHisTrap excel(GEヘルスケア社)を用いた。より具体的には、平衡化溶液として20mMリン酸ナトリウム、0.5M NaCl、pH7.4を使用した。また、洗浄液として20mMリン酸ナトリウム、0.5M NaCl、10mMイミダゾール、pH7.4を使用した。また、溶出液として、20mMリン酸ナトリウム、0.5M NaCl、500mMイミダゾール、pH7.4を使用した。精製条件は、流速1mL/分、カラム平衡化10CV、カラム洗浄40CV、溶出1mL/フラクション(計50CV)、カラム再平衡化5CVとした。6xHis tagによる精製サンプルを、更に精製する場合にはStrep-tag(登録商標)/Strep-Tactin(登録商標)システムを使用した。Strep-Tactin(登録商標)Superflow(登録商標)(iba社)を用いて、説明書にしたがって精製した。より具体的には、まず、試薬として、Buffer W(100mM Tris-HCl、150mM NaCl、1mM EDTA、pH8.0)、Buffer E(100mM Tris-HCl、150mM NaCl、1mM EDTA、2.5mM desthiobiotin、pH8.0)、Buffer R(100mM Tris-HCl、150mM NaCl、1mM EDTA、1mM HABA、pH8.0)を準備した。続いて、カラムを2CVのBuffer Wで平衡化し、サンプルをロードし、1CVのBuffer Wで5回洗浄し、3CVのBuffer Eでウイルス糖タンパクを溶出した。そして、カラムを5CVのBuffer Rで3回再生洗浄し、4CVのBuffer Wで2回平衡化した。タンパク質を濃縮する場合には、Amicon(登録商標)Ultra Centrifugal Filter Devicesを用いて、説明書にしたがって濃縮した。精製されたタンパク質の濃度はNanoDrop(Thermo SCIENTIFIC社)を用いた吸光測定により測定した。
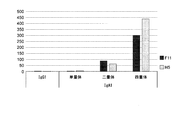
抗RSウイルスFタンパク質抗体の多量体のRSウイルスFタンパク質に対する反応性をELISAにより検討した。まず、96ウェルハーフプレートに50μLの遺伝子組換えFタンパク質(1μg/mL)を4℃で一晩固相化した後、ブロッキングを行った。続いて、抗RSウイルスFタンパク質抗体サンプルの2倍段階希釈系列を室温で2時間反応させた。続いて、PBSTを用いた洗浄後、HRP標識ヤギ抗ヒトIgA抗体(30000倍)(BETHYL LABORATORIES社)を室温で1時間反応させた。続いて、1-Step(商標)Ultra TMB-ELISA(Thermo SCIENTIFIC社)を用いて発色反応を行い、1M硫酸を加えて反応停止後、吸光度を測定した。抗RSウイルスFタンパク質抗体サンプル濃度1μg/mLにおけるOD 450nmの値(平均値±標準偏差)を図7に示した。その結果、抗RSウイルスFタンパク質抗体の抗原結合活性は、抗体が、二量体、四量体化すると有意に上昇することが確認された。
(α2m1 HC、α2m2 HC、α2(n) HC発現ベクターの作製)
IgA2のアロタイプの重鎖定常領域の遺伝子をクローニングした。具体的には、IgA2m1の重鎖定常領域をコードする遺伝子(α2m1 HC、アクセッション番号:J00221)、IgA2m2の重鎖定常領域をコードする遺伝子(α2m2 HC、アクセッション番号:M60192及びAJ012264)、IgA2(n)の重鎖定常領域をコードする遺伝子(α2(n) HC、アクセッション番号:S71043)の各塩基配列を、公共データベースであるIMGT/LIGM-DBに登録されている配列に基づいて入手し、ヒト用にコドン最適化を行い、人工遺伝子合成した。可変領域の最後のアミノ酸アラニンと定常領域の最初のアミノ酸セリンのコドンを改変してNheI切断サイトを作製した。NheI及びHindIIIで処理した合成配列を、上述のα1 HCをNheI及びHindIIIで処理したベクターにクローニングした。
PrimeSTAR(登録商標)MAX DNA Polymeraseを使用して、上述した抗インフルエンザウイルス抗体クローンB12の抗体可変領域遺伝子のPCRを行った。γ1 HC発現ベクターにクローニングした抗体遺伝子を鋳型とする場合には、α1 HC発現ベクターへの抗体遺伝子のクローニングと同様の方法を用いた。α1 HC発現ベクターにクローニングした抗体遺伝子を利用する場合には、AgeI及びNheIを用いた通常の制限酵素を用いたサブクローニング法を用いた。
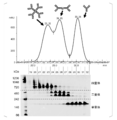
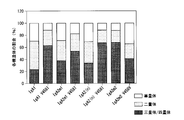
コスモスピンフィルターH(ナカライテスク社)を用いてサンプルを前処理し、サイズ排除クロマトグラフィーにより分子サイズに基づいて分離し、抗体の構造を解析した。HPLCシステムとして、Agilent 1260 Infinity(Agilent Technologies社)を用いた。また、カラムにはAgilent Bio SEC-5 500Å (Agilent Technologies社)を用いた。溶離液にはPBS(pH7.4)を用い、流速は1mL/分の条件で行った。1回の解析あたり抗体サンプルを1μg以上使用した。クロマトグラムはOpenLAB CDS ChemStation Edition(Agilent Technologies社)を用いて解析し、三量体/四量体、二量体、単量体各々に相当するピーク面積を算出し、面積比として比較した。図8Aに、サイズ排除クロマトグラフィーにより得られるクロマトグラムのIgA1、IgA2m1、IgA2m2、IgA2(n)型抗体の代表的な結果を示す。図8Bは、図8Aに基づいて、三量体/四量体、二量体、単量体抗体各々のピーク面積比を算出した結果を示すグラフである。図8Aのクロマトグラムのピーク間の谷又はピークの分離が不明瞭な場合はピークの変曲点を推測し、ベースラインへ垂直の線を引き、各々のフラクションに区分けを行い、クロマトグラムとベースラインに囲まれる面積を算出した。
IgA2m2型抗体の多量体化促進活性について解析するため、以下の解析を行った。
PrimeSTAR(登録商標)MAX DNA Polymeraseを使用して、上述したα1 HC発現ベクターを鋳型として、IgA1 HCのCH1からCH2までの配列(α1セグメント:定常領域のN末端からG342まで)をPCR増幅した。また、α2m2 HC発現ベクターを鋳型として、IgA2m2 HCのCH3以降C末までの配列(α2m2セグメント:N343から定常領域のC末端まで)をPCR増幅した。
IgA2m2の多量体化促進活性について解析するため、各種発現ベクターを以下の通りに構築した。
IgA重鎖定常領域の変異体発現ベクターを構築するため、定常領域にアミノ酸置換を伴わないよう制限酵素部位を付加した定常領域フラグメントIgA1H-NRE(配列番号28)、IgA2m2-NRE(配列番号29)を人工遺伝子合成(Genscript社)により合成した。続いて、IgA1H-NRE、IgA2m2-NREを制限酵素NheI及びHindIIIで処理し、ライゲーション用フラグメントを調製した。
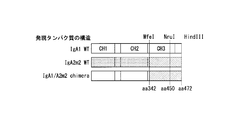
IgA1/IgA2m2キメラ重鎖発現ベクターの構築を以下の通りに行った。すなわち、pIgA2m2H-NREをMfeI及びHindIIIで処理し得られたフラグメントとMfeI及びHindIII処理したpIgA1H-NREとを連結し、IgA1重鎖のアミノ酸342~472番目の領域をIgA2m2型に置換した変異体pIgA1H/pIgA2m2-chimeraを構築した。図10Aは各変異体の構造を示す模式図である。
J鎖、SCの共発現ベクター構築のため、実施例5のpCXSN-cis#1-hJC及びpCXSN-cis#2-hSCより、cis#1-hJC ORF、cis#2-hSC ORFを切り出した。cis#1-hJC ORF、cis#2-hSC ORFをそれぞれヒトEF1プロモーターとBGH polyAから構成される発現ユニット内のプロモーターとpolyAの間に連結し、発現ベクターpEF-cis-hJC/Zeo及びpEF/cis-hSC/Zeoをそれぞれ構築した。
IgA1重鎖のCH3以降C末端までのアミノ酸配列と、これに対応するIgA2m2重鎖のアミノ酸配列とで異なるアミノ酸残基は、第411残基、第428残基、第451残基、第458残基、第467残基の5残基であるため、以下の解析を行った。
重鎖定常領域(Fc領域)のアミノ酸置換変異体を作製した。より具体的には、α2m2 HC発現ベクターを鋳型として、5種のアミノ酸置換(Y411F、E428D、M451L、I458V、A467V)が起こるように配列を改編したプライマーを用いて、PrimeSTAR(登録商標)MAX DNA Polymeraseを使用して、インバースPCRを行った。
実験例13と同様にして、Fc領域のアミノ酸置換変異体の作製及び解析を行った。以下、作製した変異体を「IgA1 F411Y」のように表記する。この場合、IgA1の定常領域の第411残基に相当するアミノ酸フェニルアラニン(F)がチロシン(Y)に置換されている。他の変異体についても同様である。
IgAの多量体化促進活性におけるIgA1重鎖内V458の役割について解析するため、V458の変異体発現ベクターを以下の通りに構築した。
IgA1重鎖458番目のVをアミノ酸各種に置換した変異体を構築するため、pIgA1H-NREを制限酵素MfeI及びHindIIIで処理しライゲーション用フラグメントを調製した。また、インサートリンカーを調製するため、V458I(配列番号32及び33)、V458A(配列番号34及び35)、V458W(配列番号36及び37)、V458C(配列番号38及び39)、V458D(配列番号40及び41)、V458E(配列番号42及び43)、V458F(配列番号44及び45)、V458G(配列番号46及び47)、V458H(配列番号48及び49)、V458K(配列番号50及び51)、V458L(配列番号52及び53)、V458M(配列番号54及び55)、V458N(配列番号56及び57)、V458P(配列番号58及び59)、V458Q(配列番号60及び61)、V458R(配列番号62及び63)、V458S(配列番号64及び65)、V458T(配列番号66及び67)、V458Y(配列番号68及び69)の組み合わせで各DNA断片を95℃で10分熱処理後に段階的に25℃まで下げてアニーリングさせた。
続いて、リポフェクション法により、作製したV458の各種変異体発現ベクターと上述した抗インフルエンザウイルス抗体クローンB12の軽鎖発現ベクター(pIgA-LC)とをC23細胞にそれぞれトランスフェクションした。
(Fc領域のアミノ酸置換変異体の作製)
C23細胞の代わりにExpi293F細胞を用いて実験例15と同様の検討を行った。具体的には、実験例15で作製した、pIgA1H-NRE-V458I、pIgA1H-NRE-V458A、pIgA1H-NRE-V458W、pIgA1H-NRE-V458E、pIgA1H-NRE-V458G、pIgA1H-NRE-V458K、pIgA1H-NRE-V458Lの発現プラスミドを使用し、実験例13と同様の実験を行った。
(Fc領域のアミノ酸置換変異体の作製)
IgA1、IgA2m1、IgA2m2、IgA2(n)について、第458残基の変異体を作製し、多量体化における役割を検討した。α2m1 HCのアミノ酸置換変異体を作製する場合、α2m1 HC発現ベクターを鋳型として、目的のアミノ酸置換(V458I)が起こるように配列を改編したプライマーを用いて、PrimeSTAR(登録商標)MAX DNA Polymeraseを使用したインバースPCRを行った。続いて、増幅したPCR産物の5’末端をT4ポリヌクレオチドキナーゼを用いてリン酸化し、T4DNAリガーゼにより環状に連結させた。続いて、反応産物で大腸菌を形質転換し、プラスミドを抽出し、シークエンスにより目的のアミノ酸置換を起こす変異が導入されたことを確認した。α2(n) HCについても同様にして第458残基のアミノ酸変異を有する変異体を作製した。α1 HCについては実験例14、α2m2 HCは実験例13で作製した変異体を用いた。
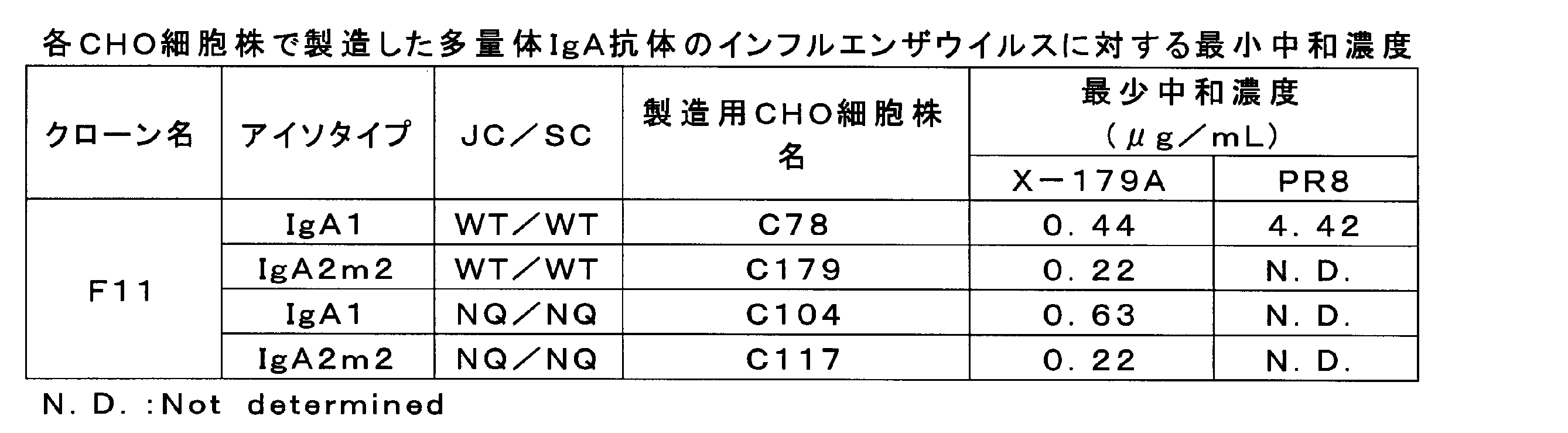
上述したspERt技術を用いて四量体IgA抗体を製造し、以下の方法で解析した。
J/SC安定発現CHO株C23に抗インフルエンザウイルス抗体クローンF11の軽鎖発現ベクターpIgA-LCと、IgA1重鎖発現ベクターpIgA1-HC又はIgA2m2重鎖発現ベクターpIgA2m2-HCとをリポフェクション法にてトランスフェクションした。ピューロマイシン(10μg/ml)による薬剤選択を経て、IgA1重鎖及び軽鎖を安定に発現するCHO株C78、並びにIgA2m2重鎖及び軽鎖を安定に発現するCHO株C179を樹立した。
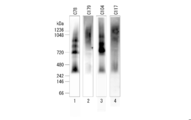
上述した細胞株C78、C179、C104及びC117を、それぞれ5%ウシ胎児血清含有DMEMにて7日間培養し、培養液を低速遠心とポアサイズ0.45μmのフィルターを用いたろ過により清澄化後、IgA抗体をCaptureSelect human Fc affinity matrix(ライフテクノロジーズ社製)を用いて実験例1~4と同様にして精製した。
spERt技術によるIgA抗体の生産性増強効果について検討した。
実験例12に記載の方法と同様にして、p180及びSF3b4を安定に発現するCHO-K1細胞株1C17を樹立した。
各クローンの多量体を作製するため、CHO-K1S細胞に、上述したpIgA-LCと、pEF-cis-hJC/Zeoと、pEF/cis-hSC/Zeoと、pIgA1-HC又はpIgA2m2-HCとをリポフェクション法によりトランスフェクションした。
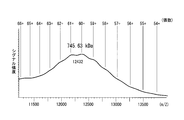
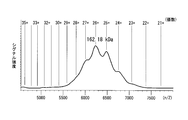
実験例4と同様に調製したIgA1、IgA2m2の多量体(四量体)分画成分の分子量を、質量分析計を用いて測定した。ここで、IgA1にはpCXSN-hSCを用いてタグの無いSCを作製した。また、IgA2m2にはpCXSN-hSC-HisTagを用いてタグ付きSCを発現させて各多量体を作製した。
多量体画分中の各サブユニットの構成比を高精度に定量するため、安定同位体標識ペプチドを内部標準とした質量分析による新規定量方法を確立した。
0~2分:A液(0.1%ギ酸)98%、B液(100%アセトニトリル)2%;
2.1~6分:A液98~50%、B液2~50%;
6.1~8分:A液10%、B液90%;
8.1~10分:A液98%、B液2%。
Claims (15)
- 多量体IgA型遺伝子組換え抗体。
- 重鎖定常領域の第458番目のアミノ酸残基が疎水性アミノ酸に由来するアミノ酸残基である、請求項1に記載の多量体IgA型遺伝子組換え抗体。
- 四量体の含有量が全IgAの20モル%以上である、請求項1又は2に記載の多量体IgA型遺伝子組換え抗体。
- 請求項1~3のいずれか一項に記載の多量体IgA型遺伝子組換え抗体を有効成分として含有する医薬。
- 感染症の治療又は予防用である、請求項4に記載の医薬。
- IgA型抗体重鎖タンパク質、抗体軽鎖タンパク質、抗体J鎖タンパク質及び分泌成分タンパク質を1つの細胞内で共発現させる工程を含む、多量体IgA型抗体の製造方法。
- 前記IgA型抗体重鎖タンパク質は、遺伝子組換えによりIgG型からIgA型に変換されたものである、請求項6に記載の製造方法。
- 前記工程において、更にp180タンパク質及びSF3b4タンパク質を前記細胞内で共発現させる、請求項6又は7に記載の製造方法。
- 前記細胞がCHO YA7細胞株(受託番号NITE BP-01535)である、請求項6~8のいずれか一項に記載の製造方法。
- 前記工程は、IgA型抗体重鎖タンパク質、抗体軽鎖タンパク質、抗体J鎖タンパク質及び分泌成分タンパク質を発現するための発現ベクターを前記細胞内に導入することにより行われ、
前記発現ベクターは、プロモーターの下流で、かつ、IgA型抗体重鎖タンパク質、抗体軽鎖タンパク質、抗体J鎖タンパク質又は分泌成分タンパク質をコードする核酸の開始コドンの上流に、RNA結合タンパク質が認識、結合又は相互作用するcis-エレメントを有する、請求項6~9のいずれか一項に記載の製造方法。 - 前記cis-エレメントが、配列モチーフGAN1-(X)n-ACN2(nは3~6の整数であり、N1及びN2は、それぞれ独立して、A、T、G、Cのいずれかである。)からなる塩基配列を1~数個含む、請求項10に記載の製造方法。
- 前記cis-エレメントが、
配列番号21~23のいずれかに示される塩基配列、
配列番号21~23のいずれかに示される塩基配列において、1~数個の塩基が欠失、置換又は付加されている塩基配列からなり、かつRNA結合タンパク質が認識、結合若しくは相互作用する塩基配列、
配列番号21~23のいずれかに示される塩基配列と同一性が80%以上である塩基配列からなり、かつ、RNA結合タンパク質が認識、結合若しくは相互作用する塩基配列、又は、
配列番号21~23のいずれかに示される塩基配列からなる核酸と相補的な塩基配列からなる核酸とストリンジェントな条件下でハイブリダイズすることができる塩基配列からなり、かつRNA結合タンパク質が認識、結合若しくは相互作用する塩基配列からなる、請求項10又は11に記載の製造方法。 - 抗体を多量体IgA型化する工程を含む、前記抗体の抗原結合活性又は中和活性を向上させる方法。
- 前記抗体は、IgG型抗体である、請求項13に記載の方法。
- 前記工程が、前記抗体の重鎖可変領域を有するIgA型抗体重鎖タンパク質、前記抗体の軽鎖タンパク質、抗体J鎖タンパク質及び分泌成分タンパク質を1つの細胞内で共発現させる工程を含む、請求項13又は14に記載の方法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20196341.0A EP3786181A1 (en) | 2014-07-18 | 2015-07-21 | Polymeric iga-type recombinant antibody and use thereof |
| JP2016534515A JP6564777B2 (ja) | 2014-07-18 | 2015-07-21 | 多量体IgA型遺伝子組換え抗体を含む組成物及びその利用 |
| US15/326,569 US10925962B2 (en) | 2014-07-18 | 2015-07-21 | Polymeric IgA-type recombinant antibody and use thereof |
| EP15822054.1A EP3170839B1 (en) | 2014-07-18 | 2015-07-21 | POLYMERIC IgA-TYPE RECOMBINANT ANTIBODY AND USE THEREOF |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014148328 | 2014-07-18 | ||
| JP2014-148328 | 2014-07-18 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2016010161A1 true WO2016010161A1 (ja) | 2016-01-21 |
Family
ID=55078646
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2015/070742 WO2016010161A1 (ja) | 2014-07-18 | 2015-07-21 | 多量体IgA型遺伝子組換え抗体及びその利用 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US10925962B2 (ja) |
| EP (2) | EP3786181A1 (ja) |
| JP (1) | JP6564777B2 (ja) |
| WO (1) | WO2016010161A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2671477C2 (ru) * | 2016-12-30 | 2018-10-31 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Московский государственный университет имени М.В. Ломоносова" (МГУ) | РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA2m1F16-ht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IGA2m1 |
| WO2021193553A1 (ja) * | 2020-03-23 | 2021-09-30 | 東興薬品工業株式会社 | 多量体IgA抗体の作製法及び多重特異性多量体IgA抗体 |
| JP2022522985A (ja) * | 2019-01-22 | 2022-04-21 | ジェネンテック, インコーポレイテッド | 免疫グロブリンa抗体、並びに産生及び使用の方法 |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20220004979A (ko) | 2019-03-27 | 2022-01-12 | 유엠씨 우트레크트 홀딩 비.브이. | 조작된 iga 항체 및 사용 방법 |
| US20220033851A1 (en) * | 2020-08-03 | 2022-02-03 | Roger B. Swartz | mRNA, episomal and genomic integrated lentiviral and gammaretroviral vector expression of dimeric immunoglobulin A and polymeric immunoglobulin A to Enable Mucosal and Hematological Based Immunity/Protection via Gene Therapy for Allergens, viruses, HIV, bacteria, pneumonia, infections, pathology associated proteins, systemic pathologies, cancer, toxins and unnatural viruses. CAR engineered and non-CAR engineered immune cell expression of dimeric immunoglobulin A and polymeric immunoglobulin A. |
| CA3229487A1 (en) * | 2021-08-20 | 2023-02-23 | Adam WAICKMAN | Iga monoclonal antibodies for treating flavivirus infection |
| WO2023044419A2 (en) * | 2021-09-17 | 2023-03-23 | The Board Of Trustees Of The University Of Illinois | Chimeric secretory component polypeptides and uses thereof |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013087914A1 (en) * | 2011-12-16 | 2013-06-20 | Synthon Biopharmaceuticals B.V. | EXPRESSION OF SECRETORY IgA ANTIBODIES IN DUCKWEED |
| WO2014157429A1 (ja) * | 2013-03-26 | 2014-10-02 | 株式会社 ニッピ | タンパク質の製造方法 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995004081A1 (en) * | 1993-07-30 | 1995-02-09 | Oravax, Inc. | MONOCLONAL IgA ANTIBODY AGAINST RESPIRATORY SYNCYTIAL VIRUS |
| US6063905A (en) * | 1997-01-07 | 2000-05-16 | Board Of Regents, The University Of Texas System | Recombinant human IGA-J. chain dimer |
| JP6086743B2 (ja) | 2013-01-31 | 2017-03-01 | 株式会社吉野工業所 | 詰め替え容器 |
-
2015
- 2015-07-21 US US15/326,569 patent/US10925962B2/en active Active
- 2015-07-21 EP EP20196341.0A patent/EP3786181A1/en not_active Withdrawn
- 2015-07-21 JP JP2016534515A patent/JP6564777B2/ja active Active
- 2015-07-21 WO PCT/JP2015/070742 patent/WO2016010161A1/ja active Application Filing
- 2015-07-21 EP EP15822054.1A patent/EP3170839B1/en active Active
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013087914A1 (en) * | 2011-12-16 | 2013-06-20 | Synthon Biopharmaceuticals B.V. | EXPRESSION OF SECRETORY IgA ANTIBODIES IN DUCKWEED |
| WO2014157429A1 (ja) * | 2013-03-26 | 2014-10-02 | 株式会社 ニッピ | タンパク質の製造方法 |
Non-Patent Citations (5)
| Title |
|---|
| JOHANSEN, FE. ET AL.: "Recombinant expression of polymeric IgA: incorporation of J chain and secretory component of human origin", EUROPEAN JOURNAL OF IMMUNOLOGY, vol. 29, no. 5, 1999, pages 1701 - 1708, XP002331960, DOI: doi:10.1002/(SICI)1521-4141(199905)29:05<1701::AID-IMMU1701>3.0.CO;2-Z * |
| LI, C. ET AL.: "Construction of a Chimeric Secretory IgA and Its Neutralization Activity against Avian Influenza Virus H5N1", JOURNAL OF IMMUNOLOGY RESEARCH, vol. 394127, 13 February 2014 (2014-02-13), pages 1 - 10, XP055385659 * |
| LORIN, V. ET AL.: "Efficient generation of human IgA monoclonal antibodies", JOURNAL OF IMMUNOLOGICAL METHODS, vol. 422, 22 April 2015 (2015-04-22), pages 102 - 110, XP029239942, DOI: doi:10.1016/j.jim.2015.04.010 * |
| MURAMATSU, M. ET AL.: "Comparison of Antiviral Activity between IgA and IgG Specific to Influenza Virus Hemagglutinin: Increased Potential of IgA for Heterosubtypic Immunity", PLOS ONE, vol. 9, no. 1, 17 January 2014 (2014-01-17), pages e85582, XP055385668 * |
| See also references of EP3170839A4 * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2671477C2 (ru) * | 2016-12-30 | 2018-10-31 | Федеральное государственное бюджетное образовательное учреждение высшего образования "Московский государственный университет имени М.В. Ломоносова" (МГУ) | РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pBiPr-ABIgA2m1F16-ht ДЛЯ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИММУНОГЛОБУЛИНА А ИЗОТИПА IGA2m1 |
| JP2022522985A (ja) * | 2019-01-22 | 2022-04-21 | ジェネンテック, インコーポレイテッド | 免疫グロブリンa抗体、並びに産生及び使用の方法 |
| WO2021193553A1 (ja) * | 2020-03-23 | 2021-09-30 | 東興薬品工業株式会社 | 多量体IgA抗体の作製法及び多重特異性多量体IgA抗体 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3170839A1 (en) | 2017-05-24 |
| US10925962B2 (en) | 2021-02-23 |
| JPWO2016010161A1 (ja) | 2017-06-01 |
| EP3170839B1 (en) | 2020-10-28 |
| JP6564777B2 (ja) | 2019-08-21 |
| US20170340732A1 (en) | 2017-11-30 |
| EP3786181A1 (en) | 2021-03-03 |
| EP3170839A4 (en) | 2018-01-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6564777B2 (ja) | 多量体IgA型遺伝子組換え抗体を含む組成物及びその利用 | |
| CA2956000C (en) | An anti-ctla4 monoclonal antibody or antigen binding fragment thereof, a pharmaceutical composition and use | |
| US11926657B2 (en) | Neutralizing anti-influenza binding molecules and uses thereof | |
| AU2016363455A1 (en) | Full human antibody against respiratory syncytial virus | |
| CA3052903A1 (en) | Anti human annexin a1 antibody | |
| JPWO2016010160A1 (ja) | 抗インフルエンザウイルス抗体及びその利用 | |
| CN105542003B (zh) | 一种针对rsv粘附g蛋白表面抗原的全人源单克隆抗体 | |
| RU2777073C1 (ru) | Однодоменное антитело для нейтрализации вирусов и его модификации, и способ их применения для экстренной профилактики заболеваний, вызываемых вирусом гриппа А | |
| WO2023105087A1 (en) | Novel flt3 antibodies and antibody-drug-conjugates based thereon, therapeutic methods and uses thereof in combination with tyrosine kinase inhibitors | |
| TW202411247A (zh) | 針對流感神經胺酸酶的廣泛中和抗體 | |
| EP3122772A1 (en) | Chimerization and characterization of a monoclonal antibody with potent neutralizing activity across multiple influenza a h5n1 clades | |
| NZ505932A (en) | Human cmrf-35-h9 receptor which binds IgM |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 15822054 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2016534515 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2015822054 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2015822054 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15326569 Country of ref document: US |