TW202140010A - 控釋組合物 - Google Patents
控釋組合物 Download PDFInfo
- Publication number
- TW202140010A TW202140010A TW110103421A TW110103421A TW202140010A TW 202140010 A TW202140010 A TW 202140010A TW 110103421 A TW110103421 A TW 110103421A TW 110103421 A TW110103421 A TW 110103421A TW 202140010 A TW202140010 A TW 202140010A
- Authority
- TW
- Taiwan
- Prior art keywords
- release composition
- controlled release
- water
- composition according
- soluble polymer
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2031—Organic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, polyethylene oxide, poloxamers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
- A61K9/2866—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
Landscapes
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Diabetes (AREA)
- Epidemiology (AREA)
- Cardiology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Neurosurgery (AREA)
- Heart & Thoracic Surgery (AREA)
- Neurology (AREA)
- Endocrinology (AREA)
- Pulmonology (AREA)
- Dermatology (AREA)
- Urology & Nephrology (AREA)
- Obesity (AREA)
- Emergency Medicine (AREA)
- Psychology (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本發明之一個目的係提供控釋組合物,該控釋組合物可防止活性成分之血中濃度突然升高且可長時間維持血中濃度。
Description
本發明係關於一種控釋組合物,其包含(1)水溶性聚合物,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。本發明亦關於控釋組合物,其包含(1)水溶性聚合物,(2)水溶性添加劑,及(3)至少一種活性成分,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。此外,本發明係關於一種本發明之控釋組合物之用途,一種藉由投與本發明之控釋組合物來預防及/或治療疾病之方法,及一種製備本發明之控釋組合物之方法。
持續釋放型組合物可逐漸釋放活性成分,且因此可在長時間內維持活性成分之血中濃度。持續釋放型組合物具有諸如以下之優點:由於活性成分之持續釋放而致活性成分功效持續,降低由於防止活性成分之血中濃度突然升高所致之副作用,由於投藥頻率降低而減少麻煩的用藥及防止用藥無效,及提高用藥順服性,且因此,最近,已對於許多活性成分推進持續釋放型組合物之開發。水凝膠基質製劑為持續釋放型調配物之一個實例。水凝膠基質製劑可藉由調整凝膠基質材料之膠凝速率或速度來控制活性成分之釋放。
已知希樂普,2-{4-[N-(5,6-二苯基吡嗪-2-基)-N-異丙基胺基]丁基氧基}-N-(甲基磺醯基)乙醯胺(後文稱為「化合物A」)具有極佳前列腺素I2
(後文稱為「PGI2
」)受體促效作用且顯示各種醫學作用,諸如血小板聚集抑制作用、血管擴張作用、支氣管平滑肌擴張作用、脂質沉積抑制作用及白血球活化抑制作用(參見,例如PTL 1至PTL 6)。目前,包含化合物A作為活性成分之製劑係以常見錠劑之形式用作肺動脈高血壓之治療劑(PTL 7)。
[引文清單]
[專利文獻]
[PTL 1] WO 2002/088084
[PTL 2] WO 2009/157396
[PTL 3] WO 2009/107736
[PTL 4] WO 2009/154246
[PTL 5] WO 2009/157397
[PTL 6] WO 2009/157398
[PTL 7] WO 2017/098998
[PTL 8] WO 2010/150865
[PTL 9] US 2014/0221397
[PTL 10] US 2011/0178103
[PTL 11] US 2011/0015211
[PTL 12] US 2011/0118254
[PTL 13] US 2011/0105518
[非專利文獻]
[NPL 1] Uptravi Tablets 0.2 mg, Uptravi Tablets 0.4 mg, Pharmaceutical Interview Form revised on November 2016 (第2版)
[NPL 2] Hepatology,2007,第45卷,第1期,第159至169頁
[NPL 3] PubMed: Nihon Yakurigaku Zasshi,2001年2月,117(2),第123至130頁,摘要
[NPL 4] International Angiology,29,增刊1至第2期,第49至54頁,2010
[NPL 5] Japanese Journal of Clinical Immunology,第16卷,第5期,第409至414頁,1993
[NPL 6] Japanese Journal of Thrombosis and Hemostasis,第1卷,第2期,第94至105頁,1990,摘要
[NPL 7] The Journal of Rheumatology,第36卷,第10期,第2244至2249頁,2009
[NPL 8] The Japanese Journal of Pharmacology,第43卷,第1期,第81至90頁,1987
[NPL 9] British Heart Journal,第53卷,第2期,第173至179頁,1985
[NPL 10] The Lancet,1,4880,pt 1,第569至572頁,1981
[NPL 11] European Journal of Pharmacology,449,第167至176頁,2002
[NPL 12] The Journal of Clinical Investigation,117,第464至72頁,2007
[NPL 13] American Journal of Physiology Lung Cellular and Molecular Physiology,296: L648-L656,2009
[技術問題]
本發明之一個目的係提供可防止活性成分之血中濃度突然升高且可長時間維持血中濃度之控釋組合物。
[問題解決方案]
作為用於達成以上目的之深入研究的結果,本發明者發現包含化合物A作為活性成分之醫藥組合物中存在化合物A之控制釋放在哺乳動物中可變之問題。
本發明者亦已發現,包含可形成具有一定膠凝強度之水凝膠之水溶性聚合物之控釋組合物可長時間維持化合物A之血中濃度,且因此完成本發明。
亦即,本發明係關於如以下[1]至[29]中任一項之控釋組合物(後文亦稱為「本發明之控釋組合物」)。此外,本發明係關於如以下[30]至[32]之控釋組合物之用途,藉由投與控釋組合物來預防及/或治療疾病之方法及製備控釋組合物之方法。
[1] 一種控釋組合物,其包含(1)水溶性聚合物,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。
[2] 如[1]之控釋組合物,其中(1)水溶性聚合物之水溶液在10重量%或更小之濃度下具有1000 mPa・s或更大之黏度。
[3] 如[1]之控釋組合物,其中(1)水溶性聚合物為選自包含聚環氧乙烷(PEO);纖維素衍生物,較佳地羥丙基甲基纖維素(hypromellose;HPMC)、甲基纖維素、羥乙基纖維素、羥丙基纖維素(HPC)、羥乙基甲基纖維素、羧甲基纖維素、羧甲基纖維素鈉;聚乙烯醇(PVA);海藻酸;海藻酸之鹼金屬鹽;海藻酸銨;角叉菜膠;黃原膠及阿拉伯膠(Arabic gum)之群之至少一者。
[4] 如[1]之控釋組合物,其中(1)水溶性聚合物為基於組合物總重量計25至70重量%。
[5] 如[1]至[4]中任一項之控釋組合物,其進一步包含(2)水溶性添加劑。
[6] 如[5]之控釋組合物,其中可將1 g (2)水溶性添加劑溶解於6 ml或更少之水中。
[7] 如[5]或[6]中任一項之控釋組合物,其中(2)水溶性添加劑為選自包含聚乙烯吡咯啶酮(PVP)及糖(較佳糖醇)之群之至少一者。
[8] 如[5]至[7]中任一項之控釋組合物,其中(2)水溶性添加劑為基於組合物總重量計20至65重量%。
[9] 如[1]至[8]中任一項之控釋組合物,其進一步包含(3)活性成分。
[10] 如[9]之控釋組合物,其中(3)活性成分為希樂普。
[11] 如[9]或[10]之控釋組合物,其中(3)活性成分為基於組合物總重量計0.05至1重量%。
[12] 如[1]至[11]中任一項之控釋組合物,其中(1)水溶性聚合物及(2)水溶性添加劑之比為1:0.3至1:2.5。
[13] 如[1]至[12]中任一項之控釋組合物,其中(1)水溶性聚合物為選自包含聚環氧乙烷(PEO)及羥丙基甲基纖維素(HPMC)之群之至少一者。
[14] 如[13]之控釋組合物,其中該PEO之分子量之範圍為900,000至7,000,000,較佳地2,000,000至7,000,000。
[15] 如[13]或[14]之控釋組合物,其中該PEO為基於組合物總重量計20至70重量%。
[16] 如[13]至[15]中任一項之控釋組合物,其中在2重量%之濃度下,該HPMC之水溶液之黏度之範圍為3000至140000 mP・s。
[17] 如[13]至[16]中任一項之控釋組合物,其中該HPMC為基於組合物總重量計5至20重量%。
[18] 如[5]至[17]中任一項之控釋組合物,其中(2)水溶性添加劑為選自包含聚乙烯吡咯啶酮(PVP)及D-甘露醇之群之至少一者。
[19] 如[18]之控釋組合物,其中該PVP之K值為10至120,較佳20至40。
[20] 如[18]或[19]之控釋組合物,其中該PVP為基於組合物總重量計10至65重量%。
[21] 如[18]至[20]中任一項之控釋組合物,其中D-甘露醇為基於組合物總重量計10至25重量%。
[22] 如[1]至[21]中任一項之控釋組合物,其中該水凝膠之強度為小於5N。
[23] 如[1]至[22]中任一項之控釋組合物,其中該水凝膠之強度係在將組合物放入37℃的水中6小時後藉由移動速度為10 mm/min及感測器尺寸為13.3 mm直徑之流變儀測定。
[24] 如[1]至[23]中任一項之控釋組合物,其中該控釋組合物係呈錠劑或膜衣錠之形式。
[25] 一種控釋組合物,其包含(1)水溶性聚合物,(2)水溶性添加劑,及(3)至少一種活性成分,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。
[26] 如[1]至[25]中任一項之控釋組合物,其中該活性成分之釋放率在溶解測試中於6小時後為0至50%及/或在溶解測試中於24小時後為70至100%。
[27] 如[1]至[26]中任一項之控釋組合物,其中該控釋組合物具有400至800%之保水力。
[28] 如[1]至[27]中任一項之控釋組合物,其係用於治療疾病。
[29] 如[28]之控釋組合物,其中該疾病為選自包含與糖尿病性神經病變、糖尿病性壞疽、周邊循環紊亂、慢性動脈阻塞、間歇性跛行、硬皮病、血栓形成、肺動脈高血壓、心肌梗塞、心絞痛、腎絲球腎炎、糖尿病性腎病、慢性腎衰竭、支氣管哮喘、間質性肺炎、肺纖維化、慢性阻塞性肺病、腎小管間質性腎炎、發炎性腸病或與椎管狹窄相關之症狀之群之至少一者。
[30] 一種如[1]至[29]中任一項之控釋組合物於製造用於治療疾病的藥物之用途。
[31] 一種預防及/或治療疾病之方法,該方法包括對有此需要的個體投與適宜量之如[1]至[29]中任一項之控釋組合物。
[32] 一種製備如[1]至[29]中任一項之控釋組合物之方法。
本發明係關於一種控釋組合物,其包含(1)水溶性聚合物,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。本發明亦關於一種控釋組合物,其包含(1)水溶性聚合物,(2)水溶性添加劑,及(3)至少一種活性成分,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。此外,本發明係關於一種藉由投與本發明之控釋組合物來預防及/或治療疾病之方法,及一種製備本發明之控釋組合物之方法。後文中,詳細描述本發明。
(1)水溶性聚合物
「水溶性聚合物」如本文所用係指當其溶解在水中時變得高度黏性之聚合物。
在本發明之一個實施例中,(1)水溶性聚合物之水溶液在10重量%或更小之濃度下具有1000 mPa・s或更大之黏度。
特別地,水溶性聚合物之水溶液在25℃下具有1000 mPa•s或更大之黏度,較佳地在25℃下濃度為0.01至10重量%,更佳地在25℃下濃度為0.1至10重量%,又更佳地在25℃下濃度為1.0至10重量%。
在本發明之一個實施例中,濃度為10重量%或更小之(1)水溶性聚合物之水溶液在25℃下具有在1000至2000 mPa•s範圍內之黏度。
對於意欲用於本發明之控釋組合物中之水溶性聚合物,若濃度為10重量%或更小之聚合物水溶液之黏度在25℃下超過2000 mPa•s,則可調整該溶液之濃度以將黏度降低至2000 mPa•s或更小。
在本發明之一個實施例中,水溶性聚合物之水溶液之黏度可在將水溶性聚合物溶解在水中且使所得溶液保持在25℃約24小時以製備樣品之後使用旋轉黏度計(Rheometer R/S Plus,由Brookfield,Inc.製造)來測定。測量係在25℃之測量溫度及10 rpm之旋轉速度下進行,及黏度係在測量開始300秒後進行測量。
在本發明之一個實施例中,本發明之控釋組合物中水溶性聚合物之含量並無特定限制,若該水溶性聚合物形成具有適宜膠凝強度之水凝膠,則上限為例如相對於控釋組合物總重量計70重量%、55重量%或45重量%,下限為例如相對於控釋組合物重量計25重量%、30重量%或40重量%。上限及下限可組合使用,例如在相對於控釋組合物總重量計25重量%至70重量%之範圍內。
在本發明之一個實施例中,水溶性聚合物之實例包括聚環氧乙烷(PEO)、羥丙基甲基纖維素(HPMC)、甲基纖維素、羥乙基纖維素、羥丙基纖維素(HPC)、羥乙基甲基纖維素、羧甲基纖維素、羧甲基纖維素鈉、聚乙烯醇(PVA)、海藻酸、海藻酸之鹼金屬鹽、海藻酸銨、角叉菜膠、黃原膠及阿拉伯膠。特別地,以PEO及HPMC為較佳。
在本發明之一個實施例中,水溶性聚合物可單獨或組合使用且可選自聚環氧乙烷(PEO)、羥丙基甲基纖維素(HPMC)、甲基纖維素、羥乙基纖維素、羥丙基纖維素(HPC)、羥乙基甲基纖維素、羧甲基纖維素、羧甲基纖維素鈉、聚乙烯醇(PVA)、海藻酸、海藻酸之鹼金屬鹽、海藻酸銨、角叉菜膠、黃原膠及阿拉伯膠之群之至少一者,較佳係選自PEO及HPMC之群之至少一者。
在本發明之一個實施例中,PEO之分子量之範圍為900,000至7,000,000,較佳地2,000,000至7,000,000。
在本發明之一個實施例中,該PEO為基於組合物總重量計20至70重量%。
HPMC為分子中具有羥基丙氧基及甲氧基之纖維素衍生物。
在本發明之一個實施例中,在2重量%之濃度下,該HPMC之水溶液之黏度之範圍為3000至140000 mP・s。
在本發明之一個實施例中,該HPMC為基於組合物總重量計5至20重量%。
在本發明之一個實施例中,HPMC之實例包括Metolose®
60SH-4000SR (由Shin-Etsu Chemical Co., Ltd.製造)、Metolose®
60SH-8000SR (Shin-Etsu Chemical Co., Ltd.)、Metolose®
65SH-4000SR (由Shin-Etsu Chemical Co., Ltd.製造)、Metolose®
65SH-15000SR (Shin-Etsu Chemical Co., Ltd.)、Metolose®
90SH-100SR (由Shin-Etsu Chemical Co., Ltd.製造)、Metolose®
90SH-4000SR (由Shin-Etsu Chemical Co., Ltd.製造)、Metolose®
90SH-15000SR (由Shin-Etsu Chemical Co., Ltd.製造)及Metolose 90SH-100000SR (由Shin-Etsu Chemical Co., Ltd.製造),且任何此等等效物可以市售產品獲得。
HPC為分子中具有羥基丙氧基之纖維素衍生物。在本發明之一個實施例中,HPC之實例包括Klucel®
HXF (由Ashland, Inc.製造)、Klucel®
MXF (由Ashland, Inc.製造)、Klucel®
GXF (由Ashland, Inc.製造)、NISSO HPC H (由Nippon Soda Co., Ltd.製造)及NISSO HPC VH (由Nippon Soda Co., Ltd.製造),且任何此等等效物可以市售產品獲得。
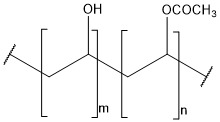
PVA為由以下通式表示且藉由聚乙酸乙烯酯之皂化獲得之聚合物化合物,該聚乙酸乙烯酯係藉由使乙酸乙烯酯單體聚合獲得。
[化學式1]
(於式中,m及n各代表正整數。)
在本發明之一個實施例中,PVA之實例包括Gohsenol®
EG-48P (由Nippon Synthetic Chemical Industry Co., Ltd.製造)及Parteck®
SRP80 (由Merck,Inc.製造),且此等中之任一者可以市售產品獲得。
在本發明之一個實施例中,海藻酸之鹼金屬鹽之實例包括海藻酸鈉及海藻酸鉀。
(2)水溶性添加劑
「水溶性添加劑」如本文所用係指可溶解在水中之添加劑。
在本發明之一個實施例中,較佳地1 g「水溶性添加劑」可溶解在6 ml或更少之水中。
在本發明之一個實施例中,本發明之控釋組合物中「水溶性添加劑」之含量並無特定限制,若該水溶性聚合物形成具有適宜膠凝強度之水凝膠,則上限為例如相對於控釋組合物總重量計65重量%、50重量%或40重量%,下限為例如相對於控釋組合物重量計25重量%、30重量%或40重量%。上限及下限可組合使用,例如在相對於控釋組合物總重量計20重量%至65重量%之範圍內。
在本發明之一個實施例中,「水溶性添加劑」為選自聚乙烯吡咯啶酮(PVP)及糖醇之群之至少一者。
在本發明之一個實施例中,「水溶性添加劑」為聚乙烯吡咯啶酮(PVP)。
在本發明之一個實施例中,PVP之K值為10至120,較佳20至40。
在本發明之一個實施例中,「水溶性添加劑」為糖醇,較佳地D-甘露醇。
在本發明之一個實施例中,D-甘露醇為基於組合物總重量計10至25重量%。
在本發明之一個實施例中,(1)水溶性聚合物及(2)水溶性添加劑之比值並無特定限制,但為1:0.3至1:2.5。
(3)活性成分
在本發明之一個實施例中,本發明之控釋組合物可包含活性成分。
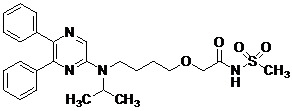
在本發明之一個實施例中,活性成分為諸如2-{4-[N-(5,6-二苯基吡嗪-2-基)-N-異丙基胺基]丁基氧基}-N-(甲基磺醯基)乙醯胺(後文稱為「化合物A」)。
[化學式2]
化合物A為描述於例如PTL 1及PTL 8中之已知化合物,且可由熟習此項技術者根據描述於此等專利文獻中之方法容易地獲得。
在本發明之一個實施例中,化合物A可為光學異構體、醫藥上可接受之鹽、非晶型形式(參見WO2017/029594、WO2017/042731、WO2018/015975等)或其晶體形式、或其混合物,尤其是化合物A之晶體形式。化合物A為希樂普(selexipag)且希樂普之溶解度在第17版日本藥典被歸類為「幾乎不溶、或不溶」。
本發明之控釋組合物中化合物A之此種晶體形式之實例包括化合物A之形式-I晶體、形式-II晶體及形式-III晶體以及化合物A之形式-IV至-IX晶體(參見WO2017/040872、WO2018/022704、WO2018/015974等)。
特別地,以如以下所列的化合物A之形式-I、形式-II及形式-III晶體為較佳,且以化合物A之形式-I晶體為更佳。
已知化合物A具有例如以下三種晶體形式(參見,例如PTL 8)。
(1)化合物A之形式-I晶體,使用Cu-Kα輻射(λ=1.54 Å)獲得其之粉末X射線繞射圖,且其在化合物A之粉末X射線繞射光譜中在以下繞射角(2θ)處顯示繞射峰:9.4°、9.8°、17.2°及19.4°。
(2)化合物A之形式-II晶體,使用Cu-Kα輻射(λ=1.54 Å)獲得其之粉末X射線繞射圖,且其在化合物A之粉末X射線繞射光譜中在以下繞射角(2θ)處顯示繞射峰:9.0°、12.9°、20.7°及22.6°。
(3)化合物A之形式-III晶體,使用Cu-Kα輻射(λ=1.54 Å)獲得其之粉末X射線繞射圖,且其在化合物A之粉末X射線繞射光譜中在以下繞射角(2θ)處顯示繞射峰:9.3°、9.7°、16.8°、20.6°及23.5°。
以上三種晶體形式之粉末X射線繞射光譜圖表顯示於圖1至3中。此等晶體形式之粉末X射線繞射光譜使用RINT-Ultima III (由Rigaku Corporation製造)來測量 (標靶:Cu,電壓:40 kV,電流:40 mA,掃描速度:4°/min)。
在本發明之一個實施例中,本發明之控釋組合物之活性成分可為化合物A之活性形式,其為下式之化合物:,
後文稱為「化合物B」。
在本發明之一個實施例中,化合物B可為光學異構體、醫藥上可接受之鹽、其非晶型形式或晶體形式、或其混合物,作為活性成分。
在本發明之一個實施例中,為本發明之控釋組合物之活性成分之化合物A之含量並無特定限制,但較佳在相對於控釋組合物總重量計0.05重量%至1.0重量%之範圍內。
(4)水凝膠之強度
一種控釋組合物,其包含(1)水溶性聚合物,且該水溶性聚合物在水中形成水凝膠,該水凝膠具有一定強度。
在本發明之一個實施例中,水凝膠之強度之上限為10N,較佳為5N,且下限並無特定限制,假若可測量強度,例如0.2N。上限及下限可組合使用。特別地,水凝膠之強度例如為小於10N、小於5N、0.2N至10N、及0.2N至5N。
在本發明之一個實施例中,水凝膠之強度係在將本發明之組合物放入37℃的水中6小時後藉由移動速度為10 mm/min及感測器尺寸為13.3 mm直徑之流變儀來測量。
在本發明之一個實施例中,水凝膠之強度可特定如下測量;
(I) 將錠劑放在不鏽鋼篩(JIS Z 8801,2006,孔徑:1 mm,線徑(WIRE DIA):0.56 mm)上,且然後將該組錠劑及篩浸泡於37℃水中。6小時後,自水取出該組錠劑及篩。
(II) 將篩上的錠劑自頂部壓下且記錄負載之時間依賴性變化(單位:N)以便計算錠劑之膠凝強度。
設備:數位式測力計(IMADA,ZTA-50N)及標準型立式電動試驗台(IMADA,MX2-500N)
條件:移動速度10 mm/min,感測器形狀13.3 mm直徑平頭 (IMADA、A-2、及每0.1秒數據採樣率
(III) 膠凝強度定義為負載(單位:N)相對於時間之反曲點。反曲點經計算為滿足以下條件(i)至(iv)之F (n)之最小值。
(i) ΔF(n)=F(n+1)-F(n)
(ii) ΔF(n)>0.1 N
(iii) ΔF(n)>2ΔF(n-1)
(iv) ΔF(n+1)>2ΔF(n-1)
F(n)為在第n次中測得的負載。
(5)活性成分之釋放率
在本發明之一個實施例中,根據第17版日本藥典(例如JP溶解測試方法2(槳法)),本發明之控釋組合物在溶解測試中於6小時後具有0至50%之活性成分釋放率及/或在溶解測試中於24小時後具有70至100%之活性成分釋放率,測試液體:900 mL JP 第2版溶解測試流體,槳速:200 rpm,及液體溫度:37℃。
在本發明之一個實施例中,控釋組合物形成在溶解測試中6小時不崩解之水凝膠。
(6)保水力
在本發明之一個實施例中,本發明之控釋組合物具有400至800%之保水力。
(7)其他添加劑
在本發明之一個實施例中,本發明之控釋組合物可包含除以上提及之組分以外的醫藥上可接受之添加劑,只要不抑制本發明之作用即可。例如,添加劑諸如賦形劑、黏結劑、崩解劑、流化劑、潤滑劑、塑化劑、着色劑、味道掩蔽劑或矯味劑可根據需要以適當量摻合在其中。此等添加劑可單獨使用,或此等添加劑中之兩者或更多者可組合使用。
在本發明之一個實施例中,「其他添加劑」之量並無特定限制,但例如在相對於控釋組合物總重量計0重量%至55重量%之範圍內。
在本發明之一個實施例中,其他添加劑之實例包括玉米澱粉、微晶纖維素、經低取代之羥丙基纖維素及硬脂酸鎂。
在本發明之一個實施例中,添加劑之實例包括羥丙基甲基纖維素2910 ( 6 mPa・s)、丙二醇、二氧化鈦、黃氧化鐵、氧化鐵紅及用於塗佈之棕櫚蠟。
(8)其他活性成分
在本發明之一個實施例中,只要其不抑制本發明之作用,除如以上所述之組分外,本發明之控釋組合物可包含醫藥活性成分,諸如用於治療或預防如以上所述的疾病之藥劑、用於如以上所述的疾病之研究性新穎活性成分及類似者。
(9)控釋組合物之形狀
在本發明之一個實施例中,本發明之控釋組合物之形狀可為(但不限於)圓形、橢圓形、長橢圓形、奇形怪狀(odd shape) (諸如甜甜圈形狀(doughnut shape))或類似者。
本發明之控釋組合物之錠劑厚度並無特定限制,但適宜地例如在1 mm至10 mm之範圍內,且較佳在2 mm至9 mm之範圍內。
本發明之控釋組合物之尺寸並無特定限制,然而,例如短軸(就圓形錠劑而言,直徑)適宜地在1 mm至20 mm之範圍內,且較佳例如在2 mm至14 mm之範圍內。
本發明之控釋組合物之重量並無特定限制,但適宜地在5 mg至1000 mg之範圍內。
(10)用於製備本發明之控釋組合物之方法
本發明之控釋組合物可使用以上提及的各種類型之添加劑藉由醫藥技術領域中之習知方法來製備。
本發明之控釋組合物可藉由例如以下來製備:將作為活性成分之化合物A與各種類型之添加劑混合,接著直接壓縮模製,或藉由將作為活性成分之化合物A及各種類型之添加劑造粒,接著壓縮模製所得顆粒本身或所得顆粒與另一添加劑之混合物。
壓縮模製方法並無特定限制,及可適宜地選擇已知裝置,及可以例如使用裝置,諸如壓縮測試裝置、油壓機或製錠機器或類似者之方法為例。壓縮測試裝置之實例包括通用材料測試裝置(AUTOGRAPH,由Shimadzu Corporation製造)。製錠機器之實例包括旋轉製錠機器(Clean Press Correct 12,由Kikusui Seisakusho,Ltd.製造)。
關於壓縮模製時的壓力,可適宜地選擇適於所需裝置及所需壓縮模製材料之條件。
此外,可藉由用以上提及的壓縮模製材料填充膠囊來製備膠囊調配物。作為膠囊,可使用已知膠囊,及可以例如明膠膠囊及HPMC膠囊為例。膠囊之尺寸並無特定限制,只要該尺寸能使膠囊填充本發明之控釋組合物即可,然而,第00號至第5號膠囊可以市售產品獲得。
本發明之控釋組合物可根據需要藉由醫藥技術領域中之習知方法進行塗佈。此外,可提供用於區分組合物之標記或字母或此外之用於分割組合物之分割線。
(11)控釋組合物之用途
在本發明之一個態樣中,提供一種控釋組合物於治療或預防以上所述的疾病之用途,一種控釋組合物於製造用於治療或預防以上所述的疾病的藥物之用途,一種用於治療或預防以上所述的疾病之方法,該方法包括對有此需要的患者投與治療有效量之控釋組合物。以上所提供的相對於控釋組合物之描述適用於控釋組合物之此種用途。
(12)醫學用途
化合物A具有極佳PGI2
受體促效作用且顯示各種醫學作用,諸如血小板聚集抑制作用、血管擴張作用、支氣管平滑肌擴張作用、脂質沉積抑制作用及白血球活化抑制作用(參見,例如PTL 1至PTL 6)。
在本發明之一個實施例中,本發明之控釋組合物可用作用於以下之預防劑或治療劑:暫時性腦缺血(TIA)、糖尿病性神經病變(參見例如NPL 2)、糖尿病性壞疽(參見例如NPL 2,周邊循環紊亂[例如慢性動脈阻塞(參見例如NPL 3)、間歇性跛行(參見例如NPL 4)、周邊栓塞、振動症候群或雷諾氏病(Raynaud's disease)] (參見例如NPL 5及NPL 6)、結締組織疾病[例如全身性紅斑狼瘡、硬皮病(參見例如PTL 9及NPL 7)、混合型結締組織疾病或血管炎症候群]、經皮冠狀動脈成形術(PTCA)後再阻塞/再狹窄、動脈硬化、血栓形成(例如急性期腦血栓形成或肺栓塞) (參見例如NPL 6及NPL 8)、高血壓、肺高血壓、缺血性疾病[例如腦梗塞或心肌梗塞(參見例如NPL 9)]、心絞痛(例如穩定型心絞痛或不穩定型心絞痛) (參見例如NPL 10)、腎絲球腎炎(參見例如NPL 11)、糖尿病性腎病(參見例如NPL 2)、慢性腎衰竭(參見例如PTL 10)、過敏、支氣管哮喘(參見例如NPL 12)、潰瘍、褥瘡(bedsore)、冠狀動脈介入術諸如斑塊切除術或支架植入術後再狹窄、由於透析所致之血小板減少症、其中涉及器官或組織中之纖維生成之疾病[例如腎臟疾病{例如腎小管間質腎炎(參見例如PTL 11)}、呼吸道疾病{例如間質性肺炎(肺纖維化) (參見例如PTL 11)、慢性阻塞性肺病(參見例如NPL 13)}、消化疾病(例如肝硬化、病毒性肝炎、慢性胰腺炎或胃硬癌)、心血管疾病(例如心肌纖維化)、骨或關節疾病(例如骨髓纖維化或類風濕性關節炎)、皮膚疾病(例如術後瘢痕、燒傷瘢痕、瘢痕疙瘩(keloid)或肥厚性瘢痕)、產科疾病(例如子宮纖维瘤)、泌尿疾病(例如前列腺肥大)、其他疾病(例如阿茲海默氏症(Alzheimer's disease)、硬化性腹膜炎、I型糖尿病及術後臟器黏連)]、勃起功能障礙(例如糖尿病性勃起功能障礙、心因性勃起功能障礙、精神病性勃起功能障礙、由於慢性腎衰竭所致之勃起功能障礙、前列腺切除盆腔手術後勃起功能障礙或與老化或動脈硬化相關之血管性勃起功能障礙)、發炎性腸病(例如潰瘍性結腸炎、克羅恩氏病(Crohn's disease)、腸結核、缺血性結腸炎或與貝西氏病(Behcet disease)相關之腸潰瘍) (參見例如PTL 12)、胃炎、胃潰瘍、缺血性眼病(例如視網膜動脈阻塞、視網膜靜脈阻塞或缺血性視神經病變)、突然聽力損失、骨缺血性壞死、由於投與非類固醇抗發炎劑(NSAID) (例如雙氯芬酸、美洛昔康(meloxicam)、奧沙普秦(oxaprozin)、萘丁美酮(nabumetone)、吲哚美辛(indomethacin)、布洛芬(ibuprofen)、酮洛芬(ketoprofen)、萘普生(naproxen)或塞來昔布(celecoxib))引起之腸損傷(並無特定限制,只要其係發生在例如十二指腸、小腸或大腸中之損傷,不論如何,例如發生在十二指腸、小腸或大腸中之黏膜損傷諸如糜爛或潰瘍)、或與椎管狹窄(例如頸椎管狹窄、胸椎管狹窄、腰椎管狹窄、共存頸椎及腰椎管狹窄或骶椎管狹窄)相關之症狀(例如麻痺、感覺遲鈍、疼痛、麻木或行走能力下降) (參見PTL 13)。
此外,本發明之控釋組合物亦可用作用於基因療法或血管生成療法諸如自體骨髓移植之加速劑、或用於周邊動脈或血管生成療法之恢復中之血管生成之加速劑。
特別地,本發明之控釋組合物可用作用於治療或預防糖尿病性神經病變、糖尿病性壞疽、周邊循環紊亂、慢性動脈阻塞、間歇性跛行、硬皮病、血栓形成、肺動脈高壓、心肌梗塞、心絞痛、腎絲球腎炎、糖尿病性腎病、慢性腎衰竭、支氣管哮喘、間質性肺炎(肺纖維化)、慢性阻塞性肺病、腎小管間質性腎炎、發炎性腸病或與椎管狹窄相關之症狀之藥劑。
(13)給藥方案
在本發明之一個實施例中,只要其不抑制本發明之效應,本發明之控釋組合物之劑量可考慮待投與的個體之症狀、年齡、性別及類似者,但在口服之情況下通常約為0.05 mg至5.0 mg化合物A/成人/天,且該劑量可一次或分成2至4次,較佳地一天一次投與。
在本發明之一個實施例中,只要其不抑制本發明之效應,本發明之控釋組合物可與用於治療或預防之另一種活性成分或以上所述的研究性新穎活性成分組合使用。
(14)控釋製劑/控釋調配物
術語「控釋組合物」可與術語「控釋製劑」或「控釋調配物」互換使用。以上關於控釋組合物所提供的描述適用於此種控釋製劑及控釋調配物。
[實例]
下文中,將參考實例及比較實例更詳細地描述本發明,然而,本發明之範疇不限於此等實例之範圍。
表1:調配物清單
| 組分 | 參考例1 | 參考例2 | 實例1 |
| 希樂普 | 0.4 | 0.4 | 0.4 |
| D-甘露醇 | - | 107.6 | 107.6 |
| 羥丙基纖維素 | - | 4 | 4 |
| 微晶纖維素 | 8.6 | - | - |
| 預糊化澱粉 | 20 | - | - |
| 羥丙基甲基纖維素2208 (100,000 mPa・s) | 75 | 50 | 50 |
| 聚環氧乙烷 | - | 200 | 200 |
| 聚乙烯吡咯啶酮K30 | - | - | 133 |
| 聚乙二醇6000 (MW:8600) | - | 133 | - |
| 碳酸鈉 | 5 | - | - |
| 硬脂酸鎂 | 1 | 5 | 5 |
| 核心錠劑總計 | 110 | 500 | 500 |
| 羥丙基甲基纖維素2910 (6 mPa・s) | 3.8 | - | - |
| 丙二醇 | 0.7 | - | - |
| 二氧化鈦 | 0.5 | - | - |
| 黃氧化鐵 | 補充至適量 | - | - |
| 膜層總計 | 5 | - | - |
| 膜衣錠總計 | 115 | - | - |
表2:調配物清單
| 組分 | 實例2 | 實例3 | 實例4 | 實例5 | 實例6 | 實例7 |
| 希樂普 | 0.4 | 0.4 | 0.4 | 0.4 | 0.4 | 0.4 |
| D-甘露醇 | 72.4 | 72.4 | 72.4 | 72.4 | 72.4 | 72.4 |
| 玉米澱粉 | 48 | 48 | 48 | 48 | 48 | 48 |
| 經低取代之羥丙基纖維素 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 |
| 羥丙基纖維素 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 聚環氧乙烷 | 100 | 144 | 160 | 200 | 240 | 280 |
| 羥丙基甲基纖維素2208 (100,000 mPa・s) | 25 | 36 | 40 | 50 | 60 | 70 |
| 聚乙烯吡咯啶酮K30 | 98.4 | 201.8 | 181.8 | 131.8 | 81.8 | 170.4 |
| 硬脂酸鎂 | 3.6 | 5.2 | 5.2 | 5.2 | 5.2 | 6.6 |
| 錠劑總計 | 360 | 520 | 520 | 520 | 520 | 660 |
| 錠劑形狀 | 10 mmφ圓形 | 11 mmφ圓形 | 11 mmφ圓形 | 11 mmφ圓形 | 11 mmφ圓形 | 18*9 mm長橢圓形 |
| 壓縮力 | 10 kN | 11 kN | 11 kN | 11 kN | 11 kN | 15 kN |
表3:調配物清單
*Aquapolish P紅040.67係BIOGRUND GmbH製造的76%羥丙基甲基纖維素2910、14%丙二醇、9%二氧化鈦及1%氧化鐵紅之混合物。
| 組分 | 實例8 | 實例9 | 實例10 | 實例11 | 實例12 | 實例13 | 實例14 | 實例15 | 實例16 | 實例17 |
| 希樂普 | 0.4 | 0.4 | 1.6 | 3.2 | 0.4 | 1.6 | 3.2 | 0.4 | 1.6 | 3.2 |
| D-甘露醇 | 72.4 | 72.4 | 71.2 | 69.6 | 72.4 | 71.2 | 69.6 | 72.4 | 71.2 | 69.6 |
| 玉米澱粉 | 48 | 48 | 48 | 48 | 48 | 48 | 48 | 48 | 48 | 48 |
| 經低取代之羥丙基纖維素 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 | 6.8 |
| 羥丙基纖維素 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 聚環氧乙烷 | 200 | 144 | 144 | 144 | 200 | 200 | 200 | 240 | 240 | 240 |
| 羥丙基甲基纖維素2208 (100,000 mPa・s) | 50 | 36 | 36 | 36 | 50 | 50 | 50 | 60 | 60 | 60 |
| 聚乙烯吡咯啶酮K30 | 131.8 | 201.8 | 201.8 | 201.8 | 131.8 | 131.8 | 131.8 | 81.8 | 81.8 | 81.8 |
| 硬脂酸鎂 | 5.2 | 5.2 | 5.2 | 5.2 | 5.2 | 5.2 | 5.2 | 5.2 | 5.2 | 5.2 |
| 核心錠劑總計 | 520 | 520 | 520 | 520 | 520 | 520 | 520 | 520 | 520 | 520 |
| 羥丙基甲基纖維素2910 (6 mPa s) | 15.2 | - | - | - | - | - | - | - | - | - |
| 丙二醇 | 2.8 | - | - | - | - | - | - | - | - | - |
| 二氧化鈦 | 2 | - | - | - | - | - | - | - | - | - |
| 黃氧化鐵 | 補充至適量 | - | - | - | - | - | - | - | - | - |
| 棕櫚蠟 | 補充至適量 | - | - | - | - | - | - | - | - | - |
| 塗佈混合物 (Aquapolish P紅040.67*) | - | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 |
| 膜層總計 | 20 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 | 20.8 |
| 膜衣錠總計 | 540 | 540.8 | 540.8 | 540.8 | 540.8 | 540.8 | 540.8 | 540.8 | 540.8 | 540.8 |
<顯示於表1中之錠劑之製法>
1. 參考例1之錠劑
(1) 根據表1稱取希樂普、微晶纖維素、預糊化澱粉、羥丙基甲基纖維素2208、碳酸鈉及硬脂酸鎂且使用摻合機摻合以獲得混合粉末。
(2) 將所得的混合粉末藉由旋轉式壓製機以1200 kgf壓縮以獲得直徑為6.5 mm之錠劑。
(3) 藉由將羥丙基甲基纖維素2910、丙二醇、二氧化鈦及黃氧化鐵分散在純化水中來製備塗佈液體。藉由使用穿孔塗佈機器將所得的塗佈液體噴塗在錠劑上以獲得膜衣錠。
2. 參考例2之錠劑
(1) 根據表1稱取希樂普、D-甘露醇、羥丙基纖維素、聚環氧乙烷、羥丙基甲基纖維素2208、聚乙二醇6000及硬脂酸鎂且經混合以獲得混合粉末。
(2) 將所得的混合粉末藉由單壓製機以1200 kgf壓縮以獲得直徑為10.5 mm之錠劑。
3. 實例1之錠劑
(1) 根據表1稱取希樂普、D-甘露醇、37.6%之總聚乙烯吡咯啶酮K30且經摻合以獲得混合粉末。藉由使用流化床造粒機將10%(w/w)羥丙基纖維素水溶液噴塗至所得的混合粉末上以獲得顆粒。
(2) 根據表1稱取聚環氧乙烷、羥丙基甲基纖維素2208、其餘聚乙烯吡咯啶酮K30及硬脂酸鎂且經與所得的顆粒摻合以獲得混合粉末。
(3) 將所得的混合粉末藉由單壓製機以1200 kgf壓縮以獲得直徑為10.5 mm之錠劑。
表4:參考例1、2及實例1之組分之清單
| 組分 | 產品名稱 | 公司 |
| D-甘露醇 | Mannit P | Mitsubishi Shoji Foodtech |
| 羥丙基纖維素 | NISSO HPC-SSL | NIPPON SODA |
| 微晶纖維素 | Ceolus KG-1000 | Asahi Kasei |
| 預糊化澱粉 | SWELSTAR MX-1 | Asahi Kasei |
| 聚環氧乙烷 | PEO-20NF 2型 | SUMITOMO SEIKA |
| 羥丙基甲基纖維素2208 (100,000 mPa・s) | METOLOSE 90SH100000SR | Shin-Etsu Chemical |
| 聚乙烯吡咯啶酮K30 | Kollidon 30 | BASF |
| 聚乙二醇6000(MW:8600) | 聚乙二醇6000 (粉末) | Sanyo Chemical |
| 碳酸鈉 | 無水碳酸鈉(粉狀) | TAKASUGI Pharmaceutical |
| 硬脂酸鎂 | 植物硬脂酸鎂 (專用) | Taihei Chemical Industrial |
| 羥丙基甲基纖維素2910 (6 mPa・s) | TC-5R | Shin-Etsu Chemical |
| 丙二醇 | 丙二醇 | AGC |
| 二氧化鈦 | Tipaque A-100 | ISHIHARA SANGYO KAISHA |
| 黃氧化鐵 | 黃氧化鐵 | Taketombo |
<顯示於表2中之錠劑之製法>
(1) 根據表2稱取希樂普、D-甘露醇、玉米澱粉、經低取代之羥丙基纖維素且經摻合以獲得混合粉末。藉由使用流化床造粒機將10% (w/w)羥丙基纖維素水溶液噴塗至所得的混合粉末上以獲得顆粒。
(2) 根據表1稱取聚環氧乙烷、羥丙基甲基纖維素2208、聚乙烯吡咯啶酮K30及硬脂酸鎂且藉由摻合機與所得的顆粒摻合以獲得混合粉末。
(3) 藉由單壓製機壓縮所得的混合粉末以獲得錠劑。
<顯示於表3中之實例8之錠劑之製法>
(1) 根據表3稱取希樂普、D-甘露醇、玉米澱粉、經低取代之羥丙基纖維素且經摻合以獲得混合粉末。藉由使用流化床造粒機將10%(w/w)羥丙基纖維素水溶液噴塗至所得的混合粉末上以獲得顆粒。
(2) 根據表3稱取聚環氧乙烷、羥丙基甲基纖維素2208、聚乙烯吡咯啶酮K30及硬脂酸鎂且藉由摻合機與所得的顆粒摻合以獲得混合粉末。
(3) 將所得的混合粉末藉由旋轉式壓製機以14 kN壓縮以獲得直徑為11 mm之錠劑。
(4) 藉由將羥丙基甲基纖維素2910、丙二醇、二氧化鈦及黃氧化鐵分散在純化水中來製備塗佈液體。將所得的塗佈液體噴塗在錠劑上且以棕櫚蠟藉由使用穿孔塗佈機器連續拋光錠劑以獲得膜衣錠。
*藉由參考實例8之製法來製備表3中之其餘錠劑。
表5:實例8之組分之清單
| 組分 | 產品名稱 | 公司 |
| D-甘露醇 | Mannit P | Mitsubishi Shoji Foodtech |
| 羥丙基纖維素 | NISSO HPC-SSL | NIPPON SODA |
| 玉米澱粉 | 玉米澱粉W | NIHON SHOKUHIN KAKO |
| 經低取代之羥丙基纖維素 | LH-11 | Shin-Etsu Chemical |
| 聚環氧乙烷 | PEO-20NF 2型 | SUMITOMO SEIKA |
| 羥丙基甲基纖維素2208 (100,000 mPa・s) | METOLOSE 90SH100000SR | Shin-Etsu Chemical |
| 聚乙烯吡咯啶酮K30 | Kollidon 30 | BASF |
| 硬脂酸鎂 | 植物硬脂酸鎂(專用) | Taihei Chemical Industrial |
| 羥丙基甲基纖維素2910 (6 mPa・s) | TC-5R | Shin-Etsu Chemical |
| 丙二醇 | 丙二醇 | AGC |
| 二氧化鈦 | Tipaque A-100 | ISHIHARA SANGYO KAISHA |
| 黃氧化鐵 | 黃氧化鐵 | Taketombo |
| 棕櫚蠟 | 棕櫚蠟 | CERARICA NODA |
<錠劑之膠凝強度>
(1) 將錠劑放在不鏽鋼篩(JIS Z 8801,2006,孔徑:1 mm,線徑:0.56 mm)上,且然後將該組錠劑及篩浸泡於37℃水中。6小時後,自水取出該組錠劑及篩。
(2) 將篩上的錠劑自頂部壓下且記錄負載(單位:N)之時間依賴性變化以便計算錠劑之膠凝強度。
設備:數位式測力計(IMADA,ZTA-50N)及標準型立式電動試驗台(IMADA,MX2-500N)
條件:移動速度10 mm/min,感測器形狀13.3 mm直徑平頭(IMADA、A-2-、及每0.1秒數據採樣率
(3) 膠凝強度定義為負載(單位:N)對時間之反曲點。反曲點經計算為滿足以下條件(i)至(iv)之F(n)之最小值。
(i) ΔF(n)=F(n+1)-F(n)
(ii) ΔF(n)>0.1 N
(iii) ΔF(n)>2ΔF(n-1)
(iv) ΔF(n+1)>2ΔF(n-1)
F(n)為在第n次中測得的負載。
表6:錠劑之膠凝強度
| 膠凝強度(N) | |
| 參考例1 | >10 |
| 參考例2 | >10 |
| 實例1 | 2.81 |
| 實例2 | 0.85 |
| 實例3 | 0.75 |
| 實例4 | 1.06 |
| 實例5 | 2.70 |
| 實例6 | 7.99 |
| 實例7 | 2.97 |
| 實例8 | 2.88 |
| 實例12 | 3.09 |
<溶解測試>
(1) 將錠劑放入第17版日本藥典(後文稱為「JP」)籃狀沉降器中,藉由JP溶解測試方法2 (槳法)進行溶解測試。
(2) 溶解測試使用900 mL第2版JP流體,該溶解測試係以200 rpm之槳速進行。
(3) 此測試係在37℃之液體溫度下進行。
(4) 藉由高效液相層析法測量希樂普之釋放率。
表7:希樂普自錠劑之釋放率
| 參考例1 | 參考例2 | 實例1 | ||
| 時間 (小時) | 釋放率(%) | 釋放率(%) | 釋放率(%) | |
| 0 | 0 | 0 | 0 | |
| 2 | 12.2 | 6.1 | 6.5 | |
| 6 | 34.1 | 19.6 | 21.0 | |
| 8 | 44.3 | - | - | |
| 10 | 53.8 | 37.0 | 37.0 | |
| 12 | - | 41.1 | - | |
| 14 | - | - | 52.8 | |
| 16 | 78.8 | 60.0 | - | |
| 18 | - | - | 68.7 | |
| 20 | 91.2 | 77.4 | - | |
| 24 | 98.3 | 89.8 | 91.4 |
表8:希樂普自錠劑之釋放率
| 實例2 | 實例3 | 實例4 | 實例5 | 實例6 | 實例7 | 實例8 | 實例12 | |
| 時間 (小時) | 釋放率 (%) | 釋放率(%) | 釋放率(%) | 釋放率(%) | 釋放率(%) | 釋放率(%) | 釋放率(%) | 釋放率(%) |
| 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| 2 | 15.3 | 8.8 | 8.6 | 6.8 | 7.1 | 5.9 | 7.5 | 8.3 |
| 6 | 35.9 | 28.1 | 27.7 | 20.8 | 19.2 | 17.8 | 20.8 | 24.8 |
| 10 | 61.8 | 55.1 | 45.7 | 36.6 | 32.0 | 31.6 | 36.7 | 42.6 |
| 16 | 95.2 | 86.8 | 74.5 | 63.9 | 52.2 | 57.4 | 61.4 | 65.1 |
| 20 | 101.8 | 100.8 | 93.5 | 78.7 | 67.6 | 72.7 | 76.2 | 81.5 |
| 24 | 98.1 | 97.9 | 99.9 | 90.5 | 81.5 | 85.3 | 87.4 | 95.5 |
<保水力>
(1) 將錠劑放在不鏽鋼篩(JIS Z 8801,2006,孔徑:1 mm,線徑:0.56 mm)上,且然後將該組錠劑及篩浸泡於37℃水中6小時。
(2) 自水取出錠劑且然後測定溶脹錠劑重量。
(3) 由下式計算保水力。
保水力(%)=溶脹錠劑重量(mg)/測試前的錠劑重量(mg)×100
表9:錠劑之保水力
| 保水力(%) | |
| 參考例1 | 680 |
| 參考例2 | 634 |
| 實例1 | 599 |
| 實例2 | 622 |
| 實例3 | 560 |
| 實例4 | 560 |
| 實例5 | 591 |
| 實例6 | 608 |
| 實例7 | 605 |
| 實例8 | 557 |
| 實例12 | 568 |
<崩解>
(1) 將錠劑放入第17版日本藥典(後文稱為「JP」)籃狀沉降器中,藉由JP溶解測試方法2 (槳法)進行溶解測試。
(2) 溶解測試使用900 mL第2版JP流體,該溶解測試係以200 rpm之槳速進行。
(3) 此測試係在37℃之液體溫度下進行。
(4) 當錠劑在溶解測試中6小時未維持其形狀(錠劑溶解,消失,經分離),將視為錠劑崩解。
表10:錠劑之崩解
*IR為Uptravi 0.4 mg錠劑(NIPPON SYINYAKU之銷售產品)。
| 崩解 | |
| IR | 崩解 |
| 參考例1 | 未崩解 |
| 參考例2 | 未崩解 |
| 實例1 | 未崩解 |
| 實例2 | 未崩解 |
| 實例3 | 未崩解 |
| 實例4 | 未崩解 |
| 實例5 | 未崩解 |
| 實例6 | 未崩解 |
| 實例7 | 未崩解 |
| 實例8 | 未崩解 |
| 實例12 | 未崩解 |
<犬活體內研究>
將測試錠劑以0.4 mg/錠劑/身體之劑量水平與20 ml水一起經口投與給禁食17小時的雄性小獵犬(n = 6)。
在以每次0.6 mL之劑量經口給藥後(給藥後0.5、1、2、4、6、8、10、12及24小時)在麻醉下自頭靜脈收集血液樣品放入肝素化管中且立即用冰冷卻樣品。
該等管經離心(15000 rpm,4℃,5分鐘)且將血漿轉移至樣品管並在−20℃下冷凍直至分析。
藉由LC-MS/MS方法測定血漿樣品中希樂普之濃度。
藥物動力學分析
利用Phoenix WinNonlin 7.0版 (Certara Princeton, NJ)來計算得藥物動力學參數。
表11:犬活體內研究之結果
*IR為Uptravi 0.4 mg錠劑(NIPPON SYINYAKU之銷售產品)。
[工業適用性]
| 調配物 | C最大 | t最大 | AUC0 至最後一次 |
| (ng/mL) | (小時) | (ng·h/mL) | |
| IR* | 48.5±8.8 | 1.0±0.0 | 102±21 |
| 參考例1 | 9.23±5.94 | 3.4±2.0 | 40.9±41.2 |
| 參考例2 | 4.55±3.49 | 5.2±1.1 | 35.4±32.2 |
| 實例1 | 17.9±9.2 | 6.0±2.0 | 101±47 |
因此,本發明之控釋組合物可用作維持活性成分以恆定速率長時間釋放所需的持續釋放型製劑。
Claims (32)
- 一種控釋組合物,其包含(1)水溶性聚合物,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。
- 如請求項1之控釋組合物,其中(1)該水溶性聚合物之水溶液在10重量%或更小之濃度下具有1000 mPa・s或更大之黏度。
- 如請求項1之控釋組合物,其中(1)該水溶性聚合物為選自包含聚環氧乙烷(PEO);纖維素衍生物,較佳地羥丙基甲基纖維素(hypromellose;HPMC)、甲基纖維素、羥乙基纖維素、羥丙基纖維素(HPC)、羥乙基甲基纖維素、羧甲基纖維素、羧甲基纖維素鈉;聚乙烯醇(PVA)、海藻酸、海藻酸之鹼金屬鹽、海藻酸銨、角叉菜膠、黃原膠及阿拉伯膠(Arabic gum)之群之至少一者。
- 如請求項1之控釋組合物,其中(1)該水溶性聚合物為基於該組合物總重量計25至70重量%。
- 如請求項1至4中任一項之控釋組合物,其進一步包含(2)水溶性添加劑。
- 如請求項5之控釋組合物,其中可將1 g (2)該水溶性添加劑溶解於6 ml或更少之水中。
- 如請求項5或6中任一項之控釋組合物,其中(2)該水溶性添加劑為選自包含聚乙烯吡咯啶酮(PVP)及糖,較佳地糖醇之群之至少一者。
- 如請求項5至7中任一項之控釋組合物,其中(2)該水溶性添加劑為基於該組合物總重量計20至65重量%。
- 如請求項1至8中任一項之控釋組合物,其進一步包含(3)活性成分。
- 如請求項9之控釋組合物,其中(3)該活性成分為希樂普(selexipag)。
- 如請求項9或10之控釋組合物,其中(3)該活性成分為基於該組合物總重量計0.05至1重量%。
- 如請求項1至11中任一項之控釋組合物,其中(1)該水溶性聚合物及(2)該水溶性添加劑之比為1:0.3至1:2.5。
- 如請求項1至12中任一項之控釋組合物,其中(1)該水溶性聚合物為選自包含聚環氧乙烷(PEO)及羥丙基甲基纖維素(HPMC)之群之至少一者。
- 如請求項13之控釋組合物,其中該PEO之分子量之範圍為900,000至7,000,000,較佳地2,000,000至7,000,000。
- 如請求項13或14之控釋組合物,其中該PEO為基於該組合物總重量計20至70重量%。
- 如請求項13至15中任一項之控釋組合物,其中在2重量%之濃度下,該HPMC之水溶液之黏度範圍為3000至140000 mP・s。
- 如請求項13至16中任一項之控釋組合物,其中該HPMC為基於該組合物總重量計5至20重量%。
- 如請求項5至17中任一項之控釋組合物,其中(2)該水溶性添加劑為選自包含聚乙烯吡咯啶酮(PVP)及D-甘露醇之群之至少一者。
- 如請求項18之控釋組合物,其中該PVP之K值為10至120,較佳地20至40。
- 如請求項18或19之控釋組合物,其中該PVP為基於該組合物總重量計10至65重量%。
- 如請求項18至20中任一項之控釋組合物,其中D-甘露醇為基於該組合物總重量計10至25重量%。
- 如請求項1至21中任一項之控釋組合物,其中該水凝膠之該強度為小於5N。
- 如請求項1至22中任一項之控釋組合物,其中該水凝膠之該強度係在將該組合物放入37℃的水中6小時後藉由移動速度為10 mm/min及感測器尺寸為13.3 mm直徑之流變儀測得。
- 如請求項1至23中任一項之控釋組合物,其中該控釋組合物係呈錠劑或膜衣錠之形式。
- 一種控釋組合物,其包含(1)水溶性聚合物,(2)水溶性添加劑,及(3)至少一種活性成分,其中該水溶性聚合物在水中形成水凝膠且該水凝膠之強度為小於10N。
- 如請求項1至25中任一項之控釋組合物,其中該活性成分之釋放率在溶解測試中於6小時後為0至50%及/或在溶解測試中於24小時後為70至100%。
- 如請求項1至26中任一項之控釋組合物,其中該控釋組合物具有400至800%之保水力。
- 如請求項1至27中任一項之控釋組合物,其係用於治療疾病。
- 如請求項28中任一項之控釋組合物,其中該疾病為選自包含與糖尿病性神經病變、糖尿病性壞疽、周邊循環紊亂、慢性動脈阻塞、間歇性跛行、硬皮病、血栓形成、肺動脈高血壓、心肌梗塞、心絞痛、腎絲球腎炎、糖尿病性腎病、慢性腎衰竭、支氣管哮喘、間質性肺炎、肺纖維化、慢性阻塞性肺病、腎小管間質性腎炎、發炎性腸病及椎管狹窄相關之症狀之群之至少一者。
- 一種如請求項1至29中任一項之控釋組合物於製造用於治療疾病之藥物的用途。
- 一種預防及/或治療疾病之方法,該方法包括對有此需要的個體投與適宜量之如請求項1至29中任一項之控釋組合物。
- 一種製備如請求項1至29中任一項之控釋組合物之方法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020-014880 | 2020-01-31 | ||
| JP2020014880 | 2020-01-31 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202140010A true TW202140010A (zh) | 2021-11-01 |
Family
ID=77079418
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW110103421A TW202140010A (zh) | 2020-01-31 | 2021-01-29 | 控釋組合物 |
Country Status (4)
| Country | Link |
|---|---|
| AR (1) | AR121207A1 (zh) |
| TW (1) | TW202140010A (zh) |
| UY (1) | UY39054A (zh) |
| WO (1) | WO2021153716A1 (zh) |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2179829T3 (es) * | 1992-09-18 | 2003-02-01 | Yamanouchi Pharma Co Ltd | Preparacion de hidrogel de liberacion prolongada. |
| TWI478712B (zh) * | 2008-09-30 | 2015-04-01 | Astellas Pharma Inc | 釋控性醫藥組成物 |
| GB201400412D0 (en) * | 2014-01-10 | 2014-02-26 | Heart Biotech Ltd | Pharmaceutical formulations for the treatment of pulmonary arterial hypertension |
| WO2017042731A1 (en) * | 2015-09-10 | 2017-03-16 | Lupin Limited | Amorphous form of selexipag and solid dispersion thereof |
| EP3192502A1 (en) * | 2016-01-15 | 2017-07-19 | Sandoz Ag | Pharmaceutical composition of selexipag |
| EP3335699A1 (en) * | 2016-12-15 | 2018-06-20 | H e x a l Aktiengesellschaft | Selexipag formulation in liquisolid system |
| CA3082009A1 (en) * | 2017-11-16 | 2019-05-23 | Nippon Shinyaku Co., Ltd. | Controlled-release preparation |
| US20240024311A1 (en) * | 2019-02-03 | 2024-01-25 | Jayendrakumar Dasharathlal Patel | A controlled release pharmaceutical composition of selexipag or it's active metabolite |
| EP3705115B1 (en) * | 2019-03-07 | 2021-06-30 | Alfred E. Tiefenbacher (GmbH & Co. KG) | Composition containing selexipag |
| WO2020255157A1 (en) * | 2019-06-20 | 2020-12-24 | Aizant Drug Research Solutions Private Limited | Stable solid dosage form of selexipag and process for preparation thereof |
-
2021
- 2021-01-29 WO PCT/JP2021/003157 patent/WO2021153716A1/en active Application Filing
- 2021-01-29 AR ARP210100224A patent/AR121207A1/es unknown
- 2021-01-29 TW TW110103421A patent/TW202140010A/zh unknown
- 2021-01-29 UY UY0001039054A patent/UY39054A/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| AR121207A1 (es) | 2022-04-27 |
| WO2021153716A1 (en) | 2021-08-05 |
| UY39054A (es) | 2021-07-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2012043709A1 (ja) | 難溶性薬物の溶解性改善製剤 | |
| TWI750143B (zh) | 含有2-{4-[n-(5,6-二苯基吡-2-基)-n-異丙基胺基]丁基氧基}-n-(甲基磺醯基)乙醯胺之醫藥組合物 | |
| JP2010530355A (ja) | 医薬固形製剤及びその製造方法 | |
| WO2011102506A1 (ja) | 経口用徐放性固形製剤 | |
| US11382912B2 (en) | Controlled-release preparation | |
| CA3154802A1 (en) | Pharmaceutical composition comprising selexipag | |
| JP2022173401A (ja) | 結晶 | |
| JP2010536798A (ja) | 難溶性薬物の生体利用率を制御するための方法及び組成物 | |
| WO2009084041A2 (en) | Pharmaceutical compositions of dexibuprofen | |
| WO2019163822A1 (ja) | 粒状組成物、粒状組成物の製造方法、および粒状組成物の溶出性改善方法 | |
| JP2021533109A (ja) | 多嚢胞性卵巣症候群の治療に有用な医薬品有効成分の三重組合せの即時放出製剤 | |
| TW202140010A (zh) | 控釋組合物 | |
| EP3697392A1 (en) | Tablets comprising tamsulosin and solifenacin | |
| JP2021517586A (ja) | レナリドミド胃内滞留型徐放錠及びその調製方法 | |
| RU2669920C2 (ru) | Фармацевтическая композиция с контролируемым высвобождением, основанная на прионовой кислоте | |
| EP2793853B1 (en) | Pharmaceutical formulations of flurbiprofen and glucosamin | |
| WO2022034914A1 (ja) | 易溶性固形製剤およびその製法 | |
| WO2024024865A1 (ja) | レボドパ持続性製剤 | |
| WO2023238929A1 (ja) | ピミテスピブを含有する医薬組成物 | |
| TWI743059B (zh) | 二氟甲基鳥氨酸及舒林酸(sulindac),固定劑量組合調配物 | |
| JP2022112698A (ja) | アピキサバン含有医薬組成物 | |
| US20110028526A1 (en) | Valsartan solid oral dosage forms and methods of making such formulations | |
| JP2023547736A (ja) | メロキシカム含有医薬組成物 | |
| TW201607568A (zh) | 包含1-[6-(嗎啉-4-基)嘧啶-4-基]-4-(1h-1,2,3-三唑-1-基)-1h-吡唑-5-醇鈉之醫藥劑型 | |
| WO2022042644A1 (zh) | 依达拉奉缓释药物组合物、制备方法及应用 |