RU2713373C1 - Method of extracting sodium chloride from waste water - Google Patents
Method of extracting sodium chloride from waste water Download PDFInfo
- Publication number
- RU2713373C1 RU2713373C1 RU2019122130A RU2019122130A RU2713373C1 RU 2713373 C1 RU2713373 C1 RU 2713373C1 RU 2019122130 A RU2019122130 A RU 2019122130A RU 2019122130 A RU2019122130 A RU 2019122130A RU 2713373 C1 RU2713373 C1 RU 2713373C1
- Authority
- RU
- Russia
- Prior art keywords
- sodium chloride
- wastewater
- nacl
- waste water
- acetone
- Prior art date
Links
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 title claims abstract description 71
- 239000011780 sodium chloride Substances 0.000 title claims abstract description 35
- 239000002351 wastewater Substances 0.000 title claims abstract description 33
- 238000000034 method Methods 0.000 title claims abstract description 19
- CSCPPACGZOOCGX-UHFFFAOYSA-N acetone Substances CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims abstract description 25
- 239000002244 precipitate Substances 0.000 claims description 7
- 230000001376 precipitating effect Effects 0.000 claims description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 abstract description 4
- 239000000126 substance Substances 0.000 abstract description 2
- 238000002425 crystallisation Methods 0.000 abstract 1
- 230000008025 crystallization Effects 0.000 abstract 1
- 238000000605 extraction Methods 0.000 abstract 1
- 238000004519 manufacturing process Methods 0.000 description 11
- 229920005989 resin Polymers 0.000 description 10
- 239000011347 resin Substances 0.000 description 10
- 150000003839 salts Chemical class 0.000 description 8
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 239000000243 solution Substances 0.000 description 5
- 238000001704 evaporation Methods 0.000 description 4
- 230000008020 evaporation Effects 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 239000003513 alkali Substances 0.000 description 3
- 238000005303 weighing Methods 0.000 description 3
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- 239000004593 Epoxy Substances 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- RWYFURDDADFSHT-RBBHPAOJSA-N diane Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1.C1=C(Cl)C2=CC(=O)[C@@H]3CC3[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(C)=O)(OC(=O)C)[C@@]1(C)CC2 RWYFURDDADFSHT-RBBHPAOJSA-N 0.000 description 2
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000007033 dehydrochlorination reaction Methods 0.000 description 1
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 1
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 1
- 238000009776 industrial production Methods 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01D—COMPOUNDS OF ALKALI METALS, i.e. LITHIUM, SODIUM, POTASSIUM, RUBIDIUM, CAESIUM, OR FRANCIUM
- C01D3/00—Halides of sodium, potassium or alkali metals in general
- C01D3/04—Chlorides
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/58—Treatment of water, waste water, or sewage by removing specified dissolved compounds
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Hydrology & Water Resources (AREA)
- Environmental & Geological Engineering (AREA)
- Water Supply & Treatment (AREA)
- Materials Engineering (AREA)
- Inorganic Chemistry (AREA)
- Removal Of Specific Substances (AREA)
Abstract
Description
Изобретение относится к способу выделения из сточной воды хлористого натрия - сырья для электролитического получения хлора и щелочи.The invention relates to a method for the separation of sodium chloride from waste water, a feedstock for the electrolytic production of chlorine and alkali.
В ряде производств химической промышленности образуются сточные воды, обогащенные хлористым натрием. К таким производствам относятся процессы получения эпихлоргидрина, эпоксидно-диановых смол и других производств, в которых используется прием щелочного дегидрохлорирования. Концентрация хлористого натрия в сточных водах может составлять 10-26% масс. Утилизация таких сточных вод вызывает большие трудности из-за высокого содержания солей, не удаляемых на станциях биологической очистки.In a number of chemical industry productions, wastewater enriched with sodium chloride is formed. Such industries include processes for the preparation of epichlorohydrin, epoxy-diane resins and other industries that use alkaline dehydrochlorination. The concentration of sodium chloride in wastewater can be 10-26% of the mass. The disposal of such wastewater causes great difficulties due to the high content of salts that cannot be removed at biological treatment plants.
В то же время сточные воды с высокой концентрацией NaCl являются потенциальным источником этой соли - сырья для промышленного получения хлора и щелочи.At the same time, wastewater with a high concentration of NaCl is a potential source of this salt, a raw material for the industrial production of chlorine and alkali.
Известен способ выпарки воды с образованием кристаллической соли [CN 207158994]. В другом способе сточную воду, содержащую NaCl, упаривают до насыщения, и вводят в нее хлористый водород [CN 102847337], уменьшающий растворимость хлористого натрия. Однако эти методы требуют высоких энергетических затрат на выпарку воды, не могут обеспечить чистоту образующейся твердой соли и в то же время приводят к образованию сточной воды, насыщенной другим минеральным соединением.A known method of evaporation of water with the formation of a crystalline salt [CN 207158994]. In another method, the wastewater containing NaCl is evaporated to saturation and hydrogen chloride [CN 102847337] is introduced into it, which reduces the solubility of sodium chloride. However, these methods require high energy costs for the evaporation of water, cannot ensure the purity of the resulting solid salt, and at the same time lead to the formation of wastewater saturated with another mineral compound.
Наиболее близким к заявляемому является способ очистки сточной воды от хлористого натрия [SU 706331, C02F 1/02, опуб. 30.12.1979]. В соответствии с изобретением сточные воды, содержащие 9% масс. NaCl, подвергаются упариванию до содержания соли 20-25% масс. В образовавшийся насыщенный раствор NaCl добавляется NaOH до его концентрации в образовавшемся растворе 500-600 г/л. Введение щелочи в раствор приводит к уменьшению растворимости NaCl, в результате чего соль выпадает в осадок.Closest to the claimed is a method of treating wastewater from sodium chloride [SU 706331, C02F 1/02, publ. 12/30/1979]. In accordance with the invention, wastewater containing 9% of the mass. NaCl, are evaporated to a salt content of 20-25% of the mass. NaOH is added to the resulting saturated NaCl solution to its concentration in the resulting solution of 500-600 g / l. The introduction of alkali into the solution leads to a decrease in the solubility of NaCl, as a result of which the salt precipitates.
Недостатком этого изобретения является низкая степень выделения NaCl из сточной воды.The disadvantage of this invention is the low degree of separation of NaCl from wastewater.
Задачей изобретения является разработка способа, позволяющего увеличить степень выделения хлористого натрия из сточной воды по сравнению с прототипом без необходимости предварительного выпаривания для образования насыщенного раствора NaCl.The objective of the invention is to develop a method to increase the degree of separation of sodium chloride from wastewater compared with the prototype without the need for preliminary evaporation to form a saturated solution of NaCl.
Данная задача решается тем, что в способе выделения хлористого натрия из сточной воды, включающем введение в сточную воду осадителя, кристаллизацию хлористого натрия, выпадение его в осадок и отделение выпавшего осадка от раствора, в качестве осадителя используют ацетон в количестве, превышающем массу исходной сточной воды более чем в 4,7 раза.This problem is solved in that in the method of separating sodium chloride from wastewater, including introducing a precipitant into the wastewater, crystallizing sodium chloride, precipitating it and separating the precipitated precipitate from the solution, acetone is used as a precipitant in an amount exceeding the weight of the original wastewater more than 4.7 times.
Технический результат от использования предлагаемого изобретения заключается в увеличении степени выделения кристаллического хлористого натрия из сточной воды.The technical result from the use of the invention is to increase the degree of separation of crystalline sodium chloride from wastewater.
Примеры, иллюстрирующие, но не ограничивающие, настоящее изобретение.Examples illustrating, but not limiting, the present invention.
Пример 1 (по прототипу)Example 1 (prototype)
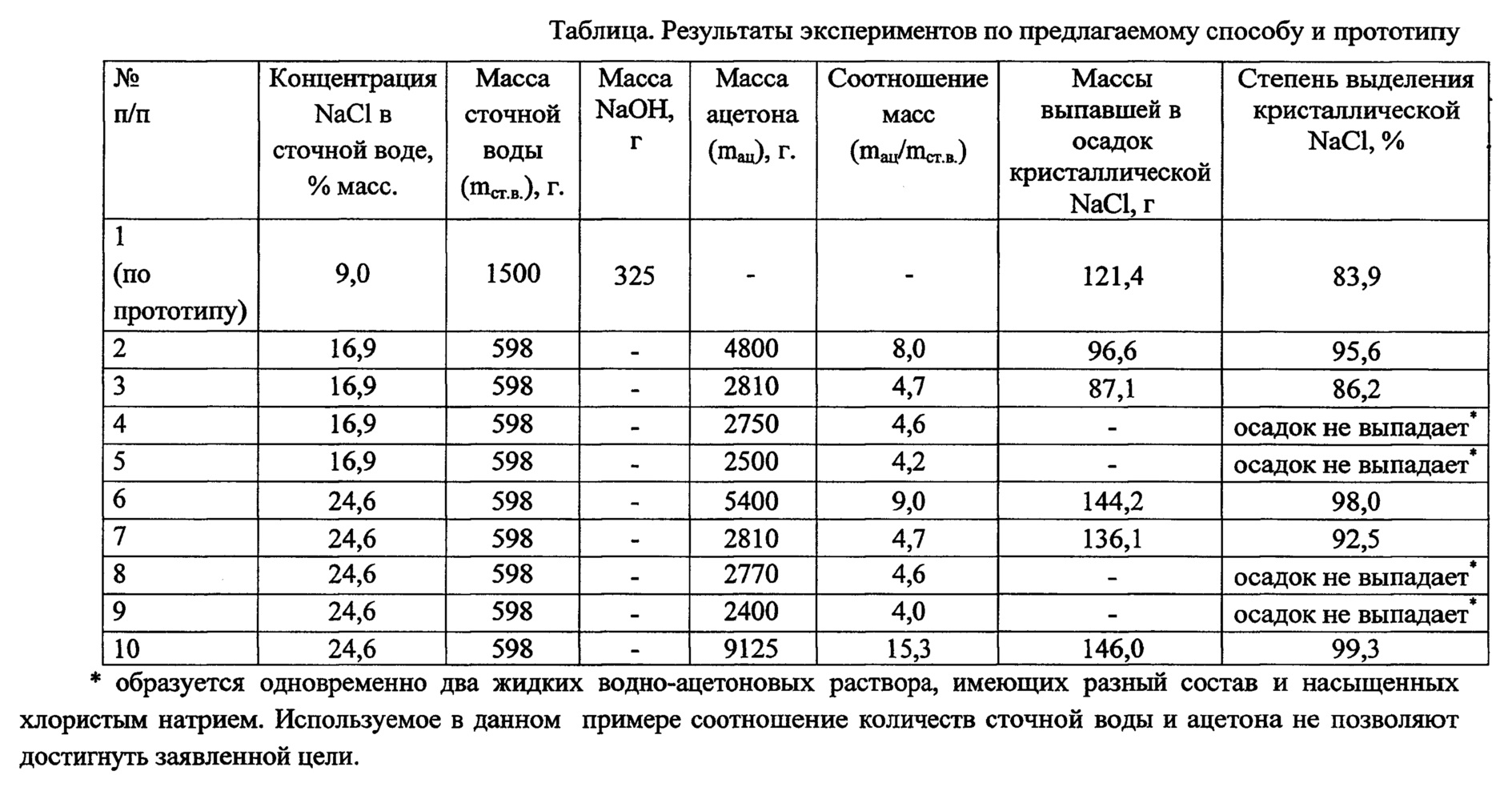
Сточную воду массой 1500 г, содержащую 9% масс. NaCl, упаривают до концентрации соли 23% масс. В образовавшийся раствор добавляют 325 г NaOH. При этом в осадок выпадает кристаллический NaCl. Результаты примера приведены в таблице.Wastewater weighing 1,500 g, containing 9% of the mass. NaCl, evaporated to a salt concentration of 23% of the mass. 325 g of NaOH are added to the resulting solution. In this case, crystalline NaCl precipitates. The results of the example are shown in the table.
Пример 2Example 2
Сточную воду производства эпоксидно-диановых смол, содержащую 16,87% масс. NaCl, массой 598 г смешивают с 4800 г ацетона. При этом в осадок выпадает кристаллический NaCl.Wastewater from the production of epoxy diane resins containing 16.87% of the mass. NaCl, weighing 598 g, is mixed with 4800 g of acetone. In this case, crystalline NaCl precipitates.
Результаты примера приведены в таблице.The results of the example are shown in the table.
Пример 3Example 3
Процесс выделения NaCl из сточной воды производства эпоксидно-диановых смол проводят аналогично примеру 2. Отличие состоит в том, что количество добавляемого ацетона составляет 2810 г.The process of separating NaCl from wastewater for the production of epoxy-diane resins is carried out analogously to example 2. The difference is that the amount of added acetone is 2810 g.
Результаты примера приведены в таблице.The results of the example are shown in the table.
Пример 4Example 4
Процесс выделения NaCl из сточной воды производства эпоксидно-диановых смол проводят аналогично примеру 2. Отличие состоит в том, что количество добавляемого ацетона составляет 2750 г.The process of separating NaCl from wastewater for the production of epoxy-diane resins is carried out analogously to example 2. The difference is that the amount of added acetone is 2750 g.
Результаты примера приведены в таблице.The results of the example are shown in the table.
Пример 5Example 5
Процесс выделения NaCl из сточной воды производства эпоксидно-диановых смол проводят аналогично примеру 2. Отличие состоит в том, что количество добавляемого ацетона составляет 2500 г.The process of separating NaCl from wastewater for the production of epoxy-diane resins is carried out analogously to example 2. The difference is that the amount of added acetone is 2500 g.
Результаты примера приведены в таблице.The results of the example are shown in the table.
Пример 6Example 6
Сточную воду производства эпоксидно-диановых смол, содержащую 24,58% масс. NaCl, массой 598 г смешивают с 5400 г ацетона. При этом в осадок выпадает кристаллический NaCl.Wastewater from the production of epoxy diane resins containing 24.58% by weight. NaCl, weighing 598 g, is mixed with 5400 g of acetone. In this case, crystalline NaCl precipitates.
Результаты примера приведены в таблице.The results of the example are shown in the table.
Пример 7Example 7
Процесс выделения NaCl из сточной воды производства эпоксидно-диановых смол проводят аналогично примеру 6. Отличие состоит в том, что количество добавляемого ацетона составляет 2900 г.The process of separating NaCl from wastewater for the production of epoxy-diane resins is carried out analogously to example 6. The difference is that the amount of added acetone is 2900 g.
Результаты примера приведены в таблице.The results of the example are shown in the table.
Пример 8Example 8
Процесс выделения NaCl из сточной воды производства эпоксидно-диановых смол проводят аналогично примеру 6. Отличие состоит в том, что количество добавляемого ацетона составляет 2770 г. Результаты примера приведены в таблице.The process of separating NaCl from wastewater for the production of epoxy-diane resins is carried out analogously to example 6. The difference is that the amount of added acetone is 2770 g. The results of the example are shown in the table.
Пример 9Example 9
Процесс выделения NaCl из сточной воды производства эпоксидно-диановых смол проводят аналогично примеру 6. Отличие состоит в том, что количество добавляемого ацетона составляет 2400 г. Результаты примера приведены в таблице.The process of separating NaCl from wastewater for the production of epoxy-diane resins is carried out analogously to example 6. The difference is that the amount of added acetone is 2400 g. The results of the example are shown in the table.
Пример 10Example 10
Процесс выделения NaCl из сточной воды производства эпоксидно-диановых смол проводят аналогично примеру 6. Отличие состоит в том, что количество добавляемого ацетона составляет 9125 г. Результаты примера приведены в таблице.The process of separating NaCl from wastewater for the production of epoxy-diane resins is carried out analogously to example 6. The difference is that the amount of added acetone is 9125 g. The results of the example are shown in the table.
Таким образом, результаты, представленные в таблице, показывают, что осадок NaCl выпадает при массовом избытке ацетона более чем 4,7; при этом указанный прием позволяет увеличить степень выделения кристаллической соли по сравнению с прототипом без необходимости предварительного выпаривания.Thus, the results presented in the table show that NaCl precipitates when there is a mass excess of acetone of more than 4.7; while this technique allows you to increase the degree of allocation of crystalline salts compared with the prototype without the need for preliminary evaporation.
Claims (1)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019122130A RU2713373C1 (en) | 2019-07-15 | 2019-07-15 | Method of extracting sodium chloride from waste water |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2019122130A RU2713373C1 (en) | 2019-07-15 | 2019-07-15 | Method of extracting sodium chloride from waste water |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2713373C1 true RU2713373C1 (en) | 2020-02-04 |
Family
ID=69624801
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2019122130A RU2713373C1 (en) | 2019-07-15 | 2019-07-15 | Method of extracting sodium chloride from waste water |
Country Status (1)
| Country | Link |
|---|---|
| RU (1) | RU2713373C1 (en) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2795234C1 (en) * | 2020-06-30 | 2023-05-02 | Чжуне Чантянь Интернэшнл Инджиниринг Ко., Лтд. | Method and system for self-induced separation of fluoride- and chloride-ions in fluoride and chloride-containing wastewater |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU442152A1 (en) * | 1972-10-27 | 1974-09-05 | Горьковский Филиал Всесоюзного Научно-Исследовательского И Проектного Института Нефтеперерабатывающей И Нефтехимической Промышленности | Method of extracting sodium chloride from wastewater electrical oil desalting plants |
| SU706331A1 (en) * | 1976-05-26 | 1979-12-30 | Предприятие П/Я В-8130 | Method of waste water purification from sodium chloride |
| DE10230437A1 (en) * | 2002-07-06 | 2004-01-22 | Walter Heinelt | Organic flocculants useful in water treatment are obtained from renewable sources by (preferably multistage) extraction from protein-containing materials |
| RU2263116C2 (en) * | 2000-04-14 | 2005-10-27 | Дау Агросайенсиз Ллс | Chloride removing in method for preparing phosphonomethyliminodiacetic acid |
| RU2277513C2 (en) * | 2002-06-24 | 2006-06-10 | Париченко Александр Валентинович | Method for complex processing iodine-bromine-containing sodium-chloride waters |
-
2019
- 2019-07-15 RU RU2019122130A patent/RU2713373C1/en active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU442152A1 (en) * | 1972-10-27 | 1974-09-05 | Горьковский Филиал Всесоюзного Научно-Исследовательского И Проектного Института Нефтеперерабатывающей И Нефтехимической Промышленности | Method of extracting sodium chloride from wastewater electrical oil desalting plants |
| SU706331A1 (en) * | 1976-05-26 | 1979-12-30 | Предприятие П/Я В-8130 | Method of waste water purification from sodium chloride |
| RU2263116C2 (en) * | 2000-04-14 | 2005-10-27 | Дау Агросайенсиз Ллс | Chloride removing in method for preparing phosphonomethyliminodiacetic acid |
| RU2277513C2 (en) * | 2002-06-24 | 2006-06-10 | Париченко Александр Валентинович | Method for complex processing iodine-bromine-containing sodium-chloride waters |
| DE10230437A1 (en) * | 2002-07-06 | 2004-01-22 | Walter Heinelt | Organic flocculants useful in water treatment are obtained from renewable sources by (preferably multistage) extraction from protein-containing materials |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2795234C1 (en) * | 2020-06-30 | 2023-05-02 | Чжуне Чантянь Интернэшнл Инджиниринг Ко., Лтд. | Method and system for self-induced separation of fluoride- and chloride-ions in fluoride and chloride-containing wastewater |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| SU778707A3 (en) | Method of purifying sodium chloride solution | |
| WO2017181759A1 (en) | Method for manufacturing anhydrous lithium chloride using lithium-containing wastewater | |
| US4115219A (en) | Brine purification process | |
| CA2945309A1 (en) | Method for barium and norm removal from produced water | |
| RU2713373C1 (en) | Method of extracting sodium chloride from waste water | |
| AU2006201116B2 (en) | A cost effective process for the preparation of solar salt having high purity and whiteness | |
| JP5167448B2 (en) | Method for removing calcium and magnesium ions in water | |
| RU2036838C1 (en) | Method for purification of sodium chloride | |
| US3846081A (en) | Process for separating sodium sulfate from brines | |
| RU2230029C2 (en) | Method for additional saturation and treatment of natural ground liquor fr om impurity of calcium and magnesium ions | |
| RU2565681C1 (en) | Method of producing barium chloride dihydrate | |
| US3421877A (en) | Method of precipitating potash from a phosphate mixture | |
| SU999455A1 (en) | Method for softening water | |
| SU343568A1 (en) | Method of purifing mercury-containing waste water | |
| RU2237021C1 (en) | Aluminum-containing coagulator preparation method | |
| RU2334678C2 (en) | Method of sulphate-ion absorption in metal chloride aqueous solutions | |
| US6812011B2 (en) | Process for the removal of calcium ions from the brine by marine cyanobacteria | |
| RU2060973C1 (en) | Chloride-sulfate sewage or natural waters treatment method | |
| Halmeredova et al. | POSSIBILITIES OF OBTAINING HIGH PURITY MgO FROM LOCAL RAW BISCHOFITE MINERAL | |
| KR20240103265A (en) | Purifying method of bittern | |
| SU138223A1 (en) | The method of intensifying the brine cleaning process for the electrolysis of sodium chloride | |
| WO2007110733A1 (en) | A process for the recovery of superior quality and super white industrial grade salt from subsoil/sea brines | |
| RU1824379C (en) | Process for separating water-soluble barium salts from solid waste after leaching-out of barium sulfide melt | |
| JPS583973B2 (en) | Rinofukumu aluminum case | |
| SU1074821A1 (en) | Process for preparing magnesium hydroxide |