RU2655170C2 - Производные 1-фенил-2-пиридинилалкиловых спиртов в качестве ингибиторов фосфодиэстеразы - Google Patents
Производные 1-фенил-2-пиридинилалкиловых спиртов в качестве ингибиторов фосфодиэстеразы Download PDFInfo
- Publication number
- RU2655170C2 RU2655170C2 RU2015121045A RU2015121045A RU2655170C2 RU 2655170 C2 RU2655170 C2 RU 2655170C2 RU 2015121045 A RU2015121045 A RU 2015121045A RU 2015121045 A RU2015121045 A RU 2015121045A RU 2655170 C2 RU2655170 C2 RU 2655170C2
- Authority
- RU
- Russia
- Prior art keywords
- mmol
- alkyl
- group
- substituted
- cyclopropylmethoxy
- Prior art date
Links
- 229940082638 cardiac stimulant phosphodiesterase inhibitors Drugs 0.000 title 1
- 239000002571 phosphodiesterase inhibitor Substances 0.000 title 1
- 150000001875 compounds Chemical class 0.000 claims abstract description 186
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical group C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 claims abstract description 61
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 claims abstract description 56
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims abstract description 48
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 claims abstract description 39
- 150000003839 salts Chemical class 0.000 claims abstract description 35
- 125000005843 halogen group Chemical group 0.000 claims abstract description 29
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 21
- 125000001424 substituent group Chemical group 0.000 claims abstract description 20
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims abstract description 17
- 150000001204 N-oxides Chemical class 0.000 claims abstract description 16
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims abstract description 15
- 125000002757 morpholinyl group Chemical group 0.000 claims abstract description 13
- 239000003814 drug Substances 0.000 claims abstract description 12
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 claims abstract description 10
- 208000006673 asthma Diseases 0.000 claims abstract description 10
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 8
- 208000026935 allergic disease Diseases 0.000 claims abstract description 6
- 125000006700 (C1-C6) alkylthio group Chemical group 0.000 claims abstract description 5
- 206010012438 Dermatitis atopic Diseases 0.000 claims abstract description 5
- 201000008937 atopic dermatitis Diseases 0.000 claims abstract description 5
- 125000004076 pyridyl group Chemical group 0.000 claims abstract description 5
- 206010039085 Rhinitis allergic Diseases 0.000 claims abstract description 4
- 208000024780 Urticaria Diseases 0.000 claims abstract description 4
- 201000010105 allergic rhinitis Diseases 0.000 claims abstract description 4
- 230000002401 inhibitory effect Effects 0.000 claims abstract description 4
- 101100296720 Dictyostelium discoideum Pde4 gene Proteins 0.000 claims abstract 3
- 101100082610 Plasmodium falciparum (isolate 3D7) PDEdelta gene Proteins 0.000 claims abstract 3
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 68
- 229910052757 nitrogen Inorganic materials 0.000 claims description 38
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 34
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 34
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 23
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 22
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 14
- 125000004432 carbon atom Chemical group C* 0.000 claims description 14
- 229910052760 oxygen Inorganic materials 0.000 claims description 11
- 125000004193 piperazinyl group Chemical group 0.000 claims description 11
- 125000004429 atom Chemical group 0.000 claims description 10
- 125000002950 monocyclic group Chemical group 0.000 claims description 10
- 208000023504 respiratory system disease Diseases 0.000 claims description 10
- 201000010099 disease Diseases 0.000 claims description 9
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims description 8
- 208000000884 Airway Obstruction Diseases 0.000 claims description 7
- 229910052799 carbon Inorganic materials 0.000 claims description 7
- 229910052717 sulfur Inorganic materials 0.000 claims description 7
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 6
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 6
- 239000000443 aerosol Substances 0.000 claims description 5
- 238000004519 manufacturing process Methods 0.000 claims description 5
- 125000003545 alkoxy group Chemical group 0.000 claims description 4
- 239000003937 drug carrier Substances 0.000 claims description 4
- 230000002265 prevention Effects 0.000 claims description 4
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 3
- 229940112141 dry powder inhaler Drugs 0.000 claims description 3
- 229940071648 metered dose inhaler Drugs 0.000 claims description 2
- 239000006199 nebulizer Substances 0.000 claims 3
- 239000003595 mist Substances 0.000 claims 2
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 claims 2
- 210000002345 respiratory system Anatomy 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 218
- 239000000126 substance Substances 0.000 abstract description 21
- 230000000694 effects Effects 0.000 abstract description 18
- 229910052739 hydrogen Inorganic materials 0.000 abstract description 14
- 125000000217 alkyl group Chemical group 0.000 abstract description 9
- 201000009961 allergic asthma Diseases 0.000 abstract 1
- 208000028004 allergic respiratory disease Diseases 0.000 abstract 1
- XSXHWVKGUXMUQE-UHFFFAOYSA-N osmium dioxide Inorganic materials O=[Os]=O XSXHWVKGUXMUQE-UHFFFAOYSA-N 0.000 abstract 1
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 396
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 369
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 255
- 230000015572 biosynthetic process Effects 0.000 description 244
- 238000003786 synthesis reaction Methods 0.000 description 239
- 239000000243 solution Substances 0.000 description 198
- 238000004949 mass spectrometry Methods 0.000 description 174
- 239000002904 solvent Substances 0.000 description 135
- 239000011734 sodium Substances 0.000 description 134
- -1 for example Substances 0.000 description 126
- 235000019439 ethyl acetate Nutrition 0.000 description 125
- 239000011541 reaction mixture Substances 0.000 description 125
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 123
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical class Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 116
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 113
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 113
- 239000012043 crude product Substances 0.000 description 94
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 92
- 238000000746 purification Methods 0.000 description 89
- 239000012074 organic phase Substances 0.000 description 83
- 238000000034 method Methods 0.000 description 78
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 70
- 239000012267 brine Substances 0.000 description 68
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 68
- 239000000047 product Substances 0.000 description 64
- 239000007787 solid Substances 0.000 description 61
- 239000012044 organic layer Substances 0.000 description 59
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 58
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 57
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 50
- 238000005481 NMR spectroscopy Methods 0.000 description 49
- 239000000741 silica gel Substances 0.000 description 49
- 229910002027 silica gel Inorganic materials 0.000 description 49
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 48
- PSHKMPUSSFXUIA-UHFFFAOYSA-N n,n-dimethylpyridin-2-amine Chemical compound CN(C)C1=CC=CC=N1 PSHKMPUSSFXUIA-UHFFFAOYSA-N 0.000 description 46
- ILVXOBCQQYKLDS-UHFFFAOYSA-N pyridine N-oxide Chemical class [O-][N+]1=CC=CC=C1 ILVXOBCQQYKLDS-UHFFFAOYSA-N 0.000 description 43
- 238000003818 flash chromatography Methods 0.000 description 42
- 238000006243 chemical reaction Methods 0.000 description 41
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 38
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 35
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 34
- 102000011017 Type 4 Cyclic Nucleotide Phosphodiesterases Human genes 0.000 description 34
- 108010037584 Type 4 Cyclic Nucleotide Phosphodiesterases Proteins 0.000 description 34
- 229920006395 saturated elastomer Polymers 0.000 description 34
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 33
- MSYGAHOHLUJIKV-UHFFFAOYSA-N 3,5-dimethyl-1-(3-nitrophenyl)-1h-pyrazole-4-carboxylic acid ethyl ester Chemical compound CC1=C(C(=O)OCC)C(C)=NN1C1=CC=CC([N+]([O-])=O)=C1 MSYGAHOHLUJIKV-UHFFFAOYSA-N 0.000 description 28
- 238000002953 preparative HPLC Methods 0.000 description 26
- 239000003153 chemical reaction reagent Substances 0.000 description 23
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 23
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 22
- 239000003921 oil Substances 0.000 description 21
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 21
- 239000002243 precursor Substances 0.000 description 21
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 20
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical class OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 20
- QARBMVPHQWIHKH-UHFFFAOYSA-N methanesulfonyl chloride Chemical compound CS(Cl)(=O)=O QARBMVPHQWIHKH-UHFFFAOYSA-N 0.000 description 20
- 239000003208 petroleum Substances 0.000 description 20
- 230000002829 reductive effect Effects 0.000 description 20
- 229910052938 sodium sulfate Inorganic materials 0.000 description 20
- 235000011152 sodium sulphate Nutrition 0.000 description 20
- 239000012359 Methanesulfonyl chloride Substances 0.000 description 19
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 18
- 239000008346 aqueous phase Substances 0.000 description 18
- 229940126214 compound 3 Drugs 0.000 description 18
- 238000001914 filtration Methods 0.000 description 18
- 239000000725 suspension Substances 0.000 description 18
- 238000002360 preparation method Methods 0.000 description 16
- 239000003054 catalyst Substances 0.000 description 15
- 239000000706 filtrate Substances 0.000 description 15
- 239000002244 precipitate Substances 0.000 description 15
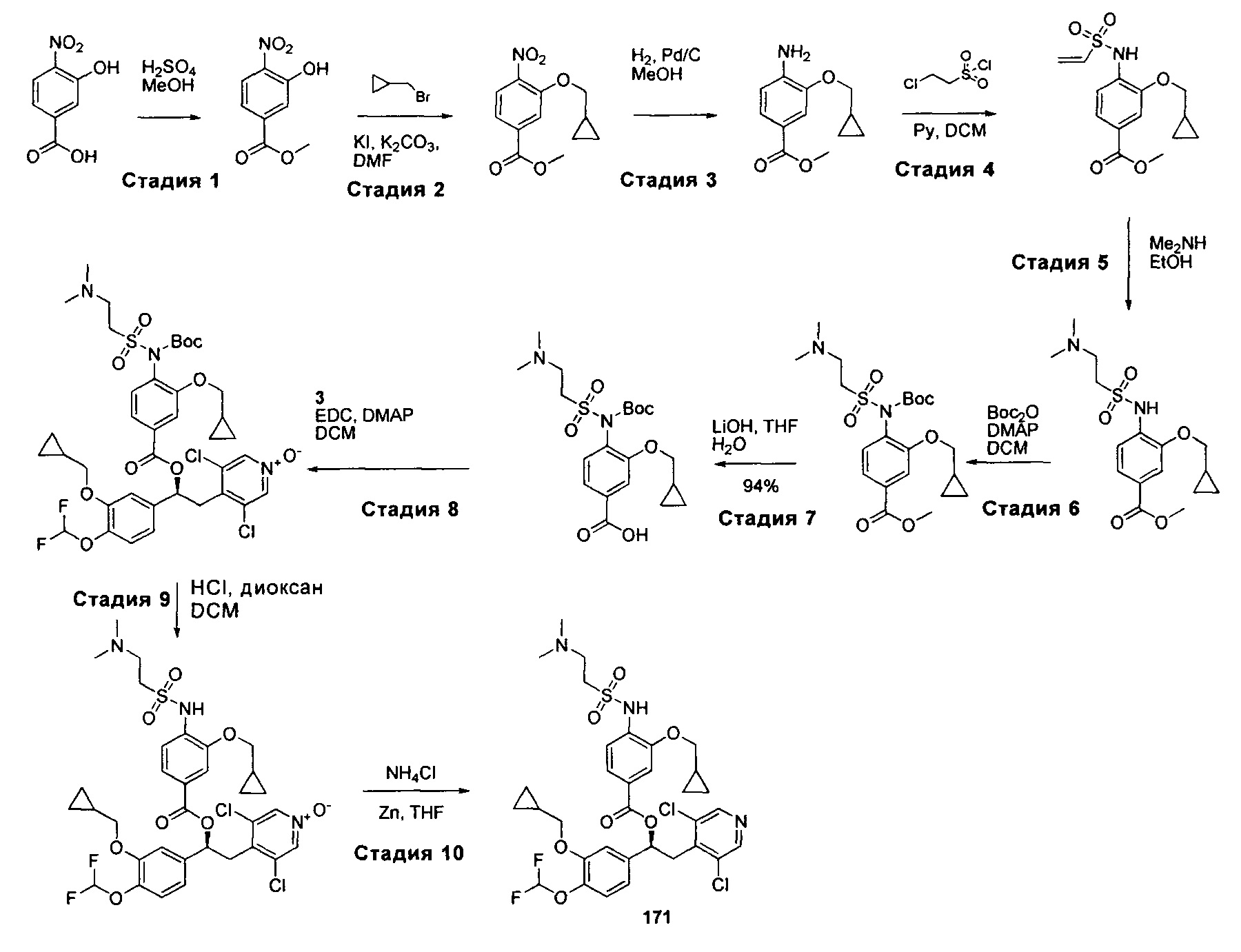
- QGXYRJFTOQJWBR-HNNXBMFYSA-N (1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethanol Chemical compound C([C@H](O)C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)C1=C(Cl)C=[N+]([O-])C=C1Cl QGXYRJFTOQJWBR-HNNXBMFYSA-N 0.000 description 14
- 229910052763 palladium Inorganic materials 0.000 description 14
- DYAUJEIALQJPGW-ZDUSSCGKSA-N (1s)-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)-1-(3,4-dimethoxyphenyl)ethanol Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H](O)CC1=C(Cl)C=[N+]([O-])C=C1Cl DYAUJEIALQJPGW-ZDUSSCGKSA-N 0.000 description 13
- 125000001231 benzoyloxy group Chemical group C(C1=CC=CC=C1)(=O)O* 0.000 description 13
- 239000000460 chlorine Substances 0.000 description 13
- 125000002947 alkylene group Chemical group 0.000 description 12
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 12
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 11
- 125000003118 aryl group Chemical group 0.000 description 11
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 10
- 239000003112 inhibitor Substances 0.000 description 10
- 239000000543 intermediate Substances 0.000 description 10
- 239000002587 phosphodiesterase IV inhibitor Substances 0.000 description 10
- 239000000843 powder Substances 0.000 description 10
- 238000012799 strong cation exchange Methods 0.000 description 10
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 10
- NBJHDLKSWUDGJG-UHFFFAOYSA-N 4-(2-chloroethyl)morpholin-4-ium;chloride Chemical compound Cl.ClCCN1CCOCC1 NBJHDLKSWUDGJG-UHFFFAOYSA-N 0.000 description 9
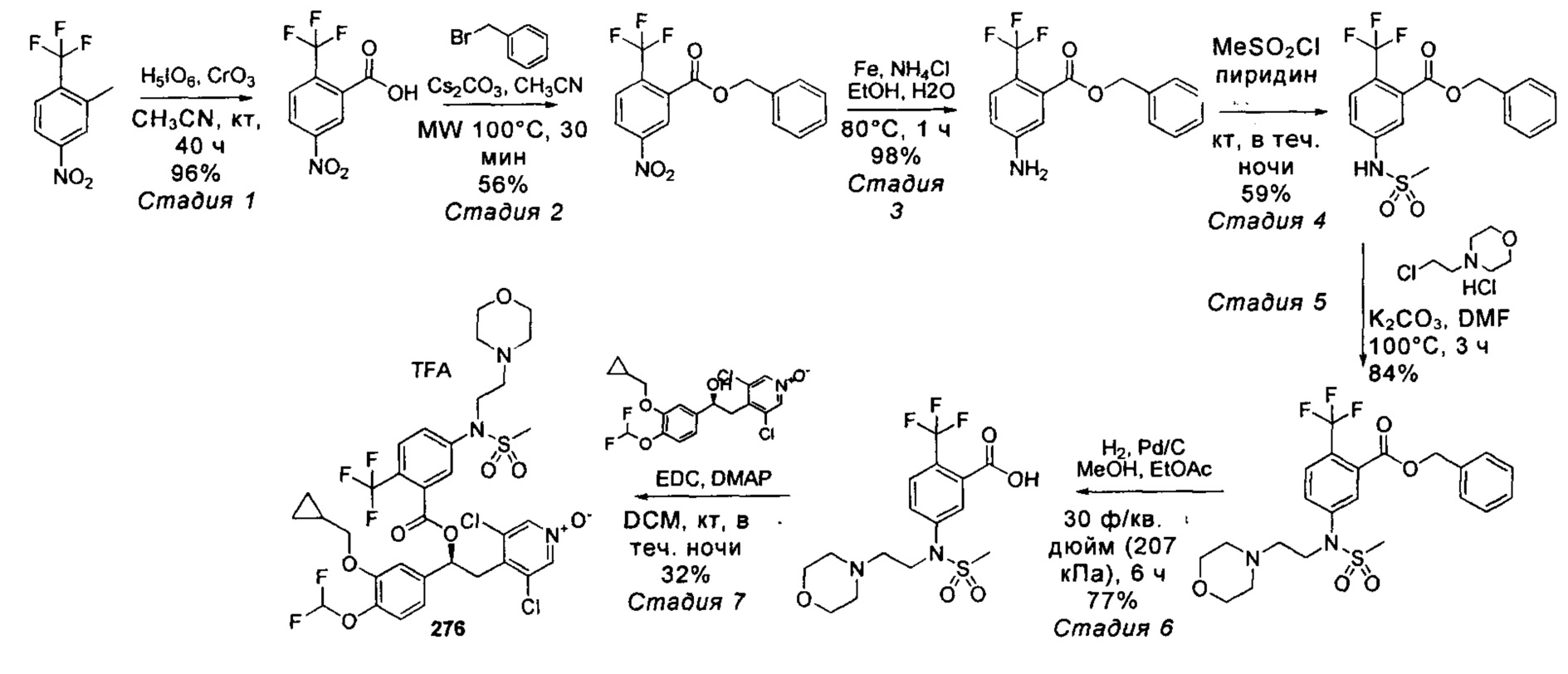
- NVSGZALPIBBBHJ-UHFFFAOYSA-N 5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-2-(trifluoromethyl)benzoic acid Chemical compound C=1C=C(C(F)(F)F)C(C(O)=O)=CC=1N(S(=O)(=O)C)CCN1CCOCC1 NVSGZALPIBBBHJ-UHFFFAOYSA-N 0.000 description 9
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 9
- 229940123932 Phosphodiesterase 4 inhibitor Drugs 0.000 description 9
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical class OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 9
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical class [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 9
- 239000013058 crude material Substances 0.000 description 9
- OMCTZIDLDSYPOA-UHFFFAOYSA-N methyl 4-formyl-3-hydroxybenzoate Chemical compound COC(=O)C1=CC=C(C=O)C(O)=C1 OMCTZIDLDSYPOA-UHFFFAOYSA-N 0.000 description 9
- 239000012071 phase Substances 0.000 description 9
- 239000003643 water by type Substances 0.000 description 9
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 8
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 8
- SKXJCVSNYQCJPO-UHFFFAOYSA-N benzyl 4-methoxy-3-nitrobenzoate Chemical compound C1=C([N+]([O-])=O)C(OC)=CC=C1C(=O)OCC1=CC=CC=C1 SKXJCVSNYQCJPO-UHFFFAOYSA-N 0.000 description 8
- 210000004027 cell Anatomy 0.000 description 8
- 239000003480 eluent Substances 0.000 description 8
- 239000003039 volatile agent Substances 0.000 description 8
- VHCSBTPOPKFYIU-UHFFFAOYSA-N 2-chloroethanesulfonyl chloride Chemical compound ClCCS(Cl)(=O)=O VHCSBTPOPKFYIU-UHFFFAOYSA-N 0.000 description 7
- BTBLBVBMPFYTAB-UHFFFAOYSA-N 3-(cyclopropylmethoxy)-4-formylbenzoic acid Chemical compound OC(=O)C1=CC=C(C=O)C(OCC2CC2)=C1 BTBLBVBMPFYTAB-UHFFFAOYSA-N 0.000 description 7
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 7
- PLQYUCHTKRSOPN-UHFFFAOYSA-N benzyl 3-amino-4-methoxybenzoate Chemical compound C1=C(N)C(OC)=CC=C1C(=O)OCC1=CC=CC=C1 PLQYUCHTKRSOPN-UHFFFAOYSA-N 0.000 description 7
- AGEZXYOZHKGVCM-UHFFFAOYSA-N benzyl bromide Chemical compound BrCC1=CC=CC=C1 AGEZXYOZHKGVCM-UHFFFAOYSA-N 0.000 description 7
- 239000000284 extract Substances 0.000 description 7
- 125000001072 heteroaryl group Chemical group 0.000 description 7
- PPCWEDFQZMONBE-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-formylbenzoate Chemical compound COC(=O)C1=CC=C(C=O)C(OCC2CC2)=C1 PPCWEDFQZMONBE-UHFFFAOYSA-N 0.000 description 7
- WYSLGSINIUGBBN-UHFFFAOYSA-N 2-(3,5-dichloropyridin-4-yl)-1-(3,4-dimethoxyphenyl)ethanol Chemical compound C1=C(OC)C(OC)=CC=C1C(O)CC1=C(Cl)C=NC=C1Cl WYSLGSINIUGBBN-UHFFFAOYSA-N 0.000 description 6
- ZAPMTSHEXFEPSD-UHFFFAOYSA-N 4-(2-chloroethyl)morpholine Chemical compound ClCCN1CCOCC1 ZAPMTSHEXFEPSD-UHFFFAOYSA-N 0.000 description 6
- NSYRZWASUWJVHA-UHFFFAOYSA-N 4-fluoro-3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoic acid;hydrochloride Chemical compound Cl.C=1C(C(O)=O)=CC=C(F)C=1N(S(=O)(=O)C)CCN1CCOCC1 NSYRZWASUWJVHA-UHFFFAOYSA-N 0.000 description 6
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- KQUWGGFZSKCNBW-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonyloxy]benzoate Chemical compound CN(C)CCS(=O)(=O)OC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 KQUWGGFZSKCNBW-LJAQVGFWSA-N 0.000 description 6
- FELKNKYFKPEIAC-QHCPKHFHSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-amino-4-methoxybenzoate Chemical compound C1=C(N)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl FELKNKYFKPEIAC-QHCPKHFHSA-N 0.000 description 6
- QQGCRYBWNJSLAN-XIFFEERXSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 5-[cyclopropylmethyl(methylsulfonyl)amino]-2-(2-morpholin-4-ylethoxy)benzoate Chemical compound C=1C=C(OCCN2CCOCC2)C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=1N(S(=O)(=O)C)CC1CC1 QQGCRYBWNJSLAN-XIFFEERXSA-N 0.000 description 6
- 150000001298 alcohols Chemical class 0.000 description 6
- 239000012298 atmosphere Substances 0.000 description 6
- 150000001721 carbon Chemical group 0.000 description 6
- 230000003197 catalytic effect Effects 0.000 description 6
- 238000004140 cleaning Methods 0.000 description 6
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 6
- 230000005764 inhibitory process Effects 0.000 description 6
- 229910000027 potassium carbonate Inorganic materials 0.000 description 6
- 125000006239 protecting group Chemical group 0.000 description 6
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 6
- 238000001946 ultra-performance liquid chromatography-mass spectrometry Methods 0.000 description 6
- PVOAHINGSUIXLS-UHFFFAOYSA-N 1-Methylpiperazine Chemical compound CN1CCNCC1 PVOAHINGSUIXLS-UHFFFAOYSA-N 0.000 description 5
- YLQBMQCUIZJEEH-UHFFFAOYSA-N Furan Chemical compound C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 5
- 101000851058 Homo sapiens Neutrophil elastase Proteins 0.000 description 5
- RUOFEFCMHWDXKC-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-4-(trifluoromethoxy)benzoate Chemical compound C=1C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C(OC(F)(F)F)C=1N(S(=O)(=O)C)CCN1CCOCC1 RUOFEFCMHWDXKC-LJAQVGFWSA-N 0.000 description 5
- MGVQTDUVHPBISW-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-hydroxy-5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C=1C(O)=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=1N(S(=O)(=O)C)CCN1CCOCC1 MGVQTDUVHPBISW-LJAQVGFWSA-N 0.000 description 5
- VARHSHPWXKGCDF-MHZLTWQESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-methylsulfonyloxy-4-(morpholin-4-ylmethyl)benzoate Chemical compound CS(=O)(=O)OC1=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C1CN1CCOCC1 VARHSHPWXKGCDF-MHZLTWQESA-N 0.000 description 5
- PHOZKCCATQUABR-XIFFEERXSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-(cyclopropylmethoxy)-3-[[2-(4-hydroxypiperidin-1-yl)acetyl]oxymethyl]benzoate Chemical compound C1CC(O)CCN1CC(=O)OCC1=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C1OCC1CC1 PHOZKCCATQUABR-XIFFEERXSA-N 0.000 description 5
- AGLKDNVWFUPNID-NDEPHWFRSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-[(4-hydroxypiperidin-1-yl)methyl]benzoate Chemical compound C1CC(O)CCN1CC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1 AGLKDNVWFUPNID-NDEPHWFRSA-N 0.000 description 5
- WGAJZOQTRSYMFN-HKBQPEDESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-[2-(4-methylpiperazin-1-yl)ethyl-methylsulfonylamino]benzoate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1N(S(C)(=O)=O)CCN1CCN(C)CC1 WGAJZOQTRSYMFN-HKBQPEDESA-N 0.000 description 5
- BKCJWDGWPZVRSD-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methylsulfanyl-3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound CSC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1N(S(C)(=O)=O)CCN1CCOCC1 BKCJWDGWPZVRSD-LJAQVGFWSA-N 0.000 description 5
- FUYBOJVZHMVHNP-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-2-(trifluoromethyl)benzoate Chemical compound C=1C=C(C(F)(F)F)C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=1N(S(=O)(=O)C)CCN1CCOCC1 FUYBOJVZHMVHNP-LJAQVGFWSA-N 0.000 description 5
- TVLCPPKXBQFYJY-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloropyridin-4-yl)ethyl] 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonylamino]benzoate Chemical compound CN(C)CCS(=O)(=O)NC1=CC=C(C(=O)O[C@@H](CC=2C(=CN=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 TVLCPPKXBQFYJY-LJAQVGFWSA-N 0.000 description 5
- 239000002253 acid Substances 0.000 description 5
- 239000004480 active ingredient Substances 0.000 description 5
- 235000019270 ammonium chloride Nutrition 0.000 description 5
- AEILLAXRDHDKDY-UHFFFAOYSA-N bromomethylcyclopropane Chemical compound BrCC1CC1 AEILLAXRDHDKDY-UHFFFAOYSA-N 0.000 description 5
- DODUOCYKSQVFSW-UHFFFAOYSA-N methyl 2-hydroxy-4-nitrobenzoate Chemical compound COC(=O)C1=CC=C([N+]([O-])=O)C=C1O DODUOCYKSQVFSW-UHFFFAOYSA-N 0.000 description 5
- RLLPKYHTNFTXCB-UHFFFAOYSA-N methyl 3-[2-bromoethyl(methylsulfonyl)amino]-4-methoxybenzoate Chemical compound COC(=O)C1=CC=C(OC)C(N(CCBr)S(C)(=O)=O)=C1 RLLPKYHTNFTXCB-UHFFFAOYSA-N 0.000 description 5
- ABELEDYNIKPYTP-UHFFFAOYSA-N methyl 3-amino-4-fluorobenzoate Chemical compound COC(=O)C1=CC=C(F)C(N)=C1 ABELEDYNIKPYTP-UHFFFAOYSA-N 0.000 description 5
- IGZVMSNMPKWRKJ-UHFFFAOYSA-N methyl 4-amino-2-(cyclopropylmethoxy)benzoate Chemical compound COC(=O)C1=CC=C(N)C=C1OCC1CC1 IGZVMSNMPKWRKJ-UHFFFAOYSA-N 0.000 description 5
- 229940021182 non-steroidal anti-inflammatory drug Drugs 0.000 description 5
- QQOXBFUTRLDXDP-UHFFFAOYSA-N p-Aminosalicylic acid methyl ester Chemical compound COC(=O)C1=CC=C(N)C=C1O QQOXBFUTRLDXDP-UHFFFAOYSA-N 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- 238000011894 semi-preparative HPLC Methods 0.000 description 5
- 239000012453 solvate Substances 0.000 description 5
- 238000003756 stirring Methods 0.000 description 5
- WYSLGSINIUGBBN-ZDUSSCGKSA-N (1s)-2-(3,5-dichloropyridin-4-yl)-1-(3,4-dimethoxyphenyl)ethanol Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H](O)CC1=C(Cl)C=NC=C1Cl WYSLGSINIUGBBN-ZDUSSCGKSA-N 0.000 description 4
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 4
- MAHPJVZDUAZCFX-UHFFFAOYSA-N 3-(cyclopropylmethoxy)-4-(methanesulfonamidomethyl)benzoic acid Chemical compound CS(=O)(=O)NCC1=CC=C(C(O)=O)C=C1OCC1CC1 MAHPJVZDUAZCFX-UHFFFAOYSA-N 0.000 description 4
- OTVNZCIGNATQOA-AUWJEWJLSA-N 3-(cyclopropylmethoxy)-4-[(z)-methoxyiminomethyl]benzoic acid Chemical compound CO\N=C/C1=CC=C(C(O)=O)C=C1OCC1CC1 OTVNZCIGNATQOA-AUWJEWJLSA-N 0.000 description 4
- BSXNVOQJLGBWLK-UHFFFAOYSA-N 3-(cyclopropylmethoxy)-4-[[(2-methylpropan-2-yl)oxycarbonyl-methylsulfonylamino]methyl]benzoic acid Chemical compound CC(C)(C)OC(=O)N(S(C)(=O)=O)CC1=CC=C(C(O)=O)C=C1OCC1CC1 BSXNVOQJLGBWLK-UHFFFAOYSA-N 0.000 description 4
- DGFPAXDGMBJAGI-UHFFFAOYSA-N 3-(cyclopropylmethoxy)-4-phenylmethoxybenzoic acid Chemical compound C1CC1COC1=CC(C(=O)O)=CC=C1OCC1=CC=CC=C1 DGFPAXDGMBJAGI-UHFFFAOYSA-N 0.000 description 4
- QERVNOKASLAHRB-UHFFFAOYSA-N 3-(methanesulfonamidomethyl)-4-(2-morpholin-4-ylethoxy)benzoic acid;hydrochloride Chemical compound Cl.CS(=O)(=O)NCC1=CC(C(O)=O)=CC=C1OCCN1CCOCC1 QERVNOKASLAHRB-UHFFFAOYSA-N 0.000 description 4
- YDINJXAQACKSIR-UHFFFAOYSA-N 3-[[(2-methylpropan-2-yl)oxycarbonyl-methylsulfonylamino]methyl]-4-(2-morpholin-4-ylethoxy)benzoic acid Chemical compound CC(C)(C)OC(=O)N(S(C)(=O)=O)CC1=CC(C(O)=O)=CC=C1OCCN1CCOCC1 YDINJXAQACKSIR-UHFFFAOYSA-N 0.000 description 4
- CCJLDXIQEDPUAJ-UHFFFAOYSA-N 3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-4-phenylmethoxybenzoic acid Chemical compound C=1C(C(O)=O)=CC=C(OCC=2C=CC=CC=2)C=1N(S(=O)(=O)C)CCN1CCOCC1 CCJLDXIQEDPUAJ-UHFFFAOYSA-N 0.000 description 4
- RPAPJTAUMMPQTE-UHFFFAOYSA-N 3-acetyloxy-5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoic acid Chemical compound OC(=O)C1=CC(OC(=O)C)=CC(N(CCN2CCOCC2)S(C)(=O)=O)=C1 RPAPJTAUMMPQTE-UHFFFAOYSA-N 0.000 description 4
- JSMLGVRLNULZNZ-UHFFFAOYSA-N 3-hydroxy-5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoic acid Chemical compound C=1C(O)=CC(C(O)=O)=CC=1N(S(=O)(=O)C)CCN1CCOCC1 JSMLGVRLNULZNZ-UHFFFAOYSA-N 0.000 description 4
- HQCBBKCBTJTSMB-UHFFFAOYSA-N 3-methylsulfonyloxy-4-(morpholin-4-ylmethyl)benzoic acid Chemical compound CS(=O)(=O)OC1=CC(C(O)=O)=CC=C1CN1CCOCC1 HQCBBKCBTJTSMB-UHFFFAOYSA-N 0.000 description 4
- GDBCQTKUSLDFRP-UHFFFAOYSA-N 3-nitro-4-(trifluoromethoxy)benzoic acid Chemical compound OC(=O)C1=CC=C(OC(F)(F)F)C([N+]([O-])=O)=C1 GDBCQTKUSLDFRP-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- OAHBDSHKDYQNTF-UHFFFAOYSA-N 4-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-3-[2-(oxan-2-yloxy)ethoxy]benzoic acid Chemical compound C=1C=C(C(O)=O)C=C(OCCOC2OCCCC2)C=1N(S(=O)(=O)C)CCN1CCOCC1 OAHBDSHKDYQNTF-UHFFFAOYSA-N 0.000 description 4
- OWYMEUCMYFFMPF-UHFFFAOYSA-N 4-methoxy-3-[2-(4-methylpiperazin-1-yl)ethylsulfonyl-[(2-methylpropan-2-yl)oxycarbonyl]amino]benzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1N(C(=O)OC(C)(C)C)S(=O)(=O)CCN1CCN(C)CC1 OWYMEUCMYFFMPF-UHFFFAOYSA-N 0.000 description 4
- ZDLJNUMEHCOUPW-UHFFFAOYSA-N 4-methoxy-3-[[2-(4-methylpiperazin-1-yl)-2-oxoethyl]-methylsulfonylamino]benzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1N(S(C)(=O)=O)CC(=O)N1CCN(C)CC1 ZDLJNUMEHCOUPW-UHFFFAOYSA-N 0.000 description 4
- RWVVUCBHEBYETD-UHFFFAOYSA-N 5-(methanesulfonamidomethyl)-2-methoxybenzoic acid Chemical compound COC1=CC=C(CNS(C)(=O)=O)C=C1C(O)=O RWVVUCBHEBYETD-UHFFFAOYSA-N 0.000 description 4
- NJCMFCUSHLOWIW-UHFFFAOYSA-N 5-[cyclopropylmethyl(methylsulfonyl)amino]-2-(2-morpholin-4-ylethoxy)benzoic acid;hydrochloride Chemical compound Cl.C=1C=C(OCCN2CCOCC2)C(C(O)=O)=CC=1N(S(=O)(=O)C)CC1CC1 NJCMFCUSHLOWIW-UHFFFAOYSA-N 0.000 description 4
- XBARJDIECXHLTI-UHFFFAOYSA-N 5-nitro-2-(trifluoromethyl)benzoic acid Chemical compound OC(=O)C1=CC([N+]([O-])=O)=CC=C1C(F)(F)F XBARJDIECXHLTI-UHFFFAOYSA-N 0.000 description 4
- BDAGIHXWWSANSR-UHFFFAOYSA-N Formic acid Chemical class OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 4
- WAUBBBTZRCAKKO-HKBQPEDESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 2-methoxy-5-[[methylsulfonyl(2-morpholin-4-ylethyl)amino]methyl]benzoate Chemical compound C1=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C(OC)=CC=C1CN(S(C)(=O)=O)CCN1CCOCC1 WAUBBBTZRCAKKO-HKBQPEDESA-N 0.000 description 4
- BKCXCCSPLWKOQW-NDEPHWFRSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(cyclopropylmethoxy)-4-(methanesulfonamidomethyl)benzoate Chemical compound CS(=O)(=O)NCC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 BKCXCCSPLWKOQW-NDEPHWFRSA-N 0.000 description 4
- CJGFWENAAWFMPA-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonylamino]benzoate Chemical compound CN(C)CCS(=O)(=O)NC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 CJGFWENAAWFMPA-LJAQVGFWSA-N 0.000 description 4
- QCNMTKVZBAORQY-QHCPKHFHSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(methanesulfonamido)-4-methylsulfanylbenzoate Chemical compound C1=C(NS(C)(=O)=O)C(SC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl QCNMTKVZBAORQY-QHCPKHFHSA-N 0.000 description 4
- DNGHDWJQODSDFH-PMERELPUSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(methanesulfonamidomethyl)-4-(2-morpholin-4-ylethoxy)benzoate Chemical compound CS(=O)(=O)NCC1=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C1OCCN1CCOCC1 DNGHDWJQODSDFH-PMERELPUSA-N 0.000 description 4
- PQQYOZUKJXWHEN-NDEPHWFRSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[(2-bromoacetyl)oxymethyl]-4-(cyclopropylmethoxy)benzoate Chemical compound ClC1=C[N+]([O-])=CC(Cl)=C1C[C@@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)OC(=O)C(C=C1COC(=O)CBr)=CC=C1OCC1CC1 PQQYOZUKJXWHEN-NDEPHWFRSA-N 0.000 description 4
- DZQAMSARSOKUTB-NDEPHWFRSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[2-[bis(2-hydroxyethyl)amino]ethylsulfonyloxy]-4-methoxybenzoate Chemical compound C1=C(OS(=O)(=O)CCN(CCO)CCO)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl DZQAMSARSOKUTB-NDEPHWFRSA-N 0.000 description 4
- QMFHTSHVEIQZGD-WMUWJOOSSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[[2-[(2s,5r)-2,5-dimethylpiperazin-1-yl]acetyl]amino]-4-methoxybenzoate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1NC(=O)CN1C[C@@H](C)NC[C@@H]1C QMFHTSHVEIQZGD-WMUWJOOSSA-N 0.000 description 4
- YUPFSSHKFYNIDP-WMUWJOOSSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[[3-[(2s,5r)-2,5-dimethylpiperazin-1-yl]-3-oxopropanoyl]amino]-4-methoxybenzoate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1NC(=O)CC(=O)N1C[C@@H](C)NC[C@@H]1C YUPFSSHKFYNIDP-WMUWJOOSSA-N 0.000 description 4
- FYUPKTBGFGXVEV-QFIPXVFZSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-amino-4-methylsulfanylbenzoate Chemical compound C1=C(N)C(SC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl FYUPKTBGFGXVEV-QFIPXVFZSA-N 0.000 description 4
- NQPMZMOLUJWVRD-DEOSSOPVSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-ethenylsulfonyloxy-4-methoxybenzoate Chemical compound C1=C(OS(=O)(=O)C=C)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl NQPMZMOLUJWVRD-DEOSSOPVSA-N 0.000 description 4
- PZCMRYAWWGWNEQ-QHCPKHFHSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-hydroxy-4-methoxybenzoate Chemical compound C1=C(O)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl PZCMRYAWWGWNEQ-QHCPKHFHSA-N 0.000 description 4
- FDFNSYKTKJZLDS-MHZLTWQESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-(cyclopropylmethoxy)-3-(hydroxymethyl)benzoate Chemical compound OCC1=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C1OCC1CC1 FDFNSYKTKJZLDS-MHZLTWQESA-N 0.000 description 4
- AMPVJSXSLHCALV-SANMLTNESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-[2-(dimethylamino)ethylsulfamoyl]benzoate Chemical compound C1=CC(S(=O)(=O)NCCN(C)C)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl AMPVJSXSLHCALV-SANMLTNESA-N 0.000 description 4
- UOYIYMGGWMZTNO-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-fluoro-3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C=1C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C(F)C=1N(S(=O)(=O)C)CCN1CCOCC1 UOYIYMGGWMZTNO-LJAQVGFWSA-N 0.000 description 4
- AKOYBIKLOMEATC-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-hydroxy-3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C=1C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C(O)C=1N(S(=O)(=O)C)CCN1CCOCC1 AKOYBIKLOMEATC-LJAQVGFWSA-N 0.000 description 4
- QXGCWROEZFPBRY-NDEPHWFRSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-(2-morpholin-4-ylethylsulfamoyl)benzoate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1S(=O)(=O)NCCN1CCOCC1 QXGCWROEZFPBRY-NDEPHWFRSA-N 0.000 description 4
- XSBPZLUVBZJWPN-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-(2-morpholin-4-ylethylsulfonylamino)benzoate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1NS(=O)(=O)CCN1CCOCC1 XSBPZLUVBZJWPN-LJAQVGFWSA-N 0.000 description 4
- LXVOOZULLCHBLI-PMERELPUSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-[[2-(4-methylpiperazin-1-yl)-2-oxoethyl]-methylsulfonylamino]benzoate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1N(S(C)(=O)=O)CC(=O)N1CCN(C)CC1 LXVOOZULLCHBLI-PMERELPUSA-N 0.000 description 4
- SVBDUSYJETXHTF-QFIPXVFZSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methylsulfanyl-3-nitrobenzoate Chemical compound C1=C([N+]([O-])=O)C(SC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl SVBDUSYJETXHTF-QFIPXVFZSA-N 0.000 description 4
- MCSNSMASUYVJNV-VWLOTQADSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 5-(methanesulfonamidomethyl)-2-methoxybenzoate Chemical compound COC1=CC=C(CNS(C)(=O)=O)C=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl MCSNSMASUYVJNV-VWLOTQADSA-N 0.000 description 4
- KYASKMLWNGANFW-DEOSSOPVSA-N [(1s)-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)-1-(3,4-dimethoxyphenyl)ethyl] 3-(cyclopropylmethoxy)-4-(methanesulfonamido)benzoate Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H](OC(=O)C=1C=C(OCC2CC2)C(NS(C)(=O)=O)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl KYASKMLWNGANFW-DEOSSOPVSA-N 0.000 description 4
- XIZYDHQSAIJYDV-MHZLTWQESA-N [(1s)-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)-1-(3,4-dimethoxyphenyl)ethyl] 3-(cyclopropylmethoxy)-4-[(2-methylpropan-2-yl)oxycarbonyl-methylsulfonylamino]benzoate Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H](OC(=O)C=1C=C(OCC2CC2)C(N(C(=O)OC(C)(C)C)S(C)(=O)=O)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl XIZYDHQSAIJYDV-MHZLTWQESA-N 0.000 description 4
- XXROGKLTLUQVRX-UHFFFAOYSA-N allyl alcohol Chemical compound OCC=C XXROGKLTLUQVRX-UHFFFAOYSA-N 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- LPVGSXMJZMREDE-UHFFFAOYSA-N benzyl 3-(ethenylsulfonylamino)-4-methoxybenzoate Chemical compound C1=C(NS(=O)(=O)C=C)C(OC)=CC=C1C(=O)OCC1=CC=CC=C1 LPVGSXMJZMREDE-UHFFFAOYSA-N 0.000 description 4
- XZCFWEOIUDYHAY-UHFFFAOYSA-N benzyl 3-(methanesulfonamido)-4-methoxybenzoate Chemical compound C1=C(NS(C)(=O)=O)C(OC)=CC=C1C(=O)OCC1=CC=CC=C1 XZCFWEOIUDYHAY-UHFFFAOYSA-N 0.000 description 4
- KFIAJZHABCPMKL-UHFFFAOYSA-N benzyl 3-hydroxy-4-nitrobenzoate Chemical compound C1=C([N+]([O-])=O)C(O)=CC(C(=O)OCC=2C=CC=CC=2)=C1 KFIAJZHABCPMKL-UHFFFAOYSA-N 0.000 description 4
- NSELGVMBLDAUKB-UHFFFAOYSA-N benzyl 4-(methanesulfonamido)-3-[2-(oxan-2-yloxy)ethoxy]benzoate Chemical compound CS(=O)(=O)NC1=CC=C(C(=O)OCC=2C=CC=CC=2)C=C1OCCOC1CCCCO1 NSELGVMBLDAUKB-UHFFFAOYSA-N 0.000 description 4
- ITMPJXWMAFOINN-UHFFFAOYSA-N benzyl 4-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-3-[2-(oxan-2-yloxy)ethoxy]benzoate Chemical compound C=1C=C(C(=O)OCC=2C=CC=CC=2)C=C(OCCOC2OCCCC2)C=1N(S(=O)(=O)C)CCN1CCOCC1 ITMPJXWMAFOINN-UHFFFAOYSA-N 0.000 description 4
- LQMJUSOWNKNXLD-UHFFFAOYSA-N benzyl 4-amino-3-[2-(oxan-2-yloxy)ethoxy]benzoate Chemical compound NC1=CC=C(C(=O)OCC=2C=CC=CC=2)C=C1OCCOC1CCCCO1 LQMJUSOWNKNXLD-UHFFFAOYSA-N 0.000 description 4
- ZKXXVZADUWIAMJ-UHFFFAOYSA-N benzyl 4-methoxy-3-[2-(4-methylpiperazin-1-yl)ethylsulfonyl-[(2-methylpropan-2-yl)oxycarbonyl]amino]benzoate Chemical compound COC1=CC=C(C(=O)OCC=2C=CC=CC=2)C=C1N(C(=O)OC(C)(C)C)S(=O)(=O)CCN1CCN(C)CC1 ZKXXVZADUWIAMJ-UHFFFAOYSA-N 0.000 description 4
- XQDIRFLGDZJRRI-UHFFFAOYSA-N benzyl 4-methoxy-3-[2-(4-methylpiperazin-1-yl)ethylsulfonylamino]benzoate Chemical compound COC1=CC=C(C(=O)OCC=2C=CC=CC=2)C=C1NS(=O)(=O)CCN1CCN(C)CC1 XQDIRFLGDZJRRI-UHFFFAOYSA-N 0.000 description 4
- WTKMYFADPQYRAA-UHFFFAOYSA-N benzyl 4-methoxy-3-[[2-(4-methylpiperazin-1-yl)-2-oxoethyl]-methylsulfonylamino]benzoate Chemical compound COC1=CC=C(C(=O)OCC=2C=CC=CC=2)C=C1N(S(C)(=O)=O)CC(=O)N1CCN(C)CC1 WTKMYFADPQYRAA-UHFFFAOYSA-N 0.000 description 4
- CJEGVOHRKGTLAD-UHFFFAOYSA-N benzyl 4-nitro-3-[2-(oxan-2-yloxy)ethoxy]benzoate Chemical compound [O-][N+](=O)C1=CC=C(C(=O)OCC=2C=CC=CC=2)C=C1OCCOC1CCCCO1 CJEGVOHRKGTLAD-UHFFFAOYSA-N 0.000 description 4
- XMVJCYVIXLJWNN-UHFFFAOYSA-N benzyl 5-(methanesulfonamido)-2-(trifluoromethyl)benzoate Chemical compound CS(=O)(=O)NC1=CC=C(C(F)(F)F)C(C(=O)OCC=2C=CC=CC=2)=C1 XMVJCYVIXLJWNN-UHFFFAOYSA-N 0.000 description 4
- HBOMETFRAMFHMY-UHFFFAOYSA-N benzyl 5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-2-(trifluoromethyl)benzoate Chemical compound C=1C=C(C(F)(F)F)C(C(=O)OCC=2C=CC=CC=2)=CC=1N(S(=O)(=O)C)CCN1CCOCC1 HBOMETFRAMFHMY-UHFFFAOYSA-N 0.000 description 4
- JGZBXSDRYWNHLN-UHFFFAOYSA-N benzyl 5-amino-2-(trifluoromethyl)benzoate Chemical compound NC1=CC=C(C(F)(F)F)C(C(=O)OCC=2C=CC=CC=2)=C1 JGZBXSDRYWNHLN-UHFFFAOYSA-N 0.000 description 4
- BEUDBXJFQHNOCJ-UHFFFAOYSA-N benzyl 5-nitro-2-(trifluoromethyl)benzoate Chemical compound [O-][N+](=O)C1=CC=C(C(F)(F)F)C(C(=O)OCC=2C=CC=CC=2)=C1 BEUDBXJFQHNOCJ-UHFFFAOYSA-N 0.000 description 4
- 239000002775 capsule Substances 0.000 description 4
- 229910052801 chlorine Inorganic materials 0.000 description 4
- 239000012230 colorless oil Substances 0.000 description 4
- 239000003246 corticosteroid Substances 0.000 description 4
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 4
- 230000008034 disappearance Effects 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 239000000839 emulsion Substances 0.000 description 4
- 239000012467 final product Substances 0.000 description 4
- 239000006260 foam Substances 0.000 description 4
- 239000001257 hydrogen Substances 0.000 description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 4
- 239000005457 ice water Substances 0.000 description 4
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 4
- UUUXFKWEIRMJNU-UHFFFAOYSA-N methyl 2-(cyclopropylmethoxy)-4-(methanesulfonamido)benzoate Chemical compound COC(=O)C1=CC=C(NS(C)(=O)=O)C=C1OCC1CC1 UUUXFKWEIRMJNU-UHFFFAOYSA-N 0.000 description 4
- KXPKVSKNKRTCQK-UHFFFAOYSA-N methyl 2-(cyclopropylmethoxy)-4-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound COC(=O)C1=CC=C(N(CCN2CCOCC2)S(C)(=O)=O)C=C1OCC1CC1 KXPKVSKNKRTCQK-UHFFFAOYSA-N 0.000 description 4
- WCZVTNSXTILSGW-UHFFFAOYSA-N methyl 2-(cyclopropylmethoxy)-4-nitrobenzoate Chemical compound COC(=O)C1=CC=C([N+]([O-])=O)C=C1OCC1CC1 WCZVTNSXTILSGW-UHFFFAOYSA-N 0.000 description 4
- QYPDHCHCOWWYES-UHFFFAOYSA-N methyl 2-hydroxy-4-(methanesulfonamido)benzoate Chemical compound COC(=O)C1=CC=C(NS(C)(=O)=O)C=C1O QYPDHCHCOWWYES-UHFFFAOYSA-N 0.000 description 4
- MMNPNHJYJDNHMZ-UHFFFAOYSA-N methyl 2-hydroxy-4-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C1=C(O)C(C(=O)OC)=CC=C1N(S(C)(=O)=O)CCN1CCOCC1 MMNPNHJYJDNHMZ-UHFFFAOYSA-N 0.000 description 4
- ZBEZRRYKGWVIMY-UHFFFAOYSA-N methyl 3-(aminomethyl)-4-(2-morpholin-4-ylethoxy)benzoate Chemical compound NCC1=CC(C(=O)OC)=CC=C1OCCN1CCOCC1 ZBEZRRYKGWVIMY-UHFFFAOYSA-N 0.000 description 4
- ZHCBNAAPOHJATE-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-(ethenylsulfonylamino)benzoate Chemical compound COC(=O)C1=CC=C(NS(=O)(=O)C=C)C(OCC2CC2)=C1 ZHCBNAAPOHJATE-UHFFFAOYSA-N 0.000 description 4
- LAQFAJSUXDSQCD-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-(methanesulfonamidomethyl)benzoate Chemical compound COC(=O)C1=CC=C(CNS(C)(=O)=O)C(OCC2CC2)=C1 LAQFAJSUXDSQCD-UHFFFAOYSA-N 0.000 description 4
- PWRUWUQDFWAZFL-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonylamino]benzoate Chemical compound COC(=O)C1=CC=C(NS(=O)(=O)CCN(C)C)C(OCC2CC2)=C1 PWRUWUQDFWAZFL-UHFFFAOYSA-N 0.000 description 4
- LVJFJXBIPUDCMY-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonyloxy]benzoate Chemical compound COC(=O)C1=CC=C(OS(=O)(=O)CCN(C)C)C(OCC2CC2)=C1 LVJFJXBIPUDCMY-UHFFFAOYSA-N 0.000 description 4
- GTUWALDPIDUBBV-UHFFFAOYSA-N methyl 3-(methanesulfonamido)-4-methoxybenzoate Chemical compound COC(=O)C1=CC=C(OC)C(NS(C)(=O)=O)=C1 GTUWALDPIDUBBV-UHFFFAOYSA-N 0.000 description 4
- YHJOMFXHMFDMIX-UHFFFAOYSA-N methyl 3-(methanesulfonamidomethyl)-4-(2-morpholin-4-ylethoxy)benzoate Chemical compound CS(=O)(=O)NCC1=CC(C(=O)OC)=CC=C1OCCN1CCOCC1 YHJOMFXHMFDMIX-UHFFFAOYSA-N 0.000 description 4
- GQIPMZGSSISOIX-UHFFFAOYSA-N methyl 3-[2-bromoethyl(methylsulfonyl)amino]-4-(trifluoromethyl)benzoate Chemical compound COC(=O)C1=CC=C(C(F)(F)F)C(N(CCBr)S(C)(=O)=O)=C1 GQIPMZGSSISOIX-UHFFFAOYSA-N 0.000 description 4
- WLZWNRDLMBRUJP-UHFFFAOYSA-N methyl 3-[2-hydroxyethyl(methylsulfonyl)amino]-4-(trifluoromethyl)benzoate Chemical compound COC(=O)C1=CC=C(C(F)(F)F)C(N(CCO)S(C)(=O)=O)=C1 WLZWNRDLMBRUJP-UHFFFAOYSA-N 0.000 description 4
- IAGWTVJDNLQGSR-UHFFFAOYSA-N methyl 3-[2-hydroxyethyl(methylsulfonyl)amino]-4-methoxybenzoate Chemical compound COC(=O)C1=CC=C(OC)C(N(CCO)S(C)(=O)=O)=C1 IAGWTVJDNLQGSR-UHFFFAOYSA-N 0.000 description 4
- UPNMSXWOENFYAO-UHFFFAOYSA-N methyl 3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-4-(trifluoromethoxy)benzoate Chemical compound COC(=O)C1=CC=C(OC(F)(F)F)C(N(CCN2CCOCC2)S(C)(=O)=O)=C1 UPNMSXWOENFYAO-UHFFFAOYSA-N 0.000 description 4
- INVMOQROZJDLEJ-UHFFFAOYSA-N methyl 3-amino-4-(trifluoromethoxy)benzoate Chemical compound COC(=O)C1=CC=C(OC(F)(F)F)C(N)=C1 INVMOQROZJDLEJ-UHFFFAOYSA-N 0.000 description 4
- QVDWKLDUBSJEOG-UHFFFAOYSA-N methyl 3-amino-4-methoxybenzoate Chemical compound COC(=O)C1=CC=C(OC)C(N)=C1 QVDWKLDUBSJEOG-UHFFFAOYSA-N 0.000 description 4
- NTJFWIPXFQXYCW-UHFFFAOYSA-N methyl 3-formyl-4-(2-morpholin-4-ylethoxy)benzoate Chemical compound O=CC1=CC(C(=O)OC)=CC=C1OCCN1CCOCC1 NTJFWIPXFQXYCW-UHFFFAOYSA-N 0.000 description 4
- ASEMUOVTGHOBBO-UHFFFAOYSA-N methyl 3-hydroxy-4-(morpholin-4-ylmethyl)benzoate Chemical compound OC1=CC(C(=O)OC)=CC=C1CN1CCOCC1 ASEMUOVTGHOBBO-UHFFFAOYSA-N 0.000 description 4
- LMWHWUCLXWFORF-UHFFFAOYSA-N methyl 3-hydroxy-5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound COC(=O)C1=CC(O)=CC(N(CCN2CCOCC2)S(C)(=O)=O)=C1 LMWHWUCLXWFORF-UHFFFAOYSA-N 0.000 description 4
- VLSGTXHJDGRDKE-UHFFFAOYSA-N methyl 3-methylsulfonyloxy-4-(morpholin-4-ylmethyl)benzoate Chemical compound CS(=O)(=O)OC1=CC(C(=O)OC)=CC=C1CN1CCOCC1 VLSGTXHJDGRDKE-UHFFFAOYSA-N 0.000 description 4
- QDJLEHDFWYPPHD-UHFFFAOYSA-N methyl 4-(aminomethyl)-3-(cyclopropylmethoxy)benzoate Chemical compound COC(=O)C1=CC=C(CN)C(OCC2CC2)=C1 QDJLEHDFWYPPHD-UHFFFAOYSA-N 0.000 description 4
- PUBAASALCFKMJT-UHFFFAOYSA-N methyl 4-(methanesulfonamidomethyl)benzoate Chemical compound COC(=O)C1=CC=C(CNS(C)(=O)=O)C=C1 PUBAASALCFKMJT-UHFFFAOYSA-N 0.000 description 4
- ILCLDQTXEQWPAE-UHFFFAOYSA-N methyl 4-(morpholin-4-ylmethyl)-3-phenylmethoxybenzoate Chemical compound C=1C=CC=CC=1COC1=CC(C(=O)OC)=CC=C1CN1CCOCC1 ILCLDQTXEQWPAE-UHFFFAOYSA-N 0.000 description 4
- LQRZHIVYZGWFGB-UHFFFAOYSA-N methyl 4-amino-3-(cyclopropylmethoxy)benzoate Chemical compound COC(=O)C1=CC=C(N)C(OCC2CC2)=C1 LQRZHIVYZGWFGB-UHFFFAOYSA-N 0.000 description 4
- LGLFHVXTTCMVOQ-UHFFFAOYSA-N methyl 4-fluoro-3-(methanesulfonamido)benzoate Chemical compound COC(=O)C1=CC=C(F)C(NS(C)(=O)=O)=C1 LGLFHVXTTCMVOQ-UHFFFAOYSA-N 0.000 description 4
- VILSIMFYXAMMAW-UHFFFAOYSA-N methyl 4-fluoro-3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound COC(=O)C1=CC=C(F)C(N(CCN2CCOCC2)S(C)(=O)=O)=C1 VILSIMFYXAMMAW-UHFFFAOYSA-N 0.000 description 4
- HGZZYRKDSMPGPO-UHFFFAOYSA-N methyl 4-formyl-3-phenylmethoxybenzoate Chemical compound COC(=O)C1=CC=C(C=O)C(OCC=2C=CC=CC=2)=C1 HGZZYRKDSMPGPO-UHFFFAOYSA-N 0.000 description 4
- NGLZXWWLUPRXNB-UHFFFAOYSA-N methyl 4-methoxy-3-[2-(4-methylpiperazin-1-yl)ethyl-methylsulfonylamino]benzoate Chemical compound COC(=O)C1=CC=C(OC)C(N(CCN2CCN(C)CC2)S(C)(=O)=O)=C1 NGLZXWWLUPRXNB-UHFFFAOYSA-N 0.000 description 4
- JFKUPTRYVDEPDY-UHFFFAOYSA-N methyl 5-(aminomethyl)-2-methoxybenzoate Chemical compound COC(=O)C1=CC(CN)=CC=C1OC JFKUPTRYVDEPDY-UHFFFAOYSA-N 0.000 description 4
- PXKICGMBEHOZDP-UHFFFAOYSA-N methyl 5-(methanesulfonamidomethyl)-2-methoxybenzoate Chemical compound COC(=O)C1=CC(CNS(C)(=O)=O)=CC=C1OC PXKICGMBEHOZDP-UHFFFAOYSA-N 0.000 description 4
- XJKWVPNWHOCFBR-UHFFFAOYSA-N methyl 5-formyl-2-hydroxybenzoate Chemical compound COC(=O)C1=CC(C=O)=CC=C1O XJKWVPNWHOCFBR-UHFFFAOYSA-N 0.000 description 4
- 210000003097 mucus Anatomy 0.000 description 4
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 4
- 125000003386 piperidinyl group Chemical group 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 230000002441 reversible effect Effects 0.000 description 4
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 4
- 235000017557 sodium bicarbonate Nutrition 0.000 description 4
- 239000007858 starting material Substances 0.000 description 4
- 238000001665 trituration Methods 0.000 description 4
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 4
- KBIKNIIKMKRAFK-ZDUSSCGKSA-N 1-o-tert-butyl 2-o-(5-formyl-2-methoxyphenyl) (2s)-pyrrolidine-1,2-dicarboxylate Chemical compound COC1=CC=C(C=O)C=C1OC(=O)[C@H]1N(C(=O)OC(C)(C)C)CCC1 KBIKNIIKMKRAFK-ZDUSSCGKSA-N 0.000 description 3
- BVUFUOPSKSMAHP-WNJJXGMVSA-N 1-o-tert-butyl 2-o-[5-[(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethoxy]carbonyl-2-methoxyphenyl] (2s)-pyrrolidine-1,2-dicarboxylate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OC(=O)[C@@H]1CCCN1C(=O)OC(C)(C)C BVUFUOPSKSMAHP-WNJJXGMVSA-N 0.000 description 3
- JTKNXLCKQCJQKS-VWLOTQADSA-N 2-(cyclopropylmethoxy)-4-[(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethoxy]carbonylbenzoic acid Chemical compound OC(=O)C1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 JTKNXLCKQCJQKS-VWLOTQADSA-N 0.000 description 3
- JTKXVJHQYFFAGM-UHFFFAOYSA-N 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonyl-[(2-methylpropan-2-yl)oxycarbonyl]amino]benzoic acid Chemical compound CN(C)CCS(=O)(=O)N(C(=O)OC(C)(C)C)C1=CC=C(C(O)=O)C=C1OCC1CC1 JTKXVJHQYFFAGM-UHFFFAOYSA-N 0.000 description 3
- ZWMBJPCVBLONPE-UHFFFAOYSA-N 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonyloxy]benzoic acid Chemical compound CN(C)CCS(=O)(=O)OC1=CC=C(C(O)=O)C=C1OCC1CC1 ZWMBJPCVBLONPE-UHFFFAOYSA-N 0.000 description 3
- FPRLJTYFTWLVTB-UHFFFAOYSA-N 3-(cyclopropylmethoxy)-4-phenylmethoxybenzaldehyde Chemical compound C1CC1COC1=CC(C=O)=CC=C1OCC1=CC=CC=C1 FPRLJTYFTWLVTB-UHFFFAOYSA-N 0.000 description 3
- NCJFBEXOHFTWOH-UHFFFAOYSA-N 3-[(2-bromoacetyl)amino]-4-methoxybenzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1NC(=O)CBr NCJFBEXOHFTWOH-UHFFFAOYSA-N 0.000 description 3
- QUUXIMMDHZSOLM-DEOSSOPVSA-N 3-[5-[(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethoxy]carbonyl-2-methoxyanilino]-3-oxopropanoic acid Chemical compound C1=C(NC(=O)CC(O)=O)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl QUUXIMMDHZSOLM-DEOSSOPVSA-N 0.000 description 3
- KTHZZXMXPIMIES-UHFFFAOYSA-N 3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-4-(trifluoromethoxy)benzoic acid;hydrochloride Chemical compound Cl.C=1C(C(O)=O)=CC=C(OC(F)(F)F)C=1N(S(=O)(=O)C)CCN1CCOCC1 KTHZZXMXPIMIES-UHFFFAOYSA-N 0.000 description 3
- VQTODPFBMHRRTP-UHFFFAOYSA-N 3-methylsulfonyloxy-4-phenylmethoxybenzoic acid Chemical compound CS(=O)(=O)OC1=CC(C(O)=O)=CC=C1OCC1=CC=CC=C1 VQTODPFBMHRRTP-UHFFFAOYSA-N 0.000 description 3
- FAEOEDOSHZIZAD-UHFFFAOYSA-N 4-[2-(dimethylamino)ethyl-[(2-methylpropan-2-yl)oxycarbonyl]sulfamoyl]benzoic acid Chemical compound CN(C)CCN(C(=O)OC(C)(C)C)S(=O)(=O)C1=CC=C(C(O)=O)C=C1 FAEOEDOSHZIZAD-UHFFFAOYSA-N 0.000 description 3
- PXCYVRHHRXRMKQ-UHFFFAOYSA-N 4-[2-(dimethylamino)ethylsulfamoyl]benzoic acid Chemical compound CN(C)CCNS(=O)(=O)C1=CC=C(C(O)=O)C=C1 PXCYVRHHRXRMKQ-UHFFFAOYSA-N 0.000 description 3
- XXJUZDYYYONGAR-UHFFFAOYSA-N 4-[2-(dimethylamino)ethylsulfonyl-[(2-methylpropan-2-yl)oxycarbonyl]amino]benzoic acid Chemical compound CN(C)CCS(=O)(=O)N(C(=O)OC(C)(C)C)C1=CC=C(C(O)=O)C=C1 XXJUZDYYYONGAR-UHFFFAOYSA-N 0.000 description 3
- QCQCHGYLTSGIGX-GHXANHINSA-N 4-[[(3ar,5ar,5br,7ar,9s,11ar,11br,13as)-5a,5b,8,8,11a-pentamethyl-3a-[(5-methylpyridine-3-carbonyl)amino]-2-oxo-1-propan-2-yl-4,5,6,7,7a,9,10,11,11b,12,13,13a-dodecahydro-3h-cyclopenta[a]chrysen-9-yl]oxy]-2,2-dimethyl-4-oxobutanoic acid Chemical compound N([C@@]12CC[C@@]3(C)[C@]4(C)CC[C@H]5C(C)(C)[C@@H](OC(=O)CC(C)(C)C(O)=O)CC[C@]5(C)[C@H]4CC[C@@H]3C1=C(C(C2)=O)C(C)C)C(=O)C1=CN=CC(C)=C1 QCQCHGYLTSGIGX-GHXANHINSA-N 0.000 description 3
- ONEWKMDXHNFYRS-UHFFFAOYSA-N 4-methoxy-3-(2-morpholin-4-ylethylsulfamoyl)benzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1S(=O)(=O)NCCN1CCOCC1 ONEWKMDXHNFYRS-UHFFFAOYSA-N 0.000 description 3
- GQTMCPQQCKHXCA-LBPRGKRZSA-N 4-methoxy-3-[(2s)-1-[(2-methylpropan-2-yl)oxycarbonyl]pyrrolidine-2-carbonyl]oxybenzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1OC(=O)[C@H]1N(C(=O)OC(C)(C)C)CCC1 GQTMCPQQCKHXCA-LBPRGKRZSA-N 0.000 description 3
- ANXBDAFDZSXOPQ-UHFFFAOYSA-N 4-methoxy-3-nitrobenzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1[N+]([O-])=O ANXBDAFDZSXOPQ-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- WVDDGKGOMKODPV-UHFFFAOYSA-N Benzyl alcohol Chemical compound OCC1=CC=CC=C1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 3
- OJPJGVKWZUPLEG-UHFFFAOYSA-N C1=CC=C(C=C1)COC2=C(C=C(C=C2)C=O)CS(=O)(=O)O Chemical compound C1=CC=C(C=C1)COC2=C(C=C(C=C2)C=O)CS(=O)(=O)O OJPJGVKWZUPLEG-UHFFFAOYSA-N 0.000 description 3
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical class OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 102000004861 Phosphoric Diester Hydrolases Human genes 0.000 description 3
- 108090001050 Phosphoric Diester Hydrolases Proteins 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- VVBNAGCRKCPBKH-PMERELPUSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(2-hydroxyethoxy)-4-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C=1C=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C(OCCO)C=1N(S(=O)(=O)C)CCN1CCOCC1 VVBNAGCRKCPBKH-PMERELPUSA-N 0.000 description 3
- XEKMIMLXSBSZDC-MHZLTWQESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(cyclopropylmethoxy)-4-formylbenzoate Chemical compound ClC1=C[N+]([O-])=CC(Cl)=C1C[C@@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)OC(=O)C1=CC=C(C=O)C(OCC2CC2)=C1 XEKMIMLXSBSZDC-MHZLTWQESA-N 0.000 description 3
- IZKJAXPYASGJAB-VWLOTQADSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(ethenylsulfonylamino)-4-methoxybenzoate Chemical compound C1=C(NS(=O)(=O)C=C)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl IZKJAXPYASGJAB-VWLOTQADSA-N 0.000 description 3
- XOHXUXUFWWJKLY-DEOSSOPVSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[(2-chloroacetyl)amino]-4-methoxybenzoate Chemical compound C1=C(NC(=O)CCl)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl XOHXUXUFWWJKLY-DEOSSOPVSA-N 0.000 description 3
- FVBHWIOOVMMBCL-BHVANESWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-4-phenylmethoxybenzoate Chemical compound C=1C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C(OCC=2C=CC=CC=2)C=1N(S(=O)(=O)C)CCN1CCOCC1 FVBHWIOOVMMBCL-BHVANESWSA-N 0.000 description 3
- AMLJEWZNRSOLHX-NDEPHWFRSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-methylsulfonyloxy-4-(2-morpholin-4-ylethoxy)benzoate Chemical compound CS(=O)(=O)OC1=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C1OCCN1CCOCC1 AMLJEWZNRSOLHX-NDEPHWFRSA-N 0.000 description 3
- FYGOFUFDRCEPJB-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-methylsulfonyloxy-4-phenylmethoxybenzoate Chemical compound CS(=O)(=O)OC1=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C1OCC1=CC=CC=C1 FYGOFUFDRCEPJB-LJAQVGFWSA-N 0.000 description 3
- VRFJBEHMJNXNAO-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-[2-(dimethylamino)ethyl-[(2-methylpropan-2-yl)oxycarbonyl]sulfamoyl]benzoate Chemical compound C1=CC(S(=O)(=O)N(C(=O)OC(C)(C)C)CCN(C)C)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl VRFJBEHMJNXNAO-LJAQVGFWSA-N 0.000 description 3
- CEOQODDPGDSJPP-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-[2-(dimethylamino)ethylsulfonyl-[(2-methylpropan-2-yl)oxycarbonyl]amino]benzoate Chemical compound C1=CC(N(C(=O)OC(C)(C)C)S(=O)(=O)CCN(C)C)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl CEOQODDPGDSJPP-LJAQVGFWSA-N 0.000 description 3
- GGXWODUFGRVGRR-LJAQVGFWSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-[3-bromopropyl(methylsulfonyl)amino]-3-(cyclopropylmethoxy)benzoate Chemical compound BrCCCN(S(=O)(=O)C)C1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 GGXWODUFGRVGRR-LJAQVGFWSA-N 0.000 description 3
- QULRTJLWNUSSKZ-QHCPKHFHSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-formylbenzoate Chemical compound ClC1=C[N+]([O-])=CC(Cl)=C1C[C@@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)OC(=O)C1=CC=C(C=O)C=C1 QULRTJLWNUSSKZ-QHCPKHFHSA-N 0.000 description 3
- DQIOFLLSYBUZIA-QFIPXVFZSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-hydroxy-3-methylsulfonyloxybenzoate Chemical compound C1=C(O)C(OS(=O)(=O)C)=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=C1 DQIOFLLSYBUZIA-QFIPXVFZSA-N 0.000 description 3
- UBDQEJLXCNLVMA-SANMLTNESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-[(2-methylpropan-2-yl)oxycarbonylamino]benzoate Chemical compound C1=C(NC(=O)OC(C)(C)C)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl UBDQEJLXCNLVMA-SANMLTNESA-N 0.000 description 3
- BJVWTYIKUJSBDV-IZEXYCQBSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-[(2s)-3-methyl-2-[(2-methylpropan-2-yl)oxycarbonylamino]butanoyl]oxybenzoate Chemical compound C1=C(OC(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)C)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl BJVWTYIKUJSBDV-IZEXYCQBSA-N 0.000 description 3
- FQYRVLZSYPHZQT-MHZLTWQESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-[[3-[(2-methylpropan-2-yl)oxy]-3-oxopropanoyl]amino]benzoate Chemical compound C1=C(NC(=O)CC(=O)OC(C)(C)C)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl FQYRVLZSYPHZQT-MHZLTWQESA-N 0.000 description 3
- LGKYEVWZGWLDRJ-QHCPKHFHSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-nitrobenzoate Chemical compound C1=C([N+]([O-])=O)C(OC)=CC=C1C(=O)O[C@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl LGKYEVWZGWLDRJ-QHCPKHFHSA-N 0.000 description 3
- VNASTCRZVSCERF-PMERELPUSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] [4-methoxy-3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]phenyl] carbonate Chemical compound C([C@H](OC(=O)OC1=CC=C(C(=C1)N(CCN1CCOCC1)S(C)(=O)=O)OC)C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)C1=C(Cl)C=[N+]([O-])C=C1Cl VNASTCRZVSCERF-PMERELPUSA-N 0.000 description 3
- BGHLEQFUVRNEEB-PMERELPUSA-N [(1s)-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)-1-(3,4-dimethoxyphenyl)ethyl] 3-(cyclopropylmethoxy)-4-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C1=C(OC)C(OC)=CC=C1[C@@H](OC(=O)C=1C=C(OCC2CC2)C(N(CCN2CCOCC2)S(C)(=O)=O)=CC=1)CC1=C(Cl)C=[N+]([O-])C=C1Cl BGHLEQFUVRNEEB-PMERELPUSA-N 0.000 description 3
- KJGQVQWKOGDQAG-CRYYWNKWSA-N [(1s)-2-(3,5-dichloropyridin-4-yl)-1-(3,4-dimethoxyphenyl)ethyl] (2r)-2-(6-methoxynaphthalen-2-yl)propanoate Chemical compound C([C@H](OC(=O)[C@H](C)C1=CC2=CC=C(C=C2C=C1)OC)C=1C=C(OC)C(OC)=CC=1)C1=C(Cl)C=NC=C1Cl KJGQVQWKOGDQAG-CRYYWNKWSA-N 0.000 description 3
- 125000005237 alkyleneamino group Chemical group 0.000 description 3
- 125000003277 amino group Chemical group 0.000 description 3
- PGUKZRGYIKUFSK-UHFFFAOYSA-N benzyl 4-(ethenylsulfonylamino)benzoate Chemical compound C1=CC(NS(=O)(=O)C=C)=CC=C1C(=O)OCC1=CC=CC=C1 PGUKZRGYIKUFSK-UHFFFAOYSA-N 0.000 description 3
- SQFXNYAYHJCGNL-UHFFFAOYSA-N benzyl 4-[2-(dimethylamino)ethylsulfonyl-[(2-methylpropan-2-yl)oxycarbonyl]amino]benzoate Chemical compound C1=CC(N(C(=O)OC(C)(C)C)S(=O)(=O)CCN(C)C)=CC=C1C(=O)OCC1=CC=CC=C1 SQFXNYAYHJCGNL-UHFFFAOYSA-N 0.000 description 3
- DZDSMEOFNCWCOX-UHFFFAOYSA-N benzyl 4-[2-(dimethylamino)ethylsulfonylamino]benzoate Chemical compound C1=CC(NS(=O)(=O)CCN(C)C)=CC=C1C(=O)OCC1=CC=CC=C1 DZDSMEOFNCWCOX-UHFFFAOYSA-N 0.000 description 3
- DAOPOOMCXJPWPK-UHFFFAOYSA-N benzyl 4-aminobenzoate Chemical compound C1=CC(N)=CC=C1C(=O)OCC1=CC=CC=C1 DAOPOOMCXJPWPK-UHFFFAOYSA-N 0.000 description 3
- XCQFGJYVKKCUFX-UHFFFAOYSA-N benzyl 4-nitrobenzoate Chemical compound C1=CC([N+](=O)[O-])=CC=C1C(=O)OCC1=CC=CC=C1 XCQFGJYVKKCUFX-UHFFFAOYSA-N 0.000 description 3
- 229940124748 beta 2 agonist Drugs 0.000 description 3
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical compound C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- 238000004296 chiral HPLC Methods 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical class OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000000470 constituent Substances 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 229960001334 corticosteroids Drugs 0.000 description 3
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 3
- 239000011737 fluorine Substances 0.000 description 3
- 229910052731 fluorine Inorganic materials 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 125000005842 heteroatom Chemical group 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 3
- 230000001965 increasing effect Effects 0.000 description 3
- 238000001802 infusion Methods 0.000 description 3
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 3
- ATVHLMIJCMVKOS-UHFFFAOYSA-N methyl 2-hydroxy-5-(methanesulfonamido)benzoate Chemical compound COC(=O)C1=CC(NS(C)(=O)=O)=CC=C1O ATVHLMIJCMVKOS-UHFFFAOYSA-N 0.000 description 3
- WQDWSGVSVSTUNJ-OVCLIPMQSA-N methyl 3-(cyclopropylmethoxy)-4-[(e)-methoxyiminomethyl]benzoate Chemical compound CO\N=C\C1=CC=C(C(=O)OC)C=C1OCC1CC1 WQDWSGVSVSTUNJ-OVCLIPMQSA-N 0.000 description 3
- ZMMYFCMFBUYSMJ-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-[2-(dimethylamino)ethylsulfonyl-[(2-methylpropan-2-yl)oxycarbonyl]amino]benzoate Chemical compound COC(=O)C1=CC=C(N(C(=O)OC(C)(C)C)S(=O)(=O)CCN(C)C)C(OCC2CC2)=C1 ZMMYFCMFBUYSMJ-UHFFFAOYSA-N 0.000 description 3
- JDFVSSCQAPWJEQ-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-hydroxybenzoate Chemical compound COC(=O)C1=CC=C(O)C(OCC2CC2)=C1 JDFVSSCQAPWJEQ-UHFFFAOYSA-N 0.000 description 3
- XJAGTAYJYBVTIH-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-nitrobenzoate Chemical compound COC(=O)C1=CC=C([N+]([O-])=O)C(OCC2CC2)=C1 XJAGTAYJYBVTIH-UHFFFAOYSA-N 0.000 description 3
- ZTIGRQULKBJMMA-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-4-phenylmethoxybenzoate Chemical compound C1CC1COC1=CC(C(=O)OC)=CC=C1OCC1=CC=CC=C1 ZTIGRQULKBJMMA-UHFFFAOYSA-N 0.000 description 3
- ZWSMBBMMWQPBEL-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C=1C(N(CCN2CCOCC2)S(C)(=O)=O)=CC(C(=O)OC)=CC=1OCC1CC1 ZWSMBBMMWQPBEL-UHFFFAOYSA-N 0.000 description 3
- DMOYDERCJRMAFM-UHFFFAOYSA-N methyl 3-(methanesulfonamido)-4-phenylmethoxybenzoate Chemical compound CS(=O)(=O)NC1=CC(C(=O)OC)=CC=C1OCC1=CC=CC=C1 DMOYDERCJRMAFM-UHFFFAOYSA-N 0.000 description 3
- RDRJNJPVRMYWDC-UHFFFAOYSA-N methyl 3-[2-(4-methylpiperazin-1-yl)ethyl-methylsulfonylamino]-4-(trifluoromethyl)benzoate Chemical compound COC(=O)C1=CC=C(C(F)(F)F)C(N(CCN2CCN(C)CC2)S(C)(=O)=O)=C1 RDRJNJPVRMYWDC-UHFFFAOYSA-N 0.000 description 3
- QCILDCGFOCXEGP-UHFFFAOYSA-N methyl 3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-4-phenylmethoxybenzoate Chemical compound C1COCCN1CCN(S(C)(=O)=O)C1=CC(C(=O)OC)=CC=C1OCC1=CC=CC=C1 QCILDCGFOCXEGP-UHFFFAOYSA-N 0.000 description 3
- UEGCRFNWTGYVKX-UHFFFAOYSA-N methyl 3-hydroxy-4-nitrobenzoate Chemical compound COC(=O)C1=CC=C([N+]([O-])=O)C(O)=C1 UEGCRFNWTGYVKX-UHFFFAOYSA-N 0.000 description 3
- QDKSJOXKTZEEHQ-UHFFFAOYSA-N methyl 3-nitro-4-(trifluoromethoxy)benzoate Chemical compound COC(=O)C1=CC=C(OC(F)(F)F)C([N+]([O-])=O)=C1 QDKSJOXKTZEEHQ-UHFFFAOYSA-N 0.000 description 3
- UJOZRSAQYNOMTN-UHFFFAOYSA-N methyl 4-[2-(dimethylamino)ethyl-[(2-methylpropan-2-yl)oxycarbonyl]sulfamoyl]benzoate Chemical compound COC(=O)C1=CC=C(S(=O)(=O)N(CCN(C)C)C(=O)OC(C)(C)C)C=C1 UJOZRSAQYNOMTN-UHFFFAOYSA-N 0.000 description 3
- JOXUIZNMFHWBPS-UHFFFAOYSA-N methyl 4-[2-(dimethylamino)ethylsulfamoyl]benzoate Chemical compound COC(=O)C1=CC=C(S(=O)(=O)NCCN(C)C)C=C1 JOXUIZNMFHWBPS-UHFFFAOYSA-N 0.000 description 3
- QTZOGTKFQAMLSE-UHFFFAOYSA-N methyl 4-methoxy-3-(2-morpholin-4-ylethylsulfamoyl)benzoate Chemical compound COC(=O)C1=CC=C(OC)C(S(=O)(=O)NCCN2CCOCC2)=C1 QTZOGTKFQAMLSE-UHFFFAOYSA-N 0.000 description 3
- APQCEGQKJYOCQM-UHFFFAOYSA-N methyl 5-[cyclopropylmethyl(methylsulfonyl)amino]-2-(2-morpholin-4-ylethoxy)benzoate Chemical compound COC(=O)C1=CC(N(CC2CC2)S(C)(=O)=O)=CC=C1OCCN1CCOCC1 APQCEGQKJYOCQM-UHFFFAOYSA-N 0.000 description 3
- VBFBXEHXHSBZPR-UHFFFAOYSA-N methyl 5-[cyclopropylmethyl(methylsulfonyl)amino]-2-hydroxybenzoate Chemical compound C1=C(O)C(C(=O)OC)=CC(N(CC2CC2)S(C)(=O)=O)=C1 VBFBXEHXHSBZPR-UHFFFAOYSA-N 0.000 description 3
- MXUHMQZOATZRIK-UHFFFAOYSA-N methyl 5-amino-2-hydroxybenzoate Chemical compound COC(=O)C1=CC(N)=CC=C1O MXUHMQZOATZRIK-UHFFFAOYSA-N 0.000 description 3
- CNRMXICSYWVJRD-UHFFFAOYSA-N methyl 5-formyl-2-methoxybenzoate Chemical compound COC(=O)C1=CC(C=O)=CC=C1OC CNRMXICSYWVJRD-UHFFFAOYSA-N 0.000 description 3
- 150000007522 mineralic acids Chemical class 0.000 description 3
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 description 3
- 150000007524 organic acids Chemical class 0.000 description 3
- 230000003647 oxidation Effects 0.000 description 3
- 238000007254 oxidation reaction Methods 0.000 description 3
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 3
- 239000003380 propellant Substances 0.000 description 3
- MNDBXUUTURYVHR-UHFFFAOYSA-N roflumilast Chemical compound FC(F)OC1=CC=C(C(=O)NC=2C(=CN=CC=2Cl)Cl)C=C1OCC1CC1 MNDBXUUTURYVHR-UHFFFAOYSA-N 0.000 description 3
- 229960002586 roflumilast Drugs 0.000 description 3
- HJORMJIFDVBMOB-UHFFFAOYSA-N rolipram Chemical compound COC1=CC=C(C2CC(=O)NC2)C=C1OC1CCCC1 HJORMJIFDVBMOB-UHFFFAOYSA-N 0.000 description 3
- 229950005741 rolipram Drugs 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 229910052708 sodium Inorganic materials 0.000 description 3
- 230000009885 systemic effect Effects 0.000 description 3
- PGZCVLUQTJRRAA-DTWKUNHWSA-N tert-butyl (2r,5s)-2,5-dimethylpiperazine-1-carboxylate Chemical compound C[C@H]1CN(C(=O)OC(C)(C)C)[C@H](C)CN1 PGZCVLUQTJRRAA-DTWKUNHWSA-N 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 3
- ZQEBQGAAWMOMAI-ZETCQYMHSA-N (2s)-1-[(2-methylpropan-2-yl)oxycarbonyl]pyrrolidine-2-carboxylic acid Chemical compound CC(C)(C)OC(=O)N1CCC[C@H]1C(O)=O ZQEBQGAAWMOMAI-ZETCQYMHSA-N 0.000 description 2
- 125000006709 (C5-C7) cycloalkenyl group Chemical group 0.000 description 2
- IANQTJSKSUMEQM-UHFFFAOYSA-N 1-benzofuran Chemical compound C1=CC=C2OC=CC2=C1 IANQTJSKSUMEQM-UHFFFAOYSA-N 0.000 description 2
- FCEHBMOGCRZNNI-UHFFFAOYSA-N 1-benzothiophene Chemical compound C1=CC=C2SC=CC2=C1 FCEHBMOGCRZNNI-UHFFFAOYSA-N 0.000 description 2
- GCUOLJOTJRUDIZ-UHFFFAOYSA-N 2-(2-bromoethoxy)oxane Chemical compound BrCCOC1CCCCO1 GCUOLJOTJRUDIZ-UHFFFAOYSA-N 0.000 description 2
- SYZRZLUNWVNNNV-UHFFFAOYSA-N 2-bromoacetyl chloride Chemical compound ClC(=O)CBr SYZRZLUNWVNNNV-UHFFFAOYSA-N 0.000 description 2
- LDLCZOVUSADOIV-UHFFFAOYSA-N 2-bromoethanol Chemical compound OCCBr LDLCZOVUSADOIV-UHFFFAOYSA-N 0.000 description 2
- UZJJZWUXLJFWGO-UHFFFAOYSA-N 3-[2-(4-methylpiperazin-1-yl)ethyl-methylsulfonylamino]-4-(trifluoromethyl)benzoic acid Chemical compound C1CN(C)CCN1CCN(S(C)(=O)=O)C1=CC(C(O)=O)=CC=C1C(F)(F)F UZJJZWUXLJFWGO-UHFFFAOYSA-N 0.000 description 2
- FDGAEAYZQQCBRN-UHFFFAOYSA-N 3-amino-4-methoxybenzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1N FDGAEAYZQQCBRN-UHFFFAOYSA-N 0.000 description 2
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 2
- XLDLRRGZWIEEHT-UHFFFAOYSA-N 3-hydroxy-4-nitrobenzoic acid Chemical compound OC(=O)C1=CC=C([N+]([O-])=O)C(O)=C1 XLDLRRGZWIEEHT-UHFFFAOYSA-N 0.000 description 2
- HUNGEAFDVLSPAM-UHFFFAOYSA-N 3-hydroxy-4-phenylmethoxybenzaldehyde Chemical compound OC1=CC(C=O)=CC=C1OCC1=CC=CC=C1 HUNGEAFDVLSPAM-UHFFFAOYSA-N 0.000 description 2
- FDDHFCWYCKQKGY-UHFFFAOYSA-N 4-formyl-3-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(C=O)C(O)=C1 FDDHFCWYCKQKGY-UHFFFAOYSA-N 0.000 description 2
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 description 2
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 2
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 2
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 2
- 102100021854 Inhibitor of nuclear factor kappa-B kinase subunit beta Human genes 0.000 description 2
- 101710205525 Inhibitor of nuclear factor kappa-B kinase subunit beta Proteins 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 102000043136 MAP kinase family Human genes 0.000 description 2
- 108091054455 MAP kinase family Proteins 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical class CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- KFSLWBXXFJQRDL-UHFFFAOYSA-N Peracetic acid Chemical compound CC(=O)OO KFSLWBXXFJQRDL-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical class OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- KAESVJOAVNADME-UHFFFAOYSA-N Pyrrole Chemical compound C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 206010040070 Septic Shock Diseases 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- 206010047700 Vomiting Diseases 0.000 description 2
- GMUNDEQPAQFWPJ-HBHOUVCGSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(cyclopropylmethoxy)-4-[[4-[(2-methylpropan-2-yl)oxycarbonylamino]cyclohexyl]carbamoyl]benzoate Chemical compound C1CC(NC(=O)OC(C)(C)C)CCC1NC(=O)C1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 GMUNDEQPAQFWPJ-HBHOUVCGSA-N 0.000 description 2
- VZUMBAWPUOYCAB-HKBQPEDESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-acetyloxy-5-[methylsulfonyl(2-morpholin-4-ylethyl)amino]benzoate Chemical compound C([C@H](OC(=O)C=1C=C(C=C(C=1)OC(=O)C)N(CCN1CCOCC1)S(C)(=O)=O)C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)C1=C(Cl)C=[N+]([O-])C=C1Cl VZUMBAWPUOYCAB-HKBQPEDESA-N 0.000 description 2
- XCLYICBAZRPGHS-PMERELPUSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-[[methylsulfonyl(2-morpholin-4-ylethyl)amino]methyl]benzoate Chemical compound C=1C=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=CC=1CN(S(=O)(=O)C)CCN1CCOCC1 XCLYICBAZRPGHS-PMERELPUSA-N 0.000 description 2
- SFYAXIFVXBKRPK-QFIPXVFZSA-N abediterol Chemical compound C([C@H](O)C=1C=2C=CC(=O)NC=2C(O)=CC=1)NCCCCCCOCC(F)(F)C1=CC=CC=C1 SFYAXIFVXBKRPK-QFIPXVFZSA-N 0.000 description 2
- 239000000556 agonist Substances 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 102000015395 alpha 1-Antitrypsin Human genes 0.000 description 2
- 108010050122 alpha 1-Antitrypsin Proteins 0.000 description 2
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 208000010668 atopic eczema Diseases 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 2
- 208000029028 brain injury Diseases 0.000 description 2
- 229940124630 bronchodilator Drugs 0.000 description 2
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 2
- 229910000024 caesium carbonate Inorganic materials 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 125000004186 cyclopropylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C1([H])[H] 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 2
- 150000004683 dihydrates Chemical class 0.000 description 2
- 239000003085 diluting agent Substances 0.000 description 2
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 2
- 239000006196 drop Substances 0.000 description 2
- 239000002532 enzyme inhibitor Substances 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000000796 flavoring agent Substances 0.000 description 2
- XTULMSXFIHGYFS-VLSRWLAYSA-N fluticasone furoate Chemical compound O([C@]1([C@@]2(C)C[C@H](O)[C@]3(F)[C@@]4(C)C=CC(=O)C=C4[C@@H](F)C[C@H]3[C@@H]2C[C@H]1C)C(=O)SCF)C(=O)C1=CC=CO1 XTULMSXFIHGYFS-VLSRWLAYSA-N 0.000 description 2
- 235000013355 food flavoring agent Nutrition 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 229920000159 gelatin Polymers 0.000 description 2
- 235000019322 gelatine Nutrition 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- 102000052502 human ELANE Human genes 0.000 description 2
- XNXVOSBNFZWHBV-UHFFFAOYSA-N hydron;o-methylhydroxylamine;chloride Chemical compound Cl.CON XNXVOSBNFZWHBV-UHFFFAOYSA-N 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 230000002757 inflammatory effect Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 229910052500 inorganic mineral Inorganic materials 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- JVTZFYYHCGSXJV-UHFFFAOYSA-N isovanillin Chemical compound COC1=CC=C(C=O)C=C1O JVTZFYYHCGSXJV-UHFFFAOYSA-N 0.000 description 2
- 150000002576 ketones Chemical class 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 239000003591 leukocyte elastase inhibitor Substances 0.000 description 2
- 150000002617 leukotrienes Chemical class 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 238000004811 liquid chromatography Methods 0.000 description 2
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 2
- 235000010755 mineral Nutrition 0.000 description 2
- 239000011707 mineral Substances 0.000 description 2
- 239000002829 mitogen activated protein kinase inhibitor Substances 0.000 description 2
- 239000012452 mother liquor Substances 0.000 description 2
- 201000006417 multiple sclerosis Diseases 0.000 description 2
- 239000003149 muscarinic antagonist Substances 0.000 description 2
- DILRJUIACXKSQE-UHFFFAOYSA-N n',n'-dimethylethane-1,2-diamine Chemical compound CN(C)CCN DILRJUIACXKSQE-UHFFFAOYSA-N 0.000 description 2
- LNOPIUAQISRISI-UHFFFAOYSA-N n'-hydroxy-2-propan-2-ylsulfonylethanimidamide Chemical compound CC(C)S(=O)(=O)CC(N)=NO LNOPIUAQISRISI-UHFFFAOYSA-N 0.000 description 2
- JERXUPDBWDWFCF-UHFFFAOYSA-N n-(3,5-dichloropyridin-4-yl)-2-[1-[(4-fluorophenyl)methyl]pyrrolo[2,3-b]pyridin-3-yl]-2-oxoacetamide Chemical compound C1=CC(F)=CC=C1CN1C2=NC=CC=C2C(C(=O)C(=O)NC=2C(=CN=CC=2Cl)Cl)=C1 JERXUPDBWDWFCF-UHFFFAOYSA-N 0.000 description 2
- IFYDWYVPVAMGRO-UHFFFAOYSA-N n-[3-(dimethylamino)propyl]tetradecanamide Chemical compound CCCCCCCCCCCCCC(=O)NCCCN(C)C IFYDWYVPVAMGRO-UHFFFAOYSA-N 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- 239000000041 non-steroidal anti-inflammatory agent Substances 0.000 description 2
- 230000010494 opalescence Effects 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 239000006186 oral dosage form Substances 0.000 description 2
- 239000007800 oxidant agent Substances 0.000 description 2
- 210000001711 oxyntic cell Anatomy 0.000 description 2
- 239000006072 paste Substances 0.000 description 2
- 239000003186 pharmaceutical solution Substances 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 125000000587 piperidin-1-yl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 2
- HDOWRFHMPULYOA-UHFFFAOYSA-N piperidin-4-ol Chemical compound OC1CCNCC1 HDOWRFHMPULYOA-UHFFFAOYSA-N 0.000 description 2
- FGIUAXJPYTZDNR-UHFFFAOYSA-N potassium nitrate Chemical compound [K+].[O-][N+]([O-])=O FGIUAXJPYTZDNR-UHFFFAOYSA-N 0.000 description 2
- 239000003755 preservative agent Substances 0.000 description 2
- 229940099982 prolastin Drugs 0.000 description 2
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 2
- 230000010410 reperfusion Effects 0.000 description 2
- 239000012047 saturated solution Substances 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- UKLNMMHNWFDKNT-UHFFFAOYSA-M sodium chlorite Chemical compound [Na+].[O-]Cl=O UKLNMMHNWFDKNT-UHFFFAOYSA-M 0.000 description 2
- 229960002218 sodium chlorite Drugs 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- 238000011200 topical administration Methods 0.000 description 2
- WJUFSDZVCOTFON-UHFFFAOYSA-N veratraldehyde Chemical compound COC1=CC=C(C=O)C=C1OC WJUFSDZVCOTFON-UHFFFAOYSA-N 0.000 description 2
- JWZZKOKVBUJMES-UHFFFAOYSA-N (+-)-Isoprenaline Chemical compound CC(C)NCC(O)C1=CC=C(O)C(O)=C1 JWZZKOKVBUJMES-UHFFFAOYSA-N 0.000 description 1
- XWTYSIMOBUGWOL-UHFFFAOYSA-N (+-)-Terbutaline Chemical compound CC(C)(C)NCC(O)C1=CC(O)=CC(O)=C1 XWTYSIMOBUGWOL-UHFFFAOYSA-N 0.000 description 1
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 1
- CMWTZPSULFXXJA-SECBINFHSA-N (2R)-2-(6-methoxy-2-naphthalenyl)propanoic acid Chemical compound C1=C([C@@H](C)C(O)=O)C=CC2=CC(OC)=CC=C21 CMWTZPSULFXXJA-SECBINFHSA-N 0.000 description 1
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 1
- SZXBQTSZISFIAO-ZETCQYMHSA-N (2s)-3-methyl-2-[(2-methylpropan-2-yl)oxycarbonylamino]butanoic acid Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)OC(C)(C)C SZXBQTSZISFIAO-ZETCQYMHSA-N 0.000 description 1
- UDQTXCHQKHIQMH-KYGLGHNPSA-N (3ar,5s,6s,7r,7ar)-5-(difluoromethyl)-2-(ethylamino)-5,6,7,7a-tetrahydro-3ah-pyrano[3,2-d][1,3]thiazole-6,7-diol Chemical compound S1C(NCC)=N[C@H]2[C@@H]1O[C@H](C(F)F)[C@@H](O)[C@@H]2O UDQTXCHQKHIQMH-KYGLGHNPSA-N 0.000 description 1
- 125000006526 (C1-C2) alkyl group Chemical group 0.000 description 1
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 description 1
- 125000006552 (C3-C8) cycloalkyl group Chemical group 0.000 description 1
- NDAUXUAQIAJITI-LBPRGKRZSA-N (R)-salbutamol Chemical compound CC(C)(C)NC[C@H](O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-LBPRGKRZSA-N 0.000 description 1
- MIOPJNTWMNEORI-GMSGAONNSA-N (S)-camphorsulfonic acid Chemical class C1C[C@@]2(CS(O)(=O)=O)C(=O)C[C@@H]1C2(C)C MIOPJNTWMNEORI-GMSGAONNSA-N 0.000 description 1
- 150000005529 1,3-benzodioxoles Chemical class 0.000 description 1
- VEFLKXRACNJHOV-UHFFFAOYSA-N 1,3-dibromopropane Chemical compound BrCCCBr VEFLKXRACNJHOV-UHFFFAOYSA-N 0.000 description 1
- 125000004214 1-pyrrolidinyl group Chemical group [H]C1([H])N(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- OLFLFCAHZFGBNS-UHFFFAOYSA-N 1664-31-9 Chemical compound C1=CC([N+](=O)[O-])=CC=C1C(=O)NCCN1CCCCC1 OLFLFCAHZFGBNS-UHFFFAOYSA-N 0.000 description 1
- LLZIVCIANZGPFN-UHFFFAOYSA-N 2,2-dimethylpropane-1,3-diamine;hydrochloride Chemical compound Cl.NCC(C)(C)CN LLZIVCIANZGPFN-UHFFFAOYSA-N 0.000 description 1
- MSKVEPYBCUHZMR-UHFFFAOYSA-N 2-[3-[(4-nitrophenyl)methyl]-2,4,5-trioxoimidazolidin-1-yl]acetic acid Chemical compound O=C1C(=O)N(CC(=O)O)C(=O)N1CC1=CC=C([N+]([O-])=O)C=C1 MSKVEPYBCUHZMR-UHFFFAOYSA-N 0.000 description 1
- 125000000022 2-aminoethyl group Chemical group [H]C([*])([H])C([H])([H])N([H])[H] 0.000 description 1
- XFUOEOASGSUIBP-UHFFFAOYSA-N 2-chloro-1-(4-methylpiperazin-1-yl)ethanone;hydron;chloride Chemical compound Cl.CN1CCN(C(=O)CCl)CC1 XFUOEOASGSUIBP-UHFFFAOYSA-N 0.000 description 1
- NWCDDUFGSQYJRM-UHFFFAOYSA-N 2-methyl-4-nitro-1-(trifluoromethyl)benzene Chemical compound CC1=CC([N+]([O-])=O)=CC=C1C(F)(F)F NWCDDUFGSQYJRM-UHFFFAOYSA-N 0.000 description 1
- DBCKRBGYGMVSTI-UHFFFAOYSA-N 2-oxo-7-[2-[2-[3-(2-phenylethoxy)propylsulfonyl]ethylazaniumyl]ethyl]-3h-1,3-benzothiazol-4-olate Chemical compound C1=2SC(=O)NC=2C(O)=CC=C1CCNCCS(=O)(=O)CCCOCCC1=CC=CC=C1 DBCKRBGYGMVSTI-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- CMLFRMDBDNHMRA-UHFFFAOYSA-N 2h-1,2-benzoxazine Chemical compound C1=CC=C2C=CNOC2=C1 CMLFRMDBDNHMRA-UHFFFAOYSA-N 0.000 description 1
- YBHYECGRNFZJPC-UHFFFAOYSA-N 3,5-dichloro-4-methylpyridine Chemical compound CC1=C(Cl)C=NC=C1Cl YBHYECGRNFZJPC-UHFFFAOYSA-N 0.000 description 1
- YNJSNEKCXVFDKW-UHFFFAOYSA-N 3-(5-amino-1h-indol-3-yl)-2-azaniumylpropanoate Chemical compound C1=C(N)C=C2C(CC(N)C(O)=O)=CNC2=C1 YNJSNEKCXVFDKW-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- NGGGZUAEOKRHMA-UHFFFAOYSA-N 3-[(2-methylpropan-2-yl)oxy]-3-oxopropanoic acid Chemical compound CC(C)(C)OC(=O)CC(O)=O NGGGZUAEOKRHMA-UHFFFAOYSA-N 0.000 description 1
- JMWYNUHGKFJVIB-QGFXQWJDSA-N 3-[(3R,9S,12S,15S,18S,24S,30S,33S,36S,39S,42S,45S,48S)-12-(4-aminobutyl)-15-(3-amino-3-oxopropyl)-30-[(2S)-butan-2-yl]-39-[(1R)-1-hydroxyethyl]-33-(hydroxymethyl)-9-[(4-hydroxyphenyl)methyl]-36-methyl-45-octyl-2,8,11,14,17,23,29,32,35,38,41,44,47-tridecaoxo-1,7,10,13,16,22,28,31,34,37,40,43,46-tridecazapentacyclo[46.3.0.03,7.018,22.024,28]henpentacontan-42-yl]propanoic acid Chemical compound C([C@H]1C(=O)N2CCC[C@@H]2C(=O)N2CCC[C@H]2C(=O)N[C@H](C(N[C@@H](CCC(O)=O)C(=O)N[C@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N2CCC[C@H]2C(=O)N2CCC[C@H]2C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N1)[C@@H](C)CC)[C@@H](C)O)=O)CCCCCCCC)C1=CC=C(O)C=C1 JMWYNUHGKFJVIB-QGFXQWJDSA-N 0.000 description 1
- SUTVXKNVAGOKFS-UHFFFAOYSA-N 3-[2-(4-methylpiperazin-1-yl)ethyl-methylsulfonylamino]-4-(trifluoromethyl)benzoic acid;hydrochloride Chemical compound Cl.C1CN(C)CCN1CCN(S(C)(=O)=O)C1=CC(C(O)=O)=CC=C1C(F)(F)F SUTVXKNVAGOKFS-UHFFFAOYSA-N 0.000 description 1
- XFJRBEVDOKKLPS-UHFFFAOYSA-N 3-[methylsulfonyl(2-morpholin-4-ylethyl)amino]-4-(trifluoromethoxy)benzoic acid Chemical compound C=1C(C(O)=O)=CC=C(OC(F)(F)F)C=1N(S(=O)(=O)C)CCN1CCOCC1 XFJRBEVDOKKLPS-UHFFFAOYSA-N 0.000 description 1
- WFSPEVFSRUTRCN-UHFFFAOYSA-N 3-amino-4-fluorobenzoic acid Chemical compound NC1=CC(C(O)=O)=CC=C1F WFSPEVFSRUTRCN-UHFFFAOYSA-N 0.000 description 1
- BIAVGWDGIJKWRM-FQEVSTJZSA-N 3-hydroxy-2-phenyl-n-[(1s)-1-phenylpropyl]quinoline-4-carboxamide Chemical compound N([C@@H](CC)C=1C=CC=CC=1)C(=O)C(C1=CC=CC=C1N=1)=C(O)C=1C1=CC=CC=C1 BIAVGWDGIJKWRM-FQEVSTJZSA-N 0.000 description 1
- RATSANVPHHXDCT-UHFFFAOYSA-N 4-(trifluoromethoxy)benzoic acid Chemical compound OC(=O)C1=CC=C(OC(F)(F)F)C=C1 RATSANVPHHXDCT-UHFFFAOYSA-N 0.000 description 1
- UBMGTTRDNUKZMT-UHFFFAOYSA-N 4-[(1-hydroxy-3h-2,1-benzoxaborol-5-yl)oxy]benzene-1,2-dicarbonitrile Chemical compound C=1C=C2B(O)OCC2=CC=1OC1=CC=C(C#N)C(C#N)=C1 UBMGTTRDNUKZMT-UHFFFAOYSA-N 0.000 description 1
- PTCSSXYPZOFISK-UHFFFAOYSA-N 4-chlorosulfonylbenzoic acid Chemical compound OC(=O)C1=CC=C(S(Cl)(=O)=O)C=C1 PTCSSXYPZOFISK-UHFFFAOYSA-N 0.000 description 1
- HJRQIHYNWZEWHF-UHFFFAOYSA-N 4-methoxy-3-[(2-methylpropan-2-yl)oxycarbonylamino]benzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1NC(=O)OC(C)(C)C HJRQIHYNWZEWHF-UHFFFAOYSA-N 0.000 description 1
- SKDHHIUENRGTHK-UHFFFAOYSA-N 4-nitrobenzoyl chloride Chemical compound [O-][N+](=O)C1=CC=C(C(Cl)=O)C=C1 SKDHHIUENRGTHK-UHFFFAOYSA-N 0.000 description 1
- UKWUOTZGXIZAJC-UHFFFAOYSA-N 4-nitrosalicylic acid Chemical compound OC(=O)C1=CC=C([N+]([O-])=O)C=C1O UKWUOTZGXIZAJC-UHFFFAOYSA-N 0.000 description 1
- LSLYOANBFKQKPT-DIFFPNOSSA-N 5-[(1r)-1-hydroxy-2-[[(2r)-1-(4-hydroxyphenyl)propan-2-yl]amino]ethyl]benzene-1,3-diol Chemical compound C([C@@H](C)NC[C@H](O)C=1C=C(O)C=C(O)C=1)C1=CC=C(O)C=C1 LSLYOANBFKQKPT-DIFFPNOSSA-N 0.000 description 1
- IHOXNOQMRZISPV-YJYMSZOUSA-N 5-[(1r)-1-hydroxy-2-[[(2r)-1-(4-methoxyphenyl)propan-2-yl]azaniumyl]ethyl]-2-oxo-1h-quinolin-8-olate Chemical compound C1=CC(OC)=CC=C1C[C@@H](C)NC[C@H](O)C1=CC=C(O)C2=C1C=CC(=O)N2 IHOXNOQMRZISPV-YJYMSZOUSA-N 0.000 description 1
- UTCFOFWMEPQCSR-UHFFFAOYSA-N 5-formylsalicylic acid Chemical compound OC(=O)C1=CC(C=O)=CC=C1O UTCFOFWMEPQCSR-UHFFFAOYSA-N 0.000 description 1
- IJRKLHTZAIFUTB-UHFFFAOYSA-N 5-nitro-2-(2-phenylethylamino)benzoic acid Chemical compound OC(=O)C1=CC([N+]([O-])=O)=CC=C1NCCC1=CC=CC=C1 IJRKLHTZAIFUTB-UHFFFAOYSA-N 0.000 description 1
- XDBHURGONHZNJF-UHFFFAOYSA-N 6-[2-(3,4-diethoxyphenyl)-1,3-thiazol-4-yl]pyridine-2-carboxylic acid Chemical compound C1=C(OCC)C(OCC)=CC=C1C1=NC(C=2N=C(C=CC=2)C(O)=O)=CS1 XDBHURGONHZNJF-UHFFFAOYSA-N 0.000 description 1
- JFHROPTYMMSOLG-UHFFFAOYSA-N 6-[3-(dimethylcarbamoyl)phenyl]sulfonyl-4-(3-methoxyanilino)-8-methylquinoline-3-carboxamide Chemical compound COC1=CC=CC(NC=2C3=CC(=CC(C)=C3N=CC=2C(N)=O)S(=O)(=O)C=2C=C(C=CC=2)C(=O)N(C)C)=C1 JFHROPTYMMSOLG-UHFFFAOYSA-N 0.000 description 1
- KKYABQBFGDZVNQ-UHFFFAOYSA-N 6-[5-[(cyclopropylamino)-oxomethyl]-3-fluoro-2-methylphenyl]-N-(2,2-dimethylpropyl)-3-pyridinecarboxamide Chemical compound CC1=C(F)C=C(C(=O)NC2CC2)C=C1C1=CC=C(C(=O)NCC(C)(C)C)C=N1 KKYABQBFGDZVNQ-UHFFFAOYSA-N 0.000 description 1
- QNQZWEGMKJBHEM-UHFFFAOYSA-N 6-methyl-5-(2-methylpyrazol-3-yl)-n-[(5-methylsulfonylpyridin-2-yl)methyl]-2-oxo-1-[3-(trifluoromethyl)phenyl]pyridine-3-carboxamide Chemical compound O=C1N(C=2C=C(C=CC=2)C(F)(F)F)C(C)=C(C=2N(N=CC=2)C)C=C1C(=O)NCC1=CC=C(S(C)(=O)=O)C=N1 QNQZWEGMKJBHEM-UHFFFAOYSA-N 0.000 description 1
- HCCNBKFJYUWLEX-UHFFFAOYSA-N 7-(6-methoxypyridin-3-yl)-1-(2-propoxyethyl)-3-(pyrazin-2-ylmethylamino)pyrido[3,4-b]pyrazin-2-one Chemical compound O=C1N(CCOCCC)C2=CC(C=3C=NC(OC)=CC=3)=NC=C2N=C1NCC1=CN=CC=N1 HCCNBKFJYUWLEX-UHFFFAOYSA-N 0.000 description 1
- NJIAKNWTIVDSDA-FQEVSTJZSA-N 7-[4-(1-methylsulfonylpiperidin-4-yl)phenyl]-n-[[(2s)-morpholin-2-yl]methyl]pyrido[3,4-b]pyrazin-5-amine Chemical compound C1CN(S(=O)(=O)C)CCC1C1=CC=C(C=2N=C(NC[C@H]3OCCNC3)C3=NC=CN=C3C=2)C=C1 NJIAKNWTIVDSDA-FQEVSTJZSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- NVOYVOBDTVTBDX-AGUVMIOSSA-N 8g15t83e6i Chemical class C1([C@@H](CO)C(=O)OC2C[C@@H]3[N+]([C@H](C2)[C@@H]2[C@H]3O2)(C)CC)=CC=CC=C1 NVOYVOBDTVTBDX-AGUVMIOSSA-N 0.000 description 1
- HJCMDXDYPOUFDY-WHFBIAKZSA-N Ala-Gln Chemical compound C[C@H](N)C(=O)N[C@H](C(O)=O)CCC(N)=O HJCMDXDYPOUFDY-WHFBIAKZSA-N 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 206010002556 Ankylosing Spondylitis Diseases 0.000 description 1
- 206010051113 Arterial restenosis Diseases 0.000 description 1
- 201000001320 Atherosclerosis Diseases 0.000 description 1
- 206010003694 Atrophy Diseases 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 208000009137 Behcet syndrome Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- 206010006458 Bronchitis chronic Diseases 0.000 description 1
- VOVIALXJUBGFJZ-KWVAZRHASA-N Budesonide Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@@H]2[C@@H]1[C@@H]1C[C@H]3OC(CCC)O[C@@]3(C(=O)CO)[C@@]1(C)C[C@@H]2O VOVIALXJUBGFJZ-KWVAZRHASA-N 0.000 description 1
- IIWFDIRNHIBKKI-UHFFFAOYSA-N C(C)(C)(C)OC(=O)NC1CCC(CC1)NC(=O)C1=C(C=C(C(=O)OC(CC2=[N+](C=C(C=C2Cl)Cl)[O-])C2=CC(=C(C=C2)OC(F)F)OCC2CC2)C=C1)OCC1CC1 Chemical compound C(C)(C)(C)OC(=O)NC1CCC(CC1)NC(=O)C1=C(C=C(C(=O)OC(CC2=[N+](C=C(C=C2Cl)Cl)[O-])C2=CC(=C(C=C2)OC(F)F)OCC2CC2)C=C1)OCC1CC1 IIWFDIRNHIBKKI-UHFFFAOYSA-N 0.000 description 1
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 1
- LERNTVKEWCAPOY-VOGVJGKGSA-N C[N+]1(C)[C@H]2C[C@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)C(O)(c1cccs1)c1cccs1 Chemical compound C[N+]1(C)[C@H]2C[C@H](C[C@@H]1[C@H]1O[C@@H]21)OC(=O)C(O)(c1cccs1)c1cccs1 LERNTVKEWCAPOY-VOGVJGKGSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 1
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 1
- 208000032544 Cicatrix Diseases 0.000 description 1
- IHDDYKNRVLPVEV-FFKPOUSOSA-N Cl.COC1=C(OC)C(OC)=CC(C(=O)N2C[C@](CCN3CCC4(CC3)[S@](CC3=CC=CC=C34)=O)(OCC2)C=2C=C(Cl)C(Cl)=CC=2)=C1 Chemical compound Cl.COC1=C(OC)C(OC)=CC(C(=O)N2C[C@](CCN3CCC4(CC3)[S@](CC3=CC=CC=C34)=O)(OCC2)C=2C=C(Cl)C(Cl)=CC=2)=C1 IHDDYKNRVLPVEV-FFKPOUSOSA-N 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 206010010741 Conjunctivitis Diseases 0.000 description 1
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 206010012442 Dermatitis contact Diseases 0.000 description 1
- ZAFNJMIOTHYJRJ-UHFFFAOYSA-N Diisopropyl ether Chemical compound CC(C)OC(C)C ZAFNJMIOTHYJRJ-UHFFFAOYSA-N 0.000 description 1
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 1
- 208000006926 Discoid Lupus Erythematosus Diseases 0.000 description 1
- 102000002149 Elafin Human genes 0.000 description 1
- 108010015972 Elafin Proteins 0.000 description 1
- 206010014824 Endotoxic shock Diseases 0.000 description 1
- 208000018522 Gastrointestinal disease Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 239000001828 Gelatine Substances 0.000 description 1
- 206010018364 Glomerulonephritis Diseases 0.000 description 1
- 208000023105 Huntington disease Diseases 0.000 description 1
- 206010020649 Hyperkeratosis Diseases 0.000 description 1
- 229940122296 IKK2 inhibitor Drugs 0.000 description 1
- HEFNNWSXXWATRW-UHFFFAOYSA-N Ibuprofen Chemical compound CC(C)CC1=CC=C(C(C)C(O)=O)C=C1 HEFNNWSXXWATRW-UHFFFAOYSA-N 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 1
- 208000001126 Keratosis Diseases 0.000 description 1
- 239000005909 Kieselgur Substances 0.000 description 1
- 239000005411 L01XE02 - Gefitinib Substances 0.000 description 1
- 206010069698 Langerhans' cell histiocytosis Diseases 0.000 description 1
- 229940122696 MAP kinase inhibitor Drugs 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- GMPKIPWJBDOURN-UHFFFAOYSA-N Methoxyamine Chemical compound CON GMPKIPWJBDOURN-UHFFFAOYSA-N 0.000 description 1
- 102100023482 Mitogen-activated protein kinase 14 Human genes 0.000 description 1
- UCHDWCPVSPXUMX-TZIWLTJVSA-N Montelukast Chemical compound CC(C)(O)C1=CC=CC=C1CC[C@H](C=1C=C(\C=C\C=2N=C3C=C(Cl)C=CC3=CC=2)C=CC=1)SCC1(CC(O)=O)CC1 UCHDWCPVSPXUMX-TZIWLTJVSA-N 0.000 description 1
- 206010028813 Nausea Diseases 0.000 description 1
- 208000012902 Nervous system disease Diseases 0.000 description 1
- 208000025966 Neurological disease Diseases 0.000 description 1
- RCPIMTCZGQJSGZ-UHFFFAOYSA-N O1C(=O)C=2C(CC)=CC(OC)=CC=2N=C1C1=CC=CN=C1N1CCC(N(C)C)C1 Chemical compound O1C(=O)C=2C(CC)=CC(OC)=CC=2N=C1C1=CC=CN=C1N1CCC(N(C)C)C1 RCPIMTCZGQJSGZ-UHFFFAOYSA-N 0.000 description 1
- YMHNCPFKPFDJIA-UHFFFAOYSA-N OCCC(C=CC=C1)(C(C=C2OCC3CC3)=CC=C2OC(F)F)N1O Chemical compound OCCC(C=CC=C1)(C(C=C2OCC3CC3)=CC=C2OC(F)F)N1O YMHNCPFKPFDJIA-UHFFFAOYSA-N 0.000 description 1
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 1
- 208000007542 Paresis Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Chemical class OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 102000001253 Protein Kinase Human genes 0.000 description 1
- 208000003251 Pruritus Diseases 0.000 description 1
- 201000004681 Psoriasis Diseases 0.000 description 1
- 206010037549 Purpura Diseases 0.000 description 1
- 241001672981 Purpura Species 0.000 description 1
- 208000006311 Pyoderma Diseases 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 208000018569 Respiratory Tract disease Diseases 0.000 description 1
- 241001303601 Rosacea Species 0.000 description 1
- RUOGJYKOQBFJIG-UHFFFAOYSA-N SCH-351591 Chemical compound C12=CC=C(C(F)(F)F)N=C2C(OC)=CC=C1C(=O)NC1=C(Cl)C=[N+]([O-])C=C1Cl RUOGJYKOQBFJIG-UHFFFAOYSA-N 0.000 description 1
- 206010039793 Seborrhoeic dermatitis Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Chemical class OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 206010042496 Sunburn Diseases 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- YEEZWCHGZNKEEK-UHFFFAOYSA-N Zafirlukast Chemical compound COC1=CC(C(=O)NS(=O)(=O)C=2C(=CC=CC=2)C)=CC=C1CC(C1=C2)=CN(C)C1=CC=C2NC(=O)OC1CCCC1 YEEZWCHGZNKEEK-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- LVEVCWMLRIHHHS-MHZLTWQESA-N [(1S)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-[(1,1-dioxo-1,4-thiazinan-4-yl)methyl]benzoate Chemical compound [O-][n+]1cc(Cl)c(C[C@H](OC(=O)c2ccc(CN3CCS(=O)(=O)CC3)cc2)c2ccc(OC(F)F)c(OCC3CC3)c2)c(Cl)c1 LVEVCWMLRIHHHS-MHZLTWQESA-N 0.000 description 1
- VCFBPAOSTLMYIV-SANMLTNESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-(cyclopropylmethoxy)-4-(methanesulfonamido)benzoate Chemical compound CS(=O)(=O)NC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1OCC1CC1 VCFBPAOSTLMYIV-SANMLTNESA-N 0.000 description 1
- MCZJBWORIYBPRR-PMERELPUSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 3-[2-(4-methylpiperazin-1-yl)ethyl-methylsulfonylamino]-4-(trifluoromethyl)benzoate Chemical compound C1CN(C)CCN1CCN(S(C)(=O)=O)C1=CC(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)=CC=C1C(F)(F)F MCZJBWORIYBPRR-PMERELPUSA-N 0.000 description 1
- BGMMPTPNASYCCJ-MHZLTWQESA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-(cyclopropylmethoxy)-3-formylbenzoate Chemical compound ClC1=C[N+]([O-])=CC(Cl)=C1C[C@@H](C=1C=C(OCC2CC2)C(OC(F)F)=CC=1)OC(=O)C(C=C1C=O)=CC=C1OCC1CC1 BGMMPTPNASYCCJ-MHZLTWQESA-N 0.000 description 1
- NCZQYIWCDVMDIN-PMERELPUSA-N [(1s)-1-[3-(cyclopropylmethoxy)-4-(difluoromethoxy)phenyl]-2-(3,5-dichloro-1-oxidopyridin-1-ium-4-yl)ethyl] 4-methoxy-3-[2-(4-methylpiperazin-1-yl)ethylsulfonylamino]benzoate Chemical compound COC1=CC=C(C(=O)O[C@@H](CC=2C(=C[N+]([O-])=CC=2Cl)Cl)C=2C=C(OCC3CC3)C(OC(F)F)=CC=2)C=C1NS(=O)(=O)CCN1CCN(C)CC1 NCZQYIWCDVMDIN-PMERELPUSA-N 0.000 description 1
- ANGKOCUUWGHLCE-HKUYNNGSSA-N [(3s)-1,1-dimethylpyrrolidin-1-ium-3-yl] (2r)-2-cyclopentyl-2-hydroxy-2-phenylacetate Chemical compound C1[N+](C)(C)CC[C@@H]1OC(=O)[C@](O)(C=1C=CC=CC=1)C1CCCC1 ANGKOCUUWGHLCE-HKUYNNGSSA-N 0.000 description 1
- YPFLFUJKZDAXRA-UHFFFAOYSA-N [3-(carbamoylamino)-2-(2,4-dichlorobenzoyl)-1-benzofuran-6-yl] methanesulfonate Chemical compound O1C2=CC(OS(=O)(=O)C)=CC=C2C(NC(N)=O)=C1C(=O)C1=CC=C(Cl)C=C1Cl YPFLFUJKZDAXRA-UHFFFAOYSA-N 0.000 description 1
- 229950000192 abediterol Drugs 0.000 description 1
- TVWAEQRFKRTYIG-JIDHJSLPSA-N acetic acid;4-[(1r)-2-[6-[2-[(2,6-dichlorophenyl)methoxy]ethoxy]hexylamino]-1-hydroxyethyl]-2-(hydroxymethyl)phenol Chemical compound CC(O)=O.C1=C(O)C(CO)=CC([C@@H](O)CNCCCCCCOCCOCC=2C(=CC=CC=2Cl)Cl)=C1 TVWAEQRFKRTYIG-JIDHJSLPSA-N 0.000 description 1
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 description 1
- 239000012346 acetyl chloride Substances 0.000 description 1
- ASMXXROZKSBQIH-VITNCHFBSA-N aclidinium Chemical compound C([C@@H](C(CC1)CC2)OC(=O)C(O)(C=3SC=CC=3)C=3SC=CC=3)[N+]21CCCOC1=CC=CC=C1 ASMXXROZKSBQIH-VITNCHFBSA-N 0.000 description 1
- 229940019903 aclidinium Drugs 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 239000003513 alkali Substances 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 229910001420 alkaline earth metal ion Inorganic materials 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 208000002205 allergic conjunctivitis Diseases 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 208000004631 alopecia areata Diseases 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- VZTDIZULWFCMLS-UHFFFAOYSA-N ammonium formate Chemical compound [NH4+].[O-]C=O VZTDIZULWFCMLS-UHFFFAOYSA-N 0.000 description 1
- 230000002052 anaphylactic effect Effects 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 229940065524 anticholinergics inhalants for obstructive airway diseases Drugs 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- IMOZEMNVLZVGJZ-QGZVFWFLSA-N apremilast Chemical compound C1=C(OC)C(OCC)=CC([C@@H](CS(C)(=O)=O)N2C(C3=C(NC(C)=O)C=CC=C3C2=O)=O)=C1 IMOZEMNVLZVGJZ-QGZVFWFLSA-N 0.000 description 1
- 229960001164 apremilast Drugs 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 208000024998 atopic conjunctivitis Diseases 0.000 description 1
- 230000037444 atrophy Effects 0.000 description 1
- 125000002393 azetidinyl group Chemical group 0.000 description 1
- 229960003060 bambuterol Drugs 0.000 description 1
- ANZXOIAKUNOVQU-UHFFFAOYSA-N bambuterol Chemical compound CN(C)C(=O)OC1=CC(OC(=O)N(C)C)=CC(C(O)CNC(C)(C)C)=C1 ANZXOIAKUNOVQU-UHFFFAOYSA-N 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- QDWCLHABHDGMFY-UHFFFAOYSA-N benzyl 3-amino-4-fluorobenzoate Chemical compound C1=C(F)C(N)=CC(C(=O)OCC=2C=CC=CC=2)=C1 QDWCLHABHDGMFY-UHFFFAOYSA-N 0.000 description 1
- 235000019445 benzyl alcohol Nutrition 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 1
- 230000006931 brain damage Effects 0.000 description 1
- 231100000874 brain damage Toxicity 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- LKXYJYDRLBPHRS-UHFFFAOYSA-N bromocyclopropane Chemical compound BrC1CC1 LKXYJYDRLBPHRS-UHFFFAOYSA-N 0.000 description 1
- 206010006451 bronchitis Diseases 0.000 description 1
- 229960004436 budesonide Drugs 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical class O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 238000013262 cAMP assay Methods 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000007894 caplet Substances 0.000 description 1
- 235000011089 carbon dioxide Nutrition 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 1
- 229950010713 carmoterol Drugs 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- CFBUZOUXXHZCFB-OYOVHJISSA-N chembl511115 Chemical compound COC1=CC=C([C@@]2(CC[C@H](CC2)C(O)=O)C#N)C=C1OC1CCCC1 CFBUZOUXXHZCFB-OYOVHJISSA-N 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 239000000812 cholinergic antagonist Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 208000007451 chronic bronchitis Diseases 0.000 description 1
- 229950001653 cilomilast Drugs 0.000 description 1
- 229960001117 clenbuterol Drugs 0.000 description 1
- STJMRWALKKWQGH-UHFFFAOYSA-N clenbuterol Chemical compound CC(C)(C)NCC(O)C1=CC(Cl)=C(N)C(Cl)=C1 STJMRWALKKWQGH-UHFFFAOYSA-N 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940126543 compound 14 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940125807 compound 37 Drugs 0.000 description 1
- 229940125936 compound 42 Drugs 0.000 description 1
- 229940126545 compound 53 Drugs 0.000 description 1
- 238000002591 computed tomography Methods 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 208000010247 contact dermatitis Diseases 0.000 description 1
- 239000006184 cosolvent Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 239000007822 coupling agent Substances 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- USZAGAREISWJDP-UHFFFAOYSA-N crisaborole Chemical compound C=1C=C2B(O)OCC2=CC=1OC1=CC=C(C#N)C=C1 USZAGAREISWJDP-UHFFFAOYSA-N 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 208000004921 cutaneous lupus erythematosus Diseases 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000392 cycloalkenyl group Chemical group 0.000 description 1
- 125000006254 cycloalkyl carbonyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 238000004807 desolvation Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- MDCUNMLZLNGCQA-HWOAGHQOSA-N elafin Chemical compound N([C@H](C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N1CCC[C@H]1C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N[C@@H](CCCCN)C(=O)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H]1C(=O)N2CCC[C@H]2C(=O)N[C@H](C(=O)N[C@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H]2CSSC[C@H]3C(=O)NCC(=O)N[C@@H](CCSC)C(=O)N[C@@H](C)C(=O)N[C@@H](CSSC[C@H]4C(=O)N5CCC[C@H]5C(=O)NCC(=O)N[C@H](C(N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H]5N(CCC5)C(=O)[C@H]5N(CCC5)C(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCSC)NC(=O)[C@H](C)NC2=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(=O)N4)C(=O)N[C@@H](CSSC1)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N3)=O)[C@@H](C)CC)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(N)=O)C(O)=O)[C@@H](C)CC)[C@@H](C)CC)[C@@H](C)CC)[C@@H](C)O)C(C)C)C(C)C)C(=O)[C@@H]1CCCN1C(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)N MDCUNMLZLNGCQA-HWOAGHQOSA-N 0.000 description 1
- 238000000132 electrospray ionisation Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 230000001804 emulsifying effect Effects 0.000 description 1
- CSOBIBXVIYAXFM-BYNJWEBRSA-N ensifentrine Chemical compound c-12cc(OC)c(OC)cc2CCn(c(n2CCNC(N)=O)=O)c-1c\c2=N/c1c(C)cc(C)cc1C CSOBIBXVIYAXFM-BYNJWEBRSA-N 0.000 description 1
- 208000003401 eosinophilic granuloma Diseases 0.000 description 1
- 125000004185 ester group Chemical group 0.000 description 1
- 125000005745 ethoxymethyl group Chemical group [H]C([H])([H])C([H])([H])OC([H])([H])* 0.000 description 1
- VFRSADQPWYCXDG-LEUCUCNGSA-N ethyl (2s,5s)-5-methylpyrrolidine-2-carboxylate;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.CCOC(=O)[C@@H]1CC[C@H](C)N1 VFRSADQPWYCXDG-LEUCUCNGSA-N 0.000 description 1
- FHFPUTPROUXAAC-UHFFFAOYSA-N ethyl 3-nitro-4-(trifluoromethoxy)benzoate Chemical compound CCOC(=O)C1=CC=C(OC(F)(F)F)C([N+]([O-])=O)=C1 FHFPUTPROUXAAC-UHFFFAOYSA-N 0.000 description 1
- 229960001022 fenoterol Drugs 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 229960001469 fluticasone furoate Drugs 0.000 description 1
- WMWTYOKRWGGJOA-CENSZEJFSA-N fluticasone propionate Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(OC(=O)CC)[C@@]2(C)C[C@@H]1O WMWTYOKRWGGJOA-CENSZEJFSA-N 0.000 description 1
- 229960000289 fluticasone propionate Drugs 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 229960002848 formoterol Drugs 0.000 description 1
- BPZSYCZIITTYBL-UHFFFAOYSA-N formoterol Chemical compound C1=CC(OC)=CC=C1CC(C)NCC(O)C1=CC=C(O)C(NC=O)=C1 BPZSYCZIITTYBL-UHFFFAOYSA-N 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 210000004051 gastric juice Anatomy 0.000 description 1
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 description 1
- 229960002584 gefitinib Drugs 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 229960002462 glycopyrronium bromide Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 125000006588 heterocycloalkylene group Chemical group 0.000 description 1
- 150000005828 hydrofluoroalkanes Chemical class 0.000 description 1
- 230000001969 hypertrophic effect Effects 0.000 description 1
- 229960001680 ibuprofen Drugs 0.000 description 1
- 125000002632 imidazolidinyl group Chemical group 0.000 description 1
- 210000002865 immune cell Anatomy 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 229960004078 indacaterol Drugs 0.000 description 1
- QZZUEBNBZAPZLX-QFIPXVFZSA-N indacaterol Chemical compound N1C(=O)C=CC2=C1C(O)=CC=C2[C@@H](O)CNC1CC(C=C(C(=C2)CC)CC)=C2C1 QZZUEBNBZAPZLX-QFIPXVFZSA-N 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 1
- 239000003701 inert diluent Substances 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229940125369 inhaled corticosteroids Drugs 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- OEXHQOGQTVQTAT-JRNQLAHRSA-N ipratropium Chemical compound O([C@H]1C[C@H]2CC[C@@H](C1)[N@@+]2(C)C(C)C)C(=O)C(CO)C1=CC=CC=C1 OEXHQOGQTVQTAT-JRNQLAHRSA-N 0.000 description 1
- 229960001888 ipratropium Drugs 0.000 description 1
- 229940039009 isoproterenol Drugs 0.000 description 1
- ZLTPDFXIESTBQG-UHFFFAOYSA-N isothiazole Chemical compound C=1C=NSC=1 ZLTPDFXIESTBQG-UHFFFAOYSA-N 0.000 description 1
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 1
- 230000007803 itching Effects 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- DKYWVDODHFEZIM-UHFFFAOYSA-N ketoprofen Chemical compound OC(=O)C(C)C1=CC=CC(C(=O)C=2C=CC=CC=2)=C1 DKYWVDODHFEZIM-UHFFFAOYSA-N 0.000 description 1
- 229960000991 ketoprofen Drugs 0.000 description 1
- 229940043355 kinase inhibitor Drugs 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 229950008204 levosalbutamol Drugs 0.000 description 1
- 201000011486 lichen planus Diseases 0.000 description 1
- 239000000865 liniment Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229950003265 losmapimod Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 239000006166 lysate Substances 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical class OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Chemical class 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- KBOPZPXVLCULAV-UHFFFAOYSA-N mesalamine Chemical compound NC1=CC=C(O)C(C(O)=O)=C1 KBOPZPXVLCULAV-UHFFFAOYSA-N 0.000 description 1
- 229960004963 mesalazine Drugs 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- BMAMQYNHUPUMSD-UHFFFAOYSA-N methyl 3-(cyclopropylmethoxy)-5-(methanesulfonamido)benzoate Chemical compound COC(=O)C1=CC(NS(C)(=O)=O)=CC(OCC2CC2)=C1 BMAMQYNHUPUMSD-UHFFFAOYSA-N 0.000 description 1
- NYRVKNIUXMLMTE-UHFFFAOYSA-N methyl 3-[bis(methylsulfonyl)amino]-4-(trifluoromethyl)benzoate Chemical compound COC(=O)C1=CC=C(C(F)(F)F)C(N(S(C)(=O)=O)S(C)(=O)=O)=C1 NYRVKNIUXMLMTE-UHFFFAOYSA-N 0.000 description 1
- CXRFEVOHNGTEOG-UHFFFAOYSA-N methyl 3-amino-4-phenylmethoxybenzoate Chemical compound NC1=CC(C(=O)OC)=CC=C1OCC1=CC=CC=C1 CXRFEVOHNGTEOG-UHFFFAOYSA-N 0.000 description 1
- ADSJCWKOKYOJSZ-UHFFFAOYSA-N methyl 3-formyl-4-hydroxybenzoate Chemical compound COC(=O)C1=CC=C(O)C(C=O)=C1 ADSJCWKOKYOJSZ-UHFFFAOYSA-N 0.000 description 1
- GIZCKBSSWNIUMZ-UHFFFAOYSA-N methyl 4-(aminomethyl)benzoate;hydrochloride Chemical compound Cl.COC(=O)C1=CC=C(CN)C=C1 GIZCKBSSWNIUMZ-UHFFFAOYSA-N 0.000 description 1
- GRVDJDISBSALJP-UHFFFAOYSA-N methyloxidanyl Chemical group [O]C GRVDJDISBSALJP-UHFFFAOYSA-N 0.000 description 1
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 description 1
- 229950001768 milveterol Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- WOFMFGQZHJDGCX-ZULDAHANSA-N mometasone furoate Chemical compound O([C@]1([C@@]2(C)C[C@H](O)[C@]3(Cl)[C@@]4(C)C=CC(=O)C=C4CC[C@H]3[C@@H]2C[C@H]1C)C(=O)CCl)C(=O)C1=CC=CO1 WOFMFGQZHJDGCX-ZULDAHANSA-N 0.000 description 1
- 229960002744 mometasone furoate Drugs 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 229960005127 montelukast Drugs 0.000 description 1
- PWDYHMBTPGXCSN-VCBMUGGBSA-N n,n'-bis[3,5-bis[(e)-n-(diaminomethylideneamino)-c-methylcarbonimidoyl]phenyl]decanediamide Chemical compound NC(N)=N/N=C(\C)C1=CC(C(=N/N=C(N)N)/C)=CC(NC(=O)CCCCCCCCC(=O)NC=2C=C(C=C(C=2)C(\C)=N\N=C(N)N)C(\C)=N\N=C(N)N)=C1 PWDYHMBTPGXCSN-VCBMUGGBSA-N 0.000 description 1
- DPHDSIQHVGSITN-UHFFFAOYSA-N n-(3,5-dichloropyridin-4-yl)-2-[1-[(4-fluorophenyl)methyl]-5-hydroxyindol-3-yl]-2-oxoacetamide Chemical compound C1=C(C(=O)C(=O)NC=2C(=CN=CC=2Cl)Cl)C2=CC(O)=CC=C2N1CC1=CC=C(F)C=C1 DPHDSIQHVGSITN-UHFFFAOYSA-N 0.000 description 1
- OKFDRAHPFKMAJH-UHFFFAOYSA-N n-(3,5-dichloropyridin-4-yl)-4-(difluoromethoxy)-8-(methanesulfonamido)dibenzofuran-1-carboxamide Chemical compound C=12C3=CC(NS(=O)(=O)C)=CC=C3OC2=C(OC(F)F)C=CC=1C(=O)NC1=C(Cl)C=NC=C1Cl OKFDRAHPFKMAJH-UHFFFAOYSA-N 0.000 description 1
- BHCJHYIMNHXLOM-WVDRJWPYSA-N n-[(e,2r)-1-(3,4-dichlorophenyl)-5-oxo-5-[[(3r)-2-oxoazepan-3-yl]amino]pent-3-en-2-yl]-n-methyl-3,5-bis(trifluoromethyl)benzamide Chemical compound C([C@@H](N(C)C(=O)C=1C=C(C=C(C=1)C(F)(F)F)C(F)(F)F)\C=C\C(=O)N[C@H]1C(NCCCC1)=O)C1=CC=C(Cl)C(Cl)=C1 BHCJHYIMNHXLOM-WVDRJWPYSA-N 0.000 description 1
- ZVULMJYRVAVKCP-UHFFFAOYSA-N n-[2-(diethylamino)ethyl]-n-[2-[2-(4-hydroxy-2-oxo-3h-1,3-benzothiazol-7-yl)ethylamino]ethyl]-3-(2-naphthalen-1-ylethoxy)propanamide Chemical compound C1=CC=C2C(CCOCCC(=O)N(CCNCCC=3C=4SC(=O)NC=4C(O)=CC=3)CCN(CC)CC)=CC=CC2=C1 ZVULMJYRVAVKCP-UHFFFAOYSA-N 0.000 description 1
- BMKINZUHKYLSKI-DQEYMECFSA-N n-[2-hydroxy-5-[(1r)-1-hydroxy-2-[2-[4-[[(2r)-2-hydroxy-2-phenylethyl]amino]phenyl]ethylamino]ethyl]phenyl]formamide Chemical compound C1([C@@H](O)CNC2=CC=C(C=C2)CCNC[C@H](O)C=2C=C(NC=O)C(O)=CC=2)=CC=CC=C1 BMKINZUHKYLSKI-DQEYMECFSA-N 0.000 description 1
- DRMJRHUMYBYDIX-UHFFFAOYSA-N n-[4-[5-(4-fluorophenyl)-3-methyl-2-methylsulfinylimidazol-4-yl]pyridin-2-yl]acetamide Chemical compound C1=NC(NC(=O)C)=CC(C=2N(C(=NC=2C=2C=CC(F)=CC=2)S(C)=O)C)=C1 DRMJRHUMYBYDIX-UHFFFAOYSA-N 0.000 description 1
- RWIVICVCHVMHMU-UHFFFAOYSA-N n-aminoethylmorpholine Chemical compound NCCN1CCOCC1 RWIVICVCHVMHMU-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000008693 nausea Effects 0.000 description 1
- 201000008383 nephritis Diseases 0.000 description 1
- 230000000926 neurological effect Effects 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- 229950000175 oglemilast Drugs 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 229960004286 olodaterol Drugs 0.000 description 1
- COUYJEVMBVSIHV-SFHVURJKSA-N olodaterol Chemical compound C1=CC(OC)=CC=C1CC(C)(C)NC[C@H](O)C1=CC(O)=CC2=C1OCC(=O)N2 COUYJEVMBVSIHV-SFHVURJKSA-N 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 108010068338 p38 Mitogen-Activated Protein Kinases Proteins 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000005191 phase separation Methods 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 1
- 125000004482 piperidin-4-yl group Chemical group N1CCC(CC1)* 0.000 description 1
- ISWRGOKTTBVCFA-UHFFFAOYSA-N pirfenidone Chemical compound C1=C(C)C=CC(=O)N1C1=CC=CC=C1 ISWRGOKTTBVCFA-UHFFFAOYSA-N 0.000 description 1
- 229960003073 pirfenidone Drugs 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 235000010333 potassium nitrate Nutrition 0.000 description 1
- 239000004323 potassium nitrate Substances 0.000 description 1
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 1
- 229960004583 pranlukast Drugs 0.000 description 1
- UAJUXJSXCLUTNU-UHFFFAOYSA-N pranlukast Chemical compound C=1C=C(OCCCCC=2C=CC=CC=2)C=CC=1C(=O)NC(C=1)=CC=C(C(C=2)=O)C=1OC=2C=1N=NNN=1 UAJUXJSXCLUTNU-UHFFFAOYSA-N 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 108060006633 protein kinase Proteins 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 208000020016 psychiatric disease Diseases 0.000 description 1
- CPNGPNLZQNNVQM-UHFFFAOYSA-N pteridine Chemical compound N1=CN=CC2=NC=CN=C21 CPNGPNLZQNNVQM-UHFFFAOYSA-N 0.000 description 1
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 229960002720 reproterol Drugs 0.000 description 1
- WVLAAKXASPCBGT-UHFFFAOYSA-N reproterol Chemical compound C1=2C(=O)N(C)C(=O)N(C)C=2N=CN1CCCNCC(O)C1=CC(O)=CC(O)=C1 WVLAAKXASPCBGT-UHFFFAOYSA-N 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 201000004700 rosacea Diseases 0.000 description 1
- 229960002052 salbutamol Drugs 0.000 description 1
- 150000003873 salicylate salts Chemical class 0.000 description 1
- 231100000241 scar Toxicity 0.000 description 1
- 230000037387 scars Effects 0.000 description 1
- 201000000980 schizophrenia Diseases 0.000 description 1
- 208000008742 seborrheic dermatitis Diseases 0.000 description 1
- 229950011005 semapimod Drugs 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000036303 septic shock Effects 0.000 description 1
- 229950005229 sibenadet Drugs 0.000 description 1
- 238000007086 side reaction Methods 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 239000002594 sorbent Substances 0.000 description 1
- 208000020431 spinal cord injury Diseases 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008174 sterile solution Substances 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 230000006103 sulfonylation Effects 0.000 description 1
- 238000005694 sulfonylation reaction Methods 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000012134 supernatant fraction Substances 0.000 description 1
- 230000003319 supportive effect Effects 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 238000001308 synthesis method Methods 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 229950011332 talnetant Drugs 0.000 description 1
- 229960000195 terbutaline Drugs 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 229950002896 tetomilast Drugs 0.000 description 1
- PASYJVRFGUDDEW-WMUGRWSXSA-J tetrasodium;[[(2r,3s,5r)-5-(4-amino-2-oxopyrimidin-1-yl)-3-hydroxyoxolan-2-yl]methoxy-oxidophosphoryl] [[[(2r,3s,4r,5r)-5-(2,4-dioxopyrimidin-1-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-oxidophosphoryl]oxy-oxidophosphoryl] phosphate Chemical compound [Na+].[Na+].[Na+].[Na+].O=C1N=C(N)C=CN1[C@@H]1O[C@H](COP([O-])(=O)OP([O-])(=O)OP([O-])(=O)OP([O-])(=O)OC[C@@H]2[C@H]([C@@H](O)[C@@H](O2)N2C(NC(=O)C=C2)=O)O)[C@@H](O)C1 PASYJVRFGUDDEW-WMUGRWSXSA-J 0.000 description 1
- WROMPOXWARCANT-UHFFFAOYSA-N tfa trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC(=O)C(F)(F)F WROMPOXWARCANT-UHFFFAOYSA-N 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 231100001274 therapeutic index Toxicity 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 125000001984 thiazolidinyl group Chemical group 0.000 description 1
- 125000004568 thiomorpholinyl group Chemical group 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- GZNAASVAJNXPPW-UHFFFAOYSA-M tin(4+) chloride dihydrate Chemical compound O.O.[Cl-].[Sn+4] GZNAASVAJNXPPW-UHFFFAOYSA-M 0.000 description 1
- FWPIDFUJEMBDLS-UHFFFAOYSA-L tin(II) chloride dihydrate Substances O.O.Cl[Sn]Cl FWPIDFUJEMBDLS-UHFFFAOYSA-L 0.000 description 1
- LERNTVKEWCAPOY-DZZGSBJMSA-N tiotropium Chemical compound O([C@H]1C[C@@H]2[N+]([C@H](C1)[C@@H]1[C@H]2O1)(C)C)C(=O)C(O)(C=1SC=CC=1)C1=CC=CS1 LERNTVKEWCAPOY-DZZGSBJMSA-N 0.000 description 1
- 229940110309 tiotropium Drugs 0.000 description 1
- 229960000257 tiotropium bromide Drugs 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 231100000583 toxicological profile Toxicity 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Chemical class OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- OYYDSUSKLWTMMQ-JKHIJQBDSA-N trospium Chemical compound [N+]12([C@@H]3CC[C@H]2C[C@H](C3)OC(=O)C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CCCC1 OYYDSUSKLWTMMQ-JKHIJQBDSA-N 0.000 description 1
- 229960001491 trospium Drugs 0.000 description 1
- 238000000825 ultraviolet detection Methods 0.000 description 1
- 229960004026 vilanterol Drugs 0.000 description 1
- 230000008673 vomiting Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 229960004764 zafirlukast Drugs 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D295/00—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms
- C07D295/04—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms
- C07D295/14—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
- C07D295/155—Heterocyclic compounds containing polymethylene-imine rings with at least five ring members, 3-azabicyclo [3.2.2] nonane, piperazine, morpholine or thiomorpholine rings, having only hydrogen atoms directly attached to the ring carbon atoms with substituted hydrocarbon radicals attached to ring nitrogen atoms substituted by carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals with the ring nitrogen atoms and the carbon atoms with three bonds to hetero atoms separated by carbocyclic rings or by carbon chains interrupted by carbocyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/89—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members with hetero atoms directly attached to the ring nitrogen atom
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene or sparfloxacin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/0065—Inhalators with dosage or measuring devices
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M15/00—Inhalators
- A61M15/009—Inhalators using medicine packages with incorporated spraying means, e.g. aerosol cans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61M—DEVICES FOR INTRODUCING MEDIA INTO, OR ONTO, THE BODY; DEVICES FOR TRANSDUCING BODY MEDIA OR FOR TAKING MEDIA FROM THE BODY; DEVICES FOR PRODUCING OR ENDING SLEEP OR STUPOR
- A61M16/00—Devices for influencing the respiratory system of patients by gas treatment, e.g. mouth-to-mouth respiration; Tracheal tubes
- A61M16/10—Preparation of respiratory gases or vapours
- A61M16/14—Preparation of respiratory gases or vapours by mixing different fluids, one of them being in a liquid phase
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D213/00—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members
- C07D213/02—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members
- C07D213/04—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D213/60—Heterocyclic compounds containing six-membered rings, not condensed with other rings, with one nitrogen atom as the only ring hetero atom and three or more double bonds between ring members or between ring members and non-ring members having three double bonds between ring members or between ring members and non-ring members having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D213/61—Halogen atoms or nitro radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Engineering & Computer Science (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Pulmonology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Epidemiology (AREA)
- Anesthesiology (AREA)
- Biomedical Technology (AREA)
- Heart & Thoracic Surgery (AREA)
- Hematology (AREA)
- Biophysics (AREA)
- Emergency Medicine (AREA)
- Immunology (AREA)
- Dermatology (AREA)
- Otolaryngology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Изобретение относится к соединению общей формулы (I), его N-оксидам по пиридиновому кольцу и их фармацевтически приемлемым солям:
, где: R1 и R2 являются разными или одинаковыми и независимо выбраны из группы, состоящей из: линейного (С1-С6)-алкила, возможно замещенного одним заместителем, выбранным из (С3-С7)-циклоалкила; (С1-С6)-галогеналкила; (С3-С7)-циклоалкила; R3 представляет собой Н или представляет собой один или два заместителя, независимо выбранных из атомов галогена; Z представляет собой группу (СН2)m, где m равно 0; А представляет собой фенильное кольцо, возможно замещенное одним заместителем R4, который выбран из группы, состоящей из: линейного (С1-С6)-алкила, замещенного одним морфолинилом; разветвленного (С1-С6)-алкила, возможно замещенного одним (С3-С7)-циклоалкилом; (С1-С6)-галогеналкила; (С1-С6)-алкилтио; атома галогена; и OR7, где R7 выбран из группы, состоящей из Н; (С1-С10)-алкила, возможно замещенного радикалом, выбранным из (С3-С7)-циклоалкила, морфолинила, фенила и пиридинила; и (С1-С10)-алкила, замещенного одной группой ОН; (С1-С6)-галогеналкила; (С3-С7)-циклоалкила; W выбран из группы, состоящей из: -NR9SO2R10, -CH2NR13SO2R14, -SO2NR15R16, -NHSO2R17, -OSO2R18, -NHCOR26, где R9, R10, R13, R14, R15, R16, R17, R18, R26 определены в формуле изобретения. Изобретение также относится к фармацевтической композиции, обладающей PDE4-ингибирующей активностью, на основе соединений формулы (I), к устройству, содержащему данную композицию. Технический результат: получены новые соединения и фармацевтические композиции на их основе, которые могут найти применение в медицине для лечения аллергического болезненного состояния или заболеваний дыхательных путей, таких как атопический дерматит, крапивница, аллергический ринит, астма и COPD. 5 н. и 9 з.п. ф-лы, 22 табл., 37 пр.
.
Description
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к ингибиторам фермента фосфодиэстеразы 4 (PDE4). Более конкретно, изобретение относится к соединениям, являющимся производными 1-фенил-2-пиридинилалкиловых спиртов, к способам получения таких соединений, композициям, содержащим их, и их терапевтическому применению.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Обструкция дыхательных путей является характерной чертой ряда тяжелых респираторных заболеваний, включая астму и хроническую обструктивную болезнь легких (COPD). События, приводящие к обструкции дыхательных путей, включают отек стенок дыхательных путей, избыточное образование слизи и воспаление.
Лекарственные средства для лечения респираторных заболеваний, таких как астма и COPD, в настоящее время вводят путем ингаляции. Одним из преимуществ ингаляционного способа над системным способом является возможность доставки лекарственного средства непосредственно к месту действия, что позволяет избежать любых системных побочных эффектов, обеспечивая, таким образом, более быстрый клинический ответ и более высокий терапевтический индекс.
В настоящее время ингаляционные кортикостероиды представляют собой предпочтительную поддерживающую терапию для лечения астмы, и вместе с бронхолитическими бета2-агонистами, используемыми для ослабления острых симптомов, они образуют основу современной терапии данного заболевания. Существующее на сегодняшний момент лечение COPD в большой степени является симптоматическим и осуществляется посредством применения бронхорасширяющей терапии ингаляционными
антихолинергическими средствами и ингаляционными агонистами бета2-адренорецепторов. Однако кортикостероиды не снижают воспалительный ответ при COPD, в отличие от их действия при астме.
Другой класс терапевтических агентов, которые рассматриваются в связи с их противовоспалительным действием в отношении лечения таких воспалительных респираторных заболеваний, как астма и COPD, представлен ингибиторами ферментов фосфодиэстераз (PDE), в частности фосфодиэстеразы 4-го типа (далее обозначаемой как PDE4).
В документах предшествующего уровня техники описаны различные соединения, действующие в качестве ингибиторов PDE4. Однако применимость некоторых ингибиторов PDE4 первого поколения, таких как ролипрам и пикламиласт, ограничена их нежелательными побочными эффектами. Указанные эффекты включают тошноту и рвоту вследствие их действия на PDE4 в центральной нервной системе и секрецию желудочного сока вследствие их действия на PDE4 в париетальных клетках в кишечнике.
Причина указанных побочных эффектов всесторонне исследована.
Обнаружено, что PDE4 существует в двух различных формах, представленных разными конформациями, которые были обозначены как PDE4 с высокоаффинным сайтом связывания ролипрама, или HPDE4, главным образом присутствующая в центральной нервной системе и в париетальных клетках, и PDE4 с низкоаффинным сайтом связывания ролипрама, или LPDE4, которая обнаружена в иммунных и воспалительных клетках (Jacobitz S. et al., Mol. Pharmacol., 1996, 50, 891-899). Хотя обе формы, по-видимому, проявляют каталитическую активность, они различаются по своей чувствительности к ингибиторам. В частности, оказывается, что соединения с высокой аффинностью к LPDE4 в меньшей степени способны вызывать такие побочные эффекты, как тошнота, рвота и повышенная желудочная секреция.
Попытка направленного воздействия на LPDE4 привела к небольшому улучшению в избирательности у ингибиторов PDE4 второго поколения, таких как рофлумиласт. Тем не менее для достижения приемлемого профиля побочных эффектов дозировку рофлумиласта уменьшают.
В документах предшествующего уровня техники описаны и другие классы соединений, действующих в качестве ингибиторов PDE4.
Например, в ЕР 1634606 описаны, среди прочего, такие производные кетонов, как производные бензофурана или 1,3-бензодиоксола.
В WO 9402465 описаны, среди прочего, производные кетонов общей формулы
где R1 представляет собой низший алкил, a R2 может представлять собой алкил, алкенил, циклоалкил, циклоалкенил, циклотиоалкил или циклотиоалкенил.
WO 9535281 (Celltech Therapeutics) относится к тризамещенным фенильным производным.
В WO 2009/018909 описаны производные 1-фенил-2-пиридинилалкиловых спиртов, имеющие общую формулу приведенную ниже:
в качестве ингибиторов фермента фосфодиэстеразы 4 (PDE4).
В WO 2009/077068 описаны другие производные 1-фенил-2-пиридинилалкиловых спиртов, имеющие общую формулу, приведенную ниже:
в качестве ингибиторов фермента фосфодиэстеразы 4 (PDE4).
В WO 2010/089107 описаны другие производные 1-фенил-2-пиридинилалкиловых спиртов, имеющие общую формулу, приведенную ниже:
в качестве ингибиторов фермента фосфодиэстеразы 4 (PDE4).
Несмотря на то, что к настоящему времени некоторые ингибиторы PDE4 уже описаны, как упомянуто выше, потребность в других ингибиторах PDE4 все еще существует. В частности, все еще существует потребность в других ингибиторах PDE4, обладающих высокой аффинностью к ферменту PDE4.
Особенно выгодной будет также идентификация других ингибиторов PDE4, обладающих и высокой аффинностью к ферменту PDE4, и хорошей растворимостью в воде и/или в водной системе.
Соответственно, помимо использования в ингаляционных препаратах в форме сухого порошкового ингалятора, находящегося под давлением дозирующего ингалятора или не содержащей пропеллентов распыляемой композиции, указанные соединения, благодаря своей способности всасываться и возможности изготовления из них препаратов, также могли бы быть введены другими путями, такими как пероральный или трансдермальный, а также в форме любых других фармацевтических растворов, таких как, например, растворы для введения посредством инъекции, инфузии или для введения в глаз.
Настоящее изобретение решает вышеупомянутую потребность путем предоставления соединений по изобретению.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к соединениям общей формулы (I), действующим в качестве ингибиторов фермента фосфодиэстеразы 4 (PDE4), к способам их получения, композициям, содержащим их, к терапевтическим применениям и комбинациям с другими фармацевтически активными ингредиентами, среди которых имеются, например, такие, которые используются в настоящее время в лечении респираторных расстройств, например бета2-агонисты, кортикостероиды, ингибиторы митоген-активируемой протеинкиназы (MAP-киназы) Р38, ингибиторы киназы нуклеарного фактора каппа-В, бета-субъединицы (IKK2), ингибиторы эластазы нейтрофилов человека (HNE), М3-антагонисты, модуляторы лейкотриенов, нестероидные противовоспалительные лекарственные средства (NSAID) и регуляторы слизеобразования.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Изобретение относится к соединениям общей формулы (I), действующим в качестве ингибиторов фермента фосфодиэстеразы 4 (PDE4), к способам их получения, содержащим их композициям и к их терапевтическим применениям.
Согласно изобретению предложены соединения формулы (I)
где:
R1 и R2 являются разными или одинаковыми и независимо выбраны из группы, состоящей из:
Н;
линейного или разветвленного (С1-С6)-алкила, возможно замещенного одним или более заместителями, выбранными из (С3-С7)-циклоалкила и (С5-С7)- циклоалкенила;
(С1-С6)-галогеналкила;
(С3-С7)-циклоалкила;
(С5-С7)-циклоалкенила;
линейного или разветвленного (С2-С6)-алкенила и
линейного или разветвленного (С2-С6)-алкинила;
R3 представляет собой Н или представляет собой один или более заместителей, независимо выбранных из группы, состоящей из CN, NO2, CF3 и атомов галогена;
Z представляет собой группу (СН2)m, где m равно 0 или 1;
А представляет собой фенильное кольцо, возможно замещенное одним или более заместителями R4, которые могут быть одинаковыми или разными и независимо выбранными из группы, состоящей из:
линейного или разветвленного (С1-С6)-алкила, возможно замещенного одним или более чем одним (С3-С7)-циклоалкилом или (С3-С7)- гетероциклоалкилом;
(С1-С6)-галогеналкила;
(С1-С6)-алкилтио;
атома галогена;
NH2 и
OR7, где R7 выбран из группы, состоящей из
- Н;
- (С1-С10)-алкила, возможно замещенного радикалом, выбранным из (С3-С7)-циклоалкила, (С3-С7)-гетероциклоалкила, арила и гетероарила;
- (С1-С10)-алкила, замещенного одной группой ОН;
- (С1-С6)-галогеналкила;
- (С3-С7)-циклоалкила;
- (С1-С4)алкиламинокарбонила;
- (С1-С4)алкилоксикарбонила;
- (С3-С7)-гетероциклоалкила, возможно замещенного (С1-С4)-алкилом, и
- группы R5R6N-(С1-С10)алкилен, где R5 и R6 независимо выбраны из группы, состоящей из Н, линейного или разветвленного (С1-С6)-алкила, или вместе с атомом азота, к которому они присоединены, образуют насыщенное, частично насыщенное или ненасыщенное кольцо, причем эти кольца возможно замещены (С1-С4)-алкилом, атомами галогена или группой R7R8N-(C1-С4)алкилен, где R7 и R8 являются разными или одинаковыми и независимо выбраны из группы, состоящей из Н, линейного или разветвленного (C1-С6)-алкила, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо;
W выбран из группы, состоящей из:
-NR9SO2R10, где
R9 выбран из группы, состоящей из
(С1-С10)-алкила, возможно замещенного (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, (С3-С7)-гетероциклоалкил-карбонилом, причем любое такое кольцо возможно может быть замещено одним или более чем одним (С1-С4)-алкилом или ОН; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН; и
R10 выбран из группы, состоящей из
(С1-С4)-алкила, возможно замещенного (С3-С7)-циклоалкилом;
(С3-С7)-циклоалкила и
фенила, каждый из которых возможно может быть замещен одним или более чем одним атомом галогена либо одной или более чем одной (С1-С4)-алкильной группой;
- -CH2NR13SO2R14, где
R13 выбран из группы, состоящей из:
Н;
(С3-С7)-циклоалкила;
(С1-С10)-алкила, возможно замещенного (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
R14 выбран из группы, состоящей из:
(С1-С4)-алкила;
(С3-С7)-гетероциклоалкил-(С1-С4)алкилена;
фенила, каждый из которых возможно может быть замещен одним или более чем одним атомом галогена или (С1-С4)-алкильной группой;
-(С1-С4)алкилен-(С3-С7)-гетероциклоалкила, который возможно может быть замещен одной или более группами, выбранными из: оксо, ОН, SH, (C1-С4)-алкила и гидрокси(С1-С6)алкилена;
-(С3-С7)-гетероциклоалкильного кольца, которое возможно может быть замещено одной или более группами, выбранными из: оксо, ОН, SH, (С1-С4)-алкила и гидрокси(С1-С6)алкилена;
-(С1-С4)алкилен-амино-(С3-С7)-тетероциклоалкила, который возможно может быть замещен одной или более группами, выбранными из: оксо, ОН, SH, (С1-С4)-алкила и гидрокси(С1-С6)алкилена;
-SO2NR15R16, где
R15 выбран из группы, состоящей из Н и (С1-С10)-алкила; и
R16 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С3-С7)- циклоалкилом или (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН; или
R15 и R16 вместе с атомом азота, к которому они присоединены, образуют (С3-С7)-гетероциклоалкильное кольцо, возможно замещенное одним или более (С1-С4)-алкилом;
-NHSO2R17, где
R17 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С3-С7)-циклоалкильным, (С3-С7)-гетероциклоалкильным, арильным и гетероарильным кольцом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
-OSO2R18, где
R18 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенный атомом галогена, ОН, (C1-C4-алкоксилом, (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, арилом или гетероарилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом, и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
-OC(O)R19, где
R19 выбран из группы, состоящей из:
(С3-С7)-циклоалкила, (С3-С7)-гетероциклоалкила, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
(С1-С10)-алкила, возможно замещенного одним или более чем одним атомом галогена, ОН, NH2, (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом, и
группы R11R12N-(С1-С10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
-C(O)R20, где
R20 выбран из группы, состоящей из:
-NR21R22, где R21 и R22 независимо выбраны из: Н, (С1-С6)- алкила, (С3-С7)-циклоалкила и (С3-С7)-гетероциклоалкил(С1-С4)алкилена, каждый из которых возможно может быть замещен (С1-С4)-алкилом, ОН, NH2, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное гетероциклическое кольцо, которое возможно может быть замещено (С1-С4)-алкилом, ОН или NH2;
-OR23, где R23 представляет собой (С1-С10)-алкил, замещенный одним или более чем одним атомом галогена, ОН, (С3-С7)циклоалкилом, (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
-NH-(С1-С4)алкилен-NR24R25, где
R24 и R25, одинаковые или разные, независимо выбраны из Н и (С1-С6)-алкила, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо, возможно замещенное одной или более (С1-С4)-алкильными группами;
-NHCOR26, где
R26 выбран из группы, состоящей из:
группы R27R28N-(C1-C6)алкилен, где R27 и R28, одинаковые или разные, независимо выбраны из Н, (С1-С6)-алкила, возможно замещенного ОН или NH2, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо, возможно замещенное одной или более группами (С1-С4)-алкил, ОН или NH2;
группы R27R28N-карбонил-(C1-C6)алкилен, где R27 и R28, одинаковые или разные, независимо выбраны из Н, (С1-С6)-алкила, возможно замещенного ОН или NH2, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо, возможно замещенное одной или более группами (С1-С4)-алкил, ОН или NH2;
(С3-С7)-гетероциклоалкильного кольца, которое возможно может быть замещено одной или более группами, выбранными из: оксо, ОН, SH или гидрокси(С1-С6)алкилена;
-NH-(С1-С4)алкилен-OR29, где R29 представляет собой Н или (С1-С6)-алкил;
-CH2OC(O)R30, где R30 выбран из
(С3-С7)-циклоалкила,
(С3-С7)-гетероциклоалкила, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
(С1-С10)-алкила, замещенного одним или более чем одним атомом галогена, ОН, (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено ОН или (С1-С4)-алкилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
их N-оксиды по пиридиновому кольцу и их фармацевтически приемлемые соли.
Изобретение также включает соответствующие N-оксиды по пиридиновому кольцу соединений формулы (I), которые представлены формулой (Ia)
где R1, R2, R3, z, А и W являются такими, как описано выше для соединений формулы (I).
Изобретение также охватывает фармацевтически приемлемые соли и/или их сольваты.
Термин «фармацевтически приемлемые соли», используемый в данном описании, относится к производным соединений формулы (I) или соответствующих им N-оксидов по пиридиновому кольцу, при этом исходное соединение подходящим образом модифицировано путем превращения по любой свободной кислотной или основной группе, если они присутствуют, в соответствующую соль присоединения с использованием основания или кислоты, традиционно считающимися фармацевтически приемлемыми.
Таким образом, подходящие примеры указанных солей могут включать соли присоединения минеральных или органических кислот, образованные с участием основных остатков, таких как аминогруппы, а также таких остатков минеральных или органических кислот, как карбоксильные группы.
Катионы неорганических оснований, которые можно подходящим образом использовать для получения солей по изобретению, включают ионы щелочных или щелочноземельных металлов, таких как калий, натрий, кальций или магний.
Соли, полученные взаимодействием исходного соединения, действующего в качестве основания, с неорганической или органической кислотой с образованием соли, включают, например, соли соляной кислоты, серной кислоты, фосфорной кислоты, метансульфоновой кислоты, камфорсульфоновой кислоты, щавелевой кислоты, малеиновой кислоты, янтарной кислоты и лимонной кислоты.
Специалистам в области органической химии очевидно, что многие органические соединения могут образовывать комплексы с растворителями, в которых их приводят во взаимодействие или из которых они выпадают в осадок или кристаллизуются. Эти комплексы известны как «сольваты». Фармацевтически приемлемые сольваты соединения по изобретению включены в объем данного изобретения.
В объем настоящего изобретения также включены полиморфы и кристаллические формы соединений формулы (I), их N-оксидов по пиридиновому кольцу или фармацевтически приемлемые солей или их сольватов.
Далее, соединения формулы (I), соответствующие N-оксиды по пиридиновому кольцу, варианты, энантиомеры, их диастереоизомеры, их фармацевтически приемлемые соли и сольваты и их полиморфы или кристаллические формы, определенные в любом аспекте изобретения (за исключением промежуточных соединений, описанных при изложении химических методов) обозначаются как «соединения по изобретению».
Изобретение также включает способ получения соединений по изобретению.
Согласно настоящему изобретению также предложены фармацевтические композиции на основе соединений по изобретению, по отдельности или в комбинации, в смеси с одним или более чем одним фармацевтически приемлемым носителем.
В другом аспекте согласно настоящему изобретению предложено применение соединений по изобретению в качестве лекарственного средства.
В одном из аспектов согласно настоящему изобретению предложено применение соединений по изобретению для изготовления лекарственного средства.
В частности, согласно настоящему изобретению предложено применение соединений по изобретению для предупреждения и/или лечения любого заболевания, характеризующегося повышенной активностью фосфодиэстеразы 4 (PDE4), и/или где желательно ингибирование активности PDE4.
В частности, соединения по изобретению, как таковые или в комбинации с другими активными ингредиентами, можно вводить для предупреждения и/или лечения заболевания дыхательных путей, характеризующегося обструкцией дыхательных путей, такого как астма и COPD.
В другом аспекте согласно настоящему изобретению предложено применение соединений по изобретению для изготовления лекарственного средства для предупреждения и/или лечения любого заболевания, характеризующегося повышенной активностью фосфодиэстеразы 4 (PDE4), и/или там, где желательно ингибирование активности PDE4.
Кроме того, согласно настоящему изобретению предложен способ предупреждения и/или лечения любого заболевания, где желательно ингибирование PDE4, включающий введение пациенту, нуждающемуся в таком лечении, терапевтически эффективного количества соединения по изобретению.
Определения
Использованный в данном описании термин «атомы галогена» включает в себя атомы фтора, хлора, брома и йода, предпочтительно хлора.
Использованный в данном описании термин «(С1-Cx)-алкил», где x представляет собой целое число больше 1, относится к алкильным группам с прямой и разветвленной цепью, где количество составляющих атомов углерода находится в диапазоне от 1 до х. В частности, алкильными группами являются метил, этил, н-пропил, изопропил и трет-бутил.
По аналогии, термин «(С1-Сх)алкилен» относится к двухвалентному (C1-Cx)алкильному радикалу, где (С1-Сх)алкил является таким, как определено выше.
Термин «(С1-Cx)-алкоксил», где x представляет собой целое число больше 1, относится к прямым и разветвленным алкоксигруппам, где количество составляющих атомов углерода находится в диапазоне от 1 до x. В частности, алкоксильными группами являются метоксильная, этоксильная, н-пропоксильная, изопропоксильная и трет-бутоксильная.
Выражение «(С1-Cx)галогеналкил» относится к определенным выше «(С1-Cx)алкильным» группам, где один или более атомов водорода заменены на один или более атомов галогена, которые могут быть одинаковыми или отличаться друг от друга.
Таким образом, примеры указанных (С1-С6)галогеналкильных групп могут включать галогенированные, полигалогенированные и полностью галогенированные алкильные группы, где все атомы водорода заменены на атомы галогена, например трифторметильную или дифторметильную группы.
Термин «(С1-Cx)-алкилтио», где x представляет собой целое число больше 1, относится к группам алкил-S- с прямой и разветвленной цепью, где количество составляющих атомов углерода находится в диапазоне от 1 до х. В частности, алкилтиогруппами являются метилтио, этилтио, н-пропилтио, изопропилтио и трет-бутилтио.
Термин «(С3-Cy)-циклоалкил», где у представляет собой целое число больше или равное 3, относится к насыщенным циклическим углеводородным группам, содержащим от 3 до y атомов углерода в кольце. Примеры включают циклопропил, циклобутил, циклопентил, циклогексил и циклогептил.
Производное выражение «(С3-Cy)-гетероциклоалкил» относится к моноциклическим (С3-Cy)циклоалкильным группам, в которых по меньшей мере один атом углерода в кольце заменен на гетероатом (например, N, NH, S или О). Неограничивающие примеры (С3-Cy)-гетероциклоалкила представлены: пирролидинилом, имидазолидинилом, тиазолидинилом, пиперазинилом, пиперидинилом, морфолинилом, тиоморфолинилом, азетидинилом и их монооксидом или диоксидом.
По аналогии, термин «(С3-Cy)-гетероциклоалкилен» относится к двухвалентному (С3-Cy)-гетероциклоалкильному радикалу, где (С3-Cy)-гетероциклоалкил является таким, как определено выше.
Выражение «(С3-Cy)циклоалкилкарбонил» относится к группам (С3-Cy)-циклоалкилCO, где группа «(С3-Cy)циклоалкил» имеет определенное выше значение.
Термин «(С2-Cz)алкенил» относится к прямым или разветвленным, конъюгированным или неконъюгированным углеродным цепям с одной или более двойными связями, в цис- или транс-конфигурации, где количество атомов находится в диапазоне от 2 до 6.
Термин «(С5-Cz)-циклоалкенил», где z представляет собой целое число больше или равное 5, относится к циклическим углеводородным группам, содержащим от 5 до z атомов углерода в кольце и одну или более двойных связей.
Термин «(С2-С6)алкинил» относится к прямым или разветвленным углеродным цепям с одной или более тройными связями, где количество атомов находится в диапазоне от 2 до 6.
Термин «(С3-Cy)-гетероциклоалкил(С1-Сх)алкилен» относится к вышеупомянутой группе «(С1-Сх)алкилен», в которой один концевой атом углерода связан с «(С3-Cy)-гетероциклоалкильной» группой.
Используемое в данном описании выражение «кольцевая система» относится к моно- или бициклическим кольцевым системам, которые могут быть насыщенными, частично ненасыщенными или ненасыщенными, таким как арил, (С3-С8)-циклоалкил, (С3-С7)-гетероциклоалкил или гетероарил, имеющим от 5 до 11 атомов в кольце, где по меньшей мере один атом в кольце является гетероатомом (например, N, S или О).
Выражение «арил» относится к моно- или би-кольцевым системам, имеющим от 6 до 10 атомов в кольце, где по меньшей мере одно кольцо является ароматическим.
Выражение «гетероарил» относится к моно- или би-кольцевым системам, имеющим от 5 до 11 атомов в кольце, где по меньшей мере одно кольцо является ароматическим и где по меньшей мере один атом в кольце является гетероатомом (например, N, NH, S или О).
Примеры подходящих арильных или 5,6-членных гетероарильных моноциклических систем включают радикалы, например, бензола, тиофена, пиррола, пиразола, имидазола, изоксазола, оксазола, изотиазола, тиазола, пиридина, фурана и тому подобного.
Примеры подходящих арильных или гетероарильных бициклических систем включают радикалы нафталина, бифенилена, пурина, птеридина, бензотриазола, хинолина, изохинолина, индола, изоиндола, бензотиофена, дигидробензодиоксина, дигидробензодиоксепина, бензоксазина и тому подобного.
В описании настоящего изобретения, если не указано иное, R3 представляет собой атом Н или, альтернативно, один или более заместителей, которые указаны ранее. Если же их больше одного, то указанные заместители на пиридильном кольце присутствуют в любом свободном положении.
Специалистам в данной области техники будет очевидно, что соединения общей формулы (I) содержат по меньшей мере один стереогенный центр, а именно, представленный ниже атомом углерода (1) со звездочкой, и таким образом существуют в виде оптических стереоизомеров.
Если соединения по изобретению имеют по меньшей мере один стереогенный центр, то они, соответственно, могут существовать в виде энантиомеров. Если в соединениях по изобретению имеются два или более стереогенных центра, то они помимо всего прочего могут существовать в виде диастереоизомеров. Следует понимать, что все такие изомеры и их смеси в любой пропорции включены в объем настоящего изобретения.
В предпочтительном воплощении настоящее изобретение относится к соединениям формулы (I)', представляющим собой соединения формулы (I), их N-оксидам по пиридиновому кольцу и их фармацевтически приемлемым солям, определенным выше, при этом абсолютная конфигурация атома углерода (1) является такой, которая показана ниже:
Абсолютная конфигурация атома углерода (1) присваивается на основании номенклатуры Кана-Ингольда-Прелога с учетом приоритетов для групп.
В одном из предпочтительных воплощений соединений формулы (I) абсолютной конфигурацией атома углерода (1) является (S).
В предпочтительном воплощении согласно изобретению предложены соединения формулы (I), где
R1 и R2 являются разными или одинаковыми и независимо выбраны из группы, состоящей из:
Н;
линейного или разветвленного (С1-С6)-алкила, возможно замещенного одним или более заместителями, выбранными из (С3-С7)-циклоалкила;
(С1-С6)-галогеналкила;
R3 представляет собой один или более заместителей, выбранных из CF3 и атомов галогена;
Z представляет собой группу (СН2)m, где m равно 0 или 1;
А представляет собой фенильное кольцо, возможно замещенное одним или более заместителями R4, которые могут быть одинаковыми или разными и независимо выбранными из группы, состоящей из:
линейного или разветвленного (С1-С6)-алкила, возможно замещенного одним или более чем одним (С3-С7)-циклоалкилом или (С3-С7)-гетероциклоалкилом;
(С1-С6)-галогеналкила;
(C1-С6)-алкилтио;
атома галогена;
NH2 и
OR7, где R7 выбран из группы, состоящей из
Н;
(С1-С10)-алкила, возможно замещенного радикалом, выбранным из (С3-С7)-циклоалкила, (С3-С7)-гетероциклоалкила, арила и гетероарила;
(С1-С10)-алкила, замещенного одной группой ОН;
(С1-С6)-галогеналкила;
(С3-С7)-циклоалкила и
группы R5R6N-(C1-C10)алкилен, где R5 и R6 независимо выбраны из группы, состоящей из Н, линейного или разветвленного (С1-С6)-алкила, или вместе с атомом азота, к которому они присоединены, образуют насыщенное, частично насыщенное или ненасыщенное кольцо, причем эти кольца возможно замещены (С1-С4)-алкилом, атомами галогена или группой R7R8N-(C1-С4)алкилен, где R7 и R8 являются разными или одинаковыми и независимо выбраны из группы, состоящей из Н, линейного или разветвленного (С1-С6)-алкила, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо;
W выбран из группы, состоящей из:
-NR9SO2R10, где
R9 выбран из группы, состоящей из
(С1-С10)-алкила, возможно замещенного (С3-С7)-гетероциклоалкилом, (С3-С7)-гетероциклоалкилкарбонилом, причем любое такое кольцо возможно может быть замещено одним или более (С1-С4)-алкилом или ОН; и
группы R11R12N-(С1-С10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН; и
R10 выбран из группы, состоящей из
(С1-С4)-алкила, возможно замещенного (С3-С7)-циклоалкилом;
(С3-С7)циклоалкила и
фенила, каждый из которых возможно может быть замещен одним или более чем одним атомом галогена либо одной или более чем одной (С1-С4)-алкильной группой;
-CH2NR13SO2R14, где
R13 выбран из группы, состоящей из:
Н;
(С1-С10)-алкила, возможно замещенного (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
R14 выбран из группы, состоящей из:
(С1-С4)-алкила;
(С3-С7)-гетероциклоалкил-(С1-С4)алкилена;
фенила, каждый из которых возможно может быть замещен одним или более чем одним атомом галогена либо одной или более чем одной (С1-С4)-алкильной группой;
-(С1-С4)алкилен-(С3-С7)-гетероциклоалкила, который возможно может быть замещен одной или более группами, выбранными из: оксо, ОН, (С1-С4)-алкила и гидрокси(С1-С6)алкилена;
-(С3-С7)-гетероциклоалкильного кольца, которое возможно может быть замещено одной или более группами, выбранными из: оксо, ОН, (С1-С4)-алкила и гидрокси(С1-С6)алкилена;
-(С1-С4)алкилен-амино-(С3-С7)-гетероциклоалкила, который возможно может быть замещен одной или более группами, выбранными из: оксо, ОН, (C1-С4)-алкила и гидрокси(С1-С6)алкилена;
-SO2NR15R16, где
R15 представляет собой Н; и
R16 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С3-С7)-гетероциклоалкилом, который возможно может быть замещен (С1-С4)-алкилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н, метил, этил, гидроксиметил, гидроксиэтил; или
R15 и R16 вместе с атомом азота, к которому они присоединены, образуют (С3-С7)-гетероциклоалкильное кольцо, возможно замещенное одним или более (С1-С4)-алкилом;
-NHSO2R17, где
R17 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С3-С7)циклоалкильным, (С3-С7)-гетероциклоалкильным, арильным и гетероарильным кольцом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
-OSO2R18, где
R18 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного атомом галогена, ОН, (С1-С4)-алкоксилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
-OC(O)R19, где
R19 представляет собой (С1-С10)-алкил, возможно замещенный одним или более чем одним атомом галогена, ОН, NH2, (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
-C(O)R20, где
R20 выбран из группы, состоящей из:
-NR21R22, где R21 и R22 независимо выбраны из: Н, (C1-С6)-алкила, (С3-С7)-циклоалкила и (С3-С7)-гетероциклоалкил(С1-С4)алкилена, каждый из которых возможно может быть замещен (С1-С4)-алкилом, ОН, NH2, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное гетероциклическое кольцо, которое возможно может быть замещено (С1-С4)-алкилом, ОН или NH2;
-OR23, где R23 представляет собой (С1-С10)-алкил, замещенный одним или более чем одним атомом галогена, ОН, (С3-С7)циклоалкилом, (С3-С7)-гетероциклоалкилом, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
-NH-(C1-C4)алкилен-NR24R25, где
R24 и R25, одинаковые или разные, независимо выбраны из Н и (С1-С6)-алкила, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо, возможно замещенное одной или более (С1-С4)-алкильными группами;
-NHCOR26, где
R26 выбран из группы, состоящей из:
группы R27R28N-(C1-C6)алкилен, где R27 и R28, одинаковые или разные, независимо выбраны из Н, (С1-С6)-алкила, возможно замещенного ОН или NH2, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо, возможно замещенное одной или более группами (С1-С4)-алкил, ОН или NH2;
группы R27R28N-карбонил-(C1-C6)алкилен, где R27 и R28, одинаковые или разные, независимо выбраны из Н, (С1-С6)-алкила, возможно замещенного ОН или NH2, или вместе с атомом азота, к которому они присоединены, образуют насыщенное или частично насыщенное кольцо, возможно замещенное одной или более группами (С1-С4)-алкил, ОН или NH2;
(С3-С7)-гетероциклоалкильного кольца, которое возможно может быть замещено одной или более группами, выбранными из: оксо, ОН, SH или гидрокси(С1-С6)алкилена;
-NH-(С1-С4)алкилен-OR29, где R29 представляет собой Н или (C1-С6)-алкил; и
-CH2OC(O)R30, где R30 выбран из (С1-С10)-алкила, замещенного одним или более чем одним атомом галогена, ОН, (С3-С7)-гетероциклоалкилом, возможно замещенным ОН или (С1-С4)-алкилом;
их N-оксиды по пиридиновому кольцу и их фармацевтически приемлемые соли.
В еще более предпочтительном воплощении изобретения предложены соединения формулы (I), где
R1 и R2 являются разными или одинаковыми и независимо выбраны из группы, состоящей из водорода, метила, этила, дифторметила, циклопропилметила или циклопропила;
R3 представляет собой один или более заместителей, выбранных из CF3, атомоа фтора и хлора, предпочтительно они представляют собой два одинаковых заместителя в положениях 3 и 5 пиридильного кольца;
Z представляет собой группу (СН2)m, где m равно 0;
А представляет собой фенильное кольцо, возможно замещенное одним или более заместителями R4, которые могут быть одинаковыми или разными и независимо выбранными из группы, состоящей из:
линейного или разветвленного (С1-С2)-алкила, возможно замещенного одним или более (С3-С7)-гетероциклоалкилом и предпочтительно 4-морфолинилом;
трифторметила;
метилтио;
атома галогена, выбранного из атома фтора или хлора; и
OR7, где R7 выбран из группы, состоящей из
Н;
(С1-С4)-алкила, возможно замещенного радикалом, выбранным из ОН, циклопропила, 4-морфолинила, 1- или 4-пиперидинила, 4-пиридинила и фенила;
трифторметила или дифторметила; и
W выбран из группы, состоящей из:
-NR9SO2R10, где
R9 выбран из группы, состоящей из
(С1-С4)-алкила, возможно замещенного 4-морфолинилом, 1-пиперидинилом, 1-пирролидинилом, пиперазинилом, 1,2-тиазолидин-3-илом, пиперазин-1-илкарбонилом, причем любое такое кольцо возможно может быть замещено одним или более метилом, этилом или ОН; и
группы R11R12N-(C1-C3)алкилен, где R11 и R12 независимо представляют собой Н или метил, возможно замещенный группой ОН; и
R10 выбран из группы, состоящей из циклопропилметила и циклопропила;
-CH2NR13SO2R14, где
R13 выбран из группы, состоящей из Н, 4-морфолинометила и 4-морфолиноэтила;
R14 выбран из группы, состоящей из метила, этила и фенила, возможно замещенных одним или более чем одним атомом галогена либо одной или более чем одной (С1-С4)-алкильной группой;
-(С1-С2)алкилен-(С3-С7)-гетероциклоалкила, который возможно может быть замещен одной или более группами, выбранными из: оксо, ОН, метила, гидроксиметила и 2-гидроксиэтила;
-(С3-С7)-гетероциклоалкильного кольца, которое возможно может быть замещено одной или более группами, выбранными из: оксо, ОН, метила, гидроксиметила и 2-гидроксиэтила;
-(С1-С4)алкилен-амино-(С3-С7)-гетероциклоалкила, который может представлять собой, например 4-пираниламинометильную группу;
-SO2NR15R16, где
R15 представляет собой Н; и
R16 выбран из группы, состоящей из
4-морфолинометила,
2-(4-морфолино)этила,
4-метилпиперазинометила,
2-(4-метилпиперазино)этила; и
группы R11R12N-(C1-C2)алкилен, где R11 и R12 независимо представляют собой Н, метил, этил, гидроксиметил, гидроксиэтил; или
R15 и R16 вместе с атомом азота, к которому они присоединены, образуют пиперазинильное, морфолинильное или пиперидинильное кольцо, возможно замещенное одной или более метильной группой;
-NHSO2R17, где
R17 выбран из группы, состоящей из
пиперазинильного, морфолинильного и пиперидинильного кольца, каждое из которых возможно замещено одной или более метильной группой; и
аминоэтильной, метиламиноэтильной, диметиламино-этильной, гидроксиметиламиноэтильной и бис(гидроксиметил)амино-этильной групп;
-OSO2R18, где
R18 выбран из группы, состоящей из:
метоксиметила,
этоксиметила и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н, метил, этил, гидроксиметил или 2-гидроксиэтил;
-OC(O)R19, где
R19 представляет собой (С1-С10)-алкил, возможно замещенный одним или более NH2;
-C(O)R20, где
R20 выбран из группы, состоящей из:
-NR21R22, где R21 представляет собой Н; R22 выбран из (С3-С6)-циклоалкила и (С3-С7)-гетероциклоалкил(С1-С2)алкилена, каждый из которых возможно может быть замещен (С1-С4)-алкилом или NH2, или вместе с атомом азота, к которому они присоединены, образуют пиперазинильное или пиперидинильное кольцо, которое возможно может быть замещено метилом;
-OR23, где R23 представляет собой (С1-С3)-алкил, замещенный (С3-С6)-гетероциклоалкилом, возможно замещенным метилом;
-NHCOR26, где
R26 выбран из группы, состоящей из:
группы R27R28N-(C1-C6)алкилен, где R27 и R28, одинаковые или разные, независимо выбраны из Н, метила, гидроксиметила, этила или 2-гидроксиэтила, или вместе с атомом азота, к которому они присоединены, образуют насыщенное кольцо, возможно замещенное одной или более группами метил, ОН или NH2;
группы R27R28N-карбонил-(C1-C6)алкилен, где R27 и R28 представляют собой (С1-С6)алкил и вместе с атомом азота, к которому они присоединены, образуют насыщенное кольцо, замещенное одним или более метилом;
(С3-С7)-гетероциклоалкильного кольца, которое возможно может быть замещено одной или более группами, выбранными из: оксо, ОН, SH или гидрокси(С1-С6)алкилена;
-NH-(C1-C4)алкилен-OR29, где R29 представляет собой Н или (С1-С6)-алкил; и
-CH2OC(O)R30, где R30 выбран из 1-пиперидинилметила, 2-(1-пиперидинил)этила, 1-пирролидинилметила, 2-(1-пирролидинил)этила, пиперазинилметила и 2-(пиперазинил)этила, причем все эти кольца возможно замещены ОН или метилом;
их N-оксиды по пиридиновому кольцу и их фармацевтически приемлемые соли.
Соединения по изобретению наделены как высокой аффинностью к ферменту PDE4, так и хорошей растворимостью в воде и/или в водной системе, что может обеспечить им благоприятную в случае перорального или трансдермального введения способность всасываться и/или возможность изготовления из них препаратов в любых фармацевтических растворах, таких как растворы для введения посредством инъекции, инфузии или для введения в глаз.
Соединения по изобретению могут быть получены согласно соответствующей модификации подходов к синтезу, описанных ниже в экспериментальном разделе в примерах 1-39.
Описанные ниже способы не следует рассматривать как ограничивающие объем способов синтеза, доступных для получения соединений по изобретению.
Описанный способ имеет особое преимущество, поскольку допускает должное модулирование посредством любого надлежащего варианта, известного специалисту, с целью получения любого из желаемых соединений по изобретению. Такие варианты включены в объем настоящего изобретения.
Из всего сказанного выше, специалисту должно быть понятно, что любая из описанных групп может быть представлена в том виде, как она есть, или в любой надлежащим образом защищенной форме.
В частности, перед проведением алкилирования, ацилирования, сочетания, окисления или сульфонилирования необходимо защитить функциональные группы, присутствующие в соединениях по изобретению или их промежуточных соединениях, которые могли бы привести к развитию нежелательной побочной реакции и образованию побочных продуктов. Аналогичным образом, по завершении указанных реакций может быть осуществлено последующее удаление защиты у тех же защищенных групп.
В настоящем изобретении, если не указано иное, термин «защитная группа» обозначает защитную группу, используемую для сохранения функциональности группы, с которой она связана. Обычно защитные группы используют для сохранения функциональности амино-, гидроксильных или карбоксильных групп. Таким образом, соответствующие защитные группы могут включать, например бензил, бензилоксикарбонил, трет-бутоксикарбонил, группы сложных алкиловых или бензиловых эфиров или им подобные, которые хорошо известны специалистам в данной области техники (см. в качестве общей ссылки T.W. Green; Protective Groups in Organic Synthesis (Wiley, N.Y. 1999)).
Аналогичным образом, избирательное введение и удаление защиты в случае любой из указанных групп, например, включая карбонильные, гидроксильные или аминогруппы, может быть выполнено в соответствии с очень хорошо известными способами, обычно используемыми в области химического органического синтеза.
N-оксиды по 4-пиридинильному кольцу соединений общей формулы (I) и их варианты могут быть получены в соответствии со способами, доступными из литературных источников и хорошо известными специалисту. Например, они могут быть получены в результате растворения соединения общей формулы (I) или его вариантов в CH2Cl2 или CHCl3, затем добавления окисляющего агента, такого как м-хлорпербензойная кислота (mСРВА), к полученному раствору. Другими окисляющими агентами, которые могут быть использованы, являются перекись водорода, пербензойная кислота и надуксусная кислота.
Альтернативно, особенно для таких соединений, которые содержат функциональные группы, чувствительные к окислению, соответствующие N-оксиды получают путем осуществления стадии окисления до введения других функциональных групп.
В одном из воплощений способ получения соединений формулы (I) или их вариантов осуществляют, исходя из N-оксида по пиридиновому кольцу промежуточных соединений, таким образом делая возможным получение соединения формулы (I) или его вариантов в форме N-оксидов по пиридиновому кольцу.
Возможное образование солей соединений формулы (I) или их N-оксидов по пиридиновому кольцу может быть осуществлено путем надлежащего превращения любой из свободных кислотных или аминогрупп с получением соответствующих фармацевтически приемлемых солей. В этом случае условия работы, используемые для возможного образования солей соединений по изобретению, также находятся в компетенции специалиста.
Из всего сказанного выше специалисту должно быть понятно, что описанный выше способ, охватывающий любой его вариант для получения подходящих соединений по изобретению, можно легко модифицировать, если адаптировать реакционные условия к конкретным потребностям, например, путем выбора соответствующих агентов сочетания, растворителей и защитных групп, в зависимости от ситуации.
Согласно настоящему изобретению также предложены фармацевтические композиции соединений по изобретению в смеси с одним или более чем одним фармацевтически приемлемым носителем, например, с такими, которые описаны в Remington's Pharmaceutical Sciences Handbook, XVII Ed., Mack Pub., N.Y., U.S.A.
Введение соединений по настоящему изобретению может быть выполнено в соответствии с потребностями пациента, например перорально, интраназально, парентерально (подкожно, внутривенно, внутримышечно, интрастернально и путем инфузии), путем ингаляции, ректально, вагинально, местно, локально, трансдермально и путем глазного введения. Для введения соединений по изобретению можно использовать различные твердые пероральные лекарственные формы, включая такие твердые формы, как таблетки, желатиновые капсулы, капсулы, каплеты, гранулы, пастилки для рассасывания и нерасфасованные порошки. Соединения по настоящему изобретению или соединения формулы (II) можно вводить по отдельности или в комбинации с различными фармацевтически приемлемыми носителями, разбавителями (такими как сахароза, маннит, лактоза, крахмалы) и эксципиентами, известными в данной области техники, включая, но не ограничиваясь этим суспендирующие агенты, солюбилизаторы, буферные агенты, связующие вещества, разрыхлители, консерванты, красители, корригенты, смазывающие вещества и тому подобное. Кроме того, при введении соединений по настоящему изобретению или соединений формулы (II) имеют преимущество капсулы, таблетки и гели с замедленным высвобождением.
Для введения соединений по изобретению также можно использовать различные жидкие пероральные лекарственные формы, включая водные и неводные растворы, эмульсии, суспензии, сиропы и эликсиры. Такие лекарственные формы также могут содержать известные в данной области подходящие инертные разбавители, такие как вода, и известные в данной области подходящие эксципиенты, такие как консерванты, увлажняющие агенты, подсластители, корригенты, а также агенты для эмульгирования и/или суспендирования соединений по изобретению или соединений формулы (II). Соединения по настоящему изобретению можно вводить, например, внутривенно в форме изотонического стерильного раствора. Также возможны другие препараты.
Суппозитории для ректального введения соединений по настоящему изобретению могут быть приготовлены путем смешивания соединения с подходящим эксципиентом, таким как масло какао, салицилаты и полиэтиленгликоли.
Композиции для вагинального введения могут быть в форме крема, геля, пасты, пены или аэрозоля, содержащих помимо активного ингредиента такие подходящие носители, которые известны в данной области техники.
Фармацевтическая композиция для местного введения может быть в форме кремов, мазей, линиментов, лосьонов, эмульсий, суспензий, гелей, растворов, паст, порошков, спреев и капель, подходящих для применения на коже, для введения в глаз, ухо или нос. Местное введение также может включать трансдермальное введение с применением таких средств, как трансдермальные пластыри.
Для лечения заболеваний дыхательных путей соединения по изобретению предпочтительно вводят путем ингаляции.
Ингаляционные препараты включают ингаляционные порошки, пропеллентсодержащие дозирующие аэрозоли или не содержащие пропеллентов ингаляционные композиции.
Для введения в виде сухого порошка можно применять однодозовые или многодозовые ингаляторы, известные из предшествующего уровня техники. В этом случае порошок может быть внесен в желатиновые, пластиковые или другие капсулы, картриджи или блистерные упаковки или находиться в резервуаре.
К порошкообразным соединениям по изобретению может быть добавлен разбавитель или носитель, обычно нетоксичный и химически инертный в отношении соединений по изобретению, например лактоза или любое другое вспомогательное вещество, подходящее для улучшения вдыхаемой фракции.
Ингаляционные аэрозоли, содержащие газообразный пропеллент, такой как гидрофторалканы, могут содержать соединения по изобретению либо в растворе, либо в форме диспергированных или суспендированных микронизированных частиц. Композиции, приводимые в движение с помощью пропеллента, также могут содержать другие ингредиенты, такие как сорастворители, стабилизаторы и возможно другие эксципиенты.
Ингаляционные композиции без пропеллента, содержащие соединения по изобретению, могут быть в форме растворов или суспензий в водной, спиртовой или водноспиртовой среде, и их доставка может быть осуществлена посредством струйных или ультразвуковых небулайзеров, известных из предшествующего уровня техники, или посредством небулайзеров мягкого аэрозоля, таких как Respimat®.
Соединения по изобретению могут быть введены в виде единственного активного агента или в комбинации с другими фармацевтически активными ингредиентами, включая ингредиенты, используемые в настоящее время в лечении респираторных расстройств, например бета2-агонисты, антимускариновые агенты, кортикостероиды, ингибиторы митоген- активируемых протеинкиназ (МАР-киназы Р38), ингибиторы киназы нуклеарного фактора каппа-В, бета-субъединицы (IKK2), ингибиторы эластазы нейтрофилов человека (HNE), ингибиторы фосфодиэстеразы 4 (PDE4), модуляторы лейкотриенов, нестероидные противовоспалительные агенты (NSAID) и регуляторы слизеобразования.
Согласно настоящему изобретению также предложены комбинации соединения по изобретению с β2-агонистом, выбранным из группы, состоящей из кармотерола, вилантерола (GSK-642444), индакатерола, милветерола, арформотерола, формотерола, сальбутамола, левалбутерола, тербуталина, AZD-3199, олодатерола (BI-1744-CL), абедитерола (LAS-100977), бамбутерола, изопротеренола, прокатерола, кленбутерола, репротерола, фенотерола и ASF-1020 и их солей.
Согласно настоящему изобретению также предложены комбинации соединения по изобретению с кортикостероидом, выбранным из группы, состоящей из флутиказона пропионата, флутиказона фуроата, мометазона фуроата, белкометазона дипропионата, циклесонида, будесонида, GSK 685698, GSK 870086.
Согласно настоящему изобретению также предложены комбинации соединения по изобретению с антимускариновым агентом, выбранным из группы, состоящей из солей аклидиния, тиотропия, ипратропия, троспия, гликопиррония и окситропия.
Согласно настоящему изобретению также предложены комбинации соединения по изобретению с ингибитором PDE4, выбранным из группы, состоящей из AN-2728, AN-2898, CBS-3595, апремиласта, ELB-353, KF-66490, K-34, LAS-37779, IBFB-211913, AWD-12-281, ципамфиллина, циломиласта, рофлумиласта, BAY19-8004 и SCH-351591, AN-6415, indus-82010, TPI-PD3, ELB- 353, СС-11050, GSK-256066, оглемиласта, ОХ-914, тетомиласта, МЕМ-1414 и RPL-554.
Согласно настоящему изобретению также предложены комбинации соединения по изобретению с ингибитором МАР-киназы Р38, выбранным из группы, состоящей из семапимода, талмапимода, пирфенидона, РН-797804, GSK-725, минокина (minokine) и лосмапимода и их солей.
В предпочтительном воплощении согласно настоящему изобретению предложены комбинации соединения по изобретению с ингибитором IKK2.
Согласно изобретению также предложены комбинации соединения по изобретению с ингибитором HNE, выбранным из группы, состоящей из ААТ, ADC-7828, аэрива (aeriva), TAPI, АЕ-3763, KRP-109, АХ-9657, POL-6014, AER-002, AGTC-0106, респрива (respriva), AZD-9668, земайра, ААТ IV, PGX-100, элафина, SPHD-400, проластина С и проластина ингаляционного.
Согласно изобретению также предложены комбинации соединения по изобретению с модулятором лейкотриенов, выбранным из группы, состоящей из монтелукаста, зафирлукаста и пранлукаста.
Согласно изобретению также предложены комбинации соединения по изобретению с NSAID, выбранным из группы, состоящей из ибупрофена и кетопрофена.
Согласно изобретению также предложены комбинации соединения по изобретению с регулятором слизеобразования, выбранным из группы, состоящей из INS-37217, диквафозола, сибенадета, CS-003, талнетанта, DNK- 333, MSI-1956 и гефитиниба.
Дозировки соединений по настоящему изобретению зависят от ряда факторов, включая конкретное подлежащее лечению заболевание, тяжесть симптомов, путь введения, частоту введения лекарственных средств, конкретное используемое соединение, эффективность, токсикологический профиль и фармакокинетический профиль соединения.
Преимущественно соединения по изобретению могут быть введены, например, в дозировке от 0,001 до 1000 мг/сутки, предпочтительно от 0,1 до 500 мг в сутки.
При введении путем ингаляции дозировка соединений по изобретению составляет преимущественно от 0,01 до 20 мг в сутки, предпочтительно от 0,1 до 10 мг в сутки.
Предпочтительно, соединения по изобретению, как таковые или в комбинации с другими активными ингредиентами, могут быть введены для предупреждения и/или лечения любого обструктивного респираторного заболевания, такого как астма, хронический бронхит и хроническая обструктивная болезнь легких (COPD).
Тем не менее соединения по изобретению могут быть введены для предупреждения и/или лечения любых заболеваний, при которых необходимо ингибирование PDE4. Указанные заболевания включают аллергические заболевания, такие как атопический дерматит, крапивница, аллергический ринит, аллергический конъюнктивит, весенний конъюнктивит, эозинофильная гранулема, псориаз, воспалительный артрит, ревматоидный артрит, септический шок, язвенный колит, болезнь Крона, реперфузионное повреждение миокарда и головного мозга, хронический гломерулонефрит, эндотоксический шок, кистозный фиброз, артериальный рестеноз, атеросклероз, кератоз, ревматоидный спондилит, остеоартрит, парез (pyresis), сахарный диабет, пневмокониоз, контактную экзему токсического и аллергического характера, атопическую экзему, себорейную экзему, простой лишай, солнечный ожог, зуд в аногенитальной зоне, гнездную алопецию, гипертрофические рубцы, дискоидную красную волчанку, системную красную волчанку, фолликулярные и обширные пиодермии, эндогенные и экзогенные акне, розовые угри, болезнь Бехчета, анафилактическую пурпуру, нефрит, воспалительное заболевание кишечника, лейкоз, рассеянный склероз, желудочно-кишечные заболевания, аутоиммунные заболевания и тому подобное.
Они также включают неврологические и психиатрические расстройства, такие как болезнь Альцгеймера, рассеянный склероз, амиотрофический боковой склероз (ALS), множественная системная атрофия (MSA), шизофрения, болезнь Паркинсона, болезнь Гентингтона, болезнь Пика, депрессия, инсульт и повреждение спинного мозга.
Теперь настоящее изобретение будет описано далее посредством приведенных ниже неограничивающих примеров.
Экспериментальный раздел
Химические названия соединений создавали, используя программное обеспечение «Structure То Name Enterprise», версия 10.0, Cambridge.
Очистка с использованием предварительно упакованного сильного катионообменного (SCX) картриджа относится к использованию Isolute SCX, сильного катионообменного сорбента.
Методики, использованные для образования солей
Если не указано иное, трифторацетатные соли и соли муравьиной кислоты, описанные в экспериментальном разделе, получали в соответствии со следующей методикой: соединения, содержащие один или более основных центров и очищенные препаративной высокоэффективной жидкостной хроматографией (HPLC), получали в виде соли муравьиной кислоты (способ 1) или соли трифторуксусной кислоты (способ 2), сразу после того, как очищенные фракции, собранные по окончании хроматографии, упаривали при пониженном давлении без какой-либо дополнительной основной обработки.
Если не указано иное, любую другую соль получали путем обработки данного основания раствором соответствующей кислоты в условиях, известных специалисту.
При необходимости, стехиометрию солей определяли посредством ЯМР.
Определение ЯМР-характеристик
ЯМР-спектры регистрировали или:
1Н-ЯМР спектры регистрировали на спектрометре 400 МГц Varian AS400. Химические сдвиги приведены в виде величин δ в млн-1 относительно триметилсилана (TMS) в качестве внутреннего стандарта. Константы спин-спинового взаимодействия (величины J) приведены в герцах (Гц), а мультиплетности приведены с использованием следующего сокращения (s = синглет, d = дублет, t = триплет, q = квартет, m = мультиплет, br = уширенный, nd = не определяли);
или:
1Н-ЯМР-спектры регистрировали на спектрометре Bruker ARX300 при 300,13 МГц (1Н), используя дейтерированные растворители, такие как дейтерированный диметилсульфоксид (DMSO-d6) или дейтерированный хлороформ (CDCl3). Данный прибор был оснащен многоядерным обратным зондом и устройством для контроля температуры. Химические сдвиги выражают в виде числа частей на миллион (млн-1) в сторону слабого поля относительно сигнала тетраметилсилана (в единицах δ). Мультиплетность указывают следующим образом: (s) синглет, (d) дублет, (dd) дублет дублета, (ddd) триплет дублета, (t) триплет, (dt) дублет триплета, (q) квартет, (m) мультиплет, (br s) уширенный сигнал. Константы спин-спинового взаимодействия J выражают в единицах герц (Гц).
Препаративная HPLC - метод 1
Колонка: препаративная Symmetry, С18, 17 мкм, 19×300, от Waters.
Скорость потока: 20 мл/мин.
Подвижная фаза: 90% H2O, 10% ацетонитрила, 0,05% трфторксусной кислоты (TFA) (А), 10% H2O, 90% ацетонитрила, 0,05% TFA (В).
Градиент:
Тот же градиент, но без TFA в подвижной фазе, использовали для препаративной HPLC в нейтральных условиях.
Препаративная HPLC - метод 2
Micromass ZQ; устройство ввода пробы 2767; фотодиодный матричный детектор 2996; все от Waters.
Колонка: препаративная для масс-спектрометрии (MS), XTerra, С18 (5 мкм, 19×150 мм, Waters); скорость потока 20 мл/мин с MS-детекцией или детекцией в ультрафиолете (УФ) при 254 нм.
Градиент:
Элюент:
растворитель A (вода : MeCN : НСООН, 95:5:0,05);
растворитель В (вода : MeCN : HCOOH, 5:95:0,05).
Препаративная HPLC - метод 3
Micromass ZQ/устройство ввода пробы 2767, от Waters.
Фотодиодный матричный детектор: 2996.
Колонка: препаративная для MS, XTerra, С18, 10 мкм, 19×300.
Скорость потока: 20 мл/мин.
Подвижные фазы: H2O, 0,1% TFA (А); ацетонитрил, 0,1% TFA (В).
Градиент:
Кондиционирование:
Хиральная HLPC
Энантиомерную чистоту определяли на HPLC-системе 1050 от Hewlett Packard, используя колонку Chiracel OD (5 мкм; 4,6×250 мм) с элюированием изократической смесью гексана и изопропанола в разных соотношениях, которые указаны в каждом конкретном примере.
Скорость потока 0,8 мл/мин.
УФ-детекция при 230 нм.
Определение оптического вращения (активности)
Значения удельного вращения для соединений измеряли с использованием поляриметра модели 241 или 341 от Perkin Elmer.
| Температура (°С) | 25 |
| Длина пути (дм) | 1 |
| Длина волны | D-линия натрия (589 нм) |
Значения [МН]+ для MS/ESI+ (электрораспылительная ионизация) приведенные в тексте ниже, могут быть получены или с использованием MS-прибора ZQ от Waters (или его эквивалента), или с использованием системы сверхэффективной жидкостной хроматографии (UPLC) от Waters.
MS-прибор: ZQ от Waters (или его эквивалент)
Полярность ES+
| Капилляр (кВ) | 3,00 |
| Сопло (В) | 20,00 |
| Экстрактор (В) | 3,00 |
| Радиочастотная (RF) линза (В) | 1,0 |
Полярность ES-
| Капилляр (кВ) | 3,00 |
| Сопло (В) | 20,00 |
| Экстрактор (В) | 3,00 |
| RF линза (В) | 1,0 |
| Температура источника (°С) | 110 |
| Температура десольватации (°С) | 210 |
Поток газа через сопло (л/ч) 150
| Десольватирующий поток газа (л/ч) | 650 |
| Диапазон масс: | от 100 до 950 |
| Время сканирования (с): | 0,32 |
| Задержка между сканированиями (с): | 0,03 |
Система для жидкостной хроматографии (LC): UPLC Acquitv от Waters
Система: для UPLC от Waters в сочетании с ZQ Micromass и сопряженная с фотодиодным матричным (PDA) детектором 2996.
Колонка: для UPLC, Acquity ВЕН, С18; 1,7 мкм; 50×2,1 мм.
Метод: TFA long.
Условия: ESI+, 3,2 кВ, 25 В, 350°C.
Длина волны: PBI
Подробные пути и методики синтеза соединений из конкретных примеров приведены в примерах 1-39.
В приведенных далее методиках после каждого исходного вещества иногда приводится ссылка на идентификационный номер соединения. Это предусмотрено исключительно для помощи специалисту-химику. Исходное вещество получали не обязательно из партии, на которую дана ссылка.
В том случае, когда дается ссылка на применение «похожей» или «аналогичной» методики, которая будет понятна специалистам в данной области техники, то такая методика может включать незначительные изменения, например, в температуре реакции, количестве реагентов/растворителей, продолжительности реакции, условиях обработки или условиях хроматографической очистки.
Некоторые соединения или промежуточные соединения, упомянутые в настоящей патентной заявке и использованные для синтеза соединения по настоящему изобретению, описаны в предыдущих патентных заявках, которые приведены в Таблице 1.
Пример 1
Синтез (S)-3,5-дихлор-4-(2-(3,4-диметоксифенил)-2-гидроксиэтил)пиридин-1-оксида (соединения 1)
Схема 1
Стадия 1. Синтез 2-(3,5-дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этанола (2)
3,5-Дихлор-4-метилпиридин (54 г; 331 ммоль) растворяли в безводном THF (480 мл) в атмосфере аргона и охлаждали при -78°C в бане со смесью сухой лед/ацетон. По каплям добавляли 1 н. раствор гексаметилдисилазида лития (LHMDS) в THF (331 мл; 331 ммоль), поддерживая температуру при -78°C. Смесь перемешивали при -78°C в течение 1 ч. После этого по каплям добавляли раствор 3,4-диметоксибензальдегида (50 г; 301 ммоль) в безводном THF (120 мл), поддерживая температуру при -78°C. По завершении добавления смесь оставляли нагреваться до комнатной температуры (KT).
Реакционную смесь выливали в лед и воду (1 л), и смесь перемешивали до тех пор, пока не образовывался обильный осадок. Твердое вещество отфильтровывали и растворяли в этилацетате (500 мл), сушили над Na2SO4 и растворитель выпаривали под вакуумом. Кристаллизацию неочищенного вещества проводили в смеси CHCl3/гексан. Осадок отфильтровывали, промывали гексаном и сушили под вакуумом при 40°C в течение 8 ч, получая 55 г (выход 45%). Маточную жидкость упаривали под вакуумом при 40°C, растворяли в этилацетате (200 мл) и экстрагировали, используя 200 мл воды. Органический раствор сушили над Na2SO4 и растворитель выпаривали под вакуумом при 40°C. Кристаллизацию неочищенного вещества проводили в смеси CHCl3/гексан и получали еще 15 г желаемого продукта (общий выход 70%).
Стадия 2. Синтез ((S)-2-(3,5-дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этил)-2-(6-метоксинафталин-2-ил)пропаноата (11)
2-(3,5-Дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этанол (соединение 2; 50 г; 152 ммоль) и имеющуюся в продаже (R)-2-(6-метоксинафталин-2-ил)пропановую кислоту (соединение 10; 38,6 г; 168 ммоль), диметиламинопиридин (DMAP) (20,5 г; 168 ммоль) и 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC) (43,8 г; 229 ммоль) растворяли в диметилформамиде (DMF) (300 мл), и реакционную смесь перемешивали при КТ в течение 2 ч. По окончании этого времени добавляли воду (500 мл), и раствор перемешивали, пока не начинал выпадать осадок. Твердое вещество отфильтровывали и растворяли в дихлорметане (DCM) (500 мл). Органический раствор промывали 1 н. водным раствором HCl (2×500 мл), насыщенным водным раствором NaHCO3 (500 мл) и сушили над Na2SO4. Растворитель выпаривали под вакуумом, твердый остаток подвергали обработке ультразвуком в EtOH (300 мл) и растирали в течение 1 ч. Полученный осадок собирали фильтрованием и сушили под вакуумом при 40°C в течение 4 ч, получая указанное в заголовке соединение (79 г; выход 99%) в виде смеси диастереоизомеров.
Стадия 3. Синтез (R)-((S)-2-(3,5-дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этил)-2-(6-метоксинафталин-2-ил)пропаноата (12)
((S)-2-(3,5-Дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этил)-2-(6-метоксинафталин-2-ил)пропаноат (79 г; 146 ммоль), растворенный в CHCl3 (100 мл), медленно добавляли МеОН (30 мл) до появления устойчивой опалесценции и смесь оставляли при КТ на 2 ч. Образовавшееся твердое вещество собирали фильтрованием и перекристаллизовывали с использованием системы растворителей CHCl3/MeOH (70 мл/20 мл), получая 35 г желаемого соединения (выход 88%, ее 98%).
Анализ с использованием хиральной HPLC: Rt=42,33 мин (быстро элюирующийся изомер); элюент: гексан : изопропанол, 97:3.
1Н ЯМР (600 МГц, ХЛОРОФОРМ-d) δ млн-1 8.04 (s, 2Н), 7.67 (d, J=8,79 Гц, 1Н), 7.58 (d, J=8,52 Гц, 1Н), 7.53 (m, 1Н), 7.12-7.20 (m, 3Н), 6.95 (dd, J=8,24; 1,92 Гц, 1Н), 6.78-6.88 (m, 2Н), 6.14 (dd, J=10,44; 4,12 Гц, 1Н), 3.95 (s, 3Н), 3.88 (s, 3Н), 3.78-3.81 (m, 4Н), 3.55 (dd, J=13,73; 10,44 Гц, 1Н), 3.14 (dd, J=13,60; 4,26 Гц, 1Н), 1.44 (d, J=7,14 Гц, 3Н).
Стадия 4. Синтез (S)-2-(3,5-дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этанола (13)
(R)-((S)-2-(3,5-Дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этил)-2-(6- метоксинафталин-2-ил)пропаноат (30 г; 56 ммоль) растворяли в МеОН и медленно добавляли толуол. К суспензии медленно добавляли трет-бутилат калия. Смесь перемешивали в течение 24 ч при КТ. Реакционную смесь разбавляли водой (500 мл) и водную смесь экстрагировали CHCl3 (500 мл). Органический слой сушили над Na2SO4 и растворитель выпаривали под вакуумом. Остаток кристаллизовали из CHCl3 (100 мл) и гексана (20 мл; до появления устойчивой опалесценции). Маточную жидкость концентрировали и перекристаллизовывали таким же образом, получая вторую партию желаемого соединения. Суммарно получали 16 г желаемого соединения (выход 87%).
Анализ с использованием хиральной HPLC: Rt=58,03 мин; элюент: гексан : изопропанол 95:5. (с=0,506; метанол).
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.47 (s, 2Н), 6.96-7.15 (m, 1Н), 6.87 (m, 2Н), 4.93-5.21 (m, 1Н), 4.50 (d, J=3,97 Гц, 1Н), 3.78 (s, 6Н), 3.44 (dd, J=12,79; 8,38 Гц, 1Н), 3.22 (dd, J=13,01; 5,51 Гц, 1Н).
MS/ESI+ [МН]+: 328,19.
Стадия 5. Синтез (S)-3,5-дихлор-4-(2-(3,4-диметоксифенил)-2-гидроксиэтил)пиридин-1-оксида (1)
(S)-2-(3,5-Дихлорпиридин-4-ил)-1-(3,4-диметоксифенил)этанол (4 г; 12 ммоль) растворяли в этилацетате и в раствор добавляли м-хлорпербензойную (m-СРВ) кислоту. Смесь перемешивали при КТ в течение 5 ч. Образовавшееся твердое вещество собирали фильтрованием, промывали этилацетатом и сушили под вакуумом, получая 1,72 г указанного в заголовке соединения (выход 41%). Анализ с использованием хиральной HPLC: Rt=22,16 мин; элюент: гексан: изопропанол, 6:4. (с=0,253; метанол/CHCl3 1:1). MS/ESI+ [МН]+: 344,19.
1Н ЯМР (400 МГц, хлороформ-d] δ млн-1 8.15 (s, 2Н), 6.99 (m, 1Н), 6.79-6.88 (m, 2Н), 5.03 (dd, J=8,50; 5,32 Гц, 1Н), 3.75-3.98 (m, 6Н), 3.42 (dd, J=13,57; 8,56 Гц, 1Н), 3.19 (dd, J=13,51; 5,32 Гц, 1Н), 2.06-2.15 (m, 1Н).
Пример 2
Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоилокси)-2-(3,4-диметоксифенил)этил)пиридин-1-оксида (соединения 14)
Схема 2
Стадия 1. Синтез (S)-4-(2-(4-(N-(трет-бутоксикарбонил)-метилсульфонамидо)-3-(циклопропилметокси)бензоилокси)-2-(3,4-диметоксифенил)этил)-3,5-дихлорпиридин-1-оксида (15)
(S)-3,5-Дихлор-4-(2-(3,4-диметоксифенил)-2-гидроксиэтил)пиридин-1-оксид (734 мг; 2,13 ммоль) растворяли в DMF (5,5 мл). Добавляли 1-этил-3-(3-диметил-аминопропил)карбодиимид (EDAC) (840 мг; 4,36 ммоль), DMAP (390 мг; 3,2 ммоль) и соединение 9 (1,23 г; 3,2 ммоль). Смесь перемешивали при КТ в течение 1 ч, затем добавляли воду и водную фазу дважды экстрагировали AcOEt. Объединенную органическую фазу промывали 1 н. HCl, сушили над Na2SO4 и упаривали досуха. Неочищенное вещество растирали с н-гексаном, получая 1,87 г желаемого соединения (выход 90%). MS/ESI+ 710,15 [МН]+.
Стадия 2. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(метилсульфонамидо)бензоилокси)-2-(3,4-диметоксифенил)этил)-пиридин-1-оксида (16)
(S)-4-(2-(4-(N-(трет-Бутоксикарбонил)метилсульфонамидо)-3-(циклопропилметокси)бензоилокси)-2-(3,4-диметоксифенил)этил)-3,5-дихлорпиридин-1-оксид (240 мг; 0,34 ммоль) растворяли в DMF (4,5 мл) и раствор перемешивали при 100 градусах в течение 5 суток до полного завершения реакции. Затем смесь оставляли охлаждаться до КТ и добавляли воду. Водную фазу дважды экстрагировали EtOAc. Органическую фазу сушили над Na2SO4 и упаривали досуха. Неочищенное вещество растирали с Et2O, получая указанное в заголовке соединение (160 мг; выход 80%). MS/ESI+ 610,09 [МН]+.
1Н ЯМР (400 МГц, хлороформ-d) δ млн-1 8.15 (s, 2Н), 7.70 (dd, J=8,38; 1,65 Гц, 1Н), 7.59 (d, J=8,44 Гц, 1Н), 7.47 (d, J=1,59 Гц, 1Н), 7.21 (m, 1Н), 6.95-7.08 (m, 2Н), 6.87 (d, J=8,31 Гц, 1Н), 6.29 (dd, J=10,15; 4,28 Гц, 1Н), 3.82 и 4.02 (2s, 6Н, 3Н каждый), 3.72 (dd, J=14,00; 10,09 Гц, 1Н), 3.34 (dd, J=14,06; 4,28 Гц, 1Н), 3.06 (s, 3Н), 1.22-1.36 (m, 1Н), 0.60-0.77 (m, 2Н), 0.35 (q, J=5,01 Гц, 2Н).
Стадия 3. Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоилокси)-2-(3,4-диметоксифенил)этил)пиридин-1-оксида (14)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(метилсульфонамидо)-бензоилокси)-2-(3,4-диметоксифенил)этил)пиридин-1-оксид (40 мг; 0,065 ммоль) растворяли в DMF (1 мл). Добавляли K2CO3 (25 мг; 0,18 ммоль) и 4-(2-хлорэтил)морфолин (20 мг; 0,133 ммоль) и смесь перемешивали при 45 градусах в течение ночи. Затем реакционную смесь оставляли охлаждаться до КТ и добавляли воду. Водную фазу дважды экстрагировали AcOEt и органический слой сушили над Na2SO4. Растворитель выпаривали под вакуумом, получая неочищенный продукт, который очищали препаративной HPLC (метод 2) и кристаллизовали из смеси 1/1 петролейный эфир/диэтиловый эфир. Образование соли происходило после обработки смесью HCl/AcOEt, и получали гидрохлорид (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоилокси)-2-(3,4-диметоксифенил)этил)-пиридин-1-оксида (10 мг; 0,013 ммоль; выход 20%). MS/ESI+ 724,2 [МН]+.
1Н ЯМР (400 МГц, хлороформ-d) δ млн-1 8.16 (s, 2Н), 7.61-7.71 (m, 1Н), 7.53 (m, 1Н), 7.33-7.45 (m, 1Н), 6.92-7.06 (m, 2Н), 6.87 (d, J=8,38 Гц, 1Н), 6.22-6.32 (m, 1Н), 3.84-3.96 (m, 12Н), 3.65-3.78 (m, 1Н), 3.28-3.41 (m, 1Н), 3.00 (s, 3Н), 2.4-1.5 (m, 6Н), 1.25 (m, 1Н), 0.69 (d, J=7,94 Гц, 2Н), 0.37 (d, J=4,41 Гц, 2Н).
Соединения, перечисленные в Таблице 2, получали, используя стадии и методики синтеза, аналогичные описанным в Примере 2, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Карбоновую кислоту синтезировали, следуя методике, аналогичной для соединения 9 (WO 2010/089107 Пример 18, стадия 1-6).
Соединения, перечисленные в Таблице 3, получали, используя стадии и методики синтеза, аналогичные описанным в примере 2, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Ссылки на методики синтезов различных спиртов приведены в Таблице 1.
Карбоновую кислоту синтезировали, следуя той же методике, что и для соединения 9 (WO 2010/089107, пример 18, схема 2, стадия 4-6).
Пример 3
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(1,1-диоксотиоморфолинилметил)-бензоилокси)-этил)пиридин-1-оксида (соединения 37)
Схема 3
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксид (соединение 3; 40 мг; 0,095 ммоль) растворяли в DMF (1,5 мл). Добавляли EDAC (55 мг; 0,285 ммоль), DMAP (14 мг; 0,114 ммоль) и 1,1-диоксотиоморфолинилметил)-бензойную кислоту (39 мг; 0,143 ммоль). Смесь перемешивали при КТ в течение 1 ч, затем добавляли воду и водную фазу дважды экстрагировали AcOEt. Объединенную органическую фазу промывали 1 н. HCl, сушили над Na2SO4 и упаривали досуха, получая 40 мг желаемого соединения (выход 65%). MS/ESI+ 671,1 [МН]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.27 (s, 2Н), 8.05 (d, J=7,06 Гц, 2Н), 7.54 (d, J=7,94 Гц, 2Н), 7.31 (m, 1Н), 7.20 (q, J=8,38 Гц, 2Н), 6.92 (t, J=75,00 Гц, 1Н), 6.34 (dd, J=9,26; 4,41 Гц, 1Н), 3.98 (d, J=7,06 Гц, 2Н), 3.70-3.83 (m, 3Н), 3.41-3.50 (m, 1Н), 3.07 (d, J=3,97 Гц, 4Н), 2.99 (d, J=4,41 Гц, 4Н), 1.22-1.35 (m, 1Н), 1.11 (t, J=7,06 Гц, 1Н), 0.55-0.64 (m, 2Н), 0.33-0.42 (m, 2Н).
Соединения, перечисленные в Таблице 4, получали, используя стадии и методики синтеза, аналогичные описанным в примере 3, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 4
Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-гидрокси-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (соединения 42)
Схема 4
Стадия 1. Синтез метил-4-(бензилокси)-3-(метилсульфонамидо)-бензоата (47)
Метил-3-амино-4-(бензилокси)бензоат (1,7 г; 6,61 ммоль) растворяли в пиридине (5 мл), затем при 0°C добавляли метансульфонилхлорид (0,62 мл; 7,93 ммоль) и смесь перемешивали при КТ в течение 2 ч. Реакцию гасили, используя 1 н. HCl, и продукт экстрагировали этилацетатом. Органическую фазу промывали 1 н. HCl (2×30 мл) и рассолом, затем сушили над Na2SO4. Растворитель удаляли, получая 1,7 г желаемого промежуточного соединения (выход: 77%).
Стадия 2. Синтез метил-4-(бензилокси)-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензоата (46)
Метил-4-(бензилокси)-3-(метилсульфонамидо)бензоат (700 мг; 2,1 ммоль) растворяли в DMF (5 мл). Добавляли K2CO3 (580 мг; 4,2 ммоль) и 4-(2-хлорэтил)морфолин (628 мг; 4,2 ммоль). Смесь перемешивали при 60°C в течение 3 ч. Реакцию гасили водой и продукт экстрагировали этилацетатом. Органический слой промывали H2O (2х) и насыщенным раствором NaCl, сушили над Na2SO4 и упаривали под вакуумом, получая 750 мг желаемого соединения (выход 80%).
Стадия 3. Синтез 4-(бензилокси)-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензойной кислоты (45)
Метил-4-(бензилокси)-3-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоат (750 мг; 1,7 ммоль) растворяли в THF (10 мл). Добавляли 1 н. LiOH (1,5 мл) и полученную смесь перемешивали при КТ в течение 5 ч. рН подводили до нейтрального значения, добавляя 1 н. HCl. и затем летучие вещества удаляли под вакуумом, получая 650 мг неочищенного продукта.
Стадия 4. Синтез (S)-4-(2-(4-(бензилокси)-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (44)
Соединение 3 (200 мг; 0,5 ммоль) и 4-(бензилокси)-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензойную кислоту (652 мг; 1,5 ммоль) растворяли в DMF (5 мл), затем добавляли EDC (767 мг; 4 ммоль) и DMAP (122 мг; 1 ммоль). Смесь перемешивали при КТ в течение 24 ч, затем гасили путем добавления воды, и продукт экстрагировали этилацетатом. Органическую фазу промывали насыщенным раствором K2CO3 (2х), водой (2х) и рассолом, сушили над Na2SO4 и упаривали под вакуумом, получая 350 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.25 (s, 2Н), 8.00-8.14 (m, 2Н), 7.58 (d, J=7,06 Гц, 2Н), 7.27-7.48 (m, 5Н), 7.13-7.24 (m, 2Н), 6.69-6.91-7.11 (t, 1Н, CHF2), 6.32 (dd, J=9,70; 4,85 Гц, 1Н), 5.35 (s, 2Н), 3.91-4.05 (m, 2Н), 3.74 (dd, J=14,11; 9,70 Гц, 3Н), 3.33-3.54 (m, 5Н), 2.91 (s, 3Н), 2.19-2.50 (m, 6Н), 1.18-1.36 (m, 1Н), 0.54-0.66 (m, 2H), 0.39 (q, J=4,85 Гц, 2H).
MS/ESI+ 836,2 [MH]+.
Стадия 5. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-гидрокси-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (43)
(S)-4-(2-(4-(Бензилокси)-3-(N-(2-морфолиноэтил)-метилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (120 мг; 0,14 ммоль) растворяли в ацетоне (10 мл), затем добавляли 5%-ный Pd/Ba2SO4 (149 мг; 0,07 ммоль) и смесь гидрировали, встряхивая смесь в аппарате Парра (H2: 30 ф/кв. дюйм (207 кПа)) в течение 30 мин. Добавляли дополнительно 5%-ный Pd/Ba2SO4 (149 мг; 0,07 ммоль) и встряхивание продолжали в течение 30 мин. Катализатор отфильтровывали через набивку целита, и растворитель выпаривали под вакуумом. Неочищенный продукт очищали препаративной HPLC (метод 1), получая 50 мг указанного в заголовке соединения.
MS/ESI+ 712,15 [МН]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.22 (m, 1Н), 8.07 (d, J=2,21 Гц, 1Н), 7.98 (d, J=6,62 Гц, 2Н), 7.40 (d, J=6,62 Гц, 1Н), 7.28 (m, 1Н), 7.04-7.22 (m, 2Н), 6.65-7.04 (m, 2Н), 6.20-6.28 (m, 1Н), 3.95 (d, J=5,73 Гц, 2Н), 3.73 (t, J=4,41 Гц, 6Н), 3.48-3.60 (m, 1Н), 3.31-3.43 (m, 1Н), 3.04 (s, 3Н), 2.75-2.62 (m, 6Н), 1.19-1.37 (m, 1Н), 0.60 (d, J=7,06 Гц, 2Н), 0.37 (d, J=4,85 Гц, 2Н).
Стадия 6. Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-гидрокси-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (42)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-гидрокси-3-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоилокси)этил)-пиридин-1-оксид (50 мг; 0,07 ммоль) растворяли в этилацетате (1,5 мл) и добавляли 2 н. HCl/Et2O (100 мкл). Добавляли Et2O (5 мл) до тех пор, пока не образовывался обильный осадок. Указанное в заголовке соединение (35 мг) получали фильтрованием (выход 67%). MS/ESI+ 746,2 [МН]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 10.33-10.77 (m, bs Н), 8.31 (s, 2Н), 7.99-8.12 (m, 1Н), 7.79-7.98 (m, 1Н), 7.27-7.36 (m, 1Н), 7.05-7.27 (m, 3Н), 6.90 (t, J=75,00 Гц, 1Н), 6.20-6.38 (m, 1Н), 5.60-5.90 (m, bs Н), 3.85-4.41 (m, 8Н), 3.69-3.81 (m, 1Н), 3.22-3.63 (m, 7Н), 3.14 (s, 3Н), 1.16-1.39 (m, 1Н), 0.53-0.68 (m, 2Н), 0.29-0.48 (m, 2Н).
Соединения, перечисленные в Таблице 5, получали, используя стадии и методики синтеза, аналогичные описанным в примере 4, стадия 1-4, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами.
Пример 5
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-фтор-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (соединения 53)
Схема 5
Стадия 1. Получение метил-3-амино-4-фторбензоата (54)
К смеси 3-амино-4-фторбензойной кислоты (1 г; 6,45 ммоль) в MeOH (20 мл), по каплям добавляли конц. H2SO4 (0,687 мл; 12,89 ммоль) и реакционную смесь кипятили с обратным холодильником в течение 20 часов. После охлаждения до комнатной температуры растворитель выпаривали, и остаток распределяли между насыщ. водн. раствором NaHCO3 и этилацетатом; органическую фазу промывали рассолом, сушили над Na2SO4 и упаривали досуха, получая метил-3-амино-4-фторбензоат в виде коричневого твердого вещества (0,970 г; 5,73 ммоль; выход 89%; MS/ESI+ 170,0 [МН]+) (43).
Стадия 2. Получение метил-4-фтор-3-(метилсульфонамидо)-бензоата (55)
Раствор метил-3-амино-4-фторбензоата (0,970 г; 5,73 ммоль) в безводном пиридине (12 мл) охлаждали до 0°С и по каплям добавляли метансульфонилхлорид (0,577 мл; 7,45 ммоль). Полученную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 3 часов. Растворитель выпаривали, и остаток распределяли между DCM и насыщ. водн. раствором NaHCO3. Органический слой промывали рассолом и сушили над Na2SO4; растворитель выпаривали и остаток очищали флэш-хроматографией на колонке с силикагелем (этилацетат : петролейный эфир, 35:65), получая метил-4-фтор-3-(метилсульфонамидо)бензоат в виде беловатого порошка (0,400 г; 1,618 ммоль; выход 28,2%; MS/ESI+ 248,1 [МН]+).
Стадия 3. Получение метил-4-фтор-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоата (56)
К раствору метил-4-фтор-3-(метилсульфонамидо)бензоата (0,400 г; 1,618 ммоль) в безводном DMF (16,200 мл) в атмосфере N2 добавляли K2CO3 (0,492 г; 3,56 ммоль), затем гидрохлорид 4-(2-хлорэтил)морфолина (0,361 г; 1,941 ммоль). Полученную белую суспензию нагревали до 70°С в течение 1 часа, перемешивали при комнатной температуре в течение ночи и нагревали до 70°С в течение еще 3,5 часа. Добавляли воду (20 мл) и смесь экстрагировали несколько раз этиловым эфиром (25 мл × 5). Объединенные органические слои сушили над Na2SO4 и упаривали досуха. Остаток очищали флэш-хроматографией на колонке с силикагелем (этилацетат : петролейный эфир, 85:15), получая метил-4-фтор-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензоат в виде бесцветного масла (0,512 г; 1,421 ммоль; выход 88%; MS/ESI+ 361,0 [MH]+).
Стадия 4. Получение гидрохлорида 4-фтор-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензойной кислоты (57)
Метил-4-фтор-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензоат (0,504 г; 1,398 ммоль) растворяли в диоксане (14,000 мл) и добавляли водн. 6 н. HCl (1,398 мл; 8,39 ммоль). Смесь нагревали до 70°С в течение 24 часов. Добавляли дополнительное количество водн. 6 н. HCl (2,80 мл; 16,78 ммоль) в виде трех порций, нагревая до 100°С в течение 4 часов. Летучие вещества удаляли под вакуумом, получая гидрохлорид 4-фтор-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензойной кислоты в виде бледно-желтого твердого вещества (0,518 г; 1,353 ммоль; выход 97%; MS/ESI+ 347,0 [МН]+). Этот продукт использовали без какой-либо дополнительной очистки.
Стадия 5. Получение (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-фтор-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (53)
Гидрохлорид 4-фтор-3-(N-(2-морфолиноэтил)метилсульфонамидо)-бензойной кислоты (0,180 г; 0,470 ммоль) суспендировали в безводном DCM (13,100 мл); последовательно добавляли (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксид (0,165 г; 0,392 ммоль), EDC (0,225 г; 1,175 ммоль) и DMAP (0,096 г; 0,784 ммоль) и смесь перемешивали при комнатной температуре в течение 5 часов. Добавляли вторую порцию гидрохлорида 4-фтор-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензойной кислоты (0,030 г; 0,078 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Смесь разбавляли DCM (20 мл) и промывали 1 н. водн. раствором HCl (15 мл×3). Органическую фазу сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (DCM : MeOH, 97:3), получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-фтор-3-(N-(2-морфолиноэтил)метилсульфонамидо)бензоилокси)-этил)пиридин-1-оксид в виде белого пористого твердого вещества (0,202 г; 0,270 ммоль; выход 69%; MS/ESI+ 748,52 [МН]+, [αD]=-30,52, с=0,5; МеОН).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.53 (s, 2Н), 7.97-8.14 (m, 2Н), 7.49 (t, 1Н), 7.23 (d, 1Н), 7.20 (d, 1Н), 7.09 (dd, 1Н), 7.06 (t, 1Н), 6.19 (dd, 1Н), 3.95 (dd, 1Н), 3.90 (dd, 1Н), 3.66-3.81 (m, 2Н), 3.64 (dd, 1Н), 3.31-3.44 (m, 5Н), 3.13 (s, 3Н), 2.32-2.45 (m, 2Н), 2.11-2.31 (m, 4Н), 1.05-1.39 (m, 1Н), 0.46-0.67 (m, 2Н), 0.20-0.44 (m, 2Н).
Соединения, перечисленные в Таблице 6, получали, используя стадии и методики синтеза, аналогичные описанным в примере 5, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами.
Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 6
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(5-(N-(циклопропилметил)-метилсульфонамидо)-2-(2-морфолиноэтокси)бензоилокси)этил)-пиридин-1-оксида (62)
Схема 6
Стадия 1. Синтез метил-5-амино-2-гидроксибензоата (63)
5-Амино-2-гидроксибензойную кислоту (10 г; 65,3 ммоль) суспендировали в МеОН (150 мл) и по каплям добавляли 96%-ную серную кислоту (12 мл; 225 ммоль). Смесь нагревали при температуре дефлегмации в течение 96 ч, затем охлаждали до КТ; часть растворителя выпаривали (оставляли 90 мл) и добавляли 5%-ный раствор NaHCO3 (щелочной рН). Смесь экстрагировали AcOEt. Объединенные органические слои промывали рассолом, сушили над Na2SO4 и упаривали. Желаемый продукт получали в виде твердого вещества (9,68 г; выход 89%) и использовали в следующей реакции без дополнительной очистки.
MS/ESI+ 168 [МН]+.
Стадия 2. Синтез метил-2-гидрокси-5-(метилсульфонамидо)-бензоата (64)
Метил-5-амино-2-гидроксибензоат (9,58 г; 57,3 ммоль) растворяли в DCM (150 мл). Добавляли пиридин (9,27 мл; 115 ммоль) и метансульфонилхлорид (4,47 мл; 57,3 ммоль). Реакционную смесь перемешивали при КТ в течение 4 ч и затем добавляли воду (50 мл) и 6 М HCl (15 мл). Начинало кристаллизоваться розовое твердое вещество. Это твердое вещество извлекали фильтрованием и промывали водой. Указанное в заголовке соединение получали в виде розового твердого вещества (13 г; выход 92%) и использовали в следующей реакции без дополнительной очистки.
MS/ESI+ 246 [MH]+.
Стадия 3. Синтез метил-5-(N-(циклопропилметил)-метилсульфонамидо)-2-гидроксибензоата (65)
Метил-2-гидрокси-5-(метилсульфонамидо)бензоат (5,565 г; 22,69 ммоль) растворяли в ацетонитриле (250 мл). Добавляли бромметил-циклопропан (4,59 г; 34 ммоль) и карбонат калия (6,27 г; 45,4 ммоль) и смесь перемешивали при КТ в течение 4 суток. Реакционную смесь выливали в ледяную воду (200 мл) и добавляли 36%-ный HCl до рН 1. Затем смесь экстрагировали AcOEt, органический слой сушили над Na2SO4 и растворитель выпаривали. Полученный неочищенный продукт очищали флэш-хроматографией на силикагеле (петролейный эфир : AcOEt, 4:1), получая 4,75 г желаемого продукта (выход 70%).
MS/ESI+ 300 [МН]+.
Стадия 4. Синтез метил-5-(N-(циклопропилметил)-метилсульфонамидо)-2-(2-морфолиноэтокси)бензоата (66)
Смесь метил-5-(N-(циклопропилметил)метилсульфонамидо)-2-гидроксибензоата (200 мг; 0,668 ммоль), гидрохлорида 4-(2-хлорэтил)морфолина (149 мг; 0,802 ммоль) и K2CO3 (231 мг; 1,670 ммоль) в 10 мл DMF перемешивали в течение 4 ч при 80°С. Смесь выливали в воду и дважды экстрагировали AcOEt, затем экстракт промывали рассолом, сушили и упаривали, получая желаемый продукт (259 мг; выход 94%), который использовали на следующей стадии без дополнительной очистки.
MS/ESI+ 413,0 [МН]+.
Стадия 5. Синтез гидрохлорида 5-(N-(циклопропилметил)метилсульфонамидо)-2-(2-морфолиноэтокси)-бензойной кислоты (67)
Смесь метил-5-(N-(циклопропилметил)метилсульфонамидо)-2-(2-морфолиноэтокси)бензоата (260 мг; 0,630 ммоль) и конц. HCl (1,5 мл; 18,00 ммоль) в 3 мл диоксана нагревали при 100°С в течение 1 ч, используя облучение микроволнами. Смесь упаривали, получая указанное в заголовке соединение (303 мг; количественный выход), которое использовали на следующей стадии без дополнительной очистки.
MS/ESI+ 434,9 [МН]+.
Стадия 6. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(5-(N-(циклопропилметил)-метилсульфонамидо)-2-(2-морфолиноэтокси)бензоилокси)этил)-пиридин-1-оксида (62)
Смесь гидрохлорида 5-(N-(циклопропилметил)метилсульфонамидо)-2-(2-морфолиноэтокси)бензойной кислоты (303 мг; 0,627 ммоль), соединения 3 (220 мг; 0,522 ммоль), DMAP (128 мг; 1,045 ммоль) и EDC (250 мг; 1,306 ммоль) в 25 мл безводного DCM перемешивали в течение ночи при КТ. Смесь промывали разбавленной HCl и рассолом, затем сушили и упаривали. Неочищенный продукт очищали препаративной HPLC; фракции, содержащие продукт, подщелачивали, используя NaHCO3, и экстрагировали AcOEt, затем промывали рассолом, сушили и упаривали, получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(5-(N-(циклопропилметил)метилсульфонамидо)-2-(2-морфолиноэтокси)-бензоилокси)этил)пиридин-1-оксид (31 мг; выход 7,41%).
MS/ESI+ 800,27 [МН]+,
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.53 (s, 2Н), 7.64 (d, 1Н), 7.58 (dd, 1Н), 7.21 (d, 1Н), 7.20 (d, 1Н), 7.16 (d, 1Н), 7.06 (dd, 1Н), 7.06 (t, 1Н), 6.17 (dd, 1Н), 4.15 (t, 2Н), 3.93 (dd, 1Н), 3.87 (dd, 1Н), 3.56 (dd, 1Н), 3.49-3.53 (m, 4Н), 3.47 (d, 2Н), 3.32 (dd, 1Н), 2.97 (s, 3Н), 2.56-2.69 (m, 2Н), 2.33-2.45 (m, 4Н), 1.11-1.23 (m, 1Н), 0.72-0.92 (m, 1Н), 0.48-0.63 (m, 2Н), 0.25-0.47 (m, 4Н), -0.07-0.19 (m, 2Н).
MS/ESI+ 800,27 [МН]+.
Пример 7
Синтез трифторацетата (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)бензоилокси)этил)-пиридин-1-оксида (68)
Схема 7
Стадия 1. Получение метил-3-амино-4-метоксибензоата (69)
Смесь 3-амино-4-метоксибензойной кислоты (2,00 г; 11,96 ммоль) и серной кислоты (1,275 мл; 23,93 ммоль) в МеОН (25 мл) нагревали до температуры дефлегмации в течение 24 часов. После охлаждения до комнатной температуры растворитель удаляли под вакуумом, и остаток распределяли между насыщ. водн. раствором NaHCO3 и этилацетатом Органический слой сушили над Na2SO4 и упаривали досуха, получая метил-3-амино-4-метоксибензоат в виде беловатого порошка (2,00 г; 11;04 ммоль; выход 92%; MS/ESI+ 182,1 [МН]+).
Стадия 2. Получение метил-4-метокси-3-(метилсульфонамидо)бензоата (70)
Раствор метил-3-амино-4-метоксибензоата (2,00 г; 11,04 ммоль) в безводном пиридине (25 мл) охлаждали до 0°С и по каплям добавляли метансульфонилхлорид (1,115 мл; 14,35 ммоль). Реакционную смесь оставляли нагреваться до комнатной температуры и перемешивали в течение 3 часов. Растворитель выпаривали досуха и остаток распределяли между DCM и 2 н. водн. раствором HCl; органический слой промывали рассолом, сушили над Na2SO4 и растворитель удаляли под вакуумом. Остаток растирали с iPr2O и полученное твердое вещество собирали фильтрованием, получая метил-4-метокси-3-(метилсульфонамидо)бензоат в виде беловатого порошка (2,6 г; 10,03 ммоль; выход 91%; MS/ESI+ 260,1 [МН]+).
Стадия 3. Получение метил-3-(N-(2-гидроксиэтил)-метилсульфонамидо)-4-метоксибензоата (71)
Смесь метил-4-метокси-3-(метилсульфонамидо)бензоата (0,300 г; 1,157 ммоль), 2-бромэтанола (0,434 г; 3,47 ммоль) и K2CO3 (0,320 г; 2,314 ммоль) в ацетонитриле (5 мл) нагревали, используя облучение микроволнами, при 110°С в течение 5 часов. Растворитель выпаривали, и остаток обрабатывали этилацетатом. Неорганические соли отфильтровывали и фильтрат упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (петролейный эфир : этилацетат, 1:9), получая метил-3-(N-(2-гидроксиэтил)-метилсульфонамидо)-4-метоксибензоат в виде светло-коричневого масла (0,200 г; 0,659 ммоль; выход 57,0%; MS/ESI+ 326,3 [MNa]+).
Стадия 4. Получение метил-3-(N-(2-бромэтил)-метилсульфонамидо)-4-метоксибензоата (72)
К раствору метил-3-(N-(2-гидроксиэтил)метилсульфонамидо)-4-метоксибензоата (0,200 г; 0,659 ммоль) и трифенилфосфина (0,173 г; 0,659 ммоль) в безводном DCM (3 мл), порциями при комнатной температуре добавляли CBr4 (219 мг; 0,659 ммоль) в атмосфере азота и смесь перемешивали в течение 30 минут. Растворитель удаляли под вакуумом и остаток очищали флэш-хроматографией на колонке с силикагелем (этилацетат : петролейный эфир, 9:1), получая метил-3-(N-(2-бромэтил)метилсульфонамидо)-4-метоксибензоат в виде белого твердого вещества (0,150 г; 0,410 ммоль; выход 62,1%; MS/ESI+ 365,9-367,9 [МН]+).
Стадия 5. Получение метил-4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)бензоата (73)
Смесь метил-3-(N-(2-бромэтил)метилсульфонамидо)-4-метоксибензоата (0,150 г; 0,410 ммоль), 1-метилпиперазина (0,041 г; 0,410 ммоль) и K2CO3 (0,085 г; 0,614 ммоль) в ацетонитриле (3 мл) нагревали, используя облучение микроволнами, при 130°С в течение 3 часов. Нерастворимый остаток отфильтровывали, и фильтрат упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (DCM : MeOH: 32%-ный водн. NH4OH, 95:5:0,5), получая метил-4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)-бензоат в виде светло-коричневого масла (0,140 г; 0,363 ммоль; выход 89%; MS/ESI+ 386,4 [МН]+).
Стадия 6. Получение трифторацетата (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)бензоилокси)этил)-пиридин-1-оксида (68)
К раствору метил-4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)бензоата (0,140 г; 0,363 ммоль) в THF (5 мл), добавляли раствор LiOH*H2O (0,183 г; 0,436 ммоль) в воде (0,5 мл) и смесь перемешивали при комнатной температуре в течение 24 часов. Растворитель выпаривали под вакуумом. Сухое твердое неочищенное вещество суспендировали в смеси 1/1 DCM/DMF, содержащей EDC (0,209 г; 1,089 ммоль), (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксид (0,137 г; 0,327 ммоль) и DMAP (0,44 г; 0,363 ммоль), и полученный раствор перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали, и остаток распределяли между этилацетатом и насыщ. водн. раствором NaHCO3. Органическую фазу промывали рассолом и сушили над Na2SO4; растворитель удаляли под вакуумом и остаток очищали флэш-хроматографией на колонке с силикагелем (DCM : МеОН : 32%-ный водн. NH4OH, 95:5:0,5), получая 0,150 г желаемого продукта. Потребовалась дополнительная очистка препаративной HPLC (метод 3), чтобы получить (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)бензоилокси)этил)-пиридин-1-оксид в виде трифторацетатной соли (белый порошок) (0,068 г; 0,077 ммоль, выход 21,10%; чистота по LC-MS (BPI): 99,2%; MS/ESI+ 773,36 [МН]+, [αD]=-30,48, с=0,5; DCM).
Пример 8
Синтез (3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(N-(3-((2S,5R)-2,5-диметилпиперазин-1-ил)пропил)метилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (74)
Схема 8
Стадия 1. Синтез (S)-4-(2-(4-(N-(3-бромпропил)метилсульфонамидо)-3-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)-3,5-дихлорпиридин-1-оксида (75)
К раствору (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(циклопропилметокси)-4-(метилсульфонамидо)-бензоилокси)этил)пиридин-1-оксида (соед. 7; 1 г; 1,5 ммоль), растворенного в DMF (10 мл), добавляли 1,3-дибромпропан (1,52 мл; 15 ммоль) и K2CO3 (414 мг; 3 ммоль) и смесь перемешивали при 40°С в течение 6 ч. Реакционную смесь разбавляли водой и затем экстрагировали этилацетатом. Органическую фазу промывали водой (3×30 мл), сушили над Na2SO4 и упаривали досуха. Твердое вещество растирали с петролейным эфиром и отфильтровывали, получая 700 мг желаемого продукта (выход: 58%).
MS/ESI+ 808,51 [МН]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.28 (s, 2Н), 7.68 (dd, J=7,94; 1,76 Гц, 1Н), 7.63 (d, J=1,76 Гц, 1Н), 7.44 (d, J=8,38 Гц, 1Н), 7.32 (d, J=1,76 Гц, 1Н), 7.15-7.25 (m, 2Н), 6.92 (t, J=75,00 Гц, 1Н), 6.31 (dd, J=9,92; 4,63 Гц, 1Н), 4.07 (d, J=7,06 Гц, 2Н), 3.99 (d, J=7,06 Гц, 2Н), 3.86 (t, J=6,62 Гц, 2Н), 3.77 (dd, J=14,33; 9,92 Гц, 1Н), 3.56 (t, J=6,62 Гц, 2Н), 3.44 (dd, J=14,11; 4,41 Гц, 1Н), 3.09 (s, 3Н), 1.96-2.03 (m, 2Н), 1.34-1.46 (m, 1Н), 1.21-1.33 (m, 1Н), 0.64-0.75 (m, 2Н), 0.54-0.63 (m, 2Н), 0.42-0.51 (m, 2Н), 0.34-0.41 (m, 2Н).
Стадия 2. Синтез 4-((S)-2-(4-(N-(3-((2S,5R)-4-(трет-бутоксикарбонил)-2,5-диметилпиперазин-1-ил)пропил)-метилсульфонамидо)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (76)
К раствору (S)-4-(2-(4-(N-(3-бромпропил)метилсульфонамидо)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (200 мг; 0,21 ммоль) в DMF (4 мл) добавляли (2R,5S)-трет-бутил-2,5-диметилпиперазин-1-карбоксилат (135 мг; 0,63 ммоль) и K2CO3 (58 мг; 0,42 ммоль) и смесь перемешивали при КТ в течение ночи. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органическую фазу промывали водой, сушили над Na2SO4 и упаривали досуха, получая 250 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 3. Синтез 3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(N-(3-((2S,5R)-2,5-диметилпиперазин-1-ил)пропил)метилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)пиридин-1-оксида (74)
4-((S)-2-(4-(N-(3-((2S,5R)-4-(трет-Бутоксикарбонил)-2,5-диметилпиперазин-1-ил)пропил)метилсульфонамидо)-3-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (250 мг; 0,26 ммоль) растворяли в смеси 4 М HCl/диоксан и реакционную смесь перемешивали при КТ в течение 6 ч. Растворитель выпаривали под вакуумом, и остаток распределяли между насыщенным раствором NaHCO3 и этилацетатом. Органическую фазу сушили над Na2SO4 и упаривали под вакуумом. Полученный неочищенный продукт очищали полупрепаративной HPLC, получая 150 мг конечного соединения (выход: 68%).
MS/ESI+ 841,8 [МН]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.23 (s, 2Н), 7.67 (d, J=7,94 Гц, 1Н), 7.61 (d, J=1,32 Гц, 1Н), 7.40 (d, J=7,94 Гц, 1Н), 7.32 (d, J=1,32 Гц, 1Н), 7.13-7.24 (m, 2Н), 6.91 (t, J=75,00 Гц, 1Н), 6.31 (dd, J=9,70; 4,41 Гц, 1Н), 4.05 (d, J=7,06 Гц, 2Н), 3.98 (d, J=6,62 Гц, 2Н), 3.65-3.87 (m, 4Н), 3.43 (dd, J=14,11; 4,41 Гц, 2Н), 2.93-3.07 (d, 3Н), 2.79 (d, J=12,79 Гц, 2Н), 2.39 (m, 1Н), 2.10 (s, 3Н), 1.72-1.84 (m, 1H), 1.57 (m, 2H), 1.32-1.47 (m, 1H), 1.21-1.31 (m, 1H), 1.11 (dd, J=6,84; 4,19 Гц, 1H), 1.01 (d, J=6,62 Гц, 1H), 0.91 (d, J=5,73 Гц, 3H), 0.64-0.73 (m, 2H), 0.55-0.63 (m, 2H), 0.45 (d, J=4,41 Гц, 2H), 0.37 (d, J=5,73 Гц, 2H).
Соединения, перечисленные в Таблице 7, получали, используя стадии и методики синтеза, аналогичные описанным в примере 8, схема 8, стадия 1-2, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 9
Синтез 2,2,2-трифторацетата (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(2-гидрокси-4-(N-(2-(морфолин-4-ий)этил)метилсульфонамидо)бензоилокси)этил)-пиридин-1-оксида (соединения 81)
Схема 9
Стадия 1. Получение метил-2-гидрокси-4-нитробензоата (82)
К раствору 2-гидрокси-4-нитробензойной кислоты (3 г; 16,38 ммоль) в МеОН (150 мл), охлажденному до 0°С (в бане с ледяной водой), по каплям добавляли концентрированную серную кислоту (15 мл). Реакционную смесь нагревали до комнатной температуры, затем нагревали при 80°С в течение 16 ч. MeOH частично удаляли под вакуумом и в смесь добавляли воду. Бледно-желтый осадок, который образовывался, отфильтровывали и промывали большим количеством воды. После сушки получали метил-2-гидрокси-4-нитробензоат в виде бледно-желтого твердого вещества (3,03 г; 15,37 ммоль; выход 94%; чистота по UPLC-MS: 98%; MS/ESI+, [МН]+ не детектируется).
Стадия 2. Получение метил-4-амино-2-гидроксибензоата (83)
К суспензии 10%-ного Pd/C (100 мг) в МеОН (40 мл) в сосуде Парра емкостью 500 мл добавляли метил-2-гидрокси-4-нитробензоат (1,3 г; 6,59 ммоль). Реакционную смесь встряхивали в атмосфере Н2 (30 ф/кв. дюйм (207 кПа)) в течение 1 ч. Катализатор отфильтровывали через набивку целита и маточные жидкости упаривали под вакуумом. Получали метил-4-амино-2-гидроксибензоат в виде желтого твердого вещества (1,08 г; 6,46 ммоль; выход 98%, Чистота по UPLC-MS: 100%; MS/ESI+ 167,9 [MH]+).
Стадия 3. Получение метил-2-гидрокси-4-(метилсульфонамидо)-бензоата (84)
К раствору метил-4-амино-2-гидроксибензоата (1,08 г; 6,46 ммоль) в DCM (100 мл) добавляли пиридин (1,043 мл; 12,92 ммоль) и метансульфонилхлорид (0,600 мл; 7,75 ммоль) при комнатной температуре. Реакционную смесь перемешивали при этой же температуре в течение 48 ч. К смеси добавляли 2 н. HCl, органическую фазу отделяли, сушили (сульфат натрия), фильтровали и упаривали под вакуумом. Получали метил-2-гидрокси-4-(метилсульфонамидо)бензоат в виде розового твердого вещества (0,87 г; 3,55 ммоль; выход 54,9%; чистота по UPLC-MS: 95%; MS/ESI+ 245,8; 167,9 [МН]+) и использовали в том виде, как есть, в следующей реакции без дополнительной очистки.
Стадия 4. Получение метил-2-гидрокси-4-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоата (85)
К раствору метил-2-гидрокси-4-(метилсульфонамидо)бензоата (0,435 г; 1,774 ммоль) в CH3CN (50 мл) добавляли K2CO3 (0,368 г; 2,66 ммоль) при комнатной температуре. Реакционную смесь перемешивали при этой же температуре в течение 10 мин, затем добавляли гидрохлорид 4-(2-хлорэтил)морфолина (0,330 г; 1,774 ммоль) в виде одной порции. Суспензию перемешивали при 80°С в течение ночи. CH3CN удаляли под вакуумом и оставшееся неочищенное вещество распределяли между насыщенным водным раствором NH4Cl и DCM. Органическую фазу отделяли и водную фазу нейтрализовали и экстрагировали DCM. Объединенные органические экстракты сушили (сульфат натрия), фильтровали и упаривали под вакуумом. После очистки флэш-хроматографией на силикагеле (DCM : MeOH, 95:5) получали метил-2-гидрокси-4-(N-(2-морфолиноэтил)метилсульфонамидо)бензоат в виде бледно-желтого масла (0,21 г; 0,586 ммоль; выход 33,0%; чистота по UPLC-MS: 95%; MS/ESI+ 358,9 [MH]+).
Стадия 5. Получение 2,2,2-трифторацетата 4-(2-(N-(4-карбокси-3-гидроксифенил)метилсульфонамидо)этил)морфолин-4-ия (86)
К раствору метил-2-гидрокси-4-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоата (0,21 г; 0,586 ммоль) в смеси THF : MeOH (4:1) (20 мл) добавляли 1М гидроксид лития (1,172 мл; 1,172 ммоль). Реакционную смесь перемешивали при 80°С в течение 16 ч. Растворители выпаривали под вакуумом. После очистки обращенно-фазовой препаративной HPLC получали 2,2,2-трифторацетат 4-(2-(N-(4-карбокси-3-гидроксифенил)-метилсульфонамидо)этил)морфолин-4-ия в виде белого твердого вещества (0,1 г; 0,218 ммоль; выход 37,2%; чистота по UPLC-MS: 100%; MS/ESI+ 345,0 [МН]+).
Стадия 6. Получение 2,2,2-трифторацетата (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(2-гидрокси-4-(N-(2-(морфолин-4-ий)этил)метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (81)
К раствору 2,2,2-трифторацетата 4-(2-(N-(4-карбокси-3-гидроксифенил)-метилсульфонамидо)-этил)морфолин-4-ия (0,1 г; 0,218 ммоль) в DCM (10 мл) добавляли соединение 3 (0,092 г; 0,218 ммоль), EDC (0,042 г; 0,218 ммоль) и DMAP (0,053 г; 0,436 ммоль) при комнатной температуре. Реакционную смесь перемешивали при этой же температуре в течение ночи. К реакционной смеси добавляли 2 н. HCl, органическую фазу отделяли, сушили (сульфат натрия), фильтровали и упаривали под вакуумом. Полученный неочищенный продукт очищали обращенно-фазовой препаративной HPLC. Получали 2,2,2-трифторацетат (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(2-гидрокси-4-(N-(2-(морфолин-4-ий)этил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида в виде беловатого твердого вещества (0,032 г; 0,037 ммоль; выход 17,04%; Чистота по LC-MS: 100%; MS/ESI+ 746,22 [МН]+, [αD]=-37,84, с=0,5; МеОН).
Соединения, перечисленные в Таблице 8, получали, используя стадии и методики синтеза, аналогичные описанным в примере 9, схема 9, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами.
Пример 10
Получение (S)-3,5-дихлор-4-(2-(2-(циклопропилметокси)-4-(N-(2-(морфолин-4-ий)этил)метилсульфонамидо)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (соединения 91)
Схема 10
Стадия 1. Получение метил-2-(циклопропилметокси)-4-нитробензоата (92)
К раствору метил-2-гидрокси-4-нитробензоата (0,5 г; 2,54 ммоль) в CH3CN (30 мл) добавляли K2CO3 (0,701 г; 5,07 ммоль) при комнатной температуре. Реакционную смесь перемешивали при этой же температуре в течение 15 минут, затем добавляли (бромметил)циклопропан (0,372 мл; 3,80 ммоль). Реакционную смесь нагревали до 80°С и перемешивали в течение 48 ч. Растворитель удаляли под вакуумом и неочищенный продукт распределяли между насыщенным раствором NH4Cl и DCM. Органическую фазу отделяли, сушили (сульфат натрия), фильтровали и упаривали под вакуумом. Получали метил-2-(циклопропилметокси)-4-нитробензоат в виде бледно-желтого твердого вещества (0,49 г; 1,950 ммоль; выход 77%; MS/ESI+, [МН]+ не детектируется) и использовали на следующей стадии без дополнительной очистки.
Стадия 2. Получение метил-4-амино-2-(циклопропилметокси)-бензоата(93)
К суспензии 10%-ного Pd/C (0,05 г; 2,070 ммоль) в MeOH (40 мл) в сосуде Парра емкостью 250 мл добавляли метил-2-(циклопропилметокси)-4-нитробензоат (0,49 г; 1,950 ммоль). Реакционную смесь встряхивали в атмосфере водорода (30 ф/кв. дюйм (207 кПа)) в течение 1 ч. Катализатор удаляли фильтрованием и раствор упаривали под вакуумом. Получали метил-4-амино-2-(циклопропилметокси)бензоат в виде бесцветного масла (0,27 г; 1,220 ммоль; выход 62,6%; MS/ESI+ 221,9; 243,9 [МН]+) и использовали на следующей стадии без дополнительной очистки.
Стадия 3. Получение метил-2-(циклопропилметокси)-4-(метилсульфонамидо)бензоата (94)
К раствору метил-4-амино-2-(циклопропилметокси)бензоата (0,27 г; 1,220 ммоль) в DCM (20 мл) добавляли пиридин (0,197 мл; 2,441 ммоль) и метансульфонилхлорид (0,113 мл; 1,464 ммоль) при комнатной температуре. Реакционную смесь перемешивали при этой же температуре в атмосфере азота в течение 3 суток. К смеси добавляли 2 н. HCl, органическую фазу отделяли, сушили (сульфат натрия), фильтровали и упаривали досуха. Получали метил-2-(циклопропилметокси)-4-(метилсульфонамидо)бензоат в виде бледно-желтого масла (0,35 г; 1,169 ммоль; выход 96%; MS/ESI+ 300,0 [МН]+) и использовали на следующей стадии без дополнительной очистки.
Стадия 4. Получение метил-2-(циклопропилметокси)-4-(N-(2-морфолиноэтил)метилсульфонамидо)бензоата (95)
К раствору метил-2-(циклопропилметокси)-4-(метилсульфонамидо)-бензоата (0,35 г; 1,169 ммоль) в CH3CN (20 мл) при комнатной температуре добавляли K2CO3 (0,323 г; 2,338 ммоль) и полученную таким образом суспензию перемешивали при этой же температуре в течение 10 минут. Добавляли гидрохлорид 4-(2-хлорэтил)морфолина (0,326 г; 1,754 ммоль) и смесь нагревали при 80°С в течение 20 ч. Растворитель удаляли при пониженном давлении и неочищенное соединение распределяли между водой и DCM. Органический слой отделяли, сушили (сульфат натрия), фильтровали и упаривали досуха. Получали метил-2-(циклопропилметокси)-4-(N-(2-морфолиноэтил)-метилсульфонамидо)-бензоат в виде бледно-желтого масла (0,42 г; 1,018 ммоль; выход 87%; MS/ESI+ 412,9 [МН]+) и использовали на следующей стадии без дополнительной очистки.
Стадия 5. Получение 2,2,2-трифторацетата 4-(2-(N-(4-карбокси-3-(циклопропилметокси)фенил)-метилсульфонамидо)этил)морфолин-4-ия (96)
К раствору метил-2-(циклопропилметокси)-4-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоата (0,42 г; 1,018 ммоль) в THF (30 мл) добавляли 1М раствор гидроксида лития (2,036 мл; 2,036 ммоль). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Растворители удаляли под вакуумом и оставшееся неочищенное вещество очищали обращенно-фазовой препаративной HPLC. Получали 2,2,2-трифторацетат 4-(2-(N-(4-карбокси-3-(циклопропилметокси)фенил)-метилсульфонамидо)этил)морфолин-4-ия в виде бесцветного вязкого масла (0,19 г; 0,371 ммоль; выход 36,4%; MS/ESI+ 398,9 [МН]+).
Стадия 6. Получение (S)-3,5-дихлор-4-(2-(2-(циклопропилметокси)-4-(N-(2-(морфолин-4-ий)этил)метилсульфонамидо)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (91)
К раствору 2,2,2-трифторацетата 4-(2-(N-(4-карбокси-3-(циклопропилметокси)фенил)-метилсульфонамидо)этил)морфолин-4-ия (0,19 г; 0,371 ммоль) в DCM (20 мл) при комнатной температуре добавляли (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксид (0,171 г; 0,408 ммоль), EDC (0,071 г; 0,371 ммоль) и DMAP (0,091 г; 0,741 ммоль). Реакционную смесь перемешивали при этой же температуре в течение 16 ч. Добавляли 2 н. HCl, органическую фазу отделяли, сушили (сульфат натрия), фильтровали и упаривали под вакуумом. Неочищенный продукт очищали препаративной HPLC (метод 1). Получали 2,2,2-трифторацетат (S)-3,5-дихлор-4-(2-(2-(циклопропилметокси)-4-(N-(2-(морфолин-4-ий)этил)-метилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-пиридин-1-оксида в виде беловатого твердого вещества (0,04 г; 0,044 ммоль; выход 11,80%; MS/ESI+ 800,23 [МН]+, [αD]=-8,8; с=0,5; MeOH).
Соединения, перечисленные в Таблице 9, получали, используя стадии и методики синтеза, аналогичные описанным в примере 10, схема 1, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами.
Пример 11
Синтез (S)-4-(2-(3-(2-(бис(2-гидроксиэтил)амино)этилсульфонилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (99)
Схема 11
Стадия 1. Синтез (S)-1-трет-бутил-2-(5-формил-2-метоксифенил)пирролидин-1,2-дикарбоксилата (105)
3-Гидрокси-4-метоксибензальдегид (200 мг; 1,315 ммоль) растворяли в DMF (5 мл), затем добавляли (S)-1-(трет-бутоксикарбонил)пирролидин-2-карбоновую кислоту (290 мг; 1,347 ммоль) и DMAP (50 мг; 0,410 ммоль). Реакционную смесь подвергали обработке ультразвуком в течение 30 мин и перемешивали в течение примерно 2 ч при КТ. По окончании этого времени реакционную смесь разбавляли, используя K2CO3 (50 мл), и экстрагировали диизопропиловым эфиром (50 мл). Органический экстракт промывали конц. раствором K2CO3 (6×50 мл). Раствор сушили над Na2SO4 и растворитель удаляли при пониженном давлении, получая 400 мг желаемого продукта (выход 87%).
Стадия 2. Синтез (S)-3-(1-(трет-бутоксикарбонил)пирролидин-2-карбонилокси)-4-метоксибензойной кислоты (104)
(S)-1-трет-Бутил-2-(5-формил-2-метоксифенил)пирролидин-1,2-дикарбоксилат (380 мг; 1,088 ммоль) растворяли в уксусной кислоте и охлаждали до 0°С, используя ледяную баню. Добавляли сульфаминовую кислоту (106 мг; 1,088 ммоль), затем по каплям добавляли хлорит натрия (180 мг; 1,990 ммоль), предварительно растворенный в воде (0,5 мл). Реакционную смесь перемешивали при КТ в течение ночи, разбавляли водой (30 мл) и экстрагировали этилацетатом (40 мл). Растворитель удаляли при пониженном давлении и маслянистый остаток растирали с использованием системы растворителей хлороформ:гексан (10:90), получая белое твердое вещество. Твердое вещество отфильтровывали и промывали водой (100 мл), после чего сушили в вакуумном сушильном шкафу в течение ночи, получая 300 мг указанного в заголовке соединения (выход 75%).
Стадия 3. Синтез 4-((S)-2-(3-((S)-1-(трет-бутоксикарбонил)пирролидин-2-карбонилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (103)
В результате сочетания соединения 3 с (S)-3-(1-(трет-бутоксикарбонил)пирролидин-2-карбонилокси)-4-метоксибензойной кислотой в тех же условиях и в соответствии с методикой эксперимента, показанной в примере 4, на схеме 4, на стадии 4, получали соответствующее сложноэфирное производное с количественным выходом.
Стадия 4. Синтез гидрохлорида 3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-((S)-пирролидин-2-карбонилокси)бензоилокси)этил)пиридин-1-оксида (102)
4-((S)-2-(3-((S)-1-(трет-Бутоксикарбонил)пирролидин-2-карбонилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (620 мг; 0,808 ммоль) растворяли в HCl/AcOEt 4 М (2,0 мл) и перемешивали в течение 2 ч при КТ. Растворитель удаляли при пониженном давлении, получая неочищенный продукт, который перекристаллизовывали из смеси AcOEt : гексан (1:2). Твердое вещество отфильтровывали, получая указанное в заголовке соединение (480 мг; выход 89%). MS/ESI+ 667,1 [МН]+.
1Н ЯМР (400 МГц, хлороформ-d) δ млн-1 8.29 (s, 2Н), 7.90 (d, J=9,00 Гц, 1Н), 7.73 (m, 1Н), 7.12-7.23 (m, 1Н), 6.93-7.10 (m, 3Н), 6.39-6.85 (m, 1Н, CHF2), 6.20 (dd, J=9,78; 3,91 Гц, 1Н), 4.83 (br. s., 1Н), 3.77-3.96 (m, 5Н), 3.53-3.76 (m, 2Н), 3.34 (d, J=11,35 Гц, 1Н), 1.80-2.70 (m, 6Н), 1.27 (d, J=4,30 Гц, 1Н), 0.58-0.75 (m, 2H), 0.37 (q, J=5,09 Гц, 2H).
Стадия 5. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-гидрокси-4-метоксибензоилокси)этил)-пиридин-1-оксида (101)
Гидрохлорид 3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-((S)-пирролидин-2-карбонилокси)-бензоилокси)этил)пиридин-1-оксида (150,0 мг; 0,2 ммоль) растворяли в MeOH (2,0 мл), затем добавляли насыщ. раствор NaHCO3 (2,0 мл). Раствор перемешивали при КТ в течение 5 ч. MeOH выпаривали под вакуумом и водную фазу подкисляли 1 М HCl (50 мл) и затем экстрагировали AcOEt (50 мл; х3). Органический экстракт сушили над Na2SO4 (1,0 г) и растворитель удаляли при пониженном давлении, получая 100,0 мг желаемого продукта в виде белого порошка (выход 78,0%).
MS/ESI+ 570,366 [МН]+.
Стадия 6. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(винилсульфонилокси)-бензоилокси)-этил)пиридин-1-оксида (100)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(3-гидрокси-4-метоксибензоилокси)этил)пиридин-1-оксид (30 мг; 0,05 ммоль) растворяли в DCM (2,5 мл), затем добавляли триэтиламин (TEA) (8,4 мкл; 0,06 ммоль) и 2-хлорэтансульфонилхлорид (6,3 мкл; 0,06 ммоль) и смесь перемешивали при КТ в течение 30 мин. Реакционную смесь разбавляли DCM и промывали 1 н. HCl (2×10 мл). Органическую фазу сушили над Na2SO4 и упаривали под вакуумом, получая 30 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 7. Синтез (S)-4-(2-(3-(2-(бис(2-гидроксиэтил)амино)-этилсульфонилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (99)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-метокси-3-(винилсульфонилокси)бензоилокси)этил)пиридин-1-оксид (30 мг; 0,045 ммоль) растворяли в EtOH (1,5 мл), затем добавляли диэтаноламин (9,5 мкл; 0,09 ммоль) и реакционную смесь перемешивали при КТ в течение 30 мин. Растворитель выпаривали и неочищенный продукт очищали полупрепаративной HPLC, получая 20 мг конечного продукта (выход 59%). MS/ESI+ 765,3 [МН]+, 787,2 [MNa]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.27 (s, 2Н), 7.93-8.07 (m, 2Н), 7.27-7.35 (m, 2Н), 7.18-7.24 (m, 1Н), 7.13-7.18 (m, 1Н), 6.91 (t, J=75,00 Гц, 1Н), 6.31 (dd, J=9,70; 4,41 Гц, 1Н), 4.03 (s, 3Н), 3.98 (dd, J=6,62; 3,97 Гц, 2Н), 3.65-3.82 (m, 3Н), 3.53-3.62 (m, 4Н), 3.43 (dd, J=14,11; 4,41 Гц, 1Н), 3.20-3.29 (m, 2Н), 2.72-2.78 (m, 4Н), 1.27 (m, 1Н), 0.60 (d, J=6,62 Гц, 2Н), 0.34-0.42 (m, 2Н).
Соединения, перечисленные в Таблице 10, получали, используя стадии и методики синтеза, аналогичные описанным в примере 11, схема 11, стадии 1-3, 5-7, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Синтез гидрохлорида 4-((S)-2-(3-((S)-2-амино-3-метилбутаноилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)-3,5-дихлорпиридин-1-оксида (соединения 109)
Схема 12
Стадия 1. Синтез 4-((S)-2-(3-((S)-2-(трет-бутоксикарбониламино)-3-метилбутаноилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (110)
После сочетания (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-гидрокси-4-метоксибензоилокси)этил)пиридин-1-оксида (20 мг; 0,035 ммоль) (соед. 101, полученного, как описано в примере 11, схема 11, стадии 1-5) с (S)-Boc-валином (20 мг; 0,092 ммоль) в тех же условиях и в соответствии с методикой эксперимента, показанной в примере 10, схема 10, стадия 6, получали соответствующее сложноэфирное производное с количественным выходом. MS/ESI+ 768,2 [МН]+.
Стадия 2. Синтез гидрохлорида 4-((S)-2-(3-((S)-2-амино-3-метилбутаноилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)-3,5-дихлорпиридин-1-оксида (109)
4-((S)-2-(3-((S)-2-(трет-Бутоксикарбониламино)-3-метилбутаноилокси)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (20 мг; 0,026 ммоль) подвергали реакции удаления защиты (как описано в примере 11, схема 11, стадии 4), получая желаемый продукт (15 мг; 0,021 ммоль; выход 81%). MS/ESI+ 669,07 [МН]+.
1Н ЯМР (400 МГц, ХЛОРОФОРМ-d) δ млн-1 9.22 (br. s., 3Н), 8.40 (s, 2Н), 7.73-7.93 (m, 2Н), 7.15 (d, J=7,83 Гц, 1Н), 7.03-7.10 (m, 1Н), 7.01 (m, 1Н), 6.93 (d, J=8,61 Гц, 1Н), 6.38-6.61-6.83 (t, 1Н, CHF2), 6.20 (dd, J=9,20; 4,50 Гц, 1Н), 4.27 (br. s., 1Н), 3.80-3.98 (m, 5Н), 3.62 (d, J=4,30 Гц, 1Н), 3.33 (d, J=10,17 Гц, 1Н), 2.51-2.75 (m, 1H), 1.13-1.34 (m, 7H), 0.53-0.71 (m, 2H), 0.29-0.45 (m, 2H).
Пример 13
Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонилокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)пиридин-1-оксида (111)
Схема 13
Стадия 1. Синтез 4-(бензилокси)-3-(циклопропилметокси)-бензальдегида (119)
4-(Бензилокси)-3-гидроксибензальдегид (640 мг; 2,8 ммоль) растворяли в DMF (5 мл), затем добавляли K2CO3 (774 мг; 5,6 ммоль) и (бромметил)циклопропан (544 мкл; 5.6 ммоль) и смесь перемешивали при 90°С в течение 2 ч. Реакционную смесь разбавляли Et2O и органическую фазу промывали насыщ. раствором NaHCO3, водой и рассолом, сушили над Na2SO4 и упаривали под вакуумом, получая 750 мг желаемого продукта (выход 95%).
Стадия 2. Синтез 4-(бензилокси)-3-(циклопропилметокси)бензойной кислоты (118)
4-(Бензилокси)-3-(циклопропилметокси)бензойную кислоту получали из соединения 4-(бензилокси)-3-(циклопропилметокси)бензальдегида, следуя методике, описанной в примере 11, схема 11, стадия 2.
Стадия 3. Синтез метил-4-(бензилокси)-3-(циклопропилметокси)-бензоата (117)
4-(Бензилокси)-3-(циклопропилметокси)бензойную кислоту (300 мг; 1 ммоль) растворяли в MeOH (6 мл), затем добавляли тионилхлорид (109 мкл; 1,5 ммоль) и смесь перемешивали при 70°С в течение 2 ч. Растворитель удаляли, неочищенный продукт растирали в петролейном эфире и отфильтровывали, получая 200 мг желаемого продукта (выход 64%).
Стадия 4. Синтез метил-3-(циклопропилметокси)-4-гидроксибензоата (116)
Метил-4-(бензилокси)-3-(циклопропилметокси)бензоат (200 мг; 0,64 ммоль) растворяли в MeOH, затем добавляли Pd/Ba2SO4 5% (136 мг; 0,064 ммоль) и смесь встряхивали на аппарате Парра при давлении водорода 35 ф/кв. дюйм (242 кПа) в течение 1 ч. Катализатор отфильтровывали на набивке диатомовой земли и растворитель выпаривали под вакуумом, получая 130 мг желаемого продукта (выход 91%).
Стадия 5. Синтез метил-3-(циклопропилметокси)-4-(винилсульфонилокси)бензоата (115)
Метил-3-(циклопропилметокси)-4-(винилсульфонилокси)бензоат получали из метил-3-(циклопропилметокси)-4-гидроксибензоата, следуя методике, описанной в примере 11, схема 11, стадия 6.
Стадия 6. Синтез метил-3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонилокси)бензоата (114)
Метил-3-(циклопропилметокси)-4-(2-(диметиламино)-этилсульфонилокси)-бензоат получали из метил-3-(циклопропилметокси)-4-(винилсульфонилокси)бензоата, следуя методике, описанной в примере 11, схема 11, стадия 7, с использованием диэтиламина вместо диэтаноламина.
Стадия 7. Синтез 3-(циклопропилметокси)-4-(2-(диметиламино)-этилсульфонилокси)бензойной кислоты (113)
Метил-3-(циклопропилметокси)-4-(2-(диметиламино)-этилсульфонилокси)-бензоат (190 мг; 0,53 ммоль) растворяли в THF (3 мл), затем добавляли 1 н. LiOH (2 мл) и смесь перемешивали при КТ в течение 2 суток. Реакционную смесь подкисляли до рН 7 путем добавления 1 н. HCl и экстрагировали этилацетатом. Органическую фазу сушили над Na2SO4 и упаривали под вакуумом. Неочищенный продукт очищали полупрепаративной HPLC, получая 47 мг конечного продукта (выход: 26%).
Стадия 8. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонилокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (112)
Указанное в заголовке соединение получали из 3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонилокси)бензойной кислоты, следуя методике, описанной в примере 2, стадия 1.
Стадия 9. Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонилокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)пиридин-1-оксида (111)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(2-(диметиламино)-этилсульфонилокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)пиридин-1-оксид (10 мг; 0,013 ммоль) растворяли растворе HCl/этилацетат (500 мкл) и выдерживали при КТ в течение 2 ч, затем растворитель удаляли. Неочищенный продукт сушили в вакуумном сушильном шкафу, получая 10 мг конечного продукта.
MS/ESI+ 745,2 [МН]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 13.29-13.80 (bs, 1Н), 8.29 (s, 2Н), 7.67-7.77 (m, 2Н), 7.57 (d, J=8,38 Гц, 1Н), 7.32 (d, J=1,76 Гц, 1Н), 7.13-7.25 (m, 2Н), 6.61 (t, 1Н, CHF2), 6.32 (dd, J=9,70; 4,41 Гц, 1Н), 4.26-4.42 (m, 2Н), 4.11 (d, J=7,06 Гц, 2Н), 3.99 (d, J=6,62 Гц, 2Н), 3.76 (dd, J=9,04; 5,07 Гц, 3Н), 3.44 (dd, J=14,11; 4,41 Гц, 1Н), 2.05-2.10 (m, 6Н), 1.39-1.53 (m, 1Н), 1.22-1.34 (m, 1Н), 0.63-0.73 (m, 2Н), 0.55-0.63 (m, 2Н), 0.44-0.52 (m, 2Н), 0.34-0.41 (m, 2Н).
Соединение из Таблицы 11 получали в соответствии со стадиями и методиками синтеза, аналогичными описанным в примере 13, схема 13, стадии 5-8, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 14
Синтез гидрохлорида 4-((S)-2-(4-((1s,4R)-4-аминоциклогексилкарбамоил)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (121)
Схема 14
Стадия 1. Синтез метил-3-(циклопропилметокси)-4-формилбензоата (125)
К раствору метил-4-формил-3-гидроксибензоата (50 мг; ммоль) в DMF (1 мл) добавляли циклопропилбромид (0,5 мл; ммоль) и карбонат калия (50 мг; ммоль) при КТ. Реакционную смесь перемешивали при 60°С в течение 3 ч, затем выливали в воду и водную фазу дважды экстрагировали AcOEt. Объединенные органические фазы сушили над Na2SO4 и растворитель удаляли при пониженном давлении, получая 50 мг указанного в заголовке соединения (ммоль; выход %), которое использовали на следующей стадии без дополнительной очистки. MS/ESI+ 180,04 [МН]+.
Стадия 2. Синтез 3-(циклопропилметокси)-4-формилбензойной кислоты (126)
К раствору метил-3-(циклопропилметокси)-4-формилбензоата (50 мг; ммоль) в THF (2 мл) добавляли 1 М LiOH (1 мл) и смесь перемешивали при КТ в течение ночи.
Добавляли 1 М HCl для осаждения продукта, который отфильтровывали, получая желаемое соединение (50 мг; ммоль), которое использовали на следующей стадии без дополнительной очистки.
MS/ESI+ 234,09 [МН]+.
Стадия 3. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(циклопропилметокси)-4-формилбензоилокси)-этил)пиридин-1-оксида (124)
Соединение 3 (200,0 мг; 0,48 ммоль) и 3-(циклопропилметокси)-4-формилбензойную кислоту (200,0 мг; 0,9 ммоль) растворяли в DCM (20 мл), после чего добавляли DMAP (100,0 мг; 0,82 ммоль) и EDC-HCl (200 мг; 1,04 ммоль). Реакционную смесь перемешивали при КТ в течение 3 ч, затем разбавляли водой (50 мл) и экстрагировали DCM (50 мл). Органическую фазу промывали 1 н. HCl и насыщ. раствором K2CO3. Полученный органический экстракт сушили над Na2SO4 и растворитель удаляли при пониженном давлении, получая 200 мг указанного в заголовке соединения (выход 67,5%) в виде желтого масла. MS/ESI+ 622,44 [МН]+.
1Н ЯМР (400 МГц, хлороформ-d) δ млн-1 10.59 (s, 1Н), 8.15 (s, 2Н), 7.84-7.96 (m, 1Н), 7.65-7.73 (m, 1Н), 7.55-7.59 (m, 1Н), 7.15-7.23 (m, 1Н), 6.96-7.12 (m, 2Н), 6.41-6.63-6.85 (t, 1Н, CHF2), 6.20-6.34 (m, 1Н), 3.85-4.12 (m, 4Н), 3.59-3.76 (m, 1Н), 3.26-3.40 (m, 1Н), 1.21-1.41 (m, 2Н), 0.52-0.77 (m, 4Н), 0.29-0.46 (m, 4Н).
Стадия 4. Синтез (S)-4-(2-(4-карбокси-3-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)-3,5-дихлорпиридин-1-оксида (123)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(3-(циклопропилметокси)-4-формилбензоилокси)этил)пиридин-1-оксид (200,0 мг; 0,32 ммоль) растворяли в уксусной кислоте (4 мл) и охлаждали до 0°С (в бане с ледяной водой). Добавляли сульфаминовую кислоту (46,8 мг; 0,48 ммоль), затем по каплям добавляли хлорит натрия (34,9 мг; 0,386 ммоль), предварительно растворенный в воде (0,5 мл). Реакционную смесь перемешивали при КТ в течение 3 ч. Добавляли воду и водную фазу экстрагировали этилацетатом. Растворитель удаляли при пониженном давлении и маслянистый остаток перекристаллизовывали из системы растворителей 2-пропанол/гептан (10:90) при -20°С. Осадок отфильтровывали, сушили в вакуумном сушильном шкафу при 40°С, получая указанное в заголовке соединение в виде белого твердого вещества (67 мг; выход 32,7%). MS/ESI+ 638,44 [МН]+.
Стадия 5. Синтез (S)-4-(2-(4-(4-(трет-бутоксикарбониламино)-циклогексилкарбамоил)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (122)
(S)-4-(2-(4-Карбокси-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (20 мг; 0, 0,031 ммоль) растворяли в DMF (1,0 мл) и добавляли (S)-1-(трет-бутоксикарбонил)пирролидин-2-карбоновую кислоту (20,0 мг; 0,093 ммоль), затем EDC (20,0 мг; 0,104 ммоль) и DMAP (10,0 мг; 0,082 ммоль). Раствор перемешивали при КТ в течение 6 ч. По окончании этого времени реакционную смесь разбавляли 15 мл 1 М HCl и экстрагировали AcOEt (15 мл). Органическую фазу экстрагировали 1М HCl (15 мл; х3) и конц. раствором K2CO3 (3×15 мл). Полученный органический экстракт сушили над Na2SO4 и растворитель удаляли при пониженном давлении. Неочищенный маслянистый остаток очищали препаративной HPLC, получая 20,0 мг указанного в заголовке соединения (выход 76%).
Стадия 6. Синтез гидрохлорида 4-((S)-2-(4-((1s,4R)-4-аминоциклогексилкарбамоил)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (121)
(S)-4-(2-(4-(4-(трет-Бутоксикарбониламино)циклогексилкарбамоил)-3-(циклопропилметокси)бензоилокси-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (20 мг; 0,024 ммоль) растворяли в HCl/AcOEt 4М (0,3 мл) и перемешивали в течение 30 мин при КТ. По окончании этого времени добавляли 1 М HCl (5 мл) и реакционную смесь экстрагировали AcOEt (5 мл). Полученный органический экстракт сушили над Na2SO4 и растворитель удаляли при пониженном давлении, получая желаемый продукт (15 мг; выход 85%). MS/ESI+ 733,88 [MH]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 8.28 (s, 2Н), 8.12-8.22 (m, 1Н), 7.65-7.78 (m, 2Н), 7.29-7.39 (m, 1Н), 7.15-7.26 (m, 2Н), 6.90 (t, J=75,00 Гц, 1Н), 6.30-6.41 (m, 1Н), 4.11-4.36 (m, 3Н), 3.92-4.06 (m, 2Н), 3.65-3.83 (m, 1Н), 3.38-3.51 (m, 1Н), 2.16-2.28 (m, 3Н), 1.63-1.99 (m, 6Н), 1.17-1.39 (m, 2Н), 0.50-0.78 (m, 6Н), 0.27-0.43 (m, 2Н).
Соединения, перечисленные в Таблице 12, получали в соответствии со стадиями и методиками синтеза, аналогичными описанным в примере 14, схема 14, стадии 1-5, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Стадию образования соли (стадию 6) проводили только тогда, когда есть указание на образование соли.
Пример 15
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-морфолиноэтил)-сульфамоил)-бензоилокси)этил)пиридин-1-оксида (133)
Схема 15
Стадия 1. Синтез метил-4-метокси-3-(N-(2-морфолиноэтил)-сульфамоил)бензоата (134)
К перемешиваемому раствору метил-3-(хлорсульфонил)-4-метоксибензоата (400 мг; 1,511 ммоль) и TEA (0,421 мл; 3,02 ммоль) в DCM (7 мл) порциями добавляли 2-морфолиноэтанамин (236 мг; 1,813 ммоль). Смесь перемешивали при КТ в течение 2 ч. Реакционную смесь разбавляли DCM, промывали 0,5 М HCl, рассолом, сушили над Na2SO4 и упаривали при пониженном давлении. Желаемый продукт получали в виде твердого вещества (540 мг; выход 100%) и использовали в следующей реакции без дополнительной очистки.
MS/ESI+ 359 [МН]+.
Стадия 2. Синтез 4-метокси-3-(N-(2-морфолиноэтил)сульфамоил)-бензойной кислоты (135)
К перемешиваемому раствору метил-4-метокси-3-(N-(2-морфолиноэтил)сульфамоил)бензоата (540 мг; 1,507 ммоль) в MeOH (10 мл) по каплям добавляли 1 М раствор гидроксида лития (5 мл; 5,00 ммоль). Смесь перемешивали при КТ в течение 4 ч, затем смесь охлаждали при 0°С (в бане с ледяной водой) и по каплям добавляли 6 М HCl до достижения рН 4-5. Выпавшее в осадок белое твердое вещество собирали фильтрованием. Желаемый продукт получали в виде твердого вещества (480 мг; выход 93%) и использовали в следующей реакции без дополнительной очистки.
MS/ESI+ 345 [МН]+.
Стадия 3. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-морфолиноэтил)-сульфамоил)-бензоилокси)этил)пиридин-1-оксида (133)
4-Метокси-3-(N-(2-морфолиноэтил)сульфамоил)бензойную кислоту (146 мг; 0,424 ммоль) суспендировали в безводном DCM (10 мл) в атмосфере N2; после этого добавляли DMAP (24,86 мг; 0,203 ммоль) и EDC (156 мг; 0,814 ммоль). Смесь перемешивали при КТ в течение 1 ч. К смеси добавляли соединение 3 (171 мг; 0,407 ммоль) в виде одной порции и реакционную смесь перемешивали в течение ночи при КТ. Смесь концентрировали при пониженном давлении и очищали флэш-хроматографией на силикагеле (DCM : ацетон, 1:1), получая 212 мг желаемого продукта в виде белого твердого вещества. Потребовалось провести вторую флэш-хроматографию на силикагеле (DCM : MeOH, 10:0,5), и получали желаемый продукт (170 мг; выход 56%). MS/ESI+ 746,23 [МН]+. (с=0,50; DCM).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.53 (s, 2Н), 8.33 (d, 1Н), 8.18 (dd, 1Н), 7.36 (d, 1Н), 7.13-7.25 (m, 3Н), 7.03-7.11 (m, 1Н), 7.07 (t, 1Н), 6.20 (dd, 1Н), 4.00 (s, 3Н), 3.86-3.98 (m, 2Н), 3.63 (dd, 1Н), 3.38-3.45 (m, 4Н), 3.31-3.38 (m, 1Н), 2.93 (dd, 2Н), 2.26 (t, 2Н), 2.14-2.21 (m, 4Н), 1.16-1.28 (m, 1Н), 0.51-0.62 (m, 2Н), 0.30-0.40 (m, 2Н).
Соединение из Таблицы 13 получали в соответствии со стадиями и методиками синтеза, аналогичными описанным в примере 15, схема 15, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 16
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(N-(2-(диметиламино)этил)сульфамоил)-бензоилокси)этил)пиридин-1-оксида (соединения 137)
Схема 16
Стадия 1. Синтез 4-(N-(2-(диметиламино)этил)сульфамоил)-бензойной кислоты (142)
4-(Хлорсульфонил)бензойную кислоту (500 мг; 2,266 ммоль) растворяли в DCM (50 мл). Добавляли N1,N1-диметилэтан-1,2-диамин (999 мг; 11,33 ммоль) и полученный раствор перемешивали при комнатной температуре в течение 24 часов. Примечание: раствор становился красным. Добавляли HCl (4 М раствор в диоксане, 10 мл), чтобы полностью перевести в солевую форму продукт и избыток N1,N1-диметилэтан-1,2-диамина. Растворитель выпаривали, и неочищенный продукт (1,7 г) использовали в следующей реакции без дополнительной очистки.
Стадия 2. Синтез метил-4-(N-(2-(диметиламино)этил)сульфамоил)-бензоата (141)
Неочищенную 4-(N-(2-(диметиламино)этил)сульфамоил)бензойную кислоту (1,7 г; 2,497 ммоль) растворяли в МеОН (100 мл); добавляли хлористый водород, 4 М раствор в диоксане (5 мл; 20,00 ммоль), и полученную смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь упаривали досуха, затем распределяли между EtOAc (100 мл) и водным раствором NaHCO3 (5%-ным (масс/масс), 100 мл). Органический слой сушили над Na2SO4 и упаривали досуха, получая желаемый продукт в виде белого твердого вещества (610 мг; 2,130 ммоль, выход 85%; MS/ESI+ 287 [МН]+) и использовали в следующей реакции без дополнительной очистки.
Стадия 3. Синтез метил-4-(N-(трет-бутоксикарбонил)-N-(2-(диметиламино)этил)сульфамоил)бензоата (140)
Метил-4-(N-(2-(диметиламино)этил)сульфамоил)бензоат (610 мг; 2,130 ммоль) растворяли в DCM (50 мл). Добавляли Boc2O (0,495 мл; 2,130 ммоль) и DMAP (260 мг; 2,130 ммоль) и смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь промывали 1 н. HCl (2×20 мл). Органический слой сушили над Na2SO4 и упаривали досуха. Получали неочищенный желаемый продукт (780 мг; 2,018 ммоль; выход 95%; MS/ESI+ 387 [МН]+) и использовали в следующей реакции без дополнительной очистки.
Стадия 4. Синтез 4-(N-(трет-бутоксикарбонил)-N-(2-(диметиламино)этил)сульфамоил)бензойной кислоты (139)
Метил-4-(N-(трет-бутоксикарбонил)-N-(2-(диметиламино)этил)-сульфамоил)-бензоат (0,78 г; 2,018 ммоль) растворяли в тетрагидрофуране (15 мл). Добавляли 1 н. раствор LiOH (2,220 мл; 2,220 ммоль), и смесь перемешивали при комнатной температуре в течение 24 ч. Реакционную смесь разбавляли EtOAc (60 мл), добавляли 1 н. HCl и проводили разделение фаз. Органический слой сушили над Na2SO4 и упаривали досуха, получая неочищенный желаемый продукт (220 мг; 0,591 ммоль; выход 29,3%; MS/ESI+ 373 [МН]+), который использовали в следующей реакции без дополнительной очистки.
Стадия 5. Синтез (S)-4-(2-(4-(N-(трет-бутоксикарбонил)-N-(2-(диметиламино)этил)сульфамоил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (138)
Соединение 3 (200 мг; 0,476 ммоль) растворяли в DCM (20 мл). Добавляли DMAP (29,1 мг; 0,238 ммоль), EDC (182 мг; 0,952 ммоль) и 4-(N-(трет-бутоксикарбонил)-N-(2-(диметиламино)этил)сульфамоил)бензойную кислоту (220 мг; 0,591 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь промывали насыщ. водн. раствором NaHCO3 (30 мл) и 1 н. HCl (2×30 мл); органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный желаемый продукт (290 мг; 0,374 ммоль; выход 79%; MS/ESI+ 774,3 [МН]+) использовали в следующей реакции без дополнительной очистки.
Стадия 6. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(N-(2-(диметиламино)этил)-сульфамоил)-бензоилокси)этил)пиридин-1-оксида (137)
(S)-4-(2-(4-(N-(трет-Бутоксикарбонил)-N-(2-(диметиламино)этил)-сульфамоил)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)-3,5-дихлорпиридин-1-оксид (290 мг; 0,374 ммоль) растворяли в DCM (20 мл). Добавляли 4 н. раствор HCl в диоксане (3 мл; 12,00 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь упаривали досуха, растворяли в DCM (30 мл) и промывали 5%-ным водн. раствором NaHCO3 (30 мл). Органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: DCM : EtOAc от 8:2 до 7:3), получая 120 мг желаемого продукта в виде бесцветного масла. Масло растворяли в DCM (20 мл) и добавляли 4 н. раствор HCl в диоксане (0,5 мл); полученный раствор упаривали досуха, получая желаемый продукт в виде гидрохлоридной соли (102 мг; 0,143 ммоль; выход 38,3%; MS/ESI+ 673,87 [МН]+, [αD]=-54,9, с=0,51; DCM).
Пример 17
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензоилокси)этил)пиридин-1-оксида (соединения 143)
Схема 17
Стадия 1. Синтез метил-3-формил-4-(2-морфолиноэтокси)-бензоата (152)
Смесь метил-3-формил-4-гидроксибензоата (0,800 г; 4,44 ммоль), гидрохлорида 4-(2-хлорэтил)морфолина (1,653 г; 8,88 ммоль) и K2CO3 (1,227 г; 8,88 ммоль) в CH3CN (5 мл) нагревали, используя облучение микроволнами (MW), при 100°С в течение 2 ч. Смесь распределяли между этилацетатом и водой. Органическую фазу сушили над Na2SO4, растворитель удаляли и неочищенный продукт очищали флэш-хроматографией на силикагеле (DCM : MeOH от 99:1 до 97:3), получая метил-3-формил-4-(2-морфолиноэтокси)бензоат в виде бледно-желтого твердого вещества (1,177 г; выход 90%).
MS/ESI+ 294,2 [МН]+.
Стадия 2. Синтез (Е)-метил-3-((метоксиимино)метил)-4-(2-морфолиноэтокси)бензоата (151)
Раствор метил-3-формил-4-(2-морфолиноэтокси)бензоата (0,450 г; 1,534 ммоль) и гидрохлорида O-метилгидроксиламина (0,141 г; 1,688 ммоль) в пиридине (15 мл) нагревали при 60°С в течение 1 ч. Растворитель удаляли и неочищенный продукт распределяли между этилацетатом и 5%-ным раствором Na2HCO3. Органическую фазу сушили над Na2SO4, растворитель удаляли, получали неочищенный (Е)-метил-3-((метоксиимино)метил)-4-(2-морфолиноэтокси)бензоат в виде белого твердого вещества (0,492 г; выход 99%) и использовали на следующей стадии без дополнительной очистки. MS/ESI+ 323,2 [МН]+.
Стадия 3. Синтез метил-3-(аминометил)-4-(2-морфолиноэтокси)- бензоата (150)
Смесь (Е)-метил-3-((метоксиимино)метил)-4-(2-морфолиноэтокси)-бензоата (0,492 г; 1,526 ммоль), 10%-ного Pd/C (0,050 г; 0,047 ммоль) и конц. HCl (0,093 мл; 3,05 ммоль) в MeOH (30 мл) гидрировали в аппарате Парра при давлении 35 ф/кв. дюйм (242 кПа) в течение 48 ч. Добавляли Pd/C (0,030 г; 0,028 ммоль) и HCl (0,023 мл; 0,763 ммоль) и смесь гидрировали при давлении 35 ф/кв. дюйм (242 кПа) в течение еще 24 ч. Катализатор отфильтровывали и остаток распределяли между этилацетатом и 5%-ным раствором NaHCO3. Водную фазу дважды экстрагировали DCM и небольшим количеством MeOH, объединенные органические слои сушили над Na2SO4 и растворитель удаляли. Получали метил-3-(аминометил)-4-(2-морфолиноэтокси)бензоат в виде бесцветного масла (0,405 г; выход 90%) и использовали на следующей стадии без дополнительной очистки. MS/ESI+ 295,2; 278,2 [МН]+.
Стадия 4. Синтез метил-3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензоата (149)
Смесь метил-3-(аминометил)-4-(2-морфолиноэтокси)бензоата (0,405 г; 1,376 ммоль) в пиридине (15 мл) охлаждали до 0°С и добавляли метансульфонилхлорид (0,118 мл; 1,514 ммоль). Смесь нагревали до КТ и перемешивали в течение 48 ч. Растворитель удаляли и неочищенный продукт распределяли между этилацетатом и 5%-ным раствором NaHCO3. Органическую фазу сушили над Na2SO4 и растворитель выпаривали. Неочищенный продукт очищали флэш-хроматографией на силикагелевом картридже (DCM : MeOH, 99:1), получая метил-3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензоат в виде белого твердого вещества (0,233 г; выход 45,5%). MS/ESI+ 373,2 [MH]+.
Стадия 5. Синтез гидрохлорида 3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензойной кислоты (148)
Раствор метил-3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)-бензоата (0,233 г; 0,626 ммоль) и 6 н. HCl (2,61 мл; 15,64 ммоль) в диоксане нагревали при 70°С в течение 36 ч. Растворитель удаляли и остаток сушили под вакуумом, получая гидрохлорид 3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензойной кислоты в виде беловатого твердого вещества (0,245 г; выход 99%), который использовали на следующей стадии без дополнительной очистки. MS/ESI+ 359,2 [МН]+.
Стадия 6. Синтез аллил-3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензоата (147)
Смесь гидрохлорида 3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензойной кислоты (0,245 г; 0,620 ммоль), карбонилдиимидазола (CDI) (0,121 г; 0,745 ммоль) и TEA (0,086 мл; 0,620 ммоль) в ацетонитриле (30 мл) нагревали до 70°С в течение 3 ч. Растворитель удаляли, неочищенный продукт растворяли в проп-2-ен-1-оле (10 мл; 146 ммоль) и нагревали до 70°С в течение 2 ч, затем при КТ в течение выходных. Смесь разбавляли этилацетатом и промывали насыщ. раствором NH4Cl (х4) и 5%-ным раствором NaHCO3. Органическую фазу сушили над Na2SO4 и растворитель удаляли. Неочищенный продукт очищали с использованием SCX-картриджа (DCM : MeOH=1:1; МеОН : конц. NH3=90:10). Получали аллил-3- (метилсульфонамидометил)-4-(2-морфолиноэтокси)бензоат в виде белого твердого вещества (0,215 г; выход 87%) и использовали на следующей стадии без дополнительной очистки. MS/ESI+ 399,2 [МН]+.
Стадия 7. Синтез аллил-3-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-4-(2-морфолиноэтокси)бензоата (146)
Раствор аллил-3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)-бензоата (0,215 г; 0,540 ммоль), ди-трет-бутилдикарбоната (0,130 г; 0,594 ммоль) и DMAP (0,073 г; 0,594 ммоль) в DCM (20 мл) перемешивали при КТ в течение 1 ч. Смесь промывали, используя 0,5 н. раствор HCl и 5%-ный раствор NaHCO3. Органический слой сушили над Na2SO4 и растворитель удаляли. Получали неочищенный аллил-3-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-4-(2-морфолиноэтокси)бензоат в виде бесцветного аморфного вещества (0,251 г; выход 93%), которое использовали на следующей стадии без дополнительной очистки. MS/ESI+ 499,3 [МН]+.
Стадия 8. Синтез 3-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-4-(2-морфолиноэтокси)бензойной кислоты (145)
Смесь аллил-3-((N-(трет-бутоксикарбонил)метилсульфонамидо)-метил)-4-(2-морфолиноэтокси)бензоата (0,251 г; 0,503 ммоль), тетракис(трифенилфосфин)палладия, связанного с полимером, (содержание 0,5-0,9 ммоль/г) (0,700 г; 0,503 ммоль) и пиперидина (0,050 мл; 0,503 ммоль) в THF нагревали до 50°С в течение 48 ч. Смесь распределяли между насыщ. раствором NH4Cl и этилацетатом и водную фазу несколько раз экстрагировали этилацетатом. Объединенные органические слои промывали 5%-ным раствором NaHCO3. Основную водную фазу подкисляли, используя 1 н. раствор HCl (рН 5), и экстрагировали этилацетатом. Органический слой сушили над Na2SO4 и растворитель удаляли. Получали 3-((N-(трет-бутоксикарбонил)метилсульфонамидо)-метил)-4-(2-морфолиноэтокси)-бензойную кислоту в виде бледно-желтого аморфного вещества (0,116 г; выход 50,3%) и использовали на следующей стадии без дополнительной очистки. MS/ESI+ 459,3; 359,3 [МН]+.
Стадия 9. Синтез (S)-4-(2-(3-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-4-(2-морфолиноэтокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (144)
Смесь 3-((N-(трет-бутоксикарбонил)метилсульфонамидо)метил)-4-(2-морфолиноэтокси)бензойной кислоты (0,116 г; 0,253 ммоль), соединения 3 (0,097 г; 0,230 ммоль), EDC (0,132 г; 0,690 ммоль) и DMAP (0,014 г; 0,115 ммоль) в DCM перемешивали при КТ в течение выходных. Смесь разбавляли DCM и дважды промывали 1 н. раствором HCl и 5%-ным раствором NaHCO3. Органическую фазу сушили над Na2SO4 и растворитель удаляли. Остаток очищали фильтрованием на SCX-картридже (DCM : MeOH=1:1; MeOH : NH4OH=90:10). Основную фракцию распределяли между этилацетатом и водой, и органическую фазу промывали рассолом и сушили над Na2SO4. Растворитель удаляли, получали (S)-4-(2-(3-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-4-(2-морфолиноэтокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид в виде бесцветного аморфного вещества (0,108 г; выход 54,6%) и использовали на следующей стадии без дополнительной очистки. MS/ESI+ 860,6 [МН]+.
Стадия 10. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензоилокси)этил)пиридин-1-оксида (143)
К раствору (S)-4-(2-(3-((N-(трет-бутоксикарбонил)-метилсульфонамидо)-метил)-4-(2-морфолиноэтокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (0,108 г; 0,125 ммоль) в DCM (10 мл) добавляли 4 М HCl в диоксане (2 мл; 8,00 ммоль) и смесь перемешивали при КТ в течение ночи. Смесь распределяли между DCM и 5%-ным раствором NaHCO3 и органическую фазу сушили над Na2SO4. Растворитель удаляли и неочищенный продукт очищали фильтрованием через силикагелевый картридж (DCM : MeOH от 99:1 до 98:2), получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонамидометил)-4-(2-морфолиноэтокси)бензоилокси)этил)пиридин-1-оксид в виде бесцветного аморфного вещества (0,056 г; выход 59,0%). MS/ESI+ 760,04 [МН]+. (с=0,44; МеОН).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.53 (s, 2Н), 8.00 (d, 1Н), 7.93 (dd, 1Н), 7.31 (t, 1Н), 7.21 (d, 1Н), 7.20 (d, 1Н), 7.15 (d, 1Н), 7.08 (dd, 1Н), 7.06 (t, 1Н), 6.21 (dd, 1Н), 4.24 (t, 2Н), 4.16 (d, 2Н), 3.93 (d, 2Н), 3.53-3.66 (m, 5Н), 3.34 (dd, 1Н), 2.88 (s, 3Н), 2.74-2.81 (m, 2Н), 2.53-2.61 (m, 4Н), 1.10-1.22 (m, 1Н), 0.45-0.63 (m, 2Н), 0.28-0.45 (m, 2Н).
Соединение из Таблицы 14 получали, используя стадии и методики синтеза, аналогичные описанным в примере 17, схема 17, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 18
Синтез ((S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-((4-метокси-3-(N-(2-морфолиноэтил)-метилсульфонамидо)фенокси)карбонилокси)этил)пиридин-1-оксида (154)
Схема 18
Стадия 1. Синтез метил-4-(метилсульфонамидометил)бензоата (156)
К раствору гидрохлорида метил-4-(аминометил)бензоата (2 г; 9,92 ммоль) в пиридине (90 мл) добавляли метансульфонилхлорид (1,183 мл; 14,88 ммоль) и смесь перемешивали при КТ в течение 3 ч. Растворитель выпаривали, остаток распределяли между этилацетатом (100 мл) и 1 н. раствором HCl (100 мл) и водный слой экстрагировали этилацетатом (3×100 мл). Объединенные органические слои сушили над Na2SO4, и растворитель удаляли, получая неочищенный метил-4-(метилсульфонамидометил)бензоат в виде бледно-желтого твердого вещества (2,8 г), которое использовали на следующей стадии без какой-либо дополнительной очистки. MS/ESI+ 244,1 [МН]+.
Стадия 2. Синтез хлорида 4-(2-(N-(4-карбоксибензил)-метилсульфонамидо)этил)морфолин-4-ия (155)
К раствору метил-4-(метилсульфонамидометил)бензоата (по расчетам 9,92 ммоль) в CH3CN (100 мл) добавляли гидрохлорид 4-(2-хлорэтил)морфолина (2,75 г; 14,80 ммоль) и K2CO3 (2,045 г; 14,80 ммоль) и смесь кипятили с обратным холодильником в течение 3 ч. Твердое вещество отфильтровывали, растворитель выпаривали и полученное желтое масло растворяли в диоксане (50 мл). Добавляли 12 н. водный HCl (50 мл; 600 ммоль) и смесь нагревали до 70°С в течение 3 ч. Растворитель удаляли под вакуумом и полученный неочищенный продукт очищали растиранием с CH3CN, получая хлорид 4-(2-(N-(4-карбоксибензил)метилсульфонамидо)-этил)морфолин-4-ия в виде белого твердого вещества (2,4 г; выход 64% за 3 стадии). MS/ESI+ 739,0 [МН]+.
Стадия 3. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-((N-(2-морфолиноэтил)-метилсульфонамидо)-метил)бензоилокси)этил)пиридин-1-оксида (154)
К раствору хлорида 4-(2-(N-(4-карбоксибензил)метилсульфонамидо)-этил)морфолин-4-ия (1,0 г; 2,64 ммоль) в DCM (35 мл) добавляли соединение 3 (1,109 г; 2,64 ммоль), EDC (1,518 г; 7,92 ммоль) и DMAP (0,161 г; 1,320 ммоль) и смесь перемешивали при КТ в течение 3 ч. К реакционной смеси добавляли этанол (50 мл) и осадок собирали фильтрованием, получая 1,3 г желаемого соединения. Этот продукт далее очищали флэш-хроматографией на колонке с силикагелем (DCM/MeOH, 9:1), получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-((N-(2-морфолиноэтил)метилсульфонамидо)-метил)бензоилокси)этил)пиридин-1-оксид в виде белого твердого вещества (1,100 г; выход 56%). MS/ESI+ 744,41 [МН]+. (с=0,5; DCM).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.54 (s, 2Н), 7.96-8.04 (m, 2Н), 7.43-7.58 (m, 2Н), 7.22 (d, 1Н), 7.20 (d, 1Н), 7.09 (dd, 1Н), 7.06 (t, 1Н), 6.22 (dd, 1Н), 4.46 (s, 2Н), 3.93 (d, 2Н), 3.62 (dd, 1Н), 3.44-3.53 (m, 4Н), 3.35 (dd, 1Н), 3.24 (t, 2Н), 3.08 (s, 3Н), 2.33 (t, 2Н), 2.21-2.30 (m, 4Н), 1.01-1.32 (m, 1Н), 0.48-0.66 (m, 2Н), 0.25-0.48 (m, 2Н).
Пример 19
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-((N-(2-морфолиноэтил)метилсульфонамидо)метил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (157)
Схема 19
Стадия 1. Синтез метил-4-формил-3-гидроксибензоата (170)
4-Формил-3-гидроксибензойную кислоту (1 г; 6,02 ммоль) суспендировали в МеОН (50 мл). Добавляли серную кислоту (несколько капель) и полученную смесь нагревали до 60°С в течение 6 ч. Реакционную смесь разбавляли этилацетатом (150 мл) и промывали рассолом (2×100 мл). Органический слой сушили над Na2SO4 и упаривали досуха, получая метил-4-формил-3-гидроксибензоат (0,970 г; 5,38 ммоль, выход 89%). Соединение использовали на следующей стадии без дополнительной очистки. MS/ESI+ 181,1 [МН]+.
Стадия 2. Синтез метил-3-(циклопропилметокси)-4-формилбензоата (169)
Метил-4-формил-3-гидроксибензоат (0,97 г; 5,38 ммоль) растворяли в ацетонитриле (30 мл). Добавляли карбонат калия (1,488 г; 10,77 ммоль) и (бромметил)циклопропан (0,945 г; 7,00 ммоль) и смесь нагревали до 60°С при энергичном перемешивании в течение 30 ч. Реакционную смесь выливали в воду (100 мл), подкисляли водн. 36%-ным HCl (рН 1) и затем экстрагировали этилацетатом (2×100 мл). Органическую фазу сушили над Na2SO4 и упаривали досуха. Неочищенный метил-3-(циклопропилметокси)-4-формилбензоат (1,100 г; выход 87%) использовали на следующей стадии без дополнительной очистки. MS/ESI+ 235,1 [МН]+.
Стадия 3. Синтез 3-(циклопропилметокси)-4-формилбензойной кислоты (168)
Метил-3-(циклопропилметокси)-4-формилбензоат (1,1 г; 4,70 ммоль) растворяли в THF (60 мл) и добавляли 1 н. раствор гидроксида лития в воде (5,64 мл; 5,64 ммоль). Смесь перемешивали при КТ в течение 3 суток, затем разбавляли этилацетатом (100 мл) и промывали 1 н. водн. раствором HCl (50 мл). Органический слой сушили над Na2SO4 и упаривали досуха, получая 3-(циклопропилметокси)-4-формилбензойную кислоту (0,940 г; выход 91%). Это промежуточное соединение использовали на следующей стадии без дополнительной очистки. MS/ESI+ 221,1 [МН]+.
Стадия 4. Синтез (Z)-3-(циклопропилметокси)-4-((метоксиимино)-метил)бензойной кислоты (167)
Раствор 3-(циклопропилметокси)-4-формилбензойной кислоты (0,560 г; 2,54 ммоль) и гидрохлорида O-метилгидроксиламина (0,234 г; 2,80 ммоль) в пиридине (12 мл) нагревали до 60°С в течение 1 ч. Растворитель удаляли, неочищенный продукт растворяли в этилацетате и промывали 1 н. водн. раствором HCl и рассолом. Органический слой сушили над сульфатом натрия, растворитель выпаривали и получали (Z)-3-(циклопропилметокси)-4-((метоксиимино)метил)бензойную кислоту в виде белого твердого вещества (0,620 г; выход 98%). Этот продукт использовали на следующей стадии без какой-либо дополнительной очистки. MS/ESI+ 272,3 [MNa]+.
Стадия 5. Синтез (Z)-метил-3-(циклопропилметокси)-4-((метоксиимино)метил)бензоата (166)
Раствор (Z)-3-(циклопропилметокси)-4-((метоксиимино)метил)-бензойной кислоты (0,620 г; 2,487 ммоль) и CDI (0,444 г; 2,74 ммоль) в ацетонитриле (40 мл) нагревали до 70°С в течение 3 ч, оставляли стоять при КТ в течение ночи и затем нагревали до 70°С в течение еще 1 часа. Растворитель удаляли, неочищенный продукт растворяли в МеОН (30 мл) и нагревали до 70°С в течение 1,5 ч. Растворитель удаляли, неочищенный продукт растворяли в этилацетате и дважды промывали 1 н. водн. раствором HCl и рассолом. Органический слой сушили над сульфатом натрия и упаривали досуха, получая (Z)-метил-3-(циклопропилметокси)-4-((метоксиимино)метил)бензоат в виде желтого масла (0,635 г; выход 97%). MS/ESI+ 264,1 [МН]+.
Стадия 6. Синтез метил-4-(аминометил)-3-(циклопропилметокси)-бензоата (165)
(Z)-Метил-3-(циклопропилметокси)-4-((метоксиимино)метил)бензоат (0,635 г; 2,412 ммоль) растворяли в МеОН до полного растворения и добавляли 10%-ный Pd/C (0,070 г; 0,066 ммоль), затем 37%-ный водный HCl (0,297 мл; 3,62 ммоль). Смесь гидрировали при 35 ф/кв. дюйм (242 кПа) в течение ночи в аппарате Парра. Катализатор отфильтровывали, фильтрат упаривали досуха и остаток распределяли между этилацетатом и насыщ. водн. раствором NaHCO3. Органический слой промывали рассолом, сушили над Na2SO4 и удаляли растворитель. Получали метил-4-(аминометил)-3-(циклопропилметокси)бензоат в виде бледно-желтого аморфного вещества (0,530 г; выход 93%). Это промежуточное соединение использовали без какой-либо дополнительной очистки. MS/ESI+ 236,2 [МН]+.
Стадия 7. Синтез метил-3-(циклопропилметокси)-4-(метилсульфонамидометил)бензоата (164)
Раствор метил-4-(аминометил)-3-(циклопропилметокси)бензоата (0,530 г; 2,253 ммоль) в пиридине (20 мл) охлаждали до 0°С и добавляли метансульфонилхлорид (0,193 мл; 2,478 ммоль). Смесь оставляли нагреваться до КТ и перемешивали в течение 3 ч. Добавляли новую порцию метансульфонилхлорида (0,088 мл; 1,127 ммоль) в течение 2 ч и смесь перемешивали при КТ в течение ночи. Растворитель удаляли и неочищенный продукт распределяли между этилацетатом и 1 н. водн. раствором HCl. Органическую фазу промывали 5%-ным водн. раствором NaHCO3 и сушили над Na2SO4. Растворитель выпаривали досуха и неочищенный продукт очищали фильтрованием через силикагелевый картридж (петролейный эфир : этилацетат от 70:30 до 60:40), получая метил-3-(циклопропилметокси)-4-(метилсульфонамидометил)бензоат в виде бледно-желтого твердого вещества (0,435 г; выход 61,6%). MS/ESI+ 336,3 [MNa]+.
Стадия 8. Синтез 3-(циклопропилметокси)-4-(метилсульфонамидометил)бензойной кислоты (163)
К раствору метил-3-(циклопропилметокси)-4-(метилсульфонамидометил)бензоата (0,435 г; 1,388 ммоль) в THF (20 мл) добавляли 1 н. водный раствор LiOH (1,527 мл; 1,527 ммоль) и смесь перемешивали при КТ в течение ночи. Добавляли вторую порцию 1 н. водного раствора LiOH (1,388 мл; 1,388 ммоль) и смесь перемешивали при КТ в течение еще 24 ч. Реакционную смесь подкисляли 1 н. водн. раствором HCl и экстрагировали этилацетатом. Органический слой промывали рассолом и сушили над Na2SO4; растворитель удаляли под вакуумом, получая неочищенную 3-(циклопропилметокси)-4-(метилсульфонамидометил)-бензойную кислоту в виде бледно-желтого твердого вещества (0,400 г; выход 96%). Это промежуточное соединение использовали без какой-либо дополнительной очистки. MS/ESI+ 322,2 [MNa]+.
Стадия 9. Синтез аллил-3-(циклопропилметокси)-4-(метилсульфонамидометил)бензоата (162)
Смесь 3-(циклопропилметокси)-4-(метилсульфонамидометил)-бензойной кислоты (0,350 г; 1,169 ммоль) и CDl (0,209 г; 1,286 ммоль) в ацетонитриле (35 мл) нагревали до 70°С в течение 3 ч. Растворитель удаляли под вакуумом; остаток растворяли в аллиловом спирте (10 мл; 147 ммоль), нагревали до 70°С в течение 30 минут и оставляли стоять при КТ в течение ночи. Реакционную смесь распределяли между этилацетатом и насыщ. водн. раствором NH4Cl. Органическую фазу сушили над Na2SO4, растворитель удаляли и неочищенный продукт очищали фильтрованием через силикагелевый картридж (петролейный эфир : этилацетат, 70:30), получая аллил-3-(циклопропилметокси)-4-(метилсульфонамидометил)бензоат в виде белого твердого вещества (0,320 г; выход 81%). MS/ESI+ 340,2 [МН]+.
Стадия 10. Синтез аллил-4-((N-(трет-бутоксикарбонил)- метилсульфонамидо)метил)-3-(циклопропилметокси)бензоата (161)
Раствор аллил-3-(циклопропилметокси)-4-(метилсульфонамидометил)-бензоата (0,320 г; 0,943 ммоль), ди-трет-бутилдикарбоната (0,226 г; 1,037 ммоль) и DMAP (0,115 г; 0,943 ммоль) в DCM (30 мл) перемешивали при КТ в течение 1 ч. Реакционную смесь промывали 1 н. водн. раствором HCl и рассолом; органическую фазу сушили над Na2SO4 и растворитель удаляли под вакуумом, получая аллил-4-((N-(трет-бутоксикарбонил)метилсульфонамидо)метил)-3-(циклопропилметокси)бензоат в виде бесцветного аморфного вещества (0,385 г; выход 93%) Этот продукт использовали на следующей стадии без дополнительной очистки. MS/ESI+ 462,2 [MNa]+.
Стадия 11. Синтез 4-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-3-(циклопропилметокси)бензойной кислоты (160)
Смесь аллил-4-((N-(трет-бутоксикарбонил)метилсульфонамидо)-метил)-3-(циклопропилметокси)бензоата (0,385 г; 0,876 ммоль), пиперидина (0,087 мл; 0,876 ммоль) и полимера, связанного с тетракис(трифенилфосфин)палладием, (содержание 0,5-0,9 ммоль/г; 1 г; 0,876 ммоль) в THF (70 мл) нагревали до 50°С в течение 24 ч. Добавляли вторую порцию полимера, связанного с тетракис(трифенилфосфин)-палладием, (содержание 0,5-0,9 ммоль/г; 0,300 г; 0,263 ммоль) и пиперидина (0,030 мл; 0,303 ммоль) и смесь нагревали до 50°С в течение еще 24 ч. Полимер отфильтровывали и промывали этилацетатом. Фильтрат промывали насыщ. водн. раствором NH4Cl; органический слой сушили над Na2SO4 и растворитель удаляли. Неочищенную 4-((N-(трет-бутоксикарбонил)метилсульфонамидо)метил)-3-(циклопропилметокси)-бензойную кислоту получали в виде темно-желтого твердого вещества (0,350 г; выход 100%) и использовали без какой-либо дополнительной очистки. MS/ESI+ 422,2 [MNa]+.
Стадия 12. Синтез (S)-4-(2-(4-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (159)
Смесь 4-((N-(трет-бутоксикарбонил)метилсульфонамидо)метил)-3-(циклопропилметокси)бензойной кислоты (0,350 г; 0,876 ммоль), EDC (0,420 г; 2,190 ммоль), DMAP (0,045 г; 0,365 ммоль) и соединения 3, (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксида, (0,307 г; 0,730 ммоль) в DCM (30 мл) перемешивали при КТ в течение ночи. Реакционную смесь разбавляли DCM и промывали водн. 5%-ным раствором NaHCO3, водн. 1 н. раствором HCl и рассолом. Органический слой сушили над Na2SO4, растворитель удаляли под вакуумом и остаток очищали флэш-хроматографией на силикагелевом картридже (DCM : этилацетат от 80:20 до 70:30), получая (S)-4-(2-(4-((N-(трет-бутоксикарбонил)-метилсульфонамидо)метил)-3-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид в виде белого аморфного вещества (0,305 г; выход 52,1%). MS/ESI+ 801,3 [МН]+.
Стадия 13. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(циклопропилметокси)-4-(метилсульфонамидометил)бензоилокси)этил)пиридин-1-оксида (158)
Смесь (S)-4-(2-(4-((N-(трет-бутоксикарбонил)метилсульфонамидо)-метил)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (0,305 г; 0,380 ммоль) и 4 М HCl в Et2O (3 мл; 12,00 ммоль) в DCM (25 мл) перемешивали при КТ в течение ночи. Летучие вещества удаляли под вакуумом и неочищенный продукт очищали путем растирания с EtOH, получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(циклопропилметокси)-4-(метилсульфонамидометил)бензоилокси)этил)-пиридин-1-оксид в виде белого твердого вещества (0,207 г; выход 78%). MS/ESI+ 700,96 [МН]+. , с=0,54; МеОН.
Стадия 14. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-((N-(2-морфолиноэтил)метилсульфонамидо)метил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (157)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(3-(циклопропилметокси)-4-(метилсульфонамидометил)-бензоилокси)этил)-пиридин-1-оксид (100 мг; 0,24 ммоль) растворяли в DMF (1 мл). Добавляли 4-(2-хлорэтил)морфолин (64 мг; 0,43 ммоль) и K2CO3 (30 мг; 0,21 ммоль) и смесь перемешивали при 60°С в течение 4 ч. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органическую фазу сушили над Na2SO4 и упаривали под вакуумом. Неочищенный продукт очищали полупрепаративной HPLC, получая 8,1 мг конечного соединения. MS/ESI+ 814,2 [МН]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 13.65-13.95 (bs, 1Н), 8.30 (s, 2Н), 7.66-7.75 (m, 1Н), 7.53-7.65 (m, 2Н), 7.30-7.36 (m, 1Н), 7.15-7.25 (m, 2Н), 6.90 (t, J=75,00 Гц, 1Н), 6.27-6.42 (m, 1Н), 4.48 (s, 2Н), 3.99 (d, J=6,62 Гц, 10Н), 3.69-3.82 (m, 1Н), 3.29-3.47 (m, 3Н), 3.03-3.27 (m, 4Н), 2.97 (s, 3Н), 1.35-1.50 (m, 1Н), 0.79-1.00 (m, 1Н), 0.54-0.71 (m, 4Н), 0.32-0.52 (m, 4Н).
Пример 20
Синтез (S)-1-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3,5-дихлорпиридин-4-ил)этил-3-(циклопропилметокси)-4-(2-(диметиламино)-этилсульфонамидо)бензоата (171)
Схема 20
Стадия 1. Синтез метил-3-гидрокси-4-нитробензоата (180)
3-Гидрокси-4-нитробензойную кислоту (5,17 г; 28,2 ммоль) растворяли в метаноле (100 мл; 2466 ммоль), получая суспензию, и затем добавляли 50%-ную H2SO4 в воде (0,25 мл; 2,345 ммоль). Реакционную смесь перемешивали при 60°С в течение 6 суток, затем растворитель выпаривали и желтый остаток растворяли в AcOEt и воде. Водную фазу экстрагировали AcOEt, органическую фазу сушили над Na2SO4 и концентрировали, получая желаемый продукт в виде желтого твердого вещества. (5,53 г; выход 99%).
Стадия 2. Синтез метил-3-(циклопропилметокси)-4-нитробензоата (179)
Метил-3-гидрокси-4-нитробензоат (5,53 г; 28,1 ммоль) растворяли в безводном DMF (65 мл) в атмосфере N2. Добавляли иодид калия (1,397 г; 8,42 ммоль), карбонат калия (12,79 г; 93 ммоль) и затем (бромметил)циклопропан (5,44 мл; 56,1 ммоль). Реакционную смесь энергично перемешивали при 50°С в течение ночи. Растворитель выпаривали и остаток обрабатывали AcOEt и водой. Водную фазу экстрагировали AcOEt, объединенный органический слой сушили над Na2SO4 и концентрировали, получая желаемый продукт в виде желтого твердого вещества (7 г; выход 100%). MS/ESI+ 252 [MH]+.
Стадия 3. Синтез метил-4-амино-3-(циклопропилметокси)бензоата (178)
Смесь метил-3-(циклопропилметокси)-4-нитробензоата (0,890 г; 3,54 ммоль) и 10%-ного Pd/C (0,80 г; 7,52 ммоль) в МеОН (80 мл) гидрировали в аппарате Парра при давлении 15 ф/кв. дюйм (104 кПа) в течение 2 ч. Катализатор отфильтровывали и растворитель удаляли. Получали неочищенный метил-4-амино-3-(циклопропилметокси)бензоат в виде бледно-желтого твердого вещества (0,760 г; выход 97%) и использовали на следующей стадии без дополнительной очистки. MS/ESI+ 222,3 [MH]+.
Стадия 4. Синтез метил-3-(циклопропилметокси)-4-(винилсульфонамидо)бензоата (177)
Раствор метил-4-амино-3-(циклопропилметокси)бензоата (0,760 г; 3,43 ммоль) и пиридина (3,33 мл; 41,2 ммоль) в DCM (60 мл) охлаждали до 0°С и по каплям добавляли 2-хлорэтансульфонилхлорид (0,431 мл; 4,12 ммоль). Смесь нагревали до КТ и перемешивали в течение 1 ч. Смесь разбавляли DCM и промывали 1 н. раствором HCl и рассолом. Органическую фазу сушили над Na2SO4 и растворитель удаляли. Неочищенный продукт очищали фильтрованием через силикагелевый картридж (петролейный эфир : этилацетат от 90:10 до 70:30), получая метил-3-(циклопропилметокси)-4-(винилсульфонамидо)бензоат в виде бледно-оранжевого твердого вещества (0,788 г; выход 73,7%). MS/ESI+ 334,2 [MNa]+.
Стадия 5. Синтез метил-3-(циклопропилметокси)-4-(2- (диметиламино)этилсульфонамидо)бензоата (176)
К раствору метил-3-(циклопропилметокси)-4-(винилсульфонамидо)-бензоата (0,788 г; 2,53 ммоль) в EtOH (30 мл) добавляли 5,6 М диметиламин в EtOH (0,678 мл; 3,80 ммоль) и смесь перемешивали при КТ в течение 1 ч. Растворитель удаляли, получали неочищенный метил-3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонамидо)бензоат в виде желтого масла (0,902 г; выход 100%) и использовали на следующей стадии без дополнительной очистки. MS/ESI+ 357,4 [MH]+.
Стадия 6. Синтез метил-4-(N(трет-бутоксикарбонил)-2-(диметиламино)этилсульфонамидо)-3-(циклопропилметокси)бензоата (175)
Раствор метил-3-(циклопропилметокси)-4-(2-(диметиламино)-этилсульфонамидо)бензоата (0,902 г; 2,53 ммоль), Boc2O (0,552 г; 2,53 ммоль) и DMAP (0,309 г; 2,53 ммоль) в DCM (40 мл) перемешивали при КТ в течение 1 ч. Смесь промывали водой и рассолом, органическую фазу сушили над Na2SO4 и растворитель удаляли. Неочищенный продукт (1,15 г; выход 100%) использовали на следующей стадии без дополнительной очистки. MS/ESI+ 457,3 [MH]+.
Стадия 7. Синтез 4-(N-(трет-бутоксикарбонил)-2-(диметиламино)этилсульфонамидо)-3-(циклопропилметокси)-бензойной кислоты (174)
Смесь метил-4-(N-(трет-бутоксикарбонил)-2-(диметиламино)-этилсульфонамидо)-3-(циклопропилметокси)бензоата (1,155 г; 2,53 ммоль) и 1 н. раствора LiOH (3,79 мл; 3,79 ммоль) в H2O перемешивали при КТ в течение 24 ч. Смесь разбавляли этилацетатом и водой и добавляли 1 н. HCl до рН 5. Проводили разделение фаз, органический слой промывали рассолом и сушили над Na2SO4. Растворитель удаляли и получали желаемый продукт в виде бледно-оранжевого аморфного вещества (0,660 г; 1,491 ммоль; выход 59,0%). Значение рН водной фазы подводили до 6, и ее экстрагировали этилацетатом. Органическую фазу сушили над Na2SO4 и растворитель удаляли. Получали желаемый продукт в виде бесцветного аморфного вещества (0,394 г; выход 35,2%). Общее количество продукта (1,05 г; выход 94%) использовали на следующей стадии без дополнительной очистки. MS/ESI+ 443,3 [MH]+.
Стадия 8. Синтез (S)-4-(2-(4-(N-(трет-бутоксикарбонил)-2-(диметиламино)этилсульфонамидо)-3-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)-3,5-дихлорпиридин-1-оксида (173)
Раствор 4-(N-(трет-бутоксикарбонил)-2-(диметиламино)-этилсульфонамидо)-3-(циклопропилметокси)бензойной кислоты (0,411 г; 0,928 ммоль), EDC (0,411 г; 2,142 ммоль), DMAP (0,044 г; 0,357 ммоль) и соединения 3 (0,300 г; 0,714 ммоль) в DCM (30 мл) перемешивали при КТ в течение 24 ч. Смесь промывали 5%-ным раствором NaHCO3 и рассолом; органический слой сушили над Na2SO4 и растворитель удаляли. Неочищенный продукт очищали флэш-хроматографией на силикагелевом картридже (DCM : MeOH от 99:1 до 98:2), получая (S)-4-(2-(4-(N-(трет-бутоксикарбонил)-2-(диметиламино)этилсульфонамидо)-3-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид в виде бледно-желтого аморфного вещества (0,455 г; выход 75%). MS/ESI+ 844,4 [MH]+.
Стадия 9. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-{2-(диметиламино)этилсульфонамидо)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (172)
Раствор (S)-4-(2-(4-(N-(трет-бутоксикарбонил)-2-(диметиламино)-этилсульфонамидо)-3-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (0,455 г; 0,539 ммоль) и 4 М HCl (4 мл; 16,00 ммоль) в диоксане в DCM (25 мл) перемешивали при КТ в течение ночи. Растворитель удаляли, неочищенный продукт растворяли в этилацетате и промывали насыщ. NaHCO3 и рассолом. Органическую фазу сушили над Na2SO4, растворитель удаляли и неочищенный продукт фильтровали через SCX-картридж (DCM : MeOH=1:1; водн. NH3 : MeOH=1:9). Основную фазу распределяли между этилацетатом и рассолом, и водную фазу экстрагировали этилацетатом. Объединенные органические слои сушили над Na2SO4 и растворитель удаляли. Получали (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-пиридин-1-оксид в виде бледно-желтого аморфного вещества (0,321 г; выход 80%). MS/ESI+ 744,02 [MH]+. (с=0,53; МеОН).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 10.49 (br. s., 1Н), 9.69 (s, 1Н), 8.56 (s, 2Н), 7.59 (dd, 1Н), 7.52 (d, 1Н), 7.43 (d, 1Н), 7.22 (d, 1Н), 7.21 (d, 1Н), 7.07 (dd, 1Н), 7.06 (t, 1Н), 6.19 (dd, 1Н), 3.97 (d, 2Н), 3.93 (d, 2Н), 3.73-3.80 (m, 2Н), 3.62 (dd, 1Н), 3.45-3.56 (m, 2Н), 3.26-3.41 (m, 1Н), 2.80 (d, 6Н), 1.28-1.41 (m, 1Н), 1.15-1.27 (m, 1Н), 0.60-0.69 (m, 2Н), 0.51-0.60 (m, 2Н), 0.39-0.47 (m, 2Н), 0.24-0.38 (m, 2Н).
Стадия 10. Синтез (S)-1-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3,5-дихлорпиридин-4-ил)этил-3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонамидо)-бензоата (171)
К раствору (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонамидо)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (0,321 г; 0,431 ммоль) в THF (25 мл) добавляли раствор хлорида аммония (0,922 г; 17,24 ммоль) в воде (5 мл), затем цинковую пыль (1,409 г; 21,55 ммоль). Смесь перемешивали при КТ в течение 30 мин, затем фильтровали через набивку целита и фильтрат разбавляли этилацетатом и промывали рассолом. Органический слой сушили над Na2SO4 и растворитель удаляли. Неочищенный продукт очищали фильтрованием через силикагелевый картридж (DCM : MeOH, 99:1). Получали (S)-1-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3,5-дихлорпиридин-4-ил)этил-3-(циклопропилметокси)-4-(2-(диметиламино)этилсульфонамидо)бензоат в виде бледно-желтого аморфного вещества (0,250 г; выход 80%). MS/ESI+ 727,95 [MH]+. ; с=0,55; МеОН.
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 9.99 (br. s., 1Н), 9.71 (br. s., 1Н), 8.61 (s, 2Н), 7.57 (dd, 1Н), 7.49 (d, 1Н), 7.42 (d, 1Н), 7.22 (d, 0Н), 7.21 (d, 1Н), 7.08 (dd, 1Н), 7.07 (t, 1Н), 6.26 (dd, 1Н), 3.83-4.01 (m, 4Н), 3.65-3.79 (m, 3Н), 3.38-3.57 (m, 3Н), 2.79 (s, 5Н), 1.25-1.39 (m, 1Н), 1.06-1.27 (m, 2Н), 0.49-0.70 (m, 4Н), 0.22-0.48 (m, 4Н).
Пример 21
Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(2-(диметиламино)этилсульфонамидо)-бензоилокси)этил)пиридин-1-оксида (соединения 181)
Схема 21
Стадия 1. Синтез бензил-4-нитробензоата (188)
4-Нитробензоилхлорид (1 г; 5,39 ммоль) растворяли в безводном DCM (30 мл) в атмосфере N2; добавляли DMAP (0,329 г; 2,69 ммоль) и бензиловый спирт (0,616 мл; 5,93 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 4 суток. К реакционной смеси добавляли насыщ. раствор NaHCO3 и DCM; водную фазу дважды экстрагировали DCM, органические слои промывали 1 н. HCl, сушили над сульфатом натрия и упаривали досуха, получая желаемый продукт (1,5 г; 5,83 ммоль; выход 100%; чистота по UPLC-MS: 100%).
Стадия 2. Синтез бензил-4-аминобензоата (187)
Бензил-4-нитробензоат (1,5 г; 5,83 ммоль) растворяли в THF (40 мл), добавляли дигидрат SnCl2 (5,92 г; 26.2 ммоль) и смесь перемешивали при 45°С в течение 3 ч. К реакционной смеси добавляли насыщ. раствор NaHCO3 и EtOAc, смесь фильтровали через набивку целита. Раствор разделяли и водную фазу экстрагировали EtOAc. Объединенные органические слои сушили над сульфатом натрия и растворитель выпаривали. Желаемый продукт получали в виде бледно-желтого твердого вещества (1,25 г; 5,50 ммоль; выход 94%; MS/ESI+ 228,1 [MH]+) и использовали на следующей стадии без дополнительной очистки.
Стадия 3. Синтез бензил-4-(винилсульфонамидо)бензоата (186)
Бензил-4-аминобензоат (620 мг; 2,73 ммоль) растворяли в DCM (20 мл). Добавляли пиридин (1 мл; 12,36 ммоль), затем 2-хлорэтансульфонилхлорид (0,371 мл; 3,55 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь разбавляли DCM (20 мл) и промывали 1 н. HCl (2×50 мл). Органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный желаемый продукт (0,8 г; 2,52 ммоль, выход 92%) использовали на следующей стадии без дополнительной очистки.
Стадия 4. Синтез бензил-4-(2-(диметиламино)этилсульфонамидо)-бензоата (185)
Бензил-4-(винилсульфонамидо)бензоат (800 мг; 2,52 ммоль) растворяли в THF (30 мл). Добавляли 5,6 М диметиламин в EtOH (0,585 мл; 3,28 ммоль) и смесь перемешивали при комнатной температуре в течение ночи. Излишек реагентов и растворители удаляли при пониженном давлении, получая неочищенный желаемый продукт (0,89 г; 2,45 ммоль, выход 97%; MS/ESI+ 363 [MH]+), который использовали на следующей стадии без дополнительной очистки.
Стадия 5. Синтез бензил-4-(N-(трет-бутоксикарбонил)-2-(диметиламино)этилсульфонамидо)бензоата (184)
Бензил-4-(2-(диметиламино)этилсульфонамидо)бензоат (890 мг; 2,456 ммоль) растворяли в DCM (40 мл). Добавляли DMAP (300 мг; 2,456 ммоль) и ди-трет-бутилдикарбонат (536 мг; 2,456 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь промывали 1 н. HCl (2×20 мл), органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный желаемый продукт (0,96 г; 2,075 ммоль, выход 85%) использовали на следующей стадии без дополнительной очистки.
Стадия 6. Синтез 4-(N-(трет-бутоксикарбонил)-2-(диметиламино)этилсульфонамидо)бензойной кислоты (183)
Бензил-4-(N-(трет-бутоксикарбонил)-2-(диметиламино)-этилсульфонамидо)-бензоат (0,96 г; 2,075 ммоль) растворяли в тетрагидрофуране (40 мл). Добавляли формиат аммония (1,7 г; 27,0 ммоль), воду (20,0 мл) и 10%-ный (масс/масс.) Pd/C (0,200 г; 0,188 ммоль) и смесь перемешивали при комнатной температуре в течение 36 часов. Затем реакционную смесь фильтровали через набивку целита, разбавляли EtOAc (100 мл) и промывали водой (2×80 мл). Органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный желаемый продукт (0,53 г; 1,423 ммоль; выход 68,6%) использовали на следующей стадии без дополнительной очистки.
Стадия 7. Синтез (S)-4-(2-(4-(N-(трет-бутоксикарбонил)-2-(диметиламино)этилсупьфонамидо)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (182)
Соединение 3 (200 мг; 0,476 ммоль) растворяли в DCM (20 мл). Добавляли DMAP (29,1 мг; 0,238 ммоль), EDC (182 мг; 0,952 ммоль) и 4-(N-(трет-бутоксикарбонил)-2-(диметиламино)этилсульфонамидо)бензойную кислоту (266 мг; 0,714 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь промывали насыщ. водн. раствором NaHCO3 (30 мл) и 1 н. HCl (2×30 мл); органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный желаемый продукт (0,27 г; 0,349 ммоль, выход 73,2%) использовали на следующей стадии без дополнительной очистки.
Стадия 8. Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(2-(диметиламино)этилсульфонамидо)-бензоилокси)этил)пиридин-1-оксида (181)
(S)-4-(2-(4-(N-(трет-Бутоксикарбонил)-2-(диметиламино)-этилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (270 мг; 0,349 ммоль) растворяли в DCM (20 мл). Добавляли 4 н. раствор HCl в диоксане (3 мл; 12,00 ммоль) и полученную смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь упаривали досуха, перерастворяли в DCM (30 мл) и промывали 5%-ным водн. раствором NaHCO3 (30 мл). Органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: DCM : EtOAc от 8:2 до 7:3), получая 80 мг желаемого продукта в смеси с соответствующим производным спирта. Другие попытки очистки с использованием кристаллизации и SCX-картриджа были неудачными. Окончательно продукт очищали препаративной HPLC (метод 1). HPLC-фракции (20 мл; растворитель: H2O+CH3CN+0,1% TFA) разбавляли рассолом (20 мл) и DCM (40 мл). Органический слой сушили над Na2SO4 и упаривали досуха. Полученное таким образом масло растворяли в DCM (50 мл) и добавляли 4 н. раствор HCl в диоксане (0,1 мл); полученный раствор упаривали досуха, получая желаемый продукт в виде гидрохлоридной соли (10 мг; 0,014 ммоль; выход 4,0%; MS/ESI+ 673,79 [MH]+).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 10.75 (s, 1Н), 9.98 (br. s., 1Н), 8.56 (s, 2Н), 7.87-8.05 (m, 2Н), 7.25-7.41 (m, 2Н), 7.21 (d, 1Н), 7.21 (d, 1Н), 7.08 (dd, 1Н), 7.06 (t, 1Н), 6.20 (dd, 1Н), 3.93 (d, 2Н), 3.70-3.81 (m, 1Н), 3.58-3.66 (m, 1Н), 3.40-3.53 (m, 4Н), 2.79 (s, 6Н), 1.09-1.32 (m, 1Н), 0.47-0.65 (m, 2Н), 0.16-0.46 (m, 2Н).
Пример 22
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(2-морфолиноэтилсульфонамидо)-бензоилокси)этил)пиридин-1-оксида (соединения 189)
Схема 22
Стадия 1. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-нитробензоилокси)этил)-пиридин-1-оксида (192)
4-Метокси-3-нитробензойную кислоту (244 мг; 1,237 ммоль), DMAP (76 мг; 0,619 ммоль), EDC (474 мг; 2,475 ммоль), соединение 3 (520 мг; 1,237 ммоль) растворяли в DCM (60 мл) и полученную смесь перемешивали при комнатной температуре в течение 1 ч. Смесь промывали 1 н. раствором HCl (2×60 мл) и насыщ. водн. раствором NaHCO3 (1×60 мл). Органическую фазу сушили над Na2SO4 и упаривали досуха. Неочищенный желаемый продукт (0,71 г; 1,185 ммоль, выход 96%) использовали на следующей стадии без дополнительной очистки.
Стадия 2. Синтез (S)-4-(2-(3-амино-4-метоксибензоилокси)-2-(3-(цикпопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (191)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-метокси-3-нитробензоилокси)этил)пиридин-1-оксид (710 мг; 1,185 ммоль) растворяли в тетрагидрофуране (100 мл). Добавляли дигидрат SnCl2 (1336 мг; 5,92 ммоль) и полученную смесь перемешивали при 40°С в течение 24 часов. Реакционную смесь разбавляли 5%-ным водным раствором NaHCO3 (300 мл) и EtOAc (400 мл): получали густую эмульсию. Эмульсию фильтровали через набивка целита, получая таким образом две прозрачные фазы. Органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на силикагеле (элюент: от DCM : EtOAc, 8:2, до чистого EtOAc, затем EtOAc: МеОН, 95:5), получая желаемый продукт (180 мг; 0,316 ммоль; выход 26,7%; MS/ESI+ 569 [MH]+).
Стадия 3. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(винилсульфонамидо)-бензоилокси)-этил)пиридин-1-оксида (190)
(S)-4-(2-(3-Амино-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (180 мг; 0,316 ммоль) растворяли в DCM (50 мл). Добавляли пиридин (0,077 мл; 0,948 ммоль) и 2-хлорэтансульфонилхлорид (61,8 мг; 0,379 ммоль) и смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь разбавляли DCM (50 мл) и промывали 1 н. HCl (2×50 мл). Органический слой сушили над Na2SO4 и упаривали досуха, получая неочищенный желаемый продукт (199 мг; 0,302 ммоль; выход 95%), который использовали на следующей стадии без дополнительной очистки.
Стадия 8. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(2-морфолиноэтил-сульфонамидо)-бензоилокси)этил)пиридин-1-оксида (189)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-метокси-3-(винилсульфонамидо)бензоилокси)этил)пиридин-1-оксид (199 мг; 0,302 ммоль) растворяли в THF (30 мл). Добавляли морфолин (26,3 мкл; 0,302 ммоль) и смесь перемешивали при комнатной температуре в течение 24 часов. Реакционную смесь выливали в воду (50 мл) и экстрагировали EtOAc (2×50 мл). Органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на силикагелевом картридже (элюент: DCM : EtOAc от 8:2 до 1:1, затем чистый EtOAc), получая 80 мг желаемого продукта в виде коричневатого масла. Проводили дополнительную очистку с использованием препаративной LC-MS. После элюирования собирали фракции и упаривали их досуха; остаток растворяли в DCM (10 мл) и обрабатывали 4 н. раствором HCl в диоксане (100 мкл); раствор упаривали досуха, получая желаемый продукт в форме гидрохлоридной соли в виде белого аморфного вещества (30 мг; 0,038 ммоль; выход 12,7%; MS/ESI+ 746,1 [MH]+, [αD]=-38,8; с=0,36; DCM).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 10.51 (s, 1Н), 9.65 (br. s., 1Н), 8.55 (s, 2Н), 7.91 (dd, 1Н), 7.88 (d, 1Н), 7.18-7.26 (m, 3Н), 7.06 (dd, 1Н), 7.07 (t, 1Н), 6.19 (dd, 1Н), 3.95 (s, 3Н), 3.89-3.94 (m, 4Н), 3.41-3.81 (m, 10Н), 3.00-3.27 (m, 2Н), 1.15-1.28 (m, 1Н), 0.51-0.64 (m, 2Н), 0.26-0.41 (m, 2Н).
Пример 23
Синтез 3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(3-((2S,5R)-2,5-диметилпиперазин-1-ил)-3-оксопропанамидо)-4-метоксибензоилокси)этил)пиридин-1-оксида (193)
Схема 23
Стадия 1. Синтез (S)-4-(2-(3-(трет-бутоксикарбониламино)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)-3,5-дихлорпиридин-1-оксида (198)
Соединение 3 (500 мг; 1,2 ммоль) и 3-(трет-бутоксикарбониламино)-4- метоксибензойную кислоту (481 мг; 1,8 ммоль) растворяли в DMF (5 мл). Добавляли DMAP (176 мг; 1,44 ммоль) и EDC (690 мг; 3,6 ммоль) и смесь перемешивали при КТ в течение ночи. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органическую фазу промывали 1 н. HCl (2х), насыщенным раствором NaHCO3 и рассолом, сушили над Na2SO4 и упаривали под вакуумом, получая 650 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 2. Синтез (S)-4-(2-(3-амино-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (197)
(S)-4-(2-(3-(трет-Бутоксикарбониламино)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (650 мг; 0,97 ммоль) растворяли в смеси 4 М HCl/диоксан (5 мл) и смесь перемешивали при КТ в течение ночи. Реакционную смесь разбавляли насыщ. раствором NaHCO3 и затем экстрагировали этилацетатом. Органическую фазу промывали водой, сушили над Na2SO4 и упаривали под вакуумом, получая 600 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 3. Синтез (S)-4-(2-(3-(3-трет-бутокси-3-оксопропанамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-этил)-3,5-дихлорпиридин-1-оксида (196)
(S)-4-(2-(3-Амино-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (100 мг; 0,17 ммоль) и 3-трет-бутокси-3-оксопропановую кислоту (31 мкл; 0,2 ммоль) растворяли в DMF (1,5 мл). Добавляли DMAP (24 мг; 0,2 ммоль) и EDC (65 мг; 0,34 ммоль) и смесь перемешивали при КТ в течение 2 ч. Реакцию гасили водой и продукт экстрагировали этилацетатом. Органическую фазу промывали 1 н. HCl (2х), насыщенным раствором NaHCO3 и рассолом, сушили над Na2SO4 и упаривали под вакуумом, получая 150 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 4. Синтез (S)-4-(2-(3-(2-карбоксиацетамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)-3,5-дихлорпиридин-1-оксида (195)
(S)-4-(2-(3-(3-трет-Бутокси-3-оксопропанамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)-3,5-дихлорпиридин-1-оксид (150 мг; неочищенный) растворяли в смеси 4 М HCl/диоксан (1,5 мл) и смесь перемешивали при КТ в течение 6 ч. Реакционную смесь разбавляли водой и затем экстрагировали этилацетатом. Органическую фазу сушили над Na2SO4 и упаривали под вакуумом, получая 140 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 5. Синтез 4-((S)-2-(3-(3-((2S,5R)-4-(трет-бутоксикарбонил)-2,5-диметилпиперазин-1-ил)-3-оксопропанамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (194)
(S)-4-(2-(3-(2-Карбоксиацетамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (40 мг; 0,06 ммоль) и (2R,5S)-трет-бутил-2,5-диметилпиперазин-1-карбоксилат (26 мг; 0,12 ммоль) растворяли в DMF (2 мл), затем добавляли DMAP (15 мг; 0,12 ммоль) и EDC (34 мг; 0,18 ммоль) и смесь перемешивали при КТ в течение 2 ч. Реакционную смесь разбавляли водой и затем экстрагировали этилацетатом. Органическую фазу сушили над Na2SO4 и упаривали под вакуумом, получая 50 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 6. Синтез 3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(3-((2S,5R)-2,5-диметилпиперазин-1-ил)-3-оксопропанамидо)-4-метоксибензоилокси)этил)пиридин-1-оксида (193)
4-((S)-2-(3-(3-((2S,5R)-4-(трет-Бутоксикарбонил)-2,5-диметилпиперазин-1-ил)-3-оксопропанамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (50 мг; неочищенный) растворяли в смеси 4 М HCl/диоксан (1,5 мл) и смесь перемешивали при КТ в течение 5 ч. Растворитель выпаривали под вакуумом и неочищенный продукт очищали препаративной HPLC (метод 2), получая 20 мг конечного продукта.
1Н ЯМР (400 МГц, ацетон) δ млн-1 10.18-10.46 (bs, 1Н), 9.16 (d, J=1,76 Гц, 1Н), 8.24 (s, 2Н), 7.79 (dd, J=8,82; 2,21 Гц, 1Н), 7.31 (m, 1Н), 7.17-7.25 (m, 1Н), 7.07-7.15 (m, 2Н), 6.91 (t, J=75,00 Гц, 1Н), 6.19-6.44 (m, 1Н), 3.92-4.06 (m, 5Н), 3.66-3.75 (m, 1Н), 3.48-3.62 (m, 2Н), 3.41 (dd, J=14,11; 4,41 Гц, 1Н), 3.19 (m, 6Н), 1.21-1.43 (m, 6Н), 1.14 (d, J=9,26 Гц, 1Н), 0.60 (dd, J=8,16; 1,54 Гц, 2Н), 0.40 (d, J=4,41 Гц, 2Н).
MS/ESI+ 727,95 [MH]+: 751,4.
Соединение, приведенное в Таблице 15, получали, используя стадии и методики синтеза, аналогичные описанным в примере 23, схема 23, стадии 1-3, 6, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 24
Синтез 3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(2-((2S,5R)-2,5-диметилпиперазин-1-ил)ацетамидо)-4-метоксибензоилокси)этил)пиридин-1-оксида (соединения 200)
Схема 24
Стадия 1. Синтез 3-(2-бромацетамидо)-4-метоксибензойной кислоты (203)
3-Амино-4-метоксибензойную кислоту (300 г; 1,8 ммоль) растворяли в DCM (10 мл). Добавляли DMAP (440 мг; 3,6 ммоль) и к смеси медленно по каплям добавляли 2-бромацетилхлорид (225 мкл; 2,7 ммоль). Реакционную смесь перемешивали при КТ в течение 1 ч, затем разбавляли DCM и промывали 1 н. HCl (х2). Органическую фазу сушили над Na2SO4 и упаривали под вакуумом, получая 300 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки (выход: 58%).
Стадия 2. Синтез (S)-3,5-дихлор-4-(2-(3-(2-хлорацетамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)пиридин-1-оксида (202)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(гидроксиэтил)пиридин-1-оксид, соединение 3 (200 мг; 0,5 ммоль) и 3-(2-бромацетамидо)-4-метоксибензойную кислоту (288 мг; 1 ммоль) растворяли в DMF (5 мл), затем добавляли EDC (288 мг; 1,5 ммоль) и DMAP (122 мг; 1 ммоль). Смесь перемешивали при КТ в течение ночи, затем гасили путем добавления воды и экстрагировали AcOEt. Органическую фазу промывали 1 н. HCl (2х), насыщенным раствором NaHCO3 и рассолом, сушили над Na2SO4 и упаривали под вакуумом, получая 140 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 3. Синтез 4-((S)-2-(3-(2-((2S,5R)-4-(трет-бутоксикарбонил)-2,5-диметилпиперазин-1-ил)ацетамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (201)
(S)-3,5-Дихлор-4-(2-(3-(2-хлорацетамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксид (30 мг; 0,05 ммоль) растворяли в DMF (1,5 мл), затем добавляли (2R,5S)-трет-бутил-2,5-диметилпиперазин-1-карбоксилат (32 мг; 0,15 ммоль) и K2CO3 (14 мг; 0,1 ммоль) и смесь перемешивали при КТ в течение ночи. Реакционную смесь разбавляли водой и затем экстрагировали этилацетатом. Органическую фазу промывали водой, сушили над Na2SO4 и упаривали досуха, получая 40 мг неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 4. Синтез 3,5-дихлор-4-((S)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(2-((2S,5R)-2,5-диметилпиперазин-1-ил)ацетамидо)-4-метоксибензоилокси)этил)пиридин-1-оксида (200)
4-((S)-2-(3-(2-((2S,5R)-4-(трет-Бутоксикарбонил)-2,5-диметилпиперазин-1-ил)ацетамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (40 мг; 0,05 ммоль) растворяли в 4 М HCl/диоксан (1,5 мл) и смесь перемешивали при КТ в течение 5 ч, затем ее упаривали под вакуумом и очищали полупрепаративной HPLC, получая 25 мг конечного соединения (выход: 69%). MS/ESI+ 723,4 [MH]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 9.00-9.27 (m, 1Н), 8.25 (s, 2Н), 8.14 (s, 1Н), 7.63-7.86 (m, 1Н), 7.33 (d, J=1,76 Гц, 1Н), 7.00-7.27 (m, 3Н), 6.91 (t, J=75,00 Гц, 1Н), 6.26-6.39 (m, 1Н), 4.06 (s, 2Н), 3.82-4.03 (m, 3Н), 3.66-3.77 (m, 1Н), 3.28-3.51 (m, 3Н), 2.88-3.00 (m, 2Н), 2.80-2.87 (m, 1Н), 2.35-2.47 (m, 1Н), 2.09 (m, 3Н), 1.19-1.36 (m, 1Н), 0.98-1.05 (m, 3Н), 0.60 (dd, J=8,16; 1,54 Гц, 2Н), 0.32-0.46 (m, 2Н).
Соединения, перечисленные в Таблице 16, получали, используя стадии и методики синтеза, аналогичные описанным в примере 24, схема 24, стадии 1-4, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 25
Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонилокси)-4-(2-морфолиноэтокси)-бензоилокси)этил)пиридин-1-оксида (соединения 207)
Схема 25
Стадия 1. Синтез 2-(бензилокси)-5-формилфенил-метансульфоната (212)
Указанное в заголовке соединение получали из 4-(бензилокси)-3-гидроксибензальдегида, следуя методике, описанной в примере 13, стадия 5, с использованием метилсульфонилхлорида вместо 2-хлорэтансульфонилхлорида.
Стадия 2. Синтез 4-(бензилокси)-3-(метилсульфонилокси)-бензойной кислоты (211)
Указанное в заголовке соединение получали из 2-(бензилокси)-5-формилфенилметансульфоната, следуя методике, описанной в примере 13, стадия 2.
Стадия 3. Синтез (S)-4-(2-(4-(бензилокси)-3-(метилсульфонилокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (210)
Соединение 3 (1,5 г; 3,6 ммоль) и 4-(бензилокси)-3-(метилсульфонилокси)бензойную кислоту (1,5 г; 4,7 ммоль) растворяли в DMF (10 мл), затем добавляли EDC (2,1 г; 10,8 ммоль) и DMAP (484 мг; 4 ммоль). Смесь перемешивали при КТ в течение 2 ч, затем гасили путем добавления воды. Осадок отфильтровывали и далее растворяли в AcOEt. Органическую фазу промывали 1 н. HCl (2х), насыщенным раствором NaHCO3 (2х) и рассолом, сушили над Na2SO4 и упаривали под вакуумом. Неочищенное вещество кристаллизовали из EtOH, получая 1,8 г желаемого соединения (выход: 69%).
MS/ESI+ 724,55 [MH]+.
1Н ЯМР (400 МГц, хлороформ-d) δ млн-1 8.16 (s, 2Н), 8.01 (d, J=1,96 Гц, 1Н), 7.93 (dd, J=8,61; 1,96 Гц, 1Н), 7.34-7.49 (m, 5Н), 7.18 (d, J=8,61 Гц, 1Н), 7.10 (d, J=9,00 Гц, 1Н), 6.98-7.06 (m, 2Н), 6.38-6.63-6.85 (t, 1Н, CHF2), 6.24 (dd, J=9,98; 4,11 Гц, 1Н), 5.20 (s, 2Н), 3.91 (dd, J=6,85; 4,89 Гц, 2Н), 3.69 (dd, J=14,09; 10,17 Гц, 1Н), 3.31 (dd, J=14,09; 4,30 Гц, 1Н), 3.10 (s, 3Н), 1.28 (d, J=7,04 Гц, 1Н), 0.59-0.73 (m, 2Н), 0.34-0.45 (m, 2Н).
Стадия 4. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-гидрокси-3-(метилсульфонилокси)-бензоилокси)этил)пиридин-1-оксида (209)
(S)-4-(2-(4-(Бензилокси)-3-(метилсульфонилокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (1,8 г; 2,5 ммоль) растворяли в этилацетате (50 мл), добавляли 5%-ный Pd/Ba2SO4 (5,85 г; 2,75 ммоль) и смесь гидрировали в аппарате Парра (Н2: 30 ф/кв. дюйм (207 кПа)) в течение 1 ч. Катализатор отфильтровывали через набивку целита и растворитель выпаривали под вакуумом, получая 1,5 г неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
MS/ESI+ 634,43 [MH]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 10.08 (bs, 1Н), 8.19 (s, 2Н), 8.01 (d, J=2,20 Гц, 1Н), 7.90 (dd, J=8,38; 1,76 Гц, 1Н), 7.30 (d, J=1,76 Гц, 1Н), 7.13-7.23 (m, 3Н), 6.91 (t, J=75,00 Гц, 1Н), 6.31 (dd, J=9,70; 4,41 Гц, 1Н), 3.91-4.03 (m, 2Н), 3.74 (dd, J=14,11; 9,70 Гц, 1Н), 3.43 (dd, J=14,11; 4,41 Гц, 1Н), 3.34 (s, 3Н), 1.22-1.36 (m, 1Н), 0.52-0.66 (m, 2Н), 0.31-0.45 (m, 2Н).
Стадия 5. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонилокси)-4-(2-морфолиноэтокси)бензоилокси)этил)пиридин-1-оксида (208)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-гидрокси-3-(метилсульфонилокси)бензоилокси)этил)пиридин-1-оксид (1,5 г; 2,4 ммоль) растворяли в DMF (10 мл), затем добавляли 4-(2- хлорэтил)морфолин (1,1 г; 7,2 ммоль) и K2CO3 (431 мг; 3,12 ммоль) и смесь перемешивали при 40°С в течение 4 ч. Реакцию гасили водой, осадок отфильтровывали и растворяли в этилацетате (50 мл). Органическую фазу промывали 1 н. HCl (4,8 мл; 4,8 ммоль), водой (50 мл), насыщенным раствором NaHCO3 (50 мл) и насыщенным раствором NaCl, сушили над Na2SO4 и упаривали под вакуумом, получая 1,8 г неочищенного продукта, который использовали на следующей стадии без какой-либо дополнительной очистки.
Стадия 6. Синтез гидрохлорида (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонилокси)-4-(2-морфолиноэтокси)бензоилокси)этил)-пиридин-1-оксида (207)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(3-(метилсульфонилокси)-4-(2-морфолиноэтокси)бензоилокси)-этил)пиридин-1-оксид растворяли в ацетоне и добавляли смесь 7 М HCl/диоксан (343 мкл; 2,5 ммоль). Растворитель выпаривали, полученную соль растворяли в CHCl3 и по каплям добавляли в Et2O (200 мл). Осадок отфильтровывали, получая 1,4 г конечного соединения (выход: 78%). MS/ESI+ 747,3 [MH]+.
1Н ЯМР (400 МГц, ацетон) δ млн-1 13.86-14.37 (bs, 1Н), 8.25 (s, 2Н), 8.06 (dd, J=8,60; 1,98 Гц, 1Н), 8.01 (d, J=2,21 Гц, 1Н), 7.41 (d, J=8,82 Гц, 1Н), 7.32 (d, J=1,76 Гц, 1Н), 7.13-7.24 (m, 2Н), 6.91 (t, J=75,00 Гц, 1Н), 6.32 (dd, J=9,70; 4,41 Гц, 1Н), 4.89 (t, J=4,63 Гц, 2Н), 4.15 (d, J=11,91 Гц, 2Н), 3.88-4.05 (m, 4Н), 3.52-3.82 (m, 5Н), 3.36-3.49 (m, 4Н), 3.30 (d, J=9,26 Гц, 2Н), 1.27 (m, 1Н), 0.60 (dd, J=7,94; 1,32 Гц, 2Н), 0.29-0.47 (m, 2Н).
Соединение, приведенное в Таблице 17, получали в соответствии со стадиями и методиками синтеза, аналогичными описанным в примере 25, схема 25, стадии 1-5, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 26
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(2-(4-метилпиперазин-1-ил)этилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (215)
Схема 26
Стадия 1. Синтез бензил-4-метокси-3-нитробензоата (222)
К раствору 4-метокси-3-нитробензойной кислоты (1 г; 5,07 ммоль) в безводном DMF (50 мл) добавляли карбонат цезия (0,992 г; 3,04 ммоль) и смесь перемешивали при КТ в течение 1 ч. Добавляли бензилбромид (0,724 мл; 6,09 ммоль) и реакционную смесь перемешивали при КТ в течение 2 ч. Добавляли дополнительное количество карбоната цезия (0,413 г; 1,268 ммоль) и бензилбромида (0,302 мл; 2,54 ммоль), перемешивая при той же температуре в течение 6 ч. Смесь подкисляли 1 М водн. раствором HCl и дважды экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (петролейный эфир: этилацетат, от 95:5 до 80:20), получая бензил-4-метокси-3-нитробензоат в виде белого твердого вещества (1,450 г; 5,05 ммоль; выход 100%).
Стадия 2. Синтез бензил-3-амино-4-метоксибензоата (221)
К суспензии бензил-4-метокси-3-нитробензоата (1,450 г; 5,05 ммоль) в этаноле (38 мл) и воде (16 мл) добавляли хлорид аммония (0,189 г; 3,534 ммоль), затем порошок железа (1,693 г; 30,29 ммоль). Реакционную смесь нагревали до 80°С в течение 2,5 ч. Смесь фильтровали и фильтрат упаривали досуха. Остаток растворяли в этилацетате и промывали водой и рассолом; органическую фазу сушили над Na2SO4 и растворитель удаляли под вакуумом, получая бензил-3-амино-4-фторбензоат в виде желтого масла (1,0837 г; выход 83,3%). Этот продукт использовали без какой-либо дополнительной очистки. MS/ESI+ 258,0 [MH]+.
Стадия 3. Синтез бензил-4-метокси-3-(винилсульфонамидо)-бензоата (220)
Раствор бензил-3-амино-4-метоксибензоата (1,0837 г; 4,21 ммоль) и пиридина (4,09 мл; 50,5 ммоль) в DCM (55 мл) охлаждали до 0°С. Добавляли 2-хлорэтансульфонилхлорид (0,528 мл; 5,05 ммоль) и реакционную смесь перемешивали в атмосфере азота при КТ в течение ночи. Добавляли вторую порцию 2-хлорэтансульфонилхлорида (0,220 мл; 2,106 ммоль) и смесь перемешивали при этой же температуре в течение еще 4 ч. Смесь промывали 1 н. водн. раствором HCl и рассолом; органическую фазу сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (петролейный эфир: этилацетат, 7:3), получая бензил-4-метокси-3-(винилсульфонамидо)бензоат в виде бледно-желтого масла (1,1423 г; выход 78%). MS/ESI+ 348,0 [MH]+.
Стадия 4. Синтез бензил-4-метокси-3-(2-(4-метилпиперазин-1-ил)этилсульфонамидо)бензоата (219)
К раствору бензил-4-метокси-3-(винилсульфонамидо)бензоата (1,1423 г; 3,29 ммоль) в этаноле (40 мл) добавляли N-метилпиперазин (0,548 мл; 4,93 ммоль) и смесь перемешивали при КТ в течение ночи. Растворитель удаляли под вакуумом, остаток растворяли в этилацетате и промывали водн. раствором NaHCO3 и рассолом; органическую фазу сушили над Na2SO4, растворитель выпаривали и неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (DCM : MeOH, 95:5), получая бензил-4-метокси-3-(2-(4-метилпиперазин-1-ил)этилсульфонамидо)бензоат в виде желтого масла (1,38 г; выход 94%). MS/ESI+ 448,1 [MH]+.
Стадия 5. Синтез бензил-3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензоата (218)
К раствору бензил-4-метокси-3-(2-(4-метилпиперазин-1-ил)-этилсульфонамидо)бензоата (1,38 г; 3,08 ммоль) в DCM (30 мл) добавляли DMAP (0,414 г; 3,39 ммоль) и ди-трет-бутилдикарбонат (0,740 г; 3,39 ммоль) и смесь перемешивали при КТ в течение 4 ч. Добавляли дополнительное количество DMAP (0,828 г; 6,79 ммоль) и ди-трет-бутилдикарбоната (1,48 г; 6,78 ммоль) и перемешивание продолжали в течение 24 ч при той же температуре. Смесь промывали водой, 5%-ным водн. раствором NaHCO3 и рассолом; органическую фазу сушили над Na2SO4 и упаривали досуха, получая бензил-3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензоат в виде белого твердого вещества (1,680 г; выход 99%). Этот неочищенный продукт использовали без какой-либо дополнительной очистки. MS/ESI+ 548,2 [MH]+.
Стадия 6. Синтез 3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензойной кислоты (217)
Смесь бензил-3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензоата (1,680 г; 3,07 ммоль) и каталитического количества 10%-ного Pd/C (суспендированного в 3 мл воды) в МеОН (25 мл) гидрировали в аппарате Парра при давлении 30 ф/кв. дюйм (207 кПа) в течение 5 ч. Катализатор отфильтровывали и растворитель выпаривали досуха, получая 3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензойную кислоту в виде желтого твердого вещества (1,400 г; выход 100%). Этот продукт использовали на следующей стадии без очистки. MS/ESI+ 458,1 [MH]+.
Стадия 7. Синтез (S)-4-(2-(3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (216)
Смесь 3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензойной кислоты (0,4 г; 0,874 ммоль), соединения 3 (0,334 г; 0,795 ммоль), EDC (0,457 г; 2,384 ммоль) и DMAP (0,146 г; 1,192 ммоль) в DCM (30 мл) перемешивали при КТ в течение 4 ч. Смесь промывали водой, водн. раствором NaHCO3 и рассолом; органическую фазу сушили над Na2SO4 и растворитель удаляли под вакуумом. Остаток очищали флэш-хроматографией на колонке с силикагелем (DCM : MeOH, 98:2), получая (S)-4-(2-(3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-этил)-3,5-дихлорпиридин-1-оксид в виде белого твердого вещества (0,261 г; выход 38,2%). MS/ESI+ 859,3 [MH]+.
Стадия 8. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(2-(4-метилпиперазин-1- ил)этилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (215)
К раствору (S)-4-(2-(3-(N-(трет-бутоксикарбонил)-2-(4-метилпиперазин-1-ил)этилсульфонамидо)-4-метоксибензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (0,261 г; 0,304 ммоль) в DCM (20 мл) добавляли 4 М HCl в диоксане (1,518 мл; 6,07 ммоль) и реакционную смесь перемешивали при КТ в течение ночи. Летучие вещества удаляли под вакуумом, остаток обрабатывали водн. раствором NaHCO3 и дважды экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над Na2SO3 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (DCM : MeOH от 98:2 до 90:10), получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(2-(4-метилпиперазин-1-ил)этилсульфонамидо)бензоилокси)этил)пиридин-1-оксид в виде беловатой пены (0,0703 г; выход 30,5%). MS/ESI+ 759,41 [MH]+. (с=0,33; МеОН).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 9.14 (br. s., 1Н), 8.53 (s, 2Н), 7.96 (d, 1Н), 7.82 (dd, 1Н), 7.14-7.24 (m, 3Н), 7.00-7.08 (m, 1Н), 7.06 (t, 1Н), 6.20 (dd, 1Н), 3.92-4.00 (m, 2Н), 3.91 (s, 3Н), 3.59 (dd, 1Н), 3.33 (dd, 1Н), 3.19-3.27 (m, 2Н), 2.67-2.78 (m, 2Н), 2.30-2.43 (m, 4Н), 2.17-2.30 (m, 4Н), 2.11 (s, 3Н), 1.09-1.30 (m, 1Н), 0.50-0.65 (m, 2Н), 0.26-0.46 (m, 2Н).
Соединения, перечисленные в Таблице 18, получали, используя стадии и методики синтеза, аналогичные описанным в примере 26, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 27
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(2-гидроксиэтокси)-4-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (соединения 225)
Схема 27
Стадия 1. Синтез бензил-3-гидрокси-4-нитробензоата (232)
К раствору 3-гидрокси-4-нитробензойной кислоты (1,1 г; 5,976 ммоль) в безводном DMF (55 мл) добавляли бикарбонат натрия (0,606 г; 7,205 ммоль) и смесь перемешивали при КТ в течение 45 минут. Добавляли бензилбромид (0,857 мл; 7,22205 ммоль) и реакционную смесь нагревали до 50°С в течение 5 ч. Добавляли вторую порцию бикарбоната натрия (0,115 г; 1,365 ммоль) и бензилбромида (0,162 мл; 1,365 ммоль), реакционную смесь нагревали до 50°С в течение еще 1 часа и оставляли стоять при КТ в течение ночи. Добавляли 1 н. водн. раствор HCl и смесь дважды экстрагировали этилацетатом. Объединенные органические слои промывали рассолом, сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (петролейный эфир: этилацетат, 98:2), получая бензил-3-гидрокси-4-нитробензоат в виде желтого твердого вещества (1,600 г; выход 100%).
Стадия 2. Синтез бензил-4-нитро-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоата (231)
К раствору бензил-3-гидрокси-4-нитробензоата (1,6 г; 5,86 ммоль) в безводном DMF (50 мл) добавляли 2-(2-бромэтокси)тетрагидро-2Н-пиран (1,238 мл; 8,20 ммоль) и K2CO3 (1,133 г; 8,20 ммоль) и реакционную смесь нагревали до 100°С в течение 48 ч. Добавляли вторую порцию 2-(2-бромэтокси)тетрагидро-2Н-пирана (0,442 мл; 2,93 ммоль) и K2CO3 (0,405 г; 2,93 ммоль) и смесь перемешивали при 100°С в течение еще 6 ч. Реакционную смесь разбавляли 1 н. раствором HCl и экстрагировали несколько раз этилацетатом. Объединенные органические слои промывали рассолом, сушили над Na2SO4 и упаривали досуха. Остаток очищали флэш-хроматографией на колонке с силикагелем (петролейный эфир: этилацетат, от 95:5 до 90:10), получая бензил-4-нитро-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоат в виде желтого масла (0,7884 г; выход 33,5%). MS/ESI+ 424,0 [MNa]+.
Стадия 3. Синтез бензил-4-амино-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоата (230)
К суспензии бензил-4-нитро-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоата (0,707 г; 1,761 ммоль) в этаноле (15 мл) и воде (7 мл) добавляли хлорид аммония (0,066 г; 1,233 ммоль), затем порошок железа (0,590 г; 10,57 ммоль). Полученную смесь нагревали до 80°С в течение 2 ч, охлаждали до КТ и фильтровали. Фильтрат упаривали досуха, остаток растворяли в этилацетате и промывали водой и рассолом. Органическую фазу сушили над Na2SO4 и растворитель удаляли под вакуумом, получая бензил-4-амино-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоат в виде желтого масла (0,652 г; выход 100%). Этот продукт использовали без какой-либо дополнительной очистки. MS/ESI+ 372,1 [MNa]+.
Стадия 4. Синтез бензил-4-(метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоата (229)
Раствор бензил-4-амино-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)- бензоата (0,652 г; 1,755 ммоль) в пиридине (20 мл) охлаждали до 0°С и добавляли метансульфонилхлорид (0,150 мл; 1,931 ммоль). Реакционную смесь перемешивали при КТ в течение ночи и нагревали до 50°С в течение 2 ч. После охлаждения до КТ добавляли дополнительное количество метансульфонилхлорида (0,232 мл; 2,984 ммоль) в течение 24 ч. Растворитель удаляли под вакуумом, остаток растворяли в этилацетате и промывали 1 н. водн. раствором HCl и затем рассолом. Органический слой сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (петролейный эфир: этилацетат, 75:25), получая бензил-4-(метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоат в виде желтого масла (0,720 г; выход 91%). MS/ESI+ 472,0 [MNa]+.
Стадия 5. Синтез бензил-4-(N-(2-морфолиноэтил)-метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)-бензоата (228)
К раствору бензил-4-(метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоата (0,720 г; 1,602 ммоль) в DMF (25 мл) добавляли K2CO3 (0,531 г; 3,84 ммоль) и гидрохлорид 4-(2-хлорэтил)морфолина (0,358 г; 1,922 ммоль). Реакционную смесь нагревали до 70°С в течение 5 ч и до 80°С в течение 1 ч. Смесь распределяли между этилацетатом и водой; органическую фазу промывали рассолом, сушили над Na2SO3 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (100% этилацетат), получая бензил-4-(N-(2-морфолиноэтил)метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоат в виде желтого масла (0,680 г; выход 75%). MS/ESI+ 563,2 [MH]+.
Стадия 6. Синтез 4-(N-(2-морфолиноэтил)метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензойной кислоты (227)
Смесь бензил-4-(N-(2-морфолиноэтил)метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоата (0,680 г; 1,209 ммоль) и суспензии в воде (2 мл) 10%-ного (масс/масс.) Pd/C (0,643 г; 0,604 ммоль) в метаноле (15 мл) гидрировали в аппарате Парра при давлении 30 ф/кв. дюйм (207 кПа) в течение 3,5 ч. Катализатор отфильтровывали и фильтрат упаривали досуха, получая 4-(N-(2-морфолиноэтил)метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензойную кислоту в виде бледно-красного масла (0,428 г; выход 74,9%). Этот продукт использовали без какой-либо дополнительной очистки. MS/ESI+ 473,1 [MH]+.
Стадия 7. Синтез 3,5-дихлор-4-((28)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(N-(2-морфолиноэтил)-метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)-бензоилокси)этил)пиридин-1-оксида (226)
Смесь 4-(N-(2-морфолиноэтил)метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензойной кислоты (0,428 г; 0,906 ммоль), (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксида (0,346 г; 0,823 ммоль), EDC (0,474 г; 2,470 ммоль) и DMAP (0,151 г; 1,235 ммоль) в DCM (20 мл) перемешивали при КТ в течение 4 ч. Реакционную смесь промывали насыщ. водн. раствором NH4Cl, водн. раствором NaHCO3 и рассолом; органическую фазу сушили над Na2SO4 и растворитель удаляли под вакуумом. Этот неочищенный продукт фильтровали через силикагелевый картридж (DCM : MeOH, 99:1), получая указанное в заголовке соединение в виде белой пены (0,566 г; выход 79%). MS/ESI+ 874,2 [MH]+.
Стадия 8. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(2-гидроксиэтокси)-4-(N-(2-морфолиноэтил)метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (225)
3,5-Дихлор-4-((2S)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-(N-(2-морфолиноэтил)метилсульфонамидо)-3-(2-(тетрагидро-2Н-пиран-2-илокси)этокси)бензоилокси)этил)пиридин-1-оксид (0,250 г; 0,286 ммоль) наносили на SCX-картридж, элюируя сначала смесью 1:1 DCM : MeOH, а затем смесью 9:1 МеОН : водн. 32%-ный NH4OH. Летучие вещества удаляли под вакуумом и остаток очищали флэш-хроматографией на колонке с силикагелем (DCM : MeOH от 99:1 до 95:5), получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(2-гидроксиэтокси)-4-(N-(2-морфолиноэтил)метилсульфонамидо)бензоилокси)-этил)пиридин-1-оксид в виде белой пены (0,113 г; выход 50,0%). MS/ESI+ 790,53 [MH]+. ; с=0,32; МеОН.
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.56 (s, 2Н), 7.58 (d, 1Н), 7.58 (dd, 1Н), 7.40 (d, 1Н), 7.24 (d, 1Н), 7.20 (d, 1Н), 7.09 (dd, 1Н), 7.06 (t, 1Н), 6.19 (dd, 1Н), 4.88 (t, 1Н), 4.05-4.26 (m, 2Н), 3.94 (d, 2Н), 3.79 (q, 2Н), 3.69 (t, 2Н), 3.64 (dd, 1Н), 3.39-3.46 (m, 4Н), 3.35 (dd, 1Н), 3.08 (s, 3Н), 2.32 (t, 2Н), 2.16-2.29 (m, 4Н), 1.10-1.32 (m, 1Н), 0.48-0.66 (m, 2Н), 0.23-0.46 (m, 2Н).
Пример 28
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонилокси)-4-(морфолинометил)-бензоилокси)этил)пиридин-1-оксида (соединения 233)
Схема 28
Стадия 1. Синтез метил-4-формил-3-гидроксибензоата (239)
4-Формил-3-гидроксибензойную кислоту (1,2 г; 7,22 ммоль) растворяли в МеОН (10 мл). Добавляли SOCl2 (1,054 мл; 14,45 ммоль) и реакционную смесь перемешивали при 60°С в течение 3 ч до полного завершения реакции. Реакционную смесь концентрировали, неочищенное вещество растирали в гексане и фильтровали, получая метил-4-формил-3-гидроксибензоат (1,3 г; 7,22 ммоль; выход 100%). MS/ESI+ 181,04 [MH]+.
Стадия 2. Синтез метил-3-(бензилокси)-4-формилбензоата (238)
Метил-4-формил-3-гидроксибензоат (312 мг; 1,732 ммоль) растворяли в DMF (3 мл). Добавляли (бромметил)бензол (592 мг; 3,46 ммоль) и K2CO3 (359 мг; 2,60 ммоль) и реакционную смесь перемешивали при КТ в течение 3 суток до полного завершения реакции. Реакционную смесь разбавляли водой и осадок отфильтровывали, растворяли в этилацетате и промывали водой (2х). Органическую фазу сушили над Na2SO4 и концентрировали под вакуумом, получая метил-3-(бензилокси)-4-формилбензоат (423 мг; 1,565 ммоль; выход 90%). MS/ESI+ 271,09 [MH]+.
Стадия 3. Синтез метил-3-(бензилокси)-4-(морфолинометил)-бензоата (237)
Метил-3-(бензилокси)-4-формилбензоат (423 мг; 1,565 ммоль) растворяли в безводном THF (3,5 мл), добавляли морфолин (205 мг; 2,348 ммоль) и уксусную кислоту (141 мг; 2,348 ммоль) и смесь перемешивали при КТ в течение 30 мин. Добавляли триацетоксигидроборат натрия (498 мг; 2,348 ммоль) и смесь перемешивали при КТ в течение 2 ч до полного завершения реакции. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органическую фазу промывали насыщ. раствором NaHCO3, водой и рассолом, сушили над Na2SO4 и концентрировали под вакуумом, получая метил-3-(бензилокси)-4-(морфолинометил)бензоат (491 мг; 1,438 ммоль; выход 92%). MS/ESI+ 342,17 [MH]+.
Стадия 4. Синтез метил-3-гидрокси-4-(морфолинометил)бензоата (236)
Метил-3-(бензилокси)-4-(морфолинометил)бензоат (491 мг; 1,438 ммоль) растворяли в МеОН (20 мл) и затем добавляли 5%-ный Pd/C (306 мг; 2,88 ммоль). Раствор встряхивали в атмосфере водорода (35 ф/кв. дюйм (242 кПа)) в аппарате Парра в течение 1 ч. Катализатор отфильтровывали и растворитель удаляли под вакуумом, получая метил-3-гидрокси-4-(морфолинометил)бензоат (317 мг; 1,262 ммоль; выход 88%). MS/ESI+ 252,12 [MH]+.
Стадия 5. Синтез метил-3-(метилсульфонилокси)-4-(морфолинометил)бензоата (235)
Метил-3-гидрокси-4-(морфолинометил)бензоат (317 мг; 1,262 ммоль) растворяли в DCM (10 мл). Добавляли метансульфонилхлорид (217 мг; 1,892 ммоль) и TEA (191 мг; 1,892 ммоль) и реакционную смесь перемешивали при КТ в течение 1 ч до полного завершения реакции. Реакционную смесь разбавляли DCM и экстрагировали водой (2х), рассолом, сушили над Na2SO4 и концентрировали под вакуумом, получая метил-3-(метилсульфонилокси)-4-(морфолинометил)бензоат (420 мг; 1,275 ммоль; выход 101%). MS/ESI+ 330,10 [MH]+.
Стадия 6. Синтез 3-(метилсульфонилокси)-4-(морфолинометил)бензойной кислоты (234)
Метил-3-(метилсульфонилокси)-4-(морфолинометил)бензоат (420 мг; 1,275 ммоль) растворяли в THF (6 мл). Добавляли 1 М LiOH (2,5 мл; 1,275 ммоль) и реакционную смесь перемешивали при КТ в течение ночи до полного завершения реакции. Реакционную смесь разбавляли 1 н. раствором HCl с целью нейтрализации и концентрировали под вакуумом, получая 3-(метилсульфонилокси)-4-(морфолинометил)бензойную кислоту (400 мг; 1,268 ммоль; выход 99%). MS/ESI+ 316,08 [MH]+.
Стадия 7. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонилокси)-4-(морфолинометил)бензоилокси)этил)пиридин-1-оксида (233)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксид (60 мг; 0,143 ммоль), 3-(метилсульфонилокси)-4-(морфолинометил)бензойную кислоту (400 мг; 1,268 ммоль), N,N-диметилпиридин-4-амин (20,93 мг; 0,171 ммоль) и гидрохлорид N1-((этилимино)метилен)-N3,N3-диметилпропан-1,3-диамина (219 мг; 1,142 ммоль) растворяли в DMF (2 мл). Реакционную смесь перемешивали при КТ в течение 3 суток до полного завершения реакции. Реакционную смесь разбавляли водой и экстрагировали AcOEt. Органическую фазу промывали водой, сушили над Na2SO4 и концентрировали под вакуумом. Неочищенный продукт очищали препаративной HPLC, получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонилокси)-4-(морфолинометил)бензоилокси)этил)пиридин-1-оксид (30 мг; 0,042 ммоль; выход 29,3%). MS/ESI+ 716,9 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 8.56 (s, 2Н), 7.94-8.01 (m, 1Н), 7.90- 7.92 (m, 1Н), 7.63-7.78 (m, 1Н), 7.18-7.24 (m, 2Н), 7.02-7.11 (m, 2Н), 6.07-6.26 (m, 1Н), 3.86-3.98 (m, 2Н), 3.47-3.69 (m, 11Н), 2.35-2.42 (m, 4Н), 1.13-1.27 (m, 1Н), 0.50-0.63 (m, 2Н), 0.30-0.41 (m, 2Н).
Соединения, перечисленные в Таблице 19, получали в соответствии со стадиями и методиками синтеза, аналогичными описанным в примере 28, схема 28, стадии 2-7, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 29
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-((4-гидроксипиперидин-1-ил)метил)бензоилокси)этил)пиридин-1-оксида (соединения 242)
Схема 29
Стадия 1. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-формилбензоилокси)этил)пиридин-1-оксида (243)
EDC (593 мг; 3,09 ммоль) добавляли к раствору соединения 3 (1 г; 2,38 ммоль), 2-(3-(4-нитробензил)-2,4,5-триоксоимидазолидин-1-ил)уксусной кислоты (464 мг; 3,09 ммоль) и DMAP (87 мг; 0,714 ммоль) в CH2Cl2 (10 мл) при КТ в атмосфере азота. Смесь перемешивали при КТ в течение ночи. Затем смесь разбавляли CH2Cl2 и промывали насыщенным раствором NaHCO3, 0,1 н. раствором HCl и рассолом. Органическую фазу сушили над Na2SO4 и растворитель выпаривали. Получали (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-формилбензоилокси)этил)пиридин-1-оксид в виде бледно-желтого аморфного вещества (1,24 г; выход 94%).
Стадия 2. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-((4-гидроксипиперидин-1-ил)метил)-бензоилокси)-этил)пиридин-1-оксида (242)
Раствор (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-формилбензоилокси)этил)пиридин-1-оксида (250 мг; 0,452 ммоль) и пиперидин-4-ола (55 мг; 0,543 ммоль) в безводном THF (12 мл) перемешивали в атмосфере аргона в течение 15 минут при КТ. Затем добавляли NaCNBH3 (71,9 мг; 0,34 ммоль) и СН3СООН (13 мкл; 0,27 ммоль) и смесь перемешивали при КТ в течение 24 ч. Растворитель удаляли, неочищенный продукт растворяли в этилацетате и промывали насыщ. раствором NaHCO3 и рассолом. Органическую фазу сушили над Na2SO4 и растворитель удаляли. Получали (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-((4-гидроксипиперидин-1-ил)метил)бензоилокси)-этил)пиридин-1-оксид в виде желтого аморфного вещества (122 мг; 0,191 ммоль), которое очищали препаративной HPLC, получая 47 мг указанного в заголовке соединения в виде белого твердого вещества (выход 32%). MS/ESI+ 637,49 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 8.56 (s, 2Н), 7.94 (d, J=7,83 Гц, 2Н), 7.43 (d, J=7,83 Гц, 2Н), 7.16-7.27 (m, 2Н), 7.08 (d, J=10,27 Гц, 2Н), 6.12-6.25 (m, 1Н), 4.53 (d, J=2,69 Гц, 1Н), 3.92 (d, J=6,85 Гц, 2Н), 3.55-3.70 (m, 1Н), 3.40-3.50 (m, 3Н), 2.63 (d, J=10,52 Гц, 2Н), 2.04 (m, 2Н), 1.68 (m, 2Н), 1.39 (m, 2Н), 1.11-1.27 (m, 1Н), 0.55 (d, J=6,85 Гц, 2Н), 0.34 (d, J=3,42 Гц, 2Н).
Соединения, перечисленные в Таблице 20, получали, используя стадии и методики синтеза, аналогичные описанным в примере 29, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 30
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(2-метокси-5-((N-(2-морфолиноэтил)-метилсульфонамидо)метил)бензоилокси)этил)пиридин-1-оксида (251)
Схема 30
Стадия 1. Синтез метил-5-формил-2-гидроксибензоата (258)
Раствор 5-формил-2-гидроксибензойной кислоты (1,6 г; 9,63 ммоль) и каталитического количества конц. H2SO4 в МеОН (100 мл) нагревали до температуры дефлегмации в течение 48 ч. Смесь распределяли между EtOAc и водн. 5%-ным NaHCO3; органическую фазу сушили над сульфатом натрия и растворитель удаляли, получая метил-5-формил-2-гидроксибензоат (1,66 г; 9,21 ммоль; выход 96%; MS/ESI+ 180,9 [MH]+). Этот продукт использовали без очистки.
Стадия 2. Синтез метил-5-формил-2-метоксибензоата (257)
Смесь метил-5-формил-2-гидроксибензоата (0,500 г; 2,78 ммоль), карбоната калия (0,767 г; 5,55 ммоль) и подметана (0,208 мл; 3,33 ммоль) в ацетонитриле (20 мл) перемешивали при КТ в течение 1 ч. Добавляли дополнительное количество подметана (0,312 мл; 4,99 ммоль) и реакционную смесь нагревали, используя облучение микроволнами, при 100°С в течение 1 ч и затем в течение еще 30 минут. Смесь распределяли между EtOAc и 1 н. HCl и органическую фазу промывали 1 н. NaOH и рассолом. Органический слой сушили над сульфатом натрия и растворитель удаляли, получая метил-5-формил-2-метоксибензоат (0,352 г; 1,813 ммоль; выход 65%; MS/ESI+ 194,9 [MH]+), который использовали без очистки.
Стадия 3. Синтез (Е)-метил-2-метокси-5-((метоксиимино)-метил)бензоата (256)
Раствор гидрохлорида метил-5-формил-2-метоксибензоата (0,352 г; 1,813 ммоль) и O-метилгидроксиламина (0,167 г; 1,994 ммоль) в пиридине (20 мл) нагревали при 60°С в течение 2 ч. Растворитель удаляли под вакуумом и неочищенный продукт распределяли между EtOAc и 1 н. HCl. Органическую фазу промывали рассолом и сушили над сульфатом натрия; растворитель удаляли, получая (Е)-метил-2-метокси-5-((метоксиимино)метил)бензоат (0,395 г; 1,770 ммоль; выход 98%; MS/ESI+ 224,0 [MH]+). Неочищенный продукт использовали без очистки.
Стадия 4. Синтез метил-5-(аминометил)-2-метоксибензоата (255)
Смесь (Е)-метил-2-метокси-5-((метоксиимино)метил)бензоата (0,395 г; 1,770 ммоль), 10%-ного Pd/C (каталитического количества) и конц. HCl (0,108 мл; 1,740 ммоль) в МеОН (50 мл) гидрировали в аппарате Парра под давлением 35 ф/кв. дюйм (242 кПа) в течение 40 ч. Катализатор отфильтровывали, фильтрат упаривали досуха и остаток очищали фильтрованием на SCX-картридже (DCM : MeOH, 1:1; водн. конц. NH4OH : MeOH, 1:9). Основные фракции упаривали, получая метил-5-(аминометил)-2-метоксибензоат (0,271 г; 1,388 ммоль; выход 78%).
Стадия 5. Синтез метил-2-метокси-5-(метилсульфонамидометил)-бензоата (254)
К раствору метил-5-(аминометил)-2-метоксибензоата (0,271 г; 1,388 ммоль) и пиридина (1,123 мл; 13.88 ммоль) в DCM (30 мл) по каплям добавляли метансульфонилхлорид (0,162 мл; 2,082 ммоль) и смесь перемешивали при КТ в течение 2 ч. Добавляли дополнительное количество метансульфонилхлорида (0,216 мл; 2,776 ммоль), в течение 22 ч перемешивая при той же температуре. Смесь разбавляли DCM и промывали 2 н. раствором HCl и водой; органический слой сушили над сульфатом натрия и растворитель удаляли. Неочищенный продукт очищали фильтрованием через силикагелевый картридж (DCM : EtOAc, 90:10), получая метил-2-метокси-5-(метилсульфонамидометил)бензоат (0,304 г; 1,112 ммоль; выход 80%; MS/ESI+ 274,0 [MH]+).
Стадия 6. Синтез 2-метокси-5-(метилсульфонамидометил)-бензойной кислоты (253)
К раствору метил-2-метокси-5-(метилсульфонамидометил)бензоата (0,304 г; 1,112 ммоль) в THF (15 мл) добавляли 1 н. водный раствор LiOH (1,335 мл; 1,335 ммоль) и смесь перемешивали при КТ в течение ночи. Добавляли дополнительное количество 1 н. LiOH (0,700 мл; 0,700 ммоль) и реакционную смесь перемешивали при этой же температуре в течение еще 8 ч. Смесь распределяли между EtOAc и 1 н. HCl; органический слой сушили над сульфатом натрия и растворитель удаляли, получая 2-метокси-5-(метилсульфонамидометил)бензойную кислоту (0,170 г; 0,656 ммоль; выход 59%; MS/ESI+ 259,9 [MH]+).
Стадия 7. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(2-метокси-5-(метилсульфонамидометил)-бензоилокси)этил)пиридин-1-оксида (252)
К смеси (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксида (0,230 г; 0,546 ммоль), EDC (0,282 г; 1,476 ммоль) и DMAP (0,160 г; 1,311 ммоль) в DCM (20 мл) добавляли 2-метокси-5-(метилсульфонамидометил)бензойную кислоту (0,170 г; 0,656 ммоль) и реакционную смесь перемешивали при КТ в течение 1 ч. Смесь промывали 1 н. HCl и 5%-ным водн. раствором NaHCO3; органическую фазу сушили над сульфатом натрия, растворитель удаляли и неочищенный продукт очищали препаративной HPLC (метод 3), получая (S)-3,5-дихлор-4-(2- (3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(2-метокси-5- (метилсульфонамидометил)бензоилокси)этил)пиридин-1-оксид (0,145 г; 0,219 ммоль; выход 40%; MS/ESI+ 661,26 [MH]+, [αD]=-27,80, с=0,49; МеОН).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.55 (s, 2Н), 7.65 (d, 1Н), 7.48-7.56 (m, 2Н), 7.21 (d, 1Н), 7.18 (d, 1Н), 7.14 (d, 1Н), 7.06 (dd, 1Н), 7.07 (t, 1Н), 6.19 (dd, 1Н), 4.12 (s, 2Н), 3.94 (dd, 1Н), 3.90 (dd, 1Н), 3.79 (s, 3Н), 3.52 (dd, 1Н), 3.32 (dd, 1Н), 2.86 (s, 3Н), 1.09-1.33 (m, 1Н), 0.49-0.66 (m, 2Н), 0.27-0.43 (m, 2Н).
Стадия 8. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(2-метокси-5-((N-(2-морфолиноэтил)-метилсульфонамидо)метил)бензоилокси)этил)пиридин-1-оксида (251)
К раствору (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(2-метокси-5-(метилсульфонамидометил)-бензоилокси)-этил)пиридин-1-оксида (40 мг; 0,06 ммоль) в DMF (2 мл) добавляли K2CO3 (17 мг; 0,12 ммоль) и 4-(2-хлорэтил)морфолин (18 мг; 0,12 ммоль). Реакционную смесь нагревали до 45°С в течение 4 ч и до 60°С в течение 2 ч. Смесь распределяли между этилацетатом и водой; органическую фазу промывали рассолом, сушили над Na2SO3 и упаривали досуха. Неочищенный продукт очищали препаративной HPLC (метод 2), получая желаемый продукт (15 мг; выход 32%). MS/ESI+ 773,8 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 8.56 (s, 2Н), 7.70 (m, 1Н), 7.55 (d, J=8,38 Гц, 1Н), 6.98-7.32 (m, 5Н), 6.18 (d, J=3,97 Гц, 1Н), 4.32 (s, 2Н), 3.91 (t, J=6,39 Гц, 2Н), 3.79 (s, 3Н), 3.28 (m, 5Н), 3.48 (m, 1Н), 3.19 (m, 2Н), 3.06 (s, 3Н), 2.20-2.35 (m, 6Н), 1.21 (m, 1Н), 0.56 (d, J=7,06 Гц, 2Н), 0.35 (d, J=3,53 Гц, 2Н).
Пример 31
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (соединения 259)
Схема 31
Стадия 1. Синтез бензил-4-метокси-3-нитробензоата (264)
К раствору 4-метокси-3-нитробензойной кислоты (1 г; 5,07 ммоль) в безводном DMF (50 мл) добавляли бикарбонат натрия (0,511 г; 6,09 ммоль) и бензилбромид (0,724 мл; 6,09 ммоль) и реакционную смесь перемешивали при 50°С в течение 4 ч. Смесь обрабатывали 1 н. раствором HCl и дважды экстрагировали AcOEt; объединенные органические слои промывали рассолом, сушили над Na2SO4 и упаривали досуха. Неочищенный продукт очищали флэш-хроматографией на силикагеле (петролейный эфир/AcOEt, 9/1), получая бензил-4-метокси-3-нитробензоат (1,2539 г; 4,36 ммоль; выход 86%; MS/ESI+ 288,1 [MH]+).
Стадия 2. Синтез бензил-3-амино-4-метоксибензоата (263)
К суспензии бензил-4-метокси-3-нитробензоата (1,2539 г; 4,36 ммоль) в EtOH (25 мл) и воде (12 мл) добавляли хлорид аммония (0,163 г; 3,06 ммоль), затем порошок железа (1,463 г; 26.2 ммоль) и реакционную смесь нагревали при 80°С в течение 2 ч. Нерастворенное вещество отфильтровывали и фильтрат упаривали досуха. Остаток растворяли в EtOAc и промывали водой и рассолом; органическую фазу сушили над Na2SO4 и растворитель удаляли, получая бензил-3-амино-4-метоксибензоат (1,035 г; 4,02 ммоль; выход 92%; MS/ESI+ 257,9 [MH]+). Этот продукт использовали без какой-либо дополнительной очистки.
Стадия 3. Синтез бензил-4-метокси-3-(метилсульфонамидо)бензоата (262)
К раствору бензил-3-амино-4-метоксибензоата (1,035 г; 4,02 ммоль) в пиридине (40 мл), охлажденному до 0°С, добавляли метансульфонилхлорид (0,376 мл; 4,83 ммоль) и смесь перемешивали при КТ в течение ночи. Растворитель выпаривали, и остаток распределяли между EtOAc и 1 н. HCl; органическую фазу промывали рассолом и сушили над Na2SO4. Растворитель удаляли под вакуумом и неочищенный продукт очищали путем растирания с диэтиловым эфиром, получая бензил-4-метокси-3-(метилсульфонамидо)бензоат (0,920 г; 2,74 ммоль; выход 68,2%; MS/ESI+ 336,0 [MH]+).
Стадия 4. Синтез бензил-4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)метилсульфонамидо)бензоата (261)
Смесь бензил-4-метокси-3-(метилсульфонамидо)бензоата (0,500 г; 1,491 ммоль), гидрохлорида 2-хлор-1-(4-метилпиперазин-1-ил)этанона (0,381 г; 1,789 ммоль) и карбоната калия (0,495 г; 3,58 ммоль) в DMF (15 мл) нагревали при 70°С в течение 1 ч. Смесь разбавляли EtOAc и промывали водой и несколько раз рассолом. Органическую фазу сушили над сульфатом натрия, растворитель удаляли и неочищенный продукт очищали флэш-хроматографией на колонке с силикагелем (EtOAc : МеОН от 90:10 до 80:20), получая бензил-4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)метилсульфонамидо)бензоат (0,561 г; 1,180 ммоль; выход 79%; MS/ESI+ 475,9 [MH]+).
Стадия 5. Синтез 4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)метилсульфонамидо)бензойной кислоты (260)
Бензил-4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)-метилсульфонамидо)бензоат (0,555 г; 1,167 ммоль) растворяли в МеОН (22,200 мл) и добавляли 10%-ный (масс/масс.) Pd/C (0,248 г; 0,233 ммоль). Полученную смесь гидрировали в аппарате Парра при давлении 30 ф/кв. дюйм (207 кПа) в течение 1 ч. Катализатор отфильтровывали и промывали, используя МеОН, EtOAc и DCM. Объединенные фильтраты упаривали досуха, получая 4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)-метилсульфонамидо)бензойную кислоту (0,339 г; 0,880 ммоль; выход 75%; MS/ESI+ 386,1 [MH]+).
Стадия 5. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (259)
4-Метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)-метилсульфонамидо)бензойную кислоту (0,200 г; 0,519 ммоль) суспендировали в безводном DCM (3,459 мл) и, перемешивая при комнатной температуре, последовательно добавляли (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксид (0,145 г; 0,346 ммоль), EDC (0,199 г; 1,038 ммоль) и DMAP (0,0423 г; 0,346 ммоль). Реакцию в этой суспензии проводили в течение 24 ч при КТ. Смесь упаривали и остаток очищали флэш-хроматографией на колонке с силикагелем SNAP (DCM/MeOH, от 95/5 до 93/7), получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-метокси-3-(N-(2-(4-метилпиперазин-1-ил)-2-оксоэтил)метилсульфонамидо)бензоилокси)-этил)пиридин-1-оксид (197 мг; 0,250 ммоль; выход 72,3%; MS/ESI+ 787,24 [MH]+, [αD]=-41,60, с=0,5; МеОН).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.52 (s, 2Н), 8.15 (d, 1Н), 7.99 (dd, 1Н), 7.16-7.26 (m, 3Н), 7.06 (dd, 1Н), 7.06 (t, 1Н), 6.19 (dd, 1Н), 4.43 (s, 2Н), 3.94 (d, 2Н), 3.93 (s, 3Н), 3.62 (dd, 1Н), 3.33-3.45 (m, 4Н), 3.33 (dd, 1Н), 3.08 (s, 3Н), 2.20-2.36 (m, 4Н), 2.17 (s, 3Н), 1.07-1.39 (m, 1Н), 0.49-0.66 (m, 2Н), 0.22-0.46 (m, 2Н).
Пример 32
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(N-(2-морфолиноэтил)-метилсульфонамидо)-4-(трифторметокси)бензоилокси)этил)пиридин-1-оксида (соединения 265):
Схема 32
Стадия 1. Синтез 3-нитро-4-(трифторметокси)бензойной кислоты (270)
К раствору 4-(трифторметокси)бензойной кислоты (900 мг; 4,37 ммоль) в конц. H2SO4 (9 мл), охлажденному до 0°С, добавляли раствор нитрата калия (486 мг; 4,80 ммоль) в конц. H2SO4 (4,5 мл) и реакционную смесь перемешивали при этой же температуре в течение 2 ч. Смесь обрабатывали, используя H2O (50 мл), и экстрагировали EtOAc (150 мл). Органическую фазу промывали рассолом (2×100 мл), сушили над Na2SO4 и упаривали досуха, получая 3-нитро-4-(трифторметокси)бензойную кислоту (2) (1,05 г; 4,18 ммоль; выход 96%; MS/ESI+ 252,1 [MH]+). Этот продукт использовали без очистки.
Стадия 2. Синтез метил-3-нитро-4-(трифторметокси)бензоата (269)
К раствору 3-нитро-4-(трифторметокси)бензойной кислоты (1,05 г; 4,18 ммоль) в МеОН (40 мл) добавляли конц. H2SO4 (0,446 мл) и полученную смесь нагревали до температуры дефлегмации в течение ночи. Растворитель удаляли под вакуумом и к остатку добавляли насыщ. водный раствор NaHCO3 (60 мл). Смесь экстрагировали EtOAc (2×100 мл), объединенные органические слои сушили над Na2SO4, фильтровали и упаривали, получая метил-3-нитро-4-(трифторметокси)бензоат (1,05 г; 3,96 ммоль; выход 95%; MS/ESI+ 265,9 [MH]+).
Стадия 3. Синтез метил-3-амино-4-(трифторметокси)бензоата (268)
К раствору этил-3-нитро-4-(трифторметокси)бензоата (1,0 г; 3,77 ммоль) в МеОН (20 мл) добавляли каталитическое количество Pd/C (10%-ного, масс/масс.) и смесь гидрировали в аппарате Парра при давлении 20 ф/кв. дюйм (138 кПа) в течение 2 ч. Катализатор отфильтровывали и фильтрат упаривали досуха, получая метил-3-амино-4-(трифторметокси)бензоат (730 мг; 3,10 ммоль; выход 82%; MS/ESI+ 235,9 [MH]+).
Стадия 4. Синтез метил-3-(N-(2-морфолиноэтил)-метилсульфонамидо)-4-(трифторметокси)бензоата (267)
К раствору метил-3-амино-4-(трифторметокси)бензоата (730 мг; 3,10 ммоль) в безводном пиридине (8 мл), охлажденному при 0°С, добавляли метансульфонилхлорид (0,721 мл; 9,31 ммоль), смесь оставляли нагреваться до КТ и перемешивали в течение ночи. Растворитель удаляли под вакуумом, остаток обрабатывали насыщ. водным раствором NaHCO3 (50 мл) и экстрагировали EtOAc (2×150 мл). Объединенные органические слои сушили над Na2SO4, фильтровали и упаривали при пониженном давлении. Остаток растирали с Et2O (20 мл), получая 1,00 г неочищенного продукта. 500 мг этого неочищенного продукта растворяли в безводном DMF (10 мл), добавляли гидрохлорид 4-(2-хлорэтил)морфолина (401 мг; 2,156 ммоль), затем K2CO3 (496 мг; 3,59 ммоль) и реакционную смесь нагревали при 100°С в течение ночи. Растворитель удаляли под вакуумом и остаток распределяли между EtOAc и водой; органическую фазу промывали рассолом и сушили над сульфатом натрия. Растворитель удаляли и неочищенный продукт очищали флэш-хроматографией на силикагеле (DCM : EtOAc от 90:10 до 100% EtOAc), получая метил-3-(N-(2-морфолиноэтил)метилсульфонамидо)-4-(трифторметокси)бензоат (600 мг; 1,407 ммоль; выход 91% (более 50% в расчете на исходное вещество); MS/ESI+ 426,9 [MH]+).
Стадия 5. Синтез гидрохлорида 3-(N-(2-морфолиноэтил)-метилсульфонамидо)-4-(трифторметокси)бензойной кислоты (266)
К раствору метил-3-(N-(2-морфолиноэтил)метилсульфонамидо)-4-(трифторметокси)бензоата (600 мг; 1,407 ммоль) в диоксане (10 мл) добавляли 6 М водный HCl (2,814 мл; 16,89 ммоль) и смесь нагревали при 100°С в течение 4 ч. Летучие вещества удаляли под вакуумом, получая гидрохлорид 3-(N-(2-морфолиноэтил)метилсульфонамидо)-4-(трифторметокси)бензойной кислоты (600 мг; 1,337 ммоль; выход 95%; MS/ESI+ 412,9 [MH]+).
Стадия 6. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(N-(2-морфолиноэтил)-метилсульфонамидо)-4-(трифторметокси)бензоилокси)этил)пиридин-1-оксида (265)
Смесь 3-(N-(2-морфолиноэтил)метилсульфонамидо)-4-(трифторметокси)бензойной кислоты (236 мг; 0,571 ммоль), (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)пиридин-1-оксида (200 мг; 0,476 ммоль), EDC (128 мг; 0,666 ммоль) и DMAP (116 мг; 0,952 ммоль) в безводном DCM (10 мл) перемешивали при КТ в течение 3 суток. Реакционную смесь обрабатывали 1 М раствором HCl и дважды экстрагировали DCM. Объединенные органические слои промывали рассолом, сушили над Na2SO4, фильтровали и упаривали. Неочищенный продукт очищали флэш-хроматографией на силикагеле (DCM/MeOH от 98/2 до 90/10). Потребовалась дополнительная очистка флэш-хроматографией на силикагелевом картридже (DCM/MeOH, 99/1) для получения (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(N-(2-морфолиноэтил)метилсульфонамидо)-4-(трифторметокси)бензоилокси)этил)пиридин-1-оксида (28 мг; 0,034 ммоль; выход 7,22%; MS/ESI+ 814,06 [MH]+, [αD]=-20,55, с=0,510; DCM).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.54 (s, 2Н), 8.11 (d, 1Н), 8.11 (dd, 1Н), 7.55-7.66 (m, 1Н), 7.23 (d, 1Н), 7.20 (d, 1Н), 7.09 (dd, 1Н), 7.06 (t, 1Н), 6.20 (dd, 1Н), 3.83-4.03 (m, 2Н), 3.55-3.80 (m, 3Н), 3.31-3.42 (m, 5Н), 3.15 (s, 3Н), 2.09-2.46 (m, 6Н), 1.06-1.38 (m, 1Н), 0.45-0.69 (m, 2Н), 0.21-0.45 (m, 2Н).
Пример 33
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(N-(2-(4-метилпиперазин-1-ил)этил)-метилсульфонамидо)-4-(трифторметил)бензоилокси)этил)пиридин-1-оксида (соединения 271)
Схема 33
Стадия 1. Синтез метил-3-(N-(2-гидроксиэтил)-метилсульфонамидо)-4-(трифторметил)бензоата (275)
Смесь метил-3-(N-(метилсульфонил)метилсульфонамидо)-4-(трифторметил)бензоата (1,12 г; 2,98 ммоль), 2-бромэтанола (0,847 мл; 11,94 ммоль) и K2CO3 (825 мг; 5,97 ммоль) в CH3CN (20 мл) разливали в два флакона и нагревали, используя облучение микроволнами, при 110°С в течение 2 ч. Растворитель удаляли при пониженном давлении и остаток очищали флэш-хроматографией на силикагеле (петролейный эфир/EtOAc, 80/20), получая метил-3-(N-(2-гидроксиэтил)метилсульфонамидо)-4-(трифторметил)бензоат (700 мг; 2,051 ммоль; выход 69%; MS/ESI+ 342,0 [MH]+).
Стадия 2. Синтез метил-3-(N-(2-бромэтил)метилсульфонамидо)-4-(трифторметил)бензоата (274)
Суспензию PS-PPh3 (содержание: 1,88 ммоль/г; 2,3 г; 1,324 ммоль) в безводном DCM (40 мл) перемешивали в течение 30 минут при КТ; добавляли CBr4 (874 мг; 2,64 ммоль) и метил-3-(N-(2-гидроксиэтил)-метилсульфонамидо)-4-(трифторметил)бензоат (500 мг; 1,465 ммоль) и полученную смесь перемешивали при КТ в течение 1,5 ч. Смолу отфильтровывали и фильтрат упаривали досуха, получая метил-3-(N-(2-бромэтил)метилсульфонамидо)-4-(трифторметил)бензоат (590 мг; 1,460 ммоль; количественный выход; MS/ESI+ 403,8-405,7 [MH]+). Это промежуточное соединение использовали без какой-либо дополнительной очистки.
Стадия 3. Синтез метил-3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)-4-(трифторметил)бензоата (273)
Смесь метил-3-(N-(2-бромэтил)метилсульфонамидо)-4-(трифторметил)бензоата (780 мг; 1,930 ммоль), K2CO3 (400 мг; 2,89 ммоль) и 1-метилпиперазина (0,536 мл; 4,82 ммоль) в CH3CN (40 мл) разливали в два флакона и нагревали при 130°С в течение 1 ч, используя облучение микроволнами (MW). Растворитель удаляли при пониженном давлении и остаток смешивали с неочищенным продуктом, полученным при выполнении той же реакции с количеством исходного соединения 58 мг (0,143 ммоль). Объединенные неочищенные продукты очищали флэш-хроматографией на силикагеле (DMC/MeOH от 97/3 до 95/5), получая метил-3-((N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)-4-(трифторметил)бензоат (600 мг; 1,418 ммоль; выход 47%; MS/ESI+ 424,0 [MH]+).
Стадия 4. Синтез 3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)-4-(трифторметил)бензойной кислоты (272)
К раствору метил-3-(N-(2-(4-метилпиперазин-1-ил)этил)-метилсульфонамидо)-4-(трифторметил)бензоата (460 мг; 1,086 ммоль) в диоксане (11 мл) добавляли 6 н. водный раствор HCl (2,173 мл; 13,04 ммоль) и реакционную смесь нагревали при 100°С в течение 2 ч. Летучие вещества удаляли под вакуумом, получая гидрохлорид 3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)-4-(трифторметил)-бензойной кислоты (440 мг; 0,988 ммоль; выход 92%; MS/ESI+ 409,8 [MH]+).
Стадия 5. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(N-(2-(4-метилпиперазин-1-ил)этил)-метилсульфонамидо)-4-(трифторметил)бензоилокси)этил)пиридин-1-оксида (271)
Смесь гидрохлорида 3-(N-(2-(4-метилпиперазин-1-ил)этил)-метилсульфонамидо)-4-(трифторметил)бензойной кислоты (234 мг; 0,525 ммоль), (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-гидроксиэтил)пиридин-1-оксида (200 мг; 0,476 ммоль), EDC (128 мг; 0,666 ммоль) и DMAP (116 мг; 0,952 ммоль) в безводном DCM (8 мл) перемешивали при КТ в течение ночи. Реакционную смесь обрабатывали 1 М раствором HCl и водную фазу дважды экстрагировали DCM. Объединенные органические слои промывали рассолом, сушили над Na2SO4, фильтровали и упаривали. Неочищенный продукт очищали флэш-хроматографией на силикагеле (DCM/MeOH от 97/3 до 90/10), получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(N-(2-(4-метилпиперазин-1-ил)этил)метилсульфонамидо)-4-(трифторметил)бензоилокси)этил)пиридин-1-оксид (186 мг; 0,229 ммоль; выход 48,2%; MS/ESI+ 811,19 [MH]+, [αD]=-19,36, с=0,500; DCM).
1Н ЯМР (300 МГц, DMSO-d6) δ млн-1 8.54 и 8.55 (s, 2Н), 8.17 (d, 1Н), 8.10 (s, 1Н), 7.96 (dd, 1Н), 7.18-7.27 (m, 2Н), 7.06-7.13 (m, 1Н), 7.06 и 7.07 (t, 1Н), 6.10-6.32 (m, 1Н), 3.92 (t, 2Н), 3.75-4.07 (m, 1Н), 3.45-3.75 (m, 2Н), 3.37 (dt, 1Н), 3.19 (s, 3Н), 2.30-2.43 (m, 4Н), 2.06-2.24 (m, 4Н), 1.92-2.05 (m, 2Н), 1.98 и 2.00 (s, 3Н), 1.14-1.32 (m, 1Н), 0.44-0.70 (m, 2Н), 0.12-0.44 (m, 2Н).
Пример 34
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(5-(N-(2-морфолиноэтил)-метилсульфонамидо)-2-(трифторметил)бензоилокси)этил)пиридин-1-оксида, соли 2,2,2-трифторуксусной кислоты (соединения 276)
Схема 34
Стадия 1. Синтез 5-нитро-2-(трифторметил)бензойной кислоты (282)
К раствору 2-метил-4-нитро-1-(трифторметил)бензола (1 г; 4,87 ммоль) в CH3CN (30 мл) добавляли H5IO6 (5,56 г; 24,37 ммоль) и CrO3 (0,126 мл; 3,40 ммоль) и реакционную смесь перемешивали при КТ в течение 2 ч. Добавляли дополнительное количество CrO3 (0,0722 мл; 1,950 ммоль) и смесь перемешивали при КТ в течение ночи. К реакционной смеси добавляли iPrOH (150 мл), и цвет суспензии изменялся на зеленый. Осадок отфильтровывали и фильтрат упаривали досуха; твердый остаток растирали с AcOEt (40 мл) и отфильтровывали, получая 5-нитро-2-(трифторметил)бензойную кислоту (1,1 г; 4,68 ммоль; выход 96%).
Стадия 2. Синтез бензил-5-нитро-2-(трифторметил)бензоата (281) К раствору 5-нитро-2-(трифторметил)бензойной кислоты (1,0 г; 4,25 ммоль) и бензилбромида (0,506 мл; 4,25 ммоль) в CH3CN (8 мл) добавляли Cs2CO3 (416 мг; 1,276 ммоль) и полученную смесь нагревали при 100°С при облучении микроволнами (MW) в течение 30 минут. Реакционную смесь концентрировали под вакуумом и остаток распределяли между водой и EtOAc. Органическую фазу сушили над Na2SO4, растворитель удаляли при пониженном давлении и неочищенный продукт очищали флэш-хроматографией на силикагеле (петролейный эфир/DCM, 95/5), получая бензил-5-нитро-2-(трифторметил)бензоат (770 мг; 2,367 ммоль; выход 56%).
Стадия 3. Синтез бензил-5-амино-2-(трифторметил)бензоата (280)
К суспензии бензил-5-нитро-2-(трифторметил)бензоата (770 мг; 2,367 ммоль) в этаноле (8 мл) и воде (4 мл) добавляли хлорид аммония (253 мг; 4,73 ммоль) в виде одной порции. Смесь нагревали при 80°С, добавляли порошок железа (793 мг; 14.20 ммоль) и реакционную смесь перемешивали при этой же температуре в течение 1 ч. Смесь фильтровали через набивку целита и фильтрат упаривали досуха. Остаток растворяли в EtOAc и промывали водой и рассолом; органическую фазу сушили над Na2SO4 и растворитель удаляли, получая бензил-5-амино-2-(трифторметил)бензоат (688 мг; 2,330 ммоль; выход 98%; MS/ESI+ 296,0 [MH]+). Это промежуточное соединение использовали без очистки.
Стадия 4. Синтез бензил-5-(метилсульфонамидо)-2-(трифторметил)бензоата (279)
К раствору бензил-5-амино-2-(трифторметил)бензоата (688 мг; 2,330 ммоль) в безводном пиридине (6 мл), охлажденному до 0°С, по каплям добавляли метансульфонилхлорид (0,198 мл; 2,56 ммоль) и реакционную смесь перемешивали при КТ в течение ночи. Летучие вещества удаляли под вакуумом, остаток обрабатывали насыщ. водным раствором NaHCO3 и дважды экстрагировали EtOAc; объединенные органические слои сушили над Na2SO4, растворитель удаляли и неочищенный продукт очищали путем растирания с Et2O (100 мл), получая бензил-5-(метилсульфонамидо)-2- (трифторметил)бензоат (510 мг; 1,366 ммоль; выход 59%).
Стадия 5. Синтез бензил-5-(N-(2-морфолиноэтил)-метилсульфонамидо)-2-(трифторметил)бензоат (278)
Бензил-5-(метилсульфонамидо)-2-(трифторметил)бензоат (510 мг; 1,366 ммоль) растворяли в безводном DMF (6 мл) и добавляли гидрохлорид 4-(2- хлорэтил)морфолина (381 мг; 2,049 ммоль), затем K2CO3 (529 мг; 3,82 ммоль). Реакционную смесь нагревали при 100°С в течение 3 ч. Смесь распределяли между этилацетатом и водой; органический слой промывали несколько раз рассолом и сушили над сульфатом натрия. Растворитель удаляли при пониженном давлении и неочищенный продукт очищали флэш-хроматографией на силикагеле (EtOAc/петролейный эфир, от 80/20 до AcOEt), получая бензил-5-(N-(2-морфолиноэтил)метилсульфонамидо)-2-(трифторметил)бензоат (560 мг; 1,151 ммоль; выход 84%; MS/ESI+ 487,1 [MH]+).
Стадия 6. Синтез 5-(N-(2-морфолиноэтил)метилсульфонамидо)-2- (трифторметил)бензойной кислоты (277)
Смесь бензил-5-(N-(2-морфолиноэтил)метилсульфонамидо)-2-(трифторметил)бензоата (560 мг; 1,151 ммоль) и каталитического количества 10%-ного Pd/C в AcOEt (5 мл) и МеОН (15 мл) гидрировали в аппарате Парра при давлении 30 ф/кв. дюйм (207 кПа) в течение 6 ч. Катализатор отфильтровывали и растворитель удаляли под вакуумом; неочищенный остаток растирали с МеОН (5 мл), получая после фильтрования 5-(N-(2-морфолиноэтил)метилсульфонамидо)-2-(трифторметил)бензойную кислоту (350 мг; 0,883 ммоль; выход 77%; MS/ESI+ 396,9 [MH]+).
Стадия 5. Синтез 2,2,2-трифторацетатной соли (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(5-(N-(2-морфолиноэтил)-метилсульфонамидо)-2-(трифторметил)бензоилокси)- этил)пиридин-1-оксида (276)
Смесь 5-(N-(2-морфолиноэтил)метилсульфонамидо)-2-(трифторметил)бензойной кислоты (200 мг; 0,505 ммоль), (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-гидроксиэтил)-пиридин-1-оксида (177 мг; 0,420 ммоль), EDC (121 мг; 0,631 ммоль) и DMAP (128 мг; 1,051 ммоль) в безводном DCM перемешивали при КТ в течение 3 ч. Добавляли дополнительное количество 5-(N-(2-морфолиноэтил)-метилсульфонамидо)-2-(трифторметил)бензойной кислоты (7) (167 мг; 0,420 ммоль), EDC (81 мг; 0,420 ммоль) и DMAP (25,7 мг; 0,210 ммоль) и реакционную смесь перемешивали при КТ в течение ночи. Смесь промывали водой и рассолом; органическую фазу сушили над Na2SO4, фильтровали и упаривали. Неочищенный продукт очищали флэш-хроматографией на силикагеле (DCM/MeOH, 95/05) и затем еще раз хроматографией на силикагеле (DCM/AcOEt, 60/40, затем DCM/MeOH, 90/10). Полученный продукт растирали с EtOH (3 мл) и окончательно очищали препаративной HPLC, получая 2,2,2-трифторацетатную соль (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(5-(N-(2- морфолиноэтил)метилсульфонамидо)-2-(трифторметил)бензоилокси)-этил)пиридин-1-оксида (121 мг; 0,133 ммоль; выход 31,6%; MS/ESI+ 798,1 [MH]+, [αD]=-2,513, с=0,390; DCM).
1Н ЯМР (300 МГц, DMSO-d6 +Na2CO3) δ млн-1 8.56 (s, 2Н), 7.91 (d, 1Н), 7.83 (dd, 1Н), 7.78 (d, 1Н), 7.21 (d, 1Н), 7.17 (d, 1Н), 7.03 (dd, 1Н), 7.09 (t, 1Н), 6.20 (dd, 1Н), 3.94 (dd, 1Н), 3.87 (dd, 1Н), 3.85 (t, 2Н), 3.60 (dd, 1Н), 3.36-3.47 (m, 4Н), 3.40 (dd, 1Н), 3.13 (s, 3Н), 2.39 (t, 2Н), 2.18-2.32 (m, 4Н), 1.12-1.31 (m, 1Н), 0.48-0.69 (m, 2Н), 0.25-0.48 (m, 2Н).
Пример 35
Синтез (S)-3,5-дихлор-4-(2-(4-(циклопропилметокси)-3-((2-(4-гидроксипиперидин-1-ил)ацетокси)метил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенила)этил)пиридин-1-оксида (соединения 283)
Схема 35
Стадия 1. Синтез (S)-3,5-дихлор-4-(2-(4-(циклопропилметокси)-3-(гидроксиметил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)пиридин-1-оксида (285)
(S)-3,5-Дихлор-4-(2-(4-(циклопропилметокси)-3-формилбензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксид (100 мг; 0,161 ммоль), полученный как указано в примере 14, схема 16, стадии 1-3, растворяли в МеОН (2 мл). Добавляли NaBH4 (18,2 мг; 0,482 ммоль) и смесь перемешивали при КТ в течение 2 ч. Реакционную смесь разбавляли 1 М HCl и экстрагировали этилацетатом. Органическую фазу промывали 1 н. HCl и рассолом, сушили над Na2SO4 и концентрировали под вакуумом, получая (S)-3,5-дихлор-4-(2-(4-(циклопропилметокси)-3-(гидроксиметил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксид (90 мг; 0,144 ммоль; выход 90%). MS/ESI+ 624,5 [MH]+.
Стадия 2. Синтез (S)-4-(2-(3-((2-бромацетокси)метил)-4-(циклопропилметокси)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (284)
(S)-3,5-Дихлор-4-(2-(4-(циклопропилметокси)-3-(гидроксиметил)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-пиридин-1-оксид (50 мг; 0,080 ммоль) растворяли в DCM (1,5 мл). Добавляли 2-бромацетилхлорид (16,38 мг; 0,104 ммоль) и TEA (0,044 мл; 0,317 ммоль) и смесь перемешивали при КТ в течение 1,5 ч до полного завершения реакции. Реакционную смесь разбавляли 1 н. раствором HCl и экстрагировали DMC. Органическую фазу промывали 1 н. HCl, 5%-ным раствором NaHCO3 и рассолом, сушили над Na2SO4 и концентрировали под вакуумом, получая (S)-4-(2-(3-((2-бромацетокси)метил)-4-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (50 мг; 0,067 ммоль; выход 84%). MS/ESI+ 746,39 [MH]+.
Стадия 3. Синтез (S)-3,5-дихлор-4-(2-(4-(циклопропилметокси)-3-((2-(4-гидроксипиперидин-1-ил)ацетокси)метил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)пиридин-1-оксида (283)
(S)-4-(2-(3-((2-Бромацетокси)метил)-4-(циклопропилметокси)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (50 мг; 0,067 ммоль) растворяли в DMF. Добавляли пиперидин-4-ол (20,35 мг; 0,201 ммоль) и K2CO3 (11,12 мг; 0,080 ммоль) и реакционную смесь перемешивали при КТ в течение 2 ч до полного завершения реакции. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органическую фазу сушили над Na2SO4 и концентрировали под вакуумом. Неочищенный продукт очищали препаративной HPLC, получая (S)-3,5-дихлор-4-(2-(4-(циклопропилметокси)-3-((2-(4-гидроксипиперидин-1-ил)ацетокси)метил)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)пиридин-1-оксид (18 мг; 0,024 ммоль; выход 35,0%). MS/ESI+ 764,9 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 8.55 (s, 2Н), 7.93 (m, 2Н), 6.96-7.31 (m, 5Н), 6.03-6.28 (m, 1Н), 5.12 (s, 2Н), 4.52 (bs, 1Н), 3.85-4.08 (m, 4Н), 3.51-3.66 (m, 1Н), 3.41-3.50 (m, 2Н), 3.23 (m, 2Н), 2.71 (d, J=11,03 Гц, 2Н), 2.23 (m, 2Н), 1.67 (d, J=10,14 Гц, 2Н), 1.36 (d, J=9,70 Гц, 2Н), 1.23 (m, 2Н), 0.56 (m, 4Н), 0.35 (m, 4Н).
Соединение, приведенное в Таблице 21, получали в соответствии со стадиями и методиками синтеза, аналогичными описанным в примере 35, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами. Конкретные изменения в условиях экспериментов или методах очистки указаны в таблице.
Пример 36
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-гидрокси-5-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (соединения 287)
Схема 36
Стадия 1. Синтез метил-3-(циклопропилметокси)-5-(N-(2-морфолиноэтил)метилсульфонамидо)бензоата (292)
Метил-3-(циклопропилметокси)-5-(метилсульфонамидо)бензоат (202 мг; 0,675 ммоль) (полученный согласно той же методике, которая описана в WO 2010/089107, схема 2, пример 16, стадии 1-4, исходя из метилового эфира 3-гидрокси-5-нитро-бензойной кислоты), приводили во взаимодействие так, как описано в примере 5, схема 5, стадия 3, получая желаемый продукт (152 мг; 0,368 ммоль; выход 55%). MS/ESI+ 299,08 [MH]+.
Стадия 2. Синтез метил-3-гидрокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)бензоата (291)
Метил-3-(циклопропилметокси)-5-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоат (50 мг; 0,121 ммоль) растворяли в TFA (1,5 мл; 19,47 ммоль). Реакционную смесь перемешивали при КТ в течение 4 ч до полного завершения реакции. Растворитель концентрировали под вакуумом, получая метил-3-гидрокси-5-(N-(2-морфолиноэтил)-метилсульфонамидо)-бензоат (40 мг; 0,112 ммоль; выход 92%). MS/ESI+ 359,12 [MH]+.
Стадия 3. Синтез 3-гидрокси-5-(N-(2-морфолиноэтил)-метилсульфонамидо)бензойной кислоты (290)
Метил-3-гидрокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоат (40 мг; 0,112 ммоль) растворяли в МеОН (1,5 мл). Добавляли 1 М раствор NaOH (500 мкл) и реакционную смесь перемешивали при 50°С в течение 2 ч до полного завершения реакции. Реакционную смесь нейтрализовали, используя 1 н. раствор HCl, и концентрировали, получая 3-гидрокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)бензойную кислоту (60 мг; 0,174 ммоль; выход 156%). MS/ESI+ 345,11 [MH]+.
Стадия 4. Синтез 3-ацетокси-5-(N-(2-морфолиноэтил)-метилсульфонамидо)бензойной кислоты (289)
3-Гидрокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)бензойную кислоту (200 мкл; 0,764 ммоль) растворяли в DCM (2 мл). Добавляли ацетилхлорид (60 мг; 0,764 ммоль) и DMAP (100 мг; 0,819 ммоль). Реакционную смесь перемешивали при КТ в течение 2 ч до полного завершения реакции. Реакционную смесь концентрировали, неочищенное вещество растирали в гексане, фильтровали и сушили в вакуумном сушильном шкафу, получая 3-ацетокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)-бензойную кислоту (60 мг; 0,155 ммоль; выход 20,31%). MS/ESI+ 387,42 [MH]+.
Стадия 5. Синтез (S)-4-(2-(3-ацетокси-5-(N-(2-морфолинозтил)-метилсульфонамидо)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (288)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-гидроксиэтил)пиридин-1-оксид (20 мг; 0,048 ммоль), 3-ацетокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)бензойную кислоту (60 мг; 0,155 ммоль), DMAP (20 мг; 0,164 ммоль) и EDC (100 мг; 0,522 ммоль) растворяли в DMF (1,5 мл). Реакционную смесь перемешивали при 40°С в течение 8 ч до полного завершения реакции. Реакционную смесь разбавляли водой и осадок растворяли в этилацетате. Органическую фазу сушили над Na2SO4 и концентрировали под вакуумом, получая (S)-4-(2-(3-ацетокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (30 мг; 0,038 ммоль; выход 80%). MS/ESI+ 788,64 [MH]+.
Стадия 6. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-гидрокси-5-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (287)
(S)-4-(2-(3-Ацетокси-5-(N-(2-морфолиноэтил)метилсульфонамидо)-бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид растворяли в МеОН (1,5 мл). Добавляли насыщ. раствор бикарбоната натрия (500 мкл) и реакционную смесь перемешивали при КТ в течение 2 ч до полного завершения реакции. Реакционную смесь разбавляли водой, экстрагировали этилацетатом и концентрировали под вакуумом. Неочищенный продукт очищали препаративной HPLC, получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-гидрокси-5-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)-пиридин-1-оксид (10 мг; 0,013 ммоль). MS/ESI+ 745,8 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 10.03-10.22 (s, 1Н), 8.43-8.69 (s, 2Н), 7.38-7.45 (m, 1Н), 7.31-7.38 (m, 1Н), 7.16-7.28 (m, 2Н), 7.00-7.12 (m, 3Н), 6.05-6.25 (m, 1Н), 3.84-3.97 (m, 2Н), 3.66-3.78 (m, 2Н), 3.55-3.65 (m, 1Н), 3.47 (m, 5Н), 3.02 (s, 3Н), 2.23-2.38 (m, 6Н), 1.08-1.33 (m, 1Н), 0.49-0.67 (m, 2Н), 0.24-0.45 (m, 2Н).
Пример 37
Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(метилтио)-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (соединения 293)
Схема 37
Стадия 1. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(метилтио)-3-нитробензоилокси)этил)-пиридин-1-оксида (296)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-гидроксиэтил)пиридин-1-оксид (240 мг; 0,571 ммоль), N,N-диметилпиридин-4-амин (84 мг; 0,685 ммоль), гидрохлорид N1-((этилимино)метилен)-N3,N3- диметилпропан-1,3-диамина (328 мг; 1,713 ммоль) растворяли в DMF (2 мл). Реакционную смесь перемешивали при КТ в течение ночи. Реакционную смесь разбавляли, используя 1 н. HCl, осадок отфильтровывали, промывали 1 н. HCl, растворяли в этилацетате и экстрагировали 1 н. раствором HCl, 5%-ным раствором NaHCO3 и рассолом. Органическую фазу сушили над Na2SO4 и концентрировали под вакуумом, получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-(метилтио)-3-нитробензоилокси)этил)пиридин-1-оксид (300 мг; 0,487 ммоль; выход 85%). MS/ESI+ 615,43 [MH]+.
Стадия 2. Синтез (S)-4-(2-(3-амино-4-(метилтио)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксида (295)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-(метилтио)-3-нитробензоилокси)этил)пиридин-1-оксид (320 мг; 0,520 ммоль) растворяли в THF (5 мл). Добавляли дигидрат хлорида олова(II) (587 мг; 2,60 ммоль) и смесь перемешивали при КТ в течение ночи. Растворитель концентрировали под вакуумом, неочищенный продукт растворяли в этилацетате и промывали 1 н. раствором HCl, рассолом, сушили над Na2SO4 и концентрировали под вакуумом. 20 мг неочищенного продукта очищали препаративной HPLC, получая (S)-4-(2-(3-амино-4-(метилтио)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)этил)-3,5-дихлорпиридин-1-оксид (10 мг; 0,017 ммоль; выход 3,29%). MS/ESI+ 584,8 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 8.57 (s, 2Н), 7.27-7.31 (m, 1Н), 7.19 (m, 4Н), 7.01-7.10 (m, 2Н), 6.06-6.27 (m, 1Н), 5.29 (s, 2Н), 3.91 (d, J=7,06 Гц, 2Н), 3.51-3.64 (m, 1Н), 3.29 (m, 1Н), 2.43 (s, 3Н), 1.12-1.30 (m, 1Н), 0.48-0.62 (m, 2Н), 0.26-0.41 (m, 2Н).
Стадия 3. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(3-(метилсульфонамидо)-4-(метилтио)-бензоилокси)этил)пиридин-1-оксида (294)
(S)-4-(2-(3-Амино-4-(метилтио)бензоилокси)-2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)этил)-3,5-дихлорпиридин-1-оксид (200 мг; 0,342 ммоль) растворяли в DCM (3 мл). Добавляли метансульфонилхлорид (0,053 мл; 0,683 ммоль) и пиридин (0,028 мл; 0,342 ммоль) и реакционную смесь перемешивали при КТ в течение 8 ч до полного завершения реакции. Реакционную смесь промывали 1 н. раствором HCl и рассолом, сушили над Na2SO4 и концентрировали под вакуумом. 30 мг неочищенного продукта очищали препаративной HPLC, получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(3-(метилсульфонамидо)-4-(метилтио)бензоилокси)этил)пиридин-1-оксид (20 мг; 0,030 ммоль; выход 8,82%). MS/ESI+ 663,0 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 9.32-9.56 (bs, 1Н), 8.55 (s, 2Н), 7.83-7.93 (m, 1Н), 7.76-7.82 (m, 1Н), 7.33-7.44 (m, 1Н), 7.17-7.24 (m, 2Н), 7.00-7.10 (m, 2Н), 6.12-6.27 (m, 1Н), 3.85-3.97 (m, 2Н), 3.52-3.66 (m, 1Н), 3.36-3.42 (m, 1Н), 3.01 (s, 3Н), 2.49 (s, 3Н), 1.18-1.27 (m, 1H), 0.50-0.61 (m, 2H), 0.31-0.40 (m, 2H).
Стадия 4. Синтез (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)фенил)-2-(4-(метилтио)-3-(N-(2-морфолиноэтил)-метилсульфонамидо)бензоилокси)этил)пиридин-1-оксида (293)
(S)-3,5-Дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(3-(метилсульфонамидо)-4-(метилтио)бензоилокси)этил)пиридин-1-оксид (50 мг; 0,075 ммоль) растворяли в DMF. Добавляли 4-(2-хлорэтил)морфолин (56,4 мг; 0,377 ммоль) и K2CO3 (20,83 мг; 0,151 ммоль), и реакционную смесь перемешивали при 45°С в течение 6 ч до полного завершения реакции. Реакционную смесь разбавляли водой и экстрагировали AcOEt. Органическую фазу сушили над Na2SO4 и концентрировали под вакуумом. Неочищенный продукт очищали препаративной HPLC, получая (S)-3,5-дихлор-4-(2-(3-(циклопропилметокси)-4-(дифторметокси)-фенил)-2-(4-(метилтио)-3-(N-(2-морфолиноэтил)-метилсульфонамидо)-бензоилокси)этил)пиридин-1-оксид (30 мг; 0,039 ммоль; выход 51,3%). MS/ESI+ 776,3 [MH]+.
1Н ЯМР (400 МГц, DMSO-d6) δ млн-1 8.55 (d, J=10,14 Гц, 2Н), 7.92-8.00 (m, 1Н), 7.87 (t, J=2,21 Гц, 1Н), 7.37-7.45 (m, 1Н), 7.21 (d, J=7,94 Гц, 2Н), 7.07 (m, 2Н), 6.13-6.24 (m, 1Н), 3.93 (d, J=7,06 Гц, 2Н), 3.70-3.84 (m, 1Н), 3.48-3.67 (m, 2Н), 3.39 (d, J=4,41 Гц, 4Н), 3.18 (m, 1Н), 3.18 (s, 3Н), 2.50 (s, 3Н), 2.07-2.45 (m, 6Н), 1.14-1.29 (m, 1Н), 0.50-0.63 (m, 2Н), 0.27-0.42 (m, 2Н).
Соединение, приведенное в Таблице 22, получали в соответствии со стадиями и методиками синтеза, аналогичными описанным в примере 37, путем приведения во взаимодействие соответствующих предшественников (имеющихся в продаже или синтезированных специалистом в данной области техники) с подходящими реагентами.
ФАРМАКОЛОГИЧЕСКАЯ АКТИВНОСТЬ СОЕДИНЕНИЙ ПО ИЗОБРЕТЕНИЮ
Определение PDE4-ингибирующей активности in vitro в анализе бесклеточных лизатов
Активность PDE4 определяли в супернататах клеточных лизатов человеческих моноцитов U937. Клетки культивировали, собирали и готовили фракцию супернатанта по существу так, как описано в Torphy TJ et al., J. Pharmacol. Exp.Ther., 1992, 263: 1195-1205.
Клетки U937 (Клеточный банк, Межлабораторная коллекция клеточных линий (ICLC), номер в ICLC HTL94002) выращивали при 37°С, 5% CO2 в среде RPMI 1640 с GlutaMAX™-I, дополненной 10% фетальной телячьей сыворотки и пенициллином-стрептомицином в концентрации 100 мкг/мл (Gibco).
Клетки собирали и дважды промывали посредством центрифугирования (150 × g; 8 мин) в холодном забуференном фосфатом физиологическом растворе (PBS). Промытые клетки ресуспендировали в холодном буфере Кребса-Рингера-Хенселейта в конечной концентрации 20×106 клеток/мл и подвергали обработке ультразвуком. После центрифугирования при 15000 × g в течение 20 мин супернатанты объединяли, разделяли на аликвоты и хранили при -80°С.
Активность PDE4 определяли в супернататах клеток по исчезновению цАМФ (циклоаденозинмонофосфат) из инкубационных смесей.
Концентрацию тестируемых соединений изменяли в диапазоне от 10-12 М до 10-6 М. Реакции останавливали посредством тепловой инактивации фермента (2,5 минут при 100°С), и содержание оставшегося цАМФ определяли с использованием набора «LANCE cAMP Assay» от PerkinElmer, следуя инструкциям поставщиков.
Результаты для тестируемых соединений, представляющих собой репрезентативные соединения по изобретению, выраженные в виде среднего значения концентрации тестируемого соединения в нМ, вызывающей 50%-ное ингибирование исчезновения цАМФ (IC50), составляют меньше 1 нМ.
Процент ингибирования активности PDE4 рассчитывали, принимая исчезновение цАМФ в отсутствии ингибиторов за 100%, а исчезновения цАМФ в образцах, подвергнутых тепловой инактивации, за 0%.
Claims (124)
1. Соединение общей формулы (I)
где:
R1 и R2 являются разными или одинаковыми и независимо выбраны из группы, состоящей из:
линейного (С1-С6)-алкила, возможно замещенного одним заместителем, выбранным из (С3-С7)-циклоалкила;
(С1-С6)-галогеналкила;
(С3-С7)-циклоалкила;
R3 представляет собой Н или представляет собой один или два заместителя, независимо выбранных из атомов галогена;
Z представляет собой группу (СН2)m, где m равно 0;
А представляет собой фенильное кольцо, возможно замещенное одним заместителем R4, который выбран из группы, состоящей из:
линейного (С1-С6)-алкила, замещенного одним морфолинилом;
разветвленного (С1-С6)-алкила, возможно замещенного одним (С3-С7)-циклоалкилом;
(С1-С6)-галогеналкила;
(С1-С6)-алкилтио;
атома галогена;
и
OR7, где R7 выбран из группы, состоящей из
Н;
(С1-С10)-алкила, возможно замещенного радикалом, выбранным из (С3-С7)-циклоалкила, морфолинила, фенила и пиридинила; и
(С1-С10)-алкила, замещенного одной группой ОН;
(С1-С6)-галогеналкила;
(С3-С7)-циклоалкила;
W выбран из группы, состоящей из:
-NR9SO2R10, где
R9 выбран из группы, состоящей из
(С1-С10)-алкила, замещенного (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, (С3-С7)-гетероциклоалкилкарбонилом, где гетероциклоалкил представляет собой моноциклическую (С3-С7)-циклоалкильную группу, в которой один или два атома углерода заменены на N, NH, S или O, причем гетероциклоалкил возможно может быть замещен одним или двумя (С1-С4)-алкилами или ОН; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН; и
R10 выбран из группы, состоящей из
(С1-С4)-алкила, возможно замещенного (С3-С7)-циклоалкилом; и (С3-С7)циклоалкила;
-CH2NR13SO2R14, где
R13 выбран из группы, состоящей из:
Н;
(С3-С7)-циклоалкила, замещенного морфолинилом;
(С1-С10)-алкила, замещенного (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, где гетероциклоалкил представляет собой моноциклическую (С3-С7)-циклоалкильную группу, в которой один или два атома углерода заменены на N, NH, S или O, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
R14 выбран из группы, состоящей из:
(С1-С4)-алкила;
-SO2NR15R16, где
R15 представляет собой Н; и
R16 выбран из группы, состоящей из:
(С1-С10)-алкила, замещенного (С3-С6)-гетероциклоалкилом, где гетероциклоалкил представляет собой моноциклическую (С3-С7)-циклоалкильную группу, в которой два атома углерода заменены на N, NH или O, причем гетероциклоалкил возможно может быть замещен (С1-С4)-алкилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой (С1-С6)-алкил; или
R15 и R16 вместе с атомом азота, к которому они присоединены, образуют пиперазинил, замещенный одним (С1-С4)-алкилом;
-NHSO2R17, где
R17 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С3-С7)-гетероциклоалкильным кольцом, которое представляет собой моноциклическую (С3-С6)-циклоалкильную группу, в которой два атома углерода заменены на N, NH или O, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом; (С1-С10)-алкила, возможно замещенного (С3-С7)-гетероциклоалкилом,
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой (С1-С6)-алкил;
-OSO2R18, где
R18 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С3-С7)-циклоалкилом, (С1-С4)-алкоксилом или морфолинилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
-NHCOR26, где
R26 выбран из группы, состоящей из:
группы R27R28N-(C1-C6)алкилен, где R27 и R28, одинаковые или разные, независимо выбраны из Н, (С1-С6)-алкила, возможно замещенного ОН, или вместе с атомом азота, к которому они присоединены, образуют пиперазинил, замещенный одной или двумя группами (С1-С4)-алкил;
группы R27R28N-карбонил-(C1-C6)алкилен, где R27 и R28, вместе с атомом азота, к которому они присоединены, образуют пиперазинильное кольцо, возможно замещенное одной или двумя группами (С1-С4)-алкил;
морфолинильного кольца; и
его N-оксиды по пиридиновому кольцу и их фармацевтически приемлемые соли.
2. Соединение по п. 1, представляющее собой N-оксид по пиридиновому кольцу, представленное формулой (Ia),
где R1 R2, R3, Z, А и W такие, как определено в п. 1.
3. Соединение по п. 1, представленное формулой (I)', где абсолютная конфигурация атома углерода (1) является такой, как показано ниже:
где R1, R2, R3, Z, А и W являются такими, как определено в п. 1 или 2 для соединений формулы (I) и их N-оксидов по пиридиновому кольцу, или его фармацевтически приемлемые соли.
4. Соединение по п. 1, где
R1 и R2 являются разными или одинаковыми и независимо выбраны из группы, состоящей из:
линейного (С1-С6)-алкила, возможно замещенного одним заместителем, выбранным из (С3-С7)-циклоалкила;
(С1-С6)-галогеналкила;
R3 представляет собой один или два заместителя, выбранных из атомов галогена;
Z представляет собой группу (СН2)m, где m равно 0;
А представляет собой фенильное кольцо, возможно замещенное одним заместителем R4, который выбран из группы, состоящей из:
линейного (С1-С6)-алкила, замещенного одним морфолинилом;
(С1-С6)-галогеналкила;
(С1-С6)-алкилтио;
атома галогена;
и
OR7, где R7 выбран из группы, состоящей из
Н;
(С1-С10)-алкила, возможно замещенного радикалом, выбранным из (С3-С7)-циклоалкила, морфолинила, фенила и пиридинила;
(С1-С10)-алкила, замещенного одной группой ОН;
(С1-С6)-галогеналкила;
(С3-С7)-циклоалкила;
W выбран из группы, состоящей из:
-NR9SO2R10, где
R9 выбран из группы, состоящей из
(С1-С10)-алкила, замещенного (С3-С7)-гетероциклоалкилом, (С3-С7)-гетероциклоалкилкарбонилом, где гетероциклоалкил представляет собой моноциклическую (С3-С7)-циклоалкильную группу, в которой один или два атома углерода заменены на N, NH, S или O, причем гетероциклоалкил возможно может быть замещен одним или двумя (С1-С4)-алкилами или ОН; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой Н или (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН; и
R10 выбран из группы, состоящей из
(С1-С4)-алкила, возможно замещенного (С3-С7)-циклоалкилом; и (С3-С7)циклоалкила;
-CH2NR13SO2R14, где
R13 выбран из группы, состоящей из:
Н;
(С1-С10)-алкила, замещенного (С3-С7)-циклоалкилом, (С3-С7)-гетероциклоалкилом, где гетероциклоалкил представляет собой моноциклическую (С3-С7)-циклоалкильную группу, в которой один или два атома углерода заменены на N, NH, S или O, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
R14 выбран из группы, состоящей из:
(С1-С4)-алкила;
-SO2NR15R16, где
R15 представляет собой Н; и
R16 выбран из группы, состоящей из:
(С1-С10)-алкила, замещенного (С3-С6)-гетероциклоалкилом, где гетероциклоалкил представляет собой моноциклическую (С3-С7)-циклоалкильную группу, в которой два атома углерода заменены на N, NH или O, причем гетероциклоалкил возможно может быть замещен (С1-С4)-алкилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой метил или этил; или
R15 и R16 вместе с атомом азота, к которому они присоединены, образуют пиперазинил, замещенный одним (С1-С4)-алкилом;
-NHSO2R17, где
R17 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С3-С7)-гетероциклоалкильным кольцом, которое представляет собой моноциклическую (С3-С6)-циклоалкильную группу, в которой два атома углерода заменены на N, NH или O, причем любое такое кольцо возможно может быть замещено (С1-С4)-алкилом;
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой (С1-С6)-алкил;
-OSO2R18, где
R18 выбран из группы, состоящей из:
(С1-С10)-алкила, возможно замещенного (С1-С4)-алкоксилом; и
группы R11R12N-(C1-C10)алкилен, где R11 и R12 независимо представляют собой (С1-С6)-алкил, каждый из которых возможно может быть замещен группой ОН;
-NHCOR26, где
R26 выбран из группы, состоящей из:
группы R27R28N-(C1-C6)алкилен, где R27 и R28, одинаковые или разные, независимо выбраны из Н, (С1-С6)-алкила, возможно замещенного ОН, или вместе с атомом азота, к которому они присоединены, образуют пиперазинил, возможно замещенный одной или двумя группами (С1-С4)-алкил;
группы R27R28N-карбонил-(C1-C6)алкилен, где R27 и R28, вместе с атомом азота, к которому они присоединены, образуют пиперазинильное кольцо, возможно замещенное одной или двумя группами (С1-С4)-алкил;
морфолинильного кольца; и
его N-оксиды по пиридиновому кольцу и их фармацевтически приемлемые соли.
5. Фармацевтическая композиция, обладающая PDE4-ингибирующей активностью, содержащая соединение формулы (I) по любому из пп. 1-4 и один или более чем один фармацевтически приемлемый носитель и/или эксципиент.
6. Соединение формулы (I) по п. 1 для применения в качестве лекарственного средства, обладающего PDE4-ингибирующей активностью.
7. Соединение формулы (I) по п. 1 для применения в предупреждении и/или лечении аллергического болезненного состояния или заболевания дыхательных путей, характеризующегося обструкцией дыхательных путей.
8. Соединение для применения по п. 7, где заболевание дыхательных путей, характеризующееся обструкцией дыхательных путей, выбрано из астмы и хронической обструктивной болезни легких (COPD).
9. Соединение для применения по п. 7, где аллергическое болезненное состояние выбрано из атопического дерматита, крапивницы и аллергического ринита.
10. Применение соединения формулы (I) по любому из пп. 1-4 для изготовления лекарственного средства для предупреждения и/или лечения аллергического болезненного состояния или заболевания дыхательных путей, характеризующегося обструкцией дыхательных путей.
11. Применение по п. 10, где заболевание дыхательных путей, характеризующееся обструкцией дыхательных путей, выбрано из астмы и COPD.
12. Применение по п. 10, где аллергическое болезненное состояние выбрано из атопического дерматита, крапивницы и аллергического ринита.
13. Устройство, представляющее собой однодозовый или многодозовый ингалятор сухого порошка, дозирующий ингалятор или небулайзер мягкого аэрозоля (soft mist), содержащее фармацевтическую композицию по п. 5.
14. Набор, содержащий фармацевтические композиции по п. 5 и устройство, которое может представлять собой однодозовый или многодозовый ингалятор сухого порошка, дозирующий ингалятор или небулайзер мягкого аэрозоля (soft mist).
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP12195738 | 2012-12-05 | ||
| EP12195738.5 | 2012-12-05 | ||
| PCT/EP2013/075540 WO2014086865A1 (en) | 2012-12-05 | 2013-12-04 | 1-phenyl-2-pyridinyl alkyl alcohol derivatives as phosphodiesterase inhibitors |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2015121045A RU2015121045A (ru) | 2017-01-11 |
| RU2655170C2 true RU2655170C2 (ru) | 2018-05-24 |
Family
ID=47325924
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2015121045A RU2655170C2 (ru) | 2012-12-05 | 2013-12-04 | Производные 1-фенил-2-пиридинилалкиловых спиртов в качестве ингибиторов фосфодиэстеразы |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US9944612B2 (ru) |
| EP (1) | EP2928869B1 (ru) |
| KR (1) | KR102192739B1 (ru) |
| CN (2) | CN104822659A (ru) |
| AR (1) | AR093796A1 (ru) |
| BR (1) | BR112015012724A2 (ru) |
| CA (1) | CA2893628C (ru) |
| ES (1) | ES2716142T3 (ru) |
| HK (1) | HK1213551A1 (ru) |
| PL (1) | PL2928869T3 (ru) |
| RU (1) | RU2655170C2 (ru) |
| TR (1) | TR201907092T4 (ru) |
| TW (1) | TWI628166B (ru) |
| WO (1) | WO2014086865A1 (ru) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2216327A1 (en) | 2009-02-06 | 2010-08-11 | CHIESI FARMACEUTICI S.p.A. | Benzoic acid (1-phenyl-2-pyridin-4-yl)ethyl esters as phosphodiesterase inhibitors |
| ES2759514T3 (es) | 2013-10-22 | 2020-05-11 | Chiesi Farm Spa | Procedimiento de preparación de un inhibidor de PDE4 |
| TW201710254A (zh) * | 2015-06-01 | 2017-03-16 | 吉斯藥品公司 | 胺基酯衍生物 |
| AR104822A1 (es) * | 2015-06-01 | 2017-08-16 | Chiesi Farm Spa | Derivado de aminoésteres |
| WO2019129586A1 (en) * | 2017-12-28 | 2019-07-04 | Chiesi Farmaceutici S.P.A. | Use of 1-phenyl-2-pyridinyl alkyl alcohol derivatives for treating cystic fibrosis |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2235095C2 (ru) * | 1998-10-06 | 2004-08-27 | Дайниппон Фармасьютикал Ко., Лтд. | 2,3-дизамещенное производное пиридина, способы его получения, содержащая его фармацевтическая композиция и промежуточный продукт для его получения |
| WO2009018909A2 (en) * | 2007-08-08 | 2009-02-12 | Chiesi Farmaceutici S.P.A. | Derivatives of 1-phenyl-2-pyridinyl alkyl alcohols as phosphodiesterase inhibitors |
| WO2010089107A1 (en) * | 2009-02-06 | 2010-08-12 | Chiesi Farmaceutici S.P.A. | Benzoic acid (1-phenyl-2-pyridin-4-yl) ethyl esters as phosphodiesterase inhibitors |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1994002465A1 (en) | 1992-07-28 | 1994-02-03 | Rhone-Poulenc Rorer Limited | INHIBITORS OF c-AMP PHOSPHODIESTERASE AND TNF |
| US5786354A (en) | 1994-06-21 | 1998-07-28 | Celltech Therapeutics, Limited | Tri-substituted phenyl derivatives and processes for their preparation |
| SE9903995D0 (sv) * | 1999-11-03 | 1999-11-03 | Astra Ab | New combination |
| WO2004096274A1 (ja) | 2003-03-31 | 2004-11-11 | Kyowa Hakko Kogyo Co., Ltd. | 気道内投与剤 |
| DE602007012105D1 (de) * | 2006-07-14 | 2011-03-03 | Chiesi Farma Spa | Derivate von 1-phenyl-2-pyridinylalkylenalkohole als phosphodiesteraseinhibitoren |
| JP2008174213A (ja) * | 2006-12-20 | 2008-07-31 | Nsk Ltd | 舵角可変式ステアリング装置 |
| EP2070913A1 (en) * | 2007-12-14 | 2009-06-17 | CHIESI FARMACEUTICI S.p.A. | Ester derivatives as phosphodiesterase inhibitors |
| EP2110375A1 (en) | 2008-04-14 | 2009-10-21 | CHIESI FARMACEUTICI S.p.A. | Phosphodiesterase-4 inhibitors belonging to the tertiary amine class |
| AU2012266514A1 (en) | 2011-06-06 | 2014-01-09 | Chiesi Farmaceutici S.P.A. | Derivatives of 1-phenyl-2-pyridinyl alkyl alcohols as phosphodiesterase inhibitors |
| EP2760838B1 (en) | 2011-09-26 | 2017-05-10 | Chiesi Farmaceutici S.p.A. | Derivatives of 1-phenyl-2-pyridinyl alkyl alcohols as phosphodiesterase inhibitors |
| RU2637945C2 (ru) | 2012-06-04 | 2017-12-08 | КЬЕЗИ ФАРМАЧЕУТИЧИ С.п.А. | Производные 1-фенил-2-пиридинил-алкиловых спиртов в качестве ингибиторов фосфодиэстеразы |
-
2013
- 2013-12-04 AR ARP130104493A patent/AR093796A1/es active IP Right Grant
- 2013-12-04 CN CN201380063353.XA patent/CN104822659A/zh active Pending
- 2013-12-04 TR TR2019/07092T patent/TR201907092T4/tr unknown
- 2013-12-04 BR BR112015012724A patent/BR112015012724A2/pt not_active Application Discontinuation
- 2013-12-04 ES ES13814850T patent/ES2716142T3/es active Active
- 2013-12-04 RU RU2015121045A patent/RU2655170C2/ru active
- 2013-12-04 KR KR1020157017275A patent/KR102192739B1/ko active IP Right Grant
- 2013-12-04 PL PL13814850T patent/PL2928869T3/pl unknown
- 2013-12-04 CN CN201911008774.8A patent/CN110698459B/zh active Active
- 2013-12-04 TW TW102144352A patent/TWI628166B/zh active
- 2013-12-04 CA CA2893628A patent/CA2893628C/en active Active
- 2013-12-04 EP EP13814850.7A patent/EP2928869B1/en active Active
- 2013-12-04 WO PCT/EP2013/075540 patent/WO2014086865A1/en active Application Filing
- 2013-12-05 US US14/097,445 patent/US9944612B2/en active Active
-
2016
- 2016-02-15 HK HK16101442.4A patent/HK1213551A1/zh unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2235095C2 (ru) * | 1998-10-06 | 2004-08-27 | Дайниппон Фармасьютикал Ко., Лтд. | 2,3-дизамещенное производное пиридина, способы его получения, содержащая его фармацевтическая композиция и промежуточный продукт для его получения |
| WO2009018909A2 (en) * | 2007-08-08 | 2009-02-12 | Chiesi Farmaceutici S.P.A. | Derivatives of 1-phenyl-2-pyridinyl alkyl alcohols as phosphodiesterase inhibitors |
| WO2010089107A1 (en) * | 2009-02-06 | 2010-08-12 | Chiesi Farmaceutici S.P.A. | Benzoic acid (1-phenyl-2-pyridin-4-yl) ethyl esters as phosphodiesterase inhibitors |
Also Published As
| Publication number | Publication date |
|---|---|
| US20140155391A1 (en) | 2014-06-05 |
| CA2893628C (en) | 2021-11-30 |
| US9944612B2 (en) | 2018-04-17 |
| RU2015121045A (ru) | 2017-01-11 |
| HK1213551A1 (zh) | 2016-07-08 |
| WO2014086865A1 (en) | 2014-06-12 |
| BR112015012724A2 (pt) | 2017-07-11 |
| AR093796A1 (es) | 2015-06-24 |
| CA2893628A1 (en) | 2014-06-12 |
| EP2928869B1 (en) | 2019-02-20 |
| CN110698459B (zh) | 2023-05-05 |
| TR201907092T4 (tr) | 2019-06-21 |
| TW201439067A (zh) | 2014-10-16 |
| KR102192739B1 (ko) | 2020-12-18 |
| ES2716142T3 (es) | 2019-06-10 |
| EP2928869A1 (en) | 2015-10-14 |
| KR20150092214A (ko) | 2015-08-12 |
| CN104822659A (zh) | 2015-08-05 |
| CN110698459A (zh) | 2020-01-17 |
| TWI628166B (zh) | 2018-07-01 |
| PL2928869T3 (pl) | 2019-08-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN106946848B (zh) | 作为磷酸二酯酶抑制剂的1-苯基-2-吡啶基烷基醇的衍生物 | |
| US9265768B2 (en) | Derivatives of 1-phenyl-2-pyridinyl alkyl alcohols as phosphodiesterase inhibitors | |
| US9440954B2 (en) | Derivatives of 1-phenyl-2-pyridinyl alkyl alcohols as phosphodiesterase inhibitors | |
| RU2655170C2 (ru) | Производные 1-фенил-2-пиридинилалкиловых спиртов в качестве ингибиторов фосфодиэстеразы | |
| OA13247A (en) | Phenyl or pyridyl amide coumpounds as prostaglandin E2 antagonists. | |
| EP2928879B1 (en) | Phenylethylpyridine derivatives as pde4-inhibitors and muscarinic receptor antagonists | |
| CA2893663A1 (en) | Phenylethylpyridine derivatives as pde4-inhibitors | |
| RU2567548C2 (ru) | Производные сложного аминоэфира алкалоида и их лекарственные композиции | |
| RU2580835C2 (ru) | Алкалоидные производные на основе сложных аминоэфиров и композиции лекарственных средств, содержащие их | |
| EP3152204B1 (en) | Carbamate derivatives which are both phosphodiesterase 4 (pde4) enzyme inhibitors and muscarinic m3 receptor antagonists | |
| TW201302726A (zh) | 作為磷酸二酯酶抑制劑之1-苯基-2-吡啶基烷基醇衍生物 |