RU2637795C2 - Анализ образцов для масс-цитометрии - Google Patents
Анализ образцов для масс-цитометрии Download PDFInfo
- Publication number
- RU2637795C2 RU2637795C2 RU2015123440A RU2015123440A RU2637795C2 RU 2637795 C2 RU2637795 C2 RU 2637795C2 RU 2015123440 A RU2015123440 A RU 2015123440A RU 2015123440 A RU2015123440 A RU 2015123440A RU 2637795 C2 RU2637795 C2 RU 2637795C2
- Authority
- RU
- Russia
- Prior art keywords
- ablation
- injector
- laser
- jet
- sample
- Prior art date
Links
- 238000004458 analytical method Methods 0.000 title claims abstract description 30
- 238000012083 mass cytometry Methods 0.000 title description 2
- 238000002679 ablation Methods 0.000 claims abstract description 158
- 238000009616 inductively coupled plasma Methods 0.000 claims abstract description 96
- 238000000608 laser ablation Methods 0.000 claims abstract description 90
- 238000000034 method Methods 0.000 claims abstract description 72
- 238000012546 transfer Methods 0.000 claims abstract description 63
- 150000002500 ions Chemical class 0.000 claims abstract description 19
- 239000000758 substrate Substances 0.000 claims description 41
- 239000000463 material Substances 0.000 claims description 29
- 230000015572 biosynthetic process Effects 0.000 claims description 10
- 230000005855 radiation Effects 0.000 claims description 10
- 230000007423 decrease Effects 0.000 claims 1
- 238000001095 inductively coupled plasma mass spectrometry Methods 0.000 abstract description 9
- 238000000095 laser ablation inductively coupled plasma mass spectrometry Methods 0.000 abstract description 8
- 230000000694 effects Effects 0.000 abstract description 2
- 239000000126 substance Substances 0.000 abstract 1
- 239000007789 gas Substances 0.000 description 116
- 239000000523 sample Substances 0.000 description 85
- 239000002245 particle Substances 0.000 description 19
- 238000002347 injection Methods 0.000 description 16
- 239000007924 injection Substances 0.000 description 16
- 238000004140 cleaning Methods 0.000 description 15
- 238000005070 sampling Methods 0.000 description 15
- 230000003287 optical effect Effects 0.000 description 10
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 8
- 238000003384 imaging method Methods 0.000 description 8
- 238000001514 detection method Methods 0.000 description 7
- 230000008901 benefit Effects 0.000 description 6
- 239000012472 biological sample Substances 0.000 description 6
- 230000032258 transport Effects 0.000 description 6
- 239000011324 bead Substances 0.000 description 5
- 229910052786 argon Inorganic materials 0.000 description 4
- 230000001186 cumulative effect Effects 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 230000037427 ion transport Effects 0.000 description 3
- 238000004949 mass spectrometry Methods 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 239000010453 quartz Substances 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 238000000559 atomic spectroscopy Methods 0.000 description 2
- 239000012620 biological material Substances 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 108090000623 proteins and genes Proteins 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 230000001052 transient effect Effects 0.000 description 2
- 238000012935 Averaging Methods 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 0 CC(C)ICC(*)CCCN Chemical compound CC(C)ICC(*)CCCN 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 241001212228 Sesbania drummondii Species 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- DZHSAHHDTRWUTF-SIQRNXPUSA-N amyloid-beta polypeptide 42 Chemical compound C([C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](C)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)NCC(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(O)=O)[C@@H](C)CC)C(C)C)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@@H](NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C(C)C)C1=CC=CC=C1 DZHSAHHDTRWUTF-SIQRNXPUSA-N 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- CEKJAYFBQARQNG-UHFFFAOYSA-N cadmium zinc Chemical compound [Zn].[Cd] CEKJAYFBQARQNG-UHFFFAOYSA-N 0.000 description 1
- 108010011475 cadmium-binding protein Proteins 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000013553 cell monolayer Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 238000005553 drilling Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 239000001307 helium Substances 0.000 description 1
- 229910052734 helium Inorganic materials 0.000 description 1
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 238000013115 immunohistochemical detection Methods 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 238000009434 installation Methods 0.000 description 1
- 238000000555 laser ablation inductively coupled plasma time-of-flight mass spectrometry Methods 0.000 description 1
- 238000012621 laser-ablation inductively coupled plasma technique Methods 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 229910052745 lead Inorganic materials 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 229910052594 sapphire Inorganic materials 0.000 description 1
- 239000010980 sapphire Substances 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000010865 sewage Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 239000000107 tumor biomarker Substances 0.000 description 1
- 229910052724 xenon Inorganic materials 0.000 description 1
- FHNFHKCVQCLJFQ-UHFFFAOYSA-N xenon atom Chemical compound [Xe] FHNFHKCVQCLJFQ-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1404—Fluid conditioning in flow cytometers, e.g. flow cells; Supply; Control of flow
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N15/14—Electro-optical investigation, e.g. flow cytometers
- G01N15/1434—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement
- G01N15/1436—Electro-optical investigation, e.g. flow cytometers using an analyser being characterised by its optical arrangement the optical arrangement forming an integrated apparatus with the sample container, e.g. a flow cell
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J49/00—Particle spectrometers or separator tubes
- H01J49/02—Details
- H01J49/04—Arrangements for introducing or extracting samples to be analysed, e.g. vacuum locks; Arrangements for external adjustment of electron- or ion-optical components
- H01J49/0459—Arrangements for introducing or extracting samples to be analysed, e.g. vacuum locks; Arrangements for external adjustment of electron- or ion-optical components for solid samples
- H01J49/0463—Desorption by laser or particle beam, followed by ionisation as a separate step
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J49/00—Particle spectrometers or separator tubes
- H01J49/02—Details
- H01J49/10—Ion sources; Ion guns
- H01J49/105—Ion sources; Ion guns using high-frequency excitation, e.g. microwave excitation, Inductively Coupled Plasma [ICP]
-
- G01N15/01—
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N15/00—Investigating characteristics of particles; Investigating permeability, pore-volume, or surface-area of porous materials
- G01N15/10—Investigating individual particles
- G01N2015/1006—Investigating individual particles for cytology
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J49/00—Particle spectrometers or separator tubes
- H01J49/26—Mass spectrometers or separator tubes
- H01J49/34—Dynamic spectrometers
- H01J49/40—Time-of-flight spectrometers
Abstract
Изобретение относится к способам и устройствам для анализа образцов с использованием масс-спектрометрии индуктивно связанной плазмы, полученной лазерной абляцией (LA-ICP-MS). Способ масс-цитометрического анализа на основе лазерной абляции с использованием лазерно-абляционного масс-цитометра содержит этапы, при которых: направляют импульсы лазерного пучка на множество участков образца; захватывают каждую абляционную струю по отдельности; переносят каждую из захваченных по отдельности абляционных струй в индуктивно связанную плазму (ICP); ионизируют каждую из по отдельности захваченных и перенесенных абляционных струй в ICP, генерируя ионы для масс-цитометрического анализа. Причем лазерно-абляционный масс-цитометр содержит инжектор, выполненный с возможностью переноса абляционных струй в ICP; инжектор имеет впускной канал инжектора, расположенный в лазерно-абляционном источнике, впускной канал инжектора выполнен с возможностью захвата абляционных струй. Способ дополнительно содержит этапы, при которых: вводят поток газа захвата для введения абляционных струй в конус образца инжектора; и вводят поток газа переноса отдельно от потока газа захвата в инжектор для переноса абляционных струй из конуса образца в IPC. Технический результат - повышение точности клеточного анализа. 3 н. и 16 з.п. ф-лы, 10 ил.
Description
Перекрестная ссылка на родственные заявки
[1] Данная заявка испрашивает приоритет по предварительной патентной заявке США № 61/812,893, поданной 17 апреля 2013 г., содержание которой в полном объеме включено в данное описание посредством ссылки.
Область техники, к которой относится изобретение
[2] Это изобретение относится к устройству и способам лазерной абляции для клеточного анализа посредством масс-цитометрии.
Уровень техники
[3] Лазерная абляция, объединенная с масс-спектрометрией индуктивно связанной плазмы (ICP-MS) можно использовать для формирования изображения биологических образцов (клеток, тканей и т.д.), помеченных элементными маркерами. Каждый лазерный импульс генерирует струю подвергнутого абляции материала из образца, который может переноситься с целью ионизации для дальнейшего анализа масс-анализатором. Информация, полученная из лазерных импульсов в каждом положении на образце, затем может использоваться для формирования изображения образца на основании этого анализируемого содержания. Однако этот подход имеет ограничения в отношении возможности различать каждую отдельную струю подвергнутого абляции материала, создаваемую из каждого импульса лазерной абляции на образце.
Сущность изобретения
[4] В одном аспекте изобретение предусматривает способ масс-цитометрического анализа на основе лазерной абляции содержащий: направление импульсов лазерного пучка на образец для генерации струи образца для каждого из импульсов; захват каждой струи по отдельности для каждого из импульсов; перенос захваченных по отдельности струй в ICP; и ионизацию по отдельности захваченных и перенесенных в ICP струй и генерацию ионов для масс-цитометрического анализа.
[5] В соответствующем аспекте изобретение предусматривает лазерно-абляционный масс-цитометр, содержащий: лазерно-абляционный источник для генерации абляционной струи из образца и инжектор, выполненный с возможностью связывать лазерно-абляционный источник с ICP масс-цитометра; инжектор, имеющий впускной канал, расположенный в лазерно-абляционном источнике, причем впускной канал выполнен с возможностью захвата абляционной струи по мере генерации абляционной струи; и впускной канал газа, присоединенный к впускному каналу инжектора для пропускания газа между ними для переноса захваченной абляционной струи в ICP.
[6] Также, для иллюстрации, но не ограничения, раскрыты следующие иллюстративные аспекты изобретения.
[7] Аспект 1. Раскрыт способ масс-цитометрического анализа на основе лазерной абляции с использованием лазерно-абляционного масс-цитометра, причем способ содержит: a) направление импульсов лазерного пучка на множество участков образца для генерации абляционной струи образца для каждого из импульсов; b) захват каждой абляционной струи по отдельности; c) перенос каждой из захваченных по отдельности абляционных струй в индуктивно связанную плазму (ICP); и d) ионизацию каждой из по отдельности захваченных и перенесенных абляционных струй в ICP, таким образом, генерируя ионы для масс-цитометрического анализа.
[8] Аспект 2. Способ аспекта 1, в котором лазерно-абляционный масс-цитометр содержит: лазерно-абляционный источник для генерации абляционных струй из образца; источник ICP для создания ICP; и инжектор, выполненный с возможностью переноса абляционных струй в ICP; инжектор, имеющий впускной канал инжектора, расположенный в лазерно-абляционном источнике, причем впускной канал инжектора выполнен с возможностью захвата абляционных струй; и впускной канал газа, присоединенный к впускному каналу инжектора, выполненный с возможностью пропускать газ из впускного канала газа во впускной канал инжектора для переноса захваченной абляционной струи в ICP.
[9] Аспект 3. Способ аспекта 2, в котором впускной канал инжектора выполнен с возможностью полного или частичного захвата абляционной струи по мере генерации абляционной струи.
[10] Аспект 4. Способ любого из аспектов 1-3, в котором абляционная струя генерируется лазерным импульсом, направленным на мишень, содержащую образец, расположенный на подложке.
[11] Аспект 5. Способ любого из аспектов 1-3, в котором абляционная струя генерируется лазерным импульсом, направленным через прозрачную мишень, содержащую образец.
[12] Аспект 6. Способ аспекта 5, в котором прозрачная мишень содержит прозрачную подложку, на которой располагается образец.
[13] Аспект 7. Способ любого из аспектов 2-6, в котором впускной канал инжектора имеет форму конуса образца, причем более узкая часть конуса является апертурой впускного канала инжектора.
[14] Аспект 8. Способ аспекта 7, в котором конус образца располагается вблизи области, где генерируется абляционная струя.
[15] Аспект 9. Способ аспекта 8, в котором конус образца располагается на расстоянии около 100 мкм от поверхности мишени.
[16] Аспект 10. Способ любого из аспектов 7-9, в котором диаметр апертуры a) является регулируемым; b) имеет размер, препятствующий возмущению абляционной струи при ее прохождении в инжектор; и/или c) примерно равен диаметру в поперечном сечении абляционной струи.
[17] Аспект 11. Способ аспекта 7, в котором диаметр апертуры составляет около 100 мкм.
[18] Аспект 12. Способ любого из аспектов 4-12, дополнительно содержащий введение потока газа в область между впускным каналом инжектора и мишенью, для помощи в направлении струи через впускной канал инжектора.
[19] Аспект 13. Способ аспекта 13, в котором поток газа перпендикулярен мишени и перпендикулярен осевой линии просвета инжектора, по меньшей мере, в части просвета, ближайшей к впускному каналу инжектора.
[20] Аспект 14. Способ аспекта 12 или 13, в котором мишень является прозрачной мишенью.
[21] Аспект 15. Способ любого из аспектов 12-14, в котором поток газа содержит аргон.
[22] Аспект 16. Способ любого из аспектов 12-15, дополнительно содержащий введение потока газа переноса в инжектор для переноса струи к ICP.
[23] Аспект 17. Способ аспекта 16, в котором расход газа составляет около 0.1 литра в минуту, расход газа переноса составляет около 0.9 литра в минуту.
[24] Аспект 18. Способ аспектов 16 или 17, в котором поток газа переноса содержит аргон.
[25] Аспект 19. Способ любого из аспектов 1-4, 7-13 или 15-18, в котором образец располагается на подложке, и абляционная струя генерируется лазерным импульсом, направленным на образец со стороны образца.
[26] Аспект 20. Способ любого из аспектов 2-19, в котором впускной канал газа выполнен с возможностью направлять поток газа чистки под высоким давлением вблизи зоны, где формируется абляционная струя, для направления абляционной струи к впускному каналу инжектора.
[27] Аспект 21. Способ аспекта 20, в котором впускной канал газа содержит форсунку, апертура которой меньше диаметра впускного канала инжектора.
[28] Аспект 22. Способ любого из аспектов 1-21, в котором лазерный пучок генерируется фемтосекундным лазером.
[29] Аспект 23. Способ аспекта 1, в котором абляционная струя генерируется лазерным импульсом, направленным через прозрачную мишень, содержащую прозрачную подложку и образец.
[30] Аспект 24. Способ аспекта 23, в котором лазерно-абляционный масс-цитометр содержит: лазер для генерации абляционных струй из образца; факел индуктивно связанной плазмы (ICP); инжектор, выполненный с возможностью переноса абляционных струй в ICP, создаваемую факелом ICP; причем инжектор содержит стенку и просвет, и часть стенки инжектора образована прозрачной подложкой; причем инжектор содержит впускной канал инжектора для введения потока газа в просвет текущий, и прозрачная подложка располагается между впускным каналом инжектора и факелом ICP; образец присоединен к прозрачной подложке со стороны просвета; абляционные струи формируются ориентированными перпендикулярно просвету инжектора и формируются целиком в просвете инжектора; и каждая абляционная струя по отдельности захватывается газом, текущим через просвет инжектора к ICP.
[31] Аспект 25. Способ аспекта 24, в котором положение мишени фиксируется в ходе анализа.
[32] Аспект 26. Способ аспекта 25, в котором направление импульсов лазерного пучка на множество участков образца содержит перемещение лазерного пучка на участки, представляющие интерес, по неподвижному образцу.
[33] Аспект 27. Способ аспекта 26, в котором лазерный пучок перемещается в растровом режиме для формирования изображения.
[34] Аспект 28. Способ аспекта 24, в котором положение мишени изменяется в ходе анализа.
[35] Аспект 29. Способ аспекта 28, в котором, в ходе анализа, лазерный пучок остается неподвижным, и мишень перемещается.
[36] Аспект 30. Способ любого из аспектов 4-29, в котором положение мишени фиксируется в ходе анализа.
[37] Аспект 31. Способ аспекта 30, в котором, в ходе анализа, лазерный пучок остается неподвижным, и мишень перемещается.
[38] Аспект 32. Способ любого из аспектов 4-29, в котором положение мишени перемещается в ходе анализа.
[39] Аспект 33. Способ любого из аспектов 1-32, в котором импульсы лазерного пучка создают абляционные пятна размером в 1 мкм.
[40] Аспект 34. Способ любого предыдущего аспекта, в котором диаметр в поперечном сечении абляционной струи составляет порядка 100 мкм.
[41] Аспект 35. Способ любого предыдущего аспекта, в котором инжектор представляет собой трубку с внутренним диаметром около 1 мм.
[42] Аспект 36. Способ любого предыдущего аспекта, в котором абляционные струи, сформированные каждым лазерным импульсом, содержат частицы образца размерами около 1 мкм или менее.
[43] Аспект 37. Способ любого предыдущего аспекта, в котором расхождение абляционной струи при ее переносе в ICP поддерживается в пределах внутреннего диаметра просвета инжектора.
[44] Аспект 38. Лазерно-абляционный масс-цитометр, содержащий: лазерно-абляционный источник для генерации абляционных струй из образца; лазер, который излучает лазерный пучок с поверхности, причем поверхность ориентирована так, чтобы пучок направлялся на образец, содержащийся в лазерно-абляционном источнике; факел индуктивно связанной плазмы (ICP); инжектор, выполненный с возможностью связывать лазерно-абляционный источник с ICP, создаваемой факелом ICP; инжектор, имеющий впускной канал инжектора, расположенный в лазерно-абляционном источнике, причем впускной канал инжектора выполнен с возможностью захвата абляционной струи по мере генерации абляционной струи; и впускной канал газа, присоединенный к впускному каналу инжектора, причем впускной канал инжектора выполнен с возможностью пропускать газ из впускного канала газа во впускной канал инжектора для переноса захваченной абляционной струи в ICP.
[45] Аспект 39. Цитометр аспекта 38, выполненный так, что лазерный пучок ориентирован непосредственно к отверстию впускного канала инжектора.
[46] Аспект 40. Цитометр аспекта 39, выполненный так, что лазерный пучок выровнен с просветом инжектора, по меньшей мере, в части просвета, ближайшей к впускному каналу инжектора.
[47] Аспект 41. Цитометр аспекта 39, выполненный так, что проекция лазерного пучка перпендикулярна осевой линии просвета инжектора, по меньшей мере, в части просвета, ближайшей к впускному каналу инжектора.
[48] Аспект 42. Цитометр любого из аспектов 38-41, в котором лазерно-абляционный источник выполнен с возможностью принимать прозрачную мишень.
[49] Аспект 43. Цитометр аспекта 42, дополнительно содержащий прозрачную мишень.
[50] Аспект 44. Цитометр аспектов 42 или 43, в котором прозрачная мишень содержит прозрачную подложку и образец.
[51] Аспект 45. Цитометр любого из аспектов 38-44, в котором диаметр апертуры впускного канала инжектора меньше внутреннего диаметра инжектора.
[52] Аспект 46. Цитометр любого из аспектов 38-44, в котором впускной канал инжектора имеет форму конуса образца.
[53] Аспект 47. Цитометр аспекта 46, в котором конус образца располагается вблизи зоны, где генерируются абляционные струи.
[54] Аспект 48. Цитометр аспекта 46, в котором диаметр апертуры является регулируемым.
[55] Аспект 49. Цитометр любого из аспектов 45-48, содержащий прозрачную мишень.
[56] Аспект 50. Цитометр любого из аспектов 38-49, дополнительно содержащий впускной канал потока газа, выполненный с возможностью направлять газ перпендикулярно осевой линии просвета инжектора, по меньшей мере, в части просвета, ближайшей к впускному каналу инжектора.
[57] Аспект 51. Цитометр любого из аспектов 38-50, дополнительно содержащий впускной канал потока газа, выполненный с возможностью направлять газ по поверхности прозрачной мишени к апертуре, для помощи в направлении абляционной струи через впускной канал инжектора.
[58] Аспект 52. Цитометр аспекта 51, в котором впускной канал инжектора имеет форму конуса образца, дополнительно содержащий впускной канал потока газа переноса, расположенный с возможностью направлять газ в просвет инжектора.
[59] Аспект 53. Цитометр аспекта 38, содержащий впускной канал газа чистки под высоким давлением, выполненный с возможностью направлять абляционные струи во впускной канал инжектора.
[60] Аспект 54. Цитометр аспекта 53, в котором впускной канал газа чистки под высоким давлением содержит форсунку, апертура которой меньше апертуры впускного канала инжектора.
[61] Аспект 55. Лазерно-абляционный масс-цитометр, содержащий: фемтосекундный лазер для генерации абляционных струй из образца; факел индуктивно связанной плазмы (ICP); инжектор, выполненный с возможностью переноса абляционных струй в ICP, создаваемую факелом ICP; причем инжектор содержит стенку и просвет, и часть стенки инжектора образована прозрачной подложкой, причем упомянутая прозрачная подложка выполнена с возможностью принимать образец; причем инжектор содержит впускной канал инжектора для введения газа в просвет, причем прозрачная подложка располагается между впускным каналом инжектора и факелом ICP.
[62] Аспект 56. Цитометр аспекта 55, в котором прозрачная подложка подвижна относительно других частей стенки инжектора.
[63] Аспект 57. Цитометр аспекта 56, в котором прозрачная подложка может перемещаться в растровом режиме относительно других частей стенки инжектора.
[64] Аспект 58. Система лазерной абляции, содержащая a) лазер, способный создавать лазерное излучение; b) лазерную абляционную ячейку, содержащую прозрачную подложку для удержания анализируемого образца или платформу, выполненную с возможностью принимать прозрачную подложку; и c) инжектор для переноса абляционной струи в ICP, причем упомянутый инжектор содержит отверстие инжектора, причем (a), (b) и (c) выполнены так, что лазерное излучение исходит с одной стороны платформы или подложки, и отверстие инжектора находится с другой стороны.
[65] Аспект 59. Система аспекта 58, в котором лазерное излучение проходит через оптическое окно в абляционную ячейку.
[66] Аспект 60. Система аспекта 59, в котором отверстие инжектора выполнено так, что абляция области подложки приводит к формированию абляционной струи по ходу поверхности, из которой испускается лазерное излучение.
[67] Аспект 61. Система аспекта 60, в которой поверхностью является линза или зеркало.
[68] Аспект 62. Система аспекта 61, в которой отверстие инжектора выполнено так, что абляция области подложки приводит к формированию абляционной струи, по меньшей мере, частично в инжекторе.
[69] Аспект 63. Система любого из аспектов 58-62, содержащая (a) источник газа переноса для создания потока газа переноса в инжекторе, (b) источник газа захвата для создания потока газа захвата в абляционной ячейке, или оба (a) и (b).
[70] Аспект 64. Система любого из аспектов 58-63, в которой платформа перемещается в направлениях x-y или x-y-z.
[71] Аспект 65. Система любого из аспектов 58-63, содержащая биологический образец на прозрачной подложке.
[72] Аспект 66. Способ любого из аспектов 7-11, в которой лазерный пучок проходит через упомянутую апертуру.
[73] Аспект 67. Способ аспекта 66, в которой абляционная струя расширяется к поверхности, от которой испускается лазерный пучок.
[74] Аспект 68. Система масс-спектрометрии индуктивно связанной плазмы, полученной лазерной абляцией, содержащая: лазерно-абляционный источник для генерации абляционной струи из образца; лазер, который излучает лазерный пучок, причем упомянутый пучок проходит через объектив к образцу, содержащемуся в лазерно-абляционном источнике; факел индуктивно связанной плазмы (ICP); и инжектор, выполненный с возможностью связывать лазерно-абляционный источник с ICP, создаваемой факелом ICP; причем инжектор проходит через отверстие в объективе; инжектор, имеющий впускной канал инжектора, расположенный в лазерно-абляционном источнике, причем впускной канал инжектора выполнен с возможностью захвата абляционной струи по мере генерации абляционной струи.
[75] Аспект 69. Система аспекта 68, в которой лазерный пучок отражается от зеркала в объектив.
[76] аспект 70. Система аспекта 69, в которой инжектор проходит через отверстие в зеркале.
[77] Аспект 71. Система любого из аспектов 68-70, в которой абляционный источник содержит впускной канал для потока газа захвата.
[78] Аспект 72. Система любого из аспектов 68-71, в которой абляционный источник содержит платформу, выполненную с возможностью принимать мишень.
[79] Аспект 73. Система масс-спектрометрии индуктивно связанной плазмы, полученной лазерной абляцией, выполненная с возможностью использования согласно любому раскрытому здесь способу.
Краткое описание чертежей
[80] Специалисту в данной области техники понятно, что чертежи, описанные ниже, служат только в целях иллюстрации. Чертежи никоим образом не призваны ограничивать объем изобретения.
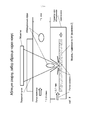
[81] Фиг.1 - схема лазерно-абляционного масс-цитометра.
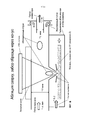
[82] Фиг.2 - схема варианта осуществления лазерно-абляционного источника, показанного на фиг.1, демонстрирующая забор образца лазерной абляционной струи через апертуру, выполненную с возможностью переноса струи в инжектор.
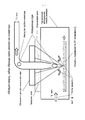
[83] Фиг.3 - вид альтернативной конфигурации, аналогичной показанной на фиг.2, где струя отбирается непосредственно в инжектор.
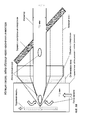
[84] Фиг.4 и фиг.5 - схемы различных других вариантов осуществления лазерно-абляционного источника, показанного на фиг.1, демонстрирующие генерацию и забор образца лазерной абляционной струи в инжекторе.
[85] Фиг.6 - вид альтернативной конфигурации, аналогичной показанной на фиг.2, но демонстрирующий поток "чистки под высоким давлением", направленный перпендикулярно формированию струи, для направления струи для переноса в инжектор.
[86] Фиг.7 - вариант осуществления, где исследуемый образец освещается лазерным светом сверху.
[87] Фиг.8 - вариант осуществления в котором часть оболочечного потока отводится в качестве жертвенного потока, тогда как сердцевина оболочечного потока, содержащая поток газа захвата и материал струи, подводится.
[88] Фиг.9 демонстрирует компоновку, в которой струя отбирается в инжектор, который проходит через объектив.
[89] Фиг.10 демонстрирует компоновку, в которой струя отбирается в инжектор, который проходит через объектив и зеркало.
Подробное описание различных вариантов осуществления
[90] Следует понимать, что употребление наименования различных элементов в соответствии с принципами настоящего изобретения охватывает "один или более" или "по меньшей мере, один", если из контекста явно не следует обратное.
[91] Настоящее изобретение относится к лазерной абляции, объединенной с масс-спектрометрией индуктивно связанной плазмы (LA-ICP-MS). LA-ICP-MS описана для измерения эндогенных элементов в биологических материалов и, в частности, для формирования изображения путем обнаружения антител, маркированных элементами. См., например, Antonov, A. and Bandura, D., 2012, U.S. Pat. Pub. 2012/0061561, включенный сюда посредством ссылки; Seuma et al., "Combination of immunohistochemistry and laser ablation ICP mass spectrometry for imaging of cancer biomarkers" 2008, Proteomics 8:3775-3784; Hutchinson et al. "Imaging and spatial distribution of β-amyloid peptide and metal ions in Alzheimer's plaques by laser ablation-inductively coupled plasma-mass spectrometry" Analytical biochemistry 2005, 346.2:225- 233; Becker et al. "Laser ablation inductively coupled plasma mass spectrometry (LA-ICP- MS) in elemental imaging of biological tissues and in proteomics." 2007, Journal of Analytical Atomic Spectrometry 22.7:736-744; Binet, et al., "Detection and characterization of zinc- and cadmium-binding proteins in Escherichia coli by gel electrophoresis and laser ablation-inductively coupled plasma-mass spectrometry" Analytical Biochemistry 2003,318:30-38; Quinn, et al., "Simultaneous determination of proteins using an element-tagged immunoassay coupled with ICP-MS detection Journal of Analytical Atomic Spectrometry" 2002, 17:892-96; Sharma, et al., "Sesbania drummondii cell cultures: ICP-MS determination of the accumulation of Pb and Cu Microchemical Journal" 2005, 81:163-69; и Giesen et al. "Multiplexed immunohistochemical detection of tumor markers in breast cancer tissue using laser ablation inductively coupled plasma mass spectrometry" 2011, Anal. Chem. 83:8177-8183, каждый из которых включен сюда посредством ссылки.
[92] Настоящее изобретение предусматривает способы масс-цитометрического анализа на основе лазерной абляции, в которых импульсы лазерного пучка направляются на образец для генерации струи образца для каждого из импульсов; каждая струя по отдельности захватывается для каждого из импульсов; каждая по отдельности захваченная струе переносится в ICP; и каждой из по отдельности захваченных и перенесенных в ICP струй ионизируется и ионы для масс-цитометрического анализа генерируются, и устройства для осуществления способа. В различных вариантах осуществления, лазерно-абляционный масс-цитометр может иметь лазерно-абляционный источник для генерации абляционной струи из образца и инжектор, выполненный с возможностью связывать лазерно-абляционный источник с ICP масс-цитометра. В некоторых вариантах осуществления инжектор может иметь впускной канал, расположенный в лазерно-абляционном источнике, благодаря чему, впускной канал может быть выполнен с возможностью захвата абляционной струи по мере генерации абляционной струи. Впускной канал газа может быть присоединен к впускному каналу инжектора для пропускания газа между ними для переноса захваченной абляционной струи в ICP.
[93] В одном аспекте изобретение предусматривает лазерно-абляционный масс-цитометр, который имеет (i) лазерно-абляционный источник, (ii) инжектор, выполненный с возможностью связывать лазерно-абляционный источник с ICP, создаваемой источником ICP; и (iii) масс-анализатор.
[94] Лазерно-абляционный источник, также именуемый "абляционной ячейкой", заключает в себе образец в ходе абляции. Обычно абляционная ячейка включает в себя окно, прозрачное для лазерного света, чтобы энергия лазера могла попадать на образец. В необязательном порядке, абляционная ячейка включает в себя платформу для удержания анализируемого образца. В некоторых вариантах осуществления платформа подвижна в измерениях x-y или x-y-z. В приведенных здесь чертежах и примерах, лазерно-абляционный источник иногда показана как открытая компоновка. Однако такие конфигурации служат исключительно для иллюстрации, и можно понять, что присутствует некоторая форма подходящей оболочки для предотвращения загрязнения или инфильтрации из внешней среды. Например, лазерно-абляционный источник может быть помещен в камеру, снабженную впускными каналами газа и/или оптическими портами, для обеспечения внутренней среды, подходящий для захвата и переноса абляционной струи для анализа масс в ICP. Впускные каналы газа и оптический(е) порт(ы) располагаются так, чтобы ориентация лазерного пучка, образец, расширение струи, и инжектор пригодны для раскрытых здесь способов и устройств. Очевидно, что абляционная ячейка, в общем случае, является газонепроницаемой (за исключением особых выходов и портов).
[95] Лазеры, используемые для лазерной абляции согласно изобретению, в общем случае, делятся на три категории: фемтосекундные импульсные лазеры, дальнеультрафиолетовые импульсные лазеры и импульсные лазеры с длиной волны, выбранной для сильного поглощения в подвергнутом абляции материале ("избирательные по длине волны лазеры"). Дальнеультрафиолетовые и лазеры с конкретной длиной волны, обычно работают с наносекундными или пикосекундными импульсами. Каждый класс лазеров имеют свои недостатки и достоинства и может быть выбран в зависимости от конкретного применения. В некоторых вариантах осуществления, лазер представляет собой фемтосекундный импульсный лазер выполненное с возможностью работать с частотой импульсов от 10 до 10000 Гц. Фемтосекундные лазеры известны (см., например, Jhanis et al., "Rapid bulk analysis using femtosecond laser ablation inductively coupled plasma time-of-flight mass spectrometry" J. Anal. At. Spectrom., 2012, 27:1405-1412.
[96] Фемтосекундные лазеры позволяют осуществлять лазерную абляцию практически всех материалов при условии достаточной плотности мощности для лазерной абляции. Этого можно добиться даже со сравнительно низкой энергией импульса, когда пучок точно сфокусирован, например, до диаметра в 1 мкм и имеет малую длительность (сфокусирован по времени). Дальнеультрафиолетовые лазеры также могут вызывать абляцию большого класса материалов, поскольку большинство широко используемых материалов поглощают дальнеультрафиолетовые фотоны. В абляции с помощью лазера избирательного по длине волны можно использовать лазеры с конкретной длиной волны лазера усиленного поглощения в материале подложки. Преимуществом лазера с конкретной длиной волны может быть стоимость и простота лазера и оптической системы, хотя и с более ограниченным спектром материалов подложки. Подходящие лазеры могут иметь разные принципы работы, например, твердотельные (например, Nd:YAG), эксимерные лазеры, оптоволоконные лазеры и OPO лазеры.
[97] Полезное свойство света фемтосекундного лазера состоит в том, что он поглощается только при достижении пороговой плотности мощности. Таким образом, схождение фемтосекундного лазерного света может проходить через более толстое сечение материала, не испытывая поглощения или не вызывая никаких повреждений и все же приводя к абляции того же материала прямо на поверхности, где происходит фокусировка. Затем фокус может постепенно перемещаться внутрь материала, в то время как слои образца подвергаются абляции. Наносекундные лазерные импульсы могут частично поглощаться подложкой, но при этом по-прежнему вызывать абляцию, поскольку плотность энергия в фокальной точке является наивысшей (при условии, что ее достаточно для абляции).
[98] Лазерному импульсу можно придавать форму с использованием апертуру, его можно гомогенизировать (при необходимости) с использованием гомогенизатора пучка, фокусировать, например, с использованием объектива, для создания пятна желаемого размера менее 10 мкм. Иллюстративные размеры пятна включают в себя диаметры (или области абляции эквивалентных размеров других форм) в диапазоне 0.10-3 мкм (например, около 0.3 мкм), 1-5 мкм (например, около 3 мкм), 1- 10 мкм (например, около 1, около 2, около 3, около 4 или около 5 мкм), менее 10 мкм и менее 5 мкм. В конкретных вариантах осуществления, лазерная система выполнена с возможностью работы с достаточно сфокусированными лазерными импульсами, чтобы обеспечивать абляцию области образца порядка 1 мкм, например, от 100 мкм до 1 мкм. Абляция столь малого масштаба создает очень малое количество материала струи, что, в свою очередь, гарантирует, что размер струи остается малым. Чем меньше струя, тем с большей вероятностью она будет оставаться в середине потока газа захвата, не контактируя со стенками абляционной ячейки или газопроводов инжектора. Абляция в масштабе 1 мкм также означает, что расстояние между поверхностью, подвергнутой абляции, и областью, где расширение струи замедляется, и где начинает преобладать внешний газ, очень мало. Это расстояние может составлять от нескольких микрон до нескольких сотен микрон. В некоторых версиях изобретения присутствует поток газа захвата, где струя перестает расширяться. Таким образом, для иллюстрации, но не ограничения, на некоторых прилагаемых чертежах показано, что расстояние между поверхностью, подвергнутой абляции, и областью с потоком газа захват составляет около 100 мкм.
[99] Хотя абляция в масштабе 1 мкм (или менее) имеет преимущество для определенных вариантов применения (например, формирования изображения), способы и инструменты изобретения также полезны при создании более крупных абляционных пятен, например абляционных пятен диаметром от около 5 до около 35 мкм, например в диапазоне 5-15 мкм, 10-20 мкм, 15-25 мкм, 20-30 мкм и 25-35 мкм. В некоторых вариантах применения, предусматривающих создание больших абляционных пятен, захватывается лишь часть материала струи.
[100] В некоторых вариантах осуществления, лазер располагается вне лазерно-абляционного источника, и лазерный пучок (энергия лазера) поступает в лазерно-абляционный источник, например, через оптическое окно. Используемый здесь лазерный пучок можно описать как излучаемый с поверхности (например, линзы или зеркала лазера), причем поверхность может быть ориентирована с возможностью направлять пучок в конкретное положение или рисунок положений. Для простоты описания изобретения, можно считать, что направленный пучок имеет конкретную ориентацию; ориентацию пучка можно представить воображаемой линией, выровненной с пучком и выходящей за пределы фактического пучка (например, когда пучок падает на непрозрачную поверхность). Как явствует из контекста, ориентация или положение лазерного пучка иногда определяется как ориентация или положение, которые создавал бы пучок выключенного лазерного источника, если бы лазер был включен.
[101] Масс-анализаторы для использования в изобретении можно выбирать на основании потребностей оператора или конкретного применения. Иллюстративные типы масс-анализаторов включают в себя квадрупольный, времяпролетный, магнитный секторный, высокого разрешения, одно- или многоколлекторные масс-спектрометры ICP. Обычно времяпролетные масс-спектрометры используются для регистрации быстрых переходных событий с длительностями переноса, ожидаемыми для установки быстрой ICP, полученной лазерной абляцией.
[102] Ионы создаются, когда частицы абляционной струи входят в плазму (индуктивно связанную плазму, ICP), поддерживаемую в источнике ICP или факеле ICP.
[103] Масс-цитометр можно использовать для анализа или формирования изображения биологического образца, который может располагаться на прозрачной подложке. В вариантах осуществления формирования изображения, лазер, в общем случае, может работать в режиме непрерывной последовательности импульсов или в режиме пакетов импульсов, направленных в разные позиции образца, именуемые "пятнами, представляющими интерес" или "положениями или зонами абляции". Импульсы могут направляться в пятна, образующие заданный рисунок, например растр для формирования двухмерного изображения. Альтернативно, можно подвергать абляции множество отдельных пятен в разных положениях (например, соответствующих отдельным клеткам). В некоторых вариантах осуществления, лазер излучает пакет импульсов, создающий струи, выходящие из одного и того же пикселя (т.е. одного и того же положения на мишени). Предполагается, что абляционные струи, создаваемые отдельными импульсами в пакете, сливаются в одну струю и распространяются в инструменте таким образом, что их можно отличить от струи, создаваемой из другого пикселя. Для различения отдельных пикселей, промежуток времени между пакетами (опросами пикселя, которые могут состоять из одного единственного импульса или 100 импульсов), поддерживается выше некоторого предела, определяемого расхождением по времени ионного сигнала (на детекторе) из отдельного пикселя.
[104] Как описано ниже, один признак изобретения состоит в том, что абляционная струя переносится из участка формирования струи в ICP в процессе, который позволяет по отдельности анализировать каждую отдельную струю образца. Струя переносится из зоны формирования в ICP, по меньшей мере, частично, через патрубок или инжекторную трубку ("инжектор"). Трубка может быть сформирована, например, сверлением подходящего материала для создания просвета (например, просвет с круглым, прямоугольным или другим поперечным сечением) для переноса струи. Инжекторная трубка иногда имеет внутренний диаметр в диапазоне от 0.2 мм до 3 мм. В некоторых вариантах осуществления инжекторный патрубок имеет меньший диаметр, например, будучи объединен с микроканальным устройством или включен в его состав. В некоторых вариантах осуществления, внутренний диаметр инжектора изменяется вдоль инжектора. Например, инжектор может иметь заостренный конец. Длина инжектора иногда составляет от 1 см до 100 см. В некоторых вариантах осуществления длина не превышает 10 см (например, составляя 1-10 см), не превышает 5 см (например, составляя 1-5 см) или не превышает 3 см (например, составляя 0.1-3 см). Инжектор может быть сформирован, без ограничения, из металла (например, стали), кварца, стекла, сапфира или других материалов. В некоторых вариантах осуществления просвет инжектора является прямолинейным на всем своем протяжении, или почти на всем своем протяжении, от абляционного источника до ICP. В некоторых вариантах осуществления просвет инжектора не является прямолинейным на всем своем протяжении и изменяет ориентацию. Например, патрубок может делать плавный изгиб на 90 градусов. Эта конфигурация позволяет струе первоначально перемещаться в вертикальной плоскости, пока ось на впускном канале инжектора указывает прямо вверх, и перемещаться горизонтально, в направлении факела ICP (который обычно ориентирован горизонтально, чтобы пользуются преимуществом конвекционного охлаждения). В некоторых вариантах осуществления инжектор является прямолинейным на протяжении, по меньшей мере, 0.1 см, по меньшей мере, 0.5 см или, по меньшей мере, 1 см от апертуры, через которую поступает или формируется струя.
[105] Используемая здесь "осевая линия" просвета инжектора представляет собой воображаемую линию, проходящую через центр или выходящую из просвета, в необязательном порядке, линию, совпадающую с осью симметрии, и является полезной опорой для ориентации. Например, лазерный пучок, ориентация расширения струи и осевая линия могут быть выровнены друг с другом. В другом примере, ориентация расширения струи может быть перпендикулярна (например, ортогональна) осевой линии.
[106] В соответствии с принципами настоящего изобретения, каждая отдельная струя образца может по отдельности анализироваться масс-анализатором. В одном аспекте, устройство выполнено так, что расхождение струи в абляционной ячейке (абляционном источнике) и инжекторе меньше расхождения, которое происходит в источнике ICP и масс-анализаторе. В одном аспекте, струи могут по отдельности анализироваться за счет переноса каждой абляционной струи в ICP за период времени в пределах совокупного времени переноса струи в ICP и детектирования ионов масс-анализатором. Это можно осуществлять путем захвата каждой струи образца потоком газа и согласно конфигурации переноса, благодаря чему, отношение расширения струи в течение периода времени переноса (т.е. переноса абляционной струи из участка абляции в плазму) к расширению в течение периода времени переноса ионов (т.е. переноса ионов из плазмы в масс-анализатор) меньше или равно единице.
[107] В общем случае, предельный размер частицы образца, которую источник ионов ICP может эффективно испарять и ионизировать в целях аналитического детектирования, составляет порядка 10 мкм или менее. Частицы, создаваемые лазерной абляцией в масштабе 1 мкм, меньше 1 мкм и хорошо подходят для источника ионов ICP. Для анализа отдельных частиц (который, например, может осуществляться с использованием прибора CyTOF®, Fluidigm Canada Inc.), типичная частота, с которой эти частицы можно ионизировать и аналитически детектировать, может быть функцией совокупного расширения или расхождения времени переноса образца в плазме, пока частицы испаряются и ионизируются, и расширения или расхождения по времени переноса ионов между ICP и масс-анализатором для его детектирования. В общем случае совокупное расширение или расхождение по времени может составлять порядка 200 мкс. В результате, для частиц размером 10 мкм или менее, которые пространственно разделены, анализ каждой отдельной частицы может обеспечиваться переносом каждой частицы в ICP за период времени порядка 200 мкс. В некоторых вариантах осуществления частицы переносятся в ICP менее чем за 200 мкс, или менее чем за 150 мкс. Соответственно, в системе введения образца, где формирование изображения биологических образцов может осуществляться посредством лазерной абляции, лазерная система может быть выполнена с возможностью работы с достаточно сфокусированными лазерными импульсами, чтобы обеспечивать абляцию области образца порядка 1 мкм, например с применением фемтосекундного импульсного лазера. В этой конфигурации, абляционные струи, сформированные каждым лазерным импульсом, могут включать в себя частицы образца размерами обычно около 1 мкм или менее. В определенных описанных здесь условия, эти частицы могут захватываться и переноситься в соответствии с необходимым периодом времени переноса, что позволяет ICP эффективно испарять и ионизировать каждую отдельную струю.
[108] Дополнительно, когда лазер выдает непрерывную последовательность импульсов, например, в случае растровой развертки по поверхности образца для формирования двухмерного изображения, индивидуальность каждой струи и пространственное разделение между каждой парой последовательных струй могут поддерживаться между зоной формирования струи и точкой испарения и ионизации в источнике ионов ICP. Например, при переносе струи через патрубок, например, инжекторную трубку, показанную на фиг.1, частицы в струе могут распространяться и расширяться наружу в радиальном направлении, прежде чем войти в плазму ICP. Расхождение частиц, создаваемых в струе, может зависеть от их коэффициента диффузии, профиля скоростей потока переноса и распределения плотности частиц по мере его формирования и развития в ходе переноса в ICP. Например, размер пятна фемтосекундной лазерной абляции 1 мкм позволяет создавать струю с начальным диаметром в поперечном сечении около 100 мкм или менее до дополнительного расхождения в ходе ее переноса. Степень расхождения струи также может быть функцией размера подвергнутой абляции частицы; для более крупных частиц свойственно более медленное диффузное расхождение, но более высокий импульс, что приводит к потенциальным потерям вследствие контакта с внутренними стенками инжекторной трубки. Таким образом, желательно минимизировать расхождение струи и/или переносить струю в ICP в течение достаточного времени, чтобы испарять и ионизировать до того, как степень расхождения будет представлять какие-либо эффекты канализации.
[109] Соответственно, в различных вариантах осуществления, использование лазера для абляции пятен образца размером 1 мкм и эффективного переноса струи таким образом, чтобы расхождение, поддерживаемое в пределах внутреннего диаметра инжекторной трубки, могло достигаться за счет иллюстративных компоновок, описанных здесь и в прилагаемых чертежах.
[110] Для данной системы лазерной абляции и данного образца, абляционные струи расширяются после лазерной абляции, пока не достигнут характерного объема, именуемого "объемом забора образца". Желательно, чтобы система была выполнена с возможностью минимизации объема забора образца, и повышения скорости, с которой поток газа уносит струю из объема забора образца. Сочетание малого объема забора образца и быстрого потока газа снижает расхождение по времени переноса струи в инжектор. Объем забора образца можно описать огибающей струи в момент, когда скорость расширения струи любого размера падает значительно ниже (~10 раз) скорости звука в окружающих газообразных средах. Без ограничения, иллюстративные объемы забора образца могут составлять от 10-6 мм3 до 10 мм3. Часто объем забора образца составляет от 0.001 мм3 до 1 мм3. Поток газа захвата, при наличии, течет в, по меньшей мере, часть объема забора образца и несет, по меньшей мере, часть струи в инжектор, после чего, она может переноситься потоком газа переноса в IPC. Желательно, чтобы скорость потока газа захвата, когда он поступает в объем забора образца, была существенной (например, >1 м/с, >10 м/с, >100 м/с или > 500 м/с). В некоторых вариантах осуществления скорость потока газа захвата, когда он поступает в объем забора образца, можно оценивать путем измерения скорости потока газа захвата в инжектор (например, через апертуру инжектор). В некоторых вариантах осуществления эта измеренная скорость >1 м/с, >10 м/с, >100 м/с или > 500 м/с. В отличие от настоящего изобретения, в отсутствие быстрого удаления струи, она будет продолжать расширяться и диффундировать, нежелательно заполняя всю абляционную ячейку.
[111] В одном аспекте, изобретение предусматривает конфигурацию лазерной абляции, в которой лазерный пучок направляется на мишень. В одном варианте осуществления, мишень содержит подложку и образец, расположенный на подложке. В одном варианте осуществления подложка прозрачна, и мишень является прозрачной мишенью.
[112] В одном аспекте, изобретение предусматривает конфигурацию лазерной абляции (рассмотренную ниже в контексте фиг.2, но без ограничения), для "сквозной" абляции. В этой конфигурации, импульс лазерного пучка направляется через прозрачную мишень, и струя образца ("абляционная струя" или "струя") формируется по ходу пучка в инжектор. Также см. Фиг.3-5. Сквозное облучение мишени имеет преимущество в оптимизации расширения переноса по времени вследствие удаления оптических элементов (окон, объективов и т.д.) из прямолинейного пути струи. В одном аспекте, изобретение предусматривает систему лазерной абляции, содержащую (a) лазер, способный создавать лазерное излучение; (b) лазерную абляционную ячейку (или лазерно-абляционный источник), куда можно вводить прозрачную мишень, и инжектор с отверстием, через которое может входить абляционная струя, причем лазерное излучение исходит от поверхности на одной стороне прозрачной мишени, и отверстие инжектора находится на другой стороне. Другие признаки, которые могут быть включены в систему, описаны на протяжении этого раскрытия, включающего в себя примеры.
[113] Согласно фиг.1, a лазерно-абляционный масс-цитометр содержит лазерно-абляционный источник, который может быть соединен с инжектором, например, трубкой изготовленной из кварца или другого, в общем случае, подходящего материала и установленного для доставки образца в источнике индуктивно связанной плазме (ICP), также именуемом факелом ICP. Плазма факела ICP может испарять и ионизировать образец для формирования ионов, которые может принимать масс-анализатор.
[114] В различных вариантах осуществления согласно фиг.2, образец, представляющий интерес, может быть выполнен с возможностью лазерной абляции с использованием образца, форматированного для совместимости с прозрачной мишенью. Образец можно помещать на прозрачную подложку, включать в прозрачную подложку или можно формировать в качестве прозрачной мишени. Подходящие подложки, прозрачные для лазерного света, может содержать стекло, пластик, кварц и другие материалы. В общем случае, подложка является, по существу, планарной или плоской. В некоторых вариантах осуществления подложка является искривленной. В некоторых вариантах осуществления подложки имеют толщину от 0.1 мм до 3 мм,. В некоторых вариантах осуществления, подложка кодируется (см., например, Antonov A. и Bandura D., 2012, U.S. Pat. Pub. 2012/0061561, включенную сюда посредством ссылки). В этой конфигурации, импульс лазерного пучка направляется через прозрачную мишень, и струя образца ("абляционная струя" или "струя") формируется по ходу пучка в инжектор.
[115] Инжектор, или инжекторная трубка, может иметь впускной канал, выполненный с возможностью захвата абляционной струи; например, впускной канал, сформированный как конус образца, имеющий малое отверстие или апертуру, как показано на фиг.2. В этой конфигурации, конус образца может располагаться вблизи области, или зоны, где формируется струя. Например, отверстие конуса образца может располагаться на расстоянии от 10 мкм до 1000 мкм от прозрачной мишени, например, на расстоянии около 100 мкм от прозрачной мишени. В результате, абляционная струя может генерироваться и формироваться, по меньшей мере, частично в расширяющейся области конуса. В некоторых вариантах осуществления, диаметр апертуры и/или размеры промежутка (включая углы) регулируются для обеспечения оптимизации в различных условиях. Например, когда струя имеет диаметр в поперечном сечении порядка 100 мкм, можно использовать апертуру диаметром порядка 100 мкм с достаточным просветом для предотвращения возмущения струи при ее прохождении.
[116] В такой конфигурации инжектор может продолжаться по ходу конуса забора образца для приема абляционной струи, чтобы содействовать движению струи и сохранять пространственную индивидуальность каждой следующей струи как функцию лазерных импульсов. Соответственно, поток газа можно вводить для помощи в направлении струи через апертуру конуса забора образца для захвата (поток газа захвата) каждой струи по отдельности, тогда как дополнительный поток газа можно вводить в инжектор для переноса (поток газа переноса или оболочечный поток) каждой по отдельности захваченной струи к ICP. Другой функцией потока переноса или оболочечного потока является предотвращение контакта частиц, создаваемых в струе, со стенками инжектора. Газ(ы) могут представлять собой, например, но без ограничения, аргон, ксенон, гелий, азот или их смеси. В некоторых вариантах осуществления газом является аргон. Расход газа захвата и расход газа переноса могут быть одинаковыми или разными.
[117] На основании этого раскрытия специалист в данной области техники может выбирать или определять значения расхода газа, подходящие для настоящего изобретения. Полный расход через инжектор обычно определяется требованиями источника ионизации ICP. Лазерная абляционная установка должна обеспечивать расход, удовлетворяющий этим требованиям. Например, на фиг.2, а также другие фигуры, демонстрирующие различные конфигурации, инжекторная трубка, в общем случае, описана с внутренним диаметром 1 мм совместно с совокупным расходом газа около 1 литра в минуту (0.1 литра в минуту расход газа захвата плюс расход газа переноса 0.9 литра в минуту). Предполагается, что инжекторы меньшего или большего диаметра, совместно с соответственно выбранными значениями расхода газа, можно применять к различным геометриям, представленным с аналогичными ожидаемыми результатами. Желательно создавать условия для поддержания газовая динамика без турбулентности в инжекторной трубке для сохранения индивидуальности каждой отдельной абляционной струи.
[118] Как описано здесь, при данной конкретной конфигурации элементов (например, конкретная конфигурация положений впускного канала газа, апертур, свойств инжектора и других элементов), значений расхода газа захвата и переноса выбираются так, чтобы каждая абляционная струя переносилась в ICP за период времени, укладывающийся в совокупное время переноса струи между ICP и масс-анализатором для его детектирования. Это можно осуществлять путем захвата каждой струи образца потоком газа и согласно конфигурации переноса, благодаря чему, отношение расширения струи в течение периода времени переноса к расширению в течение периода времени переноса ионов меньше или равно единице. То есть, расширение по времени (или расхождение по времени) сигнала переноса, что важно. Устройства ICP-MS (например, инструмент ICP-TOF CyTOF®, Fluidigm Canada Inc.) характеризуются внутренним расширением сигнала. В случае лазерной абляции, действие инжекции единичной струи может быть быстрым или медленным по сравнению с расхождением по времени на самом ICP-MS. Расхождение струи перед плазмой зависит от конструкции абляционной ячейки и канала доставки струи (инжектора). Желательно, чтобы лазерная абляционная ячейка и ее система доставки образца (инжектор) не расширяли первоначальную абляционную струю сверх внутреннего расширения оставшегося инструмента. Это условие гарантирует, что пик сигнала детектирования, создаваемого абляционной струей является острым (по времени), поскольку может соответствовать выбранному инструменту. Если расхождение струи гораздо дольше, чем расхождение в ICP-MS, событие лазерной абляции единичным импульсном, окажется гораздо шире на детекторе. Однако если расхождение в сечении лазерной абляции меньше инструментального расхождения, инструментальное расхождение преобладает над полным расхождением. Таким образом, инструментальное расхождение можно измерить с использованием калибровочных бусин и затем измерять полное расхождение от единичного лазерного импульса и сравнивать эти два числа. Если расхождение от лазерной абляции меньше расхождения от инструмента, полное расхождение будет менее чем в 2 раза превышать инструментальное расхождение.
[119] Характерное инструментальное расширение по времени можно измерять экспериментально, например, с использованием помеченных клеток или калибровочных бусин. Всякий раз, когда единичная бусина поступает в масс-цитометр (например, инструмент ICP-TOF CyTOF®), бусина подвергается испарению и ионизации в плазме и затем проходит через масс-анализатор, пока ее сигнал не достигнет детектора. Переходное событие детектируется и используется для записи информации о конкретной бусине, например, ширины переходного сигнала (который представляет расхождение по времени от единичного события) и значения расхождения, которое происходит, начиная с источника ICP и заканчивая на детекторе.
[120] В некоторых вариантах осуществления, устройство выполнено так, что допускает расхождение по времени от 10 до 1000 мкс для пути, заданного между образцом и ионным детектором масс-анализатора.
[121] Типичные значения расхода газа захвата составляют от 0.1 до 1 л/мин. Оптимальный расход газа захвата можно определять экспериментально, но обычно находится на нижней границе диапазона (например, около 0.1 л/мин). Типичные значения расхода газа переноса составляют от 0.1 до 1 л/мин. Оптимальный расход газа переноса можно определять экспериментально, но обычно находится на верхней границе диапазона (например, около 0.9 л/мин). В некоторых вариантах осуществления, расход газа захвата ниже расхода газа переноса. В ряде случаев расход газа переноса может быть равно 0, например, если расход газа захвата приблизительно равен 1 л/мин. Расход газа переноса часто составляет 0.4-1 л/мин (например, 0.4, 0.6, 0.8 или 1 л/мин).
[122] Для иллюстрации, в конфигурации, показанной на фиг.2, расход газа, подаваемого для захвата струи через конус забора образца может составлять около 0.1 литра в минуту, тогда как поток газа переноса около 0.9 литра в минуту может проходить через инжекторную трубку внутренним диаметром 1 мм. Потоки газа и ориентацию их введения можно оптимизировать для эффективного захвата и переноса каждой абляционной струи таким образом, что каждая струя поддерживает свою индивидуальность.
[123] В различных вариантах осуществления согласно фиг.3, конус забора образца, показанный на фиг.2, можно исключить, в результате чего, вместо апертуры можно поместить инжектор с открытым концом. В этой конфигурации питающий газ можно вводить с совокупным расходом около 1 литра в минуту, чтобы иметь возможность захвата и переноса каждой абляционной струи по отдельности и непосредственно в инжектор. В некоторых вариантах осуществления расстояние между поверхностью прозрачной мишени и впускным каналом инжектора равно 500 мкм или менее, например, менее около 200 мкм, менее около 100 мкм или менее около 50 мкм. В конфигурации, показанной на фиг.3, не существует отдельных потока газа захвата и потока газа переноса. Вместо этого, единичный поток газа направляет струю через апертуру и переносит по отдельности захваченную струю в ICP. В этой компоновке, расход газа часто составляет от 0.2 литра в минуту до 2 литров в минуту.
[124] В различных вариантах осуществления, абляционная струя может формироваться непосредственно в инжекторной трубке, причем направление ее формирования ориентировано поперечно, как указано на фиг.4 и фиг.5. С аналогичной конфигурацией прозрачной мишени, как описано согласно фиг.2, каждая абляционная струя может захватываться потоком газа (около 1 литра в минуту) и переноситься далее в ICP. Поскольку прозрачная мишень, представленная на фиг.4, находится в фиксированном положении относительно инжекторной трубки, положение каждого абляционного пятна может изменяться для обеспечения возможностей сканирования. Например, абляция падающим лазерным пучком может перемещаться в различные пятна, представляющие интерес, по неподвижному образцу или перемещаться в растровом режиме для обеспечения усиленной возможности формирование изображения. В общем случае, в операции растровой развертки, импульсный лазер действует непрерывно, поскольку положение абляции изменяется согласно заданному рисунку. Альтернативно, в различных вариантах осуществления, лазерный пучок может оставаться неподвижным, в то время как мишень может быть выполнена с возможностью перемещения для обеспечения абляции в разных пятнах, как показано на фиг.5.
[125] В различных вариантах осуществления согласно фиг.6, лазерный пучок может падать на мишень со стороны образца. В этом примере, образец может располагаться на подложке, и каждый импульс лазерного пучка может генерировать абляционную струю, расширяющуюся в направлении падения лазерного света. Лазерный свет может быть примерно ортогонален подложке или может быть ориентирован под другими углами, в результате чего, абляционное пятно растягивается (например, превращаясь из окружности в эллипс). Ограничение на угол лазерного света состоит в том, что свет сам сходится в конусе. Для фокусировки пучка в пятно размером порядка 1 мкм требуется, чтобы угол раствора конуса был весьма большим (что часто выражается как работа с высокой числовой апертурой). Это означает, что значительный наклон лазерного пучка может влиять на возможность фокусировки лазера в пятно малого размера.
[126] Фиг.6 демонстрирует использование "чистки под высоким давлением". Поток газа "чистки под высоким давлением" может направляться вблизи (например, на расстоянии около 100 мкм) от зоны, где формируется струя. Поток газа "чистки под высоким давлением" может действовать силой на абляционную струю, или перенаправлять струю к впускному концу инжекторной трубки, эффективно захватывая каждую струю при ее формирования или генерации. В конфигурации, аналогичной описанной согласно вышеприведенным примерам, можно обеспечить инжекторную трубку с потоком газа (около 0.9 литра в минуту в этой иллюстрации) для захвата и переноса струи к ICP. В различных вариантах осуществления, например, поток "чистки под высоким давлением" можно обеспечить путем доставки потока газа (около 0.1 литра в минуту), через узкую форсунку (например, около 100 мкм в диаметре) для создания струи газа, позволяющей перенаправлять каждую следующую абляционную струю в инжекторную трубку. Источник потока газа чистки под высоким давлением (например, форсунка) можно именовать "впускным каналом газа", поскольку она является впускным каналом потока газа чистки под высоким давлением к струе. Альтернативно, источник потока газа чистки под высоким давлением можно именовать "портом". Например, поток газа "чистки под высоким давлением" может выходить из форсунки на расстояние от 50 мкм до 200 мкм из лазерного абляционного пятна (зоны формирования струи). Очевидно, что используемый в этом контексте термин "форсунка" не относится ни к какой конкретной структуре, но относится к выпускному каналу, откуда выходит газ чистки под высоким давлением. Как показано на фиг.6, диаметр форсунки чистки под высоким давлением меньше внутреннего диаметра (или размер эквивалентного поперечного сечения) инжектора. Например, диаметр форсунки может составлять от 10% до 50% диаметра инжектора. В некоторых вариантах осуществления чистка под высоким давлением направляет струю во впускной канал инжектора конической формы.
[127] Фиг.7 демонстрирует вариант осуществления, где исследуемый образец освещается лазерным светом сверху. Лазерный свет фокусируется объективом, затем проходит через оптическое окно и, наконец, поступает в герметичную абляционную камеру через конический патрубок. Коническая форма патрубка позволяет пропускать лазерный свет к мишени, причем патрубок обеспечен для того, чтобы газ захвата выходил из камеры. Газ захвата несет содержимое абляционной струи и затем объединяется с оболочечным потоком. Выбирая размеры газовых каналов и значений расхода, можно гарантировать, что поток газа захвата окружен оболочечным потоком, и что пробка из абляционной струи остается вблизи оси потока инжектора. Это положение струи способствует скорейшему переносу струи с уменьшенным расхождением по времени.
[128] Фиг.8 демонстрирует конфигурацию, аналогичную показанной на фиг.7 и демонстрирует, что более сильный оболочечный поток можно использовать для окружения потока материалом струи в центре потока. Фиг.8 демонстрирует, что часть оболочечного потока отводится в качестве жертвенного потока, тогда как сердцевина оболочечного потока, содержащая поток газа захвата и материал струи, подводится в короткий патрубок, который подает этот поток в ICP.
[129] Подход использования жертвенного потока, представленный на фиг.8, можно применять к другим вышеописанным конфигурациям. В таких вариантах осуществления предполагается, что инжектор имеет две части с разными внутренними диаметрами. Главное преимущество конфигурации жертвенного потока состоит в том, что поток газа захвата и материал струи остаются вблизи центра трубопровода, где профиль скоростей потока газа является почти плоским, т.е. разные части захваченной струи продвигаются с аналогичными скоростями.
[130] Фиг.9 демонстрирует другой вариант осуществления, где лазерный пучок освещает образец сверху. В данном случае струя отбирается в патрубок забора образца, размещенный примерно перпендикулярно мишени. Материал струи окружен потоком газа захвата, который также действует как оболочечный поток. Газовая динамика захвата струи, показанная на фиг.9, сходна с показанной на фиг.3, где используется сквозное облучение мишени. Поскольку лазерный свет на фиг.9 также распространяется перпендикулярно мишени (поскольку является газопроводом) объектив и оптическое окно имеют отверстие для газопровода. После прохождения через объектив, патрубок изгибается для отвода образца с оптического пути и перемещения его в источник ионов ICP.
[131] Фиг.10 демонстрирует компоновку, в которой лазерная абляция и забор образца из струи осуществляются аналогично варианту осуществления, показанному на фиг.9. Однако во избежание изгибания далее по ходу газопровода, лазерный свет альтернативно изгибается с использованием зеркала. В данном случае, оптическое окно, объектив и зеркало имеют отверстия, через которые проходит газопровод, несущий газ захвата и материал струи.
[132] Хотя принципы настоящего изобретения описаны в связи с различными вариантами осуществления, это не означает, что принципы настоящего изобретения ограничены такими вариантами осуществления. Напротив, принципы настоящего изобретения охватывают различные альтернативы, модификации и эквиваленты, что очевидно специалистам в данной области техники. Например, в различных примерах, проиллюстрированных на чертежах, в общем случае, описано, что инжекторная трубка имеет внутренний диаметр 1 мм при совокупном расходе газа около 1 литра в минуту (0.1 плюс 0.9 литра в минуту). Предполагается, что инжекторы меньшего или большего диаметра, совместно с соответственно выбранными значениями расхода газа, можно применять к различным геометриям, представленным с аналогичными ожидаемыми результатами. Однако может быть желательно поддерживать условия газовой динамики без турбулентности или почти без турбулентности в инжекторной трубке для сохранения индивидуальности каждой отдельной абляционной струи.
[133] Кроме того, в ряде случаев повышенных частот повторения лазерных импульсов, более чем одна абляционная струя может по отдельности захватываться и переноситься в ICP в пределах совокупного расхождения по времени переноса как рассмотрено выше. Например, при частоте повторения 10 кГц импульсный лазер может генерировать две абляционные струи за 200 мкс, которые затем можно переносить в ICP для ионизации. Ионы, генерируемые из двух отдельных струй, можно анализировать как единичный отдельный пакет ионов масс-анализатором. В результате, пока лазер остается на одном и том же абляционном пятне или пока скорость перемещения лазера по трассе непрерывных пятен меньше частоту повторения, абляционные струи, и, следовательно, ионы, могут обеспечивать совокупный анализ масс на одном и том же абляционном пятне или, соответственно, обеспечивать среднее распределение массы вдоль трассы. Следует отметить, что можно применять частоту повторения лазера порядка нескольких МГц, что позволяет получить сигнал, представляющий усреднение большого количества лазерных импульсов. Лазер также может выдавать группы импульсов для обеспечения промежутка в потоке данных между отдельными положениями забора образца (или пикселями).
[134] Следует понимать, что способы и устройства изобретения можно использовать для любого из различных типов образцов, например, биологических образцов. В одном подходе образом являться клеточный материал, например, срез ткани, клеточный монослой, клеточный препарат и т.п. Образом может быть тонко рассеченная биологическая ткань толщиной до 100 мкм, образец ткани толщина порядка миллиметров или нерассеченный образец ткани. В одном примере, можно использовать тонкие срезы ткани (например, срезы, заключенные в парафин). Для иллюстрации, некоторые срезы ткани имеют толщину от 10 нм до 10 мкм. В ряде случаев, образцом является группа клеток или одна или более выбранных клеток из группы клеток. См., например, Antonov, A. and Bandura, D., 2012, U.S. Pat. Pub. 2012/0061561, включенный сюда посредством ссылки.
[135] В некоторых вариантах осуществления, биологический материал помечается элементными маркерами, например, как описано в U.S. Pat. Pub. US2010/0144056, включенной в данное описание в порядке ссылки. A биологический образец, содержащий клетки, белки, клеточные материалы, представляющие интерес, можно помечать одним или несколькими разными металлосопряженными антителами.
[136] Хотя вышеприведенное изобретение описано на конкретных примерах в целях ясности и понимания, специалисты в данной области техники, ознакомившись с этим раскрытием, смогут предложить различные изменения в форме и деталях, не выходя за рамки истинного объема изобретения, заданного в нижеследующей формуле изобретения. Изобретение, таким образом, не ограничивается конкретными изложенными выше компонентами или деталями методологии или конструкции. Сверх того, что необходимо или присуще самим процессам, не предусмотрено никакого конкретного порядка этапов или стадий способов или процессов, описанных в этом раскрытии, в том числе, в чертежах. Во многих случаях порядок этапов процесса может изменяться без изменения цели, результата или сущности описанных способов. Все упомянутые здесь публикации и патентные документы включены в данное описание в порядке ссылки, как если бы было конкретно и индивидуально указано, что каждая такая публикация или документ подлежит включению в данное описание в порядке ссылки. Упоминание публикаций и патентных документов (патентов, опубликованных патентных заявок и неопубликованных патентных заявок) не означает, что любой такой документ относится к уровню техники, а также не позволяет делать выводы о его содержании или дате.
Claims (54)
1. Способ масс-цитометрического анализа на основе лазерной абляции с использованием лазерно-абляционного масс-цитометра, содержащий этапы, при которых:
направляют импульсы лазерного пучка на множество участков образца для генерации абляционной струи образца для каждого из импульсов;
захватывают каждую абляционную струю по отдельности;
переносят каждую из захваченных по отдельности абляционных струй в индуктивно связанную плазму (ICP); и
ионизируют каждую из по отдельности захваченных и перенесенных абляционных струй в ICP, таким образом, генерируя ионы для масс-цитометрического анализа;
причем лазерно-абляционный масс-цитометр содержит инжектор, выполненный с возможностью переноса абляционных струй в ICP;
при этом инжектор имеет впускной канал инжектора, расположенный в лазерно-абляционном источнике,
причем впускной канал инжектора выполнен с возможностью захвата абляционных струй; при этом впускной канал инжектора имеет форму конуса образца, причем более узкая часть конуса образца является апертурой впускного канала инжектора, при этом конус образца располагается вблизи области, где генерируется абляционная струя; и
способ дополнительно содержит этапы, при которых:
вводят поток газа захвата для введения абляционных струй в конус образца инжектора; и
вводят поток газа переноса отдельно от потока газа захвата в инжектор для переноса абляционных струй из конуса образца в IPC.
2. Способ по п. 1, в котором лазерно-абляционный масс-цитометр дополнительно содержит:
лазерно-абляционный источник для генерации абляционных струй из образца;
источник ICP для создания ICP; и
впускной канал газа, присоединенный к впускному каналу инжектора, выполненный с возможностью пропускать газ из впускного канала газа во впускной канал инжектора для переноса захваченной абляционной струи в ICP.
3. Способ по п. 2, дополнительно содержащий этап, при котором вводят поток газа в область между впускным каналом инжектора и областью, где генерируется абляционная струя для направления абляционной струи через впускной канал инжектора; и при этом поток газа перпендикулярен области, где генерируется абляционная струя, и перпендикулярен осевой линии просвета инжектора, ближайшего к впускному каналу инжектора.
4. Способ по п. 2, в котором поддерживают расхождение абляционных струй в пределах внутреннего диаметра просвета инжектора.
5. Способ по п. 1, в котором диаметр апертуры
является регулируемым; имеет размер, препятствующий возмущению абляционной струи при ее прохождении в инжектор; или
равен диаметру в поперечном сечении абляционной струи или больше диаметра в поперечном сечении абляционной струи.
6. Способ по п. 1, в котором абляционная струя генерируется лазерным импульсом, который является направленным через прозрачную мишень, содержащую образец, и при этом прозрачная мишень содержит прозрачную подложку, на которой располагается образец.
7. Способ по п. 1, в котором лазерный пучок генерируют фемтосекундным лазером.
8. Способ по п. 1, в котором положение образца изменяют в ходе анализа и при этом в ходе анализа лазерный пучок остается неподвижным.
9. Способ по п. 1, в котором положение образца фиксируют в ходе анализа.
10. Способ по п. 1, в котором импульсы лазерного пучка создают абляционные пятна размером в 1 мкм или менее.
11. Способ по п. 1, в котором длина окружности внешней поверхности конуса образца уменьшается в направлении к апертуре.
12. Способ по п. 1, в котором инжектор дополнительно включает часть жертвенного потока, где часть оболочечного потока, окружающая материал струи, отводится до введения материала струи в IPC.
13. Способ масс-цитометрического анализа на основе лазерной абляции с использованием лазерно-абляционного масс-цитометра, содержащий этапы, при которых:
направляют импульсы лазерного пучка на множество участков образца для генерации абляционной струи образца для каждого из импульсов;
захватывают каждую абляционную струю по отдельности;
переносят каждую из захваченных по отдельности абляционных струй в индуктивно связанную плазму (ICP); и
ионизируют каждую из по отдельности захваченных и перенесенных абляционных струй в ICP, таким образом, генерируя ионы для масс-цитометрического анализа;
причем лазерно-абляционный масс-цитометр содержит:
лазерно-абляционный источник для генерации абляционных струй из образца;
источник ICP для создания ICP;
инжектор, выполненный с возможностью переноса абляционных струй в ICP;
при этом инжектор имеет впускной канал инжектора, расположенный в лазерно-абляционном источнике,
причем впускной канал инжектора выполнен с возможностью захвата абляционных струй; и
впускной канал газа, присоединенный к впускному каналу инжектора, выполненный с возможностью пропускать газ из впускного канала газа во впускной канал инжектора для переноса захваченной абляционной струи в ICP;
и способ дополнительно содержит этапы, при которых:
вводят поток газа в область между впускным каналом инжектора и областью, где генерируется абляционная струя для направления абляционной струи через впускной канал инжектора; и при этом поток газа перпендикулярен области, где генерируется абляционная струя, и перпендикулярен осевой линии просвета инжектора, ближайшего к впускному каналу инжектора;
вводят поток газа переноса в инжектор для переноса абляционных струй в IPC; и
при этом расход газа составляет около 0.1 литра в минуту, расход газа переноса составляет около 0.9 литра в минуту.
14. Система лазерной абляции, содержащая:
лазер, способный создавать лазерное излучение;
лазерную абляционную ячейку, содержащую прозрачную подложку для удержания анализируемого образца или платформу, выполненную с возможностью принимать прозрачную подложку; и
инжектор для переноса абляционной струи в ICP, причем упомянутый инжектор содержит конус образца, причем более узкая часть конуса образца формирует отверстие инжектора, и
источник газа переноса для создания потока газа переноса в инжекторе, и
источник газа захвата для создания потока газа захвата в абляционной ячейке.
15. Система по п. 14, в которой отверстие инжектора выполнено таким образом, что абляция области подложки приводит к формированию абляционной струи по ходу поверхности, из которой испускается лазерное излучение.
16. Система по 15, в которой указанная поверхность представляет собой линзу или зеркало.
17. Система по 14, в которой длина окружности внешней поверхности конуса образца уменьшается в направлении к отверстию инжектора.
18. Система по п. 14, в которой инжектор дополнительно включает часть жертвенного потока, где часть оболочечного потока, окружающая материал струи, отводится до введения материала струи в IPC.
19. Система по п. 14, в которой лазер, лазерная абляционная ячейка и инжектор выполнены таким образом, что лазерное излучение исходит с одной стороны платформы или подложки, и отверстие инжектора находится с другой стороны платформы или подложки.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361812893P | 2013-04-17 | 2013-04-17 | |
| US61/812,893 | 2013-04-17 | ||
| PCT/CA2014/050387 WO2014169394A1 (en) | 2013-04-17 | 2014-04-17 | Sample analysis for mass cytometry |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2015123440A RU2015123440A (ru) | 2017-05-22 |
| RU2637795C2 true RU2637795C2 (ru) | 2017-12-07 |
Family
ID=51730644
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2015123440A RU2637795C2 (ru) | 2013-04-17 | 2014-04-17 | Анализ образцов для масс-цитометрии |
Country Status (8)
| Country | Link |
|---|---|
| US (6) | US9589779B2 (ru) |
| EP (2) | EP2987177B1 (ru) |
| JP (1) | JP6230693B2 (ru) |
| CN (1) | CN105190829B (ru) |
| CA (2) | CA3191952A1 (ru) |
| RU (1) | RU2637795C2 (ru) |
| SG (2) | SG10201808165YA (ru) |
| WO (1) | WO2014169394A1 (ru) |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2013382989B2 (en) | 2013-03-22 | 2018-06-07 | Eth Zurich | Laser ablation cell |
| CA3191952A1 (en) | 2013-04-17 | 2014-10-23 | Fluidigm Canada Inc. | Sample analysis for mass cytometry |
| CA2924284C (en) | 2013-09-13 | 2022-01-04 | The Board Of Trustees Of The Leland Stanford Junior University | Multiplexed imaging of tissues using mass tags and secondary ion mass spectrometry |
| GB201403625D0 (en) * | 2014-02-28 | 2014-04-16 | Asrepresented By The Sec Dep Of Health And Human Services The | Multiplexed imaging of tissue samples by mass cytometry |
| EP3195346B1 (en) * | 2014-09-18 | 2020-05-06 | Universiteit Gent | Laser ablation probe |
| CA2972500C (en) | 2014-12-31 | 2023-09-12 | Fluidigm Canada Inc. | Structured biological samples for analysis by mass cytometry |
| US20160260598A1 (en) * | 2015-02-04 | 2016-09-08 | Fluidigm Canada Inc. | Laser enabled imaging mass cytometry |
| US9766224B2 (en) | 2015-03-25 | 2017-09-19 | The Board Of Trustees Of The Leland Stanford Junior University | Single cell analysis using secondary ion mass spectrometry |
| US9797879B2 (en) | 2015-04-23 | 2017-10-24 | The Board Of Trustees Of The Leland Stanford Junior University | Method for multiplexed sample analysis by photoionizing secondary sputtered neutrals |
| EP3494591A1 (en) * | 2016-08-02 | 2019-06-12 | Fluidigm Canada Inc. | Laser ablation system |
| WO2018115415A1 (en) * | 2016-12-22 | 2018-06-28 | Advanced Osteotomy Tools - Aot Ag | Laser device and tissue characterizing method |
| US11092519B1 (en) * | 2017-02-06 | 2021-08-17 | Elemental Scientific Lasers, Llc | System and method for automated sampling and analysis |
| JP7078382B2 (ja) * | 2017-11-22 | 2022-05-31 | 藤太郎 今坂 | 飛行時間型質量分析装置及び質量分析方法 |
| JP7146905B2 (ja) * | 2018-04-18 | 2022-10-04 | 株式会社エス・テイ・ジャパン | レーザーアブレーション装置および分析装置 |
| WO2019246033A1 (en) * | 2018-06-18 | 2019-12-26 | Fluidigm Canada Inc. | High resolution imaging apparatus and method |
| KR102577694B1 (ko) * | 2018-09-11 | 2023-09-12 | 주식회사 엘지에너지솔루션 | 검출 감도 향상을 위한 레이저 탈착-dart-ms 시스템 및 이에 사용되는 인터페이스 유닛 |
| CN111954917B (zh) * | 2018-09-11 | 2023-11-07 | 株式会社 Lg新能源 | 接口单元 |
| WO2020092236A1 (en) * | 2018-10-29 | 2020-05-07 | Fluidigm Canada Inc. | Inductively coupled plasma torch with reverse vortex flow and method of operation |
| CN109668818A (zh) * | 2018-12-26 | 2019-04-23 | 宁波大学 | 基于激光烧蚀的细胞分析装置及方法 |
| EP3911760A4 (en) * | 2019-01-15 | 2022-10-12 | Fluidigm Canada Inc. | DIRECT IONIZATION IN IMAGING MASS SPECTROMETRY |
| WO2020228475A1 (en) * | 2019-05-15 | 2020-11-19 | Shanghai Polaris Biology Co., Ltd. | Sample transport apparatus for mass spectrometry |
| CA3140663A1 (en) * | 2019-06-18 | 2020-12-24 | Paul Corkum | Improved mass cytometry |
| WO2021168213A1 (en) * | 2020-02-19 | 2021-08-26 | Elemental Scientific Lasers, Llc | Variable beam size via homqgenizer movement |
| EP3943197A1 (en) * | 2020-07-20 | 2022-01-26 | The Provost, Fellows, Scholars and other Members of Board of Trinity College Dublin | Jet deposition using laser-produced dry aerosol |
| US11776801B2 (en) | 2020-09-18 | 2023-10-03 | Standard Biotools Canada Inc. | Inductively coupled plasma based atomic analysis systems and methods |
| US11443933B1 (en) * | 2020-10-30 | 2022-09-13 | Agilent Technologies, Inc. | Inductively coupled plasma mass spectrometry (ICP-MS) with ion trapping |
| JP2022131579A (ja) | 2021-02-26 | 2022-09-07 | キオクシア株式会社 | 分析装置および分析方法 |
| CN113218846A (zh) * | 2021-03-18 | 2021-08-06 | 上海交通大学 | 一种面向于单细胞质谱流式分析的icp装置 |
| WO2022217345A1 (en) * | 2021-04-14 | 2022-10-20 | Kimia Analytics Inc. | A system to generate a high yield of negative ions for icp-ms |
| AT525093B1 (de) * | 2021-10-05 | 2022-12-15 | Univ Wien Tech | Vorrichtung zur Aufnahme eines Feststoff-Probenmaterials |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7180058B1 (en) * | 2005-10-05 | 2007-02-20 | Thermo Finnigan Llc | LDI/MALDI source for enhanced spatial resolution |
| DE102008049833A1 (de) * | 2008-10-01 | 2010-04-22 | Forschungszentrum Jülich GmbH | Verfahren und Vorrichtung zur Durchführung einer quantitativen ortsaufgelösten Lokal- und Verteilunganalyse chemischer Elemente und in-situ Charakterisierung der ablatierten Oberflächenregionen |
| US20120074307A1 (en) * | 2009-04-08 | 2012-03-29 | Sabine Becker | Method and device for carrying out a quantitative spatially-resolved local and distribuition analysis of chemical elements and in situ characterization of the ablated surface regions |
| US20120099103A1 (en) * | 2009-07-10 | 2012-04-26 | University Of Florida Research Foundation, Inc. | Method and apparatus to laser ablation-laser induced breakdown spectroscopy |
Family Cites Families (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2177507B (en) | 1985-06-13 | 1989-02-15 | Mitsubishi Electric Corp | Laser mass spectroscopic analyzer |
| DE4108462C2 (de) * | 1991-03-13 | 1994-10-13 | Bruker Franzen Analytik Gmbh | Verfahren und Vorrichtung zum Erzeugen von Ionen aus thermisch instabilen, nichtflüchtigen großen Molekülen |
| DE4200497A1 (de) | 1992-01-10 | 1993-07-15 | Bayer Ag | Verfahren und vorrichtung zur schnellen identifizierung von kunststoffen mit hilfe der massenspektrometrie |
| JP2870364B2 (ja) * | 1993-06-29 | 1999-03-17 | 日本鋼管株式会社 | レーザー気化分析方法及び装置 |
| US5526110A (en) | 1994-07-08 | 1996-06-11 | Iowa State University Research Foundation, Inc. | In situ calibration of inductively coupled plasma-atomic emission and mass spectroscopy |
| US5777324A (en) | 1996-09-19 | 1998-07-07 | Sequenom, Inc. | Method and apparatus for maldi analysis |
| JPH11201945A (ja) * | 1998-01-09 | 1999-07-30 | Jeol Ltd | レーザーアブレーション装置 |
| US5965884A (en) * | 1998-06-04 | 1999-10-12 | The Regents Of The University Of California | Atmospheric pressure matrix assisted laser desorption |
| EP1430508A1 (en) * | 2001-09-17 | 2004-06-23 | MDS Inc., doing business as MDS Sciex | Method and apparatus for cooling and focusing ions |
| US6683277B1 (en) | 2002-12-20 | 2004-01-27 | Osram Opto Semiconductors | Laser ablation nozzle assembly |
| US7135674B2 (en) * | 2004-01-22 | 2006-11-14 | Thermo Finnigan Llc | Method and apparatus for FAIMS with a laser-based ionization source |
| US20080020474A1 (en) | 2004-03-30 | 2008-01-24 | Riken | Method of Analyzing Biosample by Laser Ablation and Apparatus Therefor |
| WO2008019492A1 (en) | 2006-08-15 | 2008-02-21 | Alexei Antonov | Apparatus and method for elemental analysis of particles by mass spectrometry |
| WO2008058004A2 (en) | 2006-11-02 | 2008-05-15 | Winnik Mitchell A | Particles containing detectable elemental code |
| US20110024615A1 (en) | 2006-12-29 | 2011-02-03 | Tanner Scott D | Cell injector for flow cytometer having mass spectrometer detector and method for using same |
| US8174691B1 (en) * | 2007-03-15 | 2012-05-08 | Arkansas State University—Jonesboro | Detection of a component of interest with an ultraviolet laser and method of using the same |
| US9079268B2 (en) * | 2007-09-14 | 2015-07-14 | Robert C. Fry | Analytical laser ablation of solid samples for ICP, ICP-MS, and FAG-MS analysis |
| US8207494B2 (en) * | 2008-05-01 | 2012-06-26 | Indiana University Research And Technology Corporation | Laser ablation flowing atmospheric-pressure afterglow for ambient mass spectrometry |
| US9383260B1 (en) * | 2008-05-05 | 2016-07-05 | Applied Spectra, Inc. | Laser ablation analysis system |
| ES2741664T3 (es) * | 2009-02-02 | 2020-02-11 | Light Matter Interaction Inc | Método y sistema de desorción ablativa blanda |
| DE202010010932U1 (de) * | 2010-04-19 | 2011-10-07 | Witec Wissenschaftliche Instrumente Und Technologie Gmbh | Vorrichtung zur Abbildung einer Probenoberfläche |
| US8519330B2 (en) * | 2010-10-01 | 2013-08-27 | Ut-Battelle, Llc | Systems and methods for laser assisted sample transfer to solution for chemical analysis |
| US8879064B2 (en) * | 2011-12-23 | 2014-11-04 | Electro Scientific Industries, Inc. | Apparatus and method for transporting an aerosol |
| US8598488B2 (en) * | 2011-12-23 | 2013-12-03 | Electro Scientific Industries, Inc. | Method and apparatus for adjusting radiation spot size |
| EP2948973A2 (en) * | 2013-01-28 | 2015-12-02 | Westfälische Wilhelms-Universität Münster | Parallel elemental and molecular mass spectrometry analysis with laser ablation sampling |
| WO2014114808A2 (en) * | 2013-01-28 | 2014-07-31 | Westfälische Wilhelms-Universität Münster | Laser ablation atmospheric pressure ionization mass spectrometry |
| US20140227776A1 (en) * | 2013-02-14 | 2014-08-14 | Electro Scientific Industries, Inc. | Laser ablation cell and torch system for a compositional analysis system |
| US20140268134A1 (en) * | 2013-03-15 | 2014-09-18 | Electro Scientific Industries, Inc. | Laser sampling methods for reducing thermal effects |
| AU2013382989B2 (en) * | 2013-03-22 | 2018-06-07 | Eth Zurich | Laser ablation cell |
| CA3191952A1 (en) | 2013-04-17 | 2014-10-23 | Fluidigm Canada Inc. | Sample analysis for mass cytometry |
| US20160260598A1 (en) * | 2015-02-04 | 2016-09-08 | Fluidigm Canada Inc. | Laser enabled imaging mass cytometry |
-
2014
- 2014-04-17 CA CA3191952A patent/CA3191952A1/en active Pending
- 2014-04-17 US US14/783,791 patent/US9589779B2/en active Active
- 2014-04-17 SG SG10201808165YA patent/SG10201808165YA/en unknown
- 2014-04-17 JP JP2016507962A patent/JP6230693B2/ja active Active
- 2014-04-17 CA CA2895360A patent/CA2895360C/en active Active
- 2014-04-17 RU RU2015123440A patent/RU2637795C2/ru active
- 2014-04-17 EP EP14784995.4A patent/EP2987177B1/en active Active
- 2014-04-17 SG SG11201504874QA patent/SG11201504874QA/en unknown
- 2014-04-17 WO PCT/CA2014/050387 patent/WO2014169394A1/en active Application Filing
- 2014-04-17 EP EP20150581.5A patent/EP3690923A1/en active Pending
- 2014-04-17 CN CN201480009995.6A patent/CN105190829B/zh active Active
-
2017
- 2017-01-18 US US15/408,806 patent/US9952132B2/en active Active
-
2018
- 2018-04-18 US US15/956,403 patent/US10241023B2/en active Active
-
2019
- 2019-02-07 US US16/270,421 patent/US10705006B2/en active Active
-
2020
- 2020-06-08 US US16/895,009 patent/US11099116B2/en active Active
-
2021
- 2021-07-22 US US17/382,764 patent/US11630050B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7180058B1 (en) * | 2005-10-05 | 2007-02-20 | Thermo Finnigan Llc | LDI/MALDI source for enhanced spatial resolution |
| DE102008049833A1 (de) * | 2008-10-01 | 2010-04-22 | Forschungszentrum Jülich GmbH | Verfahren und Vorrichtung zur Durchführung einer quantitativen ortsaufgelösten Lokal- und Verteilunganalyse chemischer Elemente und in-situ Charakterisierung der ablatierten Oberflächenregionen |
| US20120074307A1 (en) * | 2009-04-08 | 2012-03-29 | Sabine Becker | Method and device for carrying out a quantitative spatially-resolved local and distribuition analysis of chemical elements and in situ characterization of the ablated surface regions |
| US20120099103A1 (en) * | 2009-07-10 | 2012-04-26 | University Of Florida Research Foundation, Inc. | Method and apparatus to laser ablation-laser induced breakdown spectroscopy |
Non-Patent Citations (1)
| Title |
|---|
| Journal of Analytical Atomic Spectrometry. 2007.01.01. Vol. 22, Nr. 7, c. 736. * |
Also Published As
| Publication number | Publication date |
|---|---|
| US10241023B2 (en) | 2019-03-26 |
| SG11201504874QA (en) | 2015-07-30 |
| US20190271630A1 (en) | 2019-09-05 |
| CA2895360A1 (en) | 2014-10-23 |
| US9952132B2 (en) | 2018-04-24 |
| CN105190829B (zh) | 2018-04-03 |
| EP2987177A1 (en) | 2016-02-24 |
| EP2987177B1 (en) | 2020-01-08 |
| US20180306695A1 (en) | 2018-10-25 |
| RU2015123440A (ru) | 2017-05-22 |
| EP3690923A1 (en) | 2020-08-05 |
| US11630050B2 (en) | 2023-04-18 |
| CA2895360C (en) | 2023-05-02 |
| US10705006B2 (en) | 2020-07-07 |
| JP6230693B2 (ja) | 2017-11-15 |
| CN105190829A (zh) | 2015-12-23 |
| US20220178809A1 (en) | 2022-06-09 |
| US9589779B2 (en) | 2017-03-07 |
| WO2014169394A1 (en) | 2014-10-23 |
| CA3191952A1 (en) | 2014-10-23 |
| EP2987177A4 (en) | 2016-11-30 |
| US11099116B2 (en) | 2021-08-24 |
| JP2016522887A (ja) | 2016-08-04 |
| US20160056031A1 (en) | 2016-02-25 |
| US20200408662A1 (en) | 2020-12-31 |
| SG10201808165YA (en) | 2018-10-30 |
| US20170248507A1 (en) | 2017-08-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2637795C2 (ru) | Анализ образцов для масс-цитометрии | |
| CA2907483C (en) | Laser ablation cell | |
| US20160260598A1 (en) | Laser enabled imaging mass cytometry | |
| US10622199B2 (en) | Laser ablation system | |
| JP2014521189A (ja) | Maldiイオン源に連結したイオンガイド | |
| TW201443415A (zh) | 用於減少熱效應的雷射取樣方法 | |
| US20230215714A1 (en) | Plasma and sampling geometries for imaging mass cytometry | |
| EP3240014A1 (en) | Laser ablation cell | |
| WO2005091328A1 (en) | Apparatus and method for directing gas towards a specimen |