RU2560431C2 - Пептиды foxm1 и вакцины, содержащие их - Google Patents
Пептиды foxm1 и вакцины, содержащие их Download PDFInfo
- Publication number
- RU2560431C2 RU2560431C2 RU2011138160/10A RU2011138160A RU2560431C2 RU 2560431 C2 RU2560431 C2 RU 2560431C2 RU 2011138160/10 A RU2011138160/10 A RU 2011138160/10A RU 2011138160 A RU2011138160 A RU 2011138160A RU 2560431 C2 RU2560431 C2 RU 2560431C2
- Authority
- RU
- Russia
- Prior art keywords
- cancer
- present
- foxm1
- peptides
- peptide
- Prior art date
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims abstract description 346
- 102000004196 processed proteins & peptides Human genes 0.000 title claims description 213
- 229960005486 vaccine Drugs 0.000 title description 14
- 101150034834 Foxm1 gene Proteins 0.000 title 1
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 claims abstract description 179
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 159
- 201000011510 cancer Diseases 0.000 claims abstract description 132
- 108010008599 Forkhead Box Protein M1 Proteins 0.000 claims abstract description 131
- 238000000034 method Methods 0.000 claims abstract description 115
- 102000007237 Forkhead Box Protein M1 Human genes 0.000 claims abstract description 114
- 210000000612 antigen-presenting cell Anatomy 0.000 claims abstract description 103
- 102000040430 polynucleotide Human genes 0.000 claims abstract description 67
- 108091033319 polynucleotide Proteins 0.000 claims abstract description 67
- 239000002157 polynucleotide Substances 0.000 claims abstract description 67
- 239000000203 mixture Substances 0.000 claims abstract description 53
- 230000001939 inductive effect Effects 0.000 claims abstract description 30
- 108010075704 HLA-A Antigens Proteins 0.000 claims abstract description 28
- 102000011786 HLA-A Antigens Human genes 0.000 claims abstract description 28
- 230000028993 immune response Effects 0.000 claims abstract description 19
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 17
- 230000002980 postoperative effect Effects 0.000 claims abstract description 9
- 239000000427 antigen Substances 0.000 claims description 52
- 108091007433 antigens Proteins 0.000 claims description 51
- 102000036639 antigens Human genes 0.000 claims description 51
- 150000001413 amino acids Chemical group 0.000 claims description 49
- 229940024606 amino acid Drugs 0.000 claims description 48
- 210000001808 exosome Anatomy 0.000 claims description 36
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 24
- 239000004480 active ingredient Substances 0.000 claims description 22
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 20
- 238000011282 treatment Methods 0.000 claims description 20
- 238000001727 in vivo Methods 0.000 claims description 17
- 238000000338 in vitro Methods 0.000 claims description 15
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims description 10
- 229930182817 methionine Natural products 0.000 claims description 10
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 claims description 8
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 claims description 8
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 claims description 7
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 claims description 7
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 claims description 4
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims description 4
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 claims description 4
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 claims description 4
- 238000012258 culturing Methods 0.000 claims description 4
- 229960000310 isoleucine Drugs 0.000 claims description 4
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 claims description 4
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 claims description 4
- 125000001433 C-terminal amino-acid group Chemical group 0.000 claims 1
- 239000000126 substance Substances 0.000 abstract description 48
- 230000014509 gene expression Effects 0.000 abstract description 38
- 230000000694 effects Effects 0.000 abstract description 28
- 239000003814 drug Substances 0.000 abstract description 21
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 abstract description 20
- 201000010099 disease Diseases 0.000 abstract description 19
- 239000012634 fragment Substances 0.000 abstract description 13
- 230000006698 induction Effects 0.000 abstract description 13
- 230000003211 malignant effect Effects 0.000 abstract description 2
- 238000002560 therapeutic procedure Methods 0.000 abstract description 2
- 239000003795 chemical substances by application Substances 0.000 abstract 1
- 210000004027 cell Anatomy 0.000 description 121
- 235000001014 amino acid Nutrition 0.000 description 45
- 108090000623 proteins and genes Proteins 0.000 description 44
- 108010074328 Interferon-gamma Proteins 0.000 description 27
- 108091008874 T cell receptors Proteins 0.000 description 27
- 230000027455 binding Effects 0.000 description 27
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 26
- 150000007523 nucleic acids Chemical class 0.000 description 25
- 238000004519 manufacturing process Methods 0.000 description 23
- 102000039446 nucleic acids Human genes 0.000 description 23
- 108020004707 nucleic acids Proteins 0.000 description 23
- 102000008070 Interferon-gamma Human genes 0.000 description 22
- 239000000523 sample Substances 0.000 description 22
- 125000003275 alpha amino acid group Chemical group 0.000 description 21
- 235000018102 proteins Nutrition 0.000 description 21
- 102000004169 proteins and genes Human genes 0.000 description 21
- 208000005718 Stomach Neoplasms Diseases 0.000 description 20
- 210000004443 dendritic cell Anatomy 0.000 description 20
- 206010017758 gastric cancer Diseases 0.000 description 20
- 230000002265 prevention Effects 0.000 description 20
- 201000011549 stomach cancer Diseases 0.000 description 20
- 229960003130 interferon gamma Drugs 0.000 description 19
- 239000013598 vector Substances 0.000 description 19
- 229920001184 polypeptide Polymers 0.000 description 16
- 208000032791 BCR-ABL1 positive chronic myelogenous leukemia Diseases 0.000 description 15
- 208000010833 Chronic myeloid leukaemia Diseases 0.000 description 15
- 208000033761 Myelogenous Chronic BCR-ABL Positive Leukemia Diseases 0.000 description 15
- 206010041067 Small cell lung cancer Diseases 0.000 description 15
- 239000003153 chemical reaction reagent Substances 0.000 description 15
- 230000004048 modification Effects 0.000 description 15
- 238000012986 modification Methods 0.000 description 15
- 208000002154 non-small cell lung carcinoma Diseases 0.000 description 15
- 208000000587 small cell lung carcinoma Diseases 0.000 description 15
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 description 15
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 14
- 206010005003 Bladder cancer Diseases 0.000 description 14
- 206010006187 Breast cancer Diseases 0.000 description 14
- 208000026310 Breast neoplasm Diseases 0.000 description 14
- 206010008342 Cervix carcinoma Diseases 0.000 description 14
- 206010009944 Colon cancer Diseases 0.000 description 14
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 14
- 206010025323 Lymphomas Diseases 0.000 description 14
- 206010033128 Ovarian cancer Diseases 0.000 description 14
- 206010061535 Ovarian neoplasm Diseases 0.000 description 14
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 14
- 206010060862 Prostate cancer Diseases 0.000 description 14
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 14
- 206010038389 Renal cancer Diseases 0.000 description 14
- 208000006265 Renal cell carcinoma Diseases 0.000 description 14
- 206010068771 Soft tissue neoplasm Diseases 0.000 description 14
- 208000024313 Testicular Neoplasms Diseases 0.000 description 14
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 14
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 14
- 201000010881 cervical cancer Diseases 0.000 description 14
- 201000007270 liver cancer Diseases 0.000 description 14
- 208000014018 liver neoplasm Diseases 0.000 description 14
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 14
- 201000008968 osteosarcoma Diseases 0.000 description 14
- 201000002528 pancreatic cancer Diseases 0.000 description 14
- 208000008443 pancreatic carcinoma Diseases 0.000 description 14
- 201000010174 renal carcinoma Diseases 0.000 description 14
- 201000005112 urinary bladder cancer Diseases 0.000 description 14
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 13
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 13
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 13
- 201000004101 esophageal cancer Diseases 0.000 description 13
- 208000025189 neoplasm of testis Diseases 0.000 description 13
- 201000003120 testicular cancer Diseases 0.000 description 13
- 210000001519 tissue Anatomy 0.000 description 13
- 125000000539 amino acid group Chemical group 0.000 description 12
- 239000000463 material Substances 0.000 description 12
- 201000007909 oculocutaneous albinism Diseases 0.000 description 12
- 108010013476 HLA-A24 Antigen Proteins 0.000 description 11
- 108020004999 messenger RNA Proteins 0.000 description 11
- 230000006870 function Effects 0.000 description 10
- 229940079593 drug Drugs 0.000 description 9
- 108091005601 modified peptides Proteins 0.000 description 9
- 108020004705 Codon Proteins 0.000 description 7
- 238000002965 ELISA Methods 0.000 description 7
- 101100221606 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) COS7 gene Proteins 0.000 description 7
- 238000001514 detection method Methods 0.000 description 7
- 208000024334 diffuse gastric cancer Diseases 0.000 description 7
- 238000003114 enzyme-linked immunosorbent spot assay Methods 0.000 description 7
- 238000009169 immunotherapy Methods 0.000 description 7
- 230000008569 process Effects 0.000 description 7
- 238000013519 translation Methods 0.000 description 7
- 108010002350 Interleukin-2 Proteins 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 238000011321 prophylaxis Methods 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- 150000003839 salts Chemical class 0.000 description 6
- 230000000638 stimulation Effects 0.000 description 6
- 238000006467 substitution reaction Methods 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 102100037850 Interferon gamma Human genes 0.000 description 5
- 241000700605 Viruses Species 0.000 description 5
- 238000007792 addition Methods 0.000 description 5
- 239000002671 adjuvant Substances 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 238000009472 formulation Methods 0.000 description 5
- 230000002163 immunogen Effects 0.000 description 5
- -1 painkillers Substances 0.000 description 5
- 108020004414 DNA Proteins 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 239000002585 base Substances 0.000 description 4
- 230000004071 biological effect Effects 0.000 description 4
- 239000012472 biological sample Substances 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 238000009396 hybridization Methods 0.000 description 4
- 229910052739 hydrogen Inorganic materials 0.000 description 4
- 230000014828 interferon-gamma production Effects 0.000 description 4
- 150000002632 lipids Chemical class 0.000 description 4
- 239000011159 matrix material Substances 0.000 description 4
- 210000001616 monocyte Anatomy 0.000 description 4
- 125000003729 nucleotide group Chemical group 0.000 description 4
- 210000005259 peripheral blood Anatomy 0.000 description 4
- 239000011886 peripheral blood Substances 0.000 description 4
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 4
- 239000004033 plastic Substances 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 239000013641 positive control Substances 0.000 description 4
- 230000001629 suppression Effects 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- 230000001225 therapeutic effect Effects 0.000 description 4
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 3
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 description 3
- 108091034117 Oligonucleotide Proteins 0.000 description 3
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 3
- 235000004279 alanine Nutrition 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 238000002619 cancer immunotherapy Methods 0.000 description 3
- 229940022399 cancer vaccine Drugs 0.000 description 3
- 230000001472 cytotoxic effect Effects 0.000 description 3
- 239000003085 diluting agent Substances 0.000 description 3
- 238000010790 dilution Methods 0.000 description 3
- 239000012895 dilution Substances 0.000 description 3
- 239000003937 drug carrier Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 229940044627 gamma-interferon Drugs 0.000 description 3
- 230000001900 immune effect Effects 0.000 description 3
- 210000004698 lymphocyte Anatomy 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 210000000056 organ Anatomy 0.000 description 3
- 230000000144 pharmacologic effect Effects 0.000 description 3
- 239000013612 plasmid Substances 0.000 description 3
- 230000000644 propagated effect Effects 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 210000002966 serum Anatomy 0.000 description 3
- 238000013518 transcription Methods 0.000 description 3
- 230000035897 transcription Effects 0.000 description 3
- 238000001890 transfection Methods 0.000 description 3
- 210000004881 tumor cell Anatomy 0.000 description 3
- 230000003612 virological effect Effects 0.000 description 3
- 108700028369 Alleles Proteins 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 150000008574 D-amino acids Chemical class 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 241000283073 Equus caballus Species 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 102000014150 Interferons Human genes 0.000 description 2
- 108010050904 Interferons Proteins 0.000 description 2
- 108010063738 Interleukins Proteins 0.000 description 2
- 102000015696 Interleukins Human genes 0.000 description 2
- 102000007557 Melanoma-Specific Antigens Human genes 0.000 description 2
- 108010071463 Melanoma-Specific Antigens Proteins 0.000 description 2
- 206010027476 Metastases Diseases 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- 241000009328 Perro Species 0.000 description 2
- 108020004511 Recombinant DNA Proteins 0.000 description 2
- 241000282898 Sus scrofa Species 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 230000000259 anti-tumor effect Effects 0.000 description 2
- 230000005809 anti-tumor immunity Effects 0.000 description 2
- 230000000890 antigenic effect Effects 0.000 description 2
- 230000005975 antitumor immune response Effects 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000011651 chromium Substances 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 238000012790 confirmation Methods 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 231100000517 death Toxicity 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 239000010432 diamond Substances 0.000 description 2
- 239000013604 expression vector Substances 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 238000013467 fragmentation Methods 0.000 description 2
- 238000006062 fragmentation reaction Methods 0.000 description 2
- 238000001415 gene therapy Methods 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000013595 glycosylation Effects 0.000 description 2
- 238000006206 glycosylation reaction Methods 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 230000003053 immunization Effects 0.000 description 2
- 238000002649 immunization Methods 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 229940079322 interferon Drugs 0.000 description 2
- 238000010253 intravenous injection Methods 0.000 description 2
- 238000002372 labelling Methods 0.000 description 2
- 210000001821 langerhans cell Anatomy 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000002502 liposome Substances 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 210000002433 mononuclear leukocyte Anatomy 0.000 description 2
- 239000002773 nucleotide Substances 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- NRNCYVBFPDDJNE-UHFFFAOYSA-N pemoline Chemical compound O1C(N)=NC(=O)C1C1=CC=CC=C1 NRNCYVBFPDDJNE-UHFFFAOYSA-N 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 230000026731 phosphorylation Effects 0.000 description 2
- 238000006366 phosphorylation reaction Methods 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- 230000037452 priming Effects 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 230000001177 retroviral effect Effects 0.000 description 2
- 208000000649 small cell carcinoma Diseases 0.000 description 2
- 229910001415 sodium ion Inorganic materials 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 238000010532 solid phase synthesis reaction Methods 0.000 description 2
- 238000010561 standard procedure Methods 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 229910052717 sulfur Inorganic materials 0.000 description 2
- 238000007910 systemic administration Methods 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- 239000003053 toxin Substances 0.000 description 2
- 231100000765 toxin Toxicity 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 229910052721 tungsten Inorganic materials 0.000 description 2
- 238000002255 vaccination Methods 0.000 description 2
- 229910052727 yttrium Inorganic materials 0.000 description 2
- UKAUYVFTDYCKQA-UHFFFAOYSA-N -2-Amino-4-hydroxybutanoic acid Natural products OC(=O)C(N)CCO UKAUYVFTDYCKQA-UHFFFAOYSA-N 0.000 description 1
- LEBVLXFERQHONN-UHFFFAOYSA-N 1-butyl-N-(2,6-dimethylphenyl)piperidine-2-carboxamide Chemical compound CCCCN1CCCCC1C(=O)NC1=C(C)C=CC=C1C LEBVLXFERQHONN-UHFFFAOYSA-N 0.000 description 1
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 208000023275 Autoimmune disease Diseases 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- 241000193830 Bacillus <bacterium> Species 0.000 description 1
- 241000193738 Bacillus anthracis Species 0.000 description 1
- 102100035793 CD83 antigen Human genes 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 241001227713 Chiron Species 0.000 description 1
- 241000282552 Chlorocebus aethiops Species 0.000 description 1
- 102000009016 Cholera Toxin Human genes 0.000 description 1
- 108010049048 Cholera Toxin Proteins 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 108091026890 Coding region Proteins 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 102000053602 DNA Human genes 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 238000011510 Elispot assay Methods 0.000 description 1
- 102000004533 Endonucleases Human genes 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 102000004457 Granulocyte-Macrophage Colony-Stimulating Factor Human genes 0.000 description 1
- 108010017213 Granulocyte-Macrophage Colony-Stimulating Factor Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000946856 Homo sapiens CD83 antigen Proteins 0.000 description 1
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 1
- PMMYEEVYMWASQN-DMTCNVIQSA-N Hydroxyproline Chemical compound O[C@H]1CN[C@H](C(O)=O)C1 PMMYEEVYMWASQN-DMTCNVIQSA-N 0.000 description 1
- 108010002586 Interleukin-7 Proteins 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- UKAUYVFTDYCKQA-VKHMYHEASA-N L-homoserine Chemical compound OC(=O)[C@@H](N)CCO UKAUYVFTDYCKQA-VKHMYHEASA-N 0.000 description 1
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical compound CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- 239000012097 Lipofectamine 2000 Substances 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- 108010046117 N-palmitoyl-5,6-dipalmitoyl-S-glycerylcysteinyl-seryl-serine Proteins 0.000 description 1
- 108091061960 Naked DNA Proteins 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 241000282577 Pan troglodytes Species 0.000 description 1
- 241001504519 Papio ursinus Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 206010035148 Plague Diseases 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 241000293871 Salmonella enterica subsp. enterica serovar Typhi Species 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 108010008038 Synthetic Vaccines Proteins 0.000 description 1
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 229910052770 Uranium Inorganic materials 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 229940037003 alum Drugs 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- ILRRQNADMUWWFW-UHFFFAOYSA-K aluminium phosphate Chemical compound O1[Al]2OP1(=O)O2 ILRRQNADMUWWFW-UHFFFAOYSA-K 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 229940041181 antineoplastic drug Drugs 0.000 description 1
- 101150080488 apa gene Proteins 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 238000003556 assay Methods 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 102000015736 beta 2-Microglobulin Human genes 0.000 description 1
- 108010081355 beta 2-Microglobulin Proteins 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 238000001815 biotherapy Methods 0.000 description 1
- 229960003150 bupivacaine Drugs 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000007969 cellular immunity Effects 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 239000012531 culture fluid Substances 0.000 description 1
- 238000012136 culture method Methods 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 229940127089 cytotoxic agent Drugs 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000012217 deletion Methods 0.000 description 1
- 230000037430 deletion Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000000368 destabilizing effect Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 229910003460 diamond Inorganic materials 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- PMMYEEVYMWASQN-UHFFFAOYSA-N dl-hydroxyproline Natural products OC1C[NH2+]C(C([O-])=O)C1 PMMYEEVYMWASQN-UHFFFAOYSA-N 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 239000012636 effector Substances 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 210000003038 endothelium Anatomy 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- UHBYWPGGCSDKFX-VKHMYHEASA-N gamma-carboxy-L-glutamic acid Chemical compound OC(=O)[C@@H](N)CC(C(O)=O)C(O)=O UHBYWPGGCSDKFX-VKHMYHEASA-N 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 208000024200 hematopoietic and lymphoid system neoplasm Diseases 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 229960002591 hydroxyproline Drugs 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 230000002998 immunogenetic effect Effects 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 238000002991 immunohistochemical analysis Methods 0.000 description 1
- 230000001024 immunotherapeutic effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000000126 in silico method Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- LSDPWZHWYPCBBB-UHFFFAOYSA-O methylsulfide anion Chemical compound [SH2+]C LSDPWZHWYPCBBB-UHFFFAOYSA-O 0.000 description 1
- 239000000693 micelle Substances 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 102000035118 modified proteins Human genes 0.000 description 1
- 108091005573 modified proteins Proteins 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 229920005615 natural polymer Polymers 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- IPCSVZSSVZVIGE-UHFFFAOYSA-N palmitic acid group Chemical group C(CCCCCCCCCCCCCCC)(=O)O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 229940023041 peptide vaccine Drugs 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- BZQFBWGGLXLEPQ-REOHCLBHSA-N phosphoserine Chemical compound OC(=O)[C@@H](N)COP(O)(O)=O BZQFBWGGLXLEPQ-REOHCLBHSA-N 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 238000009117 preventive therapy Methods 0.000 description 1
- 230000009862 primary prevention Effects 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 235000019833 protease Nutrition 0.000 description 1
- 238000002331 protein detection Methods 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 238000010188 recombinant method Methods 0.000 description 1
- 229940124551 recombinant vaccine Drugs 0.000 description 1
- 239000013074 reference sample Substances 0.000 description 1
- 238000003757 reverse transcription PCR Methods 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 210000004872 soft tissue Anatomy 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010186 staining Methods 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- 125000004434 sulfur atom Chemical group 0.000 description 1
- 230000020382 suppression by virus of host antigen processing and presentation of peptide antigen via MHC class I Effects 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 230000009258 tissue cross reactivity Effects 0.000 description 1
- FGMPLJWBKKVCDB-UHFFFAOYSA-N trans-L-hydroxy-proline Natural products ON1CCCC1C(O)=O FGMPLJWBKKVCDB-UHFFFAOYSA-N 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- XVQKZSLOGHBCET-INVHGPFASA-N tripalmitoyl-S-glyceryl-cysteinyl-seryl-serine Chemical compound CCCCCCCCCCCCCCCC(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O)CSCC(OC(=O)CCCCCCCCCCCCCCC)COC(=O)CCCCCCCCCCCCCCC XVQKZSLOGHBCET-INVHGPFASA-N 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/10—Cellular immunotherapy characterised by the cell type used
- A61K40/11—T-cells, e.g. tumour infiltrating lymphocytes [TIL] or regulatory T [Treg] cells; Lymphokine-activated killer [LAK] cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/42—Cancer antigens
- A61K40/4242—Transcription factors, e.g. SOX or c-MYC
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- C07K14/4701—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals not used
- C07K14/4748—Tumour specific antigens; Tumour rejection antigen precursors [TRAP], e.g. MAGE
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Toxicology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Oncology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Настоящее изобретение относится к области иммунологии. Предложен выделенный пептид, обладающий способностью индуцировать цитотоксические Т-лимфоциты (ЦТЛ) в присутствии антигенпредставляющих клеток (АПК), несущих HLA-A*2402, и представляющий собой фрагмент белка FOXM1. Также рассмотрены: выделенный полинуклеотид, кодирующий пептид по изобретению; композиция для индуцирования ЦТЛ и фармацевтическая композиция для лечения и/или профилактики рака, экспрессирующего FOXM1, и/или предупреждения его послеоперационных рецидивов, содержащие в качестве активного начала пептид по изобретению; способы индуцирования АПК и ЦТЛ; выделенная АПК со способностью индуцировать ЦТЛ; а также способ индуцирования иммунного ответа против рака, экспрессирующего FOXM1, у субъекта. Данное изобретение обеспечивает индуцирование иммунного ответа против клеток, экспрессирующих FOXM1, что может найти дальнейшее применение в терапии различных заболеваний, в том числе злокачественных, связанных с повышенной экспрессией белка FOXM1. 8 н. и 3 з.п. ф-лы, 3 ил., 2 табл.
Description
Область техники
Приоритет
Настоящая заявка утверждает преимущество Предварительной заявки США No. 61/153408, поданной 18 февраля 2009 года, полное содержание которой включено в данное описание посредством ссылки.
Настоящее изобретение относится к области биологической науки, в частности, к области терапии онкологических заболеваний. В частности, настоящее изобретение относится к новым пептидам, которые чрезвычайно эффективны в качестве противораковых вакцин, и лекарственным средствам для лечения и предупреждения опухолей.
Предпосылки изобретения
Было показано, что CD8 положительные ЦТЛ узнают эпитопные пептиды, полученные из опухолеспецифических антигенов (ОСА), на молекуле класса I главного комплекса гистосовместимости (ГКГС), а затем уничтожают опухолевые клетки. С момента обнаружения семейства меланомных антигенов (MAGE) как первого примера ОСА при помощи иммунологических подходов были обнаружены многие другие ОСА (NPL 1: Boon T, Int J Cancer 1993 May 8, 54(2): 177-80; NPL 2: Boon T & van der Bruggen P, J Exp Med 1996 Mar 1, 183(3): 725-9), и в настоящее время некоторые из ОСА находятся в процессе клинических исследований как иммунотерапевтические мишени.
Идентификация новых ОСА, которые индуцируют сильные и специфические противоопухолевые иммунные ответы, обеспечивает дальнейшее развитие клинического применения стратегии пептидных вакцинаций при различных типах рака (NPL 3: Harris CC, J Natl Cancer Inst 1996 Oct 16, 88(20): 1442-55; NPL 4: Butterfield LH et al, Cancer Res 1999 Jul 1, 59(13): 3134-42; NPL 5: Vissers JL et al., Cancer Res 1999 Nov 1, 59(21): 5554-9; NPL 6: van der Burg SH et al., J Immunol 1996 May 1, 156(9): 3308-14; NPL 7: Tanaka F et al., Cancer Res 1997 Oct 15, 57(20): 4465-8; NPL 8: Fujie T et al., Int J Cancer 1999 Jan 18, 80(2): 169-72; NPL 9: Kikuchi M et al., Int J Cancer 1999 May 5, 81(3): 459-66; NPL 10: Oiso M et al., Int J Cancer 1999 May 5, 81(3): 387-94).До настоящего времени сообщалось о нескольких клинических испытаниях с использованием этих опухолеспецифических антигенов. К сожалению, до сих пор в этих испытаниях противораковых вакцин можно было наблюдать лишь низкие частоты реального ответа (NPL 11: Belli F et al., J Clin Oncol 2002 Oct 15, 20(20): 4169-80; NPL 12: Coulie PG et al., Immunol Rev 2002 Oct, 188: 33-42; NPL 13: Rosenberg SA et al., Nat Med 2004 Sep, 10(9): 909-15).
Подходящий ОСА необходим для пролиферации и выживания раковых клеток, как мишени для иммунотерапии, поскольку использование таких ОСА может свести к минимуму хорошо известный риск иммунного избежания раковых клеток, присущего удалению, мутированию или супрессии ОСА, как последствие проводимой в терапевтических целях иммунной селекции.
Список цитирования
Непатентная литература
[NPL 1] Boon T, bit J Cancer 1993 May 8, 54(2): 177-80;
[NPL 2] Boon T & van der Braggen P, J Exp Med 1996 Mar 1, 183(3): 725-9;
[NPL 3] Harris CC, J Natl Cancer Inst 1996 Oct 16, 88(20): 1442-55;
[NPL 4] Butterfield LH et al., Cancer Res 1999 Jul 1, 59(13): 3134-42;
[NPL 5] Vissers JL et al., Cancer Res 1999 Nov 1, 59(21): 5554-9;
[NPL 6] van der Burg SH et al., J Immunol 1996 May 1, 156(9): 3308-14;
[NPL 7] Tanaka F et al., Cancer Res 1997 Oct 15, 57(20): 4465-8;
[NPL 8] Fujie T et al., Int J Cancer 1999 Jan 18, 80(2): 169-72;
[NPL 9] Kikuchi M et al., Int J Cancer 1999 May 5, 81(3): 459-66;
[NPL 10] Oiso M et al., Int J Cancer 1999 May 5, 81(3): 387-94) ;
[NPL 11] Belli F et al., J Clin Oncol 2002 Oct 15, 20(20): 4169-80;
[NPL 12] Coulie PG et al., Immunol Rev 2002 Oct, 188: 33-42;
[NPL 13] Rosenberg SA et al., Nat Med 2004 Sep, 10(9): 909-15).
Краткое описание изобретения
Настоящее изобретение основывается, в частности, на открытии подходящих мишеней иммунотерапии. Поскольку ОСА обычно воспринимаются иммунной системы в качестве «своих» и, вследствие этого, зачастую не обладают иммуногенностью, открытие соответствующих мишеней является чрезвычайно важным. Как отмечалось выше, FOXM1 (SEQ ID NO: 34, кодируемая геном с GenBank Accession No. NM_202002.1 (SEQ ID NO: 33)) был идентифицирован как активируемый в раковых тканях, таких как острый миелоидный лейкоз (AML), рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелоидный лейкоз (CML), колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, немелкоклеточный рак легкого (NSCLC), лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого (SCLC), опухоль мягких тканей и опухоль яичка. Таким образом, FOXM1 представляет собой подходящую мишень иммунотерапии.
Настоящее изобретение основывается, по меньшей мере, частично, на идентификации специфических эпитопных пептидов FOXM1, которые обладают способностью индуцировать цитотоксические Т-лимфоциты (ЦТЛ), специфические для FOXM1. Как подробно обсуждается ниже, мононуклеарные клетки периферической крови (PBMC), полученные от здоровых доноров, стимулировали при помощи HLA-A*2402-связывающихся подходящих пептидов, полученных из FOXM1. Затем были образованы линии ЦТЛ со специфической цитотоксичностью в отношении HLA-А24-положительных клеток-мишеней, подвергнутых импульсному взаимодействию с каждым из подходящих пептидов. Данные результаты показывают, что эти пептиды представляют собой HLA-А24-рестриктированные эпитопные пептиды, которые могут индуцировать сильные и специфические иммунные ответы в отношении клеток, экспрессирующих FOXM1. Эти результаты показывают, что FOXM1 является сильным иммуногеном и его эпитопы представляют собой эффективные мишени для иммунотерапии опухолей.
Соответственно, предметом настоящего изобретения является предоставление выделенных пептидов, связывающихся с HLA-антигеном, которые представляют собой FOXM1 (SEQ ID NO: 34) или его фрагменты. Предполагается, что настоящие пептиды обладают способностью индуцировать ЦТЛ. Их можно использовать для индуцирования ЦТЛ ex vivo или можно вводить субъекту для индукции иммунного ответа против раков, таких как острый миелоцитарный лейкоз, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, хронический миелоцитарный лейкоз, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, SCLC, опухоль мягких тканей и опухоль яичка. Предпочтительно, пептиды представляют собой нонапептиды или декапептиды, и более предпочтительно, состоят из последовательности аминокислот, выбранной из группы SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, демонстрирующих сильную способность индуцирования ЦТЛ.
Настоящее изобретение предусматривает модифицированные пептиды, обладающие аминокислотной последовательностью SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, где одна, две или несколько аминокислот заменены или добавлены, при условии, что модифицированные пептиды сохраняют исходную способность индуцировать ЦТЛ.
Далее, настоящее изобретение предоставляет выделенные полинуклеотиды, кодирующие любой из пептидов по настоящему изобретению. Эти полинуклеотиды можно использовать для индуцирования или подготовки антиген-экспрессирующих клеток (АПК) со способностью индуцировать ЦТЛ или можно вводить субъекту для индуцирования иммунного ответа против рака, а также для настоящих пептидов.
При введении субъекту настоящие пептиды представляются на поверхности АПК и затем индуцируют ЦТЛ, нацеленные на соответствующие пептиды. Таким образом, аспектом настоящего изобретения является предоставление композиций или веществ, включая любые пептиды или полинуклеотиды по настоящему изобретению, для индуцирования ЦТЛ. Кроме того, композиции или вещества, включая любые из пептидов или полинуклеотидов, можно применять для лечения и/или предупреждения онкологических заболеваний, таких как AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого (SCLC), опухоль мягких тканей и опухоль яичка, и/или для предупреждения послеоперационных рецидивов этих. Таким образом, еще одним предметом настоящего изобретения является предоставление фармацевтических композиций и веществ для лечения и/или для профилактики онкологических заболеваний, и/или для предупреждения их послеоперационных рецидивов, которые включают любой из пептидов или полинуклеотидов по настоящему изобретению. Вместо настоящих пептидов или полинуклеотидов или в дополнение к настоящим пептидам или полинуклеотидам настоящие фармацевтические композиции или вещества могут включать, в качестве активных ингредиентов, АПК или экзосомы, которые представляют любой из настоящих пептидов.
Пептиды или полинуклеотиды по настоящему изобретению можно использовать для индуцирования АПК, которые представляют на своей поверхности комплекс HLA-антигена и настоящего пептида, например, путем контактирования АПК, полученных от субъекта, с настоящим пептидом или введения полинуклеотида, кодирующего настоящий пептид, в АПК. Такие АПК обладают высокой способностью индуцировать ЦТЛ против пептидов-мишеней и пригодны для иммунотерапии рака. Таким образом, еще одним предметом настоящего изобретения является предоставление способов индуцирования АПК, способных индуцировать ЦТЛ, а также АПК, полученных этими способами.
Еще одним предметом настоящего изобретения является предоставление способа индуцирования ЦТЛ, который включает стадию совместного культивирования CD8-положительных клеток с АПК или экзосомами, представляющими пептид по настоящему изобретению на своей поверхности, или стадию введения гена, который включает полинуклеотид, кодирующий субъединицу Т-клеточного рецептора (ТКР), связывающийся с настоящим пептидом. ЦТЛ, получаемые настоящими способами, также находят применение при лечении и/или предупреждении раков, таких как AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка. Таким образом, еще одним предметом настоящего изобретения является предоставление ЦТЛ, получаемых настоящими способами.
Более того, еще одним предметом настоящего изобретения является предоставление способов индуцирования иммунного ответа против раков, которые включают в себя способы введения веществ или композиций, содержащих FOXM1 или фрагменты этого, полинуклеотиды, кодирующих FOXM1 или фрагменты этого, или экзосомы или АПК, представляющие FOXM1 или фрагменты этого.
Настоящее изобретение можно применять к любому заболеванию, связанному со сверхэкспрессией FOXM1, включая рак, такой как AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка.
Следует понимать, что как предшествующее краткое описание настоящего изобретения, так и следующее ниже подробное описание представляют собой типичные варианты осуществления и не ограничивают настоящее изобретение или других альтернативных вариантов осуществления настоящего изобретения.
Краткое описание чертежей
Различные аспекты и приложения настоящего изобретения станут очевидными для любого специалиста в данной области после рассмотрения краткого описания фигур и подробного описания настоящего изобретения и его предпочтительных вариантов осуществления, которые следуют.
[фиг.1a-f] Фиг.1 показывает фотографии, демонстрирующие результаты интерферон-гамма ELISPOT-анализа на ЦТЛ, индуцированных пептидами, полученными из FOXM1. ЦТЛ в лунках с номерами #1, #4 и #7, стимулированные пептидами FOXM1-А24-9-262(SEQ ID NO: 2) (a), #7 - FOXM1-А24-9-351(SEQ ID NO: 7) (b), #5 - FOXM1-А24-9-57(SEQ ID NO: 8) (c), #3 - FOXM1-А24-10-240(SEQ ID NO: 16) (d), #6 - FOXM1-А24-10-318(SEQ ID NO: 25) (e) и #4 - FOXM1-А24-10-390(SEQ ID NO:30) (f), продемонстрировали сильное продуцирование интерферона-гамма по сравнению с контролем, соответственно.
[фиг. 1g-h] ЦТЛ в лунках с номерами #4 с FOXM 1-А24-10-238(SEQ ID NO:31) (g) продемонстрировали сильное продуцирование интерферона-гамма по сравнению с контролем, соответственно. Наоборот, в качестве типичного случая отрицательных данных, не было показано специфическое продуцирование интерферона-гамма от ЦТЛ, стимулированных пептидом FOXM1-А24-9-316(SEQ ID NO: 1) против подвергнутых импульсному взаимодействию с пептидом клеток-мишеней (h). На фигурах, «+» указывает на продуцирование интерферона-гамма против клеток-мишеней, подвергнутых импульсному воздействию с соответствующим пептидом, и «-» указывает на продуцирование интерферона-гамма против клеток-мишеней, не подвергнутых импульсному воздействию никаким пептидом. Площадь лунки этих изображений показывает, что клетки из соответствующих лунок были размножены, чтобы образовать линии ЦТЛ.
[фиг.2] Фигура 2 показывает линейные графики, демонстрирующие продуцирование интерферона-гамма линиями ЦТЛ, стимулированными пептидами FOXM1-А24-9-262(SEQ ID NO: 2) (a), FOXM1-А24-10-240(SEQ ID NO: 16) (b), FOXM1-А24-10-318(SEQ ID NO: 25) (c) и FOXM1-А24-10-238(SEQ ID NO:31) (d), детектируемое при помощи интерферон-гамма ИФА-анализа. Она продемонстрировала, что линии ЦТЛ, образованные путем стимулирования каждым пептидом, показали сильное продуцирование интерферона-гамма по сравнению с контролем. На фигурах, «+» указывает на продуцирование интерферона-гамма против клеток-мишеней, подвергнутых импульсному воздействию с соответствующим пептидом, и «-» указывает на продуцирование интерферона-гамма против клеток-мишеней, не подвергнутых импульсному воздействию никаким пептидом.
[фиг.3] Фигура 3 демонстрирует продуцирование интерферона-гамма клонами ЦТЛ, образованными ограниченным разведением из линий ЦТЛ, стимулированных пептидами FOXM1-А24-9-262(SEQ ID NO: 2) (a), FOXM1-А24-10-240(SEQ ID NO: 16) (b) и FOXM1-А24-10-238(SEQ ID NO: 31) (c). Она продемонстрировала, что линии ЦТЛ, образованные путем стимулирования каждым пептидом, показали сильное продуцирование интерферона-гамма по сравнению с контролем. На фигурах, «+» указывает на продуцирование интерферона-гамма против клеток-мишеней, подвергнутых импульсному воздействию с соответствующим пептидом, и «-» указывает на продуцирование интерферона-гамма против клеток-мишеней, не подвергнутых импульсному воздействию никаким пептидом.
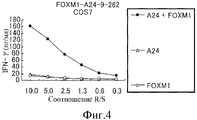
[фиг.4] Фигура 4 показывает линейные графики, демонстрирующие специфическую ЦТЛ-активность в отношении клеток-мишеней, которые экзогенно экспрессируют FOXM1 и HLA-A*2402. Клетки COS7, трансфицированные HLA-A*2402 или полноразмерным геном FOXM1, были подготовлены в качестве контроля. Клон ЦТЛ, образованный с пептидом FOXM1-А24-9-262(SEQ ID NO: 2), демонстрировал специфическую ЦТЛ-активность в отношении клеток COS7, трансфицированных как FOXM1, так и HLA-A*2402 (черный ромб). С другой стороны, не было зафиксировано никакой значительной специфической ЦТЛ-активности в отношении клеток-мишеней, экспрессирующих либо HLA-A*2402 (белый треугольник), либо FOXM1 (белый круг).
Описание вариантов осуществления
Несмотря на то что любые способы и материалы, аналогичные или эквивалентные тем, которые описаны в настоящем документе, могут быть использованы в практике или тестировании вариантов осуществления настоящего изобретения, сейчас описываются предпочтительные способы, приборы и материалы. При этом до описания настоящих материалов и способов следует понимать, что настоящее изобретение не ограничивается конкретными размерами, формами, величинами, материалами, методиками, протоколами и т.п., описанными в данном документе, поскольку они могут меняться в соответствии со стандартным экспериментированием и оптимизацией. Следует также понимать, что терминология, используемая при описании, предназначена лишь для целей описания конкретных версий или вариантов осуществления и не предназначена для ограничения объема настоящего изобретения, который ограничивается только прилагаемыми пунктами формулы изобретения.
Раскрытие каждой публикации, патента или заявки на патент, упомянутых в данном описании, специально включено здесь посредством ссылки в полном объеме. При этом ничто в настоящем документе не может быть истолковано в качестве признания того, что настоящее изобретение не дает права датировать более ранним числом такое раскрытие на основании изобретения или до изобретения.
В случае конфликта настоящее описание, включая определения, должно являться определяющим. Кроме того, материалы, способы и примеры приведены только в качестве иллюстрации и не предназначены для ограничения.
I. Определения
Формы единственного числа, как используется здесь, означают «по меньшей мере один», если иное специально не указано.
Термины «полипептид», «пептидные» и «белок» используются взаимозаменяемо в данном документе по отношению к полимеру из аминокислотных остатков. Термины относятся к аминокислотным полимерам, в которых один или несколько аминокислотных остатков представляет собой модифицированный остаток или не встречающийся в природе остаток, такой как искусственный химический миметик соответствующей аминокислоты естественного происхождения, а также к аминокислотным полимерам естественного происхождения.
Термин «аминокислоты», как используется здесь, относится к аминокислотам естественного происхождения и синтетическим аминокислотам, а также к аналогам аминокислот и миметикам аминокислот, которые функционируют аналогично аминокислотам естественного происхождения. Аминокислоты естественного происхождения представляют собой аминокислоты, кодируемые генетическим кодом, а также аминокислоты, модифицированные после трансляции в клетках (например, гидроксипролин, гамма-карбоксиглутаминовая кислота, и О-фосфосерин). Выражение «аминокислотный аналог» относится к соединениям, которые обладают той же основной химической структурой (альфа-углеродный атом, связанный с водородом, карбоксильная группа, аминогруппа и R-группа), что и у аминокислоты естественного происхождения, но имеет модифицированную R-группу или модифицированный каркас (например, гомосерин, альфа-аминокапроновая кислота, метионин, сульфоксид, метионинметилсульфоний). Выражение «миметик аминокислоты» относится к химическим соединениям, которые имеют отличные структуры, но аналогичные с обычными аминокислотами функции.
Аминокислоты могут называться здесь по их широко известным трехбуквенным символам или однобуквенными символами, рекомендованными Биохимической номенклатурной комиссией IUPAC-IUB.
Термины «ген», «полинуклеотидов», «нуклеотиды» и «нуклеиновые кислоты» используются взаимозаменяемо здесь и, если специально не указано, сходно с аминокислотами называют по их общепринятым однобуквенным кодам.
Если не определено иначе, термин «рак» относится к ракам, сверхэкспрессирующим ген FOXM1, примеры которых включают, в качестве неограничивающих примеров, AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка.
Если не определено иначе, термины «цитотоксический Т-лимфоцит», «цитотоксическая Т-клетка» и «ЦТЛ» используются взаимозаменяемо здесь, и, если иное специально не указано, относятся к подгруппе Т-лимфоцитов, которые способны распознавать «не свои» клетки (например, опухолевые клетки, инфицированные вирусом клетки) и индуцировать гибель таких клеток.
Если не определено иначе, все технические и научные термины, используемые в настоящем документе, имеют такой же смысл, как это обычно понимается любым специалистом в области, к которой относится настоящее изобретение.
II. Пептиды
Для демонстрации того, что пептиды, полученные из FOXM1, действуют в качестве антигенов, узнаваемых ЦТЛ, пептиды, полученные из FOXM1 (SEQ ID NO: 34) анализировали для определения того, представляли ли они собой антигенные эпитопы, рестриктированные по HLA-А24, которые представляют собой часто встречающиеся аллели HLA (Date Y et al., Tissue Antigens 47: 93-101, 1996; Kondo A et al., J Immunol 155: 4307-12, 1995; Kubo RT et al., J Immunol 152: 3913-24, 1994).
HLA-А24-связывающие подходящие пептиды, полученные из FOXM1, определяли по их аффинности связывания с HLA-А24. Следующие пептиды представляют собой подходящие пептиды:
После стимуляции Т-клеток in vitro дендритными клетками (ДК), нагруженными этими пептидами, были успешно образованы ЦТЛ с использованием каждого из следующих пептидов:
Эти образованные ЦТЛ демонстрируют сильную специфическую ЦТЛ-активность в отношении клеток-мишеней, подвергавшихся импульсному взаимодействию с соответствующими пептидами. Эти результаты показывают, что FOXM1 представляет собой антиген, узнающийся ЦТЛ, и что проверенные пептиды являются эпитопными пептидами FOXM1, рестриктированными по HLA-А24.
Поскольку ген FOXM1 сверхэкспрессируется в раковых клетках, таких как AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка, и не экспрессируется в большинстве нормальных органов, он представляет собой хорошую мишень для иммунотерапии. Таким образом, настоящее изобретение предоставляет нанопептиды (пептиды, состоящие из девяти аминокислотных остатков), и декапептиды (пептиды, состоящие из десяти аминокислотных остатков), соответствующие ЦТЛ-распознаваемым эпитопам FOXM1. Альтернативно, настоящее изобретение предоставляет выделенный пептид, который связывается с HLA-антигеном и индуцирует цитотоксические Т-лимфоциты (ЦТЛ), где пептид состоит из аминокислотной последовательности SEQ ID NO: 34 или является ее иммунологически активным фрагментом. Предпочтительные примеры нанопептидов и декапептидов по настоящему изобретению включают те пептиды, которые состоят из аминокислотной последовательности, выбранной из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31.
В большинстве случаев можно использовать программы из системы программного обеспечения, доступные, например, в Интернете, такие как программы, описанные в in Parker КС et al, J Immunol 1994 Jan 1, 152(1): 163-75, Buus et al. (Tissue Antigens., 62:378-84, 2003) и Nielsen et al. (Protein Sci, 12:1007-17, 2003, Bioinformatics, 20(9): 1388-97, 2004), для расчета аффинностей связывания между различными пептидами и HLA-антигенами in silico. Аффинность связывания с HLA-антигенами можно определять, как описано, например, в ссылках на Parker KC et al., J Immunol 1994 Jan 1, 152(1): 163-75; и Kuzushima K et al., Blood 2001, 98(6): 1872-81. Способы определения аффинности связывания описаны, например, в: Journal of Immunological Methods, 1995, 185: 181-190; Protein Science, 2000, 9: 1838-1846. Вследствие этого с помощью таких программ из системы программного обеспечения можно выбрать фрагменты, полученные из FOXM1, которые обладают высокой аффинностью связывания с HLA-антигенами. Таким образом, настоящее изобретение охватывает пептиды, состоящие из любых фрагментов, полученные из FOXM1, которые связываются с HLA-антигенами, выявленными с помощью таких известных программ. Пептидом по настоящему изобретению может являться пептид, состоящий из полноразмерного FOXM1.
Пептиды по настоящему изобретению могут быть фланкированы дополнительными аминокислотными остатками, при условии, что получающийся пептид сохраняет свою способность индуцировать ЦТЛ. Аминокислотные остатки, фланкирующие настоящие пептиды, могут состоять из любых видов аминокислот, при условии, что они не влияют на способность исходного пептида индуцировать ЦТЛ. Таким образом, настоящее изобретение охватывает пептиды, которые включают в себя пептиды, полученные из FOXM1, и обладают аффинностью связывания с HLA-антигенами. В основном такие пептиды меньше, чем около 40 аминокислот, часто меньше, чем около 20 аминокислот, и обычно меньше, чем около 15 аминокислот.
В большинстве случаев, модификация одного, двух или нескольких аминокислот в пептиде не будет влиять на функцию пептида, а в некоторых случаях будет даже усиливать нужную функцию исходного пептида. В самом деле, модифицированные пептиды (т.е., пептиды, состоящие из последовательности аминокислот, в которой один, два или несколько аминокислотных остатков были модифицированы (т.е., заменены, удалены, добавлены или встроены по сравнению с исходной контрольный последовательностью), как известно, сохраняют биологическую активность исходного пептида (Mark et al., Proc Natl Acad Sci USA 1984, 81: 5662-6; Zoller and Smith, Nucleic Acids Res 1982, 10: 6487-500; Dalbadie-McFarland et al., Proc Natl Acad Sci USA 1982, 79: 6409-13). Таким образом, в одном варианте осуществления пептиды по настоящему изобретению могут обладать как способностью индуцировать ЦТЛ, так и аминокислотной последовательностью, выбранной из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, где добавлена, встроена и/или заменена одна, две или даже несколько аминокислот.
Специалисты в данной области признают, что отдельные добавления или замены в аминокислотной последовательности, которые изменяют одну аминокислоту или небольшой процент аминокислот, имеют тенденцию к сохранению свойств боковой цепи исходной аминокислоты. Как таковые, их часто называют «консервативными заменами», или «консервативными модификациями», при которых изменение белка дает в результате модифицированный белок, имеющих функции, аналогичные функциям исходного белка. В рассматриваемой области известны списки консервативных замен, обеспечивающих функционально сходные аминокислоты. Примеры особенностей боковых цепей аминокислот, желательных для консервативности, включают, например, гидрофобные аминокислоты (A, I, L, M, F, P, W, Y, V), гидрофильные аминокислоты (R, D, N, C, E, Q, G, H, K, S, T), и боковые цепи, имеющие следующие общие функциональные группы или характеристики: алифатическая боковая цепь (G, A, V, L, I, P); боковая цепь, содержащая гидроксильную группу (S, T, Y); боковая цепь, содержащая атом серы (C, M); боковая цепь, содержащая карбоновую кислоту и амид (D, N, E, Q); боковая цепь, содержащая основание (R, K, H); и боковая цепь, содержащая ароматическую группу (H, F, Y, W). Кроме того, каждая из следующих восьми групп содержит аминокислоты, которые в рассматриваемой области принимаются в качестве консервативных замен друг для друга:
1) Аланин (А), Глицин (G);
2) Аспарагиновая кислота (D), Глутаминовая кислота (E);
3) Аспарагин (N), Глутамин (Q); 4) Аргинин (R), Лизин (K);
5) Изолейцин (I), Лейцин (L), Метионин (M), Валин (V);
6) Фенилаланин (F), Тирозин (Y), Триптофан (W);
7) Серин (S), Треонин (T); и
8) Цистеин (C), Метионин (М) (см., например, Creighton, Proteins 1984).
Такие консервативно модифицированные пептиды рассматриваются также как пептиды по настоящему изобретению. При этом пептиды по настоящему изобретению не ограничиваются этим и могут включать неконсервативные модификации, при условии, что модифицированный пептид сохраняет способность индуцировать ЦТЛ исходного пептида. Более того, модифицированные пептиды не должны исключать ЦТЛ-индуцирующих пептидов полиморфных вариантов, межвидовых гомологов и аллелей FOXM1.
Для сохранения необходимой способности индуцировать ЦТЛ можно изменять (вставлять, удалять, добавлять и/или заменять) небольшое число (например, 1, 2 или несколько) или небольшой процент аминокислот. В настоящем документе термин «несколько» означает 5 или меньше аминокислот, например, 4, 3 или меньше. Доля аминокислот, подлежащих модифицированию, составляет предпочтительно 20% или меньше, более предпочтительно 15% или меньше, даже более предпочтительно 10% или меньше, или от 1% до 5%.
Более того, в пептидах по настоящему изобретению можно встраивать, замещать или добавлять аминокислотные остатки, или аминокислотные остатки можно удалять для обеспечения более высокой аффинности связывания. При использовании в контексте иммунотерапии, настоящие пептиды должны быть представлены на поверхности клетки или экзосомы, предпочтительно в качестве комплекса с HLA-антигеном. В дополнение к пептидам, которые обнаруживаются в природе, поскольку закономерность последовательностей пептидов, обнаруживаемых путем связывания с HLA-антигенами, уже известна (J Immunol 1994 года, 152: 3913; Immunogenetics 1995, 41: 178; J Immunol 1994 г., 155: 4307), модификации, основанные на такой закономерности, можно вводить в иммуногенные пептиды по настоящему изобретению. Например, для увеличения HLA-А24-связывания может быть желательна замена второй с N-конца аминокислоты фенилаланином, тирозином, метионином или триптофаном, и/или аминокислоты на C-конце фенилаланином, лейцином, изолейцином, триптофаном или метионином. Таким образом, пептиды, имеющие аминокислотные последовательности, выбранные из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, где вторая аминокислота с N-конца аминокислотной последовательности SEQ ID NO заменяется фенилаланином, тирозином, метионином или триптофаном, и пептидами, и/или где C-конец аминокислотной последовательности SEQ ID NO заменяется фенилаланином, лейцином, изолейцином, триптофаном или метионином, охватываются настоящим изобретением.
Настоящее изобретение также рассматривает добавление одной, двух или нескольких аминокислот с N- и/или C-конца описанных пептидов. Такие модифицированные пептиды, обладающие высокой аффинностью связывания с HLA-антигеном и сохранившие способность индуцировать ЦТЛ, также включены в настоящее изобретение.
При этом в случае, когда пептидная последовательность идентична части аминокислотной последовательности эндогенного или экзогенного белка, имеющего отличные функции, могут индуцироваться побочные эффекты, такие как аутоиммунные расстройства и/или аллергические симптомы по отношению к определенным веществам. Поэтому предпочтительно сначала провести поиски гомологий с использованием имеющихся баз данных, чтобы избежать ситуации, при которой последовательность пептида соответствует аминокислотной последовательности другого белка. В случае, когда из поисков гомологий становится ясно, что не существует пептид даже с отличиями в 1 или 2 аминокислоты по сравнению с реальным пептидом, реальный пептид можно изменить в целях повышения его аффинности связывания с HLA-антигенами, и/или увеличения его способности индуцировать ЦТЛ без какой-либо опасности таких побочных эффектов.
Несмотря на то что ожидается, что пептиды, обладающие высокой аффинностью связывания с HLA-антигенами, как описано выше, будут очень эффективными, подходящие пептиды, которые выбирают в зависимости от наличия высокой аффинности связывания в качестве индикатора, дополнительно проверяют на наличие способности индуцировать ЦТЛ. В настоящем документе выражение «способность индуцировать ЦТЛ» указывает на способность пептида индуцировать ЦТЛ, в случае представленности на антигенпредставляющих клетках (АПК). Кроме того, «способность индуцировать ЦТЛ» включает в себя способность пептида индуцировать активацию ЦТЛ, пролиферацию ЦТЛ, способствовать ЦТЛ-лизису клеток-мишеней и увеличивать продукцию гамма-интерферона ЦТЛ.
Подтверждение способности индуцировать ЦТЛ достигается путем индуцирования АПК, несущих ГКГС-антигены человека (например, B-лимфоцитов, макрофагов и дендритных клеток (ДК)), или, более конкретно, ДК, полученных из мононуклеарных лейкоцитов периферической крови человека, и после стимуляции пептидами, смешивания с CD8-положительными клетками, а затем измерения гамма-интерферона, продуцированного и высвобожденного цитотоксическими Т-лимфоцитами против клеток-мишеней. В качестве реакционной системы можно использовать трансгенных животных, которые были выведены для экспрессии HLA-антигена человека (например, те, которые описаны в BenMohamed L, Krishnan R, Longmate J, Auge C, Low L, Primus J, Diamond DJ, Hum Immunol 2000 Aug, 61(8): 764-79, родственные статьи, книги Linkout Induction of CTL response by a minimal epitope vaccine in HLA A*0201/DRl transgenic mice: dependence on HLA class II restricted T(H) response. Например, клетки-мишени можно метить радиоактивным изотопом 51Cr и подобным, и цитотоксическую активность можно рассчитать по радиоактивности, высвобожденной из клетки-мишени. Альтернативно, способность индуцировать ЦТЛ можно оценивать путем определения гамма-интерферона, продуцированного и высвобожденного ЦТЛ в присутствии АПК, которые несут иммобилизованные пептиды, и визуализации зоны ингибирования на среде с помощью моноклональных антител против IFN-гамма.
Как результат проверки способности пептидов индуцировать ЦТЛ, как описано выше, было обнаружено, что нонапептиды или декапептиды, выбранные из пептидов, состоящих из аминокислотных последовательностей, показанных SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, демонстрировали чрезвычайно высокую способность индуцировать ЦТЛ, а также высокую аффинность связывания с HLA-антигеном. Таким образом, эти пептиды являются примером предпочтительного варианта осуществления настоящего изобретения.
Более того, результаты анализа гомологий показали, что эти пептиды не имеют значительной гомологии с пептидами, полученными от любых других известных генных продуктов человека. Это снижает возможность неизвестных или нежелательных иммунных реакций в случае применения для иммунотерапии. В силу вышесказанного, и с этой точки зрения эти пептиды находят применение для вызывания иммунитета против FOXM1 у больных раком. Итак, пептиды по настоящему изобретению, предпочтительно, пептиды, состоящие из последовательности аминокислот, выбранных из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31.
В дополнение к модификации настоящих пептидов, рассмотренных выше, описанные пептиды дополнительно могут быть связаны с другими веществами, при условии, что они сохраняют способность индуцировать ЦТЛ исходного пептида. К типичным веществам относятся: белки, пептиды, липиды, сахара и цепи сахаров, ацетильные группы, природные и синтетические полимеры и др. Настоящие пептиды могут содержать модификации, такие как гликозилирование, окислении боковой цепи и/или фосфорилирование; при условии, что модификации не уничтожают биологическую активность исходного пептида. Такие типы модификаций могут придавать дополнительные функции (например, функции мишени и функции доставки) и/или стабилизировать пептиды.
Например, для увеличения стабильности полипептида in vivo, как известно в рассматриваемой области, вводятся D-аминокислоты, миметики аминокислоты или аминокислоты, отсутствующие в природе; эта концепция также может быть принята для настоящих полипептидов. Стабильность полипептида можно определить рядом способов. Например, для проверки стабильности можно использовать пептидазы и различные биологические среды, такие как сыворотка и плазма крови человека (смотри, например, Verhoef et al., Eur J Drug Metab Pharmacokin 1986, 11: 291-302).
Более того, как отмечалось выше, среди модифицированных пептидов, которые подвергались заменам, удалениям или добавлениям одного, двух или нескольких аминокислотных остатков, можно проводить скрининг или отбирать пептиды, обладающие той же или более высокой активностью по сравнению с исходными пептидами. Вследствие этого настоящее изобретение также предоставляет способ скрининга и отбора модифицированных пептидов, обладающих той же или более высокой активностью по сравнению с исходными. Например, способ может включать в себя стадии:
а: замена, удаление или добавление, по меньшей мере, одного аминокислотного остатка у пептида по настоящему изобретению:,
b: определение активности указанного пептида:,
c: отбор пептида, обладающего той же или более высокой активностью по сравнению с исходным.
Здесь, пептиды по настоящему изобретению также могут описываться как «пептид(ы) FOXM1» или «полипептид(ы) FOXM1».
III. Подготовка пептидов FOXM1
Пептиды по настоящему изобретению можно подготовить с использованием известных способов. Например, пептиды можно подготовить синтетически, с помощью технологии рекомбинантных ДНК или химического синтеза. Пептиды по настоящему изобретению можно синтезировать по отдельности или в качестве больших полипептидов, состоящих из двух или нескольких пептидов. Затем пептиды можно выделить, т.е. очистить или отделить так, чтобы в существенной степени освободить от других природных белков клеток-хозяев и их фрагментов, или каких-либо других химических веществ.
Пептиды по настоящему изобретению могут содержать модификации, как, например, гликозилирование, окисление боковой цепи и фосфорилирование, при условии, что модификации не уничтожают биологической активности пептидов, как описано в настоящем документе. Другие модификации включают встраивание D-аминокислот или других аминокислотных миметиков, которые можно использовать, например, для увеличения времени полужизни пептидов в сыворотке крови.
Пептид по настоящему изобретению можно получить путем химического синтеза на основе выбранной последовательности аминокислот. Примеры традиционных способов пептидного синтеза, которые можно применить для синтеза, включают, в качестве неограничивающих примеров, следующие:
Альтернативно, настоящие пептиды можно получить, применяя любые известные генно-инженерные способы для получения пептидов (например, Morrison J, J Bacteriology 1977, 132: 349-51; Clark-Curtiss & Curtiss, Methods in Enzymology (eds. Wu et al.) 1983, 101: 347-62). Например, во-первых, подготавливают подходящий вектор, несущий полинуклеотид, кодирующий реальный пептид в экспрессируемой форме (например, ниже регуляторной последовательности, соответствующей промоторной последовательности), и трансформируют соответствующую клетку хозяина. Клетку хозяина затем культивируют для продуцирования представляющего интерес пептида. Пептид также можно продуцировать in vitro, применяя систему трансляции in vitro.
IV. Полинуклеотиды
Настоящее изобретение также предоставляет полинуклеотиды, которые кодируют любые из вышеупомянутых пептидов по настоящему изобретению. Они включают полинуклеотиды, полученные из гена FOXM1 природного происхождения (GenBank Accession No. NM_202002.1 (SEQ ID NO: 33)), а также полинуклеотиды, имеющие их консервативно модифицированные нуклеотидные последовательности. Здесь выражение «консервативно модифицированная нуклеотидная последовательность» относится к последовательностям, которые кодируют идентичные или по существу идентичные аминокислотные последовательности. Из-за вырожденности генетического кода большое количество функционально идентичных нуклеиновых кислот кодирует любой заданный белок. Например, каждый из кодонов GCA, GCC, GCG и GCU кодирует аминокислоту аланин. Таким образом, в каждом положении, где аланин точно определяется кодоном, кодон может быть изменен на любой из соответствующих кодонов, записанных без модификации кодированного полипептида. Такие варианты нуклеиновых кислот представляют собой «молчащие варианты», которые являются одним из видов консервативно модифицированных вариантов. Каждая последовательность нуклеиновых кислот в настоящем документе, которая кодирует пептид, также характеризует каждый возможный молчащий вариант нуклеиновой кислоты. Любой специалист в рассматриваемой области признает, что каждый кодон в нуклеиновой кислоте (за исключением AUG, который обычно является единственным кодоном для метионина, и TGG, который обычно является единственным кодоном для триптофана) можно изменить для получения функционально идентичной молекулы. Соответственно, каждый молчащий вариант нуклеиновой кислоты, которая кодирует пептид, в неявном виде описывается в каждой раскрытой последовательности.
Полинуклеотид по настоящему изобретению может состоять из ДНК, РНК и их производных. Как известно в рассматриваемой области, молекула ДНК состоит из оснований, таких как основания естественного происхождения A, T, C, G, и T заменяется на U в РНК. Любой специалист признает, что основания, не встречающиеся в природе, равным образом включаются в полинуклеотиды.
Полинуклеотид по настоящему изобретению может кодировать несколько пептидов по настоящему изобретению с присутствием встраиваемых аминокислотных последовательностей или без таковых. Например, встраиваемая аминокислотная последовательность может обеспечивать участок расщепления (например, последовательность распознавания ферментом) полинуклеотида или транслированных пептидов. Более того, полинуклеотид может включать любые дополнительные последовательности для кодирующего последовательности, кодирующей пептид по настоящему изобретению. Например, полинуклеотид может представлять собой рекомбинантный полинуклеотид, который включает регуляторные последовательности, необходимые для экспрессии пептида, или может представлять собой экспрессионный вектор (плазмиду) с маркерными генами и т.д. В большинстве случаев, такие рекомбинантные полинуклеотиды можно подготовить путем манипуляции с полинуклеотидами с помощью обычных рекомбинантных способов, используя, например, полимеразы и эндонуклеазы.
Для получения полинуклеотидов по настоящему изобретению можно применять способы как рекомбинантного, так и химического синтеза. Например, полинуклеотид можно получить путем встраивания в соответствующий вектор, который может экспрессироваться при трансфекции в компетентные клетки. Альтернативно, полинуклеотид можно амплифицировать с помощью методик ПЦР или экспрессии в соответствующих хозяевах (смотри, например, Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York, 1989). Кроме того, полинуклеотид можно синтезировать с использованием твердофазных способов, как описано в Beaucage SL & Iyer RP, Tetrahedron 1992, 48: 2223-311; Matthes et al., EMBO J 1984, 3: 801-5.
V. Экзосомы
Настоящее изобретение дополнительно предоставляет внутриклеточные везикулы, называемые экзосомами, которые представляют комплексы, образуемые между пептидами по настоящему изобретению и HLA-антигенами на их поверхности. Экзосомы можно подготовить, например, с помощью способов, подробно изложенных в патентной заявке Японии Kohyo Publications Nos. Hei 11-510507 и WO99/03499, и можно подготовить с использованием АПК, полученных от пациентов, которые подвергаются лечению и/или профилактике. Экзосомы по настоящему изобретению можно прививать в качестве вакцины, подобно пептидам по настоящему изобретению.
Тип HLA-антигенов, содержащихся в комплексах, должен соответствовать таковому у субъектов, требующих лечения и/или профилактики. Например, среди японского населения широко распространен HLA-А24 (в частности, А*2402) и, следовательно, он являлся бы подходящим для лечения японского пациента. Использование типа А24, который высоко экспрессируется среди японцев и европейцев, является благоприятным для получения эффективных результатов. Как правило, в клинике тип HLA-антигена пациента, требующего лечения, исследуют заранее, что дает возможность соответствующей селекции пептидов, имеющих высокий уровень аффинности связывания с определенным антигеном, или имеющих способность индуцировать ЦТЛ путем представления антигена. Кроме того, в целях получения пептидов, обладающих как высоким уровнем аффинности связывания, так и способностью индуцировать ЦТЛ, можно выполнять замену, вставку и/или добавление 1, 2, или нескольких аминокислот на основе аминокислотной последовательности частичного пептида природного FOXM1.
При использовании HLA-антигенов типа А24 для экзосомы по настоящему изобретению находят применение пептиды, имеющие последовательность любой из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31.
VI. Антигенпредставляющие клетки (АПК)
Настоящее изобретение также предоставляет выделенные АПК, которые представляют комплексы, образованные на их поверхности между HLA-антигенами и пептидами по настоящему изобретению. АПК можно получать от пациентов, которые подвергаются лечению и/или профилактике, и можно вводить в качестве вакцины сами по себе или в комбинации с другими лекарствами, включая пептиды по настоящему изобретению, экзосомы или ЦТЛ.
АПК не ограничиваются определенным видом клеток и включают ДК, клетки Лангерганса, макрофаги, лимфоциты и активированные Т-клетки, которые, как известно, представляют белковоподобные антигены на своей клеточной поверхности так, чтобы они узнавались лимфоцитами. Поскольку ДК являются представляющими АПК, которые обладают наилучшим индуцирующим действием на ЦТЛ среди АПК, ДК находят применение в качестве АПК по настоящему изобретению.
Например, АПК по настоящему изобретению можно получить путем индуцирования ДК из моноцитов периферической крови и затем контактирования (стимулирования) их с пептидами по настоящему изобретению in vitro и ex vivo и in vivo. Когда пептиды по настоящему изобретению вводят субъектам, АПК, которые представляют пептиды по настоящему изобретению, индуцируются в организме субъекта. Таким образом, АПК по настоящему изобретению можно получить путем сбора АПК от субъекта после введения пептидов по настоящему изобретению субъекту. Кроме того, АПК по настоящему изобретению можно получить путем контактирования АПК, полученных от субъекта, с пептидом по настоящему изобретению.
АПК по настоящему изобретению можно вводить субъекту отдельно или в комбинации с другими лекарственными средствами, включая пептиды, экзосомы или ЦТЛ по настоящему изобретению, для индукции у субъекта иммунного ответа против рака. Например, введение ex vivo может включать стадии:
а: сбор АПК от первого субъекта,
b: контактирование АПК со стадии а) с пептидом и
c: введение АПК со стадии b) второму субъекту.
Первый субъект и второй субъект могут являться одним и тем же индивидуумом, или это могут быть разные индивидуумы. АПК, полученные на стадии b, могут применяться в качестве вакцины для лечения и/или предупреждения рака, в том числе AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого (SCLC), опухоль мягких тканей и опухоль яичка.
Настоящее изобретение также предоставляет способ или процесс для производства фармацевтической композиции, индуцирующей АПК, где способ включает стадию примешивания или составления рецептуры пептида по настоящему изобретению с фармацевтически приемлемым носителем.
В соответствии с аспектом настоящего изобретения, АПК имеют высокий уровень способности индуцирования ЦТЛ. В термине «высокий уровень способности индуцировать ЦТЛ», высокий уровень относится к уровню таковой для АПК, не контактирующей с пептидом или контактирующей с пептидами, которые не могут индуцировать ЦТЛ. Такие АПК, имеющие высокий уровень способности индуцировать ЦТЛ, можно подготовить при помощи способа, который включает стадию передачи полинуклеотида, кодирующего пептид по настоящему изобретению, к АПК в условиях in vitro, а также способов, упомянутых выше. Введенные гены могут быть в виде ДНК или РНК. Примеры способов введения включают, без особых ограничений, различные способы, традиционно выполняемые в этой области, такие как липофекция, электропорация и кальцийфосфатный способ. А именно, это можно выполнить, как описано в Cancer Res 1996, 56: 5672-7; J Immunol 1998, 161: 5607-13; J Exp Med 1996, 184: 465-72; Опубликованный японский перевод международных публикаций No. 2000-509281. После переноса гена в АПК ген претерпевает в клетке транскрипцию, трансляцию и т.д., а затем полученный белок процессируется ГКГС Класса I или Класса II, и проходит через путь представления до представленных пептидов.
VII. Цитотоксические Т-лимфоциты (ЦТЛ)
ЦТЛ, индуцированный против любого из пептидов по настоящему изобретению, усиливает иммунную реакцию в отношении раковых клеток in vivo и, таким образом, может быть использован подобно пептидам как таковым. Таким образом, настоящее изобретение также предоставляет выделенные ЦТЛ, которые специфически индуцируются или активируются при помощи любого из настоящих пептидов.
Такие ЦТЛ можно получить путем (1) введения пептида(ов) по настоящему изобретению субъекту, сбора ЦТЛ от субъекта; или (2) контактирования (стимулирования) полученных от субъекта АПК, и CD8-положительных клеток или мононуклеарных лейкоцитов периферической крови in vitro с пептидом(ами) по настоящему изобретению, а затем выделения ЦТЛ; или (3) контактирования CD8-положительных клеток или мононуклеарных лейкоцитов периферической крови in vitro с АПК или экзосомами, представляющими комплекс HLA-антигенов и настоящего пептида на своей поверхности и последующего выявления ЦТЛ; или (4) введения гена, включающего полинуклеотид, кодирующий субъединицу Т-клеточного рецептора (ТКР), связывающийся с пептидом по настоящему изобретению, для ЦТЛ. Вышеупомянутые АПК и экзосомы можно подготовить с помощью способов, описанных выше, и способ (4) подробно описан ниже в разделе «VIII. Т-клеточный рецептор (ТКР)».
ЦТЛ по настоящему изобретению можно получать от пациентов, которые подвергаются лечению и/или профилактике, и можно вводить сами по себе или в комбинации с другими лекарственными средствами, в том числе пептидами по настоящему изобретению или экзосомами с целью регулирования воздействий. Полученные ЦТЛ действуют конкретно в отношении клеток-мишеней, представляющих пептиды по настоящему изобретению, например, те же пептиды, что использовались для индукции. Клетки-мишени могут представлять собой клетки, которые эндогенно экспрессируют FOXM1, такие как раковые клетки или клетки, трансфицированные геном FOXM1, и клетки, которые представляют пептид по настоящему изобретению на поверхности клеток за счет стимуляции пептидом, также могут служить в качестве мишени для атаки активированных ЦТЛ.
VIII. Т-клеточный рецептор (ТКР)
Настоящее изобретение также предоставляет композицию, содержащую нуклеиновые кислоты, кодирующие полипептиды, которые способны образовывать субъединицы T-клеточного рецептора (ТКР), и способы ее применения. Субъединицы ТКР обладают способностью образовывать ТКР, которые придают специфичность Т-клеткам в отношении опухолевых клеток, экспрессирующих FOXM1. С помощью известных в данной области способов можно идентифицировать нуклеиновые кислоты альфа- и бета- цепей, как ТКР-субъединиц ЦТЛ, индуцированных одним или несколькими пептидами по настоящему изобретению (WO2007/032255 и Morgan et al., J Immunol, 171, 3288 (2003)). Например, способ ПЦР является предпочтительным для анализа ТКР. ПЦР-праймеры для анализа могут представлять собой, например, праймеры 5'-R (5'-gtctaccaggcattcgcttcat-3») в качестве праймеров с 5'-стороны (SEQ ID NO: 35) и праймеры 3-Тра-С (5'-tcagctggaccacagccgcagcgt-3'), специфические для C-области альфа-цепи ТКР (SEQ ID NO: 36), праймеры 3-Pra-Cl (5'-tcagaaatcctttctcttgac-3'), специфические для C1-области бета-цепи ТКР (SEQ ID NO: 37) или праймеры 3-TRbeta-C2 (5'-ctagcctctggaatcctttctctt-3'), специфические для C2-области бета-цепи ТКР (SEQ ID NO: 38), в качестве праймеров с 3'-стороны, но без ограничения. Производные ТКР могут с высокой авидностью связывать клетки-мишени, представляющие пептид FOXM1, и необязательно опосредовать эффективное уничтожение клеток-мишеней, представляющих пептида FOXM1 in vivo и in vitro.
Нуклеиновые кислоты, кодирующие субъединицы ТКР, могут быть включены в соответствующие векторы, например ретровирусные векторы. Эти векторы хорошо известны в рассматриваемой области. Нуклеиновые кислоты или векторы, содержащие их, можно эффективно передавать в Т-клетки, например в Т-клетки пациента. Предпочтительно, настоящее изобретение предоставляет готовую к использованию композицию, дающую возможность быстрой модификации собственных Т-клеток пациента (или таковых другого млекопитающего) для того, чтобы быстро и легко продуцировать модифицированные Т-клетки, имеющие превосходные свойства уничтожать раковые клетки.
Специфический ТКР представляет собой рецептор, способный специфически распознавать комплекс пептида по настоящему изобретению и молекулы HLA, придающий Т-клетке специфическую активность по отношению к клетке-мишени в случае, когда ТКР находится на поверхности Т-клетки. Специфическое распознавание вышеупомянутого комплекса можно подтвердить любыми известными способами, и предпочтительные способы включают, например, тетрамерный анализ с использованием молекулы HLA и пептида по настоящему изобретению, и анализ ELISPOT. Проведением анализа ELISPOT можно подтвердить, что T-клетка, экспрессирующая ТКР на клеточной поверхности, распознает клетки с помощью ТКР и что сигнал передается внутриклеточно. Подтверждение того, что вышеупомянутый комплекс может придавать T-клеточную цитотоксическую активность в случае, когда комплекс существует на Т-клеточной поверхности, можно также получить при помощи известного способа. Предпочтительный способ включает, например, определение цитотоксической активности против HLA-положительной клетки-мишени, такой как анализ высвобождения хрома.
Кроме того, настоящее изобретение представляет ЦТЛ, которые подготавливают путем передачи нуклеиновых кислот, кодирующих полипептиды ТКР-субъединиц, которые связываются с пептидом FOXM1, например, SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, в контексте HLA-А24. Трансдуцированные ЦТЛ способны направляться к раковым клеткам in vivo, и могут быть наращены при помощи известных способов культивирования in vitro (смотри, Kawakami et al., J Immunol., 142, 3452-3461 (1989)). ЦТЛ по настоящему изобретению можно применять для образования иммуногенной композиции, полезной при лечении или профилактике рака у пациента, нуждающегося в терапии и защите (WO2006/031221).
IX. Фармацевтические вещества или композиции
Предупреждение и профилактика включает любую активность, которая уменьшает бремя смертности или процент смертности от заболевания. Предупреждение и профилактика может осуществляться «на первичном, вторичном и третичном уровнях предупреждения». В то время как первичные предупреждение и профилактика предотвращают развитие заболевания, вторичный и третичный уровни предупреждения и профилактики включают мероприятия, направленные на предупреждение и профилактику прогрессирования заболевания и появления симптомов, а также ослабления негативного воздействия уже существующего заболевания путем восстановления функций и уменьшения связанных с заболеванием осложнений. Кроме того, предупреждение и профилактика включают в себя широкий спектр профилактических терапий, направленных на смягчение тяжести конкретного расстройства, например, снижение распространения и метастазирования опухолей, уменьшение ангиогенеза. Лечение и/или профилактика рака или, и/или предупреждения их послеоперационных рецидивов включает в себя любую из следующих стадий, как, например, хирургическое удаление раковой клетки, подавление роста раковых клеток, инволюция или регрессии опухоли, индукция ремиссии и подавление возникновения рака, регрессия опухоли и уменьшение или подавление метастазов. Эффективное лечение и/или профилактика рака уменьшает смертность и улучшает прогноз для индивидуумов, имеющих рак, снижает уровень онкомаркеров в крови, ослабляет обнаруживаемые симптомы, сопровождающие рак. Например, снижение или улучшение симптомов, составляющие эффективное лечение и/или предупреждение, включают 10%, 20%, 30% и более уменьшение, или стабилизацию заболевания.
Поскольку экспрессия FOXM1 специфически увеличена в раках, включая AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка, по сравнению с нормальной тканью, пептиды по настоящему изобретению или полинуклеотиды, кодирующие такие пептиды, можно применять для лечения и/или профилактики рака и опухоли, и/или предупреждения их послеоперационных рецидивов. Таким образом, настоящее изобретение предоставляет лекарственное вещество или композицию для лечения и/или профилактики рака или опухоли, и/или предупреждения их послеоперационных рецидивов, которое включает один или несколько пептидов по настоящему изобретению, или полинуклеотиды, кодирующие пептиды в качестве активного ингредиента. Альтернативно, настоящие пептиды можно экспрессировать на поверхности любой из вышеупомянутых экзосом или клеток, таких как АПК, для использования в лекарственных веществах или композициях. Кроме того, вышеупомянутые ЦТЛ, которые нацеливают любой из пептидов по настоящему изобретению, также можно использовать в качестве активного ингредиента настоящих лекарственных веществ или композиций.
В другом варианте осуществления, настоящее изобретение также предоставляет применение активного ингредиента, выбранного из:
(a) пептида по настоящему изобретению;
(b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто здесь, в экспрессируемой форме;
(c) APC или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению
в производстве фармацевтической композиции или вещества для лечения рака или опухоли.
Альтернативно, настоящее изобретение дополнительно предоставляет активный ингредиент, выбранный из:
(a) пептида по настоящему изобретению;
((b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто здесь, в экспрессируемой форме;
(c) APC или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению
для применения при лечении рака или опухоли.
Альтернативно, настоящее изобретение дополнительно предоставляет способ или процесс для изготовления фармацевтической композиции или вещества для лечения рака или опухоли, где способ или процесс включает стадию составления рецептуры фармацевтически или физиологически приемлемого носителя с активным ингредиентом, выбранным из:
(a) пептида по настоящему изобретению;
((b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто здесь, в экспрессируемой форме;
(c) APC или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению в качестве активных ингредиентов.
В другом варианте осуществления, настоящее изобретение также предоставляет способ или процесс для изготовления фармацевтической композиции или вещества для лечения рака или опухоли, где способ или процесс включает стадии примешивания активного ингредиента с фармацевтически или физиологически приемлемым носителем, где активный ингредиент выбирают из:
(a) пептида по настоящему изобретению;
((b) нуклеиновой кислоты, кодирующей такой пептид, как раскрыто здесь, в экспрессируемой форме;
(c) APC или экзосомы, представляющей пептид по настоящему изобретению на своей поверхности; и
(d) цитотоксической Т-клетки по настоящему изобретению.
Альтернативно, фармацевтическую композицию или вещество или настоящее изобретение может применять либо для профилактики рака или опухоли, либо для предупреждения их послеоперационных рецидивов, либо и для того и другого.
Настоящие фармацевтические вещества или композиции находят применение в качестве вакцины. В контексте настоящего изобретения выражение «вакцина» (также именуемая как «иммуногенная композиция») относится к веществу, которое имеет функцию индуцирования противоопухолевого иммунитета после прививки животным.
Фармацевтические вещества или композиции по настоящему изобретению можно применять для лечения и/или предупреждения раков и опухолей, и/или предупреждения их послеоперационных рецидивов у субъектов или пациентов, включая человека и любых других млекопитающих, включая, в качестве неограничивающих примеров, мышь, крысу, морскую свинку, кролика, кошку, собаку, овцу, козу, свинью, крупный рогатый скот, лошадь, обезьяну, бабуина и шимпанзе, в частности, коммерчески важных животных или домашних животных.
В соответствии с настоящим изобретением оказалось, что пептиды, обладающие любой аминокислотной последовательностью из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, представляют собой HLA- А24-рестриктированные эпитопные пептиды или подходящие пептиды, которые могут индуцировать сильный и специфический иммунный ответ. Вследствие этого настоящие фармацевтические вещества или композиции, которые включают любые из этих пептидов, обладающих аминокислотными последовательностями SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, особенно подходят для введения субъектам, чей HLA-антиген представляет собой HLA-А24. То же относится и к фармацевтическим веществам и композициям, которые включают полинуклеотиды, кодирующие любой из этих пептидов (т.е., полинуклеотиды по настоящему изобретению).
Раки или опухоли, подлежащие лечению фармацевтическими веществами или композициями по настоящему изобретению, не ограничены и включают любой рак или опухоль, в который вовлечен FOXM1 (например, сверхэкспрессируется), включая, например, AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфома, остеосаркома, рак яичников, рак поджелудочной железы, рак предстательной железы, почечная карцинома, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка.
Настоящие фармацевтические вещества или композиции могут содержать, в дополнение к вышеупомянутым активным ингредиентам, другие пептиды, которые обладают способностью индуцировать ЦТЛ против раковых клеток, другие полинуклеотиды, кодирующие другие пептиды, другие клетки, которые представляют другие пептиды, или подобное. Здесь, другие пептиды, которые обладают способностью индуцировать ЦТЛ против раковых клеток, служат примером специфических антигенов рака (например, идентифицированные ОСА), но не ограничиваются этим.
Если необходимо, фармацевтические вещества или композиции по настоящему изобретению могут дополнительно включать другие терапевтические вещества в качестве активного ингредиента, при условии, что вещество не ингибирует противоопухолевый эффект активного ингредиента, например, любой из настоящих пептидов. Например, составы могут включать противовоспалительные вещества, обезболивающие, вещества для химиотерапии и подобное. Дополнительно к включению других терапевтических веществ в лекарственное средство как таковое, лекарственные средства по настоящему изобретению можно также применять последовательно или одновременно с одной или несколькими другими фармакологическими веществами. Количества лекарственного средства и фармакологического вещества зависят, например, от типа применяемого фармакологического вещества(в), подлежащего лечению заболевания и графика и способов введения.
Следует понимать, что в дополнение к ингредиентам, подробно упомянутым здесь, фармацевтические вещества или композиции по настоящему изобретению могут включать и другие композиции, общепринятые в данной области, с учетом типа рассматриваемого состава.
В одном варианте осуществления настоящего изобретения, настоящие фармацевтические вещества или композиции могут быть включены в готовые изделия и комплекты, содержащие материалы, полезные для лечения патологических состояний подлежащего лечению заболевания, например, рака. Готовое изделие может включать контейнер любого из настоящих фармацевтических веществ или композиций, с этикеткой. Соответствующие контейнеры включают бутылки, флаконы и пробирки. Контейнеры могут быть образованы из различных материалов, таких как стекло или пластик. Надпись на контейнере должна указывать, что композиция применяется для лечения или предупреждения одного или нескольких состояний заболевания. Этикетки могут также содержать предписание по введению и так далее.
В дополнение к контейнеру, описанному выше, комплект, включающий фармацевтическую субстанцию или композицию по настоящему изобретению, может необязательно дополнительно включать второй контейнер, размещающий фармацевтически приемлемый разбавитель. Он также может включать другие материалы, желательные с коммерческой точки зрения и с точки зрения пользователя, включая другие буферы, разбавители, фильтры, иглы, шприцы и вкладыши с инструкцией по применению.
Фармацевтические вещества или композиции, при желании, могут быть представлены в упаковке или дозаторном устройстве, которое может содержать одну или несколько единичных лекарственных форм, содержащих активный ингредиент. Упаковка может, например, включать металлическую или пластиковую фольгу, такую как блистерная упаковка. Упаковка или дозаторное устройство может сопровождаться инструкциями для введения.
(1) Фармацевтические вещества или композиции, содержащие пептиды в качестве активного ингредиента
Пептиды по настоящему изобретению можно вводить непосредственно в качестве фармацевтического вещества или композиции, или, при необходимости, чтобы были составлены путем общепринятых способов подбора составов. В последнем случае, в дополнение к пептидам по настоящему изобретению, носители, наполнители и подобное, которые обычно используются для лекарств, могут быть включены как соответствующие без особых ограничений. Примерами таких носителей являются стерилизованная вода, физиологический раствор, фосфатный буфер, культуральная жидкость и подобное. Более того, фармацевтические вещества или композиции могут при необходимости содержать стабилизаторы, суспензии, консерванты, сурфактанты и подобное. Фармацевтические вещества или композиции по настоящему изобретению можно применять для противоопухолевых назначений.
Для индуцирования ЦТЛ in vivo пептиды по настоящему изобретению можно подготовить в виде комбинации, состоящей из двух или нескольких пептидов по настоящему изобретению. Пептидная комбинация может иметь форму смеси или может соединяться друг с другом с помощью стандартных методик. Например, пептиды могут быть химически связаны или экспрессироваться в качестве единой слитой полипептидной последовательности. Пептиды в комбинации могут быть одинаковыми или различными. Благодаря введению пептидов по настоящему изобретению пептиды с высокой плотностью представляются при помощи HLA-антигенов на АПК, затем индуцируются ЦТЛ, которые специфически реагируют на комплекс, образовавшийся между представленным пептидом и HLA-антигеном. Альтернативно, АПК (например, ДК) отбирают у субъектов, а затем стимулируют пептидами по настоящему изобретению для получения АПК, которые представляют любой из пептидов по этому изобретению на своей клеточной поверхности. Эти АПК повторно вводят субъектам для индуцирования ЦТЛ у субъектов, и, как следствие, агрессивность по отношению к опухолеспецифическому эндотелию может увеличиться.
Фармацевтические вещества или композиции для лечения и/или предупреждения рака или опухоли, которые включают пептида по настоящему изобретению в качестве активного ингредиента, также может включать адъювант для, как известно, эффективного индуцирования клеточного иммунитета. Альтернативно, фармацевтические вещества или композиции можно вводить с другими активными ингредиентами или вводить при помощи составов в гранулах. Адъювант относится к соединению, которое усиливает иммунный ответ против белка при введении одновременно (или последовательно) с белком, обладающим иммунологической активностью. Адъюванты, рассматриваемые здесь, включают те, которые описаны в литературе (Clin Microbiol Rev 1994, 7: 277-89). Примеры подходящих адъювантов включают фосфат алюминия, гидроокись алюминия, квасцы, холерный токсин, токсин сальмонеллы и подобные, но не ограничиваются этим.
Более того, можно удобно использовать липосомные составы, гранулированные составы, в которых пептид связывается с бусами диаметром несколько микрометров, и составы, в которых липид связывается с пептидом.
В другом варианте осуществления настоящего изобретения, пептиды по настоящему изобретению можно также вводить в виде фармацевтически приемлемой соли. Предпочтительные примеры солей включают соли щелочных металлов, соли металлов, соли на органической основе, соли органических кислот и соли неорганических кислот.
В некоторых вариантах осуществления, фармацевтические вещества или композиции по настоящему изобретению могут дополнительно включать компонент, который праймирует ЦТЛ. Липиды были определены в качестве веществ, способных праймировать ЦТЛ in vivo в отношении вирусных антигенов. Например, остатки пальмитиновой кислоты можно присоединять к эпсилон- и альфа- аминогруппе остатка лизина, а затем присоединять к пептиду по настоящему изобретению. Липидированный пептид затем можно либо вводить непосредственно в мицеллу или частицу, включенную в липосому, либо эмульгировать в адъюванте. В качестве другого примера липидного праймирования ЦТЛ ответов, липопротеины E. coli, такие как, например, трипальмитоил-S-глицерилцистеинил-серил-серин (P3CSS) можно использовать для праймирования ЦТЛ в случае ковалентного присоединения к соответствующему пептиду (смотри, например, Deres et al., Nature 1989, 342: 561-4).
Способ введения может быть оральным, внутрикожным, подкожным, внутривенной инъекцией или подобным, и находит применение системное введение или местное введение поблизости от участков-мишеней. Введение можно осуществлять посредством единичного введения или поддерживать с помощью нескольких введений. Дозу пептидов по настоящему изобретению можно соответствующим образом корректировать в зависимости от подлежащего лечению заболевания, возраста пациента, массы, способа введения и подобного, и она обычно составляет от 0,001 мг до 1000 мг, например, от 0,001 мг до 1000 мг, например, от 0,1 мг до 10 мг, и может вводиться от одного раза в несколько дней до одного раза в несколько месяцев. Любой специалист в рассматриваемой области может соответствующим образом подобрать подходящую дозу.
(2) Фармацевтические вещества или композиции, содержащие полинуклеотиды в качестве активного ингредиента
Фармацевтические вещества или композиции по настоящему изобретению также могут содержать нуклеиновые кислоты, кодирующие описанные здесь пептиды в экспрессируемой форме. Здесь, выражение «в экспрессируемой форме» означает, что полинуклеотид в случае введения в клетку будет экспрессироваться in vivo, в качестве полипептида, который индуцирует противоопухолевый иммунитет. В типичном варианте осуществления, последовательности нуклеиновых кислот представляющего интерес полинуклеотида включает регуляторные элементы, необходимые для экспрессии полинуклеотида. Полинуклеотид(ы) можно приспособить таким образом, чтобы получить стабильную вставку в геном клетки-мишени (смотри, например, Thomas KR & Capecchi MR, Cell 1987, 51: 503-12 для описания векторов с кассетами для гомологичной рекомбинации). Смотри, например, Wolff et al., Science 1990, 247: 1465-8; Патент США No. 5580859; 5589466; 5804566; 5739118; 5736524; 5679647; и WO 98/04720. Примеры технологий доставки на основе ДНК включают «голую ДНК», облегченную (бупивакаин, полимеры, пептид-опосредованная) доставку, катионные липидные комплексы, и опосредованную частицами («генной пушки») или опосредованную давлением доставку (смотри, например, Патент США No 5922687).
Пептиды по настоящему изобретению можно экспрессировать при помощи вирусных или бактериальных векторов. Примеры экспрессионных векторов включают ослабленных вирусных хозяев, таких как вакцинного вируса или вируса чумы птиц. Этот подход предполагает использование вакцинного вируса, например, в качестве вектора для экспрессии нуклеотидных последовательностей, кодирующих пептид. После введения в хозяина рекомбинантный вакцинный вирус экспрессирует иммуногенный пептид, и, посредством этого, вызывает иммунный ответ. Вакцинные векторы и способы пригодны для протоколов иммунизации, как описано, например, в патенте США No 4722848. Другим вектором является БЦЖ (бацилла Кальметта-Герена). Векторы БЦЖ описаны в Stover et al., Nature 1991, 351: 456-60. Наблюдается широкое разнообразие других векторов, пригодных для терапевтического введения или иммунизации, например, аденовирусные и связанные с аденовирусными векторами, ретровирусные векторы, векторы Salmonella typhi, векторы на основе обезвреженного сибиреязвенного токсина и подобные. Смотри, например, See, e.g., Shata et al., MoI Med Today 2000, 6: 66-71; Shedlock et al., J Leukoc Biol 2000, 68: 793-806; Hipp et al., In Vivo 2000, 14: 571-85.
Доставка полинуклеотида в организме субъекта может являться либо непосредственной, и в этом случае субъект непосредственно подвергается действию вектора, несущего полинуклеотид, или опосредованной, в случае чего клетки сначала трансформируют представляющим интерес полинуклеотидом in vitro, а затем клетки трансплантируют субъекту. Эти два подхода известны, соответственно, как генные терапии in vivo и ex vivo.
Для общего обзора способов генной терапии, смотри Goldspiel et al., Clinical Pharmacy 1993, 12: 488-505; Wu и Wu, Biotherapy 1991, 3: 87-95; Tolstoshev, Ann Rev Pharmacol Toxicol 1993, 33: 573-96; Mulligan, Science 1993, 260: 926-32; Morgan & Anderson, Ann Rev Biochem 1993, 62: 191-217; Trends in Biotechnology 1993, 11(5): 155-215). Способы, широко известные в области технологии рекомбинантной ДНК, которые также могут быть использованы для настоящего изобретения, описаны в Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, NY, 1993; и Krieger, Gene Transfer и Expression, A Laboratory Manual, Stockton Press, NY, 1990.
Способ введения может быть оральным, внутрикожным, подкожным, внутривенной инъекцией или подобным, и находит применение системное введение или местное введение поблизости от участков-мишеней. Введение можно осуществлять посредством единичного введения или поддерживать с помощью нескольких введений. Дозу пептидов по настоящему изобретению можно соответствующим образом корректировать в зависимости от подлежащего лечению заболевания, возраста пациента, массы, способа введения и подобного, и она обычно составляет от 0,001 мг до 1000 мг, например, от 0,001 мг до 1000 мг, например, от 0,1 мг до 10 мг, и может вводиться от одного раза в несколько дней до одного раза в несколько месяцев. Любой специалист в рассматриваемой области может соответствующим образом подобрать подходящую дозу.
X. Способы применения пептидов, экзосом, АПК и ЦТЛ
Пептиды и полинуклеотиды по настоящему изобретению можно использовать для индуцирования АПК и ЦТЛ. Экзосомы и АПК по настоящему изобретению также можно использовать для индуцирования ЦТЛ. Пептиды, полинуклеотиды, экзосомы и АПК можно использовать в комбинации с любыми другими соединениями, при условии, что соединения не ингибируют их способность индуцирования ЦТЛ. Таким образом, любое из вышеупомянутых фармацевтических веществ или композиций по настоящему изобретению можно применять для индуцирования ЦТЛ, и дополнительно к этому, те, которые включают пептиды и полинуклеотиды, можно также применять для индуцирования АПК, как обсуждается и описывается ниже.
(1) Способ индуцирования антиген-представляющих клеток (АПК)
Настоящее изобретение предоставляет способы индуцирования или подготовки АПК с высокой способностью индуцировать ЦТЛ при помощи пептидов или полинуклеотидов по настоящему изобретению. Способы по настоящему изобретению включают стадию контактирования АПК с пептидами по настоящему изобретению in vitro и ex vivo и in vivo. Например, способ контактирования АПК с пептидами ex vivo могут включать стадии:
a: сбор АПК от субъекта:, и
b: контактирование АПК со стадии а) с пептидом.
АПК не ограничиваются определенным видом клеток и включают ДК, клетки Лангерганса, макрофаги, В-клетки и активированные Т-клетки, которые, как известно, представляют белковоподобные антигены на своей клеточной поверхности так, чтобы они узнавались лимфоцитами. ДК могут предпочтительно использоваться из-за их самой сильной среди АПК способности индуцировать ЦТЛ. Любые пептиды по настоящему изобретению можно использовать в качестве пептида со стадии b самого по себе или в комбинации с другими пептидами по настоящему изобретению.
Альтернативно, пептиды по настоящему изобретению можно вводить субъекту для контактирования пептидов с АПК in vivo. В результате в организме субъекта можно индуцировать АПК с высокой способностью индуцировать ЦТЛ. Таким образом, в настоящее изобретение также рассматривает способ введения пептидов по настоящему изобретению субъекту для индуцирования АПК in vivo. Также возможно введение субъекту полинуклеотидов, кодирующих пептиды по настоящему изобретению, в экспрессируемой форме, так, чтобы пептиды по настоящему изобретению экспрессировались и контактировали с АПК in vivo для индуцирования вследствие этого АПК с высокой способностью индуцировать ЦТЛ в организме субъекта. Таким образом настоящее изобретение также предусматривает способ введения полинуклеотидов по настоящему изобретению субъекту для индуцирования АПК in vivo. Выражение «экспрессируемая форма» определено выше, в разделе «IX. Фармацевтические вещества или композиции».
(2) Фармацевтические вещества или композиции, содержащие полинуклеотиды в качестве активного ингредиента.
Более того, настоящее изобретение включает введение полинуклеотида по настоящему изобретению в АПК для индуцирования или подготовки АПК, способных индуцировать ЦТЛ. Например, способ может включать стадии:
а: сбор АПК от субъекта:, и
b: введение полинуклеотида, кодирующего пептид по настоящему изобретению.
Стадию b можно выполнять, как описано выше в разделе «VI. Антигенпредставляющие клетки».
Альтернативно, настоящее изобретение предоставляет способ подготовки антигенпредставляющей клетки (АПК), которая специфически индуцирует активность ЦТЛ против FOXM1, где способ включает одну из следующих стадий:
(a) Контактирование АПК с пептидом по настоящему изобретению in vitro, ex vivo или in vivo; и
(b) введение полинуклеотида, кодирующего пептид по настоящему изобретению, в АПК.
(2) Способ индуцирования ЦТЛ
Более того, настоящее изобретение предоставляет способы индуцирования ЦТЛ с помощью пептидов, полинуклеотидов, или экзосом или АПК по настоящему изобретению.
Настоящее изобретение также предоставляет способы индуцирования ЦТЛ с помощью полинуклеотида, кодирующего полипептид, который способен образовывать субъединицу Т-клеточного рецептора (ТКР), распознающую комплекс пептидов по настоящему изобретению и HLA-антигенов. Предпочтительно, способы индуцирования ЦТЛ включают, по меньшей мере, одну стадию, выбранную из группы, состоящей из:
а) контактирование CD8-положительных Т-клеток с антигенпредставляющей клеткой и/или экзосомой, которая представляет на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению; и
b) введение полинуклеотида, кодирующего полипептид, который способен образовывать ТКР-субъединицу, узнающую комплекс пептида по настоящему изобретению и HLA-антигена в CD8-положительных клетках.
В случае, когда пептиды, полинуклеотиды, АПК, или экзосомы по настоящему изобретению вводят субъекту, в организме субъекта индуцируются ЦТЛ, и возрастает сила иммунный ответа, нацеленного на раковые клетки. Таким образом, настоящее изобретение также предусматривает способ, который включает стадию введения пептидов, полинуклеотидов, АПК или экзосом по настоящему изобретению субъекту для индуцирования ЦТЛ.
Альтернативно, можно также индуцировать ЦТЛ путем их использования ex vivo. В таком случае, после индукции ЦТЛ, активированные ЦТЛ можно было бы вернуть субъекту. Например, способ по настоящему изобретению для индуцирования ЦТЛ может включать стадии:
а) сбор АПК от субъекта;
б) контактирование АПК со стадии а) с пептидом; и
c) совместное культивирование АПК со стадии b) с CD8-положительными клетками.
АПК, совместно культвируемые с CD8-положительными клетками в вышеприведенной стадии c также можно подготовить путем передачи гена, который включает полинуклеотид по настоящему изобретению, в АПК, как описано выше в разделе «VI. Антигенпредставляющие клетки», но без ограничения этим, и любые АПК, которые эффективно представляют на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению, можно использовать для быстрого способа.
Вместо таких АПК можно также использовать экзосомы, которые представляют на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению. А именно, настоящее изобретение также предусматривает способ, при котором экзосомы, представляющие на своей поверхности комплекс HLA-антигена и пептида по настоящему изобретению, совместно культивируют с CD8-положительными клетками. Такие экзосомы можно подготовить при помощи способов, описанных выше в разделе «V. Экзосомы».
Более того, ЦТЛ можно индуцировать введением гена, который включает полинуклеотид, кодирующий ТКР-субъединицу, связывающуюся с пептидом по настоящему изобретению в CD8-положительных клетках. Такую передачу можно осуществлять, как описано выше в разделе «VIII. Т-клеточный рецептор (ТКР)».
Кроме того, настоящее изобретение предоставляет способ или процесс изготовления фармацевтического вещества или композиции, индуцирующего ЦТЛ, где способ включает стадию примешивания или составления рецептуры пептида по настоящему изобретению с фармацевтически приемлемым носителем.
(3) Способ индукцирования иммунного ответа
Более того, настоящее изобретение предоставляет способы индукцирования иммунного ответа в отношении заболеваний, связанных с FOXM1. Подходящее заболевание включает рак, примеры которого включают AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, почечную карциному, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка.
Способы включают стадию введения веществ или композиций, содержащих любой из пептидов по настоящему изобретению или полинуклеотиды, кодирующие их. Настоящий способ по изобретению также предусматривает введение экзосом или АПК, представляющих любой из пептидов по настоящему изобретению. Более подробно смотри в пункте «IX. Фармацевтические вещества или композиции», особенно в части, описывающей применение фармацевтических веществ или композиций по настоящему изобретению в качестве вакцин. Кроме того, экзосомы и АПК, которые можно использовать в настоящих способах для индукцирования иммунного ответа, подробно описаны в пунктах «V. Экзосомы», «VI. Антигенпредставляющие клетки (АПК)», и (1) и (2) «X. Способы использования пептидов, экзосом, АПК и ЦТЛ», смотри выше.
Настоящее изобретение также предоставляет способ или процесс для изготовления фармацевтического вещества или композиции, индуцирующей иммунный ответ, где способ включает стадию примешивания или составления рецептуры пептида по настоящему изобретению с фармацевтически приемлемым носителем.
Альтернативно, способ по настоящему изобретению может включать стадию введения вакцины или фармацевтической композиции, которая содержит:
(a) пептида по настоящему изобретению;
(b) нуклеиновую кислоту, кодирующую такой пептид, как раскрыто здесь, в экспрессируемой форме;
(c) APC или экзосому, представляющую пептид по настоящему изобретению на своей поверхности;
(d) цитотоксическую Т-клетку по настоящему изобретению.
В настоящем изобретении рак, сверхэкспрессирующий FOXM1, можно лечить с помощью этих активных ингредиентов. Рак включает, в качестве неограничивающих примеров, AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, почечную карциному, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка. Соответственно, перед введением вакцин или фармацевтических композиций, содержащих активные ингредиенты, предпочтительно подтвердить, что уровень экспрессии FOXM1 в подлежащий лечению раковых клетках или тканях увеличен по сравнению с нормальными клетками того же органа. Таким образом, в одном варианте осуществления, настоящее изобретение предоставляет способ лечения рака, (сверх)экспрессирующего FOXM1, который может включать стадии:
i) определение уровня экспрессии FOXM1 в раковых клетках или тканях, полученных от субъекта с подлежащим лечению раком;
ii) сравнение уровня экспрессии FOXM1 с нормальным контролем; и
iii) введение, по меньшей мере, одного компонента, выбранного из группы, состоящей из (a) - (d), описанной выше, субъекту с раком, сверхэкспрессирующим FOXM1 по сравнению с нормальным контролем. Альтернативно, настоящее изобретение также предоставляет вакцину и фармацевтическую композицию, содержащую, по меньшей мере, один компонент, выбранный из группы, состоящей из (a) - (d), описанной выше, для применения при введении субъекту с раком, сверхэкспрессирующим FOXM1. Иными словами, настоящее изобретение дополнительно предоставляет способ идентификации субъекта, подлежащего лечению полипептидом FOXM1 по настоящему изобретению, который может включать стадию определения уровня экспрессии FOXM1 в полученных от субъекта раковых клетках или тканях, где увеличение уровня по сравнению с нормальным контрольным уровнем гена указывает на то, что субъект имеет рак, который можно лечить полипептидом FOXM1 по настоящему изобретению. Способ лечения рака по настоящему изобретению будет описан более подробно ниже.
Подлежащий лечению при помощи настоящего способа субъект предпочтительно является млекопитающим. Типичные млекопитающие включают, в качестве неограничивающих примеров, человека, отличного от человека примата, мышь, крысу, собаку, кошку, лошадь и корову.
В соответствии с настоящим изобретением, определяют уровень экспрессии FOXM1 в раковых клетках или тканях, полученных от субъекта. Уровень экспрессии можно определить на уровне продукта транскрипции (нуклеиновой кислоты), используя способы, известные в рассматриваемой области. Например, мРНК FOXM1 можно количественно определить с помощью зондов при помощи способов гибридизации (например, Нозерн-гибридизации). Определение можно проводить на чипе или матрице. Использование матрицы является предпочтительным для определения уровня экспрессии FOXM1. Специалист в рассматриваемой области может подготовить такие зонды, используя информацию о последовательности FOXM1. Например, в качестве зондов можно использовать кДНК FOXM1. При необходимости, зонды можно пометить с помощью подходящей метки, такой как красители, флуоресцентные вещества и изотопы, и уровень экспрессии гена можно детектировать по интенсивности гибридизованных меток.
Более того, продукт транскрипции FOXM1 (например, SEQ ID NO: 34) можно количественно определять при помощи праймеров с использованием способов на основе амплификации (например, RT-PCR). Такие праймеры можно также подготовить на основе имеющейся информации о последовательности гена.
В конкретном плане, зонд или праймер, используемый в настоящем способе, гибридизуется при жестких, умеренно жестких или нежестких условиях с мРНК FOXM1. Как используется здесь, выражение «строгие условия (гибридизации)» означает условия, при которых зонд или праймер будет гибридизоваться со своей последовательностью-мишенью, но не с другой последовательностью. Жесткие условия являются зависимыми от последовательности и будут разными при различных условиях. Специфическая гибридизация более длинных последовательностей наблюдается при более высоких температурах, чем более коротких последовательностей. Как правило, температуру при жестких условиях выбирают на приблизительно 5 градусов С ниже, чем на тепловая температура плавления (Tm) для конкретной последовательности, при определенной ионной силе и pH. Tm представляет собой температуру (при определенной ионной силе, pH и концентрации нуклеиновых кислот), при которой 50% зондов, комплементарных своей последовательности-мишени, гибридизуются с последовательностью-мишенью в равновесии. Поскольку последовательность-мишень, как правило, присутствует в избытке, при Tm 50% зондов находятся в равновесии. Как правило, жесткими будут условия, при которых концентрация соли составляет менее чем около 1,0 М ионов натрия, как правило, от около 0,01 до 1,0 М ионов натрия (или других солей) при рН от 7,0 до 8,3, и температура составляет, по меньшей мере, около 30 градусов C для коротких зондов или праймеров (например, от 10 до 50 нуклеотидов) и, по меньшей мере, около 60 градусов С для более длинных зондов или праймеров. Жесткие условия также можно достичь добавлением дестабилизирующих веществ, таких, как формамид.
Альтернативно, продукт трансляции детектировать для диагностики по настоящему изобретению. Например, можно определить количество белка FOXM1 (SEQ ID NO: 34). Способы определения количества белка как продукта трансляции включают способы иммуноанализа, в которых используется антитело, специфически узнающее белок. Антитело может являться моноклональным и поликлональным. Более того, для детектирования можно использовать любой фрагмент или модификацию (например, химерное антитело, scFv, Fab, F(ab')2, Fv и т.д.) антитела, при условии, что фрагмент или модифицированное антитело сохраняет способность связывания с белком FOXM1. Способы подготовки этих видов антител для детектирования белков известны в рассматриваемой области, и любой способ можно использовать по настоящему изобретению для подготовки таких антител и их эквивалентов.
В качестве еще одного способа детектирования уровня экспрессии гена FOXM1, основанного на его продукте трансляции, можно определять интенсивность окраски при помощи иммуногистохимического анализа с использованием антител против белка FOXM1. То есть при этом определении сильное окрашивание указывает на увеличенное присутствие белка/ увеличенный уровень и в то же время на высокий уровень экспрессии гена FOXM1.
Уровень экспрессии гена-мишени, например, в том числе гена FOXM1, в раковых клетках можно определить как увеличенный, если уровень превышает контрольный уровень (например, уровень в нормальных клетках) соответствующего гена-мишени, например, на 10%, 25% или 50%, или увеличен до более чем в 1,1 раза, более чем в 1,5 раза, более чем в 2,0 раза, больше чем в 5,0 раз, более чем в 10,0 раз или больше.
Контрольный уровень можно определять одновременно с раковыми клетками, используя предварительно собранные и сохраненные образец(ы) от субъекта/субъектов, чей статус заболевания (злокачественное и доброкачественное) известен. Кроме того, в качестве нормального контроля можно использовать нормальные клетки, полученные из не-раковых участков органа, который имеет подлежащий лечению рак. Альтернативно, контрольный уровень может определить при помощи статистического способа на основании результатов, полученных путем анализа ранее определенного(ых) уровня(ней) экспрессии гена FOXM1 в образцах, полученных от субъектов, чей статус заболевания известен. Кроме того, контрольный уровень можно получать из базы данных примеров экспрессий в ранее проверенных клетках. Более того, в соответствии с аспектом данного изобретения, уровень экспрессии гена FOXM1 в биологическом образце можно сравнивать с несколькими контрольными уровнями, которые определяются из нескольких эталонных образцов. Предпочтительным является использование контрольного уровня, определенного по эталонному образцу, полученному из тканей того же типа, что биологический образец, полученный от субъект. Более того, предпочтительно использовать стандартное значение уровней экспрессии гена FOXM1 в популяции с известным статусом заболевания. Стандартное значение можно получить любым способом, известным в рассматриваемой области. Например, диапазон от среднее +/-2 С.О. до среднее +/-3 С.О. можно использовать в качестве стандартного значения.
В контексте настоящего изобретения, контрольный уровень, определенный по биологическому образцу, о котором известно, что он не является раковым, называется «нормальным контрольным уровнем». С другой стороны, если контрольный уровень определяется из ракового биологического образца, то он называется «раковым контрольным уровнем».
В случае, когда уровень экспрессии гена FOXM1 увеличен по сравнению с нормальным контрольным уровнем или сходен/эквивалентен раковому контрольному уровню, субъекту может быть диагностирован подлежащий лечению рак. Более конкретно, настоящее изобретение предоставляет способ (i) диагностики того, имеет ли субъект подлежащий лечению рак, и/или (ii) выбора субъекта для лечения рака, который включает стадии:
а) определение уровня экспрессии FOXM1 в раковых клетках или ткани(ях), полученные от субъекта, у которого подозревается рак, подлежащий лечению;
б) сравнение уровня экспрессии FOXM1 с нормальным контрольным уровнем;
c) диагностика субъекта, как имеющего подлежащий лечению рак, на предмет увеличения уровня экспрессии FOXM1 по сравнению с нормальным контрольным уровнем; и
d) выбор субъекта для лечения рака, если субъект диагностируется как имеющий подлежащий лечению рак, со стадии c).
Альтернативно, такой способ включает стадии:
а) определение уровня экспрессии FOXM1 в раковых клетках или ткани(ях), полученные от субъекта, у которого подозревается рак, подлежащий лечению;
б) сравнение уровня экспрессии FOXM1 с раковым контрольным уровнем;
c) диагностика субъекта, как имеющего подлежащий лечению рак, на предмет увеличения уровня экспрессии FOXM1 по сравнению с раковым контрольным уровнем; и
d) выбор субъекта для лечения рака, если субъект диагностируется как имеющий подлежащий лечению рак, со стадии c).
Настоящее изобретение также предоставляет комплект для определения субъекта, страдающего от рака, которого можно лечить полипептидами FOXM1 по настоящему изобретению, который также может быть полезен при оценке и/или мониторинге эффективности иммунотерапии рака. Предпочтительно, рак включает, в качестве неограничивающих примеров, AML, рак мочевого пузыря, рак молочной железы, рак шейки матки, холангиоцеллюлярный рак, CML, колоректальный рак, рак пищевода, рак желудка, рак желудка диффузного типа, рак печени, NSCLC, лимфому, остеосаркому, рак яичников, рак поджелудочной железы, рак предстательной железы, почечную карциному, мелкоклеточный рак легкого, опухоль мягких тканей и опухоль яичка. Конкретнее, комплект предпочтительно включает, по меньшей мере, один реактив для детектирования экспрессии гена FOXM1 в полученных от субъекта раковых клетках, который может быть выбран из группы:
(a) реактив для детектирования мРНК в гене FOXM1;
(b) реактив для детектирования белка FOXM1; и
(c) реактив для детектирования биологической активности белка FOXM1.
Подходящие реактивы для детектирования мРНК в гене FOXM1 включают нуклеиновые кислоты, которые специфически связываются с или идентифицируют мРНК FOXM1, такие как олигонуклеотиды, которые имеют последовательность, комплементарную части мРНК FOXM1. Эти виды олигонуклеотидов являются примером праймеров и зондов, которые являются специфическими для мРНК FOXM1. Эти виды олигонуклеотидов можно подготовить, основываясь на способах, известных в рассматриваемой области. Если необходимо, реактив для детектирования мРНК FOXM1 можно иммобилизовать на твердой матрице. Более того, в комплект может быть включен более, чем один реактив для детектирования мРНК FOXM1.
С другой стороны, подходящие реактивы для детектирования белка FOXM1 включают антитела к белку FOXM1. Антитело может являться моноклональным и поликлональным. Более того, можно использовать любой фрагмент или модификацию (например, химерное антитело, scFv, Fab, F(ab')2, Fv и т.д.) антитела в качестве реактива, при условии, что фрагмент или модифицированное антитело сохраняет способность связывания с белком FOXM1. Способы подготовки этих виды антител для детектирования белков известны в рассматриваемой области, и любой способ можно использовать по настоящему изобретению для подготовки таких антител и их эквивалентов. Кроме того, антитела могут быть мечены молекулами, генерирующими сигнал, при помощи непосредственного соединение или методик опосредованной маркировки. Метки и способы мечения антител и детектирования связывания со своими мишенями известны в рассматриваемой области, и для настоящего изобретения можно использовать любые метки и способы. Кроме того, в комплект может быть включен более, чем один реактив для детектирования белка FOXM1.
Комплект может содержать более чем один из вышеупомянутых реактивов. Например, образцы тканей, полученные от субъектов без рака, или страдающих или не страдающих от рака могут служить в качестве полезных контрольных реактивов. Комплект по настоящему изобретению может дополнительно включать другие материалы, желательные с коммерческой точки зрения и точки зрения потребителя, включая буферы, разбавители, фильтры, иглы, шприцы и вкладыши (например, напечатанные, кассета, CD-ROM и т.д.) с инструкцией по применению. Эти реактивы и подобные можно сохранять в контейнере с этикеткой. Соответствующие контейнеры включают бутылки, флаконы и пробирки. Контейнеры могут быть сформированы из различных материалов, таких как стекло или пластик.
В варианте осуществления настоящего изобретения в случае, когда реактивом является зонд против мРНК FOXM1, реактив может быть иммобилизован на твердой матрице, как, например, пористая полоска, для образования, по меньшей мере, одного участка детекции. Область измерения или детекции на пористой полоске может включать несколько участков, каждый из которых содержит нуклеиновую кислоту (зонд). Индикаторная полоска может также содержать участки для отрицательного и/или положительного контролей. Альтернативно, контрольный участок может быть расположен на полосе, отделенной от индикаторной полоски. Необязательно, различные участки детекции могут содержать разное количество иммобилизованных нуклеиновых кислот, то есть, большее количество на первом участке детекции и меньшие количества на последующих участках. При добавлении тестируемого образца ряд участков, отображающих детектируемый сигнала, обеспечивает количественную индикацию количества мРНК FOXM1, присутствующей в образце. Участки детекции можно скомпоновать в любой подходящей детектируемой форме и, как правило, они представлены в форме полосы или точки, перекрывающей в ширину индикаторную полоску.
Комплект по настоящему изобретению может дополнительно включать образец положительного контроля или стандартный образец FOXM1. Образец положительного контроля по настоящему изобретению можно подготовить путем сбора FOXM1-положительных образцов, а затем анализа в них уровней FOXM1. Альтернативно, очищенный белок FOXM1 или полинуклеотид можно добавлять к клеткам, которые не экспрессируют FOXM1, для образования положительного образца или образца FOXM1. В настоящем изобретении очищенный FOXM1 может являться рекомбинантный белок. Уровень FOXM1 в образце положительного контроля составляет, например, больше, чем малозначимая величина.
Следующие примеры приведены для иллюстрации настоящего изобретения и для помощи специалистам при его изготовлении и применении. Примеры в любом случае не предназначены для ограничения иным образом сферы применения данного изобретения.
Примеры
Материалы и способы
Клеточные линий
TISI, HLA-A*2402 положительная B-лимфобластоидная клеточная линия, была приобретена в Клеточном и генном банке IHWG (Сиэтл, WA). COS7, линия почечных клеток африканской зеленой мартышки, была приобретена в ATCC.
Селекция подходящих пептидов, полученных из FOXM1
9-мерные и 10-мерные пептиды, полученных из FOXM1, которые связываются с молекулой HLA-A*2402, были предсказаны с помощью программного обеспечения для предсказания связывания «BIMAS» (www-bimas.cit.nih.gov/molbio/hla_bind) (Parker etal.(J Immunol 1994, 152(1): 163-75), Kuzushima et al. (Blood 2001, 98(6): 1872-81)) и "NetMHC 3.0" (www.cbs.dtu.dk/services/NetMHC/) (Buus et al. (Tissue Antigens., 62:378-84, 2003), Nielsen et al. (Protein Sci., 12:1007-17, 2003, Bioinformatics, 20(9): 1388-97, 2004)). Эти пептиды были синтезированы Biosynthesis (Льюисвилл, штат Техас) в соответствии со стандартным способом твердофазного синтеза и очищены при помощи обратнофазной высокоэффективной жидкостной хроматографии (ВЭЖХ). Чистоту (>90%) и идентичность пептидов определяли путем аналитической ВЭЖХ и масс-спектрометрического анализа, соответственно. Пептиды растворяли в диметилсульфоксиде до 20 мг/мл и хранили при -80 градусах С.
Индукция ЦТЛ in vitro
Полученные на основе моноцитов дендритные клетки (ДК) были использованы в качестве антигенпредставляющих клеток для индуцирования ответов цитотоксических Т-лимфоцитов (ЦТЛ) в отношении пептидов, представленных на лейкоцитарном антигене человека (HLA). ДК были образованы в экспериментах in vitro, как описано в другом месте (Nakahara S et al., Cancer Res 2003 JuI 15, 63(14): 4112-8). В конкретном плане, мононуклеарные клетки периферической крови (PBMC), полученные от нормальных добровольцев (HLA-A*2402 положительные) при помощи раствора Ficoll-Plaque (Pharmacia), разделяли при помощи адгезии по пластиковым чашкам Петри (Becton Dickinson) с тем, чтобы обогатить их как фракцию моноцитов. Обогащенную моноцитами популяцию культивировали в присутствии 1000 ед./мл гранулоцит-макрофаг колониестимулирующего фактора (R&D Системы) и 1000 ед./мл интерлейкина (IL)-4 (R&D System) в среде AIM-V (Invitrogen), содержащей 2% инактивированной теплом аутологичной сыворотки крови (AS). После 7 дней культивирования цитокин-индуцированные ДК были подвергнуты импульсному взаимодействию с 20 мкг/мл каждого из синтезированных пептидов в присутствии 3 мкг/мл бета2-микроглобулина в течение 3 часов при 37 градусов C в среде AIM-V. Оказалось, что образованные клетки экспрессировали DC-специфические молекулы, такие как CD80, CD83, CD86 и HLA II класса, на своей клеточной поверхности (данные не представлены). Эти подвергнутые импульсному пептидному воздействию ДК затем инактивировали облучением рентгеновскими лучами (20 Гр) и смешивали в соотношении 1:20 с аутологичными CD8+ Т-клетками, полученными путем положительной селекции с использованием CD8 Positive Isolation Kit (Dynal). Эти культуры вносили в 48-луночный планшет (Corning); каждая лунка содержала 1,5×104 подвергнутых импульсному пептидному воздействию ДК, 3×105 CD8+ Т-клеток и 10 нг/мл IL-7 (R&D System) в 0,5 мл среды AIM-V/2% AS. Три дня спустя в эти культуры добавляли IL-2 (CHIRON) до конечной концентрации 20 МЕ/мл. На 7 и 14 день Т-клетки дополнительно стимулировали с помощью аутологичных подвергнутых импульсному пептидному воздействию ДК. ДК каждый раз подготавливали тем же способом, что описан выше. ЦТЛ тестировали против подвергнутых импульсному пептидному воздействию клеток TISI после 3-го раунда пептидной стимуляции на 21 день. (Tanaka H et al., Br J Cancer 2001 Jan 5, 84(1): 94-9; Umano Y et al., Br J Cancer 2001 Apr 20, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9).
Методика размножения ЦТЛ
ЦТЛ размножали в культуре при помощи способа, аналогичного описанному (Walter EA et al., N Engl J Med 1995 Oct 19, 333(16): 1038-44; Riddell SR et al., Nat Med 1996 Feb, 2(2): 216-23). Всего 5×104 ЦТЛ суспендировали в 25 мл среды AIM-V/5% AS с 2 видами B-лимфобластоидных клеточных линий человека, инактивированных митомицином С, в присутствии 40 нг/мл моноклонального антитела анти-CD3 (Pharmingen). Через один день после начала культивирований к культуре добавляли 120 МЕ/мл IL-2. Культуры подпитывали свежей средой AIM-V/5% AS, содержащей 30 МЕ/мл IL-2, на 5, 8 и 11 день. (Tanaka H et al., Br J Cancer 2001 Jan 5, 84(1): 94-9; Umano Y et al., Br J Cancer 2001 Apr 20, 84(8): 1052-7; Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9).
Образование клонов ЦТЛ
В 96-луночном планшете для микротитрования с круглодонными лунками (Nalge Nunc International) были сделаны разведения для получения 0,3, 1, и 3 ЦТЛ/лунку. ЦТЛ культивировали с 2 видами B-лимфобластоидных клеточных линий человека (1×104 клеток/лунку), 30 нг/мл антитела анти-CD3 и 125 ед/мл IL-2 в 150 мкл/лунку среды AIM-V, содержащей 5% AS. К среде через 10 дней добавляли 50 мкл/лунку IL-2, чтобы достичь конечной концентрации 125 ед/мл IL-2. Активность ЦТЛ проверяли на 14-й день и клоны ЦТЛ размножали, используя тот же способ, что и описанный выше (Uchida N et al., Clin Cancer Res 2004 Dec 15, 10(24): 8577-86; Suda T et al., Cancer Sci 2006 May, 97(5): 411-9; Watanabe T et al., Cancer Sci 2005 Aug, 96(8): 498-506).
Специфическая активность ЦТЛ
Для исследования специфической активности ЦТЛ проводили интерферон(IFN)-гамма иммуноферментный спот-анализ (ELISPOT) и IFN-гамма иммуноферментный твердофазный анализ (ИФА). В конкретном плане, подвергнутых импульсному пептидному воздействию TISI (1×104 клеток/лунку) подготавливали в качестве клеток-стимуляторов. Культивируемые в 48 лунках клетки использовали в качестве иммунокомпетентных клеток. IFN-гамма ELISPOT-анализ и IFN-гамма ИФА-анализа выполняли в рамках процедуры изготовления.
Трансфекция плазмидами
кДНК, кодирующая открытую рамку считывания генов-мишеней или HLA-A*2402, амплифицировали при помощи ПЦР. ПЦР-амплифицированные продукты клонировали в вектор pCAGGS. Плазмиды трансфицировали в COS7, которая является отрицательной по генам-мишеням и HLA-А24 линией клеток, используя липофектамин 2000 (Invitrogen) в соответствии с рекомендациями изготовителя. Через 2 дня после трансфекции трансфицированные клетки собирали при помощи ЭДТК (Invitrogen) и использовали в качестве клеток-мишеней (5×104 клеток/лунку) для анализа активности ЦТЛ.
Результаты
Предсказание HLA-А24-связывающихся пептидов, полученных из FOXM1
Таблицы 1a и 1b демонстрируют HLA-А24-связывающиеся 9-мерные и 10-мерные пептиды FOXM1 в порядке высокой аффинности связывания. 29 пептидов (SEQ ID NO: 1-12 и SEQ ID NO: 15-31) были предсказаны BIMAS и 3 пептида (SEQ ID NO: 13-14 и SEQ ID NO: 32) были предсказаны NetMHC 3.0. В общей сложности были отобраны и изучены 32 пептида с потенциальной способностью связываться с HLA-А24 для того, чтобы определить эпитопные пептиды.
Начальная позиция указывает номер аминокислотного остатка от N-конца FOXM1
Балльная оценка связывания и константа диссоциации [Kd (нМ)], полученные от «BIMAS» и «NetMHC 3.0».
Индукция ЦТЛ предсказанными пептидами из FOXM1, рестриктированными по HLA-A*2402, и образование линий ЦТЛ, стимулированных пептидами, полученными из FOXM1.
ЦТЛ для пептидов, полученных из FOXM1, образовывали в соответствии с протоколами, как описано в разделе «Материалы и Способы». Специфическую ЦТЛ-активность пептидов определяли интерферон-гамма ELISPOT-анализом (Фигуры 1a-g). Он показал, что лунки с номерами #1, #4 и #7, стимулированными FOXM1-А24-9-262(SEQ ID NO: 2) (a), #7 - FOXM1-А24-9-351(SEQ ID NO: 7) (b), #5 - FOXM1-А24-9-57(SEQ ID NO: 8) (c), #3 - FOXM1-А24-10-240(SEQ ID NO: 16) (d), #6 - FOXM1-А24-10-318(SEQID NO: 25) (e), #4 - FOXM1-А24-10-390(SEQ ID NO: 30) (f) и #5 - FOXM1-А24-10-238(SEQ ID NO:31) (g) продемонстрировали сильное продуцирование интерферона-гамма по сравнению с контрольными лунками. С другой стороны, не было обнаружено сильного продуцирования интерферона-гамма при индуцировании другими пептидами, показанными в Таблицах 1a и 1b, несмотря на то, что эти пептиды обладали возможной активностью связывания с HLA-A*2402. Например, типично отрицательными являются данные по ЦТЛ-ответу, стимулированному FOXM1-А24-9-316(SEQ ID NO: 1) в отношении подвергнутых импульсному пептидному воздействию клеток-мишеней (h). В результате, он показал, что 7 пептидов, полученных из FOXM1, были отобраны в качестве пептидов, которые могли сильно индуцировать ЦТЛ.
Создание линий и клонов ЦТЛ против пептидов, полученных из FOXM1
Клетки, которые продемонстрировали пептид-специфическую ЦТЛ-активность, обнаруженную при помощи интерферон-гамма ELISPOT-анализа в лунках с номерами #4 - с FOXM1-А24-9-262(SEQ ID NO: 2) (a), #3 - с FOXM1-А24-10-240(SEQ ID NO: 16) (b), #6 - с FOXM1-А24-10-318(SEQ ID NO: 25) (c) и #5 - с FOXM 1-А24-10-238(SEQ ID NO: 31) (d), размножали и образовывали линии ЦТЛ. ЦТЛ-активности этих линий ЦТЛ определяли интерферон-гамма ИФА-анализом (Фиг.2а-d). Он показал, что все линии ЦТЛ продемонстрировали сильное продуцирование интерферона-гамма в отношении клеток-мишеней, подвергнутых импульсному воздействию соответствующим пептидом, по сравнению с клетками-мишенями без импульсного пептидного воздействия. Более того, клоны ЦТЛ были образованы путем ограничивающих разведений из линий ЦТЛ, и продуцирование IFN-гамма клонами ЦТЛ против клеток-мишеней, подвергнутых импульсному пептидному воздействию, определяли при помощи интерферон-гамма ИФА-анализа. Сильное продуцирование интерферона-гамма было выявлено у клонов ЦТЛ, стимулированных FOXM1-А24-9-262(SEQ ID NO: 2) (a), FOXM1-А24-10-240(SEQ ID NO: 16) (b) и FOXM1-А24-10-238(SEQ ID NO: 31) (c) на Фиг.3.
Специфическая ЦТЛ-активность в отношении клеток-мишеней, экзогенно экспрессирующих FOXM1 и HLA-A*2402
Образованные линии и клоны ЦТЛ, образованные в отношении этих пептидов, были исследованы на их способность распознавать клетки-мишени, которые эндогенно экспрессируют гены FOXM1 и HLA- A*2402. Специфическую ЦТЛ-активность против клеток COS7, трансфицированных как полноразмерным геном FOXM1, так и геном HLA-A*2402 (специфическая модель для клеток-мишеней, которые экзогенно экспрессируют гены FOXM1 и HLA-A*2402) проверяли при помощи линий и клонов ЦТЛ, образованных соответствующим пептидом, в качестве эффекторных клеток. Клетки COS7, трансфицированные либо полноразмерным геном FOXM1, либо HLA-A*2402, были подготовлены в качестве контроля. На Фиг.4, ЦТЛ, стимулированные с FOXM1-А24-9-262(SEQ ID NO: 2), показали сильную ЦТЛ-активность против клеток COS7, экспрессирующих как FOXM1, так и HLA-A*2402. С другой стороны, никакой значительной специфической ЦТЛ-активности в отношении контроля не наблюдалось. Таким образом, эти данные четко показали, что пептид FOXM1-А24-9-262(SEQ ID NO: 2) эндогенно процессировался и экспрессировался на клетках-мишенях с молекулами HLA-A*2402 и узнавался ЦТЛ. Эти результаты свидетельствуют, что этот пептид, полученный из FOXM1, может быть полезным при применении противораковых вакцин для больных с опухолями, экспрессирующими FOXM1.
Анализ гомологий антигенных пептидов
ЦТЛ, стимулированные FOXM1-A24-9-262 (SEQ ID NO: 2), FOXM1-A24-9-351 (SEQ ID NO: 7), FOXM1-A24-9-57 (SEQ ID NO: 8), FOXM1-A24-10-240 (SEQ ID NO: 16), FOXM1-A24-10-318 (SEQ ID NO: 25), FOXM1-A24-10-390 (SEQ ID NO: 30) и FOXM1-A24-10-238 (SEQ ID NO: 31) продемонстрировали значительную и специфическую ЦТЛ-активность. Этот результат может быть связан с тем, что последовательности FOXM1-A24-9-262 (SEQ ID NO: 2), FOXM1-A24-9-351 (SEQ ID NO: 7), FOXM1-A24-9-57 (SEQ ID NO: 8), FOXM1-A24-10-240 (SEQ ID NO: 16) FOXM1-A24-10-318 (SEQ ID NO: 25) FOXM1-A24-10-390 (SEQ ID NO: 30) и FOXM1-A24-10-238 (SEQ ID NO: 31) гомологичны пептидам, полученным из других молекул, которые, как известно, повышают чувствительность иммунной системы человека. Чтобы исключить такую возможность, для этих пептидных последовательностей были проведены анализы гомологий, используя в качестве запросов алгоритм BLAST (www.ncbi.nlm.nih.gov/blast/blast.cgi), который не выявил никаких последовательностей со значительной гомологией. Результаты анализов гомологий показывает, что последовательности FOXM1-A24-9-262 (SEQ ID NO: 2), FOXM1-A24-9-351 (SEQ ID NO: 7), FOXM1-A24-9-57 (SEQ ID NO: 8), FOXM1-A24-10-240 (SEQ ID NO: 16) FOXM1-A24-10-318 (SEQ ID NO: 25) FOXM1-A24-10-390 (SEQ ID NO: 30) и FOXM1-A24-10-238 (SEQ ID NO: 31) являются уникальными и, таким образом, существует небольшая возможность того, что, по нашим представлениям, эти молекулы повышают непредусмотренный иммунологический ответа на некоторые посторонние молекулы.
В заключение, были идентифицированы новые HLA-А24 эпитопные пептиды, полученных из FOXM1. Более того, было продемонстрировано, что эпитопный пептид из FOXM1 может применяться для иммунотерапии рака.
Применяемость в производственных условиях
Настоящее изобретение представляет новые ОСА, особенно те, которые получены из FOXM1, которые индуцировают сильные и специфические противоопухолевые иммунные ответы и имеют применимость для широкого спектра типов рака. Такие ОСА полезны в качестве пептидных вакцин против заболеваний, связанных с FOXM1, например, рака, в частности, AML, рака мочевого пузыря, рака молочной железы, рака шейки матки, холангиоцеллюлярного рака, CML, колоректального рака, рака пищевода, рака желудка, рака желудка диффузного типа, рака печени, NSCLC, лимфомы, остеосаркомы, рака яичников, рака поджелудочной железы, рака предстательной железы, почечной карциномы, мелкоклеточного рака легкого, опухоли мягких тканей и опухоли яичка.
Несмотря на то что настоящее изобретение описано здесь подробно и с учетом конкретных вариантов его осуществления, следует понимать, что вышеприведенное описание носит примерный и разъяснительный характер и предназначено для иллюстрации настоящего изобретения и его предпочтительных вариантов осуществления. Путем проведения экспериментов любой специалист в рассматриваемой области без труда признает, что различные изменения и модификация могут быть сделаны в этом без отступления от сущности и области применения настоящего изобретения, объем и границы которого определены в прилагаемых пунктах формулы изобретения.
Claims (11)
1. Выделенный пептид, обладающий способностью индуцировать цитотоксические Т-лимфоциты (ЦТЛ) в присутствии антигенпредставляющих клеток (АПК), несущих HLA-A*2402, где пептид выбран из группы, состоящей из:
(a) выделенного пептида, который состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31,
(b) выделенного пептида, который состоит из аминокислотной последовательности SEQ ID NO: 2, 7, 8, 16, 25, 30 или 31, в которой вторая аминокислота от N-конца, выбранная из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, замещена аминокислотой, выбранной из группы фенилаланина, тирозина, метионина и триптофана, и/или С-концевая аминокислота, выбранная из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, замещена аминокислотой, выбранной из группы фенилаланина, лейцина, изолейцина и триптофана.
(a) выделенного пептида, который состоит из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31,
(b) выделенного пептида, который состоит из аминокислотной последовательности SEQ ID NO: 2, 7, 8, 16, 25, 30 или 31, в которой вторая аминокислота от N-конца, выбранная из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, замещена аминокислотой, выбранной из группы фенилаланина, тирозина, метионина и триптофана, и/или С-концевая аминокислота, выбранная из группы, состоящей из SEQ ID NO: 2, 7, 8, 16, 25, 30 и 31, замещена аминокислотой, выбранной из группы фенилаланина, лейцина, изолейцина и триптофана.
2. Выделенный пептид по п.1, который представляет собой нонапептид или декапептид.
3. Выделенный полинуклеотид, кодирующий пептид по п.1 или 2.
4. Композиция для индуцирования ЦТЛ, где композиция содержит в качестве активного ингредиента один или несколько пептидов по п.1 или 2 в подходящей дозе, где указанная композиция составлена для введения субъекту, у которого HLA-антиген представляет собой HLA-A*2402.
5. Фармацевтическая композиция для лечения и/или профилактики рака, экспрессирующего FOXM1, и/или предупреждения его послеоперационных рецидивов, где композиция содержит в качестве активного ингредиента один или несколько пептидов по п.1 или 2 в подходящей дозе, где указанная фармацевтическая композиция составлена для введения субъекту, у которого HLA-антиген представляет собой HLA-A*2402.
6. Фармацевтическая композиция по п.5, которая составлена для лечения рака.
7. Способ индуцирования антигенпредставляющих клеток (АПК) со способностью индуцировать ЦТЛ, включающий одну из следующих стадий:
(a) контактирование АПК, несущих HLA-A*2402, с пептидом по п.1 или 2 in vitro, ex vivo или in vivo; и
(b) введение полинуклеотида, кодирующего пептид по п.1 или 2 в экспрессируемой форме, в АПК, несущую HLA-A*2402.
(a) контактирование АПК, несущих HLA-A*2402, с пептидом по п.1 или 2 in vitro, ex vivo или in vivo; и
(b) введение полинуклеотида, кодирующего пептид по п.1 или 2 в экспрессируемой форме, в АПК, несущую HLA-A*2402.
8. Способ индуцирования ЦТЛ при помощи любого из способов, включающих, по меньшей мере, одну из следующих стадий:
(a) совместное культивирование CD8-положительных Т-клеток с АПК, которые представляют на своей поверхности комплекс HLA-А*2402 и пептида по п.1 или 2;
(b) совместное культивирование CD8-положительных Т-клеток с экзосомами, которые представляют на своей поверхности комплекс HLA-A*2402 и пептида по п.1 или 2.
(a) совместное культивирование CD8-положительных Т-клеток с АПК, которые представляют на своей поверхности комплекс HLA-А*2402 и пептида по п.1 или 2;
(b) совместное культивирование CD8-положительных Т-клеток с экзосомами, которые представляют на своей поверхности комплекс HLA-A*2402 и пептида по п.1 или 2.
9. Выделенная АПК со способностью индуцировать ЦТЛ, которая представляет на своей поверхности комплекс HLA-A*2402 и пептид по п.1 или 2.
10. АПК по п.9, которая индуцирована способом по п.7.
11. Способ индуцирования иммунного ответа против рака, экспрессирующего FOXM1, у субъекта, у которого HLA-антиген представляет собой HLA-A*2402, где указанный способ включает стадию введения субъекту композиции, содержащей пептид по п.1 или 2.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15340809P | 2009-02-18 | 2009-02-18 | |
| US61/153,408 | 2009-02-18 | ||
| PCT/JP2010/001005 WO2010095428A1 (en) | 2009-02-18 | 2010-02-17 | Foxm1 peptides and vaccines containing the same |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2011138160A RU2011138160A (ru) | 2013-03-27 |
| RU2560431C2 true RU2560431C2 (ru) | 2015-08-20 |
Family
ID=42633716
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2011138160/10A RU2560431C2 (ru) | 2009-02-18 | 2010-02-17 | Пептиды foxm1 и вакцины, содержащие их |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US8617562B2 (ru) |
| EP (1) | EP2408912B1 (ru) |
| JP (1) | JP5728717B2 (ru) |
| KR (1) | KR101713586B1 (ru) |
| CN (1) | CN102405285B (ru) |
| BR (1) | BRPI1008887A2 (ru) |
| CA (1) | CA2752560C (ru) |
| DK (1) | DK2408912T3 (ru) |
| ES (1) | ES2618896T3 (ru) |
| IL (1) | IL214435A0 (ru) |
| MX (1) | MX2011008763A (ru) |
| RU (1) | RU2560431C2 (ru) |
| SG (1) | SG173751A1 (ru) |
| TW (1) | TWI469791B (ru) |
| WO (1) | WO2010095428A1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12195559B2 (en) | 2018-08-02 | 2025-01-14 | Oncotherapy Science, Inc. | CDCA1-derived peptide and vaccine containing same |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2696597C (en) | 2007-08-20 | 2017-05-16 | Oncotherapy Science, Inc. | Foxm1 peptide and medicinal agent comprising the same |
| US20150359864A1 (en) * | 2012-03-09 | 2015-12-17 | Oncotherapy Science, Inc. | Pharmaceutical composition containing peptides |
| GB201410686D0 (en) * | 2014-06-16 | 2014-07-30 | Immunocore Ltd & Adaptimmune Ltd | Peptides |
| SG10201913659SA (en) * | 2015-10-08 | 2020-03-30 | Oncotherapy Science Inc | Foxm1-derived peptide, and vaccine including same |
| CN105524159B (zh) * | 2015-11-16 | 2021-04-09 | 西南交通大学 | 具有癌细胞选择性杀伤和迁移抑制作用的多肽分子与用途 |
| CN105999227B (zh) * | 2016-08-12 | 2019-08-06 | 湖南大学 | FOXM1蛋白氮端(1-234 aa)的表达及其用途 |
| EP3522909A4 (en) | 2016-10-07 | 2020-07-08 | Board of Regents, The University of Texas System | HLA RESTRICTED VGLL1 PEPTIDES AND THEIR USE |
| JP7260553B2 (ja) * | 2017-10-06 | 2023-04-18 | ザ・ユニバーシティ・オブ・シカゴ | がん特異的抗原に対するtリンパ球のスクリーニング |
| CN109055327B (zh) * | 2018-07-23 | 2021-04-06 | 浙江工业大学 | 醛酮还原酶突变体及其应用 |
| CN114591400B (zh) * | 2022-03-29 | 2022-10-21 | 西南交通大学 | 一组靶向FoxM1-DBD多肽及其应用 |
Family Cites Families (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4722848A (en) | 1982-12-08 | 1988-02-02 | Health Research, Incorporated | Method for immunizing animals with synthetically modified vaccinia virus |
| US5703055A (en) | 1989-03-21 | 1997-12-30 | Wisconsin Alumni Research Foundation | Generation of antibodies through lipid mediated DNA delivery |
| US5804566A (en) | 1993-08-26 | 1998-09-08 | The Regents Of The University Of California | Methods and devices for immunizing a host through administration of naked polynucleotides with encode allergenic peptides |
| US5679647A (en) | 1993-08-26 | 1997-10-21 | The Regents Of The University Of California | Methods and devices for immunizing a host against tumor-associated antigens through administration of naked polynucleotides which encode tumor-associated antigenic peptides |
| US5739118A (en) | 1994-04-01 | 1998-04-14 | Apollon, Inc. | Compositions and methods for delivery of genetic material |
| US5736524A (en) | 1994-11-14 | 1998-04-07 | Merck & Co.,. Inc. | Polynucleotide tuberculosis vaccine |
| US5922687A (en) | 1995-05-04 | 1999-07-13 | Board Of Trustees Of The Leland Stanford Junior University | Intracellular delivery of nucleic acids using pressure |
| US20030198642A1 (en) | 1995-08-03 | 2003-10-23 | Johannes J. Geuze | Cell derived antigen presenting vesicles |
| US5853719A (en) | 1996-04-30 | 1998-12-29 | Duke University | Methods for treating cancers and pathogen infections using antigen-presenting cells loaded with RNA |
| CA2262006A1 (en) | 1996-07-26 | 1998-02-05 | Sloan-Kettering Institute For Cancer Research | Method and reagents for genetic immunization |
| US5861278A (en) | 1996-11-01 | 1999-01-19 | Genetics Institute, Inc. | HNF3δ compositions |
| EP0846761A1 (en) | 1996-12-09 | 1998-06-10 | Introgene B.V. | A novel transcription factor expressed in cycling cells, nucleic acid molecules encoding said transcription factor and its promoter region and uses thereof |
| FR2766205B1 (fr) | 1997-07-16 | 2002-08-30 | Inst Nat Sante Rech Med | Nouveau procede de sensibilisation de cellules presentatrices d'antigene et nouveaux moyens pour la mise en oeuvre du procede |
| US6747137B1 (en) | 1998-02-13 | 2004-06-08 | Genome Therapeutics Corporation | Nucleic acid sequences relating to Candida albicans for diagnostics and therapeutics |
| ES2294844T3 (es) | 1998-06-25 | 2008-04-01 | Green Peptide Co., Ltd. | Peptidos antigenicos tumorales derivados de ciclofilina b. |
| US20030235557A1 (en) | 1998-09-30 | 2003-12-25 | Corixa Corporation | Compositions and methods for WT1 specific immunotherapy |
| AU2002305858B2 (en) | 2001-06-04 | 2007-08-23 | Basf Plant Science Gmbh | Sugar and lipid metabolism regulators in plants II |
| US20040142325A1 (en) | 2001-09-14 | 2004-07-22 | Liat Mintz | Methods and systems for annotating biomolecular sequences |
| CA2469274A1 (en) | 2001-12-10 | 2003-06-19 | Kyogo Itoh | Tumor antigens |
| WO2004019761A2 (en) * | 2002-08-28 | 2004-03-11 | The Board Of Trustees Of The University Of Illinois | Methods of treating age-related defects and diseases |
| JP4679149B2 (ja) | 2002-09-30 | 2011-04-27 | オンコセラピー・サイエンス株式会社 | ヒト膵癌に関連する遺伝子およびポリペプチド |
| US20050260639A1 (en) | 2002-09-30 | 2005-11-24 | Oncotherapy Science, Inc. | Method for diagnosing pancreatic cancer |
| TW200413725A (en) | 2002-09-30 | 2004-08-01 | Oncotherapy Science Inc | Method for diagnosing non-small cell lung cancers |
| US20060024692A1 (en) | 2002-09-30 | 2006-02-02 | Oncotherapy Science, Inc. | Method for diagnosing non-small cell lung cancers |
| US7635673B2 (en) | 2003-03-25 | 2009-12-22 | The Board Of Trustees Of The University Of Illinois | Methods of inhibiting tumor cell proliferation |
| JP4579246B2 (ja) | 2003-09-24 | 2010-11-10 | オンコセラピー・サイエンス株式会社 | 乳癌を診断する方法 |
| DK1697399T3 (en) | 2003-12-12 | 2017-03-06 | Government Of The United States Of America As Repr By The Secr Of The Dept Of Health And Human Servi | Human cytotoxic t lymphocyte epitope and its agonist epitope from the non-variable number of muc-1 tandem repeat sequences |
| EP1747284A4 (en) | 2004-02-06 | 2009-03-11 | Wyeth Corp | DIAGNOSTICS AND THERAPEUTICS OF CANCER |
| EP1737979B9 (en) | 2004-03-23 | 2011-09-21 | Oncotherapy Science, Inc. | Method for diagnosing non-small cell lung cancer |
| JP2007530921A (ja) | 2004-03-24 | 2007-11-01 | オンコセラピー・サイエンス株式会社 | 非小細胞肺癌に対する腫瘍マーカーおよび治療標的としてのadam8 |
| US7915036B2 (en) | 2004-09-13 | 2011-03-29 | The United States Of America As Represented By The Secretary, Department Of Health And Human Services | Compositions comprising T cell receptors and methods of use thereof |
| JP2006141208A (ja) | 2004-11-16 | 2006-06-08 | Univ Of Tokushima | 多発性骨髄腫、白血病、悪性リンパ腫、肺癌等の免疫療法剤 |
| WO2006085684A2 (en) | 2005-02-10 | 2006-08-17 | Oncotherapy Science, Inc. | Method of diagnosing bladder cancer |
| EP2295602B1 (en) | 2005-07-27 | 2012-07-11 | Oncotherapy Science, Inc. | Method of prognosing cancers |
| CN101283106A (zh) | 2005-07-27 | 2008-10-08 | 肿瘤疗法科学股份有限公司 | 小细胞肺癌的诊断方法 |
| EP1930433B1 (en) | 2005-09-13 | 2016-03-16 | Mie University | T-cell receptor and nucleic acid encoding the receptor |
| EP1806413A1 (en) * | 2006-01-06 | 2007-07-11 | Oligene GmbH | An in-vitro-method and means for determination of different tumor types and predicting success of surgical procedures in ovarian cancer |
| EP2018440A1 (en) | 2006-04-20 | 2009-01-28 | Oncotherapy Science, Inc. | NMU-GHSR1b/NTSR1 ONCOGENIC SIGNALING PATHWAY AS A THERAPEUTIC TARGET FOR LUNG CANCER |
| CA2696701C (en) | 2007-08-20 | 2017-01-24 | Oncotherapy Science, Inc. | Cdca1 peptide and pharmaceutical agent comprising the same |
| CA2696597C (en) | 2007-08-20 | 2017-05-16 | Oncotherapy Science, Inc. | Foxm1 peptide and medicinal agent comprising the same |
| CN105601725B (zh) | 2009-03-18 | 2019-08-09 | 肿瘤疗法科学股份有限公司 | Neil3肽及包含它的疫苗 |
-
2010
- 2010-02-11 TW TW99104319A patent/TWI469791B/zh not_active IP Right Cessation
- 2010-02-17 EP EP10743558.8A patent/EP2408912B1/en active Active
- 2010-02-17 ES ES10743558.8T patent/ES2618896T3/es active Active
- 2010-02-17 DK DK10743558.8T patent/DK2408912T3/en active
- 2010-02-17 MX MX2011008763A patent/MX2011008763A/es active IP Right Grant
- 2010-02-17 BR BRPI1008887A patent/BRPI1008887A2/pt not_active IP Right Cessation
- 2010-02-17 CA CA2752560A patent/CA2752560C/en not_active Expired - Fee Related
- 2010-02-17 KR KR1020117021513A patent/KR101713586B1/ko active IP Right Grant
- 2010-02-17 US US13/202,078 patent/US8617562B2/en active Active
- 2010-02-17 JP JP2011535341A patent/JP5728717B2/ja active Active
- 2010-02-17 SG SG2011059441A patent/SG173751A1/en unknown
- 2010-02-17 CN CN201080017145.2A patent/CN102405285B/zh active Active
- 2010-02-17 RU RU2011138160/10A patent/RU2560431C2/ru not_active IP Right Cessation
- 2010-02-17 WO PCT/JP2010/001005 patent/WO2010095428A1/en active Application Filing
-
2011
- 2011-08-03 IL IL214435A patent/IL214435A0/en unknown
Non-Patent Citations (1)
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US12195559B2 (en) | 2018-08-02 | 2025-01-14 | Oncotherapy Science, Inc. | CDCA1-derived peptide and vaccine containing same |
Also Published As
| Publication number | Publication date |
|---|---|
| ES2618896T3 (es) | 2017-06-22 |
| BRPI1008887A2 (pt) | 2016-03-01 |
| TW201032821A (en) | 2010-09-16 |
| JP5728717B2 (ja) | 2015-06-03 |
| CN102405285A (zh) | 2012-04-04 |
| IL214435A0 (en) | 2011-09-27 |
| WO2010095428A1 (en) | 2010-08-26 |
| JP2012517799A (ja) | 2012-08-09 |
| CA2752560C (en) | 2017-01-24 |
| SG173751A1 (en) | 2011-09-29 |
| CN102405285B (zh) | 2015-04-22 |
| KR101713586B1 (ko) | 2017-03-08 |
| TWI469791B (zh) | 2015-01-21 |
| EP2408912A4 (en) | 2013-04-17 |
| DK2408912T3 (en) | 2017-03-20 |
| CA2752560A1 (en) | 2010-08-26 |
| EP2408912A1 (en) | 2012-01-25 |
| RU2011138160A (ru) | 2013-03-27 |
| KR20110117241A (ko) | 2011-10-26 |
| US20120156231A1 (en) | 2012-06-21 |
| EP2408912B1 (en) | 2017-01-18 |
| MX2011008763A (es) | 2011-09-09 |
| AU2010216980A1 (en) | 2011-08-25 |
| US8617562B2 (en) | 2013-12-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2560431C2 (ru) | Пептиды foxm1 и вакцины, содержащие их | |
| RU2550695C2 (ru) | Олигопептиды imp-3 и содержащие их вакцины | |
| JP5564730B2 (ja) | Mphosph1ペプチドおよびそれを含むワクチン | |
| US20140199335A1 (en) | C1orf59 peptides and vaccines including the same | |
| US9745343B2 (en) | Method of inducing an immune response by administering WDRPUH epitope peptides | |
| WO2010070877A1 (en) | Elovl7 epitope peptides and vaccines containing the same | |
| AU2010216980B2 (en) | FOXM1 peptides and vaccines containing the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20180218 |