RU2485940C2 - Композиция, содержащая полиненасыщенные жирные кислоты и активированный уголь - Google Patents
Композиция, содержащая полиненасыщенные жирные кислоты и активированный уголь Download PDFInfo
- Publication number
- RU2485940C2 RU2485940C2 RU2010121714/15A RU2010121714A RU2485940C2 RU 2485940 C2 RU2485940 C2 RU 2485940C2 RU 2010121714/15 A RU2010121714/15 A RU 2010121714/15A RU 2010121714 A RU2010121714 A RU 2010121714A RU 2485940 C2 RU2485940 C2 RU 2485940C2
- Authority
- RU
- Russia
- Prior art keywords
- composition according
- oral composition
- fish oil
- activated carbon
- tablet
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2072—Pills, tablets, discs, rods characterised by shape, structure or size; Tablets with holes, special break lines or identification marks; Partially coated tablets; Disintegrating flat shaped forms
- A61K9/2086—Layered tablets, e.g. bilayer tablets; Tablets of the type inert core-active coat
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/201—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids having one or two double bonds, e.g. oleic, linoleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/20—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids
- A61K31/202—Carboxylic acids, e.g. valproic acid having a carboxyl group bound to a chain of seven or more carbon atoms, e.g. stearic, palmitic, arachidic acids having three or more double bonds, e.g. linolenic
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
- A61K31/23—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin of acids having a carboxyl group bound to a chain of seven or more carbon atoms
- A61K31/232—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin of acids having a carboxyl group bound to a chain of seven or more carbon atoms having three or more double bonds, e.g. etretinate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/44—Elemental carbon, e.g. charcoal, carbon black
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Emergency Medicine (AREA)
- Hematology (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Obesity (AREA)
- Diabetes (AREA)
- Coloring Foods And Improving Nutritive Qualities (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Изобретение относится к медицине и фармакологии и представляет собой пероральную композицию для регулирования уровня липидов в крови, предотвращения или снижения риска развития атеросклеротических изменений, расстройств или заболеваний, содержащую рыбий жир или перилловое масло и активированный уголь. Изобретение обеспечивает предотвращение неприятного рыбного запаха. 11 з.п. ф-лы, 3 пр., 1 ил.
Description
Настоящее изобретение относится к пероральной композиции, не имеющей неприятного аромата, запаха или вкуса, содержащей полиненасыщенные жирные кислоты (ПНЖК), а также активированный уголь, способу ее получения и ее применению в качестве пищевой добавки или в качестве биологически активной добавки для регулирования уровня липидов в крови, предотвращения или снижения риска развития атеросклеротических изменений, расстройств или заболеваний.
Полиненасыщенные жирные кислоты (ПНЖК) являются активными компонентами, например в рыбьем жире, и отвечают за показательно низкие уровни липидов в крови и низкий уровень заболеваемости гипертонией, что было показано в эпидемиологическом исследовании у инуитов (М.Н.Davidson, P.R.Liebson, Cardiovascular Reviews&Reports 1986, 7, 461-472). В частности, концентрация в крови холестерина липопротеинов низкой плотности (ЛПНП) уменьшается, а аналогичный показатель для холестерина липопротеинов высокой плотности (ЛПВП) увеличивается. Ишемическая болезнь сердца (ИБС) является основной причиной смертности в западных странах, и высокие уровни холестерина в плазме, а точнее соотношение ЛПНП/ЛПВП, в значительной мере связаны с риском ИБС (Willett and Sacks, N.Eng. J. Med. 1991, 121, 324).
ПНЖХ, обнаруженные в рыбьем жире, имеют углеродные цепи, содержащие 18, 20 или 22 атома, и могут быть разделены на n-3 омега и n-6 омега жирные кислоты, которые являются незаменимыми для организма человека. В частности, омега-3 жирные кислоты - эйкозапентеновая кислота (ЭПК) и докозагексеновая кислота (ДГК) - найдены только в рыбе и другой морской флоре и фауне. По этой причине рыбий жир является важнейшим пищевым источником омега-3 жирных кислот.
Стандартная пищевая добавка ПНЖК достигается путем ежедневного приема 500-1000 мг жидкого рыбьего жира. Рыбий жир обычно принимают в капсулах в целях предотвращения запаха и аромата рыбы. Тем не менее, некоторые люди испытывают дискомфорт в желудочно-кишечном тракте из-за рыбного запаха даже спустя несколько часов после приема рыбьего жира. Причиной является то, что после расщепления желеобразной оболочки в желудочно-кишечном тракте объемистая доза рыбьего жира выделяется в виде макроскопической капли, что препятствует всасыванию рыбьего жира. Проблемы неприятного запаха, аромата, а также всасывания частично могут быть решены с помощью микродисперсных препаратов рыбьего жира в виде порошкообразной или водной основы, как описано в ЕР 0276772. Однако даже микродисперсная гранула или порошок рыбьего жира обладают сохраняющимся рыбным запахом при прессовании в простые таблетки, так что в препараты необходимо добавлять ароматизаторы или антиоксиданты.
Ароматизаторы используются для подавления рыбного запаха рыбьего жира, как описано, например, в JP 08092587 или JP 08228678. Маскировка вкуса также достигается за счет добавления молочных продуктов в препараты рыбьего жира, как описано, например, в US 2003/0198728 или в JP 2002-204656, или за счет нанесения покрытия или заключения ПНЖК в капсулы, как описано, например, в WO 2004/016720 и WO 2005/029978.
Причина рыбного запаха рыбьего жира основана на окислении ненасыщенной части ПНЖК. В целях предотвращения окисления и стабилизации ПНЖК в препарат могут быть добавлены антиоксиданты, например, токоферол, как описано, например в DE 20105126 или в ЕР 1155620.
Задачей данного изобретения является предоставить пероральную композицию, содержащую ПНЖК, не имеющую неприятного аромата или запаха, а также избежать сложной и дорогостоящей технологии маскировки вкуса.
Неожиданно было обнаружено, что неприятного или рыбного запаха композиции согласно данному изобретению можно избежать.
Задачей данного изобретения является композиция для приема внутрь, содержащая полиненасыщенные жирные кислоты (ПНЖК) и активированный уголь. Композиция для приема внутрь согласно изобретению не имеет рыбного или неприятного запаха, аромата или вкуса.
Согласно настоящему изобретению полиненасыщенные жирные кислоты (ПНЖК), включают, однако, без ограничения, рыбий жир, перилловое масло, омега-3 жирные кислоты, омега-6 жирные кислоты, арахидоновую кислоту, линолевую кислоту, альфа-линолевую кислоту, дигомо-гамма-линолевую кислоту, эйкозапентеновую кислоту (ЭПК), докозагексеновую кислоту (ДГК), а также их смеси. Предпочтительными являются рыбий жир, омега-3 жирные кислоты, эйкозапентеновая кислота (ЭПК), докозагексеновая кислота (ДГК) и их смеси. Наиболее предпочтительно используется рыбий жир, содержащий эйкозапентеновую кислоту (ЭПК) и докозагексеновую кислоту (ДГК).
В предпочтительном варианте выполнения композиция согласно изобретению содержит ПНЖК, в частности порошок или гранулят рыбьего жира в количестве от 5% до 70%, более предпочтительно от 40% до 60% в пересчете на массу композиции. Общее количество используемых в композиции ПНЖК, в частности, порошка или гранулята рыбьего жира, составляет 100 мг - 1000 мг, предпочтительно 400 мг - 900 мг.
В наиболее предпочтительном варианте выполнения композиция согласно изобретению содержит эйкозапентеновую кислоту (ЭПК) в количестве от 0,5% до 10%, предпочтительно от 1,5% до 4% от массы композиции или в количестве от 1% до 20%, предпочтительно от 3% до 8% от массы порошка или гранулята рыбьего жира, содержащихся в композиции. Общее количество ЭПК в композиции составляет 10 мг - 100 мг, предпочтительно 15 мг - 50 мг.
В наиболее предпочтительном варианте выполнения композиция согласно изобретению содержит докозагексеновую кислоту (ДГК) в количестве от 0,5% до 10%, предпочтительно от 1% до 4% от массы композиции или в количестве от 1% до 20%, предпочтительно от 2% до 6% от массы порошка или гранулята рыбьего жира, содержащихся в композиции. Общее количество ДГК в композиции составляет 10 мг - 50 мг, предпочтительно 15 мг - 30 мг.
ПНЖК, в частности рыбий жир, содержащий эйкозапентеновую кислоту (ЭПК) и докозагексеновую кислоту (ДГК), используется предпочтительно в микродисперсной форме в виде гранулята или порошка, в порошкообразной или водной основе, как описано в ЕР 0 276 772. Предпочтительными являются гранулят или порошок рыбьего жира.
В предпочтительном варианте выполнения порошкообразная основа порошка или гранулята рыбьего жира содержит, по меньшей мере, гомогенный защитный коллоид, поверхностно-активное вещество, при необходимости разбавитель, стабилизатор и дополнительные фармацевтические наполнители. В случае водной основы упомянутые компоненты используются в виде водного раствора.
Защитные коллоиды порошкообразной основы включают, однако, без ограничения, полипептиды, такие как желатин, казеин, казеинат, полисахариды, такие как крахмал, декстрин, пектин, гуммиарабик, молоко, сухое молоко, поливиниловые спирты, поливинилпирролидон, сополимеры винилпирролидона и винилацетата, сополимеры акриловой кислоты и метакриловой кислоты со сложными эфирами акриловой кислоты или метакриловой кислоты, метилцеллюлозу, карбоксиметилцеллюлозу, гидроксипропилцеллюлозу, альгинаты или их смеси.
Разбавители порошкообразной основы включают, однако, без ограничения, сахар или сахарные спирты, например сахарозу, лактозу, инвертный сахар, сорбит, маннит или глицерин.
Стабилизаторы порошкообразной основы включают, однако, без ограничения, токоферол, трет-бутилгидрокситолуол, трет-бутилгидроксианизол и этоксихин.
Поверхностно-активные вещества порошкообразной основы включают, однако, без ограничения, сложные эфиры длинноцепочечных жирных кислот и аскорбиновой кислоты, сложные эфиры моно- и диглицерина и жирных кислот и их оксиэтилированные производные, сложные эфиры моноглицеридов жирных кислот и уксусной кислоты, лимонная кислота, молочная кислота, диацетилтартрат, соли 2-(2'-стеароиллактил)молочной кислоты, полиглицериновые сложные эфиры жирных кислот, сложные эфиры жирных кислот и сорбита, пропиленгликолевые сложные эфиры жирных кислот, аскорбилпальмитат и лецитин.
Порошкообразная основа содержит рыбий жир в количестве от 5% до 70%, предпочтительно от 50% до 60%, один или более поверхностно-активных веществ в количестве от 1% до 30%, предпочтительно от 5% до 15%, защитный коллоид в количестве от 5% до 50%, предпочтительно от 10% до 40%, разбавитель в количестве от 0% до 70%, предпочтительно от 3% до 35% от сухой массы порошка или гранулята рыбьего жира.
В предпочтительном варианте выполнения порошкообразная основа содержит рыбий жир в виде маленьких частиц со средним размером менее 10 мкм, более предпочтительно менее 1 мкм, наиболее предпочтительно менее 0,5 мкм.
Порошок или гранулят рыбьего жира может быть изготовлен, как описано в ЕР 0276772.
Композиция согласно изобретению содержит активированный уголь в количестве от 0,1% до 10%, предпочтительно от 1% до 5% от массы композиции. Общее количество, используемое в композиции, составляет от 5 мг до 200 мг, предпочтительно от 10 мг до 100 мг.
Частицы активированного угля согласно данному изобретению предпочтительно содержат по меньшей мере 90% частиц с размером менее 100 мкм.
Функцией активированного угля согласно изобретению является поглощение неприятного или рыбного запаха, аромата или вкуса.
Композиция согласно изобретению может содержать дополнительные активные компоненты, такие как витамины и минералы. Витамины включают, однако, без ограничения, витамин А, бета-каротин, витамин С (аскорбиновую кислоту), витамин D3 (холекальциферол), витамин Е (токоферола ацетат), витамин В1 (тиамин), витамин В2 (рибофлавин), никотинамид, витамин В5 (пантотеновую кислоту), витамин В6 (пиридоксин), фолиевую кислоту, витамин В12 (цианокобаламин), витамин K1, витамин K2, главным образом, менахинон 7-10, а также биотин. Минералы включают, однако, без ограничения, соли железа, соли меди, соли кальция, такие как карбонат кальция, фосфат кальция, глицерофосфат кальция; соли магния, такие как фосфат магния, сульфат магния (дигидрат) или оксид магния; соли цинка, такие как цитрат цинка; соли селена, такие как селенат натрия; йодид калия, соли марганца, такие как сульфат марганца; соли молибденовой кислоты, такие как молибдат натрия; соли хрома, такие как хлорид хрома; хлорид натрия и хлорид калия.
Композиция согласно настоящему изобретению может использоваться в качестве пищевой добавки или биологически активной добавки для регулирования уровня липидов в крови, предотвращения или снижения риска развития атеросклеротических изменений, расстройств или заболеваний у пациента. Композиция согласно изобретению также может быть использована в качестве пищевой или биологически активной добавки для развития и поддержания познавательных функций, связанных, например, со зрением, памятью, речью и т.д., или для облегчения и/или предупреждения заболеваний кровеносных сосудов, сердечно-сосудистых, цереброваскулярных и нервных заболеваний, таких как, например, гипертония, инфаркт миокарда, болезнь Альцгеймера, болезнь Паркинсона и депрессия, или в целях облегчения гормональных, иммунологических нарушений или ожирения. Кроме того, она может использоваться в качестве пищевой или биологически активной добавки во вспомогательных методах лечения диабета, рака и/или воспалительных процессов. В качестве пациента согласно предмету данного изобретения выступает млекопитающее, включая человека. Применение в качестве пищевой или биологически активной добавки особенно предпочтительно для беременных женщин, детей и пожилых людей.
Другим объектом изобретения является способ регулирования уровня липидов в крови, предотвращения или снижения риска развития атеросклеротических изменений, расстройств или заболеваний, для развития и поддержания познавательных функций, связанных, например, со зрением, памятью, речью и т.д., для облегчения и/или предупреждения заболеваний кровеносных сосудов, сердечно-сосудистых, цереброваскулярных и нервных заболеваний, таких как, например, гипертония, инфаркт миокарда, болезнь Альцгеймера, болезнь Паркинсона и депрессия, или для облегчения гормональных, иммунологических нарушений или ожирения, или для вспомогательных методов лечения диабета, рака и/или воспалительных процессов посредством приема композиции согласно изобретению в качестве пищевой добавки или биологически активной добавки пациентом, который согласно предмету данного изобретения является млекопитающим, включая человека, главным образом, беременных женщин, детей и пожилых людей.
Композиция согласно изобретению принимается внутрь перорально один или более, предпочтительно до трех, более предпочтительно до двух раз в день. При каждом приеме количество лекарственных форм, принятых в одно и то же время, не должно превышать двух.
Тем не менее, в некоторых случаях может быть предпочтительным отклоняться от указанных количеств в зависимости от массы тела, индивидуальной переносимости активных компонентов, типа лекарства, а также времени или интервала, в течение которого осуществляется прием лекарств. Например, в некоторых случаях может оказаться достаточно количеств, меньших, чем вышеупомянутые минимальные количества, в то время как в других случаях необходимо превысить верхний установленный предел.
Компонентами лекарственной формы для приема внутрь являются такие, которые являются приемлемыми для фармацевтических препаратов и пищевых добавок и физиологически приемлемы, например: в качестве наполнителей - производные целлюлозы (например, микрокристаллическая целлюлоза), сахара (например, лактоза), сахарные спирты (например, маннит, сорбит), неорганические наполнители (например, фосфаты кальция), связующие вещества (например, поливинилпирролидон, желатин, производные крахмала и производные целлюлозы), а также все остальные вспомогательные вещества, необходимые для производства композиций фармацевтических препаратов и пищевых добавок с требуемыми свойствами, например, смазывающие вещества (стеарат магния), например, разрыхлители (например, полимерно сшитый поливинилпирролидон, натрийкарбоксиметилцеллюлоза), например, смачиватели (например, лаурилсульфат натрия), например, агенты, замедляющие высвобождение, (например, производные целлюлозы, производные полиакриловой кислоты), например: цветные пигменты, например, газообразующие парные реагенты.
Вспомогательные вещества для фармацевтических препаратов и пищевых добавок, известные специалисту в данной области техники, также описаны, например, в следующем справочном руководстве: "Handbook of Pharmaceutical Excipients", Rowe R.C., Sheskey P.J. & Weller, P.J., American Pharmaceutical Association, Washington, 4th edition 2003.
Композиция согласно изобретению включает таблетку, таблетку, покрытую оболочкой, многослойную таблетку, таблетку с гранулами, покрытыми оболочкой, таблетку с ядром, таблетку с ядром, покрытым оболочкой, или препараты немедленного, замедленного, а также пролонгированного действия.
Предпочтительной является таблетка, таблетка, покрытая оболочкой, или многослойная таблетка. Наиболее предпочтительной из композиций является таблетка, в которой активированный уголь диспергирован в основе таблетки, трехслойная таблетка, в которой активированный уголь находится в двух наружных слоях, или таблетка, покрытая оболочкой, в которой активированный уголь содержится в оболочке.
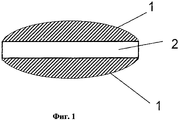
На Фиг.1 показана трехслойная таблетка, в которой активированный уголь находится в двух наружных слоях (1), а ПНЖК находится во внутреннем слое (2).
Упомянутая здесь композиция изготавливается общепринятыми способами. Например, таблетки можно изготавливать путем смешивания и/или гранулирования активных компонентов совместно со вспомогательными веществами для образования смеси, которую в конце прессуют в таблетки. Необязательно разные смеси, содержащие различные компоненты и наполнители, можно предварительно смешать и объединить в окончательную смесь, которая затем прессуется в таблетки, или предварительные смеси можно спрессовать в многослойную таблетку. В случае шипучей рецептуры пару кислота/основание можно добавить, например, к окончательной смеси, или кислоту и основание добавляют в смесь в разное время. Также основание и кислота могут быть добавлены в разные смеси, которые в конце объединяются.
Преимуществом композиции согласно данному изобретению является то, что не имеется никакого неприятного или рыбного запаха, аромата или вкуса даже после хранения в течение нескольких недель, и композиция согласно изобретению может обойтись без какого-либо ароматизатора или антиоксиданта.
Композиция согласно данному изобретению обладает хорошим и/или быстрым всасыванием ПНЖК после приема композиции. Кроме того, эта композиция облегчает быстрый прием, при желании без воды или питья.
Композиция согласно изобретению имеет подходящую твердость и прочность таблеток на истирание, чтобы быть изготовленной без ущерба для целостности гранул, т.е. ПНЖК не выделяются из основы таблетки.
Преимуществом композиции согласно данному изобретению является то, что для изготовления композиции не требуется сложной и дорогостоящей технологии маскировки вкуса, известной из уровня техники, такой как покрытие гранул оболочкой, добавление антиоксидантов или помещение ПНЖК в капсулу. Композицию согласно данному изобретению можно получить с помощью несложных и общеизвестных стандартных способов. Другим хорошо известным методом маскировки вкуса является добавление ароматизаторов, чтобы скрыть и замаскировать неприятный запах. Этот способ маскировки вкуса, как правило, ограничивается лишь несколькими подходящими ароматами, которые приходится выбирать в каждом случае. Однако в композиции согласно данному изобретению не требуются ароматизирующие вещества для маскировки вкуса.
Пример 1
Трехслойная таблетка согласно Фиг.1, состоящая из двух наружных слоев А и внутреннего слоя В, отличающаяся тем, что внутренний слой В состоит из:
- 600 мг сухого порошка рыбьего жира (омега-3, 18:12), включающего 28,2 мг ЭПК и 20 мг ДГК
- 64 мг безводного двухосновного фосфата кальция
- 40 мг циклодекстрина
- 40 мг гидроксипропилцеллюлозы
- 40 мг бентонита
- 4 мг диоксида кремния
- 4 мг стеарата магния
- 8 мг дезодорированного экстракта розмарина;
а каждый из двух наружных слоев А состоит из:
- 25 мг активированного угля (90% частиц имеют размер менее 100 мкм, потери при прокаливании при 600°С: ≤1%, потери при высушивании: ≤10%)
- 25 мг гидроксипропилцеллюлозы
- 50 мг микрокристаллической целлюлозы
Процесс изготовления Примера 1
Компоненты слоя В смешивают друг с другом в барабанном смесителе в течение 20 мин и за 5 мин до окончания добавляют смазывающее вещество, - стеарат магния, - для получения конечной смеси 1, которой затем заполняют подающий механизм 1 устройства для изготовления многослойных таблеток. Компоненты слоя А смешивают друг с другом в барабанном смесителе в течение 20 мин для получения конечной смеси 2, которой затем заполняют подающие механизмы 2 и 3 устройства для изготовления многослойных таблеток. Затем трехслойную таблетку прессуют ротационным прессом.
Пример 2
Таблетка, состоящая из:
- 600 мг сухого порошка рыбьего жира (омега-3, 18:12), включающего 28,2 мг ЭПК и 20 мг ДГК
- 64 мг безводного двухосновного фосфата кальция
- 40 мг циклодекстрина
- 40 мг гидроксипропилцеллюлозы
- 40 мг бентонита
- 4 мг диоксида кремния
- 4 мг стеарата магния
- 8 мг дезодорированного экстракта розмарина
- 50 мг активированного угля (90% частиц имеют размер менее 100 мкм, потери при прокаливании при 600°С: ≤1%, потери при высушивании: ≤10%)
- 50 мг гидроксипропилцеллюлозы
- 100 мг микрокристаллической целлюлозы
Прогресс изготовления Примера 2
Способ прямого прессования
Все компоненты смешивают друг с другом в барабанном смесителе в течение 20 мин и при необходимости за 5 мин до окончания добавляют смазывающее вещество - стеарат магния. Конечную смесь прессуют в таблетки при помощи ротационного пресса.
Пример 3
Покрытая оболочкой таблетка, содержащая ядро, состоящее из:
- 600 мг сухого порошка рыбьего жира (омега-3, 18:12), включающего 28,2 мг ЭПК и 20 мг ДГК
- 384 мг безводного двухосновного фосфата кальция
- 48 мг циклодекстрина
- 60 мг гидроксипропилцеллюлозы
- 60 мг бентонита
- 60 мг повидона (kollidon VA 60 мелкодисперсный)
- 6 мг диоксида кремния
- 6 мг стеарата магния
- 12 мг дезодорированного экстракта розмарина, а также покрытие, состоящее из:
- 15,5 мг активированного угля (90% частиц имеют размер менее 100 мкм, потери при прокаливании при 600°С: ≤1%, потери при высушивании: ≤10%)
- 15 мг шеллака
- 22,5 мг гидроксипропилметилцеллюлозы
- 9 мг триацетина
Процесс изготовления Примера 3
Все компоненты ядра смешивают друг с другом в барабанном смесителе в течение 20 мин и при необходимости за 5 мин до окончания добавляют смазывающее вещество - стеарат магния. Смесь прессуют в таблетки с помощью ротационного пресса. После этого на таблетки наносят покрывающую суспензию, состоящую из активированного угля, шеллака, гидроксипропилметилцеллюлозы, триацетина и дистиллированной воды.
Результаты
Примеры 1, 2 и 3 не имеют никакого неприятного или рыбного вкуса или запаха.
Claims (12)
1. Пероральная композиция для регулирования уровня липидов в крови, предотвращения или снижения риска развития атеросклеротических изменений, расстройств или заболеваний, содержащая рыбий жир или перилловое масло и активированный уголь.
2. Пероральная композиция по п.1, в которой рыбий жир представляет собой порошок или гранулят рыбьего жира.
3. Пероральная композиция по п.2, в которой средний размер частиц порошка рыбьего жира составляет менее 10 мкм.
4. Пероральная композиция по п.1, содержащая от 5% до 70% от массы композиции полиненасыщенных жирных кислот, содержащихся в рыбьем жире или перилловом масле.
5. Пероральная композиция по п.1, содержащая от 100 мг до 1000 мг полиненасыщенных жирных кислот, содержащихся в рыбьем жире или перилловом масле.
6. Пероральная композиция по п.1, содержащая, по меньшей мере, один дополнительный минерал и/или витамин.
7. Пероральная композиция по п.1, представляющая собой пероральную пищевую или биологически активную добавку.
8. Пероральная композиция по п.1, представляющая собой таблетку, таблетку, покрытую оболочкой, или многослойную таблетку.
9. Пероральная композиция по п.1, в которой частицы активированного угля содержат, по меньшей мере, 90% частиц, имеющих размер менее 100 мкм.
10. Пероральная композиция по п.1, представляющая собой таблетку, в матрице которой диспергирован активированный уголь.
11. Пероральная композиция по п.1, представляющая собой трехслойную таблетку, в двух наружных слоях которой находится активированный уголь.
12. Пероральная композиция по любому из пп.1-11, представляющая собой таблетку, покрытую оболочкой, при этом активированный уголь находится в оболочке.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP07291306.4 | 2007-10-30 | ||
| EP07291306 | 2007-10-30 | ||
| PCT/EP2008/008882 WO2009056247A1 (en) | 2007-10-30 | 2008-10-21 | Composition comprising polyunsaturated fatty acids and activated charcoal |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2010121714A RU2010121714A (ru) | 2011-12-10 |
| RU2485940C2 true RU2485940C2 (ru) | 2013-06-27 |
Family
ID=40344798
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2010121714/15A RU2485940C2 (ru) | 2007-10-30 | 2008-10-21 | Композиция, содержащая полиненасыщенные жирные кислоты и активированный уголь |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US20100260893A1 (ru) |
| EP (1) | EP2214638B1 (ru) |
| AR (1) | AR070759A1 (ru) |
| AT (1) | ATE541560T1 (ru) |
| AU (1) | AU2008317920B2 (ru) |
| BR (1) | BRPI0818568A2 (ru) |
| CA (1) | CA2703816C (ru) |
| ES (1) | ES2379034T3 (ru) |
| MX (1) | MX2010003703A (ru) |
| PE (1) | PE20091076A1 (ru) |
| PL (1) | PL2214638T3 (ru) |
| RU (1) | RU2485940C2 (ru) |
| TW (1) | TW200942229A (ru) |
| UY (1) | UY31410A1 (ru) |
| WO (1) | WO2009056247A1 (ru) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8784904B2 (en) | 2008-04-10 | 2014-07-22 | U.S. Nutraceuticals, LLC | Plant derived seed extract rich in essential fatty acids derived from perilla seed: composition of matter, manufacturing process and use |
| US9770047B2 (en) | 2008-04-10 | 2017-09-26 | U.S. Nutraceuticals, LLC | Perilla seed composition |
| US8586104B2 (en) | 2008-04-10 | 2013-11-19 | U.S. Nutraceuticals, LLC | Plant derived seed extract rich in essentially fatty acids derived from Salvia hispanica L. seed: composition of matter, manufacturing process and use |
| US9610313B2 (en) | 2008-04-10 | 2017-04-04 | U.S. Nutraceuticals | Eye health composition and method using plant derived seed extract rich in essential fatty acids derived from perilla seed and carotenoids |
| CA2803980A1 (en) * | 2010-07-01 | 2012-01-05 | Delante Health As | Coated effervescent tablet |
| WO2013070856A1 (en) * | 2011-11-09 | 2013-05-16 | Denovo Inc. | Toxin decontaminant food product and method of treating disorders of the gastrointestinal tract |
| RU2524358C2 (ru) * | 2012-07-24 | 2014-07-27 | Федеральное государственное бюджетное учреждение "Научно-исследовательский институт питания РАМН" Российской академии медицинских наук (ФГБУ "НИИ питания" РАМН) | Функциональный пищевой ингредиент с заданным липидным профилем |
| EP2994165A4 (en) * | 2013-05-10 | 2017-01-04 | Nitromega Corp. | Nutritional or dietary supplements containing fatty acids and nitrite |
| EA025006B1 (ru) * | 2013-08-22 | 2016-11-30 | Федеральное государственное бюджетное учреждение "Научно-исследовательский институт питания РАМН" Российской академии медицинских наук (ФГБУ "НИИ питания" РАМН) | Функциональный пищевой ингредиент с заданным липидным профилем |
| CN105935145B (zh) * | 2015-12-18 | 2019-09-20 | 重庆两江药物研发中心有限公司 | 一种鱼油植物甾醇复合片剂及其制备方法 |
| CN105919946B (zh) * | 2016-05-31 | 2019-03-12 | 福格森(武汉)生物科技股份有限公司 | 一种dha微丸的制备方法 |
| EA201991467A1 (ru) * | 2016-12-15 | 2019-11-29 | Состав смеси, содержащий силикат и микробные и/или растительные клетки и полиненасыщенную жирную кислоту, имеющую по меньшей мере 20 атомов углерода (lc-pufa) | |
| CN111067876B (zh) * | 2019-12-04 | 2022-08-16 | 宁夏大学 | 一种α-亚麻酸双层片及其制备方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE20105126U1 (de) * | 2001-03-23 | 2002-01-31 | Bartz, Volker, 35440 Linden | Fischöl zur oralen Einnahme |
| RU2199317C2 (ru) * | 1997-02-21 | 2003-02-27 | Абботт Лаборэтриз | Способ снижения заболеваемости некротическим энтероколитом у детей (варианты) |
| WO2007015201A1 (en) * | 2005-08-03 | 2007-02-08 | Sasol Technology (Proprietary) Limited | Transport and erection of very large vessels |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3702031A1 (de) | 1987-01-24 | 1988-08-04 | Basf Ag | Verfahren zur herstellung von mikrodispersen fischoelpraeparaten |
| US5780039A (en) * | 1992-04-23 | 1998-07-14 | Novartis Nutrition Ag | Orally-ingestible nutrition compositions having improved palatability |
| JPH0892587A (ja) | 1994-09-22 | 1996-04-09 | Baiotsukusu:Kk | 魚臭のマスキング法 |
| JP3534881B2 (ja) | 1995-02-23 | 2004-06-07 | 太陽化学株式会社 | 乳化組成物 |
| US6630192B2 (en) | 1995-04-07 | 2003-10-07 | Brandeis University | Increasing the HDL level and the HDL/LDL ratio in human serum by balancing saturated and polyunsaturated dietary fatty acids |
| US6479545B1 (en) * | 1999-09-30 | 2002-11-12 | Drugtech Corporation | Formulation for menopausal women |
| ATE301401T1 (de) * | 2000-05-18 | 2005-08-15 | Mega Healthcare As Q | Nahrungsergänzungsmittel mit vitaminen, mineralien und mehrfach ungesättigten fettsäuren |
| JP2002204656A (ja) | 2001-01-10 | 2002-07-23 | Yakult Honsha Co Ltd | 発酵乳飲食品及びその製造方法 |
| JP2004531399A (ja) * | 2001-06-25 | 2004-10-14 | ファルマシア・コーポレーション | 圧縮コーティング錠剤を製造する方法および装置 |
| DE60301677T2 (de) * | 2002-02-04 | 2006-07-06 | Kyowa Hakko Kogyo Co., Ltd. | Pharmazeutische und Lebenmittelzusammensetzungen mit einem Di- oder Oligosaccharid, das die Insulinfreisetzung steigert |
| WO2004016720A2 (en) | 2002-08-14 | 2004-02-26 | E.I. Du Pont De Nemours And Company | Coated polyunsaturated fatty acid-containing particles and coated liquid pharmaceutical-containing particles |
| AU2003290516A1 (en) * | 2002-08-14 | 2004-04-08 | E.I. Du Pont De Nemours And Company | Solid flowable powder with high liquid loading |
| US20070031475A1 (en) | 2003-09-26 | 2007-02-08 | Nestec S.A. | Nutritional composition with unsaturated fatty acids and trace elements |
| DE602004001969T2 (de) * | 2004-02-20 | 2007-03-15 | Mattern, Udo | Orale pharmazeutische Zusammensetzung und Verfahren zu ihrer Herstellung |
| US20060083786A1 (en) * | 2004-07-29 | 2006-04-20 | Glenmark Pharmaceuticals Limited | Taste masking pharmaceutical composition containing levocetirizine |
| GB0516069D0 (en) * | 2005-08-04 | 2005-09-14 | Imp College Innovations Ltd | Pharmaceutical and use thereof |
-
2008
- 2008-10-20 UY UY31410A patent/UY31410A1/es not_active Application Discontinuation
- 2008-10-21 EP EP08845987A patent/EP2214638B1/en active Active
- 2008-10-21 PE PE2008001803A patent/PE20091076A1/es not_active Application Discontinuation
- 2008-10-21 BR BRPI0818568 patent/BRPI0818568A2/pt not_active Application Discontinuation
- 2008-10-21 CA CA2703816A patent/CA2703816C/en active Active
- 2008-10-21 WO PCT/EP2008/008882 patent/WO2009056247A1/en active Application Filing
- 2008-10-21 ES ES08845987T patent/ES2379034T3/es active Active
- 2008-10-21 RU RU2010121714/15A patent/RU2485940C2/ru active
- 2008-10-21 AU AU2008317920A patent/AU2008317920B2/en active Active
- 2008-10-21 MX MX2010003703A patent/MX2010003703A/es active IP Right Grant
- 2008-10-21 AT AT08845987T patent/ATE541560T1/de active
- 2008-10-21 PL PL08845987T patent/PL2214638T3/pl unknown
- 2008-10-29 TW TW097141493A patent/TW200942229A/zh unknown
- 2008-10-30 AR ARP080104763A patent/AR070759A1/es unknown
-
2010
- 2010-04-30 US US12/799,744 patent/US20100260893A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2199317C2 (ru) * | 1997-02-21 | 2003-02-27 | Абботт Лаборэтриз | Способ снижения заболеваемости некротическим энтероколитом у детей (варианты) |
| DE20105126U1 (de) * | 2001-03-23 | 2002-01-31 | Bartz, Volker, 35440 Linden | Fischöl zur oralen Einnahme |
| WO2007015201A1 (en) * | 2005-08-03 | 2007-02-08 | Sasol Technology (Proprietary) Limited | Transport and erection of very large vessels |
Non-Patent Citations (1)
| Title |
|---|
| BENATTI P., PELUSO G., NICOLAI R., CALVANI M. Polyunsaturated fatty acids: biochemical, nutritional and epigenetic properties. J. Am. Coll. Nutr. 2004 Aug; 23(4):281-302. * |
Also Published As
| Publication number | Publication date |
|---|---|
| MX2010003703A (es) | 2010-07-30 |
| ES2379034T3 (es) | 2012-04-20 |
| AU2008317920A1 (en) | 2009-05-07 |
| AU2008317920B2 (en) | 2014-03-13 |
| EP2214638B1 (en) | 2012-01-18 |
| TW200942229A (en) | 2009-10-16 |
| WO2009056247A1 (en) | 2009-05-07 |
| BRPI0818568A2 (pt) | 2015-04-22 |
| PL2214638T3 (pl) | 2012-06-29 |
| US20100260893A1 (en) | 2010-10-14 |
| AR070759A1 (es) | 2010-05-05 |
| ATE541560T1 (de) | 2012-02-15 |
| RU2010121714A (ru) | 2011-12-10 |
| PE20091076A1 (es) | 2009-07-25 |
| EP2214638A1 (en) | 2010-08-11 |
| CA2703816A1 (en) | 2009-05-07 |
| UY31410A1 (es) | 2009-05-29 |
| CA2703816C (en) | 2016-07-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2485940C2 (ru) | Композиция, содержащая полиненасыщенные жирные кислоты и активированный уголь | |
| RU2493842C2 (ru) | Распадающаяся во рту композиция, содержащая полиненасыщенные жирные кислоты, не имеющая неприятного запаха или вкуса | |
| JP2008501686A (ja) | 栄養製剤 | |
| JP4969763B2 (ja) | 臭気性オイルを含有する摂取可能な組成物 | |
| US20050101670A1 (en) | Nutritional supplements | |
| US20040101554A1 (en) | Nutritional formulations | |
| JP2003500445A (ja) | 栄養補助物 | |
| TW200538054A (en) | Multi-vitamin and mineral nutritional supplements | |
| RU2381025C2 (ru) | Композиция для лечения глаз, содержащая омега-3 жирные кислоты и омега-6 жирные кислоты | |
| WO2007055327A1 (ja) | ゼリー組成物 | |
| KR20230027221A (ko) | 연질 젤라틴 캡슐 | |
| EP3261458A1 (en) | Compositions comprising co-q10, krill oil and vitamin d | |
| US20090082447A1 (en) | Pharmaceutical Compositions Containing Omega 3 Fatty Acids | |
| GB2527802A (en) | Tablet with differentiated absorption |