RU2268054C2 - Сочетанная терапия с использованием пентафторбензолсульфонамидов - Google Patents
Сочетанная терапия с использованием пентафторбензолсульфонамидов Download PDFInfo
- Publication number
- RU2268054C2 RU2268054C2 RU2002105374/15A RU2002105374A RU2268054C2 RU 2268054 C2 RU2268054 C2 RU 2268054C2 RU 2002105374/15 A RU2002105374/15 A RU 2002105374/15A RU 2002105374 A RU2002105374 A RU 2002105374A RU 2268054 C2 RU2268054 C2 RU 2268054C2
- Authority
- RU
- Russia
- Prior art keywords
- cisplatin
- compound
- platinum
- treatment
- antitumor
- Prior art date
Links
- 0 COc1cc(*)ccc1* Chemical compound COc1cc(*)ccc1* 0.000 description 2
- XDWNHOSDTKPHPQ-UHFFFAOYSA-N CCOC(CNC(Nc1cc([Es])ccc1OC)=O)=O Chemical compound CCOC(CNC(Nc1cc([Es])ccc1OC)=O)=O XDWNHOSDTKPHPQ-UHFFFAOYSA-N 0.000 description 1
- FSXLOWIFSZNIMV-UHFFFAOYSA-N COc(c(NC(N)=O)c1)ccc1NS(c(c(F)c(c(F)c1F)F)c1F)(=O)=O Chemical compound COc(c(NC(N)=O)c1)ccc1NS(c(c(F)c(c(F)c1F)F)c1F)(=O)=O FSXLOWIFSZNIMV-UHFFFAOYSA-N 0.000 description 1
- MHNRFPKPZCPBID-UHFFFAOYSA-N COc(c(O)c1)ccc1NS(c(c(F)c(c(F)c1F)F)c1F)(=O)=O Chemical compound COc(c(O)c1)ccc1NS(c(c(F)c(c(F)c1F)F)c1F)(=O)=O MHNRFPKPZCPBID-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
- A61K31/282—Platinum compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/18—Sulfonamides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K33/00—Medicinal preparations containing inorganic active ingredients
- A61K33/24—Heavy metals; Compounds thereof
- A61K33/243—Platinum; Compounds thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Landscapes
- Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Inorganic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Weting (AREA)
Abstract
Изобретение относится к области медицины и фармакологии и касается композиции для лечения пролиферативных заболеваний, содержащей координационный комплекс платины с противоопухолевым средством и производное пентафторбензолсульфонамида, а также способа лечения с использованием указанной композиции. Композиция обладает синергическим действием. 3 н. и 10 з.п. ф-лы, 5 ил.
Description
Область техники, к которой относится изобретение
Настоящее изобретение относится к композициям пентафторбензолсульфонамидов и цисплатина, которые способны ингибировать пролиферацию аномальных клеток.
Уровень техники
Рак - это общее название широкого круга злокачественных изменений клеток, характеризующихся нерегулируемым ростом, утратой дифференциации и способностью вторгаться в местные ткани и метастазировать. Эти опухолевые губительные новообразования воздействуют в той или иной мере на каждую ткань и орган в организме. В последние десятилетия разработано и создано множество терапевтических средств для лечения различных видов рака. К наиболее распространенным видам противоопухолевых средств относятся: ДНК-алкилирующие агенты (например, циклофосфамид, ифосфамид), антиметаболиты (например, метотрексат, антагонист фолата и 5-фторурацил, пиримидиновый антагонист), средства, разрывающие микротрубочки (например, винкристин, винбластин, пакметаксель), интеркаляторы ДНК (например, доксорубицин, дауномицин, цисплатин) и гормонотерапию (например, тамоксифен, флутамид). Идеальное противоопухолевое средство должно селективно разрушать раковые клетки с обширным спектром терапевтического действия в отношении незлокачественных клеток. Эффективность воздействия на злокачественные клетки должна сохраняться и после продолжительного действия лекарства. К сожалению, ни одно из применяемых ныне химиотерапевтических средств не является идеальным. Большинство из них обладает очень узкими терапевтическими индексами и практически в каждом случае в раковых клетках, подвергнутых воздействию сублетальных концентраций химиотерапевтического средства, будет повышаться устойчивость в отношении этого средства, и очень часто - перекрестная устойчивость к нескольким другим противоопухолевым средствам.
Разработка новых противораковых средств привела к новым способам и режимам лечения и новым комбинациям, которые оказываются более эффективными в борьбе с этой болезнью.
Поэтому одним из объектов настоящего изобретения являются композиции, которые прямо или косвенно оказывают токсичное действие на активно делящиеся клетки и могут использоваться для лечения рака.
Другой объект изобретения относится к способам уничтожения активно размножающихся клеток, таких как раковые, бактериальные или эпителиальные клетки, лечения всех видов рака и пролиферативных состояний. Еще один объект касается способов лечения других болезненных состояний, характеризующихся наличием быстро размножающихся клеток, таких как псориаз и другие кожные заболевания.
Дополнительные объекты, свойства и преимущества будет понятны специалистам в данной области из нижеследующих описания и формулы изобретения.
Сущность изобретения
В одном аспекте настоящее изобретение касается композиции, которые могут использоваться для лечения рака и других заболеваний, связанных с пролиферацией аномальных клеток. Композиции включают цисплатин (или содержащий платину координационный комплекс, например, карбоплатин) и соединение формулы:
В вышеприведенной формуле R означает водород, замещенный или незамещенный (С1-С10)алкил или замещенный или незамещенный (С3-С6)алкенил. Ar представляет собой замещенную или незамещенную арильную группу или замещенную или незамещенную гетероарильную группу.
В другом аспекте настоящее изобретение касается способа лечения рака и других пролиферативных заболеваний с помощью вышеуказанных композиций.
Краткое описание чертежей.
Фиг.1 представляет собой график, который иллюстрирует синергетические эффекты соединения 1 и цисплатина при обработке МХ-1 ксенотрансплантатов рака молочной железы человека у безтимусных голых мышей, при применении полуоптимальных доз каждого из лекарственных средств.
Фиг.2 представляет собой график, который иллюстрирует синергетические эффекты соединения 2 и цисплатина при обработке МХ-1 ксенитрансплантатов рака молочной железы человека у безтимусных голых мышей, при применении полуоптимальных доз каждого из лекарственных средств.
Фиг.3 представляет график, иллюстрирующий падение синергетической активности между 5-фторурацилом и соединением 2 против МХ-1 ксенотрансплантатов рака молочной железы человека у безтимусных голых мышей.
Фиг.4 представляет график, иллюстрирующий падение синергетической активности между адриамицином и соединением 2 против МХ-1 ксенотрансплантатов рака молочной железы человека у безтимусных голых мышей.
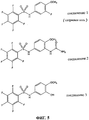
Фиг.5 показывает структуру соединения 1, соединения 2 и соединения 3.
Описание отдельных вариантов осуществления изобретения
Определения
Термин «алкил», сам по себе или как часть другого заместителя, означает, если иное не оговорено, нормальную (прямую) и разветвленную цепочку или циклический углеводородный радикал, или их сочетание, который может быть полностью насыщенным, содержать одну или несколько ненасыщенных связей и может включать ди- и мультивалентные радикалы, с указанием количества атомов углерода (т.е. C1-С10 означает от одного до десяти атомов углерода). Примерами насыщенных углеводородных радикалов являются, например, следующие группы: метил, этил, н-пропил, изопропил, н-бутил, трет-бутил, изобутил, втор-бутил, циклогексил, (циклогексил)метил, циклопропилметил, их гомологи и изомеры, например н-пентил, н-гексил, н-гептил, н-октил и т.п. Ненасыщенная алкильная группа - это такая, в которой имеется одна или несколько двойных связей или тройных связей. Примеры ненасыщенных алкильных групп включают винил, 2-пропенил, кротил, 2-изопентенил, 2-(бутадиенил), 2,4-пентадиенил, 3-(1,4-пентадиенил), этинил, 1- и 3-пропинил, 3-бутинил и более высшие гомологи и изомеры. Подразумевается, что термин «алкил», если не оговаривается иное, также включает алкильные производные, которые более детально определены ниже под термином «гетероалкил». Алкильные группы, в которых содержатся только углеводородные группы, называют «гомоалкильными».
Термин «алкилен», сам по себе или как часть другого заместителя, означает двухвалентный радикал, выбранный из алканов, например -CH2CH2CH2CH2-, а кроме того, включает группы, которые ниже названы как «гетероалкилен».
Обычно алкильная (или алкиленовая) группа содержит от 1 до 24 атомов углерода, причем такие группы с 10 и меньшим числом атомов углерода являются предпочтительными в настоящем изобретении. «Низший алкил» или «низший алкилен» представляют собой более короткую алкильную или алкиленовую цепочку, обычно имеющую восемь или еще меньше атомов углерода.
Термины «алкокси», «алкиламино» и «алкилтио» (или тиоалкокси) используются в их обычном смысле и относятся к таким алкильным группам, которые прикреплены к остатку молекулы через атом кислорода, аминогруппу или атом серы, соответственно.
Термин «гетероалкил», сам по себе или в сочетании с другим термином, означает, если иное не оговорено, стабильную нормальную или разветвленную цепочку, или циклический углеводородный радикал, или их сочетание, состоящие из определенного количества атомов углерода и от одного до трех гетероатомов, выбранных из группы, состоящей из О, N, Si и S, и где атомы азота и серы могут быть необязательно окислены, а гетероатом азота - необязательно кватернизован. Гетероатомы О, N и S могут размещаться внутри гетероалкильной группы. Гетероатом Si может находиться в любом положении гетероалкильной группы, включая положение, в котором алкильная группа присоединена к остальной части молекулы. Примерами могут быть -СН2-СН2-O-СН3-, -CH2-CH2-NH-СН3-, -СН2-СН2-N(СН3)-СН3, -CH2-S-СН2-СН3, -СН2-СН2-S(O)-СН3, -СН2-СН2-S(O)2-СН3, -СН=СН-О-СН3, -Si(СН3)3, -СН2-СН=N-ОСН3 и -СН=СН-N(СН3)-СН3. Два гетероатома могут следовать друг за другом, как, например: -СН2-NH-ОСН3 и -СН2-O-Si(СН3)3. Аналогично, термин «гетероалкилен», сам по себе или как часть другого заместителя означает двухвалентный радикал, полученный из гетероалкила, как, например: -CH2-CH2-S-CH2-CH2- и -CH2-S-CH2-CH2-NH-CH2-. В гетероалкиленовых группах гетероатомы могут также находиться на одном или обоих концах цепочки (например, алкиленокси, алкилендиокси, алкиленамино, алкилендиамино и т.п.). Более того, для алкиленовых и гетероалкиленовых соединяющих групп никакой ориентации этой соединяющей группы не предусматривается.
Термины «циклоалкил» и «гетероциклоалкил», сами по себе или в комбинации с другими терминами, отражают, если не оговорено иное, циклические варианты «алкила» и «гетероалкила» соответственно. Кроме того, в гетероциклоалкиле гетероатом может находиться в том положении, которым гетероалкил присоединен к основной части молекулы. Примерами циклоалкилов являются циклопентил, циклогексил, 1-циклогексенил, 3-циклогексенил, циклогептил и т.п. Примерами гетероциклоалкилов являются 1-(1,2,5,6-тетрагидропиридил), 1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-морфолинил, 3-морфолинил, тетрагидрофуран-2-ил, тетрагидрофуран-3-ил, тетрагидротиен-2-ил, тетрагидротиен-3-ил, 1-пиперазинил, 2-пиперазинил и т.п.
Термин «гало» или «галоген», сами по себе или как часть другого заместителя, означают, если не оговорено иное, атом фтора, хлора, брома или иода.
Кроме того, считается, что такой термин как «галоалкил» включает моногалоалкил и полигалоалкил. Например, подразумевается, что термин "гало(С1-С4)алкил" включает трифторметил, 2,2,2-трифторэтил, 4-хлорбутил, 3-бромпропил и т.п.
Термин «арил» означает, если иное не оговорено, полиненасыщенный, как правило, ароматический углеводородный заместитель, который может представлять собой одну единственную циклическую структуру или несколько колец (до трех колец), которые либо сконденсированы вместе, либо соединены между собой ковалентной связью. Термин «гетероарил» относится к арильным группам (в виде циклов или колец), которые не содержат вовсе или содержат до четырех гетероатомов, выбранных из N, О и S, в которых атомы азота и серы могут быть необязательно окислены, а атом(ы) азота - необязательно кватернизован(ы). Гетероарильная группа может быть присоединена к остальной части молекулы через гетероатом. Неограничивающими примерами арильных и гетероарильных групп являются фенил, 1-нафтил, 4-бифенил, 1-пирролил, 2-пирролил, 3-пирролил, 3-пиразолил, 2-имидазолил, 4-имидазолил, пиразинил, 2-оксазолил, 4-оксазолил, 2-фенил-4-оксазолил, 5-оксазолил, 3-изоксазолил, 5-изоксазолил, 2-тиазолил, 4-тиазолил, 5-тиазолил, 2-фурил, 3-фурил, 2-тиенил, 3-тиенил, 2-пиридил, 3-пиридил, 4-пиридил, 2-пиримидил, 5-бензотиазолил, пуринил, 2-бензимидазолил, 5-индолил, 1-изохинолил, 5-изохинолил, 2-хиноксалинил, 5-хиноксалинил, 3-хинолил и 6-хинолил. Заместители для каждой из вышеуказанных арильных и гетероарильных циклических систем выбраны из группы подходящих заместителей, которые указаны ниже.
Для краткости термин «арил» при использовании в сочетании с другими терминами (например, арилокси, арилтиокси, арилалкил) включает и арильные и гетероарильные циклы, как определено выше.
Таким образом, подразумевается, что термин «арилалкил» включает такие радикалы, в которых арильная группа присоединена к алкильной группе (например, бензил, фенэтил, пиридилметил и т.п.), включая и те алкильные группы, в которых углеродный атом (например, метиленовая группа) замещен, например, атомом кислорода (например, феноксиметил, 2-пиридилоксиметил, 3-(1-нафтилокси)пропил и т.п.).
Подразумевается, что каждый из вышеупомянутых терминов (например, «алкил», «гетероалкил», «арил» и «гетероарил») обозначает и замещенные, и незамещенные формы указанного радикала. Предпочтительные заместители для каждого типа радикалов приведены ниже.
Заместителями алкильных и гетероалкильных радикалов (включая группы, часто называемые как алкилен, алкенил, гетероалкилен, гетероалкенил, алкинил, циклоалкил, гетероциклоалкил, циклоалкенил и гетероциклоалкенил) могут быть различные группы, выбранные из: -OR', =О, =NR’, =N-OR', -NR’R’’, -SR’, - галоген, -SiR’R''R’’’, -OC(O)R’, -C(O)R’, -CO2R’, -CONR’R’’, -OC(O)NR’R’’, -NR’’C(O)R’, -NR’-C(O)NR’’R’’’, -NR''C(O)2R’, -NH-C(NH2)=NH, -NR’C(NH2)=NH, -NH-C(NH2)=NR’, -S(O)R’, -S(O)2R’, -S(О)2NR’R'', - CN и NO; в количестве от нуля до (2m’+1), где m' - общее число атомов углерода в каждом радикале. R', R'' и R''' - каждый независимо представляет собой водород, ненасыщенный (C1-C8)-алкил и гетероалкил, незамещенный арил, арил, замещенный 1-3 атомами галогенов, незамещенный алкил, алкокси или тиоалкоксигруппы или арил-(С1-С2)алкильные группы. Если R' и R'' присоединены к одному и тому же атому азота, они могут образовывать вместе с атомом азота 5-, 6- или 7-членное кольцо. Например, подразумевается, что -NR'R'' включает 1-пирролидинил и 4-морфолинил. Из вышеприведенных разъяснений любому специалисту в данной области будет понятно, что под термином «алкил» подразумеваются такие группы как галоалкильные (например, -CF3 и -CH2CF3) и ацильная (например, -С(О)СН3, -С(О)CF3, -С(О)СН2ОСН3 и т.п.).
Аналогично, заместители для арильных и гетероарильных групп могут быть различными и выбранными из: -галоген, -OR’, -OC(О)R’, -NR’R’’, -SR’, -R’, -CN, -NO2, -CO2R’, - CONR’R’’, -C(O)R’, -OC(О)NR'R’’, -NR’’C(О)R’, -NR’’C(О)2R’, -NR’-C(О)NR’’R’’’, -NH-C(NH2)=NH, -NR’C(NH2)=NH, -NH-C(NH2)=NR’, -S(О)R’, -S(О)2R', -S(O2)NR'R'', -N3,-CH(Ph)2, перфтор (С1-С4)алкокси и перфтор (С1-С4)алкил, в количестве от нуля до общего числа открытых валентностей в ароматической циклической системе; и где R', R'' и R''' независимо выбраны из водорода, (C1-C8)алкила и гетероалкила, незамещенных арила и гетероарила, (незамещенный арил)-(С1-С2)алкила и (незамещенный арил)окси-(С1-С4)алкила.
Два заместителя у смежных атомов арильного или гетероарильного кольца необязательно могут быть замещены заместителем формулы -T-C(O)-(CH2)q-U-, где Т и U независимо являются -NH-, -О-, -СН2- или простой связью, a q - целое число от 0 до 2. Или же два заместителя у смежных атомов арильного или гетероарильного кольца необязательно могут быть замещены заместителем формулы -А-(СН2)r-В-, где А и В независимо представляют собой -СН2-, -O-, -NH-, -S-, -S(O)-, -S(O)2, -S(O)2NR'- или простую связь, а r - целое число от 1 до 3. Одна из простых связей образованного таким образом нового цикла необязательно может замещаться двойной связью. Или же два заместителя у смежных атомов арильного или гетероарильного кольца необязательно могут быть замещены заместителем формулы -(CH2)s-X-(CH2)t, где s и t независимо друг от друга являются простыми числами от 0 до 3, а Х представляет собой -О-, -NR'-, -S-, -S(О)-, -S(О)2- или -S(О)2NR’-. Заместитель R’ в -NR’- и -S(О)2NR’- выбран из водорода или незамещенного (С1-С6)алкила.
В использованном здесь значении термин «гетероатом» означает кислород (О), азот (N), серу (S) и кремний (Si).
Термин «фармацевтически приемлемые соли» означают соли активных соединений, которые получаются на основе относительно нетоксичных кислот или оснований в зависимости от конкретных заместителей описываемых здесь соединений. Если соединения настоящего изобретения содержат функциональные группы кислого характера, соли присоединения основания могут быть получены при взаимодействии нейтральной формы таких соединений с избытком желаемого основания либо непосредственно, либо в среде подходящего инертного растворителя. Примеры фармацевтически приемлемых солей присоединения оснований включают соли натрия, калия, кальция, аммония, органической аминогруппы или магния и им подобные. Если соединения настоящего изобретения содержат функциональные группы оснóвного характера, соли присоединения кислот могут быть получены при взаимодействии нейтральной формы таких соединений избытком желаемой кислоты либо непосредственно, либо в среде подходящего инертного растворителя. Примеры фармацевтически приемлемых солей включают соли, полученные с использованием неорганических кислот, таких как хлористоводородная, бромистоводородная, азотная, угольная, моногидрогенугольная, фосфорная, метафосфорная кислота, дигидрогенфосфорная, серная, моногидрогенсерная, йодисто-водородная или фосфористая кислота и т.п., а также соли, полученные с помощью относительно нетоксичных органических кислот, как, например, уксусная, пропионовая, изомасляная, щавелевая, малеиновая, малоновая, бензойная, янтарная, пробковая, фумаровая, миндальная, фталевая, бензолсульфокислота, п-толилсульфокислота, лимонная, винная, метансульфокислота и т.п. Сюда же относятся соли аминокислот, такие как аргинаты и им подобные, и соли органических кислот, таких как глюкуроновая кислота или галактуроновая кислота и им подобные (см. например, Berge, S.M., et al, «Pharmaceutical Salts», Journal of Pharmaceutical Science, 1977, 66, 1-19).
Некоторые конкретные соединения настоящего изобретения содержат и основные, и кислотные функциональные группы, которые позволяют этим соединениям превращаться и в соли присоединения основания, и в соли присоединения кислот.
Нейтральные формы соединений могут быть восстановлены путем контактирования соли с основанием или кислотой и выделением предшествующего соединения обычным путем. Предшествующая форма соединения отличается от различных солевых форм определенными физическими свойствами, например растворимостью в полярных растворителях, но в других отношениях эти соли эквивалентны предшествующим формам соединения, созданного для целей настоящего изобретения.
Помимо солевых форм по настоящему изобретению предусматриваются соединения, представляющие собой формы пролекарства. Пролекарства на основе соединений данного изобретения описываются здесь как соединения, которые с легкостью подвергаются химическим превращениям в физиологических условиях и переходят в соединения данного изобретения. Кроме того, пролекарства могут быть переведены в соединения настоящего изобретения химическими и биохимическими методами в среде ex vivo. Например, пролекарства могут медленно превращаться в соединения настоящего изобретения, будучи помещенными в емкость из трансдермального лоскута подходящим ферментом или химическим реагентом.
Некоторые соединения данного изобретения могут существовать в несольватированных формах, а также и в сольватированных формах, включая и гидраты. В общем, сольватированные формы эквивалентны несольватированным формам, и их следуют считать подпадающими под объем данного изобретения. Некоторые соединения настоящего изобретения могут существовать в нескольких кристаллических или аморфных формах. В целом все физические формы эквивалентны для целей, решаемых данным изобретением, и их следует считать включенными в объем настоящего изобретения.
Некоторые соединения данного изобретения имеют асимметрические атомы углерода (оптические центры) или двойные связи; эти рацематы, диастереоизомеры, геометрические изомеры и индивидуальные изомеры также следует считать включенными в объем данного изобретения.
Соединения настоящего изобретения могут также содержать неприродное количество изотопов при одном или нескольких атомах, составляющих такие соединения. Например, соединения могут быть помечены радиоактивными изотопами, такими как, например, тритий (3Н), иод-125 (125I) или углерод-14 (14С).
Все изотопосодержащие варианты соединений настоящего изобретения, неважно - радиоактивны они или нет, включены в объем настоящего изобретения.
Общие замечания
Недавно были описаны некоторые арилсульфонамиды, предлагаемые для лечения заболеваний и болезненных состояний, возникающих из-за пролиферации аномальных клеток и повышенных уровней холестерина в плазме. См., например, РСТ публикации WO 97/30677, WO 98/05315 и WO 99/10320. Представителями этого нового класса противораковых средств являются пентафторбензолсульфонамиды, описанные в WO 98/05315.
Полагают, что эти средства оказывают свое действие за счет связывания β-тубулина и разрывания микротубулярного образования (См. публикацию по активности Т-соединений).
В последующих поданных заявках были также раскрыты и другие пентафторбензолсульфонамиды: заявка №60/090681, поданная 25 июня 1998 и 09/336062, поданная 18 июня 1999; №60/093570, поданная 20 июля 1998, и 09/353976, поданная 15 июля 1999, и №60/100888, поданная 23 сентября 1998.
Клинические испытания по оценке пентафторбензолсульфонамидов как соединений, пригодных для лечения рака, являются положительными.
Цисплатин (цис-диаминдихлорплатина (II)) представляет собой координационный комплекс с платиной, открытый в 1965 г. как цитотоксическое средство. Он имеет широкий спектр активности как противоопухолевое средство и особенно эффективен при лечении эпителиальных злокачественных опухолей. Другие координационные комплексы с платиной, изученные при клинических испытаниях, включают карбоплатин, тетраплатин, ормиплатин, ипроплатин и оксалиплатин (см. Kelland, Crit. Rev. Oncol. Hematol., 15:191-219 (1993)).
Ныне оценено действие композиции цисплатина и производного пентафторбензолсульфонамида на опухолевые ксенотрансплантаты у мышей; и совершенно неожиданно были обнаружены синергетические уровни активности.
Описание предпочтительных вариантов изобретения
Композиции
В одном аспекте настоящего изобретения предлагаются композиции, включающие противоопухолевый координационный комплекс с платиной и соединение формулы:
или их фармацевтически приемлемая соль.
В вышеприведенной формуле R представляет собой атом водорода, замещенный или незамещенный (C1-С10)-алкил или замещенный или незамещенный (С3-С6)алкенил. Ar представляет собой замещенную или незамещенную арильную группу или замещенную или незамещенную гетероарильную группу.
В предпочтительных вариантах осуществления изобретения R представляет собой атом водорода или замещенную или незамещенную (C1-C4)алкильную группу, более предпочтительны водород, метил или этил.
Также предпочтительны такие варианты, в которых Ar представляет собой замещенную арильную группу или замещенную гетероарильную группу, предпочтительно такую, в которой только одна циклическая структура (например, замещенный фенил, замещенный пиридил или замещенный пиримидил). Особенно предпочтительно, когда Ar - замещенный фенил. В тех вариантах воплощения изобретения, в которых Ar является замещенным фенилом, заместители, как правило, присутствуют в количестве от одного до трех. Предпочтительные заместители выбраны из группы, включающей: -галоген, -OR’, -OC(О)R’, -NR’R’’, -SR’, -R’, -CN, -NO2, -CO2R’, -CONR’R’’, -C(О)R’, -OC(О)NR’R’’, -NR’’C(О)R’, -NR’’C(О)2R’, -NR’-C(О)NR’’R’’’, -NH-C(NH2)=NH, -NR’C(NH2)=NH, -NH-C-(NH2)=NR’, перфтор (С1-С4)алкокси и перфтор (С1-С4)алкил, где R’,R’’ и R’’’ независимо выбраны из атома водорода, (С1-С4)алкила, незамещенного арила и гетероарила, (незамещенный арил)-(С1-С4)алкила и (незамещенный арил)окси-(С1-С4)алкила. Особенно предпочтительными заместителями являются галоген, (С1-С4)алкил, -OR’,-OC(О)R’, -NR’R’’, -CO2R’, -CONR’R’’, -C(О)R’, -OC(O)NR’R’’, -NR’’C(О)R’, -NR’’C(О)2R’, -NR’-C(О)NR’’R’’’, перфтор (С1-С4)алкокси и перфтор (С1-С4)алкил, в которых R’, R’’ и R’’’ представляют собой водород или (С1-С4)алкил. Еще более предпочтительными являются варианты, в которых Ar выбран из:
В самых предпочтительных вариантах изобретения пентафторбензолсульфонамиды, используемые в композициях, выбирают из:
Композиции настоящего изобретения содержат также противоопухолевый координационный комплекс с платиной. Примерами таких комплексов являются цисплатин, карбоплатин, тетраплатин, ормиплатин, ипроплатин, оксалиплатин и т.п. Предпочтительно координационный комплекс с платиной представляет собой цисплатин или карбоплатин, более предпочтительно - цисплатин.
Способы лечения пролиферативных заболеваний.
Данное изобретение предусматривает также и способы лечения пролиферативных заболеваний. В одном варианте лечение осуществляют, используя композицию, содержащую каждое из двух средств, описанных выше. Согласно другому варианту лечение предусматривает раздельное назначение противоопухолевого координационного комплекса с платиной и пентафторфенилсульфонамида формулы I.
i. Комбинационная композиция.
В этом варианте изобретения композицию из двух (описанных выше) средств назначают пациенту, нуждающемуся в лечении. Количество каждого средства обычно будет меньше, чем количество, которое должно производить лечебный эффект, при введении одного такого средства. Точный способ введения будет зависеть от пациента и решения врача, но предпочтительно вводить внутривенно.
ii. Композиции, используемые при последовательном введении компонентов (введение каждого компонента по отдельности).
В этом варианте изобретения описываются стандартные правила введения цисплатина (как представителя противоопухолевых координационных комплексов с платиной) и соединения I (как представителя соединений формулы I). Любой специалист в данной области поймет, что врачом могут быть произведены различные изменения в зависимости от специфики конкретных средств, отобранных для использования и режима и продолжительности введения.
Цисплатин предпочтительно вводят однократно и внутривенно в первый день периода введения соединения I, примерно 4 часа спустя после введения соединения I в первый день. Для поддержания достаточной гидратации 1 литр нормального физраствора с 20 мэкв KCl на литр и 1 мг сульфата магния вводят до и после введения цисплатина со скоростью около 250 мл/час.
Количество цисплатина при введении предпочтительно равно 25-300 мг/м2 площади поверхности тела пациента, более предпочтительно 50-150 мг/м2 и самое предпочтительное - 75-100 мг/м2. Дополнительная жидкость может быть введена для поддержания соответствующего мочеотделения. Цисплатин предпочтительно вводят вместе с 500 мл нормального физраствора, содержащего 12,5 мг маннитола, спустя один час. Или же доза цисплатина, указанная в предыдущем абзаце, может быть введена в течение 2-5-дневного периода. Вплоть до 100 мг/день/м2 площади поверхности тела пациента может быть введено ежедневно в течение пяти следующих друг за другом дней.
Спустя период около 28-42 дней, предпочтительно 28 дней, от первого дня периода введения соединения I можно проводить другой (следующий) цикл введения, при том, что соединение I вводится в первый день и во все последующие дни этого периода, а цисплатин вводится в первый день или, менее предпочтительно, в течение периода с 2-го по 5-ый день. Например, для пятидневного периода введения соединения I, однодневного периода введения цисплатина и при 28-дневном цикле лечения, лечение будет иметь место в течение 5 дней (лечение соединением I в каждый первый день после пяти и цисплатином - в первый день), с последующими далее 28-5=23 днями, в течение которых никакого лечения не назначается, с последующими пятью днями лечения в качестве старта нового цикла лечения.
Лечебные курсы могут быть продолжены до тех пор, пока не будет достигнут клинический результат или до возникновения побочных эффектов от лечения. Дозы соединения I и/или цисплатина могут быть снижены с каждым новым циклом лечения, если возникают неудовлетворительные побочные эффекты. Действительно предпочтительно постепенно отрегулировать дозу соединения I при поддерживании постоянной дозы цисплатина.
Обычным, но приемлемым побочным эффектом от действия цисплатина являются тошнота и рвота. Они могут быть смягчены введением антиэметиков (например, ондансетрона, гранисетрона, декадрона, халдола, бенадрила, ативана и др.).
Конечно, и другие формы введения обеих активных ингредиентов, в той мере, в какой это возможно, предлагаются, например, с помощью назального спрея, трансдермально с помощью суппозиториев форм длительного действия (пролонгированного выделения), путем инъекции IV и т.д. Любая форма введения будет оказывать влияние настолько долго, сколько будет выделяться из дозировки, не разрушаясь, активный ингредиент.
Эффективность лечения может быть определена с помощью специальных клинических испытаний. В таком исследовании могут быть задействованы пациенты с заметными или поддающимися оценке величины опухолями. Заметная опухоль - это такая, которая может быть оценена, по крайней мере, в двух измерениях, например, опухоль легкого, окруженная пронизанной воздухом легочной тканью, узелок на коже или поверхностный лимфоузел. Поддающаяся оценке опухоль - эта такая, которая может быть измерена в одном направлении, как, например, опухоль легкого, не полностью окруженная воздушной легочной тканью, или пальпируемая брюшная масса, или расположенная в мягкой ткани масса, которая может быть измерена в одном направлении. Считают, что опухолевые маркеры, которые, как было показано, дают высокую степень корреляции со степенью тяжести заболевания, будут также разработаны для оцениваемых (в цифрах) заболеваний, как, например, PSA для рака простаты, СА-125 для рака яичника, СА-15-3 для рака молочной железы и т.д.
Опухоль следует измерить или оценить до и после лечения с помощью каких-либо средств, обеспечивающих самое точное измерение, например СТ-сканирование, MRI - сканирование, ультразвукография и т.д. Новые опухоли или их отсутствие в предварительно облученных областях также могут использоваться для оценки противоопухолевого эффекта. Критерий для оценки результата будет аналогичен критерию WHO Handbook of Reporting Results of Cancer Treatment, WHO Offset Publication 1979, 49-World Health Organization, Geneva. Определяются следующие результаты для опухолей, оцениваемых в двух и одном измерении.
Полный отклик: полное исчезновение всех клинически определяемых злокачественных симптомов, определенное на основе двух наблюдений, произведенных с интервалом не менее чем в четыре недели.
Частичный отклик: (а) для оцененных в двух измерениях опухолей уменьшение, по крайней мере, на 50% суммарное на все продукты самых больших перпендикулярных диаметров всех оцениваемых опухолей согласно определению на основе двух наблюдений, произведенных с интервалом не менее чем в четыре недели; (b) для неизмеряемых оцениваемых опухолей уменьшение, по крайней мере, на 50% суммарно на все опухоли самого большого диаметра согласно определению на основе двух наблюдений, произведенных с интервалом не менее чем в четыре недели. В случаях, когда у пациента были множественные опухоли, не является необходимым показать частичный отклик, как определено выше, не регрессирование всех опухолей, но само отсутствие прогрессирующих опухолей и вновь возникших опухолей.
Стабильность в течении заболевания: (а) для измеряемых в двух измерениях опухолей - от менее чем 50% уменьшения до менее чем 25% увеличения на сумму продуктов самых больших перпендикулярных диаметров всех оцениваемых опухолей; (b) для неизмеряемых оцениваемых опухолей - от менее чем 50% уменьшения до менее чем 25% увеличения на сумму диаметров всех опухолей. Для (а) и (b) никаких новых опухолей не должно появляться.
Отсутствие клинического отклика, т.е. прогрессирующее заболевание определяют как увеличение более чем на 50% в продукте самых больших перпендикулярных диаметров для, по крайней мере, одной измеряемой в двух направлениях опухоли или увеличение более чем на 25% в измеряемом направлении, по крайней мере, одной не имеющей измерения оцениваемой опухоли.
Конечно, устранение или смягчение других известных симптомов рака, особенно тех, которые были перечислены выше, могут также использоваться для оценки эффективности изобретения.
Степень развития ракового заболевания должна быть оценена, т.е. опухоли подвергнуты измерению и т.д. не более чем за 14 дней до начала лечения. Эти заболевания следует заново оценить спустя 28 дней после дня №1 введения первой дозы соединения I и цисплатина. Двадцать восемь дней спустя этого первоначального введения может быть начат уже другой период введения и оценивания, осуществляемого 28 дней спустя после старта этого второго цикла. Циклы лечения могут быть продолжены, пока не будет достигнут клинический результат или неприемлемая токсичность.
Другой аспект данного изобретения состоит в лечении рака со сниженными побочными эффектами, обычно связанными с применением цисплатина. Эта цель достигается применением более низких доз двух активных ингредиентов или более короткой продолжительностью дозирования, обеспечиваемой синергетическим эффектом композиции.
Самым распространенным побочным эффектом цисплатина является нефротоксичность. Дозы, лимитирующие токсичность, будут обуславливать содержание сывороточного креатинина более чем 2,2 мг/дл, сохраняющееся в течение более двух недель от момента введения.
ПРИМЕРЫ
Пример 1
Данный пример иллюстрирует синергизм действия цисплатина и 2-фтор-1-метокси-4-(пентафторфенилсульфонамидо)бензола в виде натриевой соли против МХ-1 ксенотрансплантатов опухоли молочной железы человека у безтимусных голых мышей.
Натриевая соль 2-фтор-1-метокси-4-(пентафторфенилсульфонамидо)бензола (Соединение I) предотвращает полимеризацию микротрубочек за счет ковалентного связывания с β-тубулином и ингибирует рост и возможность клонирования у культивируемых клеток различных опухолей. На его активность не влияет фенотипическая устойчивость к различным лекарственным средствам (MDR).
Установлено, что доза соединения I 30 мг/кг/час, введенная внутривенно в течение 4 часов, весьма эффективна для ингибирования роста МХ-1 ксенотрансплантатов опухоли молочной железы человека у безтимусных бесшерстных мышей. Цисплатин также очень эффективен в отношении подавления этой опухоли. Действие обоих средств сопровождалось потерей веса тела.
Назначение полуоптимальных доз цисплатина 3 мг/кг внутривенно в виде болюса или 15 мг/кг/час соединения 1 внутривенной инфузией в течение 4 часов сравнивали по эффективности воздействия на МХ-1 с одновременным введением средств. Совместное введение соединения I и цисплатина привело к значительному повышению эффективности воздействия по сравнению с использованием каждого лекарства по отдельности (см. Фиг.1). Такое одновременное назначение полуоптимальных доз приводило к гораздо меньшей потере веса тела и смертности, чем наблюдаемые при раздельном лечении указанными соединениями в эффективной дозе. Этот факт указывает, что введение комбинации полуоптимиальных доз соединения I и цисплатина приводит к синергетическому ингибированию роста опухоли при меньшей лекарственной токсичности.
Аналогичные результаты были получены для N-(1-метокси-4-(пентафторфенилсульфонамидо)бензолмочевины (Соединение 2, см. Фиг.2). Композиции из соединения 2 и либо 5-фторурацила (Фиг.3), либо адриамицина (Фиг.4) не показывают таких результатов.
На все опубликованные источники и патентные документы, указанные в данном описании, были специально или отдельно приведены ссылки. Несмотря на то, что заявленное изобретение описано подробно с использованием подтверждающих примеров, способствующих более ясному пониманию изложенного, специалисту в данной области будет очевидно, что в соответствии с описанным данным изобретением возможны некоторые его изменения и модификации без ущерба для идеи или объема нижеследующей формулы изобретения.
Claims (13)
2. Композиция по п.1, в которой указанный противоопухолевый координационный комплекс с платиной выбран из группы, состоящей из цисплатина, карбоплатина, тетраплатина, ормиплатина, ипроплатина и оксалиплатина.
3. Композиция по п.1, в которой указанный противоопухолевый координационный комплекс с платиной представляет собой цисплатин.
6. Способ лечения пролиферативного заболевания, предусматривающий введение лицу, нуждающемуся в таком лечении, эффективного количества композиции по п.1.
8. Способ по п.7, в котором противоопухолевый координационный комплекс с платиной выбран из группы, состоящей из цисплатина, карбоплатина, тетраплатина, ормиплатина, ипроплатина и оксалиплатина.
10. Способ по п.7, в котором указанную первую дозу и указанную вторую дозу вводят последовательно.
11. Способ по п.10, в котором указанную вторую дозу вводят прежде указанной первой дозы.
12. Способ по п.10, в котором указанную первую дозу вводят прежде указанной второй дозы.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US14643699P | 1999-07-29 | 1999-07-29 | |
| US60/146,436 | 1999-07-29 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2002105374A RU2002105374A (ru) | 2004-01-10 |
| RU2268054C2 true RU2268054C2 (ru) | 2006-01-20 |
Family
ID=22517356
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2002105374/15A RU2268054C2 (ru) | 1999-07-29 | 2000-07-27 | Сочетанная терапия с использованием пентафторбензолсульфонамидов |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US6355628B1 (ru) |
| EP (1) | EP1206256B8 (ru) |
| JP (1) | JP2003505513A (ru) |
| KR (1) | KR100685059B1 (ru) |
| CN (1) | CN1181819C (ru) |
| AT (1) | ATE294574T1 (ru) |
| AU (1) | AU775305B2 (ru) |
| CA (1) | CA2380078C (ru) |
| DE (1) | DE60019937T2 (ru) |
| DK (1) | DK1206256T3 (ru) |
| ES (1) | ES2241639T3 (ru) |
| IL (2) | IL147890A0 (ru) |
| PT (1) | PT1206256E (ru) |
| RU (1) | RU2268054C2 (ru) |
| WO (1) | WO2001008693A2 (ru) |
| ZA (1) | ZA200200889B (ru) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EA001367B1 (ru) * | 1996-02-22 | 2001-02-26 | Туларик, Инк. | Пентафторбензолсульфонамиды и их аналоги |
| EP0939627B1 (en) * | 1996-07-19 | 2003-09-10 | Tularik, Inc. | Pentafluorobenzenesulfonamides and analogs |
| EA003924B1 (ru) * | 1998-09-23 | 2003-10-30 | Туларик, Инк. | Арилсульфонанилидмочевины |
| AU2002234165A1 (en) | 2000-11-03 | 2002-05-27 | Tularik, Inc. | Combination therapy using pentafluorobenzenesulfonamides and antineoplastic agents |
| US20050250854A1 (en) * | 2000-11-03 | 2005-11-10 | Amgen Inc. | Combination therapy using pentafluorobenzenesulfonamides and antineoplastic agents |
| FR2834641B1 (fr) * | 2002-01-14 | 2005-04-22 | Ct Regional De Lutte Contre Le | Protection de la neurotoxicite de l'oxaliplatine par administration de calcium et de magnesium |
| CN1968685B (zh) * | 2003-11-19 | 2014-05-14 | 张立新 | 互动药物的筛选 |
| US10238831B2 (en) | 2013-09-08 | 2019-03-26 | Qool Therapeutics, Inc. | Temperature measurement and feedback for therapeutic hypothermia |
| EP3261593B1 (en) | 2015-02-23 | 2021-11-03 | Qool Therapeutics, Inc. | Systems and methods for endotracheal delivery of frozen particles |
| US11186549B2 (en) | 2017-08-29 | 2021-11-30 | Rutgers, The State University Of New Jersey | Therapeutic indazoles |
| EP3684754A4 (en) * | 2017-09-21 | 2021-06-02 | Dalriada Therapeutics Inc. | PENTAFLUOROPHENYL SULFONAMIDE COMPOUNDS, COMPOSITIONS AND ASSOCIATED USES |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1955207A (en) | 1931-09-16 | 1934-04-17 | Ig Farbenindustrie Ag | Mothproofing agent |
| US2402623A (en) | 1943-06-24 | 1946-06-25 | Rohm & Haas | Nu-nitroaryl haloarylsulphonamides |
| CH362688A (de) | 1957-09-10 | 1962-06-30 | Geigy Ag J R | Verfahren zur Herstellung von neuen Arylsulfonarylamiden |
| GB1242057A (en) | 1968-07-04 | 1971-08-11 | Ici Ltd | Derivatives of 4-hydroxytetrafluoropyridine and the use thereof as plant growth regulators |
| NL174644C (nl) | 1970-04-13 | 1984-07-16 | Minnesota Mining & Mfg | Werkwijze ter bereiding van een herbicide verbinding; tevens werkwijze voor de bereiding van een preparaat met herbicide werking. |
| DE3623184A1 (de) | 1986-07-10 | 1988-01-14 | Kali Chemie Ag | Verfahren zur herstellung von n-fluorsulfonamiden |
| US4883914A (en) | 1987-08-17 | 1989-11-28 | American Cyanamid Company | Benzenesulfonyl carboxamide compounds useful as herbicidal agents |
| DE3804990A1 (de) | 1988-02-18 | 1989-08-31 | Basf Ag | Herbizid wirksame, heterocyclisch substituierte sulfonamide |
| FR2645537B1 (fr) | 1989-04-05 | 1994-03-04 | Fabre Medicament Pierre | Nouveaux sulfonamides derives d'acides benzocycliques ou benzoheterocycliques, leur preparation et leur application en therapeutique |
| FR2665440B1 (fr) | 1990-07-31 | 1994-02-04 | Lipha | Nouveaux cycloalkylsulfonamides substitues, procedes de preparation et medicaments les contenant. |
| US5189211A (en) | 1990-08-01 | 1993-02-23 | Taisho Pharmaceutical Co., Ltd. | Sulfonamide derivatives |
| ATE167473T1 (de) | 1990-08-20 | 1998-07-15 | Eisai Co Ltd | Sulfonamid-derivate |
| WO1996040629A1 (en) | 1995-06-07 | 1996-12-19 | Sugen, Inc. | Tyrphostin-like compounds for the treatment of cell proliferative disorders or cell differentiation disorders |
| EA001367B1 (ru) | 1996-02-22 | 2001-02-26 | Туларик, Инк. | Пентафторбензолсульфонамиды и их аналоги |
| EP0939627B1 (en) * | 1996-07-19 | 2003-09-10 | Tularik, Inc. | Pentafluorobenzenesulfonamides and analogs |
| DK0932402T3 (da) * | 1996-10-15 | 2004-11-08 | Searle Llc | Metode til anvendelse af cyclooxygenase-2-inhibitorer ved behandling og forebyggelse af neoplasi |
| TR199901703T2 (xx) * | 1996-11-19 | 2000-07-21 | G.D. Searle & Co. | Siklooksijenaz-2 inhibit�rlerini anti-anjiyojenik ajanlar olarak kullanma y�ntemi. |
| US5773236A (en) | 1997-04-25 | 1998-06-30 | Molecule Probes, Inc. | Assay for glutathiane transferase using polyhaloaryl-substituted reporter molecules |
| CA2335559A1 (en) * | 1998-06-25 | 1999-12-29 | Tularik Inc. | Arylsulfonanilide phosphates |
| EA003924B1 (ru) * | 1998-09-23 | 2003-10-30 | Туларик, Инк. | Арилсульфонанилидмочевины |
| WO2000035865A2 (en) * | 1998-12-17 | 2000-06-22 | Tularik Inc. | Tubulin-binding agents |
| CO5170498A1 (es) * | 1999-05-28 | 2002-06-27 | Abbott Lab | Biaril sulfonamidas son utiles como inhibidores de proliferacion celular |
-
2000
- 2000-07-27 PT PT00953755T patent/PT1206256E/pt unknown
- 2000-07-27 ES ES00953755T patent/ES2241639T3/es not_active Expired - Lifetime
- 2000-07-27 DE DE60019937T patent/DE60019937T2/de not_active Expired - Fee Related
- 2000-07-27 CA CA002380078A patent/CA2380078C/en not_active Expired - Fee Related
- 2000-07-27 JP JP2001513423A patent/JP2003505513A/ja active Pending
- 2000-07-27 AT AT00953755T patent/ATE294574T1/de not_active IP Right Cessation
- 2000-07-27 WO PCT/US2000/020763 patent/WO2001008693A2/en active IP Right Grant
- 2000-07-27 AU AU66152/00A patent/AU775305B2/en not_active Ceased
- 2000-07-27 IL IL14789000A patent/IL147890A0/xx active IP Right Grant
- 2000-07-27 DK DK00953755T patent/DK1206256T3/da active
- 2000-07-27 KR KR1020027001254A patent/KR100685059B1/ko not_active IP Right Cessation
- 2000-07-27 EP EP00953755A patent/EP1206256B8/en not_active Expired - Lifetime
- 2000-07-27 CN CNB00810977XA patent/CN1181819C/zh not_active Expired - Fee Related
- 2000-07-27 US US09/627,041 patent/US6355628B1/en not_active Expired - Fee Related
- 2000-07-27 RU RU2002105374/15A patent/RU2268054C2/ru not_active IP Right Cessation
-
2002
- 2002-01-29 IL IL147890A patent/IL147890A/en not_active IP Right Cessation
- 2002-01-31 ZA ZA200200889A patent/ZA200200889B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP2003505513A (ja) | 2003-02-12 |
| EP1206256B8 (en) | 2005-06-29 |
| EP1206256B1 (en) | 2005-05-04 |
| AU775305B2 (en) | 2004-07-29 |
| CA2380078C (en) | 2008-05-06 |
| CN1181819C (zh) | 2004-12-29 |
| IL147890A0 (en) | 2002-08-14 |
| IL147890A (en) | 2007-07-04 |
| DE60019937D1 (de) | 2005-06-09 |
| DK1206256T3 (da) | 2005-08-15 |
| KR100685059B1 (ko) | 2007-02-22 |
| CA2380078A1 (en) | 2001-02-08 |
| RU2002105374A (ru) | 2004-01-10 |
| PT1206256E (pt) | 2005-09-30 |
| WO2001008693A2 (en) | 2001-02-08 |
| EP1206256A2 (en) | 2002-05-22 |
| WO2001008693A3 (en) | 2001-05-25 |
| US6355628B1 (en) | 2002-03-12 |
| ZA200200889B (en) | 2003-03-26 |
| ES2241639T3 (es) | 2005-11-01 |
| AU6615200A (en) | 2001-02-19 |
| CN1367690A (zh) | 2002-09-04 |
| KR20020050225A (ko) | 2002-06-26 |
| DE60019937T2 (de) | 2006-05-04 |
| ATE294574T1 (de) | 2005-05-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2587013C2 (ru) | Комбинированная химиотерапия | |
| RU2268054C2 (ru) | Сочетанная терапия с использованием пентафторбензолсульфонамидов | |
| IL167633A (en) | Use of zd6474 combined with gemcitabine in the preparation of medicaments and as medicaments for the production of an angiogenic and/or vascular permeability reducing effect and pharmaceutical compositions and kits comprising such combination | |
| JP2010159271A (ja) | エポシロンを含有する組合せ剤およびその医薬上の使用 | |
| BG107843A (bg) | Ефективно антитуморно лечение | |
| US6822001B2 (en) | Combination therapy using pentafluorobenzenesulfonamides and antineoplastic agents | |
| JP2015533165A (ja) | 組み合わせ | |
| AU2002328921A1 (en) | Combinations comprising epothilones and pharmaceutical uses thereof | |
| WO2007132221A1 (en) | Combined anticancer pyrimidine-thiazole aurora kinase inhibitors | |
| RU2284818C2 (ru) | Комбинированная химиотерапия | |
| JP2004532260A (ja) | デメチルカンタリジンをプラチナ含有抗がん剤と組み合わせて含む組成物およびその用途 | |
| TWI307628B (en) | Use of zd0473 in combination with a non-platinum based anti-cancer agent | |
| KR20060036058A (ko) | 결장직장암의 치료를 위한 혈관 손상 활성을 갖는 5fu,cpt-11 또는 5-fu 및 cpt-11과 함께 zd6126을포함하는 조성물 | |
| RU2279277C2 (ru) | Лечение разделенными дозами агентов с сосудоразрушающей активностью | |
| AU2008203233B2 (en) | Combinations comprising epothilones and pharmaceutical uses thereof | |
| KR20110104932A (ko) | Ave8062 및 도세탁셀이 조합된 항종양 조합물 | |
| JPH0288524A (ja) | 抗腫瘍剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20090728 |