RU2073685C1 - Полипептиды или их соли, фармацевтическая композиция, обладающая противовирусной активностью в отношении вируса иммунодефицита человека - Google Patents
Полипептиды или их соли, фармацевтическая композиция, обладающая противовирусной активностью в отношении вируса иммунодефицита человека Download PDFInfo
- Publication number
- RU2073685C1 RU2073685C1 SU915052258A SU5052258A RU2073685C1 RU 2073685 C1 RU2073685 C1 RU 2073685C1 SU 915052258 A SU915052258 A SU 915052258A SU 5052258 A SU5052258 A SU 5052258A RU 2073685 C1 RU2073685 C1 RU 2073685C1
- Authority
- RU
- Russia
- Prior art keywords
- cys
- polypeptide
- polypeptides
- positions
- arg
- Prior art date
Links
- 108090000765 processed proteins & peptides Proteins 0.000 title claims abstract description 104
- 102000004196 processed proteins & peptides Human genes 0.000 title claims abstract description 87
- 229920001184 polypeptide Polymers 0.000 title claims abstract description 85
- 150000003839 salts Chemical class 0.000 title claims abstract description 16
- 241000725303 Human immunodeficiency virus Species 0.000 title claims abstract description 15
- 230000000840 anti-viral effect Effects 0.000 title claims abstract description 14
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 5
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 claims abstract description 13
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 claims description 16
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 claims description 13
- 239000004475 Arginine Substances 0.000 claims description 9
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 claims description 9
- 150000001875 compounds Chemical class 0.000 claims description 9
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 claims description 8
- 239000004472 Lysine Substances 0.000 claims description 8
- 125000000539 amino acid group Chemical group 0.000 claims description 7
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 claims description 5
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 claims description 5
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 claims description 4
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 claims description 3
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 claims description 3
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 claims description 3
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 claims description 3
- 229960000310 isoleucine Drugs 0.000 claims description 3
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 claims description 3
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 claims description 3
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 claims description 3
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 claims description 3
- 239000004474 valine Substances 0.000 claims description 3
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 claims description 2
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 claims description 2
- 235000004279 alanine Nutrition 0.000 claims description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 2
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 claims description 2
- 125000000430 tryptophan group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C2=C([H])C([H])=C([H])C([H])=C12 0.000 claims description 2
- 238000000034 method Methods 0.000 abstract description 44
- 230000000694 effects Effects 0.000 abstract description 12
- 230000015572 biosynthetic process Effects 0.000 abstract description 9
- 239000000126 substance Substances 0.000 abstract description 8
- 239000003814 drug Substances 0.000 abstract description 7
- 238000010532 solid phase synthesis reaction Methods 0.000 abstract description 7
- 238000003786 synthesis reaction Methods 0.000 abstract description 7
- 230000003647 oxidation Effects 0.000 abstract description 6
- 238000007254 oxidation reaction Methods 0.000 abstract description 6
- 239000013543 active substance Substances 0.000 abstract 1
- 239000011347 resin Substances 0.000 description 29
- 229920005989 resin Polymers 0.000 description 29
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 27
- 235000001014 amino acid Nutrition 0.000 description 22
- 229940024606 amino acid Drugs 0.000 description 22
- 229920000642 polymer Polymers 0.000 description 22
- 150000001413 amino acids Chemical class 0.000 description 21
- 125000006239 protecting group Chemical group 0.000 description 19
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 17
- VEFCXXLAPLJBFG-UHFFFAOYSA-N n,n-dimethoxy-1,1-diphenylmethanamine Chemical compound C=1C=CC=CC=1C(N(OC)OC)C1=CC=CC=C1 VEFCXXLAPLJBFG-UHFFFAOYSA-N 0.000 description 16
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 15
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 14
- 238000006482 condensation reaction Methods 0.000 description 14
- -1 tert-butylthio Chemical group 0.000 description 14
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 13
- 239000000243 solution Substances 0.000 description 13
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 12
- DHHKPEUQJIEKOA-UHFFFAOYSA-N tert-butyl 2-[6-(nitromethyl)-6-bicyclo[3.2.0]hept-3-enyl]acetate Chemical compound C1C=CC2C(CC(=O)OC(C)(C)C)(C[N+]([O-])=O)CC21 DHHKPEUQJIEKOA-UHFFFAOYSA-N 0.000 description 11
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 10
- 239000000203 mixture Substances 0.000 description 10
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 9
- 235000018417 cysteine Nutrition 0.000 description 9
- 239000002158 endotoxin Substances 0.000 description 9
- VVQIIIAZJXTLRE-QMMMGPOBSA-N (2s)-2-amino-6-[(2-methylpropan-2-yl)oxycarbonylamino]hexanoic acid Chemical compound CC(C)(C)OC(=O)NCCCC[C@H](N)C(O)=O VVQIIIAZJXTLRE-QMMMGPOBSA-N 0.000 description 8
- 235000009697 arginine Nutrition 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 241001529572 Chaceon affinis Species 0.000 description 7
- 238000003776 cleavage reaction Methods 0.000 description 7
- 230000007017 scission Effects 0.000 description 7
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- 125000004202 aminomethyl group Chemical group [H]N([H])C([H])([H])* 0.000 description 6
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 5
- ODKSFYDXXFIFQN-BYPYZUCNSA-N L-arginine Chemical compound OC(=O)[C@@H](N)CCCN=C(N)N ODKSFYDXXFIFQN-BYPYZUCNSA-N 0.000 description 5
- 230000036436 anti-hiv Effects 0.000 description 5
- 210000004027 cell Anatomy 0.000 description 5
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 5
- 238000011161 development Methods 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- FEMOMIGRRWSMCU-UHFFFAOYSA-N ninhydrin Chemical compound C1=CC=C2C(=O)C(O)(O)C(=O)C2=C1 FEMOMIGRRWSMCU-UHFFFAOYSA-N 0.000 description 5
- 125000006850 spacer group Chemical group 0.000 description 5
- 125000003396 thiol group Chemical group [H]S* 0.000 description 5
- HBOMLICNUCNMMY-XLPZGREQSA-N zidovudine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](N=[N+]=[N-])C1 HBOMLICNUCNMMY-XLPZGREQSA-N 0.000 description 5
- 229960002555 zidovudine Drugs 0.000 description 5
- WTKQMHWYSBWUBE-UHFFFAOYSA-N (3-nitropyridin-2-yl) thiohypochlorite Chemical compound [O-][N+](=O)C1=CC=CN=C1SCl WTKQMHWYSBWUBE-UHFFFAOYSA-N 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- 108010070741 Tachypleus tridentatus tachyplesin peptide Proteins 0.000 description 4
- 125000003275 alpha amino acid group Chemical group 0.000 description 4
- 150000001408 amides Chemical group 0.000 description 4
- 125000003277 amino group Chemical group 0.000 description 4
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 230000003013 cytotoxicity Effects 0.000 description 4
- 231100000135 cytotoxicity Toxicity 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 4
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 4
- KCCSOSBUHIQUOT-UHFFFAOYSA-N n,n'-di(propan-2-yl)methanediimine;1-hydroxybenzotriazole Chemical compound CC(C)N=C=NC(C)C.C1=CC=C2N(O)N=NC2=C1 KCCSOSBUHIQUOT-UHFFFAOYSA-N 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- ZJQFYZCNRTZAIM-PMXBASNASA-N tachyplesin Chemical compound C([C@H]1C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@H](C(N[C@H]2CSSC[C@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=3C=CC=CC=3)NC(=O)[C@@H](NC(=O)[C@H](CC=3C4=CC=CC=C4NC=3)NC(=O)[C@@H](N)CCCCN)CSSC[C@H](NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC=3C=CC(O)=CC=3)NC2=O)C(=O)N[C@@H](CCCNC(N)=N)C(N)=O)C(=O)N1)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZJQFYZCNRTZAIM-PMXBASNASA-N 0.000 description 4
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 4
- BDNKZNFMNDZQMI-UHFFFAOYSA-N 1,3-diisopropylcarbodiimide Chemical compound CC(C)N=C=NC(C)C BDNKZNFMNDZQMI-UHFFFAOYSA-N 0.000 description 3
- 208000030507 AIDS Diseases 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 3
- 125000001433 C-terminal amino-acid group Chemical group 0.000 description 3
- QOSSAOTZNIDXMA-UHFFFAOYSA-N Dicylcohexylcarbodiimide Chemical compound C1CCCCC1N=C=NC1CCCCC1 QOSSAOTZNIDXMA-UHFFFAOYSA-N 0.000 description 3
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 3
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 3
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 3
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 3
- 239000002259 anti human immunodeficiency virus agent Substances 0.000 description 3
- 229940124411 anti-hiv antiviral agent Drugs 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- BGRWYRAHAFMIBJ-UHFFFAOYSA-N diisopropylcarbodiimide Natural products CC(C)NC(=O)NC(C)C BGRWYRAHAFMIBJ-UHFFFAOYSA-N 0.000 description 3
- MGHPNCMVUAKAIE-UHFFFAOYSA-N diphenylmethanamine Chemical compound C=1C=CC=CC=1C(N)C1=CC=CC=C1 MGHPNCMVUAKAIE-UHFFFAOYSA-N 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 3
- 208000015181 infectious disease Diseases 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- SHDMMLFAFLZUEV-UHFFFAOYSA-N n-methyl-1,1-diphenylmethanamine Chemical compound C=1C=CC=CC=1C(NC)C1=CC=CC=C1 SHDMMLFAFLZUEV-UHFFFAOYSA-N 0.000 description 3
- OQYBTXFHTQYWCZ-DEOSSOPVSA-N (2r)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-3-[(4-methylphenyl)methylsulfanyl]propanoic acid Chemical compound C1=CC(C)=CC=C1CSC[C@@H](C(O)=O)NC(=O)OCC1C2=CC=CC=C2C2=CC=CC=C21 OQYBTXFHTQYWCZ-DEOSSOPVSA-N 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- KRHYYFGTRYWZRS-UHFFFAOYSA-N Fluorane Chemical compound F KRHYYFGTRYWZRS-UHFFFAOYSA-N 0.000 description 2
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 229920005654 Sephadex Polymers 0.000 description 2
- 239000012507 Sephadex™ Substances 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- 150000008065 acid anhydrides Chemical class 0.000 description 2
- 239000004480 active ingredient Substances 0.000 description 2
- 230000000844 anti-bacterial effect Effects 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 244000309464 bull Species 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- 238000010511 deprotection reaction Methods 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- DNJIEGIFACGWOD-UHFFFAOYSA-N ethanethiol Chemical compound CCS DNJIEGIFACGWOD-UHFFFAOYSA-N 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 238000004992 fast atom bombardment mass spectroscopy Methods 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 238000002523 gelfiltration Methods 0.000 description 2
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 229910000040 hydrogen fluoride Inorganic materials 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 235000014705 isoleucine Nutrition 0.000 description 2
- 235000005772 leucine Nutrition 0.000 description 2
- RLSSMJSEOOYNOY-UHFFFAOYSA-N m-cresol Chemical compound CC1=CC=CC(O)=C1 RLSSMJSEOOYNOY-UHFFFAOYSA-N 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 235000006109 methionine Nutrition 0.000 description 2
- 229930182817 methionine Natural products 0.000 description 2
- 230000001590 oxidative effect Effects 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 235000019260 propionic acid Nutrition 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- FTVLMFQEYACZNP-UHFFFAOYSA-N trimethylsilyl trifluoromethanesulfonate Chemical compound C[Si](C)(C)OS(=O)(=O)C(F)(F)F FTVLMFQEYACZNP-UHFFFAOYSA-N 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 235000014393 valine Nutrition 0.000 description 2
- UMRUUWFGLGNQLI-QFIPXVFZSA-N (2s)-2-(9h-fluoren-9-ylmethoxycarbonylamino)-6-[(2-methylpropan-2-yl)oxycarbonylamino]hexanoic acid Chemical compound C1=CC=C2C(COC(=O)N[C@@H](CCCCNC(=O)OC(C)(C)C)C(O)=O)C3=CC=CC=C3C2=C1 UMRUUWFGLGNQLI-QFIPXVFZSA-N 0.000 description 1
- DYWUPCCKOVTCFZ-LBPRGKRZSA-N (2s)-2-amino-3-[1-[(2-methylpropan-2-yl)oxycarbonyl]indol-3-yl]propanoic acid Chemical compound C1=CC=C2N(C(=O)OC(C)(C)C)C=C(C[C@H](N)C(O)=O)C2=C1 DYWUPCCKOVTCFZ-LBPRGKRZSA-N 0.000 description 1
- OIXLLKLZKCBCPS-RZVRUWJTSA-N (2s)-2-azanyl-5-[bis(azanyl)methylideneamino]pentanoic acid Chemical compound OC(=O)[C@@H](N)CCCNC(N)=N.OC(=O)[C@@H](N)CCCNC(N)=N OIXLLKLZKCBCPS-RZVRUWJTSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical compound C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- IPDWABJNXLNLRA-UHFFFAOYSA-N 2,3-dihydroxybutanedioic acid;2-hydroxypropane-1,2,3-tricarboxylic acid Chemical compound OC(=O)C(O)C(O)C(O)=O.OC(=O)CC(O)(C(O)=O)CC(O)=O IPDWABJNXLNLRA-UHFFFAOYSA-N 0.000 description 1
- WFIYPADYPQQLNN-UHFFFAOYSA-N 2-[2-(4-bromopyrazol-1-yl)ethyl]isoindole-1,3-dione Chemical compound C1=C(Br)C=NN1CCN1C(=O)C2=CC=CC=C2C1=O WFIYPADYPQQLNN-UHFFFAOYSA-N 0.000 description 1
- DOUWDRHKWNWOIT-UHFFFAOYSA-N 2-[3-[1-amino-2-(9H-fluoren-9-ylmethoxy)-1-(4-methoxyphenyl)-2-oxoethyl]-4-methoxyphenyl]propanoic acid Chemical compound C(=O)(OCC1C2=CC=CC=C2C2=CC=CC=C12)C(C1=CC=C(C=C1)OC)(C=1C=C(C=CC=1OC)C(C(=O)O)C)N DOUWDRHKWNWOIT-UHFFFAOYSA-N 0.000 description 1
- YVOOPGWEIRIUOX-UHFFFAOYSA-N 2-azanyl-3-sulfanyl-propanoic acid Chemical compound SCC(N)C(O)=O.SCC(N)C(O)=O YVOOPGWEIRIUOX-UHFFFAOYSA-N 0.000 description 1
- KIUMMUBSPKGMOY-UHFFFAOYSA-N 3,3'-Dithiobis(6-nitrobenzoic acid) Chemical compound C1=C([N+]([O-])=O)C(C(=O)O)=CC(SSC=2C=C(C(=CC=2)[N+]([O-])=O)C(O)=O)=C1 KIUMMUBSPKGMOY-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- 125000004217 4-methoxybenzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1OC([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000006181 4-methyl benzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])C([H])([H])* 0.000 description 1
- GANZODCWZFAEGN-UHFFFAOYSA-N 5-mercapto-2-nitro-benzoic acid Chemical compound OC(=O)C1=CC(S)=CC=C1[N+]([O-])=O GANZODCWZFAEGN-UHFFFAOYSA-N 0.000 description 1
- QNAYBMKLOCPYGJ-UHFFFAOYSA-N Alanine Chemical compound CC([NH3+])C([O-])=O QNAYBMKLOCPYGJ-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- KCBAMQOKOLXLOX-BSZYMOERSA-N CC1=C(SC=N1)C2=CC=C(C=C2)[C@H](C)NC(=O)[C@@H]3C[C@H](CN3C(=O)[C@H](C(C)(C)C)NC(=O)CCCCCCCCCCNCCCONC(=O)C4=C(C(=C(C=C4)F)F)NC5=C(C=C(C=C5)I)F)O Chemical compound CC1=C(SC=N1)C2=CC=C(C=C2)[C@H](C)NC(=O)[C@@H]3C[C@H](CN3C(=O)[C@H](C(C)(C)C)NC(=O)CCCCCCCCCCNCCCONC(=O)C4=C(C(=C(C=C4)F)F)NC5=C(C=C(C=C5)I)F)O KCBAMQOKOLXLOX-BSZYMOERSA-N 0.000 description 1
- 241000239216 Carcinoscorpius Species 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- LUJVWKKYHSLULQ-ZKWXMUAHSA-N Gly-Ile-Cys Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](CS)C(=O)O)NC(=O)CN LUJVWKKYHSLULQ-ZKWXMUAHSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 208000031886 HIV Infections Diseases 0.000 description 1
- 208000037357 HIV infectious disease Diseases 0.000 description 1
- 206010061598 Immunodeficiency Diseases 0.000 description 1
- 208000029462 Immunodeficiency disease Diseases 0.000 description 1
- 125000000510 L-tryptophano group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C(C([H])([H])[C@@]([H])(C(O[H])=O)N([H])[*])C2=C1[H] 0.000 description 1
- 102000002704 Leucyl aminopeptidase Human genes 0.000 description 1
- 108010004098 Leucyl aminopeptidase Proteins 0.000 description 1
- SVJRVFPSHPGWFF-DCAQKATOSA-N Lys-Cys-Arg Chemical compound [H]N[C@@H](CCCCN)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O SVJRVFPSHPGWFF-DCAQKATOSA-N 0.000 description 1
- DZQYZKPINJLLEN-KKUMJFAQSA-N Lys-Cys-Tyr Chemical compound C1=CC(=CC=C1C[C@@H](C(=O)O)NC(=O)[C@H](CS)NC(=O)[C@H](CCCCN)N)O DZQYZKPINJLLEN-KKUMJFAQSA-N 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 241000238124 Paralithodes camtschaticus Species 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 241000239222 Tachypleus Species 0.000 description 1
- HXMJXDNSFVNSEH-IHPCNDPISA-N Trp-Cys-Tyr Chemical compound C1=CC=C2C(=C1)C(=CN2)C[C@@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC3=CC=C(C=C3)O)C(=O)O)N HXMJXDNSFVNSEH-IHPCNDPISA-N 0.000 description 1
- 208000036142 Viral infection Diseases 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 238000005273 aeration Methods 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229920003180 amino resin Polymers 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 125000005605 benzo group Chemical group 0.000 description 1
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- IYYIVELXUANFED-UHFFFAOYSA-N bromo(trimethyl)silane Chemical compound C[Si](C)(C)Br IYYIVELXUANFED-UHFFFAOYSA-N 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical compound C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- MKRTXPORKIRPDG-UHFFFAOYSA-N diphenylphosphoryl azide Chemical compound C=1C=CC=CC=1P(=O)(N=[N+]=[N-])C1=CC=CC=C1 MKRTXPORKIRPDG-UHFFFAOYSA-N 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- YAGKRVSRTSUGEY-UHFFFAOYSA-N ferricyanide Chemical compound [Fe+3].N#[C-].N#[C-].N#[C-].N#[C-].N#[C-].N#[C-] YAGKRVSRTSUGEY-UHFFFAOYSA-N 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 210000003677 hemocyte Anatomy 0.000 description 1
- 238000011141 high resolution liquid chromatography Methods 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 230000007813 immunodeficiency Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000005342 ion exchange Methods 0.000 description 1
- 229920006008 lipopolysaccharide Polymers 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 229940100688 oral solution Drugs 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 1
- 238000004007 reversed phase HPLC Methods 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 235000004400 serine Nutrition 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000011146 sterile filtration Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000005931 tert-butyloxycarbonyl group Chemical group [H]C([H])([H])C(OC(*)=O)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 125000002088 tosyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])S(*)(=O)=O 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- ITMCEJHCFYSIIV-UHFFFAOYSA-N triflic acid Chemical compound OS(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-N 0.000 description 1
- 125000002221 trityl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C([*])(C1=C(C(=C(C(=C1[H])[H])[H])[H])[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 239000006216 vaginal suppository Substances 0.000 description 1
- 125000002987 valine group Chemical group [H]N([H])C([H])(C(*)=O)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 230000009385 viral infection Effects 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Virology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Oncology (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Communicable Diseases (AREA)
- Tropical Medicine & Parasitology (AREA)
- AIDS & HIV (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Abstract
Назначение: в биохимии и медицине. Сущность изобретения: полипептиды формулы I: А1-Тrр-Сys-А2-А3 Lys-Cys-A2-A3-Gly-A4Cys-A2-А3-Сys-Аrg NH2, где A = H, Lys, Arg; A2 = Tyr, Ple, Trр; A3 = Arg, Lys; А4 = Ala, Val, Leu, Ile, Ser, Met и две пары цистеиновых остатков в положениях 3- и 16- и положениях 7- и 12- могут быть соединены дисульфидным мостиком -S-S- или их соли; получены при использовании твердофазного метода синтеза, замыкание дисульфидных мостиков между 3- и 16- и 7-и 12- остатками цистеина осуществляют при химическом окислении на воздухе; фармацевтическая композиция, обладающая противовирусной активностью в отношении вируса иммунодефицита человека, содержащая в качестве активного начала эффективное количество полипептида 1 или его соли. 2 с.п. ф-лы, 4 табл., 4 ил.
Description
Настоящее изобретение относится к новому полипептиду или его соли. Более конкретно, данное изобретение относится к новому полипептиду, проявляющему сильное сродство с липополисахаридами, в частности эндотоксинами, и имеющему улучшенную противобактериальную активность и улучшенную противовирусную активность, его фармацевтически приемлемой соли, а также анти-ВИЧ средству, содержащему в качестве эффективного компонента данный полипептид.
На сегодняшний день, как показано в следующих литературных источниках, были приведены Nakamura, Iwanaga, Niwa, et al. полипептиды (Tachyplesin и PoIypgemusin), проявляющие сродство с эндотоксинами и полученные из камчатских крабов, а также их фармакологические свойства ( J. Biol. Chem. 263, 16709-16713 (1988); Опубликованная прошедшая экспертизу заявка на патент N 500194/1990; Chem. Pharm. BuII. 37, 2661-2664 (1989); Выложенная японская патентная публикация N 53799/1990; Выложенная японская патентная публикация N 152987/1990; Выложенная японская патентная публикация N 167230/1990; J. Biochem. 106- 663-668 (1989); Taicha (Metabolism), 26, 310-311 (1989).
Что касается полипептидов, имеющих сродство с эндотоксинами, выделенными из камчатских крабов (род Tachypleus, род Lumulus и род Carcinoscorpius), то существуют пять структурных аналогов и каждый из них представляет собой полипептид, имеющий циклическую структуру, включающую 17 или 18 натуральных аминокислот. Кроме того, эти полипептиды проявляют крайне аналогичные свойства и такой полипептид является весьма интересным в качестве ключевых веществ, посредством которых камчатские крабы способны адаптироваться к изменениям их внешней и сохранять свой вид от древних времен до наших дней в качестве живого ископаемого.
С другой стороны, в отношении сохранения существования человека, представители которого чрезвычайно дифференцированы, требуются лекарственные средства, которые, как ожидают, имеют профилактическое или терапевтическое воздействие на синдром приобретенного иммунодефицита (СПИД), вызванный заражением вирусом человеческого иммунодефицита (ВИЧ).
Заявитель обратил внимание на вышеупомянутые эндотоксинсродственные полипептиды, которые, предположительно, имеют связь с сильной сохранностью видов камчатских крабов, и проделал исследование зависимости структурных изменений этих веществ от активности против вируса иммунодефицита человека (ВИЧ). В результате исследования заявитель обнаружил новые полипептиды, по существу отличающиеся от общей структуры известных эндотоксин-сродственных полипептидов камчатских крабов, и установил, что эти новые полипептиды оказывают превосходное влияние, которое выражается в том, что значения их противо-ВИЧ активности в 10 раз, или более, превосходят значения активности известного эндотоксинсродстенного полипептида.
Настоящее изобретение основано на данном открытии и относится к новому полипептиду, представленному следующей формулой (I):
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A1-Trp-Cys-A2-A3-Lys-A4-A2- A3-Gly-A4-A4-A2-A3-
15 16 17 18
A3-Cys-Arg-A5 (I),
где А1 обозначает атом водорода или один или два аминокислотных остатка аминокислот, выбранных из лизина и аргинина. A2 самостоятельно обозначает остаток тирозина, фенилаланина или триптофана, А3 самостоятельно обозначает остаток аргинина или лизина, А4 самостоятельно обозначает остаток аланина, валина, лейцина, изолейцина, серина, цистеина или метионина, А5 обозначает -ОН (полученный из карбоксильной группы) или -NH2 (полученный из кислотно-амидной группы), Сys обозначает остаток цистеина, Gly обозначает остаток глицина, Lys обозначает остаток лизина, Arg обозначает остаток аргинина и Тrp обозначает остаток триптофана; причем остатки цистеина в положениях 3 и 16 могут соединяться посредством дисульфидной связи (-S-S-), и когда положения 7 и 12 оба означают остатки цистеина, они могут соединяться посредством дисульфидной связи (-S-S-) или его соли.
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A1-Trp-Cys-A2-A3-Lys-A4-A2- A3-Gly-A4-A4-A2-A3-
15 16 17 18
A3-Cys-Arg-A5 (I),
где А1 обозначает атом водорода или один или два аминокислотных остатка аминокислот, выбранных из лизина и аргинина. A2 самостоятельно обозначает остаток тирозина, фенилаланина или триптофана, А3 самостоятельно обозначает остаток аргинина или лизина, А4 самостоятельно обозначает остаток аланина, валина, лейцина, изолейцина, серина, цистеина или метионина, А5 обозначает -ОН (полученный из карбоксильной группы) или -NH2 (полученный из кислотно-амидной группы), Сys обозначает остаток цистеина, Gly обозначает остаток глицина, Lys обозначает остаток лизина, Arg обозначает остаток аргинина и Тrp обозначает остаток триптофана; причем остатки цистеина в положениях 3 и 16 могут соединяться посредством дисульфидной связи (-S-S-), и когда положения 7 и 12 оба означают остатки цистеина, они могут соединяться посредством дисульфидной связи (-S-S-) или его соли.
Новый полипептид в соответствии с настоящим изобретением имеет важную характеристику, заключающуюся в том, что, хотя в известных полипептидах, полученных из камчатских крабов, аминокислотный остаток в положении 6 представляет собой остаток валина (Val), его 6-положение занимает остаток лизина (Lys), основной аминокислотный остаток, имеющий совершенно другое свойство, нежели имеет остаток валина.
Новый полипептид или его соль в соответствии с настоящим изобретением описаны более подробно ниже.
Новый полипептид предлагаемого изобретения может быть получен известным способом, например методом твердофазного синтеза. А именно прямоцепочечный полипептид настоящего изобретения, имеющий вышеприведенную формулу (I), может быть получен связыванием карбоксильной группы N-защищенного аргина с нерастворимым полимером, имеющим аминогруппы, непосредственно или, в некоторых случаях, посредством спейсера, имеющего функциональную группу, способную связываться с карбоксильной группой, и карбоксильную группу, последовательно связующую в соответствии с методом твердофазного синтеза соответствующие защищенные аминокислоты в положении от 16 до 1 аминокислотной последовательности, представленной следующей формулой (I):
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A1-Trp-Cys-A2-A3-Lys-A4-A2-A3-Gly-A4-A4-A2-A3-
15 16 17 18
A3-Cys-Arg-A5 (I),
где А1, A2, A3, A4, Cys, Gly, Lys, Аrg и Тrp имеют значения, приведенные выше для формулы (I), с последующим элиминированием (отщеплением) нерастворимого полимера и защитных групп аминокислот. В данном случае карбоксильное окончание аминокислотного остатка в положении 17 может быть либо свободным (А5 соответствует -ОН), либо превращенным в амид кислоты (А5 соответствует -NР2. Кроме того, в полученном полипептиде два цистеина в положениях 3 и 16 могут образовать дисульфидную связь (-S-S-) посредством меркаптогрупп.
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A1-Trp-Cys-A2-A3-Lys-A4-A2-A3-Gly-A4-A4-A2-A3-
15 16 17 18
A3-Cys-Arg-A5 (I),
где А1, A2, A3, A4, Cys, Gly, Lys, Аrg и Тrp имеют значения, приведенные выше для формулы (I), с последующим элиминированием (отщеплением) нерастворимого полимера и защитных групп аминокислот. В данном случае карбоксильное окончание аминокислотного остатка в положении 17 может быть либо свободным (А5 соответствует -ОН), либо превращенным в амид кислоты (А5 соответствует -NР2. Кроме того, в полученном полипептиде два цистеина в положениях 3 и 16 могут образовать дисульфидную связь (-S-S-) посредством меркаптогрупп.
Более того, когда положение 7 и положение 12 оба обозначают остатки цистеина, эти цистеины могут образовать также дисульфидную связь.
Что касается образования этих дисульфидных связей, то обе пары групп цистеина можно превратить в дисульфидную связь, например, окислением кислородом воздуха, либо дисульфидную связь можно образовать в соответствии с методом Atherton, E. et al. J. Chem. Soc. Perkin Trans, I, 1985, 2065, a именно с использованием стадий селективной защиты меркаптогрупп любой пары цистеинов в положениях 3 и 16 в положениях 7 и 12 с помощью защитной группы, т-Bus (трет-бутилтио) и меркаптогрупп любой пары цистеинов с помощью защитной группы Асm (ацетамидометил); освобождения от защиты т-Bus, частично окисляя меркаптогруппы; а затем освобождения от защиты Аcm в соответствии с известным способом.
Соответствующими аминокислотами, используемыми в методе твердофазного синтеза, могут быть традиционные L-формы или традиционные D-формы.
Что касается нерастворимых полимеров, имеющих аминогруппы для использования в синтезе нового полипептида настоящего изобретения, то можно использовать любые такие полимеры, если они только могут связываться через их аминогруппы с карбоксильной группой N-защищенного аргинина у С-окончания или, в некоторых случаях, с карбоксильной группой присоединенного спейсера, после чего их можно элиминировать (отщепить).
Примерами таких нерастворимых полимеров являются аминометиловые полимеры (аминометилированные стирол-дивинилбензоловые сополимеры), бензгидриламиновые полимеры, метилбензгидриламиновые полимеры и аминометилфеноксиметиловые полимеры и их производные, а так далее. При использовании бензгидриламинового полимера, метилбензгидриламинового полимера, диметоксибензгидриламинового (DMВНА) полимера или аминометилфеноксиметилового полимера амид непосредственно получают отщеплением, однако аминометиловый полимер является предпочтительным с точки зрения выхода.
В качестве спейсера, имеющего функциональную группу, способную связываться с карбоксильной группой, и карбоксильную группу, можно упомянуть, например, спейсер, способный превращать карбоксильную группу аргинина в сложный п-карбоксиметилбензиловый эфир, однако нет никакого конкретного ограничения в отношении спейсера.
Защищенная аминокислота представляет собой аминокислоту, функциональные группы которой защищены с помощью защитной группы известным способом, при этом различные защищенные аминокислоты поставляются на рынок.
При синтезе полипептида предлагаемого изобретения предпочитают выбирать любую одну из числа следующих защитных групп. Защитной группой для α-аминогруппы аминокислоты является Вос (трет-бутилоксикарбонил) или Fmoc (9-фторфенилметилоксикарбонил). Защитной группой для гуанидиногруппы аргинина (Аrg) является Tos (тозил), NO2 (нитро, Мtr (4-метокси-2,3,6-триметилбензолсульфонил) или Pmc (2,2,5,7,8-пентаметилхроман-6-сульфонил). В качестве защитной группы для меркаптогруппы цистеина (Сys) можно упомянуть BzI (бензио), MBzI (4-метоксибензил), 4-MeBzI (4-метилбензил), Аcm (ацетамидометил), Тrt (тритил), Npys (3-нитро-2-пиридинсульфенил), т-Bu (трет-бутил) или т-Bus (трет-бутилтио), причем предпочтительными являются МВzl, 4-MeBzl, Тrt- Acm и Npys. Защитной группой для гидроксильной группы торозина (Туr) является Bzl, Cl2Bzl (2,6-дихлорбензил) или т-Bu, однако группа может не быть защищенной. Защитной группой для e-аминогруппы лизина (Lys) является Z (бензилоксикарбонил)= СlZ (2-хлоробензилоксикарбонил), Вос или Npys. Предпочтительно выбирать в качестве определенной защитной группы группу из числа известных pеr se в соответствии с условиями синтеза пептида.
Сочетание (связывание) защищенных аминокислот можно осуществить в соответствии с обычным методом конденсации, таким как, например, метод DCC (дициклогексилкарбодиимида), метод DIPCDI (диизопропилкарбодиимида) [Tartar, A. et al. J. Org. Chem. 44: 5000 (1979)] метод активного сложного эфира, метод смешанного или симметричного ангидрида кислоты, метод карбонилдиимидазола, метод DCC-HOBt (1-гидроксибензотриазола) [Konig W. et al. Chem. Ber. 103, 788, 2024, 2034, (1970)] или метод дифенилфосфорилазида, однако предпочтительными являются метод DCC, метод DCC-HOBt, метод DIPCDI-HOBt и метод симметричного ангидрида кислоты. Данную реакцию конденсации обычно осуществляют в органическом растворителе, таком как дихлорметан или диметилформамид, или смеси растворителей. В качестве агента освобождения от защиты для a-аминогруппы используют смесь трифторуксусной кислоты и дихлорметана, смесь НСl и диоксана, смесь пиперидина и диметилформамида и так далее, при этом соответствующий выбор осуществляют в соответствии с типом защитной группы. Кроме того, степень развития реакции конденсации в каждой стадии синтеза прослеживают с помощью метода Е. Kaiser et al. [Anal. Biochem. 34, 595 (1970)] (метод нингидрин-реакции).
В соответствии с вышеупомянутыми способами можно получить защищенную пептидную смолу, имеющую желаемую аминокислотную последовательность.
При использовании в качестве нерастворимого полимера производного аминометиловой смолы последнюю можно отщепить, например, путем обработки защищенной пептидной смолы аммиаком в подходящем растворителе. Полученный защищенный пептид затем обрабатывают фтороводородом с получением полипептидного амида, представленного вышеприведенной формулой и свободного от защитных групп. Когда в качестве нерастворимого полимера используют бензгидриламиновый полимер, метилбензгидриламиновый полимер, аминометилфеноксиметиловый полимер или DMBHA полимер [Funakoshi, S. et al. J. Chem, Commun. 1988, 382] полимер и защитные группы можно отщепить одновременно путем обработки защищенного пептидного полимера фтороводородом, TF MSA (трифторметансульфокислотой) [публикация Academic Press, под редакцией E. Gross; Yajima, H. et al. "The Peptides", том 5, стр. 65 (1983)] TMSOTf (триметилсилилтрифлатом) [Fujii, N. et al. J.Chem. Soc. Chem. Commun. 1987, 274] или TMSBr (триметилфилилбромидом) [Fujii, N, et al. Chem. Pharm. Bull. 35, 3880 (1987)] и так далее.
Затем, при желании, полученный полипептид восстанавливают 2-меркаптоэтанолом, DTT (дитиотрейтолом) или аналогичным агентом с получением меркаптогрупп цистеинов восстановленной формы, после чего окисляют с получением циклического полипептида, принадлежащего изобретению.
Окислительную обработку можно осуществить известным методом. Обычно используют такой окислитель, как кислород в воздухе или феррицианат (например, феррицианид калия).
Полученный таким образом полипептид можно выделить и очистить способами, хорошо известными per. se для полипептидов, например, экстракцией, перекристаллизацией, различными хроматографиями (гель-фильтрацией, ионообменной, распределительной, адсорбционной, обращеннофазовой), электрофорезом, противоточным распределением и так далее, при этом наиболее эффективным средством является обращеннофазовая жидкостная хроматография высокого разрешения.
В качестве специфических примеров полипептидов настоящего изобретения, представленных формулой (1), можно упомянуть полипептиды следующих формул (11) (22) (см. фиг.1, 2). В этих формулах (1) (22) каждый символ обозначает соответствующий аминокислотный остаток посредством международно принятого трехбуквенного выражения. Каждый символ обозначает остаток следующих аминокислот.
Arg Аргинин Trp Триптофан
Cys Цистеин Tyr Тирозин
Lys Лизин Gly Глицин
Phe Фенилаланин Ile Изолейцин
Ser Серин Leu Лейцин
Met Метионин Val Валин
Ala Аланин
Полученные таким образом полипептиды настоящего изобретения, представленные формулой (1), аналогично известным полипептидам, полученным из камчатских крабов, имеют способность связываться с эндотоксинами, обладают противобактериальной активностью, активностью гемолизировать эндотоксин-сенсибилизированные гемоциты и противовирусной активностью, в особенности хорошей противовирусной активностью в отношении вируса иммунодефицита человека (ВИЧ). А именно, эти полипептиды проявляют анти-ВИЧ активность в десять или более раз выше активности Tachyplesin I известного полипептида, а некоторые полипептиды в соответствии с настоящим изобретением проявляют анти-ВИЧ активностью, в несколько тысяч раз более высокую, нежели активность Tachylesin I.
Cys Цистеин Tyr Тирозин
Lys Лизин Gly Глицин
Phe Фенилаланин Ile Изолейцин
Ser Серин Leu Лейцин
Met Метионин Val Валин
Ala Аланин
Полученные таким образом полипептиды настоящего изобретения, представленные формулой (1), аналогично известным полипептидам, полученным из камчатских крабов, имеют способность связываться с эндотоксинами, обладают противобактериальной активностью, активностью гемолизировать эндотоксин-сенсибилизированные гемоциты и противовирусной активностью, в особенности хорошей противовирусной активностью в отношении вируса иммунодефицита человека (ВИЧ). А именно, эти полипептиды проявляют анти-ВИЧ активность в десять или более раз выше активности Tachyplesin I известного полипептида, а некоторые полипептиды в соответствии с настоящим изобретением проявляют анти-ВИЧ активностью, в несколько тысяч раз более высокую, нежели активность Tachylesin I.
В известных полипептидах, полученных из камчатских крабов, выявлено в качестве их структурных характеристик, что благодаря наличию четырех остатков Cys в положениях 3, 7, 12 и 16 они принимают b-пластинчатую структуру так, что часть в положениях 9 и 10 представляет собой оборотный участок под действием b-оборота, и пептидный участок от 3 до 8 положения, а также пептидный участок от 11 до 16 положения расположены напротив друг друга, тогда как четыре остатка Cys в положениях 3 и 16 и в положениях 7 и 12 связываются посредством соответственных двух дисульфидных связей (-S-S-). Что касается структурных характеристик для проявления противовирусной активности полипептидов, положение 6 которых превращено в Lys, то существование структурных частей, составляющие аминокислотные последовательности которых крайне не похожи друг на друга, как видно в 3Cys4A2 5A3 6Lys, обращенной в сторону 13A2 14A3 15A3 16Cys, в основном необходимо, тогда как 2Тrp и 17Arg являются обязательными. Отличие также состоит в том, что посредством связывания основной аминокислоты, приписанной положению A1 с этими структурными частями в положении 1, получается структура таким образом, что чрезвычайно высоко проявляется анти-ВИЧ активность.
Полипептид настоящего изобретения, представленный формулой (1), проявляет основное свойство благодаря характеристике составляющих аминокислот и таким образом образует соли путем присоединения кислот. Например, полипептид образует соль с неорганической кислотой (хлористоводородной кислотой, бромистоводородной кислотой, фосфорной кислотой, азотной кислотой, серной кислотой и так далее) или органической карбоновой кислотой (уксусной кислотой, пропионовой кислотой, малеиновой кислотой, янтарной кислотой, яблочной кислотой, лимонной кислотой, винной кислотой, салициловой кислотой и так далее) или органической сульфокислотой (метансульфокислотой, п-толуолсульфокислотой и так далее). Полипептид настоящего изобретения, представленный формулой (1), может быть использован в качестве фармацевтически приемлемой соли.
Лекарственное средство в соответствии с настоящим изобретением получают в виде фармацевтической композиции, включающей полипептид, представленный формулой (1), или его соль в качестве активного компонента, а также фармакологически приемлемый носитель, выбранный в соответствии с методом введения и формой вводимого лекарственного средства. А именно лекарственное средство настоящего изобретения вводят перорально или парентерально вирусное заболевание in vivo или часть вирусной инфекции in vitro и лекарственное средство может быть получено в виде препарата такого, как порошок, гранулы, раствор для инъекции или перорального введения, таблетки, суппозитории, вагинальные суппозитории, мазь, крем или аэрозоль, с использованием подходящих фармацевтических носителей в соответствии с методом введения.
Когда лекарственный препарат настоящего изобретения вводят непосредственно как инъекцию в живой организм, полипептид или его соль настоящего изобретения можно вводить непрерывно или с промежутками в количестве от 10 до 5000 мг на кг массы тела человека из расчета на одни сутки с использованием капельного внутривенного вливания в виде раствора в физиологическом растворе.
Фиг. 3 показывает схематическое изображение стадий синтеза нового полипептида в соответствии с настоящим изобретением.
Предлагаемое изобретение описано ниже более подробно в примерах, однако не ограничивается ими в объеме и сущности.
Используют следующие аппараты и реагенты.
Аппарат для проведения ЖХВР (жидкостной хроматографии высокого разрешения): Уотерс Ко, (США), модель 600;
колонка аппарата: Асахипак ОDP-90 (Асахи Кемикал Индастри Ко. Отл);
аминокислота Fmoc: производство Кокусан Кагаку Ко. Лтд;
аминосмола и конденсирующее средство: производство Пептид Кенкюшо Ко. Лтд;
FAB-MS (масс-спектрограф с бомбардировкой пучками быстрых атомов): УG Ко. (США), модель ZAB-SE.
колонка аппарата: Асахипак ОDP-90 (Асахи Кемикал Индастри Ко. Отл);
аминокислота Fmoc: производство Кокусан Кагаку Ко. Лтд;
аминосмола и конденсирующее средство: производство Пептид Кенкюшо Ко. Лтд;
FAB-MS (масс-спектрограф с бомбардировкой пучками быстрых атомов): УG Ко. (США), модель ZAB-SE.
Пример 1. Синтез полипептида (А) следующей формулы
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
Arg-Trp-Cys-Tyr-Arg-Lys-Cys-Tyr-Arg-Cly-Ile-Cys-Tyr-Arg-Lys-Cys-Arg-N- H2 (A)
В вышеприведенной формуле (А) Arg, Trp, Cys, Tyr, Lys, Gly и Ile обозначают вышеуказанные аминокислотные остатки, а остатки Cys в положениях 3 и 16 и в положениях 7 и 12 связаны соответственно с помощью дисульфидной связи.
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
Arg-Trp-Cys-Tyr-Arg-Lys-Cys-Tyr-Arg-Cly-Ile-Cys-Tyr-Arg-Lys-Cys-Arg-N- H2 (A)
В вышеприведенной формуле (А) Arg, Trp, Cys, Tyr, Lys, Gly и Ile обозначают вышеуказанные аминокислотные остатки, а остатки Cys в положениях 3 и 16 и в положениях 7 и 12 связаны соответственно с помощью дисульфидной связи.
(1) Введение в аминометиловую смолу Fmoc-DMBHA-CH2CH2COOH[(3-(a-Fmoc-амино-4-метоксибензил)-4-метоксифенил)пропионовой кислоты]
270 мг (0,2 моль) аминометиловой смолы (0,74 мэкв/г) и 268,5 мг (0,5 ммоль, 2,5 экв) Fmoc-SMBHA-CH2CH2COOH (молекулярная масса 537) помещают в колонку для твердофазного синтеза и реакцию конденсации осуществляют в течение 2 часов с использованием метода DIPCD I-HOBt в ДМФ в соответствии со способом Guo, L. et al. [Chem. Pharm, Bull. 36, 4989 (1988)] После завершения реакции конденсации осуществляют сочетание для защиты свободных аминогрупп, используя уксусный ангидрид (смолу DMBHA).
270 мг (0,2 моль) аминометиловой смолы (0,74 мэкв/г) и 268,5 мг (0,5 ммоль, 2,5 экв) Fmoc-SMBHA-CH2CH2COOH (молекулярная масса 537) помещают в колонку для твердофазного синтеза и реакцию конденсации осуществляют в течение 2 часов с использованием метода DIPCD I-HOBt в ДМФ в соответствии со способом Guo, L. et al. [Chem. Pharm, Bull. 36, 4989 (1988)] После завершения реакции конденсации осуществляют сочетание для защиты свободных аминогрупп, используя уксусный ангидрид (смолу DMBHA).
(2) Введение аргинина в положении 17 в смолу DMBHA).
После отщепления групп F от смолы DMBHA, полученной в стадии (1), с помощью 20% пиперидина (ДМФ, прибавляют 2,5 экв. Fmoc-Aro (Mtr)-Oн на основе DMBHA и реакцию конденсации осуществляют в ДМФ с помощью метода DIPCDI-HOB. Степень развития реакции конденсации прослеживают путем измерения в соответствии с нингидрин-тестом Kaiser, E. et al. [And Biochem. 34, 595 (1970)]
(3) Введение цистеина в положении 16.
(3) Введение цистеина в положении 16.
После отщепления групп Fmoc смолы DMBHA, полученной в стадии (2), в которую введен аргини, с помощью 20% пиперидина (ДМФ прибавляют 2,5 экв. Fmoc-Cys (MBzl)-OH на основе смолы DMBHA, а реакцию конденсации осуществляют в ДМФ методом DIPCDI-HOBt. Cтепень развития реакции конденсации прослеживают аналогично стадии (2) путем измерения в соответствии с нингидрин-тестом.
(4) Введение аминокислот в положениях от 15 до 1.
Аналогично вышеприведенным методикам, Lys (Boc), Arg-(Mtr), Tyr(т-Bu), Cys(MBzl), Ile, Gly, Arg(Mtr), Tyr(т-Bu), Gys(MBzl), Lys(Boc), Arg(Mtr), Tyr(т-Bu), Cys(MBzl), Trp и Arg(Mtr)-остатки в соответствии с последовательностью от С-концевой аминокислоты последовательно вводят в смолу DMBHA с получением защищенной с помощью защитной группы пептидной (А) смолы.
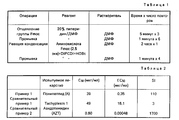
Реакцию конденсации каждой аминокислоты в твердофазном синтезе осуществляют в соответствии с условиями, приведенными в табл. 1.
(5) Получение пептида (А) путем отщепления защитных групп и операции по отношению смолы и частичной очистке.
Смолу пептида (А), защищенного с помощью защитной группы, которую получают в стадиях (1) (4), подвергают обработке 20% пиперидином (ДМФ с целью отщепления группы Fmoc, а затем подвергают реакции при температуре 25oС в течение 2 часов в системе 1 М TMSOTf-тиоанизол) трифторуксусная кислота (10 мл трифторуксусной кислоты в присутствии м-крезола (100 экв.) и этантиола (300 экв. ) на 100 мг смолы. Смолу отфильтровывают из реакционной смеси и дважды промывают с помощью 1 мл трифторуксусной кислоты, после чего 100 мл охлажденного на льду сухого простого эфира прибавляют в смесь фильтрата и промывки, образованный осадок центрифугируют и остаток промывают холодным простым эфиром, растворяют в 10 мл 4 н. раствора АсОН, 830 мг; 80 экв. дитиотрейтола прибавляют и смесь перемешивают при комнатной температуре в течение ночи. Реакционный раствор центрифугируют, супернатант обрабатывают с помощью Сефадекс G-10 (3,7x50 см), гель-фильтруют с помощью 4 н. раствора АсОН, после чего фракцию, которая прошла через колонку Сефадекс без остановки, собирают в виде основной части элюата и лиофилизируют с получением в виде порошка частично очищенного нециклизованного полипептида (А).
(6) Получение полипептида (А) окислением на воздухе.
С другой стороны, половину количества фракции, которая прошла через колонку Сефадекс без остановки при гель-фильтрации, доводят до рН 7,5 концентрированным водным аммиаком и подвергают окислению на воздухе с помощью аэрации с тем, чтобы осуществить реакцию замыкания цикла. После завершения окисления на воздухе циклизованный пептид (А) адсорбируют на 10 г смолы Диаион НР-20, десорбируют и элюируют с помощью 60% СН3CN (в 1 н. растворе АсОН) и элюат концентрируют при комнатной температуре при пониженном давлении с тем, чтобы отщепить CH3CN, а затем лиофилизируют с получением порошка. Порошок растворяют в малом количестве воды и раствор вливают на Асахипак и очищают жидкостной хроматографией высокого разрешения (ЖХВР-Модель 600, производство Уотерс Ко.), используя градиентное элюирование с помощью СH3CN, с получением пептида (А) единственного пика с выходом 27% (значение вычислено на основе смолы пептида (А), защищенного с помощью защитной группы).
(7) Анализ полипептида
Значение аминокислотного состава с перевариванием лейцин-аминопептидазой полипептида, очищенного в стадии (6) выше, хорошо согласуется с вычисленным значением состава на основе аминокислотной последовательности формулы (А). Кроме того, при определении значения молекулярной массы с помощью FAB-MS вычисленное значение (M+H+) cоставляет 2309, 786, а с другой стороны, найденное значение составляет 2310, 048.
Значение аминокислотного состава с перевариванием лейцин-аминопептидазой полипептида, очищенного в стадии (6) выше, хорошо согласуется с вычисленным значением состава на основе аминокислотной последовательности формулы (А). Кроме того, при определении значения молекулярной массы с помощью FAB-MS вычисленное значение (M+H+) cоставляет 2309, 786, а с другой стороны, найденное значение составляет 2310, 048.
Удельное вращение [α] полученного полипептида составляет +14,2o (C= 0,3, 1 н. раствор уксусной кислоты).
Пример 2 и сравнительные примеры 1 и 2.
Противовирусная активность в отношении вируса иммунодефицита человека (ВИЧ)
Противовирусная активность в отношении ВИЧ полипептида (А), синтезированного в примере 1, исследуют и оценивают в соответствии со следующим способом.
Противовирусная активность в отношении ВИЧ полипептида (А), синтезированного в примере 1, исследуют и оценивают в соответствии со следующим способом.
ВИЧ-зараженные клетки МТ-4 (2,5х104 клеток/лунку, множественность заражения (МО1):0,001) немедленно после заражения прибавляют вместе с испытуемым веществом при различных изменениях в концентрации в титрационный микропланшет с 96 лунками. После инкубации при температуре 7oC в течение 5 суток в инкубаторе СО2 число выживших клеток измеряют методом МТТ (Pauwels et al. J. Virol. Methods, 20, 309-321 (1988)). Противовирусную активность выражают в виде концентрации, при которой происходит 50% ингибирование целлюлярного поражения вследствие заражения ВИЧ (ЕС50:50% эффективная концентрация). С другой стороны, с целью обнаружения цитотоксичности испытуемого вещества относительно клеток МТ-4 не зараженные вирусом клетки инкубируют, как описано выше, вместе с испытуемым соединением при различных изменениях в концентрации. Цитотоксичность выражают в виде 50% цитотоксичной концентрации (СС50) вследствие испытуемого вещества. Кроме того, грубое отношение СС50 и ЕС50 (CC50/EC50) выражают в виде эффективного отношения (SI).
Таблица 2 показывает значения EC50, CC50 и SI полипептида (А), а также Tachyplesin I, известного полипептида, имеющего сродство с эндотоксинами, и азидотимидина, противо-ВИЧ агента, при этом оба последних используют для сравнения.
Как видно из вышеприведенной таблицы, полипептид (А) в соответствии с настоящим изобретением имеет несколько более высокую цитотоксичность, нежели Tachyplesin I, анти-ВИЧ активность которого выявлена ранее, однако проявляет противовирусную активность при концентрации 1/50. В сравнении с азидотимидином полипептид (А) имеет значение ЕС50 при более высокой концентрации, однако в 60 раз более высокую СС50, что указывает на низкую цитотоксичность.
Пример 3.
Таблица 3 показывает структурные формулы и физические свойства различных полипептидов настоящего изобретения, полученных аналогично примеру 1, а также их противовирусную активность в отношении ВИЧ, исследованную и оцененную аналогично примеру 2.
В соединениях данного примера в вышеуказанной таблице остатки Сys в положениях 3, 7, 12 и 16 связаны посредством дисульфидной связи между положениями 3 и 16 и между положениями 7 и 12, если не указано что-либо иное.
Кроме того, в вышеприведенной таблице "AZT" обозначает азидотимидин (общее название: зидовудин).
В соответствии с настоящим изобретением можно получить новый полипептид или его соль, имеющие противовирусную активность в отношении вируса иммунодефицита человека (ВИЧ), а также противо-ВИЧ средство, содержащее данный полипептид или его соль в качестве эффективного ингредиента.
Ниже приведены два рабочих примера, которые иллюстрируют два случая получения соединения формулы 1.
Cлучай 1. Способ получения соединения, когда А1=H.
Когда А1= H, этот случай соответствует соединению, которое начинается с триптофана (Trp) в положении +2 в формуле (1).
Этот вариант уже был проиллюстрирован соединением (1) в таблице 3. Соединение (1) получают только изменением наименования соответствующего целевого продукта из (А) в (1) по примеру 1 (стр. 16) и заменой операции (4) на странице 17 так, как это показано ниже, операциями (1) (3) и (5) (6), сохраняемыми в том виде, как они присутствуют.
Операция (4) должна быть изменена следующим образом.
(4) Введение аминокислот в положениях с 15- по 2-.
Подобно изложенному выше, остатки Lys(Boc), Arg(Mtr) Tyr(t-Bu), Cys(MBzl), Ile, Gly, Arg(Mtr), Tyr(t-Bu), Cys(MBzl), Lys(Boc), Arg(Mtr), Tyr(t-Bu), Cys(MBzl) и Trp в соответствии с последовательностью, начиная с С-концевой аминокислоты, последовательно вводились в смолу DMBHA с получением пептида (1) на смоле, защищенного защитной группой.
Случай 2. Способ получения соединения, когда A1=лизин.
Получение соединения 23 должно быть дополнено следующим новым примером 4, причем общая схема синтеза остается по существу той же, что дана на фиг. 1.
Пример 4.
Синтез полипептида (23) следующей формулы:
(1) Введение в аминометильную смолу Fmoc-DMBHA-CH2CH2COOH (3-(α-Fmoc-амино-4-метоксибензил)-4-метоксифенил)пропионовой кислоты.
(1) Введение в аминометильную смолу Fmoc-DMBHA-CH2CH2COOH (3-(α-Fmoc-амино-4-метоксибензил)-4-метоксифенил)пропионовой кислоты.
Процесс должен проводиться в тех же условиях, что и в примере 1.
(2) Введение лизина из положения 17 в смолу DMBHA.
После удаления Fmoc-групп из смолы DMBHA, полученной в (1) с помощью 20% -ного пиперидина (диметилформамид, 2,5 экв. Fmoc Lys(Boc)-OH было добавлено в расчете на DMBHA-смолу и реакцию конденсации осуществляли в ДМФ в соответствии с методом DIPCDI-HOBt.
За развитием реакции конденсации следили с помощью нингидринного теста по методике, описанной в Kaiser E. и др. (And Biochem, 34, 595 (1970)).
(3) Введение цистеина из положения -16:
После удаления Fmoc-групп из DMBHA-смолы, полученной в (2), в которую был введен лизин, с помощью 20%-ного пиперидина (ДМФ, добавлено 2,5 экв. Fmoc-Cys(MBzl)-OH в рассчете на DMBHA смолу и проведена реакция конденсации в ДМФ методом DIPCDI-HOBt. Развитие реакции конденсации оценивалось аналогично тому, как указано в (2), согласно нингидринному тесту.
После удаления Fmoc-групп из DMBHA-смолы, полученной в (2), в которую был введен лизин, с помощью 20%-ного пиперидина (ДМФ, добавлено 2,5 экв. Fmoc-Cys(MBzl)-OH в рассчете на DMBHA смолу и проведена реакция конденсации в ДМФ методом DIPCDI-HOBt. Развитие реакции конденсации оценивалось аналогично тому, как указано в (2), согласно нингидринному тесту.
(4) Введение аминокислот из положений от 15- до 1-.
Как и выше, в смолу DMBHA были последовательно введены остатки Lys(Boc), Arg(Mtr), Tyr-(t-Bu), Cys(MBzl), Ile, Gly, Lys(Boc), Tyr(t-Bu), Cys-(MBzl); Lys(Boc), Arg(Mtr), Tyr(t-Bu), Cys(MBzl), Trp и Lys(Boc) в соответствии с последовательностью, начиная с С-концевой аминокислоты, с получением пептида (23) на смоле, защищенного блокирующей группой.
Каждая реакция конденсации аминокислоты, осуществляемая твердофазным синтезом, проводилась таким же образом, как и процесс по примеру 1 (таблица 1).
(5) Получение пептида (23) удалением защитных групп и стадия выделения смолы и частичная очистка.
Процесс следует проводить так же, как и в примере 1.
(6) Получение полипептида (23) окислением на воздухе.
Процесс следует проводить так же, как в примере 1.
Величина удельного вращения [α] , полученного полипептида (23) составила +18,6o (C=0,1; 1N AcOH).
Для доказательства того, что положения 3- и 16-, а также положения 7- и 12- нового полипептида каждое соединено дисульфидным мостиком, использован полипептид А по примеру 1.
а) Новые полипептиды благодаря наличию четырех Cys остатков в положении 3, 7, 12 и 16 и благодаря присутствию остатка Gly, в положении 10 имеют β-слоистую структуру, так что часть его в положениях 9 и 10 находится в повернутом положении по отношению к b-витку и пептидная часть с положения 3 до положения 8 и пептидная часть с положения 11 до положения 16 располагаются лицом друг к другу, и, кроме того, четыре Cys остатка в положениях 3- и 16- и в положениях 7- и 12- легко связываются химически при окислении на воздухе двумя соответствующими дисульфидными мостиками (-S-S-) (см. описание, стр. 13).
Что касается образования восстановленной формулы (Cys-SH) полипептида, то на полипептид действуют восстановительными агентами, такими как: 2-меркаптоэтанол и дитиотрейтол, и, таким образом, может быть установлено наличие восстановленной формы полипептида (см. описание, стр. 9 и стр. 18).
Каждая форма окисленного или восстановленного полипептида проявляет одинаковую степень воздействия на антивирусную активность по отношению к вирусу иммунодефицита человека (СПИД). Сравните символы (3) и (3Н) в таблице 3 описания.
(b) Доказательство факта, что в молекуле полипептида А отсутствует группа Cys-SH (пример 1).
Наличие остатка Сys-SH в полипептиде А определялось методом Ellman/G.L. Ellman, Arch. Biochem Biophys 82, стр. 70 (1959).
Более детально: раствор полипептида А обрабатывали реактивом DTNB 5,5-дитио-бис(2-нитробензойная кислота) и образующуюся 2-нитро-5-меркаптобензойную кислоту анализировали на спектрофотометре (при длине волны 412 нм).
В результате не наблюдалось абсорбции при длине волны 412 нм и, таким образом, было подтверждено отсутствие -SH групп в молекуле полипептида [a]
(c) Доказательства факта, что дисульфидные мостики в полипептиде [A] образуются соответственно между Cys положений 3- и 16- и между Cys положений 7- и 12-.
(c) Доказательства факта, что дисульфидные мостики в полипептиде [A] образуются соответственно между Cys положений 3- и 16- и между Cys положений 7- и 12-.
Положение дисульфидных мостиков в полипептиде [A] определялось из аминокислотных составов пептидов, которые были получены триптическим расщеплением исходного полипептида [A] с использованием следующей методики:
32 мкг полипептида [A] расщепляли трипсином в течение 12 часов при 37oC в соотношении энзима к субстрату 1:32 (по весу) в 80 мкл раствора аммонийной соли муравьиной кислоты с концентрацией 50 мМ (рН 6,5), содержащего й мМ СаСl2.
32 мкг полипептида [A] расщепляли трипсином в течение 12 часов при 37oC в соотношении энзима к субстрату 1:32 (по весу) в 80 мкл раствора аммонийной соли муравьиной кислоты с концентрацией 50 мМ (рН 6,5), содержащего й мМ СаСl2.
Продукт расщепления разделяли с применением обращенно-фазовой высокоэффективной жидкостной хроматографии на колонке с Cosmosil 5C18-P (4,6x250 мм).
Элюирование осуществлялось с линейным градиентом 0≈50% ацетонитрила в 0,1% трифторуксусной кислоте в течение 50 минут.
Хроматограмма процесса изображена на фиг. 4.
Каждый из фрагментов Р-1 и Р-2 анализировали на автоматическом пептидном анализаторе и их аминокислотные составы показаны в табл. 4.
Из результатов таблицы 4 стало известно, что структура полипептидов (Р-1 и Р-2), образующихся в результате расщепления трипсином полипептида А формулы:
имеет следующий вид:
Фрагмент Р-1 Фрагмент Р-2
2 3 4 5 6 7 8 9
Trp Cys Tyr Arg OH Lys Cys Tyr Arg OH
Lys Cys Arg NH2 Gly Ile Cys Tyr Arg OH
15 16 17 10 11 12 13 14
Таким образом, результаты подтверждают, то два дисульфидных мостика расположены между положениями Сys 3- и Cys-16 и положениями Cys7- и Cys12-.
имеет следующий вид:
Фрагмент Р-1 Фрагмент Р-2
2 3 4 5 6 7 8 9
Trp Cys Tyr Arg OH Lys Cys Tyr Arg OH
Lys Cys Arg NH2 Gly Ile Cys Tyr Arg OH
15 16 17 10 11 12 13 14
Таким образом, результаты подтверждают, то два дисульфидных мостика расположены между положениями Сys 3- и Cys-16 и положениями Cys7- и Cys12-.
Примеры, иллюстрирующие фармацевтическую композицию.
Капсулы для орального применения
Полипептид [A] (активный ингредиент) 100 мг
Кукурузный крахмал 300 мг
Стеарат магния 10 мг
Микрокристаллическая целлюлоза 590 мг 1000 мг
Компоненты перемешивают до получения однородной смеси и наполняют ею твердые желатиновые капсулы (200 мг на каждую).
Полипептид [A] (активный ингредиент) 100 мг
Кукурузный крахмал 300 мг
Стеарат магния 10 мг
Микрокристаллическая целлюлоза 590 мг 1000 мг
Компоненты перемешивают до получения однородной смеси и наполняют ею твердые желатиновые капсулы (200 мг на каждую).
Препарат для инъекций
Полипептид [3] (активный ингредиент) 10 мг
Кондроитин сульфат натрия 10 мг
Указанные компоненты растворяют в 2 мл 5%-ного водного раствора маннита (для переливания крови) и полученный раствор подвергают стерильной фильтрации. Фильтрат растворяют в 200 мл 5%-ного раствора маннита (для переливания крови) и полученный раствор используют для внутривенного вливания.
Полипептид [3] (активный ингредиент) 10 мг
Кондроитин сульфат натрия 10 мг
Указанные компоненты растворяют в 2 мл 5%-ного водного раствора маннита (для переливания крови) и полученный раствор подвергают стерильной фильтрации. Фильтрат растворяют в 200 мл 5%-ного раствора маннита (для переливания крови) и полученный раствор используют для внутривенного вливания.
Claims (2)
1. Полипептиды общей формулы
где А1 атом водорода или один или два аминокислотных остатка, такие, как лизин и аргинин;
А2 независимо тирозиновый, фенилаланиновый или триптофановый остаток;
А2 независимо аргининовый или лизиновый остаток;
А4 независимо аланиновый, валиновый, лейциновый, изолейциновый, сериновый или метиониновый остаток,
и две пары цистеиновых остатков в положениях 3 и 16 и положениях 7 и 12 могут быть соединены дисульфидными мостиками (- S S -) или их соли.
где А1 атом водорода или один или два аминокислотных остатка, такие, как лизин и аргинин;
А2 независимо тирозиновый, фенилаланиновый или триптофановый остаток;
А2 независимо аргининовый или лизиновый остаток;
А4 независимо аланиновый, валиновый, лейциновый, изолейциновый, сериновый или метиониновый остаток,
и две пары цистеиновых остатков в положениях 3 и 16 и положениях 7 и 12 могут быть соединены дисульфидными мостиками (- S S -) или их соли.
2. Фармацевтическая композиция, обладающая противовирусной активностью в отношении вируса иммунодефицита человека, содержащая в качестве активного начала производное полипептида, отличающаяся тем, что в качестве производного полипептида она содержит эффективное количество соединения формулы 1 по п. 1 или его соли.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP238922/90 | 1990-09-11 | ||
| JP23892290 | 1990-09-11 | ||
| PCT/JP1991/001201 WO1992004374A1 (en) | 1990-09-11 | 1991-09-10 | Novel polypeptide and anti-hiv drug prepared therefrom |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2073685C1 true RU2073685C1 (ru) | 1997-02-20 |
Family
ID=17037269
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| SU915052258A RU2073685C1 (ru) | 1990-09-11 | 1991-09-10 | Полипептиды или их соли, фармацевтическая композиция, обладающая противовирусной активностью в отношении вируса иммунодефицита человека |
Country Status (21)
| Country | Link |
|---|---|
| US (1) | US5571892A (ru) |
| EP (1) | EP0502198B1 (ru) |
| JP (1) | JP3178835B2 (ru) |
| KR (1) | KR0184604B1 (ru) |
| AT (1) | ATE132163T1 (ru) |
| AU (1) | AU638606B2 (ru) |
| BG (1) | BG60621B1 (ru) |
| BR (1) | BR9105902A (ru) |
| CA (1) | CA2068327C (ru) |
| CZ (1) | CZ280870B6 (ru) |
| DE (1) | DE69115878T2 (ru) |
| DK (1) | DK0502198T3 (ru) |
| ES (1) | ES2081491T3 (ru) |
| FI (1) | FI922044A (ru) |
| GR (1) | GR3018879T3 (ru) |
| HU (1) | HUT61579A (ru) |
| NO (1) | NO921829L (ru) |
| OA (1) | OA10030A (ru) |
| RO (1) | RO109653B1 (ru) |
| RU (1) | RU2073685C1 (ru) |
| WO (1) | WO1992004374A1 (ru) |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3266311B2 (ja) * | 1991-05-02 | 2002-03-18 | 生化学工業株式会社 | 新規ポリペプチドおよびこれを用いる抗hiv剤 |
| JP3361830B2 (ja) * | 1992-03-30 | 2003-01-07 | 生化学工業株式会社 | 抗菌性組成物及びそれを有効成分とする薬剤 |
| CN1038841C (zh) * | 1993-10-14 | 1998-06-24 | 生化学工业株式会社 | 新型多肽以及由其制备的抗人类免疫缺陷病毒制剂 |
| CA2268011A1 (en) | 1996-10-15 | 1998-04-23 | Seikagaku Corporation | Polypeptide transition metal salts and method of enhancing anti-hiv activity of polypeptide |
| AU6518698A (en) * | 1997-03-28 | 1998-10-22 | Seikagaku Corporation | Novel anti-hiv complexes and medicinal compositions |
| MXPA02001349A (es) * | 1999-08-09 | 2002-07-22 | Tripep Ab | Inhibidores de la polimerizacion de proteinas y metodos de uso. |
| US6593455B2 (en) * | 2001-08-24 | 2003-07-15 | Tripep Ab | Tripeptide amides that block viral infectivity and methods of use thereof |
| EP1436317A1 (en) * | 2001-09-19 | 2004-07-14 | Tripep Ab | Molecules that block viral infectivity and methods of use thereof |
| US20050096319A1 (en) * | 2003-02-21 | 2005-05-05 | Balzarini Jan M.R. | Identification of compounds that inhibit replication of human immunodeficiency virus |
| NZ541883A (en) * | 2003-02-21 | 2008-12-24 | Tripep Ab | Glycinamide derivative for inhibiting HIV replication |
| USD941948S1 (en) | 2016-07-20 | 2022-01-25 | Razor Usa Llc | Two wheeled board |
| USD803963S1 (en) | 2016-07-20 | 2017-11-28 | Razor Usa Llc | Two wheeled board |
| USD837323S1 (en) | 2018-01-03 | 2019-01-01 | Razor Usa Llc | Two wheeled board |
| USD807457S1 (en) | 2016-07-20 | 2018-01-09 | Razor Usa Llc | Two wheeled board |
| USD840872S1 (en) | 2016-07-20 | 2019-02-19 | Razor Usa Llc | Two wheeled board |
| JP2021506671A (ja) | 2017-12-22 | 2021-02-22 | レイザー・ユーエスエー・エルエルシー | 電動バランス車両 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA1337781C (en) * | 1987-08-21 | 1995-12-19 | Takanori Nakamura | Polypeptide from horseshoe crab exhibiting affinity for lipopolysaccharide and method of preparation |
| JP2641744B2 (ja) * | 1988-08-18 | 1997-08-20 | マルハ株式会社 | 新規ペプチド及び抗菌剤 |
| JP2641742B2 (ja) * | 1988-08-18 | 1997-08-20 | マルハ株式会社 | 新規ペプチド及び抗菌剤 |
| JP2798711B2 (ja) * | 1988-09-26 | 1998-09-17 | 生化学工業株式会社 | ポリペプチド系抗ウィルス剤 |
| JP3266311B2 (ja) * | 1991-05-02 | 2002-03-18 | 生化学工業株式会社 | 新規ポリペプチドおよびこれを用いる抗hiv剤 |
| JP2500194B2 (ja) | 1993-08-10 | 1996-05-29 | 株式会社ヴァンドームヤマダ | 商品発注システム |
-
1991
- 1991-09-10 BR BR9105902A patent/BR9105902A/pt not_active Application Discontinuation
- 1991-09-10 WO PCT/JP1991/001201 patent/WO1992004374A1/ja active IP Right Grant
- 1991-09-10 HU HU9201540A patent/HUT61579A/hu unknown
- 1991-09-10 JP JP51480791A patent/JP3178835B2/ja not_active Expired - Fee Related
- 1991-09-10 RO RO92-200638A patent/RO109653B1/ro unknown
- 1991-09-10 US US07/856,026 patent/US5571892A/en not_active Expired - Fee Related
- 1991-09-10 RU SU915052258A patent/RU2073685C1/ru not_active IP Right Cessation
- 1991-09-10 CA CA002068327A patent/CA2068327C/en not_active Expired - Fee Related
- 1991-09-10 EP EP91915604A patent/EP0502198B1/en not_active Expired - Lifetime
- 1991-09-10 ES ES91915604T patent/ES2081491T3/es not_active Expired - Lifetime
- 1991-09-10 AU AU84480/91A patent/AU638606B2/en not_active Ceased
- 1991-09-10 KR KR1019920701101A patent/KR0184604B1/ko not_active IP Right Cessation
- 1991-09-10 AT AT91915604T patent/ATE132163T1/de not_active IP Right Cessation
- 1991-09-10 DK DK91915604.2T patent/DK0502198T3/da active
- 1991-09-10 DE DE69115878T patent/DE69115878T2/de not_active Expired - Fee Related
-
1992
- 1992-05-06 FI FI922044A patent/FI922044A/fi unknown
- 1992-05-07 CZ CS921394A patent/CZ280870B6/cs not_active IP Right Cessation
- 1992-05-08 NO NO92921829A patent/NO921829L/no not_active Application Discontinuation
- 1992-05-11 OA OA60206A patent/OA10030A/en unknown
- 1992-05-11 BG BG96323A patent/BG60621B1/bg unknown
-
1996
- 1996-02-01 GR GR960400273T patent/GR3018879T3/el unknown
Non-Patent Citations (1)
| Title |
|---|
| NaKamura, Jwanaga, Niwa * |
Also Published As
| Publication number | Publication date |
|---|---|
| US5571892A (en) | 1996-11-05 |
| HU9201540D0 (en) | 1992-08-28 |
| NO921829L (no) | 1992-07-09 |
| EP0502198B1 (en) | 1995-12-27 |
| AU638606B2 (en) | 1993-07-01 |
| DE69115878T2 (de) | 1996-06-05 |
| EP0502198A4 (en) | 1993-05-05 |
| FI922044A0 (fi) | 1992-05-06 |
| OA10030A (en) | 1996-10-14 |
| CA2068327C (en) | 2002-01-01 |
| EP0502198A1 (en) | 1992-09-09 |
| FI922044A (fi) | 1992-05-06 |
| DE69115878D1 (de) | 1996-02-08 |
| CZ280870B6 (cs) | 1996-04-17 |
| RO109653B1 (ro) | 1995-04-28 |
| NO921829D0 (no) | 1992-05-08 |
| HUT61579A (en) | 1993-01-28 |
| CS139492A3 (en) | 1992-09-16 |
| DK0502198T3 (da) | 1996-01-29 |
| AU8448091A (en) | 1992-03-30 |
| WO1992004374A1 (en) | 1992-03-19 |
| ATE132163T1 (de) | 1996-01-15 |
| JP3178835B2 (ja) | 2001-06-25 |
| BG96323A (bg) | 1993-12-24 |
| GR3018879T3 (en) | 1996-05-31 |
| BR9105902A (pt) | 1994-06-28 |
| BG60621B1 (bg) | 1995-10-31 |
| CA2068327A1 (en) | 1992-03-12 |
| ES2081491T3 (es) | 1996-03-16 |
| KR0184604B1 (ko) | 1999-05-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3266311B2 (ja) | 新規ポリペプチドおよびこれを用いる抗hiv剤 | |
| RU2073685C1 (ru) | Полипептиды или их соли, фармацевтическая композиция, обладающая противовирусной активностью в отношении вируса иммунодефицита человека | |
| KR100208873B1 (ko) | 폴리펩타이드 및 그것으로 부터 제조된 항-hiv 제제 | |
| US7595298B2 (en) | Polypeptides having anti-HIV activity and compositions comprising same | |
| RU2079509C1 (ru) | Производные пептидов, обладающие способностью регулировать пролиферацию клеток, и способы ингибирования клеточной пролиферации человека и животного (варианты) | |
| RU2083589C1 (ru) | Полипептиды или их соли и фармацевтическая композиция | |
| FR2608160A1 (fr) | Nouveaux derives peptidiques et leur application notamment en therapeutique | |
| JPH07252299A (ja) | ヒルジン誘導体およびその製造方法 | |
| IE66837B1 (en) | Hexapeptides with sulphate ester groups | |
| WO2014148489A1 (ja) | 環状ペプチド | |
| JPH032195A (ja) | プロテアーゼ阻害剤 | |
| JPH11130799A (ja) | 低カルシウム血症のイン・ビボ活性の顕著な増大が可能な超強力なカルシトニン類縁体 | |
| DK144563B (da) | Analogifremgangsmaade til fremstilling af do eller tritriacontapeptider eller -peptidderiveter eller syreadditionssalte eller zinkcomplexer deraf | |
| JPH0925240A (ja) | 医薬組成物 | |
| JPH10324700A (ja) | 新規抗hiv複合体及び医薬組成物 | |
| JP2001270897A (ja) | 生理活性ペプチド |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20030911 |