KR20220106120A - 이차 전지, 휴대 정보 단말기, 및 차량 - Google Patents
이차 전지, 휴대 정보 단말기, 및 차량 Download PDFInfo
- Publication number
- KR20220106120A KR20220106120A KR1020227016961A KR20227016961A KR20220106120A KR 20220106120 A KR20220106120 A KR 20220106120A KR 1020227016961 A KR1020227016961 A KR 1020227016961A KR 20227016961 A KR20227016961 A KR 20227016961A KR 20220106120 A KR20220106120 A KR 20220106120A
- Authority
- KR
- South Korea
- Prior art keywords
- active material
- lithium
- positive electrode
- secondary battery
- preferable
- Prior art date
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0567—Liquid materials characterised by the additives
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/42—Methods or arrangements for servicing or maintenance of secondary cells or secondary half-cells
- H01M10/4235—Safety or regulating additives or arrangements in electrodes, separators or electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
- H01M4/583—Carbonaceous material, e.g. graphite-intercalation compounds or CFx
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/027—Negative electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/028—Positive electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2220/00—Batteries for particular applications
- H01M2220/20—Batteries in motive systems, e.g. vehicle, ship, plane
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2220/00—Batteries for particular applications
- H01M2220/30—Batteries in portable systems, e.g. mobile phone, laptop
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
- H01M2300/0037—Mixture of solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0048—Molten electrolytes used at high temperature
- H01M2300/0051—Carbonates
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
- H01M4/583—Carbonaceous material, e.g. graphite-intercalation compounds or CFx
- H01M4/587—Carbonaceous material, e.g. graphite-intercalation compounds or CFx for inserting or intercalating light metals
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- General Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Physics & Mathematics (AREA)
- Materials Engineering (AREA)
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
이차 전지의 구성을 궁리함으로써 적어도 고온에 견딜 수 있는 이차 전지를 실현한다. 플루오린화 마그네슘과, 플루오린화 리튬과, 니켈원과, 알루미늄원을 각각 미분쇄한 후에 코발트산 리튬 분말과 혼합하여 제 1 혼합물을 제작하는 제 1 단계와, 코발트산 리튬의 내열 온도 미만의 온도에서 가열하여 제 2 혼합물을 제작하는 제 2 단계를 가지는 제작 방법에 의하여 얻어진 양극 활물질을 사용하고, 전해액에 LiBOB를 가하는 이차 전지이다.
Description
본 발명은 물건, 방법, 또는 제작 방법에 관한 것이다. 또는 본 발명은 공정(process), 기계(machine), 제품(manufacture), 또는 조성물(composition of matter)에 관한 것이다. 특히 본 발명의 일 형태는 반도체 장치, 표시 장치, 발광 장치, 이차 전지, 축전 장치, 기억 장치, 이들의 구동 방법, 또는 이들의 제조 방법에 관한 것이다. 특히 본 발명의 일 형태는 이차 전지, 축전 장치, 및 그 제작 방법에 관한 것이다.
또한 본 명세서 중에서 이차 전지 또는 축전 장치란, 축전 기능을 가지는 소자 및 장치 전반을 가리키는 것이다.
근년, 리튬 이온 이차 전지, 리튬 이온 커패시터, 공기 전지, 전고체 전지 등 다양한 축전 장치의 개발이 활발히 이루어지고 있다. 특히 고출력, 고에너지 밀도인 리튬 이온 이차 전지는, 휴대 전화기, 스마트폰, 태블릿, 또는 노트북형 컴퓨터와 같은 휴대 정보 단말기, 휴대 음악 플레이어, 디지털 카메라, 의료 기기, 또는 하이브리드 자동차(HEV), 전기 자동차(EV), 또는 플러그인 하이브리드 자동차(PHEV)와 같은 차세대 클린 에너지 자동차 등, 반도체 산업의 발전과 함께 그 수요가 급속하게 확대되고 있으며, 충전이 가능한 에너지 공급원으로서 현대의 정보화 사회에 있어 불가결한 것이 되었다.
또한 전기 자동차(EV)는 전동 모터만을 구동부로 하는 차량이지만, 엔진 등의 내연 기관과 전동 모터를 모두 구비한 하이브리드 자동차도 있다. 자동차에 사용되는 이차 전지는 복수 개를 하나의 전지 팩으로 하고, 복수 세트의 전지 팩이 자동차의 하부에 배치된다.
이와 같이, 리튬 이온 이차 전지는 여러 가지 분야 또는 용도로 사용되고 있다. 이러한 상황에 있어서, 리튬 이온 이차 전지에 요구되는 특성으로서는 고에너지 밀도, 고사이클 특성, 및 다양한 동작 환경에서의 안전성 등이 있다.
특허문헌 1에는 전해액에 리튬비스옥살레이토보레이트(LiBOB)를 첨가한 이차 전지가 개시(開示)되어 있다.
또한 형석(플루오린화 칼슘) 등의 플루오린화물은 오래전부터 제철 등에 있어서 융제로서 사용되고 있으며, 물성의 연구가 진행되고 왔다(비특허문헌 1).
W. E. Counts, R. Roy, and E. F. Osborn, "Fluoride Model Systems: II, The Binary Systems CaF2-BeF2, MgF2-BeF2, and LiF-MgF2", Journal of the American Ceramic Society, 36 [1] 12-17 (1953).
전기 자동차는 동작 상태나 환경에 의존하여 온도 변화가 일어나기 쉽기 때문에, 온도에 대한 안전 대책이 필요하다. 전기 자동차에 탑재되는 부품 중에서도 이차 전지는 전기 자동차의 동력원으로서 가장 중요한 기능을 가진다. 한편으로, 정상적으로 동작할 수 있는 온도는, 전기 자동차의 사용 환경에 대하여 허용 범위가 좁다는 문제가 있다.
온도 환경이 정상 범위에서 벗어나면 이차 전지의 충방전 성능이나 수명에 큰 영향을 미칠 가능성이 있기 때문에, 가능한 한 일정한 온도 환경하에서 사용되는 것이 요구된다. 이차 전지는 주변 환경의 문제뿐만 아니라, 충방전에 의하여 대량의 전류가 흐르는 것으로 인하여도 이차 전지 자체의 온도가 상승된다.
또한 이차 전지의 구성에 사용되는 전해액에는 유기 용매가 사용된다. 그러나 유기 용매는 휘발성 및 저인화점을 가지기 때문에, 이 유기 용매를 리튬 이온 이차 전지에 사용한 경우, 내부 단락이나 과충전 등에 기인한 리튬 이온 이차 전지의 내부 온도의 상승으로 인한 리튬 이온 이차 전지의 파열이나 발화 등이 발생할 가능성이 있다. 또한 전해액의 일부(리튬염)는 가수 분해 반응으로 플루오린화 수소산을 발생시키고, 이 플루오린화 수소산은 금속을 부식시키기 때문에 전지의 신뢰성이 우려된다.
그래서 이차 전지의 구성을 궁리함으로써 적어도 고온에 견딜 수 있는 이차 전지를 실현하는 것을 과제 중 하나로 한다.
또한 전기 자동차는 대용량의 이차 전지를 탑재하기 때문에, 용량이 줄어든 후에 만충전으로 할 때에는 충전 시간이 길어지는 경우가 있다. 급속 충전을 하기 위해서는 고전압으로의 충전에 견디는 이차 전지가 요구되고 있다. 본 발명의 일 형태는 높은 충전 전압으로의 충전이 가능한 이차 전지를 제공하는 것을 과제 중 하나로 한다.
또는 본 발명의 일 형태는 고온에서의 열화나, 높은 충전 전압에서의 열화가 적은 축전 장치를 제공하는 것을 과제 중 하나로 한다. 또는 본 발명의 일 형태는 신규 축전 장치나 전자 기기 등을 제공하는 것을 과제 중 하나로 한다.
이차 전지에 인가되는 충전 전압을 상승시킬 수 있으면, 높은 전압으로 충전할 수 있는 시간이 길어져, 단위 시간당 충전량이 커지므로, 충전 시간이 단축된다. 리튬 이온 이차 전지로 대표되는 전기 화학 셀의 분야에 있어서, 4.5V를 초과하는 고전압이 되면 전지가 열화된다.
이차 전지에 인가되는 충전 전압을 상승시키면 부반응이 발생하여 전지 성능이 대폭적으로 저하되는 경우가 있다. 부반응이란, 활물질 또는 전해액이 화학 반응을 일으킴으로써 생기는 반응물의 형성 또는 산화나 전해액의 분해의 촉진 등을 가리킨다. 또한 전해액의 분해에 의하여 가스의 발생 및 체적의 팽창이 일어나는 경우도 있다.
본 발명의 일 형태는 전해액에 붕소계 첨가제를 가하는 이차 전지이다. 붕소계 첨가제로서는 LiBOB, 리튬다이플루오로옥살레이토보레이트(LiDFOB)를 사용할 수도 있다.
또한 본 발명의 일 형태는 플루오린을 함유시킨 양극 활물질 입자를 사용한다.
플루오린을 함유시킨 양극 활물질 입자의 제작 방법은, 리튬 산화물과 플루오린화물을 넣은 용기를 가열로 내에 배치하는 제 1 공정과, 가열로 내를 산소를 포함하는 분위기에서 가열하는 제 2 공정을 가지고, 제 2 공정의 가열 온도는 750℃ 이상 950℃ 이하이다. 제 2 공정의 가열 온도는 리튬 산화물과 플루오린화물이 가지는 원소의 상호 확산이 일어나는 온도이면 좋고, 플루오린화물이 LiF 및 MgF2를 가지는 경우에는, 도 13에 나타낸 바와 같이 LiF와 MgF2의 공융점 P는 742℃ 부근(T1)이기 때문에, 제 2 공정의 가열 온도를 742℃ 이상으로 하는 것이 바람직하다.
상기에 있어서, 가열 온도는 775℃ 이상 925℃ 이하인 것이 바람직하다. 800℃ 이상 900℃ 이하인 것이 더 바람직하다.
또한 상기에 있어서, 가열하기 전 또는 가열 중에 용기에 뚜껑을 덮는 공정을 포함하고, 플루오린화물이 플루오린화 리튬인 것이 바람직하다. 가열 중에는, 뚜껑을 덮음으로써 용기 내의 공간에서 가스화된 플루오린화물의 농도가 일정한 상태 또는 저감되지 않는 상태를 유지하고, 이에 따라 입자의 표층부에 플루오린을 포함시킬 수 있다. 뚜껑을 사용함으로써, 플루오린화물을 포함하는 분위기에서 양극 활물질을 간편하고 저렴하게 어닐링할 수 있다. 본 명세서 등에 있어서 표층부란, 양극 활물질의 표면으로부터 10nm 정도까지의 영역을 말한다. 금 및/또는 크랙에 의하여 생긴 면을 표면이라고 하여도 좋다. 또한 양극 활물질의 표층부보다 깊은 영역을 내부로 한다. 또한 양극 활물질의 표층부를 표면 근방이라고 부르는 경우도 있다.
리튬, 전이 금속(코발트, 니켈, 망가니즈 등), 및 산소를 가지는 복합 산화물은 결함 및 변형이 적은 층상 암염형 결정 구조를 가지는 것이 바람직하다. 그러므로 불순물이 적은 복합 산화물인 것이 바람직하다. 리튬, 전이 금속, 및 산소를 가지는 복합 산화물에 불순물이 많이 포함되면 결함 또는 변형이 많은 결정 구조가 될 가능성이 높아진다.
불순물을 포함시키지 않기 위해서도, 플루오린화물을 혼합한 후 뚜껑을 덮고 가열함으로써 양극 활물질의 표면 개질을 수행하는 것이 바람직하다. 뚜껑을 덮는 타이밍으로서는, 가열 전의 용기를 가열로에 배치하기 전, 용기를 가열로에 배치한 후, 및 가열 중에서의 플루오린화물이 용융되기 전 중 어느 하나의 타이밍이면 좋다.
상기 제작 방법으로 함으로써, 양극 활물질 입자에 플루오린을 함유시킬 수 있고, 플루오린에 의하여 양극 활물질 표면의 젖음성(wettability)이 좋게 되므로 균질화, 평탄화가 가능하다. 이러한 식으로 얻어지는 양극 활물질 입자와 LiBOB의 조합은 고전압으로의 충방전의 반복에 있어서 결정 구조가 붕괴되기 어려우므로, 이러한 식으로 얻어지는 양극 활물질 입자와 LiBOB의 조합을 가지는 이차 전지는 사이클 특성이 대폭적으로 향상된다.
또한 LiBOB의 첨가량이 지나치게 많으면 초기 용량이 저하될 우려가 있기 때문에, 전해액 중에서 LiBOB가 차지하는 비율은 0.1중량% 초과 3중량% 미만으로 하는 것이 바람직하다.
또한 양극 활물질 입자는 층상 구조를 가지고, 전이 금속, 구체적으로는 코발트가 용출되지 않도록 알루미늄이나 마그네슘을 첨가하여, 양극 활물질 입자의 외부 표면을 포함하는 영역(입자의 표층부)을 기계적 또는 화학적으로 튼튼하게 한다. 또한 양극 활물질 입자의 외측에 망가니즈를 넣음으로써도 전이 금속, 구체적으로는 니켈 또는 코발트가 용출되지 않도록 억제할 수 있다.
또한 이차 전지에는 양극, 음극, 도전재, 세퍼레이터, 전해액, 리튬염이 적어도 사용된다.
리튬염으로서는 예를 들어, 염화 리튬(LiCl), 플루오린화 리튬(LiF), 과염소산 리튬(LiClO4), 테트라플루오로붕산(LiBF4), LiAsF6, LiPF6, Li(CF3SO3), Li(FSO2)2N(소위 LiFSA), Li(CF3SO2)2N(소위 LiTFSA) 등이 있다.
리튬염은 전해액 중의 Li 이온의 이동을 돕는 역할을 한다. 전극에 사용되는 알루미늄과의 적합성, 비용면 등에서 LiPF6을 사용하는 것이 바람직하다. 다만 LiPF6은, 고온에서 불안정적이고 고온으로 인한 분해 등에 의하여 플루오린화 수소산을 발생시키기 때문에, 이차 전지의 열화의 원인이 될 우려가 있다.
전해액으로서는 캐리어 이온의 이동이 가능한 재료를 사용한다. 전해액의 용매로서는 비양성자성 유기 용매가 바람직하다. 비양성자성 유기 용매의 대표적인 예로서는, 에틸렌카보네이트(EC), 프로필렌카보네이트(PC), 다이메틸카보네이트, 다이에틸카보네이트(DEC), γ-뷰틸로락톤, 아세토나이트릴, 다이메톡시에테인, 테트라하이드로퓨란 등이 있고, 이들 중 하나 또는 복수를 사용할 수 있다. 또한 전해액의 용매로서 겔화된 고분자 재료를 사용하면, 누액성(漏液性) 등에 대한 안전성이 향상된다. 또한 축전지의 박형화 및 경량화가 가능하다. 겔화된 고분자 재료의 대표적인 예로서는, 실리콘(silicone) 겔, 아크릴 겔, 아크릴로나이트릴 겔, 폴리에틸렌옥사이드계 겔, 폴리프로필렌옥사이드계 겔, 플루오린계 폴리머의 겔 등이 있다.
전해액으로서는, 상기 중에서도 에틸렌카보네이트(EC)와 다이에틸카보네이트(DEC)가 내열성이 높기 때문에 바람직하다.
첨가제로서 LiBOB를 사용하면, 양극 활물질 표면에 제 1 피막을 형성하고 음극 활물질 표면에 제 2 피막을 형성함으로써, 전이 금속의 용출을 방지하고, LiPF6의 분해를 방지하고, 전해액의 분해를 방지할 수 있다. 높은 온도 그리고 4.5V 이상의 고전압 조건에서의 충방전을 수행하면, 전이 금속의 용출 및 LiPF6의 분해가 발생될 우려가 있다. 제 1 피막 및 제 2 피막은 이차 전지 셀의 제작 직후에는 거의 형성되지 않고, 이차 전지의 충방전에 의하여 충방전 시에 생기는 전하를 사용하여 형성된다. 이차 전지 셀의 제작 시에, 가스 빼기를 위한 통전, 소위 에이징(aging) 처리를 수행하는 경우에는 통전 시에 형성되는 경우도 있다.
또한 LiPF6은 미량의 분해이면, 플루오린화 수소산이 음극 계면에 양질의 피막을 형성하는 데에 기여하는 경우가 있다. LiPF6이 분해되어 발생하는 플루오린화물 이온이 양질의 피막을 형성함으로써, 양극에 사용된 알루미늄의 부식, 특히 알루미늄의 공식(pitting corrosion)이 방지된다.
상기와 같이, 고전압으로의 충전이 가능한 양극 활물질과, LiBOB를 조합하는 구성으로 함으로써, 리튬염의 하나인 LiPF6을 사용하여도 고온 시의 안정성이 확보되고, 또한 고온 사이클 특성의 대폭적인 개선에 효과가 있으므로, 현저한 상승 효과가 얻어진다.
충전 전압 4.5V, 45℃ 또는 60℃에서의 이차 전지의 사이클 특성을 향상시킬 수 있다. 따라서 급속 충전에서의 사이클 특성이 좋고, 고온에서의 열화나 높은 충전 전압에서의 열화가 적은 축전 장치를 실현할 수 있다.
도 1의 (A), (B)는 이차 전지의 사이클 특성을 나타낸 도면이다.
도 2는 첨가량과 방전 용량의 관계를 나타낸 그래프이다.
도 3은 본 발명의 일 형태를 나타내는 양극 활물질의 제작 흐름의 일례이다.
도 4는 본 발명의 일 형태를 나타내는 양극 활물질의 제작 흐름의 일례이다.
도 5의 (A), (B), (C)는 이차 전지의 제작예를 설명하는 도면이다.
도 6의 (A), (B)는 래미네이트형 이차 전지를 설명하는 도면이다.
도 7의 (A)는 양극의 상면도이고, 도 7의 (B)는 음극의 상면도이고, 도 7의 (C)는 적층체를 설명하는 도면이다.
도 8의 (A)는 래미네이트형 이차 전지의 상면도이고, 도 8의 (B)는 단면도를 설명하는 도면이다.
도 9의 (A)는 이차 전지의 사시도이고, 도 9의 (B)는 그 단면 사시도이고, 도 9의 (C)는 복수의 이차 전지를 포함하는 전지 팩의 사시도이고, 도 9의 (D)는 그 상면도이다.
도 10은 양극 활물질의 결정 구조와 자성(磁性)을 설명하는 도면이다.
도 11은 종래예의 양극 활물질의 결정 구조와 자성을 설명하는 도면이다.
도 12의 (A), (B), (C), (D), (E)는 전자 기기를 나타낸 사시도이다.
도 13은 플루오린화 리튬과 플루오린화 마그네슘의 조성 및 온도의 관계를 나타낸 상평형도이다.
도 14의 (A)는 이차 전지 내부에서의 양극 활물질과, 그 주변에 배치되는 전해액, 첨가제 등의 상황을 나타낸 모델도이고, 도 14의 (B)는 종래를 나타낸 모델도이다.
도 15는 화학 반응식을 나타낸 도면이다.
도 16은 화학 반응식을 나타낸 도면이다.
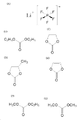
도 17의 (A)는 리튬염의 일종을 나타내는 화학식이고, 도 17의 (B), (C), (D)는 전해액을 나타내는 화학식이고, 도 17의 (E)는 첨가제를 나타내는 화학식이고, 도 17의 (F), (G)는 전해액을 나타내는 화학식이다.
도 18은 본 발명의 일 형태를 나타내는 이차 전지의 일부를 확대한 모델도이다.
도 19는 이차 전지의 사이클 특성을 나타낸 도면이다.
도 2는 첨가량과 방전 용량의 관계를 나타낸 그래프이다.
도 3은 본 발명의 일 형태를 나타내는 양극 활물질의 제작 흐름의 일례이다.
도 4는 본 발명의 일 형태를 나타내는 양극 활물질의 제작 흐름의 일례이다.
도 5의 (A), (B), (C)는 이차 전지의 제작예를 설명하는 도면이다.
도 6의 (A), (B)는 래미네이트형 이차 전지를 설명하는 도면이다.
도 7의 (A)는 양극의 상면도이고, 도 7의 (B)는 음극의 상면도이고, 도 7의 (C)는 적층체를 설명하는 도면이다.
도 8의 (A)는 래미네이트형 이차 전지의 상면도이고, 도 8의 (B)는 단면도를 설명하는 도면이다.
도 9의 (A)는 이차 전지의 사시도이고, 도 9의 (B)는 그 단면 사시도이고, 도 9의 (C)는 복수의 이차 전지를 포함하는 전지 팩의 사시도이고, 도 9의 (D)는 그 상면도이다.
도 10은 양극 활물질의 결정 구조와 자성(磁性)을 설명하는 도면이다.
도 11은 종래예의 양극 활물질의 결정 구조와 자성을 설명하는 도면이다.
도 12의 (A), (B), (C), (D), (E)는 전자 기기를 나타낸 사시도이다.
도 13은 플루오린화 리튬과 플루오린화 마그네슘의 조성 및 온도의 관계를 나타낸 상평형도이다.
도 14의 (A)는 이차 전지 내부에서의 양극 활물질과, 그 주변에 배치되는 전해액, 첨가제 등의 상황을 나타낸 모델도이고, 도 14의 (B)는 종래를 나타낸 모델도이다.
도 15는 화학 반응식을 나타낸 도면이다.
도 16은 화학 반응식을 나타낸 도면이다.
도 17의 (A)는 리튬염의 일종을 나타내는 화학식이고, 도 17의 (B), (C), (D)는 전해액을 나타내는 화학식이고, 도 17의 (E)는 첨가제를 나타내는 화학식이고, 도 17의 (F), (G)는 전해액을 나타내는 화학식이다.
도 18은 본 발명의 일 형태를 나타내는 이차 전지의 일부를 확대한 모델도이다.
도 19는 이차 전지의 사이클 특성을 나타낸 도면이다.
이하에서는 본 발명의 실시형태에 대하여 도면을 사용하여 자세히 설명한다. 다만 본 발명은 이하의 설명에 한정되지 않고, 그 형태 및 자세한 사항을 다양하게 변경할 수 있다는 것은 통상의 기술자라면 용이하게 이해할 수 있다. 또한 본 발명은 이하의 실시형태의 기재 내용에 한정하여 해석되는 것은 아니다.
(실시형태 1)
본 실시형태의 이차 전지는 리튬과, 전이 금속과, 마그네슘과, 산소와, 플루오린을 가지는 양극 활물질과, 리튬비스옥살레이토보레이트(LiBOB)를 포함하는 전해액을 가진다. 전이 금속은 코발트, 니켈, 망가니즈 중 적어도 하나이다. 양극 활물질은 알루미늄을 더 포함한다. 전해액은 리튬염과, 상기 리튬염을 용해시키는 다이에틸카보네이트 및 에틸렌카보네이트를 포함한다. 리튬염은 헥사플루오로인산 리튬이다. 음극 활물질은 인조 흑연이다. 또한 양극 활물질에 도전재를 가한 혼합물을 사용하여도 좋고, 그 도전재로서는 아세틸렌 블랙(AB)이나 VGCF(등록 상표)나 산화 그래핀 화합물을 사용하여도 좋다. 그 중에서도 산화 그래핀 화합물은 표면적이 작고, 전해액의 분해를 억제할 수 있기 때문에 바람직하다.
그래핀 화합물은 도전성이 높다는 우수한 전기 특성과, 유연성 및 기계적 강도가 높다는 우수한 물리 특성을 가지는 경우가 있다. 또한 그래핀 화합물은 평면적인 형상을 가진다. 그래핀 화합물은 접촉 저항이 낮은 면접촉을 가능하게 한다. 또한 얇더라도 도전성이 매우 높은 경우가 있어, 소량으로 활물질층 내에서 도전 경로를 효율적으로 형성할 수 있다. 따라서 도전 조제로서 그래핀 화합물을 사용함으로써, 활물질과 도전 조제의 접촉 면적을 크게 할 수 있기 때문에 바람직하다. 또한 전기적인 저항을 감소시킬 수 있는 경우가 있어 바람직하다. 여기서 그래핀 화합물로서 예를 들어, 그래핀, 다층 그래핀, 멀티 그래핀, 산화 그래핀, 다층 산화 그래핀, 멀티 산화 그래핀, 환원된 산화 그래핀, 환원된 다층 산화 그래핀, 환원된 멀티 산화 그래핀, 그래핀 퀀텀닷(quantum dot) 등이 있다. 환원된 산화 그래핀은 Reduced Graphene Oxide(이하 RGO)라고도 불린다. 여기서 RGO는 예를 들어 산화 그래핀(GO: Graphene Oxide)을 환원함으로써 얻어지는 화합물을 가리킨다. 입경이 작은 활물질 입자, 예를 들어 1μm 이하의 활물질 입자를 사용하는 경우에는 활물질 입자의 비표면적이 크기 때문에 활물질 입자들을 연결하는 도전 경로가 더 많이 필요하게 된다. 이러한 경우에는 소량으로도 도전 경로를 효율적으로 형성할 수 있는 그래핀 화합물을 사용하는 것이 특히 바람직하다. 또한 본 명세서 등에서 산화 그래핀이란, 탄소와 산소를 가지고, 시트 형상을 가지고, 작용기, 특히 에폭시기, 카복시기, 또는 하이드록시기를 가지는 것을 말한다. 또한 복수의 그래핀 화합물끼리 결합함으로써 그물 형상의 그래핀 화합물 시트(이하 그래핀 화합물 넷 또는 그래핀 넷이라고 함)를 형성할 수 있다. 활물질을 그래핀 넷이 피복하는 경우에 그래핀 넷은 활물질끼리 결합시키는 바인더로서도 기능할 수 있다. 따라서 바인더의 양을 줄일 수 있거나 또는 사용하지 않게 할 수 있기 때문에, 전극 체적이나 전극 중량에서 차지하는 활물질의 비율을 높일 수 있다. 즉 이차 전지의 용량을 증가시킬 수 있다.
도 1의 (A) 및 (B)에, 리튬과, 코발트와, 니켈과, 알루미늄과, 산소와, 플루오린을 가지는 양극 활물질과, 리튬비스옥살레이토보레이트를 1중량% 포함하는 전해액을 가지는 이차 전지의 사이클 특성을 나타내었다. 도 1의 (A)는 45℃, 4.5V 충전의 조건에서의 사이클 특성을 나타낸 것이고, 도 1의 (B)는 60℃, 4.5V 충전의 조건에서의 사이클 특성을 나타낸 것이다. 또한 도 19에는 충전 사이클 수의 가로축을 800으로 한 결과도 나타내었고, 유지율 80%에 상당하는 사이클 수가 600인 것을 나타낸다. 또한 도 19에서의 사이클 수 300의 부분이 도 1의 (A)에 상당한다.
도 1의 (A)에 있어서, 사이클 조건으로서는 충전을 CCCV(0.5C, 4.5V, 종지 전류 0.2C), 방전을 CC(0.5C, 3.0V)로 하고 45℃에서 사이클 특성을 평가하였다. 또한 도 1의 (B)에 있어서, 사이클 조건으로서는 충전을 CCCV(0.5C, 4.5V, 종지 전류 0.2C), 방전을 CC(0.5C, 3V)로 하고 60℃에서 사이클 특성을 평가하였다. 또한 도 1의 (A)에 있어서, 첨가제를 가한 이차 전지의 초기 방전 용량은 191.4mAh/g이었다.
또한 이들 이차 전지의 전해액은 LiBOB 외에, 리튬염인 헥사플루오로인산 리튬과, 상기 리튬염을 용해시키는 다이에틸카보네이트 및 에틸렌카보네이트를 포함한다. 에틸렌카보네이트와 다이에틸카보네이트의 비는 3:7이다.
첨가제인 LiBOB는 용매에 용해되기 어려워, 도 2에 나타낸 바와 같이 첨가량이 많아지면 방전 용량이 저하된다. 도 2는 세로축에 최대 방전 용량을 취하고, 첨가제를 가하지 않은 이차 전지, LiBOB 1중량%의 이차 전지, LiBOB 1.5중량%의 이차 전지, LiBOB 2중량%의 이차 전지 각각의 값을 나타내는 그래프이다. 또한 도 2는 45℃, 3V 내지 4.5V에서 0.5C 내지 0.2C의 충전을 수행하고, 컷오프 전압까지 도달하면 0.5C로 방전한 결과를 나타낸 것이다. 또한 첨가량이 지나치게 많으면, 저온에서 LiBOB의 석출이 발생할 우려가 있기 때문에, 전해액 중에서 LiBOB가 차지하는 비율은 0.1중량% 초과 3중량% 미만으로 하는 것이 바람직하다.
또한 양극 활물질에도 특징이 있고, 리튬과, 코발트와, 마그네슘과, 알루미늄과, 니켈과, 산소와, 플루오린을 가지는 양극 활물질이다. 이 양극 활물질과, 전해액과, 첨가제를 조합함으로써 도 1에 나타낸 바와 같이 현저한 효과가 나타난다.
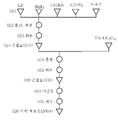
양극 활물질의 제작에 대하여 도 3에 나타낸 제작 흐름을 사용하여 이하에서 설명한다.
<단계 S21>
먼저 혼합물(901)의 재료로서 플루오린원이나 염소원 등의 할로젠원, 마그네슘원, 니켈원, 및 알루미늄원을 준비한다. 또한 리튬원도 준비하는 것이 바람직하다.
플루오린원으로서는 예를 들어 플루오린화 리튬, 플루오린화 마그네슘 등을 사용할 수 있다. 그 중에서도 플루오린화 리튬은 융점이 848℃로 비교적 낮아, 후술하는 어닐링 공정에서 용융되기 쉽기 때문에 바람직하다. 염소원으로서는 예를 들어 염화 리튬, 염화 마그네슘 등을 사용할 수 있다. 마그네슘원으로서는 예를 들어 플루오린화 마그네슘, 산화 마그네슘, 수산화 마그네슘, 탄산 마그네슘 등을 사용할 수 있다. 리튬원으로서는 예를 들어 플루오린화 리튬, 탄산 리튬을 사용할 수 있다. 즉 플루오린화 리튬은 리튬원으로서도 플루오린원으로서도 사용할 수 있다. 또한 플루오린화 마그네슘은 플루오린원으로서도 마그네슘원으로서도 사용할 수 있다.
본 실시형태에서는 플루오린원 및 리튬원으로서 플루오린화 리튬 LiF를 준비하고, 플루오린원 및 마그네슘원으로서 플루오린화 마그네슘 MgF2를 준비하는 것으로 한다(도 3의 단계 S21).
플루오린화 리튬 LiF과 플루오린화 마그네슘 MgF2는 LiF:MgF2=65:35(몰비) 정도로 혼합하면 융점이 저하되는 효과가 가장 높아진다. 한편 플루오린화 리튬이 많아지면 리튬 과잉이 되어 사이클 특성이 악화될 우려가 있다. 그러므로 플루오린화 리튬 LiF과 플루오린화 마그네슘 MgF2의 몰비는 LiF:MgF2=x:1(0≤x≤1.9)인 것이 바람직하고, LiF:MgF2=x:1(0.1≤x≤0.5)인 것이 더 바람직하고, LiF:MgF2=x:1(x=0.33 근방)인 것이 더욱 바람직하다.
니켈원으로서는 예를 들어 수산화 니켈(Ni(OH)2)을 사용할 수 있다. 이때 니켈원은 미분쇄되어 있는 것이 바람직하다. 예를 들어 볼밀, 비드밀 등을 사용하고, 아세톤을 용매로 하여 수산화 니켈을 혼합 및 분쇄함으로써, 미분쇄된 수산화 니켈을 얻을 수 있다.
알루미늄원으로서는 예를 들어 수산화 알루미늄(Al(OH)3)을 사용할 수 있다. 알루미늄원은 미분쇄되어 있는 것이 바람직하다. 예를 들어 볼밀, 비드밀 등을 사용하고, 아세톤을 용매로 하여 수산화 알루미늄을 혼합 및 분쇄함으로써, 미분쇄된 수산화 알루미늄을 얻을 수 있다.
또한 다음의 혼합 및 분쇄 공정을 습식으로 수행하는 경우에는 용매를 준비한다. 용매로서는 아세톤 등의 케톤, 에탄올 및 아이소프로판올 등의 알코올, 에터, 다이옥세인, 아세토나이트릴, N-메틸-2-피롤리돈(NMP) 등을 사용할 수 있다. 리튬과 반응하기 어려운 비양성자성 용매를 사용하는 것이 더 바람직하다. 본 실시형태에서는 아세톤을 사용한다(도 3의 단계 S21 참조).
<단계 S22>
다음으로 상술한 혼합물(901)의 재료를 혼합 및 분쇄한다(도 3의 단계 S22). 혼합은 건식 또는 습식으로 수행할 수 있지만 습식은 더 작게 분쇄할 수 있기 때문에 바람직하다. 혼합에는 예를 들어 볼밀, 비드밀 등을 사용할 수 있다. 볼밀을 사용하는 경우에는 예를 들어 미디어로서 지르코니아 볼을 사용하는 것이 바람직하다. 이 혼합 및 분쇄 공정을 충분히 수행하여 혼합물(901)을 미분쇄하는 것이 바람직하다.
혼합 수단으로서 블렌더, 믹서기, 볼밀을 사용한 혼합이 적합하다.
<단계 S23, 단계 S24>
위에서 혼합, 분쇄한 재료를 회수하여(도 3의 단계 S23), 혼합물(901)을 얻는다(도 3의 단계 S24).
혼합물(901)은 예를 들어 메디안 지름(D50)이 600nm 이상 20μm 이하인 것이 바람직하고, 1μm 이상 10μm 이하인 것이 더 바람직하다. 이러한 식으로 미분쇄된 혼합물(901)이면, 추후의 공정에서 리튬, 전이 금속, 및 산소를 가지는 복합 산화물과 혼합할 때 복합 산화물 입자의 표면에 혼합물(901)을 균일하게 부착시키기 쉽다. 혼합물(901)이 복합 산화물 입자의 표면에 균일하게 부착되면, 가열 후에 복합 산화물 입자의 표층부에 할로젠 및 마그네슘을 빠짐없이 분포시키기 쉽기 때문에 바람직하다. 표층부에 할로젠 및 마그네슘이 포함되지 않는 영역이 있으면, 충전 상태에서 상술한 의사 스피넬형 결정 구조가 되기 어려워질 우려가 있다.
<단계 S25>
단계 S25에서, 미리 합성된 리튬, 전이 금속, 및 산소를 가지는 복합 산화물을 사용한다.
미리 합성된 리튬, 전이 금속, 및 산소를 가지는 복합 산화물을 사용하는 경우, 불순물이 적은 것을 사용하는 것이 바람직하다. 본 명세서 등에서는, 리튬, 전이 금속, 및 산소를 가지는 복합 산화물, 그리고 양극 활물질에 대해서는 주성분을 리튬, 코발트, 니켈, 망가니즈, 알루미늄, 및 산소로 하고, 상기 주성분 이외의 원소를 불순물로 한다. 예를 들어 글로 방전 질량 분석법으로 분석하였을 때, 불순물 농도의 합계가 10,000ppm wt 이하인 것이 바람직하고, 5000ppm wt 이하인 것이 더 바람직하다. 특히 타이타늄 등의 전이 금속 및 비소의 불순물 농도의 합계가 3000ppm wt 이하인 것이 바람직하고, 1500ppm wt 이하인 것이 더 바람직하다.
예를 들어 미리 합성된 코발트산 리튬으로서, NIPPON CHEMICAL INDUSTRIAL CO., LTD. 제조의 코발트산 리튬 입자(상품명: CELLSEED C-10N)를 사용할 수 있다. 이것은 메디안 지름(D50)이 약 12μm이고, 글로 방전 질량 분석법(GD-MS)에 의한 불순물 분석에서, 마그네슘 농도 및 플루오린 농도가 50ppm wt 이하이고, 칼슘 농도, 알루미늄 농도, 및 실리콘 농도가 100ppm wt 이하이고, 니켈 농도가 150ppm wt 이하이고, 황 농도가 500ppm wt 이하이고, 비소 농도가 1100ppm wt 이하이고, 리튬, 코발트, 및 산소 이외의 기타 원소의 농도가 150ppm wt 이하인 코발트산 리튬이다.
단계 S25에서의 리튬, 전이 금속, 및 산소를 가지는 복합 산화물은 결함 및 변형이 적은 층상 암염형 결정 구조를 가지는 것이 바람직하다. 그러므로 불순물이 적은 복합 산화물인 것이 바람직하다. 리튬, 전이 금속, 및 산소를 가지는 복합 산화물에 불순물이 많이 포함되면 결함 또는 변형이 많은 결정 구조가 될 가능성이 높아진다.
<단계 S31>
다음으로 혼합물(901)과, 리튬, 전이 금속, 및 산소를 가지는 복합 산화물을 혼합한다(도 3의 단계 S31). 리튬, 전이 금속, 및 산소를 가지는 복합 산화물 중의 전이 금속의 원자수 TM와 혼합물(902)이 가지는 마그네슘의 원자수 MgMix1의 비는 TM:MgMix1=1:y(0.005≤y≤0.05)인 것이 바람직하고, TM:MgMix1=1:y(0.007≤y≤0.04)인 것이 더 바람직하고, TM:MgMix1=1:0.02 정도인 것이 더욱 바람직하다.
단계 S31의 혼합은, 복합 산화물 입자를 파괴하지 않도록, 단계 S22의 혼합보다 완만한 조건으로 하는 것이 바람직하다. 예를 들어, 단계 S22의 혼합보다 회전수가 적거나 또는 시간이 짧은 조건으로 하는 것이 바람직하다. 또한 습식보다 건식이 더 완만한 조건이라고 할 수 있다. 혼합에는 예를 들어 볼밀, 비드밀 등을 사용할 수 있다. 볼밀을 사용하는 경우에는 예를 들어 미디어로서 지르코니아 볼을 사용하는 것이 바람직하다.
위에서 혼합한 재료를 회수하여(도 3의 단계 S32), 혼합물(903)을 얻는다(도 3의 단계 S33).
다음으로 혼합물(903)을 가열한다(도 3의 단계 S34). 본 공정은 어닐링 또는 소성이라고 부르는 경우가 있다. 어닐링을 수행함으로써 LiMO2가 생성된다. 그러므로 온도나 시간, 분위기, 어닐링을 수행하는 혼합물(903)의 중량 등, 단계 S34를 수행하는 조건이 중요하다. 또한 본 명세서에서 어닐링에는 혼합물(903)을 가열하는 경우나, 적어도 혼합물(903)을 배치한 가열로를 가열하는 경우도 그 의미에 포함된다. 본 명세서에서 가열로란, 어떤 물질이나 혼합물에 대하여 열처리(어닐링)를 실시하기 위하여 사용하는 장치이고, 히터부와, 플루오린화물을 포함하는 분위기 및 적어도 600℃에 견디는 내벽을 가진다. 또한 가열로에는 가열로 내부를 감압하는 기능 및 가압하는 기능 중 적어도 한쪽을 가지는 펌프가 제공되어도 좋다. 예를 들어 S34의 어닐링 중에 가압하여도 좋다.
S34의 어닐링 온도는 코발트산 리튬(S25)과 플루오린화물의 반응이 진행되는 온도 이상일 필요가 있다. 여기서 말하는 반응이 진행되는 온도란, 코발트산 리튬과 플루오린화물이 가지는 원소의 상호 확산이 발생하는 온도이면 좋다. 그러므로 이들 재료의 용융 온도보다 낮아도 좋다. 예를 들어 산화물에서는 용융 온도 Tm의 0.757배(탐만 온도 Td)에서 고상 확산이 발생한다. 그러므로 예를 들어 500℃ 이상이면 좋다.
다만 혼합물(903)의 적어도 일부가 용융하는 온도 이상이면 반응이 더 진행되기 쉬워 바람직하다. 그러므로 어닐링 온도는 플루오린화물의 공융점 이상인 것이 바람직하다. 플루오린화물이 LiF 및 MgF2를 가지는 경우, 도 13(비특허문헌 1, 도 1471-A를 인용하여 가필하였음)에 나타낸 바와 같이, LiF와 MgF2의 공융점 P는 742℃ 부근(T1)이기 때문에, S34의 어닐링 온도를 742℃ 이상으로 하는 것이 바람직하다.
S34의 어닐링 온도는 높으면 반응이 진행되기 쉬워 어닐링 시간을 짧게 할 수 있으므로 생산성이 높아 바람직하다.
다만 어닐링 온도는 LiCoO2의 분해 온도(1130℃) 이하일 필요가 있다. 또한 LiCoO2의 분해 온도는 1130℃이지만, 그 근방의 온도에서는 미량이지만 LiCoO2가 분해될 것이 우려된다. 그러므로 어닐링 온도로서는 1130℃ 이하가 바람직하고, 1000℃ 이하가 더 바람직하고, 950℃ 이하가 더욱 바람직하고, 900℃ 이하가 더욱더 바람직하다.
따라서, 어닐링 온도로서는 500℃ 이상 1130℃ 이하가 바람직하고, 500℃ 이상 1000℃ 이하가 더 바람직하고, 500℃ 이상 950℃ 이하가 더욱 바람직하고, 500℃ 이상 900℃ 이하가 더욱더 바람직하다. 또한 742℃ 이상 1130℃ 이하가 바람직하고, 742℃ 이상 1000℃ 이하가 더 바람직하고, 742℃ 이상 950℃ 이하가 더욱 바람직하고, 742℃ 이상 900℃ 이하가 더욱더 바람직하다. 또한 800℃ 이상 1130℃ 이하가 바람직하고, 800℃ 이상 1000℃ 이하가 더 바람직하고, 800℃ 이상 950℃ 이하가 더욱 바람직하고, 800℃(T2) 이상 900℃(T3) 이하(범위 L)가 가장 바람직하다. 또한 830℃ 이상 1130℃ 이하가 바람직하고, 830℃ 이상 1000℃ 이하가 더 바람직하고, 830℃ 이상 950℃ 이하가 더욱 바람직하고, 830℃ 이상 900℃ 이하가 더욱더 바람직하다.
더 구체적으로는 플루오린화물로서 LiF를 사용하고 뚜껑을 덮고 S34의 어닐링을 수행함으로써, 사이클 특성 등이 양호한 양극 활물질을 제작할 수 있다. 또한 플루오린화물로서 LiF 및 MgF2를 사용하면, LiCoO2와의 반응이 촉진되어, LiMO2가 생성된다고 생각된다.
또한 본 실시형태에서는 플루오린화물인 LiF가 융제로서 기능하는 것으로 생각된다. 따라서 가열로 내부의 용적이 용기의 용적에 비하여 크고 LiF는 산소보다 가볍기 때문에, 휘발하여 혼합물(903) 중의 LiF가 감소되면 LiMO2의 생성이 억제될 것이 예상된다. 그러므로 LiF의 휘발을 억제하면서 가열할 필요가 있다. 또한 LiF를 사용하지 않은 경우에도, 코발트산 리튬 표면의 Li와 F가 반응하여 LiF가 생겨 휘발할 가능성도 있다. 그러므로 LiF보다 융점이 높은 플루오린화물을 사용하는 경우에도 마찬가지로 휘발의 억제가 필요하다.
그래서 LiF를 포함하는 분위기에서 혼합물(903)을 가열함으로써, 즉 가열로 내의 LiF의 분압이 높은 상태로 혼합물(903)을 가열함으로써, 혼합물(903) 중의 LiF의 휘발을 억제한다. 공융 혼합물을 형성하는 플루오린화물(LiF 또는 MgF)을 사용하고 뚜껑을 덮고 어닐링함으로써, 어닐링 온도를 LiCoO2의 분해 온도(1130℃) 이하, 구체적으로는 742℃ 이상 1000℃ 이하로 저온화할 수 있어, LiMO2의 생성을 효율적으로 진행시킬 수 있다. 그러므로 특성이 양호한 양극 활물질을 형성할 수 있고, 또한 어닐링 시간을 단축할 수도 있다.
상기 단계 S34의 어닐링은 적절한 온도 및 시간으로 수행하는 것이 바람직하다. 적절한 온도 및 시간은 코발트산 리튬(S25)의 입자의 크기 및 조성 등의 조건에 따라 변화된다. 입자가 작은 경우에는 입자가 큰 경우보다 낮은 온도 또는 짧은 시간으로 하는 것이 더 바람직한 경우가 있다. S34의 어닐링 후에 뚜껑을 빼는 공정을 가진다.
예를 들어 코발트산 리튬(S25)의 입자의 메디안 지름(D50)이 12μm 정도인 경우, 어닐링 시간은 예를 들어 3시간 이상이 바람직하고, 10시간 이상이 더 바람직하다.
한편, 코발트산 리튬(S25)의 입자의 메디안 지름(D50)이 5μm 정도인 경우, 어닐링 시간은 예를 들어 1시간 이상 10시간 이하가 바람직하고, 2시간 정도가 더 바람직하다.
어닐링 후의 강온(降溫) 시간은 예를 들어 10시간 이상 50시간 이하로 하는 것이 바람직하다.
위에서 어닐링한 재료를 회수한다(도 3의 단계 S35). 또한 입자를 체로 치는 것이 바람직하다. 상기 공정을 통하여, 본 발명의 일 형태의 양극 활물질(200A)을 제작할 수 있다(도 3의 단계 S36).
또한 양극 활물질은 상기 구성에 한정되지 않고, 니켈과 알루미늄을 사용하지 않는 양극 활물질이어도, 이 양극 활물질과, 전해액과, 첨가제를 조합함으로써 현저한 효과를 얻을 수 있다.
니켈과 알루미늄을 사용하지 않는 양극 활물질의 제작의 다른 예에 대하여 도 4에 나타낸 제작 흐름을 사용하여 이하에서 설명한다.
도 4의 단계 S11에 나타낸 바와 같이, 우선 혼합물(902)의 재료로서 플루오린원인 플루오린화 리튬, 및 마그네슘원인 플루오린화 마그네슘을 준비한다. 플루오린화 리튬은 융점이 848℃로 비교적 낮아, 후술하는 어닐링 공정에서 용융되기 쉽기 때문에 바람직하다. 즉 플루오린화 리튬은 리튬원으로서도 플루오린원으로서도 사용할 수 있다. 또한 플루오린화 마그네슘은 플루오린원으로서도 마그네슘원으로서도 사용할 수 있다.
도 4에서는, 플루오린원 및 리튬원으로서 플루오린화 리튬 LiF을 준비하고, 플루오린원 및 마그네슘원으로서 플루오린화 마그네슘 MgF2를 준비한다(도 4의 단계 S11). 플루오린화 리튬 LiF과 플루오린화 마그네슘 MgF2의 몰비는 LiF:MgF2=x:1(0≤x≤1.9)인 것이 바람직하고, LiF:MgF2=x:1(0.1≤x≤0.5)인 것이 더 바람직하고, LiF:MgF2=x:1(x=0.33 근방)인 것이 더욱 바람직하다.
또한 다음의 혼합 및 분쇄 공정을 습식으로 수행하는 경우에는 용매를 준비한다. 용매로서는 아세톤 등의 케톤, 에탄올 및 아이소프로판올 등의 알코올, 에터, 다이옥세인, 아세토나이트릴, N-메틸-2-피롤리돈(NMP) 등을 사용할 수 있다. 리튬과 반응하기 어려운 비양성자성 용매를 사용하는 것이 더 바람직하다. 본 실시형태에서는 아세톤을 사용한다(도 4의 단계 S11 참조).
다음으로 상술한 혼합물(902)의 재료를 혼합 및 분쇄한다(도 4의 단계 S12). 혼합은 건식 또는 습식으로 수행할 수 있지만 습식은 더 작게 분쇄할 수 있기 때문에 바람직하다. 혼합에는 예를 들어 볼밀, 비드밀 등을 사용할 수 있다. 볼밀을 사용하는 경우에는 예를 들어 미디어로서 지르코니아 볼을 사용하는 것이 바람직하다. 이 혼합 및 분쇄 공정을 충분히 수행하여 혼합물(902)을 미분쇄하는 것이 바람직하다.
위에서 혼합, 분쇄한 재료를 회수하여(도 4의 단계 S13), 혼합물(902)을 얻는다(도 4의 단계 S14).
혼합물(902)은 예를 들어 D50이 600nm 이상 20μm 이하인 것이 바람직하고, 1μm 이상 10μm 이하인 것이 더 바람직하다. 이러한 식으로 미분쇄된 혼합물(902)이면, 추후의 공정에서 리튬, 전이 금속, 및 산소를 가지는 복합 산화물과 혼합할 때 복합 산화물 입자의 표면에 혼합물(902)을 균일하게 부착시키기 쉽다. 혼합물(902)이 복합 산화물 입자의 표면에 균일하게 부착되면, 가열 후에 복합 산화물 입자의 표층부에 할로젠 및 마그네슘을 빠짐없이 분포시키기 쉽기 때문에 바람직하다. 표층부에 할로젠 및 마그네슘이 포함되지 않는 영역이 있으면, 충전 상태에서 상술한 의사 스피넬형 결정 구조가 되기 어려워질 우려가 있다.
다음으로, 단계 S25에 나타낸 바와 같이 리튬원을 준비한다. 단계 S25에서, 미리 합성된 리튬, 전이 금속, 및 산소를 가지는 복합 산화물을 사용한다.
예를 들어 미리 합성된 코발트산 리튬으로서, NIPPON CHEMICAL INDUSTRIAL CO., LTD. 제조의 코발트산 리튬 입자(상품명: CELLSEED C-10N)를 사용할 수 있다. 이것은 메디안 지름(D50)이 약 12μm이고, 글로 방전 질량 분석법(GD-MS)에 의한 불순물 분석에서, 마그네슘 농도 및 플루오린 농도가 50ppm wt 이하이고, 칼슘 농도, 알루미늄 농도, 및 실리콘 농도가 100ppm wt 이하이고, 니켈 농도가 150ppm wt 이하이고, 황 농도가 500ppm wt 이하이고, 비소 농도가 1100ppm wt 이하이고, 리튬, 코발트, 및 산소 이외의 기타 원소의 농도가 150ppm wt 이하인 코발트산 리튬이다.
단계 S25에서의 리튬, 전이 금속, 및 산소를 가지는 복합 산화물은 결함 및 변형이 적은 층상 암염형 결정 구조를 가지는 것이 바람직하다. 그러므로 불순물이 적은 복합 산화물인 것이 바람직하다. 리튬, 전이 금속, 및 산소를 가지는 복합 산화물에 불순물이 많이 포함되면 결함 또는 변형이 많은 결정 구조가 될 가능성이 높아진다.
다음으로 혼합물(902)과, 리튬, 전이 금속, 및 산소를 가지는 복합 산화물을 혼합한다(도 4의 단계 S31). 리튬, 전이 금속, 및 산소를 가지는 복합 산화물 중의 전이 금속의 원자수 TM와 혼합물(902)이 가지는 마그네슘의 원자수 MgMix1의 비는 TM:MgMix1=1:y(0.005≤y≤0.05)인 것이 바람직하고, TM:MgMix1=1:y(0.007≤y≤0.04)인 것이 더 바람직하고, TM:MgMix1=1:0.02 정도인 것이 더욱 바람직하다.
단계 S31의 혼합은, 복합 산화물 입자를 파괴하지 않도록, 단계 S12의 혼합보다 완만한 조건으로 하는 것이 바람직하다. 예를 들어, 단계 S12의 혼합보다 회전수가 적거나 또는 시간이 짧은 조건으로 하는 것이 바람직하다. 또한 습식보다 건식이 더 완만한 조건이라고 할 수 있다. 혼합에는 예를 들어 볼밀, 비드밀 등을 사용할 수 있다. 볼밀을 사용하는 경우에는 예를 들어 미디어로서 지르코니아 볼을 사용하는 것이 바람직하다.
위에서 혼합한 재료를 회수하여(도 4의 단계 S32), 혼합물 B를 얻는다(도 4의 단계 S33).
다음으로 혼합물 B를 가열한다(도 4의 단계 S34).
어닐링은 적절한 온도 및 시간으로 수행하는 것이 바람직하다. 적절한 온도 및 시간은 단계 S25에서의 리튬, 전이 금속, 및 산소를 가지는 복합 산화물 입자의 크기 및 조성 등의 조건에 따라 변화된다. 입자가 작은 경우에는 입자가 큰 경우보다 낮은 온도 또는 짧은 시간으로 하는 것이 더 바람직한 경우가 있다.
예를 들어 단계 S25의 입자의 메디안 지름(D50)이 12μm 정도인 경우, 어닐링 온도는 예를 들어 600℃ 이상 950℃ 이하가 바람직하다. 어닐링 시간은 예를 들어 3시간 이상이 바람직하고, 10시간 이상이 더 바람직하고, 60시간 이상이 더욱 바람직하다.
한편 단계 S25의 입자의 메디안 지름(D50)이 5μm 정도인 경우, 어닐링 온도는 예를 들어 600℃ 이상 950℃ 이하가 바람직하다. 어닐링 시간은 예를 들어 1시간 이상 10시간 이하가 바람직하고, 2시간 정도가 더 바람직하다.
어닐링 후의 강온 시간은 예를 들어 10시간 이상 50시간 이하로 하는 것이 바람직하다.
혼합물 B를 어닐링하면, 혼합물 B 중 융점이 낮은 재료(예를 들어 플루오린화 리튬, 융점 848℃)가 먼저 용융되고 복합 산화물 입자의 표층부에 분포되는 것으로 생각된다. 다음으로 이 용융된 재료의 존재에 의하여 다른 재료의 융점 강하가 일어나 다른 재료가 용융되는 것으로 추측된다. 예를 들어 플루오린화 마그네슘(융점 1263℃)이 용융되고, 복합 산화물 입자의 표층부에 분포되는 것으로 생각된다.
이 혼합물 B가 가지는 원소는, 복합 산화물 입자 내부보다 표층부 및 입계 근방에서 빠르게 확산된다. 그러므로 마그네슘 및 할로젠은 표층부 및 입계 근방에서 내부보다 농도가 높아진다. 후술하는 바와 같이, 표층부 및 입계 근방의 마그네슘 농도가 높으면 결정 구조의 변화를 더 효과적으로 억제할 수 있다.
위에서 어닐링한 재료를 회수하여(도 4의 단계 S35), 양극 활물질(200B)을 얻는다(도 4의 단계 S36).
상기와 같이 함으로써 얻어지는 양극 활물질(200B)을 사용한 이차 전지에, LiBOB를 첨가한 전해액을 사용하면 45℃ 이상의 사이클 특성에서 양호한 결과를 얻을 수 있다.
(실시형태 2)
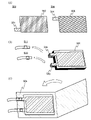
래미네이트형 이차 전지의 제작 방법의 일례에 대하여 도 5의 (B) 및 (C)를 사용하여 설명한다.
우선 음극(506), 세퍼레이터(507), 및 양극(503)을 적층한다.
도 5의 (A)에는 양극(503) 및 음극(506)의 외관도를 나타내었다. 양극(503)은 양극 집전체(501)를 가지고, 양극 활물질층(502)은 양극 집전체(501)의 표면에 형성된다. 양극 활물질, 아세틸렌 블랙(AB), 및 폴리플루오린화 바이닐리덴(PVDF)을 양극 활물질:AB:PVDF=95:3:2(중량비)로 혼합한 슬러리를 양극 집전체(501)에 도포하고, 선압 120kN/m로 120℃의 프레스를 수행함으로써 양극 활물질층(502)을 형성한다. AB는 도전재(도전 조제라고도 불림)로서 사용하였다. 혼합의 순서는 우선 활물질과, AB와, 40%의 폴리플루오린화 바이닐리덴(PVDF)을 혼합하고, 균일하게 될 때까지 혼련한 후, 나머지(60%) PVDF를 넣고, NMP를 혼합함으로써 점도 조정을 수행하여, 슬러리를 제작한다. 도포 후에는 통풍 건조로에서 80℃, 30분의 건조를 수행한다.
또한 양극(503)은 양극 집전체(501)가 일부 노출되는 영역(이하 탭(tab) 영역이라고 함)을 가진다. 음극(506)은 음극 집전체(504)를 가지고, 음극 활물질층(505)은 음극 집전체(504)의 표면에 형성되어 있다. 또한 음극(506)은 음극 집전체(504)가 일부 노출되는 영역, 즉 탭 영역을 가진다. 양극 및 음극이 가지는 탭 영역의 면적이나 형상은 도 5의 (A)에 나타낸 예에 한정되지 않는다.
도 5의 (B)에, 적층된 음극(506), 세퍼레이터(507), 및 양극(503)을 나타내었다. 여기서는 음극을 5개, 양극을 4개 사용하는 예를 나타내었다. 다음으로, 양극(503)의 탭 영역들을 서로 접합하고, 최표면에 위치하는 양극의 탭 영역과 양극 리드 전극(510)을 접합한다. 접합에는 예를 들어 초음파 용접 등을 사용하면 좋다. 마찬가지로 음극(506)의 탭 영역들을 서로 접합하고, 최표면에 위치하는 음극의 탭 영역과 음극 리드 전극(511)을 접합한다.
다음으로, 외장체(509) 위에 음극(506), 세퍼레이터(507), 및 양극(503)을 배치한다.
다음으로, 도 5의 (C)에 나타낸 바와 같이, 외장체(509)를 파선으로 나타낸 부분에서 접는다. 그 후, 외장체(509)의 외주부를 접합한다. 접합에는 예를 들어 열 압착 등을 사용하면 좋다. 이때 추후에 전해액(508)을 도입할 수 있도록, 외장체(509)의 일부(또는 한 변)에 접합되지 않는 영역(이하 도입구라고 함)을 제공한다.
다음으로, 외장체(509)에 제공된 도입구로부터, 전해액(508)을 외장체(509)의 내측에 도입한다. 전해액(508)의 도입은, 감압 분위기하 또는 불활성 분위기하에서 수행하는 것이 바람직하다. 본 실시형태에서는 리튬염으로서 1mol/l의 LiPF6을 사용하고, 용매로서 EC:DEC를 3:7의 비율(체적비)로 사용하고, 첨가제로서 LiBOB를 1중량%로 사용하고, 합계 600μL을 도입구로부터 넣는다. 그리고 마지막에 도입구를 접합한다. 이러한 식으로, 래미네이트형 이차 전지(500)를 제작할 수 있다.
양극(503)에 앞의 실시형태에서 설명한 양극 활물질 입자와 LiBOB를 사용함으로써, 열화가 적고, 안전성이 높은 이차 전지(500)로 할 수 있다.
다음으로, 이차 전지를 제작한 후의 에이징에 대하여 설명한다. 이차 전지를 제작한 후에 에이징을 수행하는 것이 바람직하다. 에이징의 조건의 일례에 대하여 이하에서 설명한다. 먼저 0.001C 이상 0.2C 이하의 레이트로 충전을 수행한다. 온도는 예를 들어 실온 이상, 60℃ 이하로 하면 좋다. 여기서, 양극이나 음극의 반응 전위가 전해액(508)의 전위창의 범위를 초과하는 경우에는 이차 전지의 충방전에 의하여 전해액이 분해되는 경우가 있다. 전해액이 분해되어 가스가 발생한 경우, 그 가스가 셀 내에 축적되면 전해액이 전극 표면과 접할 수 없는 영역이 발생한다. 즉 전극의 실효적인 반응 면적이 축소되고, 실효적인 저항이 높아진다.
또한 저항이 지나치게 높아지면, 음극 전위가 감소되어 흑연에 대한 리튬의 삽입이 일어남과 동시에, 흑연 표면에 대한 리튬의 석출도 일어난다. 이 리튬의 석출은 용량의 저하를 초래하는 경우가 있다. 예를 들어 리튬이 석출된 후에 표면에 피막 등이 성장되면, 표면에 석출된 리튬을 다시 용출할 수 없어, 용량에 기여하지 않는 리튬이 증가된다. 또한 석출된 리튬이 물리적으로 붕락되어, 전극과의 도통을 잃은 경우에도, 역시나 용량에 기여하지 않는 리튬이 발생한다. 따라서 음극 전극의 전위가 충전 전압의 상승에 의하여 리튬 전위까지 도달하기 전에 가스를 빼는 것이 바람직하다.
또한 가스 빼기를 한 후에 실온보다 높은 온도, 바람직하게는 30℃ 이상 60℃ 이하, 더 바람직하게는 35℃ 이상 50℃ 이하에서, 예를 들어 1시간 이상 100시간 이하 충전 상태를 유지하여도 좋다. 처음에 수행하는 충전 시에, 표면에서 분해된 전해액은 흑연의 표면에 피막을 형성한다. 따라서 예를 들어 가스 빼기를 한 후에 실온보다 높은 온도로 유지함으로써, 형성된 피막이 치밀해지는 경우도 생각된다.
또한 가스 빼기를 한 후에 불필요한 전해액을 제거하는 경우도 있다. 다만 미량이기 때문에 전지의 중량 변화 등에는 거의 영향을 주지 않는 것으로 간주한다.
래미네이트형 이차 전지의 예에 대하여 도 6의 (A) 및 (B)를 참조하여 설명한다.
도 6의 (A)에 래미네이트형 이차 전지(500)의 외관도의 일례를 나타내었다. 또한 도 6의 (B)에 래미네이트형 이차 전지(500)의 외관도의 다른 일례를 나타내었다.
도 6의 (A) 및 (B)에서는 양극(503), 음극(506), 세퍼레이터(507), 외장체(509), 양극 리드 전극(510), 및 음극 리드 전극(511)이 포함된다.
래미네이트형 이차 전지(500)는 직사각형의 복수의 양극(503), 세퍼레이터(507), 및 직사각형의 복수의 음극(506)을 가진다.
도 5에서는 적층의 예를 나타내었지만 권회체를 사용하는 경우도 있다. 이 경우에는 세퍼레이터(507)를 사이에 두고 음극(506)과 양극(503)이 중첩되어 적층되고, 상기 적층 시트를 권회한다.
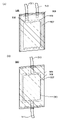
도 7의 (A)에 형상이 L자상의 양극 집전체(701) 및 양극 활물질층(702)을 가지는 양극을 나타내었다. 또한 양극은 양극 집전체(701)가 일부 노출된 영역(이하 탭 영역이라고 함)을 가진다. 또한 도 7의 (B)에 형상이 L자상의 음극 집전체(704) 및 음극 활물질층(705)을 가지는 음극을 나타내었다. 음극은 음극 집전체(704)가 일부 노출된 영역, 즉 탭 영역을 가진다.
도 7의 (C)는 양극(703)을 4층, 음극(706)을 4층 각각 적층시킨 경우의 사시도이다. 또한 도 7의 (C)에서는, 간략화를 위하여, 양극(703)과 음극(706) 사이에 제공되는 세퍼레이터는 점선으로 도시하였다.
도 8의 (A)에 나타낸 래미네이트형 이차 전지는 L자상의 양극 집전체(701) 및 양극 활물질층(702)을 가지는 양극(703)과, L자상의 음극 집전체(704) 및 음극 활물질층(705)을 가지는 음극(706)과, 세퍼레이터(707)와, 전해액(708)과, 외장체(709)를 가진다. 외장체(709) 내부에 제공된 양극(703)과 음극(706) 사이에 세퍼레이터(707)가 설치되어 있다. 또한 외장체(709) 내부는 전해액(708)으로 채워져 있다.
도 8의 (A)에 나타낸 래미네이트형 이차 전지에서, 양극 집전체(701) 및 음극 집전체(704)는, 외부와 전기적으로 접촉되는 단자로서의 역할도 겸한다. 그러므로 양극 집전체(701) 및 음극 집전체(704)의 일부는, 외장체(709)로부터 외측으로 노출되도록 배치되어도 좋다. 또한 양극 집전체(701) 및 음극 집전체(704)를 외장체(709)로부터 외측으로 노출시키지 않고, 리드 전극을 사용하여 이 리드 전극과 양극 집전체(701) 또는 음극 집전체(704)를 초음파 접합시켜 리드 전극이 외측으로 노출되도록 하여도 좋다.
래미네이트형 이차 전지에서, 외장체(709)로서는 예를 들어 폴리에틸렌, 폴리프로필렌, 폴리카보네이트, 이오노머, 폴리아마이드 등의 재료로 이루어지는 막 위에 알루미늄, 스테인리스, 구리, 니켈 등의 가요성이 뛰어난 금속 박막을 제공하고, 이 금속 박막 위에 외장체의 외면으로서 폴리아마이드계 수지, 폴리에스터계 수지 등의 절연성 합성 수지막을 제공한 3층 구조의 래미네이트 필름을 사용할 수 있다.
또한 래미네이트형 이차 전지의 단면 구조의 일례를 도 8의 (B)에 나타내었다. 도 8의 (A)에서는 간략화를 위하여 생략하였지만, 실제로는 복수의 전극층으로 구성된다.
도 8의 (B)에서는, 일례로서, 전극층의 개수를 16개로 하였다. 도 8의 (B)에서는 음극 집전체(704) 8층과 양극 집전체(701) 8층의 총 16층의 구조를 나타내었다. 또한 도 8의 (B)는 도 8의 (A)의 쇄선을 따른 양극 추출부의 단면을 나타낸 것이고, 8층의 음극 집전체(704)가 초음파 접합되어 있다. 물론, 전극층의 개수는 16개에 한정되지 않으며, 많아도 좋고 적어도 좋다. 전극층의 개수가 많은 경우에는 더 용량이 큰 이차 전지로 할 수 있다. 또한 전극층의 개수가 적은 경우에는 박형화할 수 있다.
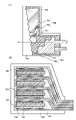
또한 원통형 이차 전지의 예에 대하여 도 9의 (A) 내지 (D)를 참조하여 설명한다. 도 9의 (A)에 나타낸 바와 같이, 원통형 이차 전지(600)는 상면에 양극캡(전지 뚜껑)(601)을 가지고, 측면 및 밑면에 전지 캔(외장 캔)(602)을 가진다. 이들 양극캡과 전지 캔(외장 캔)(602)은 개스킷(절연 패킹)(610)에 의하여 절연된다.
도 9의 (B)는 원통형 이차 전지의 단면을 모식적으로 나타낸 도면이다. 중공 원통형 전지 캔(602)의 안쪽에는, 세퍼레이터(605)를 사이에 두고 띠 형상의 양극(604)과 음극(606)이 권회된 전지 소자가 제공되어 있다. 도시하지 않았지만, 전지 소자는 센터 핀을 중심으로 하여 권회되어 있다. 전지 캔(602)은 한끝이 닫혀 있고, 다른 한끝이 열려 있다. 전지 캔(602)에는 전해액에 대하여 내식성이 있는 니켈, 알루미늄, 타이타늄 등의 금속, 또는 이들의 합금이나, 이들과 다른 금속의 합금(예를 들어 스테인리스강 등)을 사용할 수 있다. 또한 전해액으로 인한 부식을 방지하기 위하여 니켈이나 알루미늄 등으로 피복하는 것이 바람직하다. 전지 캔(602)의 안쪽에서 양극, 음극, 및 세퍼레이터가 권회된 전지 소자는 대향하는 한 쌍의 절연판(608, 609) 사이에 끼워진다. 또한 전지 소자가 제공된 전지 캔(602)의 내부에는 비수전해액(미도시)이 주입되어 있다. 비수전해액으로서는 코인형 이차 전지와 같은 것을 사용할 수 있다.
원통형 축전지에 사용되는 양극 및 음극은 권회되기 때문에, 집전체의 양면에 활물질을 형성하는 것이 바람직하다. 양극(604)에는 양극 단자(양극 집전 리드)(603)가 접속되고, 음극(606)에는 음극 단자(음극 집전 리드)(607)가 접속된다. 양극 단자(603) 및 음극 단자(607)에는 각각 알루미늄 등의 금속 재료를 사용할 수 있다. 양극 단자(603)는 안전 밸브 기구(612)에, 음극 단자(607)는 전지 캔(602)의 바닥에 각각 저항 용접된다. 안전 밸브 기구(612)는 PTC(Positive Temperature Coefficient) 소자(611)를 통하여 양극캡(601)과 전기적으로 접속되어 있다. 안전 밸브 기구(612)는 전지의 내압 상승이 소정의 문턱값을 초과한 경우에, 양극캡(601)과 양극(604) 사이의 전기적인 접속을 절단하는 것이다. 또한 PTC 소자(611)는 온도가 상승한 경우에 저항이 증대되는 열감 저항 소자이며, 저항의 증대에 의하여 전류량을 제한하여 이상 발열을 방지하는 것이다. PTC 소자에는 타이타늄산 바륨(BaTiO3)계 반도체 세라믹 등을 사용할 수 있다.
또한 도 9의 (C)와 같이, 복수의 이차 전지(600)를 도전판(613)과 도전판(614) 사이에 끼워 모듈(615)을 구성하여도 좋다. 복수의 이차 전지(600)는 병렬로 접속되어도 좋고, 직렬로 접속되어도 좋고, 병렬로 접속된 후 직렬로 접속되어도 좋다. 복수의 이차 전지(600)를 가지는 모듈(615)을 구성함으로써, 큰 전력을 추출할 수 있다.
도 9의 (D)는 모듈(615)의 상면도이다. 도면을 명료화하기 위하여 도전판(613)을 점선으로 나타내었다. 도 9의 (D)에 나타낸 바와 같이 모듈(615)은 복수의 이차 전지(600)를 전기적으로 접속하는 도선(導線)(616)을 가져도 좋다. 도선(616) 위에 도전판을 중첩하여 제공할 수 있다. 또한 복수의 이차 전지(600) 사이에 온도 제어 장치(617)를 가져도 좋다. 이차 전지(600)가 과열되었을 때에는 온도 제어 장치(617)에 의하여 냉각하고, 이차 전지(600)가 지나치게 냉각되었을 때에는 온도 제어 장치(617)에 의하여 가열할 수 있다. 그러므로 모듈(615)의 성능이 외기 온도의 영향을 받기 어려워진다.
양극(604)에 앞의 실시형태에서 설명한 형성 방법에 의하여 형성된 양극 활물질을 사용함으로써, 열화가 적고, 안전성이 높은 원통형 이차 전지(600)로 할 수 있다.
(실시형태 3)
[양극 활물질의 구조]
코발트산 리튬(LiCoO2) 등, 층상 암염형 결정 구조를 가지는 재료는 방전 용량이 높아, 이차 전지의 양극 활물질로서 우수하다는 것이 알려져 있다. 층상 암염형 결정 구조를 가지는 재료로서 예를 들어, LiMO2로 나타내어지는 복합 산화물이 있다. 원소 M의 일례로서 Co, Ni, Mn 중에서 선택되는 하나 이상을 들 수 있다. 또한 원소 M의 일례로서 Co, Ni, Mn 중에서 선택되는 하나 이상에 더하여, Al 및 Mg 중에서 선택되는 하나 이상을 들 수 있다.
전이 금속 화합물에서의 얀-텔러 효과는 전이 금속의 d-오비탈의 전자수에 따라, 그 효과의 크기가 다른 것이 알려져 있다.
니켈을 가지는 화합물에서는 얀-텔러 효과로 인하여 변형이 발생하기 쉬운 경우가 있다. 따라서 LiNiO2에서, 고전압으로의 충방전을 수행한 경우, 변형에 기인하는 결정 구조의 붕괴가 발생할 우려가 있다. LiCoO2에서는, 얀-텔러 효과의 영향이 작은 것이 시사되므로 고전압으로의 충방전에 대한 내성이 더 우수한 경우가 있어 바람직하다.
도 10 및 도 11을 사용하여 양극 활물질에 대하여 설명한다. 도 10 및 도 11에서는 양극 활물질이 가지는 전이 금속으로서 코발트를 사용하는 경우에 대하여 설명한다.
<종래의 양극 활물질>
도 11에 나타낸 양극 활물질은 할로젠 및 마그네슘이 첨가되지 않는 코발트산 리튬(LiCoO2)이다. 도 11에 나타낸 코발트산 리튬은 충전 심도에 따라 결정 구조가 변화된다.
도 11에 나타낸 바와 같이, 충전 심도가 0(방전 상태)인 코발트산 리튬은 공간군 R-3m의 결정 구조를 가지는 영역을 가지고, 리튬이 팔면체(Octahedral) 자리를 점유하고, 단위 격자 중에 CoO2층이 3층 존재한다. 그러므로 이 결정 구조를 O3형 결정 구조라고 하는 경우가 있다. 또한 CoO2층이란 코발트에 산소가 6배위한 팔면체 구조가 모서리 공유 상태로 평면에서 연속한 구조를 말한다.
또한 충전 심도가 1일 때는 공간군 P-3m1의 결정 구조를 가지고, 단위 격자 중에 CoO2층이 1층 존재한다. 그러므로 이 결정 구조를 O1형 결정 구조라고 하는 경우가 있다.
또한 충전 심도가 0.8 정도일 때의 코발트산 리튬은 공간군 R-3m의 결정 구조를 가진다. 이 구조는, P-3m1(O1)과 같은 CoO2 구조와 R-3m(O3)과 같은 LiCoO2 구조가 번갈아 적층된 구조라고도 할 수 있다. 그러므로 이 결정 구조를 H1-3형 결정 구조라고 하는 경우가 있다. 또한 실제로는 H1-3형 결정 구조는 단위 격자당 코발트 원자의 수가 다른 구조의 2배이다. 다만 도 11을 비롯하여 본 명세서에서는 다른 구조와 비교하기 쉽게 하기 위하여 H1-3형 결정 구조의 c축을 단위 격자의 2분의 1로 한 도면으로 나타내었다.
H1-3형 결정 구조는 일례로서, 단위 격자에서의 코발트와 산소의 좌표를 Co(0, 0, 0.42150±0.00016), O1(0, 0, 0.27671±0.00045), O2(0, 0, 0.11535±0.00045)로 나타낼 수 있다. O1 및 O2는 각각 산소 원자이다. 이와 같이, H1-3형 결정 구조는 1개의 코발트 및 2개의 산소를 사용한 단위 격자로 나타내어진다. 한편 후술하는 바와 같이, 본 발명의 일 형태의 O3'형 결정 구조는 바람직하게는 1개의 코발트 및 1개의 산소를 사용한 단위 격자로 나타내어진다. 이는 O3'형 결정 구조의 경우와 H1-3형 구조의 경우에서, 코발트와 산소의 대칭성이 다르고, O3'형 결정 구조가 H1-3형 구조에 비하여 O3 구조로부터의 변화가 더 작은 것을 시사한다. 양극 활물질이 가지는 결정 구조를 나타내는 단위 격자를 선택하는 데에 있어, 예를 들어 XRD 패턴의 릿펠트 해석(Rietveld analysis)에서 GOF의 값이 보다 작아지는 것을 사용하는 것이 더 바람직하다.
리튬 금속의 산화 환원 전위를 기준으로 충전 전압이 4.6V 이상이 될 정도로 높은 전압으로의 충전, 또는 충전 심도가 0.8 이상이 될 정도로 깊은 심도의 충전과 방전을 반복하면, 코발트산 리튬은 H1-3형 결정 구조와 방전 상태의 R-3m(O3)의 구조 사이에서 결정 구조의 변화(즉 비평형(非平衡)적인 상(相)변화)를 반복하게 된다.
하지만 이 2개의 결정 구조들에는 CoO2층의 위치에 큰 차이가 있다. 도 11에서 점선 및 화살표로 나타낸 바와 같이, H1-3형 결정 구조에서는 CoO2층이 R-3m(O3)에서 크게 어긋나 있다. 이러한 큰 구조 변화는 결정 구조의 안정성에 악영향을 미칠 수 있다.
게다가 체적의 차이도 크다. 동수의 코발트 원자당으로 비교하였을 때, H1-3형 결정 구조와 방전 상태의 O3형 결정 구조의 체적의 차이는 3.0% 이상이다.
또한 H1-3형 결정 구조가 가지는, P-3m1(O1) 등 CoO2층이 연속한 구조는 불안정적일 가능성이 높다.
따라서 고전압으로의 충방전을 반복하면 코발트산 리튬의 결정 구조는 붕괴된다. 결정 구조의 붕괴가 사이클 특성의 악화를 일으킨다. 이는, 결정 구조가 붕괴됨으로써 리튬이 안정적으로 존재할 수 있는 자리가 감소하고, 또한 리튬의 삽입·탈리가 어려워지기 때문이라고 생각된다.
<본 발명의 일 형태의 양극 활물질>
<<내부>>
본 발명의 일 형태에서 제작되는 양극 활물질(904)은 고전압으로의 충방전의 반복에 있어서, CoO2층의 위치에 차이가 나는 것을 저감할 수 있다. 또한 체적의 변화를 작게 할 수 있다. 따라서 상기 화합물은 우수한 사이클 특성을 실현할 수 있다. 또한 상기 화합물은 고전압의 충전 상태에서 안정적인 결정 구조를 가질 수 있다. 따라서 상기 화합물은 고전압의 충전 상태를 유지한 경우에 있어서, 단락이 발생되기 어려운 경우가 있다. 이러한 경우에는 안전성이 더 향상되기 때문에 바람직하다.
본 발명의 일 형태의 양극 활물질에서는, 충분히 방전된 상태와 고전압으로 충전된 상태에서, 결정 구조의 변화 및 동수의 전이 금속 원자당으로 비교한 경우의 체적의 차이가 작다.
본 발명의 일 형태의 양극 활물질(904)의 충방전 전후의 결정 구조를 도 10에 나타내었다. 양극 활물질(904)은 리튬과, 전이 금속으로서 코발트와, 산소를 가지는 복합 산화물이다. 상기에 더하여 첨가 원소로서 마그네슘을 가지는 것이 바람직하다. 또한 첨가 원소로서 플루오린, 염소 등의 할로젠을 가지는 것이 바람직하다.
도 10의 충전 심도 0(방전 상태)의 결정 구조는 도 11과 같은 R-3m(O3)이다. 한편 양극 활물질(904)은 충분히 충전된 충전 심도의 경우, H1-3형 결정 구조와는 다른 구조의 결정을 가진다. 본 구조는 공간군 R-3m이고, 스피넬형 결정 구조가 아니지만, 코발트, 마그네슘 등의 이온이 산소 6배위 위치를 차지하고, 양이온의 배열이 스피넬형과 비슷한 대칭성을 가진다. 또한 본 구조의 CoO2층의 대칭성은 O3형과 같다. 따라서 본 명세서 등에서는 본 구조를 O3'형 결정 구조 또는 의사 스피넬형 결정 구조라고 호칭한다. 따라서 O3'형 결정 구조를 의사 스피넬형 결정 구조로 바꿔 말하여도 좋다. 또한 도 10에 나타낸 O3'형 결정 구조의 도면에서는 코발트 원자의 대칭성과 산소 원자의 대칭성을 설명하기 위하여 리튬의 표시를 생략하였지만, 실제로는 CoO2층들 간에, 코발트에 대하여 예를 들어 20atomic% 이하의 리튬이 존재한다. 또한 O3형 결정 구조 및 O3'형 결정 구조는 둘 다, CoO2층들 간, 즉 리튬 자리에 마그네슘이 희박하게 존재하는 것이 바람직하다. 또한 산소 자리에 플루오린 등의 할로젠이 랜덤하며 희박하게 존재하는 것이 바람직하다.
또한 O3'형 결정 구조에서는, 리튬 등의 경원소는 산소 4배위 위치를 차지하는 경우가 있고, 이러한 경우도 이온의 배열이 스피넬형과 비슷한 대칭성을 가진다.
또한 O3'형 결정 구조는 층간에 랜덤하게 Li을 가지지만 CdCl2형 결정 구조와 유사한 결정 구조라고도 할 수 있다. 이 CdCl2형과 유사한 결정 구조는 니켈산 리튬을 충전 심도 0.94까지 충전하였을 때(Li0.06NiO2)의 결정 구조와 가깝지만, 순수한 코발트산 리튬, 또는 코발트를 많이 포함하는 층상 암염형 양극 활물질은 일반적으로 이러한 결정 구조를 취하지 않는 것으로 알려져 있다.
본 발명의 일 형태의 양극 활물질(904)에서는, 고전압으로 충전되어 대량의 리튬이 탈리되었을 때의 결정 구조의 변화가 종래의 양극 활물질보다 억제된다. 예를 들어 도 10에서 점선으로 나타낸 바와 같이, 이 결정 구조들 사이에서는 CoO2층의 위치의 차이가 거의 없다.
보다 자세하게 설명하면, 본 발명의 일 형태의 양극 활물질(904)은 충전 전압이 높은 경우에도 구조의 안정성이 높다. 예를 들어 종래의 양극 활물질에서는 리튬 금속의 전위를 기준으로 4.6V 정도의 충전 전압에서는 H1-3형 결정 구조가 되지만, 본 발명의 일 형태의 양극 활물질(904)에서는 상기 4.6V 정도의 충전 전압에서도 R-3m(O3)의 결정 구조를 유지할 수 있다. 더 높은 충전 전압, 예를 들어 리튬 금속의 전위를 기준으로 4.65V 내지 4.7V 정도의 전압에서도 본 발명의 일 형태의 양극 활물질(904)에서는 O3'형 결정 구조를 취할 수 있다. 충전 전압을 4.7V보다 더 높이면 본 발명의 일 형태의 양극 활물질(904)에서 겨우 H1-3형 결정이 관측되는 경우가 있다. 또한 충전 전압이 더 낮은 경우, 예를 들어 충전 전압이 리튬 금속의 전위를 기준으로 4.5V 이상 4.6V 미만에서도 본 발명의 일 형태의 양극 활물질(904)에서는 O3'형 결정 구조를 취할 수 있는 경우가 있다.
또한 이차 전지에서 예를 들어 음극 활물질로서 흑연을 사용하는 경우에는 상기보다 흑연의 전위만큼 이차 전지의 전압이 저하된다. 흑연의 전위는 리튬 금속의 전위를 기준으로 0.05V 내지 0.2V 정도이다. 그러므로 예를 들어 음극 활물질에 흑연을 사용한 이차 전지의 전압이 4.3V 이상 4.5V 이하에서도 본 발명의 일 형태의 양극 활물질(904)에서는 R-3m(O3)의 결정 구조를 유지할 수 있고, 충전 전압을 더 높인 범위, 예를 들어 이차 전지의 전압이 4.5V 초과 4.6V 이하에서도 O3'형 결정 구조를 취할 수 있다. 또한 충전 전압이 더 낮은 경우, 예를 들어 이차 전지의 전압이 4.2V 이상 4.3V 미만에서도 본 발명의 일 형태의 양극 활물질(904)에서는 O3'형 결정 구조를 취할 수 있는 경우가 있다.
그러므로 본 발명의 일 형태의 양극 활물질(904)에서는 고전압으로 충방전을 반복하여도 결정 구조가 붕괴되기 어렵다.
또한 양극 활물질(904)에서, 충전 심도 0의 O3형 결정 구조와 충전 심도 0.8의 O3'형 결정 구조의 단위 격자당 체적의 차이는 2.5% 이하, 더 자세하게는 2.2% 이하이다.
또한 O3'형 결정 구조는 단위 격자에서의 코발트와 산소의 좌표를 Co(0, 0, 0.5), O(0, 0, x), 0.20≤x≤0.25의 범위 내로 나타낼 수 있다.
CoO2층들 간, 즉 리튬 자리에 랜덤하며 희박하게 존재하는 첨가 원소, 예를 들어 마그네슘에는 CoO2층의 위치에 차이가 나는 것을 저감할 수 있는 효과가 있다. 따라서 CoO2층들 간에 마그네슘이 존재하면 O3'형 결정 구조가 되기 쉬워진다. 그러므로 마그네슘은 본 발명의 일 형태의 양극 활물질(904)의 입자 전체에 분포되는 것이 바람직하다. 또한 입자 전체에 마그네슘을 분포시키기 위하여 본 발명의 일 형태의 양극 활물질(904)의 제작 공정에서 가열 처리를 수행하는 것이 바람직하다.
그러나 가열 처리의 온도가 지나치게 높으면 양이온 혼합(cation mixing)이 일어나 첨가 원소, 예를 들어 마그네슘이 코발트 자리에 들어갈 가능성이 높아진다. 코발트 자리에 존재하는 마그네슘에는 고전압으로의 충전 시에 R-3m의 구조를 유지하는 효과가 없다. 또한 가열 처리의 온도가 지나치게 높으면 코발트가 환원되어 2가가 되거나, 리튬이 증발된다는 등의 악영향도 우려된다.
그래서 입자 전체에 마그네슘을 분포시키기 위한 가열 처리 전에, 플루오린 화합물 등의 할로젠 화합물을 코발트산 리튬에 첨가하는 것이 바람직하다. 할로젠 화합물을 첨가함으로써 코발트산 리튬의 융점 강하가 일어난다. 융점 강하시킴으로써 양이온 혼합이 일어나기 어려운 온도에서 입자 전체에 마그네슘을 분포시키는 것이 용이해진다. 또한 플루오린 화합물이 존재하면, 전해액이 분해되어 생긴 플루오린화 수소산에 대한 내식성이 향상되는 것을 기대할 수 있다.
또한 마그네슘 농도를 원하는 값 이상으로 높게 하면, 결정 구조의 안정화에 대한 효과가 작게 되는 경우가 있다. 마그네슘이 리튬 자리뿐만 아니라, 코발트 자리에도 들어가게 되기 때문이라고 생각된다. 본 발명의 일 형태의 양극 활물질이 가지는 마그네슘의 원자수는 전이 금속의 원자수의 0.001배 이상 0.1배 이하가 바람직하고, 0.01배보다 크고 0.04배 미만이 더 바람직하고, 0.02배 정도가 더욱 바람직하다. 여기서 제시한 마그네슘의 농도는 예를 들어, ICP-MS 등을 이용하여 양극 활물질의 입자 전체를 원소 분석하여 얻어진 값이어도 좋고, 양극 활물질의 제작 과정에서의 원료의 배합의 값에 기초하여도 좋다.
코발트산 리튬에 코발트 이외의 금속(첨가 원소)으로서 예를 들어 니켈, 알루미늄, 망가니즈, 타이타늄, 바나듐, 및 크로뮴 중에서 선택되는 하나 이상의 금속을 첨가하여도 좋고, 특히 니켈 및 알루미늄 중 하나 이상을 첨가하는 것이 바람직하다. 망가니즈, 타이타늄, 바나듐, 및 크로뮴은 안정적으로 4가를 취하기 쉬운 경우가 있어, 구조 안정화에 크게 기여하는 경우가 있다. 첨가 원소를 첨가함으로써 본 발명의 일 형태의 양극 활물질에서는 예를 들어, 고전압으로의 충전 상태에서 결정 구조가 더 안정되는 경우가 있다. 여기서 본 발명의 일 형태의 양극 활물질에 있어서, 첨가 원소는 코발트산 리튬의 결정성을 크게 바꾸지 않는 농도로 첨가되는 것이 바람직하다. 예를 들어 상술한 얀-텔러 효과 등이 발현되지 않을 정도의 양인 것이 바람직하다.
도 10 중의 범례로 나타낸 바와 같이, 니켈, 망가니즈를 비롯한 전이 금속 및 알루미늄은 코발트 자리에 존재하는 것이 바람직하지만, 일부가 리튬 자리에 존재하여도 좋다. 또한 마그네슘은 리튬 자리에 존재하는 것이 바람직하다. 산소는 일부가 플루오린과 치환되어 있어도 좋다.
본 발명의 일 형태의 양극 활물질의 마그네슘 농도가 높아질수록 양극 활물질의 용량이 감소되는 경우가 있다. 그 요인으로서 예를 들어, 리튬 자리에 마그네슘이 들어감으로써 충방전에 기여하는 리튬량이 감소된다는 가능성이 생각된다. 또한 과잉의 마그네슘이 충방전에 기여하지 않는 마그네슘 화합물을 생성하는 경우도 있다. 본 발명의 일 형태의 양극 활물질이 마그네슘에 더하여 첨가 원소로서 니켈을 가짐으로써, 중량당 및 체적당 용량을 높일 수 있는 경우가 있다. 또한 본 발명의 일 형태의 양극 활물질이 마그네슘에 더하여 첨가 원소로서 알루미늄을 가짐으로써, 중량당 및 체적당 용량을 높일 수 있는 경우가 있다. 또한 본 발명의 일 형태의 양극 활물질이 마그네슘에 더하여 니켈 및 알루미늄을 가짐으로써, 중량당 및 체적당 용량을 높일 수 있는 경우가 있다.
이하에서 본 발명의 일 형태의 양극 활물질이 가지는 마그네슘 등의 원소의 농도를 원자수를 사용하여 나타낸다.
본 발명의 일 형태의 양극 활물질이 가지는 니켈의 원자수는 코발트의 원자수의 10% 이하가 바람직하고, 7.5% 이하가 더 바람직하고, 0.05% 이상 4% 이하가 더욱 바람직하고, 0.1% 이상 2% 이하가 특히 바람직하다. 여기서 제시한 니켈의 농도는 예를 들어, ICP-MS 등을 이용하여 양극 활물질의 입자 전체를 원소 분석하여 얻어진 값이어도 좋고, 양극 활물질의 제작 과정에서의 원료의 배합의 값에 기초하여도 좋다.
고전압으로 충전된 상태를 장시간 유지하면, 양극 활물질로부터 전이 금속이 전해액에 용출되어 결정 구조가 붕괴될 우려가 생긴다. 그러나 상기 비율로 니켈을 가짐으로써, 양극 활물질(904)로부터의 전이 금속의 용출을 억제할 수 있는 경우가 있다.
본 발명의 일 형태의 양극 활물질이 가지는 알루미늄의 원자수는 코발트의 원자수의 0.05% 이상 4% 이하가 바람직하고, 0.1% 이상 2% 이하가 더 바람직하다. 여기서 제시한 알루미늄의 농도는 예를 들어, ICP-MS 등을 이용하여 양극 활물질의 입자 전체를 원소 분석하여 얻어진 값이어도 좋고, 양극 활물질의 제작 과정에서의 원료의 배합의 값에 기초하여도 좋다.
본 발명의 일 형태의 양극 활물질은 첨가 원소 X를 가지는 것이 바람직하고, 첨가 원소 X로서 인을 사용하는 것이 바람직하다. 또한 본 발명의 일 형태의 양극 활물질은 인과 산소를 포함하는 화합물을 가지는 것이 더 바람직하다.
본 발명의 일 형태의 양극 활물질이 첨가 원소 X를 포함하는 화합물을 가짐으로써 고전압의 충전 상태를 유지한 경우에서, 단락이 발생되기 어려운 경우가 있다.
본 발명의 일 형태의 양극 활물질이 첨가 원소 X로서 인을 가지는 경우에는 전해액의 분해에 의하여 발생한 플루오린화 수소와 인이 반응하여 전해액 중의 플루오린화 수소 농도가 저하될 가능성이 있다.
전해액이 LiPF6을 가지는 경우, 가수 분해에 의하여 플루오린화 수소가 발생하는 경우가 있다. 또한 양극의 구성요소로서 사용되는 PVDF와 알칼리의 반응에 의하여 플루오린화 수소가 발생하는 경우도 있다. 전해액 중의 플루오린화 수소 농도가 저하됨으로써 집전체의 부식 및/또는 피막의 벗겨짐을 억제할 수 있는 경우가 있다. 또한 PVDF의 겔화 및/또는 불용화로 인한 접착성의 저하를 억제할 수 있는 경우가 있다.
본 발명의 일 형태의 양극 활물질이 첨가 원소 X에 더하여 마그네슘을 가지는 경우, 고전압의 충전 상태에서의 안정성이 매우 높다. 첨가 원소 X가 인인 경우, 인의 원자수는 코발트의 원자수의 1% 이상 20% 이하가 바람직하고, 2% 이상 10% 이하가 더 바람직하고, 3% 이상 8% 이하가 더욱 바람직하고, 또한 마그네슘의 원자수는 코발트의 원자수의 0.1% 이상 10% 이하가 바람직하고, 0.5% 이상 5% 이하가 더 바람직하고, 0.7% 이상 4% 이하가 더욱 바람직하다. 여기서 제시한 인 및 마그네슘의 농도는 예를 들어, ICP-MS 등을 이용하여 양극 활물질의 입자 전체를 원소 분석하여 얻어진 값이어도 좋고, 양극 활물질의 제작 과정에서의 원료의 배합의 값에 기초하여도 좋다.
양극 활물질이 크랙을 가지는 경우, 그 내부에 인, 더 구체적으로는 예를 들어 인과 산소를 포함하는 화합물이 존재함으로써 크랙의 진행이 억제되는 경우가 있다.
또한 도 10에서 화살표로 나타낸 산소 원자에서 알 수 있듯이, O3형 결정 구조와 O3'형 결정 구조에서는 산소 원자의 대칭성이 미묘하게 다르다. 구체적으로는 O3형 결정 구조에서는 산소 원자가 점선으로 나타낸 (-1 0 2)면을 따라 정렬되고, 한편 O3'형 결정 구조의 산소 원자는 엄밀하게는 (-1 0 2)면을 따라 정렬되지 않는다. 이는, O3'형 결정 구조에서는 리튬의 감소에 따라 4가의 코발트가 증가되고 얀-텔러의 왜곡이 크게 되어 CoO6의 팔면체 구조가 변형된 것에 기인한다. 또한 리튬의 감소에 따라 CoO2층의 산소끼리의 반발이 강해진 것도 영향을 준다.
마그네슘은 본 발명의 일 형태의 양극 활물질(904)의 입자 전체에 분포되는 것이 바람직하고, 이에 더하여 표층부의 마그네슘 농도가 입자 전체의 평균보다 높은 것이 바람직하다. 예를 들어 XPS 등으로 측정되는 표층부의 마그네슘 농도가 ICP-MS 등으로 측정되는 입자 전체의 평균의 마그네슘 농도보다 높은 것이 바람직하다.
또한 본 발명의 일 형태의 양극 활물질(904)이 코발트 이외의 원소, 예를 들어 니켈, 알루미늄, 망가니즈, 철, 및 크로뮴 중에서 선택되는 하나 이상의 금속을 가지는 경우에 있어서, 상기 금속의 입자 표층부에서의 농도가 입자 전체의 평균보다 높은 것이 바람직하다. 예를 들어 XPS 등으로 측정되는 표층부의 코발트 이외의 원소의 농도가 ICP-MS 등으로 측정되는 입자 전체의 평균의 상기 원소의 농도보다 높은 것이 바람직하다.
입자 표면은 이를테면 전부가 결정 결함이며, 게다가 충전 시에는 표면에서 리튬이 빠져나가기 때문에 내부보다 리튬 농도가 낮아지기 쉬운 부분이다. 그러므로 불안정해지기 쉬워 결정 구조가 붕괴되기 쉬운 부분이다. 표층부의 마그네슘 농도가 높으면 결정 구조의 변화를 더 효과적으로 억제할 수 있다. 또한 표층부의 마그네슘 농도가 높으면, 전해액이 분해되어 생긴 플루오린화 수소산에 대한 내식성이 향상되는 것도 기대할 수 있다.
또한 플루오린 등의 할로젠도 본 발명의 일 형태의 양극 활물질(904)의 표층부에서의 농도가 입자 전체의 평균보다 높은 것이 바람직하다. 전해액에 접한 영역인 표층부에 할로젠이 존재함으로써, 플루오린화 수소산에 대한 내식성을 효과적으로 향상시킬 수 있다.
상술한 바와 같이 본 발명의 일 형태의 양극 활물질(904)의 표층부는 내부보다 첨가 원소, 예를 들어 마그네슘 및 플루오린의 농도가 높은, 내부와 다른 조성인 것이 바람직하다. 또한 그 조성으로서 상온에서 안정적인 결정 구조를 가지는 것이 바람직하다. 따라서 표층부는 내부와 다른 결정 구조를 가져도 좋다. 예를 들어 본 발명의 일 형태의 양극 활물질(904)의 표층부 중 적어도 일부가 암염형 결정 구조를 가져도 좋다. 또한 표층부와 내부가 다른 결정 구조를 가지는 경우, 표층부와 내부의 결정 배향이 실질적으로 일치하는 것이 바람직하다.
층상 암염형 결정 및 암염형 결정의 음이온은 입방 최조밀 쌓임 구조(면심 입방 격자 구조)를 취한다. O3'형 결정도 음이온은 입방 최조밀 쌓임 구조를 취한다고 추정된다. 이들이 접할 때 음이온으로 구성되는 입방 최조밀 쌓임 구조의 방향이 일치하는 결정면이 존재한다. 다만 층상 암염형 결정 및 O3'형 결정의 공간군은 R-3m이고, 암염형 결정의 공간군 Fm-3m(일반적인 암염형 결정의 공간군) 및 Fd-3m(가장 단순한 대칭성을 가지는 암염형 결정의 공간군)과는 다르기 때문에, 상기 조건을 만족시키는 결정면의 밀러 지수는 층상 암염형 결정 및 O3'형 결정과, 암염형 결정 사이에서 다르다. 본 명세서에서는 층상 암염형 결정, O3'형 결정, 및 암염형 결정에서, 음이온으로 구성되는 입방 최조밀 쌓임 구조의 방향이 일치하는 상태를, 결정 배향이 실질적으로 일치한다고 하는 경우가 있다.
2개의 영역의 결정 배향이 실질적으로 일치하는지는 TEM(transmission electron microscope) 이미지, STEM(scanning transmission electron microscope) 이미지, HAADF-STEM(high-angle annular dark field scanning transmission electron microscope) 이미지, ABF-STEM(annular bright-field scanning transmission electron microscope) 이미지 등에서 판단할 수 있다. X선 회절(XRD), 전자 회절, 중성자 회절 등도 판단의 재료로 할 수 있다. 결정의 배향이 실질적으로 일치되어 있으면, TEM 이미지 등에서, 양이온과 음이온이 직선으로 번갈아 배열된 열의 방향의 차가 5도 이하, 더 바람직하게는 2.5도 이하인 것을 관찰할 수 있다. 또한 TEM 이미지 등에서 산소, 플루오린을 비롯한 경원소는 명확하게 관찰될 수 없는 경우가 있지만, 이러한 경우에는 금속 원소의 배열에 의하여 배향의 일치를 판단할 수 있다.
다만 표층부가, MgO만을 포함하거나 또는 MgO과 CoO(II)가 고용된 구조만을 가지면 리튬의 삽입·탈리가 어려워진다. 그러므로 표층부는 적어도 코발트를 가지고 방전 상태에서는 리튬도 가져, 리튬의 삽입·탈리 경로를 가질 필요가 있다. 또한 마그네슘보다 코발트의 농도가 높은 것이 바람직하다.
또한 첨가 원소 X는 본 발명의 일 형태의 양극 활물질(904)의 입자의 표층부에 위치하는 것이 바람직하다. 예를 들어 본 발명의 일 형태의 양극 활물질(904)은 첨가 원소 X를 가지는 피막으로 덮여 있어도 좋다.
<<입계>>
본 발명의 일 형태의 양극 활물질(904)이 가지는 첨가 원소 X는 내부에 랜덤하며 희박하게 존재하여도 좋지만, 일부는 입계에 편석되는 것이 더 바람직하다.
바꿔 말하면, 본 발명의 일 형태의 양극 활물질(904)의 입계 및 그 근방의 첨가 원소 X의 농도도 내부의 다른 영역보다 높은 것이 바람직하다.
입자 표면과 마찬가지로 결정립계도 면 결함이다. 그러므로 불안정해지기 쉬워 결정 구조의 변화가 시작되기 쉽다. 그러므로 입계 및 그 근방의 첨가 원소 X의 농도가 높으면 결정 구조의 변화를 더 효과적으로 억제할 수 있다.
또한 입계 및 그 근방의 첨가 원소 X의 농도가 높은 경우, 본 발명의 일 형태의 양극 활물질(904)의 입자의 입계를 따라 크랙이 생긴 경우에도, 크랙에 의하여 생긴 표면 근방에서 첨가 원소 X의 농도가 높아진다. 따라서 크랙이 생긴 후의 양극 활물질도 플루오린화 수소산에 대한 내식성을 높일 수 있다.
또한 본 명세서 등에 있어서, 결정립계의 근방이란 입계로부터 10nm 정도까지의 영역을 말한다.
<입경>
양극 활물질(904)은 입경이 지나치게 크면 리튬의 확산이 어려워지거나 집전체에 코팅된 경우에 활물질층의 표면이 지나치게 거칠어진다는 등의 문제가 있다. 한편, 지나치게 작으면 집전체에 코팅하였을 때 활물질층을 담지(擔持)하기 어렵게 되거나 전해액과의 반응이 과잉으로 진행된다는 등의 문제도 생긴다. 그러므로 평균 입경(D50: 메디안경이라고도 함)이 1μm 이상 100μm 이하인 것이 바람직하고, 2μm 이상 40μm 이하인 것이 더 바람직하고, 5μm 이상 30μm 이하인 것이 더욱 바람직하다.
<분석 방법>
어떤 양극 활물질이 고전압으로 충전되었을 때 O3'형 결정 구조를 나타내는지 여부는, 고전압으로 충전된 양극을 XRD, 전자 회절, 중성자 회절, 전자 스핀 공명(ESR), 핵자기 공명(NMR) 등을 사용하여 해석함으로써 판단할 수 있다. 특히 XRD는, 양극 활물질이 가지는 코발트 등의 전이 금속의 대칭성을 고분해능으로 해석할 수 있거나, 결정성의 정도 및 결정의 배향성을 비교할 수 있거나, 격자의 주기성 변형 및 결정자 크기의 해석이 가능하거나, 이차 전지를 해체하여 얻은 양극을 그대로 측정하여도 충분한 정확도를 얻을 수 있다는 등의 점에서 바람직하다.
본 발명의 일 형태의 양극 활물질(904)은 상술한 바와 같이, 고전압으로 충전된 상태와 방전 상태 사이에서 결정 구조의 변화가 적다는 것이 특징이다. 고전압으로 충전된 상태에서 방전 상태와의 변화가 큰 결정 구조가 50wt% 이상을 차지하는 재료는 고전압으로의 충방전에 견딜 수 없기 때문에 바람직하지 않다. 그리고 첨가 원소를 첨가하는 것만으로는 목적하는 결정 구조를 가지지 않는 경우가 있다는 점에 주의하여야 한다. 예를 들어 마그네슘 및 플루오린을 가지는 코발트산 리튬이라는 점에서 공통적이어도, 고전압으로 충전된 상태에서, O3'형 결정 구조가 60wt% 이상을 차지하는 경우와, H1-3형 결정 구조가 50wt% 이상을 차지하는 경우가 있다. 또한 소정의 전압으로는 O3'형 결정 구조가 거의 100wt%가 되고, 상기 소정의 전압을 더 올리면 H1-3형 결정 구조가 발생하는 경우도 있다. 따라서 본 발명의 일 형태의 양극 활물질(904)인지 여부를 판단하기 위해서는 XRD를 비롯한 결정 구조에 대한 해석이 필요하다.
다만 고전압으로 충전된 상태 또는 방전 상태의 양극 활물질은 대기에 노출되면 결정 구조의 변화를 일으키는 경우가 있다. 예를 들어 O3'형 결정 구조에서 H1-3형 결정 구조로 변화되는 경우가 있다. 따라서 시료는 모두 아르곤 분위기 등의 불활성 분위기에서 취급하는 것이 바람직하다.
(실시형태 4)
본 실시형태에서는 본 발명의 일 형태인 이차 전지를 전자 기기 또는 이동체에 실장하는 예에 대하여 설명한다.
우선 실시형태 3의 일부에서 설명한 이차 전지를 전자 기기에 실장하는 예를 도 12의 (A) 내지 (E)에 나타낸다. 이차 전지를 적용한 전자 기기로서는 예를 들어 텔레비전 장치(텔레비전 또는 텔레비전 수신기라고도 함), 컴퓨터용 등의 모니터, 디지털 카메라, 디지털 비디오 카메라, 디지털 액자, 휴대 전화기(휴대 전화, 휴대 전화 장치라고도 함), 휴대용 게임기, 휴대 정보 단말기, 음향 재생 장치, 파친코기 등의 대형 게임기 등이 있다.
또한 이동체, 대표적으로는 자동차에 이차 전지를 적용할 수 있다. 자동차로서는 하이브리드 자동차(HEV), 전기 자동차(EV), 또는 플러그인 하이브리드 자동차(PHEV) 등의 차세대 클린 에너지 자동차를 들 수 있고, 자동차에 탑재하는 전원의 하나로서 이차 전지를 적용할 수 있다. 이동체는 자동차에 한정되지 않는다. 예를 들어, 이동체로서는 전철, 모노레일, 선박, 비행체(헬리콥터, 무인 항공기(드론), 비행기, 로켓), 전기 자전거, 전동 바이크 등도 들 수 있고, 이들 이동체에 본 발명의 일 형태의 이차 전지를 적용할 수 있다.
또한 주택에 설치된 지상 설치형 충전 장치나, 상업 시설에 설치된 충전 스테이션에 본 실시형태의 이차 전지를 적용하여도 좋다.
도 12의 (A)는 휴대 전화기의 일례를 나타낸 것이다. 휴대 전화기(2100)는 하우징(2101)에 제공된 표시부(2102) 외에도, 조작 버튼(2103), 외부 접속 포트(2104), 스피커(2105), 마이크로폰(2106) 등을 가진다. 또한 휴대 전화기(2100)는 이차 전지(2107)를 가진다.
휴대 전화기(2100)는 이동 전화, 전자 메일, 문장 열람 및 작성, 음악 재생, 인터넷 통신, 컴퓨터 게임 등의 다양한 애플리케이션을 실행할 수 있다.
조작 버튼(2103)은 시각 설정 외에, 전원의 온/오프 동작, 무선 통신의 온/오프 동작, 매너 모드의 실행 및 해제, 전력 절약 모드의 실행 및 해제 등, 다양한 기능을 가질 수 있다. 예를 들어 휴대 전화기(2100)에 제공된 운영 체계에 의하여, 조작 버튼(2103)의 기능을 자유로이 설정할 수도 있다.
또한 휴대 전화기(2100)는 통신 규격에 따른 근거리 무선 통신을 실행할 수 있다. 예를 들어 무선 통신이 가능한 헤드세트와 상호 통신함으로써 핸즈프리로 통화할 수도 있다.
또한 휴대 전화기(2100)는 외부 접속 포트(2104)를 가지고, 커넥터를 통하여 다른 정보 단말기와 직접 데이터를 송수신할 수 있다. 또한 외부 접속 포트(2104)를 통하여 충전을 할 수도 있다. 또한 충전 동작은 외부 접속 포트(2104)를 통하지 않고 무선 급전으로 수행하여도 좋다.
휴대 전화기(2100)는 센서를 가지는 것이 바람직하다. 센서로서는 예를 들어 지문 센서, 맥박 센서, 체온 센서 등의 인체 센서나, 터치 센서, 가압 센서, 가속도 센서 등이 탑재되는 것이 바람직하다.
도 12의 (B)는 복수의 로터(2302)를 가지는 무인 항공기(2300)이다. 무인 항공기(2300)는 드론이라고 불리는 경우도 있다. 무인 항공기(2300)는 본 발명의 일 형태인 이차 전지(2301)와, 카메라(2303)와, 안테나(미도시)를 가진다. 무인 항공기(2300)는 안테나를 통하여 원격 조작할 수 있다. 본 발명의 일 형태의 이차 전지는 안전성이 높기 때문에, 장기간에 걸쳐 장시간 안전하게 사용할 수 있고, 무인 항공기(2300)에 탑재되는 이차 전지로서 적합하다.
또한 도 12의 (C)에 나타낸 바와 같이, 본 발명의 일 형태의 이차 전지(2601)를 복수로 가지는 이차 전지(2602)를 하이브리드 자동차(HEV), 전기 자동차(EV), 플러그인 하이브리드 자동차(PHEV), 또는 그 외의 전자 기기에 탑재하여도 좋다.
도 12의 (D)에 이차 전지(2602)가 탑재된 차량의 일례를 나타내었다. 차량(2603)은 주행을 위한 동력원으로서 전기 모터를 사용하는 전기 자동차이다. 또는 주행을 위한 동력원으로서 전기 모터와 엔진을 적절히 선택하여 사용할 수 있는 하이브리드 자동차이다. 전기 모터를 사용하는 차량(2603)은 복수의 ECU(Electronic Control Unit)를 가지고, ECU에 의하여 엔진 제어 등을 수행한다. ECU는 마이크로컴퓨터를 포함한다. ECU는 전기 차량에 제공된 CAN(Controller Area Network)에 접속된다. CAN은 차량 내의 LAN으로서 사용되는 직렬 통신 규격의 하나이다. 본 발명의 일 형태의 이차 전지를 사용하여 ECU의 전원으로서 기능시킴으로써, 안전성이 높고, 항속 거리가 긴 차량을 실현할 수 있다.
이차 전지는 전기 모터(미도시)를 구동시킬 뿐만 아니라, 헤드라이트나 실내등 등의 발광 장치에 전력을 공급할 수 있다. 또한 이차 전지는 차량(2603)이 가지는 속도계, 회전 속도계, 내비게이션 시스템 등의 표시 장치 및 반도체 장치에 전력을 공급할 수 있다.
차량(2603)은 이차 전지(2602)가 가지는 이차 전지에 플러그인 방식이나 비접촉 급전 방식 등으로 외부의 충전 설비로부터 전력을 공급받음으로써 충전될 수 있다.
도 12의 (E)는 지상 설치형 충전 장치(2604)로부터 케이블을 통하여 차량(2603)을 충전하는 상태를 나타낸 것이다. 충전 시에는, 충전 방법이나 커넥터의 규격 등으로서 CHAdeMO(등록 상표)나 콤보 등의 소정의 방식을 적절히 사용하면 좋다. 예를 들어 플러그인 기술을 사용하여, 외부로부터의 전력 공급에 의하여 차량(2603)에 탑재된 이차 전지(2602)를 충전할 수 있다. 충전은 ACDC 컨버터 등의 변환 장치를 통하여 교류 전력을 직류 전력으로 변환함으로써 수행할 수 있다. 충전 장치(2604)는 도 12의 (E)와 같이 주택에 구비된 것이어도 좋고, 상업 시설에 제공된 충전 스테이션이어도 좋다.
또한 도시하지 않았지만, 수전 장치를 차량에 탑재하고, 지상의 송전 장치로부터 전력을 비접촉으로 공급하여 충전할 수도 있다. 이 비접촉 급전 방식의 경우에는 도로나 외벽에 송전 장치를 조합함으로써, 정차 시뿐만 아니라 주행 시에도 충전을 할 수 있다. 또한 이 비접촉 급전 방식을 이용하여 차량들 사이에서 전력을 송수신하여도 좋다. 또한 차량의 외장부에 태양 전지를 제공하여, 정차 시나 주행 시에 이차 전지를 충전하여도 좋다. 이와 같은 비접촉 전력 공급에는 전자기 유도 방식이나 자기장 공명 방식을 이용할 수 있다.
또한 도 12의 (E)에 나타낸 주택은 본 발명의 일 형태인 이차 전지를 가지는 축전 시스템(2612)과 태양 전지판(2610)을 가진다. 축전 시스템(2612)은 배선(2611) 등을 통하여 태양 전지판(2610)에 전기적으로 접속되어 있다. 또한 축전 시스템(2612)과 지상 설치형 충전 장치(2604)가 전기적으로 접속되어도 좋다. 태양 전지판(2610)으로 얻은 전력으로 축전 시스템(2612)을 충전할 수 있다. 또한 축전 시스템(2612)에 저장된 전력으로 차량(2603)이 가지는 이차 전지(2602)를 충전 장치(2604)를 통하여 충전할 수 있다.
축전 시스템(2612)에 저장된 전력은 주택 내의 다른 전자 기기에도 공급될 수 있다. 따라서 정전 등으로 인하여 상용 전원으로부터 전력을 공급받을 수 없을 때에도, 본 발명의 일 형태에 따른 축전 시스템(2612)을 무정전 전원으로서 사용함으로써, 전자 기기를 이용할 수 있다.
본 실시형태는 다른 실시형태와 적절히 조합하여 사용할 수 있다.
(실시형태 5)
본 실시형태에서는 양극 활물질 입자, 전해액, 첨가제 등의 관계에 대하여 이하에서 설명한다.
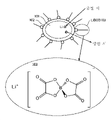
도 14의 (A)는 실시형태 1 또는 실시형태 2의 이차 전지 내부에서의 복수의 양극 활물질과, 그 주변에 배치되는 전해액, 첨가제 등의 상황을 나타낸 모델도이다. 도 14의 (A)의 왼쪽에 복수의 입자, 오른쪽에 하나의 입자를 확대한 모델도를 나타내었다.
도 14의 (A)에는, 충방전을 수행함으로써 Li+ 이온이 양극 활물질(200A)의 입자 내로 이동 또는 전해액 중으로 이동되는 상태를 나타내었다.
양극 활물질(200A)의 입자의 표층부에는 Mg, Al, Ni가 편재되어 있으며, 또한 표면의 적어도 일부에 첨가제의 피막이 형성되어 있는 상태를 나타내었다. 첨가제의 피막은 LiBOB의 붕소(B)의 부분이 양극 활물질(200A)의 입자의 일부에 부착됨으로써 형성된다. Mg, Al, Ni가 편재되어 있는 영역에는 플루오린도 포함되어 있고, 입자 내에 포함되는 전이 금속, 대표적으로는 코발트(또는 망가니즈, 니켈 등)의 전해액으로의 용출을 억제하고 있다. 또한 피막도 전이 금속의 전해액으로의 용출을 억제하고 있다. 또한 피막은 전해액과의 부반응도 억제하고 있다. Mg, Al, Ni가 편재되어 있는 영역의 존재와 피막의 상승 효과에 의하여, 신뢰성이 대폭적으로 향상된다.
또한 비교예로서, 도 14의 (B)는 종래의 이차 전지 내부에서의 복수의 LiCoO2 입자의 충방전 시의 상황을 나타낸 모델도이다. 도 14의 (B)의 왼쪽에 복수의 입자, 오른쪽에 하나의 입자를 확대한 모델도를 나타내었다. 또한 도 18은 양극 활물질 입자(101)와 첨가제(103)의 관계를 나타낸 모델의 일례이다. 도 18에 나타낸 바와 같이, 전해액에 LiBOB를 첨가함으로써, 양극 활물질 입자(101)의 표층부(102)에 LiBOB가 접촉되는 부분과 접촉되지 않는 부분이 생겨, 충방전 시에는 LiBOB가 접촉되는 부분들 사이의 틈을 Li가 출입한다. 전해액에 LiBOB를 적당량 첨가함으로써 양극 활물질 입자(101)에 포함된 니켈이나 망가니즈 등의 용출을 억제할 수 있다. 전해액에 첨가하는 LiBOB의 최적량이란, LiBOB가 양극 활물질 입자(101)의 표층부(102)에 접촉하고 있는 상태가 되는 양이 바람직하다.
도 14의 (B)에 나타낸 바와 같이, 충방전을 수행함으로써 Li+ 이온이 LiCoO2 입자 내로 이동 또는 전해액 중으로 이동되는 상태를 나타내었다. 또한 충방전을 수행함으로써, LiCoO2 입자 내에 포함되는 전이 금속, 대표적으로는 코발트(또는 망가니즈, 니켈 등)가 전해액으로 용출되는 것을 나타내었다. 용출된 코발트는 이차 전지의 음극에 부착되어, 열화가 촉진된다는 과제가 있다.
또한 실시형태 1 또는 실시형태 2의 이차 전지에서는 전해액 중에 리튬염으로서 도 17의 (A)에 나타낸 LiPF6을 사용하였다. 또한 전해액으로서 도 17의 (B)에 나타낸 다이에틸카보네이트(DEC)와 도 17의 (C)에 나타낸 에틸렌카보네이트(EC)를 사용하였다.
상기와 같은 이차 전지 내부에서 생기는 화학 반응으로서는 도 15 또는 도 16을 들 수 있다.
또한 전해액의 다른 용매로서 도 17의 (D)에 나타낸 프로필렌카보네이트(PC)와, 도 17의 (F)에 나타낸 에틸메틸카보네이트(EMC)와, 도 17의 (G)에 나타낸 다이메틸카보네이트(DMC)를 사용할 수 있다. 또한 전해액의 다른 용매로서는 뷰틸렌카보네이트, 클로로에틸렌카보네이트, γ-뷰틸로락톤, γ-발레로락톤, 폼산 메틸, 아세트산 메틸, 아세트산 에틸, 프로피온산 메틸, 프로피온산 에틸, 프로피온산 프로필, 뷰티르산 메틸, 1,3-다이옥세인, 1,4-다이옥세인, 다이메톡시에테인(DME), 다이메틸설폭사이드, 다이에틸에터, 메틸다이글라임, 아세토나이트릴, 벤조나이트릴, 테트라하이드로퓨란, 설포레인, 설톤 등 중 1종 또는 2종 이상을 임의의 조합 및 비율로 사용할 수 있다. 또한 본 실시형태에서는 첨가제로서 LiBOB뿐만 아니라, 다른 첨가제(바이닐렌카보네이트(VC), 프로페인설톤(PS), tert-뷰틸벤젠(TBB), 플루오로에틸렌카보네이트(FEC), 숙시노나이트릴, 아디포나이트릴 등의 다이나이트릴 화합물 등)를 가하여도 좋다. 또한 도 17의 (E)에 나타낸 바이닐렌카보네이트(VC)는 첨가제이다.
본 실시형태는 다른 실시형태와 적절히 조합하여 사용할 수 있다.
200A: 양극 활물질, 200B: 양극 활물질, 500: 이차 전지, 501: 양극 집전체, 502: 양극 활물질층, 503: 양극, 504: 음극 집전체, 505: 음극 활물질층, 506: 음극, 507: 세퍼레이터, 508: 전해액, 509: 외장체, 510: 양극 리드 전극, 511: 음극 리드 전극, 600: 이차 전지, 601: 양극캡, 602: 전지 캔, 603: 양극 단자, 604: 양극, 605: 세퍼레이터, 606: 음극, 607: 음극 단자, 608: 절연판, 609: 절연판, 611: PTC 소자, 612: 안전 밸브 기구, 613: 도전판, 614: 도전판, 615: 모듈, 616: 도선, 617: 온도 제어 장치, 902: 혼합물, 903: 혼합물, 2100: 휴대 전화기, 2101: 하우징, 2102: 표시부, 2103: 조작 버튼, 2104: 외부 접속 포트, 2105: 스피커, 2106: 마이크로폰, 2107: 이차 전지, 2300: 무인 항공기, 2301: 이차 전지, 2302: 로터, 2303: 카메라, 2601: 이차 전지, 2602: 이차 전지, 2603: 차량, 2604: 충전 장치, 2610: 태양 전지판, 2611: 배선, 2612: 축전 시스템
Claims (7)
- 이차 전지로서,
리튬과, 전이 금속과, 마그네슘과, 산소와, 플루오린을 가지는 양극 활물질과, 리튬비스옥살레이토보레이트를 포함하는 전해액을 가지는, 이차 전지. - 제 1 항에 있어서,
상기 전이 금속은 코발트, 니켈, 망가니즈 중 적어도 하나인, 이차 전지. - 제 1 항 또는 제 2 항에 있어서,
상기 양극 활물질은 알루미늄을 더 포함하는, 이차 전지. - 제 1 항 내지 제 3 항 중 어느 한 항에 있어서,
상기 전해액은 리튬염과, 상기 리튬염을 용해시키는 다이에틸카보네이트 및 에틸렌카보네이트를 포함하는, 이차 전지. - 제 4 항에 있어서,
상기 리튬염은 헥사플루오로인산 리튬인, 이차 전지. - 제 1 항 내지 제 5 항 중 어느 한 항에 있어서,
상기 이차 전지의 음극 활물질은 흑연인, 이차 전지. - 제 1 항 내지 제 6 항 중 어느 한 항에 있어서,
상기 전해액 중에서 상기 리튬비스옥살레이토보레이트가 차지하는 비율은 0.1중량% 초과 3중량% 미만인, 이차 전지.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2019-219137 | 2019-12-03 | ||
| JP2019219137 | 2019-12-03 | ||
| JP2019223652 | 2019-12-11 | ||
| JPJP-P-2019-223652 | 2019-12-11 | ||
| JP2020185764 | 2020-11-06 | ||
| JPJP-P-2020-185764 | 2020-11-06 | ||
| PCT/IB2020/061166 WO2021111257A1 (ja) | 2019-12-03 | 2020-11-26 | 二次電池、携帯情報端末、及び車両 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220106120A true KR20220106120A (ko) | 2022-07-28 |
Family
ID=76222332
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227016961A KR20220106120A (ko) | 2019-12-03 | 2020-11-26 | 이차 전지, 휴대 정보 단말기, 및 차량 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220416239A1 (ko) |
| JP (1) | JPWO2021111257A1 (ko) |
| KR (1) | KR20220106120A (ko) |
| CN (1) | CN114762165A (ko) |
| WO (1) | WO2021111257A1 (ko) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019179758A (ja) | 2017-06-26 | 2019-10-17 | 株式会社半導体エネルギー研究所 | 正極活物質の作製方法 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3687665B2 (ja) * | 2002-07-16 | 2005-08-24 | 日亜化学工業株式会社 | 非水電解液二次電池用正極活物質および非水電解液二次電池 |
| CN102522590B (zh) * | 2011-12-26 | 2014-09-17 | 华为技术有限公司 | 一种非水有机电解液、包含它的锂离子二次电池及其制备方法和终端通讯设备 |
| JP2013164992A (ja) * | 2012-02-10 | 2013-08-22 | Toyota Motor Corp | 非水電解液二次電池 |
| JP6628697B2 (ja) * | 2015-09-30 | 2020-01-15 | パナソニック株式会社 | 非水電解質二次電池 |
| KR102264634B1 (ko) * | 2017-09-08 | 2021-06-15 | 주식회사 엘지에너지솔루션 | 리튬 이차전지용 양극 활물질, 이의 제조 방법, 이를 포함하는 리튬 이차전지용 양극 및 리튬 이차전지 |
-
2020
- 2020-11-26 US US17/780,049 patent/US20220416239A1/en active Pending
- 2020-11-26 WO PCT/IB2020/061166 patent/WO2021111257A1/ja active Application Filing
- 2020-11-26 KR KR1020227016961A patent/KR20220106120A/ko unknown
- 2020-11-26 JP JP2021562203A patent/JPWO2021111257A1/ja active Pending
- 2020-11-26 CN CN202080083917.6A patent/CN114762165A/zh active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2019179758A (ja) | 2017-06-26 | 2019-10-17 | 株式会社半導体エネルギー研究所 | 正極活物質の作製方法 |
Non-Patent Citations (1)
| Title |
|---|
| W. E. Counts, R. Roy, and E. F. Osborn, "Fluoride Model Systems: II, The Binary Systems CaF2-BeF2, MgF2-BeF2, and LiF-MgF2", Journal of the American Ceramic Society, 36 [1] 12-17 (1953). |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2021111257A1 (ja) | 2021-06-10 |
| JPWO2021111257A1 (ko) | 2021-06-10 |
| CN114762165A (zh) | 2022-07-15 |
| US20220416239A1 (en) | 2022-12-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6797619B2 (ja) | 非水電解質電池、電池パック及び車両 | |
| CN107204454B (zh) | 电极、非水电解质电池、电池包及车辆 | |
| JP6024457B2 (ja) | 二次電池およびそれに用いる二次電池用電解液 | |
| WO2012014793A1 (ja) | リチウムイオン二次電池 | |
| KR101898380B1 (ko) | 비수 전해질 전지, 비수 전해질 전지 팩, 및 차량 | |
| US10461313B2 (en) | Nonaqueous electrolyte battery, battery module, and battery pack | |
| KR20210066723A (ko) | 양극 활물질, 이차 전지, 전자 기기 | |
| KR20240016321A (ko) | 이차 전지, 전자 기기, 및 비행체 | |
| WO2021130610A1 (ja) | 正極活物質層、活物質層、正極、二次電池および車両 | |
| WO2021144660A1 (ja) | 正極活物質、二次電池、電子機器、および車両 | |
| JPWO2018062202A1 (ja) | 非水電解質電池及び電池パック | |
| KR20230049081A (ko) | 전극, 음극 활물질, 음극, 이차 전지, 이동체, 및 전자 기기, 음극 활물질의 제작 방법, 그리고 음극의 제작 방법 | |
| KR20230017795A (ko) | 이차 전지 및 차량 | |
| JP2022045263A (ja) | 正極活物質、二次電池、二次電池の作製方法、電子機器、及び車両 | |
| KR20220133190A (ko) | 양극 활물질, 이차 전지, 전자 기기 | |
| WO2021111257A1 (ja) | 二次電池、携帯情報端末、及び車両 | |
| WO2021111249A1 (ja) | 正極活物質、二次電池および車両 | |
| WO2021105813A1 (ja) | 二次電池、正極活物質の作製方法、携帯情報端末、および車両 | |
| US20230198008A1 (en) | Secondary battery, and vehicle including secondary battery | |
| US20230238583A1 (en) | Secondary battery, and vehicle including secondary battery | |
| WO2022034414A1 (ja) | 二次電池、電子機器、車両、及び正極活物質の作製方法 | |
| KR20230038213A (ko) | 전극, 이차 전지, 이동체, 전자 기기, 및 리튬 이온 이차 전지용 전극의 제작 방법 | |
| CN116685557A (zh) | 正极、正极的制造方法、二次电池、电子设备、蓄电系统以及车辆 | |
| KR20230156083A (ko) | 복합 산화물의 제작 방법, 양극, 리튬 이온 이차 전지, 전자 기기, 축전 시스템, 및 이동체 | |
| CN116998085A (zh) | 蓄电装置管理系统以及电子设备 |