KR20220047972A - 렐루골릭스의 고체-상태 형태 - Google Patents
렐루골릭스의 고체-상태 형태 Download PDFInfo
- Publication number
- KR20220047972A KR20220047972A KR1020227003478A KR20227003478A KR20220047972A KR 20220047972 A KR20220047972 A KR 20220047972A KR 1020227003478 A KR1020227003478 A KR 1020227003478A KR 20227003478 A KR20227003478 A KR 20227003478A KR 20220047972 A KR20220047972 A KR 20220047972A
- Authority
- KR
- South Korea
- Prior art keywords
- relugolix
- anhydrous
- dmf
- dcm
- volume
- Prior art date
Links
- AOMXMOCNKJTRQP-UHFFFAOYSA-N 1-[4-[1-[(2,6-difluorophenyl)methyl]-5-[(dimethylamino)methyl]-3-(6-methoxypyridazin-3-yl)-2,4-dioxothieno[2,3-d]pyrimidin-6-yl]phenyl]-3-methoxyurea Chemical compound C1=CC(NC(=O)NOC)=CC=C1C1=C(CN(C)C)C(C(=O)N(C=2N=NC(OC)=CC=2)C(=O)N2CC=3C(=CC=CC=3F)F)=C2S1 AOMXMOCNKJTRQP-UHFFFAOYSA-N 0.000 title claims abstract description 247
- 229950004238 relugolix Drugs 0.000 title claims abstract description 246
- 239000012453 solvate Substances 0.000 claims abstract description 62
- 238000000034 method Methods 0.000 claims abstract description 25
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 23
- 201000010099 disease Diseases 0.000 claims abstract description 16
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 13
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-dimethylformamide Substances CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 claims description 145
- 238000000634 powder X-ray diffraction Methods 0.000 claims description 35
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 claims description 34
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 26
- 239000012296 anti-solvent Substances 0.000 claims description 25
- 238000003756 stirring Methods 0.000 claims description 18
- 238000000113 differential scanning calorimetry Methods 0.000 claims description 16
- 239000002244 precipitate Substances 0.000 claims description 14
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical group COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 claims description 11
- 239000000203 mixture Substances 0.000 claims description 11
- 238000002360 preparation method Methods 0.000 claims description 11
- 239000002002 slurry Substances 0.000 claims description 9
- 239000002904 solvent Substances 0.000 claims description 9
- 239000003960 organic solvent Substances 0.000 claims description 8
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 claims description 7
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 claims description 6
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 claims description 6
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 6
- 150000001875 compounds Chemical class 0.000 claims description 5
- 238000002156 mixing Methods 0.000 claims description 5
- 201000009273 Endometriosis Diseases 0.000 claims description 4
- 206010060862 Prostate cancer Diseases 0.000 claims description 4
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims description 4
- 206010067269 Uterine fibrosis Diseases 0.000 claims description 4
- 239000013078 crystal Substances 0.000 claims description 4
- 239000003814 drug Substances 0.000 claims description 4
- 229940011051 isopropyl acetate Drugs 0.000 claims description 4
- RWGFKTVRMDUZSP-UHFFFAOYSA-N isopropyl-benzene Natural products CC(C)C1=CC=CC=C1 RWGFKTVRMDUZSP-UHFFFAOYSA-N 0.000 claims description 4
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical group CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 claims description 4
- 238000001704 evaporation Methods 0.000 claims description 3
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 claims description 2
- 125000002592 cumenyl group Chemical group C1(=C(C=CC=C1)*)C(C)C 0.000 claims description 2
- 238000004519 manufacturing process Methods 0.000 abstract description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 57
- 239000007787 solid Substances 0.000 description 12
- 239000008186 active pharmaceutical agent Substances 0.000 description 9
- 238000002411 thermogravimetry Methods 0.000 description 9
- 239000000463 material Substances 0.000 description 8
- 238000005481 NMR spectroscopy Methods 0.000 description 7
- 238000004458 analytical method Methods 0.000 description 7
- 208000035475 disorder Diseases 0.000 description 7
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 7
- 238000005160 1H NMR spectroscopy Methods 0.000 description 6
- 238000001035 drying Methods 0.000 description 6
- 239000012535 impurity Substances 0.000 description 6
- 150000003839 salts Chemical class 0.000 description 6
- 238000004467 single crystal X-ray diffraction Methods 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 5
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000010511 deprotection reaction Methods 0.000 description 4
- 238000001938 differential scanning calorimetry curve Methods 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 239000000126 substance Substances 0.000 description 4
- 238000001757 thermogravimetry curve Methods 0.000 description 4
- 238000003809 water extraction Methods 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 230000006911 nucleation Effects 0.000 description 3
- 238000010899 nucleation Methods 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- 238000005033 Fourier transform infrared spectroscopy Methods 0.000 description 2
- 239000000579 Gonadotropin-Releasing Hormone Substances 0.000 description 2
- 101000857870 Squalus acanthias Gonadoliberin Proteins 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 239000000306 component Substances 0.000 description 2
- 238000004090 dissolution Methods 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- XLXSAKCOAKORKW-AQJXLSMYSA-N gonadorelin Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 XLXSAKCOAKORKW-AQJXLSMYSA-N 0.000 description 2
- 229940035638 gonadotropin-releasing hormone Drugs 0.000 description 2
- 239000010410 layer Substances 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 238000010926 purge Methods 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 238000001069 Raman spectroscopy Methods 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 238000002441 X-ray diffraction Methods 0.000 description 1
- NAUDKYVGHCCLOT-LAQCMFAESA-N [(8r,9s,10r,13s,14s,17r)-17-ethynyl-13-methyl-3-oxo-1,2,6,7,8,9,10,11,12,14,15,16-dodecahydrocyclopenta[a]phenanthren-17-yl] acetate;(8r,9s,13s,14s,17s)-13-methyl-6,7,8,9,11,12,14,15,16,17-decahydrocyclopenta[a]phenanthrene-3,17-diol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1.C1CC2=CC(=O)CC[C@@H]2[C@@H]2[C@@H]1[C@@H]1CC[C@](C#C)(OC(=O)C)[C@@]1(C)CC2 NAUDKYVGHCCLOT-LAQCMFAESA-N 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 239000004067 bulking agent Substances 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 239000012876 carrier material Substances 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- 230000037213 diet Effects 0.000 description 1
- 235000005911 diet Nutrition 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000008029 eradication Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 239000007972 injectable composition Substances 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 238000000399 optical microscopy Methods 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 230000037081 physical activity Effects 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 238000003828 vacuum filtration Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C231/00—Preparation of carboxylic acid amides
- C07C231/12—Preparation of carboxylic acid amides by reactions not involving the formation of carboxamide groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C233/00—Carboxylic acid amides
- C07C233/01—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms
- C07C233/02—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having nitrogen atoms of carboxamide groups bound to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals
- C07C233/03—Carboxylic acid amides having carbon atoms of carboxamide groups bound to hydrogen atoms or to acyclic carbon atoms having nitrogen atoms of carboxamide groups bound to hydrogen atoms or to carbon atoms of unsubstituted hydrocarbon radicals with carbon atoms of carboxamide groups bound to hydrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/13—Crystalline forms, e.g. polymorphs
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Endocrinology (AREA)
- Reproductive Health (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
Abstract
본 발명은 렐루골릭스(relugolix)의 고체-상태(solid-state) DMF 용매화물에 관한 것이며, 무수 렐루골릭스의 형태 A 및 형태 C로 지칭되는 렐루골릭스의 고체-상태 무수 형태에 관한 것이다. 본 발명은 추가로 렐루골릭스의 고체-상태 DMF 용매화물, 및 무수 렐루골릭스의 형태 A, 형태 B 및 형태 C 각각의 제조 방법에 관한 것이다. 본 발명은 또한 렐루골릭스의 DMF 용매화물, 또는 무수 렐루골릭스의 형태 A 또는 형태 C를 포함하는 약제학적 조성물에 관한 것이며, 렐루골릭스의 DMF 용매화물, 또는 무수 렐루골릭스의 형태 A 또는 형태 C를 사용하여 질환을 치료하는 방법에 관한 것이다.
Description
본 발명은 렐루골릭스(relugolix)의 고체-상태(solid-state) DMF 용매화물 및 무수 형태 및 이의 제조 방법에 관한 것이다. 추가로, 본 발명은 또한 렐루골릭스의 신규한 형태를 포함하는 약제학적 조성물 및 그러한 형태를 사용하여 질환을 치료하는 방법에 관한 것이다.
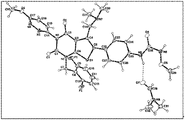
화학명이 1-[4-[1-[(2,6-다이플루오로페닐)-메틸]-5-[(다이메틸아미노)메틸]-3-(6-메톡시피리다진-3-일)-2,4-다이옥소티에노-[2,3-d]피리미딘-6-일]페닐]-3-메톡시우레아인 렐루골릭스는 경구 활성 비펩티드 성선자극호르몬-방출 호르몬(GnRH)-수용체 길항제이다. 렐루골릭스는 하기 구조를 갖는다:
렐루골릭스는 자궁 섬유증과 관련된 증상의 치료제로서 일본에서 승인되었다. 자궁내막증-관련 통증 및 전립선암에 대한 치료제로서의 렐루골릭스의 효능을 평가하기 위한 연구가 진행 중이다.
미국 특허 제10,464,945호는 렐루골릭스의 테트라하이드로푸란 용매화물의 결정질 형태, 및 대략 8.932°, 16.607°, 및 17.328°에서 2-세타(2θ) 피크를 갖는 x-선 분말 회절 패턴을 나타내는 다른 결정질 형태를 개시한다. 다른 XRPD 피크는 대략 7.384°, 9.933°, 12.076°, 22.202°, 22.761°, 및 27.422° 2θ를 포함한다.
국제특허 공개 WO2019/178304호는 렐루골릭스의 여러 형태를 개시한다. 구체적으로, 형태 F는 등구조 다형체로서 기술되며, 즉, 무수물, 수화물, 바람직하게는 반수화물, 또는 용매화물일 수 있다. 이는 6.9, 7.5, 9.5, 13.9 및 18.1° 2θ ± 0.2° 2θ에서 피크를 갖는 X-선 분말 회절 패턴을 특징으로 한다. 형태 G는 5.4, 8.4, 10.7 및 12.1° 2θ ± 0.2° 2θ에서 피크를 갖는 X-선 분말 회절 패턴을 특징으로 한다. 다형체적으로 순수한 형태 G는 3.4, 5.6, 9.6, 13.3 및 17.4° 2θ ± 0.2° 2θ에서 피크를 갖는 X-선 분말 회절 패턴을 특징으로 한다. 형태 H는 6.2, 8.6, 15.9, 19.0 및 19.6° 2θ ± 0.2° 2θ에서 피크를 갖는 X-선 분말 회절 패턴을 특징으로 한다. 형태 J는 헤미 아세토니트릴 용매화물, 반수화물로서 기술된다. 국제특허 공개 WO 2019/178304호는 또한 렐루골릭스의 비정질 형태를 개시한다.
더 구체적으로 약 20.1, 24.3 및 9.0° 2θ로부터 선택되는 적어도 2개 이상의 X-선 분말 회절 피크를 갖는, 렐루골릭스의 DMF 용매화물, 또는 약 10.7, 20.9 및 19.2° 2θ 또는 약 8.3, 6.8, 7.7, 및 19.9° 2θ로부터 선택되는 X-선 분말 회절 피크를 갖는, 렐루골릭스의 무수 결정질 형태에 대한 개시는 없다.
본 발명은 렐루골릭스의 DMF 용매화물의 형태 A로 지칭되는, 렐루골릭스의 고체-상태 DMF 용매화물에 관한 것이며, 무수 렐루골릭스의 형태 A 및 형태 C로 지칭되는, 렐루골릭스의 고체-상태 무수 형태에 관한 것이다. 본 발명은 추가로 렐루골릭스의 DMF 용매화물의 형태 A, 및 무수 렐루골릭스의 형태 A, 형태 B 및 형태 C 각각의 제조 방법에 관한 것이다. 본 발명은 또한 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C 중 어느 하나를 포함하는 약제학적 조성물에 관한 것이며, 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C 중 어느 하나를 사용하여 질환을 치료하는 방법에 관한 것이다.
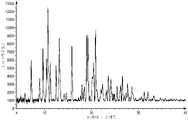
도 1은 렐루골릭스의 DMF 용매화물의 형태 A의 단결정으로부터 계산된 XRPD 패턴(하부) 및 렐루골릭스의 DMF 용매화물의 형태 A의 실제 XRPD 패턴(상부)의 오버레이를 제공한다.
도 2는 SCXRD로부터 식별되는 렐루골릭스의 DMF 용매화물의 형태 A의 3차원 구조를 제공한다.
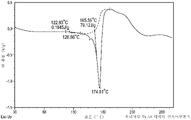
도 3은 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 DSC 플롯을 제공한다.
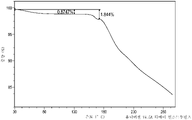
도 4는 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 TGA 플롯을 제공한다.
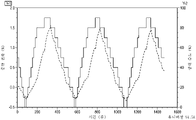
도 5는 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 DVS 플롯을 제공한다.
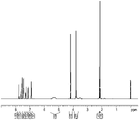
도 6은 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 1H-NMR 플롯을 제공한다.
도 7은 무수 렐루골릭스의 형태 A의 대표적인 XRPD 패턴을 제공한다.
도 8은 무수 렐루골릭스의 형태 A의 대표적인 DSC 플롯을 제공한다.
도 9는 무수 렐루골릭스의 형태 A의 대표적인 TGA 플롯을 제공한다.
도 10은 무수 렐루골릭스의 형태 A의 대표적인 DVS 플롯을 제공한다.
도 11은 무수 렐루골릭스의 형태 A의 대표적인 1H-NMR 플롯을 제공한다.
도 12는 무수 렐루골릭스의 형태 B의 대표적인 XRPD 패턴을 제공한다.
도 13은 무수 렐루골릭스의 형태 B의 대표적인 DSC 플롯을 제공한다.
도 14는 무수 렐루골릭스의 형태 B의 대표적인 TGA 플롯을 제공한다.
도 15는 무수 렐루골릭스의 형태 B의 대표적인 DVS 플롯을 제공한다.
도 16은 무수 렐루골릭스의 형태 B의 대표적인 1H-NMR 플롯을 제공한다.
도 17은 무수 렐루골릭스의 형태 C의 대표적인 XRPD 패턴을 제공한다.
도 18은 무수 렐루골릭스의 형태 C의 대표적인 DSC 플롯을 제공한다.
도 19는 무수 렐루골릭스의 형태 C의 대표적인 TGA 플롯을 제공한다.
도 20은 무수 렐루골릭스의 형태 C의 대표적인 DVS 플롯을 제공한다.
도 21은 무수 렐루골릭스의 형태 C의 대표적인 1H-NMR 플롯을 제공한다.
도 2는 SCXRD로부터 식별되는 렐루골릭스의 DMF 용매화물의 형태 A의 3차원 구조를 제공한다.
도 3은 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 DSC 플롯을 제공한다.
도 4는 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 TGA 플롯을 제공한다.
도 5는 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 DVS 플롯을 제공한다.
도 6은 렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 1H-NMR 플롯을 제공한다.
도 7은 무수 렐루골릭스의 형태 A의 대표적인 XRPD 패턴을 제공한다.
도 8은 무수 렐루골릭스의 형태 A의 대표적인 DSC 플롯을 제공한다.
도 9는 무수 렐루골릭스의 형태 A의 대표적인 TGA 플롯을 제공한다.
도 10은 무수 렐루골릭스의 형태 A의 대표적인 DVS 플롯을 제공한다.
도 11은 무수 렐루골릭스의 형태 A의 대표적인 1H-NMR 플롯을 제공한다.
도 12는 무수 렐루골릭스의 형태 B의 대표적인 XRPD 패턴을 제공한다.
도 13은 무수 렐루골릭스의 형태 B의 대표적인 DSC 플롯을 제공한다.
도 14는 무수 렐루골릭스의 형태 B의 대표적인 TGA 플롯을 제공한다.
도 15는 무수 렐루골릭스의 형태 B의 대표적인 DVS 플롯을 제공한다.
도 16은 무수 렐루골릭스의 형태 B의 대표적인 1H-NMR 플롯을 제공한다.
도 17은 무수 렐루골릭스의 형태 C의 대표적인 XRPD 패턴을 제공한다.
도 18은 무수 렐루골릭스의 형태 C의 대표적인 DSC 플롯을 제공한다.
도 19는 무수 렐루골릭스의 형태 C의 대표적인 TGA 플롯을 제공한다.
도 20은 무수 렐루골릭스의 형태 C의 대표적인 DVS 플롯을 제공한다.
도 21은 무수 렐루골릭스의 형태 C의 대표적인 1H-NMR 플롯을 제공한다.
본 발명은 렐루골릭스의 DMF 용매화물의 형태 A로 지칭되는, 렐루골릭스의 고체-상태 DMF 용매화물, 및 무수 렐루골릭스의 형태 A 및 형태 C로 지칭되는, 렐루골릭스의 무수 형태; 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C 중 어느 하나를 포함하는 약제학적 조성물; 렐루골릭스의 DMF 용매화물의 형태 A, 및 무수 렐루골릭스의 형태 A, 형태 B 및 형태 C 각각의 제조 방법; 및 자궁 섬유증, 자궁내막증 또는 전립선암을 갖는 환자를 치료하기 위한 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C 중 어느 하나의 용도에 관한 것이다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 용어 "고체-상태 형태"는 결정질 또는 다형성 형태, 비정질 상, 및 용매화물을 포함한다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 용어 "약" 및 "대략"은, 특정 고체 형태를 특성화하기 위해 제공되는 수치 값 또는 값들의 범위, 예를 들어, 용융, 탈수, 탈용매화 또는 유리 전이 이벤트(event)를 포함하는, 예를 들어 DSC 또는 TGA 열적 이벤트를 기술하는 것과 같은, 예를 들어 특정 온도 또는 온도 범위; 예를 들어 온도 또는 습도의 함수로서의 질량 변화와 같은 질량 변화; 예를 들어, 질량 또는 백분율의 관점에서의 용매 또는 물 함량; 또는 예를 들어, IR 또는 라만 분광법 또는 XRPD에 의한 분석에서와 같은 피크 위치와 관련하여 사용될 때, 값 또는 값들의 범위가 특정 고체 형태를 여전히 기술하면서 당업자에게 합리적인 것으로 여겨지는 정도로 벗어날 수 있음을 나타낸다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 용어 "약제학적 조성물"은 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C 중 어느 하나의 약제학적 유효량 및 약제학적으로 허용가능한 부형제를 포함하는 것으로 의도된다. 본 명세서에 사용되는 바와 같이, 용어 "약제학적 조성물"은 정제, 환제, 분말, 액체, 현탁액, 에멀젼, 과립, 캡슐, 좌약, 또는 주사 제제와 같은 약제학적 조성물을 포함한다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 본 명세서에 사용되는 용어 "결정질" 및 관련 용어는 화합물, 물질, 개질물, 재료, 성분 또는 생성물을 설명하기 위해 사용될 때, 달리 명시되지 않는 한, 화합물, 물질, 개질물, 재료, 성분 또는 생성물이 X-선 회절에 의해 결정할 때 실질적으로 결정질임을 의미한다. 예를 들어, 문헌[Remington: The Science and Practice of Pharmacy, 21st edition, Lippincott, Williams and Wilkins, Baltimore, Md. (2005)]; 및 문헌[The United States Pharmacopeia, 23rd ed., 1843-1844 (1995)]을 참조한다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 용어 "부형제"는 약제학적으로 허용가능한 유기 또는 무기 담체 물질을 지칭한다. 부형제는 강력한 활성 성분을 함유하는 벌킹-업(bulking-up) 제형을 위해(따라서 종종 "벌킹제", "충전제", 또는 "희석제"로 지칭됨), 또는 약물 흡수 또는 용해성을 촉진하는 것과 같은 최종 투여 형태 내의 활성 성분에 치료적 향상을 부여하기 위해 포함되는, 약물의 활성 성분과 함께 제형화되는 천연 또는 합성 물질일 수 있다. 부형제는 또한 예상 저장 수명에 걸친 변성 방지와 같은 시험관내 안정성에 도움이 되는 것에 더하여, 예를 들어, 분말 유동성 또는 비-점착(non-stick) 특성을 촉진함으로써, 활성 물질의 취급에 도움이 되도록 제조 공정에서 유용할 수 있다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 용어 "환자"는 치료, 관찰 또는 실험의 대상이 된 동물, 바람직하게는 포유류, 가장 바람직하게는 인간을 지칭한다. 바람직하게는, 환자는 치료 및/또는 예방할 질환 또는 장애의 적어도 하나의 증상을 경험하였고/경험하였거나 나타내었다. 또한, 환자는 치료 및/또는 예방할 장애, 질환 또는 병태의 어떠한 증상도 나타내지 않았을 수 있지만, 의사, 임상의 또는 기타 의료 전문가에 의해 상기 장애, 질환 또는 병태가 발생할 위험이 있는 것으로 간주되었다.
본 명세서에 사용된 바와 같이 그리고 달리 명시되지 않는 한, 본 명세서에서 용어 "다형체", "다형성 형태"또는 관련 용어는, 분자의 상이한 배열 또는 배좌, 염의 이온, 또는 결정질 격자 내의 용매의 첨가 및 배열의 결과로서, 2개 이상의 형태로 존재할 수 있는 API(활성 약제학적 성분) 유리 염기 또는 이의 염의 결정 형태를 지칭한다.
본 명세서에 사용된 바와 같이 그리고 달리 명시되지 않는 한, 다형체 또는 다형체 형태와 관련하여 용어 "실질적으로" 또는 "실질적으로 없는/순수한"은 그 형태가 약 30 중량% 미만, 약 20 중량% 미만, 약 15 중량% 미만, 약 10 중량% 미만, 약 5 중량% 미만, 또는 약 1 중량% 미만의 불순물을 함유함을 의미한다. 불순물은, 예를 들어, 용매화된 결정질 다형체 형태의 것 이외에 다른 다형체 형태, 물 및 용매를 포함할 수 있다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 용어 "치료하다", "치료하는" 및 "치료"는 질환 또는 장애, 또는 질환 또는 장애와 관련된 하나 이상의 증상의 근절 또는 개선을 지칭한다. 소정 실시 형태에서, 상기 용어는 그러한 질환 또는 장애를 갖는 환자에게 하나 이상의 치료제를 투여함으로써 질환 또는 장애의 확산 또는 악화를 최소화하는 것을 지칭한다. 일부 실시 형태에서, 상기 용어는 특정 질환의 증상의 개시 후, 다른 추가적인 활성제와 함께 또는 다른 추가적인 활성제 없이, 본 명세서에 제공된 화합물을 투여하는 것을 지칭한다.
본 명세서에 사용되는 바와 같이 그리고 달리 명시되지 않는 한, 약어 "DMF"는 다이메틸포름아미드를 지칭하고; 약어 "TBME"는 tert-부틸메틸 에테르를 지칭하고; 약어 "DCM"은 다이클로로메탄을 지칭하고; 약어 "IPAc"는 아이소프로필 아세테이트를 지칭한다.
본 발명의 목적은 실질적으로 순수하고, 안정하고, 확장 가능한, 렐루골릭스의 DMF 용매화물의 형태 A, 및 무수 렐루골릭스의 형태 A 및 형태 C로 지칭되는 렐루골릭스의 고체-상태 무수 형태에 관한 것이다. 또한 본 발명의 목적은 단리 및 취급 가능한, 렐루골릭스의 DMF 용매화물의 형태 A, 및 무수 렐루골릭스의 형태 A 및 형태 C로 지칭되는 렐루골릭스의 고체-상태 무수 형태를 제공하는 것이다. 추가로 본 발명의 목적은 렐루골릭스의 DMF 용매화물의 형태 A, 및 무수 렐루골릭스의 형태 A, 형태 B 및 형태 C 각각의 제조 방법을 제공하는 것이다. 본 발명의 또 다른 목적은 렐루골릭스의 약제학적 투여 형태를 제조하기 위한 렐루골릭스의 DMF 용매화물의 형태 A, 및 무수 렐루골릭스의 형태 A 및 형태 C의 사용 방법을 제공하는 것이다.
결정 및 비정질 형태를 특성화하기 위한 기술은 시차 주사 열량법(DSC), 열중량 분석(TGA), 동적 증기 수착(DVS), x-선 분말 회절법(XRPD), 단결정 X-선 회절(SCXRD), 양성자 핵 자기 공명(1H-NMR), 푸리에 변환 적외선 분광법(FTIR 분광법), 및 광학 현미경법을 포함하지만 이로 한정되지 않는다.
티에이 인스트루먼츠(TA Instruments) TGA Q500을 사용하여 TGA 데이터를 수집한다. 샘플(약 2 내지 5 mg)을 무게가 미리 측정된(pre-tared) 핀홀형 밀봉 기밀 알로다인 알루미늄 DSC 팬에 넣고, 약 60 mL/분으로 질소 퍼지를 사용하여 약 10℃/min의 속도로 약 30℃부터 약 300℃까지 스캔하였다.
Cu Kα 방사선원(λ = 1.54 Å), 9-포지션 샘플 홀더 및 링스아이(LYNXEYE) 초고속 검출기를 구비한 브루커(Bruker) D8 어드밴스(Advance)를 사용하여 X-선 분말 회절 패턴을 얻는다. 분석을 위해, 돔을 갖는 제로-백그라운드(zero-bac㎏round)의 공기 민감성 규소 플레이트 홀더 상에 샘플을 놓는다. 당업자는 측정된 데이터에 대해 피크 검색을 수행함으로써 °2θ 값 및 상대 강도 값이 생성되고, 브래그(Bragg) 방정식을 사용하여 °2θ 값으로부터 기기에 의해 d-간격 값을 계산할 수 있음을 인식할 것이다. 당업자는 측정된 피크에 대한 상대 강도가 예를 들어 샘플 준비, 배향 및 사용되는 기기의 결과로서 달라질 수 있음을 또한 인식할 것이다.
100 K의 온도에서 흑연-단색화 Mo-Kα 방사선(λ = 0.71073Å)을 이용하는 브루커 D8QUEST [1] CMOS 영역 검출기에서 SCXRD에 대한 X-선 강도 데이터를 수집한다.
DVS 샘플을 티에이 인스트루먼츠 Q5000SA 중량 측정 물 수착 분석기를 사용하여 분석한다. 상대 습도를 약 0 내지 95%로 조정하고, 샘플의 중량을 연속적으로 모니터링하고 상대 습도 및 시간에 대해 기록한다.
티에이 인스트루먼츠 Q10 DSC를 사용하여 DSC 데이터를 수집한다. 약 2 내지 8 mg의 샘플을 밀봉되지만 덮여 있는 기밀 알로다인 알루미늄 샘플 팬에 넣고, 약 50 mL/min의 질소 퍼지 하에서 약 30℃부터 약 300℃까지 약 10℃/min의 속도로 스캔한다. 추가로, DSC 실행은 오토-샘플러(auto-sampler) 및 RSC40이 구비된 티에이 인스트루먼츠 Q2000에서 생성된다. 기기는 T제로 기밀 밀봉된 알루미늄 팬을 T4P(또는 T4) 모드로 사용하여 약 25℃부터 약 300℃까지 약 10℃/min의 램프(ramp) 속도로 프로그래밍된다.
약 0.05%(v/v) 테트라메틸실란(TMS)을 갖는 중수소화된 다이메틸설폭사이드 및 중수소화된 클로로포름에 화합물을 용해시켜 1H NMR 샘플을 제조한다. 탑스핀(TopSpin) 소프트웨어가 장착된 브루커 어드밴스(Bruker Avance) 600 ㎒ NMR에서 주변 온도에서 스펙트럼을 수집한다. 298 K에서 1H-NMR에 대해 스캔 횟수는 16회이다.
일 실시 형태에서, 렐루골릭스의 DMF 용매화물의 형태 A는,
a) DMF 중 렐루골릭스의 용액을 반용매(anti-solvent)와 혼합하는 단계; 및
b) 렐루골릭스의 DMF 용매화물의 형태 A를 침전물로서 산출하기 위해 단계 a)의 혼합물을 교반하는 단계에 의해 제조된다.
일 실시 형태에서, DMF 중 렐루골릭스의 용액 내의 렐루골릭스 대 DMF의 비는 약 1:5의 중량(g렐루골릭스) 대 부피(mLDMF)이다. 특정 실시 형태에서, 반용매는 TBME이다. 다른 실시 형태에서, 반용매는 톨루엔이다. 예를 들어, 헵탄, 자일렌 또는 쿠멘과 같은 그러나 이로 한정되지 않는 다른 반용매가 그의 반용매 특성에 따라 사용될 수 있음이 당업자에게 명백할 것이다. 일 실시 형태에서, 약 10 내지 13배 부피의 반용매가 DMF 중 렐루골릭스의 용액과 혼합된다(중량(g렐루골릭스) 대 부피(mL반용매)). 일 실시 형태에서, 반용매는 DMF 중 렐루골릭스의 용액에 첨가된다. 특정 실시 형태에서, 주위 온도에서 침전이 발생한다. 다른 실시 형태는 DMF 중 렐루골릭스의 용액과 반용매의 혼합물의 온도를 약 30분 내지 1시간 동안 핵 형성 온도까지 감소시켜 침전물을 생성하는 단계를 추가로 포함한다. 핵 형성 온도는 당업자에 의해 용이하게 결정된다. 분당 약 2 내지 5℃로 핵 형성 온도에서부터 약 5℃까지 온도를 서서히 낮춘다. 다른 실시 형태는 더 큰 렐루골릭스 입자가 생성되는 것이다. 일 실시 형태에서, 교반하는 단계는 약 15 내지 18시간 동안 일어난다. 다른 실시 형태에서, 교반하는 단계는 더 짧은 기간 동안 일어난다. 다른 실시 형태는 침전물을 단리하는 단계를 추가로 포함한다. 다른 실시 형태는 추가적인 반용매를 사용하여 침전물의 단리를 촉진하는 단계를 추가로 포함한다. 다른 실시 형태는 추가적인 반용매를 사용하여 침전물을 세척하는 단계를 추가로 포함한다. 일 실시 형태에서, 단리하는 단계는 진공 여과에 의해 달성된다. 일 실시 형태는 침전물을 건조시키는 단계를 추가로 포함한다. 일 실시 형태에서, 건조시키는 단계는 약 45℃에서 진공 하에 수행된다. 일 실시 형태에서, 건조시키는 단계는 적어도 약 8시간 내지 하룻밤(약 16 내지 24시간) 동안 일어난다. 다른 실시 형태는 DMF에 렐루골릭스를 용해시킴으로써 DMF 중 렐루골릭스의 용액을 제조하는 단계를 추가로 포함한다. 일 실시 형태에서, 렐루골릭스는 주위 온도에서 DMF에 용해된다. 다른 실시 형태에서, 용해를 용이하게 하기 위해 열이 가해진다. 다른 실시 형태는 렐루골릭스와 DMF를 조합함으로써 DMF 중 렐루골릭스의 용액을 제조하는 단계를 추가로 포함하며, 여기서 렐루골릭스는 용액 중에서의 화학 반응에 의해, 예를 들어 탈보호에 의해 형성된다. 임의의 렐루골릭스가 그의 고체-상태 형태에 관계없이 DMF 중 렐루골릭스의 용액에 사용될 수 있다는 것이 당업자에게 명백할 것이다. 렐루골릭스의 순도에 따라, DMF 중 렐루골릭스의 용액을 제조하기 전에 임의의 또는 모든 다른 불순물을 제거하거나 물 추출에 의해 렐루골릭스로부터 임의의 또는 모든 원치 않는 염을 제거하는 것이 필요하거나 바람직할 수 있다.
다른 실시 형태에서, 무수 렐루골릭스의 형태 A는
a) 아세톤 중 렐루골릭스의 용액을 형성하는 단계로서, 렐루골릭스는 약 10배 부피의 아세톤(중량(g렐루골릭스):부피(mL아세톤)) 중에 있는, 상기 단계; 및
b) 무수 렐루골릭스의 형태 A를 침전물로서 산출하기 위해 아세톤 중 렐루골릭스의 용액을 교반하는 단계에 의해 제조된다.
일 실시 형태에서, 교반하는 단계는 약 5 내지 10분 동안 일어난다. 일 실시 형태는 아세톤 중 렐루골릭스의 용액을 형성하는 단계가 아세톤 중에 렐루골릭스를 용해시킴으로써 수행되는 것이다. 다른 실시 형태에서, 아세톤 중 렐루골릭스 용액을 형성하는 단계는 렐루골릭스와 아세톤을 조합함으로써 수행되며, 여기서, 렐루골릭스는 용액 중에서의 화학 반응에 의해, 예를 들어 탈보호에 의해 형성된다. 임의의 렐루골릭스가 그의 고체 상태 형태에 관계없이 아세톤 중 렐루골릭스의 용액을 형성하는 데 사용될 수 있으며, 아세톤 중 렐루골릭스의 용액을 형성하기 전에 임의의 또는 모든 다른 불순물을 제거하거나 물 추출에 의해 임의의 또는 모든 원치 않는 염을 제거하는 것이 바람직할 수 있음이 다시 당업자에게 명백할 것이다. 다른 실시 형태는 침전물을 단리하는 단계를 추가로 포함한다.
다른 실시 형태에서, 무수 렐루골릭스의 형태 B는
a) DCM 중 렐루골릭스의 용액을 형성하는 단계로서, 렐루골릭스는 약 20배 부피의 DCM(중량(g렐루골릭스):부피(mLDCM)) 중에 있는, 상기 단계; 및
b) 무수 렐루골릭스의 형태 B를 산출하기 위해 DCM을 증발시키는 단계에 의해 제조된다.
일 실시 형태는 DCM에 렐루골릭스를 용해시킴으로써 DCM 중 렐루골릭스의 용액을 제조하는 단계를 추가로 포함한다. 다른 실시 형태는 렐루골릭스와 DCM를 조합함으로써 DCM 중 렐루골릭스의 용액을 제조하는 단계를 추가로 포함하며, 여기서 렐루골릭스는 용액 중에서의 화학 반응에 의해, 예를 들어 탈보호에 의해 형성된다. 다른 실시 형태에서, DCM을 증발시키는 단계는 약 35℃에서 그리고 고진공 펌프 하에서 약 3시간 이상 동안 회전 증발기를 사용하여 수행된다. 임의의 렐루골릭스가 그의 고체-상태 형태에 관계없이 DCM 중 렐루골릭스의 용액에 사용될 수 있다는 것이 당업자에게 명백할 것이다. 렐루골릭스의 순도에 따라, DCM 중 렐루골릭스의 용액을 제조하기 전에 임의의 또는 모든 다른 불순물을 제거하거나 물 추출에 의해 렐루골릭스로부터 임의의 또는 모든 원치 않는 염을 제거하는 것이 필요하거나 바람직할 수 있다.
다른 실시 형태에서, 무수 렐루골릭스의 형태 B는
a) DCM 중 렐루골릭스의 용액을 반용매와 혼합하는 단계로서, 렐루골릭스는 적어도 약 20배 부피의 DCM(중량(g렐루골릭스):부피(mLDCM)) 중에 있고, 반용매는 약 1:1 비의 반용매 대 DCM(부피반용매:부피DCM)로 존재하는, 상기 단계;
b) 무수 렐루골릭스의 형태 B를 침전물로서 산출하기 위해 단계 a)의 혼합물을 일정 기간 동안 교반하는 단계에 의해 제조된다.
일 실시 형태는 DCM에 렐루골릭스를 용해시킴으로써 DCM 중 렐루골릭스의 용액을 제조하는 단계를 추가로 포함한다. 다른 실시 형태는 렐루골릭스와 DCM를 조합함으로써 DCM 중 렐루골릭스의 용액을 제조하는 단계를 추가로 포함하며, 여기서 렐루골릭스는 용액 중에서의 화학 반응에 의해, 예를 들어 탈보호에 의해 형성된다. 일 실시 형태에서, 교반하는 단계는 하룻밤(약 16 내지 24시간) 동안 일어난다. 일 실시 형태는 반용매와 혼합하기 전에 DCM 중 렐루골릭스의 용액을 소정 부피로 농축시키는 단계를 추가로 포함한다. 다양한 실시 형태에서, 반용매는 쿠멘, 사이클로헥산, TBME, 헵탄 또는 톨루엔이다. 임의의 렐루골릭스가 그의 고체-상태 형태에 관계없이 DCM 중 렐루골릭스의 용액에 사용될 수 있다는 것이 당업자에게 명백할 것이다. 렐루골릭스의 순도에 따라, DCM 중 렐루골릭스의 용액을 제조하기 전에 임의의 또는 모든 다른 불순물을 제거하거나 물 추출에 의해 렐루골릭스로부터 임의의 또는 모든 원치 않는 염을 제거하는 것이 필요하거나 바람직할 수 있다. 다른 실시 형태는 침전물을 단리하는 단계를 추가로 포함한다.
다른 실시 형태에서, 무수 렐루골릭스의 형태 C는
a) 무수 렐루골릭스의 형태 B에 약 10배 부피의 유기 용매(중량(g렐루골릭스):부피(mL유기 용매))를 첨가하는 단계; 및
b) 유기 용매와 무수 렐루골릭스의 형태 B의 혼합물을 하룻밤(약 16 내지 24시간) 동안 교반하여 무수 렐루골릭스의 형태 C의 슬러리를 생성하는 단계에 의해 제조된다.
일 실시 형태에서, 유기 용매는 아이소프로필 아세테이트 또는 2-부탄올이다. 일 실시 형태는 약 35 내지 40℃의 진공 오븐에서 하룻밤(약 16 내지 24시간) 동안 무수 렐루골릭스의 형태 C를 건조시키는 단계를 추가로 포함한다. 다른 실시 형태는 예를 들어, 경사분리(decanting) 또는 여과에 의해 슬러리로부터 무수 렐루골릭스의 형태 C를 단리하는 단계를 추가로 포함한다.
본 발명은 또한 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C, 및 약제학적으로 허용가능한 부형제를 포함하는 약제학적 조성물을 포함한다. 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C를 함유하는 약제학적 조성물은 미국 특허 제10,350,170호, 미국 특허 출원 공개 제2011/0172249호, 또는 당업계에 공지된 임의의 다른 방법에 따라 제조될 수 있다.
본 발명은 렐루골릭스의 DMF 용매화물의 형태 A, 또는 무수 렐루골릭스의 형태 A 또는 형태 C를 포함하는 약제학적 조성물을, 질환 치료를 필요로 하는 환자에게 투여함으로써 질환을 치료하는 방법을 제공한다. 렐루골릭스는 일본에서 자궁 섬유증의 치료에 대해 승인되었으며, 또한 자궁내막증 및 전립선암의 치료에 사용될 수 있다. 이는 하나 이상의 약제학적으로 허용가능한 제제, 예를 들어 저용량 에스트라디올 및 노르에틴드론 아세테이트와 조합하여 사용될 수 있다.
약제학적 조성물의 투여량은 넓은 범위에 걸쳐 달라질 수 있다. 투여되는 최적의 투여량 및 투여 요법은 당업자에 의해 용이하게 결정될 수 있으며, 투여 방식, 제제의 강도 및 질환 상태의 진행에 따라 달라질 것이다. 또한, 환자의 성별, 연령, 체중, 식이, 신체 활동, 투여 시간 및 수반되는 질환을 비롯한 치료되는 특정 환자와 관련된 요인으로 인해 투여량 및/또는 요법을 조정할 필요가 있을 것이다.
실시예
이하의 실시예 1 내지 실시예 4는 렐루골릭스의 DMF 용매화물의 형태 A, 및 무수 렐루골릭스의 형태 A, 형태 B 및 형태 C 각각의 제조의 실시 형태를 제공한다.
실시예는 당업자가 다양한 실시 형태를 제조하고 사용하는 것을 가능하게 하기 위해 제시된다. 구체적인 장치, 기술, 및 응용의 설명은 단지 예로서 제공된다. 본 명세서에 기재된 예에 대한 다양한 수정이 당업자에게 용이하게 명백할 것이며, 본 명세서에 기재된 일반적인 원리는 다양한 실시 형태의 사상 및 범위로부터 벗어남이 없이 다른 예 및 응용에 적용될 수 있다. 따라서, 다양한 실시 형태는 본 발명을 예시하는 것이며, 본 발명은 본 명세서에 기재되고 도시된 예에 한정되는 것으로 의도되지 않는다.
실시예 1
렐루골릭스의 DMF 용매화물의 형태 A의 제조
무수 렐루골릭스의 형태 B 1.63 g을 DMF(7.6 g, 8.2 mL)로 용해시킨다. 총 용액 중량(용매 + API)은 9.2 g이다. 해당 용액으로부터 동일한 양을 동일한 교반 속도(약 700 RPM)에서 동일한 크기/형상의 자기 교반 막대가 장착된 2개의 100 mL RB(둥근 바닥) 플라스크로 옮기며; 약 4.37 g의 DMF/API 용액(약 775 mg의 API)이 각 플라스크에 수용된다.
10.2 mL의 TBME(API의 중량(g)에 대해 약 13배 부피의 TBME(mL))를 한 플라스크에 첨가하고, 10.2 mL의 톨루엔(API의 중량(g)에 대해 약 13배 부피의 톨루엔(mL))을 두 번째 플라스크에 첨가한다. 각 플라스크의 내용물을 교반한다. TBME 플라스크에서는 처음 10분의 교반 내에 침전 징후가 나타난다. 톨루엔 플라스크에서는 다음 날에 침전 징후가 나타난다.
각 플라스크의 내용물을 종이 필터가 있는 부흐너 깔때기를 사용하여 별도로 진공 여과한다. 추가적인 TBME(2ㅧ4 mL)를 사용하여 TBME 플라스크 내의 모든 물질을 필터 상으로 옮긴다. 단리된 물질을 약 45℃에서 약 8시간 동안 진공 하에서 건조시킨다. 렐루골릭스의 DMF 용매화물의 형태 A 770 mg(단리 수율 89.5%)이 황색 고체로서 수득되며 이는 1:1 API 대 DMF 용매 비를 갖는다.
톨루엔 플라스크로부터 필터 상으로 물질을 옮기는 데에는 추가적인 톨루엔이 필요하지 않다. 단리된 물질을 약 45℃에서 약 8시간 동안 진공 하에서 건조시킨다. 렐루골릭스의 DMF 용매화물의 형태 A 694 mg(단리 수율 80.3%)이 황색 고체로서 수득되며 이는 1:1 API 대 DMF 용매 비를 갖는다.
렐루골릭스의 DMF 용매화물의 형태 A는 안정하며, 즉, 약 70℃에서 진공 하에서 장기간 건조(예를 들어, 약 2일) 후에 변하지 않는다. 그것은 또한 약 97% 습도 하에 주위 온도에서 1개월이 넘는 동안 변함없이 유지된다.
렐루골릭스의 DMF 용매화물의 형태 A의 XRPD 2θ 패턴 피크 및 피크에 대한 상대적인 %강도 값이 표 1에 나타나 있다.
[표 1]
각도 측정치는 ±0.2° 2θ이다. 렐루골릭스의 DMF 용매화물의 고체-상태 형태 A에 대한 핵심적인(key defining) 피크는 20.1, 24.3, 및 9.0° 2θ 중 둘 이상을 포함한다.
SCXRD에 의해 결정할 때 렐루골릭스의 DMF 용매화물의 형태 A에 대한 단결정 파라미터는 다음과 같다:
결정계: 삼사정계 공간군 P1
a = 11.1Å ± 1.5%
b = 12.0Å ± 1.5%
c = 14.0Å ± 1.5%
α = 112° ± 3°
β = 110° ± 3°
γ = 91° ± 3°
셀 부피: 1609 Å3 ± 3%
렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 샘플에 대한 XRPD 패턴(상부) 및 렐루골릭스의 DMF 용매화물의 형태 A의 단결정으로부터 계산된 XRPD 패턴(하부)이 도 1에 도시되어 있다.
SCXRD로부터 식별되는 렐루골릭스의 DMF 용매화물의 형태 A의 3차원 구조가 도 2에 도시되어 있다.
렐루골릭스의 DMF 용매화물의 형태 A의 DSC 분석은 도 3에 도시된 바와 같이 약 99℃에서의 흡열 이벤트의 개시 및 약 149℃에서의 급격한 흡열 이벤트를 나타내고, TGA 분석은 도 4에 도시된 바와 같이 약 155℃까지 약 6.7 중량%의 손실을 나타낸다.
렐루골릭스의 DMF 용매화물의 형태 A의 대표적인 DVS 플롯은 도 5에 도시된 바와 같이 약 90% RH에서 약 1% 질량의 손실을 나타낸다.
1H NMR 분석은 도 6에 도시된 바와 같이 렐루골릭스의 DMF 용매화물의 형태 A에서 DMF의 존재를 나타낸다.
실시예 2
무수 렐루골릭스의 형태 A의 제조
무수 렐루골릭스의 형태 B를 약 10배 부피의 아세톤(중량(g렐루골릭스):부피(mL아세톤))에 용해시킨다. 용액을 교반하며, 도 7에 포함된 XRPD 패턴에 의해 입증되는 바와 같이, 무수 렐루골릭스의 형태 A로서 약 5 내지 10분 내에 재결정화한다.
무수 렐루골릭스의 형태 A의 XRPD 2θ 패턴 피크 및 피크에 대한 상대적인 %강도 값이 표 2에 나타나 있다.
[표 2]
각도 측정치는 ±0.2° 2θ이다. 무수 렐루골릭스의 고체-상태 형태 A에 대한 핵심적인 피크는 10.7, 20.9, 및 19.2° 2θ 중 하나 이상을 포함한다. 일 실시 형태에서, 무수 렐루골릭스의 고체-상태 형태 A에 대한 핵심적인 피크는 10.7, 20.9, 및 19.2° 2θ 모두를 포함한다.
무수 렐루골릭스의 형태 A의 DSC 분석은 도 8에 도시된 바와 같이 약 158℃에서의 흡열 이벤트의 시작과 약 183℃에서의 흡열 이벤트를 나타낸다. TGA 분석은 도 9에 도시된 바와 같이 약 140℃까지 약 2.3 중량%의 손실을 나타낸다.
무수 렐루골릭스의 형태 A의 DVS 분석은, 샘플이 도 10에 도시된 바와 같이 약 0 내지 95%의 상대 습도 수준에 노출될 때 약 2%의 중량% 손실을 나타낸다.
1H NMR 분석은 도 11에 도시된 바와 같이 무수 렐루골릭스의 형태 A에서 2.13 ppm의 잔류 아세톤의 존재를 나타낸다.
무수 렐루골릭스의 형태 A는 DVS 후 XRPD 분석에 의해 입증된 바와 같이 다양한 습도 수준에서 안정하게 유지된다. 또한, XRPD는 진공 하에 약 30℃에서 약 18시간 동안 샘플을 건조시킨 후 변화를 나타내지 않는다.
실시예 3
무수 렐루골릭스의 형태 B의 제조
120 mL의 DCM을 8.2 g의 렐루골릭스에 첨가한다. 혼합물을 약 5분 동안 교반하여 슬러리를 생성한다. 약 100 mL의 물을 슬러리에 첨가하고 약 15분 동안 교반한다. 교반을 중단한 후, 일부 고체가 플라스크의 바닥에 남아 있고, 황색 유기 하부 층과 상부의 대부분 투명 내지 혼탁-투명한 수성 층을 갖는 이중층이 보인다. 이어서, 액체를 분별 깔때기 내에 경사분리한다. 100 mL의 DCM을 용해되지 않은 고체에 첨가하고 교반하여 슬러리를 형성한다. 100 mL의 물을 슬러리에 첨가하고, 약 15분 동안 교반하고, 액체를 분별 깔때기 내로 경사분리한다. 25 mL의 DCM을 임의의 용해되지 않은 고체에 첨가한다. 유기층을 진공 여과하여 임의의 잔류 고체를 제거한다. 가시적인 물방울을 제거하기 위해 건조제를 사용하지 않는다. 35℃에서 그리고 고진공 펌프 하에서 3시간 이상 동안 회전 증발기를 사용하여 유기층 내의 용매를 증발시킨다. 단리된 황색 고체(8.0 g, 97.6% 수율)는 무수 렐루골릭스의 형태 B로서 확인된다. 무수 렐루골릭스의 형태 B에 대한 대표적인 XRPD 패턴이 도 12에 나타나 있다.
무수 렐루골릭스의 형태 B의 XRPD 2θ 패턴 피크 및 피크에 대한 상대적인 %강도 값이 표 3에 나타나 있다.
[표 3]
각도 측정치는 ±0.2° 2θ이다. 무수 렐루골릭스의 고체 상태 형태 B에 대한 핵심적인 피크는 5.7° 2θ를 포함한다.
무수 렐루골릭스의 형태 B의 DSC 분석은 도 13에 도시된 바와 같이 약 79℃의 개시 온도에서의 용매의 손실 및 약 126℃에서의 흡열 이벤트의 시작과 약 145℃에서의 흡열 이벤트를 나타낸다. TGA 분석은 도 14에 도시된 바와 같이 약 105℃까지 약 6 중량% 초과의 손실을 나타낸다.
무수 렐루골릭스의 형태 B의 DVS 분석은, 도 15에 도시된 바와 같이 약 0 내지 95%의 상대 습도 수준에서 약 7%의 중량% 손실을 나타낸다.
무수 렐루골릭스의 형태 B의 1H NMR 분석은 이의 구조를 확인시켜 주며 도 16에 도시되어 있다.
무수 렐루골릭스의 형태 A는 DVS 후 XRPD에 의해 입증된 바와 같이 다양한 습도 수준에서 안정하게 유지된다.
실시예 4
무수 렐루골릭스의 형태 C의 제조
약 10 부피의 IPAc를 무수 렐루골릭스의 형태 B에 첨가한다(중량(g렐루골릭스):부피(mLIPAc)). 혼합물을 주위 온도에서 하룻밤 교반하여 슬러리를 생성한다. 슬러리를 경사분리하고, 단리된 물질을 약 35 내지 40℃의 진공 오븐에서 하룻밤 건조시키고 무수 렐루골릭스의 형태 C로서 확인한다.
무수 렐루골릭스의 형태 C의 XRPD 2θ 패턴 피크 및 피크에 대한 상대적인 %강도 값이 표 4에 나타나 있다.
[표 4]
각도 측정치는 ±0.2° 2θ이다. 무수 렐루골릭스의 고체-상태 형태 C에 대한 핵심적인 피크는 8.3, 6.8, 7.7, 및 19.9° 2θ 중 하나 이상을 포함한다. 일 실시 형태에서, 무수 렐루골릭스의 고체-상태 형태 C에 대한 핵심적인 피크는 8.3, 6.8, 7.7, 및 19.9° 2θ 모두를 포함한다.
무수 렐루골릭스의 형태 C에 대한 대표적인 XRPD 패턴이 도 17에 나타나 있다.
무수 렐루골릭스의 형태 C의 DSC 분석은 도 18에 도시된 바와 같이 약 140℃에서의 흡열 이벤트의 개시와 약 175℃에서의 흡열 이벤트를 나타낸다. TGA 분석은 도 19에 도시된 바와 같이 약 143℃까지 약 1% 미만의 중량 손실을 나타낸다.
무수 렐루골릭스의 형태 C의 DVS 분석은, 도 20에 도시된 바와 같이, 물질이 약 0 내지 약 95%의 상대 습도에 노출될 때, 약 2% 물 흡수 및 그 전체의 분비를 나타낸다.
1H NMR 분석은 도 21에 도시된 바와 같이 약 1.6 중량%에 해당하는 2 ppm(3H)의 아이소프로필 아세테이트의 존재를 나타낸다.
무수 렐루골릭스의 형태 C는 DVS 후 XRPD 분석에 의해 입증된 바와 같이 다양한 습도 수준에서 안정하게 유지된다.
상기 실시예는 본 발명의 이해를 돕기 위해 제시되며, 이하에 이어지는 청구범위에 기술된 개시 내용을 어떠한 방식으로든 제한하는 것으로 의도되지 않으며 제한하는 것으로 해석되어서는 안 된다.
Claims (30)
- 렐루골릭스(relugolix)의 DMF 용매화물.
- 제1항에 있어서, 렐루골릭스의 DMF 용매화물의 형태 A인, DMF 용매화물.
- 제2항에 있어서, 약 20.1, 24.3, 및 9.0° 2θ ± 0.2° 2θ로부터 선택되는 적어도 2개 이상의 X-선 분말 회절 피크를 갖는 것을 특징으로 하는, DMF 용매화물.
- 제2항에 있어서, 시차 주사 열량측정법에 의해 측정할 때 약 99℃ ± 3℃에서의 흡열 이벤트(event)의 개시를 특징으로 하는, DMF 용매화물.
- 제2항에 있어서, 시차 주사 열량측정법에 의해 측정할 때 약 149℃ ± 3℃에서의 흡열 이벤트를 특징으로 하는, DMF 용매화물.
- 제2항에 따른 DMF 용매화물의 제조 방법으로서,
a) DMF 중 렐루골릭스의 용액을 반용매(anti-solvent)와 혼합하는 단계; 및
b) 렐루골릭스의 상기 DMF 용매화물의 형태 A를 침전물로서 산출하기 위해 단계 a)의 혼합물을 교반하는 단계를 포함하는, 방법. - 제6항에 있어서, DMF 중 렐루골릭스의 상기 용액 내의 렐루골릭스 대 DMF의 비는 약 1:5의 중량(g렐루골릭스) 대 부피(mLDMF)인, 방법.
- 제6항에 있어서, 상기 반용매는 tert-부틸메틸 에테르 또는 톨루엔인, 방법.
- 제6항에 있어서, DMF 중 렐루골릭스의 상기 용액 내의 렐루골릭스 대 반용매의 비는 약 1:10 내지 약 1:13의 중량(g렐루골릭스) 대 부피(mL반용매)인, 방법.
- 제6항에 있어서, 상기 교반하는 단계는 약 15 내지 18시간 동안 일어나는, 방법.
- 제6항에 있어서, 침전물을 생성하기 위해 단계 a)의 혼합물을 교반하는 단계는 주위 온도에서 일어나는, 방법.
- 제2항에 있어서, 하기의 단결정 파라미터를 갖는, DMF 용매화물:
a = 11.1Å ± 1.5%
b = 12.0Å ± 1.5%
c = 14.0Å ± 1.5%
α = 112° ± 3°
β = 110° ± 3°
γ = 91° ± 3° - 제2항에 있어서, 약 1609 Å3 ± 3%의 셀 부피를 갖는, DMF 용매화물.
- 무수 렐루골릭스의 형태 A.
- 제14항에 있어서, 약 10.7, 20.9, 및 19.2° 2θ ± 0.2° 2θ로부터 선택되는 X-선 분말 회절 피크를 갖는 것을 특징으로 하는, 무수 렐루골릭스의 형태 A.
- 제14항에 있어서, 시차 주사 열량측정법에 의해 측정할 때 약 158℃ ± 3℃에서의 흡열 이벤트의 개시를 특징으로 하는, 무수 렐루골릭스의 형태 A.
- 제14항에 있어서, 시차 주사 열량측정법에 의해 측정할 때 약 183℃ ± 3℃에서의 흡열 이벤트를 특징으로 하는, 무수 렐루골릭스의 형태 A.
- 제14항에 따른 무수 렐루골릭스의 형태 A의 제조 방법으로서,
a) 아세톤 중 렐루골릭스의 용액을 형성하는 단계로서, 상기 렐루골릭스는 약 10배 부피의 아세톤(중량(g렐루골릭스):부피(mL아세톤)) 중에 있는, 상기 단계; 및
b) 무수 렐루골릭스의 형태 A를 침전물로서 산출하기 위해 아세톤 중 렐루골릭스의 상기 용액을 교반하는 단계를 포함하는, 방법. - 약 5.7° 2θ ± 0.2° 2θ에서 X-선 분말 회절 피크를 갖는 것을 특징으로 하는 무수 렐루골릭스의 형태 B의 제조 방법으로서,
a) DCM 중 렐루골릭스의 용액을 형성하는 단계로서, 상기 렐루골릭스는 약 20배 부피의 DCM(중량(g렐루골릭스):부피(mLDCM)) 중에 있는, 상기 단계; 및
b) 무수 렐루골릭스의 형태 B를 산출하기 위해 상기 DCM을 증발시키는 단계를 포함하는, 방법. - 약 5.7° 2θ ± 0.2° 2θ에서 X-선 분말 회절 피크를 갖는 것을 특징으로 하는 무수 렐루골릭스의 형태 B의 제조 방법으로서,
a) DCM 중 렐루골릭스의 용액을 반용매와 혼합하는 단계로서, 상기 렐루골릭스는 적어도 약 20배 부피의 DCM(중량(g렐루골릭스):부피(mLDCM)) 중에 있고, 상기 반용매는 약 1:1 비의 반용매 대 DCM(부피반용매:부피DCM)으로 존재하는, 상기 단계;
b) 무수 렐루골릭스의 형태 B를 침전물로서 산출하기 위해 단계 a)의 혼합물을 일정 기간 동안 교반하는 단계를 포함하는, 방법. - 제20항에 있어서, 상기 반용매는 쿠멘, 사이클로헥산, TBME, 헵탄 또는 톨루엔인, 방법.
- 무수 렐루골릭스의 형태 C.
- 제22항에 있어서, 약 8.3, 6.8, 7.7, 및 19.9° 2θ ± 0.2° 2θ로부터 선택되는 X-선 분말 회절 피크를 갖는 것을 특징으로 하는, 무수 렐루골릭스의 형태 C.
- 제22항에 있어서, 시차 주사 열량측정법에 의해 측정할 때 약 140℃ ± 3℃에서의 흡열 이벤트의 개시를 특징으로 하는, 무수 렐루골릭스의 형태 C.
- 제22항에 있어서, 시차 주사 열량측정법에 의해 측정할 때 약 175℃ ± 3℃에서의 흡열 이벤트를 특징으로 하는, 무수 렐루골릭스의 형태 C.
- 제22항에 따른 무수 렐루골릭스의 형태 C의 제조 방법으로서,
a) 무수 렐루골릭스의 형태 B에 약 10배 부피의 유기 용매(중량(g렐루골릭스):부피(mL유기 용매))를 첨가하는 단계; 및
b) 유기 용매와 무수 렐루골릭스의 형태 B의 혼합물을 약 16 내지 24시간 동안 교반하여 무수 렐루골릭스의 형태 C의 슬러리를 생성하는 단계를 포함하는, 방법. - 제26항에 있어서, 상기 유기 용매는 아이소프로필 아세테이트 또는 2-부탄올인, 방법.
- 제1항에 따른 렐루골릭스의 DMF 용매화물, 제14항에 따른 무수 렐루골릭스의 형태 A, 및 제22항에 따른 무수 렐루골릭스의 형태 C로부터 선택되는 화합물의 약제학적 유효량, 및 약제학적으로 허용가능한 부형제를 포함하는, 약제학적 조성물.
- 질환 치료를 필요로 하는 환자에게 제28항에 따른 약제학적 조성물을 투여하는 단계를 포함하는, 환자에서 질환을 치료하는 방법.
- 제29항에 있어서, 상기 질환은 자궁 섬유증, 자궁내막증, 또는 전립선암인, 질환을 치료하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962882297P | 2019-08-02 | 2019-08-02 | |
| US62/882,297 | 2019-08-02 | ||
| PCT/US2020/044553 WO2021026011A1 (en) | 2019-08-02 | 2020-07-31 | Solid-state forms of relugolix |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220047972A true KR20220047972A (ko) | 2022-04-19 |
Family
ID=72145496
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227003478A KR20220047972A (ko) | 2019-08-02 | 2020-07-31 | 렐루골릭스의 고체-상태 형태 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20230374030A1 (ko) |
| EP (1) | EP4007760A1 (ko) |
| JP (1) | JP2022542159A (ko) |
| KR (1) | KR20220047972A (ko) |
| CN (1) | CN114174302A (ko) |
| BR (1) | BR112022001002A2 (ko) |
| CA (1) | CA3145993A1 (ko) |
| WO (1) | WO2021026011A1 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113620972A (zh) * | 2021-02-02 | 2021-11-09 | 奥锐特药业(天津)有限公司 | 瑞卢戈利新晶型及其制备方法 |
| CN114031626A (zh) * | 2021-12-09 | 2022-02-11 | 成都科圣原医药科技有限公司 | 一种瑞卢戈利的合成方法 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2004207706B2 (en) * | 2003-01-29 | 2010-03-04 | Takeda Pharmaceutical Company Limited | Thienopyrimidine compounds and use thereof |
| WO2010026993A1 (ja) | 2008-09-03 | 2010-03-11 | 武田薬品工業株式会社 | 製剤における吸収性改善方法および吸収性が改善された製剤 |
| EP2900675B1 (en) * | 2012-09-28 | 2019-03-06 | Takeda Pharmaceutical Company Limited | Production method of thienopyrimidine derivative |
| HUE062269T2 (hu) | 2015-02-26 | 2023-10-28 | Takeda Pharmaceuticals Co | Metoxikarbamid-származékot és mannit részecskéket tartalmazó tabletta |
| WO2019178304A1 (en) | 2018-03-14 | 2019-09-19 | Teva Pharmaceuticals International Gmbh | Solid state forms of relugolix |
| EP3666776A1 (en) * | 2018-12-11 | 2020-06-17 | Sandoz AG | Hydrate of a gonadotropin-releasing hormone receptor antagonist |
-
2020
- 2020-07-31 CA CA3145993A patent/CA3145993A1/en active Pending
- 2020-07-31 CN CN202080054641.9A patent/CN114174302A/zh active Pending
- 2020-07-31 JP JP2022505338A patent/JP2022542159A/ja active Pending
- 2020-07-31 KR KR1020227003478A patent/KR20220047972A/ko unknown
- 2020-07-31 WO PCT/US2020/044553 patent/WO2021026011A1/en unknown
- 2020-07-31 US US17/597,998 patent/US20230374030A1/en active Pending
- 2020-07-31 BR BR112022001002A patent/BR112022001002A2/pt not_active Application Discontinuation
- 2020-07-31 EP EP20758031.7A patent/EP4007760A1/en not_active Withdrawn
Also Published As
| Publication number | Publication date |
|---|---|
| CN114174302A (zh) | 2022-03-11 |
| JP2022542159A (ja) | 2022-09-29 |
| EP4007760A1 (en) | 2022-06-08 |
| BR112022001002A2 (pt) | 2022-04-12 |
| US20230374030A1 (en) | 2023-11-23 |
| WO2021026011A1 (en) | 2021-02-11 |
| CA3145993A1 (en) | 2021-02-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN105131003B (zh) | 6,7‑不饱和‑7‑氨基甲酰基吗啡喃衍生物的晶体及其制备方法 | |
| KR20160121544A (ko) | N-{4-[(6,7-다이메톡시퀴놀린-4-일)옥시]페닐}-n''-(4-플루오로페닐) 사이클로프로판-1,1-다이카복스아마이드의 결정질 고체 형태, 제조 방법 및 사용 방법 | |
| EP3969449A1 (en) | New crystalline forms of n-(3-(2-(2-hydroxyethoxy)-6-morpholinopyridin-4-yl)-4-methvlphenyl)-2 (trifluoromethyl)isonicotinamide as raf inhibitors for the treatment of cancer | |
| WO2022121670A1 (zh) | Tolebrutinib的晶型及其制备方法和用途 | |
| WO2018059556A1 (zh) | 激酶抑制剂化合物的多晶型、含其的药物组合物及其制备方法和应用 | |
| KR20190093651A (ko) | ((5-(3-클로로페닐)-3-하이드록시피리딘-2-카보닐)아미노)아세트산의 신규한 결정질 형태 및 이의 제조 방법 | |
| HUE035608T2 (en) | Pharmaceutical compositions containing crystalline forms of (R) -7-chloro-N- (quinuclidin-3-yl) benzo (b) thiophene-2-carboxamide hydrochloride monohydrate | |
| KR20220047972A (ko) | 렐루골릭스의 고체-상태 형태 | |
| CZ2015110A3 (cs) | Pevné formy empagliflozinu | |
| US10793521B2 (en) | Crystalline form II of dextral oxiracetam, preparation method therefor and use thereof | |
| JP2022522395A (ja) | 選択的エストロゲン受容体分解剤の新規な塩 | |
| US20210094961A1 (en) | Form of ponatinib | |
| TWI662031B (zh) | 1-{2-氟-4-[5-(4-異丁基苯基)-1,2,4-噁二唑-3-基]-苄基}-3-吖丁啶羧酸的晶型 | |
| KR101285050B1 (ko) | 결정형 1H-이미다조[4,5-b]피리딘-5-아민,7-[5-[(시클로헥실메틸아미노)-메틸]-1H-인돌-2-일]-2-메틸, 설페이트 (1:1), 삼수화물 및 이의 약학적 용도 | |
| CN113149998B (zh) | 2-吲哚啉螺环酮类化合物或其盐、溶剂合物的无定形形式或结晶形式 | |
| US20210395232A1 (en) | Co-crystal forms of selinexor | |
| US11306062B2 (en) | Forms of fedratinib dihydrochloride | |
| US20210246159A1 (en) | Novel form of bardoxolone methyl | |
| WO2022143897A1 (zh) | A-失碳-5α雄甾烷化合物的多晶型物 | |
| JP2019529389A (ja) | ムスカリン性アセチルコリン受容体アゴニストの結晶性多形 | |
| TW202140493A (zh) | 2-吲哚啉螺環酮類化合物或其鹽、溶劑錯合物之非晶形式或結晶形式 | |
| WO2019070698A1 (en) | NEW FORMS OF IBRUTINIB | |
| WO2021176216A1 (en) | Salts and polymorphic forms of 6-chloro-7-(4-(4-chlorobenzyl)piperazin-1-yl)-2-(1,3-dimethyl-1h-pyrazol-4-yl)-3h-imidazo[4,5-b]pyridine | |
| WO2011077252A2 (en) | Metaxalone cocrystals | |
| JP2020513006A (ja) | アファチニブジマレアートの新規形態 |