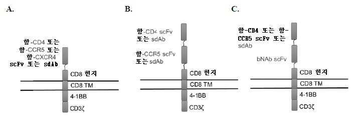
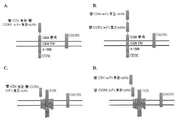
KR20210031898A - 전염병을 치료하기 위한 공동수용체 시스템 - Google Patents
전염병을 치료하기 위한 공동수용체 시스템 Download PDFInfo
- Publication number
- KR20210031898A KR20210031898A KR1020217000571A KR20217000571A KR20210031898A KR 20210031898 A KR20210031898 A KR 20210031898A KR 1020217000571 A KR1020217000571 A KR 1020217000571A KR 20217000571 A KR20217000571 A KR 20217000571A KR 20210031898 A KR20210031898 A KR 20210031898A
- Authority
- KR
- South Korea
- Prior art keywords
- cells
- domain
- engineered immune
- immune cell
- cell
- Prior art date
Links
- 208000035473 Communicable disease Diseases 0.000 title claims description 14
- 108700010039 chimeric receptor Proteins 0.000 claims abstract description 555
- 210000002865 immune cell Anatomy 0.000 claims abstract description 364
- 210000001744 T-lymphocyte Anatomy 0.000 claims abstract description 139
- 239000000427 antigen Substances 0.000 claims description 362
- 108091007433 antigens Proteins 0.000 claims description 360
- 102000036639 antigens Human genes 0.000 claims description 360
- 230000027455 binding Effects 0.000 claims description 338
- 150000007523 nucleic acids Chemical class 0.000 claims description 274
- 210000004027 cell Anatomy 0.000 claims description 256
- 102000039446 nucleic acids Human genes 0.000 claims description 239
- 108020004707 nucleic acids Proteins 0.000 claims description 239
- 230000003834 intracellular effect Effects 0.000 claims description 142
- 101710149870 C-C chemokine receptor type 5 Proteins 0.000 claims description 138
- 102100035875 C-C chemokine receptor type 5 Human genes 0.000 claims description 138
- 238000000034 method Methods 0.000 claims description 120
- 230000014509 gene expression Effects 0.000 claims description 103
- 230000011664 signaling Effects 0.000 claims description 102
- 241000282414 Homo sapiens Species 0.000 claims description 87
- 102100031650 C-X-C chemokine receptor type 4 Human genes 0.000 claims description 62
- 101000922348 Homo sapiens C-X-C chemokine receptor type 4 Proteins 0.000 claims description 61
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 60
- 239000008194 pharmaceutical composition Substances 0.000 claims description 54
- 230000000139 costimulatory effect Effects 0.000 claims description 53
- 102100031658 C-X-C chemokine receptor type 5 Human genes 0.000 claims description 50
- 101000922405 Homo sapiens C-X-C chemokine receptor type 5 Proteins 0.000 claims description 49
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 claims description 45
- 230000003472 neutralizing effect Effects 0.000 claims description 32
- 101000946860 Homo sapiens T-cell surface glycoprotein CD3 epsilon chain Proteins 0.000 claims description 27
- 102100035794 T-cell surface glycoprotein CD3 epsilon chain Human genes 0.000 claims description 27
- 241000700605 Viruses Species 0.000 claims description 24
- 206010028980 Neoplasm Diseases 0.000 claims description 23
- 230000004068 intracellular signaling Effects 0.000 claims description 23
- -1 α4β7 Proteins 0.000 claims description 23
- 208000015181 infectious disease Diseases 0.000 claims description 19
- 108091033409 CRISPR Proteins 0.000 claims description 15
- 239000013603 viral vector Substances 0.000 claims description 13
- 101150017501 CCR5 gene Proteins 0.000 claims description 12
- 201000011510 cancer Diseases 0.000 claims description 12
- 238000004519 manufacturing process Methods 0.000 claims description 11
- 108020004459 Small interfering RNA Proteins 0.000 claims description 10
- 238000010459 TALEN Methods 0.000 claims description 9
- 210000001266 CD8-positive T-lymphocyte Anatomy 0.000 claims description 8
- 238000010354 CRISPR gene editing Methods 0.000 claims description 8
- 108010043645 Transcription Activator-Like Effector Nucleases Proteins 0.000 claims description 8
- 230000036436 anti-hiv Effects 0.000 claims description 8
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 claims description 8
- 210000002443 helper t lymphocyte Anatomy 0.000 claims description 8
- 210000000581 natural killer T-cell Anatomy 0.000 claims description 7
- 230000004927 fusion Effects 0.000 claims description 6
- 210000000822 natural killer cell Anatomy 0.000 claims description 5
- 102100022718 Atypical chemokine receptor 2 Human genes 0.000 claims description 4
- 101000678892 Homo sapiens Atypical chemokine receptor 2 Proteins 0.000 claims description 4
- 108020005544 Antisense RNA Proteins 0.000 claims description 3
- 206010042971 T-cell lymphoma Diseases 0.000 claims description 3
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 claims description 3
- 239000003184 complementary RNA Substances 0.000 claims description 3
- 230000001086 cytosolic effect Effects 0.000 claims description 3
- 239000003937 drug carrier Substances 0.000 claims description 3
- 210000005259 peripheral blood Anatomy 0.000 claims description 3
- 239000011886 peripheral blood Substances 0.000 claims description 3
- 230000036039 immunity Effects 0.000 claims description 2
- 230000000415 inactivating effect Effects 0.000 claims description 2
- 230000002401 inhibitory effect Effects 0.000 claims description 2
- 101000716070 Homo sapiens C-C chemokine receptor type 9 Proteins 0.000 claims 2
- 241000598436 Human T-cell lymphotropic virus Species 0.000 claims 1
- 229960005475 antiinfective agent Drugs 0.000 claims 1
- 239000004599 antimicrobial Substances 0.000 claims 1
- 239000002246 antineoplastic agent Substances 0.000 claims 1
- 108091008034 costimulatory receptors Proteins 0.000 description 126
- 108091008874 T cell receptors Proteins 0.000 description 123
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 118
- 108090000623 proteins and genes Proteins 0.000 description 87
- 230000001939 inductive effect Effects 0.000 description 65
- 239000013598 vector Substances 0.000 description 62
- 101000946843 Homo sapiens T-cell surface glycoprotein CD8 alpha chain Proteins 0.000 description 44
- 102100034922 T-cell surface glycoprotein CD8 alpha chain Human genes 0.000 description 44
- 102000004196 processed proteins & peptides Human genes 0.000 description 43
- 229920001184 polypeptide Polymers 0.000 description 41
- 102000004169 proteins and genes Human genes 0.000 description 39
- 235000018102 proteins Nutrition 0.000 description 37
- 241000725303 Human immunodeficiency virus Species 0.000 description 35
- 239000000203 mixture Substances 0.000 description 35
- 108060003951 Immunoglobulin Proteins 0.000 description 31
- 102000018358 immunoglobulin Human genes 0.000 description 31
- 239000012634 fragment Substances 0.000 description 30
- 239000003446 ligand Substances 0.000 description 29
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 27
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 27
- 235000001014 amino acid Nutrition 0.000 description 27
- 101000851370 Homo sapiens Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 description 25
- 102100036856 Tumor necrosis factor receptor superfamily member 9 Human genes 0.000 description 25
- 108091028043 Nucleic acid sequence Proteins 0.000 description 24
- 125000003275 alpha amino acid group Chemical group 0.000 description 23
- 239000003795 chemical substances by application Substances 0.000 description 21
- 238000006467 substitution reaction Methods 0.000 description 20
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 19
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 19
- 239000011324 bead Substances 0.000 description 19
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 19
- 102000005962 receptors Human genes 0.000 description 19
- 108020003175 receptors Proteins 0.000 description 19
- 108020004414 DNA Proteins 0.000 description 18
- 201000010099 disease Diseases 0.000 description 18
- 229940024606 amino acid Drugs 0.000 description 17
- 150000001413 amino acids Chemical group 0.000 description 17
- 230000000694 effects Effects 0.000 description 16
- 230000001225 therapeutic effect Effects 0.000 description 16
- 150000002632 lipids Chemical class 0.000 description 15
- 210000004962 mammalian cell Anatomy 0.000 description 15
- 239000000546 pharmaceutical excipient Substances 0.000 description 15
- 230000001105 regulatory effect Effects 0.000 description 15
- 238000011282 treatment Methods 0.000 description 15
- 238000004458 analytical method Methods 0.000 description 14
- 210000004408 hybridoma Anatomy 0.000 description 14
- 210000004698 lymphocyte Anatomy 0.000 description 14
- 108700019146 Transgenes Proteins 0.000 description 13
- 239000000872 buffer Substances 0.000 description 13
- 238000001727 in vivo Methods 0.000 description 13
- 230000003612 virological effect Effects 0.000 description 13
- 241000699670 Mus sp. Species 0.000 description 12
- 229940079593 drug Drugs 0.000 description 12
- 239000003814 drug Substances 0.000 description 12
- 239000000243 solution Substances 0.000 description 12
- 108091007741 Chimeric antigen receptor T cells Proteins 0.000 description 11
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 11
- 102100024952 Protein CBFA2T1 Human genes 0.000 description 11
- 108010003723 Single-Domain Antibodies Proteins 0.000 description 11
- 230000004913 activation Effects 0.000 description 11
- 210000003719 b-lymphocyte Anatomy 0.000 description 11
- 210000004899 c-terminal region Anatomy 0.000 description 11
- 239000013604 expression vector Substances 0.000 description 11
- 238000000338 in vitro Methods 0.000 description 11
- 239000004055 small Interfering RNA Substances 0.000 description 11
- 239000000126 substance Substances 0.000 description 11
- 230000008685 targeting Effects 0.000 description 11
- 241001465754 Metazoa Species 0.000 description 10
- 108700008625 Reporter Genes Proteins 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 230000001419 dependent effect Effects 0.000 description 10
- 238000010586 diagram Methods 0.000 description 10
- 238000009472 formulation Methods 0.000 description 10
- 210000000987 immune system Anatomy 0.000 description 10
- 239000002502 liposome Substances 0.000 description 10
- 238000002823 phage display Methods 0.000 description 10
- 102000040430 polynucleotide Human genes 0.000 description 10
- 108091033319 polynucleotide Proteins 0.000 description 10
- 239000002157 polynucleotide Substances 0.000 description 10
- 108010002350 Interleukin-2 Proteins 0.000 description 9
- 102000000588 Interleukin-2 Human genes 0.000 description 9
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 9
- 230000006044 T cell activation Effects 0.000 description 9
- 239000008280 blood Substances 0.000 description 9
- 230000005754 cellular signaling Effects 0.000 description 9
- 230000006870 function Effects 0.000 description 9
- 229940072221 immunoglobulins Drugs 0.000 description 9
- 239000007924 injection Substances 0.000 description 9
- 238000002347 injection Methods 0.000 description 9
- 108020004999 messenger RNA Proteins 0.000 description 9
- 210000004990 primary immune cell Anatomy 0.000 description 9
- 230000008569 process Effects 0.000 description 9
- 241000701161 unidentified adenovirus Species 0.000 description 9
- 241000699666 Mus <mouse, genus> Species 0.000 description 8
- 102100022153 Tumor necrosis factor receptor superfamily member 4 Human genes 0.000 description 8
- 230000004075 alteration Effects 0.000 description 8
- 230000016784 immunoglobulin production Effects 0.000 description 8
- 230000006698 induction Effects 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- 230000020382 suppression by virus of host antigen processing and presentation of peptide antigen via MHC class I Effects 0.000 description 8
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 7
- 108050005493 CD3 protein, epsilon/gamma/delta subunit Proteins 0.000 description 7
- 241000713666 Lentivirus Species 0.000 description 7
- 210000004443 dendritic cell Anatomy 0.000 description 7
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 7
- 239000001963 growth medium Substances 0.000 description 7
- 230000001965 increasing effect Effects 0.000 description 7
- 230000035772 mutation Effects 0.000 description 7
- 238000004091 panning Methods 0.000 description 7
- 238000003752 polymerase chain reaction Methods 0.000 description 7
- 238000003127 radioimmunoassay Methods 0.000 description 7
- 241000894007 species Species 0.000 description 7
- 241001430294 unidentified retrovirus Species 0.000 description 7
- 102100027207 CD27 antigen Human genes 0.000 description 6
- 102100035793 CD83 antigen Human genes 0.000 description 6
- 102000004127 Cytokines Human genes 0.000 description 6
- 108090000695 Cytokines Proteins 0.000 description 6
- 241000701022 Cytomegalovirus Species 0.000 description 6
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 description 6
- 101000946856 Homo sapiens CD83 antigen Proteins 0.000 description 6
- 101001109503 Homo sapiens NKG2-C type II integral membrane protein Proteins 0.000 description 6
- 108010064548 Lymphocyte Function-Associated Antigen-1 Proteins 0.000 description 6
- 102100022683 NKG2-C type II integral membrane protein Human genes 0.000 description 6
- 102100021669 Stromal cell-derived factor 1 Human genes 0.000 description 6
- 108010017070 Zinc Finger Nucleases Proteins 0.000 description 6
- 239000012636 effector Substances 0.000 description 6
- 238000005516 engineering process Methods 0.000 description 6
- 238000003209 gene knockout Methods 0.000 description 6
- 238000010362 genome editing Methods 0.000 description 6
- 238000011534 incubation Methods 0.000 description 6
- 238000003780 insertion Methods 0.000 description 6
- 230000037431 insertion Effects 0.000 description 6
- 230000010354 integration Effects 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 210000000936 intestine Anatomy 0.000 description 6
- 230000004048 modification Effects 0.000 description 6
- 238000012986 modification Methods 0.000 description 6
- 239000002773 nucleotide Substances 0.000 description 6
- 125000003729 nucleotide group Chemical group 0.000 description 6
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- 239000003419 rna directed dna polymerase inhibitor Substances 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 6
- 238000013518 transcription Methods 0.000 description 6
- 230000035897 transcription Effects 0.000 description 6
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 5
- QRKPLLLQZJCOLR-UHFFFAOYSA-N 6-[2-(4-carboxybut-2-enyl)-3-hydroxy-5-oxocyclopentyl]-4-oxohexanoic acid Chemical compound OC1CC(=O)C(CCC(=O)CCC(O)=O)C1CC=CCC(O)=O QRKPLLLQZJCOLR-UHFFFAOYSA-N 0.000 description 5
- 102100032937 CD40 ligand Human genes 0.000 description 5
- 108010004889 Heat-Shock Proteins Proteins 0.000 description 5
- 102000002812 Heat-Shock Proteins Human genes 0.000 description 5
- 241000282412 Homo Species 0.000 description 5
- 101000868215 Homo sapiens CD40 ligand Proteins 0.000 description 5
- 101000679851 Homo sapiens Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 description 5
- 229940122313 Nucleoside reverse transcriptase inhibitor Drugs 0.000 description 5
- 239000004098 Tetracycline Substances 0.000 description 5
- 230000000890 antigenic effect Effects 0.000 description 5
- 230000008901 benefit Effects 0.000 description 5
- 210000001185 bone marrow Anatomy 0.000 description 5
- 238000004113 cell culture Methods 0.000 description 5
- 238000002648 combination therapy Methods 0.000 description 5
- 230000000977 initiatory effect Effects 0.000 description 5
- 239000000693 micelle Substances 0.000 description 5
- 230000005012 migration Effects 0.000 description 5
- 238000013508 migration Methods 0.000 description 5
- 210000001616 monocyte Anatomy 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 230000035755 proliferation Effects 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 230000005855 radiation Effects 0.000 description 5
- 230000010076 replication Effects 0.000 description 5
- 230000001177 retroviral effect Effects 0.000 description 5
- 150000003384 small molecules Chemical group 0.000 description 5
- 239000003381 stabilizer Substances 0.000 description 5
- 229960002180 tetracycline Drugs 0.000 description 5
- 229930101283 tetracycline Natural products 0.000 description 5
- 235000019364 tetracycline Nutrition 0.000 description 5
- 150000003522 tetracyclines Chemical class 0.000 description 5
- 230000002103 transcriptional effect Effects 0.000 description 5
- 238000001890 transfection Methods 0.000 description 5
- 238000012546 transfer Methods 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- SGKRLCUYIXIAHR-AKNGSSGZSA-N (4s,4ar,5s,5ar,6r,12ar)-4-(dimethylamino)-1,5,10,11,12a-pentahydroxy-6-methyl-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1=CC=C2[C@H](C)[C@@H]([C@H](O)[C@@H]3[C@](C(O)=C(C(N)=O)C(=O)[C@H]3N(C)C)(O)C3=O)C3=C(O)C2=C1O SGKRLCUYIXIAHR-AKNGSSGZSA-N 0.000 description 4
- 208000030507 AIDS Diseases 0.000 description 4
- 102100038080 B-cell receptor CD22 Human genes 0.000 description 4
- 102100032367 C-C motif chemokine 5 Human genes 0.000 description 4
- 108091026890 Coding region Proteins 0.000 description 4
- 230000004568 DNA-binding Effects 0.000 description 4
- 241000702421 Dependoparvovirus Species 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 4
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- 102000003886 Glycoproteins Human genes 0.000 description 4
- 108090000288 Glycoproteins Proteins 0.000 description 4
- 108020005004 Guide RNA Proteins 0.000 description 4
- 208000031886 HIV Infections Diseases 0.000 description 4
- 208000037357 HIV infectious disease Diseases 0.000 description 4
- 101000884305 Homo sapiens B-cell receptor CD22 Proteins 0.000 description 4
- 101000979342 Homo sapiens Nuclear factor NF-kappa-B p105 subunit Proteins 0.000 description 4
- 101000934341 Homo sapiens T-cell surface glycoprotein CD5 Proteins 0.000 description 4
- 101000801234 Homo sapiens Tumor necrosis factor receptor superfamily member 18 Proteins 0.000 description 4
- 101000851376 Homo sapiens Tumor necrosis factor receptor superfamily member 8 Proteins 0.000 description 4
- 108091006905 Human Serum Albumin Proteins 0.000 description 4
- 102000008100 Human Serum Albumin Human genes 0.000 description 4
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 4
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 4
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 4
- 102100034349 Integrase Human genes 0.000 description 4
- 241000829100 Macaca mulatta polyomavirus 1 Species 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 241001529936 Murinae Species 0.000 description 4
- 238000000636 Northern blotting Methods 0.000 description 4
- 102100023050 Nuclear factor NF-kappa-B p105 subunit Human genes 0.000 description 4
- 101710163270 Nuclease Proteins 0.000 description 4
- 206010035226 Plasma cell myeloma Diseases 0.000 description 4
- 101710088580 Stromal cell-derived factor 1 Proteins 0.000 description 4
- 230000024932 T cell mediated immunity Effects 0.000 description 4
- 102100025244 T-cell surface glycoprotein CD5 Human genes 0.000 description 4
- 102100033728 Tumor necrosis factor receptor superfamily member 18 Human genes 0.000 description 4
- 102100036857 Tumor necrosis factor receptor superfamily member 8 Human genes 0.000 description 4
- 208000036142 Viral infection Diseases 0.000 description 4
- 125000000539 amino acid group Chemical group 0.000 description 4
- 210000000612 antigen-presenting cell Anatomy 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 230000009286 beneficial effect Effects 0.000 description 4
- 230000004071 biological effect Effects 0.000 description 4
- 239000011575 calcium Substances 0.000 description 4
- 231100000433 cytotoxic Toxicity 0.000 description 4
- 230000001472 cytotoxic effect Effects 0.000 description 4
- 238000012217 deletion Methods 0.000 description 4
- 230000037430 deletion Effects 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 238000006471 dimerization reaction Methods 0.000 description 4
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 4
- 229960003722 doxycycline Drugs 0.000 description 4
- 210000003979 eosinophil Anatomy 0.000 description 4
- 150000004676 glycans Chemical class 0.000 description 4
- 235000011187 glycerol Nutrition 0.000 description 4
- 230000012010 growth Effects 0.000 description 4
- 239000000833 heterodimer Substances 0.000 description 4
- 208000033519 human immunodeficiency virus infectious disease Diseases 0.000 description 4
- 230000001900 immune effect Effects 0.000 description 4
- 230000003053 immunization Effects 0.000 description 4
- 210000001165 lymph node Anatomy 0.000 description 4
- 210000002540 macrophage Anatomy 0.000 description 4
- 230000001404 mediated effect Effects 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 4
- 201000000050 myeloid neoplasm Diseases 0.000 description 4
- 239000002953 phosphate buffered saline Substances 0.000 description 4
- 239000003755 preservative agent Substances 0.000 description 4
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 210000003289 regulatory T cell Anatomy 0.000 description 4
- 238000003757 reverse transcription PCR Methods 0.000 description 4
- 239000000523 sample Substances 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- 210000000952 spleen Anatomy 0.000 description 4
- 150000005846 sugar alcohols Chemical class 0.000 description 4
- 239000006228 supernatant Substances 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 230000014616 translation Effects 0.000 description 4
- 210000004881 tumor cell Anatomy 0.000 description 4
- 230000009385 viral infection Effects 0.000 description 4
- 238000001262 western blot Methods 0.000 description 4
- 102100023990 60S ribosomal protein L17 Human genes 0.000 description 3
- 206010003445 Ascites Diseases 0.000 description 3
- 108700012434 CCL3 Proteins 0.000 description 3
- 102100038078 CD276 antigen Human genes 0.000 description 3
- 101710185679 CD276 antigen Proteins 0.000 description 3
- 101150013553 CD40 gene Proteins 0.000 description 3
- 108091008928 CXC chemokine receptors Proteins 0.000 description 3
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- 102000000013 Chemokine CCL3 Human genes 0.000 description 3
- 108010055165 Chemokine CCL4 Proteins 0.000 description 3
- 102000001326 Chemokine CCL4 Human genes 0.000 description 3
- 108010055166 Chemokine CCL5 Proteins 0.000 description 3
- 102000009410 Chemokine receptor Human genes 0.000 description 3
- 108050000299 Chemokine receptor Proteins 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- 229920002307 Dextran Polymers 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 102100031351 Galectin-9 Human genes 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 3
- 108010007712 Hepatitis A Virus Cellular Receptor 1 Proteins 0.000 description 3
- 102100034459 Hepatitis A virus cellular receptor 1 Human genes 0.000 description 3
- 101100005713 Homo sapiens CD4 gene Proteins 0.000 description 3
- 101001130151 Homo sapiens Galectin-9 Proteins 0.000 description 3
- 101000935040 Homo sapiens Integrin beta-2 Proteins 0.000 description 3
- 101000934338 Homo sapiens Myeloid cell surface antigen CD33 Proteins 0.000 description 3
- 101000648507 Homo sapiens Tumor necrosis factor receptor superfamily member 14 Proteins 0.000 description 3
- 108010091358 Hypoxanthine Phosphoribosyltransferase Proteins 0.000 description 3
- 102100029098 Hypoxanthine-guanine phosphoribosyltransferase Human genes 0.000 description 3
- 102100025390 Integrin beta-2 Human genes 0.000 description 3
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 3
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 3
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 3
- 208000030289 Lymphoproliferative disease Diseases 0.000 description 3
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- 102100025243 Myeloid cell surface antigen CD33 Human genes 0.000 description 3
- 108091034117 Oligonucleotide Proteins 0.000 description 3
- 101710089372 Programmed cell death protein 1 Proteins 0.000 description 3
- 101800001494 Protease 2A Proteins 0.000 description 3
- 101800001066 Protein 2A Proteins 0.000 description 3
- 108020004511 Recombinant DNA Proteins 0.000 description 3
- 241000283984 Rodentia Species 0.000 description 3
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 3
- 238000002105 Southern blotting Methods 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- 102100028785 Tumor necrosis factor receptor superfamily member 14 Human genes 0.000 description 3
- 101710165473 Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 description 3
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 3
- 108010003533 Viral Envelope Proteins Proteins 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 3
- 238000010256 biochemical assay Methods 0.000 description 3
- 230000033228 biological regulation Effects 0.000 description 3
- 239000007975 buffered saline Substances 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 239000001506 calcium phosphate Substances 0.000 description 3
- 229910000389 calcium phosphate Inorganic materials 0.000 description 3
- 235000011010 calcium phosphates Nutrition 0.000 description 3
- 238000002659 cell therapy Methods 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 230000009260 cross reactivity Effects 0.000 description 3
- 235000018417 cysteine Nutrition 0.000 description 3
- 125000000151 cysteine group Chemical class N[C@@H](CS)C(=O)* 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 239000000539 dimer Substances 0.000 description 3
- 230000009977 dual effect Effects 0.000 description 3
- 230000005966 endogenous activation Effects 0.000 description 3
- 229940088598 enzyme Drugs 0.000 description 3
- 230000007717 exclusion Effects 0.000 description 3
- 238000000684 flow cytometry Methods 0.000 description 3
- 238000012239 gene modification Methods 0.000 description 3
- 238000001415 gene therapy Methods 0.000 description 3
- 230000005017 genetic modification Effects 0.000 description 3
- 235000013617 genetically modified food Nutrition 0.000 description 3
- 210000004602 germ cell Anatomy 0.000 description 3
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 3
- 238000002868 homogeneous time resolved fluorescence Methods 0.000 description 3
- 230000002519 immonomodulatory effect Effects 0.000 description 3
- 230000005931 immune cell recruitment Effects 0.000 description 3
- 230000028993 immune response Effects 0.000 description 3
- 238000002649 immunization Methods 0.000 description 3
- 229940124452 immunizing agent Drugs 0.000 description 3
- 230000005847 immunogenicity Effects 0.000 description 3
- 239000002955 immunomodulating agent Substances 0.000 description 3
- 229940121354 immunomodulator Drugs 0.000 description 3
- 238000001802 infusion Methods 0.000 description 3
- 238000011081 inoculation Methods 0.000 description 3
- 108010043603 integrin alpha4beta7 Proteins 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 230000005865 ionizing radiation Effects 0.000 description 3
- 210000000265 leukocyte Anatomy 0.000 description 3
- 230000007774 longterm Effects 0.000 description 3
- 201000001268 lymphoproliferative syndrome Diseases 0.000 description 3
- 230000003211 malignant effect Effects 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 3
- 230000007935 neutral effect Effects 0.000 description 3
- 238000007911 parenteral administration Methods 0.000 description 3
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 238000010814 radioimmunoprecipitation assay Methods 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 108091008146 restriction endonucleases Proteins 0.000 description 3
- 238000012552 review Methods 0.000 description 3
- 238000012216 screening Methods 0.000 description 3
- 230000019491 signal transduction Effects 0.000 description 3
- 230000000638 stimulation Effects 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- 210000001541 thymus gland Anatomy 0.000 description 3
- 238000010361 transduction Methods 0.000 description 3
- 230000026683 transduction Effects 0.000 description 3
- 230000009261 transgenic effect Effects 0.000 description 3
- 238000013519 translation Methods 0.000 description 3
- 229950010086 tregalizumab Drugs 0.000 description 3
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 3
- 241001529453 unidentified herpesvirus Species 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- 102000007469 Actins Human genes 0.000 description 2
- 108010085238 Actins Proteins 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- 108020000948 Antisense Oligonucleotides Proteins 0.000 description 2
- 208000023275 Autoimmune disease Diseases 0.000 description 2
- 230000028728 B cell mediated immunity Effects 0.000 description 2
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 102100025074 C-C chemokine receptor-like 2 Human genes 0.000 description 2
- 102100021933 C-C motif chemokine 25 Human genes 0.000 description 2
- 108091008927 CC chemokine receptors Proteins 0.000 description 2
- 102100037904 CD9 antigen Human genes 0.000 description 2
- 238000010453 CRISPR/Cas method Methods 0.000 description 2
- 102000054900 CXCR Receptors Human genes 0.000 description 2
- 102100025466 Carcinoembryonic antigen-related cell adhesion molecule 3 Human genes 0.000 description 2
- 102000000844 Cell Surface Receptors Human genes 0.000 description 2
- 108010001857 Cell Surface Receptors Proteins 0.000 description 2
- 108091035707 Consensus sequence Proteins 0.000 description 2
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 2
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 2
- WQZGKKKJIJFFOK-QTVWNMPRSA-N D-mannopyranose Chemical compound OC[C@H]1OC(O)[C@@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-QTVWNMPRSA-N 0.000 description 2
- SRBFZHDQGSBBOR-IOVATXLUSA-N D-xylopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-IOVATXLUSA-N 0.000 description 2
- 241000588724 Escherichia coli Species 0.000 description 2
- 108700039691 Genetic Promoter Regions Proteins 0.000 description 2
- HVLSXIKZNLPZJJ-TXZCQADKSA-N HA peptide Chemical compound C([C@@H](C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](C)C(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=C(O)C=C1 HVLSXIKZNLPZJJ-TXZCQADKSA-N 0.000 description 2
- 241000238631 Hexapoda Species 0.000 description 2
- 102100026122 High affinity immunoglobulin gamma Fc receptor I Human genes 0.000 description 2
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 description 2
- 101000897486 Homo sapiens C-C motif chemokine 25 Proteins 0.000 description 2
- 101000738354 Homo sapiens CD9 antigen Proteins 0.000 description 2
- 101000914337 Homo sapiens Carcinoembryonic antigen-related cell adhesion molecule 3 Proteins 0.000 description 2
- 101000913074 Homo sapiens High affinity immunoglobulin gamma Fc receptor I Proteins 0.000 description 2
- 101000994375 Homo sapiens Integrin alpha-4 Proteins 0.000 description 2
- 101000777628 Homo sapiens Leukocyte antigen CD37 Proteins 0.000 description 2
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 2
- 101000917839 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-B Proteins 0.000 description 2
- 101000946889 Homo sapiens Monocyte differentiation antigen CD14 Proteins 0.000 description 2
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 2
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 description 2
- 206010021143 Hypoxia Diseases 0.000 description 2
- 108700005091 Immunoglobulin Genes Proteins 0.000 description 2
- 102000012745 Immunoglobulin Subunits Human genes 0.000 description 2
- 108010079585 Immunoglobulin Subunits Proteins 0.000 description 2
- 102100032818 Integrin alpha-4 Human genes 0.000 description 2
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 2
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 2
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 102100031586 Leukocyte antigen CD37 Human genes 0.000 description 2
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 2
- 102100035877 Monocyte differentiation antigen CD14 Human genes 0.000 description 2
- 241000204031 Mycoplasma Species 0.000 description 2
- 108010057466 NF-kappa B Proteins 0.000 description 2
- 102000003945 NF-kappa B Human genes 0.000 description 2
- 101100445499 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) erg-1 gene Proteins 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 102000010292 Peptide Elongation Factor 1 Human genes 0.000 description 2
- 108010077524 Peptide Elongation Factor 1 Proteins 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- 108010067965 Phytochrome B Proteins 0.000 description 2
- 108010047620 Phytohemagglutinins Proteins 0.000 description 2
- 241000276498 Pollachius virens Species 0.000 description 2
- 238000012228 RNA interference-mediated gene silencing Methods 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- 108091027967 Small hairpin RNA Proteins 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 description 2
- 102000018679 Tacrolimus Binding Proteins Human genes 0.000 description 2
- 108010027179 Tacrolimus Binding Proteins Proteins 0.000 description 2
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 2
- 102000040945 Transcription factor Human genes 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 2
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 2
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 239000002671 adjuvant Substances 0.000 description 2
- 230000009824 affinity maturation Effects 0.000 description 2
- 229960003767 alanine Drugs 0.000 description 2
- 235000004279 alanine Nutrition 0.000 description 2
- 238000012867 alanine scanning Methods 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 2
- 230000000172 allergic effect Effects 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 235000006708 antioxidants Nutrition 0.000 description 2
- 239000000074 antisense oligonucleotide Substances 0.000 description 2
- 238000012230 antisense oligonucleotides Methods 0.000 description 2
- 239000008135 aqueous vehicle Substances 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 238000004166 bioassay Methods 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- YCIMNLLNPGFGHC-UHFFFAOYSA-N catechol Chemical compound OC1=CC=CC=C1O YCIMNLLNPGFGHC-UHFFFAOYSA-N 0.000 description 2
- 230000020411 cell activation Effects 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 230000022534 cell killing Effects 0.000 description 2
- 210000003169 central nervous system Anatomy 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- 239000002975 chemoattractant Substances 0.000 description 2
- 230000004186 co-expression Effects 0.000 description 2
- 230000000295 complement effect Effects 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 230000004069 differentiation Effects 0.000 description 2
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 2
- 238000010494 dissociation reaction Methods 0.000 description 2
- 230000005593 dissociations Effects 0.000 description 2
- 210000003162 effector t lymphocyte Anatomy 0.000 description 2
- 238000004520 electroporation Methods 0.000 description 2
- 230000003511 endothelial effect Effects 0.000 description 2
- 239000002158 endotoxin Substances 0.000 description 2
- 108010048367 enhanced green fluorescent protein Proteins 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 210000003743 erythrocyte Anatomy 0.000 description 2
- 210000003527 eukaryotic cell Anatomy 0.000 description 2
- 210000002950 fibroblast Anatomy 0.000 description 2
- 238000007710 freezing Methods 0.000 description 2
- 230000008014 freezing Effects 0.000 description 2
- 238000001476 gene delivery Methods 0.000 description 2
- 230000009368 gene silencing by RNA Effects 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 210000003714 granulocyte Anatomy 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 210000003630 histaminocyte Anatomy 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 229960002885 histidine Drugs 0.000 description 2
- 235000014304 histidine Nutrition 0.000 description 2
- 210000005260 human cell Anatomy 0.000 description 2
- FDGQSTZJBFJUBT-UHFFFAOYSA-N hypoxanthine Chemical compound O=C1NC=NC2=C1NC=N2 FDGQSTZJBFJUBT-UHFFFAOYSA-N 0.000 description 2
- 230000007954 hypoxia Effects 0.000 description 2
- 230000002163 immunogen Effects 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 230000008676 import Effects 0.000 description 2
- 239000000411 inducer Substances 0.000 description 2
- 239000003112 inhibitor Substances 0.000 description 2
- 230000005764 inhibitory process Effects 0.000 description 2
- 239000002850 integrase inhibitor Substances 0.000 description 2
- 229940124524 integrase inhibitor Drugs 0.000 description 2
- 102000006495 integrins Human genes 0.000 description 2
- 108010044426 integrins Proteins 0.000 description 2
- 230000002601 intratumoral effect Effects 0.000 description 2
- PGHMRUGBZOYCAA-ADZNBVRBSA-N ionomycin Chemical compound O1[C@H](C[C@H](O)[C@H](C)[C@H](O)[C@H](C)/C=C/C[C@@H](C)C[C@@H](C)C(/O)=C/C(=O)[C@@H](C)C[C@@H](C)C[C@@H](CCC(O)=O)C)CC[C@@]1(C)[C@@H]1O[C@](C)([C@@H](C)O)CC1 PGHMRUGBZOYCAA-ADZNBVRBSA-N 0.000 description 2
- PGHMRUGBZOYCAA-UHFFFAOYSA-N ionomycin Natural products O1C(CC(O)C(C)C(O)C(C)C=CCC(C)CC(C)C(O)=CC(=O)C(C)CC(C)CC(CCC(O)=O)C)CCC1(C)C1OC(C)(C(C)O)CC1 PGHMRUGBZOYCAA-UHFFFAOYSA-N 0.000 description 2
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 210000003563 lymphoid tissue Anatomy 0.000 description 2
- FVVLHONNBARESJ-NTOWJWGLSA-H magnesium;potassium;trisodium;(2r,3s,4r,5r)-2,3,4,5,6-pentahydroxyhexanoate;acetate;tetrachloride;nonahydrate Chemical compound O.O.O.O.O.O.O.O.O.[Na+].[Na+].[Na+].[Mg+2].[Cl-].[Cl-].[Cl-].[Cl-].[K+].CC([O-])=O.OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O FVVLHONNBARESJ-NTOWJWGLSA-H 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 239000003550 marker Substances 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 229910052751 metal Inorganic materials 0.000 description 2
- 239000002184 metal Substances 0.000 description 2
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 2
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 2
- 229960002216 methylparaben Drugs 0.000 description 2
- 108091070501 miRNA Proteins 0.000 description 2
- 239000002679 microRNA Substances 0.000 description 2
- 239000003607 modifier Substances 0.000 description 2
- PJUIMOJAAPLTRJ-UHFFFAOYSA-N monothioglycerol Chemical compound OCC(O)CS PJUIMOJAAPLTRJ-UHFFFAOYSA-N 0.000 description 2
- 238000002703 mutagenesis Methods 0.000 description 2
- 231100000350 mutagenesis Toxicity 0.000 description 2
- 229940042402 non-nucleoside reverse transcriptase inhibitor Drugs 0.000 description 2
- 239000002726 nonnucleoside reverse transcriptase inhibitor Substances 0.000 description 2
- 238000011275 oncology therapy Methods 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- AQIXEPGDORPWBJ-UHFFFAOYSA-N pentan-3-ol Chemical compound CCC(O)CC AQIXEPGDORPWBJ-UHFFFAOYSA-N 0.000 description 2
- 210000005105 peripheral blood lymphocyte Anatomy 0.000 description 2
- 230000035790 physiological processes and functions Effects 0.000 description 2
- 239000002504 physiological saline solution Substances 0.000 description 2
- 230000001885 phytohemagglutinin Effects 0.000 description 2
- 108010086652 phytohemagglutinin-P Proteins 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 2
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 2
- 229960003415 propylparaben Drugs 0.000 description 2
- 230000008707 rearrangement Effects 0.000 description 2
- 230000007115 recruitment Effects 0.000 description 2
- GHMLBKRAJCXXBS-UHFFFAOYSA-N resorcinol Chemical compound OC1=CC=CC(O)=C1 GHMLBKRAJCXXBS-UHFFFAOYSA-N 0.000 description 2
- 229930002330 retinoic acid Natural products 0.000 description 2
- 238000010187 selection method Methods 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 210000003491 skin Anatomy 0.000 description 2
- 210000000813 small intestine Anatomy 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000000600 sorbitol Substances 0.000 description 2
- 235000010356 sorbitol Nutrition 0.000 description 2
- 230000009870 specific binding Effects 0.000 description 2
- 210000000130 stem cell Anatomy 0.000 description 2
- 150000003431 steroids Chemical class 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 239000002562 thickening agent Substances 0.000 description 2
- 230000005026 transcription initiation Effects 0.000 description 2
- 230000002463 transducing effect Effects 0.000 description 2
- 229960001727 tretinoin Drugs 0.000 description 2
- 210000003171 tumor-infiltrating lymphocyte Anatomy 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 239000000811 xylitol Substances 0.000 description 2
- 235000010447 xylitol Nutrition 0.000 description 2
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 2
- 229960002675 xylitol Drugs 0.000 description 2
- HBOMLICNUCNMMY-XLPZGREQSA-N zidovudine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](N=[N+]=[N-])C1 HBOMLICNUCNMMY-XLPZGREQSA-N 0.000 description 2
- 229960002555 zidovudine Drugs 0.000 description 2
- 229910052725 zinc Inorganic materials 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 1
- AFWRJOYNLMVZQO-GMFATLNBSA-N (1r,2r,4as,8as)-1-[(1e,3e)-5-hydroxy-3-methylpenta-1,3-dienyl]-2,5,5,8a-tetramethyl-3,4,4a,6,7,8-hexahydro-1h-naphthalen-2-ol Chemical compound CC1(C)CCC[C@]2(C)[C@@H](/C=C/C(=C/CO)/C)[C@](C)(O)CC[C@H]21 AFWRJOYNLMVZQO-GMFATLNBSA-N 0.000 description 1
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 1
- AGBQKNBQESQNJD-SSDOTTSWSA-N (R)-lipoic acid Chemical compound OC(=O)CCCC[C@@H]1CCSS1 AGBQKNBQESQNJD-SSDOTTSWSA-N 0.000 description 1
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 1
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 1
- 102100024341 10 kDa heat shock protein, mitochondrial Human genes 0.000 description 1
- 101710122378 10 kDa heat shock protein, mitochondrial Proteins 0.000 description 1
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 1
- HTCSFFGLRQDZDE-UHFFFAOYSA-N 2-azaniumyl-2-phenylpropanoate Chemical compound OC(=O)C(N)(C)C1=CC=CC=C1 HTCSFFGLRQDZDE-UHFFFAOYSA-N 0.000 description 1
- TVZGACDUOSZQKY-LBPRGKRZSA-N 4-aminofolic acid Chemical compound C1=NC2=NC(N)=NC(N)=C2N=C1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 TVZGACDUOSZQKY-LBPRGKRZSA-N 0.000 description 1
- 108020005029 5' Flanking Region Proteins 0.000 description 1
- 102100038222 60 kDa heat shock protein, mitochondrial Human genes 0.000 description 1
- 101710154868 60 kDa heat shock protein, mitochondrial Proteins 0.000 description 1
- 208000016683 Adult T-cell leukemia/lymphoma Diseases 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 206010073478 Anaplastic large-cell lymphoma Diseases 0.000 description 1
- 235000002198 Annona diversifolia Nutrition 0.000 description 1
- 241000219195 Arabidopsis thaliana Species 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 102100022717 Atypical chemokine receptor 1 Human genes 0.000 description 1
- 102100022716 Atypical chemokine receptor 3 Human genes 0.000 description 1
- 102100034065 Atypical chemokine receptor 4 Human genes 0.000 description 1
- 241000714230 Avian leukemia virus Species 0.000 description 1
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 1
- 102100026189 Beta-galactosidase Human genes 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 102100031172 C-C chemokine receptor type 1 Human genes 0.000 description 1
- 101710149814 C-C chemokine receptor type 1 Proteins 0.000 description 1
- 102100031151 C-C chemokine receptor type 2 Human genes 0.000 description 1
- 101710149815 C-C chemokine receptor type 2 Proteins 0.000 description 1
- 102100024167 C-C chemokine receptor type 3 Human genes 0.000 description 1
- 101710149862 C-C chemokine receptor type 3 Proteins 0.000 description 1
- 101710149863 C-C chemokine receptor type 4 Proteins 0.000 description 1
- 102100036301 C-C chemokine receptor type 7 Human genes 0.000 description 1
- 102100036305 C-C chemokine receptor type 8 Human genes 0.000 description 1
- 102100036303 C-C chemokine receptor type 9 Human genes 0.000 description 1
- 101710149857 C-C chemokine receptor type 9 Proteins 0.000 description 1
- 102100036166 C-X-C chemokine receptor type 1 Human genes 0.000 description 1
- 102100028989 C-X-C chemokine receptor type 2 Human genes 0.000 description 1
- 102100028990 C-X-C chemokine receptor type 3 Human genes 0.000 description 1
- 101710082513 C-X-C chemokine receptor type 4 Proteins 0.000 description 1
- 102100025618 C-X-C chemokine receptor type 6 Human genes 0.000 description 1
- 102100025277 C-X-C motif chemokine 13 Human genes 0.000 description 1
- 108090001026 CC chemokine receptor 9 Proteins 0.000 description 1
- 102000004900 CC chemokine receptor 9 Human genes 0.000 description 1
- 102100032976 CCR4-NOT transcription complex subunit 6 Human genes 0.000 description 1
- 108010017088 CCR5 Receptors Proteins 0.000 description 1
- 102000004274 CCR5 Receptors Human genes 0.000 description 1
- 210000001239 CD8-positive, alpha-beta cytotoxic T lymphocyte Anatomy 0.000 description 1
- 108010061298 CXCR5 Receptors Proteins 0.000 description 1
- 102000012001 CXCR5 Receptors Human genes 0.000 description 1
- 101150023944 CXCR5 gene Proteins 0.000 description 1
- 102000004631 Calcineurin Human genes 0.000 description 1
- 108010042955 Calcineurin Proteins 0.000 description 1
- 241000282832 Camelidae Species 0.000 description 1
- 241000282836 Camelus dromedarius Species 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 101100507655 Canis lupus familiaris HSPA1 gene Proteins 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 108010008951 Chemokine CXCL12 Proteins 0.000 description 1
- 108010008955 Chemokine CXCL13 Proteins 0.000 description 1
- 102000006574 Chemokine CXCL13 Human genes 0.000 description 1
- 102100035294 Chemokine XC receptor 1 Human genes 0.000 description 1
- 108010035563 Chloramphenicol O-acetyltransferase Proteins 0.000 description 1
- 108020004705 Codon Proteins 0.000 description 1
- 102100030886 Complement receptor type 1 Human genes 0.000 description 1
- 102000004420 Creatine Kinase Human genes 0.000 description 1
- 108010042126 Creatine kinase Proteins 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- HEBKCHPVOIAQTA-QWWZWVQMSA-N D-arabinitol Chemical compound OC[C@@H](O)C(O)[C@H](O)CO HEBKCHPVOIAQTA-QWWZWVQMSA-N 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 1
- 230000005778 DNA damage Effects 0.000 description 1
- 231100000277 DNA damage Toxicity 0.000 description 1
- 230000007018 DNA scission Effects 0.000 description 1
- 102000052510 DNA-Binding Proteins Human genes 0.000 description 1
- 108700020911 DNA-Binding Proteins Proteins 0.000 description 1
- 241000252212 Danio rerio Species 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- UPEZCKBFRMILAV-JNEQICEOSA-N Ecdysone Natural products O=C1[C@H]2[C@@](C)([C@@H]3C([C@@]4(O)[C@@](C)([C@H]([C@H]([C@@H](O)CCC(O)(C)C)C)CC4)CC3)=C1)C[C@H](O)[C@H](O)C2 UPEZCKBFRMILAV-JNEQICEOSA-N 0.000 description 1
- 102100031780 Endonuclease Human genes 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 101710121417 Envelope glycoprotein Proteins 0.000 description 1
- 101710091045 Envelope protein Proteins 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- 101000834253 Gallus gallus Actin, cytoplasmic 1 Proteins 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 229930191978 Gibberellin Natural products 0.000 description 1
- 108010024636 Glutathione Proteins 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 1
- 102000006354 HLA-DR Antigens Human genes 0.000 description 1
- 108010058597 HLA-DR Antigens Proteins 0.000 description 1
- 102000004447 HSP40 Heat-Shock Proteins Human genes 0.000 description 1
- 108010042283 HSP40 Heat-Shock Proteins Proteins 0.000 description 1
- 239000012981 Hank's balanced salt solution Substances 0.000 description 1
- 102100034051 Heat shock protein HSP 90-alpha Human genes 0.000 description 1
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 description 1
- 102000001554 Hemoglobins Human genes 0.000 description 1
- 108010054147 Hemoglobins Proteins 0.000 description 1
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Natural products CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 description 1
- 101000678879 Homo sapiens Atypical chemokine receptor 1 Proteins 0.000 description 1
- 101000678890 Homo sapiens Atypical chemokine receptor 3 Proteins 0.000 description 1
- 101000798902 Homo sapiens Atypical chemokine receptor 4 Proteins 0.000 description 1
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 description 1
- 101000777558 Homo sapiens C-C chemokine receptor type 10 Proteins 0.000 description 1
- 101000716068 Homo sapiens C-C chemokine receptor type 6 Proteins 0.000 description 1
- 101000716065 Homo sapiens C-C chemokine receptor type 7 Proteins 0.000 description 1
- 101000716063 Homo sapiens C-C chemokine receptor type 8 Proteins 0.000 description 1
- 101000934394 Homo sapiens C-C chemokine receptor-like 2 Proteins 0.000 description 1
- 101000797762 Homo sapiens C-C motif chemokine 5 Proteins 0.000 description 1
- 101000947174 Homo sapiens C-X-C chemokine receptor type 1 Proteins 0.000 description 1
- 101000916050 Homo sapiens C-X-C chemokine receptor type 3 Proteins 0.000 description 1
- 101000856683 Homo sapiens C-X-C chemokine receptor type 6 Proteins 0.000 description 1
- 101000858064 Homo sapiens C-X-C motif chemokine 13 Proteins 0.000 description 1
- 101000804783 Homo sapiens Chemokine XC receptor 1 Proteins 0.000 description 1
- 101000727061 Homo sapiens Complement receptor type 1 Proteins 0.000 description 1
- 101001016865 Homo sapiens Heat shock protein HSP 90-alpha Proteins 0.000 description 1
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 description 1
- 101001046686 Homo sapiens Integrin alpha-M Proteins 0.000 description 1
- 101001015006 Homo sapiens Integrin beta-4 Proteins 0.000 description 1
- 101001015037 Homo sapiens Integrin beta-7 Proteins 0.000 description 1
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 1
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 1
- 101000998120 Homo sapiens Interleukin-3 receptor subunit alpha Proteins 0.000 description 1
- 101000581981 Homo sapiens Neural cell adhesion molecule 1 Proteins 0.000 description 1
- 101000617130 Homo sapiens Stromal cell-derived factor 1 Proteins 0.000 description 1
- 101001050288 Homo sapiens Transcription factor Jun Proteins 0.000 description 1
- 108010048209 Human Immunodeficiency Virus Proteins Proteins 0.000 description 1
- 241000700588 Human alphaherpesvirus 1 Species 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- UGQMRVRMYYASKQ-UHFFFAOYSA-N Hypoxanthine nucleoside Natural products OC1C(O)C(CO)OC1N1C(NC=NC2=O)=C2N=C1 UGQMRVRMYYASKQ-UHFFFAOYSA-N 0.000 description 1
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 description 1
- 102000037982 Immune checkpoint proteins Human genes 0.000 description 1
- 108091008036 Immune checkpoint proteins Proteins 0.000 description 1
- 102000009786 Immunoglobulin Constant Regions Human genes 0.000 description 1
- 108010009817 Immunoglobulin Constant Regions Proteins 0.000 description 1
- 108010067060 Immunoglobulin Variable Region Proteins 0.000 description 1
- 102000017727 Immunoglobulin Variable Region Human genes 0.000 description 1
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 description 1
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 description 1
- 108010061833 Integrases Proteins 0.000 description 1
- 102100022338 Integrin alpha-M Human genes 0.000 description 1
- 102100022297 Integrin alpha-X Human genes 0.000 description 1
- 102100033000 Integrin beta-4 Human genes 0.000 description 1
- 102100033016 Integrin beta-7 Human genes 0.000 description 1
- 102100027268 Interferon-stimulated gene 20 kDa protein Human genes 0.000 description 1
- 102000013462 Interleukin-12 Human genes 0.000 description 1
- 108010065805 Interleukin-12 Proteins 0.000 description 1
- 102100033493 Interleukin-3 receptor subunit alpha Human genes 0.000 description 1
- 108010018951 Interleukin-8B Receptors Proteins 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- 208000028257 Joubert syndrome with oculorenal defect Diseases 0.000 description 1
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- 239000004395 L-leucine Substances 0.000 description 1
- 235000019454 L-leucine Nutrition 0.000 description 1
- LRQKBLKVPFOOQJ-YFKPBYRVSA-N L-norleucine Chemical compound CCCC[C@H]([NH3+])C([O-])=O LRQKBLKVPFOOQJ-YFKPBYRVSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 241000282838 Lama Species 0.000 description 1
- 208000032004 Large-Cell Anaplastic Lymphoma Diseases 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- NNJVILVZKWQKPM-UHFFFAOYSA-N Lidocaine Chemical compound CCN(CC)CC(=O)NC1=C(C)C=CC=C1C NNJVILVZKWQKPM-UHFFFAOYSA-N 0.000 description 1
- 239000000232 Lipid Bilayer Substances 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 241000282553 Macaca Species 0.000 description 1
- 241000282560 Macaca mulatta Species 0.000 description 1
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 1
- 102100025912 Melanopsin Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 241000713333 Mouse mammary tumor virus Species 0.000 description 1
- 241000714177 Murine leukemia virus Species 0.000 description 1
- 241000699660 Mus musculus Species 0.000 description 1
- 102000003505 Myosin Human genes 0.000 description 1
- 108060008487 Myosin Proteins 0.000 description 1
- 102100027347 Neural cell adhesion molecule 1 Human genes 0.000 description 1
- 108700026244 Open Reading Frames Proteins 0.000 description 1
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 1
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 1
- 102000016979 Other receptors Human genes 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 108090000526 Papain Proteins 0.000 description 1
- 208000030852 Parasitic disease Diseases 0.000 description 1
- 206010034133 Pathogen resistance Diseases 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 208000027190 Peripheral T-cell lymphomas Diseases 0.000 description 1
- 208000002151 Pleural effusion Diseases 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 102100037935 Polyubiquitin-C Human genes 0.000 description 1
- 102100025803 Progesterone receptor Human genes 0.000 description 1
- 208000033759 Prolymphocytic T-Cell Leukemia Diseases 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 102000003923 Protein Kinase C Human genes 0.000 description 1
- 108090000315 Protein Kinase C Proteins 0.000 description 1
- 101710188315 Protein X Proteins 0.000 description 1
- 108010071563 Proto-Oncogene Proteins c-fos Proteins 0.000 description 1
- 102000007568 Proto-Oncogene Proteins c-fos Human genes 0.000 description 1
- 241001112090 Pseudovirus Species 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- MUPFEKGTMRGPLJ-RMMQSMQOSA-N Raffinose Natural products O(C[C@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](O[C@@]2(CO)[C@H](O)[C@@H](O)[C@@H](CO)O2)O1)[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 MUPFEKGTMRGPLJ-RMMQSMQOSA-N 0.000 description 1
- 102000018120 Recombinases Human genes 0.000 description 1
- 108010091086 Recombinases Proteins 0.000 description 1
- 108091027981 Response element Proteins 0.000 description 1
- JVWLUVNSQYXYBE-UHFFFAOYSA-N Ribitol Natural products OCC(C)C(O)C(O)CO JVWLUVNSQYXYBE-UHFFFAOYSA-N 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- 229920002684 Sepharose Polymers 0.000 description 1
- 241000713311 Simian immunodeficiency virus Species 0.000 description 1
- 241000269319 Squalius cephalus Species 0.000 description 1
- UQZIYBXSHAGNOE-USOSMYMVSA-N Stachyose Natural products O(C[C@H]1[C@@H](O)[C@H](O)[C@H](O)[C@@H](O[C@@]2(CO)[C@H](O)[C@@H](O)[C@@H](CO)O2)O1)[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@H](CO[C@@H]2[C@@H](O)[C@@H](O)[C@@H](O)[C@H](CO)O2)O1 UQZIYBXSHAGNOE-USOSMYMVSA-N 0.000 description 1
- 102000007451 Steroid Receptors Human genes 0.000 description 1
- 108010085012 Steroid Receptors Proteins 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 208000031672 T-Cell Peripheral Lymphoma Diseases 0.000 description 1
- 208000026651 T-cell prolymphocytic leukemia Diseases 0.000 description 1
- 238000012245 TALEN-based genome engineering Methods 0.000 description 1
- 108091036066 Three prime untranslated region Proteins 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 102000006601 Thymidine Kinase Human genes 0.000 description 1
- 108020004440 Thymidine kinase Proteins 0.000 description 1
- 102100033571 Tissue-type plasminogen activator Human genes 0.000 description 1
- 108050006955 Tissue-type plasminogen activator Proteins 0.000 description 1
- XOKJUSAYZUAMGJ-UHFFFAOYSA-N Toyocamycin Natural products C1=C(C#N)C=2C(N)=NC=NC=2N1C1OC(CO)C(O)C1O XOKJUSAYZUAMGJ-UHFFFAOYSA-N 0.000 description 1
- 102100023132 Transcription factor Jun Human genes 0.000 description 1
- 101800001690 Transmembrane protein gp41 Proteins 0.000 description 1
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 1
- MUPFEKGTMRGPLJ-UHFFFAOYSA-N UNPD196149 Natural products OC1C(O)C(CO)OC1(CO)OC1C(O)C(O)C(O)C(COC2C(C(O)C(O)C(CO)O2)O)O1 MUPFEKGTMRGPLJ-UHFFFAOYSA-N 0.000 description 1
- 108090000848 Ubiquitin Proteins 0.000 description 1
- 102000044159 Ubiquitin Human genes 0.000 description 1
- 108010056354 Ubiquitin C Proteins 0.000 description 1
- 101150117115 V gene Proteins 0.000 description 1
- 206010046865 Vaccinia virus infection Diseases 0.000 description 1
- 241001416177 Vicugna pacos Species 0.000 description 1
- 108700005077 Viral Genes Proteins 0.000 description 1
- 108020000999 Viral RNA Proteins 0.000 description 1
- 238000012452 Xenomouse strains Methods 0.000 description 1
- WTIJXIZOODAMJT-WBACWINTSA-N [(3r,4s,5r,6s)-5-hydroxy-6-[4-hydroxy-3-[[5-[[4-hydroxy-7-[(2s,3r,4s,5r)-3-hydroxy-5-methoxy-6,6-dimethyl-4-(5-methyl-1h-pyrrole-2-carbonyl)oxyoxan-2-yl]oxy-8-methyl-2-oxochromen-3-yl]carbamoyl]-4-methyl-1h-pyrrole-3-carbonyl]amino]-8-methyl-2-oxochromen- Chemical compound O([C@@H]1[C@H](C(O[C@H](OC=2C(=C3OC(=O)C(NC(=O)C=4C(=C(C(=O)NC=5C(OC6=C(C)C(O[C@@H]7[C@@H]([C@H](OC(=O)C=8NC(C)=CC=8)[C@@H](OC)C(C)(C)O7)O)=CC=C6C=5O)=O)NC=4)C)=C(O)C3=CC=2)C)[C@@H]1O)(C)C)OC)C(=O)C1=CC=C(C)N1 WTIJXIZOODAMJT-WBACWINTSA-N 0.000 description 1
- HMNZFMSWFCAGGW-XPWSMXQVSA-N [3-[hydroxy(2-hydroxyethoxy)phosphoryl]oxy-2-[(e)-octadec-9-enoyl]oxypropyl] (e)-octadec-9-enoate Chemical compound CCCCCCCC\C=C\CCCCCCCC(=O)OCC(COP(O)(=O)OCCO)OC(=O)CCCCCCC\C=C\CCCCCCCC HMNZFMSWFCAGGW-XPWSMXQVSA-N 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 208000038016 acute inflammation Diseases 0.000 description 1
- 230000006022 acute inflammation Effects 0.000 description 1
- 230000003044 adaptive effect Effects 0.000 description 1
- 201000006966 adult T-cell leukemia Diseases 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 230000000735 allogeneic effect Effects 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- UPEZCKBFRMILAV-UHFFFAOYSA-N alpha-Ecdysone Natural products C1C(O)C(O)CC2(C)C(CCC3(C(C(C(O)CCC(C)(C)O)C)CCC33O)C)C3=CC(=O)C21 UPEZCKBFRMILAV-UHFFFAOYSA-N 0.000 description 1
- AGBQKNBQESQNJD-UHFFFAOYSA-N alpha-Lipoic acid Natural products OC(=O)CCCCC1CCSS1 AGBQKNBQESQNJD-UHFFFAOYSA-N 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000001414 amino alcohols Chemical class 0.000 description 1
- 229960003896 aminopterin Drugs 0.000 description 1
- 230000000798 anti-retroviral effect Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 210000000628 antibody-producing cell Anatomy 0.000 description 1
- 238000010913 antigen-directed enzyme pro-drug therapy Methods 0.000 description 1
- 238000011225 antiretroviral therapy Methods 0.000 description 1
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229960003121 arginine Drugs 0.000 description 1
- 239000000823 artificial membrane Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 210000001130 astrocyte Anatomy 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 239000000022 bacteriostatic agent Substances 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 229960001716 benzalkonium Drugs 0.000 description 1
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 1
- 108010005774 beta-Galactosidase Proteins 0.000 description 1
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 238000010170 biological method Methods 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- HUTDDBSSHVOYJR-UHFFFAOYSA-H bis[(2-oxo-1,3,2$l^{5},4$l^{2}-dioxaphosphaplumbetan-2-yl)oxy]lead Chemical compound [Pb+2].[Pb+2].[Pb+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O HUTDDBSSHVOYJR-UHFFFAOYSA-H 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000001772 blood platelet Anatomy 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 229960005520 bryostatin Drugs 0.000 description 1
- MJQUEDHRCUIRLF-TVIXENOKSA-N bryostatin 1 Chemical compound C([C@@H]1CC(/[C@@H]([C@@](C(C)(C)/C=C/2)(O)O1)OC(=O)/C=C/C=C/CCC)=C\C(=O)OC)[C@H]([C@@H](C)O)OC(=O)C[C@H](O)C[C@@H](O1)C[C@H](OC(C)=O)C(C)(C)[C@]1(O)C[C@@H]1C\C(=C\C(=O)OC)C[C@H]\2O1 MJQUEDHRCUIRLF-TVIXENOKSA-N 0.000 description 1
- MUIWQCKLQMOUAT-AKUNNTHJSA-N bryostatin 20 Natural products COC(=O)C=C1C[C@@]2(C)C[C@]3(O)O[C@](C)(C[C@@H](O)CC(=O)O[C@](C)(C[C@@]4(C)O[C@](O)(CC5=CC(=O)O[C@]45C)C(C)(C)C=C[C@@](C)(C1)O2)[C@@H](C)O)C[C@H](OC(=O)C(C)(C)C)C3(C)C MUIWQCKLQMOUAT-AKUNNTHJSA-N 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 239000004067 bulking agent Substances 0.000 description 1
- 239000003710 calcium ionophore Substances 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 229920006317 cationic polymer Polymers 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000011712 cell development Effects 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 238000012412 chemical coupling Methods 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 230000003399 chemotactic effect Effects 0.000 description 1
- 230000035605 chemotaxis Effects 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 238000001246 colloidal dispersion Methods 0.000 description 1
- 239000000084 colloidal system Substances 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 238000007906 compression Methods 0.000 description 1
- 230000006835 compression Effects 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 239000012228 culture supernatant Substances 0.000 description 1
- 150000003999 cyclitols Chemical class 0.000 description 1
- HPXRVTGHNJAIIH-UHFFFAOYSA-N cyclohexanol Chemical compound OC1CCCCC1 HPXRVTGHNJAIIH-UHFFFAOYSA-N 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000008260 defense mechanism Effects 0.000 description 1
- 239000000412 dendrimer Substances 0.000 description 1
- 229920000736 dendritic polymer Polymers 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- UPEZCKBFRMILAV-JMZLNJERSA-N ecdysone Chemical compound C1[C@@H](O)[C@@H](O)C[C@]2(C)[C@@H](CC[C@@]3([C@@H]([C@@H]([C@H](O)CCC(C)(C)O)C)CC[C@]33O)C)C3=CC(=O)[C@@H]21 UPEZCKBFRMILAV-JMZLNJERSA-N 0.000 description 1
- 108010057988 ecdysone receptor Proteins 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 108700004025 env Genes Proteins 0.000 description 1
- 101150030339 env gene Proteins 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 210000003386 epithelial cell of thymus gland Anatomy 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- 102000015694 estrogen receptors Human genes 0.000 description 1
- 108010038795 estrogen receptors Proteins 0.000 description 1
- CJAONIOAQZUHPN-KKLWWLSJSA-N ethyl 12-[[2-[(2r,3r)-3-[2-[(12-ethoxy-12-oxododecyl)-methylamino]-2-oxoethoxy]butan-2-yl]oxyacetyl]-methylamino]dodecanoate Chemical compound CCOC(=O)CCCCCCCCCCCN(C)C(=O)CO[C@H](C)[C@@H](C)OCC(=O)N(C)CCCCCCCCCCCC(=O)OCC CJAONIOAQZUHPN-KKLWWLSJSA-N 0.000 description 1
- 230000005713 exacerbation Effects 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 210000004700 fetal blood Anatomy 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- FBPFZTCFMRRESA-GUCUJZIJSA-N galactitol Chemical compound OC[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-GUCUJZIJSA-N 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 229940014259 gelatin Drugs 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000003500 gene array Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- IXORZMNAPKEEDV-UHFFFAOYSA-N gibberellic acid GA3 Natural products OC(=O)C1C2(C3)CC(=C)C3(O)CCC2C2(C=CC3O)C1C3(C)C(=O)O2 IXORZMNAPKEEDV-UHFFFAOYSA-N 0.000 description 1
- 239000003448 gibberellin Substances 0.000 description 1
- 229940050410 gluconate Drugs 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 235000004554 glutamine Nutrition 0.000 description 1
- 229960002743 glutamine Drugs 0.000 description 1
- 229960003180 glutathione Drugs 0.000 description 1
- 229960002449 glycine Drugs 0.000 description 1
- 210000000224 granular leucocyte Anatomy 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 238000003306 harvesting Methods 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 238000002744 homologous recombination Methods 0.000 description 1
- 230000006801 homologous recombination Effects 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 230000004727 humoral immunity Effects 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 238000012872 hydroxylapatite chromatography Methods 0.000 description 1
- 229950010245 ibalizumab Drugs 0.000 description 1
- 230000005965 immune activity Effects 0.000 description 1
- 102000027596 immune receptors Human genes 0.000 description 1
- 108091008915 immune receptors Proteins 0.000 description 1
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 description 1
- 238000012760 immunocytochemical staining Methods 0.000 description 1
- 230000002584 immunomodulator Effects 0.000 description 1
- 238000001114 immunoprecipitation Methods 0.000 description 1
- 239000003547 immunosorbent Substances 0.000 description 1
- 230000001024 immunotherapeutic effect Effects 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 238000000530 impalefection Methods 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000005414 inactive ingredient Substances 0.000 description 1
- 229960000367 inositol Drugs 0.000 description 1
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 1
- 108010021315 integrin beta7 Proteins 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 238000001361 intraarterial administration Methods 0.000 description 1
- 238000010212 intracellular staining Methods 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 238000011835 investigation Methods 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 229960003136 leucine Drugs 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 229960004194 lidocaine Drugs 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 235000019136 lipoic acid Nutrition 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000001294 liquid chromatography-tandem mass spectrometry Methods 0.000 description 1
- 244000144972 livestock Species 0.000 description 1
- 239000003589 local anesthetic agent Substances 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 230000001926 lymphatic effect Effects 0.000 description 1
- 229960003646 lysine Drugs 0.000 description 1
- RLSSMJSEOOYNOY-UHFFFAOYSA-N m-cresol Chemical compound CC1=CC=CC(O)=C1 RLSSMJSEOOYNOY-UHFFFAOYSA-N 0.000 description 1
- 238000002826 magnetic-activated cell sorting Methods 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 208000020968 mature T-cell and NK-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 108010005417 melanopsin Proteins 0.000 description 1
- 210000004779 membrane envelope Anatomy 0.000 description 1
- 210000003071 memory t lymphocyte Anatomy 0.000 description 1
- 229940100630 metacresol Drugs 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- MYWUZJCMWCOHBA-VIFPVBQESA-N methamphetamine Chemical compound CN[C@@H](C)CC1=CC=CC=C1 MYWUZJCMWCOHBA-VIFPVBQESA-N 0.000 description 1
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 238000010208 microarray analysis Methods 0.000 description 1
- 210000000274 microglia Anatomy 0.000 description 1
- 238000000520 microinjection Methods 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 238000009126 molecular therapy Methods 0.000 description 1
- 210000002864 mononuclear phagocyte Anatomy 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 210000002464 muscle smooth vascular Anatomy 0.000 description 1
- 201000005962 mycosis fungoides Diseases 0.000 description 1
- 229940105132 myristate Drugs 0.000 description 1
- 239000002088 nanocapsule Substances 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 210000000440 neutrophil Anatomy 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 238000011580 nude mouse model Methods 0.000 description 1
- 244000039328 opportunistic pathogen Species 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 229960003104 ornithine Drugs 0.000 description 1
- 229940043515 other immunoglobulins in atc Drugs 0.000 description 1
- 108010062490 p27 antigen Proteins 0.000 description 1
- 229940055729 papain Drugs 0.000 description 1
- 235000019834 papain Nutrition 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 230000002688 persistence Effects 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 229960003742 phenol Drugs 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 108091008695 photoreceptors Proteins 0.000 description 1
- 238000000053 physical method Methods 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 230000004983 pleiotropic effect Effects 0.000 description 1
- 108010054442 polyalanine Proteins 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 230000029279 positive regulation of transcription, DNA-dependent Effects 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 210000004986 primary T-cell Anatomy 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 108090000468 progesterone receptors Proteins 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 210000001938 protoplast Anatomy 0.000 description 1
- 239000008213 purified water Substances 0.000 description 1
- MUPFEKGTMRGPLJ-ZQSKZDJDSA-N raffinose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O2)O)O1 MUPFEKGTMRGPLJ-ZQSKZDJDSA-N 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 230000032554 response to blue light Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- HEBKCHPVOIAQTA-ZXFHETKHSA-N ribitol Chemical compound OC[C@H](O)[C@H](O)[C@H](O)CO HEBKCHPVOIAQTA-ZXFHETKHSA-N 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 230000000405 serological effect Effects 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 238000002741 site-directed mutagenesis Methods 0.000 description 1
- GNBVPFITFYNRCN-UHFFFAOYSA-M sodium thioglycolate Chemical compound [Na+].[O-]C(=O)CS GNBVPFITFYNRCN-UHFFFAOYSA-M 0.000 description 1
- 229940046307 sodium thioglycolate Drugs 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 210000004988 splenocyte Anatomy 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- UQZIYBXSHAGNOE-XNSRJBNMSA-N stachyose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO[C@@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO[C@@H]3[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO)O3)O)O2)O)O1 UQZIYBXSHAGNOE-XNSRJBNMSA-N 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- SFVFIFLLYFPGHH-UHFFFAOYSA-M stearalkonium chloride Chemical compound [Cl-].CCCCCCCCCCCCCCCCCC[N+](C)(C)CC1=CC=CC=C1 SFVFIFLLYFPGHH-UHFFFAOYSA-M 0.000 description 1
- 238000011146 sterile filtration Methods 0.000 description 1
- 238000013190 sterility testing Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000008362 succinate buffer Substances 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 229960002663 thioctic acid Drugs 0.000 description 1
- 229940035024 thioglycerol Drugs 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 239000008181 tonicity modifier Substances 0.000 description 1
- 238000011200 topical administration Methods 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- XOKJUSAYZUAMGJ-WOUKDFQISA-N toyocamycin Chemical compound C1=C(C#N)C=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O XOKJUSAYZUAMGJ-WOUKDFQISA-N 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- 238000003151 transfection method Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000011277 treatment modality Methods 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 239000013638 trimer Substances 0.000 description 1
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical class CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 1
- 150000004043 trisaccharides Chemical class 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 229940045136 urea Drugs 0.000 description 1
- 208000007089 vaccinia Diseases 0.000 description 1
- 150000002266 vitamin A derivatives Chemical class 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 229950009002 zanolimumab Drugs 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4611—T-cells, e.g. tumor infiltrating lymphocytes [TIL], lymphokine-activated killer cells [LAK] or regulatory T cells [Treg]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/463—Cellular immunotherapy characterised by recombinant expression
- A61K39/4631—Chimeric Antigen Receptors [CAR]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/4644—Cancer antigens
- A61K39/464402—Receptors, cell surface antigens or cell surface determinants
- A61K39/464429—Molecules with a "CD" designation not provided for elsewhere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/4644—Cancer antigens
- A61K39/464436—Cytokines
- A61K39/464442—Chemokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/70517—CD8
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/70521—CD28, CD152
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70578—NGF-receptor/TNF-receptor superfamily, e.g. CD27, CD30, CD40, CD95
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
- C07K14/7158—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons for chemokines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2812—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/46—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the cancer treated
- A61K2239/48—Blood cells, e.g. leukemia or lymphoma
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/02—Fusion polypeptide containing a localisation/targetting motif containing a signal sequence
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/03—Fusion polypeptide containing a localisation/targetting motif containing a transmembrane segment
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2740/00—Reverse transcribing RNA viruses
- C12N2740/00011—Details
- C12N2740/10011—Retroviridae
- C12N2740/16011—Human Immunodeficiency Virus, HIV
- C12N2740/16041—Use of virus, viral particle or viral elements as a vector
- C12N2740/16043—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
Abstract
키메라 수용체(CR), 키메라 공동수용체(CCOR) 및/또는 공동수용체(COR)를 포함하는 면역 세포(예컨대, T 세포)가 제공된다.
Description
관련 출원
본 출원은 2018년 7월 13일자로 출원된 PCT/CN2018/095650, 2019년 5월 16일자로 출원된 PCT/CN2019/087259에 대한 우선권 이익을 주장하며, 이들 각각의 내용은 전문이 본 명세서에 참조에 의해 원용된다.
본 발명의 분야
본 발명은 전염병, 예컨대, HIV를 치료하는 데 유용한 하나 이상의 조작된 수용체를 포함하는 면역 세포(예컨대, T 세포)에 관한 것이다.
T-세포 매개 면역은 항원(Ag)-특이적 T 림프구를 발달시켜 바이러스, 박테리아, 기생충 감염 또는 악성 세포를 제거하는 적응 과정이다.
Ag에 노출되면, 미경험(naive) T 세포가 활성화된 이펙터 T 세포로 성숙할 것이다. 이 과정은 항원 제시 세포(APC)의 표면에서 Ag의 제시를 통해 일어난다. 구체적으로, Ag(즉, 바이러스, 박테리아, 기생충, 또는 악성 세포) 유래의 항원성 펩타이드는 APC의 표면에 위치한 주요 조직적합성 복합체(MHC)의 일부로서 T 세포에 제시된다. T 세포의 표면에서 발견되는 T 세포 수용체(TCR)는 MHC에 결합하고 결합된 펩타이드를 인식하는 역할을 한다. 이러한 과정은 신호 전달을 촉발하여 T 세포 활성화 및 하류 면역 반응을 초래한다.
TCR에 추가적으로, T 세포는 기능적 특성화에 역할을 하는 마커 및 다른 세포 표면 수용체를 보유한다. 예를 들어, CD8을 보이는 T 세포(CD8+ T 세포, 또한 세포독성 또는 살해 T 세포라고도 알려짐)는 악성이거나, 바이러스에 감염되었거나, 다른 손상 징후를 보이는 세포를 표적화하고 파괴하는 역할을 한다. CD4를 보이는 T 세포(CD4+ T 세포, 또는 헬퍼 T 세포)는 일반적으로 다른 면역 세포의 기능을 돕는 것으로 특징지어진다. Th1, Th2, 및 Th17을 포함하여, 헬퍼 T 세포의 몇 가지 추가 하위집합이 있다. CD8+ 및 CD4+ T 세포는 항원 반응 및 T 세포 매개 면역에서 필수적인 역할을 하지만, 면역계에서의 유일한 T 세포는 아니며: 조절 T 세포(Treg) 및 자연 살해 T(NKT) 세포를 포함한 다양한 다른 부류가 존재한다.
CD4+ T 세포는 아마도 면역계에서 가장 중요한 조정 역할을 하며, T 세포 매개 면역 및 B 세포 매개, 또는 체액성 면역 둘 다에서 중심적인 역할을 한다. T 세포 매개 면역에서, 이들은 CD8+ T 세포의 활성화 및 성숙에서 역할을 한다. B 세포 매개 면역에서, 이들은 B 세포를 자극하여 증식시키고 B 세포 항체 종류 변환을 유도하는 역할을 한다.
CD4+ T 세포가 수행하는 중심 역할은 아마도 인간 면역결핍 바이러스(HIV) 감염의 여파로 가장 잘 설명된다. 상기 바이러스는 레트로바이러스이며, 이는 상기 바이러스가 숙주 세포에 들어가면 상기 바이러스의 RNA 게놈으로부터 DNA를 생성할 수 있게 하는 역전사 효소와 함께 유전 정보를 RNA로서 전달한다는 것을 의미한다. 그 다음 DNA는 감염된 숙주 세포에 통합될 수 있으며, 이 때 바이러스 유전자가 전사되고 감염된 세포에 의해 더 많은 바이러스 입자가 생성되고 방출된다.
HIV는 우선적으로 CD4+ T 세포를 표적으로 하며; 결과적으로, 면역계의 주요 조정 세포의 개체수가 감소함에 따라, 감염된 환자의 면역계는 점점 더 손상된다. 사실, HIV의 후천성 면역결핍 증후군(AIDS)으로의 진행은 환자의 CD4+ T 세포 수로 표시된다. 바이러스에 의한 CD4+ T 세포의 이러한 표적화는 또한 감염된 환자가 기회감염성 병원균을 포함한, 다양한 병원균에 대한 생산적인 면역 반응을 성공적으로 수행할 수 없게 만드는 것이다.
HIV에 대한 첫번째 치료제인 지도부딘(ZDV) 또는 아지도타이미딘(AZT)이 1987년 미국 식품의약국(FDA)의 승인을 받았다. 이 약물은 뉴클레오사이드 역전사효소 저해제(NRTI)로 분류되었다. 시간이 경과함에 따라, 바이러스 돌연변이로 인해 상기 약물이 감염을 계속 억제할 수 없게 되면서, 약물의 초기 성공률이 하락하였다. 이후 초기 항바이러스 요법(ART)을 대체하기 위해 고활성 항레트로바이러스 요법(HAART)이 도입되었다.
1990년대 중반까지, 연구자와 임상의는 NRTI와 프로테아제 저해제를 둘 다 포함하는 병용 치료의 이익을 관찰하였다. 병용 요법은 오늘날에도 계속 사용되고 있으며, 환자가 이용할 수 있는 다수의 병용 요법이 있다. 일반적으로, 병용 요법은 2가지 NRTI와, 비-뉴클레오사이드 역전사효소 저해제(NNRIT), 프로테아제 저해제, 또는 인테그라제 저해제로 이루어진다. 요컨대, 현재 병용 요법의 일부로 사용되는 6가지 부류의 약물, 즉 진입 저해제, 뉴클레오사이드 역전사효소 저해제, 뉴클레오타이드 역전사효소 저해제, 비-뉴클레오사이드 역전사효소 저해제, 프로테아제 저해제, 및 인테그라제 저해제가 있다.
다양한 약리학적 부류의 약물을 이용하여 바이러스를 표적화하는 것은 바이러스 내성을 방지하고, 감염된 환자에서 상당한 효능을 나타내었지만, 완전한 효능을 보장하기 위해서 환자의 높은 수준의 처방 준수를 필요로 한다. 사실, 처방 비준수는 약물-내성 균주의 출현을 초래할 수 있으며, 이는 환자의 질환 및 후속 합병증을 둘 다 효과적으로 관리하고 치료하는 데 추가의 어려움을 야기한다.
본 명세서에 언급된 모든 간행물, 특허, 특허 출원 및 공개된 특허 출원의 개시내용은 본 명세서에 전문이 참조로 포함된다.
일 양태에서 본 출원은 키메라 수용체(chimeric receptor: CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인, CR 막관통 도메인, 및 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR); 및 키메라 공동수용체(chimeric co-receptor: CCOR) 표적 항원을 특이적으로 인식하는 CCOR 항원 결합 도메인, CCOR 막관통 도메인, 및 세포내 CCOR 공동자극 도메인을 포함하는 키메라 공동수용체(CCOR)를 포함하는 조작된 면역 세포를 제공한다. 일부 실시형태에서, CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이다. 일부 실시형태에서, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4이다. 일부 실시형태에서, 조작된 면역 세포는 하나 이상의 공동수용체(COR)를 더 포함한다.
일 양태에서, 본 발명은 CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인, CR 막관통 도메인, 및 세포내 CR 신호전달 도메인을 포함하는 CR을 포함하는 조작된 면역 세포를 제공한다. 일부 실시형태에서, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택된다. 다른 실시형태에서, 조작된 면역 세포는 하나 이상의 COR을 더 포함한다. 일부 실시형태에서, CR 항원 결합 도메인은 CD4 결합 모이어티, CCR5 결합 모이어티, 및 항-HIV 항체 모이어티(예컨대, 광범위 중화 황체("bNAb") 모이어티) 중 적어도 2가지를 포함한다. 일부 실시형태에서, CR은 CD4 결합 모이어티 및 CCR5 결합 모이어티를 포함하는 탠덤 CR이다. 일부 실시형태에서, CR은 CD4 결합 모이어티 및 항-HIV 항체 모이어티(예컨대, bNAb 모이어티)를 포함하는 탠덤 CR이다. 일부 실시형태에서, CR은 CCR5 결합 모이어티 및 항-HIV 항체 모이어티(예컨대, bNAb 모이어티)를 포함하는 탠덤 CR이다. CD4 모이어티, CCR5 모이어티 및/또는 bNAb 모이어티는 직접 또는 링커를 통해 서로 연결될 수 있다.
일부 실시형태에서, 본 발명은 CR을 인코딩하는 제1 핵산(여기서, CR은 CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인, CR 막관통 도메인, 및 세포내 CR 신호전달 도메인을 포함함), 및 CCOR을 인코딩하는 제2 핵산(여기서, CCOR은 CCOR 표적 항원을 특이적으로 인식하는 CCOR 항원 결합 도메인, CCOR 막관통 도메인, 및 세포내 CCOR 공동자극 신호전달 도메인을 포함함)을 포함하는 조작된 면역 세포를 제공한다. 일부 실시형태에서, CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이다. 일부 실시형태에서, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4이다. 일부 실시형태에서, 면역 세포는 하나 이상의 COR을 인코딩하는 하나 이상의 핵산(들)을 더 포함한다.
일부 실시형태에서, 본 발명은 CR을 인코딩하는 핵산을 포함하는 조작된 면역 세포를 제공하며, 여기서 CR은 CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인, CR 막관통 도메인, 및 세포내 CR 신호전달 도메인을 포함한다. 일부 실시형태에서, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 면역 세포는 하나 이상의 COR을 인코딩하는 하나 이상의 핵산(들)을 더 포함한다.
상기 실시형태 중 일부 또는 그 이상에 따른 일부 실시형태에서, CR은 세포내 CR 공동자극 도메인을 더 포함한다. 다른 실시형태에서, CR은 세포내 공동자극 도메인을 포함하지 않는다.
상기 실시형태 중 하나 이상에 따른 일부 실시형태에서, CR을 인코딩하는 핵산은 유도성 프로모터 하에 있다. 다른 실시형태에서, CR을 인코딩하는 핵산은 구성적으로 발현된다.
상기 실시형태 중 임의의 하나 이상에 따른 일부 실시형태에서, CCOR 및/또는 COR을 인코딩하는 핵산은 유도성 프로모터 하에 있다. 다른 실시형태에서, CCOR 및/또는 COR을 인코딩하는 핵산은 구성적으로 발현된다. 또 다른 실시형태에서, CCOR 및/또는 COR을 인코딩하는 핵산은 면역 세포의 활성화시 유도성이다.
일부 실시형태에서, 제1 핵산 및 제2 핵산은 동일한 벡터 상에 있다. 일부 실시형태에서, 제1 핵산 및 제2 핵산은 동일한 프로모터의 제어 하에 있다. 다른 실시형태에서, 제1 핵산 및 제2 핵산은 상이한 벡터 상에 있다.
일부 실시형태에서, 하나 이상의 COR-인코딩 핵산은 제1 핵산과 동일한 벡터 상에 있다. 일부 실시형태에서, 하나 이상의 COR-인코딩 핵산은 제2 핵산과 동일한 벡터 상에 있다. 일부 실시형태에서, 하나 이상의 COR-인코딩 핵산 및 제1 핵산 또는 제2 핵산은 동일한 프로모터의 제어 하에 있다.
상기 실시형태 중 임의의 것에 따른 일부 실시형태에서, CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이다. 다른 실시형태에서, CR 표적 항원은 CD4이고, CCOR 표적 항원은 CCR5 또는 CXCR4이다.
상기 실시형태 중 임의의 것에 따른 일부 실시형태에서, 하나 이상의 COR은 CXCR5, α4β7 및 CXCR9로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 하나 이상의 COR 중 적어도 하나는 CXCR5이다. 다른 실시형태에서, 하나 이상의 COR 중 적어도 하나는 α4β7이다. 또 다른 실시형태에서, 하나 이상의 COR 중 적어도 하나는 CCR9이다. 또한 추가의 실시형태에서, 하나 이상의 COR은 α4β7 및 CCR9를 둘 다 포함한다.
상기 실시형태 중 임의의 것에 따른 일부 실시형태에서, 면역 세포는 세포 내에서 CCR5의 발현을 감소시키거나 제거하도록 변형된다. 일부 실시형태에서, CCR5 유전자는 CRISPR/Cas9, TALEN ZFN, siRNA, 및 안티센스 RNA로 이루어진 군으로부터 선택되는 방법을 사용함으로써 비활성화된다.
상기 실시형태 중 임의의 것에 따른 일부 실시형태에서, CR 항원 결합 도메인은 Fab, Fab', (Fab')2, Fv, 단일 사슬 Fc(scFv), 단일 도메인 항체(sdAb), 및 CR 표적 항원에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CR 항원 결합 도메인은 scFv 또는 sdAb이다.
상기 실시형태 중 임의의 것에 따른 일부 실시형태에서, CCOR 항원 결합 도메인은 Fab, Fab', (Fab')2, Fc, 단일 사슬 Fv(scFv), 단일 도메인 항체(sdAb), 및 CCOR 표적 항원에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CCOR 항원 결합 도메인은 scFv 또는 sdAb이다.
상기 실시형태 중 임의의 것에 따른 일부 실시형태에서, 세포내 CR 신호전달 도메인은 CD3ζ, FcRγ, FcRβ, CD3γ, CD3δ, CD3ε, CD5, CD22, CD79a, CD79b, 및 CD66d로 이루어진 군으로부터 선택된다.
상기 실시형태 중 하나 이상에 따른 일부 실시형태에서, CR 또는 CCOR 공동자극 도메인은 CD28, 4-1BB(CD137), CD27, OX40, CD27, CD40, PD-1, ICOS, 림프구 기능-연관 항원-1(LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3, TNFRSF9, TNFRSF4, TNFRSF8, CD40LG, ITGB2, KLRC2, TNFRSF18, TNFRSF14, HAVCR1, LGALS9, CD83, 및 CD83과 특이적으로 결합하는 리간드 중 하나 이상의 공동자극 도메인으로 이루어진 군으로부터 선택된다.
상기 실시형태 중 임의의 것에 따른 일부 실시형태에서, 조작된 면역 세포는 T 세포, B 세포, NK 세포, 수지상 세포, 호산구, 대식세포, 림프구 세포, 및 비만 세포로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 조작된 면역 세포는 세포독성 T 세포, 헬퍼 T 세포, 및 자연 살해 T 세포로부터 선택된다. 일부 실시형태에서, 조작된 면역 세포는 세포독성 T 세포이다.
일부 실시형태에서, 본 발명은 상기 실시형태 중 임의의 것의 조작된 면역 세포 및 약제학적으로 허용 가능한 담체를 포함하는 약제학적 조성물을 제공한다. 일부 실시형태에서, 약제학적 조성물은 적어도 2가지 상이한 유형의 조작된 면역 세포를 포함한다.
일부 실시형태에서, 본 발명은 유효량의 상기 기재된 약제학적 조성물을 개체에게 투여하는 단계를 포함하는, 개체에서 전염병을 치료하는 방법을 제공한다. 일부 실시형태에서, 전염병은 HIV 및 HTLV의 군으로부터 선택되는 바이러스에 의한 간염이다. 일부 실시형태에서, 전염병은 HIV이다.
상기 방법의 일부 실시형태에서, 개체는 인간이다.
일부 실시형태에서, 본 발명은 또한 면역 세포 집단을 제공하는 단계 및 면역 세포 집단 내로 CR을 인코딩하는 제1 핵산을 도입하는 단계를 포함하는, 조작된 면역 세포를 제조하는 방법을 제공한다.
일부 실시형태에서, CCOR을 인코딩하는 제2 핵산이 면역 세포 집단 내로 도입된다. 일부 실시형태에서, 제1 핵산 및 제2 핵산은 세포에 동시에 도입된다. 다른 실시형태에서, 제1 핵산 및 제2 핵산은 세포 내로 순차적으로 도입된다. 일부 실시형태에서, 하나 이상의 COR을 인코딩하는 하나 이상의 핵산이 면역 세포 집단 내로 도입된다. 일부 실시형태에서, 제1 핵산 및 제2 핵산 및/또는 COR을 인코딩하는 핵산이 바이러스 벡터를 통해 세포 내로 도입된다.
일부 실시형태에서, 조작된 면역 세포를 제조하는 방법은 세포에서 CCR5 유전자를 비활성화시키는 단계를 더 포함한다. 일부 실시형태에서, CCR5 유전자는 CRISPR/Cas9, TALEN ZFN, siRNA, 및 안티센스 RNA로 이루어진 군으로부터 선택되는 방법을 사용하여 비활성화된다. 일부 실시형태에서, 면역 세포 집단은 개체의 말초 혈액으로부터 수득된다. 일부 실시형태에서, 면역 세포 집단은 CD4+ 세포에 대해 추가로 풍부화된다. 다른 실시형태에서, 면역 세포 집단은 CD8+ 세포에 대해 추가로 풍부화된다.
특허 출원 및 간행물을 포함하여 본 명세서에서 인용된 모든 참고문헌은 전문이 참조로 포함된다.
도 1A 및 도 1B는 항-CCR5/CXCR4 및 항-CD4를 포함하여 상이한 항원-결합 도메인을 가지는 몇몇 예시적인 수용체 분자의 개략도.
도 2A 및 도 2B는 예시적인 일반 항원(도 2B) 및 특정 항원(HIV)(도 2A) 표적화 작제물과 CXCR5 발현의 개략도.
도 3A 및 도 3B는 예시적인 일반 항원(도 3B) 및 특정 항원(HIV)(도 3A) 표적화 작제물과 CCR9 및 α4β7의 개략도.
도 4는 예시적인 HIV 표적화 작제물과 CCR5 유전자 넉아웃의 개략도.
도 5는 HIV 표적화 작제물과, CCR9 및 α4β7과, CXCR5와, CCR5 유전자 넉아웃의 개략도.
도 6A 및 도 6B는 탠덤으로 연결된 항-CD4 또는 항-CCR5 또는 항-CXCR4 scFv 또는 sdAb(도 6A) 또는 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 6B)를 함유하는 예시적인 CAR 작제물의 개략도. 도 6C는 HIV를 인식하는 광범위 중화 항체에 일렬로 연결된 항-CD4 또는 항-CCR5 scFv 또는 sdAb를 함유하는 예시적인 CAR 작제물의 개략도.
도 7은 상이한 scFv 서열을 보유하는 CAR-T의 시험관내 스크리닝 결과. 도 7A는 14가지 항-CCR5 CAR-T의 상대적 표적-사멸 효과를 나타낸다. 도 7B는 16가지 항-CD4 CAR-T의 상대적 표적-사멸 효과를 나타낸다. 도 7C는 8가지 항-CXCR4 세포의 상대적 표적-사멸 효과를 나타낸다.
도 8A 내지 도 8E는 다양한 작제물의 CAR 발현. 8A: 형질도입되지 않은 T 세포와 비교한 항-CD4-CART 번호 13 세포에서의 CAR 발현; 도 8B: 형질도입되지 않은 T 세포와 비교한 항-CCR5-CAR T 번호 13 세포에서의 CAR 발현; 도 8C: CXCR5를 발현하는 항-CD4-CAR T 세포에서의 CAR 발현. 도 8D: CXCR5를 발현하는 항-CCR5-CAR T 세포에서의 CAR 발현; 도 8E: 항-CD4/항-CCR5 탠덤 CAR T 세포, 항-CD4/항-CCR5 탠덤 CAR-CXCR5 T 세포, 항-CD4/항-CCR5 탠덤 CAR-CXCR5-C34 T 세포에서의 CAR 발현.
도 9는 시험관내에서 항-CD4 CART 번호 13 세포의 증식. 5×105개 세포를 제0일에 CAR 렌티바이러스로 형질도입하였다. 형질도입 후 제4일, 제6일, 및 제10일에 세포를 계수하였다.
도 10A 내지 도 10F는 표적 세포에 대한 다양한 CAR-T 세포의 세포독성 효과. CFSE 표지화 팬(pan) T 세포를 표적 세포로 사용하였다. 도 10A: 항-CD4 CART 번호 13 세포; 도 10B: 항-CCR5 CART 번호 13 세포; 도 10C: CXCR5를 발현하는 항-CD4 CART 세포; 도 10D: CXCR5를 발현하는 항-CCR5CAR T 세포; 도 10e: 항-CD4-항-CCR5 탠덤 CART 세포; 도 10F: 항-CD4-항-CCR5 탠덤 CAR T 세포와 항-CD4/항-CCR5 탠덤 CAR-CXCR5-C34 T 세포 간의 비교.
도 11은 항-CD4 CAR T 번호 13 세포에 의한 사이토카인의 발현. 이펙터 항-CD4 CAR T 번호 13 세포를 표적 세포와 2:1 및 0.5:1 비율로 24시간 동안 공동배양하였다. 세포 배양물로부터 상청액을 수집하고 상청액 중 사이토카인 수준을 균질 시간 분해 형광(HTRF) 분석에 의해 검출하였다.
도 12A 및 도 12B는 항-CD4 또는 항-CCR5 scFv 또는 sdAb(도 12A), 또는 일렬로 연결된 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 12B)를 함유하는 예시적인 eTCR의 개략도. 도 12C는 CD4 번호 13 CAR-T, CD4 eTCR, CD4 eTCR 번호 11의 상대적인 표적 세포 사멸 능력을 나타낸다. 도 12D는 몇몇 CCR5 eTCR 세포의 상대적인 표적 세포 사멸 능력을 나타낸다.
도 13은 eTCR T 세포 특성화의 결과. 도 13A는 항-CD4 eTCR-T 및 항-CCR5 eTCR-T 세포에서 형질도입된 유전자 발현의 검출을 나타낸다. 도 13B는 항-CD4 eTCR-T T 세포에 의한 사이토카인의 발현을 나타낸다. 이펙터 항-CD4 eTCR T 세포를 표적 세포와 2:1 및 0.5:1 비율로 24시간 동안 공동배양하였다. 세포 배양물로부터 상청액을 수집하고 상청액 중 사이토카인 수준을 HTRF 분석에 의해 검출하였다. 도 13C는 시험관내에서 항-CD4 eTCR-T 세포의 확장을 나타낸다. 5×105개 세포를 제0일에 eTCR 렌티바이러스로 형질도입하였다. 형질도입 후 제4일, 제6일, 및 제10일에 세포를 계수하였다.
도 14A 및 도 14B. 항-CD4 및 항-CCR5 eTCR-T 세포의 세포독성 효과. 항-CD4 eTCR T 세포, 항-CCR5 eTCR T 세포 또는 대조군 UnT 세포를 CFSE 표지화 1차 T 세포와 2:1 비율로 24시간 동안 공동배양하였다. CFSE+ 세포에서 CD4+%(A) 또는 CCR5+%(B)를 유세포 분석에 의해 기록하였다.
도 15A 내지 도 15D는 항-CD4 또는 항-CCR5 scFv 또는 sdAb(도 15A 및 도 15C), 또는 일렬로 연결된 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 15B 및 도 15D)를 함유하는 예시적인 CAR 또는 eTCR의 개략도. CAR T 세포 또는 eTCR T 세포는 CXCR5를 추가로 발현한다.
도 16A 및 도 16B는 CD4-CART-CXCR5 세포 및 CCR5-CART-CXCR5 세포에서 CXCR5의 발현.
도 17A 내지 도 17D는 항-CD4 또는 항-CCR5 scFv 또는 sdAb(도 17A 및 도 17C), 또는 일렬로 연결된 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 17B 및 도 17D)를 함유하는 예시적인 CAR 또는 eTCR의 개략도. CAR T 세포 또는 eTCR T 세포는 CXCR5 및 광범위 중화 항체를 추가로 발현한다.
도 18A 및 도 18B는 바이러스 부하 제어에 대한 항-CD4 CAR T 세포의 효과. 도 18A: 항-CD4 CAR T 번호 13 세포를 바이러스가 없는 표적 세포 또는 HIV 슈도바이러스 감염 표적 세포와 1:1 비율로 24시간 동안 공동배양하였다. 항-CD19 CAR-T(서열번호 77)를 대조군 CAR-T로 사용하였다. 남은 양의 표적 세포를 실시간 PCR에 의해 검출하였다. 도 18B: 항-CD4 CAR T 번호 13 세포 또는 형질도입되지 않은 T 세포를 EGFP+ 슈도-감염 표적 세포와 표시된 비율로 24시간 동안 공동배양하였다. EGFP+ 표적 세포를 유세포 분석에 의해 검출하였다.
도 19는 유인원/인간 면역결핍 바이러스(SHIV) 감염의 제어에 대한 CAR-T 효과. 히말라야 원숭이(Rhesus macaque) CD4+ T 세포를 원숭이 말초 혈액으로부터 정제하고 4일 동안 항-CD3/CD28 비드로 활성화한 후 SHIVSF162P3으로 접종하였다. SHIV 감염된 세포를 표적 세포로 사용하였으며, 3일 동안 항-CD4 CART 번호 13, 항-CCR5 CART 번호 13 및 탠덤 항-CD4/항-CCR5 CAR-T 세포와 공동배양하였다. 도 19A는 세포내 염색에 의한 바이러스 p27 항원의 존재를 나타낸다. 도 19B는 세포 배양 상청액의 바이러스 RNA 수준 및 게놈 DNA의 통합 DNA 수준을 나타낸다.
도 20A 및 도 20B는 용량 의존적 방식으로 항-CD4 CAR T 번호 13 세포가 사멸 T 세포 림프종 세포주(SupT1 및 HH)를 사멸시킨 것을 도시한 도면.
도 21A 및 도 21B는 항-CD4 CAR T 번호 13 세포의 생체 내 효능. CDX 마우스를 3개의 그룹으로 분리하였으며: 그룹 1 마우스는 HBSS를 받았고, 그룹 2 마우스는 대조군 unT 세포를 받았으며, 그룹 3 마우스는 항-CD4 CAR T 번호 13 처리를 받았다. 도 21A는 종양 부피를 나타낸다. 도 21B는 처리 후 마우스 체중을 나타낸다.
도 22A는 T 세포 표면 상의 분할 신호 CAR 작제물의 발현. ssCCR5CD4 CAR T 세포에서, 항-CCR5 모이어티를 HA 태그 및 CD3ζ 세포내 도메인과 연결하고, 항-CD4 모이어티를 Myc 태그 및 세포내 공동자극 도메인과 연결하였다. ssCD4CCR5 CAR T 세포에서, 항-CD4 모이어티를 HA 태그 및 CD3ζ 세포내 도메인에 연결하고, 항-CCR5 모이어티를 Myc 태그 및 세포내 공동자극 도메인에 연결하였다. 2개의 모이어티를 P2A에 의해 연결하였다. UNT는 형질도입되지 않은 T 세포를 나타낸다. Myc 태그의 발현을 분할 신호 CAR 시스템의 발현에 대한 대표로서 이 도면에 나타내었다. 도 22B는 작제물의 세포독성 효과를 나타낸다. CAR T 세포 또는 UNT 세포를 CFSE 표지화 표적 세포와 0.5:1 비율로 24시간 동안 공동배양하였다.
도 23A 내지 도 23C는 CAR T 요법의 생체 내 효과. 도 23A는 항-CCR5 CAR T 번호 13 세포로 처리한 HIS 마우스에서 상이한 시점에서의 CCR5+ 세포의 백분율을 나타낸다. 도 23B는 탠덤 항-CD4 항-CCR5 CAR T 세포로 처리한 HIS 마우스에서 CCR5+ 세포의 백분율을 나타낸다. 도 23C는 탠덤 항-CD4 항-CCR5 CAR T 세포로 처리한 HIS 마우스에서 CD4+ 세포의 백분율을 나타낸다.
도 2A 및 도 2B는 예시적인 일반 항원(도 2B) 및 특정 항원(HIV)(도 2A) 표적화 작제물과 CXCR5 발현의 개략도.
도 3A 및 도 3B는 예시적인 일반 항원(도 3B) 및 특정 항원(HIV)(도 3A) 표적화 작제물과 CCR9 및 α4β7의 개략도.
도 4는 예시적인 HIV 표적화 작제물과 CCR5 유전자 넉아웃의 개략도.
도 5는 HIV 표적화 작제물과, CCR9 및 α4β7과, CXCR5와, CCR5 유전자 넉아웃의 개략도.
도 6A 및 도 6B는 탠덤으로 연결된 항-CD4 또는 항-CCR5 또는 항-CXCR4 scFv 또는 sdAb(도 6A) 또는 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 6B)를 함유하는 예시적인 CAR 작제물의 개략도. 도 6C는 HIV를 인식하는 광범위 중화 항체에 일렬로 연결된 항-CD4 또는 항-CCR5 scFv 또는 sdAb를 함유하는 예시적인 CAR 작제물의 개략도.
도 7은 상이한 scFv 서열을 보유하는 CAR-T의 시험관내 스크리닝 결과. 도 7A는 14가지 항-CCR5 CAR-T의 상대적 표적-사멸 효과를 나타낸다. 도 7B는 16가지 항-CD4 CAR-T의 상대적 표적-사멸 효과를 나타낸다. 도 7C는 8가지 항-CXCR4 세포의 상대적 표적-사멸 효과를 나타낸다.
도 8A 내지 도 8E는 다양한 작제물의 CAR 발현. 8A: 형질도입되지 않은 T 세포와 비교한 항-CD4-CART 번호 13 세포에서의 CAR 발현; 도 8B: 형질도입되지 않은 T 세포와 비교한 항-CCR5-CAR T 번호 13 세포에서의 CAR 발현; 도 8C: CXCR5를 발현하는 항-CD4-CAR T 세포에서의 CAR 발현. 도 8D: CXCR5를 발현하는 항-CCR5-CAR T 세포에서의 CAR 발현; 도 8E: 항-CD4/항-CCR5 탠덤 CAR T 세포, 항-CD4/항-CCR5 탠덤 CAR-CXCR5 T 세포, 항-CD4/항-CCR5 탠덤 CAR-CXCR5-C34 T 세포에서의 CAR 발현.
도 9는 시험관내에서 항-CD4 CART 번호 13 세포의 증식. 5×105개 세포를 제0일에 CAR 렌티바이러스로 형질도입하였다. 형질도입 후 제4일, 제6일, 및 제10일에 세포를 계수하였다.
도 10A 내지 도 10F는 표적 세포에 대한 다양한 CAR-T 세포의 세포독성 효과. CFSE 표지화 팬(pan) T 세포를 표적 세포로 사용하였다. 도 10A: 항-CD4 CART 번호 13 세포; 도 10B: 항-CCR5 CART 번호 13 세포; 도 10C: CXCR5를 발현하는 항-CD4 CART 세포; 도 10D: CXCR5를 발현하는 항-CCR5CAR T 세포; 도 10e: 항-CD4-항-CCR5 탠덤 CART 세포; 도 10F: 항-CD4-항-CCR5 탠덤 CAR T 세포와 항-CD4/항-CCR5 탠덤 CAR-CXCR5-C34 T 세포 간의 비교.
도 11은 항-CD4 CAR T 번호 13 세포에 의한 사이토카인의 발현. 이펙터 항-CD4 CAR T 번호 13 세포를 표적 세포와 2:1 및 0.5:1 비율로 24시간 동안 공동배양하였다. 세포 배양물로부터 상청액을 수집하고 상청액 중 사이토카인 수준을 균질 시간 분해 형광(HTRF) 분석에 의해 검출하였다.
도 12A 및 도 12B는 항-CD4 또는 항-CCR5 scFv 또는 sdAb(도 12A), 또는 일렬로 연결된 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 12B)를 함유하는 예시적인 eTCR의 개략도. 도 12C는 CD4 번호 13 CAR-T, CD4 eTCR, CD4 eTCR 번호 11의 상대적인 표적 세포 사멸 능력을 나타낸다. 도 12D는 몇몇 CCR5 eTCR 세포의 상대적인 표적 세포 사멸 능력을 나타낸다.
도 13은 eTCR T 세포 특성화의 결과. 도 13A는 항-CD4 eTCR-T 및 항-CCR5 eTCR-T 세포에서 형질도입된 유전자 발현의 검출을 나타낸다. 도 13B는 항-CD4 eTCR-T T 세포에 의한 사이토카인의 발현을 나타낸다. 이펙터 항-CD4 eTCR T 세포를 표적 세포와 2:1 및 0.5:1 비율로 24시간 동안 공동배양하였다. 세포 배양물로부터 상청액을 수집하고 상청액 중 사이토카인 수준을 HTRF 분석에 의해 검출하였다. 도 13C는 시험관내에서 항-CD4 eTCR-T 세포의 확장을 나타낸다. 5×105개 세포를 제0일에 eTCR 렌티바이러스로 형질도입하였다. 형질도입 후 제4일, 제6일, 및 제10일에 세포를 계수하였다.
도 14A 및 도 14B. 항-CD4 및 항-CCR5 eTCR-T 세포의 세포독성 효과. 항-CD4 eTCR T 세포, 항-CCR5 eTCR T 세포 또는 대조군 UnT 세포를 CFSE 표지화 1차 T 세포와 2:1 비율로 24시간 동안 공동배양하였다. CFSE+ 세포에서 CD4+%(A) 또는 CCR5+%(B)를 유세포 분석에 의해 기록하였다.
도 15A 내지 도 15D는 항-CD4 또는 항-CCR5 scFv 또는 sdAb(도 15A 및 도 15C), 또는 일렬로 연결된 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 15B 및 도 15D)를 함유하는 예시적인 CAR 또는 eTCR의 개략도. CAR T 세포 또는 eTCR T 세포는 CXCR5를 추가로 발현한다.
도 16A 및 도 16B는 CD4-CART-CXCR5 세포 및 CCR5-CART-CXCR5 세포에서 CXCR5의 발현.
도 17A 내지 도 17D는 항-CD4 또는 항-CCR5 scFv 또는 sdAb(도 17A 및 도 17C), 또는 일렬로 연결된 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 17B 및 도 17D)를 함유하는 예시적인 CAR 또는 eTCR의 개략도. CAR T 세포 또는 eTCR T 세포는 CXCR5 및 광범위 중화 항체를 추가로 발현한다.
도 18A 및 도 18B는 바이러스 부하 제어에 대한 항-CD4 CAR T 세포의 효과. 도 18A: 항-CD4 CAR T 번호 13 세포를 바이러스가 없는 표적 세포 또는 HIV 슈도바이러스 감염 표적 세포와 1:1 비율로 24시간 동안 공동배양하였다. 항-CD19 CAR-T(서열번호 77)를 대조군 CAR-T로 사용하였다. 남은 양의 표적 세포를 실시간 PCR에 의해 검출하였다. 도 18B: 항-CD4 CAR T 번호 13 세포 또는 형질도입되지 않은 T 세포를 EGFP+ 슈도-감염 표적 세포와 표시된 비율로 24시간 동안 공동배양하였다. EGFP+ 표적 세포를 유세포 분석에 의해 검출하였다.
도 19는 유인원/인간 면역결핍 바이러스(SHIV) 감염의 제어에 대한 CAR-T 효과. 히말라야 원숭이(Rhesus macaque) CD4+ T 세포를 원숭이 말초 혈액으로부터 정제하고 4일 동안 항-CD3/CD28 비드로 활성화한 후 SHIVSF162P3으로 접종하였다. SHIV 감염된 세포를 표적 세포로 사용하였으며, 3일 동안 항-CD4 CART 번호 13, 항-CCR5 CART 번호 13 및 탠덤 항-CD4/항-CCR5 CAR-T 세포와 공동배양하였다. 도 19A는 세포내 염색에 의한 바이러스 p27 항원의 존재를 나타낸다. 도 19B는 세포 배양 상청액의 바이러스 RNA 수준 및 게놈 DNA의 통합 DNA 수준을 나타낸다.
도 20A 및 도 20B는 용량 의존적 방식으로 항-CD4 CAR T 번호 13 세포가 사멸 T 세포 림프종 세포주(SupT1 및 HH)를 사멸시킨 것을 도시한 도면.
도 21A 및 도 21B는 항-CD4 CAR T 번호 13 세포의 생체 내 효능. CDX 마우스를 3개의 그룹으로 분리하였으며: 그룹 1 마우스는 HBSS를 받았고, 그룹 2 마우스는 대조군 unT 세포를 받았으며, 그룹 3 마우스는 항-CD4 CAR T 번호 13 처리를 받았다. 도 21A는 종양 부피를 나타낸다. 도 21B는 처리 후 마우스 체중을 나타낸다.
도 22A는 T 세포 표면 상의 분할 신호 CAR 작제물의 발현. ssCCR5CD4 CAR T 세포에서, 항-CCR5 모이어티를 HA 태그 및 CD3ζ 세포내 도메인과 연결하고, 항-CD4 모이어티를 Myc 태그 및 세포내 공동자극 도메인과 연결하였다. ssCD4CCR5 CAR T 세포에서, 항-CD4 모이어티를 HA 태그 및 CD3ζ 세포내 도메인에 연결하고, 항-CCR5 모이어티를 Myc 태그 및 세포내 공동자극 도메인에 연결하였다. 2개의 모이어티를 P2A에 의해 연결하였다. UNT는 형질도입되지 않은 T 세포를 나타낸다. Myc 태그의 발현을 분할 신호 CAR 시스템의 발현에 대한 대표로서 이 도면에 나타내었다. 도 22B는 작제물의 세포독성 효과를 나타낸다. CAR T 세포 또는 UNT 세포를 CFSE 표지화 표적 세포와 0.5:1 비율로 24시간 동안 공동배양하였다.
도 23A 내지 도 23C는 CAR T 요법의 생체 내 효과. 도 23A는 항-CCR5 CAR T 번호 13 세포로 처리한 HIS 마우스에서 상이한 시점에서의 CCR5+ 세포의 백분율을 나타낸다. 도 23B는 탠덤 항-CD4 항-CCR5 CAR T 세포로 처리한 HIS 마우스에서 CCR5+ 세포의 백분율을 나타낸다. 도 23C는 탠덤 항-CD4 항-CCR5 CAR T 세포로 처리한 HIS 마우스에서 CD4+ 세포의 백분율을 나타낸다.
본 출원은 CCR5(또는 CXCR4) 및 CD4 중 어느 하나로부터 선택되는 CR 표적 항원을 특이적으로 인식하는 키메라 수용체("CR")를 발현하는 면역 세포(예컨대, T 세포) 및 면역 세포를 활성화시킬 수 있는 세포내 CR 신호전달 도메인을 제공한다. 일부 실시형태에서, CR이 공동자극 도메인을 함유하지 않는 경우, CR은 키메라 공동 수용체("CCOR") 공동자극 도메인을 함유하고 CCR5(또는 CXCR4) 또는 CD4(CCOR 표적 항원) 중 다른 하나를 특이적으로 인식하는 키메라 공동수용체("CCOR")와 함께 공동발현될 수 있다. 따라서 CCOR은 CCOR 표적 항원의 결합 시 필요한 공동자극을 제공하여, 면역 세포가 CR 표적 항원 및 CCOR 표적 항원이 둘 다 존재하고 면역 세포에 의해 인식될 때에만 활성화되는 것을 보장한다. 면역 세포는 하나 이상의 공동수용체("COR"), 예를 들어 여포(CXCR5 수용체), 및 내장(α4β7 수용체 또는 CCR9 수용체)와 같은 원하는 위치로 면역 세포의 이동을 촉진시키는 공동수용체를 추가로 발현할 수 있다. 추가적으로, 면역 세포는 추가로 변형되어 CCR5 수용체의 발현을 감소시키거나 넉아웃시켜, 바이러스 감염에 대한 면역 세포(예컨대, CD4+ 면역 세포)의 내성을 증가시킬 수 있다.
따라서, 일 양태에서 본 발명은 CR 및 CCOR을 포함하는 면역 세포를 제공한다. 또 다른 양태에서, CR 및 COR을 포함하는 면역 세포가 제공된다. 일부 실시형태에서, 면역 세포는 CR, CCOR, 및 하나 이상의 COR을 포함한다. 일부 실시형태에서, 면역 세포는 추가로 변형되어 CCR5의 발현을 감소시키거나 넉아웃시킨다.
또한, 면역 세포에서 CR, CCOR 및/또는 COR을 발현하는 핵산 시스템이 제공된다.
또한 치료 목적을 위해 조작된 면역 세포를 제조하고 사용하는 방법뿐만 아니라, 이와 같은 방법에 유용한 키트 및 제조 물품이 제공된다.
정의
본 명세서에서 용어 "항체"는 가장 광범위한 의미로 사용되며 구체적으로 원하는 생물학적 활성을 나타내는 한 단클론성 항체(전장 단클론성 항체를 포함함), 다중특이적 항체(예를 들어, 이중특이적 항체), 및 항체 단편을 포괄한다.
용어 "천연 항체", "전장 항체", "온전한 항체" 및 "전체 항체"는 하기 정의된 바와 같이 항체 단편이 아니라 실질적으로 온전한 형태의 항체를 말하기 위해 본 명세서에서 상호교환적으로 사용된다. 상기 용어는 특히 Fc 영역을 함유하는 중쇄를 가지는 항체를 지칭한다. 천연 항체는 보통 2개의 동일한 경쇄(L) 및 2개의 동일한 중쇄(H)로 구성된, 약 150,000 달톤의 이종사량체 당단백질이다. 각각의 경쇄는 하나의 공유 이황화 결합에 의해 중쇄에 연결되는 한편, 이황화 연결의 수는 상이한 면역글로불린 아이소타입의 중쇄에 따라 다르다. 각각의 중쇄 및 경쇄는 또한 규칙적으로 이격된 사슬내 이황화 다리를 가진다. 각각의 중쇄는 하나의 말단에 가변 도메인(VH)을 가지고, 그 다음에 다수의 불변 도메인을 가진다. 각각의 경쇄는 하나의 말단에 가변 도메인(VL)을 가지고 다른 말단에 불변 도메인을 가지며; 경쇄의 불변 도메인은 중쇄의 제1 불변 도메인과 정렬되고, 경쇄 가변 도메인은 중쇄의 가변 도메인과 정렬된다. 특정 아미노산 잔기는 경쇄와 중쇄 가변 도메인 사이의 인터페이스를 형성하는 것으로 여겨진다.
용어 "불변 도메인"은 항원 결합 부위를 함유하는 면역글로불린의 다른 부분, 즉 가변 도메인에 비해 보다 보존된 아미노산 서열을 가지는 면역글로불린 분자의 부분을 지칭한다. 불변 도메인은 중쇄의 CH1, CH2 및 CH3 도메인(총칭하여, CH) 및 경쇄의 CHL(또는 CL) 도메인을 함유한다.
항체의 "가변 영역" 또는 "가변 도메인"은 항체의 중쇄 또는 경쇄의 아미노-말단 도메인을 지칭한다. 중쇄의 가변 도메인은 "VH"로 지칭될 수 있다. 경쇄의 가변 도메인은 "VL"로 지칭될 수 있다. 이들 도메인은 일반적으로 항체의 가장 가변적인 부분이며 항원-결합 부위를 함유한다.
용어 "가변"은 가변 도메인의 특정 부분이 항체 간에 서열이 광범위하게 상이하고 특정 항원에 대한 각각의 특정 항체의 결합 및 특이성에서 사용된다는 사실을 지칭한다. 그러나, 가변성은 항체의 가변 도메인 전체에 걸쳐 고르게 분포되어 있지 않다. 경쇄 및 중쇄 가변 도메인 둘 다에서 초가변 영역(HVR)이라 불리는 3개의 절편에 집중되어 있다. 가변 도메인의 보다 고도로 보존된 부분은 프레임워크 영역(FR)이라 불린다. 천연 중쇄 및 경쇄의 가변 도메인은 각각 4개의 FR 영역을 포함하는데, FR 영역은 루프 연결을 형성하는 3개의 HVR로 연결되는 베타-시트 구성을 채택하고, 일부 경우에는 베타-시트 구조의 일부를 형성한다. 각각의 사슬에서 HVR은 FR 영역에 의해 매우 근접하게 함께 유지되며, 다른 사슬로부터의 HVR과 함께 항체의 항원-결합 부위의 형성에 기여한다(문헌[Kabat et al., Sequences of Proteins of Immunological Interest, Fifth Edition, National Institute of Health, Bethesda, Md. (1991)] 참조). 불변 도메인은 항원에 대한 항체의 결합에 직접 관여하지 않지만, 항체-의존성 세포 독성에서 항체의 참여와 같은 다양한 이펙터 기능을 나타낸다.
임의의 포유동물 종 유래의 항체(면역글로불린)의 "경쇄"는 항체의 불변 도메인의 아미노산 서열을 기반으로 카파("κ") 및 람다("λ")라 불리는 2가지 명확하게 구별되는 유형 중 하나에 할당될 수 있다.
본 명세서에서 사용되는 바와 같이 용어 IgG "아이소타입" 또는 "하위부류"는 면역글로불린의 불변 영역의 화학적 및 항원적 특징에 의해 정의된 면역글로불린의 하위부류 중 임의의 것을 의미한다.
중쇄의 불변 도메인의 아미노산 서열에 따라, 항체(면역글로불린)는 상이한 부류에 할당될 수 있다. 면역글로불린의 5가지 주요 부류, 즉 IgA, IgD, IgE, IgG, 및 IgM이 있으며, 이들 중 몇몇은 하위부류(아이소타입), 예를 들어 IgG1, IgG2, IgG3, IgG4, IgA1, 및 IgA2로 추가로 나뉠 수 있다. 상이한 부류의 면역글로불린에 해당하는 중쇄 불변 도메인은 각각 α, γ, ε, γ, 및 μ로 불린다. 상이한 부류의 면역글로불린의 서브유닛 구조 및 3차원 배열은 잘 알려져 있으며, 예를 들어 문헌[Abbas et al. Cellular and Mol. Immunology, 4th ed. (W.B. Saunders, Co., 2000)]에 일반적으로 기재되어 있다. 항체는 하나 이상의 다른 단백질 또는 펩타이드와 항체의 공유 또는 비-공유 회합에 의해 형성되는 더 큰 융합 분자의 일부일 수 있다.
용어 "전장 항체", "온전한 항체" 및 "전체 항체"는 하기 정의된 바와 같이 항체 단편이 아니라 실질적으로 온전한 형태의 항체를 말하기 위해 본 명세서에서 상호교환적으로 사용된다. 상기 용어는 특히 Fc 영역을 함유하는 중쇄를 가지는 항체를 지칭한다.
"항체 단편"은, 바람직하게는 온전한 항체의 항원 결합 영역을 포함하는, 온전한 항체의 부분을 포함한다. 일부 실시형태에서, 본 명세서에 기재된 항체 단편은 항원-결합 단편이다. 항체 단편의 예는 Fab, Fab', F(ab')2, 및 Fv 단편; 디아바디(diabody); 선형 항체; 단일-사슬 항체 분자; 및 항체 단편으로 형성된 다중특이적 항체를 포함한다.
항체의 파파인 분해는 "Fab" 단편이라 불리는 2개의 동일한 항원-결합 단편을 생성하며, 이들 단편은 각각 단일 항원-결합 부위, 및 잔류 "Fc" 단편(이의 명칭은 용이하게 결정화하는 능력을 반영함)을 가진다. 펩신 처리는 2개의 항원-결합 부위를 가지고 여전히 항원을 가교할 수 있는 F(ab')2 단편을 생성한다.
"Fv"는 완전한 항원-결합 부위를 함유하는 최소 항체 단편이다. 일 실시형태에서, 2-사슬 Fv 종은 단단한 비-공유 회합으로 하나의 중쇄 및 하나의 경쇄 가변 도메인의 이량체로 이루어진다. 단일-사슬 Fv(scFv) 종에서, 2-사슬 Fv 종에서와 유사하게 경쇄 및 중쇄가 "이량체" 구조로 회합될 수 있도록 하나의 중쇄 및 하나의 경쇄 가변 도메인은 가요성 펩타이드 링커에 의해 공유적으로 연결될 수 있다. 이 배열에서 각각의 가변 도메인의 3개의 HVR은 상호작용하여 VH-VL 이량체의 표면에서 항원-결합 부위를 한정한다. 총체적으로, 6개의 HVR은 항체에 항원-결합 특이성을 부여한다. 그러나, 심지어 단일 가변 도메인(또는 항원에 특이적인 3개의 HVR만을 포함하는 Fv의 절반)도, 전체 결합 부위보다 더 낮은 친화성이기는 하지만, 항원을 인식하고 결합하는 능력을 가진다.
Fab 단편은 중쇄 및 경쇄 가변 도메인을 함유하고 또한 경쇄의 불변 도메인 및 중쇄의 제1 불변 도메인(CH1)을 함유한다. Fab' 단편은 항체 힌지 영역으로부터 하나 이상의 시스테인을 포함하여 중쇄 CH1 도메인의 카복시 말단에서 몇 개의 잔기를 추가한다는 점에서 Fab 단편과 상이하다. Fab'-SH는 본 명세서에서 불변 도메인의 시스테인 잔기(들)가 유리 티올기를 보유하는 Fab'에 대한 명칭이다. F(ab')2 항체 단편은 원래 Fab' 단편 사이에 힌지 시스테인을 가지는 Fab' 단편의 쌍으로 생성되었다. 항체 단편의 다른 화학적 커플링도 또한 알려져 있다.
"단일-사슬 Fv" 또는 "scFv" 항체 단편은 항체의 VH 및 VL 도메인을 포함하며, 여기서 이들 도메인은 단일 폴리펩타이드 사슬에 존재한다. 일반적으로, scFv 폴리펩타이드는 scFv가 항원 결합을 위해 원하는 구조를 형성할 수 있도록 하는 VH 및 VL 도메인 사이에 폴리펩타이드 링커를 더 포함한다. scFv에 대한 검토를 위하여, 예를 들어 문헌[, The Pharmacology of Monoclonal Antibodies. Springer Berlin Heidelberg, 1994. 269-315]을 참조한다.
용어 "디아바디"는 2개의 항원-결합 부위를 가지는 항체 단편을 말하며, 상기 단편은 동일한 폴리펩타이드 사슬(VH-VL)에서 경쇄 가변 도메인(VL)에 연결된 중쇄 가변 도메인(VH)을 포함한다. 동일한 사슬 상의 2개의 도메인 사이에 쌍형성을 가능하게 하기에 너무 짧은 링커를 사용함으로써, 도메인은 또 다른 사슬의 상보적 도메인과 쌍을 형성하여 2개의 항원-결합 부위를 형성하게 한다. 디아바디는 2가 또는 이중특이적일 수 있다. 디아바디는, 예를 들어 EP 404,097; WO 1993/01161; 문헌[Hudson et al., Nat. Med. 9:129-134 (2003)]; 및 [Hollinger et al., Proc. Natl. Acad. Sci. USA 90: 6444-6448 (1993)]에 보다 자세히 기재되어 있다. 트리아바디(triabody) 및 테트라바디(tetrabody)는 또한 문헌[Hudson et al., Nat. Med. 9:129-134 (2003)]에 기재되어 있다.
용어 "중쇄-단독 항체" 또는 "HCAb"는 중쇄를 포함하지만 보통 항체에서 발견되는 경쇄가 없는 기능적 항체를 지칭한다. 낙타과 동물(예컨대, 낙타, 라마, 또는 알파카)은 HCAb를 생성하는 것으로 알려져 있다.
용어 "단일 도메인 항체" 또는 "sdAb"는 단일 단량체 가변 항체 도메인으로 이루어진 항체 단편을 지칭한다. 일부 경우에, 단일 도메인 항체는 낙타과 HCAb로부터 조작되고, 이와 같은 sdAb는 본 명세서에서 "나노바디" 또는 "VHHs"로 지칭된다. 낙타과 sdAb는 알려진 가장 작은 항원-결합 항체 단편 중 하나이다(예를 들어, 문헌[Hamers-Casterman et al., Nature 363:446-8 (1993)]; [Greenberg et al., Nature 374:168-73 (1995)]; [Hassanzadeh-Ghassabeh et al., Nanomedicine (Lond), 8:1013-26 (2013)] 참조).
본 명세서에서 사용되는 바와 같은 용어 "단클론성 항체"는 실질적으로 균질한 항체 집단으로부터 수득된 항체를 말하며, 예를 들어 상기 집단을 포함하는 개별 항체는 소량으로 존재할 수 있는 가능한 돌연변이, 예를 들어 자연 발생 돌연변이를 제외하고 동일하다. 따라서, 수식어 "단클론성"은 개별 항체의 혼합물이 아닌 항체의 특징을 나타낸다. 특정 실시형태에서, 이와 같은 단클론성 항체는 전형적으로 표적에 결합하는 폴리펩타이드 서열을 포함하는 항체를 포함하며, 여기서 표적-결합 폴리펩타이드 서열은 복수의 폴리펩타이드 서열로부터 단일 표적 결합 폴리펩타이드 서열의 선택을 포함하는 과정에 의해 수득되었다. 예를 들어, 선택 과정은 복수의 클론, 예컨대, 하이브리도마 클론, 파지 클론, 또는 재조합 DNA 클론의 풀(pool)로부터 고유한 클론을 선택하는 것일 수 있다. 선택된 표적 결합 서열은, 예를 들어 표적에 대한 친화성을 개선시키기 위해, 표적 결합 서열을 인간화하기 위해, 세포 배양에서 이의 생성을 개선시키기 위해, 생체 내에서 이의 면역원성을 감소시키기 위해, 다중특이적 항체를 생성하기 위해 등등, 추가로 변경될 수 있으며, 변경된 표적 결합 서열을 포함하는 항체는 또한 본 발명의 단클론성 항체라는 것이 이해되어야 한다. 전형적으로 상이한 결정자(에피토프)에 대한 상이한 항체를 포함하는 다클론성 항체 제조와 대조적으로, 단클론성 항체 제조의 각각의 단클론성 항체는 항원 상의 단일 결정자에 대한 것이다. 이러한 특이성에 추가적으로, 단클론성 항체 제조는 전형적으로 다른 면역글로불린에 의해 오염되지 않는다는 점에서 유리하다.
수식어 "단클론성"은 실질적으로 균질한 항체 집단으로부터 수득되는 항체의 특징을 나타내며, 임의의 특정 방법에 의한 항체 생성을 필요로 하는 것으로 해석되어서는 안된다. 예를 들어, 본 발명에 따라 사용되는 단클론성 항체는, 예를 들어 하이브리도마 방법(예를 들어, 문헌[Kohler and Milstein, Nature 256:495-97 (1975)]; [Hongo et al., Hybridoma 14 (3): 253-260 (1995)], [Harlow et al., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2nd ed. 1988)]; [Hammerling et al., Monoclonal Antibodies and T-Cell Hybridomas 563-681 (Elsevier, N.Y., 1981)]), 재조합 DNA 방법(예를 들어, 미국 특허 제4,816,567호 참조), 파지-디스플레이 기술(예를 들어, 문헌[Clackson et al., Nature 352: 624-628 (1991)]; [Marks et al., J. Mol. Biol. 222: 581-597 (1992)]; [Sidhu et al., J. Mol. Biol. 338(2): 299-310 (2004)]; [Lee et al., J. Mol. Biol. 340(5): 1073-1093 (2004)]; [Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004)]; 및 [Lee et al., J. Immunol. Methods 284(1-2): 119-132 (2004)] 참조), 및 인간 면역글로불린 서열을 인코딩하는 유전자 또는 인간 면역글로불린 유전자좌의 일부 또는 전부를 가지는 동물에서 인간 또는 인간-유사 항체를 생성하는 기술(예를 들어, WO 1998/24893; WO 1996/34096; WO 1996/33735; WO 1991/10741; 문헌[Jakobovits et al., Proc. Natl. Acad. Sci. USA 90: 2551 (1993)]; [Jakobovits et al., Nature 362: 255-258 (1993)]; [Bruggemann et al., Year in Immunol. 7:33 (1993)]; 미국 특허 제5,545,807호; 제5,545,806호; 제5,569,825호; 제5,625,126호; 제5,633,425호; 및 제5,661,016호; 문헌[Marks et al., Bio/Technology 10: 779-783 (1992)]; [Lonberg et al., Nature 368: 856-859 (1994)]; [Morrison, Nature 368: 812-813 (1994)]; [Fishwild et al., Nature Biotechnol. 14: 845-851 (1996)]; [Neuberger, Nature Biotechnol. 14: 826 (1996)]; 및 [Lonberg and Huszar, Intern. Rev. Immunol. 13: 65-93 (1995)] 참조)을 포함하여, 다양한 기법에 의해 제조될 수 있다.
본 명세서에서 단클론성 항체는 구체적으로, 원하는 생물학적 활성을 나타내는 한, 중쇄 및/또는 경쇄의 일부가 특정 항체 부류 또는 하위부류에 속하거나 특정 종으로부터 유래된 항체에서 해당하는 서열과 동일하거나 이와 상동성인 한편, 사슬(들)의 나머지는 또 다른 항체 부류 또는 하위부류에 속하거나 또 다른 종으로부터 유래된 항체뿐만 아니라 이와 같은 항체의 단편에서 해당하는 서열과 동일하거나 이와 상동성인 "키메라" 항체를 포함한다(예를 들어, 미국 특허 제4,816,567호; 및 문헌[Morrison et al., Proc. Natl. Acad. Sci. USA 81:6851-6855 (1984)] 참조). 키메라 항체는 항체의 항원-결합 영역이, 예를 들어 관심 항원으로 짧은 꼬리 원숭이(macaque monkey)를 면역화시킴으로써 생성된 항체로부터 유래된 PRIMATTZED® 항체를 포함한다.
비-인간(예를 들어, 뮤린) 항체의 "인간화" 형태는 비-인간 면역글로불린으로부터 유래된 최소 서열을 함유하는 키메라 항체이다. 일 실시형태에서, 인간화 항체는 수용자의 HVR 유래의 잔기가 원하는 특이성, 친화성, 및/또는 능력을 가지는 비-인간 종(공여자 항체), 예컨대, 마우스, 래트, 토끼, 또는 비인간 영장류의 HVR 유래의 잔기로 대체된 인간 면역글로불린(수용자 항체)이다. 일부 예에서, 인간 면역글로불린의 FR 잔기는 상응하는 비-인간 잔기로 대체된다. 또한, 인간화 항체는 수용자 항체에서 또는 공여자 항체에서 발견되지 않는 잔기를 포함할 수 있다. 이러한 변형은 항체 성능을 추가로 개량하기 위해 이루어질 수 있다. 일반적으로, 인간화 항체는 적어도 하나, 및 전형적으로 2개의 가변 도메인의 전부를 실질적으로 포함할 것이며, 여기서 초가변 루프의 전부 또는 실질적으로 전부는 비-인간 면역글로불린의 것에 상응하고, FR의 전부 또는 실질적으로 전부는 인간 면역글로불린 서열의 것이다. 인간화 항체는 선택적으로 또한 면역글로불린 불변 영역(Fc)의 적어도 일부, 전형적으로 인간 면역글로불린의 것을 포함할 것이다. 추가의 세부 사항은, 예를 들어 문헌[Jones et al., Nature 321:522-525 (1986)]; [Riechmann et al., Nature 332:323-329 (1988)]; 및 [Presta, Curr. Op. Struct. Biol. 2:593-596 (1992)]을 참조한다. 또한, 예를 들어 문헌[Vaswani and Hamilton, Ann. Allergy, Asthma & Immunol. 1:105-115 (1998)]; [Harris, Biochem. Soc. Transactions 23:1035-1038 (1995)]; [Hurle and Gross, Curr. Op. Biotech. 5:428-433 (1994)]; 및 미국 특허 제6,982,321호 및 제7,087,409호를 참조한다.
"인간 항체"는 인간에 의해 생성되고/되거나 본 명세서에 개시된 바와 같은 인간 항체를 제조하기 위한 임의의 기법을 사용하여 제조된 항체의 아미노산 서열에 상응하는 아미노산 서열을 가지는 것이다. 인간 항체의 이러한 정의는 구체적으로 비-인간 항원-결합 잔기를 포함하는 인간화 항체를 배제한다. 인간 항체는 파지-디스플레이 라이브러리를 포함하여, 당업계에 알려진 다양한 기법을 사용하여 생성될 수 있다. Hoogenboom and Winter, J. Mol. Biol. 227:381 (1991); Marks et al., J. Mol. Biol. 222:581 (1991). 또한, 인간 단클론성 항체의 제조를 위해 문헌[Cole et al., Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, 77 (1985)]; [Boerner et al., J. Immunol. 147(1):86-95 (1991)]에 기재된 방법이 이용 가능하다. 또한 문헌[van Dijk and van de Winkel, Curr. Opin. Pharmacol. 5: 368-74 (2001)]을 참조한다. 인간 항체는 항원 접종에 반응하여 이와 같은 항체를 생성하도록 변형되었지만, 이의 내인성 유전자좌가 무능화된 유전자이식 동물, 예를 들어 면역화된 제노마우스(xenomice)에 항원을 투여함으로써 제조될 수 있다(예를 들어, 제노마우스(XENOMOUSE)(상표) 기술과 관련하여 미국 특허 제6,075,181호 및 제6,150,584호 참조). 또한, 예를 들어 인간 B-세포 하이브리도마 기술을 통하여 생성된 인간 항체와 관련하여 문헌[Li et al., Proc. Natl. Acad. Sci. USA 103:3557-3562 (2006)]을 참조한다.
본 명세서에서 사용되는 바와 같이, 용어 "결합한다", "~에 특이적으로 결합한다" 또는 "~에 특이적이다"는 측정가능하고 재현가능한 상호작용, 예컨대, 표적과 항체 사이의 결합을 말하며, 이는 생물학적 분자를 포함하여 이질적인 분자 집단의 존재 하에 표적의 존재의 결정인자이다. 예를 들어, 표적(이는 에피토프일 수 있음)에 결합하거나 이에 특이적으로 결합하는 항체는 다른 표적에 결합하는 것보다 더 큰 친화성, 결합성을 가지고 더 용이하게, 및/또는 더 긴 기간 동안 이러한 표적에 결합하는 항체이다. 일 실시형태에서, 비관련 표적에 대한 항체의 결합 정도는, 예를 들어 방사면역측정법(RIA)에 의해 측정될 때, 표적에 대한 항체의 결합의 약 10% 미만이다. 특정 실시형태에서, 표적에 특이적으로 결합하는 항체는 1μM 이하, 100nM 이하, 10nM 이하, 1nM 이하 또는 0.1nM 이하의 해리 상수(Kd)를 가진다. 특정 실시형태에서, 항체는 상이한 종 유래의 단백질 중에서 보존되는 단백질 상의 에피토프에 특이적으로 결합한다. 또 다른 실시형태에서, 특이적 결합은 배타적 결합을 포함할 수 있지만 이를 필요로 하지 않는다.
본 명세서에서 사용되는 바와 같이 "키메라 항원 수용체" 또는 "CAR"은, T 세포와 같은 세포에 하나 이상의 항원 특이성을 이식하는 유전적으로 조작된 수용체를 지칭한다. CAR은 또한 "인공 T-세포 수용체", "키메라 T 세포 수용체", 또는 "키메라 면역 수용체"로도 알려져 있다. 일부 실시형태에서, CAR은 종양 항원에 특이적인 항체의 세포외 가변 도메인, 및 T 세포 또는 다른 수용체의 세포내 신호전달 도메인, 예컨대, 하나 이상의 공동자극 도메인을 포함한다. "CAR-T"는 CAR을 발현하는 T 세포를 지칭한다.
본 명세서에서 사용되는 바와 같이 "T 세포 수용체" 또는 "TCR"은 MHC 분자에서 결합된 특정 항원 펩타이드에 결합하는 세포외 항원 결합 도메인을 포함하는 내인성 또는 재조합 T 세포 수용체를 지칭한다. 일부 실시형태에서, TCR은 TCRα 폴리펩타이드 사슬 및 TCRβ 폴리펩타이드 사슬을 포함한다. 일부 실시형태에서, TCR은 종양 항원에 특이적으로 결합한다.
용어 "재조합"은 (1) 천연 발생 환경에서 제거되었거나, (2) 유전자가 자연에서 발견되는 폴리펩타이드의 전부 또는 일부와 연관되지 않거나, (3) 자연에서 연결되어 있지 않은 폴리뉴클레오타이드와 작동적으로 연결되거나, (4) 자연에서 발생하지 않는 생체분자, 예를 들어 유전자 또는 단백질을 지칭한다. 용어 "재조합"은 클로닝된 DNA 단리물, 화학적으로 합성된 폴리뉴클레오타이드 유사체, 또는 이종성 시스템에 의해 생물학적으로 합성된 폴리뉴클레오타이드 유사체뿐만 아니라, 이와 같은 핵산에 의해 인코딩된 단백질 및/또는 mRNA와 관련하여 사용될 수 있다.
용어 "발현하다"는 핵산을 단백질로 번역하는 것을 지칭한다. 단백질은 발현되어 세포내에 남아있거나, 세포 표면 막의 구성요소가 되거나, 세포외 기질 또는 배지로 분비될 수 있다.
용어 "숙주 세포"는 발현 벡터의 복제 또는 발현을 지원할 수 있는 세포를 지칭한다. 숙주 세포는 원핵 세포, 예컨대, 대장균(이.콜라이(E.coli)), 또는 진핵 세포, 예컨대, 효모, 곤충 세포, 양서류 세포, 또는 포유동물 세포일 수 있다.
본 명세서에서 사용되는 바와 같이 용어 "형질감염된" 또는 "형질전환된" 또는 "형질도입된"은 외인성 핵산이 숙주 세포 내로 전달되거나 도입되는 과정을 지칭한다. "형질감염된" 또는 "형질전환된" 또는 "형질도입된" 세포는 외인성 핵산이 형질감염, 형질전환 또는 형질도입된 것이다.
용어 "생체 내"는 세포가 수득되는 유기체의 체내를 지칭한다. "생체 외" 또는 "시험관내"는 세포가 수득되는 유기체의 체외를 의미한다.
용어 "세포"는 1차 대상체 세포 및 이의 자손을 포함한다.
CD3을 발현하는 세포와 관련하여 본 명세서에서 사용되는 바와 같이 "활성화"는 세포 증식 및 사이토카인 생성을 포함하지만 이들로 제한되는 것은 아닌 CD3 신호전달 경로의 하류 이펙터 기능의 검출가능한 증가를 유도하도록 충분히 자극된 세포의 상태를 지칭한다.
단백질의 일부를 말할 때 용어 "도메인"은 단백질을 구성하는 하나 이상의 폴리펩타이드의 구조적 및/또는 기능적 관련 부분을 포함하는 것을 의미한다. 예를 들어, 이량체 수용체의 막관통 도메인은 막에 걸쳐 있는 수용체의 각각의 폴리펩타이드 사슬의 부분을 말할 수 있다. 도메인은 또한 단일 폴리펩타이드 사슬의 관련 부분을 말할 수 있다. 예를 들어, 단량체 수용체의 막관통 도메인은 막에 걸쳐 있는 수용체의 단일 폴리펩타이드 사슬의 부분을 말할 수 있다. 도메인은 또한 폴리펩타이드의 단일 부분만을 포함할 수 있다.
본 명세서에서 사용되는 바와 같은 용어 "단리된 핵산"은 게놈, cDNA, 또는 합성 기원의 핵산 또는 이들의 일부 조합을 의미하는 것으로 의도되며, 그 기원으로 인해 "단리된 핵산"은 (1) "단리된 핵산"이 자연에서 발견되는 폴리뉴클레오타이드의 전부 또는 일부와 연관되지 않거나, (2) 자연에서 연결되지 않는 폴리뉴클레오타이드와 작동 가능하게 연결되거나, (3) 더 큰 서열의 부분으로서 자연에서 발생하지 않는다.
달리 명시되지 않는 한, "아미노산 서열을 인코딩하는 뉴클레오타이드 서열"은 서로 축퇴 형태이고 동일한 아미노산 서열을 인코딩하는 모든 뉴클레오타이드 서열을 포함한다. 어구 "단백질 또는 RNA를 인코딩하는 뉴클레오타이드 서열"은 또한 단백질을 인코딩하는 뉴클레오타이드 서열이 일부 형태에서 인트론(들)을 함유할 수 있을 정도로 인트론을 포함할 수 있다.
용어 "작동 가능하게 연결된"은 이종성 핵산 서열의 발현을 초래하는 조절 서열과 이종성 핵산 서열 사이의 기능적 연결을 지칭한다. 예를 들어, 제1 핵산 서열이 제2 핵산 서열과 기능적 관계에 있을 때, 제1 핵산 서열은 제2 핵산 서열에 작동 가능하게 연결된다. 예를 들어, 프로모터가 코딩 서열의 전사 또는 발현에 영향을 미치는 경우, 프로모터는 코딩 서열에 작동 가능하게 연결된다. 일반적으로, 작동 가능하게 연결된 DNA 서열은 연속적이며, 필요한 경우 동일한 리딩 프레임에서 2개의 단백질 코딩 영역을 연결한다.
용어 "유도성 프로모터"는 하나 이상의 특정 신호를 추가하거나 제거함으로써 활성이 조절될 수 있는 프로모터를 지칭한다. 예를 들어, 유도성 프로모터는 특정 조건 세트 하에서, 예를 들어 프로모터를 활성화시키고/시키거나 프로모터의 저해를 완화하는 조건 또는 유도제의 존재 하에 작동적으로 연결된 핵산의 전사를 활성화시킬 수 있다.
본 명세서에서 사용되는 바와 같이, "치료" 또는 "치료하는"은 임상 결과를 포함하여, 유익하거나 원하는 결과를 얻기 위한 접근법이다. 본 발명의 목적을 위해, 유익하거나 원하는 임상 결과는 다음 중 하나 이상을 포함하지만 이들로 제한되는 것은 아니다: 질환으로 인한 하나 이상의 증상의 완화, 질환의 정도 감소, 질환의 안정화(예를 들어, 질환의 악화의 방지 또는 지연), 질환의 확산(예를 들어, 전이)의 방지 또는 지연, 질환의 재발의 방지 또는 지연, 질환의 진행의 지연 또는 늦춤, 질환 상태의 개선, 질환의 (부분적 또는 전체적) 완화의 제공, 질환의 치료에 필요한 하나 이상의 다른 약제 용량의 감소, 질환 진행의 지연, 삶의 질의 증가 또는 개선, 체중 증가, 및/또는 생존 연장. 또한 "치료"는 질환의 병리학적 결과(예를 들어, 암에서 종양 부피)의 감소를 포함한다. 본 발명의 방법은 이러한 치료 양태 중 임의의 하나 이상을 고려한다.
용어 "치료적 유효량"은 개체에서 질환 또는 장애를 "치료"하는 데 효과적인 본 명세서에 개시된 바와 같은 조성물의 양을 지칭한다. 전염병의 경우에, 환자의 상태를 개선할 수 있는 조성물을 포함하는 조성물의 치료적 유효량.
본 명세서에서 사용되는 바와 같이, "약제학적으로 허용 가능한" 또는 "약리학적으로 양립가능한"은 생물학적으로 또는 달리 바람직하지 않은 것이 아닌 물질을 의미하며, 예를 들어 상기 물질은 어떠한 상당한 바람직하지 않은 생물학적 효과를 야기하거나 조성물에 함유되는 조성물의 다른 구성요소 중 임의의 것과 유해한 방식으로 상호작용하지 않으면서 환자에게 투여되는 약제학적 조성물에 혼입될 수 있다. 약제학적으로 허용 가능한 담체 또는 부형제는 독성 및 제조 테스트의 필수 표준을 충족시키고/시키거나 미국 식품의약국이 준비한 비활성 성분 가이드(Inactive Ingredient Guide)에 포함되어 있다.
치료의 목적을 위한 "대상체" 또는 "개체"는 인간, 가축 및 농장 동물을 포함한 포유동물, 및 동물원, 스포츠, 또는 애완 동물, 예컨대, 개, 말, 고양이, 소 등으로 분류되는 임의의 동물을 지칭한다.
본 명세서에 기재된 본 발명의 실시형태는 실시형태로 "이루어진" 및/또는 실시형태로 "실질적으로 이루어진" 것을 포함하는 것으로 이해된다.
본 명세서에서 값 또는 파라미터의 "약"에 대한 언급은 해당 값 또는 파라미터 그 자체에 대한 변형을 포함한다(그리고 기재한다). 예를 들어, "약 X"를 언급하는 기재는 "X"의 기재를 포함한다.
본 명세서에서 사용되는 바와 같이, 값 또는 파라미터가 "아님"에 대한 언급은 일반적으로 값 또는 파라미터 "이외"를 의미하고 기재한다. 예를 들어, 방법이 X 유형의 암을 치료하는 데 사용되지 않는다는 것은 상기 방법이 X 이외의 유형의 암을 치료하는 데 사용된다는 것을 의미한다.
본 명세서 및 첨부된 청구범위에서 사용되는 바와 같이, 단수 형태("a", "또는" 및 "the")는 문맥이 달리 명확하게 지시하지 않는 한, 복수 대상을 포함한다.
공동수용체 시스템
일부 실시형태에서 본 발명은 i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)를 포함하는 조작된 면역 세포를 제공하며, 여기서 CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 키메라 수용체("CR")를 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공되며, 여기서 CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하고, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택된다.
일부 상황 하에서, CR 신호전달 도메인을 통해 생성된 신호만으로는 면역 세포의 완전한 활성화에 불충분하며 2차 또는 공동자극 신호가 또한 필요하다. 따라서, 일부 실시형태에서, 면역 세포 활성화는 2가지 별개 부류의 세포내 신호전달 서열, 즉 CR을 통해 항원-의존성 1차 활성화를 개시하는 것(예컨대, 세포내 CR 신호전달 도메인의 신호전달 서열) 및 2차 또는 공동자극 신호를 제공하는 것(본 명세서에서 "공동자극 신호전달 서열"로 지칭됨)에 의해 매개된다. 공동자극 신호전달 서열은 CR에 존재할 수 있으며; 즉, CR은 CR 공동자극 도메인을 더 포함할 수 있다.
일부 실시형태에서, 공동자극 신호전달 서열은 공동수용체에 의해 제공된다. 구체적으로, 일부 실시형태에서, a) i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR); 및 b) i) 키메라 공동수용체(CCOR) 표적 항원을 특이적으로 인식하는 CCOR 표적 항원 결합 도메인; ii) CCR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 도메인을 포함하는 키메라 공동수용체(CCOR)를 포함하는 조작된 면역 세포가 제공되며, 여기서 CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이거나, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4이다. 일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 제1 핵산으로, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하는 제1 핵산; 및 b) 키메라 공동수용체(CCOR)를 인코딩하는 제2 핵산으로, CCOR은 i) CCOR 표적 항원을 특이적으로 인식하는 CCOR 표적 항원 결합 도메인; ii) CCR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 도메인을 포함하는 제2 핵산을 포함하는 조작된 면역 세포가 제공되며, 여기서 CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이거나, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4이다. 일부 실시형태에서, CR 및 CCOR은 핵산으로부터 발현되고, 면역 세포 표면에 국재화된다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, CR은 공동자극 도메인을 포함하지 않는다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다. 유전자 발현을 파괴하기 위한 세포의 변형은, 예를 들어 RNA 간섭(예를 들어, siRNA, shRNA, miRNA), 유전자 편집(예를 들어, CRISPR- 또는 TALEN-기반 유전자 넉아웃) 등을 포함하여, 당업계에 알려진 임의의 이와 같은 기법을 포함한다.
일부 실시형태에서, 면역 세포는 하나 이상의 공동수용체를 더 포함하도록 변형된다. 따라서, 예를 들어 일부 실시형태에서, a) i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하되, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택되는 키메라 수용체(CR); 및 b) CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 공동수용체(COR)를 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, a) i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; iii) 세포내 CR 공동자극 도메인; 및 iv) 세포내 CR 신호전달 도메인을 포함하되, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택되는 키메라 수용체(CR); 및 b) CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 공동수용체(COR)를 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 면역 세포는 α4β7 및 CCR9를 둘 다 포함한다. 일부 실시형태에서, 면역 세포는 CXCR5, α4β7 및 CCR9를 전부 포함한다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다.
일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하고, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택되는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; iii) 세포내 CR 공동자극 도메인; 및 iv) 세포내 CR 신호전달 도메인을 포함하고, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택되는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 면역 세포는 α4β7을 인코딩하는 핵산 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, 면역 세포는 CXCR5를 인코딩하는 핵산, α4β7을 인코딩하는 핵산 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, CR 및 COR은 핵산으로부터 발현되고 면역 세포 표면에 국재화된다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다.
일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; iii) 세포내 CR 신호전달 도메인을 포함하는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; iii) 세포내 CR 공동자극 도메인; 및 iv) 세포내 CR 신호전달 도메인을 포함하되, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택되는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CD4 결합 모이어티 및 CCR5 결합 모이어티는 일렬로 연결된다. 일부 실시형태에서, CD4 결합 모이어티는 항-CCR5 모이어티에 대한 N-말단이다. 일부 실시형태에서, CD4 결합 모이어티는 항-CCR5 모이어티에 대한 C-말단이다. 일부 실시형태에서, 면역 세포는 α4β7을 인코딩하는 핵산 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, 면역 세포는 CXCR5를 인코딩하는 핵산, α4β7을 인코딩하는 핵산 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, CR 및 COR은 핵산으로부터 발현되고 면역 세포 표면에 국재화된다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다.
일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 광범위 중화 항체("bNAb") 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 광범위 중화 항체("bNAb") 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; iii) 세포내 CR 공동자극 도메인; 및 iv) 세포내 CR 신호전달 도메인을 포함하는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CD4 결합 모이어티 및 bNAb 모이어티는 일렬로 연결된다. 일부 실시형태에서, CD4 결합 모이어티는 bNAb 모이어티에 대한 N-말단이다. 일부 실시형태에서, CD4 결합 모이어티는 bNAb 모이어티에 대한 C-말단이다. 일부 실시형태에서, 면역 세포는 α4β7을 인코딩하는 핵산 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, 면역 세포는 CXCR5를 인코딩하는 핵산, α4β7을 인코딩하는 핵산, 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, CR 및 COR은 핵산으로부터 발현되고 면역 세포 표면에 국재화된다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다.
일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 광범위 중화 항체("bNAb") 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 광범위 중화 항체("bNAb") 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; iii) 세포내 CR 공동자극 도메인; 및 iv) 세포내 CR 신호전달 도메인을 포함하는 핵산; 및 b) 공동수용체(COR)를 인코딩하는 핵산으로, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택되는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CCR5 결합 모이어티 및 bNAb 모이어티는 일렬로 연결된다. 일부 실시형태에서, CCR5 결합 모이어티는 bNAb 모이어티에 대한 N-말단이다. 일부 실시형태에서, CCR5 결합 모이어티는 bNAb 모이어티에 대한 C-말단이다. 일부 실시형태에서, 면역 세포는 α4β7을 인코딩하는 핵산 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, 면역 세포는 CXCR5를 인코딩하는 핵산, α4β7을 인코딩하는 핵산, 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, CR 및 COR은 핵산으로부터 발현되고 면역 세포 표면에 국재화된다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다.
일부 실시형태에서, 면역 세포는 본 명세서에 기재된 CR, CCOR, 및 하나 이상의 COR을 발현하도록 조작된다. 따라서, 예를 들어, 일부 실시형태에서, a) i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR); b) i) 키메라 공동수용체(CCOR) 표적 항원을 특이적으로 인식하는 CCOR 표적 항원 결합 도메인; ii) CCR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 도메인을 포함하는 키메라 공동수용체(CCOR); 및 c) 공동수용체(COR)를 포함하는 조작된 면역 세포가 제공되며, 여기서 CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이거나, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4이다. 일부 실시형태에서, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 면역 세포는 α4β7 및 CCR9를 둘 다 포함한다. 일부 실시형태에서, 면역 세포는 CXCR5, α4β7 및 CCR9를 전부 포함한다. 일부 실시형태에서, CR은 CR 세포내 신호 전달 도메인을 포함하지 않는다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다.
일부 실시형태에서, a) 키메라 수용체(CR)를 인코딩하는 제1 핵산으로, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인; 및 iii) 세포내 CR 신호전달 도메인을 포함하는 제1 핵산; b) 키메라 공동수용체(CCOR)를 인코딩하는 제2 핵산으로, CCOR은 i) CCOR 표적 항원을 특이적으로 인식하는 CCOR 표적 항원 결합 도메인; ii) CCR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 도메인을 포함하는 제2 핵산, 및 c) 공동수용체(COR)를 인코딩하는 제3 핵산을 포함하는 조작된 면역 세포가 제공되며; 여기서 CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이거나, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4이다. 일부 실시형태에서, COR은 CXCR5, α4β7, CCR9, 또는 이들의 조합으로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 면역 세포는 α4β7을 인코딩하는 핵산 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, 면역 세포는 CXCR5를 인코딩하는 핵산, α4β7을 인코딩하는 핵산, 및 CCR9를 인코딩하는 핵산을 포함한다. 일부 실시형태에서, CR, CCOR 및 COR은 핵산으로부터 발현되고 면역 세포 표면에 국재화된다. 일부 실시형태에서, CR은 CR 세포내 신호 전달 도메인을 포함하지 않는다. 일부 실시형태에서, 면역 세포는 T 세포이다. 일부 실시형태에서, 면역 세포는 면역 세포의 CCR5의 발현을 차단하거나 감소시키도록 변형된다. 일부 실시형태에서, 면역 세포는 면역 세포의 내인성 TCR 서브유닛의 하나 또는 둘 다의 발현을 차단하거나 감소시키도록 변형된다.
일부 실시형태에서, CR을 인코딩하는 핵산 서열, CCOR을 인코딩하는 핵산 서열, 및/또는 COR을 인코딩하는 핵산 서열을 포함하는 핵산이 제공된다. 일부 실시형태에서, CR, CCOR, 및 COR 핵산 서열은 각각 상이한 벡터에 함유된다. 일부 실시형태에서, 핵산 서열의 일부 또는 전부는 동일한 벡터에 함유된다. 벡터는, 예를 들어 포유동물 발현 벡터 및 바이러스 벡터(예컨대, 레트로바이러스, 아데노바이러스, 아데노-연관 바이러스, 헤르페스 바이러스, 및 렌티바이러스로부터 유래된 것)로 이루어진 군으로부터 선택될 수 있다. 일부 실시형태에서, 하나 이상의 벡터는 면역 세포의 숙주 게놈 내로 통합된다. 일부 실시형태에서, CR, CCOR 및/또는 COR 핵산 서열은 각각 상이한 프로모터의 제어 하에 있다. 일부 실시형태에서, 프로모터는 동일한 서열을 가진다. 일부 실시형태에서, 프로모터는 상이한 서열을 가진다. 일부 실시형태에서, 핵산 서열의 일부 또는 전부는 단일 프로모터의 제어 하에 있다. 일부 실시형태에서, 프로모터의 일부 또는 전부는 유도성이다. 예를 들어, CCOR 및 COR 핵산은 면역 세포의 활성화시 유도성인 프로모터의 제어 하에 있을 수 있다. 일부 실시형태에서, 프로모터의 일부 또는 전부는 구성적이다.
상기 실시형태 중 어느 하나에 따른 일부 실시형태에서, 조작된 면역 세포는 T 세포, B 세포, NK 세포, 수지상 세포, 호산구, 대식세포, 림프구 세포, 및 비만 세포로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 조작된 면역 세포는 세포독성 T 세포, 헬퍼 T 세포, 및 자연 살해 T 세포로부터 선택된다. 일부 실시형태에서, 조작된 면역 세포는 세포독성 T 세포이다. 일부 실시형태에서, 조작된 면역 세포는 CD4 발현에 대해 풍부화된다. 일부 실시형태에서, 조작된 면역 세포는 CD8 발현에 대해 풍부화된다.
일부 실시형태에서, 조작된 면역 세포는 1차 면역 세포로부터 유래된다. 일부 실시형태에서, 조작된 면역 세포는 면역 활성을 가지도록 인공적을 유도된 세포(예를 들어, iPS 세포)로부터 유래된다. 일부 실시형태에서, 조작된 면역 세포는 CD4+ 면역 세포(또는 CD4 발현에 대해 풍부화된 면역 세포)로부터 유래된다. 일부 실시형태에서, 조작된 면역 세포는 CD8+ 면역 세포(또는 CD8 발현에 대해 풍부화된 면역 세포)로부터 유래된다.
일부 실시형태에서, CR, CCOR, 및 COR을 인코딩하는 핵산 중 2개 이상이 단일 프로모터의 제어 하에 있을 때, 핵산은 내부 리보솜 유입점(IRES) 및 자가-절단 2A 펩타이드(예컨대, P2A, T2A, E2A, 또는 F2A)를 인코딩하는 핵산으로 이루어진 군으로부터 선택되는 링커를 통해 연결될 수 있다.
키메라 수용체(CR) 작제물
본 명세서에 기재된 CR은 CR 표적 항원, CR 막관통 도메인, 및 세포내 CR 신호전달 도메인을 특이적으로 인식하는 CR 항원 결합 도메인을 포함한다.
일부 실시형태에서, CR 항원 결합 도메인은 CR 막관통 도메인에 직접 또는 간접적으로 융합된다. 예를 들어, CR은 N-말단에서 C-말단으로, CR 항원 결합 도메인, CR 막관통 도메인, 및 CR 세포내 신호전달 도메인을 포함하는 단일 폴리펩타이드일 수 있다. CR 항원 결합 도메인, CR 막관통 도메인, CR 세포내 도메인은 서로 직접적으로 또는 링커 서열을 통해 간접적으로 융합될 수 있다.
일부 실시형태에서, CR 항원 결합 도메인은 CR 막관통 도메인을 포함하는 폴리펩타이드에 비-공유적으로 결합된다. 이는, 예를 들어 하나는 CR 항원 결합 도메인에 융합되고(예를 들어, CR 항체 결합 도메인의 C-말단에 융합됨), 다른 하나는 CR 막관통 도메인에 융합되는(예를 들어, CR 막관통 도메인의 N-말단에 융합됨) 결합 쌍의 2개 구성원을 사용함으로써 달성될 수 있다. 2개의 구성요소는 결합 쌍의 2개의 구성원의 상호작용을 통해 합쳐진다. 예를 들어, CR은, i) CR 항원 결합 도메인 및 결합 쌍의 제1 구성원을 포함하는 제1 폴리펩타이드; 및 ii) 결합 쌍의 제2 구성원을 포함하는 제2 폴리펩타이드를 포함하는 세포외 도메인을 포함할 수 있으며, 여기서 제1 구성원 및 제2 구성원은 서로 비-공유적으로 결합한다. 결합 쌍의 제1 구성원은 CR 항원 결합 도메인에 직접 또는 간접적으로 융합될 수 있다. 유사하게, 결합 쌍의 제2 구성원은 CR 막관통 도메인에 직접 또는 간접적으로 융합될 수 있다. 적합한 결합 쌍은 류신 지퍼, 비오틴/스트렙트아비딘, MIC 리간드/iNKG2D 등을 포함하지만 이들 제한되는 것은 아니다. 문헌[Cell 173, 1426-1438, Oncoimmunology. 2018; 7(1): e1368604], US10259858B2를 참조한다.
일부 실시형태에서, CR 항원 결합 도메인은 2개 이상의 항원 결합 도메인을 포함한다. 예를 들어, 일부 실시형태에서, CR 항원 결합 도메인은 일렬로 연결된 CD4 결합 모이어티 및 CCR5 결합 모이어티를 포함한다. 일부 실시형태에서, CR 항원 결합 도메인은 일렬로 연결된 CD4 결합 모이어티 및 bNAb 모이어티를 포함한다. 일부 실시형태에서, CR 항원 결합 도메인은 일렬로 연결된 CCR5 결합 모이어티 및 bNAb 모이어티를 포함한다. 일부 실시형태에서, CD4 결합 모이어티, CCR5 결합 모이어티 및/또는 bNAb 모이어티는 scFv 또는 sdAb로 이루어진 군으로부터 선택된다.
일부 실시형태에서 세포내 CR 신호전달 도메인은, CD3ζ, FcRγ, FcRβ, CD3γ, CD3δ, CD3ε, CD5, CD22, CD79a, CD79b, 및 CD66d로 이루어진 군으로부터 선택되는 단백질에서 발견되는 것들을 포함하지만 이들로 제한되는 것은 아닌 기능적 1차 면역 세포 신호전달 서열을 포함한다. "기능적" 1차 면역 세포 신호전달 서열은 적절한 수용체에 작동 가능하게 커플링될 때 면역 세포 활성화 신호를 형질도입할 수 있는 서열이다. 1차 면역 세포 신호전달 서열의 단편 또는 변이체를 포함할 수 있는 "비-기능적" 1차 면역 세포 신호전달 서열은 면역 세포 활성화 신호를 형질도입할 수 없다. 본 명세서에 기재된 CCOR에는 기능적 1차 면역 세포 신호전달 서열이 없다. 일부 실시형태에서, CCOR에는 임의의 1차 면역 세포 신호전달 서열이 없다.
일부 실시형태에서, CR 막관통 도메인은, 예를 들어 CD28, CD3ε, CD3ζ, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, 또는 CD154로부터 유래된 하나 이상의 막관통 도메인을 포함한다.
CR 항원 결합 도메인은 CR 표적 항원을 특이적으로 인식하는 항체 모이어티 또는 리간드일 수 있다. 일부 실시형태에서, CR 항원 결합 도메인은 a) 다른 분자에 대한 결합 친화성의 적어도 약 10배(예를 들어, 적어도 약 10, 20, 30, 40, 50, 75, 100, 200, 300, 400, 500, 750, 1000배 또는 그 이상 중 어느 하나를 포함함)인 친화성; 또는 b) 다른 분자에의 결합에 대한 Kd의 약 1/10배 이하(예컨대, 약 1/10, 1/20, 1/30, 1/40, 1/50, 1/75, 1/100, 1/200, 1/300, 1/400, 1/500, 1/750, 1/1000배 또는 그 이하 중 어느 하나 이하)인 Kd로 표적 항원에 특이적으로 결합한다. 결합 친화성은 당업계에 알려진 방법, 예컨대, ELISA, 형광 활성화 세포 분류(FACS) 분석, 또는 방사선면역침강 분석(RIA)에 의해 결정될 수 있다. Kd는, 예를 들어 비아코어 인스트루먼츠(Biacore instruments)를 이용하는 표면 플라스몬 공명(SPR) 분석, 또는 예를 들어 사피딘 인스트루먼츠(Sapidyne instruments)를 이용하는 운동역학 배제 분석(KinExA)과 같은 당업계에 알려진 방법에 의해 결정될 수 있다.
일부 실시형태에서, CR 항원 결합 도메인은 Fab, Fab', (Fab')2, Fv, 단일 사슬 Fv(scFv), 단일 도메인 항체(sdAb), 및 CR 표적 항원에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택된다.
일부 실시형태에서, CR 항원 결합 도메인은 항체 모이어티이다. 일부 실시형태에서, 항체 모이어티는 단일특이적이다. 일부 실시형태에서, 항체 모이어티는 다중특이적이다. 일부 실시형태에서, 항체 모이어티는 이중특이적이다. 일부 실시형태에서, 항체 모이어티는 탠덤 scFv, 디아바디(Db), 단일 사슬 디아바디(scDb), 이중-친화성 재표적화(DART) 항체, 이중 가변 도메인(DVD) 항체, 화학적으로 가교된 항체, 이종다량체 항체, 또는 이종접합체 항체이다. 일부 실시형태에서, 항체 모이어티는 scFv이다. 일부 실시형태에서, 항체 모이어티는 단일 도메인 항체(sdAb)이다. 일부 실시형태에서, 항체 모이어티는 완전 인간, 인간 항체 프레임워크 영역을 가지는 반-합성, 또는 인간화된 것이다.
일부 실시형태에서 항체 모이어티는 하나 이상의 항체 모이어티(예컨대, 단클론성 항체) 또는 하나 이상의 아미노산 치환을 포함하는 이와 같은 서열의 특정 변이체로부터 유래된 특정 CDR 서열을 포함한다. 일부 실시형태에서, 변이체 서열의 아미노산 치환은 표적 항원에 결합하는 항원-결합 도메인의 능력을 실질적으로 감소시키지 않는다. 표적 항원 결합 친화성을 실질적으로 개선시키거나 일부 다른 특성, 예컨대, 표적 항원의 관련 항체와의 특이성 및/또는 교차-반응성에 영향을 미치는 변경도 또한 고려된다.
일부 실시형태에서, CR 항원 결합 도메인은 약 0.1pM 내지 약 500nM(예컨대, 약 0.1pM, 1.0pM, 10pM, 50pM, 100pM, 500pM, 1nM, 10nM, 50nM, 100nM, 또는 500nM 중 어느 하나로서 이들 값 사이의 임의의 값을 포함함)의 Kd로 CR 표적 항원에 결합한다.
일부 실시형태에서, 예를 들어, 단독으로 발현되거나 CCOR 없이 COR과 공동발현될 때, CR은 세포내 CR 공동자극 도메인을 더 포함할 수 있다. 세포내 CR 공동자극 도메인은, 예를 들어 CD28, 4-1BB(CD137), CD27, OX40, CD27, CD40, PD-1, ICOS, 림프구 기능-연관 항원-1(LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3, TNFRSF9, TNFRSF4, TNFRSF8, CD40LG, ITGB2, KLRC2, TNFRSF18, TNFRSF14, HAVCR1, LGALS9, CD83, 및 CD83과 특이적으로 결합하는 리간드를 포함하는 공동자극 분자의 세포내 도메인의 일부일 수 있다. 일부 실시형태에서, 세포내 CR 공동자극 도메인은 4-1BB의 단편을 포함한다. 일부 실시형태에서, 세포내 CCOR 공동자극 도메인은 CD28의 단편 및 4-1BB의 단편을 포함한다. 일부 실시형태에서, 예를 들어 CCOR과 공동발현될 때, CR은 기능적 공동자극 도메인을 포함하지 않는다.
따라서, 예를 들어, 일부 실시형태에서, i) CD4를 특이적으로 인식하는 키메라 수용체(CR) 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)가 제공된다. 일부 실시형태에서, i) CD4를 특이적으로 인식하는 키메라 수용체(CR) 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)를 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CD4를 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 조작된 면역 세포는 하나 이상의 COR(예컨대, CXCR5) 또는 하나 이상의 COR(예컨대, CXCR5)을 인코딩하는 핵산을 더 포함한다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CCR5를 특이적으로 인식하는 키메라 수용체(CR) 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)가 제공된다. 일부 실시형태에서, i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)를 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 조작된 면역 세포는 하나 이상의 COR(예컨대, CXCR5) 또는 하나 이상의 COR(예컨대, CXCR5)을 인코딩하는 핵산을 더 포함한다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 키메라 수용체(CR) 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)가 제공된다. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 키메라 수용체(CR) 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)를 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 키메라 수용체(CR)를 인코딩하는 핵산으로, CR은 i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CD4 결합 모이어티 및 CCR5 결합 모이어티는 일렬로 연결된다. 일부 실시형태에서, CD4 결합 모이어티는 CCR5 모이어티에 대한 N-말단이다. 일부 실시형태에서, CD4 결합 모이어티는 CCR5 모이어티에 대한 C-말단이다. 일부 실시형태에서, 조작된 면역 세포는 하나 이상의 COR(예컨대, CXCR5) 또는 하나 이상의 COR(예컨대, CXCR5)을 인코딩하는 핵산을 더 포함한다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, 본 명세서에 기재된 CR은 키메라 항원 수용체("CAR")이다. 따라서, 예를 들어, 일부 실시형태에서, i) CD4를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CD4 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CD4 CAR이 제공된다. 일부 실시형태에서, i) CD4를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CD4 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CD4 CAR을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, i) CD4를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CD4 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CD4 CAR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CR 항원 도메인은 도메인 1을 특이적으로 인식한다. 예를 들어, CR 항원 도메인은 CD4의 도메인 1을 특이적으로 인식하는 항-CD4 항체(예를 들어, scFv 또는 sdAb)일 수 있다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CCR5 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CCR5 CAR이 제공된다. 일부 실시형태에서, i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CCR5 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CCR5 CAR을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CCR5 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CCR5 CAR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 일렬의 항-CD4 항-CCR5 CAR이 제공된다. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 일렬의 항-CD4 항-CCR5 CAR을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 일렬의 항-CD4 항-CCR5 CAR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CD4 결합 모이어티 및 CCR5 결합 모이어티는 일렬로 연결된다. 일부 실시형태에서, CD4 결합 모이어티는 CCR5 결합-모이어티에 대한 N-말단이다. 일부 실시형태에서, CD4 결합 모이어티는 CCR5 결합 모이어티에 대한 C-말단이다. 일부 실시형태에서, CR 항원 도메인은 도메인 1을 특이적으로 인식한다. 예를 들어, CR 항원 도메인은 CD4의 도메인 1을 특이적으로 인식하는 항-CD4 항체(예를 들어, scFv 또는 sdAb)를 포함할 수 있다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 일렬의 항-CD4 bNAb CAR이 제공된다. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CD4 bNAb CAR을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CD4 bNAb CAR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CD4 결합 모이어티 및 bNAb 모이어티는 일렬로 연결된다. 일부 실시형태에서, CD4 결합 모이어티는 bNAb 모이어티에 대한 N-말단이다. 일부 실시형태에서, CD4 결합 모이어티는 bNAb 모이어티에 대한 C-말단이다. 일부 실시형태에서, CR 항원 도메인은 도메인 1을 특이적으로 인식한다. 예를 들어, CR 항원 도메인은 CD4의 도메인 1을 특이적으로 인식하는 항-CD4 항체(예를 들어, scFv 또는 sdAb)를 포함할 수 있다. 일부 실시형태에서, 조작된 면역 세포는, VRC01, PGT121, 3BNC117, 10-1074, N6, VRC07, VRC07-523, eCD4-IG, 10E8, 10E8v4, PG9, PGDM 1400, PGT151, CAP256.25, 35O22, 8ANC195 등을 포함하여, 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 일렬의 항-CCR5 bNAb CAR이 제공된다. 일부 실시형태에서, i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CCR5 bNAb CAR을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 힌지 서열(예컨대, CD8로부터 유래된 힌지 서열); iii) CR 막관통 도메인(예컨대, CD8 막관통 도메인), iv) 세포내 공동자극 도메인(예컨대, 4-1BB 또는 CD28로부터 유래된 공동자극 도메인); 및 v) 세포내 CR 신호전달 도메인(예컨대, CD3ζ로부터 유래된 세포내 신호전달 도메인)을 포함하는 항-CCR5 bNAb CAR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CCR5 결합 모이어티 및 bNAb 모이어티는 일렬로 연결된다. 일부 실시형태에서, CCR5 결합 모이어티는 bNAb 모이어티에 대한 N-말단이다. 일부 실시형태에서, CCR5 결합 모이어티는 bNAb 모이어티에 대한 C-말단이다. 일부 실시형태에서, 조작된 면역 세포는, VRC01, PGT121, 3BNC117, 10-1074, N6, VRC07, VRC07-523, eCD4-IG, 10E8, 10E8v4, PG9, PGDM 1400, PGT151, CAP256.25, 35O22, 8ANC195 등을 포함하여, 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, 본 명세서에 기재된 CR은 키메라 TCR 수용체("cTCR")이다. cTCR은 전형적으로 TCR 서브유닛의 전장 또는 일부, 예컨대, TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε 및 CD3δ에 (직접 또는 간접적으로) 융합된 CR 항원 결합 도메인을 포함한다. 융합 폴리펩타이드는 다른 TCR 서브유닛과 함께 기능적 TCR 복합체에 통합될 수 있고 TCR 복합체에 항원 특이성을 부여한다. 일부 실시형태에서, CR 항원 결합 도메인은 CD3ε 서브유닛의 전장 또는 일부("eTCR"로 지칭됨)에 융합된다. cTCR의 세포내 CR 신호전달 도메인은 TCR 서브유닛의 세포내 신호전달 도메인으로부터 유래될 수 있다. CR 막관통 도메인은 TCR 서브유닛으로부터 유래된다. 일부 실시형태에서, 세포내 CR 신호전달 도메인 및 CR 막관통 도메인은 동일한 TCR 서브유닛으로부터 유래된다. 일부 실시형태에서, 세포내 CR 신호전달 도메인 및 CR 막관통 도메인은 CD3ε으로부터 유래된다. 일부 실시형태에서, CR 항원 결합 도메인 및 TCR 서브유닛(또는 이의 일부)은 링커(예컨대, GS 링커)를 통해 융합될 수 있다. 일부 실시형태에서, cTCR은 TCR 서브유닛 또는 이의 일부의 세포외 도메인을 더 포함하며, 상기 세포외 도메인은 세포내 CR 신호전달 도메인 및/또는 CR 막관통 도메인이 유래된 TCR 단위와 동일하거나 상이할 수 있다.
따라서, 예를 들어, 일부 실시형태에서, i) CD4를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CD4 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 항-CD4 cTCR이 제공된다. 일부 실시형태에서, i) CD4를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CD4 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 항-CD4 cTCR을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, i) CD4를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CD4 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 항-CD4 cTCR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CR 항원 도메인은 도메인 1을 특이적으로 인식한다. 예를 들어, CR 항원 도메인은 CD4의 도메인 1을 특이적으로 인식하는 항-CD4 항체(예를 들어, scFv 또는 sdAb)일 수 있다. 일부 실시형태에서, TCR 서브유닛은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε으로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 동일한 TCR 서브유닛으로부터 유래된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 CD3ε으로부터 유래된다. 일부 실시형태에서, cTCR은 전장 CD3ε의 N-말단에 융합된 CR 항원 결합 도메인을 포함한다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CCR5 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 항-CCR5 cTCR이 제공된다. 일부 실시형태에서, i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CCR5 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 항-CCR5 cTCR을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, i) CCR5를 특이적으로 인식하는 CR 항원 결합 도메인(예를 들어, 항-CCR5 항체 모이어티, 예컨대, scFv 또는 sdAb); ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 항-CCR5 cTCR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, TCR 서브유닛은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε으로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 동일한 TCR 서브유닛으로부터 유래된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 CD3ε으로부터 유래된다. 일부 실시형태에서, cTCR은 전장 CD3ε의 N-말단에 융합된 CR 항원 결합 도메인을 포함한다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CD4 항-CCR5 cTCR이 제공된다. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CD4 항-CCR5 cTCR을 포함하는 조작된 면역 세포가 제공된다. ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CD4 항-CCR5 cTCR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CR 항원 도메인은 도메인 1을 특이적으로 인식한다. 예를 들어, CR 항원 도메인은 CD4의 도메인 1을 특이적으로 인식하는 항-CD4 항체(예를 들어, scFv 또는 sdAb)일 수 있다. 일부 실시형태에서, TCR 서브유닛은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε으로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 동일한 TCR 서브유닛으로부터 유래된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 CD3ε으로부터 유래된다. 일부 실시형태에서, cTCR은 전장 CD3ε의 N-말단에 융합된 CR 항원 결합 도메인을 포함한다. 일부 실시형태에서, CD4 결합 모이어티 및 CCR5 결합 모이어티는 일렬로 연결된다. 일부 실시형태에서, CD4 결합 모이어티는 CCR5 모이어티에 대한 N-말단이다. 일부 실시형태에서, CD4 결합 모이어티는 CCR5 모이어티에 대한 C-말단이다. 일부 실시형태에서, 조작된 면역 세포는 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CD4 bNAb cTCR이 제공된다. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CD4 bNAb cTCR을 포함하는 조작된 면역 세포가 제공된다. ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인. 일부 실시형태에서, i) CD4 결합 모이어티(예컨대, 항-CD4 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CD4 bNAb cTCR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, CR 항원 도메인은 도메인 1을 특이적으로 인식한다. 예를 들어, CR 항원 도메인은 CD4의 도메인 1을 특이적으로 인식하는 항-CD4 항체(예를 들어, scFv 또는 sdAb)를 포함할 수 있다. 일부 실시형태에서, TCR 서브유닛은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε으로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 동일한 TCR 서브유닛으로부터 유래된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 CD3ε으로부터 유래된다. 일부 실시형태에서, cTCR은 전장 CD3ε의 N-말단에 융합된 CR 항원 결합 도메인을 포함한다. 일부 실시형태에서, CD4 결합 모이어티 및 bNAb 모이어티는 일렬로 연결된다. 일부 실시형태에서, CD4 결합 모이어티는 bNAb 모이어티에 대한 N-말단이다. 일부 실시형태에서, CD4 결합 모이어티는 bNAb 모이어티에 대한 C-말단이다. 일부 실시형태에서, 조작된 면역 세포는, VRC01, PGT121, 3BNC117, 10-1074, N6, VRC07, VRC07-523, eCD4-IG, 10E8, 10E8v4, PG9, PGDM 1400, PGT151, CAP256.25, 35O22, 8ANC195 등을 포함하여, 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
일부 실시형태에서, i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CCR5 bNAb cTCR이 제공된다. 일부 실시형태에서, i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CCR5 bNAb cTCR을 포함하는 조작된 면역 세포가 제공된다. ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인. 일부 실시형태에서, i) CCR5 결합 모이어티(예컨대, 항-CCR5 항체 모이어티, 예를 들어 scFv 또는 sdAb) 및 bNAb 모이어티(예컨대, scFv 또는 sdAb)를 포함하는 CR 항원 결합 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인; ii) 선택적인 링커(예컨대, GS 링커); iii) TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인; iii) TCR 서브유닛으로부터 유래된 CR 막관통 도메인, 및 iv) TCR 서브유닛으로부터 유래된 세포내 CR 신호전달 도메인을 포함하는 일렬의 항-CCR5 bNAb cTCR을 인코딩하는 핵산을 포함하는 조작된 면역 세포가 제공된다. 일부 실시형태에서, TCR 서브유닛은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε으로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 동일한 TCR 서브유닛으로부터 유래된다. 일부 실시형태에서, CR 막관통 도메인, 세포내 CR 신호전달 도메인, 및 TCR 서브유닛 또는 이의 일부의 선택적인 세포외 도메인은 CD3ε으로부터 유래된다. 일부 실시형태에서, cTCR은 전장 CD3ε의 N-말단에 융합된 CR 항원 결합 도메인을 포함한다. 일부 실시형태에서, CCR5 결합 모이어티 및 bNAb 모이어티는 일렬로 연결된다. 일부 실시형태에서, CCR5 결합 모이어티는 bNAb 모이어티에 대한 N-말단이다. 일부 실시형태에서, CCR5 결합 모이어티는 bNAb 모이어티에 대한 C-말단이다. 일부 실시형태에서, 조작된 면역 세포는, VRC01, PGT121, 3BNC117, 10-1074, N6, VRC07, VRC07-523, eCD4-IG, 10E8, 10E8v4, PG9, PGDM 1400, PGT151, CAP256.25, 35O22, 8ANC195 등을 포함하여, 광범위 중화 항체(bNAb) 또는 bNAb를 인코딩하는 핵산을 더 포함한다.
키메라 공동자극 수용체(CCOR)
본 명세서에 기재된 키메라 공동자극 수용체(CCOR)는 CCOR 표적 항원에 특이적으로 결합하고 표적 결합시 기능적으로 발현되는 표면에서 면역 세포를 자극할 수 있게 한다. CCOR은 표적-결합 특이성, 막관통 도메인, 및 면역 세포를 자극할 수 있는 CCOR 공동자극 도메인을 제공하는 CCOR 항원 결합 도메인을 포함한다. CCOR에는 기능적 1차 면역 세포 신호전달 서열이 없다. 일부 실시형태에서, CCOR에는 어떠한 1차 면역 세포 신호전달 서열이 없다. 일부 실시형태에서, 조작된 면역 세포에서 CCOR의 발현은 유도성이다. 일부 실시형태에서, 조작된 면역 세포의 발현은 CR을 통한 신호전달시 유도성이다.
본 발명의 CCOR에서 사용하기 위한 공동자극 면역 세포 신호전달 도메인의 예는 T 세포 수용체(TCR)의 공동수용체의 세포질 서열(이는 CR과 함께 작용하여 CR 참여 후 신호 전달을 개시할 수 있음)뿐만 아니라 동일한 기능적 능력을 가지는 이들 서열 및 임의의 합성 서열의 임의의 유도체 또는 변이체를 포함한다.
세포내 CCOR 공동자극 도메인은, 예를 들어 CD28, 4-1BB(CD137), CD27, OX40, CD27, CD40, PD-1, ICOS, 림프구 기능-연관 항원-1(LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3, TNFRSF9, TNFRSF4, TNFRSF8, CD40LG, ITGB2, KLRC2, TNFRSF18, TNFRSF14, HAVCR1, LGALS9, CD83, 및 CD83과 특이적으로 결합하는 리간드를 포함하여, 공동자극 분자의 세포내 도메인의 일부일 수 있다. 일부 실시형태에서, 세포내 CCOR 공동자극 도메인은 4-1BB의 단편을 포함한다. 일부 실시형태에서, 세포내 CCOR 공동자극 도메인은 CD28의 단편 및 4-1BB의 단편을 포함한다.
일부 실시형태에서, CCOR 막관통 도메인은, 예를 들어 CD28, CD3ε, CD3ζ, CD45, CD4, CD5, CD8, CD9, CD16, CD22, CD33, CD37, CD64, CD80, CD86, CD134, CD137, 또는 CD154로부터 유래된 하나 이상의 막관통 도메인을 포함한다.
일부 실시형태에서, CCOR 항원 결합 도메인은 Fab, Fab', (Fab')2, Fv, 단일 사슬 Fv(scFv), 단일 도메인 항체(sdAb), 및 CCOR 표적 항원에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택된다. 일부 실시형태에서, CCOR 항원 결합 도메인은 a) 다른 분자에 대한 결합 친화성의 적어도 약 10배(예를 들어, 적어도 약 10, 20, 30, 40, 50, 75, 100, 200, 300, 400, 500, 750, 1000배 또는 그 이상 중 어느 하나를 포함함)인 친화성; 또는 b) 다른 분자에의 결합에 대한 Kd의 약 1/10배 이하(예컨대, 약 1/10, 1/20, 1/30, 1/40, 1/50, 1/75, 1/100, 1/200, 1/300, 1/400, 1/500, 1/750, 1/1000배 또는 그 이하 중 어느 하나 이하)인 Kd로 CCOR 표적 항원에 특이적으로 결합한다. 결합 친화성은 당업계에 알려진 방법, 예컨대, ELISA, 형광 활성화 세포 분류(FACS) 분석, 또는 방사선면역침강 분석(RIA)에 의해 결정될 수 있다. Kd는, 예를 들어 비아코어 인스트루먼츠를 이용하는 표면 플라스몬 공명(SPR) 분석, 또는 예를 들어 사피딘 인스트루먼츠를 이용하는 운동역학 배제 분석(KinExA)과 같은 당업계에 알려진 방법에 의해 결정될 수 있다.
일부 실시형태에서, CCOR 항원 결합 도메인은 Fab, Fab', (Fab')2, Fv, 단일 사슬 Fv(scFv), 단일 도메인 항체(sdAb), 및 CR 표적 항원에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택된다.
일부 실시형태에서, CCOR 항원 결합 도메인은 항체 모이어티이다. 일부 실시형태에서, 항체 모이어티는 단일특이적이다. 일부 실시형태에서, 항체 모이어티는 다중특이적이다. 일부 실시형태에서, 항체 모이어티는 이중특이적이다. 일부 실시형태에서, 항체 모이어티는 탠덤 scFv, 디아바디(Db), 단일 사슬 디아바디(scDb), 이중-친화성 재표적화(DART) 항체, 이중 가변 도메인(DVD) 항체, 화학적으로 가교된 항체, 이종다량체 항체, 또는 이종접합체 항체이다. 일부 실시형태에서, 항체 모이어티는 scFv이다. 일부 실시형태에서, 항체 모이어티는 단일 도메인 항체(sdAb)이다. 일부 실시형태에서, 항체 모이어티는 완전 인간, 인간 항체 프레임워크 영역을 가지는 반-합성, 또는 인간화된 것이다.
일부 실시형태에서 항체 모이어티는 하나 이상의 항체 모이어티(예컨대, 단클론성 항체) 또는 하나 이상의 아미노산 치환을 포함하는 이와 같은 서열의 특정 변이체로부터 유래된 특정 CDR 서열을 포함한다. 일부 실시형태에서, 변이체 서열의 아미노산 치환은 표적 항원에 결합하는 항원-결합 도메인의 능력을 실질적으로 감소시키지 않는다. 표적 항원 결합 친화성을 실질적으로 개선시키거나 일부 다른 특성, 예컨대, 표적 항원의 관련 항체와의 특이성 및/또는 교차-반응성에 영향을 미치는 변경도 또한 고려된다.
일부 실시형태에서, CCOR 항원 결합 도메인은 약 0.1pM 내지 약 500nM(예컨대, 약 0.1pM, 1.0pM, 10pM, 50pM, 100pM, 500pM, 1nM, 10nM, 50nM, 100nM, 또는 500nM 중 어느 하나로서 이들 값 사이의 임의의 값을 포함함)의 Kd로 CCOR 표적 항원에 결합한다.
CR 및 CCOR 항원-결합 도메인
본 명세서에 기재된 CR 및 CCOR은 CD4, CCR5, 및 CXCR4로 이루어진 군으로부터 선택되는 표적 항원을 특이적으로 인식한다. 상기에서 논의된 바와 같이, CR이 CD4를 특이적으로 인식할 때, CCOR은 CCR5 또는 CXCR4를 특이적으로 인식할 것이다. 대안적으로, CR이 CCR5 또는 CXCR4를 특이적으로 인식할 때, CCOR은 CD4를 특이적으로 인식할 것이다. 표적 항원 및 항원 결합 도메인은 하기 섹션에서 보다 상세히 논의되며, 이는 일반적으로 CR 항원 결합 도메인(및 CR 표적 항원)과 CCOR 항원 결합 도메인(및 CCOR 표적 항원) 둘 다에 적용 가능하다.
일부 실시형태에서, 표적 항원은 CCR5이다. CCR5는 내재성 막 단백질의 베타 케모카인 수용체 패밀리에 속하는 7개의 막관통 도메인을 가지는 G 단백질-결합 수용체이다. CCR5는 352개의 아미노산으로 구성되고 대략 41 킬로달톤(kDa)이다.
CCR5는 T 세포, 대식세포, 수지상 세포, 및 호산구를 포함하는 면역계의 세포에서 주로 발현되지만, 또한 내피, 상피, 혈관평활근 및 섬유아세포에서도 발현된다. 또한, 이는 중추신경계에서 발견되는 미세아교세포, 뉴런, 및 성상세포에서 발현된다(문헌[Barmania, F. and Pepper, MS. Applied & Translational Genomics (2013) 2(2013):3-16] 참조).
CCR5는 대부분의 HIV-I 1차 분리주에서 발현되며, 감염의 확립 및 유지에 중요하다. 초기 질환의 HIV-1 분리주는 CD4+ T 세포로의 진입을 위해 CD4와 공동수용체로서 CCR5를 사용하는 경향이 있다. CCR5는 감염되지 않은 대조군과 비교하여 HIV-감염 개체의 CD4+ T 세포에서 상향조절되는 것으로 나타났다(문헌[Ostrowski, MA, et al. J. Immunol. (1998) 161(6):3195-3201] 참조). 측정가능한 양의 개체간 CCR5 표면 발현 가변성이 존재한다.
일부 실시형태에서, 표적 항원은 CCR5의 세포외 도메인 변이체이다. 다른 실시형태에서, 표적 항원은 CCR5의 막관통 도메인 변이체이다. 또 다른 실시형태에서, 표적 항원은 CCR5의 세포외 도메인 및 막관통 도메인 변이체이다(여러 CCR5 변이체 및 생성된 HIV 감염성의 분석을 위해, 문헌[Zack Howard, OM, et al. J. Biol. Chem. (1999) 274(23):16228-16234] 참조).
일부 실시형태에서, 항원 결합 도메인은 CCR5를 인식하는 리간드, CCR5를 인식할 수 있는 이의 단편이다. CCR5를 인식하는 리간드는 MIP-lα, MIP-lβ 및 RANTES를 포함하지만 이들로 제한되는 것은 아니다. 일부 실시형태에서, 항원 결합 도메인은 CCL3으로도 알려진 MIP-1α이다. MIP-1α는 급성 염증 동안 다형핵 백혈구의 동원 및 활성화에 관여하는 사이토카인이다. 일부 실시형태에서, 항원 결합 도메인은 CCL4로도 알려진 MIP-1β이다. MIP-1β는 자연 살해 세포 및 단핵구를 포함하여 많은 면역 세포에 대한 화학유인제이다. MIP1-β는 단핵구, T 세포, B 세포를 포함한 면역계의 다양한 세포, 및 또한 섬유아세포 및 내피 및 상피 세포에 의해 생성된다. 일부 실시형태에서, 항원 결합 도메인은 CCL5로도 알려진 RANTES의 리간드이다. RANTES는 면역 부위로 백혈구를 동원하고, T 세포, 호염기구, 및 호산구를 포함한 면역계에서 다양한 세포에 대한 화학유인제로서 작용한다. 또 다른 실시형태에서, 항원 결합 도메인은 CCR5에 결합하는 또 다른 리간드이다.
일부 실시형태에서, 항원 결합 도메인은, 본 명세서에 기재된 항체 모이어티 중 임의의 것과 같은 CCR5를 인식하는 항체 모이어티이다. 예시적인 항-CCR5 항체는 WO2006103100에서 찾을 수 있으며, 이는 구체적으로 본 명세서에 참조로 포함된다.
일부 실시형태에서, 표적 항원은 CXCR4이다. C-X-C 케모카인 수용체 유형 4로도 알려진 CXCR4는 리간드 SDF-1에 결합하고 여러가지 상이한 경로를 통해 세포내 신호를 전달하여 칼슘의 증가 및/또는 cAMP 수준의 감소를 초래하는 알파-케모카인 수용체이다. 이는 CD4+ T 세포를 포함하여 면역 세포에서 주로 발현되지만, 또한 중추신경계의 세포에서도 발현된다. CXCR4는 7개의 막관통 나선이 있는 G 단백질-결합 수용체이며, 352개의 아미노산으로 구성된다.
CXCR4는 HIV 분리주가 CD4+ T 세포를 감염시키는 데 사용할 수 있는 여러가지 케모카인 수용체 중 하나이다. HIV의 T 세포 친화성(tropic) 분리주는 표면에서 CXCR4를 발현하는 CD4+ T 세포를 감염시킬 수 있다. CXCR4는 T 세포로의 HIV 진입을 위한 공동수용체이며, 특정 뮤린 항-CXCR4 항체는 T 세포로의 HIV 분리주의 진입을 저해할 수 있는 것으로 입증되었다(문헌[Hou, T. et al. (1998) J. Immunol. 160:180-188]; [Carnec, X. et al. (2005) J. Virol. 79:1930-1938] 참조). CXCR4는 세포로의 진입을 위해 바이러스에 의해 수용체로서 사용될 수 있으며, CXCR4에 대한 항체는 수용체로서 CXCR4를 사용하는 이와 같은 바이러스의 세포 진입을 저해하는 데 사용되었다. WO2008060367 및 WO2011098762를 참조한다.
CXCR4는 감염되지 않은 대조군과 비교하여 HIV-감염 개체에서 CD4+ 및 CD8+ T 세포와 CD14+ 단핵구에서 하향조절된다(문헌[Ostrowski, MA, et al. J. Immunol. (1998) 161(6):3195-3201] 참조). HIV-1 분리주는 질환이 진행함에 따라 세포 진입을 위하여 CD4와 공동수용체로서 CXCR4를 사용하며; CXCR4는 CCR5의 경우와 같이 감염 초기에 공동수용체로서 사용되지 않는다.
일부 실시형태에서, 항원 결합 도메인은 CXCR4 리간드, 예컨대, 기질 세포-유래 인자 1(SDF-1, 또는 CXCL12), 또는 CXCR4를 인식하는 이의 단편이다. SDF-1은 림프구에 대해 강력한 화학주성이며, 흉선, 비장 및 골수를 포함하지만 이들로 제한되는 것은 아닌 다수의 조직에서 발현된다. 일부 실시형태에서, 항원 결합 도메인은 SDF-1의 7가지 동형 중 하나이다. 일부 실시형태에서, 항원 결합 도메인은 MIF, 유비퀴틴, 또는 이들의 단편이다.
일부 실시형태에서, 항원 결합 도메인은, 본 명세서에 기재된 항체 모이어티 중 임의의 것과 같은 CXCR4를 인식하는 항체 모이어티이다. 예시적인 항-CXCR4 항체는 WO2008060367 및 WO2011098762에서 찾을 수 있으며, 이는 구체적으로 본 명세서에 참조로 포함된다.
일부 실시형태에서, 표적 항원은 또한 분화 클러스터 4로도 알려진 CD4이다. CD4는 면역 세포, 특히 CD4+ T 세포, 또는 헬퍼 T 세포의 표면에서 발견되는 당단백질이다. CD4는 면역글로불린 수퍼패밀리의 구성원이다. CD4는 4개의 세포외 면역글로불린 도메인(D1 내지 D4)으로 구성된다. D1 및 D3은 면역글로불린 가변 도메인과 유사성을 나타내는 반면, D2 및 D4는 면역글로불린 불변 도메인과 유사성을 나타낸다.
CD4는 HIV-1 진입 및 감염에 필요한 중요한 세포-표면 분자이다. HIV-1 진입은 T-세포 수용체 CD4의 도메인 1(D1)과 바이러스 외피(Env) 당단백질 gp120의 상호작용에 의해 촉발된다. HIV 감염이 진행함에 따라, 더 많은 수의 CD4+ T 세포가 바이러스에 의해 표적화되고 파괴되어 면역계가 점점 더 손상되고; 따라서 CD4+ T 세포 수는 개체에서 HIV/AIDS의 진행 및 단계에 대한 프록시로서 사용된다. 또한, HIV 유전자 산물인 Env, Vpu 및 Nef는 HIV 감염 동안 CD4의 하향조절에 관여한다(문헌[Tanaka, M., et al. Virology (2003) 311(2):316-325] 참조).
일부 실시형태에서, 항원 결합 도메인은 a) 다른 분자에 대한 결합 친화성의 적어도 약 10배(예를 들어, 적어도 약 10, 20, 30, 40, 50, 75, 100, 200, 300, 400, 500, 750, 1000배 또는 그 이상 중 어느 하나를 포함함)인 친화성; 또는 b) 다른 분자에의 결합에 대한 Kd의 약 1/10배 이하(예컨대, 약 1/10, 1/20, 1/30, 1/40, 1/50, 1/75, 1/100, 1/200, 1/300, 1/400, 1/500, 1/750, 1/1000배 또는 그 이하 중 어느 하나 이하)인 Kd로 CD4 D1 또는 CD4 D2/D3에 특이적으로 결합한다. 결합 친화성은 당업계에 알려진 방법, 예컨대, ELISA, 형광 활성화 세포 분류(FACS) 분석, 또는 방사선면역침강 분석(RIA)에 의해 결정될 수 있다. Kd는, 예를 들어 비아코어 인스트루먼츠를 이용하는 표면 플라스몬 공명(SPR) 분석, 또는 예를 들어 사피딘 인스트루먼츠를 이용하는 운동역학 배제 분석(KinExA)과 같은 당업계에 알려진 방법에 의해 결정될 수 있다.
일부 실시형태에서, 항원 결합 도메인은 Fab, Fab', (Fab')2, Fv, 단일 사슬 Fv(scFv), 단일 도메인 항체(sdAb), 및 CD4에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택된다.
일부 실시형태에서, 항원 결합 도메인은 항체 모이어티이다. 일부 실시형태에서, 항체 모이어티는 단일특이적이다. 일부 실시형태에서, 항체 모이어티는 다중특이적이다. 일부 실시형태에서, 항체 모이어티는 이중특이적이다. 일부 실시형태에서, 항체 모이어티는 탠덤 scFv, 디아바디(Db), 단일 사슬 디아바디(scDb), 이중-친화성 재표적화(DART) 항체, 이중 가변 도메인(DVD) 항체, 화학적으로 가교된 항체, 이종다량체 항체, 또는 이종접합체 항체이다. 일부 실시형태에서, 항체 모이어티는 scFv이다. 일부 실시형태에서, 항체 모이어티는 단일 도메인 항체(sdAb)이다. 일부 실시형태에서, 항체 모이어티는 완전 인간, 인간 항체 프레임워크 영역을 가지는 반-합성, 또는 인간화된 것이다.
일부 실시형태에서 항체 모이어티는 하나 이상의 항체 모이어티(예컨대, 본 명세서에 개시된 특이적 항체 중 임의의 것) 또는 하나 이상의 아미노산 치환을 포함하는 이와 같은 서열의 특정 변이체로부터 유래된 특정 CDR 서열을 포함한다. 일부 실시형태에서, 변이체 서열의 아미노산 치환은 표적 항원에 결합하는 항원-결합 도메인의 능력을 실질적으로 감소시키지 않는다. 표적 항원 결합 친화성을 실질적으로 개선시키거나 일부 다른 특성, 예컨대, 표적 항원의 관련 항체와의 특이성 및/또는 교차-반응성에 영향을 미치는 변경도 또한 고려된다.
일부 실시형태에서, 항원 결합 도메인은 약 0.1pM 내지 약 500nM(예컨대, 약 0.1pM, 1.0pM, 10pM, 50pM, 100pM, 500pM, 1nM, 10nM, 50nM, 100nM, 또는 500nM 중 어느 하나로서 이들 값 사이의 임의의 값을 포함함)의 Kd로 CD4 D1 또는 D2/3에 결합한다.
일부 실시형태에서, 항원 결합 도메인은 CD4의 D1에서 에피토프에 결합한다. 일부 실시형태에서, 항원 결합 도메인은 다음 영역 중 임의의 하나 이상에 속하는 에피토프에 결합한다: CD4의 아미노산 26 내지 125, 26 내지 46, 46 내지 66, 66 내지 86, 86 내지 106, 106 내지 125(여기서, 아미노산 번호매김은 서열번호 1에 따름). 일부 실시형태에서, 항원 결합 도메인은 다음 영역 중 임의의 하나 이상에 속하는 에피토프에 결합한다: 서열번호 1의 아미노산 26 내지 125, 26 내지 46, 46 내지 66, 66 내지 86, 86 내지 106, 106 내지 125. 일부 실시형태에서, 항원 결합 도메인은 약 0.1pM 내지 약 500nM(예컨대, 약 0.1pM, 1.0pM, 10pM, 50pM, 100pM, 500pM, 1nM, 10nM, 50nM, 100nM, 또는 500nM 중 어느 하나로서 이들 값 사이의 임의의 값을 포함함)으로 CD4의 D1에 결합한다. 일부 실시형태에서, CD4는 인간 CD4이다. 일부 실시형태에서, 항원 결합 도메인은, 예를 들어 WO1997013852에 개시된 바와 같은 자놀리무밥으로부터 유래된다. 일부 실시형태에서, 항원 결합 도메인은 자놀리무맙에 대한 결합에 대하여 경쟁한다. 일부 실시형태에서, 항원 결합 도메인은 자놀리무밥과 동일하거나 중첩되는 에피토프에 결합한다.
일부 실시형태에서, 항원 결합 도메인은 CD4의 D2 또는 D3에서 에피토프에 결합한다. 일부 실시형태에서, 항원 결합 도메인은 다음 영역 중 임의의 하나 이상에 속하는 에피토프에 결합한다: CD4의 아미노산 126 내지 317, 126 내지 203, 204 내지 317, 126 내지 146, 146 내지 166, 166 내지 186, 186 내지 206, 206 내지 226, 226 내지 246, 246 내지 266, 266 내지 286, 286 내지 306, 및 306 내지 317(여기서, 아미노산 번호매김은 서열번호 1에 따름). 일부 실시형태에서, 항원 결합 도메인은 다음 영역 중 임의의 하나 이상에 속하는 에피토프에 결합한다: 서열번호 1의 아미노산 126 내지 317, 126 내지 203, 204 내지 317, 126 내지 146, 146 내지 166, 166 내지 186, 186 내지 206, 206 내지 226, 226 내지 246, 246 내지 266, 266 내지 286, 286 내지 306, 및 306 내지 317. 일부 실시형태에서, 항원 결합 도메인은 약 0.1pM 내지 약 500nM(예컨대, 약 0.1pM, 1.0pM, 10pM, 50pM, 100pM, 500pM, 1nM, 10nM, 50nM, 100nM, 또는 500nM 중 어느 하나로서 이들 값 사이의 임의의 값을 포함함)의 kd로 CD4의 D2 또는 D3에 결합한다. 일부 실시형태에서, CD4는 인간 CD4이다. 일부 실시형태에서, 항원 결합 도메인은, 예를 들어 US20130195881 및 WO2004083247에 개시된 바와 같은 이발리주맙 또는 트레갈리주맙으로부터 유래된다. 일부 실시형태에서, 항원 결합 도메인은 이발리주맙 또는 트레갈리주맙에 대한 결합에 대하여 경쟁한다. 일부 실시형태에서, 항원 결합 도메인은 이발리주맙 또는 트레갈리주맙과 동일하거나 중첩되는 에피토프에 결합한다.
일부 실시형태에서, 항원 결합 도메인은 CD4에 대한 리간드, 또는 CD4에 결합할 수 있는 이의 단편이다. 일부 실시형태에서, CD4에 대한 리간드는 T 세포 활성화를 조절하고 HIV 복제를 저해하는 다면발현성 사이토카인인 IL-16이다. 다른 실시형태에서, CD4에 대한 리간드는 II형 주요 조직적합성 복합체(MHC II형)이다. MHC II형 분자는 전형적으로 B 세포, 수지상 세포, 항원 제시 세포, 단핵식세포, 및 흉선 상피 세포를 포함하여, 면역계의 항원 제시 세포에서 발견된다. 일부 실시형태에서, MHC II형 리간드는 면역계에 대한 후속 제시를 위해 CD4에 제시하기 위한 병원성 펩타이드를 제시한다.
일부 실시형태에서, 항원 결합 도메인은 외피 당단백질 gp120 또는 이의 단편이다. HIV env 유전자에 의해 인코딩되는 천연 gp120은 표적 세포에 대한 HIV의 부착에서 필수적인 역할을 하는 HIV 바이러스 외피에서 발견되는 120 kDa의 당단백질이다. gp120은 표적 세포의 효율적인 HIV 감염이 되도록 CCR5를 포함하여 케모카인 수용체 패밀리의 구성원 및 표적 세포 CD4에 결합한다. gp120 및 CD4의 복합체는 CCR5와 특이적으로 상호작용하여 MIP-1α 및 MIP-1β와 같은 자연 CCR5 리간드의 결합을 저해하는 것으로 나타났다(Wu, L., et al. (1996) Nature 384: 179-183).
일부 실시형태에서, 항원 결합 도메인이 gp120일 때, 조작된 면역 세포는 CCOR을 포함하지 않는다. 일부 실시형태에서, 조작된 면역 세포의 CR은 CR 공동자극 신호전달 도메인을 포함한다.
일부 실시형태에서, 항원 결합 도메인은 CD4, CCR5, 및 CXCR4 중 하나 이상에 결합하지 않는 변형된 gp120이다. 예를 들어, 일부 실시형태에서, 항원 결합 도메인은 CD4에 결합하지만 CCR5 또는 CXCR4에 결합하지 않는 변형된 gp120이다. 일부 실시형태에서, 항원 결합 도메인은 CCR5에 결합하지만 CD4 또는 CXCR4에 결합하지 않는 변형된 gp120이다. 일부 실시형태에서, 항원 결합 도메인은 CXCR4에 결합하지만 CCR5 또는 CD4에 결합하지 않는 변형된 gp120이다.
공동수용체("COR")
일부 실시형태에서, 조작된 면역 세포는 하나 이상의 공동수용체("COR")를 더 포함한다.
일부 실시형태에서, COR은 면역 세포의 여포로의 이동을 촉진시킨다. 일부 실시형태에서, COR은 면역 세포의 장으로의 이동을 촉진시킨다. 일부 실시형태에서, COR은 면역 세포의 피부로의 이동을 촉진시킨다.
일부 실시형태에서, COR은 CXCR5이다. 일부 실시형태에서, COR은 CCR9이다. 일부 실시형태에서, COR은 α4β7(또한 인테그린 α4β7이라고 지칭됨). 일부 실시형태에서, 조작된 면역 세포는 CXCR5, α4β7, 및 CCR9로 이루어진 군으로부터 선택되는 둘 이상의 수용체를 포함한다. 일부 실시형태에서, 조작된 면역 세포는 α4β7 및 CCR9를 둘 다 포함한다. 일부 실시형태에서, 조작된 면역 세포는 CXCR5, α4β7, 및 CCR9를 전부 포함한다.
C-C 케모카인 수용체 유형 9(CCR9)로도 알려진 CCR9는 베타 케모카인 수용체 패밀리의 구성원이며 이의 결합 리간드인 CCL25에 반응하여 화학주성을 매개한다. CCR9는 G 단백질-결합 수용체와 구조가 유사한 7개의 막관통 도메인 단백질인 것으로 예측된다. CCR9는 흉선 및 소장의 T 세포에서 발현되며, T 림프구의 발달 및 이동을 조절하는 역할을 한다(Uehara, S., et al. (2002) J. Immunol. 168(6):2811-2819). CCR9/CCL25는 면역 세포를 소장으로 유도하는 것으로 나타났다(Pabst, O., et al. (2004). J. Exp. Med. 199(3):411). 따라서 면역 세포에서 CCR9를 공동발현하면 조작된 면역 세포를 장으로 유도할 수 있다. 일부 실시형태에서, CCR9의 스플라이싱 변이체가 사용된다.
α4β7, 또는 림프구 페이어판 부착 분자(lymphocyte Peyer patch adhesion molecule; LPAM)는 림프구에서 발현되고 장-연관 림프 조직으로 T-세포의 귀소를 담당하는 인테그린이다(Petrovic, A. et al. (2004) Blood 103(4):1542-1547). α4β7은 CD49d(α4 인테그린 서브유닛을 인코딩하는 유전자인 ITGA4의 단백질 산물) 및 ITGB7(β7 인테그린 서브유닛을 인코딩하는 유전자인 ITGB4의 단백질 산물)로 구성된 이종이량체이다. 일부 실시형태에서, α4의 스플라이싱 변이체는 α4β7 이종이량체 내로 통합된다. 일부 실시형태에서, β7의 스플라이싱 변이체는 α4β7 이종이량체 내로 통합된다. 다른 실시형태에서, α4의 스플라이싱 변이체 및 β7의 스플라이싱 변이체는 이종이량체 내로 통합된다. α4β7 단독으로 또는 CCR9와 함께 공동발현은 조작된 면역 세포를 장으로 유도할 수 있다.
α4β7 및 CCR9는 둘 다 장으로의 귀소에 작용하지만, 이들이 반드시 공동조절되는 것은 아니다. 비타민 A 대사산물인 레티노산은 CCR9 및 α4β7 둘 다의 발현 유도에서 역할을 한다. 그러나 α4β7 발현은 다른 수단을 통해 유도될 수 있는 반면, CCR9 발현은 레티노산을 필요로 한다. 또한, 결장-친화성 T-세포는 α4β7만 발현하고 CCR9는 발현하지 않으며, 이는 2가지 수용체가 항상 공동발현되거나 공동조절되는 것이 아님을 나타낸다(문헌[Takeuchi, H., et al. J. Immunol. (2010) 185(9):5289-5299] 참조).
일부 실시형태에서, CCR9 및 α4β7은 장에 대한 표적화를 위한 COR로서 기능한다.
일부 실시형태에서, 면역 세포는, C-X-C 케모카인 수용체 유형 5로도 알려진 CXCR5를 발현한다. CXCR5는 CXC 케모카인 수용체 패밀리에 속하는 7개의 막관통 도메인을 함유하는 G 단백질-결합 수용체이다. CXCR5 및 이의 리간드인 케모카인 CXCL13은 림프절 및 비장을 포함한 2차 림프 조직 내의 여포로 림프구를 거래하는 데 중심적인 역할을 한다(, A. et al. (2007) Blood 110:3316-3325). 구체적으로, CXCR5는 CXCL13에 반응하여 T 세포가 림프절 B 세포 구역으로 이동할 수 있게 한다(Schaerli, P. et al. (2000) J. Exp. Med. 192(11):1553-1562). 면역 세포에서 발현될 때, CXCR5는 조작된 면역 세포를 여포에 대하여 표적화하는 COR로서 기능할 수 있다. 일부 실시형태에서, CXCR5의 스플라이싱 변이체가 사용된다.
일반적으로, 상기 논의된 COR 중 임의의 것의 비-자연 발생 변이체는 조작된 면역 세포에서 포함/발현될 수 있다. 이들 변이체는, 예를 들어 하나 이상의 돌연변이를 함유할 수 있지만, 그럼에도 불구하고 상응하는 천연 수용체의 일부 또는 그 이상의 기능을 유지할 수 있다. 예를 들어, 일부 실시형태에서 COR은 자연 발생 CCR9, α4β, 또는 CXCR5의 변이체이며, 여기서 변이체는 자연 CCR9, α4β 또는 CXCR5와 적어도 약 90%, 95%, 96%, 97%, 98%, 또는 99% 중 어느 하나로 동일한 아미노산 서열을 가진다. 일부 실시형태에서, COR은 자연 발생 CCR9, α4β, 또는 CXCR5의 변이체이며, 여기서 변이체는 천연 CCR9, α4β, 또는 CXCR5와 비교하여 약 1, 2, 3, 4, 5, 6, 7, 8, 9, 또는 10개 중 어느 하나 이하의 아미노산을 포함한다.
일부 실시형태에서, COR은 케모카인 수용체이다. 일부 실시형태에서, COR은 인테그린이다. 일부 실시형태에서, COR은 CCR1, CCR2, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, CXCR1, CXCR2, CXCR3, CXCR4, CXCR5, CXCR6, CX3CR1, XCR1, ACKR1, ACKR2, ACKR3, ACKR4, CCRL2로 이루어진 군으로부터 선택된다.
일부 실시형태에서, COR은 조작된 면역 세포가 유래된 면역 세포에서 정상적으로 발현되지 않는다. 일부 실시형태에서, COR은 조작된 면역 세포가 유래된 면역 세포에서 낮은 수준으로 발현된다.
항-HIV 항체
일부 실시형태에서 본 명세서에 기재된 조작된 면역 세포는 항-HIV 항체, 예컨대, 광범위 중화 항체("bNAb")를 추가로 발현(및 분비)한다. 일부 실시형태에서, CR이 탠덤 CR일 때, CR 항원 결합 도메인은 항-HIV 항체 모이어티(예컨대, bNAb 모이어티)를 포함할 수 있다. bNAb는 HIV 외피 단백질에 결합하고 숙주 세포 수용체 결합하는 바이러스를 차단한다. 본 명세서에 기재된 bNAb 모이어티는 광범위 중화 항체 활성 및/또는 결합 특이성을 보유하는 항체 또는 이의 단편을 지칭한다. 일부 실시형태에서, bNAb 모이어티는 scFv이다. 일부 실시형태에서, bNAb 모이어티는 sdAb이다.
bNAb는 HIV에 감염되었지만 항레트로바이러스 약을 복용하지 않고 바이러스 감염을 자연적으로 제어할 수 있는 엘리트 컨트롤러(elite controller)에서 처음 발견되었다. bNAb는 다수의 HIV 바이러스 균주를 중화시키는 중화 항체이다. bNAb는, 바이러스가 돌연변이를 겪더라도, 바이러스의 보존된 에피토프를 표적화한다. 일부 실시형태에서 본 명세서에 기재된 조작된 면역 세포는 광범위 중화 항체를 분비하여 새로운 숙주 세포의 HIV 감염을 차단할 수 있다.
일부 실시형태에서, bNAb는 gp41, V1V2 글리칸, 글리칸의 외부도메인, V3 글리칸, 또는 CD4 결합 부위의 MPER 상의 바이러스 에피토프를 특이적으로 인식한다. bNAb는 바이러스 외피 당단백질과 CD4의 상호작용을 차단한다. Mascola and Haynes, Immunol. Rev. 2013 July; 254(1):225-44. 적합한 bNAb는 VRC01, PGT-121, 3BNC117, 10-1074, N6, VRC07, VRC07-523, eCD4-IG, 10E8, 10E8v4, PG9, PGDM 1400, PGT151, CAP256.25, 35O22, 8ANC195를 포함하지만 이들로 제한되는 것은 아니다. Science Translational Medicine 23 Dec 2015: Vol. 7, Issue 319, pp. 319ra206; PLoS Pathog. 2013;9(5):e1003342; Nature. 2015 Jun 25;522(7557):487-91; Nat Med. 2017 Feb;23(2):185-191; Nature Immunologyvolume 19, pages1179-1188 (2018). 다른 적합한 광범위 중화 항체를, 예를 들어 문헌[Cohen et al., Current Opin. HIV AIDS, 2018 Jul; 13(4):366-373]; [Mascola and Haynes, Immunol. Rev. 2013 July; 254(1):225-44]에서 찾을 수 있다.
핵산
본 명세서에 기재된 CR, CCOR 및/또는 COR을 인코딩하는 핵산(또는 핵산 세트)뿐만 아니라, 상기 핵산(들)을 포함하는 벡터가 본 명세서에서 제공된다.
CR, CCOR 및/또는 COR의 발현은, 핵산이, 예를 들어 프로모터(예를 들어, 림프구-특이적 프로모터) 및 3' 비번역 영역(UTR)을 포함하여 5' 및/또는 3' 조절 요소에 작동 가능하게 연결되도록, 핵산을 적절한 발현 벡터에 삽입함으로써 달성될 수 있다. 벡터는 숙주 세포에서 복제 및 통합에 적합할 수 있다. 전형적인 클로닝 및 발현 벡터는 원하는 핵산 서열의 발현의 조절에 유용한 전사 및 번역 종결자, 개시 서열, 및 프로모터를 함유한다.
핵산은 다수 유형의 벡터 내로 클로닝될 수 있다. 예를 들어, 핵산은, 플라스미드, 파지미드, 파지 유도체, 동물 바이러스 및 코스미드를 포함하지만 이들로 제한되는 것은 아닌 벡터 내로 클로닝될 수 있다. 특히 관심 벡터는 발현 벡터, 복제 벡터, 프로브 생성 벡터, 및 서열 벡터를 포함한다.
또한, 발현 벡터는 바이러스 벡터의 형태로 세포에 제공될 수 있다. 바이러스 벡터는 당업계에 잘 알려져 있다. 벡터로서 유용한 바이러스는 레트로바이러스, 아데노바이러스, 아데노-연관 바이러스, 헤르페스 바이러스, 및 렌티바이러스를 포함하지만 이들로 제한되는 것은 아니다. 일반적으로, 적합한 벡터는 적어도 하나의 유기체에서 기능하는 복제 기점, 프로모터 서열, 편리한 제한 엔도뉴클레아제 부위, 및 하나 이상의 선별 마커를 함유한다.
포유동물 세포 내로의 유전자 전달을 위해 다수의 바이러스 기반 시스템이 개발되었다. 예를 들어, 레트로바이러스는 유전자 전달 시스템을 위한 편리한 플랫폼을 제공한다. 선택된 유전자는 벡터 내로 삽입되고 당업계에 알려진 기법을 사용하여 레트로바이러스 입자에 패키징될 수 있다. 그 다음 재조합 바이러스는 단리되고 생체 내 또는 생체 외에서 대상체의 세포로 전달될 수 있다. 다수의 레트로바이러스 시스템이 당업계에 알려져 있다. 일부 실시형태에서, 아데노바이러스 벡터가 사용된다. 다수의 아데노바이러스 벡터가 당업계에 알려져 있다. 일부 실시형태에서, 렌티바이러스 벡터가 사용된다. 렌티바이러스와 같은 레트로바이러스로부터 유래된 벡터는 이식유전자의 장기적이고 안정적인 통합과 딸 세포에서의 증식을 가능하게 하므로, 장기적인 유전자 전달을 달성하는 데 적합한 도구이다. 렌티바이러스 벡터는, 비-증식 세포, 예컨대, 간세포를 형질도입할 수 있다는 점에서, 종양-레트로바이러스(onco-retrovirus), 예컨대, 뮤린 백혈병 바이러스로부터 유래된 벡터에 비하여 추가적인 장점을 가진다. 렌티바이러스 벡터는 또한 면역원성이 낮다는 추가적인 장점을 가진다.
추가적인 프로모터 요소, 예를 들어 인핸서는 전사 개시 빈도를 조절한다. 전형적으로, 상기 요소는 시작 부위 상류의 30 내지 110 bp 영역에 위치하지만, 다수의 프로모터가 최근 시작 부위 하류에 또한 기능적 요소를 함유하는 것으로 나타났다. 프로모터 요소 사이의 간격은 빈번하게 유연적이므로, 프로모터 기능은 요소가 반전되거나 같은 간격으로 이동될 때 보존된다. 티미딘 키나제(tk) 프로모터에서, 프로모터 요소 사이의 간격은 활성이 감소하기 시작하기 전에 50 bp 간격으로 증가될 수 있다.
적합한 프로모터의 일 예는 급초기 사이토메갈로바이러스(CMV) 프로모터 서열이다. 이 프로모터 서열은 이에 작동 가능하게 연결된 임의의 폴리뉴클레오타이드 서열의 높은 수준의 발현을 구동할 수 있는 강력한 구성적 프로모터 서열이다. 적합한 프로모터의 또 다른 예는 신장 성장 인자-1α(EF-1α)이다. 그러나, 유인원 바이러스 40(SV40) 초기 프로모터, 마우스 유선 종양 바이러스(MMTV), 인간 면역결핍 바이러스(HIV) 긴 말단 반복(LTR) 프로모터, MoMuLV 프로모터, 조류 백혈병 바이러스 프로모터, 엡스타인-바 급초기 프로모터, 라우스 육종 바이러스 프로모터뿐만 아니라, 액틴 프로모터, 미오신 프로모터, 헤모글로빈 프로모터, 및 크레아틴 키나제 프로모터(이들로 제한되는 것은 아님)와 같은 인간 유전자 프로모터를 포함하지만 이들로 제한되는 것은 아닌 다른 구성적 프로모터 서열이 또한 사용될 수 있다.
폴리펩타이드 또는 이의 일부의 발현을 평가하기 위해, 세포 내로 도입될 발현 벡터는 또한 선별 마커 유전자 또는 리포터 유전자 또는 둘 다를 함유하여 바이러스 벡터를 통해 형질감염되거나 감염되고자 하는 세포 집단으로부터 발현 세포의 확인 및 선택을 용이하게 할 수 있다. 다른 양태에서, 선별 마커는 DNA의 별도 조각 상에서 운반되고 공동형질감염 절차에 사용될 수 있다. 선별 마커 및 리포터 유전자 둘 다 적절한 조절 서열이 측접하여 숙주 세포에서 발현을 가능하게 할 수 있다. 유용한 선별 마커는, 예를 들어 항생제 내성 유전자, 예컨대, 네오(neo) 등을 포함한다.
리포터 유전자는 잠재적으로 형질감염된 세포를 확인하고 조절 서열의 기능을 평가하는 데 사용된다. 일반적으로, 리포터 유전자는 수용 유기체 또는 조직에 존재하지 않거나 이에 의해 발현되지 않고 발현이 일부 용이하게 검출가능한 특성, 예를 들어 효소 활성에 의해 나타나는 폴리펩타이드를 인코딩하는 유전자이다. 리포터 유전자의 발현은 DNA가 수용 세포 내로 도입된 후 적합한 시간에 분석된다. 적합한 리포터 유전자는 루시페라제, β-갈락토시다제, 클로람페니콜 아세틸 트랜스퍼라제, 분비된 알칼리 포스파타제, 또는 녹색 형광 단백질 유전자를 인코딩하는 유전자를 포함할 수 있다. 적합한 발현 시스템은 잘 알려져 있으며, 알려진 기법을 사용하여 제조되거나 상업적으로 입수할 수 있다. 일반적으로, 가장 높은 수준의 리포터 유전자의 발현을 나타내는 최소한의 5' 측접 영역을 가지는 작제물은 프로모터로서 확인된다. 이와 같은 프로모터 영역은 리포터 유전자에 연결되어 프로모터-구동 전사를 조절하는 능력에 대하여 작용제를 평가하는 데 사용될 수 있다.
포유동물 세포에서 이종성 핵산의 존재를 확인하는 예시적인 방법은, 예를 들어 당업자에게 잘 알려진 분자 생물학적 분석, 예컨대, 서던 및 노던 블롯팅, RT-PCR 및 PCR; 예를 들어 면역학적 방법(예컨대, ELISA 및 웨스턴 블롯)에 의한, 특정 펩타이드의 존재 또는 부재의 검출과 같은 생화학적 분석을 포함한다.
포유동물 세포에서 이종성 핵산의 존재를 확인하는 예시적인 방법은, 예를 들어 당업자에게 잘 알려진 분자 생물학적 분석, 예컨대, 서던 및 노던 블롯팅, RT-PCR 및 PCR; 예를 들어 면역학적 방법(예컨대, ELISA 및 웨스턴 블롯)에 의한, 특정 펩타이드의 존재 또는 부재의 검출과 같은 생화학적 분석을 포함한다.
일부 실시형태에서, 하나 이상의 핵산 서열 각각은 별도의 벡터에 함유된다. 일부 실시형태에서, 핵산 서열 중 적어도 일부는 동일한 벡터에 함유된다. 일부 실시형태에서, 핵산 서열 전부는 동일한 벡터에 함유된다. 벡터는, 예를 들어 포유동물 발현 벡터 및 바이러스 벡터(예컨대, 레트로바이러스, 아데노바이러스, 아데노-연관 바이러스, 헤르페스 바이러스, 및 렌티바이러스로부터 유래된 것)로 이루어진 군으로부터 선택될 수 있다.
예를 들어, 일부 실시형태에서, 핵산은 CR 폴리펩타이드 사슬을 인코딩하는 제1 핵산, 선택적으로 CCOR 폴리펩타이드 사슬을 인코딩하는 제2 핵산, 선택적으로 COR 폴리펩타이드 사슬을 인코딩하는 제3 핵산, 및 선택적으로 bNAb 폴리펩타이드를 인코딩하는 제4 핵산을 포함한다. 일부 실시형태에서, 제1 핵산 서열은 제1 벡터에 함유되고/되거나, 제2 핵산은 제2 벡터에 함유되고/되거나, 제3 핵산은 제3 벡터에 함유되고/되거나, 제4 핵산은 제4 벡터에 함유된다. 일부 실시형태에서, 제1 및 제2 핵산 서열은 제1 벡터에 함유되고, 제3 핵산 서열 및/또는 제4 핵산 서열은 제2 벡터에 함유된다. 일부 실시형태에서, 제1 및 제3 핵산 서열은 제1 벡터에 함유되고, 제2 핵산 서열 및/또는 제4 핵산 서열은 제2 벡터에 함유된다. 일부 실시형태에서, 제2 및 제3 핵산 서열은 제1 벡터에 함유되고, 제1 핵산 서열 및/또는 제4 핵산 서열은 제2 벡터에 함유된다. 일부 실시형태에서, 제1, 제2, 제3, 및 선택적으로 제4 핵산 서열은 동일한 벡터에 함유된다. 일부 실시형태에서, 제1, 제2, 제3, 및 선택적으로 제4 핵산은 내부 리보솜 유입점(IRES) 및 자가-절단 2A 펩타이드(예컨대, P2A, T2A, E2A, 또는 F2A)를 인코딩하는 핵산으로 이루어진 군으로부터 선택되는 링커를 통해 서로 연결될 수 있다.
일부 실시형태에서, 제1 핵산 서열은 제1 프로모터의 제어 하에 있고/있거나, 제2 핵산 서열은 제2 프로모터의 제어 하에 있고/있거나, 제3 핵산 서열은 제3 프로모터의 제어 하에 있고/있거나, 제4 핵산 서열은 제4 프로모터의 제어 하에 있다. 일부 실시형태에서, 제1, 제2, 제3, 및/또는 제4 프로모터 중 일부 또는 전부는 동일한 서열을 가진다. 일부 실시형태에서, 제1, 제2, 제3, 및 선택적으로 제4 프로모터 중 일부 또는 전부는 상이한 서열을 가진다. 일부 실시형태에서, 제1, 제2, 제3, 및 선택적으로 제4 핵산 서열 중 일부 또는 전부는 다중시스트론성 벡터에서 단일 프로모터의 제어 하에 단일 전사체로서 발현된다. 일부 실시형태에서, 프로모터 중 하나 이상은 유도성이다. 일부 실시형태에서, 제3 및/또는 제4 핵산 서열은 유도성 프로모터에 작동 가능하게 연결된다.
일부 실시형태에서, 제1, 제2, 제3, 및 선택적으로 제4 핵산 서열 중 일부 또는 전부는 면역 세포(예컨대, T 세포)에서 유사한(예컨대, 실질적으로 또는 거의 동일한) 발현 수준을 가진다. 일부 실시형태에서, 제1, 제2, 제3, 및 선택적으로 제4 핵산 서열 중 일부는 면역 세포(예컨대, T 세포)에서 적어도 약 2배(예컨대, 적어도 약 2, 3, 4, 5배 또는 그 이상 중 어느 하나)만큼 상이한 발현 수준을 가진다. 발현은 mRNA 또는 단백질 수준에서 결정될 수 있다. mRNA 발현의 수준은, 노던 블롯팅, 정량적 RT-PCR, 마이크로어레이 분석 등을 포함하여 다양한 잘 알려진 방법을 사용하여 핵산으로부터 전사된 mRNA의 양을 측정함으로써 결정될 수 있다. 단백질 발현의 수준은 면역세포화학 염색, 효소-결합 면역흡착 분석(ELISA), 웨스턴 블롯 분석, 발광 분석, 질량 분석법, 고성능 액체 크로마토그래피, 고압 액체 크로마토그래피-탠덤 질량 분석법 등을 포함하여 알려진 방법에 의해 측정될 수 있다.
유전자를 세포(예컨대, 면역 세포) 내로 도입하고 발현하는 방법은 당업계에 알려져 있다. 발현 벡터의 맥락에서, 벡터는 당업계의 임의의 방법에 의해 숙주 세포, 예를 들어 포유동물, 박테리아, 효모, 또는 곤충 세포 내로 용이하게 도입될 수 있다. 예를 들어, 발현 벡터는 물리적, 화학적, 또는 생물학적 수단에 의해 숙주 세포 내로 전달될 수 있다.
폴리뉴클레오타이드를 숙주 세포 내로 도입하는 물리적 방법은 인산칼슘 침전, 리포펙틴, 입자 충격, 미세주입, 전기천공 등을 포함한다. 벡터 및/또는 외인성 핵산을 포함하는 세포를 생산하는 방법은 당업계에 잘 알려져 있다. 일부 실시형태에서, 숙주 세포 내로 폴리뉴클레오타이드를 도입하는 것은 인산칼슘 형질감염에 의해 수행된다.
숙주 세포 내로 관심 폴리뉴클레오타이드를 도입하는 생물학적 방법은 DNA 및 RNA 벡터의 사용을 포함한다. 바이러스 벡터, 특히 레트로바이러스 벡터는 포유동물, 예를 들어 인간 세포 내로 유전자를 삽입하기 위한 가장 널리 사용하는 방법이 되었다. 다른 바이러스 벡터는 렌티바이러스, 폭스바이러스, 단순 포진 바이러스 1, 아데노바이러스 및 아데노-연관 바이러스 등으로부터 유래될 수 있다.
숙주 세포(예컨대, 면역 세포) 내로 폴리뉴클레오타이드를 도입하기 위한 화학적 수단은 콜로이드 분산 시스템, 예컨대, 거대분자 복합체, 나노캡슐, 마이크로스피어, 비드, 및 지질-기반 시스템, 예를 들어 수중유 에멀젼, 미셀, 혼합 미셀, 및 리포좀을 포함한다. 시험관내 및 생체 내에서 전달 비히클로서 사용하기 위한 예시적인 콜로이드 시스템은 리포좀(예를 들어, 인공막 소포)이다.
비-바이러스 전달 시스템이 이용되는 경우, 예시적인 전달 비히클은 리포좀이다. 지질 제형의 사용은 숙주 세포 내로 (시험관내, 생체 외 또는 생체 내에서) 핵산을 도입하기 위해 고려된다. 또 다른 양태에서, 핵산은 지질과 회합될 수 있다. 지질과 회합된 핵산은 리포좀의 수성 내부에 캡슐화되거나, 리포좀의 지질 이중층 내에 산재되거나, 리포좀 및 올리고뉴클레오타이드 둘 다와 회합된 연결 분자를 통해 리포좀에 부착되거나, 리포좀에 포획되거나, 리포좀과 복합체화되거나, 지질을 함유하는 용액 중에 분산되거나, 지질과 혼합되거나, 지질과 결합되거나, 지질 중에 현탁액으로서 함유되거나, 미셀과 함께 함유되거나 미셀과 복합체화되거나, 그렇지 않으면 지질과 회합될 수 있다. 지질, 지질/DNA 또는 지질/발현 벡터 연관 조성물은 용액 중 임의의 특정 구조로 제한되지 않는다. 예를 들어, 이는 이중층 구조에 미셀로서, 또는 "붕괴된" 구조로 존재할 수 있다. 이는 또한 단순히 용액 중에 산재되어, 크기 또는 형상이 균일하지 않은 응집체를 형성할 수 있다. 지질은 자연적으로 발생하거나 합성 지질일 수 있는 지방 물질이다. 예를 들어, 지질은 세포질에서 자연적으로 발생하는 지방 액적뿐만 아니라, 장쇄 지방족 탄화수소 및 이의 유도체, 예컨대, 지방산, 알코올, 아민, 아미노 알코올, 및 알데하이드를 함유하는 화합물 부류를 포함한다.
숙주 세포에서 재조합 DNA 서열의 존재를 확인하기 위하여, 숙주 세포 내로 외인성 핵산을 도입하거나 그렇지 않으면 세포를 본 발명의 저해제에 노출시키는 데 사용되는 방법에 관계없이, 다양한 분석이 수행될 수 있다. 이와 같은 분석은, 예를 들어 당업자에게 잘 알려진 "분자 생물학적" 분석, 예컨대, 서던 및 노던 블롯팅, RT-PCR 및 PCR; 예를 들어 면역학적 수단(ELISA 및 웨스턴 블롯)에 의한 또는 본 발명의 범주 내에 속하는 작용제를 확인하기 위한 본 명세서에 기재된 분석에 의한, 특정 펩타이드의 존재 또는 부재의 검출과 같은 "생화학적 분석"을 포함한다.
항체 모이어티
본 명세서에 기재된 다양한 작제물(예컨대, CR 항원 결합 도메인 또는 CCOR 항원 결합 도메인)은 항체 모이어티를 포함한다. 일부 실시형태에서, 항체 모이어티는 단클론성 항체 유래의 VH 및 VL 도메인, 또는 이들의 변이체를 포함한다. 일부 실시형태에서, 항체 모이어티는 단클론성 항체 유래의 CH1 및 CL 도메인, 또는 이들의 변이체를 더 포함한다. 단클론성 항체는, 예를 들어 하이브리도마 방법, 예컨대, 문헌[Kohler and Milstein, Nature, 256:495 (1975)] 및 [Sergeeva et al., Blood, 117(16):4262-4272]에 기재된 것을 사용하여 제조될 수 있다.
하이브리도마 방법에서, 햄스터, 마우스, 또는 다른 적절한 숙주 동물은 전형적으로 면역화제로 면역화되어 면역화제에 특이적으로 결합할 항체를 생성하거나 생성할 수 있는 림프구를 유도한다. 대안적으로, 림프구는 시험관내에서 면역화될 수 있다. 면역화제는 관심 단백질의 폴리펩타이드 또는 융합 단백질, 또는 적어도 2개의 분자를 포함하는 복합체, 예컨대, 펩타이드 및 MHC 단백질을 포함하는 복합체를 포함할 수 있다. 일반적으로, 말초 혈액 림프구("PBL")는 인간 기원의 세포가 필요한 경우 사용되며, 비장 세포 또는 림프절 세포는 비-인간 포유동물 공급원이 필요한 경우 사용된다. 그 다음 림프구는 적합한 융합제, 예컨대, 폴리에틸렌 글라이콜을 사용하여 무한증식 세포와 융합되어 하이브리도마 세포를 형성한다. 무한증식 세포주는 보통 형질전환된 포유동물 세포, 특히 설치류, 소, 및 인간 기원의 골수종 세포이다. 보통, 래트 또는 마우스 골수종 세포주가 이용된다. 하이브리도마 세포는 바람직하게는 융합되지 않은 무한증식 세포의 성장 또는 생존을 저해하는 하나 이상의 물질을 함유하는 적합한 배양 배지에서 배양될 수 있다. 예를 들어, 모세포에 하이포잔틴 구아닌 포스포리보실 트랜스퍼라제(HGPRT 또는 HPRT) 효소가 없는 경우, 하이브리도마용 배양 배지는 HGPRT-결핍 세포의 성장을 방지하는 하이포잔틴, 아미노프테린 및 티미딘("HAT 배지")을 포함할 것이다.
일부 실시형태에서, 무한증식 세포주는 효율적으로 융합하고, 선택된 항체-생성 세포에 의해 항체의 안정적인 고수준 발현을 지지하며, HAT 배지와 같은 배지에 민감하다. 일부 실시형태에서, 무한증식 세포주는 뮤린 골수종 주이며, 이는, 예를 들어 솔크 인스티튜트 셀 디스트리뷰션 센터(Salk Institute Cell Distribution Center; 미국 캘리포니아주 샌디에이고 소재) 및 아메리칸 타입 컬쳐 콜렉션(American Type Culture Collection; 미국 버지니아주 매너서스 소재)로부터 입수할 수 있다. 인간 골수종 및 마우스-인간 이종골수종(heteromyeloma) 세포주는 또한 인간 단클론성 항체의 생성에 대해 설명된 바 있다. Kozbor, J. Immunol., 133:3001 (1984); Brodeur et al. Monoclonal Antibody Production Techniques and Applications (Marcel Dekker, Inc.: New York, 1987) pp. 51-63.
그 다음 하이브리도마 세포가 배양된 배양 배지는 폴리펩타이드에 대한 단클론성 항체의 존재에 대하여 분석될 수 있다. 하이브리도메 세포에 의해 생성된 단클론성 항체의 결합 특이성은 면역침강법에 의해 또는 시험관내 결합 분석, 예컨대, 방사면역측정법(RIA) 또는 효소-결합 면역흡착 분석(ELISA)에 의해 결정될 수 있다. 이와 같은 기법 및 분석은 당업계에 알려져 있다. 단클론성 항체의 결합 친화성은, 예를 들어 문헌[Munson and Pollard, Anal. Biochem., 107: 220 (1980)]의 스캐차드 분석(Scatchard analysis)에 의해 결정될 수 있다.
원하는 하이브리도마 세포가 확인된 후, 클론은 희석 절차를 제한함으로써 서브클로닝되고 표준 방법에 의해 성장될 수 있다. 상기한 Goding. 이러한 목적에 적합한 배양 배지는, 예를 들어 둘베코 수정 이글 배지(Dulbecco's Modified Eagle's Medium) 및 RPMI-1640 배지를 포함한다. 대안적으로, 하이브리도마 세포는 포유동물에서 복수로서 생체 내에서 성장될 수 있다.
서브클론에 의해 분비된 단클론성 항체는 통상적인 면역글로불린 정제 절차, 예컨대, 단백질 A-세파로스, 하이드록실아파타이트 크로마토그래피, 겔 전기영동, 투석, 또는 친화성 크로마토그래피에 의해 배양 배지 또는 복수 액으로부터 단리 또는 정제될 수 있다.
일부 실시형태에서, 항체 모이어티는 항체 모이어티 라이브러리(예컨대, scFv 또는 Fab 단편을 제시하는 파지 라이브러리)로부터 선택되는 클론 유래의 서열을 포함한다. 클론은 원하는 활성 또는 활성들을 가지는 항체 단편에 대한 조합 라이브러리를 스크리닝함으로써 확인될 수 있다. 예를 들어, 파지 디스플레이 라이브러리를 생성하고 원하는 결합 특징을 가지는 항체에 대한 이와 같은 라이브러리를 스크리닝하기 위한 다양한 방법이 당업계에 알려져 있다. 이와 같은 방법은, 예를 들어 문헌[Hoogenboom et al., Methods in Molecular Biology 178:1-37 (O'Brien et al., ed., Human Press, Totowa, N.J., 2001)]에서 검토되고, 예를 들어 문헌[McCafferty et al., Nature 348:552-554]; [Clackson et al., Nature 352: 624-628 (1991)]; [Marks et al., J. Mol. Biol. 222: 581-597 (1992)]; [Marks and Bradbury, Methods in Molecular Biology 248:161-175 (Lo, ed., Human Press, Totowa, N.J., 2003)]; [Sidhu et al., J. Mol. Biol. 338(2): 299-310 (2004)]; [Lee et al., J. Mol. Biol. 340(5): 1073-1093 (2004)]; [Fellouse, Proc. Natl. Acad. Sci. USA 101(34): 12467-12472 (2004)]; 및 [Lee et al., J. Immunol. Methods 284(1-2): 119-132(2004)]에 추가로 기재되어 있다.
특정 파지 디스플레이 방법에서, VH 및 VL 유전자의 레퍼토리는 중합효소 연쇄 반응(PCR)에 의해 개별적으로 클로닝되고 파지 라이브러리에서 무작위로 재조합되며, 이는 그 다음 문헌[Winter et al., Ann. Rev. Immunol., 12: 433-455 (1994)]에 기재된 바와 같이 항원-결합 부위에 대하여 스크리닝될 수 있다. 파지는 전형적으로 단일-사슬 Fv(scFv) 단편으로서 또는 Fab 단편으로서 항체 단편을 표시한다. 면역화 공급원 유래의 라이브러리는 하이브리도마를 구축할 필요없이 면역원에 대한 고친화성 항체를 제공한다. 대안적으로, 미경험 레퍼토리가 (예를 들어, 인간으로부터) 클로닝되어 문헌[Griffiths et al., EMBO J, 12: 725-734 (1993)]에 기재된 바와 같이 임의의 면역화 없이 광범위한 비-자가 및 또한 자가-항원에 대한 항체의 단일 공급원을 제공할 수 있다. 마지막으로, 미경험 라이브러리는 또한, 문헌[Hoogenboom and Winter, J. Mol. Biol., 227: 381-388 (1992)]에 기재된 바와 같이 줄기세포로부터 재배열되지 않은 V-유전자 절편을 클로닝하고, 무작위 서열을 함유하여 고도로 가변적인 CDR3 영역을 인코딩하고 시험관내 재배열을 수행하는 PCR 프라이머를 사용함으로써 합성적으로 제조될 수 있다. 인간 항체 파지 라이브러리를 기재하는 특허 공보는, 예를 들어 미국 특허 제5,750,373호, 및 미국 특허 공개 제2005/0079574호, 제2005/0119455호, 제2005/0266000호, 제2007/0117126호, 제2007/0160598호, 제2007/0237764호, 제2007/0292936호, 및 제2009/0002360호를 포함한다.
항체 모이어티는 파지 디스플레이를 사용하여 제조되어 표적 항원(예컨대, CD4, CCR5, 또는 CXCR4 폴리펩타이드)에 특이적인 항체에 대한 라이브러리를 스크리닝할 수 있다. 라이브러리는 적어도 1×109가지(예컨대, 적어도 약 1×109, 2.5×109, 5×109, 7.5×109, 1×1010, 2.5×1010, 5×1010, 7.5×1010, 또는 1×1011가지 중 어느 하나) 고유한 인간 항체 단편의 다양성을 가지는 인간 scFv 파지 디스플레이 라이브러리일 수 있다. 일부 실시형태에서, 라이브러리는 모든 인간 중쇄 및 경쇄 서브패밀리를 포함하는 건강한 공여자 유래의 인간 PMBC 및 비장으로부터 추출된 DNA로부터 구축된 미경험 인간 라이브러리이다. 일부 실시형태에서, 라이브러리는 다양한 질환을 가지는 환자, 예컨대, 자가면역 질환 환자, 암 환자, 및 전염병 환자로부터 단리된 PBMC로부터 추출된 DNA로부터 구축된 미경험 인간 라이브러리이다. 일부 실시형태에서, 라이브러리는 반-합성 인간 라이브러리이고, 여기서 중쇄 CDR3은 임의의 주어진 위치에서 동등하게 존재할 가능성이 있는 모든 아미노산(시스테인 제외)으로, 완전하게 무작위된다(예를 들어, 문헌[Hoet, R.M. et al., Nat. Biotechnol. 23(3):344-348, 2005] 참조). 일부 실시형태에서, 반-합성 인간 라이브러리의 중쇄 CDR3은 약 5 내지 약 24개(예컨대, 약 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 또는 24개 중 어느 하나)의 아미노산 길이를 가진다. 일부 실시형태에서, 라이브러리는 완전-합성 파지 디스플레이 라이브러리이다. 일부 실시형태에서, 라이브러리는 비-인간 파지 디스플레이 라이브러리이다.
높은 친화성으로 표적 항원에 결합하는 파지 클론은 표적 항원에 대한 파지의 반복적 결합에 의해 선택될 수 있으며, 이는 고체 지지체(예컨대, 용액 패닝용 비드 또는 세포 패닝용 포유동물 세포)에 결합된 다음, 비-결합 파지의 제거 및 특이적으로 결합된 파지의 용리가 이어진다. 용액 패닝의 예에서, 표적 항원은 고체 지지체에 대한 고정화를 위해 비오틴화될 수 있다. 비오틴화 표적 항원을 파지 라이브러리 및 고체 지지체, 예컨대, 스트렙트아비딘-접합체 다이나비드(Dynabead) M-280과 혼합한 다음, 표적 항원-파지-비드 복합체를 단리한다. 그 다음 결합된 파지 클론을 용리하고 발현 및 정제에 적절한 숙주 세포, 예컨대, 이. 콜라이 XL1-블루(Blue)를 감염시키는 데 사용한다. 세포 패닝의 예에서, CD4, CCR5, 또는 CXCR4를 발현하는 세포를 파지 라이브러리와 혼합하고, 그 후 세포를 수집하고 결합된 클론을 용리하여 발현 및정제에 적절한 숙주 세포를 감염시키는 데 사용한다. 패닝은 용액 패닝, 세포 패닝, 또는 이 둘 다의 조합으로 다수회(예컨대, 약 2, 3, 4, 5, 6회 또는 그 이상 중 어느 하나) 라운드 동안 수행되어, 표적 항원에 특이적으로 결합하는 파지 클론을 풍부화할 수 있다. 풍부화된 파지 클론은, 예를 들어 ELISA 및 FACS를 포함하여 당업계에 알려진 임의의 방법에 의해 표적 항원에 대한 특이적 결합에 대해 테스트될 수 있다.
인간 및 인간화 항체 모이어티
본 명세서에 기재된 항체 모이어티는 인간 또는 인간화된 것일 수 있다. 비-인간(예를 들어, 뮤린) 항체 모이어티의 인간화 형태는 전형적으로 비-인간 면역글로불린으로부터 유래된 최소 서열을 함유하는 키메라 면역글로불린, 면역글로불린 사슬, 또는 이들의 단편(예컨대, Fv, Fab, Fab', F(ab')2, scFv, 또는 항체의 다른 항원-결합 하위서열)이다. 인간화 항체 모이어티는 인간 면역글로불린, 면역글로불린 사슬, 또는 이의 단편(수용자 항체)을 포함하며, 여기서 수용체의 CDR 유래의 잔기는 원하는 특이성, 친화성, 및 능력을 가지는 비-인간 종(공여자 항체), 예컨대, 마우스, 래트, 또는 토끼의 CDR 유래의 잔기로 대체된다. 일부 예에서, 인간 면역글로불린의 Fv 프레임워크 잔기는 상응하는 비-인간 잔기로 대체된다. 또한, 인간화 항체 모이어티는 수용자 항체 모이어티에서도 또는 수입된 CDR 또는 프레임워크 서열에서도 발견되지 않는 잔기를 포함할 수 있다. 일반적으로, 인간화 항체 모이어티는 적어도 하나, 및 전형적으로 2개의 가변 도메인의 실질적으로 전부를 포함할 것이며, 여기서 CDR 영역의 전부 또는 실질적으로 전부는 비-인간 면역글로불린의 것에 상응하고, FR 영역의 전부 또는 실질적으로 전부는 인간 면역글로불린 컨센서스 서열의 것이다. 예를 들어, 문헌[Jones et al., Nature, 321: 522-525 (1986)]; [Riechmann et al., Nature, 332: 323-329 (1988)]; [Presta, Curr. Op. Struct. Biol., 2:593-596 (1992)]을 참조한다.
일반적으로, 인간화 항체 모이어티는 비-인간인 공급원으로부터 인간화 항체 모이어티로 도입된 하나 이상의 아미노산 잔기를 가진다. 이러한 비-인간 아미노산 잔기는 종종 "수입" 잔기로 지칭되며, 이는 전형적으로 "수입" 가변 도메인으로부터 취해진다. 일부 실시형태에 따르면, 인간화는 인간 항체 모이어티의 상응하는 서열을 설치류 CDR 또는 CDR 서열로 치환함으로써 윈터(Winter) 및 동료의 방법에 따라 본질적으로 수행될 수 있다(Jones et al., Nature, 321: 522-525 (1986); Riechmann et al., Nature, 332: 323-327 (1988); Verhoeyen et al., Science, 239: 1534-1536 (1988)). 따라서, 이와 같은 "인간화" 항체 모이어티는 항체 모이어티(미국 특허 제4,816,567호)이며, 여기서 온전한 인간 가변 도메인보다 실질적으로 더 적은 부분이 비-인간 종 유래의 상응하는 서열로 치환되었다. 실제로, 인간화 항체 모이어티는 전형적으로 일부 CDR 잔기 및 가능하게는 일부 FR 잔기가 설치류 항체의 유사한 부위 유래의 잔기로 치환된 인간 항체 모이어티이다.
인간화에 대한 대안으로서, 인간 항체 모이어티가 생성될 수 있다. 예를 들어, 면역화시 내인성 면역글로불린 생성의 부재시 인간 항체의 완전한 레퍼토리를 생성할 수 있는 유전자이식 동물(예를 들어, 마우스)을 생산하는 것이 이제 가능하다. 예를 들어, 키메라 및 생식선 돌연변이 마우스에서 항체 중쇄 결합 영역(JH) 유전자의 동형접합성 결실은 내인성 항체 생성의 완전한 저해를 초래한다고 설명되었다. 인간 생식선 면역글로불린 유전자 어레이의 이와 같은 생식선 돌연변이 마우스로의 전달은 항원 접종시 인간 항체의 생성을 초래할 것이다. 예를 들어, 문헌[Jakobovits et al., PNAS USA, 90:2551 (1993)]; [Jakobovits et al., Nature, 362:255-258 (1993)]; [Bruggemann et al., Year in Immunol., 7:33 (1993)], 미국 특허 제5,545,806호, 제5,569,825호, 제5,591,669호; 제5,545,807호; 및 WO 97/17852를 참조한다. 대안적으로, 인간 항체는 인간 면역글로불린 유전자좌를 유전자이식 동물, 예를 들어 내인성 면역글로불린 유전자가 부분적으로 또는 완전히 비활성화된 마우스 내로 도입함으로써 제조될 수 있다. 접종시, 인간 항체 생성은 유전자 재배열, 조립, 및 항체 레퍼토리를 포함하여 모든 면에 있어서 인간에서 보여지는 것과 매우 유사한 것으로 관찰된다. 이러한 접근법은, 예를 들어 미국 특허 제5,545,807호; 제5,545,806호; 제5,569,825호; 제5,625,126호; 제5,633,425호; 및 5,661,016호와, 문헌[Marks et al., Bio/Technology, 10: 779-783 (1992)]; [Lonberg et al., Nature, 368: 856-859 (1994)]; [Morrison, Nature, 368: 812-813 (1994)]; [Fishwild et al., Nature Biotechnology, 14: 845-851 (1996)]; [Neuberger, Nature Biotechnology, 14: 826 (1996)]; [Lonberg and Huszar, Intern. Rev. Immunol., 13: 65-93 (1995)]에 기재되어 있다.
인간 항체는 또한 시험관내에서 활성화된 B 세포에 의해(미국 특허 제5,567,610호 및 제5,229,275호 참조) 또는 파지 디스플레이 라이브러리를 포함하여 당업계에 알려진 다양한 기법을 사용함으로써 생성될 수 있다. 문헌[Hoogenboom and Winter, J. Mol. Biol., 227:381 (1991); Marks et al., J. Mol. Biol., 222:581 (1991)]. 콜(Cole)외 다수 및 보어너(Boerner)외 다수의 기법이 또한 인간 단클론성 항체의 제조에 이용 가능하다. 문헌[Cole et al., Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, p. 77 (1985) 및 Boerner et al., J. Immunol., 147(1): 86-95 (1991)].
추가적인 변이체
일부 실시형태에서, 본 명세서에서 제공되는 항원-결합 도메인의 아미노산 서열 변이체가 고려된다. 예를 들어, 항원-결합 도메인의 결합 친화성 및/또는 다른 생물학적 특성을 개선시키는 것이 바람직할 수 있다. 항원-결합 도메인의 아미노산 서열 변이체는 적절한 변형을 항원-결합 도메인을 인코딩하는 뉴클레오타이드 서열 내로 도입함으로써, 또는 펩타이드 합성에 의해 제조될 수 있다. 이와 같은 변형은, 예를 들어 항원-결합 도메인의 아미노산 서열내의 결실 및/또는 상기 아미노산 서열로의 삽입 및/또는 상기 아미노산 서열내 잔기의 치환을 포함한다. 최종 작제물이 원하는 특징, 예를 들어 항원-결합을 가진다면, 최종 작제물에 도달하도록 결실, 삽입, 및 치환의 임의의 조합이 이루어질 수 있다.
일부 실시형태에서, 하나 이상의 아미노산 치환을 가지는 항원-결합 도메인 변이체가 제공된다. 치환 돌연변이유발을 위한 관심 부위는 항체 모이어티의 HVR 및 FR을 포함한다. 아미노산 치환은 관심 항원-결합 도메인 내로 도입될 수 있으며, 생성물은 원하는 활성, 예를 들어 항원 결합의 유지/개선 또는 면역원성 감소에 대하여 스크리닝될 수 있다.
보존적 치환이 하기 표 4에 표시되어 있다. 본 명세서에서 논의된 변이체 CORS는 또한 이와 같은 보존적 치환을 함유할 수 있다.
아미노산은 일반적인 측쇄 특성에 따라 상이한 부류로 그룹화될 수 있다:
a. 소수성: 노르류신, Met, Ala, Val, Leu, Ile;
b. 중성 친수성: Cys, Ser, Thr, Asn, Gln;
c. 산성: Asp, Glu;
d. 염기성: His, Lys, Arg;
e. 사슬 배향에 영향을 미치는 잔기: Gly, Pro;
f. 방향족: Trp, Tyr, Phe.
비-보존적 치환은 이들 부류 중 하나의 구성원을 다른 부류로 교환하는 것을 수반할 것이다.
예시적인 치환 변이체는, 예를 들어 파지 디스플레이-기반 친화성 돌연변이 기법을 사용하여, 편리하게 생성될 수 있는 친화성 성숙 항체 모이어티이다. 간략하게, 하나 이상의 CDR 잔기가 돌연변이되고, 변이체 항체 모이어티가 파지 상에서 표시되며, 특정 생물학적 활성(예를 들어, 결합 친화성)에 대해 스크리닝된다. 변경(예를 들어, 치환)이 HVR에서 이루어져서, 예를 들어 항체 모이어티 친화성을 개선시킬 수 있다. 이와 같은 변경은 결합 친화성에 대해 테스트되는 생성된 변이체 VH 또는 VL을 이용하여, HVR "핫스팟", 즉 체세포 성숙 과정 동안 높은 빈도로 돌연변이를 겪는 코돈에 의해 인코딩되는 잔기(예를 들어, 문헌[Chowdhury, Methods Mol. Biol. 207:179-196 (2008)] 참조), 및/또는 특이성 결정 잔기(SDR)에서 이루어질 수 있다. 2차 라이브러리로부터의 구축 및 재선택에 의한 친화성 성숙은, 예를 들어 문헌[Hoogenboom et al. in Methods in Molecular Biology 178:1-37 (O'Brien et al., ed., Human Press, Totowa, NJ, (2001)]에 기재되었다.
친화성 성숙의 일부 실시형태에서, 다양성은 임의의 다양한 방법(예를 들어, 실수유발(error-prone) PCR, 사슬 셔플링, 또는 올리고뉴클레오타이드-지향(oligonucleotide-directed) 돌연변이유발)에 의해 성숙을 위해 선택된 가변 유전자 내로 도입된다. 그 다음 2차 라이브러리가 형성된다. 그 다음 라이브러리를 스크리닝하여 원하는 친화성을 가지는 임의의 항체 모이어티 변이체를 확인한다. 다양성을 도입하는 또 다른 방법은 HVR-지향 접근법을 포함하며, 여기서 몇몇 HVR 잔기(예를 들어, 한번에 4 내지 6개 잔기)가 무작위화된다. 항원 결합에 관여하는 HVR 잔기는, 예를 들어 알라닌 스캐닝 돌연변이유발 또는 모델링을 사용하여 구체적으로 확인될 수 있다. 구체적으로 CDR-H3 및 CDR-L3이 종종 표적화된다.
일부 실시형태에서, 치환, 삽입, 또는 결실은 이와 같은 변경이 항원에 결합하는 항체 모이어티의 능력을 실질적으로 감소시키지 않는 한 하나 이상의 HVR 내에서 발생할 수 있다. 예를 들어, 결합 친화성을 실질적으로 감소시키지 않는 보존적 변경(예를 들어, 본 명세서에서 제공되는 바와 같은 보존적 치환)이 HVR에서 이루어질 수 있다. 이와 같은 변경은 HVR "핫스팟" 또는 SDR의 외부에 있을 수 있다. 상기 제공된 변이체 VH 및 VL 서열의 일부 실시형태에서, 각각의 HVR은 변경되지 않거나, 1, 2 또는 3개 이하의 아미노산 치환을 함유한다.
돌연변이유발을 위해 표적화될 수 있는 항원-결합 도메인의 잔기 또는 영역의 확인을 위한 유용한 방법은 문헌[Cunningham and Wells (1989) Science, 244:1081-1085]에 의해 기재된 바와 같은 "알라닌 스캐닝 돌연변이유발"이라 불린다. 이 방법에서, 잔기 또는 표적 잔기의 그룹(예를 들어, arg, asp, his, lys, 및 glu와 같은 하전된 잔기)이 확인되고 중성 또는 음으로 하전된 아미노산(예를 들어, 알라닌 또는 폴리알라닌)으로 대체되어 항원-결합 도메인과 항원의 상호작용이 영향을 받는지 여부를 결정한다. 추가 치환이 아미노산 위치에 도입되어 초기 치환에 대한 기능적 민감성을 입증할 수 있다. 대안적으로, 또는 추가적으로, 항원-항원-결합 도메인 복합체의 결정 구조를 결정하여 항원-결합 도메인과 항원 사이의 접촉점을 확인할 수 있다. 이와 같은 접촉 잔기 및 인접 잔기는 치환을 위한 후보로서 표적화되거나 제거될 수 있다. 변이체를 스크리닝하여 변이체가 원하는 특성을 함유하는지 여부를 결정할 수 있다.
아미노산 서열 삽입은 하나의 잔기에서 100개 이상의 잔기를 함유하는 폴리펩타이드에 이르는 길이 범위의 아미노- 및/또는 카복실-말단 융합뿐만 아니라, 단일 또는 복수 아미노산 잔기의 서열내 삽입을 포함한다. 말단 삽입의 예는 N-말단 메티오닐 잔기를 가지는 항원-결합 도메인을 포함한다. 항원-결합 도메인의 다른 삽입 변이체는 항원-결합 도메인의 혈청 반감기를 증가시키는 폴리펩타이드 또는 효소(예를 들어, ADEPT에 대함)에 대한 항원-결합 도메인의 N- 또는 C-말단에의 융합을 포함한다.
핵산의 발현
본 명세서에 기재된 이종성 핵산은 면역 세포에서 일시적으로 또는 안정적으로 통합될 수 있다. 일부 실시형태에서, 이종성 핵산은 조작된 면역 세포에서 일시적으로 발현된다. 예를 들어, 이종성 핵산은 이종성 유전자 발현 카세트를 포함하는 염색체외 어레이에서 조작된 면역 세포의 핵에 존재할 수 있다. 이종성 핵산은, 바이러스 또는 비-바이러스 방법을 포함하여 당업계에 알려진 임의의 형질감염 또는 형질도입 방법을 사용하여 조작된 포유동물 내로 도입될 수 있다. 예시적인 비-바이러스 형질감염 방법은 키메라-기반 형질감염, 예컨대, 인산칼슘, 덴드리머, 리포좀, 또는 양이온성 중합체(예를 들어, DEAE-덱스트란 또는 폴리에틸렌이민)의 사용; 비-화학적 방법, 예컨대, 전기천공, 세포 압착, 초음파천공, 광학 형질감염, 임페일펙션(impalefection), 원형질체 융합, 유체역학적 전달, 또는 트랜스포존; 입자-기반 방법, 예컨대, 유전자총, 마그네토펙션(magnectofection) 또는 자석 보조(magnet assisted) 형질감염, 입자 충격의 사용; 및 하이브리드 방법, 예컨대, 뉴클레오펙션(nucleofection)을 포함하지만 이들로 제한되는 것은 아니다. 일부 실시형태에서, 이종성 핵산은 DNA이다. 일부 실시형태에서, 이종성 핵산은 RNA이다. 일부 실시형태에서, 이종성 핵산은 선형이다. 일부 실시형태에서, 이종성 핵산은 원형이다.
일부 실시형태에서, 이종성 핵산은 조작된 면역 세포의 게놈에 존재한다. 예를 들어, 이종성 핵산은, 예컨대, 부위-특이적 재조합효소 또는 인테그라제, 트랜스포사제, 전사 활성화제-유사 이펙터 뉴클레아제(TALEN®), CRISPR/Cas9, 및 아연-핑거 뉴클레아제를 사용하여, 바이러스-매개 통합, 무작위 통합, 상동성 재조합 방법, 및 부위-지향 통합 방법을 포함하지만 이들로 제한되는 것은 아닌 당업계에 알려진 임의의 방법에 의해 면역 세포 게놈 내로 통합될 수 있다. 일부 실시형태에서, 이종성 핵산은 조작된 면역 세포 게놈의 특이적으로 설계된 유전자좌에 통합된다. 일부 실시형태에서, 이종성 핵산은 조작된 면역 세포 게놈의 통합 핫스팟에 통합된다. 일부 실시형태에서, 이종성 핵산은 조작된 면역 세포 게놈의 무작위 유전자좌에 통합된다. 이종성 핵산의 다수 복제물이 단일의 조작된 면역 세포에 존재하는 경우, 이종성 핵산은 조작된 면역 세포 게놈의 복수의 유전자좌에 통합될 수 있다.
본 명세서에 기재된 이종성 핵산(예를 들어, CR, CCOR, 및 COR을 인코딩하는 핵산)은 프로모터에 작동 가능하게 연결될 수 있다. 일부 실시형태에서, 프로모터는 내인성 프로모터이다. 예를 들어, 핵산(예를 들어, CR, CCOR, 및 COR을 인코딩하는 핵산)은 당업계에 알려진 임의의 방법, 예컨대, CRISPR/Cas9 방법을 사용하여 내인성 프로모터의 하류에서 조작된 면역 세포의 게놈에 녹인(knocked-in)될 수 있다. 일부 실시형태에서, 내인성 프로모터는 풍부한 단백질, 예컨대, 베타-액틴에 대한 프로모터이다. 일부 실시형태에서, 내인성 프로모터는, 예를 들어 조작된 면역 세포의 내인성 활성화 신호에 의해 유도 가능한, 유도성 프로모터이다. 조작된 면역 세포가 T 세포인 일부 실시형태에서, 프로모터는 T 세포 활성화-의존성 프로모터(예컨대, IL-2 프로모터, NFAT 프로모터, 또는 NFκB 프로모터)이다.
일부 실시형태에서, 프로모터는 이종성 프로모터이다.
일부 실시형태에서, 이종성 핵산(예를 들어, CR, CCOR, 또는 COR을 인코딩하는 핵산)은 구성적 프로모터에 작동 가능하게 연결된다. 일부 실시형태에서, 이종성 핵산(예를 들어, CR, CCOR, 또는 COR을 인코딩하는 핵산)은 유도성 프로모터에 작동 가능하게 연결된다. 일부 실시형태에서, 구성적 프로모터는 CR을 인코딩하는 핵산에 작동 가능하게 연결되고, 유도성 프로모터는 CCOR 또는 COR을 인코딩하는 핵산에 작동 가능하게 연결된다. 일부 실시형태에서, 제1 유도성 프로모터는 CR을 인코딩하는 핵산에 작동 가능하게 연결되고, 제2 유도성 프로모터는 CCOR을 인코딩하는 핵산에 작동 가능하게 연결되거나, 그 반대이다. 일부 실시형태에서, 제1 유도성 프로모터는 CR을 인코딩하는 핵산에 작동 가능하게 연결되고, 제2 유도성 프로모터는 COR을 인코딩하는 핵산에 작동 가능하게 연결되거나, 그 반대이다. 일부 실시형태에서, 제1 유도성 프로모터는 CCOR을 인코딩하는 핵산에 작동 가능하게 연결되고, 제2 유도성 프로모터는 COR을 인코딩하는 핵산에 작동 가능하게 연결되거나, 그 반대이다. 일부 실시형태에서, 제1 유도성 프로모터는 제1 유도 조건에 의해 유도 가능하고, 제2 유도성 프로모터는 제2 유도 조건에 의해 유도 가능하다. 일부 실시형태에서, 제1 유도 조건은 제2 유도 조건과 동일하다. 일부 실시형태에서, 제1 유도성 프로모터 및 제2 유도성 프로모터는 동시에 유도된다. 일부 실시형태에서, 제1 유도성 프로모터 및 제2 유도성 프로모터는 순차적으로 유도되고, 예를 들어 제1 유도성 프로모터는 제2 유도성 프로모터 전에 유도되거나, 제1 유도성 프로모터는 제2 유도성 프로모터 후에 유도된다.
구성적 프로모터는 이종성 유전자(또한 이식유전자라고 지칭됨)가 숙주 세포에서 구성적으로 발현될 수 있게 한다. 본 명세서에서 고려되는 예시적인 구성적 프로모터는 사이토메갈로바이러스(CMV) 프로모터, 인간 신장 인자-1알파(hEF1α), 유비퀴틴 C 프로모터(UbiC), 포르포글리세로키나제 프로모터(PGK), 유인원 바이러스 40 초기 프로모터(SV40), 및 CMV 초기 인핸서와 결합된 닭 β-액틴 프로모터(CAGG)를 포함하지만 이들로 제한되는 것은 아니다. 이식유전자 발현을 구동하는 것에 대한 이와 같은 구성적 프로모터의 효율성은 수많은 연구에서 널리 비교되었다. 예를 들어, 마이클 C. 밀론(Michael C. Milone)외 다수는 1차 인간 T 세포에서 키메라 항원 수용체 발현을 구동시키는 CMV, hEF1α, UbiC 및 PGK의 효율성을 비교하였고, hEF1α 프로모터가 가장 높은 수준의 이식유전자 발현을 유도할 뿐만 아니라 CD4 및 CD8 인간 T 세포에서 최적으로 유지된다는 결론을 내렸다(Molecular Therapy, 17(8): 1453-1464 (2009)). 일부 실시형태에서, 이종성 핵산의 프로모터는 hEF1α 프로모터이다.
유도성 프로모터는 하나 이상의 조건, 예컨대, 물리적 조건, 조작된 면역 세포의 미세환경, 또는 조작된 면역 세포의 생리적 상태, 유도제(즉, 유도 작용제), 또는 이들의 조합에 의해 유도될 수 있다. 일부 실시형태에서, 유도 조건은 조작된 면역 세포, 및/또는 약제학적 조성물을 받은 대상체에서 내인성 유전자의 발현을 유도하지 않는다. 일부 실시형태에서, 유도 조건은 유도제, 조사(예컨대, 전리 방사선, 빛), 온도(예컨대, 열), 산화환원 상태, 종양 환경, 및 조작된 면역 세포의 활성화 상태로 이루어진 군으로부터 선택된다.
일부 실시형태에서, 프로모터는 유도제에 의해 유도 가능하다. 일부 실시형태에서, 유도제는 소분자, 예컨대, 화학적 화합물이다. 일부 실시형태에서, 소분자는 독시사이클린, 테트라사이클린, 알코올, 금속, 또는 스테로이드로 이루어진 군으로부터 선택된다. 화학적으로 유도된 프로모터가 가장 널리 연구되었다. 이와 같은 프로모터는 전사 활성이 소분자 화학물질, 예컨대, 독시사이클린, 테트라사이클린, 알코올, 스테로이드, 금속 및 다른 화합물의 존재 또는 부재에 의해 조절되는 프로모터를 포함한다. 역 테트라사이클린-제어 트랜스작용인자(rtTA) 및 테트라사이클린-반응성 요소 프로모터(TRE)를 가지는 독시사이클린-유도성 시스템은 현재 가장 발달된 시스템이다. WO9429442는 테트라사이클린 반응성 프로모터에 의한 진핵 세포에서 유전자 발현의 엄격한 제어를 기재한다. WO9601313은 테트라사이클린-조절 전사 조절제를 개시한다. 추가적으로, 테트(Tet) 기술, 예컨대, 테트-온(Tet-on) 시스템은, 예를 들어 테트시스템즈 닷 컴(TetSystems.com)의 웹사이트에 기재되어 있다. 알려진 임의의 화학적 조절 프로모터가 본 출원에서 치료 단백질의 발현을 구동하는 데 사용될 수 있다.
일부 실시형태에서, 유도제는 폴리펩타이드, 예컨대, 성장 인자, 호르몬, 또는 세포 표면 수용체에 대한 리간드, 예를 들어 종양 항원에 특이적으로 결합하는 폴리펩타이드이다. 일부 실시형태에서, 폴리펩타이드는 조작된 면역 세포에 의해 발현된다. 일부 실시형태에서, 폴리펩타이드는 이종성 핵산에서 핵산에 의해 인코딩된다. 다수의 폴리펩타이드 유도제가 또한 당업계에 알려져 있으며, 이는 본 발명에서 사용하기에 적합할 수 있다. 예를 들어, 엑디손 수용체-기반 유전자 스위치, 프로게스테론 수용체-기반 유전자 스위치, 및 에스트로겐 수용체 기반 유전자 스위치는 스테로이드 수용체 유래 트랜스작용인자를 이용하는 유전자 스위치에 속한다(WO9637609 및 WO9738117 등).
일부 실시형태에서, 유도제는 소분자 구성요소 및 하나 이상의 폴리펩타이드를 둘 다 포함한다. 예를 들어, 폴리펩타이드의 이량체화에 의존하는 유도성 프로모터가 당업계에 알려져 있으며, 이는 본 발명에서 사용하기에 적합할 수 있다. 1993년에 개발된 최초의 소분자 CID 시스템은 약물 FK506의 유도체인 FK1012를 사용하여 FKBP의 동종이량체화를 유도하였다. 유사한 전략을 이용함으로써, 우(Wu)외 다수는 라팔로그(Rapalog)/FKPB-FRB* 및 지베렐린/GID1-GAI 이량체화 의존성 유전자 스위치를 사용함으로써 온-스위치 방식을 통해 성공적으로 CAR-T 세포를 적정가능하게 만든다(C.-Y. Wu et al., Science 350, aab4077 (2015)). 다른 이량체화 의존성 스위치 시스템은 쿠메르마이신/GyrB-GyrB(Nature 383 (6596): 178-81), 및 HaXS/스냅(Snap)-태그-할로태그(HaloTag)(Chemistry and Biology 20 (4): 549-57)를 포함한다.
일부 실시형태에서, 프로모터는 광-유도성 프로모터이고, 유도 조건은 빛이다. 포유동물 세포에서 유전자 발현을 조절하기 위한 광 유도성 프로모터는 또한 당업계에 잘 알려져 있다(예를 들어, 문헌[Science 332, 1565-1568 (2011)]; [Nat. Methods 9, 266-269 (2012)]; [Nature 500: 472-476 (2013)]; [Nature Neuroscience 18:1202-1212 (2015)] 참조). 이와 같은 유전자 조절 시스템은 (1) DNA 결합 또는 (2) DNA 결합 단백질에 대한 전사 활성화 도메인의 동원에 대한 규정을 기반으로 한 2가지 카테고리로 대략적으로 나뉠 수 있다. 예를 들어, 청색광(480 nm)에 반응하여 NFAT의 칼시뉴린-매개 동원을 초래하는 세포내 칼슘 증가를 촉발시키는 멜라놉신을 기반으로 한 합성 포유동물 청색광 제어 전사 시스템이 개발되었고 포유동물 세포에서 테스트되었다. 보다 최근에, 모타-메타(Motta-Mena)외 다수는 인간 세포주와 제브라피쉬 배아에서 전사 개시에 대한 높은 수준의 청색광-민감성 제어를 부여하는 자연 발생 EL222 전사 인자로부터 개발된 새로운 유도성 유전자 발현 시스템을 설명하였다(Nat. Chem. Biol. 10(3):196-202 (2014)). 추가적으로, 애기장대(Arabidopsis thaliana)의 광수용체 피토크롬 B(PhyB)와 피토크롬-상호작용 인자 6(PIF6)의 적색광 유도된 상호작용은 적색광 촉발 유전자 발현 조절을 위해 이용되었다. 또한, 자외선 B(UVB)-유도성 유전자 발현 시스템이 또한 개발되어 포유동물 세포에서 표적 유전자 전사에 효과적인 것으로 입증되었다(Chapter 25 of Gene and Cell Therapy: Therapeutic Mechanisms and Strategies, Fourth Edition CRC Press, Jan. 20th,2015). 본 명세서에 기재된 임의의 광-유도성 프로모터는 본 발명에서 치료 단백질의 발현을 구동하는 데 사용될 수 있다.
일부 실시형태에서, 프로모터는 광-유도성 분자와 빛의 조합에 의해 유도되는 광-유도성 프로모터이다. 예를 들어, 화학 유도제 상의 광-절단가능 광케이징된(photocaged) 기는 광케이징된 기가 조사를 통해 또는 다른 수단에 의해 제거되지 않는 한 유도제를 비활성 상태로 유지한다. 이와 같은 광-유도성 분자는 소분자 화합물, 올리고뉴클레오타이드, 및 단백질을 포함한다. 예를 들어, 케이징된 엑디손, 락(lac) 오페론과 함께 사용하기 위한 케이징된 IPTG, 리보자임-매개 유전자 발현을 위한 케이징된 토요카마이신, 테트-온 시스템과 함께 사용하기 위한 케이징된 독시사이클린, 및 광 매개 FKBP/FRB 이량체화를 위한 케이징된 라팔로그가 개발되었다(예를 들어, 문헌[Curr Opin Chem Biol. 16(3-4): 292-299 (2012)] 참조).
일부 실시형태에서, 프로모터는 방사선-유도성 프로모터이고, 유도 조건은 방사선, 예컨대, 전리 방사선이다. 방사선 유도성 프로모터는 또한 이식유전자 발현을 제어하기 위해 당업계에 알려져 있다. 유전자 발현의 변경은 세포의 조사시 일어난다. 예를 들어, "급초기 유전자"로 알려진 유전자 그룹은 전리 방사선에 즉시 반응할 수 있다. 예시적인 급초기 유전자는 Erg-1, p21/WAF-1, GADD45알파, t-PA, c-Fos, c-Jun, NF-카파B, 및 AP1을 포함하지만 이들로 제한되는 것은 아니다. 급초기 유전자는 프로모터 영역에 방사선 반응 서열을 포함한다. 컨센서스 서열인 CC(A/T)6GG는 Erg-1 프로모터에서 발견되었으며, 이는 혈청 반응 요소로 지칭되거나 CArG 요소인 것으로 알려져 있다. 방사선 유도 프로모터와 이식유전자의 조합은 집중적으로 연구되어 왔으며, 치료 이익으로 효율적임이 입증되었다. 예를 들어, 문헌[Cancer Biol Ther. 6(7):1005-12 (2007)] 및 [Chapter 25 of Gene and Cell Therapy: Therapeutic Mechanisms and Strategies, Fourth Edition CRC Press, Jan. 20th, 2015]을 참조한다. 임의의 급초기 유전자 프로모터 또는 혈청 반응 요소를 포함하는 임의의 프로모터는 본 발명의 치료 단백질의 발현을 구동하는 데 방사선 유도성 프로모터로서 유용할 수 있다.
일부 실시형태에서, 프로모터는 열 유도성 프로모터이고, 유도 조건은 열이다. 이식유전자 발현을 구동하는 열 유도성 프로모터는 또한 당업계에서 널리 연구되어 왔다. Hsp90, Hsp70, Hsp60, Hsp40, Hsp10 등을 포함한 열 충격 또는 스트레스 단백질(HSP)은 열 또는 다른 물리적 및 화학적 스트레스 하에서 세포를 보호하는 데 중요한 역할을 한다. 열-충격 단백질(HSP) 프로모터 및 성장 저지 및 DNA 손상(GADD) 153 프로모터를 포함한 몇몇 열 유도성 프로모터가 전임상 연구에서 시도되었다. 1985년에 처음 기재된 인간 hsp70B 유전자의 프로모터는 가장 고도로 효율적인 열 유도성 프로모터 중 하나인 것으로 보인다. 후앙(Huang)외 다수는 hsp70B-EGFP, hsp70B-TNF알파 및 hsp70B-IL12 코딩 서열의 도입 후, 종양 세포가 열 처리시 매우 높은 이식유전자 발현을 나타낸 반면, 열처리의 부재시 이식유전자의 발현은 검출되지 않았다고 보고하였다. 그리고 생체 내에서 IL12 이식유전자와 열처리된 마우스 그룹에서 종양 성장이 상당히 지연되었다(Cancer Res. 60:3435 (2000)). 또 다른 과학자 그룹은 HSV-tk 자살 유전자를 hsp70B 프로모터에 연결하고 마우스 유방암을 보유하는 누드 마우스에서 시스템을 테스트하였다. 종양에 hsp70B-HSVtk 코딩 서열을 투여받고 열 처리된 마우스는 열처리하지 않은 대조군과 비교하여 종양 퇴행 및 상당한 생존율을 나타내었다(Hum. Gene Ther. 11:2453 (2000)). 당업계에 알려진 추가적인 열 유도성 프로모터는, 예를 들어 문헌[Chapter 25 of Gene and Cell Therapy: Therapeutic Mechanisms and Strategies, Fourth Edition CRC Press, Jan. 20th, 2015]에서 찾아볼 수 있다. 본 명세서에서 논의된 임의의 열-유도성 프로모터는 본 발명의 치료 단백질의 발현을 구동하는 데 사용될 수 있다.
일부 실시형태에서, 프로모터는 산화환원 상태에 의해 유도 가능하다. 산화환원 상태에 의해 유도 가능한 예시적인 프로모터는 유도성 프로모터 및 저산소증 유도성 프로모터를 포함한다. 예를 들어, 포스트 드(Post DE)외 다수는 저산소증-유도 인자(HIF)-활성 종양 세포에서 이식유전자 발현을 특이적이고 강하게 유도하는 HIF 반응성 프로모터를 개발하였다(Gene Ther. 8: 1801-1807 (2001); Cancer Res. 67: 6872-6881 (2007)).
일부 실시형태에서, 프로모터는 조작된 면역 세포의 생리학적 상태, 예컨대, 내인성 활성 신호에 의해 유도 가능하다. 조작된 면역 세포가 T 세포인 일부 실시형태에서, 프로모터는 T 세포 활성화-의존성 프로모터이며, 이는 조작된 T 세포의 내인성 활성화 신호에 의해 유도 가능하다. 일부 실시형태에서, 조작된 T 세포는 유도제, 예컨대, PMA, 이오노마이신, 또는 피토헤마글루티닌에 의해 활성화된다. 일부 실시형태에서, 조작된 T 세포는 내인성 T 세포 수용체, 또는 조작된 수용체(예컨대, 재조합 TCR, 또는 CAR)를 통해 종양 세포 상에서 종양 항원의 인식에 의해 활성화된다. 일부 실시형태에서, 조작된 T 세포는 면역 관문의 차단에 의해, 예컨대, 조작된 T 세포 또는 제2 조작된 면역 세포에 의해 발현되는 면역조절제에 의해 활성화된다. 일부 실시형태에서, T 세포 활성화-의존성 프로모터는 IL-2 프로모터이다. 일부 실시형태에서, T 세포 활성화-의존성 프로모터는 NFAT 프로모터이다. 일부 실시형태에서, T 세포 활성화-의존성 프로모터는 NFκB 프로모터이다.
어떠한 이론이나 가설에 구속되지 않으면서, IL-2 프로모터로부터 유전자 전사에 의해 개시되는 IL-2 발현은 T 세포 활성화의 주요 활성이다. 포볼 12-미리스테이트 13-아세테이트(PMA), 또는 이오노마이신, 또는 피토헤마글루티닌에 의한 인간 T 세포의 비특이적 자극은 자극된 T 세포로부터 IL-2 분비를 초래한다. IL-2 프로모터는 유전적으로 조작된 T-세포에서 활성화-유도된 이식유전자 발현에 대해 조사되었다(Virology Journal 3:97 (2006)). 본 발명자들은 IL-2 프로모터가 인간 T 세포주에서 PMA/PHA-P 활성화의 존재하에 리포터 유전자 발현을 개시하는 데 효율적이라는 것을 발견하였다. T 세포 수용체 자극은 세포내 반응의 캐스케이드를 개시하여 세포질 칼슘 농도의 증가를 야기하고 NFAT 및 NFκB 둘 다의 핵 번역을 초래한다. 활성화된 T 세포의 핵 인자(NFAT)의 구성원은 T 림프구에서 면역 반응을 매개하는 Ca2+ 의존성 전사 인자이다. NFAT는 활성화된 T 세포에서 유도성 인터류킨-2(IL-2) 발현에 중요한 것으로 나타났다(Mol Cell Biol. 15(11):6299-310 (1995); Nature Reviews Immunology 5:472-484 (2005)). 본 발명자들은 NFAT 프로모터가 인간 T 세포주에서 PMA/PHA-P 활성화의 존재하에 리포터 유전자 발현을 개시하는 데 효율적이라는 것을 발견하였다. 핵 인자 카파 B(NFκB)를 포함한 다른 경로가 또한 T 세포 활성화를 통해 이식유전자 발현을 제어하는 데 이용될 수 있다.
면역 세포
본 발명에 유용한 예시적인 면역 세포는 수지상 세포(미성숙 수지상 세포 및 성숙 수지상 세포를 포함함), T 림프구(예컨대, 미경험 T 세포, 이펙터 T 세포, 기억 T 세포, 세포독성 T 림프구, T 헬퍼 세포, 자연 살해 T 세포, Treg 세포, 종양 침윤 림프구(TIL), 및 림포카인-활성화 살해(LAK) 세포), B 세포, 자연 살해(NK) 세포, NKT 세포, γδT 세포, 단핵구, 대식세포, 호중구, 과립구, 및 이들의 조합을 포함하지만 이들로 제한되는 것은 아니다. 면역 세포의 하위집단은 당업계에 알려진 하나 이상의 세포 표면 마커(예를 들어, CD3, CD4, CD8, CD19, CD20, CD11c, CD123, CD56, CD34, CD14, CD33 등)의 존재 또는 부재에 의해 정의될 수 있다. 약제학적 조성물이 복수의 조작된 포유동물 면역 세포를 포함하는 경우, 조작된 포유동물 면역 세포는 면역 세포 유형의 특정 하위집단, 면역 세포 유형의 하위집단의 조합, 또는 둘 이상의 면역 세포 유형의 조합일 수 있다. 일부 실시형태에서, 면역 세포는 동종성 세포 집단에 존재한다. 일부 실시형태에서, 면역 세포는 면역 세포에서 증강된 이종성 세포 집단에 존재한다. 일부 실시형태에서, 조작된 면역 세포는 림프구이다. 일부 실시형태에서, 조작된 면역 세포는 림프구가 아니다. 일부 실시형태에서, 조작된 면역 세포는 입양 면역요법에 적합하다. 일부 실시형태에서, 조작된 면역 세포는 PBMC이다. 일부 실시형태에서, 조작된 면역 세포는 PBMC로부터 유래된 면역 세포이다. 일부 실시형태에서, 조작된 면역 세포는 T 세포이다. 일부 실시형태에서, 조작된 면역 세포는 CD4+ T 세포이다. 일부 실시형태에서, 조작된 면역 세포는 CD8+ T 세포이다. 일부 실시형태에서, 조작된 면역 세포는 B 세포이다. 일부 실시형태에서, 조작된 면역 세포는 NK 세포이다.
조작된 면역 세포의 제조
본 명세서에 기재된 다양한 작제물(예컨대, CR, COOR, 및/또는 COR)을 발현하는 면역 세포는 하나 이상의 핵산(예를 들어, 렌티바이러스 벡터), 예컨대, CR, CCOR 및/또는 COR을 인코딩하는 핵산을 면역 세포 내에 도입함으로써 생성될 수 있다. 일부 실시형태에서, 벡터는 바이러스 벡터이다. 바이러스 벡터의 예는 아데노바이러스 벡터, 아데노-연관 바이러스 벡터, 렌티바이러스 벡터, 레트로바이러스 벡터, 백시니아 벡터, 단순 헤스페스 바이러스 벡터, 및 이들의 유도체를 포함하지만 이들로 제한되는 것은 아니다. 바이러스 벡터 기술은 당업계에 잘 알려져 있으며, 예를 들어 문헌[Sambrook et al. (2001, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, New York)], 및 다른 바이러스학 및 분자 생물학 매뉴얼에 기재되어 있다.
포유동물 세포 내로의 유전자 전달을 위해 다수의 바이러스 기반 시스템이 개발되었다. 예를 들어, 레트로바이러스는 유전자 전달 시스템을 위한 편리한 플랫폼을 제공한다. 이종성 핵산은 당업계에 알려진 기법을 사용하여 벡터 내로 삽입되고 레트로바이러스 입자에 패키징될 수 있다. 그 다음 재조합 바이러스는 단리되어 시험관내 또는 생체 외에서 조작된 면역 세포로 전달될 수 있다. 다수의 레스토바이러스 시스템이 당업계에 알려져 있다. 일부 실시형태에서, 아데노바이러스 벡터가 사용된다. 다수의 아데노바이러스 벡터가 당업계에 알려져 있다. 일부 실시형태에서, 렌티바이러스 벡터가 사용된다. 일부 실시형태에서, 자가-비활성화 렌티바이러스 벡터가 사용된다. 예를 들어, 면역조절제(예컨대, 면역관문 저해제) 코딩 서열을 보유하는 자가-비활성화 렌티바이러스 벡터 및/또는 키메라 항원 수용체를 보유하는 자가-비활성화 렌티바이러스 벡터가 당업계에 알려진 프로토콜을 이용하여 패키징될 수 있다. 생성된 렌티바이러스 벡터는 당업계에 알려진 방법을 사용하여 포유동물 세포(예컨대, 1차 인간 T 세포)를 형질도입하는 데 사용될 수 있다.
일부 실시형태에서, 형질도입 또는 형질감염된 포유동물 세포는 이종성 핵산의 도입 후 생체 외에서 증식된다. 일부 실시형태에서, 형질도입 또는 형질감염된 포유동물 세포는 적어도 약 1일, 2일, 3일, 4일, 5일, 6일, 7일, 10일, 12일, 또는 14일 중 어느 하나 동안 배양되어 증식한다. 일부 실시형태에서, 형질도입 또는 형질감염된 포유동물 세포는 약 1일, 2일, 3일, 4일, 5일, 6일, 7일, 10일, 12일, 또는 14일 중 어느 하나 이하 동안 배양된다. 일부 실시형태에서, 형질도입 또는 형질감염된 포유동물 세포는 추가로 평가 또는 스크리닝되어 조작된 면역 세포를 선택한다.
면역 세포로의 하나 이상의 핵산의 도입은 당업계에 알려진 기법을 사용하여 달성될 수 있다. 일부 실시형태에서, 조작된 면역 세포(예컨대, 조작된 T 세포)는 생체 내에서 복제되어 표적 항원의 발현과 연관된 질환(예컨대, 바이러스 감염)의 지속된 제어로 이어질 수 있는 장기 지속성을 초래할 수 있다.
일부 실시형태에서, 본 발명은 전염병, 예컨대, HIV를 가지거나 발병할 위험이 있는 환자의 치료를 위해 본 명세서에 기재된 조작된 면역 세포를 투여하는 것에 관한 것이다. 일부 실시형태에서, 자가 림프구 주입이 치료에 사용된다. 자가 PBMC가 치료를 필요로 하는 환자로부터 수집되고 본 명세서에 기재되고 당업계에 알려진 방법을 사용하여 T 세포가 활성화되고 확장된 다음 환자에게 다시 주입된다.
일부 실시형태에서, HIV를 치료하는 데 사용하기 위한 본 명세서에 기재된 조작된 면역 세포가 제공된다. 세포는 강력한 생체 내 확장을 겪을 수 있고 혈액과 골수에서 오랜 시간 동안 높은 수준으로 유지되는 표적 항원-특이적 기억 세포를 확립할 수 있다. 일부 실시형태에서, 환자에게 주입된 조작된 면역 세포는 바이러스-감염 세포를 제거할 수 있다. 일부 실시형태에서, 환자에게 주입된 조작된 면역 세포는 바이러스-감염 세포를 제거할 수 있다.
면역 세포의 확장 및 유전적 변형 이전에, 면역 세포의 공급원은 대상체로부터 수득된다. 면역 세포는, 말초 혈액 단핵 세포, 골수, 림프절 조직, 제대혈, 흉선 조직, 감염 부위의 조직, 복수, 흉막 삼출액, 비장 조직, 및 종양을 포함하여, 다수의 공급원으로부터 수득될 수 있다. 본 발명의 일부 실시형태에서, 당업계에서 이용 가능한 다수의 면역 세포주가 사용될 수 있다. 본 발명의 일부 실시형태에서, 면역 세포는 당업자에게 알려진 다수의 기법, 예컨대, 피콜(FICOLL)(상표) 분리를 사용하여 대상체로부터 수집된 혈액 단위로부터 수득될 수 있다. 일부 실시형태에서, 개체의 순환 혈액 유래의 세포는 분리반출법에 의해 수득된다. 분리반출 생성물은 전형적으로 T 세포, 단핵구, 과립구, B 세포, 다른 유핵 백혈구, 적혈구, 및 혈소판을 포함한 림프구를 함유한다. 일부 실시형태에서, 분리반출법에 의해 수집된 세포는 세척되어 혈장 분획을 제거하고 후속 처리 단계를 위해 적절한 완충액 또는 배지에 세포를 배치할 수 있다. 일부 실시형태에서, 세포는 인산염 완충 식염수(PBS)로 세척된다. 일부 실시형태에서, 세척액에는 칼슘이 없고 마그네슘이 없을 수 있거나 모든 2가 양이온은 아니지만 많은 양이 없을 수 있다. 당업자는 세척 단계가 당업자에게 알려진 방법에 의해, 예컨대, 제조자의 지침에 따라 반자동 "통과(flow-through)" 원심분리기(예를 들어, 코브(Cobe) 2991 세포 처리기, 백스터 사이토메이트(Baxter CytoMate), 또는 헤모네틱스 셀 세이버 5(Haemonetics Cell Saver 5))를 사용함으로써 달성될 수 있다. 세척 후, 세포는 다양한 생체적합성 완충액, 예컨대, 무-Ca2+, 무-Mg2+ PBS, 플라스마라이트(PlasmaLyte) A, 또는 완충액이 있거나 없는 다른 식염수 용액 중에 재현탁될 수 있다. 대안적으로, 분리반출 샘플의 바람직하지 않은 구성요소를 제거하고 세포를 배양 배지에 직접 재현탁할 수 있다.
일부 실시형태에서, 면역 세포(예컨대, T 세포)는 적혈구를 용해하고, 예를 들어 퍼콜(PERCOLL)(상표) 구배를 통한 원심분리에 의해 또는 역류 원심성 세포분리(counterflow centrifugal elutriation)에 의해 단핵구를 고갈시킴으로써 말초 혈액 림프구로부터 단리된다. T 세포의 특정 하위집단, 예컨대, CD3+, CD28+, CD4+, CD8+, CD45RA+, 및 CD45RO+ T 세포는 양성 또는 음성 선택 기법에 의해 추가로 단리될 수 있다. 예를 들어, 일부 실시형태에서, T 세포는 원하는 T 세포의 양성 선택에 충분한 기간 동안 항-CD3/항-CD28(즉, 3×28)-접합체 비드, 예컨대, DYNABEADS® M-450 CD3/CD28 T와 함께 인큐베이션함으로써 단리된다. 일부 실시형태에서, 기간은 약 30분이다. 일부 실시형태에서, 기간은 30분 내지 36시간 이상(이들 값 사이의 모든 범위를 포함함)의 범위이다. 일부 실시형태에서, 기간은 적어도 1, 2, 3, 4, 5, 또는 6시간이다. 일부 실시형태에서, 기간은 10 내지 24시간이다. 일부 실시형태에서, 인큐베이션 기간은 24시간이다. 더 긴 인큐베이션 시간은 다른 세포 유형과 비교하여 적은 수의 T 세포가 있는 임의의 상황에서 T 세포를 단리시키는 데 사용될 수 있다. 또한, 더 긴 인큐베이션 시간의 사용은 CD8+ T 세포의 포획 효율을 증가시킬 수 있다. 따라서, T 세포가 CD3/CD28 비드에 결합하도록 허용되는 시간을 단순히 단축하거나 연장함으로써 및/또는 비드 대 T 세포의 비율을 증가시키거나 감소시킴으로써, T 세포의 하위집단은 배양 개시에 있어서 또는 이에 대해 또는 과정 동안 다른 시점에서 우선적으로 선택될 수 있다. 추가적으로, 비드 또는 다른 표면 상의 항-CD3 및/또는 항-CD28 항체의 비율을 증가시키거나 감소시킴으로써, T 세포의 하위집단은 배양 개시에 있어서 또는 이에 대해 또는 다른 원하는 시점에서 우선적으로 선택될 수 있다. 숙련된 기술자는 본 발명의 맥락에서 다수 라운드의 선택이 또한 사용될 수 있음을 인식할 것이다. 일부 실시형태에서, 활성화 및 확장 과정에서 선택 절차를 수행하고 "선택되지 않은" 세포를 사용하는 것이 바람직할 수 있다. "선택되지 않은" 세포도 또한 추가 라운드의 선택을 거칠 수 있다.
음성 선택에 의한 T 세포 집단의 풍부화는 음성으로 선택된 세포에 고유한 표면 마커에 대한 항체의 조합으로 달성될 수 있다. 한 가지 방법은 음성으로 선택된 세포에 존재하는 세포 표면 마커에 대한 단클론성 항체의 칵테일을 사용하는 유세포 분석 또는 음성 자기 면역부착을 통한 세포 분류 및/또는 선택이다. 예를 들어, 음성 선택에 의해 CD4+ 세포를 풍부화시키기 위해, 단클론성 항체 칵테일은 전형적으로 CD 14, CD20, CD11b, CD 16, HLA-DR, 및 CD8에 대한 항체를 포함한다. 일부 실시형태에서, 전형적으로 CD4+, CD25+, CD62Lhi, GITR+ 및 FoxP3+를 발현하는 조절 T 세포에 대하여 풍부화시키거나 양성으로 선택하는 것이 바람직할 수 있다. 대안적으로, 일부 실시형태에서, T 조절 세포는 항-CD25 접합된 비드 또는 다른 유사한 선택 방법에 의해 고갈된다.
양성 또는 음성 선택에 의해 원하는 세포 집단을 단리시키기 위해, 세포 및 표면(예를 들어 비드와 같은 입자)의 농도가 변할 수 있다. 일부 실시형태에서, 세포와 비드의 최대 접촉을 보장하기 위해, 비드 및 세포가 함께 혼합되는 부피를 상당히 감소시키는 것(즉, 세포의 농도를 증가시키는 것)이 바람직할 수 있다. 예를 들어, 일부 실시형태에서, 약 20억개 세포/㎖의 농도가 사용된다. 일부 실시형태에서, 약 10억개 세포/㎖의 농도가 사용된다. 일부 실시형태에서, 약 1억개 세포/㎖ 초과가 사용된다. 일부 실시형태에서, 약 1000만, 1500만, 2000만, 2500만, 3000만, 3500만, 4000만, 4500만, 또는 5000만개 세포/㎖ 중 어느 하나의 세포 농도가 사용된다. 일부 실시형태에서, 약 7500만, 8000만, 8500만, 9000만, 9500만, 또는 1억개 세포/㎖ 중 어느 하나의 세포 농도가 사용된다. 일부 실시형태에서, 약 1억 2500만 또는 약 1억 5000만개 세포/㎖의 농도가 사용된다. 고농도를 사용하면 세포 수율, 세포 활성화, 및 세포 확장의 증가를 초래할 수 있다. 또한, 높은 세포 농도의 사용은 관심 표적 항원, 예컨대, CD28-음성 T 세포, 또는 다수의 종양 세포가 존재하는 샘플(즉, 백혈병 혈액, 종양 조직 등) 유래의 표적 항원을 약하게 발현할 수 있는 세포의 보다 효율적인 포획이 가능하게 한다. 이와 같은 세포 집단은 치료 가치를 가질 수 있으며 수득하는 것이 바람직할 것이다. 예를 들어, 높은 세포 농도의 사용은 일반적으로 CD28 발현이 보다 약한 CD8+ T 세포의 보다 효율적인 선택을 가능하게 한다.
핵산(예컨대, 바람직한 CR, CCOR 및/또는 COR의 핵산)을 발현하기 위한 면역 세포의 유전적 변형 이전 또는 후와 상관없이, 면역 세포는 활성화되고 확장될 수 있다.
일부 실시형태에서, 본 명세서에 기재된 면역 세포(예컨대, T 세포)는 이에 부착된 표면과, CD3/TCR 복합체 연관 신호를 자극하는 작용제 및 T 세포의 표면에서 공동자극 분자를 자극하는 리간드의 접촉에 의해 확장된다. 구체적으로, T 세포집단은, 예컨대, 항-CD3 항체, 또는 이의 항원-결합 단편, 또는 표면에 고정된 항-CD2 항체와의 접촉에 의해, 또는 칼슘 이오노포어와 함께 단백질 키나제 C 활성화제(예를 들어, 브리오스타틴)와의 접촉에 의해 자극될 수 있다. T 세포의 표면에서 보조 분자의 공동자극을 위해, 보조 분자에 결합하는 리간드가 사용된다. 예를 들어, T 세포 집단은 T 세포의 증식을 자극하기에 적절한 조건 하에서 항-CD3 항체 및 항-CD28 항체와 접촉될 수 있다. CD4+ T 세포 또는 CD8+ T 세포의 증식을 자극하기 위해, 항-CD3 항체 및 항-CD28. 항-CD28 항체의 예는 9.3, B-T3, XR-CD28(Diaclone, 프랑스 브장송(Besancon) 소재)을 포함하며, 이는 당업계에 일반적으로 알려진 다른 방법으로 사용될 수 있다(Berg et al., Transplant Proc. 30(8):3975-3977, 1998; Haanen et al., J. Exp. Med. 190(9):13191328, 1999; Garland et al., J. Immunol. Meth. 227(1-2):53-63, 1999).
유전적 변형
일부 실시형태에서, 조작된 면역 세포는 CCR5의 발현을 차단하거나 감소시키도록 변형된 면역 세포(예컨대, T 세포)이다. 유전자 발현을 파괴하기 위한 세포의 변형은, 예를 들어 RNA 간섭(예를 들어, siRNA, shRNA, miRNA), 유전자 편집(예를 들어, CRISPR- 또는 TALEN-기반 유전자 넉아웃) 등을 포함하여, 당업계에 알려진 임의의 이와 같은 기법을 포함한다.
일부 실시형태에서, CCR5의 발현이 감소된 조작된 면역 세포(예컨대, T 세포)는 CRISPR/Cas 시스템을 사용하여 생성된다. 유전자 편집의 CRISPR/Cas 시스템에 대한 검토는, 예를 들어 문헌[Jian W & Marraffini LA, Annu. Rev. Microbiol. 69, 2015]; [Hsu PD et al., Cell, 157(6):1262-1278, 2014]; 및 [O'Connell MR et al., Nature 516: 263-266, 2014]을 참조한다. 일부 실시형태에서, T 세포의 내인성 TCR 사슬 중 하나 또는 둘 다의 발현이 감소된 조작된 면역 세포(예컨대, 조작된 T 세포)는 TALEN-기반 게놈 편집을 사용하여 생성된다.
일부 실시형태에서, CCR5 유전자(또는 TCR 유전자)는 CRISPR/Cas9 유전자 편집을 사용하여 비활성화된다. CRISPR/Cas9는 2가지 주요 특성, 즉 짧은 가이드 RNA(gRN) 및 CRISPR-연관 엔도뉴클레아제 또는 Cas 단백질을 포함한다. Cas 단백질은 gRNA에 결합할 수 있으며, 상기 gRNA는 관심 유전자에 대한 표적화 유도, 및 상기 유전자의 후속 넉아웃을 가능하게 하는 조작된 스페이서를 함유한다. 일단 표적화되면, Cas 단백질은 DNA 표적 서열을 절단하여, 유전자의 넉아웃을 초래한다.
일부 실시형태에서, CCR5 유전자(또는 TCR 유전자)는 전사 활성화제-유사 이펙터 뉴클레아제(TALEN®)-기반 게놈 편집을 사용하여 비활성화된다. TALEN®-기반 게놈 편짐은 DNA의 특정 영역을 표적화하기 위해 조작될 수 있는 제한 효소의 사용을 포함한다. 전사 활성화제-유사 이펙터(TALE) DNA-결합 도메인은 DNA 절단 도메인에 융합된다. TALE는 관심 서열에 대하여 뉴클레아제를 표적화하는 역할을 하고, 절단 도메인(뉴클레아제)은 DNA를 절단하는 역할을 하여, 해당 DNA 절편의 제거 및 후속적인 유전자 넉아웃을 초래한다.
일부 실시형태에서, CCR5 유전자(또는 TCR 유전자)는 아연 핑거 뉴클레아제(ZFN) 게놈 편집 방법을 사용하여 비활성화된다. 아연 핑거 뉴클레아제는 아연 핑거 DNA-결합 도메인 및 DNA-절단 도메인으로 구성된 인공적 제한 효소이다. ZFN DNA-결합 도메인은 DNA의 특정 영역을 표적화하기 위해 조작될 수 있다. DNA-절단 도메인은 관심 DNA 서열을 절단하는 역할을 하여, 해당 DNA 절편의 제거 및 후속적인 유전자 넉아웃을 초래한다.
일부 실시형태에서, CCR5 유전자(또는 TCR 유전자)의 발현은 작은 간섭 RNA(siRNA)를 사용함으로써 감소된다. siRNA 분자는 관심 유전자 유래의 메신저 RNA(mRNA) 전사체에 상보적인 20 내지 25개 뉴클레오타이드 길이의 올리고뉴클레오타이드 듀플렉스이다. siRNA는 파괴를 위해 이러한 mRNA를 표적화한다. 표적화를 통해, siRNA는 mRNA 전사체가 번역이 되는 것을 방지하고, 이에 의해 세포에 의해 단백질이 생성되는 것을 방지한다.
일부 실시형태에서, CCR5 유전자(또는 TCR 유전자)의 발현은 안티센스 올리고뉴클레오타이드를 사용함으로써 감소된다. mRNA를 표적화하는 안티센스 올리고뉴클레오타이드는 일반적으로 당업계에 알려져 있으며, 유전자 발현을 하향조절하기 위해 일상적으로 사용된다. 문헌[Watts, J. and Corey, D (2012) J. Pathol. 226(2):365-379]을 참조한다.
조작된 면역 세포의 풍부화
일부 실시형태에서, 본 명세서에 기재된 임의의 조작된 면역 세포에 따른 조작된 면역 세포에 대하여 이종성 세포 집단을 풍부화시키는 방법이 제공된다.
표적 항원에 특이적으로 결합하고 리간드를 표적화하는 조작된 면역 세포(예컨대, 조작된 T 세포)의 특정 하위집단이 양성 선택 기법에 의해 풍부화될 수 있다. 예를 들어, 일부 실시형태에서, 조작된 면역 세포(예컨대, 조작된 T 세포)는 원하는 조작된 면역 세포의 양성 선택에 충분한 기간 동안 표적 항원-접합체 비드 및/또는 표적 리간드-접합체 비드와 함께 인큐베이션함으로써 풍부화된다. 일부 실시형태에서, 기간은 약 30분이다. 일부 실시형태에서, 기간은 30분 내지 36시간 이상(이들 값 사이의 모든 범위를 포함함)의 범위이다. 일부 실시형태에서, 기간은 적어도 1, 2, 3, 4, 5, 또는 6시간이다. 일부 실시형태에서, 기간은 10 내지 24시간이다. 일부 실시형태에서, 인큐베이션 기간은 24시간이다. 이종성 세포 집단에서 낮은 수준으로 존재하는 조작된 면역 세포의 단리를 위해, 더 긴 인큐베이션 시간, 예컨대, 24시간을 사용하면 세포 수율을 증가시킬 수 있다. 더 긴 인큐베이션 시간은 다른 세포 유형과 비교하여 적은 수의 조작된 면역 세포가 있는 임의의 상황에서 조작된 면역 세포를 단리시키는 데 사용될 수 있다. 숙련된 기술자는 본 발명의 맥락에서 다수 라운드의 선택이 또한 사용될 수 있음을 인식할 것이다.
양성 선택에 의해 원하는 조작된 면역 세포 집단을 단리시키기 위해, 세포 및 표면(예를 들어, 비드와 같은 입자)의 농도가 변할 수 있다. 일부 실시형태에서, 세포와 비드의 최대 접촉을 보장하기 위해, 비드 및 세포가 함께 혼합되는 부피를 상당히 감소시키는 것(즉, 세포의 농도를 증가시키는 것)이 바람직할 수 있다. 예를 들어, 일부 실시형태에서, 약 20억개 세포/㎖의 농도가 사용된다. 일부 실시형태에서, 약 10억개 세포/㎖의 농도가 사용된다. 일부 실시형태에서, 약 1억개 세포/㎖ 초과가 사용된다. 일부 실시형태에서, 약 1000만, 1500만, 2000만, 2500만, 3000만, 3500만, 4000만, 4500만, 또는 5000만개 세포/㎖ 중 어느 하나의 세포 농도가 사용된다. 일부 실시형태에서, 약 7500만, 8000만, 8500만, 9000만, 9500만, 또는 1억개 세포/㎖ 중 어느 하나의 세포 농도가 사용된다. 일부 실시형태에서, 약 1억 2500만 또는 약 1억 5000만개 세포/㎖의 농도가 사용된다. 고농도를 사용하면 세포 수율, 세포 활성화, 및 세포 확장의 증가를 초래할 수 있다. 또한, 높은 세포 농도의 사용은 CR, CCOR 및/또는 COR을 약하게 발현할 수 있는 조작된 면역 세포의 보다 효율적인 포획이 가능하게 한다.
본 명세서에 기재된 임의의 이와 같은 실시형태 중 일부에서, 풍부화는 조작된 면역 세포의 고갈을 최소화하거나 실질적으로 일어나지 않게 한다. 예를 들어, 일부 실시형태에서, 풍부화는 조작된 면역 세포의 약 50% 미만(예컨대, 약 45, 40, 35, 30, 25, 20, 15, 10, 또는 5% 중 어느 하나 미만)이 고갈되는 것을 초래한다. 면역 세포 고갈은 본 명세서에 기재된 임의의 수단을 포함하여, 당업계에 알려진 임의의 수단에 의해 결정될 수 있다.
본 명세서에 기재된 임의의 이와 같은 실시형태 중 일부에서, 풍부화는 조작된 면역 세포의 말단 분화를 최소화하거나 실질적으로 일어나지 않게 한다. 예를 들어, 일부 실시형태에서, 풍부화는 조작된 면역 세포의 약 50% 미만(예컨대, 약 45, 40, 35, 30, 25, 20, 15, 10, 또는 5% 중 어느 하나 미만)이 말단 분화되는 것을 초래한다. 면역 세포 분화는 본 명세서에 기재된 임의의 수단을 포함하여, 당업계에 알려진 임의의 수단에 의해 결정될 수 있다.
본 명세서에 기재된 임의의 이와 같은 실시형태 중 일부에서, 풍부화는 조작된 면역 세포에서 CR, CCOR 및/또는 COR의 내재화를 최소화하거나 실질적으로 일어나지 않게 한다. 예를 들어, 일부 실시형태에서, 풍부화는 조작된 면역 세포에서 CR, CCOR 및/또는 COR의 약 50% 미만(예컨대, 약 45, 40, 35, 30, 25, 20, 15, 10, 또는 5% 중 어느 하나 미만)이 내재화되는 것을 초래한다. 조작된 면역 세포에서 CR, CCOR 및/또는 COR의 내재화는 본 명세서에 기재된 임의의 수단을 포함하여, 당업계에 알려진 임의의 수단에 의해 결정될 수 있다.
본 명세서에 기재된 임의의 이와 같은 실시형태 중 일부에서, 풍부화는 조작된 면역 세포의 증식 증가를 초래한다. 예를 들어, 일부 실시형태에서, 풍부화는 풍부화 후 조작된 면역 세포 수에서 적어도 약 10%(예컨대, 적어도 약 20, 30, 40, 50, 60, 70, 80, 90, 100, 200, 300, 400, 500, 1000% 또는 그 이상 중 어느 하나)의 증가를 초래한다.
따라서, 일부 실시형태에서, a) 이종성 세포 집단을 표적 항원 또는 이에 함유된 하나 이상의 에피토프를 포함하는 제1 분자 및/또는 표적 리간드 또는 이에 함유된 하나 이상의 에피토프를 포함하는 제2 분자와 접촉시켜 제1 분자에 결합된 조작된 면역 세포를 포함하는 복합체 및/또는 제2 분자에 결합된 조작된 면역 세포를 포함하는 복합체를 형성하는 단계; 및 b) 이종성 세포 집단으로부터 복합체를 분리하여, 조작된 면역 세포에 대하여 풍부화된 세포 집단을 생성하는 단계를 포함하는, CR 표적 항원에 특이적으로 결합하는 CR 및/또는 CCOR 표적 리간드에 특이적으로 결합하는 CCOR을 발현하는 조작된 면역 세포에 대하여 이종성 세포 집단을 풍부화시키기는 방법이 제공된다. 일부 실시형태에서, 제1 및/또는 제2 분자는 고체 지지체에 개별적으로 고정화된다. 일부 실시형태에서, 고체 지지체는 미립자(예컨대, 비드)이다. 일부 실시형태에서, 고체 지지체는 표면(예컨대, 웰의 바닥)이다. 일부 실시형태에서, 제1 및/또는 제2 분자는 태그로 개별적으로 표지화된다. 일부 실시형태에서, 태그는 형광 분자, 친화성 태그, 또는 자기 태그이다. 일부 실시형태에서, 방법은 제1 및/또는 제2 분자로부터 조작된 면역 세포를 용리시키는 단계 및 용리액을 회수하는 단계를 더 포함한다.
일부 실시형태에서, 면역 세포 또는 조작된 면역 세포는, 예를 들어 음성 풍부화의 사용을 통해 CD4+ 및/또는 CD8+ 세포에 대하여 풍부화되며, 이에 의해 세포 혼합물은 물리적(컬럼) 및 자기(MACS 자기 비드) 정제 단계를 둘 다 포함하는 2 단계 정제 방법을 사용하여 정제된다(Gunzer, M. et al. (2001) J. Immunol. Methods 258(1-2):55-63). 다른 실시형태에서, 세포 집단은 CD4+ 또는 CD8+ 세포의 풍부화를 위해 특별히 설계된 T 세포 풍부화 컬럼의 사용을 통해 CD4+ 및/또는 CD8+ 세포에 대하여 풍부화될 수 있다. 또 다른 실시형태에서, 세포 집단은 상업적으로 입수가능한 키트의 사용을 통해 CD4+ 세포에 대하여 풍부화될 수 있다. 일부 실시형태에서, 상업적으로 입수가능한 키트는 이지셉(EasySep)(상표) 인간 CD4+ T 세포 풍부화 키트(스템셀 테크놀로지스(Stemcell Technologies)(상표))이다. 다른 실시형태에서, 상업적으로 입수가능한 키트는 마그니소트 마우스(MagniSort Mouse) CD4+ T 세포 풍부화 키트(써모 피셔 사이언티픽(Thermo Fisher Scientific))이다. 또 다른 실시형태에서, 상업적으로 입수가능한 풍부화 키트는 당업자에게 알려진 것이다.
약제학적 조성물
본 명세서에 기재된 조작된 면역 세포(예컨대, T 세포)를 포함하는 조작된 면역 세포 조성물(예컨대, 약제학적 조성물, 또한 본 명세서에서 제형으로 지칭됨)이 제공된다.
조성물은 동일한 세포 유형의 조작된 면역 세포를 포함하고 동일한 CR 및/또는 CCOR을 발현하는 동종성 세포 집단, 또는 상이한 세포 유형의 조작된 면역 세포를 포함하고, 상이한 CR, 상이한 CCOR 및/또는 상이한 COR을 발현하는 복수의 조작된 면역 세포 집단을 포함하는 이종성 세포 집단을 포함할 수 있다. 조성물은 조작된 면역 세포가 아닌 세포를 더 포함할 수 있다.
따라서, 일부 실시형태에서, 동일한 세포 유형의 조작된 면역 세포(예컨대, 조작된 T 세포)의 동종성 세포 집단을 포함하고 동일한 CR, CCOR 및/또는 COR을 발현하는 조작된 면역 세포 조성물이 제공된다. 일부 실시형태에서, 조작된 면역 세포는 T 세포이다. 일부 실시형태에서, 조작된 면역 세포는 세포독성 T 세포, 헬퍼 T 세포, 자연 살해 T 세포, 및 억제 T 세포로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 조작된 면역 세포 조성물은 약제학적 조성물이다.
일부 실시형태에서, 상이한 세포 유형의 조작된 면역 세포를 포함하고, 상이한 CR, 상이한 CCOR, 및/또는 상이한 COR을 발현하는 복수의 조작된 면역 세포 집단을 포함하는 이종성 세포 집단을 포함하는 조작된 면역 세포 조성물이 제공된다.
일부 실시형태에서, 약제학적 조성물은 개체, 예컨대, 인간 개체에게 투여하기에 적합하다. 일부 실시형태에서, 약제학적 조성물은 주사에 적합하다. 일부 실시형태에서, 약제학적 조성물은 주입에 적합하다. 일부 실시형태에서, 약제학적 조성물에는 세포 배양 배지가 실질적으로 없다. 일부 실시형태에서, 약제학적 조성물에는 내독소 또는 알레르기성 단백질이 실질적으로 없다. 일부 실시형태에서, "실질적으로 없는"은 약제학적 조성물의 총 부피 또는 중량의 약 10%, 5%, 1%, 0.1%, 0.01%, 0.001%, 1 ppm 또는 그 이하 중 어느 하나 미만이다. 일부 실시형태에서, 약제학적 조성물에는 마이코플라스마, 종균제 및/또는 전염성 질환 작용제가 없다.
본 출원인의 약제학적 조성물은 다수의 조작된 면역 세포를 포함할 수 있다. 일부 실시형태에서, 약제학적 조성물은 조작된 면역 세포의 단일 복제물을 포함한다. 일부 실시형태에서, 약제학적 조성물은 조작된 면역 세포의 적어도 약 1, 10, 100, 1000, 104, 105, 106, 107, 108개 또는 그 이상 중 어느 하나의 복제물을 포함한다. 일부 실시형태에서, 약제학적 조성물은 단일 유형의 조작된 면역 세포를 포함한다. 일부 실시형태에서, 약제학적 조성물은 적어도 2개 유형의 조작된 면역 세포를 포함하며, 여기서 상이한 유형의 조작된 면역 세포는 세포 공급원, 세포 유형, 발현된 치료 단백질, 면역조절제, 및/또는 프로모터 등이 상이하다.
조성물의 제조 동안 다양한 시점에서, 세포를 동결보존하는 것이 필요하거나 유익할 수 있다. 용어 "냉동(frozen/freezing)" 및 "동결보존(cryopreserved/cryopreserving)"은 상호교환적으로 사용될 수 있다. 냉동은 냉동건조를 포함한다.
특정 실시형태에서, 세포는 배양 배지로부터 수확되고, 세척된 다음 치료적 유효량으로 담체 내로 농축될 수 있다. 예시적인 담체는 식염수, 완충 식염수, 생리 식염수, 물, 행크스 용액, 링거 용액, Nonnosol-R(Abbott Labs사), Plasma-Lyte A(R)(Baxter Laboratories, Inc., 미국 일리노이주 모턴 그로브 소재), 글리세롤, 에탄올, 및 이들의 조합을 포함한다.
특정 실시형태에서, 담체는 인간 혈청 알부민(HSA) 또는 다른 인간 혈청 구성요소 또는 소태아 혈청으로 보충될 수 있다. 특정 실시형태에서, 주입용 담체는 5% HSA 또는 덱스트로스가 있는 완청 식염수를 포함한다. 추가적인 등장화제는 3가 이상의 당 알코올을 포함하는 다가 당 알코올, 예컨대, 글리세린, 에리트리톨, 아라비톨, 자일리톨, 솔비톨, 또는 만니톨을 포함한다.
담체는 완충제, 예컨대, 시트레이트 완충액, 석시네이트 완충액, 타트레이트 완충액, 푸마레이트 완충액, 글루코네이트 완충액, 옥살레이트 완충액, 락테이트 완충액, 아세테이트 완충액, 포스페이트 완충액, 히스티딘 완충액, 및/또는 트라이메틸아민 염을 포함할 수 있다.
안정화제는 증량제에서 용기 벽에 대한 세포 부착을 방지하는 데 도움이 되는 첨가제에 이르기까지 기능 범위가 다양할 수 있는 광범위한 카테고리의 부형제를 지칭한다. 전형적인 안정화제는 다가 당 알코올; 아미노산, 예컨대, 아르기닌, 리신, 글리신, 글루타민, 아스파라긴, 히스티딘, 알라닌, 오르니틴, L-류신, 2-페닐알라닌, 글루탐산, 및 트레오닌; 유기 당 또는 당 알코올, 예컨대, 락토스, 트레할로스, 스타키오스, 만니톨, 솔비톨, 자일리톨, 리비톨, 미오이니시톨, 갈락티톨, 글리세롤, 및 사이클리톨, 예컨대, 이노시톨; PEG; 아미노산 중합체; 황-함유 환원제, 예컨대, 유레아, 글루타티온, 싸이옥트산, 소듐 티오글라이콜레이트, 티오글리세롤, 알파-모노티오글리세롤, 및 소듐 티오설페이트; 저분자량 폴리펩타이드(즉, 10개 미만의 잔기); 단백질, 예컨대, HSA, 소혈청 알부민, 젤라틴 또는 면역글로불린; 친수성 중합체, 예컨대, 폴리비닐피롤리돈; 단당류, 예컨대, 자일로스, 만노스, 프럭토스 및 글루코스; 이당류, 예컨대, 락토스, 말토스 및 수크로스; 삼당류, 예컨대, 라피노스, 및 다당류, 예컨대, 덱스트란을 포함할 수 있다.
필요하거나 유익한 경우, 조성물은 국소 마취제, 예컨대, 리도카인을 포함하여 주사 부위의 통증을 완화시킬 수 있다.
예시적인 방부제는 페놀, 벤질 알코올, 메타-크레졸, 메틸 파라벤, 프로필 파라벤, 옥타데실다이메틸벤질 암모늄 클로라이드, 벤즈알코늄 할라이드, 헥사메토늄 클로라이드, 알킬 파라벤, 예컨대, 메틸 또는 프로필 파라벤, 카테콜, 레조르시놀, 사이클로헥산올, 및 3-펜탄올을 포함한다.
조성물 내 치료적 유효량의 세포는 102개 초과의 세포, 103개 초과의 세포, 104개 초과의 세포, 105개 초과의 세포, 106개 초과의 세포, 107개 초과의 세포, 108개 초과의 세포, 109개 초과의 세포, 1010개 초과의 세포, 또는 1011개 초과의 세포일 수 있다.
본 명세서에 개시된 조성물 및 제형에서, 세포는 부피가 일반적으로 1ℓ 이하, 500㎖ 이하, 250㎖ 이하 또는 100㎖ 이하이다. 따라서, 투여된 세포의 밀도는 전형적으로 104개 세포/㎖, 107개 세포/㎖ 또는 108개 세포/㎖ 초과이다.
또한 본 명세서에 기재된 CR, CCOR 및/또는 COR을 인코딩하는 핵산 중 임의의 것을 포함하는 핵산 조성물(예컨대, 약제학적 조성물, 또한 본 명세서에서 제형으로 지칭됨)이 본 명세서에서 제공된다. 일부 실시형태에서, 핵산 조성물은 약제학적 조성물이다. 일부 실시형태에서, 핵산 조성물은 등장화제, 부형제, 희석제, 점증제, 안정화제, 완충액, 및/또는 방부제; 및/또는 수성 비히클, 예컨대, 정제수, 수성 당 용액, 완충 용액, 생리 식염수, 수성 중합체 용액, 또는 무-RNase 물 중 임의의 것을 더 포함한다. 첨가되는 이와 같은 첨가제 및 수성 비히클의 양은 핵산 조성물의 사용 형태에 따라 적합하게 선택될 수 있다.
본 명세서에 개시된 조성물 및 제형은, 예를 들어 주사, 주입, 관류, 또는 세척에 의한 투여를 위해 제조될 수 있다. 조성물 및 제형은 골수, 정맥내, 피내, 동맥내, 결절내, 림프내, 복강내, 병변내, 전립선내, 질내, 직장내, 국부, 척추강내, 종양내, 근육내, 방광내, 및/또는 피하 주사용으로 추가로 제형화될 수 있다.
생체 내 투여에 사용되는 제형은 멸균되어야 한다. 이는, 예를 들어 멸균 여과 막을 통한 여과에 의해 용이하게 달성된다.
부형제
본 발명의 약제학적 조성물은 치료 목적에 유용하다. 따라서, 조작된 면역 세포, 예컨대, 면역조절제 또는 다른 치료 단백질을 발현하는 생산 세포를 포함하는 다른 조성물과 달리, 본 발명의 약제학적 조성물은 개체에게 투여하기에 적합한 약제학적으로 허용 가능한 부형제를 포함한다.
적합한 약제학적으로 허용 가능한 부형제는 완충액, 예컨대, 중성 완충 식염수, 인산염 완충 식염수 등; 탄수화물, 예컨대, 글루코스, 만노스, 수크로스 또는 덱스트란, 만니톨; 단백질; 폴리펩타이드 또는 아미노산, 예컨대, 글리신; 산화방지제; 킬레이팅제, 예컨대, EDTA 또는 글루타티온; 아쥬반트(예를 들어, 수산화알루미늄); 및 방부제를 포함할 수 있다. 일부 실시형태에서, 약제학적으로 허용 가능한 부형제는 자가 혈청을 포함한다. 일부 실시형태에서, 약제학적으로 허용 가능한 부형제는 인간 혈청을 포함한다. 일부 실시형태에서, 약제학적으로 허용 가능한 부형제는 비-독성, 생체적합성, 비-면역원성, 생분해성이고, 숙주의 방어 메커니즘에 의한 인식을 피할 수 있다. 부형제는 또한 아쥬반트, 예컨대, 보존 안정화제, 습윤제, 유화제 등을 함유할 수 있다. 일부 실시형태에서, 약제학적으로 허용 가능한 부형제는 조작된 면역 세포 또는 이의 분비된 면역조절제 또는 다른 치료 단백질의 안정성을 향상시킨다. 일부 실시형태에서, 약제학적으로 허용 가능한 부형제는 조작된 면역 세포에 의해 분비된 면역조절제 또는 다른 치료 단백질의 응집을 감소시킨다. 최종 형태는 멸균될 수 있으며, 또한 주사 장치, 예컨대, 중공 바늘을 통해 용이하게 통과할 수 있다. 적절한 점도는 적절한 부형제의 선택에 의해 달성되고 유지될 수 있다.
일부 실시형태에서, 약제학적 조성물은, 예를 들어 약 5.0 내지 약 8.0, 약 6.5 내지 약 7.5, 또는 약 6.5 내지 약 7.0의 pH 범위를 포함하여, 약 4.5 내지 약 9.0의 범위로 pH를 가지도록 제형화된다. 일부 실시형태에서, 약제학적 조성물은 또한 적합한 긴장성 변형제, 예컨대, 글리세롤의 첨가에 의해 혈액과 등장성이 되도록 만들어질 수 있다.
일부 실시형태에서, 약제학적 조성물은 인간에게 투여하기에 적합하다. 일부 실시형태에서, 약제학적 조성물은 비경구 투여에 의해 인간에게 투여하기에 적합하다. 비경구 투여에 적합한 제형은 산화방지제, 완충액, 정균제, 및 제형을 의도한 수용자의 혈액과 혼화성으로 만드는 용질을 함유할 수 있는 수성 및 비-수성 등장성 멸균 주사 용액, 및 현탁화제, 가용화제, 점증제, 안정화제, 및 방부제를 포함할 수 있는 수성 및 비-수성 멸균 현탁액을 포함한다. 제형은 단일-용량 또는 다회-용량 밀폐 용기, 예컨대, 앰플 및 바이알로 제공될 수 있으며, 치료 방법, 투여 방법, 및 사용 직전에 주사를 위한 본 명세서에 기재된 투약 요법에서 멸균 액체 부형제(즉, 물)의 추가만을 필요로 하는 상태로 저장될 수 있다. 일부 실시형태에서, 약제학적 조성물은 일회용 바이알, 예컨대, 일회용 밀폐 바이알에 함유된다. 일부 실시형태에서, 약제학적 조성물은 다회용 바이알에 함유된다. 일부 실시형태에서, 약제학적 조성물은 용기에 대량으로 함유된다. 일부 실시형태에서, 약제학적 조성물은 동결보존된다.
일부 실시형태에서, 약제학적 조성물은 정맥내 투여용으로 제형화된다. 일부 실시형태에서, 약제학적 조성물은 피하 투여용으로 제형화된다. 일부 실시형태에서, 약제학적 조성물은 종양 부위로의 국소 투여용으로 제형화된다. 일부 실시형태에서, 약제학적 조성물은 종양내 주사용으로 제형화된다.
일부 실시형태에서, 약제학적 조성물은 개체에게 투여하기 위한 특정 표준을 만족해야 한다. 예를 들어, 미국 식품의약국은 21 CFR 610 및 21 CFR 610.13을 포함하여, 세포-기반 면역치료 제품에 대한 표준을 설정하는 규제 지침을 공표하였다. 약제학적 조성물의 외관, 동일성, 순도, 안전성, 및/또는 효능을 평가하는 방법은 당업계에 알려져 있다. 일부 실시형태에서, 약제학적 조성물에는 알레르기 효과를 나타낼 수 있는 관련없는 단백질, 예컨대, 조작된 포유동물 면역 세포이외에 세포 배양에서 사용되는 동물 공급원의 단백질이 실질적으로 없다. 일부 실시형태에서, "실질적으로 없는"은 약제학적 조성물의 총 부피 또는 중량의 약 10%, 5%, 1%, 0.1%, 0.01%, 0.001%, 1 ppm 또는 그 이하 중 어느 하나 미만이다. 일부 실시형태에서, 약제학적 조성물은 GMP-수준 작업장에서 제조된다. 일부 실시형태에서, 약제학적 조성물은 비경구 투여를 위해 약 5 EU/㎏ 체중/hr 미만의 내독소를 포함한다. 일부 실시형태에서, 약제학적 조성물 중 조작된 면역 세포의 적어도 약 70%가 정맥내 투여를 위해 살아 있다. 일부 실시형태에서, 약제학적 조성물은 미국 약전(USP)에 기재된 바와 같은 14일 직접 접종 테스트 방법을 사용하여 평가될 때 "성장 없음" 결과를 가진다. 일부 실시형태에서, 약제학적 조성물의 투여 전에, 조작된 면역 세포 및 약제학적으로 허용 가능한 부형제를 둘 다 포함하는 샘플은 대략적으로 최종 수확 약 48 내지 72시간 전에 (또는 배양물의 마지막 재공급과 동시에) 멸균 테스트를 위해 취해져야 한다. 일부 실시형태에서, 약제학적 조성물에는 마이코플라스마 오염이 없다. 일부 실시형태에서, 약제학적 조성물에는 검출가능한 종균제가 없다. 일부 실시형태에서, 약제학적 조성물에는 전염성 질환 작용제, 예컨대, HIV 유형 I, HIV 유형 II, HBV, HCV, 인간 T-림프친화 바이러스, 유형 I; 및 인간 T-림프친화 바이러스, 유형 II가 없다.
조작된 면역 세포를 사용하는 치료 방법
본 출원은, 전염병, EBV 양성 T 세포 림프증식성 장애, T-세포 전림프구성 백혈병, EBV-양성 T 세포 림프증식성 장애, 성인 T-세포 백혈병/림프종, 균상식육종/세자리 증후군, 원발성 피부 CD30-양성 T-세포 림프증식성 장애, 말초 T-세포 림프종(달리 명시되지 않음), 혈관면역모구 T-세포 림프종, 및 역형성 큰세포 림프종, 및 자가면역 질환을 포함하지만 이들로 제한되는 것은 아닌 질환을 치료하기 위해 조작된 면역 세포를 투여하는 방법을 추가로 제공한다.
일부 실시형태에서, 자가 림프구 주입이 치료에 사용된다. 자가 PBMC는 치료를 필요로 하는 환자로부터 수집되고 T 세포는 본 명세서에 기재되고 당업계에 알려진 방법을 사용하여 활성화 및 확장된 다음 환자에게 다시 주입된다.
세포는 강력한 생체 내 확장을 겪을 수 있고, 혈액 및 골수에서 장기간 동안 높은 수준으로 지속되는 CD4-특이적 기억 세포를 확립할 수 있다. 일부 실시형태에서, 환자에게 주입된 조작된 면역 세포는 암 또는 바이러스-감염 세포를 고갈시킬 수 있다. 일부 실시형태에서, 환자에게 주입된 조작된 면역 세포는 암 또는 바이러스-감염 세포를 제거할 수 있다. 바이러스 감염 치료는, 예를 들어 바이러스 부하, 생존 기간, 삶의 질, 단백질 발현 및/또는 활성에 의해 평가될 수 있다.
일부 실시형태에서 본 발명의 조작된 면역 세포는 개체(예를 들어, 포유동물, 예컨대, 인간)에게 투여되어 암, 예를 들어 CD4+ T 세포 림프종 또는 T-세포 백혈병을 치료할 수 있다. 따라서 일부 실시형태에서 본 출원은 본 명세서에 기재된 실시형태 중 임의의 하나에 따른 조작된 면역 세포를 포함하는 유효량의 조성물(예컨대, 약제학적 조성물)을 개체에게 투여하는 단계를 포함하는 개체에서 암을 치료하는 방법을 제공한다. 일부 실시형태에서, 암은 T 세포 림프종이다.
일부 실시형태에서, 본 명세서에 기재된 암을 치료하는 방법은 제2 항암제를 개체에게 투여하는 단계를 더 포함한다. 적합한 항암제는 CD70 표적화 약물, TRBC1, CD30 표적화 약물, CD37 표적화 약물, CCR4 표적화 약물, CHOP(사이클로포스파미드, 독소루비신, 빈크리스틴 및 프레드니손), CHOEP(사이클로포스파미드, 독소루비신, 빈크리스틴, 에토포사이드 및 프레드니손), EPOCH(에토포사이드, 빈크리스틴, 독소루비신, 사이클로포스파미드 및 프레드니손), 하이퍼(Hyper)-CVAD(사이클로포스파미드, 빈크리스틴, 독소루비신, 및 덱사메타손), HDAC 저해제, CD52 항체 벨리노스타트(Belinostat), 벤다무스틴(Bendamustine), BL-8040, 보르테조밉(Bortezomib), CPI-613, 모가물리주맙(Mogamulizumab), 넬라라빈(Nelarabine), 니볼루맙(Nivolumab), 로미뎁신(Romidepsin) 및 룩소리티닙(Ruxolitinib)을 포함하지만 이들로 제한되는 것은 아니다. 일부 실시형태에서, 제2 작용제는 면역관문 저해제(예를 들어, 항-CTLA4 항체, 항-PD1 항체, 또는 항-PD-L1 항체)이다. 일부 실시형태에서, 제2 항암제는 조작된 면역 세포와 동시에 투여된다. 일부 실시형태에서, 제2 항암제는 조작된 면역 세포의 투여와 순차적으로(예를 들어, 조작된 면역 세포의 투여 이전 또는 이후에) 투여된다. 일부 실시형태에서, 본 발명의 조작된 면역 세포 조성물은 제2, 제3, 또는 제4 작용제(예를 들어, 항신생물제, 성장 저해제, 세포독성제, 또는 화학요법제를 포함함)와 조합하여 투여되어 표적 항원 발현을 수반하는 질환 또는 장애를 치료한다.
본 발명의 조작된 면역 세포는 또한 개체(예를 들어, 포유동물, 예컨대, 인간)에게 투여되어 전염병, 예를 들어 HIV를 치료할 수 있다. 따라서 일부 실시형태에서 본 출원은 본 명세서에 기재된 실시형태 중 임의의 하나에 따른 조작된 면역 세포를 포함하는 유효량의 조성물(예컨대, 약제학적 조성물)을 개체에게 투여하는 단계를 포함하는 개체에서 전염병을 치료하는 방법을 제공한다. 일부 실시형태에서, 바이러스 감염은, 예를 들어 인간 T 세포 백혈병 바이러스(HTLV) 및 HIV(인간 면역결핍 바이러스)로부터 선택되는 바이러스에 의해 야기된다.
일부 실시형태에서, HIV를 치료하는 방법이 제공되며, 이는 본 명세서에 기재된 임의의 조작된 면역 세포를 투여하는 단계를 포함한다. HIV에는 2가지 하위유형, 즉 HIV-1 및 HIV-2가 있다. HIV-1은 세계적 유행병의 원인이며, 높은 독성과 높은 감염성을 둘 다 가진 바이러스이다. 그러나 HIV-2는 서아프리카에서만 만연하며, HIV-1만큼 독성이 있지도 않고 전염성도 없다. HIV-1 및 HIV-2 감염 사이의 독성 및 감염성의 차이는 HIV-2 감염에서 바이러스 단백질에 대하여 증가하는 더 강한 면역 반응이 발병한 개체에서 더 효율적인 제어를 유도하는 것으로 지지될 수 있다(Leligdowicz, A. et al. (2007) J. Clin. Invest. 117(10):3067-3074). 이는 또한 HIV-1의 세계적 확산과 HIV-2의 제한된 지리적 유병률에 대한 지배적인 이유일 수 있다.
HIV-2 감염이 HIV-1 감염보다 더 잘 제어되지만, HIV-2-발명 개체는 여전히 치료 이익을 얻는다. 일부 실시형태에서, 조작된 면역 세포는 HIV-1 감염을 치료하는 데 사용된다. 다른 실시형태에서, 조작된 면역 세포는 HIV-2 감염을 치료하는 데 사용된다. 일부 실시형태에서, 조작된 면역 세포는 HIV-1 및 HIV-2 감염을 치료하는 데 사용된다.
일부 실시형태에서, 본 명세서에 기재된 전염병을 치료하는 방법은 개체에게 제2 항-감염제를 투여하는 단계를 더 포함한다. 적합한 항-감염제는 항-레트로바이러스 약물, 광범위 중화 항체, 톨(toll)-유사 수용체 효현제, 잠복 재활성화제, CCR5 길항제, 면역 자극제(예를 들어, TLR 리간드), 백신, 뉴클레오사이드 역전사효소 저해제, 뉴클레오타이드 역전사효소 저해제, 비-뉴클레오사이드 역전사효소 저해제, HIV 프로테아제 저해제, 및 융합 저해제를 포함하지만 이들로 제한되는 것은 아니다. 일부 실시형태에서, 제2 항-감염제는 조작된 면역 세포와 동시에 투여된다. 일부 실시형태에서, 제2 항-감염제는 조작된 면역 세포의 투여와 순차적으로(예를 들어, 조작된 면역 세포의 투여 이전 또는 이후에) 투여된다.
일부 실시형태에서, 개체는 포유동물(예를 들어, 인간, 비-인간 영장류, 래트, 마우스, 소, 말, 돼지, 양, 염소, 개, 고양이 등)이다. 일부 실시형태에서, 개체는 인간이다. 일부 실시형태에서, 개체는 임상 환자, 임상 시험 지원자, 실험 동물 등이다. 일부 실시형태에서, 개체는 약 60세 미만(예를 들어, 약 50, 40, 30, 25, 20, 15, 또는 10세 중 어느 하나 미만을 포함함)이다. 일부 실시형태에서, 개체는 약 60세 초과(예를 들어, 70, 80, 90, 또는 100세 중 어느 하나 초과를 포함함)이다. 일부 실시형태에서, 개체는 본 명세서에 기재된 질환 또는 장애(예컨대, 암 또는 바이러스 감염) 중 하나 이상으로 진단되거나 환경적 또는 유전적으로 이에 대한 경향이 있다. 일부 실시형태에서, 개체는 본 명세서에 기재된 하나 이상의 질환 또는 장애와 연관된 하나 이상의 위험 인자를 가진다.
일부 실시형태에서, 약제학적 조성물은 체중 ㎏ 당 적어도 약 104, 105, 106, 107, 108, 또는 109개 세포 중 어느 하나의 투약량으로 투여된다. 일부 실시형태에서, 약제학적 조성물은 체중 ㎏ 당 약 104 내지 약 105, 약 105 내지 약 106, 약 106 내지 약 107, 약 107 내지 약 108, 약 108 내지 약 109, 약 104 내지 약 109, 약 104 내지 약 106, 약 106 내지 약 108, 또는 약 105 내지 약 107개 세포 중 어느 하나의 투약량으로 투여된다.
하나 초과 유형의 조작된 면역 세포가 투여되는 일부 실시형태에서, 상이한 유형의 조작된 면역 세포가, 예컨대, 단일 조성물로 동시에, 또는 임의의 적합한 순서로 순차적으로 개체에게 투여될 수 있다.
일부 실시형태에서, 약제학적 조성물은 1회 동안 투여된다. 일부 실시형태에서, 약제학적 조성물은 다수 회(예컨대, 2, 3, 4, 5, 6회 또는 그 이상 중 어느 하나) 동안 투여된다. 일부 실시형태에서, 약제학적 조성물은 1주에 1회, 2주에 1회, 3주에 1회, 4주에 1회, 1개월에 1회, 2개월에 1회, 3개월에 1회, 4개월에 1회, 5개월에 1회, 6개월에 1회, 7개월에 1회, 8개월에 1회, 9개월에 1회, 또는 1년에 1회 투여된다. 일부 실시형태에서, 투여 사이의 간격은 약 1주 내지 2주, 2주 내지 1개월, 2주 내지 2개월, 1개월 내지 2개월, 1개월 내지 3개월, 3개월 내지 6개월, 또는 6개월 내지 1년 중 어느 하나이다. 특정 환자에 대한 최적의 투약량 및 치료 요법은 질환의 징후에 대하여 환자를 모니터링하고 이에 따라 치료를 조정함으로써 의학 분야의 숙련자에 의해 용이하게 결정될 수 있다.
제조 물품 및 키트
본 발명의 일부 실시형태에서, 감염병, 예컨대, 바이러스 감염(예를 들어, HIV에 의한 감염)의 치료에 유용한 물질을 함유하는 제조 물품이 제공된다. 제조 물품은 용기 및 용기 상의 또는 용기와 연관된 라벨 또는 포장 삽입물을 포함할 수 있다. 적합한 용기는, 예를 들어 병, 바이알, 시린지 등을 포함한다. 용기는 다양한 물질, 예컨대, 유리 또는 플라스틱으로 형성될 수 있다. 일반적으로, 용기는 본 명세서에 기재된 질환 또는 장애를 치료하는 데 효과적인 조성물을 보유하고, 멸균된 접근 포트를 가질 수 있다(예를 들어, 용기는 정맥내 용액 백 또는 피하 주사 바늘에 의해 뚫을 수 있는 마개가 있는 바이알일 수 있음). 조성물 중 적어도 하나의 활성제는 면역 세포의 표면에 본 발명의 CR 및 CCOR을 제시하는 면역 세포이다. 라벨 또는 포장 삽입물은 조성물이 특정 병태를 치료하는 데 사용된다는 것을 나타낸다. 라벨 또는 포장 삽입물은 조작된 면역 세포 조성물을 환자에게 투여하기 위한 설명서를 더 포함할 것이다. 본 명세서에 기재된 조합 요법을 포함하는 제조 물품 및 키트가 또한 고려된다.
포장 삽입물은 이와 같은 치료 제품의 사용에 관한 적응증, 사용법, 투약량, 투여, 금기 및/또는 경고에 대한 정보를 함유하는 치료 제품의 상업적 패키지에 관례적으로 포함되는 설명서를 지칭한다. 다른 실시형태에서, 포장 삽입물은 조성물이 표적 항원-양성 바이러스 감염(예를 들어, HIV에 의한 감염)을 치료하는 데 사용된다는 것을 나타낸다.
추가적으로, 제조 물품은 약제학적으로 허용 가능한 완충액, 예컨대, 주사용 정균수(BWFI), 인산염-완충 식염수, 링거 용액 및 덱스트로스 용액을 포함하는 제2 용기를 더 포함할 수 있다. 이는 다른 완충액, 희석제, 필터, 바늘 및 시린지를 포함하여 상업적 및 사용자 관점에서 바람직한 다른 물질을 더 포함할 수 있다.
예를 들어, 본 명세서에 기재된 표적 항원-양성 질환 또는 장애의 치료를 위해, 선택적으로 제조 물품과 조합하여, 다양한 목적에 유용한 키트가 또한 제공된다. 본 발명의 키트는 조작된 면역 세포 조성물을 포함하는 하나 이상의 용기(또는 단위 투약 형태 및/또는 제조 물품)를 포함하고, 일부 실시형태에서 또 다른 작용제(예컨대, 본 명세서에 기재된 작용제) 및/또는 본 명세서에 기재된 방법 중 임의의 것과 함께 사용하기 위한 설명서를 더 포함한다. 키트는 치료에 적합한 개체의 선택에 대한 설명을 더 포함할 수 있다. 본 발명의 키트에 제공되는 설명서는 전형적으로 라벨 또는 포장 삽입물(예를 들어, 키트에 포함된 종이 시트)에 기록된 설명서이지만, 기계 판독가능 설명서(예를 들어, 자기 또는 광학 저장 디스크에 있는 설명서)도 또한 허용 가능하다.
예시적인 실시형태
실시형태 1. a) i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR); 및 b) i) 키메라 공동수용체(CCOR) 표적 항원을 특이적으로 인식하는 CCOR 항원 결합 도메인; ii) CCOR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 도메인을 포함하는 키메라 공동수용체(CCOR)를 포함하는 조작된 면역 세포이되, CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이거나, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4인, 조작된 면역 세포.
실시형태 2. i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)를 포함하는 조작된 면역 세포이되, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
실시형태 3. i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)를 포함하는 조작된 면역 세포이되, CR 표적 항원은 CCR5, CXCR4, 및 CD4로 이루어진 군으로부터 선택되고, CCR5, CXCR4, 또는 CD4는 광범위 중화 항체와 일렬인, 조작된 면역 세포.
실시형태 4. 실시형태 3에 있어서, 상기 광범위 중화 항체는 VRC01, PGT121, 3BNC117 또는 10-1074인, 조작된 면역 세포.
실시형태 5. 실시형태 1 내지 4 중 어느 하나에 있어서, 하나 이상의 공동수용체("COR")를 더 포함하는, 조작된 면역 세포.
실시형태 6. a) 키메라 수용체(CR)를 인코딩하는 제1 핵산으로, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 제1 핵산; 및 b) 키메라 공동수용체(CCOR)를 인코딩하는 제2 핵산으로, CCOR은 i) CCOR 표적 항원을 특이적으로 인식하는 CCOR 항원 결합 도메인; ii) CCOR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 신호전달 도메인을 포함하는 제2 핵산을 포함하는 조작된 면역 세포이되; CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4이거나, CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4인, 조작된 면역 세포.
실시형태 7. 키메라 수용체(CR)를 인코딩하는 핵산을 포함하는 조작된 면역 세포이되, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하고, CR 표적 항원은 CCR5, CXCR4 및 CD4로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
실시형태 8. 키메라 수용체(CR)를 인코딩하는 핵산을 포함하는 조작된 면역 세포이되, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하고, CR 표적 항원은 CCR5, CXCR4 및 CD4로 이루어진 군으로부터 선택되며, CCR5, CXCR4, 또는 CD4는 광범위 중화 항체와 일렬인, 조작된 면역 세포.
실시형태 9. 실시형태 8에 있어서, 상기 광범위 중화 항체는 VRC01, PGT121, 3BNC117, 10-1074인, 조작된 면역 세포.
실시형태 10. 실시형태 6 내지 9에 있어서, 하나 이상의 공동수용체("COR")를 인코딩하는 하나 이상의 핵산(들)을 더 포함하는, 조작된 면역 세포.
실시형태 11. 실시형태 1 내지 10 중 어느 하나에 있어서, 상기 CR은 키메라 항원 수용체("CAR")인, 조작된 면역 세포.
실시형태 12. 실시형태 11에 있어서, 상기 CR 막관통 도메인은 CD8α, CD4, CD28, 4-1BB, CD80, CD86, CD152 및 PD1로 이루어진 군으로부터 선택되는 분자로부터 유래되는, 조작된 면역 세포.
실시형태 13. 실시형태 12에 있어서, 상기 CR 막관통은 CD8α로부터 유래되는, 조작된 면역 세포.
실시형태 14. 실시형태 11에 있어서, 상기 세포내 CR 신호전달 도메인은 CD3ζ, FcRγ, FcRβ, CD3γ, CD3δ, CD3ε, CD5, CD22, CD79a, CD79b, 또는 CD66d로부터 유래되는, 조작된 면역 세포.
실시형태 15. 실시형태 14에 있어서, 상기 세포내 CR 신호전달 도메인은 CD3ζ로부터 유래되는 항-CD4 면역 세포 수용체.
실시형태 16. 실시형태 11 내지 15 중 어느 하나에 있어서, 상기 CR은 세포내 CR 공동자극 도메인을 더 포함하는, 조작된 면역 세포.
실시형태 17. 실시형태 16에 있어서, 상기 세포내 CR 공동자극 신호전달 도메인은 CD27, CD28, 4-1BB, OX40, CD40, PD-1, LFA-1, ICOS, CD2, CD7, LIGHT, NKG2C, B7-H3, TNFRSF9, TNFRSF4, TNFRSF8, CD40LG, ITGB2, KLRC2, TNFRSF18, TNFRSF14, HAVCR1, LGALS9, DAP10, DAP12, CD83, CD83의 리간드 및 이들의 조합으로 이루어진 군으로부터 선택되는 공동자극 분자로부터 유래되는, 조작된 면역 세포.
실시형태 18. 실시형태 17에 있어서, 상기 세포내 CR 공동자극 신호전달 도메인은 4-1-BB의 세포질 도메인을 포함하는, 조작된 면역 세포.
실시형태 19. 실시형태 11 내지 18 중 어느 하나에 있어서, CR 항원 결합 도메인의 C-말단과 CR 막관통 도메인의 N-말단 사이에 위치한 CR 힌지 도메인을 더 포함하는, 조작된 면역 세포.
실시형태 20. 실시형태 19에 있어서, 상기 CR 힌지 도메인은 CD8α로부터 유래되는, 조작된 면역 세포.
실시형태 21. 실시형태 1 내지 10 중 어느 하나에 있어서, 상기 CR은 세포내 공동자극 도메인을 포함하지 않는, 조작된 면역 세포.
실시형태 22. 실시형태 1 내지 10 중 어느 하나에 있어서, 상기 CR은 키메라 T 세포 수용체("cTCR")인, 조작된 면역 세포.
실시형태 23. 실시형태 22에 있어서, 상기 CR 막관통 도메인은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε 및 CD3δ로 이루어진 군으로부터 선택되는 TCR 서브유닛의 막관통 도메인으로부터 유래되는, 조작된 면역 세포.
실시형태 24. 실시형태 23에 있어서, 상기 CR 막관통 도메인은 CD3ε의 막관통 도메인으로부터 유래되는, 조작된 면역 세포.
실시형태 25. 실시형태 22 내지 24 중 어느 하나에 있어서, 상기 세포내 CR 신호전달 도메인은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε 및 CD3δ로 이루어진 군으로부터 선택되는 TCR 서브유닛의 세포내 신호전달 도메인으로부터 유래되는, 조작된 면역 세포.
실시형태 26. 실시형태 25에 있어서, 상기 세포내 CR 신호전달 도메인은 CD3ε의 세포내 신호전달 도메인으로부터 유래되는, 조작된 면역 세포.
실시형태 27. 실시형태 22 내지 26 중 어느 하나에 있어서, 상기 CR 막관통 도메인 및 세포내 CR 신호전달 도메인은 동일하거나 상이한 TCR 서브유닛(들)으로부터 유래되는, 조작된 면역 세포.
실시형태 28. 실시형태 22 내지 27 중 어느 하나에 있어서, 상기 CR은 TCR 서브유닛의 세포외 도메인의 일부를 더 포함하는, 조작된 면역 세포.
실시형태 29. 실시형태 22 내지 28 중 어느 하나에 있어서, 상기 CR은 CD3ε의 N-말단에 융합된 CR 항원 결합 도메인을 포함하는, 조작된 면역 세포.
실시형태 30. 실시형태 6 내지 29 중 어느 하나에 있어서, 상기 CR을 인코딩하는 핵산은 유도성 프로모터 하에 있는, 조작된 면역 세포.
실시형태 31. 실시형태 6 내지 29 중 어느 하나에 있어서, 상기 CR을 인코딩하는 핵산은 구성적으로 발현되는, 조작된 면역 세포.
실시형태 32. 실시형태 6 내지 31 중 어느 하나에 있어서, 상기 CCOR 및/또는 COR을 인코딩하는 핵산은 유도성 프로모터 하에 있는, 조작된 면역 세포.
실시형태 33. 실시형태 6 내지 31 중 어느 하나에 있어서, 상기 CCOR 및/또는 COR을 인코딩하는 핵산은 구성적으로 발현되는, 조작된 면역 세포.
실시형태 34. 32에 있어서, 상기 CCOR 및/또는 COR을 인코딩하는 핵산은 면역 세포의 활성화시 유도성인, 조작된 면역 세포.
실시형태 35. 실시형태 6 내지 34 중 어느 하나에 있어서, 상기 제1 핵산 및 제2 핵산은 동일한 벡터 상에 있는, 조작된 면역 세포.
실시형태 36. 실시형태 35에 있어서, 제1 핵산 및 제2 핵산은 동일한 프로모터의 제어 하에 있는, 조작된 면역 세포.
실시형태 37. 실시형태 6 내지 31 중 어느 하나에 있어서, 상기 제1 핵산 및 제2 핵산은 상이한 벡터 상에 있는, 조작된 면역 세포.
실시형태 38. 실시형태 10 내지 37 중 어느 하나에 있어서, 하나 이상의 COR-인코딩 핵산은 제1 핵산과 동일한 벡터 상에 있는, 조작된 면역 세포.
실시형태 39. 실시형태 10 내지 38 중 어느 하나에 있어서, 하나 이상의 COR 인코딩 핵산은 제2 핵산과 동일한 벡터 상에 있는, 조작된 면역 세포.
실시형태 40. 실시형태 38 또는 39에 있어서, 상기 하나 이상의 COR 인코딩 핵산 및 제1 핵산 또는 제2 핵산은 동일한 프로모터의 제어 하에 있는, 조작된 면역 세포.
실시형태 41. 실시형태 1 내지 40 중 어느 하나에 있어서, 상기 CR 표적 항원 CD4인, 조작된 면역 세포.
실시형태 42. 실시형태 1, 5, 6 및 10 내지 40 중 어느 하나에 있어서, 상기 CCOR 표적 항원은 CD4인, 조작된 면역 세포.
실시형태 43. 실시형태 1, 5, 6 및 10 내지 40 및 42 중 어느 하나에 있어서, 상기 CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4인, 조작된 면역 세포.
실시형태 44. 실시형태 1, 5, 6 및 10 내지 41 중 어느 하나에 있어서, 상기 CR 표적 항원은 CD4이고 CCOR 표적 항원은 CCR5 또는 CXCR4인, 조작된 면역 세포.
실시형태 45. 실시형태 41 내지 44 중 어느 하나에 있어서, 상기 CR 항원 결합 도메인 또는 CCOR 항원 결합 도메인은 CD4의 도메인 1(CD4 D1)을 특이적으로 인식하는, 조작된 면역 세포.
실시형태 46. 실시형태 5 및 10 내지 45 중 어느 하나에 있어서, 상기 하나 이상의 COR은 CXCR5, α4β7, 및 CCR9로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
실시형태 47. 실시형태 46에 있어서, 상기 하나 이상의 COR은 CXCR5인, 조작된 면역 세포.
실시형태 48. 실시형태 46 또는 47에 있어서, 상기 하나 이상의 COR은 α4β7인, 조작된 면역 세포.
실시형태 49. 실시형태 46 내지 48 중 어느 하나에 있어서, 상기 하나 이상의 COR은 CCR9인, 조작된 면역 세포.
실시형태 50. 실시형태 46 내지 49 중 어느 하나에 있어서, 상기 하나 이상의 COR은 α4β7 및 CCR9를 둘 다 포함하는, 조작된 면역 세포.
실시형태 51. 실시형태 1 내지 50 중 어느 하나에 있어서, 상기 조작된 면역 세포는 세포 내에서 CCR5의 발현을 감소시키거나 제거하도록 변형되는, 조작된 면역 세포.
실시형태 52. 실시형태 1 내지 51 중 어느 하나에 있어서, 상기 조작된 면역 세포는 항-HIV 항체를 발현하도록 변형되는, 조작된 면역 세포.
실시형태 53. 실시형태 52에 있어서, 상기 항-HIV 항체는 광범위 중화 항체인, 조작된 면역 세포.
실시형태 54. 실시형태 53에 있어서, 상기 광범위 중화 항체는 VRC01, PGT121, 3BNC117 10-1074인, 조작된 면역 세포.
실시형태 55. 실시형태 1 내지 54 중 어느 하나에 있어서, 상기 CR 항원 결합 도메인은 Fab, Fab', (Fab')2, Fv, 단일 사슬 Fc(scFv), 단일 도메인 항체(sdAb), 및 CR 표적 항원에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
실시형태 56. 실시형태 55에 있어서, 상기 CR 항원 결합 도메인은 scFv 또는 sdAb인, 조작된 면역 세포.
실시형태 57. 실시형태 1, 5, 6, 및 10 내지 56 중 어느 하나에 있어서, 상기 CCOR 항원 결합 도메인은 Fab, Fab', (Fab')2, Fv, 단일 사슬 Fc(scFv), 단일 도메인 항체(sdAb), 및 CCOR 표적 항원에 특이적으로 결합하는 펩타이드 리간드로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
실시형태 58. 실시형태 57에 있어서, 상기 CCOR 항원 결합 도메인은 scFv 또는 sdAb인, 조작된 면역 세포.
실시형태 59. 실시형태 1 내지 58 중 어느 하나에 있어서, 상기 CCOR 공동자극 도메인은 CD28, 4-1BB(CD137), CD27, OX40, CD27, CD40, PD-1, ICOS, 림프구 기능-연관 항원-1(LFA-1), CD2, CD7, LIGHT, NKG2C, B7-H3, TNFRSF9, TNFRSF4, TNFRSF8, CD40LG, ITGB2, KLRC2, TNFRSF18, TNFRSF14, HAVCR1, LGALS9, CD83, 및 CD83과 특이적으로 결합하는 리간드 중 하나 이상의 공동자극 도메인으로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
실시형태 60. 실시형태 1 내지 59 중 어느 하나에 있어서, 상기 조작된 면역 세포는 세포독성 T 세포, 헬퍼 T 세포, 자연 살해 세포, γδT 세포 및 자연 살해 T 세포로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
실시형태 61. 실시형태 60에 있어서, 상기 조작된 면역 세포는 세포독성 T 세포인, 조작된 면역 세포.
실시형태 62. 실시형태 1 내지 61 중 어느 하나의 조작된 면역 세포 및 약제학적으로 허용 가능한 담체를 포함하는 약제학적 조성물.
실시형태 63. 실시형태 62에 있어서, 상기 약제학적 조성물은 실시형태 1 내지 61 중 어느 하나에 따른 조작된 면역 세포의 적어도 2가지 상이한 유형을 포함하는 약제학적 조성물.
실시형태 64. 유효량의 실시형태 62 또는 63의 약제학적 조성물을 개체에게 투여하는 단계를 포함하는, 개체에서 전염병을 치료하는, 방법.
실시형태 65. 실시형태 64에 있어서, 상기 전염병은 HIV 및 HTLV로 이루어진 군으로부터 선택되는 바이러스에 의한 감염인, 방법.
실시형태 66. 실시형태 65에 있어서, 상기 전염병은 HIV인, 방법.
실시형태 67. 실시형태 64 내지 66에 있어서, 개체에게 제2 항-감염제를 투여하는 단계를 더 포함하는, 방법.
실시형태 68. 실시형태 67에 있어서, 상기 감염제는 항-레트로바이러스 약물, 광범위 중화 항체, 톨-유사 수용체 효현제, 잠복 재활성화제, CCR5 길항제, 면역 자극제, 및 백신으로 이루어진 군으로부터 선택되는, 방법.
실시형태 69. 유효량의 실시형태 62 또는 63의 약제학적 조성물을 개체에게 투여하는 단계를 포함하는, 개체에서 암을 치료하는, 방법.
실시형태 70. 실시형태 69에 있어서, 상기 암은 T 세포 림프종인, 방법.
실시형태 71. 실시형태 69 또는 70에 있어서, 개체에게 제2 항암제를 투여하는 단계를 더 포함하는, 방법.
실시형태 72. 실시형태 71에 있어서, 상기 제2 항암제는 CD70 표적화 약물, TRBC1, CD30 표적화 약물, CD37 표적화 약물 및 CCR4 표적화 약물로 이루어진 군으로부터 선택되는, 방법.
실시형태 73. 실시형태 64 내지 72 중 어느 하나에 있어서, 상기 개체는 인간인, 방법.
실시형태 74. a) 면역 세포 집단을 제공하는 단계; b) 상기 면역 세포 집단 내로 CR을 인코딩하는 제1 핵산을 도입하는 단계를 포함하는, 실시형태 1 내지 61 중 어느 하나의 조작된 면역 세포를 제조하는, 방법.
실시형태 75. 실시형태 74에 있어서, c) 상기 면역 세포 집단 내로 CCOR을 인코딩하는 제2 핵산을 도입하는 단계를 더 포함하는, 방법.
실시형태 76. 실시형태 75에 있어서, 상기 제1 핵산 및 제2 핵산은 세포 내로 동시에 도입되는, 방법.
실시형태 77. 실시형태 75에 있어서, 상기 제1 핵산 및 제2 핵산은 세포 내로 순차적으로 도입되는, 방법.
실시형태 78. 실시형태 74 내지 77 중 어느 하나에 있어서, 상기 면역 세포 집단 내로 하나 이상의 COR을 인코딩하는 하나 이상의 핵산을 도입하는 단계를 더 포함하는, 방법.
실시형태 79. 실시형태 74 내지 78 중 어느 하나에 있어서, 상기 제1 핵산, 제2 핵산, 및/또는 COR 인코딩 핵산은 세포 내로 바이러스 벡터를 통해 도입되는, 방법.
실시형태 80. 실시형태 74 내지 79 중 어느 하나에 있어서, 상기 면역 세포 집단 내로 광범위 중화 항체(bNAb) 또는 HIV 융합 저해 펩타이드를 인코딩하는 핵산을 도입하는 단계를 더 포함하는, 방법.
실시형태 81. 실시형태 74 내지 80 중 어느 하나에 있어서, 세포에서 CCR5 유전자를 비활성화시키는 단계를 더 포함하는, 방법.
실시형태 82. 실시형태 81에 있어서, 상기 CCR5 유전자는 CRISPR/Cas9, TALEN, ZFN, siRNA, 및 안티센스 RNA로 이루어진 군으로부터 선택되는 방법을 사용하여 비활성화되는, 방법.
실시형태 83. 실시형태 74 내지 82 중 어느 하나에 있어서, 개체의 말초 혈액으로부터 상기 면역 세포 집단을 수득하는 단계를 더 포함하는, 방법.
실시형태 84. 실시형태 83에 있어서, 상기 면역 세포 집단은 CD4+ 세포에 대해 추가로 풍부화되는, 방법.
실시형태 85. 실시형태 83 또는 84에 있어서, 상기 면역 세포 집단은 CD8+ 세포에 대해 추가로 풍부화되는, 방법.
당업자는 여러 실시형태가 본 발명의 범주 및 사상 내에서 가능하다는 것을 인식할 것이다. 이제 본 발명은 하기 비-제한적인 실시예를 참조하여 보다 상세히 설명될 것이다. 하기 실시예는 본 발명을 추가로 예시하지만, 물론 어떠한 방법으로도 그 범주를 제한하는 것으로 해석되어서는 안된다.
실시예
실시예 1: 1차 T 세포 및 다른 포유동물 세포에서 CR 및 CCOR의 발현
구성적 프로모터 hEF1α, 독시사이클린 유도성 프로모터(예컨대, 테트온), NFAT-의존성 유도성 프로모터, 또는 열 유도성 프로모터(예컨대, 인간 열 충격 단백질 70 프로모터, HSP70p)에 의해 구동되는 CR, CCOR, 및 선택적으로 COR을 인코딩하는 핵산을 가지는 렌티바이러스 벡터를 설계하고 제조한다. 1차 인간 말초 혈액 단핵 세포(PBMC)를 건강한 공여자 유래의 말초 혈액의 밀도 구배 원심분리에 의해 준비한다. 인간 1차 T 세포를 자기 비드 단리를 사용하여 PBMC로부터 정제한다. 인간 T 세포를 렌티바이러스 벡터를 이용하여 형질도입하고 며칠 동안 생체 외에서 확장시킨다. 당업계에 알려진 방법을 사용하여 수용체의 발현을 검출할 수 있다. 형질도입된 T 세포의 생물활성을 시험관내 표적 세포의 사멸 및 다른 시험관내 분석 및 생체 내 동물 모델을 통해 평가할 수 있다.
실시예 2. 재료 및 방법
세포. DMEM+10% FBS 중에 293T 세포를 유지하였다. 동결보존된 인간 말초 혈액 단핵 세포(PBMC)를 헤마케어(Hemacare)에서 구입하였다. T 세포를 T 세포 단리 키트(밀테니(Miltenyi))에 의해 PBMC로부터 단리하고, T 세포 활성화/확장 키트(밀테니)에 의해 활성화시켰다. T 세포를 AIM-V 배지 + 5% 소태아 혈청(FBS) + 300 IU/㎖ IL-2 중에 유지하였다.
플라스미드 및 렌티바이러스 생성. 키메라 항원 수용체(CAR) 유전자 또는 eTCR 유전자를 pLVX 벡터에서 EF1α 프로모터에 의해 제어하였다. 진스크립트(Genscript)에 의해 유전자를 합성하고 벡터 내로 클로닝하였다. CAR 또는 eTCR 전달 플라스미드, 2세대 렌티바이러스 패키징 플라스미드 및 VSV-G 외피 코딩 플라스미드를 이용하여 293T 세포를 형질감염시켰다. 10% 폴리에틸렌이민(PEI) 시약에 의해 플라스미드를 293T 세포 내로 형질감염시켰다. 형질 감염 후 48시간 및 72시간에 바이러스 상청액을 수확하였다. 상청액을 0.45 ㎛ 멸균 필터를 통해 여과하여 세포 잔사를 제거하였다. PEG 방법에 의해 바이러스를 농축시키고, 분취한 다음, -80℃에서 보관하였다.
CAR-T 구축. 팬 T 세포를 팬 T 세포 단리 키트(밀테니 바이오테크(Miltenyi Biotech))에 의해 PBMC로부터 풍부화시키고 T 세포 활성화/확장 키트(밀테니 바이오테크)에 의해 48시간 동안 활성화시켰다. 활성화된 T 세포를 8 ㎍/㎖ 폴리브렌(Polybrene)의 존재 하에 렌티바이러스와 함께 인큐베이션하고, 실온에서 1000 g로 1시간 동안 회전접종하였다(spinoculated). 세포를 AIM-V 배지 + 5% 소태아 혈청(FBS) + 300 IU/㎖ 재조합 인간 IL-2 중에서 확장시켰다. 형질도입 4일 후 CAR+ 또는 eTCR+ 백분율로서 유세포 분석에 의해 형질도입 효율을 결정하였다.
세포독성 분석. 표적 세포를 PBS 중에서 5분 동안 실온에서 2.5 μM CFSE를 이용하여 표지화한 후 1/10 부피의 FBS를 첨가함으로써 반응을 중지시켰다. 세포를 2회 세척하고 배양 배지에 재현탁시켰다. 이펙터 세포 및 표적 세포를 원하는 이펙터:표적 비율(E:T 비율)로 24시간 동안 공동 배양하였다. CFSE 표지화 표적 세포의 사멸을 유세포 분석에 의해 조사하였다.
SHIV 감염 분석. CD4 T 세포를 시험관내에서 4일 동안 정제하고 활성화시킨 후 SHIVSF162P3 바이러스로 감염시켰다. 상기 세포를 감염 후 제12일에 표적 세포로 사용하였다. UNT 세포, 항-CD4 CAR-T 세포, 항-CCR5 CAR-T 세포 및 탠덤 항-CD4/항-CCR5 세포를 이펙터 세포로 사용하였다. 이펙터 및 표적 세포를 0.5:1 및 2:1 비율로 72시간 동안 공동배양하였다. 바이러스 양성 세포 비율을 p27 세포내 염색에 의해 검출하였다.
유세포 분석. 항-인간 CD3, CD4, CD8, CCR5 및 p27 단클론성 항체를 바이오레전드(Biolegend) 및 BD 바이오사이언스(BD Bioscience)에서 구입하였다. 염소 항-인간 IgG, F(ab')2 다클론성 항체를 잭슨 이뮤노리서치(Jackson ImmunoResearch)에서 구입하였다. 세포를 유동 염색(flow staining)을 위해 DPBS + 2% FBS + 1 mM EDTA 중에 재현탁시켰다. BD FACS첼레스타(BD FACSCelesta) 유세포 분석기에서 데이터를 수집하고 플로우조(Flowjo) 소프트웨어(트리스타(TreeStar))에 의해 분석하였다.
HTRF 분석. 표적 세포를 이펙터 세포와 24시간 동안 공동배양하였다. 세포 배양 배지를 수확하고 HTRF 분석(Cisbio)에 의해 IFNγ 농도를 검출하였다. 제조업체의 프로토콜에 따라 분석을 수행하였다. 간략하게, 16㎕의 샘플을 분석 플레이트에서 4㎕의 미리 혼합한 항-IFNγ 항체와 혼합하였다. 플레이트를 실온 암실에서 밤새 인큐베이션하였다. PheraStar 마이크로플레이트 판독기에 의해 신호를 검출하였다.
QPCR 분석. 표적 T 세포를 또한 향상된 녹색 형광 단백질(EGFP)을 발현하는 HIV 슈도바이러스로 감염시켰다. 표적 세포를 이펙터 세포와 1:1 비율로 24시간 동안 공동배양하였다. 세포를 수확하고 게놈 DNA를 QPCR을 위해 수집하였다. 세포 게놈 DNA에서 EGFP 복제물을 검출함으로써 통합된 DNA 복제물을 검출하였다.
림프종 마우스 모델에 대한 CAR-T 처리. NCG 마우스에 피하 주사에 의해 HH 피부 T 세포 림프종 세포를 이식하였다. 종양 크기가 120㎣에 이를 때 처리를 위해 마우스를 3개 그룹으로 분리하였다. 대조군 UNT 세포 및 CAR-T 세포를 HBSS 완충액에 재현탁하였다. 꼬리-정맥 주사에 의해 세포를 마우스에 접종하였다. 한 그룹의 마우스는 대조군으로서 400㎕ HBSS를 받았다. 마우스의 한 그룹은 2,500만개의 UNT 세포를 받았고, 마지막 그룹의 마우스는 500만개의 CAR+ 항-CD4 CAR-T 세포를 받았다. 마우스를 관찰하고, 종양 크기 및 체중을 실험 종료시까지 기록하였다. 종양 크기가 2000㎣에 이를 때 마우스를 희생시켰다.
인간화 마우스 모델에서 CAR-T 생체 내 테스트. 신생아 NCG 마우스에 인간 조혈 줄기세포를 이식하여 마우스를 인간 면역 세포로 재구성하고, HIS 마우스로 명명하였다. HIS 마우스를 항-CD4, 항-CCR5 또는 탠덤 항-CD4/항-CCR5 CAR-T 세포로 처리하였다. 그리고 CD4+/CCR5+ 세포의 존재를 실험 동안 테스트하였다.
실시예 3. CAR T 세포의 평가
이 실시예는 본 출원에 예시된 다양한 CAR 작제물의 평가를 기재한다.
키메라 항원 수용체(CAR) 발현 벡터의 구축.
도 6A 및 도 6B는 일렬로 연결된 항-CD4 또는 항-CCR5 또는 항-CXCR4 scFv 또는 sdAb(도 6A) 또는 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 6B)를 함유하는 CAR 작제물의 개략도를 나타낸다. CAR은 항원 인식 도메인, 힌지, 막관통 도메인, 세포내 공동자극 도메인 4-1BB 및 CD3ζ 세포내 도메인으로 구성된다. 항원 인식 도메인은 scFv, sdAb, 링커에 의해 연결된 2개의 탠덤 scFv, 또는 링커에 의해 연결된 2개의 탠덤 sdAb일 수 있다. scFv 또는 sdAb는 인간 CD4 또는 인간 CCR5 또는 인간 CXCR4 중 임의의 것을 인식할 수 있다. 링커는 (GGGGS)n일 수 있으며, 여기서 n은 2 내지 5의 임의의 수일 수 있다. 여기서 표시된 힌지는 인간 CD8의 세포외 도메인(서열번호 2)의 일부이다. 막관통 도메인은 인간 CD8 막관통 도메인(서열번호 3)에서 유래한다. 세포내 도메인은 인간 4-1BB 세포내 영역(서열번호 4) 및 CD3ζ 신호전달 형질도입 도메인(서열번호 5)에서 유래한다. 본 실시예에서 사용된 CAR 작제물은 다음 서열을 가진다:
항-CD4 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ(항-CD4 CAR): 서열번호 11, 서열번호 49 내지 64.
항-CCR5 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ(항-CCR5 CAR): 서열번호 12, 서열번호 35 내지 48.
항-CXCR4 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ(항-CXCR4 CAR): 서열번호 65 내지 72.
항-CD4 scFv-항-CCR5 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ(탠덤 항-CD4-항-CCR5 CAR): 서열번호 13
항-CD4 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ-P2A-CXCR5(CXCR5를 갖는 항-CD4 CAR): 서열번호 14
항-CCR5 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ-P2A-CXCR5(CXCR5를 갖는 항-CCR5 CAR): 서열번호 15
항-CD4 scFv-항-CCR5 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ-P2A-CXCR5(CXCR5를 갖는 탠덤 항-CD4-항-CXCR5 CAR): 서열번호 16
항-CD4 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ-P2A-CXCR5-P2A-VRC01(CXCR5 및 VRC01을 갖는 항-CD4 CAR): 서열번호 17
항-CCR5 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ-P2A-CXCR5-P2A-VRC01(CXCR5 및 VRC01을 갖는 항-CCR5 CAR): 서열번호 18
항-CD4 scFv-항-CCR5 scFv-CD8 힌지-CD8 TM-4-1BB-CD3ζ-P2A-CXCR5-P2A-VRC01(CXCR5 및 VRC01을 갖는 탠덤 항-CD4-항-CCR5 CAR): 서열번호 19
CAR 세포 구축 및 표현형.
인간 말초 단핵 세포(PBMC)로부터 단리한 T 세포로부터 CAR-T 세포를 생성하였다. PBMC 유래의 T 세포를 시험관내에서 풍부화시키고 활성화시킨 후 CAR 유전자를 인코딩하는 렌티바이러스를 이용하여 형질도입하였다. CD8+ T 세포는 세포독성 인자, 퍼포린 및 그랜자임 B를 분비함으로써 활성화 시 표적 세포-사멸 기능을 가진다. CD8 T 세포의 세포독성 기능은 적응 면역계가 감염된 세포를 제거하고 본질적인 이상 세포 형질전환을 감시하는 데 중요하다. 표적 세포 사멸 기능은 또한 인공적으로 조작된 CAR-T 세포의 가장 중요한 기능이다. 조작된 CAR-T 세포의 세포독성 기능을 조사하기 위하여, CAR-T 세포를 팬 T 세포와 원하는 비율로 공동배양하였다. 이의 CAR-T 세포를 이펙터 세포(E)로 명명하는 한편, 팬 T 세포를 표적 세포(T)로 명명하였다. 이펙터 세포와 구별되도록 표적 세포를 CFSE로 표지화하였다. 표적 및 이펙터 세포를 24시간 동안 공동배양한 후 유세포 분석을 위해 수확하였다. CFSE-표지화 표적 세포 백분율을 기록하여 세포독성 효과를 반영하였다. 형질도입되지 않은 T 세포(UNT) 세포를 CAR-T 세포에 대한 음성 대조군으로 사용하였다. CAR-T 형질도입 1주 후, 상기 세포의 핵심 기능, 즉 표적 세포 사멸 능력을 초기 스크리닝 동안 테스트하였다. 도 7은 항-CCR5 CAR-T, 항-CD4 CAR-T 및 항-CXCR4 CAR-T 세포의 정량적 스크리닝 결과를 나타낸다. 14가지 항-CCR5 CAR-T 중에서, 번호 13이 가장 우수한 표적 사멸 효과를 가졌다. 16가지 항-CD4 CAR-T 중에서, 번호 13이 가장 효율적인 것이었다. 8가지 항-CXCR4 CAR-T 중에서, 번호 5가 가장 우수한 표적 사멸 효과를 가졌다. 항-CD4 CAR-T 번호 13을 CD4 CAR-T(서열번호 11)로 개명하였고 scFv 서열을 다음의 모든 항-CD4 설계에서 사용하였다. 항-CCR5 CAR-T 번호 13을 항-CCR5 CAR-T(서열번호 12)로 개명하였고, 이의 scFv 서열을 복합체 설계에서 사용하였다.
CAR 구조가 서로 유사하였지만, 모든 키메라 항원 수용체가 T 세포와 동일하게 형질도입될 수 있는 것은 아니었다. 염소 항-인간 IgG, F(ab')2 항체를 유세포 분석에 의한 CAR+ T 세포의 백분율을 검출하는 데 사용하였다. 도 8A 내지 8E는 형질도입 4일 후 CAR+% 세포를 나타낸다.
CAR-T 세포를 AIM-V 배지 + 5% FBS + 300 IU/㎖ IL-2 중에서 배양하였다. 세포가 융합하는 경우 세포를 더 큰 웰로 옮겼다. 신선한 완전 배지를 보충하여 세포 확장을 지원하였다. 세포 수 및 생존력을 형질도입 후 제0일, 제4일, 제6일 및 제10일에 기록하였다. 항-CD4 CAR-T 번호 13의 확장이 도 9에 도시되어 있다.
CAR-T 세포독성 분석
도 10A, 도 10B 및 도 10E는 CAR-T 세포의 세포독성 효과에 대한 유세포 분석 결과를 도시한다. 도 10A에 나타낸 바와 같이, 대조군 UNT 세포와 공동배양한 표적 세포에서 58%의 CD4+ T 세포가 있었지만, 표적 세포를 항-CD4 CAR-T 번호 13과 공동배양하였을 때 CD4+ 집단은 0%로 감소하였으며, 이는 표적에 대한 항-CD4 CAR-T 번호 13의 강력한 사멸 효과를 시사한다. 도 10B에서, 표적 세포를 UNT와 공동배양하였을 때 CCR5+ 집단은 약 15%였지만, 표적 세포를 항-CCR5 CAR-T 번호 13 세포와 공동배양하였을 때 집단은 1% 미만으로 감소하였으며, 이는 항-CCR5 CAR-T 번호 13 세포가 매우 효과적임을 시사한다. 도 10E는 탠덤 항-CD4/항-CCR5-CART의 효과를 나타낸다. 탠덤 CART 세포는 CD4 단일 양성 세포와 CCR5 단일 양성 세포를 제거하였을 뿐만 아니라, CD4/CCR5 이중 양성 집단도 효율적으로 제거하였다.
CAR-T 사이토카인 프로파일링
퍼포린 및 그랜자임 B 이외에, 활성화시 CD8+ T 세포는 또한 사이토카인 IFNγ 및 TNFα를 분비한다. 이러한 전염증성 사이토카인은 중요한 CD8+ T 세포 기능 지표이지만, 이는 또한 입양 T 세포 요법, 사이토카인 방출 증후군의 부작용에서도 역할을 할 수 있다. 시험관내 HTRF 분석에 의해 IFNγ의 생성을 검출하였다. 형질도입 후 제6일에 상청액을 수집하고 사이토카인 수준을 측정하였다. 도 11은 항-CD4 CAR-T 번호 13 세포에 의한 이들 사이토카인의 생성을 나타낸다.
실시예 4. eTCR T 세포의 평가
이 실시예는 본 출원에서 예시된 다양한 키메라 TCR 작제물의 평가를 기재한다.
항-CD4-eTCR 및 항-CCR5-eTCR 발현 벡터의 구축
T 세포 수용체 α 및 β 사슬은 CD3 ε/δ/γ/ζ 사슬과 복합체를 형성한다. TCR은 MHC에 의해 제시된 항원을 인식하여, CD3 ζ 사슬의 인산화를 야기하고 후속적으로 세포 내부의 하류 경로로 신호를 전달하여 T 세포를 활성화시킨다. 자연 T 세포 활성화는 TCR-MHC 상호작용에 의존하므로, MHC 의존성이다. 본 명세서에 기재된 이러한 키메라 TCR은 TCR 복합체를 변형시켜 MHC-독립적 방식으로 T 세포를 활성화시켰다. 변형은 CD3ε에 있으며, 이의 전체 명칭은 T-세포 표면 당단백질 CD3 엡실론 사슬(서열번호 6)이다. CD3ε 서열은 공공 데이터베이스, 예컨대, Uniprot 및 NCBI Genebank에서 입수가능하다. 서열번호 6에 열거된 서열은 Uniprot ID P07766으로부터의 것이다. 이 키메라 TCR은 본 명세서에서 eTCR로 명명된다.
eTCR 유전자는 렌티바이러스 벡터에 의해 발현되고 EF1α 프로모터에 의해 제어된다. CD3ε 신호 펩타이드 서열(서열번호 7) 다음에 항원 인식 서열이 온다. 링커 (G4S)3 서열을 항원 인식 서열과 CD3ε 서열 사이에 추가하였다(서열번호 8). DNA 서열을 최적화하고 진스크립트에서 새로 합성한 다음 게이트웨이 클로닝(Gateway Cloning)에 의해 pLVX 렌티바이러스 벡터 내로 클로닝하였다. 본 실시예에서 사용된 eTCR 작제물은 다음 서열을 가진다:
항-CD4-CD3ε(항-CD4 eTCR): 서열번호 20, 73
항-CCR5-CD3ε(항-CCR5 eTCR): 서열번호 21, 74 내지 76
항-CD4-CD3ε-P2A-CXCR5(CXCR5를 갖는 항-CD4 eTCR): 서열번호 22
항-CCR5-CD3ε-P2A-CXCR5(CXCR5를 갖는 항-CCR5 eTCR): 서열번호 23
항-CD4-항-CCR5-CD3ε-P2A-CXCR5(CXCR5를 갖는 탠덤 항CD4-항-CCR5 eTCR): 서열번호 24
항-CD4-항-CCR5-CD3ε-P2A-CXCR5-P2A-VRC01(CXCR5 및 VRC01을 갖는 탠덤 항CD4-항CCR5 eTCR): 서열번호 25
도 12A 및 도 12B는 항-CD4 또는 항-CCR5 scFv 또는 sdAb(도 12A), 또는 일렬로 연결된 항-CD4 및 항-CCR5 scFv 또는 sdAb(도 12B)를 함유하는 예시적인 eTCR의 개략도를 나타낸다. scFv, sdAb, 2개의 탠덤 scFv 또는 2개의 탠덤 sdAb는 (G4S)3 링커에 의해 CD3ε 사슬에 연결된다.
eTCR 설계를 추가로 개발할지 여부에 대한 주요 결정자로서 표적 세포 사멸 효과를 평가하였다. 조작된 eTCR-T 세포의 표적 세포 사멸 효과를 조사하기 위하여, eTCR-T 세포를 팬 T 세포와 원하는 비율로 공동배양하였다. 이의 eTCR-T 세포를 이펙터 세포(E)로 명명하는 한편, 팬 T 세포를 표적 세포(T)로 명명하였다. 이펙터 세포와 구별되도록 표적 세포를 CFSE로 표지화하였다. 표적 및 이펙터 세포를 24시간 동안 공동배양한 후 유세포 분석을 위해 수확하였다. CFSE-표지화 표적 세포 백분율을 기록하여 세포독성 효과를 반영하였다. 형질도입되지 않은 T 세포(UNT) 세포를 eTCR-T 세포에 대한 음성 대조군으로 사용하였다. 도 12C는 CD4 CAR-T 번호 13, CD4 eTCR, CD4 eTCR 번호 11의 표적 세포 사멸 효과를 정량적으로 비교하였다. CD4 eTCR 번호 11은 이발리주맙 항체 서열 유래의 항원 결합 영역을 가진다. CD4 eTCR 번호 11의 표적 세포 사멸 능력은 CD4 eTCR보다 덜 최적이다.
도 12D는 3가지 스크리닝된 항-CCR5 eTCR 작제물의 결과를 나타내었다. 3가지 항-CCR5 작제물 중에서, CCR5 eTCR이 가장 우수한 표적 세포 사멸 효과를 가졌으며 이를 추가로 연구하였다.
eTCR-T 세포 표현형
CAR-T 세포와 같이, eTCR을 코딩하는 렌티바이러스를 이용하여 활성화된 T 세포를 형질도입함으로써 eTCR 세포를 생성하였다. 모든 T 세포가 동일한 효율로 형질도입될 수 있는 것은 아니다. 염소 항-인간 IgG, F(ab')2 항체를 유세포 분석에 의한 eTCR+ T 세포의 백분율을 검출하는 데 사용하였다. 도 13A는 형질도입 4일 후 eTCR+% 세포를 나타낸다.
eTCR-T 세포 확장
eTCR-T 세포를 AIM-V 배지 + 5% FBS + 300 IU/㎖ IL-2 중에서 배양하였다. 세포가 융합하는 경우 세포를 더 큰 웰로 확장시키고 신선한 완전 배지를 보충하여 세포가 항상 이상적인 배양 조건에 있는 것을 확실하게 하였다. 세포 수 및 생존력을 형질도입 후 제0일, 제4일, 제6일 및 제10일에 기록하였다. eTCR-T 세포의 확장이 도 13C에 도시되어 있다.
eTCR-T 세포독성
도 14는 eTCR-T 매개 표적 세포 사멸의 대표적인 유세포 분석 결과를 나타낸다. 도 14A는 항-CD4 eTCR-T 세포가 표적 세포에서 CD4+ 집단을 완전히 고갈시킬 수 있는 항-CD4 eTCR T 세포의 세포독성 효과의 유세포 분석 결과를 도시한다. 항-CCR5 eTCR-T 세포는 또한 도 14B에 나타낸 바와 같이 CCR5+ 집단의 대부분을 사멸시켰다.
eTCR-T 사이토카인 프로파일링
시험관내 HTRF 분석에 의해 IFNγ의 생성을 검출하였다. eTCR-T 세포를 표적 팬 T 세포와 2:1 및 0.5:1 비율로 24시간 동안 공동배양하고 상청액을 수집하였다. 도 13B는 항-CD4 eTCR-T 세포에 의한 IFNγ 사이토카인의 생성을 나타낸다. UNT 세포를 대조군으로 사용하였다. eTCR-T 세포에 의해 분비된 IFNγ 사이토카인은 UNT 대조군 세포보다 단지 약간 더 높았다.
실시예 5. CXCR5-발현 T 세포
림프절은 중요한 2차 림프 기관이다. B 세포는 말초 혈액에서 순환하고 성숙을 위해 림프절 B 세포 여포로 들어가며, 여기서 배중심 수지상 세포 및 여포 T 헬퍼 세포의 도움으로 아이소타입 변환 및 친화성 성숙 과정을 거친다. B 세포, 수지상 세포 및 여포 T 세포는, CXCL13에 대한 수용체인 CXCR5를 발현한다. CXCL13은 배중심 기질 세포와 수지상 세포에 의해 생성되는 배중심에 높은 수준으로 있다. CD8+ T 세포는 보통 B 세포 여포에서 매우 드물다. 면역조직학 염색으로 여포 내부에 높은 수준의 HIV 바이러스가 숨어있는 것으로 나타났으며, 이는 배중심이 주요 HIV 저장소임을 시사한다. 엘리트 HIV 컨트롤러의 배중심에서 CD8+ T 세포가 증가한 것으로 보고되었다. 이러한 CD8+ T 세포는 CXCR5와 공동발현하고 높은 수준의 세포독성 이펙터 인자를 발현하며 바이러스 제어에 기여한다. 본 출원의 특정 실시형태는 CAR-T 세포 또는 eTCR-T 세포 상에서 CXCR5를 공동발현하는 것을 포함한다.
도 15는 CAR 또는 eTCR을 가지고 또한 CXCR5를 발현하는 조작된 T 세포를 예시한다. P2A 링커에 의해 CXCR5를 CAR 또는 eTCR 유전자에 연결하였다. 항원 인식 영역은 항-CD4, 항-CCR5 또는 탠덤 항-CD4/항-CCR5일 수 있다. 이는 scFv 또는 sdAb일 수 있다. 항-CXCR5 항체를 CXCR5 발현을 검출하는 데 사용하였다.
이 실험에서 사용된 CAR 및 eTCR 작제물은 상기와 동일하다. CXCR5는 다음 서열을 가진다: 서열번호 9. 도 16A는 형질도입된 항-CD4 CAR-T 세포에서 CXCR5의 발현을 도시하고, 도 16B는 항-CCR5 CAR-T 세포에서 CXCR5의 발현을 도시한다. 상기 도면에 나타낸 바와 같이, CAR+ 세포의 90% 초과는 또한 높은 수준의 CXCR5를 발현한다.
CXCR5를 발현하는 CAR-T 세포는 도 10C 및 도 10D에 나타낸 바와 같이 CXCR5가 없는 CAR-T 세포만큼 효율적으로 표적 세포를 제거할 수 있다. CXCR5를 공동발현하는 CAR-T를 이펙터 세포로 사용하였고 CFSE 표지화 팬 T 세포와 함께 24시간 동안 배양하였다. 도 10C에서, 표적 세포를 UNT 대조군 세포와 함께 배양할 때 63.8% CD4+ T 세포가 있었고, 표적 세포를 CXCR5를 공동발현하는 항-CD4 CAR-T 세포와 공동배양할 때 집단은 1.46%로 떨어졌다. 도 10D에 나타낸 바와 같이, UNT 샘플에서 CCR5+%는 21.2%인 반면, 항-CCR5 CAR-CXCR5 샘플에서 백분율은 0.609%로 감소하였다.
도 10F는 항-CD4/항-CCR5 탠덤 CAR-CXCR5-C34 T 세포의 세포독성 효과를 기재한다. 항-CD4/항-CCR5 탠덤 CAR-CXCR5-C34 T 세포는 CD4/CCR5 이중 양성 집단을 효율적으로 제거하였고 CD4 또는 CCR5 단일 양성 집단의 일부를 남겼으며, 이는 일부 질환 상황에서 안정성을 증가시킬 것이다.
실시예 6. 광범위 중화 항체-발현 T 세포
HIV 감염 집단 중에서, 소수의 사람은 항-레트로바이러스 약을 복용하지 않고 자연적으로 바이러스 감염을 제어할 수 있다. 연구는 이들이 바이러스 감염에 대한 강력한 항체 반응을 생성할 수 있음을 밝혔다. 이들 항체는 HIV 당단백질 GP160에서 비교적 보존된 영역을 인식하고 HIV의 다양한 하위유형을 중화시킬 수 있으므로, 이들 항체는 광범위 중화 항체였다. 광범위 중화 항체는 SHIV에 감염된 히말라야 원숭이에서 테스트되었으며, 중앙값 21주 동안 바이러스 부하를 제어할 수 있다. 본 출원의 특정 실시형태는 CAR-T 세포 또는 eTCR-T 세포에서 광범위 중화 항체를 공동발현하는 것을 포함한다. CAR-T 세포 및 eTCR-T 세포는 광범위 중화 항체를 분비하여 새로운 숙주 세포의 HIV 감염을 차단할 수 있다.
도 17은 항-CD4 또는 항-CCR5 또는 탠덤 항-CD4/항-CCR5 CAR 또는 eTCR, 케모카인 수용체 CXCR5 및 또한 광범위 중화 항체(bNAb)를 발현하는 조작된 T 세포를 도시한다. pLVX 렌티바이러스 벡터 내로 코딩 서열을 클로닝하였다. EF1α 프로모터에 의해 키메라 유전자 전사를 제어하였다. P2A 서열을 CAR 또는 eTCR 서열 뒤에 추가하였다. 인간 CXCR5 서열을 P2A 서열 뒤에 추가하였다. 인간 IL2 신호 펩타이드(서열번호 34)를 가지는 bNAb를 또 다른 P2A에 의해 CXCR5에 연결하였다.
본 실험에 사용된 CXCR5뿐만 아니라 CAR 및 eTCR 작제물은 상기한 바와 동일하다. VRC01은 다음 서열을 가진다: 서열번호 10. His 태그 표지화 VRC01(VRC01-6His)을 인코딩하는 CAR-T 렌티바이러스를 이용하여 T 세포를 형질도입하였다. 배양 상청액을 형질도입 후 제8일에 수확하였다. 상청액 중 VRC01 농도를 항-His 태그 항체를 사용하여 ELISA에 의해 검출하였다. 검출된 농도는 상청액에서 약 40 ng/㎖이었다.
실시예 7. CAR T 세포의 기능적 적용
항-CD4 CAR-T 세포는, HIV 감염에 대한 주요 숙주 세포인 CD4+ T 세포를 사멸시킨다. 이들 세포가 바이러스를 제거할 수 있는지 여부를 설명하기 위해, CD4+ T 세포를 시험관내에서 HIV 슈도바이러스로 감염시켰다. CAR-T 세포를 감염된 세포와 공동배양하였다. 도 18A에 나타낸 바와 같이, CAR-T 세포는 B 세포 마커 CD19(서열번호 77)를 표적화하는 대조군 CAR-T와 비교하여 바이러스 부하를 크게 감소시켰다. 바이러스 감염이 없는 세포를 검출 대조군으로 사용하였다. 도 18B에서, HIV 슈도바이러스로 성공적으로 감염된 임의의 세포가 EGFP+가 되는 HIV 슈도바이러스를 인코딩하는 EGFP로 T 세포를 감염시켰다. 이러한 세포를 표적 세포로 사용하였고 항-CD4 CAR-T 번호 13 세포 또는 UNT 세포와 공동배양하였다. 상이한 E:T 비율을 사용하였다. 세포를 24시간 동안 공동배양하였고 유세포 분석에 의해 EGFP 백분율을 검출하기 위해 세포를 수확하였다. E:T 비율이 증가함에 따라 EGFP+ 비율은 감소하였다. E:T 비율이 1:1 이상에 도달할 때 슈도바이러스+ 세포의 백분율은 거의 0으로 떨어졌다. 도 19A에서 CAR-T 작제물을 SHIV 감염된 CD4+ 표적 세포와 함께 인큐베이션하였다. 바이러스 단백질 p27을 세포내 염색에 의해 검출하였다. 2가지 상이한 이펙터 대 표적 비율, 즉 0.5:1 및 2:1을 사용하였다. p27 양성에 의해 나타낸 바와 같이 SHIV로 성공적으로 감염된 세포는 1.3% 내지 1.6%였다. CAR-T 세포로 처리된 모든 샘플에서, p27 양성은, 유동 염색 아이소타입 대조군에 가깝거나 그보다 더 낮은 0.207% 이하로 떨어졌다. 도 19B는 바이러스 RNA 및 통합된 DNA의 감소를 나타낸다. 세포 배양 상청액에서, 바이러스 역가는 UNT 세포로 처리한 샘플과 비교하여 CAR-T 세포로 처리한 샘플에서 급격하게 떨어졌다. 통합된 DNA 수준은 PCR 과정으로 인해 검출된 일부 배경 노이즈인 거의 검출할 수 없는 수준으로 떨어졌다. 이들 모든 데이터는 본 발명자의 CAR-T가 시험관내에서 SHIV 감염을 제거하는 데 매우 효율적이라는 것을 나타내었다.
본 명세서에 기재된 CAR 작제물의 생체 내 효능을 테스트하기 위해, 인간 면역계를 가지는 마우스를 사용하였다. 이에 의하여 상기 마우스를 HIS 마우스로 지칭할 것이다. 심각하게 면역손상되고 T 및 B 세포 형성이 결핍된 NOD CRISPR Prkdc IL2Rγ 마우스(NCG 마우스)로부터 HIS 마우스를 생성하였다. 신생아 NCG 마우스에 인간 조혈 줄기세포를 이식하였고 HIS 마우스로 개명하였다. 인간 조혈 세포는 마우스에서 T 및 B 세포로 발전하여 마우스에서 면역학적 틈새를 채운다. 이들 HIS 마우스는 CAR-T 세포에 대한 생체 내 테스트 모델로 사용되었다. 2가지 CAR-T 세포를 시험관내 모델인 CCR5 CAR-T(항-CCR5 CAR)(도 23A) 및 탠덤 CD4CCR5 CAR-T(항-CD4-항-CCR5 CAR)(도 23B 및 도 23C)에서 테스트하였다. UNT 세포를 대조군으로서 수용자 마우스의 별개의 그룹으로 주사하였다. 도 23A에 나타낸 바와 같이, UNT 세포 처리 마우스에서, 마우스를 UNT 세포로 접종한 후 CCR5+ 세포가 증가한 반면, 항-CCR5 CAR-T 처리 마우스에서는 관찰 기간 동안 CCR5+%가 계속 감소하였다. 관찰 기간의 종료시, 살아있는 세포 집단에서 CCR5+%는 0에 가까웠다. HIS 마우스의 또 다른 그룹은 도 23B 및 도 23C에 나타낸 바와 같이 탠덤 CD4CCR5 CAR-T로 처리하였다. CCR5+ 집단은 CAR-T 세포 처리 후 마우스 말초 혈액에서 극적으로 감소하였다. CCR5+ 집단은 말초의 살이있는 세포 집단으로부터 완전히 고갈되었다. CD4+ 집단은 또한 탠덤 CD4CCR5 CAR-T 그룹에서 원래 집단의 절반으로 감소하였다. 살아있는 세포에서 CD4+ 집단의 백분율은 CAR-T 처리 전에 약 3%였고, 관찰 기간의 종료시 1%로 감소하였다. 이들 데이터는 생체 내에서 항-CCR5 CAR-T가 말초 혈액으로부터 CCR5+ 세포를 박멸하는 데 있어서 매우 효율적이라는 것을 나타내었다. CD4+ 집단은 절반으로 감소하였고 여전히 감소하고 있었는데, 이는 CCR5+ 세포를 제거하는 것에 대한 큰 효율성 외에도, 탠덤 CD4CCR5 CAR-T는 또한 CD4+ 집단을 감소시키는 데 효과적이라는 것을 시사한다.
항-CD4 CAR-T 세포의 또 다른 적용은 CD4+ T 세포 림프종/백혈병 치료를 위한 것일 수 있다. 도 20에 나타낸 바와 같이, 상이한 투약량의 CAR-T 세포를 CD4+인 Sup-T1 및 HH T 림프아구 세포와 공동배양하였다. CAR-T 세포는 이들 종양 세포에 대하여 큰 세포독성을 나타낸 반면, UNT 대조군 세포는 종양 세포 생존력에 영향을 미치지 않았다. HH 세포를 NCG 마우스 내로 피하 이식하여 세포-유래 이종이식(CDX) 마우스 모델을 생성하였다. CAR-T 세포의 HH CDX 마우스 내로의 생체 내 접종은 CAR-T 세포가 도 21에 나타낸 바와 같이 마우스 종양 부담을 현저하게 감소시킬 수 있음을 나타내었다. CAR-T 요법을 받은 마우스는 CAR-T 접종 후 제12일에 종양이 없었다. 도 21A에 나타낸 바와 같이, 종양은 희생 기준을 충족하기 전에 행크 균형 염 용액(Hank's Balanced Salt Solution; HBSS) 완충액 또는 UNT 세포 처리 마우스에서 지속적으로 성장하였다. CAR-T 처리 마우스의 종양은 처리 후 빠르게 줄어들었고 마우스는 전체 관찰 기간 동안 생존하였다. 도 21B에서, CAR-T 처리 마우스는 아마도 더 적은 종양 부담으로 인해 HBSS 또는 UNT 처리 마우스보다 체중이 약간 덜 나갔다. 제20일쯤 질환 진행으로 인해 HBSS 또는 UNT 처리 마우스를 희생시켰으므로, 그 이후 체중 기록은 없었다.
실시예 8. 분할 CAR 시스템
분할 CAR-T 세포의 구축
본 명세서에 기재된 분할 CAR 시스템은 2가지 구성요소를 함유한다. 한가지 단백질은 세포외 항원-인식 도메인, 힌지, CD8 막관통 도메인 및 CD28 세포내 공동자극 도메인으로 구성된다. 분할 신호 CAR의 다른 단백질은 제2 항원-인식 도메인, 힌지, CD8 막관통 도메인 및 세포내 CD3제타 신호 전달 도메인으로 구성된다. 세포외 항원 인식 도메인은 하나의 구성요소에 있어서 항-CD4 scFv 또는 sdAb이고, 다른 구성요소에 있어서 항-CCR5 또는 항-CXCR4 scFv 또는 sdAb일 수 있다(도 1). 본 실시예에서, 2가지 단백질에 대한 코딩 서열을 중간에 P2A 서열과 연결하였다. 전체 코딩 서열은 pLVX 렌티바이러스 플라스미드에서 EF1α 프로모터의 제어 하에 있었다. CAR 작제물로 성공적으로 형질도입된 T 세포는 2가지 단백질을 상승적으로 발현할 것이다. T 세포는 또한 귀소 수용체를 발현할 수 있다. 귀소 수용체 중 하나는 CXCR5일 수 있으며(도 2), 이는 CXCL13 케모카인과 상호작용하고 2차 림프 기관에서 B 세포 여포로의 세포 귀소에 중요한 역할을 한다. 귀소 수용체는 또한 세포가 장으로 귀소하는 것을 돕는 상향조절된 α4β7일 수 있다(도 3).
분할 신호 CAR의 시험관내 효과
도 22는 예시적인 분할 신호 CAR-T의 시험관내 효과를 나타낸다. 이 실험에서 4가지 설계를 사용하였다. ssCD4CCR5 CAR-T에서, 항-CD4를 CD3ζ 신호전달 도메인과 연결하고 항-CCR5를 공동자극 도메인과 연결한 한편, ssCCR5CD4에서 항-CCR5 부분은 CD3제타 신호전달 도메인을 함유하고 항-CD4는 공동자극 도메인과 연결된다.
작제물은 다음 서열을 가진다:
ssCD4CCR5 CAR-T: 서열번호 26
항-CD4-CD8 힌지-CD8 TM-CD3ζ: 서열번호 27
항-CCR5-CD8 힌지-CD8 TM-4-1-BB: 서열번호 28
ssCCR5CD4 CAR-T: 서열번호 29
항-CCR5-CD8 힌지-CD8 TM-CD3ζ: 서열번호 30
항-CD4-CD8 힌지-CD8 TM-4-1-BB: 서열번호 31
ssCD4CCR5-CXCR5: 서열번호 78
ssCCR5CD4-CXCR5: 서열번호 79
2개의 모이어티를 중간에 P2A로 연결하였고, 제1 모이어티는 Myc 태그를 가졌다. Myc 발현을 도 22A에 나타낸 바와 같이 유세포 분석에 의해 검출하여 분할 신호 CAR의 발현을 나타내었다. 이들 기능을 테스트하기 위해, CFSE 표지화 팬 T 세포를 표적 세포로 사용하고 CAR-T 세포와 E:T=0.5:1로 공동인큐베이션하였다. 유세포 분석 결과는 도 23B에 도시되어 있다. 대조군 UNT 샘플에서, CD4+ 집단은 42.2%이고, CCR5+ 집단은 9.29%이며, CD4+CCR5+ 집단은 6.64%였다. ssCD4CCR5 CAR-T 및 ssCCR5CD4 CAR-T는 남아있는 CD4+CCR5+ 집단이 1% 미만인 CD4+CCR5+ 이중 양성 집단의 대부분을 사멸시켰다. ssCCR5CD4 CAR-T 샘플에서, CD4 단일 양성의 10.4% 및 CCR5 단일 양성 세포의 6.77%가 남아있었다. ssCD4CCR5 CAR-T 샘플에서 남아있는 CCR5+ 세포는 7.89%였다. ssCCR5CD4 CAR 및 ssCD4CCR5 CAR에 CXCR5의 첨가로, CAR-T 세포와 공동배양 후에도 CCR5+ 세포의 대부분을 유지하였고, CD4+ 단일 양성 세포의 약 절반이 살아 남았다. 이러한 데이터는 CD4 및 CCR5가 둘 다 동일한 세포에 존재할 때 분할 CAR이 가장 잘 작동함을 시사한다. ssCCR5CD4, ssCCR5CD4-CXCR5 및 ssCD4CCR5-CXCR5 CAR-T 세포는 다수의 CD4 단일 양성 또는 CCR5 단일 양성 세포를 남길 수 있으므로 이러한 단일 양성 세포를 사멸시키는 데 효율적이지 않았다. CCR5-친화성 HIV 감염은 동일한 세포에서 CD4 및 CCR5 둘 다의 발현을 필요로 한다. 분할 CAR은 HIV 표적 세포를 제거하지만, HIV 감염에 덜 취약한 CD4 또는 CCR5 단일 양성 세포 중 일부는 남길 수 있다.
본 발명의 실시형태에 따른 예시적인 작제물의 서열:
SEQUENCE LISTING
<110> Nanjing Legend Biotech Co., Ltd.
<120> CO-RECEPTOR SYSTEMS FOR TREATING INFECTIOUS DISEASES
<130> WO/2020/011247
<140> PCT/CN2019/095738
<141> 2019-07-12
<150> PCT/CN2018/095650
<151> 2018-07-13
<150> PCT/CN2019/087259
<151> 2019-05-16
<160> 79
<170> PatentIn version 3.5
<210> 1
<211> 458
<212> PRT
<213> Homo sapiens
<400> 1
Met Asn Arg Gly Val Pro Phe Arg His Leu Leu Leu Val Leu Gln Leu
1 5 10 15
Ala Leu Leu Pro Ala Ala Thr Gln Gly Lys Lys Val Val Leu Gly Lys
20 25 30
Lys Gly Asp Thr Val Glu Leu Thr Cys Thr Ala Ser Gln Lys Lys Ser
35 40 45
Ile Gln Phe His Trp Lys Asn Ser Asn Gln Ile Lys Ile Leu Gly Asn
50 55 60
Gln Gly Ser Phe Leu Thr Lys Gly Pro Ser Lys Leu Asn Asp Arg Ala
65 70 75 80
Asp Ser Arg Arg Ser Leu Trp Asp Gln Gly Asn Phe Pro Leu Ile Ile
85 90 95
Lys Asn Leu Lys Ile Glu Asp Ser Asp Thr Tyr Ile Cys Glu Val Glu
100 105 110
Asp Gln Lys Glu Glu Val Gln Leu Leu Val Phe Gly Leu Thr Ala Asn
115 120 125
Ser Asp Thr His Leu Leu Gln Gly Gln Ser Leu Thr Leu Thr Leu Glu
130 135 140
Ser Pro Pro Gly Ser Ser Pro Ser Val Gln Cys Arg Ser Pro Arg Gly
145 150 155 160
Lys Asn Ile Gln Gly Gly Lys Thr Leu Ser Val Ser Gln Leu Glu Leu
165 170 175
Gln Asp Ser Gly Thr Trp Thr Cys Thr Val Leu Gln Asn Gln Lys Lys
180 185 190
Val Glu Phe Lys Ile Asp Ile Val Val Leu Ala Phe Gln Lys Ala Ser
195 200 205
Ser Ile Val Tyr Lys Lys Glu Gly Glu Gln Val Glu Phe Ser Phe Pro
210 215 220
Leu Ala Phe Thr Val Glu Lys Leu Thr Gly Ser Gly Glu Leu Trp Trp
225 230 235 240
Gln Ala Glu Arg Ala Ser Ser Ser Lys Ser Trp Ile Thr Phe Asp Leu
245 250 255
Lys Asn Lys Glu Val Ser Val Lys Arg Val Thr Gln Asp Pro Lys Leu
260 265 270
Gln Met Gly Lys Lys Leu Pro Leu His Leu Thr Leu Pro Gln Ala Leu
275 280 285
Pro Gln Tyr Ala Gly Ser Gly Asn Leu Thr Leu Ala Leu Glu Ala Lys
290 295 300
Thr Gly Lys Leu His Gln Glu Val Asn Leu Val Val Met Arg Ala Thr
305 310 315 320
Gln Leu Gln Lys Asn Leu Thr Cys Glu Val Trp Gly Pro Thr Ser Pro
325 330 335
Lys Leu Met Leu Ser Leu Lys Leu Glu Asn Lys Glu Ala Lys Val Ser
340 345 350
Lys Arg Glu Lys Ala Val Trp Val Leu Asn Pro Glu Ala Gly Met Trp
355 360 365
Gln Cys Leu Leu Ser Asp Ser Gly Gln Val Leu Leu Glu Ser Asn Ile
370 375 380
Lys Val Leu Pro Thr Trp Ser Thr Pro Val Gln Pro Met Ala Leu Ile
385 390 395 400
Val Leu Gly Gly Val Ala Gly Leu Leu Leu Phe Ile Gly Leu Gly Ile
405 410 415
Phe Phe Cys Val Arg Cys Arg His Arg Arg Arg Gln Ala Glu Arg Met
420 425 430
Ser Gln Ile Lys Arg Leu Leu Ser Glu Lys Lys Thr Cys Gln Cys Pro
435 440 445
His Arg Phe Gln Lys Thr Cys Ser Pro Ile
450 455
<210> 2
<211> 45
<212> PRT
<213> Homo sapiens
<400> 2
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp
35 40 45
<210> 3
<211> 24
<212> PRT
<213> Homo sapiens
<400> 3
Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu
1 5 10 15
Ser Leu Val Ile Thr Leu Tyr Cys
20
<210> 4
<211> 42
<212> PRT
<213> Homo sapiens
<400> 4
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 5
<211> 112
<212> PRT
<213> Homo sapiens
<400> 5
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 6
<211> 207
<212> PRT
<213> Homo sapiens
<400> 6
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Asp Gly Asn Glu Glu Met Gly Gly Ile Thr
20 25 30
Gln Thr Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr
35 40 45
Cys Pro Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys
50 55 60
Asn Ile Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp
65 70 75 80
His Leu Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr
85 90 95
Val Cys Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu
100 105 110
Tyr Leu Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met
115 120 125
Ser Val Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu
130 135 140
Leu Leu Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys
145 150 155 160
Pro Val Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn
165 170 175
Lys Glu Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg
180 185 190
Lys Gly Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile
195 200 205
<210> 7
<211> 22
<212> PRT
<213> Homo sapiens
<400> 7
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln
20
<210> 8
<211> 185
<212> PRT
<213> Homo sapiens
<400> 8
Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys Val
1 5 10 15
Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro Gly
20 25 30
Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp Glu
35 40 45
Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys Glu
50 55 60
Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg Gly
65 70 75 80
Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg Val
85 90 95
Cys Glu Asn Cys Met Glu Met Asp Val Met Ser Val Ala Thr Ile Val
100 105 110
Ile Val Asp Ile Cys Ile Thr Gly Gly Leu Leu Leu Leu Val Tyr Tyr
115 120 125
Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys Pro Val Thr Arg Gly Ala
130 135 140
Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn Lys Glu Arg Pro Pro Pro
145 150 155 160
Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg Lys Gly Gln Arg Asp Leu
165 170 175
Tyr Ser Gly Leu Asn Gln Arg Arg Ile
180 185
<210> 9
<211> 372
<212> PRT
<213> Homo sapiens
<400> 9
Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu Asn Leu Glu Asp
1 5 10 15
Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn Asp Thr Ser Leu
20 25 30
Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro Leu Met Ala Ser
35 40 45
Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu Ile Phe Leu Leu
50 55 60
Gly Val Ile Gly Asn Val Leu Val Leu Val Ile Leu Glu Arg His Arg
65 70 75 80
Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His Leu Ala Val Ala
85 90 95
Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val Ala Glu Gly Ser
100 105 110
Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr Val Ile Ala Leu
115 120 125
His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala
130 135 140
Val Asp Arg Tyr Leu Ala Ile Val His Ala Val His Ala Tyr Arg His
145 150 155 160
Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val
165 170 175
Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln
180 185 190
Gly His His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn
195 200 205
Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu Tyr His Val
210 215 220
Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys Tyr Val Gly
225 230 235 240
Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln Arg Gln Lys
245 250 255
Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe Phe Leu Cys Trp
260 265 270
Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu Ala Arg Leu Lys
275 280 285
Ala Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro Val Ala Ile
290 295 300
Thr Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu Asn Pro Met
305 310 315 320
Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu Ser Arg Leu
325 330 335
Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln Leu Phe
340 345 350
Pro Ser Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser
355 360 365
Leu Thr Thr Phe
370
<210> 10
<211> 239
<212> PRT
<213> artificial sequence
<220>
<223> VRC01 scFv
<400> 10
Gln Val Gln Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu
1 5 10 15
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys
20 25 30
Thr Leu Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
35 40 45
Gly Trp Leu Lys Pro Arg Gly Gly Ala Val Asn Tyr Ala Arg Pro Leu
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Val Tyr Ser Asp Thr Ala Phe
65 70 75 80
Leu Glu Leu Arg Ser Leu Thr Val Asp Asp Thr Ala Val Tyr Phe Cys
85 90 95
Thr Arg Gly Lys Asn Cys Asp Tyr Asn Trp Asp Phe Glu His Trp Gly
100 105 110
Arg Gly Thr Pro Val Ile Val Ser Ser Gly Gly Gly Gly Ser Gly Gly
115 120 125
Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro
130 135 140
Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr Ala Ile Ile Ser Cys Arg
145 150 155 160
Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln
165 170 175
Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser Thr Arg Ala Ala Gly Ile
180 185 190
Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly Pro Asp Tyr Asn Leu Thr
195 200 205
Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly Val Tyr Tyr Cys Gln Gln
210 215 220
Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val Gln Val Asp Ile Lys
225 230 235
<210> 11
<211> 478
<212> PRT
<213> artificial sequence
<220>
<223> anti-CD4 CAR
<400> 11
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
290 295 300
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
305 310 315 320
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
325 330 335
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
340 345 350
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
355 360 365
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
370 375 380
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
385 390 395 400
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
405 410 415
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
420 425 430
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
435 440 445
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
450 455 460
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<210> 12
<211> 492
<212> PRT
<213> artificial sequence
<220>
<223> anti-CCR5 CAR
<400> 12
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Leu Ser Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr
115 120 125
Tyr Thr Ala Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
130 135 140
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu
195 200 205
Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro
245 250 255
Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 13
<211> 741
<212> PRT
<213> artificial sequence
<220>
<223> tandem antiCD4-antiCCR5 CAR
<400> 13
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly
245 250 255
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
260 265 270
Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu
275 280 285
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly Met
290 295 300
His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Leu
305 310 315 320
Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly
325 330 335
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Arg
340 345 350
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
355 360 365
Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp Val
370 375 380
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
405 410 415
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
420 425 430
Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln Gln
435 440 445
Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu
450 455 460
Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
465 470 475 480
Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr Tyr
485 490 495
Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly Thr
500 505 510
Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
515 520 525
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
530 535 540
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
545 550 555 560
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
565 570 575
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
580 585 590
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
595 600 605
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
610 615 620
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
625 630 635 640
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
645 650 655
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
660 665 670
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
675 680 685
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
690 695 700
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
705 710 715 720
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
725 730 735
Ala Leu Pro Pro Arg
740
<210> 14
<211> 872
<212> PRT
<213> artificial sequence
<220>
<223> anti-CD4 CAR with CXCR5
<400> 14
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
290 295 300
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
305 310 315 320
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
325 330 335
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
340 345 350
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
355 360 365
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
370 375 380
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
385 390 395 400
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
405 410 415
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
420 425 430
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
435 440 445
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
450 455 460
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser
465 470 475 480
Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu
485 490 495
Asn Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu
500 505 510
Asn Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn
515 520 525
Asp Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro
530 535 540
Leu Met Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu
545 550 555 560
Ile Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile Leu
565 570 575
Glu Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His
580 585 590
Leu Ala Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val
595 600 605
Ala Glu Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr
610 615 620
Val Ile Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu
625 630 635 640
Ala Cys Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val His
645 650 655
Ala Tyr Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr
660 665 670
Ile Trp Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala
675 680 685
Lys Val Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr Phe
690 695 700
Ser Gln Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe
705 710 715 720
Leu Tyr His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp
725 730 735
Cys Tyr Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro
740 745 750
Gln Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe
755 760 765
Phe Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu
770 775 780
Ala Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu
785 790 795 800
Pro Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys
805 810 815
Leu Asn Pro Met Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp
820 825 830
Leu Ser Arg Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu
835 840 845
Cys Gln Leu Phe Pro Ser Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu
850 855 860
Asn Ala Thr Ser Leu Thr Thr Phe
865 870
<210> 15
<211> 886
<212> PRT
<213> artificial sequence
<220>
<223> anti-CCR5 CAR with CXCR5
<400> 15
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Leu Ser Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr
115 120 125
Tyr Thr Ala Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
130 135 140
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu
195 200 205
Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro
245 250 255
Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser Gly Ala
485 490 495
Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro
500 505 510
Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu Asn Leu
515 520 525
Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn Asp Thr
530 535 540
Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro Leu Met
545 550 555 560
Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu Ile Phe
565 570 575
Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile Leu Glu Arg
580 585 590
His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His Leu Ala
595 600 605
Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val Ala Glu
610 615 620
Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr Val Ile
625 630 635 640
Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu Ala Cys
645 650 655
Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val His Ala Tyr
660 665 670
Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr Ile Trp
675 680 685
Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys Val
690 695 700
Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln
705 710 715 720
Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu Tyr
725 730 735
His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys Tyr
740 745 750
Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln Arg
755 760 765
Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe Phe Leu
770 775 780
Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu Ala Arg
785 790 795 800
Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro Val
805 810 815
Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu Asn
820 825 830
Pro Met Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu Ser
835 840 845
Arg Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln
850 855 860
Leu Phe Pro Ser Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn Ala
865 870 875 880
Thr Ser Leu Thr Thr Phe
885
<210> 16
<211> 1135
<212> PRT
<213> artificial sequence
<220>
<223> tandem antiCD4-antiCCR5 CAR with CXCR5
<400> 16
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly
245 250 255
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
260 265 270
Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu
275 280 285
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly Met
290 295 300
His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Leu
305 310 315 320
Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly
325 330 335
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Arg
340 345 350
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
355 360 365
Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp Val
370 375 380
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
405 410 415
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
420 425 430
Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln Gln
435 440 445
Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu
450 455 460
Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
465 470 475 480
Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr Tyr
485 490 495
Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly Thr
500 505 510
Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
515 520 525
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
530 535 540
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
545 550 555 560
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
565 570 575
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
580 585 590
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
595 600 605
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
610 615 620
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
625 630 635 640
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
645 650 655
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
660 665 670
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
675 680 685
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
690 695 700
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
705 710 715 720
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
725 730 735
Ala Leu Pro Pro Arg Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
740 745 750
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Asn Tyr Pro Leu
755 760 765
Thr Leu Glu Met Asp Leu Glu Asn Leu Glu Asp Leu Phe Trp Glu Leu
770 775 780
Asp Arg Leu Asp Asn Tyr Asn Asp Thr Ser Leu Val Glu Asn His Leu
785 790 795 800
Cys Pro Ala Thr Glu Gly Pro Leu Met Ala Ser Phe Lys Ala Val Phe
805 810 815
Val Pro Val Ala Tyr Ser Leu Ile Phe Leu Leu Gly Val Ile Gly Asn
820 825 830
Val Leu Val Leu Val Ile Leu Glu Arg His Arg Gln Thr Arg Ser Ser
835 840 845
Thr Glu Thr Phe Leu Phe His Leu Ala Val Ala Asp Leu Leu Leu Val
850 855 860
Phe Ile Leu Pro Phe Ala Val Ala Glu Gly Ser Val Gly Trp Val Leu
865 870 875 880
Gly Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His Lys Val Asn Phe
885 890 895
Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val Asp Arg Tyr Leu
900 905 910
Ala Ile Val His Ala Val His Ala Tyr Arg His Arg Arg Leu Leu Ser
915 920 925
Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly Phe Leu Leu Ala
930 935 940
Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly His His Asn Asn
945 950 955 960
Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn Gln Ala Glu Thr His
965 970 975
Ala Trp Phe Thr Ser Arg Phe Leu Tyr His Val Ala Gly Phe Leu Leu
980 985 990
Pro Met Leu Val Met Gly Trp Cys Tyr Val Gly Val Val His Arg Leu
995 1000 1005
Arg Gln Ala Gln Arg Arg Pro Gln Arg Gln Lys Ala Val Arg Val
1010 1015 1020
Ala Ile Leu Val Thr Ser Ile Phe Phe Leu Cys Trp Ser Pro Tyr
1025 1030 1035
His Ile Val Ile Phe Leu Asp Thr Leu Ala Arg Leu Lys Ala Val
1040 1045 1050
Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro Val Ala Ile Thr
1055 1060 1065
Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu Asn Pro Met
1070 1075 1080
Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu Ser Arg
1085 1090 1095
Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln
1100 1105 1110
Leu Phe Pro Gly Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn
1115 1120 1125
Ala Thr Ser Leu Thr Thr Phe
1130 1135
<210> 17
<211> 1159
<212> PRT
<213> artificial sequence
<220>
<223> anti-CD4 CAR with CXCR5 and VRC01
<400> 17
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
290 295 300
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
305 310 315 320
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
325 330 335
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
340 345 350
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
355 360 365
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
370 375 380
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
385 390 395 400
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
405 410 415
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
420 425 430
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
435 440 445
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
450 455 460
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser
465 470 475 480
Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu
485 490 495
Asn Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu
500 505 510
Asn Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn
515 520 525
Asp Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro
530 535 540
Leu Met Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu
545 550 555 560
Ile Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile Leu
565 570 575
Glu Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His
580 585 590
Leu Ala Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val
595 600 605
Ala Glu Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr
610 615 620
Val Ile Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu
625 630 635 640
Ala Cys Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val His
645 650 655
Ala Tyr Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr
660 665 670
Ile Trp Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala
675 680 685
Lys Val Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr Phe
690 695 700
Ser Gln Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe
705 710 715 720
Leu Tyr His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp
725 730 735
Cys Tyr Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro
740 745 750
Gln Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe
755 760 765
Phe Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu
770 775 780
Ala Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu
785 790 795 800
Pro Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys
805 810 815
Leu Asn Pro Met Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp
820 825 830
Leu Ser Arg Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu
835 840 845
Cys Gln Leu Phe Pro Ser Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu
850 855 860
Asn Ala Thr Ser Leu Thr Thr Phe Gly Ser Gly Ala Thr Asn Phe Ser
865 870 875 880
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Tyr
885 890 895
Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu Val Thr
900 905 910
Asn Ser Gln Val Gln Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro
915 920 925
Gly Glu Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile
930 935 940
Asp Cys Thr Leu Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu
945 950 955 960
Trp Met Gly Trp Leu Lys Pro Arg Gly Gly Ala Val Asn Tyr Ala Arg
965 970 975
Pro Leu Gln Gly Arg Val Thr Met Thr Arg Asp Val Tyr Ser Asp Thr
980 985 990
Ala Phe Leu Glu Leu Arg Ser Leu Thr Val Asp Asp Thr Ala Val Tyr
995 1000 1005
Phe Cys Thr Arg Gly Lys Asn Cys Asp Tyr Asn Trp Asp Phe Glu
1010 1015 1020
His Trp Gly Arg Gly Thr Pro Val Ile Val Ser Ser Gly Gly Gly
1025 1030 1035
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val
1040 1045 1050
Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr
1055 1060 1065
Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp
1070 1075 1080
Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser
1085 1090 1095
Gly Ser Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser
1100 1105 1110
Arg Trp Gly Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser
1115 1120 1125
Gly Asp Phe Gly Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly
1130 1135 1140
Gln Gly Thr Lys Val Gln Val Asp Ile Lys His His His His His
1145 1150 1155
His
<210> 18
<211> 1173
<212> PRT
<213> artificial sequence
<220>
<223> anti-CCR5 CAR with CXCR5 and VRC01
<400> 18
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Leu Ser Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr
115 120 125
Tyr Thr Ala Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
130 135 140
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu
195 200 205
Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro
245 250 255
Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser Gly Ala
485 490 495
Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro
500 505 510
Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu Asn Leu
515 520 525
Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn Asp Thr
530 535 540
Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro Leu Met
545 550 555 560
Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu Ile Phe
565 570 575
Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile Leu Glu Arg
580 585 590
His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His Leu Ala
595 600 605
Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val Ala Glu
610 615 620
Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr Val Ile
625 630 635 640
Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu Ala Cys
645 650 655
Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val His Ala Tyr
660 665 670
Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr Ile Trp
675 680 685
Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys Val
690 695 700
Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln
705 710 715 720
Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu Tyr
725 730 735
His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys Tyr
740 745 750
Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln Arg
755 760 765
Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe Phe Leu
770 775 780
Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu Ala Arg
785 790 795 800
Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro Val
805 810 815
Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu Asn
820 825 830
Pro Met Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu Ser
835 840 845
Arg Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln
850 855 860
Leu Phe Pro Ser Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn Ala
865 870 875 880
Thr Ser Leu Thr Thr Phe Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
885 890 895
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Tyr Arg Met
900 905 910
Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu Val Thr Asn Ser
915 920 925
Gln Val Gln Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu
930 935 940
Ser Met Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys
945 950 955 960
Thr Leu Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
965 970 975
Gly Trp Leu Lys Pro Arg Gly Gly Ala Val Asn Tyr Ala Arg Pro Leu
980 985 990
Gln Gly Arg Val Thr Met Thr Arg Asp Val Tyr Ser Asp Thr Ala Phe
995 1000 1005
Leu Glu Leu Arg Ser Leu Thr Val Asp Asp Thr Ala Val Tyr Phe
1010 1015 1020
Cys Thr Arg Gly Lys Asn Cys Asp Tyr Asn Trp Asp Phe Glu His
1025 1030 1035
Trp Gly Arg Gly Thr Pro Val Ile Val Ser Ser Gly Gly Gly Gly
1040 1045 1050
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu
1055 1060 1065
Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu Thr Ala
1070 1075 1080
Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala Trp Tyr
1085 1090 1095
Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr Ser Gly
1100 1105 1110
Ser Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly Ser Arg
1115 1120 1125
Trp Gly Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu Ser Gly
1130 1135 1140
Asp Phe Gly Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe Gly Gln
1145 1150 1155
Gly Thr Lys Val Gln Val Asp Ile Lys His His His His His His
1160 1165 1170
<210> 19
<211> 1422
<212> PRT
<213> artificial sequence
<220>
<223> tandem antiCD4-antiCCR5 CAR with CXCR5 and VRC01
<400> 19
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly
245 250 255
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
260 265 270
Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu
275 280 285
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly Met
290 295 300
His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Leu
305 310 315 320
Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly
325 330 335
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Arg
340 345 350
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
355 360 365
Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp Val
370 375 380
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
385 390 395 400
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
405 410 415
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
420 425 430
Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln Gln
435 440 445
Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu
450 455 460
Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
465 470 475 480
Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr Tyr
485 490 495
Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly Thr
500 505 510
Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
515 520 525
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
530 535 540
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
545 550 555 560
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
565 570 575
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys
580 585 590
Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr
595 600 605
Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu
610 615 620
Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro
625 630 635 640
Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly
645 650 655
Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro
660 665 670
Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr
675 680 685
Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly
690 695 700
Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln
705 710 715 720
Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln
725 730 735
Ala Leu Pro Pro Arg Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
740 745 750
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Asn Tyr Pro Leu
755 760 765
Thr Leu Glu Met Asp Leu Glu Asn Leu Glu Asp Leu Phe Trp Glu Leu
770 775 780
Asp Arg Leu Asp Asn Tyr Asn Asp Thr Ser Leu Val Glu Asn His Leu
785 790 795 800
Cys Pro Ala Thr Glu Gly Pro Leu Met Ala Ser Phe Lys Ala Val Phe
805 810 815
Val Pro Val Ala Tyr Ser Leu Ile Phe Leu Leu Gly Val Ile Gly Asn
820 825 830
Val Leu Val Leu Val Ile Leu Glu Arg His Arg Gln Thr Arg Ser Ser
835 840 845
Thr Glu Thr Phe Leu Phe His Leu Ala Val Ala Asp Leu Leu Leu Val
850 855 860
Phe Ile Leu Pro Phe Ala Val Ala Glu Gly Ser Val Gly Trp Val Leu
865 870 875 880
Gly Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His Lys Val Asn Phe
885 890 895
Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val Asp Arg Tyr Leu
900 905 910
Ala Ile Val His Ala Val His Ala Tyr Arg His Arg Arg Leu Leu Ser
915 920 925
Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly Phe Leu Leu Ala
930 935 940
Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly His His Asn Asn
945 950 955 960
Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn Gln Ala Glu Thr His
965 970 975
Ala Trp Phe Thr Ser Arg Phe Leu Tyr His Val Ala Gly Phe Leu Leu
980 985 990
Pro Met Leu Val Met Gly Trp Cys Tyr Val Gly Val Val His Arg Leu
995 1000 1005
Arg Gln Ala Gln Arg Arg Pro Gln Arg Gln Lys Ala Val Arg Val
1010 1015 1020
Ala Ile Leu Val Thr Ser Ile Phe Phe Leu Cys Trp Ser Pro Tyr
1025 1030 1035
His Ile Val Ile Phe Leu Asp Thr Leu Ala Arg Leu Lys Ala Val
1040 1045 1050
Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro Val Ala Ile Thr
1055 1060 1065
Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu Asn Pro Met
1070 1075 1080
Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu Ser Arg
1085 1090 1095
Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln
1100 1105 1110
Leu Phe Pro Gly Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn
1115 1120 1125
Ala Thr Ser Leu Thr Thr Phe Gly Ser Gly Ala Thr Asn Phe Ser
1130 1135 1140
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met
1145 1150 1155
Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1160 1165 1170
Val Thr Asn Ser Gln Val Gln Leu Val Gln Ser Gly Gly Gln Met
1175 1180 1185
Lys Lys Pro Gly Glu Ser Met Arg Ile Ser Cys Arg Ala Ser Gly
1190 1195 1200
Tyr Glu Phe Ile Asp Cys Thr Leu Asn Trp Ile Arg Leu Ala Pro
1205 1210 1215
Gly Lys Arg Pro Glu Trp Met Gly Trp Leu Lys Pro Arg Gly Gly
1220 1225 1230
Ala Val Asn Tyr Ala Arg Pro Leu Gln Gly Arg Val Thr Met Thr
1235 1240 1245
Arg Asp Val Tyr Ser Asp Thr Ala Phe Leu Glu Leu Arg Ser Leu
1250 1255 1260
Thr Val Asp Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys Asn
1265 1270 1275
Cys Asp Tyr Asn Trp Asp Phe Glu His Trp Gly Arg Gly Thr Pro
1280 1285 1290
Val Ile Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1295 1300 1305
Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr
1310 1315 1320
Leu Ser Leu Ser Pro Gly Glu Thr Ala Ile Ile Ser Cys Arg Thr
1325 1330 1335
Ser Gln Tyr Gly Ser Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln
1340 1345 1350
Ala Pro Arg Leu Val Ile Tyr Ser Gly Ser Thr Arg Ala Ala Gly
1355 1360 1365
Ile Pro Asp Arg Phe Ser Gly Ser Arg Trp Gly Pro Asp Tyr Asn
1370 1375 1380
Leu Thr Ile Ser Asn Leu Glu Ser Gly Asp Phe Gly Val Tyr Tyr
1385 1390 1395
Cys Gln Gln Tyr Glu Phe Phe Gly Gln Gly Thr Lys Val Gln Val
1400 1405 1410
Asp Ile Lys His His His His His His
1415 1420
<210> 20
<211> 456
<212> PRT
<213> artificial sequence
<220>
<223> anti-CD4 eTCR
<400> 20
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Gln Gln Trp Gly Ala Gly
20 25 30
Leu Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly
35 40 45
Gly Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser
85 90 95
Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val
145 150 155 160
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
165 170 175
Asp Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala
180 185 190
Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
195 200 205
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
210 215 220
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala
225 230 235 240
Asn Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250 255
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
260 265 270
Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys Val Ser
275 280 285
Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro Gly Ser
290 295 300
Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp Glu Asp
305 310 315 320
Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys Glu Phe
325 330 335
Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg Gly Ser
340 345 350
Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg Val Cys
355 360 365
Glu Asn Cys Met Glu Met Asp Val Met Ser Val Ala Thr Ile Val Ile
370 375 380
Val Asp Ile Cys Ile Thr Gly Gly Leu Leu Leu Leu Val Tyr Tyr Trp
385 390 395 400
Ser Lys Asn Arg Lys Ala Lys Ala Lys Pro Val Thr Arg Gly Ala Gly
405 410 415
Ala Gly Gly Arg Gln Arg Gly Gln Asn Lys Glu Arg Pro Pro Pro Val
420 425 430
Pro Asn Pro Asp Tyr Glu Pro Ile Arg Lys Gly Gln Arg Asp Leu Tyr
435 440 445
Ser Gly Leu Asn Gln Arg Arg Ile
450 455
<210> 21
<211> 462
<212> PRT
<213> artificial sequence
<220>
<223> anti-CCR5 eTCR
<400> 21
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Lys Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Asn Thr Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Asn Lys Ser Asn Asn Tyr
65 70 75 80
Ala Thr Tyr Tyr Ala Ala Ser Val Lys Asp Arg Phe Thr Ile Ser Arg
85 90 95
Asp Asp Ser Gln Ser Met Leu Tyr Leu Gln Met Asn Asn Leu Lys Thr
100 105 110
Glu Asp Thr Ala Met Tyr Tyr Cys Val Ser Leu Gly Glu Phe Ala Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
145 150 155 160
Ser Pro Thr Thr Met Ala Ala Ser Pro Gly Glu Lys Val Thr Ile Thr
165 170 175
Cys Ser Ala Thr Ser Thr Ile Asn Ser Asn Tyr Leu His Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Phe Ser Pro Lys Leu Leu Ile Tyr Arg Thr Ser Asn
195 200 205
Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Ser Tyr Ser Leu Thr Ile Gly Thr Met Glu Ala Glu Asp Val Ala Thr
225 230 235 240
Tyr Tyr Cys Gln Gln Gly Ser Thr Leu Pro Phe Thr Phe Gly Ser Gly
245 250 255
Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln
275 280 285
Thr Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys
290 295 300
Pro Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn
305 310 315 320
Ile Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His
325 330 335
Leu Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val
340 345 350
Cys Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr
355 360 365
Leu Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met Ser
370 375 380
Val Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu Leu
385 390 395 400
Leu Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys Pro
405 410 415
Val Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn Lys
420 425 430
Glu Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg Lys
435 440 445
Gly Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile
450 455 460
<210> 22
<211> 850
<212> PRT
<213> artificial sequence
<220>
<223> anti-CD4 eTCR with CXCR5
<400> 22
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Gln Gln Trp Gly Ala Gly
20 25 30
Leu Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly
35 40 45
Gly Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser
85 90 95
Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val
145 150 155 160
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
165 170 175
Asp Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala
180 185 190
Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
195 200 205
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
210 215 220
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala
225 230 235 240
Asn Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250 255
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
260 265 270
Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys Val Ser
275 280 285
Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro Gly Ser
290 295 300
Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp Glu Asp
305 310 315 320
Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys Glu Phe
325 330 335
Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg Gly Ser
340 345 350
Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg Val Cys
355 360 365
Glu Asn Cys Met Glu Met Asp Val Met Ser Val Ala Thr Ile Val Ile
370 375 380
Val Asp Ile Cys Ile Thr Gly Gly Leu Leu Leu Leu Val Tyr Tyr Trp
385 390 395 400
Ser Lys Asn Arg Lys Ala Lys Ala Lys Pro Val Thr Arg Gly Ala Gly
405 410 415
Ala Gly Gly Arg Gln Arg Gly Gln Asn Lys Glu Arg Pro Pro Pro Val
420 425 430
Pro Asn Pro Asp Tyr Glu Pro Ile Arg Lys Gly Gln Arg Asp Leu Tyr
435 440 445
Ser Gly Leu Asn Gln Arg Arg Ile Gly Ser Gly Ala Thr Asn Phe Ser
450 455 460
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Asn
465 470 475 480
Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu Asn Leu Glu Asp Leu Phe
485 490 495
Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn Asp Thr Ser Leu Val Glu
500 505 510
Asn His Leu Cys Pro Ala Thr Glu Gly Pro Leu Met Ala Ser Phe Lys
515 520 525
Ala Val Phe Val Pro Val Ala Tyr Ser Leu Ile Phe Leu Leu Gly Val
530 535 540
Ile Gly Asn Val Leu Val Leu Val Ile Leu Glu Arg His Arg Gln Thr
545 550 555 560
Arg Ser Ser Thr Glu Thr Phe Leu Phe His Leu Ala Val Ala Asp Leu
565 570 575
Leu Leu Val Phe Ile Leu Pro Phe Ala Val Ala Glu Gly Ser Val Gly
580 585 590
Trp Val Leu Gly Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His Lys
595 600 605
Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val Asp
610 615 620
Arg Tyr Leu Ala Ile Val His Ala Val His Ala Tyr Arg His Arg Arg
625 630 635 640
Leu Leu Ser Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly Phe
645 650 655
Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly His
660 665 670
His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn Gln Ala
675 680 685
Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu Tyr His Val Ala Gly
690 695 700
Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys Tyr Val Gly Val Val
705 710 715 720
His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln Arg Gln Lys Ala Val
725 730 735
Arg Val Ala Ile Leu Val Thr Ser Ile Phe Phe Leu Cys Trp Ser Pro
740 745 750
Tyr His Ile Val Ile Phe Leu Asp Thr Leu Ala Arg Leu Lys Ala Val
755 760 765
Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro Val Ala Ile Thr Met
770 775 780
Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu Asn Pro Met Leu Tyr
785 790 795 800
Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu Ser Arg Leu Leu Thr
805 810 815
Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro Gly
820 825 830
Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu Thr
835 840 845
Thr Phe
850
<210> 23
<211> 864
<212> PRT
<213> artificial sequence
<220>
<223> anti-CCR5 eTCR with CXCR5
<400> 23
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Val Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Leu Ser Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys
65 70 75 80
Tyr Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp
85 90 95
Ser Lys Asn Thr Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly
115 120 125
Tyr Tyr Thr Ala Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg
180 185 190
Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu
195 200 205
Leu Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe
245 250 255
Pro Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Gly Gly
260 265 270
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Gly Asn
275 280 285
Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys Val Ser Ile Ser
290 295 300
Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro Gly Ser Glu Ile
305 310 315 320
Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp Glu Asp Asp Lys
325 330 335
Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys Glu Phe Ser Glu
340 345 350
Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg Gly Ser Lys Pro
355 360 365
Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg Val Cys Glu Asn
370 375 380
Cys Met Glu Met Asp Val Met Ser Val Ala Thr Ile Val Ile Val Asp
385 390 395 400
Ile Cys Ile Thr Gly Gly Leu Leu Leu Leu Val Tyr Tyr Trp Ser Lys
405 410 415
Asn Arg Lys Ala Lys Ala Lys Pro Val Thr Arg Gly Ala Gly Ala Gly
420 425 430
Gly Arg Gln Arg Gly Gln Asn Lys Glu Arg Pro Pro Pro Val Pro Asn
435 440 445
Pro Asp Tyr Glu Pro Ile Arg Lys Gly Gln Arg Asp Leu Tyr Ser Gly
450 455 460
Leu Asn Gln Arg Arg Ile Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
465 470 475 480
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Asn Tyr Pro
485 490 495
Leu Thr Leu Glu Met Asp Leu Glu Asn Leu Glu Asp Leu Phe Trp Glu
500 505 510
Leu Asp Arg Leu Asp Asn Tyr Asn Asp Thr Ser Leu Val Glu Asn His
515 520 525
Leu Cys Pro Ala Thr Glu Gly Pro Leu Met Ala Ser Phe Lys Ala Val
530 535 540
Phe Val Pro Val Ala Tyr Ser Leu Ile Phe Leu Leu Gly Val Ile Gly
545 550 555 560
Asn Val Leu Val Leu Val Ile Leu Glu Arg His Arg Gln Thr Arg Ser
565 570 575
Ser Thr Glu Thr Phe Leu Phe His Leu Ala Val Ala Asp Leu Leu Leu
580 585 590
Val Phe Ile Leu Pro Phe Ala Val Ala Glu Gly Ser Val Gly Trp Val
595 600 605
Leu Gly Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His Lys Val Asn
610 615 620
Phe Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val Asp Arg Tyr
625 630 635 640
Leu Ala Ile Val His Ala Val His Ala Tyr Arg His Arg Arg Leu Leu
645 650 655
Ser Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly Phe Leu Leu
660 665 670
Ala Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly His His Asn
675 680 685
Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn Gln Ala Glu Thr
690 695 700
His Ala Trp Phe Thr Ser Arg Phe Leu Tyr His Val Ala Gly Phe Leu
705 710 715 720
Leu Pro Met Leu Val Met Gly Trp Cys Tyr Val Gly Val Val His Arg
725 730 735
Leu Arg Gln Ala Gln Arg Arg Pro Gln Arg Gln Lys Ala Val Arg Val
740 745 750
Ala Ile Leu Val Thr Ser Ile Phe Phe Leu Cys Trp Ser Pro Tyr His
755 760 765
Ile Val Ile Phe Leu Asp Thr Leu Ala Arg Leu Lys Ala Val Asp Asn
770 775 780
Thr Cys Lys Leu Asn Gly Ser Leu Pro Val Ala Ile Thr Met Cys Glu
785 790 795 800
Phe Leu Gly Leu Ala His Cys Cys Leu Asn Pro Met Leu Tyr Thr Phe
805 810 815
Ala Gly Val Lys Phe Arg Ser Asp Leu Ser Arg Leu Leu Thr Lys Leu
820 825 830
Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro Gly Trp Arg
835 840 845
Arg Ser Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu Thr Thr Phe
850 855 860
<210> 24
<211> 1113
<212> PRT
<213> artificial sequence
<220>
<223> tandem antiCD4-anti-CCR5 eTCR with CXCR5
<400> 24
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Gln Gln Trp Gly Ala Gly
20 25 30
Leu Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly
35 40 45
Gly Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser
85 90 95
Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val
145 150 155 160
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
165 170 175
Asp Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala
180 185 190
Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
195 200 205
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
210 215 220
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala
225 230 235 240
Asn Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250 255
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
260 265 270
Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser
275 280 285
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly
290 295 300
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
305 310 315 320
Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
325 330 335
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
340 345 350
Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
355 360 365
Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
385 390 395 400
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
405 410 415
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
420 425 430
Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln
435 440 445
Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn
450 455 460
Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
465 470 475 480
Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr
485 490 495
Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly
500 505 510
Thr Arg Leu Glu Ile Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly
515 520 525
Ser Gly Gly Gly Gly Ser Asp Gly Asn Glu Glu Met Gly Gly Ile Thr
530 535 540
Gln Thr Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr
545 550 555 560
Cys Pro Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys
565 570 575
Asn Ile Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp
580 585 590
His Leu Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr
595 600 605
Val Cys Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu
610 615 620
Tyr Leu Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met
625 630 635 640
Ser Val Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu
645 650 655
Leu Leu Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys
660 665 670
Pro Val Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn
675 680 685
Lys Glu Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg
690 695 700
Lys Gly Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile Gly
705 710 715 720
Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu
725 730 735
Glu Asn Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu
740 745 750
Glu Asn Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr
755 760 765
Asn Asp Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly
770 775 780
Pro Leu Met Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser
785 790 795 800
Leu Ile Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile
805 810 815
Leu Glu Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe
820 825 830
His Leu Ala Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala
835 840 845
Val Ala Glu Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys
850 855 860
Thr Val Ile Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu
865 870 875 880
Leu Ala Cys Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val
885 890 895
His Ala Tyr Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly
900 905 910
Thr Ile Trp Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe
915 920 925
Ala Lys Val Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr
930 935 940
Phe Ser Gln Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg
945 950 955 960
Phe Leu Tyr His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly
965 970 975
Trp Cys Tyr Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg
980 985 990
Pro Gln Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile
995 1000 1005
Phe Phe Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp
1010 1015 1020
Thr Leu Ala Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn
1025 1030 1035
Gly Ser Leu Pro Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu
1040 1045 1050
Ala His Cys Cys Leu Asn Pro Met Leu Tyr Thr Phe Ala Gly Val
1055 1060 1065
Lys Phe Arg Ser Asp Leu Ser Arg Leu Leu Thr Lys Leu Gly Cys
1070 1075 1080
Thr Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro Ser Trp Arg Arg
1085 1090 1095
Ser Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu Thr Thr Phe
1100 1105 1110
<210> 25
<211> 1400
<212> PRT
<213> artificial sequence
<220>
<223> tandem antiCD4-anti-CCR5 eTCR with CXCR5 and VRC01
<400> 25
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Gln Gln Trp Gly Ala Gly
20 25 30
Leu Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly
35 40 45
Gly Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly
50 55 60
Lys Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn
65 70 75 80
Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser
85 90 95
Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val
145 150 155 160
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
165 170 175
Asp Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala
180 185 190
Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
195 200 205
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
210 215 220
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala
225 230 235 240
Asn Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
245 250 255
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
260 265 270
Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser
275 280 285
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly
290 295 300
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
305 310 315 320
Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
325 330 335
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
340 345 350
Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
355 360 365
Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp
370 375 380
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
385 390 395 400
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
405 410 415
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
420 425 430
Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln
435 440 445
Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn
450 455 460
Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
465 470 475 480
Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr
485 490 495
Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly
500 505 510
Thr Arg Leu Glu Ile Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly
515 520 525
Ser Gly Gly Gly Gly Ser Asp Gly Asn Glu Glu Met Gly Gly Ile Thr
530 535 540
Gln Thr Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr
545 550 555 560
Cys Pro Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys
565 570 575
Asn Ile Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp
580 585 590
His Leu Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr
595 600 605
Val Cys Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu
610 615 620
Tyr Leu Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met
625 630 635 640
Ser Val Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu
645 650 655
Leu Leu Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys
660 665 670
Pro Val Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn
675 680 685
Lys Glu Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg
690 695 700
Lys Gly Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile Gly
705 710 715 720
Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu
725 730 735
Glu Asn Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu
740 745 750
Glu Asn Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr
755 760 765
Asn Asp Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly
770 775 780
Pro Leu Met Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser
785 790 795 800
Leu Ile Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile
805 810 815
Leu Glu Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe
820 825 830
His Leu Ala Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala
835 840 845
Val Ala Glu Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys
850 855 860
Thr Val Ile Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu
865 870 875 880
Leu Ala Cys Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val
885 890 895
His Ala Tyr Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly
900 905 910
Thr Ile Trp Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe
915 920 925
Ala Lys Val Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr
930 935 940
Phe Ser Gln Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg
945 950 955 960
Phe Leu Tyr His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly
965 970 975
Trp Cys Tyr Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg
980 985 990
Pro Gln Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile
995 1000 1005
Phe Phe Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp
1010 1015 1020
Thr Leu Ala Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn
1025 1030 1035
Gly Ser Leu Pro Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu
1040 1045 1050
Ala His Cys Cys Leu Asn Pro Met Leu Tyr Thr Phe Ala Gly Val
1055 1060 1065
Lys Phe Arg Ser Asp Leu Ser Arg Leu Leu Thr Lys Leu Gly Cys
1070 1075 1080
Thr Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro Ser Trp Arg Arg
1085 1090 1095
Ser Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu Thr Thr Phe
1100 1105 1110
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp
1115 1120 1125
Val Glu Glu Asn Pro Gly Pro Met Tyr Arg Met Gln Leu Leu Ser
1130 1135 1140
Cys Ile Ala Leu Ser Leu Ala Leu Val Thr Asn Ser Gln Val Gln
1145 1150 1155
Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu Ser Met
1160 1165 1170
Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys Thr
1175 1180 1185
Leu Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met
1190 1195 1200
Gly Trp Leu Lys Pro Arg Gly Gly Ala Val Asn Tyr Ala Arg Pro
1205 1210 1215
Leu Gln Gly Arg Val Thr Met Thr Arg Asp Val Tyr Ser Asp Thr
1220 1225 1230
Ala Phe Leu Glu Leu Arg Ser Leu Thr Val Asp Asp Thr Ala Val
1235 1240 1245
Tyr Phe Cys Thr Arg Gly Lys Asn Cys Asp Tyr Asn Trp Asp Phe
1250 1255 1260
Glu His Trp Gly Arg Gly Thr Pro Val Ile Val Ser Ser Gly Gly
1265 1270 1275
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile
1280 1285 1290
Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly Glu
1295 1300 1305
Thr Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr Gly Ser Leu Ala
1310 1315 1320
Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu Val Ile Tyr
1325 1330 1335
Ser Gly Ser Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe Ser Gly
1340 1345 1350
Ser Arg Trp Gly Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu Glu
1355 1360 1365
Ser Gly Asp Phe Gly Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe
1370 1375 1380
Gly Gln Gly Thr Lys Val Gln Val Asp Ile Lys His His His His
1385 1390 1395
His His
1400
<210> 26
<211> 898
<212> PRT
<213> artificial sequence
<220>
<223> split signal antiCD4-antiCCR5 CAR
<400> 26
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu Gln
20 25 30
Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu Thr
35 40 45
Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr Tyr
50 55 60
Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
65 70 75 80
Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
85 90 95
Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys
100 105 110
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
115 120 125
Val Ile Asn Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg
165 170 175
Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu Ala
180 185 190
Trp Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala
195 200 205
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
225 230 235 240
Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Val
325 330 335
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
340 345 350
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
355 360 365
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
370 375 380
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
385 390 395 400
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
405 410 415
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
420 425 430
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser
435 440 445
Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu
450 455 460
Asn Pro Gly Pro Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu
465 470 475 480
Ala Leu Leu Leu His Ala Ala Arg Pro Tyr Pro Tyr Asp Val Pro Asp
485 490 495
Tyr Ala Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro
500 505 510
Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser
515 520 525
Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
530 535 540
Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp
545 550 555 560
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
565 570 575
Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
580 585 590
Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala
595 600 605
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
610 615 620
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
625 630 635 640
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
645 650 655
Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn
660 665 670
Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp
675 680 685
Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
690 695 700
Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp
705 710 715 720
Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe
725 730 735
Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro
740 745 750
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
755 760 765
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
770 775 780
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
785 790 795 800
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg
805 810 815
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
820 825 830
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
835 840 845
Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg Lys Lys Leu Leu
850 855 860
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
865 870 875 880
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
885 890 895
Glu Leu
<210> 27
<211> 446
<212> PRT
<213> artificial sequence
<220>
<223> anti-CD4-CD8 hinge-CD8 TM-CD3┕
<400> 27
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu Gln
20 25 30
Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu Thr
35 40 45
Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr Tyr
50 55 60
Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
65 70 75 80
Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
85 90 95
Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys
100 105 110
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
115 120 125
Val Ile Asn Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg
165 170 175
Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu Ala
180 185 190
Trp Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala
195 200 205
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
225 230 235 240
Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Val
325 330 335
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
340 345 350
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
355 360 365
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
370 375 380
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
385 390 395 400
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
405 410 415
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
420 425 430
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
435 440 445
<210> 28
<211> 430
<212> PRT
<213> artificial sequence
<220>
<223> anti-CCR5-CD8 hinge-CD8 TM-4-1-BB
<400> 28
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gln Val
20 25 30
Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser Leu
35 40 45
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly Met
50 55 60
His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Leu
65 70 75 80
Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys Gly
85 90 95
Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu Arg
100 105 110
Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
115 120 125
Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp Val
130 135 140
Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly Ser
145 150 155 160
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr Gln
165 170 175
Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr
180 185 190
Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln Gln
195 200 205
Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu
210 215 220
Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
225 230 235 240
Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr Tyr
245 250 255
Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly Thr
260 265 270
Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr
275 280 285
Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala
290 295 300
Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe
305 310 315 320
Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val
325 330 335
Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Ser Lys Arg Ser
340 345 350
Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg Pro Gly
355 360 365
Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp Phe Ala
370 375 380
Ala Tyr Arg Ser Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
385 390 395 400
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
405 410 415
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
420 425 430
<210> 29
<211> 898
<212> PRT
<213> artificial sequence
<220>
<223> split signal antiCCR5-antiCD4 CAR
<400> 29
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu Gln
20 25 30
Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser
35 40 45
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly
50 55 60
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
65 70 75 80
Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
85 90 95
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
100 105 110
Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
115 120 125
Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp
130 135 140
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
165 170 175
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
180 185 190
Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln
195 200 205
Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn
210 215 220
Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
225 230 235 240
Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr
245 250 255
Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly
260 265 270
Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro
275 280 285
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
290 295 300
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
305 310 315 320
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
325 330 335
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Val Lys Phe
340 345 350
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
355 360 365
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
370 375 380
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
385 390 395 400
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
405 410 415
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
420 425 430
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
435 440 445
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser Gly Ala
450 455 460
Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro
465 470 475 480
Gly Pro Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu
485 490 495
Leu Leu His Ala Ala Arg Pro Tyr Pro Tyr Asp Val Pro Asp Tyr Ala
500 505 510
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
515 520 525
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
530 535 540
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
545 550 555 560
Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
565 570 575
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
580 585 590
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
595 600 605
Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr
610 615 620
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
625 630 635 640
Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp
645 650 655
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu
660 665 670
Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
675 680 685
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
690 695 700
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
705 710 715 720
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Tyr Thr
725 730 735
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
740 745 750
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
755 760 765
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
770 775 780
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
785 790 795 800
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg
805 810 815
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
820 825 830
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
835 840 845
Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg Lys Lys Leu Leu
850 855 860
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
865 870 875 880
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
885 890 895
Glu Leu
<210> 30
<211> 460
<212> PRT
<213> artificial sequence
<220>
<223> anti-CCR5-CD8 hinge-CD8 TM-CD3┕
<400> 30
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu Gln
20 25 30
Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser
35 40 45
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly
50 55 60
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
65 70 75 80
Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
85 90 95
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
100 105 110
Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
115 120 125
Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp
130 135 140
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
165 170 175
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
180 185 190
Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln
195 200 205
Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn
210 215 220
Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
225 230 235 240
Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr
245 250 255
Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly
260 265 270
Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro
275 280 285
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
290 295 300
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
305 310 315 320
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
325 330 335
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Val Lys Phe
340 345 350
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
355 360 365
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
370 375 380
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
385 390 395 400
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
405 410 415
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
420 425 430
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
435 440 445
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
450 455 460
<210> 31
<211> 416
<212> PRT
<213> artificial sequence
<220>
<223> anti-CD4-CD8 hinge-CD8 TM-4-1-BB
<400> 31
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Tyr Pro Tyr Asp Val Pro Asp Tyr Ala Gln Val
20 25 30
Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu Thr Leu
35 40 45
Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr Tyr Trp
50 55 60
Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly Glu
65 70 75 80
Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg
85 90 95
Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu
100 105 110
Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Val
115 120 125
Ile Asn Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Gly Gly
130 135 140
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln
145 150 155 160
Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg Val
165 170 175
Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu Ala Trp
180 185 190
Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala Ala
195 200 205
Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
210 215 220
Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe
225 230 235 240
Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Tyr Thr Phe Gly
245 250 255
Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg Pro
260 265 270
Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro
275 280 285
Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu
290 295 300
Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys
305 310 315 320
Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Ser Lys
325 330 335
Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro Arg Arg
340 345 350
Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro Arg Asp
355 360 365
Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
370 375 380
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
385 390 395 400
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
405 410 415
<210> 32
<211> 746
<212> PRT
<213> artificial sequence
<220>
<223> tandem antiCCR5-VRC01 CAR
<400> 32
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Leu Ser Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr
115 120 125
Tyr Thr Ala Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
130 135 140
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu
195 200 205
Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro
245 250 255
Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Gly Gly Gly
260 265 270
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val Gln Leu
275 280 285
Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu Ser Met Arg Ile
290 295 300
Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys Thr Leu Asn Trp
305 310 315 320
Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met Gly Trp Leu Lys
325 330 335
Pro Arg Gly Gly Ala Val Asn Tyr Ala Arg Pro Leu Gln Gly Arg Val
340 345 350
Thr Met Thr Arg Asp Val Tyr Ser Asp Thr Ala Phe Leu Glu Leu Arg
355 360 365
Ser Leu Thr Val Asp Asp Thr Ala Val Tyr Phe Cys Thr Arg Gly Lys
370 375 380
Asn Cys Asp Tyr Asn Trp Asp Phe Glu His Trp Gly Arg Gly Thr Pro
385 390 395 400
Val Ile Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
405 410 415
Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser
420 425 430
Leu Ser Pro Gly Glu Thr Ala Ile Ile Ser Cys Arg Thr Ser Gln Tyr
435 440 445
Gly Ser Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro Arg Leu
450 455 460
Val Ile Tyr Ser Gly Ser Thr Arg Ala Ala Gly Ile Pro Asp Arg Phe
465 470 475 480
Ser Gly Ser Arg Trp Gly Pro Asp Tyr Asn Leu Thr Ile Ser Asn Leu
485 490 495
Glu Ser Gly Asp Phe Gly Val Tyr Tyr Cys Gln Gln Tyr Glu Phe Phe
500 505 510
Gly Gln Gly Thr Lys Val Gln Val Asp Ile Lys Thr Thr Thr Pro Ala
515 520 525
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
530 535 540
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
545 550 555 560
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
565 570 575
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
580 585 590
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
595 600 605
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
610 615 620
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
625 630 635 640
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
645 650 655
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
660 665 670
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
675 680 685
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
690 695 700
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
705 710 715 720
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
725 730 735
Ala Leu His Met Gln Ala Leu Pro Pro Arg
740 745
<210> 33
<211> 732
<212> PRT
<213> artificial sequence
<220>
<223> tandem antiCD4-VRC01 CAR
<400> 33
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Gly
245 250 255
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
260 265 270
Gln Leu Val Gln Ser Gly Gly Gln Met Lys Lys Pro Gly Glu Ser Met
275 280 285
Arg Ile Ser Cys Arg Ala Ser Gly Tyr Glu Phe Ile Asp Cys Thr Leu
290 295 300
Asn Trp Ile Arg Leu Ala Pro Gly Lys Arg Pro Glu Trp Met Gly Trp
305 310 315 320
Leu Lys Pro Arg Gly Gly Ala Val Asn Tyr Ala Arg Pro Leu Gln Gly
325 330 335
Arg Val Thr Met Thr Arg Asp Val Tyr Ser Asp Thr Ala Phe Leu Glu
340 345 350
Leu Arg Ser Leu Thr Val Asp Asp Thr Ala Val Tyr Phe Cys Thr Arg
355 360 365
Gly Lys Asn Cys Asp Tyr Asn Trp Asp Phe Glu His Trp Gly Arg Gly
370 375 380
Thr Pro Val Ile Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
385 390 395 400
Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln Ser Pro Gly Thr
405 410 415
Leu Ser Leu Ser Pro Gly Glu Thr Ala Ile Ile Ser Cys Arg Thr Ser
420 425 430
Gln Tyr Gly Ser Leu Ala Trp Tyr Gln Gln Arg Pro Gly Gln Ala Pro
435 440 445
Arg Leu Val Ile Tyr Ser Gly Ser Thr Arg Ala Ala Gly Ile Pro Asp
450 455 460
Arg Phe Ser Gly Ser Arg Trp Gly Pro Asp Tyr Asn Leu Thr Ile Ser
465 470 475 480
Asn Leu Glu Ser Gly Asp Phe Gly Val Tyr Tyr Cys Gln Gln Tyr Glu
485 490 495
Phe Phe Gly Gln Gly Thr Lys Val Gln Val Asp Ile Lys Thr Thr Thr
500 505 510
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
515 520 525
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
530 535 540
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
545 550 555 560
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
565 570 575
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
580 585 590
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
595 600 605
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
610 615 620
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
625 630 635 640
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
645 650 655
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
660 665 670
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
675 680 685
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
690 695 700
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
705 710 715 720
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
725 730
<210> 34
<211> 20
<212> PRT
<213> Homo sapiens
<400> 34
Met Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1 5 10 15
Val Thr Asn Ser
20
<210> 35
<211> 492
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 1
<400> 35
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Lys Glu Ser Gly Pro Thr Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Leu Ser Gly Phe
35 40 45
Ser Leu Ser Thr Ser Gly Val Ser Val Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Ser Ile Asn Trp Asn Asp Asp Lys
65 70 75 80
Cys Tyr Ser Pro Ser Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr
85 90 95
Pro Lys Asn Gln Val Val Leu Ala Met Ser Asn Met Asp Pro Ala Asp
100 105 110
Thr Ala Thr Tyr Ser Cys Ala Leu Asp Met Pro Pro His Asp Ser Gly
115 120 125
Pro Gln Ser Phe Asp Ala Ser Asp Val Trp Gly Pro Gly Thr Met Val
130 135 140
Thr Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
145 150 155 160
Gly Gly Ser Ser Tyr Glu Leu Met Gln Leu Pro Ser Val Ser Val Ser
165 170 175
Pro Gly Gln Thr Ala Ser Ile Thr Cys Ser Gly Asp Asn Leu Gly Asp
180 185 190
Lys Tyr Ala Cys Trp Tyr Gln Gln Lys Pro Gly Arg Ser Pro Val Leu
195 200 205
Val Ile Tyr Gly Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu Arg Phe
210 215 220
Ser Gly Ser Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser Gly Thr
225 230 235 240
Gln Ala Met Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp Asp Thr Ser
245 250 255
Thr Ala Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 36
<211> 492
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 2
<400> 36
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Tyr Glu Leu Met Gln Leu Pro Ser Val Ser
20 25 30
Val Ser Pro Gly Gln Thr Ala Ser Ile Thr Cys Ser Gly Asp Asn Leu
35 40 45
Gly Asp Lys Tyr Ala Cys Trp Tyr Gln Gln Lys Pro Gly Arg Ser Pro
50 55 60
Val Leu Val Ile Tyr Gly Asp Asn Lys Arg Pro Ser Gly Ile Pro Glu
65 70 75 80
Arg Phe Ser Gly Ser Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Ser
85 90 95
Gly Thr Gln Ala Met Asp Glu Ala Asp Tyr Tyr Cys Gln Ala Trp Asp
100 105 110
Thr Ser Thr Ala Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
130 135 140
Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln Thr Leu
145 150 155 160
Thr Leu Thr Cys Thr Leu Ser Gly Phe Ser Leu Ser Thr Ser Gly Val
165 170 175
Ser Val Gly Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
180 185 190
Ala Ser Ile Asn Trp Asn Asp Asp Lys Cys Tyr Ser Pro Ser Leu Lys
195 200 205
Ser Arg Leu Thr Ile Thr Lys Asp Thr Pro Lys Asn Gln Val Val Leu
210 215 220
Ala Met Ser Asn Met Asp Pro Ala Asp Thr Ala Thr Tyr Ser Cys Ala
225 230 235 240
Leu Asp Met Pro Pro His Asp Ser Gly Pro Gln Ser Phe Asp Ala Ser
245 250 255
Asp Val Trp Gly Pro Gly Thr Met Val Thr Val Ser Ser Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 37
<211> 493
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 3
<400> 37
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Gly His Asp Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Glu
50 55 60
Gly Leu Glu Trp Ile Gly Phe Ile Phe Phe Asp Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Asn Gly Arg Val Thr Ile Ser Leu Asp Thr Ser Lys
85 90 95
Asn Gln Leu Ser Leu Arg Leu Thr Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Phe Cys Ala Arg Leu Lys Gly Ala Trp Leu Leu Ser Glu Pro
115 120 125
Pro Tyr Phe Ser Ser Asp Gly Met Asp Val Trp Gly Gln Gly Thr Thr
130 135 140
Val Thr Val Pro Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
145 150 155 160
Gly Gly Gly Ser Asn Phe Met Leu Thr Gln Pro Pro Ser Ala Ser Gly
165 170 175
Thr Pro Gly Gln Arg Val Ser Ile Ser Cys Ser Gly Ser Ser Ser Asp
180 185 190
Ile Gly Ser Asn Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr Ala
195 200 205
Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Phe Lys Ser Gly Thr Ser Ala Ser Leu Val Ile
225 230 235 240
Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp
245 250 255
Asp Glu Ser Leu Asn Gly Val Val Phe Gly Gly Gly Pro Arg Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 38
<211> 493
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 4
<400> 38
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Phe Met Leu Thr Gln Pro Pro Ser Ala Ser
20 25 30
Gly Thr Pro Gly Gln Arg Val Ser Ile Ser Cys Ser Gly Ser Ser Ser
35 40 45
Asp Ile Gly Ser Asn Thr Val Asn Trp Tyr Gln Gln Leu Pro Gly Thr
50 55 60
Ala Pro Lys Leu Leu Ile Tyr Ser Asn Asn Gln Arg Pro Ser Gly Val
65 70 75 80
Pro Asp Arg Phe Ser Gly Phe Lys Ser Gly Thr Ser Ala Ser Leu Val
85 90 95
Ile Ser Gly Leu Gln Ser Glu Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
100 105 110
Trp Asp Glu Ser Leu Asn Gly Val Val Phe Gly Gly Gly Pro Arg Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Val
130 135 140
Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu
145 150 155 160
Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Gly His Asp Tyr Trp
165 170 175
Ser Trp Ile Arg Gln Pro Pro Gly Glu Gly Leu Glu Trp Ile Gly Phe
180 185 190
Ile Phe Phe Asp Gly Ser Thr Asn Tyr Asn Pro Ser Leu Asn Gly Arg
195 200 205
Val Thr Ile Ser Leu Asp Thr Ser Lys Asn Gln Leu Ser Leu Arg Leu
210 215 220
Thr Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Phe Cys Ala Arg Leu
225 230 235 240
Lys Gly Ala Trp Leu Leu Ser Glu Pro Pro Tyr Phe Ser Ser Asp Gly
245 250 255
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Pro Ser Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 39
<211> 489
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 5
<400> 39
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Ser Trp Gly Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Ala
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Arg Gly Ser Thr Thr Tyr
65 70 75 80
Asn Pro Ser Leu Asp Gly Arg Val Thr Ile Ser Leu Asp Thr Ser Thr
85 90 95
Asn Gln Ile Ser Leu Lys Leu Thr Ser Met Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Thr Val Ala Gly Thr Ser Asp Tyr Trp Gly
115 120 125
Gln Gly Thr Leu Val Thr Val Ser Ser Gly Ser Ala Ser Ala Pro Thr
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Lys
145 150 155 160
Thr Thr Leu Thr Gln Ser Pro Ala Phe Met Ser Ala Thr Pro Gly Asp
165 170 175
Lys Val Ser Ile Ser Cys Lys Ala Ser Arg Asp Val Asp Asp Asp Val
180 185 190
Asn Trp Tyr Gln Gln Arg Pro Gly Glu Ala Pro Ile Phe Ile Ile Glu
195 200 205
Asp Ala Thr Thr Leu Val Pro Gly Ile Ser Pro Arg Phe Ser Gly Ser
210 215 220
Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Asn Asn Ile Asp Ser Glu
225 230 235 240
Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His Asp Asn Phe Pro Leu Thr
245 250 255
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 40
<211> 489
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 6
<400> 40
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Lys Thr Thr Leu Thr Gln Ser Pro Ala Phe Met
20 25 30
Ser Ala Thr Pro Gly Asp Lys Val Ser Ile Ser Cys Lys Ala Ser Arg
35 40 45
Asp Val Asp Asp Asp Val Asn Trp Tyr Gln Gln Arg Pro Gly Glu Ala
50 55 60
Pro Ile Phe Ile Ile Glu Asp Ala Thr Thr Leu Val Pro Gly Ile Ser
65 70 75 80
Pro Arg Phe Ser Gly Ser Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Asn Asn Ile Asp Ser Glu Asp Ala Ala Tyr Tyr Phe Cys Leu Gln His
100 105 110
Asp Asn Phe Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Ser Trp Gly Thr
145 150 155 160
Leu Ser Leu Thr Cys Ala Val Ser Gly Ala Ser Phe Ser Gly Tyr Tyr
165 170 175
Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Glu Ile Asn His Arg Gly Ser Thr Thr Tyr Asn Pro Ser Leu Asp Gly
195 200 205
Arg Val Thr Ile Ser Leu Asp Thr Ser Thr Asn Gln Ile Ser Leu Lys
210 215 220
Leu Thr Ser Met Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
225 230 235 240
Thr Val Ala Gly Thr Ser Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr
245 250 255
Val Ser Ser Gly Ser Ala Ser Ala Pro Thr Thr Thr Thr Pro Ala Pro
260 265 270
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
275 280 285
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
290 295 300
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
305 310 315 320
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys
325 330 335
Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg
340 345 350
Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro
355 360 365
Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser
370 375 380
Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu
385 390 395 400
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
405 410 415
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
420 425 430
Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr
435 440 445
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
450 455 460
Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala
465 470 475 480
Leu His Met Gln Ala Leu Pro Pro Arg
485
<210> 41
<211> 492
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 7
<400> 41
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Thr Leu Lys Glu Ser Gly Pro Thr Leu
20 25 30
Val Lys Pro Thr Gln Thr Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe
35 40 45
Ser Leu Arg Thr Thr Gly Glu Gly Val Gly Trp Val Arg Gln Pro Pro
50 55 60
Gly Lys Ala Leu Glu Trp Leu Ala Leu Ile Tyr Trp Asp Asp Asp Lys
65 70 75 80
Arg Tyr Ser Pro Ser Leu Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr
85 90 95
Ser Lys Lys Gln Val Val Leu Thr Met Thr Asn Val Asp Pro Ala Asp
100 105 110
Thr Ala Thr Tyr Tyr Cys Thr His Glu Gln Tyr Tyr Tyr Asp Thr Ser
115 120 125
Gly Gln Pro Tyr Tyr Phe Asp Phe Trp Gly Gln Gly Thr Leu Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asn Ile Gln Val Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Met Thr Cys Arg Ala Ser Gln Asp Ile Arg
180 185 190
Lys Asn Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Val
195 200 205
Leu Ile Tyr Asp Ala Ser Asp Leu Glu Thr Gly Ile Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ser Asp Tyr Leu
245 250 255
Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 42
<211> 492
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 8
<400> 42
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asn Ile Gln Val Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Met Thr Cys Arg Ala Ser Gln
35 40 45
Asp Ile Arg Lys Asn Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala
50 55 60
Pro Lys Val Leu Ile Tyr Asp Ala Ser Asp Leu Glu Thr Gly Ile Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ile Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Ile Ala Thr Tyr Tyr Cys Gln Gln Ser
100 105 110
Asp Tyr Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Asp Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln Thr
145 150 155 160
Leu Thr Leu Thr Cys Thr Phe Ser Gly Phe Ser Leu Arg Thr Thr Gly
165 170 175
Glu Gly Val Gly Trp Val Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp
180 185 190
Leu Ala Leu Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Ser Pro Ser Leu
195 200 205
Lys Ser Arg Leu Thr Ile Thr Lys Asp Thr Ser Lys Lys Gln Val Val
210 215 220
Leu Thr Met Thr Asn Val Asp Pro Ala Asp Thr Ala Thr Tyr Tyr Cys
225 230 235 240
Thr His Glu Gln Tyr Tyr Tyr Asp Thr Ser Gly Gln Pro Tyr Tyr Phe
245 250 255
Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 43
<211> 468
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 9
<400> 43
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Leu Val Ala Thr Ala Thr Gly Val His Ser Gln
20 25 30
Val Gln Leu Gln Gln Pro Gly Ala Gly Arg Val Arg Pro Gly Ala Ser
35 40 45
Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr Trp
50 55 60
Met Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly
65 70 75 80
Met Ile His Pro Ser Asp Ser Glu Thr Arg Leu Asn Gln Lys Phe Asn
85 90 95
Asp Arg Ala Thr Leu Thr Val Asp Lys Tyr Ser Ser Thr Ala Tyr Ile
100 105 110
Gln Leu Ser Ser Pro Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Ala
115 120 125
Arg Gly Glu Tyr Tyr Tyr Gly Ile Phe Asp Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Ala Ser Leu Ser Ala Ser Val
145 150 155 160
Gly Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Tyr Ser
165 170 175
Tyr Leu Ala Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu
180 185 190
Val Tyr Asn Ala Lys Thr Leu Thr Glu Gly Val Pro Ser Arg Phe Ser
195 200 205
Gly Ser Gly Ser Gly Thr Gln Phe Ser Leu Lys Ile Asn Ser Leu Gln
210 215 220
Pro Glu Asp Phe Gly Asn Tyr Phe Cys Gln His His Tyr Asp Thr Pro
225 230 235 240
Arg Thr Phe Gly Gly Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
245 250 255
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
260 265 270
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
275 280 285
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
290 295 300
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
305 310 315 320
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
325 330 335
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
340 345 350
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
355 360 365
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
370 375 380
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
385 390 395 400
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
405 410 415
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
420 425 430
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
435 440 445
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
450 455 460
Leu Pro Pro Arg
465
<210> 44
<211> 468
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 10
<400> 44
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ala Ser Leu Ser Ala Ser Val Gly Glu Thr Val
20 25 30
Thr Ile Thr Cys Arg Ala Ser Glu Asn Ile Tyr Ser Tyr Leu Ala Trp
35 40 45
Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val Tyr Asn Ala
50 55 60
Lys Thr Leu Thr Glu Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser
65 70 75 80
Gly Thr Gln Phe Ser Leu Lys Ile Asn Ser Leu Gln Pro Glu Asp Phe
85 90 95
Gly Asn Tyr Phe Cys Gln His His Tyr Asp Thr Pro Arg Thr Phe Gly
100 105 110
Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
115 120 125
Leu Val Ala Thr Ala Thr Gly Val His Ser Gln Val Gln Leu Gln Gln
130 135 140
Pro Gly Ala Gly Arg Val Arg Pro Gly Ala Ser Val Lys Leu Ser Cys
145 150 155 160
Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr Trp Met Asn Trp Val Lys
165 170 175
Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Met Ile His Pro Ser
180 185 190
Asp Ser Glu Thr Arg Leu Asn Gln Lys Phe Asn Asp Arg Ala Thr Leu
195 200 205
Thr Val Asp Lys Tyr Ser Ser Thr Ala Tyr Ile Gln Leu Ser Ser Pro
210 215 220
Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Ala Arg Gly Glu Tyr Tyr
225 230 235 240
Tyr Gly Ile Phe Asp Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro
245 250 255
Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys
260 265 270
Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala
275 280 285
Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu
290 295 300
Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys
305 310 315 320
Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr
325 330 335
Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly
340 345 350
Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
355 360 365
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
370 375 380
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
385 390 395 400
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
405 410 415
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
420 425 430
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
435 440 445
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
450 455 460
Leu Pro Pro Arg
465
<210> 45
<211> 493
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 11
<400> 45
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr
35 40 45
Thr Phe Ser Asn Tyr Trp Ile Gly Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Asp Ile Tyr Pro Gly Gly Asn Tyr Ile Arg
65 70 75 80
Asn Asn Glu Lys Phe Lys Asp Lys Thr Thr Leu Ser Ala Asp Thr Ser
85 90 95
Lys Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Gly Ser Ser Phe Gly Ser Asn Tyr Val Phe Ala
115 120 125
Trp Phe Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly Glu Pro
165 170 175
Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Leu Ser Ser Tyr Gly
180 185 190
His Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro Gln
195 200 205
Leu Leu Ile Tyr Glu Val Ser Asn Arg Phe Ser Gly Val Pro Asp Arg
210 215 220
Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser Arg
225 230 235 240
Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Ser Gln Ser Thr His
245 250 255
Val Pro Leu Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 46
<211> 493
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 12
<400> 46
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu
20 25 30
Pro Val Thr Pro Gly Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln
35 40 45
Arg Leu Leu Ser Ser Tyr Gly His Thr Tyr Leu His Trp Tyr Leu Gln
50 55 60
Lys Pro Gly Gln Ser Pro Gln Leu Leu Ile Tyr Glu Val Ser Asn Arg
65 70 75 80
Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr
100 105 110
Tyr Cys Ser Gln Ser Thr His Val Pro Leu Thr Phe Gly Gln Gly Thr
115 120 125
Lys Val Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Tyr Thr
165 170 175
Phe Ser Asn Tyr Trp Ile Gly Trp Val Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Asp Ile Tyr Pro Gly Gly Asn Tyr Ile Arg Asn
195 200 205
Asn Glu Lys Phe Lys Asp Lys Thr Thr Leu Ser Ala Asp Thr Ser Lys
210 215 220
Asn Thr Ala Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Gly Ser Ser Phe Gly Ser Asn Tyr Val Phe Ala Trp
245 250 255
Phe Thr Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 47
<211> 492
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 13
<400> 47
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Leu Ser Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr
115 120 125
Tyr Thr Ala Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
130 135 140
Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val
165 170 175
Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys
180 185 190
Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu
195 200 205
Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser
210 215 220
Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln
225 230 235 240
Pro Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro
245 250 255
Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 48
<211> 492
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 CAR-T No. 14
<400> 48
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln
35 40 45
Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Val
50 55 60
Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn Leu Glu Thr Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Phe Ala Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr
100 105 110
Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
115 120 125
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
145 150 155 160
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr
165 170 175
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
180 185 190
Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
195 200 205
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr
210 215 220
Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
225 230 235 240
Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met
245 250 255
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr Thr Thr
260 265 270
Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro
275 280 285
Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val
290 295 300
His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro
305 310 315 320
Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu
325 330 335
Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro
340 345 350
Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys
355 360 365
Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe
370 375 380
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
385 390 395 400
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
405 410 415
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
420 425 430
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
435 440 445
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
450 455 460
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
465 470 475 480
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 49
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 1
<400> 49
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr
65 70 75 80
Tyr Arg Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe
115 120 125
Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ile Ser Ser His Asp Leu
180 185 190
Met Gln Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Phe Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Lys Asp Asp Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 50
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 2
<400> 50
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Ser Val Ser Ile Ser Ser His Asp Leu Met Gln Trp Tyr Gln Gln Lys
50 55 60
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Phe Asn Leu Ala
65 70 75 80
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
85 90 95
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
100 105 110
Cys Gln Gln Ser Lys Asp Asp Pro Tyr Thr Phe Gly Gln Gly Thr Lys
115 120 125
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
145 150 155 160
Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
165 170 175
Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
180 185 190
Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr Tyr Arg
195 200 205
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn
210 215 220
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Ala Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe Asp Phe
245 250 255
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 51
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 3
<400> 51
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr
65 70 75 80
Tyr Arg Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe
115 120 125
Asp Phe Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ile Ser Ser His Asp Leu
180 185 190
Met Gln Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Phe Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Lys Asp Asp Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 52
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 4
<400> 52
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Ser Val Ser Ile Ser Ser His Asp Leu Met Gln Trp Tyr Gln Gln Lys
50 55 60
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Phe Asn Leu Ala
65 70 75 80
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
85 90 95
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
100 105 110
Cys Gln Gln Ser Lys Asp Asp Pro Tyr Thr Phe Gly Gln Gly Thr Lys
115 120 125
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
145 150 155 160
Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
165 170 175
Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
180 185 190
Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr Tyr Arg
195 200 205
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn
210 215 220
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val
225 230 235 240
Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe Asp Phe
245 250 255
Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 53
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 5
<400> 53
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr
65 70 75 80
Tyr Arg Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Thr Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe
115 120 125
Asp Phe Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ile Ser Ser His Asp Leu
180 185 190
Met Gln Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Phe Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Lys Asp Asp Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 54
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 6
<400> 54
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Ser Val Ser Ile Ser Ser His Asp Leu Met Gln Trp Tyr Gln Gln Lys
50 55 60
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Phe Asn Leu Ala
65 70 75 80
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
85 90 95
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
100 105 110
Cys Gln Gln Ser Lys Asp Asp Pro Tyr Thr Phe Gly Gln Gly Thr Lys
115 120 125
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
145 150 155 160
Pro Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
165 170 175
Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
180 185 190
Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr Tyr Arg
195 200 205
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn
210 215 220
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Thr
225 230 235 240
Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe Asp Phe
245 250 255
Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 55
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 7
<400> 55
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Met Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr
65 70 75 80
Tyr Arg Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Thr Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe
115 120 125
Asp Phe Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ile Ser Ser His Asp Leu
180 185 190
Met Gln Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Phe Asn Leu Ala Ser Gly Val Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Lys Asp Asp Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 56
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 8
<400> 56
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Ser Val Ser Ile Ser Ser His Asp Leu Met Gln Trp Tyr Gln Gln Lys
50 55 60
Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Asp Ala Phe Asn Leu Ala
65 70 75 80
Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
85 90 95
Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
100 105 110
Cys Gln Gln Ser Lys Asp Asp Pro Tyr Thr Phe Gly Gln Gly Thr Lys
115 120 125
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
145 150 155 160
Pro Gly Arg Ser Met Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
165 170 175
Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
180 185 190
Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr Tyr Arg
195 200 205
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn
210 215 220
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Thr
225 230 235 240
Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe Asp Phe
245 250 255
Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 57
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 9
<400> 57
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Arg Ser Met Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Thr Phe Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr
65 70 75 80
Tyr Arg Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser
85 90 95
Lys Asn Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr
100 105 110
Ala Thr Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe
115 120 125
Asp Phe Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Gly Gly Gly
130 135 140
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Leu
145 150 155 160
Thr Gln Ser Pro Ser Ser Leu Ser Val Ser Leu Gly Asp Arg Ala Thr
165 170 175
Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Ile Ser Ser His Asp Leu
180 185 190
Met Gln Trp Tyr Gln Gln Lys Pro Gly Lys Gln Pro Lys Leu Leu Ile
195 200 205
Tyr Asp Ala Phe Asn Leu Ala Ser Gly Ile Pro Ser Arg Phe Ser Gly
210 215 220
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Pro
225 230 235 240
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Lys Asp Asp Pro Tyr
245 250 255
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 58
<211> 490
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 10
<400> 58
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Val Ser Leu Gly Asp Arg Ala Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Ser Val Ser Ile Ser Ser His Asp Leu Met Gln Trp Tyr Gln Gln Lys
50 55 60
Pro Gly Lys Gln Pro Lys Leu Leu Ile Tyr Asp Ala Phe Asn Leu Ala
65 70 75 80
Ser Gly Ile Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
85 90 95
Thr Leu Thr Ile Ser Ser Val Gln Pro Glu Asp Phe Ala Thr Tyr Tyr
100 105 110
Cys Gln Gln Ser Lys Asp Asp Pro Tyr Thr Phe Gly Gln Gly Thr Lys
115 120 125
Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln
145 150 155 160
Pro Gly Arg Ser Met Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
165 170 175
Ser Asn Tyr Gly Met Ala Trp Val Arg Gln Ala Pro Gly Lys Gly Leu
180 185 190
Glu Trp Val Ala Thr Ile Ser Tyr Asp Gly Ser Ile Thr Tyr Tyr Arg
195 200 205
Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn
210 215 220
Thr Leu Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Thr
225 230 235 240
Tyr Tyr Cys Thr Arg Glu Glu Gln Tyr Ser Ser Trp Tyr Phe Asp Phe
245 250 255
Trp Gly Gln Gly Ile Leu Val Thr Val Ser Ser Thr Thr Thr Pro Ala
260 265 270
Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser
275 280 285
Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr
290 295 300
Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala
305 310 315 320
Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys
325 330 335
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
340 345 350
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
355 360 365
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg
370 375 380
Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn
385 390 395 400
Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg
405 410 415
Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro
420 425 430
Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala
435 440 445
Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His
450 455 460
Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp
465 470 475 480
Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 59
<211> 495
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 11
<400> 59
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val
20 25 30
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Val Ile His Trp Val Arg Gln Lys Pro Gly Gln
50 55 60
Gly Leu Asp Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Asp
65 70 75 80
Tyr Asp Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Thr Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Glu Lys Asp Asn Tyr Ala Thr Gly Ala
115 120 125
Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
145 150 155 160
Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly Glu
165 170 175
Arg Val Thr Met Asn Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser Thr
180 185 190
Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser
195 200 205
Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
225 230 235 240
Ser Ser Val Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln Tyr
245 250 255
Tyr Ser Tyr Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 60
<211> 495
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 12
<400> 60
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Val Thr Met Asn Cys Lys Ser Ser Gln
35 40 45
Ser Leu Leu Tyr Ser Thr Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln
50 55 60
Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr
65 70 75 80
Arg Glu Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr
85 90 95
Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Val Ala Val
100 105 110
Tyr Tyr Cys Gln Gln Tyr Tyr Ser Tyr Arg Thr Phe Gly Gly Gly Thr
115 120 125
Lys Leu Glu Ile Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gln Val Gln Leu Gln Gln Ser Gly Pro Glu Val
145 150 155 160
Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr
165 170 175
Thr Phe Thr Ser Tyr Val Ile His Trp Val Arg Gln Lys Pro Gly Gln
180 185 190
Gly Leu Asp Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr Asp
195 200 205
Tyr Asp Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Thr Ser
210 215 220
Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr
225 230 235 240
Ala Val Tyr Tyr Cys Ala Arg Glu Lys Asp Asn Tyr Ala Thr Gly Ala
245 250 255
Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser Ala
260 265 270
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
275 280 285
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
290 295 300
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile
305 310 315 320
Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val
325 330 335
Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe
340 345 350
Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly
355 360 365
Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg
370 375 380
Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln
385 390 395 400
Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp
405 410 415
Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro
420 425 430
Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp
435 440 445
Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg
450 455 460
Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr
465 470 475 480
Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 61
<211> 478
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 13
<400> 61
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln
115 120 125
Gly Thr Leu Val Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser
145 150 155 160
Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp
165 170 175
Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro
180 185 190
Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser
195 200 205
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
210 215 220
Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn
225 230 235 240
Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
290 295 300
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
305 310 315 320
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
325 330 335
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
340 345 350
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
355 360 365
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
370 375 380
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
385 390 395 400
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
405 410 415
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
420 425 430
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
435 440 445
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
450 455 460
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<210> 62
<211> 478
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 14
<400> 62
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Ser Trp Leu Ala Trp Tyr Gln His Lys Pro Gly Lys Ala
50 55 60
Pro Lys Leu Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala
100 105 110
Asn Ser Phe Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln
130 135 140
Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu Thr
145 150 155 160
Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr Tyr
165 170 175
Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
180 185 190
Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
195 200 205
Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys
210 215 220
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
225 230 235 240
Val Ile Asn Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Thr
245 250 255
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
260 265 270
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
275 280 285
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
290 295 300
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
305 310 315 320
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
325 330 335
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
340 345 350
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
355 360 365
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
370 375 380
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
385 390 395 400
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
405 410 415
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
420 425 430
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
435 440 445
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
450 455 460
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
465 470 475
<210> 63
<211> 496
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 15
<400> 63
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Glu Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe
35 40 45
Ser Phe Ser Asp Cys Arg Met Tyr Trp Leu Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Val Ile Ser Val Lys Ser Glu Asn Tyr Gly
65 70 75 80
Ala Asn Tyr Ala Glu Ser Val Arg Gly Arg Phe Thr Ile Ser Arg Asp
85 90 95
Asp Ser Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu
100 105 110
Asp Thr Ala Val Tyr Tyr Cys Ser Ala Ser Tyr Tyr Arg Tyr Asp Val
115 120 125
Gly Ala Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
130 135 140
Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu
165 170 175
Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys Ser Val Ser Thr
180 185 190
Ser Gly Tyr Ser Tyr Ile Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Pro
195 200 205
Pro Lys Leu Leu Ile Tyr Leu Ala Ser Ile Leu Glu Ser Gly Val Pro
210 215 220
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
225 230 235 240
Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln His Ser
245 250 255
Arg Glu Leu Pro Trp Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
260 265 270
Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 64
<211> 496
<212> PRT
<213> artificial sequence
<220>
<223> CD4 CAR-T No. 16
<400> 64
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu
20 25 30
Ala Val Ser Leu Gly Glu Arg Ala Thr Ile Asn Cys Arg Ala Ser Lys
35 40 45
Ser Val Ser Thr Ser Gly Tyr Ser Tyr Ile Tyr Trp Tyr Gln Gln Lys
50 55 60
Pro Gly Gln Pro Pro Lys Leu Leu Ile Tyr Leu Ala Ser Ile Leu Glu
65 70 75 80
Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe
85 90 95
Thr Leu Thr Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr
100 105 110
Cys Gln His Ser Arg Glu Leu Pro Trp Thr Phe Gly Gln Gly Thr Lys
115 120 125
Val Glu Ile Lys Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
130 135 140
Gly Gly Gly Ser Glu Glu Gln Leu Val Glu Ser Gly Gly Gly Leu Val
145 150 155 160
Lys Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ser
165 170 175
Phe Ser Asp Cys Arg Met Tyr Trp Leu Arg Gln Ala Pro Gly Lys Gly
180 185 190
Leu Glu Trp Ile Gly Val Ile Ser Val Lys Ser Glu Asn Tyr Gly Ala
195 200 205
Asn Tyr Ala Glu Ser Val Arg Gly Arg Phe Thr Ile Ser Arg Asp Asp
210 215 220
Ser Lys Asn Thr Val Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp
225 230 235 240
Thr Ala Val Tyr Tyr Cys Ser Ala Ser Tyr Tyr Arg Tyr Asp Val Gly
245 250 255
Ala Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
260 265 270
Ala Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile
275 280 285
Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala
290 295 300
Gly Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr
305 310 315 320
Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu
325 330 335
Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile
340 345 350
Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp
355 360 365
Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
370 375 380
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
385 390 395 400
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
405 410 415
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
420 425 430
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
435 440 445
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
450 455 460
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
465 470 475 480
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490 495
<210> 65
<211> 494
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 1
<400> 65
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu
20 25 30
Val Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly
35 40 45
Ser Ile Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro
50 55 60
Gly Lys Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr
65 70 75 80
Tyr Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr
85 90 95
Ser Lys Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg His Ile Leu Thr Lys Ala Ala Gly
115 120 125
Tyr Trp Tyr Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser
130 135 140
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Gln Ser Val Leu Ile Gln Pro Arg Ser Val Ser Gly Ser Pro Gly Gln
165 170 175
Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser Asp Val Gly Gly Tyr
180 185 190
Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly Lys Ala Pro Lys Leu
195 200 205
Met Ile Tyr Asp Val Ser Lys Arg Pro Ser Gly Val Pro Asp Arg Phe
210 215 220
Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu Thr Ile Ser Gly Leu
225 230 235 240
Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Cys Ser Tyr Ala Gly Ser
245 250 255
Tyr Arg Asp Tyr Val Phe Gly Thr Gly Thr Lys Leu Thr Val Leu Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 66
<211> 494
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 2
<400> 66
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Ser Val Leu Ile Gln Pro Arg Ser Val Ser
20 25 30
Gly Ser Pro Gly Gln Ser Val Thr Ile Ser Cys Thr Gly Thr Ser Ser
35 40 45
Asp Val Gly Gly Tyr Asn Tyr Val Ser Trp Tyr Gln Gln His Pro Gly
50 55 60
Lys Ala Pro Lys Leu Met Ile Tyr Asp Val Ser Lys Arg Pro Ser Gly
65 70 75 80
Val Pro Asp Arg Phe Ser Gly Ser Lys Ser Gly Asn Thr Ala Ser Leu
85 90 95
Thr Ile Ser Gly Leu Gln Ala Glu Asp Glu Ala Asp Tyr Tyr Cys Cys
100 105 110
Ser Tyr Ala Gly Ser Tyr Arg Asp Tyr Val Phe Gly Thr Gly Thr Lys
115 120 125
Leu Thr Val Leu Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
130 135 140
Gly Gly Ser Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys
145 150 155 160
Pro Ser Glu Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile
165 170 175
Ser Ser Ser Ser Tyr Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys
180 185 190
Gly Leu Glu Trp Ile Gly Ser Ile Tyr Tyr Ser Gly Ser Thr Tyr Tyr
195 200 205
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
210 215 220
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
225 230 235 240
Val Tyr Tyr Cys Ala Arg His Ile Leu Thr Lys Ala Ala Gly Tyr Trp
245 250 255
Tyr Phe Asp Leu Trp Gly Arg Gly Thr Leu Val Thr Val Ser Ser Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 67
<211> 491
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 3
<400> 67
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu
20 25 30
Leu Lys Pro Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly
35 40 45
Ser Phe Ser Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys
50 55 60
Gly Leu Glu Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr
65 70 75 80
Asn Pro Ser Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys
85 90 95
Asn Gln Phe Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala
100 105 110
Val Tyr Tyr Cys Ala Arg Gly Arg Arg Ser Ile Ala Ala Arg Pro Phe
115 120 125
Ser Phe Asp Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gln Pro
145 150 155 160
Val Leu Thr Gln Ser Pro Ser Ala Ser Gly Thr Pro Gly Gln Arg Val
165 170 175
Thr Ile Ser Cys Ser Gly Ser Ser Ser Asn Ile Gly Ile Asn Pro Val
180 185 190
Asn Trp Tyr Gln Gln Leu Pro Gly Ala Ala Pro Lys Leu Leu Ile Tyr
195 200 205
Thr Thr Asn Gln Arg Pro Ser Gly Val Pro Asp Arg Phe Ser Ala Ser
210 215 220
Lys Ser Gly Thr Ser Ala Ser Pro Ala Ile Ser Gly Leu Gln Ser Ala
225 230 235 240
Asp Glu Ala Asp Tyr Tyr Cys Ala Ala Trp Asp Asp Arg Leu Asn Gly
245 250 255
Val Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 68
<211> 491
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 4
<400> 68
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Pro Val Leu Thr Gln Ser Pro Ser Ala Ser
20 25 30
Gly Thr Pro Gly Gln Arg Val Thr Ile Ser Cys Ser Gly Ser Ser Ser
35 40 45
Asn Ile Gly Ile Asn Pro Val Asn Trp Tyr Gln Gln Leu Pro Gly Ala
50 55 60
Ala Pro Lys Leu Leu Ile Tyr Thr Thr Asn Gln Arg Pro Ser Gly Val
65 70 75 80
Pro Asp Arg Phe Ser Ala Ser Lys Ser Gly Thr Ser Ala Ser Pro Ala
85 90 95
Ile Ser Gly Leu Gln Ser Ala Asp Glu Ala Asp Tyr Tyr Cys Ala Ala
100 105 110
Trp Asp Asp Arg Leu Asn Gly Val Val Phe Gly Gly Gly Thr Lys Leu
115 120 125
Thr Val Leu Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
130 135 140
Gly Ser Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro
145 150 155 160
Ser Glu Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser
165 170 175
Gly Tyr Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu
180 185 190
Trp Ile Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser
195 200 205
Leu Lys Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe
210 215 220
Ser Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr
225 230 235 240
Cys Ala Arg Gly Arg Arg Ser Ile Ala Ala Arg Pro Phe Ser Phe Asp
245 250 255
Ile Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Thr Thr Thr Pro
260 265 270
Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu
275 280 285
Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His
290 295 300
Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu
305 310 315 320
Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr
325 330 335
Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe
340 345 350
Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg
355 360 365
Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser
370 375 380
Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr
385 390 395 400
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
405 410 415
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
420 425 430
Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
435 440 445
Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
450 455 460
His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr
465 470 475 480
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 69
<211> 493
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 5
<400> 69
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu
20 25 30
Val Gln Pro Gly Gly Ser Leu Arg Leu Ser Cys Ala Ala Ala Gly Phe
35 40 45
Thr Phe Ser Ser Tyr Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys
50 55 60
Gly Leu Glu Trp Val Ser Tyr Ile Ser Ser Arg Ser Arg Thr Ile Tyr
65 70 75 80
Tyr Ala Asp Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala
85 90 95
Lys Asn Ser Leu Tyr Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Tyr Gly Gly Gln Pro Pro Tyr Tyr
115 120 125
Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val
130 135 140
Ser Ser Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser
165 170 175
Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser
180 185 190
Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser
195 200 205
Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu
225 230 235 240
Gln Pro Glu Asp Phe Val Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr
245 250 255
Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 70
<211> 493
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 6
<400> 70
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu
20 25 30
Ser Ala Ser Val Gly Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln
35 40 45
Gly Ile Ser Ser Trp Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala
50 55 60
Pro Lys Ser Leu Ile Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Leu Gln Pro Glu Asp Phe Val Thr Tyr Tyr Cys Gln Gln Tyr
100 105 110
Asn Ser Tyr Pro Arg Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
115 120 125
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
130 135 140
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
145 150 155 160
Ser Leu Arg Leu Ser Cys Ala Ala Ala Gly Phe Thr Phe Ser Ser Tyr
165 170 175
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
180 185 190
Ser Tyr Ile Ser Ser Arg Ser Arg Thr Ile Tyr Tyr Ala Asp Ser Val
195 200 205
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
210 215 220
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
225 230 235 240
Ala Arg Asp Tyr Gly Gly Gln Pro Pro Tyr Tyr Tyr Tyr Tyr Gly Met
245 250 255
Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala Thr Thr
260 265 270
Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln
275 280 285
Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala
290 295 300
Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala
305 310 315 320
Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr
325 330 335
Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
340 345 350
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
355 360 365
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
370 375 380
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln
385 390 395 400
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
405 410 415
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
420 425 430
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
435 440 445
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
450 455 460
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
465 470 475 480
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 71
<211> 494
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 7
<400> 71
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val
20 25 30
Lys Lys Pro Gly Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr
35 40 45
Thr Phe Thr Ser Tyr Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln
50 55 60
Gly Leu Glu Trp Met Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn
65 70 75 80
Tyr Ala Gln Lys Leu Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser
85 90 95
Thr Ser Thr Ala Tyr Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr
100 105 110
Ala Val Tyr Tyr Cys Ala Arg Asp Thr Pro Gly Ile Ala Ala Arg Arg
115 120 125
Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
130 135 140
Val Ser Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
145 150 155 160
Gly Ser Ser Ser Glu Leu Thr Gln Asp Pro Ala Val Ser Val Ala Leu
165 170 175
Gly Gln Thr Val Arg Ile Thr Cys Gln Gly Asp Ser Leu Arg Lys Phe
180 185 190
Phe Ala Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Val Leu Val
195 200 205
Ile Tyr Gly Lys Asn Ser Arg Pro Ser Gly Ile Pro Asp Arg Phe Ser
210 215 220
Gly Ser Asn Ser Arg Asn Thr Ala Ser Leu Thr Ile Thr Gly Ala Gln
225 230 235 240
Ala Glu Asp Glu Gly Asp Tyr Tyr Cys Asn Ser Arg Asp Ser Arg Asp
245 250 255
Asn His Gln Val Phe Gly Ala Gly Thr Lys Val Thr Val Leu Ser Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 72
<211> 494
<212> PRT
<213> artificial sequence
<220>
<223> CXCR4 CAR-T No. 8
<400> 72
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Ser Ser Glu Leu Thr Gln Asp Pro Ala Val Ser
20 25 30
Val Ala Leu Gly Gln Thr Val Arg Ile Thr Cys Gln Gly Asp Ser Leu
35 40 45
Arg Lys Phe Phe Ala Ser Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
50 55 60
Val Leu Val Ile Tyr Gly Lys Asn Ser Arg Pro Ser Gly Ile Pro Asp
65 70 75 80
Arg Phe Ser Gly Ser Asn Ser Arg Asn Thr Ala Ser Leu Thr Ile Thr
85 90 95
Gly Ala Gln Ala Glu Asp Glu Gly Asp Tyr Tyr Cys Asn Ser Arg Asp
100 105 110
Ser Arg Asp Asn His Gln Val Phe Gly Ala Gly Thr Lys Val Thr Val
115 120 125
Leu Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
130 135 140
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
145 150 155 160
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
165 170 175
Tyr Gly Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
180 185 190
Met Gly Trp Ile Ser Ala Tyr Asn Gly Asn Thr Asn Tyr Ala Gln Lys
195 200 205
Leu Gln Gly Arg Val Thr Met Thr Thr Asp Thr Ser Thr Ser Thr Ala
210 215 220
Tyr Met Glu Leu Arg Ser Leu Arg Ser Asp Asp Thr Ala Val Tyr Tyr
225 230 235 240
Cys Ala Arg Asp Thr Pro Gly Ile Ala Ala Arg Arg Tyr Tyr Tyr Tyr
245 250 255
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Thr
260 265 270
Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser
275 280 285
Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly
290 295 300
Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp
305 310 315 320
Ala Pro Leu Ala Gly Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile
325 330 335
Thr Leu Tyr Cys Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys
340 345 350
Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys
355 360 365
Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val
370 375 380
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
385 390 395 400
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
405 410 415
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
420 425 430
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
435 440 445
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
450 455 460
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
465 470 475 480
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
485 490
<210> 73
<211> 867
<212> PRT
<213> artificial sequence
<220>
<223> CD4 eTCR No. 11
<400> 73
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Gln Gln Ser Gly Pro Glu
20 25 30
Val Val Lys Pro Gly Ala Ser Val Lys Met Ser Cys Lys Ala Ser Gly
35 40 45
Tyr Thr Phe Thr Ser Tyr Val Ile His Trp Val Arg Gln Lys Pro Gly
50 55 60
Gln Gly Leu Asp Trp Ile Gly Tyr Ile Asn Pro Tyr Asn Asp Gly Thr
65 70 75 80
Asp Tyr Asp Glu Lys Phe Lys Gly Lys Ala Thr Leu Thr Ser Asp Thr
85 90 95
Ser Thr Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
100 105 110
Thr Ala Val Tyr Tyr Cys Ala Arg Glu Lys Asp Asn Tyr Ala Thr Gly
115 120 125
Ala Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
130 135 140
Ala Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
145 150 155 160
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
165 170 175
Glu Arg Val Thr Met Asn Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
180 185 190
Thr Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
195 200 205
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
210 215 220
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
225 230 235 240
Ile Ser Ser Val Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Gln Gln
245 250 255
Tyr Tyr Ser Tyr Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
260 265 270
Arg Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
275 280 285
Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys Val
290 295 300
Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro Gly
305 310 315 320
Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp Glu
325 330 335
Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys Glu
340 345 350
Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg Gly
355 360 365
Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg Val
370 375 380
Cys Glu Asn Cys Met Glu Met Asp Val Met Ser Val Ala Thr Ile Val
385 390 395 400
Ile Val Asp Ile Cys Ile Thr Gly Gly Leu Leu Leu Leu Val Tyr Tyr
405 410 415
Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys Pro Val Thr Arg Gly Ala
420 425 430
Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn Lys Glu Arg Pro Pro Pro
435 440 445
Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg Lys Gly Gln Arg Asp Leu
450 455 460
Tyr Ser Gly Leu Asn Gln Arg Arg Ile Gly Ser Gly Ala Thr Asn Phe
465 470 475 480
Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met
485 490 495
Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu Asn Leu Glu Asp Leu
500 505 510
Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn Asp Thr Ser Leu Val
515 520 525
Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro Leu Met Ala Ser Phe
530 535 540
Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu Ile Phe Leu Leu Gly
545 550 555 560
Val Ile Gly Asn Val Leu Val Leu Val Ile Leu Glu Arg His Arg Gln
565 570 575
Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His Leu Ala Val Ala Asp
580 585 590
Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val Ala Glu Gly Ser Val
595 600 605
Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His
610 615 620
Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val
625 630 635 640
Asp Arg Tyr Leu Ala Ile Val His Ala Val His Ala Tyr Arg His Arg
645 650 655
Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly
660 665 670
Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly
675 680 685
His His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn Gln
690 695 700
Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu Tyr His Val Ala
705 710 715 720
Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys Tyr Val Gly Val
725 730 735
Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln Arg Gln Lys Ala
740 745 750
Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe Phe Leu Cys Trp Ser
755 760 765
Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu Ala Arg Leu Lys Ala
770 775 780
Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro Val Ala Ile Thr
785 790 795 800
Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu Asn Pro Met Leu
805 810 815
Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu Ser Arg Leu Leu
820 825 830
Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro
835 840 845
Gly Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu
850 855 860
Thr Thr Phe
865
<210> 74
<211> 863
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 eTCR 807
<400> 74
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Lys Gln Ser Gly Ala Glu
20 25 30
Leu Val Arg Pro Gly Ala Ser Val Lys Leu Ser Cys Lys Thr Ser Gly
35 40 45
Tyr Ile Phe Thr Asn Tyr Trp Ile His Trp Val Lys Gln Arg Ser Gly
50 55 60
Gln Gly Leu Glu Trp Ile Ala Arg Ile Tyr Pro Gly Thr Gly Ser Asn
65 70 75 80
Tyr Tyr Asn Glu Lys Leu Lys Asp Lys Ala Thr Leu Thr Thr Asp Lys
85 90 95
Ser Ser Ser Thr Val Tyr Ile Gln Leu Ser Ser Leu Lys Ser Glu Asp
100 105 110
Ser Ala Val Tyr Phe Cys Ala Arg Glu Gly Asp Tyr Tyr Gly Tyr Gly
115 120 125
Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Val Leu Thr Gln Ser Pro Ala Ser Leu Val Val Ser Leu Gly Gln Arg
165 170 175
Ala Thr Ile Ser Cys Arg Ala Ser Lys Ser Val Ser Thr Ser Gly Tyr
180 185 190
Tyr Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro Lys Leu
195 200 205
Leu Ile Tyr Leu Ala Ser Asn Leu Glu Ser Gly Val Pro Ala Arg Phe
210 215 220
Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His Pro Val
225 230 235 240
Glu Glu Glu Asp Ala Ala Thr Tyr Tyr Cys His His Ser Arg Glu Phe
245 250 255
Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Gly Gly Gly
260 265 270
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Gly Asn Glu
275 280 285
Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys Val Ser Ile Ser Gly
290 295 300
Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro Gly Ser Glu Ile Leu
305 310 315 320
Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp Glu Asp Asp Lys Asn
325 330 335
Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys Glu Phe Ser Glu Leu
340 345 350
Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg Gly Ser Lys Pro Glu
355 360 365
Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg Val Cys Glu Asn Cys
370 375 380
Met Glu Met Asp Val Met Ser Val Ala Thr Ile Val Ile Val Asp Ile
385 390 395 400
Cys Ile Thr Gly Gly Leu Leu Leu Leu Val Tyr Tyr Trp Ser Lys Asn
405 410 415
Arg Lys Ala Lys Ala Lys Pro Val Thr Arg Gly Ala Gly Ala Gly Gly
420 425 430
Arg Gln Arg Gly Gln Asn Lys Glu Arg Pro Pro Pro Val Pro Asn Pro
435 440 445
Asp Tyr Glu Pro Ile Arg Lys Gly Gln Arg Asp Leu Tyr Ser Gly Leu
450 455 460
Asn Gln Arg Arg Ile Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
465 470 475 480
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Asn Tyr Pro Leu
485 490 495
Thr Leu Glu Met Asp Leu Glu Asn Leu Glu Asp Leu Phe Trp Glu Leu
500 505 510
Asp Arg Leu Asp Asn Tyr Asn Asp Thr Ser Leu Val Glu Asn His Leu
515 520 525
Cys Pro Ala Thr Glu Gly Pro Leu Met Ala Ser Phe Lys Ala Val Phe
530 535 540
Val Pro Val Ala Tyr Ser Leu Ile Phe Leu Leu Gly Val Ile Gly Asn
545 550 555 560
Val Leu Val Leu Val Ile Leu Glu Arg His Arg Gln Thr Arg Ser Ser
565 570 575
Thr Glu Thr Phe Leu Phe His Leu Ala Val Ala Asp Leu Leu Leu Val
580 585 590
Phe Ile Leu Pro Phe Ala Val Ala Glu Gly Ser Val Gly Trp Val Leu
595 600 605
Gly Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His Lys Val Asn Phe
610 615 620
Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val Asp Arg Tyr Leu
625 630 635 640
Ala Ile Val His Ala Val His Ala Tyr Arg His Arg Arg Leu Leu Ser
645 650 655
Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly Phe Leu Leu Ala
660 665 670
Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly His His Asn Asn
675 680 685
Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn Gln Ala Glu Thr His
690 695 700
Ala Trp Phe Thr Ser Arg Phe Leu Tyr His Val Ala Gly Phe Leu Leu
705 710 715 720
Pro Met Leu Val Met Gly Trp Cys Tyr Val Gly Val Val His Arg Leu
725 730 735
Arg Gln Ala Gln Arg Arg Pro Gln Arg Gln Lys Ala Val Arg Val Ala
740 745 750
Ile Leu Val Thr Ser Ile Phe Phe Leu Cys Trp Ser Pro Tyr His Ile
755 760 765
Val Ile Phe Leu Asp Thr Leu Ala Arg Leu Lys Ala Val Asp Asn Thr
770 775 780
Cys Lys Leu Asn Gly Ser Leu Pro Val Ala Ile Thr Met Cys Glu Phe
785 790 795 800
Leu Gly Leu Ala His Cys Cys Leu Asn Pro Met Leu Tyr Thr Phe Ala
805 810 815
Gly Val Lys Phe Arg Ser Asp Leu Ser Arg Leu Leu Thr Lys Leu Gly
820 825 830
Cys Thr Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro Gly Trp Arg Arg
835 840 845
Ser Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu Thr Thr Phe
850 855 860
<210> 75
<211> 855
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 eTCR 808
<400> 75
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Gln Val Gln Leu Gln Gln Ser Gly Pro Glu
20 25 30
Leu Val Arg Pro Gly Ala Ser Val Lys Met Ser Cys Glu Ala Ser Gly
35 40 45
Tyr Ile Phe Thr Ser Tyr Trp Met His Trp Val Lys Gln Arg Pro Gly
50 55 60
Gln Gly Leu Glu Trp Ile Gly Met Ile Asp Pro Ser Asn Ser Glu Thr
65 70 75 80
Arg Leu Asn Gln Lys Phe Lys Asp Lys Ala Thr Leu Thr Val Asp Lys
85 90 95
Ser Ser Asn Thr Ala Tyr Met Gln Leu Ser Ser Leu Thr Ser Ala Asp
100 105 110
Ser Ala Val Tyr Tyr Cys Ala Arg Asp Tyr Ser Tyr Ala Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Lys Met Thr Gln
145 150 155 160
Ser Pro Ser Ser Met Tyr Ala Ser Leu Gly Glu Arg Val Thr Ile Thr
165 170 175
Cys Lys Ala Ser Gln Asp Ile Ser Ala Tyr Leu Ser Trp Phe Gln Gln
180 185 190
Lys Pro Gly Lys Ser Pro Lys Thr Leu Ile Tyr Arg Ala Asn Arg Leu
195 200 205
Val Asp Gly Val Pro Pro Arg Phe Ser Gly Ser Gly Ser Gly Gln Asp
210 215 220
Phe Ser Leu Thr Ile Ser Ser Leu Gly Tyr Glu Asp Met Gly Phe Tyr
225 230 235 240
Tyr Cys Leu Gln Tyr Asp Glu Phe Pro Asn Thr Phe Gly Gly Gly Thr
245 250 255
Lys Leu Glu Ile Thr Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
260 265 270
Gly Gly Gly Ser Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr
275 280 285
Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro
290 295 300
Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile
305 310 315 320
Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu
325 330 335
Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys
340 345 350
Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu
355 360 365
Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met Ser Val
370 375 380
Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu Leu Leu
385 390 395 400
Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys Pro Val
405 410 415
Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn Lys Glu
420 425 430
Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg Lys Gly
435 440 445
Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile Gly Ser Gly
450 455 460
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
465 470 475 480
Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu Asn
485 490 495
Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn Asp
500 505 510
Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro Leu
515 520 525
Met Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu Ile
530 535 540
Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile Leu Glu
545 550 555 560
Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His Leu
565 570 575
Ala Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val Ala
580 585 590
Glu Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr Val
595 600 605
Ile Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu Ala
610 615 620
Cys Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val His Ala
625 630 635 640
Tyr Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr Ile
645 650 655
Trp Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys
660 665 670
Val Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser
675 680 685
Gln Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu
690 695 700
Tyr His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys
705 710 715 720
Tyr Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln
725 730 735
Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe Phe
740 745 750
Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu Ala
755 760 765
Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu Pro
770 775 780
Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys Leu
785 790 795 800
Asn Pro Met Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp Leu
805 810 815
Ser Arg Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu Cys
820 825 830
Gln Leu Phe Pro Gly Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu Asn
835 840 845
Ala Thr Ser Leu Thr Thr Phe
850 855
<210> 76
<211> 856
<212> PRT
<213> artificial sequence
<220>
<223> CCR5 eTCR
<400> 76
Met Gln Ser Gly Thr His Trp Arg Val Leu Gly Leu Cys Leu Leu Ser
1 5 10 15
Val Gly Val Trp Gly Gln Glu Val Gln Leu Val Glu Ser Gly Gly Gly
20 25 30
Leu Val Gln Pro Lys Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly
35 40 45
Phe Thr Phe Asn Thr Tyr Ala Met Asn Trp Val Arg Gln Ala Pro Gly
50 55 60
Lys Gly Leu Glu Trp Val Ala Arg Ile Arg Asn Lys Ser Asn Asn Tyr
65 70 75 80
Ala Thr Tyr Tyr Ala Ala Ser Val Lys Asp Arg Phe Thr Ile Ser Arg
85 90 95
Asp Asp Ser Gln Ser Met Leu Tyr Leu Gln Met Asn Asn Leu Lys Thr
100 105 110
Glu Asp Thr Ala Met Tyr Tyr Cys Val Ser Leu Gly Glu Phe Ala Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Gly Gly Gly Gly Ser
130 135 140
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Ile Val Leu Thr Gln
145 150 155 160
Ser Pro Thr Thr Met Ala Ala Ser Pro Gly Glu Lys Val Thr Ile Thr
165 170 175
Cys Ser Ala Thr Ser Thr Ile Asn Ser Asn Tyr Leu His Trp Tyr Gln
180 185 190
Gln Lys Pro Gly Phe Ser Pro Lys Leu Leu Ile Tyr Arg Thr Ser Asn
195 200 205
Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser Gly Ser Gly Thr
210 215 220
Ser Tyr Ser Leu Thr Ile Gly Thr Met Glu Ala Glu Asp Val Ala Thr
225 230 235 240
Tyr Tyr Cys Gln Gln Gly Ser Thr Leu Pro Phe Thr Phe Gly Ser Gly
245 250 255
Thr Lys Leu Glu Ile Lys Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
260 265 270
Gly Gly Gly Gly Ser Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln
275 280 285
Thr Pro Tyr Lys Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys
290 295 300
Pro Gln Tyr Pro Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn
305 310 315 320
Ile Gly Gly Asp Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His
325 330 335
Leu Ser Leu Lys Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val
340 345 350
Cys Tyr Pro Arg Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr
355 360 365
Leu Arg Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp Val Met Ser
370 375 380
Val Ala Thr Ile Val Ile Val Asp Ile Cys Ile Thr Gly Gly Leu Leu
385 390 395 400
Leu Leu Val Tyr Tyr Trp Ser Lys Asn Arg Lys Ala Lys Ala Lys Pro
405 410 415
Val Thr Arg Gly Ala Gly Ala Gly Gly Arg Gln Arg Gly Gln Asn Lys
420 425 430
Glu Arg Pro Pro Pro Val Pro Asn Pro Asp Tyr Glu Pro Ile Arg Lys
435 440 445
Gly Gln Arg Asp Leu Tyr Ser Gly Leu Asn Gln Arg Arg Ile Gly Ser
450 455 460
Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu
465 470 475 480
Asn Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu Met Asp Leu Glu
485 490 495
Asn Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu Asp Asn Tyr Asn
500 505 510
Asp Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala Thr Glu Gly Pro
515 520 525
Leu Met Ala Ser Phe Lys Ala Val Phe Val Pro Val Ala Tyr Ser Leu
530 535 540
Ile Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val Leu Val Ile Leu
545 550 555 560
Glu Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr Phe Leu Phe His
565 570 575
Leu Ala Val Ala Asp Leu Leu Leu Val Phe Ile Leu Pro Phe Ala Val
580 585 590
Ala Glu Gly Ser Val Gly Trp Val Leu Gly Thr Phe Leu Cys Lys Thr
595 600 605
Val Ile Ala Leu His Lys Val Asn Phe Tyr Cys Ser Ser Leu Leu Leu
610 615 620
Ala Cys Ile Ala Val Asp Arg Tyr Leu Ala Ile Val His Ala Val His
625 630 635 640
Ala Tyr Arg His Arg Arg Leu Leu Ser Ile His Ile Thr Cys Gly Thr
645 650 655
Ile Trp Leu Val Gly Phe Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala
660 665 670
Lys Val Ser Gln Gly His His Asn Asn Ser Leu Pro Arg Cys Thr Phe
675 680 685
Ser Gln Glu Asn Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe
690 695 700
Leu Tyr His Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp
705 710 715 720
Cys Tyr Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro
725 730 735
Gln Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe
740 745 750
Phe Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr Leu
755 760 765
Ala Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly Ser Leu
770 775 780
Pro Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala His Cys Cys
785 790 795 800
Leu Asn Pro Met Leu Tyr Thr Phe Ala Gly Val Lys Phe Arg Ser Asp
805 810 815
Leu Ser Arg Leu Leu Thr Lys Leu Gly Cys Thr Gly Pro Ala Ser Leu
820 825 830
Cys Gln Leu Phe Pro Gly Trp Arg Arg Ser Ser Leu Ser Glu Ser Glu
835 840 845
Asn Ala Thr Ser Leu Thr Thr Phe
850 855
<210> 77
<211> 486
<212> PRT
<213> artificial sequence
<220>
<223> Anti-CD19 CAR
<400> 77
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Asp Ile Gln Met Thr Gln Thr Thr Ser Ser Leu
20 25 30
Ser Ala Ser Leu Gly Asp Arg Val Thr Ile Ser Cys Arg Ala Ser Gln
35 40 45
Asp Ile Ser Lys Tyr Leu Asn Trp Tyr Gln Gln Lys Pro Asp Gly Thr
50 55 60
Val Lys Leu Leu Ile Tyr His Thr Ser Arg Leu His Ser Gly Val Pro
65 70 75 80
Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile
85 90 95
Ser Asn Leu Glu Gln Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly
100 105 110
Asn Thr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Thr
115 120 125
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
130 135 140
Val Lys Leu Gln Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln Ser
145 150 155 160
Leu Ser Val Thr Cys Thr Val Ser Gly Val Ser Leu Pro Asp Tyr Gly
165 170 175
Val Ser Trp Ile Arg Gln Pro Pro Arg Lys Gly Leu Glu Trp Leu Gly
180 185 190
Val Ile Trp Gly Ser Glu Thr Thr Tyr Tyr Asn Ser Ala Leu Lys Ser
195 200 205
Arg Leu Thr Ile Ile Lys Asp Asn Ser Lys Ser Gln Val Phe Leu Lys
210 215 220
Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Ile Tyr Tyr Cys Ala Lys
225 230 235 240
His Tyr Tyr Tyr Gly Gly Ser Tyr Ala Met Asp Tyr Trp Gly Gln Gly
245 250 255
Thr Ser Val Thr Val Ser Ser Thr Thr Thr Pro Ala Pro Arg Pro Pro
260 265 270
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
275 280 285
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
290 295 300
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
305 310 315 320
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Lys Arg Gly Arg
325 330 335
Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln
340 345 350
Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu
355 360 365
Glu Gly Gly Cys Glu Leu Arg Val Lys Phe Ser Arg Ser Ala Asp Ala
370 375 380
Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu
385 390 395 400
Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp
405 410 415
Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu
420 425 430
Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile
435 440 445
Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr
450 455 460
Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met
465 470 475 480
Gln Ala Leu Pro Pro Arg
485
<210> 78
<211> 1292
<212> PRT
<213> artificial sequence
<220>
<223> ssCD4CCR5-CXCR5
<400> 78
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu Gln
20 25 30
Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu Thr
35 40 45
Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr Tyr
50 55 60
Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile Gly
65 70 75 80
Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
85 90 95
Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys
100 105 110
Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg
115 120 125
Val Ile Asn Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr Gly
130 135 140
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
145 150 155 160
Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp Arg
165 170 175
Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu Ala
180 185 190
Trp Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr Ala
195 200 205
Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
210 215 220
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp
225 230 235 240
Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Tyr Thr Phe
245 250 255
Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro Arg
260 265 270
Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg
275 280 285
Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly
290 295 300
Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr
305 310 315 320
Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Val
325 330 335
Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn
340 345 350
Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val
355 360 365
Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg
370 375 380
Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys
385 390 395 400
Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg
405 410 415
Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys
420 425 430
Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser
435 440 445
Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu
450 455 460
Asn Pro Gly Pro Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu
465 470 475 480
Ala Leu Leu Leu His Ala Ala Arg Pro Tyr Pro Tyr Asp Val Pro Asp
485 490 495
Tyr Ala Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro
500 505 510
Gly Arg Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser
515 520 525
Gly Tyr Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu
530 535 540
Trp Val Ser Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp
545 550 555 560
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
565 570 575
Leu Tyr Leu Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
580 585 590
Tyr Cys Ala Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala
595 600 605
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly
610 615 620
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile
625 630 635 640
Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg
645 650 655
Val Thr Ile Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn
660 665 670
Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp
675 680 685
Ala Ser Asn Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly
690 695 700
Ser Gly Thr Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp
705 710 715 720
Thr Ala Thr Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe
725 730 735
Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro
740 745 750
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
755 760 765
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
770 775 780
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
785 790 795 800
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg
805 810 815
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
820 825 830
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
835 840 845
Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg Lys Lys Leu Leu
850 855 860
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
865 870 875 880
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
885 890 895
Glu Leu Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly
900 905 910
Asp Val Glu Glu Asn Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu
915 920 925
Met Asp Leu Glu Asn Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu
930 935 940
Asp Asn Tyr Asn Asp Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala
945 950 955 960
Thr Glu Gly Pro Leu Met Ala Ser Phe Lys Ala Val Phe Val Pro Val
965 970 975
Ala Tyr Ser Leu Ile Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val
980 985 990
Leu Val Ile Leu Glu Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr
995 1000 1005
Phe Leu Phe His Leu Ala Val Ala Asp Leu Leu Leu Val Phe Ile
1010 1015 1020
Leu Pro Phe Ala Val Ala Glu Gly Ser Val Gly Trp Val Leu Gly
1025 1030 1035
Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His Lys Val Asn Phe
1040 1045 1050
Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val Asp Arg Tyr
1055 1060 1065
Leu Ala Ile Val His Ala Val His Ala Tyr Arg His Arg Arg Leu
1070 1075 1080
Leu Ser Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly Phe
1085 1090 1095
Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly
1100 1105 1110
His His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn
1115 1120 1125
Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu Tyr His
1130 1135 1140
Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys Tyr
1145 1150 1155
Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln
1160 1165 1170
Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe
1175 1180 1185
Phe Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr
1190 1195 1200
Leu Ala Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly
1205 1210 1215
Ser Leu Pro Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala
1220 1225 1230
His Cys Cys Leu Asn Pro Met Leu Tyr Thr Phe Ala Gly Val Lys
1235 1240 1245
Phe Arg Ser Asp Leu Ser Arg Leu Leu Thr Lys Leu Gly Cys Thr
1250 1255 1260
Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro Gly Trp Arg Arg Ser
1265 1270 1275
Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu Thr Thr Phe
1280 1285 1290
<210> 79
<211> 1292
<212> PRT
<213> artificial sequence
<220>
<223> ssCCR5CD4-CXCR5
<400> 79
Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu Leu Leu
1 5 10 15
His Ala Ala Arg Pro Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu Gln
20 25 30
Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg Ser
35 40 45
Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Ser Gly Tyr Gly
50 55 60
Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
65 70 75 80
Leu Ile Ser Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val Lys
85 90 95
Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Leu Tyr Leu
100 105 110
Arg Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
115 120 125
Arg Gly Arg Asn Asp Phe Trp Ser Gly Tyr Tyr Thr Ala Gly Met Asp
130 135 140
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Gly Gly Gly Gly
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp Ile Gln Met Thr
165 170 175
Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly Asp Arg Val Thr Ile
180 185 190
Thr Cys Gln Ala Ser Gln Gly Ile Arg Lys Tyr Leu Asn Trp Tyr Gln
195 200 205
Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile Tyr Asp Ala Ser Asn
210 215 220
Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly Thr
225 230 235 240
Asp Phe Thr Phe Ala Ile Ser Ser Leu Gln Pro Glu Asp Thr Ala Thr
245 250 255
Tyr Tyr Cys Gln Gln Tyr Asp Asp Phe Pro Phe Thr Phe Gly Gln Gly
260 265 270
Thr Arg Leu Glu Ile Lys Arg Thr Thr Thr Pro Ala Pro Arg Pro Pro
275 280 285
Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu Arg Pro Glu
290 295 300
Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg Gly Leu Asp
305 310 315 320
Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly Thr Cys Gly
325 330 335
Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg Val Lys Phe
340 345 350
Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu
355 360 365
Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp
370 375 380
Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys
385 390 395 400
Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala
405 410 415
Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys
420 425 430
Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr
435 440 445
Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg Gly Ser Gly Ala
450 455 460
Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro
465 470 475 480
Gly Pro Met Ala Leu Pro Val Thr Ala Leu Leu Leu Pro Leu Ala Leu
485 490 495
Leu Leu His Ala Ala Arg Pro Tyr Pro Tyr Asp Val Pro Asp Tyr Ala
500 505 510
Gln Val Gln Leu Gln Gln Trp Gly Ala Gly Leu Leu Lys Pro Ser Glu
515 520 525
Thr Leu Ser Leu Thr Cys Ala Val Tyr Gly Gly Ser Phe Ser Gly Tyr
530 535 540
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
545 550 555 560
Gly Glu Ile Asn His Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
565 570 575
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
580 585 590
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
595 600 605
Arg Val Ile Asn Trp Phe Asp Pro Trp Gly Gln Gly Thr Leu Val Thr
610 615 620
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Asp
625 630 635 640
Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly Asp
645 650 655
Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Ser Ser Trp Leu
660 665 670
Ala Trp Tyr Gln His Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile Tyr
675 680 685
Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly Ser
690 695 700
Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu
705 710 715 720
Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Tyr Thr
725 730 735
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Thr Thr Thr Pro Ala Pro
740 745 750
Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala Ser Gln Pro Leu Ser Leu
755 760 765
Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly Gly Ala Val His Thr Arg
770 775 780
Gly Leu Asp Phe Ala Cys Asp Ile Tyr Ile Trp Ala Pro Leu Ala Gly
785 790 795 800
Thr Cys Gly Val Leu Leu Leu Ser Leu Val Ile Thr Leu Tyr Cys Arg
805 810 815
Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr Pro
820 825 830
Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro Pro
835 840 845
Arg Asp Phe Ala Ala Tyr Arg Ser Lys Arg Gly Arg Lys Lys Leu Leu
850 855 860
Tyr Ile Phe Lys Gln Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu
865 870 875 880
Glu Asp Gly Cys Ser Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys
885 890 895
Glu Leu Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly
900 905 910
Asp Val Glu Glu Asn Pro Gly Pro Met Asn Tyr Pro Leu Thr Leu Glu
915 920 925
Met Asp Leu Glu Asn Leu Glu Asp Leu Phe Trp Glu Leu Asp Arg Leu
930 935 940
Asp Asn Tyr Asn Asp Thr Ser Leu Val Glu Asn His Leu Cys Pro Ala
945 950 955 960
Thr Glu Gly Pro Leu Met Ala Ser Phe Lys Ala Val Phe Val Pro Val
965 970 975
Ala Tyr Ser Leu Ile Phe Leu Leu Gly Val Ile Gly Asn Val Leu Val
980 985 990
Leu Val Ile Leu Glu Arg His Arg Gln Thr Arg Ser Ser Thr Glu Thr
995 1000 1005
Phe Leu Phe His Leu Ala Val Ala Asp Leu Leu Leu Val Phe Ile
1010 1015 1020
Leu Pro Phe Ala Val Ala Glu Gly Ser Val Gly Trp Val Leu Gly
1025 1030 1035
Thr Phe Leu Cys Lys Thr Val Ile Ala Leu His Lys Val Asn Phe
1040 1045 1050
Tyr Cys Ser Ser Leu Leu Leu Ala Cys Ile Ala Val Asp Arg Tyr
1055 1060 1065
Leu Ala Ile Val His Ala Val His Ala Tyr Arg His Arg Arg Leu
1070 1075 1080
Leu Ser Ile His Ile Thr Cys Gly Thr Ile Trp Leu Val Gly Phe
1085 1090 1095
Leu Leu Ala Leu Pro Glu Ile Leu Phe Ala Lys Val Ser Gln Gly
1100 1105 1110
His His Asn Asn Ser Leu Pro Arg Cys Thr Phe Ser Gln Glu Asn
1115 1120 1125
Gln Ala Glu Thr His Ala Trp Phe Thr Ser Arg Phe Leu Tyr His
1130 1135 1140
Val Ala Gly Phe Leu Leu Pro Met Leu Val Met Gly Trp Cys Tyr
1145 1150 1155
Val Gly Val Val His Arg Leu Arg Gln Ala Gln Arg Arg Pro Gln
1160 1165 1170
Arg Gln Lys Ala Val Arg Val Ala Ile Leu Val Thr Ser Ile Phe
1175 1180 1185
Phe Leu Cys Trp Ser Pro Tyr His Ile Val Ile Phe Leu Asp Thr
1190 1195 1200
Leu Ala Arg Leu Lys Ala Val Asp Asn Thr Cys Lys Leu Asn Gly
1205 1210 1215
Ser Leu Pro Val Ala Ile Thr Met Cys Glu Phe Leu Gly Leu Ala
1220 1225 1230
His Cys Cys Leu Asn Pro Met Leu Tyr Thr Phe Ala Gly Val Lys
1235 1240 1245
Phe Arg Ser Asp Leu Ser Arg Leu Leu Thr Lys Leu Gly Cys Thr
1250 1255 1260
Gly Pro Ala Ser Leu Cys Gln Leu Phe Pro Gly Trp Arg Arg Ser
1265 1270 1275
Ser Leu Ser Glu Ser Glu Asn Ala Thr Ser Leu Thr Thr Phe
1280 1285 1290
Claims (58)
- 조작된 면역 세포로서,
a) i) 키메라 수용체(chimeric receptor: CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인, ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR); 및
b) i) 키메라 공동수용체(chimeric co-receptor: CCOR) 표적 항원을 특이적으로 인식하는 CCOR 항원 결합 도메인; ii) CCOR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 도메인을 포함하는 키메라 공동수용체(CCOR)
를 포함하되,
상기 CR 표적 항원은 CCR5 또는 CXCR4이고 상기 CCOR 표적 항원은 CD4이거나, 또는
상기 CR 표적 항원은 CD4이고 상기 CCOR 표적 항원은 CCR5 또는 CXCR4인, 조작된 면역 세포. - 조작된 면역 세포로서,
i) 키메라 수용체(CR) 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는 키메라 수용체(CR)를 포함하되,
상기 CR 표적 항원은 CCR5, CXCR4 및 CD4로 이루어진 군으로부터 선택되는, 조작된 면역 세포. - 제1항 또는 제2항에 있어서, 상기 CCR5, CXCR4, 또는 CD4는 광범위 중화 항체와 일렬인, 조작된 면역 세포.
- 제3항에 있어서, 상기 광범위 중화 항체는 VRC01, PGT121, 3BNC117 또는 10-1074인, 조작된 면역 세포.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 하나 이상의 공동수용체("COR")를 더 포함하는, 조작된 면역 세포.
- 조작된 면역 세포로서,
a) 키메라 수용체(CR)를 인코딩하는 제1 핵산으로서, CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하는, 제1 핵산; 및
b) 키메라 공동수용체(CCOR)를 인코딩하는 제2 핵산으로서, CCOR은 i) CCOR 표적 항원을 특이적으로 인식하는 CCOR 항원 결합 도메인; ii) CCOR 막관통 도메인; 및 iii) 세포내 CCOR 공동자극 신호전달 도메인을 포함하는, 제2 핵산
을 포함하되;
상기 CR 표적 항원은 CCR5 또는 CXCR4이고 상기 CCOR 표적 항원은 CD4이거나, 또는
상기 CR 표적 항원은 CD4이고 상기 CCOR 표적 항원은 CCR5 또는 CXCR4인, 조작된 면역 세포. - 조작된 면역 세포로서,
키메라 수용체(CR)를 인코딩하는 핵산을 포함하되, 상기 CR은 i) CR 표적 항원을 특이적으로 인식하는 CR 항원 결합 도메인; ii) CR 막관통 도메인, 및 iii) 세포내 CR 신호전달 도메인을 포함하고,
상기 CR 표적 항원은 CCR5, CXCR4 및 CD4로 이루어진 군으로부터 선택되는, 조작된 면역 세포. - 제6항 또는 제7항에 있어서, 상기 CCR5, CXCR4 또는 CD4는 광범위 중화 항체와 일렬인, 조작된 면역 세포.
- 제8항에 있어서, 상기 광범위 중화 항체는 VRC01, PGT121, 3BNC117, 10-1074인, 조작된 면역 세포.
- 제6항 내지 제9항 중 어느 한 항에 있어서, 하나 이상의 공동수용체("COR")를 인코딩하는 하나 이상의 핵산(들)을 더 포함하는, 조작된 면역 세포.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 상기 CR은 키메라 항원 수용체("CAR")인, 조작된 면역 세포.
- 제11항에 있어서, 상기 CR 막관통은 CD8α로부터 유래되는, 조작된 면역 세포.
- 제11항에 있어서, 상기 세포내 CR 신호전달 도메인은 CD3ζ로부터 유래되는, 조작된 면역 세포.
- 제11항 내지 제13항 중 어느 한 항에 있어서, 상기 CR은 세포내 CR 공동자극 도메인을 더 포함하는, 조작된 면역 세포.
- 제14항에 있어서, 상기 세포내 CR 공동자극 신호전달 도메인은 4-1-BB의 세포질 도메인을 포함하는, 조작된 면역 세포.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 상기 CR은 세포내 공동자극 도메인을 포함하지 않는, 조작된 면역 세포.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 상기 CR은 키메라 T 세포 수용체("cTCR")인, 조작된 면역 세포.
- 제17항에 있어서, 상기 CR 막관통 도메인은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε 및 CD3δ로 이루어진 군으로부터 선택되는 TCR 서브유닛의 막관통 도메인으로부터 유래되는, 조작된 면역 세포.
- 제18항에 있어서, 상기 CR 막관통 도메인은 CD3ε의 막관통 도메인으로부터 유래되는, 조작된 면역 세포.
- 제17항 내지 제19항 중 어느 한 항에 있어서, 상기 세포내 CR 신호전달 도메인은 TCRα, TCRβ, TCRγ, TCRδ, CD3γ, CD3ε 및 CD3δ로 이루어진 군으로부터 선택되는 TCR 서브유닛의 세포내 신호전달 도메인으로부터 유래되는, 조작된 면역 세포.
- 제20항에 있어서, 상기 세포내 CR 신호전달 도메인은 CD3ε의 세포내 신호전달 도메인으로부터 유래되는, 조작된 면역 세포.
- 제17항 내지 제21항 중 어느 한 항에 있어서, 상기 CR 막관통 도메인 및 세포내 CR 신호전달 도메인은 동일하거나 상이한 TCR 서브유닛(들)으로부터 유래되는, 조작된 면역 세포.
- 제17항 내지 제22항 중 어느 한 항에 있어서, 상기 CR은 TCR 서브유닛의 세포외 도메인의 일부를 더 포함하는, 조작된 면역 세포.
- 제17항 내지 제23항 중 어느 한 항에 있어서, 상기 CR은 CD3ε의 N-말단에 융합된 CR 항원 결합 도메인을 포함하는, 조작된 면역 세포.
- 제1항 내지 제24항 중 어느 한 항에 있어서, 상기 CR 표적 항원은 CD4인, 조작된 면역 세포.
- 제1항, 제5항, 제6항 및 제10항 내지 제25항 중 어느 한 항에 있어서, 상기 CCOR 표적 항원은 CD4인, 조작된 면역 세포.
- 제1항, 제5항, 제6항, 제10항 내지 제24항 및 제26항 중 어느 한 항에 있어서, 상기 CR 표적 항원은 CCR5 또는 CXCR4이고 CCOR 표적 항원은 CD4인, 조작된 면역 세포.
- 제1항, 제5항, 제6항, 및 제10항 내지 제25항 중 어느 한 항에 있어서, 상기 CR 표적 항원은 CD4이고 상기 CCOR 표적 항원은 CCR5 또는 CXCR4인, 조작된 면역 세포.
- 제25항 내지 제28항 중 어느 한 항에 있어서, 상기 CR 항원 결합 도메인 또는 CCOR 항원 결합 도메인은 CD4의 도메인 1(CD4 D1)을 특이적으로 인식하는, 조작된 면역 세포.
- 제5항 및 제10항 내지 제29항 중 어느 한 항에 있어서, 상기 하나 이상의 COR은 CXCR5, α4β7, 및 CCR9로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
- 제30항에 있어서, 상기 하나 이상의 COR은 α4β7 및 CCR9를 둘 다 포함하는, 조작된 면역 세포.
- 제1항 내지 제31항 중 어느 한 항에 있어서, 상기 조작된 면역 세포는 상기 세포 내에서 CCR5의 발현을 감소시키거나 제거하도록 변형되는, 조작된 면역 세포.
- 제1항 내지 제32항 중 어느 한 항에 있어서, 상기 조작된 면역 세포는 항-HIV 항체를 발현하도록 변형되는, 조작된 면역 세포.
- 제33항에 있어서, 상기 항-HIV 항체는 광범위 중화 항체인, 조작된 면역 세포.
- 제34항에 있어서, 상기 광범위 중화 항체는 VRC01, PGT121, 3BNC117 10-1074인, 조작된 면역 세포.
- 제1항 내지 제35항 중 어느 한 항에 있어서, 상기 CR 항원 결합 도메인은 scFv 또는 sdAb인, 조작된 면역 세포.
- 제1항 내지 제36항 중 어느 한 항에 있어서, 상기 CCOR 항원 결합 도메인은 scFv 또는 sdAb인, 조작된 면역 세포.
- 제1항 내지 제37항 중 어느 한 항에 있어서, 상기 조작된 면역 세포는 세포독성 T 세포, 헬퍼 T 세포, 자연 살해 세포, γδT 세포 및 자연 살해 T 세포로 이루어진 군으로부터 선택되는, 조작된 면역 세포.
- 제1항 내지 제37항 중 어느 한 항의 조작된 면역 세포 및 약제학적으로 허용 가능한 담체를 포함하는, 약제학적 조성물.
- 제39항에 있어서, 상기 약제학적 조성물은 제1항 내지 제38항 중 어느 한 항에 따른 조작된 면역 세포의 적어도 2가지 상이한 유형을 포함하는, 약제학적 조성물.
- 유효량의 제39항 또는 제40항의 약제학적 조성물을 개체에게 투여하는 단계를 포함하는, 개체에서 전염병을 치료하는 방법.
- 제41항에 있어서, 상기 전염병은 HIV 및 HTLV로 이루어진 군으로부터 선택되는 바이러스에 의한 감염인, 방법.
- 제42항에 있어서, 상기 전염병은 HIV인, 방법.
- 제41항 내지 제43항 중 어느 한 항에 있어서, 상기 개체에게 제2 항-감염제를 투여하는 단계를 더 포함하는, 방법.
- 유효량의 제39항 또는 제40항의 약제학적 조성물을 개체에게 투여하는 단계를 포함하는, 개체에서 암을 치료하는 방법.
- 제45항에 있어서, 상기 암은 T 세포 림프종인, 방법.
- 제45항 또는 제46항에 있어서, 상기 개체에게 제2 항암제를 투여하는 단계를 더 포함하는, 방법.
- 제41항 내지 제47항 중 어느 한 항에 있어서, 상기 개체는 인간인, 방법.
- 제1항 내지 제38항 중 어느 한 항의 조작된 면역 세포를 제조하는 방법으로서,
a) 면역 세포 집단을 제공하는 단계;
b) 상기 면역 세포 집단 내로 CR을 인코딩하는 제1 핵산을 도입하는 단계
를 포함하는, 조작된 면역 세포를 제조하는 방법. - 제49항에 있어서,
c) 상기 면역 세포 집단 내로 CCOR을 인코딩하는 제2 핵산을 도입하는 단계를 더 포함하는, 방법. - 제50항에 있어서, 상기 면역 세포 집단 내로 하나 이상의 COR을 인코딩하는 하나 이상의 핵산을 도입하는 단계를 더 포함하는, 방법.
- 제49항 내지 제51항 중 어느 한 항에 있어서, 상기 제1 핵산, 제2 핵산, 및/또는 COR 인코딩 핵산은 세포 내로 바이러스 벡터를 통해 도입되는, 방법.
- 제49항 내지 제52항 중 어느 한 항에 있어서, 상기 면역 세포 집단 내로 광범위 중화 항체(bNAb) 또는 HIV 융합 저해 펩타이드를 인코딩하는 핵산을 도입하는 단계를 더 포함하는, 방법.
- 제49항 내지 제53항 중 어느 한 항에 있어서, 상기 세포에서 CCR5 유전자를 비활성화시키는 단계를 더 포함하는, 방법.
- 제54항에 있어서, 상기 CCR5 유전자는 CRISPR/Cas9, TALEN, ZFN, siRNA, 및 안티센스 RNA로 이루어진 군으로부터 선택되는 방법을 사용하여 비활성화되는, 방법.
- 제49항 내지 제55항 중 어느 한 항에 있어서, 개체의 말초 혈액으로부터 상기 면역 세포 집단을 수득하는 단계를 더 포함하는, 방법.
- 제56항에 있어서, 상기 면역 세포 집단은 CD4+ 세포에 대해 더 풍부화되는, 방법.
- 제56항 또는 제57항에 있어서, 상기 면역 세포 집단은 CD8+ 세포에 대해 더 풍부화되는, 방법.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CNPCT/CN2018/095650 | 2018-07-13 | ||
| CN2018095650 | 2018-07-13 | ||
| CNPCT/CN2019/087259 | 2019-05-16 | ||
| CN2019087259 | 2019-05-16 | ||
| PCT/CN2019/095738 WO2020011247A1 (en) | 2018-07-13 | 2019-07-12 | Co-receptor systems for treating infectious diseases |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20210031898A true KR20210031898A (ko) | 2021-03-23 |
Family
ID=69142117
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020217000571A KR20210031898A (ko) | 2018-07-13 | 2019-07-12 | 전염병을 치료하기 위한 공동수용체 시스템 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20210275589A1 (ko) |
| EP (1) | EP3820888A4 (ko) |
| JP (1) | JP7447388B2 (ko) |
| KR (1) | KR20210031898A (ko) |
| CN (1) | CN112334479A (ko) |
| AU (1) | AU2019302603A1 (ko) |
| SG (1) | SG11202012339WA (ko) |
| WO (1) | WO2020011247A1 (ko) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116064678A (zh) | 2016-01-15 | 2023-05-05 | 美国基因技术国际有限公司 | 用于活化γ-δT细胞的方法和组合物 |
| ES2911448T3 (es) | 2016-03-09 | 2022-05-19 | American Gene Tech Int Inc | Vectores combinados y métodos para el tratamiento del cáncer |
| IL300730A (en) | 2016-07-08 | 2023-04-01 | American Gene Tech Int Inc | Pre-HIV vaccine and immunotherapy |
| US11352646B2 (en) | 2018-11-05 | 2022-06-07 | American Gene Technologies International Inc. | Vector system for expressing regulatory RNA |
| US20220265711A1 (en) * | 2019-05-16 | 2022-08-25 | Nanjing Legend Biotech Co., Ltd. | Engineered immune cells comprising a recognition molecule |
| CA3170630A1 (en) * | 2020-03-03 | 2021-09-10 | American Gene Technologies International Inc. | On demand expression of exogenous factors in lymphocytes to treat hiv |
| WO2021180832A1 (en) | 2020-03-12 | 2021-09-16 | Universiteit Gent | Hybrid car and hybrid tcr cells to treat infectious diseases |
| WO2022171068A1 (en) * | 2021-02-09 | 2022-08-18 | Nanjing Legend Biotech Co., Ltd. | Engineered cells and uses thereof |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE550356T1 (de) * | 2006-05-03 | 2012-04-15 | Us Gov Health & Human Serv | Chimäre t-zellen-rezeptoren sowie entsprechende materialien und verwendungsverfahren |
| AU2013221672B2 (en) * | 2012-02-13 | 2017-11-09 | Seattle Children's Hospital D/B/A Seattle Children's Research Institute | Bispecific chimeric antigen receptors and therapeutic uses thereof |
| US10117896B2 (en) * | 2012-10-05 | 2018-11-06 | The Trustees Of The University Of Pennsylvania | Use of a trans-signaling approach in chimeric antigen receptors |
| US10836998B2 (en) * | 2014-02-14 | 2020-11-17 | Cellectis | Cells for immunotherapy engineered for targeting antigen present both on immune cells and pathological cells |
| KR20170090506A (ko) * | 2014-12-19 | 2017-08-07 | 다나-파버 캔서 인스티튜트 인크. | 키메라 항원 수용체 및 이의 사용 방법 |
| US10273300B2 (en) * | 2014-12-29 | 2019-04-30 | The Trustees Of The University Of Pennsylvania | Methods of making chimeric antigen receptor-expressing cells |
| PL3298033T5 (pl) * | 2015-05-18 | 2023-10-30 | TCR2 Therapeutics Inc. | Kompozycje i zastosowania medyczne do reprogramowania TCR z zastosowaniem białek fuzyjnych |
| US20160361360A1 (en) * | 2015-06-12 | 2016-12-15 | Immunomedics, Inc. | Disease therapy with chimeric antigen receptor (car) constructs and t cells (car-t) or nk cells (car-nk) expressing car constructs |
| MA42902A (fr) * | 2015-07-08 | 2018-05-16 | Univ Johns Hopkins | Lymphocytes infiltrant la moelle (mil) en tant que source de lymphocytes t pour une thérapie par des récepteurs chimériques d'un antigène (car) |
| US11458167B2 (en) * | 2015-08-07 | 2022-10-04 | Seattle Children's Hospital | Bispecific CAR T-cells for solid tumor targeting |
| AU2016326500A1 (en) * | 2015-09-22 | 2018-04-12 | The Trustees Of The University Of Pennsylvania | Method of redirecting T cells to treat HIV infection |
| US11052111B2 (en) * | 2015-12-08 | 2021-07-06 | Chimera Bioengineering, Inc. | Smart CAR devices and DE CAR polypeptides for treating disease and methods for enhancing immune responses |
| CN107793481A (zh) * | 2016-08-31 | 2018-03-13 | 南京传奇生物科技有限公司 | 一种靶向人cd123的嵌合受体配体及其应用 |
| IL292551B2 (en) * | 2016-10-07 | 2023-10-01 | Tcr2 Therapeutics Inc | Preparations and methods for reprogramming T-cell receptors using fusion proteins |
| CN108276493B (zh) * | 2016-12-30 | 2023-11-14 | 南京传奇生物科技有限公司 | 一种嵌合抗原受体及其应用 |
-
2019
- 2019-07-12 KR KR1020217000571A patent/KR20210031898A/ko unknown
- 2019-07-12 EP EP19834832.8A patent/EP3820888A4/en active Pending
- 2019-07-12 AU AU2019302603A patent/AU2019302603A1/en active Pending
- 2019-07-12 US US17/258,245 patent/US20210275589A1/en active Pending
- 2019-07-12 SG SG11202012339WA patent/SG11202012339WA/en unknown
- 2019-07-12 WO PCT/CN2019/095738 patent/WO2020011247A1/en unknown
- 2019-07-12 CN CN201980041985.3A patent/CN112334479A/zh active Pending
- 2019-07-12 JP JP2021500150A patent/JP7447388B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021524264A (ja) | 2021-09-13 |
| AU2019302603A1 (en) | 2021-01-14 |
| SG11202012339WA (en) | 2021-01-28 |
| CN112334479A (zh) | 2021-02-05 |
| JP7447388B2 (ja) | 2024-03-12 |
| EP3820888A1 (en) | 2021-05-19 |
| US20210275589A1 (en) | 2021-09-09 |
| EP3820888A4 (en) | 2022-04-27 |
| TW202019954A (zh) | 2020-06-01 |
| WO2020011247A1 (en) | 2020-01-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11976105B2 (en) | Antibody/T-cell receptor chimeric constructs and uses thereof | |
| JP7447388B2 (ja) | 感染性疾患の治療のための共受容体システム | |
| US20220265711A1 (en) | Engineered immune cells comprising a recognition molecule | |
| JP7228900B2 (ja) | 操作されたナチュラルキラー細胞およびその使用 | |
| CN107567461A (zh) | 制备嵌合抗原受体表达细胞的方法 | |
| JP2022513689A (ja) | 養子細胞療法におけるb細胞悪性腫瘍の投与および処置のための方法 | |
| US11078251B2 (en) | T cell receptors (TCR) and uses thereof for the diagnosis and treatment of diabetes | |
| WO2022171068A1 (en) | Engineered cells and uses thereof | |
| WO2024008177A1 (en) | Engineered cells and uses thereof | |
| JP2024062997A (ja) | 抗体/t細胞受容体キメラ構築物およびその使用 |