KR20200088348A - 내인성 t 세포 수용체의 표적화된 대체 - Google Patents
내인성 t 세포 수용체의 표적화된 대체 Download PDFInfo
- Publication number
- KR20200088348A KR20200088348A KR1020207015078A KR20207015078A KR20200088348A KR 20200088348 A KR20200088348 A KR 20200088348A KR 1020207015078 A KR1020207015078 A KR 1020207015078A KR 20207015078 A KR20207015078 A KR 20207015078A KR 20200088348 A KR20200088348 A KR 20200088348A
- Authority
- KR
- South Korea
- Prior art keywords
- tcr
- cells
- chain
- nucleic acid
- cell
- Prior art date
Links
- 108091008874 T cell receptors Proteins 0.000 title claims abstract description 351
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 title claims abstract description 327
- 210000001744 T-lymphocyte Anatomy 0.000 claims abstract description 379
- 238000000034 method Methods 0.000 claims abstract description 170
- 108090000623 proteins and genes Proteins 0.000 claims abstract description 102
- 150000007523 nucleic acids Chemical group 0.000 claims description 220
- 210000004027 cell Anatomy 0.000 claims description 192
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 131
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 118
- 108020004414 DNA Proteins 0.000 claims description 115
- 101710163270 Nuclease Proteins 0.000 claims description 101
- 102000053602 DNA Human genes 0.000 claims description 97
- 102000039446 nucleic acids Human genes 0.000 claims description 95
- 108020004707 nucleic acids Proteins 0.000 claims description 95
- 239000000427 antigen Substances 0.000 claims description 93
- 108091007433 antigens Proteins 0.000 claims description 93
- 102000036639 antigens Human genes 0.000 claims description 93
- 206010028980 Neoplasm Diseases 0.000 claims description 85
- 108020005004 Guide RNA Proteins 0.000 claims description 83
- 108091033409 CRISPR Proteins 0.000 claims description 70
- 238000003780 insertion Methods 0.000 claims description 53
- 230000037431 insertion Effects 0.000 claims description 53
- 201000011510 cancer Diseases 0.000 claims description 45
- 239000002773 nucleotide Substances 0.000 claims description 41
- 125000003729 nucleotide group Chemical group 0.000 claims description 41
- 210000004899 c-terminal region Anatomy 0.000 claims description 39
- 230000003612 virological effect Effects 0.000 claims description 33
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 29
- 238000004520 electroporation Methods 0.000 claims description 27
- 210000003162 effector t lymphocyte Anatomy 0.000 claims description 26
- 102100037272 T cell receptor beta constant 1 Human genes 0.000 claims description 23
- 108020004682 Single-Stranded DNA Proteins 0.000 claims description 13
- 230000008439 repair process Effects 0.000 claims description 13
- 210000003289 regulatory T cell Anatomy 0.000 claims description 12
- 238000001727 in vivo Methods 0.000 claims description 11
- 108010017070 Zinc Finger Nucleases Proteins 0.000 claims description 10
- 238000012258 culturing Methods 0.000 claims description 10
- 108010008532 Deoxyribonuclease I Proteins 0.000 claims description 9
- 102000007260 Deoxyribonuclease I Human genes 0.000 claims description 9
- 230000005782 double-strand break Effects 0.000 claims description 8
- 239000013603 viral vector Substances 0.000 claims description 8
- 102000004389 Ribonucleoproteins Human genes 0.000 claims description 7
- 108010081734 Ribonucleoproteins Proteins 0.000 claims description 7
- 239000012636 effector Substances 0.000 claims description 7
- 230000002103 transcriptional effect Effects 0.000 claims description 5
- 101150053558 TRBC1 gene Proteins 0.000 claims description 4
- 230000001131 transforming effect Effects 0.000 claims description 3
- 101150117561 TRBC2 gene Proteins 0.000 claims description 2
- 239000000203 mixture Substances 0.000 abstract description 27
- 102100025570 Cancer/testis antigen 1 Human genes 0.000 description 40
- 101000856237 Homo sapiens Cancer/testis antigen 1 Proteins 0.000 description 40
- 230000009258 tissue cross reactivity Effects 0.000 description 21
- 101000662909 Homo sapiens T cell receptor beta constant 1 Proteins 0.000 description 19
- 229920002477 rna polymer Polymers 0.000 description 17
- 101000662902 Homo sapiens T cell receptor beta constant 2 Proteins 0.000 description 16
- 102100037298 T cell receptor beta constant 2 Human genes 0.000 description 16
- 230000008685 targeting Effects 0.000 description 15
- 241000700605 Viruses Species 0.000 description 13
- 108020004999 messenger RNA Proteins 0.000 description 13
- 229920001184 polypeptide Polymers 0.000 description 12
- 108700028369 Alleles Proteins 0.000 description 11
- 208000023275 Autoimmune disease Diseases 0.000 description 11
- 239000002609 medium Substances 0.000 description 11
- 210000001266 CD8-positive T-lymphocyte Anatomy 0.000 description 10
- 210000004369 blood Anatomy 0.000 description 10
- 239000008280 blood Substances 0.000 description 10
- 230000000295 complement effect Effects 0.000 description 10
- 238000000338 in vitro Methods 0.000 description 10
- 108700024394 Exon Proteins 0.000 description 8
- 238000005520 cutting process Methods 0.000 description 8
- 238000002474 experimental method Methods 0.000 description 8
- 201000001441 melanoma Diseases 0.000 description 8
- 241000699670 Mus sp. Species 0.000 description 7
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 7
- 208000015181 infectious disease Diseases 0.000 description 7
- 230000001404 mediated effect Effects 0.000 description 7
- 210000004986 primary T-cell Anatomy 0.000 description 7
- 239000000047 product Substances 0.000 description 7
- 238000013518 transcription Methods 0.000 description 7
- 230000035897 transcription Effects 0.000 description 7
- 238000013519 translation Methods 0.000 description 7
- 239000013598 vector Substances 0.000 description 7
- 241000713666 Lentivirus Species 0.000 description 6
- 238000010586 diagram Methods 0.000 description 6
- 230000002147 killing effect Effects 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 230000001177 retroviral effect Effects 0.000 description 6
- 210000000952 spleen Anatomy 0.000 description 6
- 238000006467 substitution reaction Methods 0.000 description 6
- 238000010361 transduction Methods 0.000 description 6
- 230000026683 transduction Effects 0.000 description 6
- 108091026890 Coding region Proteins 0.000 description 5
- 108020004705 Codon Proteins 0.000 description 5
- 108010088729 HLA-A*02:01 antigen Proteins 0.000 description 5
- 108010002350 Interleukin-2 Proteins 0.000 description 5
- 239000000872 buffer Substances 0.000 description 5
- 230000022534 cell killing Effects 0.000 description 5
- 201000010099 disease Diseases 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 230000035755 proliferation Effects 0.000 description 5
- 230000001105 regulatory effect Effects 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- 210000000130 stem cell Anatomy 0.000 description 5
- 238000010453 CRISPR/Cas method Methods 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- 108020005202 Viral DNA Proteins 0.000 description 4
- 230000030833 cell death Effects 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 230000004927 fusion Effects 0.000 description 4
- 238000010362 genome editing Methods 0.000 description 4
- 238000010899 nucleation Methods 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 230000009467 reduction Effects 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 210000003171 tumor-infiltrating lymphocyte Anatomy 0.000 description 4
- 101150028074 2 gene Proteins 0.000 description 3
- 208000024893 Acute lymphoblastic leukemia Diseases 0.000 description 3
- 208000014697 Acute lymphocytic leukaemia Diseases 0.000 description 3
- 241000894006 Bacteria Species 0.000 description 3
- 208000035473 Communicable disease Diseases 0.000 description 3
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 3
- 102100027581 Forkhead box protein P3 Human genes 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 101000861452 Homo sapiens Forkhead box protein P3 Proteins 0.000 description 3
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 description 3
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 description 3
- 102100027268 Interferon-stimulated gene 20 kDa protein Human genes 0.000 description 3
- 208000006664 Precursor Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 238000002679 ablation Methods 0.000 description 3
- 238000011467 adoptive cell therapy Methods 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 239000011324 bead Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 210000000349 chromosome Anatomy 0.000 description 3
- 230000016396 cytokine production Effects 0.000 description 3
- -1 e.g. Proteins 0.000 description 3
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 3
- 210000002443 helper t lymphocyte Anatomy 0.000 description 3
- 230000001939 inductive effect Effects 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 230000035772 mutation Effects 0.000 description 3
- 230000006780 non-homologous end joining Effects 0.000 description 3
- 239000013641 positive control Substances 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 230000005783 single-strand break Effects 0.000 description 3
- 230000005945 translocation Effects 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 2
- 238000010354 CRISPR gene editing Methods 0.000 description 2
- 206010009944 Colon cancer Diseases 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 101100310856 Drosophila melanogaster spri gene Proteins 0.000 description 2
- 102000004190 Enzymes Human genes 0.000 description 2
- 108090000790 Enzymes Proteins 0.000 description 2
- 241000214054 Equine rhinitis A virus Species 0.000 description 2
- 241000710198 Foot-and-mouth disease virus Species 0.000 description 2
- 208000009329 Graft vs Host Disease Diseases 0.000 description 2
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 2
- 102100037850 Interferon gamma Human genes 0.000 description 2
- 108010074328 Interferon-gamma Proteins 0.000 description 2
- 108091092195 Intron Proteins 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 2
- 208000005718 Stomach Neoplasms Diseases 0.000 description 2
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 2
- 206010052779 Transplant rejections Diseases 0.000 description 2
- 125000000539 amino acid group Chemical group 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 230000004611 cancer cell death Effects 0.000 description 2
- 230000005880 cancer cell killing Effects 0.000 description 2
- 238000010822 cell death assay Methods 0.000 description 2
- 230000033077 cellular process Effects 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 208000029742 colonic neoplasm Diseases 0.000 description 2
- 230000000536 complexating effect Effects 0.000 description 2
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 230000007850 degeneration Effects 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 230000011559 double-strand break repair via nonhomologous end joining Effects 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 238000000684 flow cytometry Methods 0.000 description 2
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 206010017758 gastric cancer Diseases 0.000 description 2
- 208000024908 graft versus host disease Diseases 0.000 description 2
- 230000007062 hydrolysis Effects 0.000 description 2
- 238000006460 hydrolysis reaction Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 208000027866 inflammatory disease Diseases 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 210000004698 lymphocyte Anatomy 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 244000052769 pathogen Species 0.000 description 2
- 230000001717 pathogenic effect Effects 0.000 description 2
- 239000013610 patient sample Substances 0.000 description 2
- 239000013612 plasmid Substances 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 230000001323 posttranslational effect Effects 0.000 description 2
- 238000010839 reverse transcription Methods 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 238000004513 sizing Methods 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 201000011549 stomach cancer Diseases 0.000 description 2
- 238000001847 surface plasmon resonance imaging Methods 0.000 description 2
- 238000013414 tumor xenograft model Methods 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- ZLCOWUKVVFVVKA-WDSKDSINSA-N (2r)-3-[[(2r)-2-acetamido-2-carboxyethyl]disulfanyl]-2-aminopropanoic acid Chemical compound CC(=O)N[C@H](C(O)=O)CSSC[C@H](N)C(O)=O ZLCOWUKVVFVVKA-WDSKDSINSA-N 0.000 description 1
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 1
- VGONTNSXDCQUGY-RRKCRQDMSA-N 2'-deoxyinosine Chemical group C1[C@H](O)[C@@H](CO)O[C@H]1N1C(N=CNC2=O)=C2N=C1 VGONTNSXDCQUGY-RRKCRQDMSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- 241001156739 Actinobacteria <phylum> Species 0.000 description 1
- 208000031261 Acute myeloid leukaemia Diseases 0.000 description 1
- 108091093088 Amplicon Proteins 0.000 description 1
- 108020004491 Antisense DNA Proteins 0.000 description 1
- 241001142141 Aquificae <phylum> Species 0.000 description 1
- 241000203069 Archaea Species 0.000 description 1
- 208000028564 B-cell non-Hodgkin lymphoma Diseases 0.000 description 1
- 241000605059 Bacteroidetes Species 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- 229940123205 CD28 agonist Drugs 0.000 description 1
- 201000009030 Carcinoma Diseases 0.000 description 1
- 102000020313 Cell-Penetrating Peptides Human genes 0.000 description 1
- 108010051109 Cell-Penetrating Peptides Proteins 0.000 description 1
- 241000191368 Chlorobi Species 0.000 description 1
- 241001142109 Chloroflexi Species 0.000 description 1
- 241000192700 Cyanobacteria Species 0.000 description 1
- 102220605874 Cytosolic arginine sensor for mTORC1 subunit 2_D10A_mutation Human genes 0.000 description 1
- 241000702421 Dependoparvovirus Species 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 108010042407 Endonucleases Proteins 0.000 description 1
- 102000004533 Endonucleases Human genes 0.000 description 1
- 108060002716 Exonuclease Proteins 0.000 description 1
- 229920001917 Ficoll Polymers 0.000 description 1
- 241000192125 Firmicutes Species 0.000 description 1
- 241001663880 Gammaretrovirus Species 0.000 description 1
- 208000017604 Hodgkin disease Diseases 0.000 description 1
- 208000021519 Hodgkin lymphoma Diseases 0.000 description 1
- 208000010747 Hodgkins lymphoma Diseases 0.000 description 1
- 101001023379 Homo sapiens Lysosome-associated membrane glycoprotein 1 Proteins 0.000 description 1
- 102100034343 Integrase Human genes 0.000 description 1
- 108010061833 Integrases Proteins 0.000 description 1
- 108010002586 Interleukin-7 Proteins 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 1
- 102100035133 Lysosome-associated membrane glycoprotein 1 Human genes 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 208000033776 Myeloid Acute Leukemia Diseases 0.000 description 1
- 108091061960 Naked DNA Proteins 0.000 description 1
- 206010029260 Neuroblastoma Diseases 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 208000012868 Overgrowth Diseases 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 241000192142 Proteobacteria Species 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 241001180364 Spirochaetes Species 0.000 description 1
- 241000193996 Streptococcus pyogenes Species 0.000 description 1
- 230000005867 T cell response Effects 0.000 description 1
- 101710137500 T7 RNA polymerase Proteins 0.000 description 1
- 208000024313 Testicular Neoplasms Diseases 0.000 description 1
- 206010057644 Testis cancer Diseases 0.000 description 1
- 241001143310 Thermotogae <phylum> Species 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 239000011543 agarose gel Substances 0.000 description 1
- 150000001413 amino acids Chemical group 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 239000003816 antisense DNA Substances 0.000 description 1
- 238000002617 apheresis Methods 0.000 description 1
- 238000000429 assembly Methods 0.000 description 1
- 230000000712 assembly Effects 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 102000012740 beta Adrenergic Receptors Human genes 0.000 description 1
- 108010079452 beta Adrenergic Receptors Proteins 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 238000005251 capillar electrophoresis Methods 0.000 description 1
- 101150038500 cas9 gene Proteins 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 230000011712 cell development Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 238000002659 cell therapy Methods 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- 239000013599 cloning vector Substances 0.000 description 1
- 238000003501 co-culture Methods 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000007123 defense Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 238000002716 delivery method Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 230000034431 double-strand break repair via homologous recombination Effects 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 238000004043 dyeing Methods 0.000 description 1
- 102000013165 exonuclease Human genes 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 238000000799 fluorescence microscopy Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 108020001507 fusion proteins Proteins 0.000 description 1
- 102000037865 fusion proteins Human genes 0.000 description 1
- 238000001502 gel electrophoresis Methods 0.000 description 1
- 238000010363 gene targeting Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 201000007270 liver cancer Diseases 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 210000003071 memory t lymphocyte Anatomy 0.000 description 1
- 108091070501 miRNA Proteins 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 239000002071 nanotube Substances 0.000 description 1
- 239000002070 nanowire Substances 0.000 description 1
- 210000000581 natural killer T-cell Anatomy 0.000 description 1
- 210000004940 nucleus Anatomy 0.000 description 1
- 230000009437 off-target effect Effects 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 201000008968 osteosarcoma Diseases 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 1
- 210000001778 pluripotent stem cell Anatomy 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- GUUBJKMBDULZTE-UHFFFAOYSA-M potassium;2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid;hydroxide Chemical compound [OH-].[K+].OCCN1CCN(CCS(O)(=O)=O)CC1 GUUBJKMBDULZTE-UHFFFAOYSA-M 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 238000011533 pre-incubation Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 230000008707 rearrangement Effects 0.000 description 1
- 108010054624 red fluorescent protein Proteins 0.000 description 1
- 230000008263 repair mechanism Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000012679 serum free medium Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 201000003120 testicular cancer Diseases 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 201000002144 testis rhabdomyosarcoma Diseases 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 238000007492 two-way ANOVA Methods 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 238000012447 xenograft mouse model Methods 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4611—T-cells, e.g. tumor infiltrating lymphocytes [TIL], lymphokine-activated killer cells [LAK] or regulatory T cells [Treg]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/463—Cellular immunotherapy characterised by recombinant expression
- A61K39/4632—T-cell receptors [TCR]; antibody T-cell receptor constructs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/4644—Cancer antigens
- A61K39/464484—Cancer testis antigens, e.g. SSX, BAGE, GAGE or SAGE
- A61K39/464488—NY-ESO
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/87—Introduction of foreign genetic material using processes not otherwise provided for, e.g. co-transformation
- C12N15/90—Stable introduction of foreign DNA into chromosome
- C12N15/902—Stable introduction of foreign DNA into chromosome using homologous recombination
- C12N15/907—Stable introduction of foreign DNA into chromosome using homologous recombination in mammalian cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
- C12N5/0637—Immunosuppressive T lymphocytes, e.g. regulatory T cells or Treg
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/16—Hydrolases (3) acting on ester bonds (3.1)
- C12N9/22—Ribonucleases RNAses, DNAses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5156—Animal cells expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5158—Antigen-pulsed cells, e.g. T-cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/20—Type of nucleic acid involving clustered regularly interspaced short palindromic repeats [CRISPRs]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
- C12N2510/02—Cells for production
Abstract
본원에서는 인간 T 세포의 게놈을 편집하기 위한 방법 및 조성물을 제공한다. 일부 실시양태에서, 이종성 T 세포 수용체 (TCR)-β 쇄 및 이종성 TCR-α 쇄는 T 세포의 게놈 중 TCR 서브유닛 불변 유전자의 엑손 1 내로 삽입된다.
Description
선행 관련 출원
본 출원은 2017년 10월 27일에 출원된 미국 가출원 번호 62/578,153의 이익을 주장하며, 이 가출원은 그 전문이 본원에서 참조로 포함된다.
T 세포는 성장하고 있는 입양 세포 치료제 분야에서 가장 활발하게 연구되는 세포 유형이다. T 세포는 최소의 부작용을 갖고 고도로 특이적인 반응을 할 수 있는 그의 T 세포 수용체 (TCR)의 표적과 특이적으로 상호작용한다. 이러한 고도로 효과적이고, 특이적인 반응은 원하는 특이성을 갖는 새로운 수용체를 T 세포 내로 삽입함으로써 신규한 항원 및 표적에 대해 이루어지도록 조작될 수 있다. 그러나, 완전히 새로운 유형의 수용체를 개발하는데 많은 시간이 소요되고, 고가의 비용이 들며, 이는 신체가 자연적으로 내인성 T 세포 레퍼토리의 발생을 통해 거의 모든 가능한 항원성 표적에 결합하는 TCR을 생산한다는 사실을 활용하지도 못한다. 인간 T 세포를 수득할 수 있고, 그의 내인성 TCR을 원하는 항원 특이성을 갖는 TCR로 대체할 수 있는 능력은 입양 T 세포 요법의 개발 및 적용에서 혁신적인 것이 될 수 있다.
본 개시내용은 인간 T 세포의 게놈을 편집하기 위한 조성물 및 방법에 관한 것이다. 본 발명자들은 이종성 TCR은 T 세포의 게놈 중 표적화된 영역 내로 삽입될 수 있고, 이로써, 이종성 TCR은 내인성 TCR 프로모터의 제어 하에 있게 된다는 것을 발견하게 되었다. 본원에 제공된 방법 및 조성물을 이용하여 인간 T 세포 중 내인성 TCR을 원하는 항원 특이성을 갖는 이종성 TCR로 대체시킬 수 있다. 일부 실시양태에서, T 세포의 게놈 중 표적화된 영역은 천연 T 세포 수용체 로커스이다.
일부 실시양태에서, 본 개시내용은 인간 T 세포의 게놈을 편집하는 방법을 제공한다. 일부 실시양태에서, 방법은 인간 T 세포에서 T 세포 수용체 (TCR)-서브유닛 불변 유전자의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) TCR 서브유닛 쇄가 TCR 서브유닛의 가변 영역 및 불변 영역을 포함하는 것인 제1 이종성 TCR 서브유닛 쇄; (iii) 제2 자기-절단 펩티드 서열; (iv) 제2 이종성 TCR 서브유닛 쇄의 가변 영역; 및 (v) 내인성 TCR 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 삽입하는 것을 포함하며, 여기서 내인성 TCR 서브유닛이 TCR-알파 (TCR-α) 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-베타 (TCR-β) 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이며, 여기서 내인성 TCR 서브유닛이 TCR-β 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-β 서브유닛 쇄인 것을 포함한다. 일부 실시양태에서, 방법은 인간 T 세포에서 TCR 알파 서브유닛 불변 유전자 (TRAC)의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-β 쇄; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역; 및 (v) 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 삽입하는 것을 포함한다.
일부 실시양태에서, 방법은 인간 T 세포에서 TCR-베타 서브유닛 불변 유전자 (TRBC)의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-α 쇄; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-β 쇄의 가변 영역; 및 (v) 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 삽입하는 것을 포함한다.
일부 실시양태에서, 핵산은 핵산을 포함하는 바이러스 벡터를 T 세포 내로 도입함으로써 삽입된다. 일부 실시양태에서, 핵산은 핵산을 포함하는 비-바이러스 벡터를 T 세포 내로 도입함으로써 삽입된다. 일부 실시양태에서, 핵산은 T 세포 내로 (a) TCR-α 서브유닛 불변 유전자 (TRAC)의 엑손 1 내의 표적 영역을 절단하여 T 세포의 게놈 중에 삽입 부위를 생성하는 표적화된 뉴클레아제; 및 (b) 핵산 서열을 도입함으로써 T 세포 내로 도입함으로써 삽입되며, 여기서 핵산 서열은 상동성 지정 복구 (HDR)에 의해 삽입 부위 내로 도입된다. 일부 실시양태에서, 핵산은 T 세포 내로 (a) TCR-β 서브유닛 불변 유전자 (TRBC)의 엑손 1 내의 표적 영역을 절단하여 T 세포의 게놈 중에 삽입 부위를 생성하는 표적화된 뉴클레아제; 및 (b) 핵산 서열을 도입함으로써 T 세포 내로 도입함으로써 삽입되며, 여기서 핵산 서열은 상동성 지정 복구 (HDR)에 의해 삽입 부위 내로 도입된다. 일부 실시양태에서, 핵산의 5' 말단 및 3' 말단은 표적 영역에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태에서, 핵산의 5' 말단 및 3' 말단은 삽입 부위에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태에서, 표적화된 뉴클레아제는 삽입 부위에 이중 가닥 파단을 도입한다. 일부 실시양태에서, 핵산 서열은 이중 가닥으로 또는 단일 가닥 핵산으로서 세포 내로 도입된다. 일부 실시양태에서, 핵산은 이중 가닥 또는 단일 가닥 DNA 주형으로서 세포 내로 도입된다. 일부 실시양태에서, 핵산 서열은 선형 핵산으로서 세포 내로 도입된다.
일부 실시양태에서, 제1 자기-절단 펩티드 및 제2 자기-절단 펩티드는 동일하거나 또는 상이한 바이러스 2A 펩티드이다.
일부 실시양태에서, 표적화된 뉴클레아제는 RNA-가이드된 뉴클레아제 도메인, 전사 활성인자-유사 이펙터 뉴클레아제 (TALEN), 아연 핑거 뉴클레아제 (ZFN) 및 메가TAL로 이루어진 군으로부터 선택된다. 일부 실시양태에서, RNA-가이드된 뉴클레아제는 Cpf1 뉴클레아제 또는 Cas9 뉴클레아제이고, 방법은 세포 내로 TRAC의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함한다. 일부 실시양태에서, Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 가이드 RNA 및 핵산은 리보핵단백질 복합체 (RNP)-DNA 주형 복합체로서 세포 내로 도입되며, 여기서 RNP-DNA 주형 복합체는 (i) Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 및 가이드 RNA를 포함하는 RNP; 및 (ii) DNA 주형을 포함한다.
일부 실시양태에서, 복합체 중 RNP 대 DNA 주형의 몰비는 약 3:1 내지 약 100:1이다. 일부 실시양태에서, RNP-DNA 주형 복합체는 약 20℃ 내지 25℃의 온도에서 약 10 내지 약 30분 동안 RNP를 DNA 주형과 함께 인큐베이션함으로써 형성된다. 일부 실시양태에서, RNP-DNA 주형 복합체를 세포 내로 도입하기 전에 RNP-DNA 주형 복합체 및 세포를 혼합한다. 일부 실시양태에서, RNP-DNA 주형 복합체는 적어도 2개의 구조적으로 상이한 RNP 복합체를 포함한다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 RNP 복합체는 구조적으로 상이한 가이드 RNA를 함유한다. 일부 실시양태에서, 구조적으로 상이한 RNP 복합체는 각각 Cas9 닉카제를 포함하고, 구조적으로 상이한 가이드 RNA는 표적 영역의 반대 가닥에 하이브리드화한다.
일부 실시양태에서, 도입은 전기천공을 포함한다. 일부 실시양태에서, 핵산은 약 1 × 105 내지 약 2 × 106개 T 세포의 집단 내로 도입된다. 일부 예에서, 표적화된 뉴클레아제 및 DNA 주형은 약 1 × 105 내지 약 2 × 106개 T 세포의 집단 내로 도입된다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 DNA 주형은 세포 내로 도입된다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 DNA 주형은 비-바이러스 주형이다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 DNA 주형은 각각 항원 특이적 T 세포 수용체의 이종성 TCR-β 쇄의 가변 영역, 및 항원 특이적 T 세포 수용체의 이종성 TCR-α 쇄의 가변 영역의 고유한 조합을 코딩한다. 일부 실시양태에서, T 세포는 조절 T 세포, 이펙터 T 세포, 또는 나이브 T 세포이다. 일부 실시양태에서, T 세포는 이펙터 T 세포이며, 여기서 이펙터 T 세포는 CD8+ T 세포이다. 일부 실시양태에서, T 세포는 이펙터 T 세포이며, 여기서 이펙터 T 세포는 CD4+ T 세포이다. 일부 실시양태에서, 이펙터 T 세포는 CD4+CD8+ T 세포이다.
일부 실시양태에서, 방법은 T 세포를 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 발현을 허용하는 조건 하에서 배양하여 항원-특이적 T 세포 수용체를 형성하는 것을 추가로 포함한다. 일부 실시양태에서, 방법은 변형된 T 세포를 변형된 세포의 집단을 확장시키는데 효과적인 조건 하에서 배양하는 것을 추가로 포함한다. 일부 실시양태에서, 방법은 항원-특이적 T 세포 수용체를 발현하는 T 세포를 정제하는 것을 추가로 포함한다.
일부 실시양태에서, 본 개시내용은 (a) 인간 T 세포에서 TCR 알파 서브유닛 불변 유전자 (TRAC)의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 자기-절단 펩티드 서열; (ii) 항원 특이적 T 세포 수용체의 이종성 TCR-α 쇄; 및 (iii) 내인성 TCR 알파 서브유닛의 엑손 1의 N-말단 부분을 코딩하는 제1 핵산 서열을 삽입하는 것; 및 (b) 인간 T 세포에서 TCR 베타 서브유닛 불변 유전자 (TRBC)의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제2 자기-절단 펩티드 서열; (ii) 항원 특이적 T 세포 수용체의 이종성 TCR-β 쇄; 및 (iii) 내인성 TCR 베타 서브유닛의 엑손 1의 N-말단 부분을 코딩하는 제2 핵산 서열을 삽입하는 것을 포함하는, 인간 T 세포의 게놈을 편집하는 방법을 제공한다.
일부 실시양태에서, 제1 및/또는 제2 핵산 서열은 제1 및/또는 제2 핵산을 포함하는 바이러스 벡터를 T 세포에 도입함으로써 삽입된다. 일부 실시양태에서, 제1 및/또는 제2 핵산 서열은 제1 및/또는 제2 핵산을 포함하는 비-바이러스 벡터를 T 세포에 도입함으로써 삽입된다. 일부 실시양태에서, 제1 및 제2 핵산은 (a) TRAC의 엑손 1에 제1 삽입 부위, 및 TCR 베타 서브유닛 불변 유전자 (TRBC)의 엑손 1에 제2 삽입 부위를 생성하는 하나 이상의 표적화된 뉴클레아제; 및 (b) 제1 핵산 서열; 및 (c) 제2 핵산 서열을 도입함으로써 T 세포에 삽입되며, 여기서 제1 핵산 서열은 TRAC의 엑손 1 중 제1 삽입 부위 내로 삽입되고, 제2 핵산 서열은 상동성 지정 복구 (HDR)에 의해 TRBC의 엑손 1 중 제2 삽입 부위 내로 삽입된다. 일부 실시양태에서, 핵산 서열은 이중 가닥 또는 단일 가닥 DNA 주형으로서 세포 내로 도입된다. 일부 실시양태에서, 핵산 서열은 선형 DNA 주형으로서 세포 내로 도입된다.
일부 실시양태에서, 제1 핵산 서열의 5' 말단 및 3' 말단은 TRAC 유전자의 엑손 1 내의 표적 영역에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태에서, 제1 핵산 서열의 5' 말단 및 3' 말단은 TRAC 유전자의 엑손 1 내의 제1 삽입 부위에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태에서, 제2 핵산 서열의 5' 말단 및 3' 말단은 TRBC 유전자의 엑손 1 내의 표적 영역에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태에서, 제2 핵산 서열의 5' 말단 및 3' 말단은 TRBC 유전자의 엑손 1 내의 제2 삽입 부위에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다.
일부 실시양태에서, 하나 이상의 표적화된 뉴클레아제는 제1 및 제2 삽입 부위에 이중 가닥 파단을 도입한다. 일부 실시양태에서, 제1 자기-절단 펩티드 및 제2 자기-절단 펩티드는 동일하거나 또는 상이한 바이러스 2A 펩티드이다. 일부 실시양태에서, 하나 이상의 표적화된 뉴클레아제는 RNA-가이드된 뉴클레아제 도메인, 전사 활성인자-유사 이펙터 뉴클레아제 (TALEN), 아연 핑거 뉴클레아제 (ZFN) 또는 메가TAL로 이루어진 군으로부터 선택된다.
일부 실시양태에서, RNA-가이드된 뉴클레아제는 Cpf1 뉴클레아제 또는 Cas9 뉴클레아제이고, 방법은 세포 내로 TRAC의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 제1 가이드 RNA, 및 TRBC의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 제2 가이드 RNA를 도입하는 것을 추가로 포함한다. 일부 실시양태에서, Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 제1 가이드 RNA 및 제1 핵산은 리보핵단백질 복합체 (RNP)-DNA 주형 복합체로서 세포 내로 도입되며, 여기서 RNP-DNA 주형 복합체는 (i) Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 및 제1 가이드 RNA를 포함하는 RNP; 및 (ii) 제1 DNA 주형을 포함한다. 일부 실시양태에서, Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 제2 가이드 RNA, 및 제2 핵산은 RNP-DNA 주형 복합체로서 세포 내로 도입되며, 여기서 RNP-DNA 주형 복합체는 (i) Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 및 제2 가이드 RNA를 포함하는 RNP; 및 (ii) 제2 DNA 주형을 포함한다.
일부 실시양태에서, 복합체 중 RNP 대 DNA 주형의 몰비는 약 3:1 내지 약 100:1이다. 일부 실시양태에서, RNP-DNA 주형 복합체는 약 20℃ 내지 25℃의 온도에서 약 10 내지 약 30분 동안 RNP를 DNA 주형과 함께 인큐베이션함으로써 형성된다. 일부 실시양태에서, RNP-DNA 주형 복합체는 적어도 2개의 구조적으로 상이한 RNP 복합체를 포함한다. 일부 실시양태에서, 구조적으로 상이한 RNP 복합체는 각각 Cas9 닉카제를 포함하고, 구조적으로 상이한 가이드 RNA는 표적 영역의 반대 가닥에 하이브리드화한다. 일부 실시양태에서, 도입은 전기천공을 포함한다.
일부 실시양태에서, 제1 및 제2 핵산은 약 1 × 105 내지 약 2 × 106개 T 세포 내로 도입된다. 일부 실시양태에서, 하나 이상의 표적화된 뉴클레아제 및 제1 및 제2 핵산은 약 1 × 105 내지 약 2 × 106개 T 세포 내로 도입된다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 제1 DNA 주형은 세포 내로 도입된다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 제1 DNA 주형은 항원 특이적 T 세포 수용체의 TCR-α 쇄의 상이한 가변 영역을 포함한다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 제2 DNA 주형은 세포 내로 도입된다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 제2 DNA 주형은 항원 특이적 T 세포 수용체의 TCR-β 쇄의 상이한 가변 영역을 포함한다.
일부 실시양태에서, T 세포는 조절 T 세포, 이펙터 T 세포, 또는 나이브 T 세포이다. 일부 실시양태에서, T 세포는 이펙터 T 세포이며, 여기서 이펙터 T 세포는 CD8+ T 세포이다. 일부 실시양태에서, T 세포는 이펙터 T 세포이며, 여기서 이펙터 T 세포는 CD4+ T 세포이다. 일부 실시양태에서, 이펙터 T 세포는 CD4+CD8+ T 세포이다.
일부 실시양태에서, 방법은 T 세포를 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 발현을 허용하는 조건 하에서 배양하여 항원-특이적 T 세포 수용체를 형성하는 것을 추가로 포함한다. 일부 실시양태에서, 방법은 T 세포를 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 발현을 허용하는 조건 하에서 배양하여 항원-특이적 T 세포 수용체를 형성하는 것을 추가로 포함한다. 일부 실시양태에서, 방법은 변형된 T 세포를 변형된 세포의 집단을 확장시키는데 효과적인 조건 하에서 배양하는 것을 추가로 포함한다. 일부 실시양태에서, 방법은 항원-특이적 T 세포 수용체를 발현하는 T 세포를 정제하는 것을 추가로 포함한다.
다른 실시양태에서, 본 개시내용은 변형된 T 세포로서, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 T 세포 수용체 (TCR)-β 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역; 및 (v) 내인성 TCR 알파 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함하며, 여기서 핵산 서열은 TRAC 유전자의 엑손 1 내로 통합되는 것인 변형된 T 세포를 제공한다.
일부 실시양태에서, 본 개시내용은 변형된 T 세포로서, a) N-말단에서 C-말단으로, (i) 제1 자기-절단 서열, (ii) 이종성 TCR-α 쇄의 가변 영역, 및 (iii) 내인성 TCR-α 쇄의 N-말단 부분을 코딩하는 제1 핵산 서열; 및 b) N-말단에서 C-말단으로, (i) 제1 자기-절단 서열, (ii) 이종성 TCR-β 쇄의 가변 영역, 및 (iii) 내인성 TCR-β 쇄의 N-말단 부분을 코딩하는 제2 핵산 서열을 포함하며, 여기서 제1 핵산 서열은 TRAC 유전자의 엑손 1 내로 통합되고, 제2 핵산 서열은 TRBC 유전자의 엑손 1 내로 통합되는 것인 변형된 T 세포를 추가로 제공한다.
일부 실시양태에서, 본 개시내용은 인간 대상체에서 암을 치료하는 방법으로서, a) 대상체로부터 T 세포를 수득하는 단계; b) 이종성 항원-특이적 T 세포 수용체를 발현하도록 T 세포를 변형시키는 단계로서, 여기서 T 세포 수용체는 대상체에서 종양-특이적 항원을 인식하는 것인 단계; 및 c) 대상체에게 변형된 T 세포를 투여하는 단계를 포함하는 방법을 추가로 제공한다.
이종성 TCR-α 쇄 및 이종성 TCR-β 쇄를 발현하도록 T 세포를 변형시키기 위해 본원에 기재된 방법 및 조성물을 사용하여 인간 감마 델타 (γδ) T 세포를 또한 편집할 수 있다. 예를 들어, 일부 실시양태에서, 방법은 인간 T 세포에서 T 세포 수용체 감마 서브유닛 불변 (TRGC) 유전자의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-β 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역; 및 (v) 내인성 TCR-α의 N-말단 부분을 코딩하는 핵산 서열을 삽입하는 것을 포함한다.
다른 실시양태에서, 방법은 핵산 삽입 시, 이종성 TCR-β 및 TCR-α 서열을 코딩하는 핵산은 내인성 TCR-γ 프로모터의 제어 하에 있도록, 인간 T 세포에서 T 세포 수용체 감마 서브유닛 불변 (TRGC) 유전자의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-β 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 전장 이종성 TCR-α 쇄; 및 (v) 정지 코돈을 코딩하는 핵산 서열을 삽입하는 것을 포함한다.
다른 실시양태에서, 방법은 인간 T 세포에서 T 세포 수용체 감마 서브유닛 불변 (TRGC) 유전자의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-δ 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-γ 쇄의 가변 영역; 및 (v) 내인성 TCR-γ 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 삽입하는 것을 포함한다. 또한, 인간 T 세포에서 TRAC 유전자의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-γ 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-δ 쇄의 가변 영역; 및 (v) 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 삽입하는 것을 포함하는, 인간 T 세포의 게놈을 편집하는 방법을 또한 제공한다. 다른 실시양태에서, 방법은 핵산 삽입 시, 이종성 TCR-γ 및 TCR-δ 서열이 내인성 TCR-α 프로모터의 제어 하에 있도록, 인간 T 세포에서 T 세포 수용체 감마 서브유닛 불변 (TRAC) 유전자의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-γ 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 전장 이종성 TCR-δ 쇄; 및 (v) 정지 코돈을 코딩하는 핵산 서열을 삽입하는 것을 포함한다.
본 출원은 하기 도면을 포함한다. 도면은 조성물 및 방법의 특정 실시양태 및/또는 특징을 예시하고, 조성물및 방법의 임의의 설명(들)을 보충하기 위한 것으로 의도된다. 서면 설명이 그러한 경우임을 분명하게 명시하지 않는 한, 본 도면이 조성물 및 방법의 범주를 제한하지 않는다.
도 1a는 상동성 지정 복구를 통한, N-말단에서 C-말단으로, (i) T2A 자기-절단 펩티드 서열; (ii) 전장 (즉, 가변 영역 및 불변 영역)의 이종성 TCR-β 쇄 (NYESO-β); (iii) P2A 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역 (NYESO-α); 및 (v) 내인성 TCR 알파 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함하는 단일 비-바이러스 DNA 주형의 T 세포 내로의 삽입을 도시한 개략도이다. 상동성 지정 복구를 통한 TRAC 유전자의 엑손 1에의 DNA 주형 삽입 후, DNA 주형을 전사시키고, 번역시켜 NY-ESO-1 흑색종 신생항원을 인식하는 항원-특이적 TCR을 형성하는 전장 NYESO-β 쇄 및 전장 NYESO-α 쇄를 제조하였다.
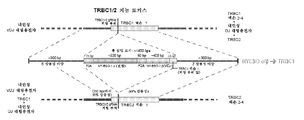
도 1b는 TCR-β 로커스 (TRBC1 또는 TRBC2)에서의 단일 비-바이러스 DNA 주형의 삽입을 도시한 개략도이다. 주형은 상동성 지정 복구를 통한 T 세포 내의, N-말단에서 C-말단으로, (i) T2A 자기-절단 펩티드 서열; (ii) 전장 (즉, 가변 영역 및 불변 영역) 이종성 TCR-α 쇄 (NYESO-α); (iii) P2A 자기-절단 펩티드 서열; (iv) 이종성 TCR-β 쇄의 가변 영역 (NYESO-β); 및 (v) 내인성 TCR 베타 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함한다.
도 2는 (a) N-말단에서 C-말단으로, (i) P2A 자기-절단 펩티드 서열, (ii) 항원 특이적 T 세포 수용체의 TCR-α 쇄의 가변 영역 (NYESO-α); 및 (iii) 내인성 TCR-α 서브유닛의 엑손 1의 N-말단 부분을 코딩하는 핵산 서열을 포함하는 비-바이러스 DNA 주형; 및 (b) N-말단에서 C-말단으로, (i) T2A 자기-절단 펩티드 서열, (ii) 항원 특이적 T 세포 수용체의 TCR-β 쇄의 가변 영역; 및 (iii) 내인성 TCR-β 서브유닛의 엑손 1의 N-말단 부분을 코딩하는 핵산 서열을 포함하는 DNA 주형을 삽입함으로써 수행된, 내인성 T 세포 α 및 T 세포 β 수용체 쇄 둘 다의 동시 대체를 도시한 개략도이다.
도 3a는 T 세포 수용체의 폴리클로날 라이브러리를 형성하기 위한 T 세포에서의 이종성 (TCR)-β 쇄 및 TCR-α 쇄의 삽입을 도시한 개략도이다. N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 전장 (예를 들어 가변 영역 및 불변 영역) 이종성 T 세포 수용체 (TCR)-β 쇄; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역; 및 (v) 내인성 TCR 알파 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 함유하는 다중의 상이한 DNA 주형, 예를 들어, 비-바이러스 DNA 주형을 동시에 전기천공하여 원하는 TCR 서열의 합성 T 세포 레퍼토리를 포함하는 T 세포의 집단을 생성하였다.
도 3b는 앞서 공지된 TCR 서열로부터, 또는 관심 내인성 T 세포 집단에서의 천연 레퍼토리로부터, 예를 들어, 대상체로부터의 T 세포 레퍼토리의 디자인을 제시하는 개략도이다. 예를 들어, TCR은 종양 침윤 림프구에 의해 발현되는 TCR, 자가면역 질환의 부위에서의 자가반응성 T 세포에 의해 발현되는 TCR, 또는 병원체 반응성 T 세포로부터의 TCR일 수 있지만, 이에 제한되지는 않는다.
도 4a는 이종성 NYESO TCR로 전기천공된 CD4+ 및 CD8+ T 세포의 FACS 분석을 제시한다. 2명의 건강한 인간 혈액 공여자로부터의 CD4+ 및 CD8+ T 세포를 상기 기재된 바와 같이, 이종성 NYESO-α 및 이종성 NYESO-β를 포함하는 비-바이러스 구축물로 전기천공하였다. 전기천공 후 4일째, 세포를 통합된 NYESO-특이적 TCR에 의해 인식되는 펩티드를 함유하는 형광 표지된 MHC-덱스트라머로 염색하였다.
도 4b는 이종성 NYESO TCR로 전기천공된 CD8+ T 세포의 FACS 분석을 제시한다. 건강한 인간 혈액 공여자로부터의 CD8+ T 세포를 상기 기재된 바와 같이, 이종성 NYESO-α 및 이종성 NYESO-β를 포함하는 비-바이러스 DNA 구축물로 전기천공하였다. 전기천공 후 4일째, 세포를 통합된 NYESO-특이적 TCR에 의해 인식되는 펩티드를 함유하는 형광 표지된 MHC-덱스트라머로 염색하였다.
도 5는 이종성 NYESO TCR로 전기천공된 CD8+ 세포의 FACS 분석이다. 세포를 도 3 및 4에서와 같이 처리하였고, NYESO MHC-덱스트라머를 이용한 항원 특이적 염색 대비로 (모든 잠재적 인간 TCR에 결합하는 항체를 이용한) TCR 발현에 대한 염색을 추가로 수행하였다. 내인성 TCR의 상동성 지정 대체가 없는 대부분의 T 세포에서, TRAC 엑손 1 gRNA에 의한 커팅 및 비-상동성 말단 연결에 의한 작은 삽입 결실 돌연변이 (indel)의 도입에 기인하여 내인성 TCR은 녹아웃되었다. 예상대로, NYESO 양성 세포는 거의 모두 TCR 발현에 대해서도 양성이었다.
도 6a는 시험관내 세포 사멸 검정법에서 이종성 NYESO TCR을 함유하는 1차 인간 T 세포가 암 세포를 사멸시킨다는 것을 제시한다.
도 6b는 사멸시키는, 이종성 NYESO TCR을 함유하는 인간 T 세포를 사용하는 시험관내 세포 사멸 검정법으로부터의 단일 시점으로부터의 결과를 제시한다.
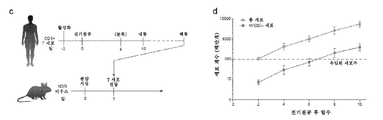
도 7a-f는 비-바이러스 TCR 대체가 이루어진 T 세포의 생체내 기능성을 제시한다. (a) 생체내 인간 항원 특이적 종양 이종이식편 모델의 다이어그램. (b) 5x106개 벌크 비-바이러스에 의해 표적화된 T 세포 전달 후 2일째 (~10% TCR+ NYESO-1+, ~10% TCR+ NYESO-1-, 및 ~80% TCR- NYESO-1-), NY-ESO-1+ 비-바이러스에 의해 편집된 T 세포는 비장 대비 종양에 우선적으로 축적되었다. 4명의 인간 T 세포 공여자 각각에 대하여 마우스 n=5. (c) 5x106개 벌크 비-바이러스에 의해 표적화된 CFSE 표지된 T 세포 전달 후 10일째, NYESO-1 TCR+ 세포는 TCR- 또는 TCR+NYESO-1- T 세포보다 더욱 큰 증식을 보였고, 비장에서보다 종양에서 더욱 큰 증식 (CFSE 낮음)을 보였다. 전달 후 10일째, 종양에서 TCR- 및 TCR+NYESO- T 세포를 찾기 어려웠다. (d) 도 8f에 요약된 데이터에 대한 종축 방향 종양 부피 트랙. (e,f) 본 실험에서, T 세포 전달 후 17일째 (d), 비-바이러스에 의해 TCR 대체된 세포는 더욱 큰 NY-ESO-1 TCR 발현 및 고갈 마커의 더 낮은 발현을 보이는 것으로 나타났다. 렌티바이러스에 의해 형질도입된 세포 및 비-바이러스 TCR 대체된 세포 전달 둘 다, 24일째 종양 부담의 유의적인 감소를 보였다. 본 실험 모델에서, 비-바이러스 TCR 대체는 렌티바이러스 형질도입과 비교하였을 때, 추가 감소를 보였다 (도 8f).
도 8a는 TCR 대체가 이루어진 CD8+ T 세포에서의 항원-특이적 시토카인 생산 및 탈과립화를 제시한다.
도 8b는 TCR 대체가 이루어진 CD8+ T 세포에 의한 항원-특이적 표적 세포 사멸을 제시한다.
도 8c는 종양 마우스 이종이식편 모델의 개략도이다.
도 8d는 입양 세포 요법을 위한 내인성 TCR의 비-바이러스 대체의 확장가능성을 제시한다.
도 8e는 생체내에서 NY-ESO-1 TCR+ T 세포가 종양으로 우선적으로 국재화된다는 것을 제시한다.
도 8f는 비-바이러스에 의해 또는 렌티바이러스에 의해 변형된 NY-ESO-1 TCR+ 또는 비히클 단독 (염수)의 입양 전달 후의 종양 성장을 제시한다. n=2 (a,b) 독립된 건강한 공여자, 여기서 기술상 삼중으로 수행된 것의 평균 및 표준 편차 (a,b). 5마리 (e) 또는 7마리의 마우스 (f)에서 n=6 (d) 또는 n=2 (e,f) 독립된 건강한 공여자, 여기서 평균 및 표준 편차 (d-f). **P<0.01, ***P<0.001, ****P<0.0001 (홈-시닥(Holm-Sidak) 다중 비교 검정과 함께 2원 ANOVA).
도 9a는 게이팅된 CD4+ 또는 CD8+ T 세포에서의 NY-ESO-1 특이적 TCR의 레트로바이러스 전달 또는 비-바이러스 TCR 대체 이후의 TCR 쌍형성오류 분석을 제시한다. TCR의 레트로바이러스 전달과 비교하였을 때, 비-바이러스 TCR 대체를 통해 TCR 쌍형성오류는 감소된다. 신규 TCR의 바이러스에 의한 도입 시, 감염된 세포는 잠재적으로는 적어도 4개의 상이한 TCR (신규 TCR-α + 신규 TCR-β; 신규 TCR-α + 내인성 TCR-β; 내인성 TCR-α 및 신규 TCR-β; 내인성 TCR-α + 내인성 TCR-β)을 발현하게 될 것이다. MHC-펩티드 다량체 (NYESO)를 포함하는 신규의 도입된 TCR (VB13.1)에서의 특이적인 베타 쇄에 대한 염색은 잠재적인 쌍형성에 오류가 있는 TCR들 (VB13.1+ NYESO-; 내인성 TCR-α + 신규 TCR-β) 중 하나를 주로 발현한 세포 대비로 도입된 TCR (VB13.1+ NYESO+; 신규 TCR-α + 신규 TCR-β)을 주로 발현한 세포 사이의 구별에 의해 TCR 쌍형성오류의 대략적인 예측값을 제공할 수 있다.
도 9b-9c는 전체 신규 TCR의 TRAC로의 표적화 (도 9b, 또는 가능하게는 TCR-β의 멀티플렉스화된 녹아웃), 전체 신규 TCR의 TRBC1 /2로의 표적화 (도 9c)에 의한 TCR 대체, 또는 TRAC로의 신규 TCR-α 및 TRBC1 /2로의 신규 TCR-β를 이용한 멀티플렉스화된 대체를 제시한다.
도 9d는 기능성 시토카인 생산이, 게이팅된 CD8+ T 세포와 유사하게 게이팅된 CD4+ T 세포에서 항원 노출 후 선택적으로 관찰되었다는 것을 제시한다 (도 8a).
도 9e는 6명의 건강한 혈액 공여자로 이루어진 코호트에 걸쳐 CD8+ 및 CD4+ T 세포 둘 다에서 전기천공 후 4일째에 비-바이러스 TCR 대체가 일관되게 관찰되었다는 것을 제시한다.
도 9f는 추가로 6명의 건강한 혈액 공여자로 이루어진 제2 코호트에서, 각 공여자로부터의 1억개의 T 세포가 NY-ESO-1 TCR 대체 HDR 주형 및 온-타겟 gRNA/Cas9로 전기천공되었다 (도 8d)는 것을 제시한다. NY-ESO-1 TCR+인 CD4+ 및 CD8+ T 세포의 백분율은 전기천공 후 확장 10일 동안에 걸쳐 일관된 것으로 나타났다.
도 9g는 비-바이러스 게놈 표적화 후 확장 10일 동안에 걸쳐, CD8+ T 세포가 CD4+ T 세포에 비해 증식상 약간의 이점을 나타내었다는 것을 제시한다.
도 9h는 명시된 흑색종 세포주와 명시된 분류된 T 세포 집단을 1:5 T 세포 대 암 세포 비로 공동-인큐베이션하였을 때의 결과를 제시한다. 공동-인큐베이션 후 72시간째, 자동 현미경 검사 (여기서 핵 RFP가 암 세포를 마킹함)에 의해 퍼센트 암 세포 전면생장률을 기록하였다. 레트로바이러스 형질도입에 의해, 또는 비-바이러스 녹인 내인성 TCR 대체에 의해, NY-ESO-1 항원 특이적 TCR을 발현하는 T 세포 둘 다, NY-ESO-1 및 HLA-A*0201 클래스 I MHC 대립유전자 둘 다를 발현하는 표적 암 세포주에서만 오직 강건한 표적 세포 사멸을 보였다.
도 9i는 NY-ESO-1+ HLA-A*0201+ A375 암 세포주의 표적 세포 사멸을 위한 온/오프 타겟 gRNA 및 온/오프 타겟 HDR 주형 매트릭스 사용 결과를 제시한다 (오프-타겟 gRNA 및 HDRT는 RAB11A-GFP 융합 단백질 녹인에 대해 특이적이었음). 온-타겟 gRNA 뿐만 아니라, 온-타겟 HDR 주형 둘 다를 갖는 세포만이 표적 세포 사멸을 보였다.
도 9j는 벌크 T 세포 편집된 집단으로부터의 분류된 NY-ESO-1+ TCR+ 세포 (온-타겟 gRNA, 온-타겟 HDR 주형)가 표적 암 세포 사멸에 대하여 강력한 용량 반응 효과를 나타내었다는 것을 제시한다. 48시간 이내에 2:1 및 그 초과의 T 세포 대 암 세포 비가 표적 암 세포의 거의 완전한 사멸을 보였다. 144시간까지, 1:16 미만의 T 세포 대 암 세포 비는 강건한 표적 세포 사멸의 증거를 보여주었다.
도 9k는, 비-바이러스 TCR 대체 후 유세포 분석법에 의해 관찰된 바, 비-바이러스 TCR 대체 T 세포에 의한 표적 세포 사멸은 특이적으로 NY-ESO-1-인식 TCR+ 세포 집단에 기인하였다는 것을 제시한다. 벌크 편집된 T 세포 집단을 시작으로 (이들 모두 온-타겟 gRNA 및 HDR 주형으로 전기천공된 것임), 본 발명자들은 별개로 3개의 세포 집단을 분류하였다: NY-ESO-1+TCR+ 세포 (비-바이러스에 의해 대체된 TCR), NY-ESO-1-TCR- 세포 (TCR 녹아웃) (회색), 및 NY-ESO-1-TCR+ 세포 (그의 천연 TCR은 유지하였지만, NY-ESO 특이적 녹인 TCR은 갖지 않은 것). 오직 분류된 NY-ESO-1+ TCR+ 집단만이 표적 세포 사멸을 보였다 (4:1 T 세포 대 암 세포 비). n=2 (a,d) 또는 n=3 (b,c) 독립된 건강한 공여자로부터 1명의 대표적인 공여자, 여기서 기술상 삼중으로 수행된 것의 평균 및 표준 편차 (d). n=6 독립된 건강한 공여자의 평균 및 표준 편차 (e,f) 또는 n=2 독립된 건강한 공여자에 대한 기술상 4회에 걸쳐 반복 수행된 것의 평균 및 표준 편차 (i-k)가 제시되어 있다. n=2 독립된 건강한 공여자에 대한 평균 및 개별 값 (h).
도 1a는 상동성 지정 복구를 통한, N-말단에서 C-말단으로, (i) T2A 자기-절단 펩티드 서열; (ii) 전장 (즉, 가변 영역 및 불변 영역)의 이종성 TCR-β 쇄 (NYESO-β); (iii) P2A 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역 (NYESO-α); 및 (v) 내인성 TCR 알파 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함하는 단일 비-바이러스 DNA 주형의 T 세포 내로의 삽입을 도시한 개략도이다. 상동성 지정 복구를 통한 TRAC 유전자의 엑손 1에의 DNA 주형 삽입 후, DNA 주형을 전사시키고, 번역시켜 NY-ESO-1 흑색종 신생항원을 인식하는 항원-특이적 TCR을 형성하는 전장 NYESO-β 쇄 및 전장 NYESO-α 쇄를 제조하였다.
도 1b는 TCR-β 로커스 (TRBC1 또는 TRBC2)에서의 단일 비-바이러스 DNA 주형의 삽입을 도시한 개략도이다. 주형은 상동성 지정 복구를 통한 T 세포 내의, N-말단에서 C-말단으로, (i) T2A 자기-절단 펩티드 서열; (ii) 전장 (즉, 가변 영역 및 불변 영역) 이종성 TCR-α 쇄 (NYESO-α); (iii) P2A 자기-절단 펩티드 서열; (iv) 이종성 TCR-β 쇄의 가변 영역 (NYESO-β); 및 (v) 내인성 TCR 베타 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함한다.
도 2는 (a) N-말단에서 C-말단으로, (i) P2A 자기-절단 펩티드 서열, (ii) 항원 특이적 T 세포 수용체의 TCR-α 쇄의 가변 영역 (NYESO-α); 및 (iii) 내인성 TCR-α 서브유닛의 엑손 1의 N-말단 부분을 코딩하는 핵산 서열을 포함하는 비-바이러스 DNA 주형; 및 (b) N-말단에서 C-말단으로, (i) T2A 자기-절단 펩티드 서열, (ii) 항원 특이적 T 세포 수용체의 TCR-β 쇄의 가변 영역; 및 (iii) 내인성 TCR-β 서브유닛의 엑손 1의 N-말단 부분을 코딩하는 핵산 서열을 포함하는 DNA 주형을 삽입함으로써 수행된, 내인성 T 세포 α 및 T 세포 β 수용체 쇄 둘 다의 동시 대체를 도시한 개략도이다.
도 3a는 T 세포 수용체의 폴리클로날 라이브러리를 형성하기 위한 T 세포에서의 이종성 (TCR)-β 쇄 및 TCR-α 쇄의 삽입을 도시한 개략도이다. N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 전장 (예를 들어 가변 영역 및 불변 영역) 이종성 T 세포 수용체 (TCR)-β 쇄; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역; 및 (v) 내인성 TCR 알파 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 함유하는 다중의 상이한 DNA 주형, 예를 들어, 비-바이러스 DNA 주형을 동시에 전기천공하여 원하는 TCR 서열의 합성 T 세포 레퍼토리를 포함하는 T 세포의 집단을 생성하였다.
도 3b는 앞서 공지된 TCR 서열로부터, 또는 관심 내인성 T 세포 집단에서의 천연 레퍼토리로부터, 예를 들어, 대상체로부터의 T 세포 레퍼토리의 디자인을 제시하는 개략도이다. 예를 들어, TCR은 종양 침윤 림프구에 의해 발현되는 TCR, 자가면역 질환의 부위에서의 자가반응성 T 세포에 의해 발현되는 TCR, 또는 병원체 반응성 T 세포로부터의 TCR일 수 있지만, 이에 제한되지는 않는다.
도 4a는 이종성 NYESO TCR로 전기천공된 CD4+ 및 CD8+ T 세포의 FACS 분석을 제시한다. 2명의 건강한 인간 혈액 공여자로부터의 CD4+ 및 CD8+ T 세포를 상기 기재된 바와 같이, 이종성 NYESO-α 및 이종성 NYESO-β를 포함하는 비-바이러스 구축물로 전기천공하였다. 전기천공 후 4일째, 세포를 통합된 NYESO-특이적 TCR에 의해 인식되는 펩티드를 함유하는 형광 표지된 MHC-덱스트라머로 염색하였다.
도 4b는 이종성 NYESO TCR로 전기천공된 CD8+ T 세포의 FACS 분석을 제시한다. 건강한 인간 혈액 공여자로부터의 CD8+ T 세포를 상기 기재된 바와 같이, 이종성 NYESO-α 및 이종성 NYESO-β를 포함하는 비-바이러스 DNA 구축물로 전기천공하였다. 전기천공 후 4일째, 세포를 통합된 NYESO-특이적 TCR에 의해 인식되는 펩티드를 함유하는 형광 표지된 MHC-덱스트라머로 염색하였다.
도 5는 이종성 NYESO TCR로 전기천공된 CD8+ 세포의 FACS 분석이다. 세포를 도 3 및 4에서와 같이 처리하였고, NYESO MHC-덱스트라머를 이용한 항원 특이적 염색 대비로 (모든 잠재적 인간 TCR에 결합하는 항체를 이용한) TCR 발현에 대한 염색을 추가로 수행하였다. 내인성 TCR의 상동성 지정 대체가 없는 대부분의 T 세포에서, TRAC 엑손 1 gRNA에 의한 커팅 및 비-상동성 말단 연결에 의한 작은 삽입 결실 돌연변이 (indel)의 도입에 기인하여 내인성 TCR은 녹아웃되었다. 예상대로, NYESO 양성 세포는 거의 모두 TCR 발현에 대해서도 양성이었다.
도 6a는 시험관내 세포 사멸 검정법에서 이종성 NYESO TCR을 함유하는 1차 인간 T 세포가 암 세포를 사멸시킨다는 것을 제시한다.
도 6b는 사멸시키는, 이종성 NYESO TCR을 함유하는 인간 T 세포를 사용하는 시험관내 세포 사멸 검정법으로부터의 단일 시점으로부터의 결과를 제시한다.
도 7a-f는 비-바이러스 TCR 대체가 이루어진 T 세포의 생체내 기능성을 제시한다. (a) 생체내 인간 항원 특이적 종양 이종이식편 모델의 다이어그램. (b) 5x106개 벌크 비-바이러스에 의해 표적화된 T 세포 전달 후 2일째 (~10% TCR+ NYESO-1+, ~10% TCR+ NYESO-1-, 및 ~80% TCR- NYESO-1-), NY-ESO-1+ 비-바이러스에 의해 편집된 T 세포는 비장 대비 종양에 우선적으로 축적되었다. 4명의 인간 T 세포 공여자 각각에 대하여 마우스 n=5. (c) 5x106개 벌크 비-바이러스에 의해 표적화된 CFSE 표지된 T 세포 전달 후 10일째, NYESO-1 TCR+ 세포는 TCR- 또는 TCR+NYESO-1- T 세포보다 더욱 큰 증식을 보였고, 비장에서보다 종양에서 더욱 큰 증식 (CFSE 낮음)을 보였다. 전달 후 10일째, 종양에서 TCR- 및 TCR+NYESO- T 세포를 찾기 어려웠다. (d) 도 8f에 요약된 데이터에 대한 종축 방향 종양 부피 트랙. (e,f) 본 실험에서, T 세포 전달 후 17일째 (d), 비-바이러스에 의해 TCR 대체된 세포는 더욱 큰 NY-ESO-1 TCR 발현 및 고갈 마커의 더 낮은 발현을 보이는 것으로 나타났다. 렌티바이러스에 의해 형질도입된 세포 및 비-바이러스 TCR 대체된 세포 전달 둘 다, 24일째 종양 부담의 유의적인 감소를 보였다. 본 실험 모델에서, 비-바이러스 TCR 대체는 렌티바이러스 형질도입과 비교하였을 때, 추가 감소를 보였다 (도 8f).
도 8a는 TCR 대체가 이루어진 CD8+ T 세포에서의 항원-특이적 시토카인 생산 및 탈과립화를 제시한다.
도 8b는 TCR 대체가 이루어진 CD8+ T 세포에 의한 항원-특이적 표적 세포 사멸을 제시한다.
도 8c는 종양 마우스 이종이식편 모델의 개략도이다.
도 8d는 입양 세포 요법을 위한 내인성 TCR의 비-바이러스 대체의 확장가능성을 제시한다.
도 8e는 생체내에서 NY-ESO-1 TCR+ T 세포가 종양으로 우선적으로 국재화된다는 것을 제시한다.
도 8f는 비-바이러스에 의해 또는 렌티바이러스에 의해 변형된 NY-ESO-1 TCR+ 또는 비히클 단독 (염수)의 입양 전달 후의 종양 성장을 제시한다. n=2 (a,b) 독립된 건강한 공여자, 여기서 기술상 삼중으로 수행된 것의 평균 및 표준 편차 (a,b). 5마리 (e) 또는 7마리의 마우스 (f)에서 n=6 (d) 또는 n=2 (e,f) 독립된 건강한 공여자, 여기서 평균 및 표준 편차 (d-f). **P<0.01, ***P<0.001, ****P<0.0001 (홈-시닥(Holm-Sidak) 다중 비교 검정과 함께 2원 ANOVA).
도 9a는 게이팅된 CD4+ 또는 CD8+ T 세포에서의 NY-ESO-1 특이적 TCR의 레트로바이러스 전달 또는 비-바이러스 TCR 대체 이후의 TCR 쌍형성오류 분석을 제시한다. TCR의 레트로바이러스 전달과 비교하였을 때, 비-바이러스 TCR 대체를 통해 TCR 쌍형성오류는 감소된다. 신규 TCR의 바이러스에 의한 도입 시, 감염된 세포는 잠재적으로는 적어도 4개의 상이한 TCR (신규 TCR-α + 신규 TCR-β; 신규 TCR-α + 내인성 TCR-β; 내인성 TCR-α 및 신규 TCR-β; 내인성 TCR-α + 내인성 TCR-β)을 발현하게 될 것이다. MHC-펩티드 다량체 (NYESO)를 포함하는 신규의 도입된 TCR (VB13.1)에서의 특이적인 베타 쇄에 대한 염색은 잠재적인 쌍형성에 오류가 있는 TCR들 (VB13.1+ NYESO-; 내인성 TCR-α + 신규 TCR-β) 중 하나를 주로 발현한 세포 대비로 도입된 TCR (VB13.1+ NYESO+; 신규 TCR-α + 신규 TCR-β)을 주로 발현한 세포 사이의 구별에 의해 TCR 쌍형성오류의 대략적인 예측값을 제공할 수 있다.
도 9b-9c는 전체 신규 TCR의 TRAC로의 표적화 (도 9b, 또는 가능하게는 TCR-β의 멀티플렉스화된 녹아웃), 전체 신규 TCR의 TRBC1 /2로의 표적화 (도 9c)에 의한 TCR 대체, 또는 TRAC로의 신규 TCR-α 및 TRBC1 /2로의 신규 TCR-β를 이용한 멀티플렉스화된 대체를 제시한다.
도 9d는 기능성 시토카인 생산이, 게이팅된 CD8+ T 세포와 유사하게 게이팅된 CD4+ T 세포에서 항원 노출 후 선택적으로 관찰되었다는 것을 제시한다 (도 8a).
도 9e는 6명의 건강한 혈액 공여자로 이루어진 코호트에 걸쳐 CD8+ 및 CD4+ T 세포 둘 다에서 전기천공 후 4일째에 비-바이러스 TCR 대체가 일관되게 관찰되었다는 것을 제시한다.
도 9f는 추가로 6명의 건강한 혈액 공여자로 이루어진 제2 코호트에서, 각 공여자로부터의 1억개의 T 세포가 NY-ESO-1 TCR 대체 HDR 주형 및 온-타겟 gRNA/Cas9로 전기천공되었다 (도 8d)는 것을 제시한다. NY-ESO-1 TCR+인 CD4+ 및 CD8+ T 세포의 백분율은 전기천공 후 확장 10일 동안에 걸쳐 일관된 것으로 나타났다.
도 9g는 비-바이러스 게놈 표적화 후 확장 10일 동안에 걸쳐, CD8+ T 세포가 CD4+ T 세포에 비해 증식상 약간의 이점을 나타내었다는 것을 제시한다.
도 9h는 명시된 흑색종 세포주와 명시된 분류된 T 세포 집단을 1:5 T 세포 대 암 세포 비로 공동-인큐베이션하였을 때의 결과를 제시한다. 공동-인큐베이션 후 72시간째, 자동 현미경 검사 (여기서 핵 RFP가 암 세포를 마킹함)에 의해 퍼센트 암 세포 전면생장률을 기록하였다. 레트로바이러스 형질도입에 의해, 또는 비-바이러스 녹인 내인성 TCR 대체에 의해, NY-ESO-1 항원 특이적 TCR을 발현하는 T 세포 둘 다, NY-ESO-1 및 HLA-A*0201 클래스 I MHC 대립유전자 둘 다를 발현하는 표적 암 세포주에서만 오직 강건한 표적 세포 사멸을 보였다.
도 9i는 NY-ESO-1+ HLA-A*0201+ A375 암 세포주의 표적 세포 사멸을 위한 온/오프 타겟 gRNA 및 온/오프 타겟 HDR 주형 매트릭스 사용 결과를 제시한다 (오프-타겟 gRNA 및 HDRT는 RAB11A-GFP 융합 단백질 녹인에 대해 특이적이었음). 온-타겟 gRNA 뿐만 아니라, 온-타겟 HDR 주형 둘 다를 갖는 세포만이 표적 세포 사멸을 보였다.
도 9j는 벌크 T 세포 편집된 집단으로부터의 분류된 NY-ESO-1+ TCR+ 세포 (온-타겟 gRNA, 온-타겟 HDR 주형)가 표적 암 세포 사멸에 대하여 강력한 용량 반응 효과를 나타내었다는 것을 제시한다. 48시간 이내에 2:1 및 그 초과의 T 세포 대 암 세포 비가 표적 암 세포의 거의 완전한 사멸을 보였다. 144시간까지, 1:16 미만의 T 세포 대 암 세포 비는 강건한 표적 세포 사멸의 증거를 보여주었다.
도 9k는, 비-바이러스 TCR 대체 후 유세포 분석법에 의해 관찰된 바, 비-바이러스 TCR 대체 T 세포에 의한 표적 세포 사멸은 특이적으로 NY-ESO-1-인식 TCR+ 세포 집단에 기인하였다는 것을 제시한다. 벌크 편집된 T 세포 집단을 시작으로 (이들 모두 온-타겟 gRNA 및 HDR 주형으로 전기천공된 것임), 본 발명자들은 별개로 3개의 세포 집단을 분류하였다: NY-ESO-1+TCR+ 세포 (비-바이러스에 의해 대체된 TCR), NY-ESO-1-TCR- 세포 (TCR 녹아웃) (회색), 및 NY-ESO-1-TCR+ 세포 (그의 천연 TCR은 유지하였지만, NY-ESO 특이적 녹인 TCR은 갖지 않은 것). 오직 분류된 NY-ESO-1+ TCR+ 집단만이 표적 세포 사멸을 보였다 (4:1 T 세포 대 암 세포 비). n=2 (a,d) 또는 n=3 (b,c) 독립된 건강한 공여자로부터 1명의 대표적인 공여자, 여기서 기술상 삼중으로 수행된 것의 평균 및 표준 편차 (d). n=6 독립된 건강한 공여자의 평균 및 표준 편차 (e,f) 또는 n=2 독립된 건강한 공여자에 대한 기술상 4회에 걸쳐 반복 수행된 것의 평균 및 표준 편차 (i-k)가 제시되어 있다. n=2 독립된 건강한 공여자에 대한 평균 및 개별 값 (h).
정의
본 명세서 및 첨부된 청구범위에서 사용된 바와 같이, 단수 형태는 문맥상 달리 명백하게 지시되지 않는 한, 복수의 지칭대상을 포함한다.
"핵산" 또는 "뉴클레오티드"라는 용어는 단일 가닥 또는 이중 가닥 형태의 데옥시리보핵산 (DNA) 또는 리보핵산 (RNA) 및 그의 중합체를 지칭한다. 달리 구체적으로 제한되지 않는 한, 상기 용어는 참조 핵산과 유사한 결합 특성을 갖고, 자연적으로 발생된 뉴클레오티드와 유사한 방식으로 대사되는 천연 뉴클레오티드의 공지된 유사체를 함유하는 핵산을 포함한다. 달리 명시되지 않는 한, 특정 핵산 서열은 또한 그의 보존적으로 변형된 변이체 (예를 들어, 축중성 코돈 치환), 대립유전자, 오르토로그, SNP 및 상보적 서열 뿐만 아니라, 명백하게 명시된 서열을 암시적으로 포함한다. 구체적으로, 하나 이상의 선택된 (또는 모든) 코돈의 제3 위치가 혼합-염기 및/또는 데옥시이노신 잔기로 치환되는 서열을 생성함으로써 축중성 코돈 치환이 달성될 수 있다 ([Batzer et al., Nucleic Acid Res. 19:5081 (1991); Ohtsuka et al., J. Biol. Chem. 260:2605-2608 (1985)]; 및 [Rossolini et al., Mol. Cell. Probes 8:91-98 (1994)]).
"유전자"라는 용어는 폴리펩티드 쇄를 생산하거나, 또는 그를 코딩하는데 관여하는 DNA의 세그먼트를 지칭할 수 있다. 이는 코딩 영역의 선행 및 후속 영역 (리더 및 트레일러) 뿐만 아니라, 개별 코딩 세그먼트 (엑손) 사이의 개입 서열 (인트론)을 포함할 수 있다. 대안적으로, "유전자"라는 용어는 비-번역된 RNA, 예컨대 rRNA, tRNA, 가이드 RNA (예를 들어, 단일 가이드 RNA), 또는 마이크로 RNA를 생산하거나, 또는 그를 코딩하는데 관여하는 DNA 세그먼트를 지칭할 수 있다.
"치료하는"이란, 임의의 객관적 또는 주관적 파라미터, 예컨대 완해; 차도; 증상의 감소 또는 질환 상태를 환자가 더 견딜 수 있게 하는 것; 변성 또는 감퇴 속도 저속화; 또는 변성의 최종 지점을 덜 쇠약하게 만드는 것을 비롯한, 질환, 병태 또는 장애의 치료 또는 호전 또는 예방에 있어서의 임의의 성공 지표를 지칭한다.
"프로모터"는 핵산의 전사를 지시하는 하나 이상의 핵산 제어 서열로서 정의된다. 본원에서 사용되는 바와 같이, 프로모터는 전사의 출발 부위 근처에 필요한 핵산 서열, 예컨대, 폴리머라제 II형 프로모터의 경우, TATA 요소를 포함한다. 프로모터는 또한 임의적으로, 원위 인핸서 또는 리프레서 요소를 포함하며, 이는 전사의 출발 부위로부터 수천개 정도로 많은 염기 쌍에 위치할 수 있다.
핵산은, 핵산이 또 다른 핵산 서열과 기능적 관계로 배치되어 있을 때, "작동가능하게 연결"되어 있는 것이다. 예를 들어, 프로모터 또는 인핸서는 그가 서열의 전사에 영향을 준다면, 코딩 서열에 작동가능하게 연결되어 있는 것이거나; 또는 리보솜 결합 부위는 그가 번역을 촉진시키도록 배치되어 있다면, 코딩 서열에 작동가능하게 연결되어 있는 것이다.
"폴리펩티드," "펩티드" 및 "단백질"은 본원에서 상호교환적으로 사용되며, 아미노산 잔기의 중합체를 지칭한다. 본원에서 사용되는 바와 같이, 상기 용어는 전장 단백질을 비롯한, 아미노산 잔기가 공유 펩티드 결합에 의해 연결된 임의의 길이의 아미노산 쇄를 포함한다.
본원에서 사용되는 바와 같이, "상보적" 또는 "상보성"이라는 용어는 뉴클레오티드 또는 핵산 사이의 특이적 염기 쌍형성을 지칭한다. 일부 실시양태에서, 예를 들어, 및 제한 없이, 가이드 RNA와 TRAC 유전자의 엑손 1 내의 표적 영역 사이의 염기 쌍형성이 기재된다. 상보적 뉴클레오티드는 일반적으로 A 및 T (또는 A 및 U), 및 G 및 C이다. 본원에 기재된 가이드 RNA는 T 세포에서 TRAC 유전자의 엑손 1 내의 게놈 서열에 완벽하게 상보적 또는 실질적으로 상보적인 (예를 들어, 1-4개의 미스매치를 갖는) 서열, 예를 들어, DNA 표적화 서열을 포함할 수 있다.
전반에 걸쳐 사용되는 바와 같이, 대상체란 개체를 의미할 수 있다. 예를 들어, 대상체는 포유동물, 예컨대 영장류, 및 더욱 구체적으로 인간이다. 상기 용어는 특정 연령 또는 성별을 지시하지는 않는다. 따라서, 남성이든 또는 여성이든 상관 없이, 성인 및 신생아 대상체가 포함되는 것으로 의도된다. 본원에서 사용되는 바와 같이, 환자 또는 대상체는 상호교환적으로 사용될 수 있고, 질환 또는 장애를 앓는 대상체를 지칭할 수 있다.
"CRISPR/Cas" 시스템은 외래 핵산에 대항한 방어를 위한 광범위한 부류의 박테리아 시스템을 지칭한다. CRISPR/Cas 시스템은 광범위한 유박테리아 및 고세균 유기체에서 발견된다. CRISPR/Cas 시스템은 타입 I, II 및 III 서브타입을 포함한다. 야생형 타입 II CRISPR/Cas 시스템은 외래 핵산을 인식하고 절단하기 위해 가이드 및 활성화 RNA와 복합체화되는 RNA-매개 뉴클레아제, 예를 들어, Cas9를 이용한다. 가이드 RNA 및 활성화 RNA 둘 다의 활성을 갖는 가이드 RNA도 또한 관련 기술분야에 공지되어 있다. 일부 경우에서, 상기 이중 활성 가이드 RNA는 단일 가이드 RNA (sgRNA)로서 지칭된다.
Cas9 상동체는 하기 분류학 군의 박테리아를 포함하나, 이에 제한되지는 않는 광범위한 유박테리아에서 발견된다: 악티노박테리아(Actinobacteria), 아쿠이피카에(Aquificae), 박테로이데테스-클로로비(Bacteroidetes - Chlorobi), 클라미디아에-베루코마이크로비아(Chlamydiae-Verrucomicrobia), 클로로플렉시(Chloroflexi), 시아노박테리아(Cyanobacteria), 피르미쿠테스(Firmicutes), 프로테오박테리아(Proteobacteria), 스피로카에테스(Spirochaetes) 및 써모토가에(Thermotogae). 예시적인 Cas9 단백질은 스트렙토코쿠스 피오게네스(Streptococcus pyogenes) Cas9 단백질이다. 추가의 Cas9 단백질 및 그의 상동체는, 예를 들어, 문헌 [Chylinksi, et al., RNA Biol. 2013 May 1; 10(5): 726-737; Nat. Rev. Microbiol. 2011 June; 9(6): 467-477]; [Hou, et al., Proc Natl Acad Sci U S A. 2013 Sep 24;110(39):15644-9]; [Sampson et al., Nature. 2013 May 9;497(7448):254-7]; 및 [Jinek, et al., Science. 2012 Aug 17;337(6096):816-21]에 기재되어 있다. 본원에 제공된 Cas9 뉴클레아제 중 임의의 변이체는 숙주 세포에서 효율적인 활성 또는 증강된 안정성을 위해 최적화될 수 있다. 따라서, 조작된 Cas9 뉴클레아제가 또한 고려된다.
본원에서 사용되는 바와 같이, "Cas9"라는 용어는 RNA-매개 뉴클레아제 (예를 들어, 박테리아 또는 고세균 기원의 것, 또는 그로부터 유래된 것)를 지칭한다. 예시적인 RNA-매개 뉴클레아제로는 상기 Cas9 단백질 및 그의 상동체를 포함한다. 다른 RNA-매개 뉴클레아제로는 Cpf1 (예를 들어, 문헌 [Zetsche et al., Cell, Volume 163, Issue 3, p759-771, 22 October 2015] 참조) 및 그의 상동체를 포함한다. 유사하게, 본원에서 사용되는 바와 같이, "Cas9 리보핵단백질" 복합체라는 용어 등은 Cas9 단백질과 crRNA (예를 들어, 가이드 RNA 또는 단일 가이드 RNA)의 복합체, Cas9 단백질과 트랜스-활성화 crRNA (tracrRNA)의 복합체, Cas9 단백질과 가이드 RNA의 복합체, 또는 그의 조합 (예를 들어, Cas9 단백질, tracrRNA 및 crRNA-가이드 RNA를 함유하는 복합체)을 지칭한다. 본원에 기재된 실시양태 중 임의의 것에서, Cas9 뉴클레아제는 Cpf1 뉴클레아제로 치환될 수 있다는 것을 이해한다.
본원에서 사용되는 바와 같이, 세포의 게놈의 편집의 맥락에서 "편집"이라는 어구는 표적 게놈 영역에서 게놈의 서열에 있어서의 구조적 변화를 유도하는 것을 지칭한다. 예를 들어, 편집은 뉴클레오티드 서열을 세포의 게놈 내로 삽입하는 형태를 취할 수 있다. 뉴클레오티드 서열은 폴리펩티드 또는 그의 단편을 코딩할 수 있다. 상기 편집은 표적 게놈 영역 내에서 이중 가닥 파단, 또는 반대 가닥 상의 한 쌍의 단일 가닥 닉을 유도하고, 표적 게놈 영역을 플랭킹함으로써 수행될 수 있다. 표적 게놈 영역에서 또는 표적 게놈 영역 내에서 단일 또는 이중 가닥 파단을 유도하는 방법은 표적 게놈 영역으로 지시되는 Cas9 뉴클레아제 도메인 또는 그의 유도체, 및 가이드 RNA 또는 가이드 RNA 쌍의 사용을 포함한다.
본원에서 사용되는 바와 같이, 핵산, 또는 핵산을 포함하는 복합체, 예를 들어, RNP-DNA 주형 복합체를 도입하는 맥락에서 "도입하는"이라는 어구는 세포 외부에서 세포 내부로의 핵산 서열 또는 the RNP-DNA 주형 복합체의 전위를 지칭한다. 일부 경우에서, 도입하는이란, 세포 외부에서 세포의 핵 내부로의 핵산 또는 복합체의 전위를 지칭한다. 전기천공, 나노와이어 또는 나노튜브와의 접촉, 수용체 매개 내재화, 세포 침투 펩티드를 통한 전위, 리포솜 매개 전위 등을 포함하나, 이에 제한되지는 않는, 상기 전위의 다양한 방법이 고려된다.
본원에서 사용되는 바와 같이, "이종성"이라는 어구는 인간 T 세포에서 자연적으로는 발견되지 않는 핵산 서열 또는 폴리펩티드를 지칭한다. "이종성 서열"이라는 용어는 자연상 주어진 T 세포에서는 보통 발견되지 않는 서열을 지칭한다. 따라서, 이종성 뉴클레오티드 또는 단백질 서열은 (a) 그의 숙주 세포에 대해 외래일 수 있거나 (즉, 세포에 대해 외인성이거나); (b) 숙주 세포에서 자연적으로 발견되지만 (즉, 내인성이지만), 세포에서 비자연적인 양 (즉, 숙주 세포에서 자연적으로 발견되는 양보다 더 많거나 더 적은 양)으로 존재할 수 있거나; 또는 (c) 숙주 세포에서 자연적으로 발견되지만, 그의 천연 로커스를 벗어나 위치할 수 있다.
본원에서 사용되는 바와 같이, 1차 세포와 관련하여 "1차"라는 어구는 형질전환되지 않거나, 또는 불멸화되지 않은 세포를 지칭한다. 상기 1차 세포는 제한된 횟수만큼 배양, 계대배양 또는 계대접종될 수 있다 (예를 들어, 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 또는 20회 배양). 일부 경우에서, 1차 세포는 시험관내 배양 조건에 맞도록 적합화된다. 일부 경우에서, 1차 세포는 유기체, 시스템, 기관 또는 조직으로부터 단리되고, 임의적으로 분류되고, 배양 또는 계대배양 없이 직접 사용된다. 일부 경우에서, 1차 세포는 자극, 활성화 또는 분화된다. 예를 들어, 1차 T 세포는 CD3, CD28 효능제, IL-2, IFN-γ 또는 그의 조합과의 접촉 (예를 들어, 그의 존재 하에서의 배양)에 의해 활성화될 수 있다.
본원에서 사용되는 바와 같이, "T 세포"라는 어구는 T 세포 수용체 분자를 발현하는 림프계 세포를 지칭한다. T 세포는 인간 알파 베타 (αβ) T 세포 및 인간 감마 델타 (γδ) T 세포를 포함한다. T 세포는 나이브 T 세포, 자극된 T 세포, 1차 T 세포 (예를 들어, 배양되지 않은 T 세포), 배양된 T 세포, 불멸화된 T 세포, 헬퍼 T 세포, 세포독성 T 세포, 기억 T 세포, 조절 T 세포, 자연 살해 T 세포, 그의 조합, 또는 그의 하위 집단을 포함하나, 이에 제한되지는 않는다. T 세포는 CD4+, CD8+, 또는 CD4+ 및 CD8+일 수 있다. T 세포는 헬퍼 세포, 예를 들어, TH1, TH2, TH3, TH9, TH17, 또는 TFH 유형의 헬퍼 세포일 수 있다. T 세포는 세포독성 T 세포일 수 있다. 조절 T 세포는 FOXP3+ 또는 FOXP3-일 수 있다. T 세포는 알파/베타 T 세포 또는 감마/델타 T 세포일 수 있다. 일부 경우에서, T 세포는 CD4+CD25고CD127저 조절 T 세포일 수 있다. 일부 경우에서, T 세포는 1형 조절 (Tr1), TH3, CD8+CD28-, Treg17, 및 Qa-1 제한된 T 세포, 또는 그의 조합 또는 하위 집단으로 이루어진 군으로부터 선택되는 조절 T 세포이다. 일부 경우에서, T 세포는 FOXP3+ T 세포이다. 일부 경우에서, T 세포는 CD4+CD25저CD127고 이펙터 T 세포이다. 일부 경우에서, T 세포는 CD4+CD25저CD127고CD45RA고CD45RO- 나이브 T 세포이다. T 세포는 유전적으로 조작된 재조합 T 세포일 수 있다. 일부 경우에서, 재조합 T 세포는 재조합 (예를 들어, 이종성) T 세포 수용체를 갖는다.
본원에서 사용되는 바와 같이, "TCR 수용체"라는 용어는 항원에 대한 반응으로 T 세포의 활성화에서 작용하는 2개의 TCR 서브유닛 쇄 (예를 들어 TCR-α 및 TCR-β, TCRγ 및 TCRδ)로 이루어진 이종이량체이다. T 세포에서 발현되었을 때, TCR 수용체의 각 TCR 서브유닛 쇄는 TCR 서브유닛 쇄를 세포막에 부착시키는 불변 영역, 및 예를 들어, 제1 TCR 서브유닛 쇄 (예를 들어, TCR-α) 및 제2 TCR 서브유닛 쇄 (예를 들어, TCR-β) 쇄가 이종이량체 TCR 수용체를 형성할 때, 항원 인식 미 결합에서 작용하는 가변 영역을 함유한다.
본원에서 사용되는 바와 같이, "비-상동성 말단 연결" 또는 NHEJ라는 용어는 DNA 가닥의 커팅된 또는 닉킹된 말단이 상동 주형 핵산을 필요로 하지 않으면서, 직접 라이게이션되는 세포성 프로세스를 지칭한다. NHEJ는 복구 부위에서 하나 이상의 뉴클레오티드의 부가, 결실, 치환 또는 그의 조합으로 이어질 수 있다.
본원에서 사용되는 바와 같이, "상동성 지정 복구" 또는 HDR라는 용어는 DNA 가닥의 커팅된 또는 닉킹된 말단이 상동성 주형 핵산으로부터의 중합에 의해 복구되는 세포성 프로세스를 지칭한다. 따라서, 원래 서열은 주형의 서열로 대체된다. 상동성 주형 핵산은 게놈 내의 다른 곳 (자매 염색분체, 상동성 염색체, 또는 동일하거나 상이한 염색체 상의 반복된 영역)에 있는 상동성 서열에 의해 제공될 수 있다. 대안적으로, 외인성 주형 핵산을 도입하여, 표적 부위에서 서열의 특이적 HDR-유도된 변이를 수득할 수 있다. 이러한 방식으로, 특이적 돌연변이가 커팅 부위에 도입될 수 있다.
본원에서 사용되는 바와 같이, 단일 가닥 DNA 주형 또는 이중 가닥 DNA 주형은 예를 들어, HDR에 의한 T 세포의 게놈을 편집하기 위한 주형으로서 세포에 의해 사용될 수 있는 DNA 올리고뉴클레오티드를 지칭한다. 일반적으로, 단일 가닥 DNA 주형 또는 이중 가닥 DNA 주형은 표적 부위에 대해 적어도 하나의 상동성 영역을 갖는다. 일부 경우에서, 단일 가닥 DNA 주형 또는 이중 가닥 DNA 주형은 표적 커팅 부위 또는 삽입 부위에 삽입되는 이종성 서열을 함유하는 영역을 플랭킹되는 2개의 상동성 영역, 예를 들어, 5' 말단 및 3' 말단을 갖는다.
본 발명의 상세한 설명
하기 설명은 본 발명의 조성물 및 방법의 다양한 측면 및 실시양태를 언급한다. 특별한 실시양태가 상기 조성물 및 방법의 범주를 정의하도록 의도되지 않는다. 오히려, 그러한 실시양태는 적어도 개시된 조성물 및 방법의 범주 내에 포함되는 다양한 조성물 및 방법의 비-제한적인 예를 제공할 뿐이다. 본 설명은 관련 기술분야의 통상의 기술자의 관점에서 판독되어야 하는 바; 통상의 기술자에게 널리 공지된 정보가 반드시 포함되는 것은 아니다.
본원에서는 인간 T 세포의 게놈을 편집하기 위한 조성물 및 방법을 제공한다. 이종성 TCR이 T 세포의 게놈 중 표적화된 영역 내로 삽입될 수 있고, 이로써, 이종성 TCR은 내인성 TCR 프로모터의 제어 하에 있게 된다는 것을 본 발명자들은 발견하게 되었다. 본원에 제공된 방법 및 조성물을 사용하여 원하는 항원 특이성을 갖는 변형된 T 세포를 제조할 수 있다. 이러한 변형된 T 세포는 대상체에서 예를 들어, 암, 자가면역 질환 또는 감염을 치료하는데 사용될 수 있다.
일부 실시양태에서, 이종성 TCR-β 쇄의 가변 영역 및 이종성 TCR-α 쇄의 가변 영역을 코딩하는 핵산 서열은 T 세포의 게놈 중 TRAC 유전자의 엑손 1 내로 삽입된다. 일부 실시양태에서, 이종성 TCR-α 쇄의 가변 영역 및 이종성 TCR-β 쇄의 가변 영역을 코딩하는 핵산 서열은 T 세포의 게놈 중, TRBC 유전자의 엑손 1 내로, 예를 들어, TRBC1 또는 TRBC2의 엑손 1 내로 삽입된다. 일부 실시양태에서, 핵산 서열은 상동성 지정 복구를 통해, 또는 다르게는 본원에 기재된 바와 같이 도입된다.
일부 실시양태에서, (a) T 세포 수용체의 이종성 TCR-α 쇄의 가변 영역을 코딩하는 제1 핵산 서열; 및 (b) 항원 특이적 T 세포 수용체의 이종성 TCR-β 쇄의 가변 영역을 코딩하는 제2 핵산 서열은 각각 TRAC 유전자의 엑손 1 및 TRBC 유전자의 엑손 1 내로 삽입된다. 일부 실시양태에서, 핵산 서열은 상동성 지정 복구를 통해, 또는 다르게는 본원에 기재된 바와 같이 도입된다.
변형된 인간 T 세포를 제조하는 방법
T 세포의 게놈을 편집하는 방법은 인간 T 세포에서 T 세포 수용체 (TCR)-서브유닛 불변 유전자의 엑손 1 내의 표적 영역 내로 핵산 서열 또는 구축물을 삽입하는 것을 포함하는 인간 T 세포의 게놈을 편집하는 방법을 포함한다. 핵산 구축물은 순차적으로 N-말단에서 C-말단으로, TCR 서브유닛 쇄이 TCR 서브유닛 쇄의 가변 영역 및 불변 영역을 포함하는 것인 제1 이종성 TCR 서브유닛 쇄, 및 제2 이종성 TCR 서브유닛 쇄의 가변 영역을 코딩한다. 구축물은 추가로 제1 이종성 TCR 서브유닛 쇄의 가변 영역에 선행하는 제1 자기-절단 펩티드, 및 제1 이종성 TCR 서브유닛 쇄와 제2 이종성 TCR 서브유닛 쇄 사이의 제2 자기-절단 펩티드를 코딩한다. 일부 방법에서, 내인성 TCR 서브유닛이 TCR-알파 (TCR-α) 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-베타 (TCR-β) 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이다. 일부 방법에서, 내인성 TCR 서브유닛이 TCR-β 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-β 서브유닛 쇄이다.
일부 실시양태에서, TCR 서브유닛 쇄의 가변 영역을 코딩하는 핵산 구축물 또는 서열은 TCR 서브유닛 쇄를 코딩하는 핵산 구축물 또는 서열, 즉, TCR 서브유닛 쇄, 예를 들어, 전장 TCR 서브유닛 쇄의 가변 영역 및 불변 영역을 코딩하는 핵산이다. 일부 예에서, 핵산은 전장 TCR-α, TCR-β, TCR-γ, 또는 TCR-δ 서브유닛 쇄를 코딩한다. 일부 예에서, 핵산 구축물 또는 서열은 제1 이종성 TCR 서브유닛 쇄 (예를 들어, 전장 TCR 서브유닛 쇄) 및 제2 이종성 TCR 서브유닛 쇄의 가변 영역을 코딩한다. 일부 예에서, 제1 및 제2 이종성 TCR 서브유닛 쇄는 상이한 것이다. 일부 예에서, 핵산 구축물은, N-말단에서 C-말단으로, 이종성, 전장 TCR-β 서브유닛 쇄 및 이종성 TCR-α 서브유닛 쇄의 가변 영역을 코딩한다. 다른 예에서, 핵산 구축물은, N-말단에서 C-말단으로, 이종성, 전장 TCR-α 서브유닛 쇄 및 이종성 TCR-β 서브유닛 쇄의 가변 영역을 코딩한다.
T 세포의 게놈을 편집하는 방법은 인간 T 세포에서 TCR-α 서브유닛 (TRAC) 유전자의 엑손 1 내의 표적 영역 내로 핵산 서열 또는 구축물을 삽입하는 것을 포함하는 인간 T 세포의 게놈을 편집하는 방법을 포함한다. 일부 실시양태에서, 표적 영역은 TRAC 유전자의 불변 도메인의 엑손 1에 존재한다. 다른 실시양태에서, 표적 영역은 TCR-α 막횡단 도메인을 코딩하는 서열 출발점 앞의 엑손 1, 엑손 2 또는 엑손 3에 존재한다. 핵산 구축물은 순차적으로, N-말단에서 C-말단으로, 이종성 T 세포 수용체 (TCR)-β 쇄의 가변 영역, 이어서, 이종성 TCR-α 쇄의 가변 영역을 코딩한다. 구축물은 추가로 이종성 TCR-β 쇄의 가변 영역에 선행하는 제1 자기-절단 펩티드, 및 이종성 TCR-β 쇄의 가변 영역과 이종성 TCR-α 쇄의 가변 영역 사이의 제2 자기-절단 펩티드를 코딩한다. 구축물은 추가로 이종성 TCR-α 쇄의 가변 영역 뒤의 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩한다. TRAC 유전자 중 삽입 부위에 의존하여, 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩하는 핵산 크기는 달라질 수 있다. 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩하는 핵산 크기는 TRAC 엑손 1의 출발점과 표적화된 삽입 부위 사이의 내인성 TRAC 핵산 서열 중 뉴클레오티드 개수에 의존하게 될 것이다. 예를 들어, TRAC 엑손 1의 출발점과 삽입 부위 사이의 뉴클레오티드 개수는 25개의 뉴클레오티드였기 때문에, 내인성 TCR-α 서브유닛의 N-말단을 코딩하는 25개의 뉴클레오티드가 구축물 내에 포함된, 도 1a를 참조한다. 유사하게, TRAC 엑손 1의 출발점과 삽입 부위 사이의 뉴클레오티드 개수가 25개 미만 또는 25개 초과 사이의 뉴클레오티드인 경우, 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩하는 25개 미만 또는 25개 초과의 뉴클레오티드의 핵산이 구축물 내에 존재할 수 있다. 일부 예에서, 핵산 구축물은, N-말단에서 C-말단으로, 제1 자기-절단 펩티드 서열, 이종성(즉, 가변 영역 및 불변 영역) TCR-β 서브유닛 쇄(예를 들어, 전장 TCR-β 서브유닛 쇄), 제2 자기-절단 펩티드 서열, 이종성 TCR-α 서브유닛 쇄의 가변 영역 및 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩한다. 예시적인 구축물은 도 1a에 제시된 것을 포함한다.
T 세포의 게놈을 편집하는 방법은 또한 인간 T 세포에서 TCR-β 서브유닛 (TRBC) 유전자의 엑손 1 내의 표적 영역 내로 핵산 서열 또는 구축물을 삽입하는 것을 포함하는 인간 T 세포의 게놈을 편집하는 방법을 포함한다. 일부 실시양태에서, 표적 영역은 TRBC1 또는 TRBC2 유전자의 엑손 1에 존재한다. 핵산 구축물은 순차적으로 N-말단에서 C-말단으로, 이종성 T 세포 수용체 (TCR)-α 쇄의 가변 영역, 이어서, 이종성 TCR-β 쇄의 가변 영역을 코딩한다. 구축물은 추가로 이종성 TCR-α 쇄의 가변 영역에 선행하는 제1 자기-절단 펩티드, 및 이종성 TCR-α 쇄의 가변 영역과 이종성 TCR-β 쇄의 가변 영역 사이의 제2 자기-절단 펩티드를 코딩한다. 구축물은 추가로 이종성 TCR-β 쇄의 가변 영역 뒤의 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩한다. TRBC1 또는 TRBC2 중 삽입 부위에 의존하여, 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩하는 핵산 크기는 달라질 수 있다. 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩하는 핵산 크기는 TRBC1 또는 TRBC2 TRBC의 엑손 1의 출발점과 표적화된 삽입 부위 사이의 내인성 TRBC 핵산 서열 중 뉴클레오티드 개수에 의존하게 될 것이다. 예를 들어, TRBC 엑손 1의 출발점과 삽입 부위 사이의 뉴클레오티드 개수는 25개의 뉴클레오티드였기 때문에, 내인성 TCR-β 서브유닛의 N-말단을 코딩하는 25개의 뉴클레오티드가 구축물 내에 포함된, 도 1b를 참조한다. 유사하게, TRBC1 또는 TRBC2 엑손 1의 출발점과 삽입 부위 사이의 뉴클레오티드 개수가 25개 미만 또는 25개 초과 사이의 뉴클레오티드인 경우, 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩하는 25개 미만 또는 25개 초과의 뉴클레오티드의 핵산이 구축물 내에 존재할 수 있다. 일부 예에서, 핵산 구축물은, N-말단에서 C-말단으로, 제1 자기-절단 펩티드, 이종성 (즉, 가변 영역 및 불변 영역) TCR-α 서브유닛 쇄 (예를 들어, 전장 TCR-α 서브유닛 쇄), 제2 자기-절단 펩티드, 이종성 TCR-β 서브유닛 쇄의 가변 영역 및 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩한다. 예시적인 구축물은 도 1b에 제시된 것들을 포함한다.
자기-절단 펩티드의 예는 자기-절단 바이러스 2A 펩티드, 예를 들어, 돼지 테스코바이러스-1 (P2A) 펩티드, 토세아 아시그나 바이러스(Thosea asigna virus) (T2A) 펩티드, 말 비염 A 바이러스 (E2A) 펩티드, 또는 구제역 바이러스 (F2A) 펩티드를 포함하나, 이에 제한되지는 않는다. 자기-절단 2A 펩티드를 통해 단일 구축물로부터 다중 유전자 생성물을 발현할 수 있다. (예를 들어, 문헌 [Chng et al. "Cleavage efficient 2A peptides for high level monoclonal antibody expression in CHO cells," MAbs 7(2): 403-412 (2015)] 참조). 일부 실시양태에서, 제1 및 제2 자기-절단 펩티드는 동일한 것이다. 다른 실시양태에서, 제1 및 제2 자기-절단 펩티드는 상이한 것이다.
삽입 시, 제1 자기-절단 펩티드, 이종성 전장 TCR-β 쇄, 제2 자기-절단 펩티드, TCR-α 쇄의 가변 영역, 및 내인성 TCR-α 서브유닛의 N-말단 부분을 상기 순서대로 코딩하는 구축물은 내인성 TCR-α 프로모터 및 TCR-α 조절 요소의 제어 하에 있게 된다. 일단, 구축물이 T 세포의 게놈 내로 및 내인성 TCR-α 프로모터의 제어 하로 도입되고 나면, T 세포는 삽입된 구축물이 융합 폴리펩티드를 코딩하는 단일 mRNA 서열로 전사될 수 있도록 허용하는 조건 하에서 배양될 수 있다. 융합 폴리펩티드는 제1 자기-절단 펩티드, 이종성 전장 TCR-β 쇄, 제2 자기-절단 펩티드, 이종성 전장 TCR-α 쇄, 및 내인성 TCR-α 서브유닛의 N-말단 부분을 상기 순서대로 포함한다.
유사하게, TRBC1 또는 TRBC2에서의 삽입 시, 제1 자기-절단 펩티드, 이종성 전장 TCR-α 쇄, 제2 자기-절단 펩티드, TCR-β 쇄의 가변 영역, 및 내인성 TCR-β 서브유닛의 N-말단 부분을 상기 순서대로 코딩하는 구축물은 내인성 TCR-β 프로모터 및 TCR-β 조절 요소의 제어 하에 있게 된다. 일단, 구축물이 T 세포의 게놈 내로 및 내인성 TCR-β 프로모터의 제어 하로 도입되고 나면, T 세포는 삽입된 구축물이 융합 폴리펩티드를 코딩하는 단일 mRNA 서열로 전사될 수 있도록 허용하는 조건 하에서 배양될 수 있다. 융합 폴리펩티드는 제1 자기-절단 펩티드, 이종성 전장 TCR-α 쇄, 제2 자기-절단 펩티드, 이종성 전장 TCR-β 쇄, 및 내인성 TCR-β 서브유닛의 N-말단 부분을 상기 순서대로 포함한다.
구축물을 TRAC 유전자의 엑손 1 내로 삽입함으로써 TRAC 유전자의 남은 엑손 (엑손 2 및 3)은 엑손 1과 함께 스플라이싱되어 최종 mRNA 서열이 된다. 상기 mRNA 서열의 번역 결과로, 3개의 별개의 폴리펩티드 서열, 즉, 막횡단 도메인이 결여된 불활성 내인성 가변 영역 펩티드 (이는 예를 들어, 소포체에서 분해될 수 있거나, 또는 번역 후 분비될 수 있음), 전장 이종성 항원-특이적 TCR-β 쇄, 및 전장 이종성 항원-특이적 TCR-α 쇄로 자기-절단되는 하나의 단백질로 발현된다 (도 1a 참조). 전장 항원 특이적 TCR-β 쇄 및 전장 항원-특이적 TCR-α 쇄는 원하는 항원-특이성을 갖는 TCR을 형성한다.
유사하게, 구축물을 TRBC1/2 유전자의 엑손 1 내로 삽입함으로써 TRBC1/2 유전자의 남은 엑손 (엑손 2-4)은 엑손 1과 함께 스플라이싱되어 최종 mRNA 서열이 된다. 상기 mRNA 서열의 번역 결과로, 3개의 별개의 폴리펩티드 서열, 즉, 막횡단 도메인이 결여된 불활성 내인성 가변 영역 펩티드 (이는 예를 들어, 소포체에서 분해될 수 있거나, 또는 번역 후 분비될 수 있음), 전장 이종성 항원-특이적 TCR-β 쇄, 및 전장 이종성 항원-특이적 TCR-α 쇄로 자기-절단되는 하나의 단백질로 발현된다. 전장 항원 특이적 TCR-β 쇄 및 전장 항원-특이적 TCR-α 쇄는 원하는 항원-특이성을 갖는 TCR을 형성한다.
대안적으로, 이종성 TCR-α 쇄 코딩 서열, 예를 들어, TCR-α 쇄의 가변 영역을 코딩하는 서열 및 이종성 TCR-β 쇄 코딩 서열, 예를 들어, TCR-β 쇄의 가변 영역을 코딩하는 서열은 T 세포의 게놈 내로 삽입되며, 여기서 이종성 TCR-α 쇄는 TRAC 유전자의 엑손 1 내로 삽입되고, 이종성 TCR-β 쇄는 TRBC 유전자의 엑손 1 내로 삽입된다. 일부 실시양태에서, 이종성 TCR-α 쇄를 코딩하는 제1 핵산 서열 또는 구축물 및 이종성 TCR-β 쇄를 코딩하는 제2 핵산 서열 또는 구축물은 TRAC 유전자의 엑손 1에 이종성 TCR-α 쇄를, 및 TRBC 유전자의 엑손 1에 이종성 TCR-β 쇄를 삽입하는데 사용된다.
제1 및 제2 핵산 구축물을 사용하는 방법에서, 이종성 TCR-α 쇄를 코딩하는 핵산의 삽입을 위한 표적 영역은 TRAC 유전자의 엑손 1에 있다. 일부 실시양태에서, 이종성 TCR-β 쇄를 코딩하는 핵산의 삽입을 위한 표적 영역은 내인성 TRBC1 또는 TRBC2 프로모터의 하류에 있고, TRBC1 또는 TRBC 2 유전자의 엑손 1에 위치한다. 제1 핵산은 순차적으로 N-말단에서 C-말단으로, 제1 자기-절단 펩티드, 이어서, 이종성 TCR-α 쇄, 이어서, 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩한다. 제2 핵산 구축물은 순차적으로 N-말단에서 C-말단으로, 제2 자기-절단 펩티드, 이어서, 이종성 TCR-β 쇄를 코딩하는 핵산, 이어서, 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩한다. 예시적인 구축물은 도 2에 제시된 것을 포함한다.
삽입 시, 제1 자기-절단 펩티드 및 이종성 TCR-α 쇄를 상기 순서대로 코딩하는 제1 구축물은 내인성 TCR-α 프로모터 및 TCR-α 조절 요소의 제어 하에 있게 된다. 제2 자기-절단 펩티드 및 이종성 TCR-β 쇄를 상기 순서대로 코딩하는 제2 구축물은 내인성 TCR-β 프로모터 및 TCR-β 조절 요소의 제어 하에 있게 된다. 일단, 구축물이 T 세포의 게놈 내로 및 내인성 TCRα 및 TCR-β프로모터의 제어 하로 도입되고 나면, T 세포는 제1 구축물 및 제2 구축물이 별개의 mRNA 서열로 전사될 수 있도록 허용하는 조건 하에서 배양된다. 구축물을 TRAC 유전자의 엑손 1 내로 삽입함으로써 TRAC 유전자의 남은 엑손 (엑손 2 및 3)은 엑손 1과 함께 스플라이싱되어 전장 이종성 TCR-α 쇄를 코딩하는 최종 mRNA 서열이 된다. 유사하게, 제2 구축물이 TRBC 유전자의 엑손 1 내로 삽입함으로써 TRBC 유전자의 남은 엑손 (엑손 2 및 3)은 엑손 1과 함께 스플라이싱되어 전장 이종성 TCR-β 쇄를 코딩하는 mRNA 서열이 된다.
제1 자기-절단 펩티드 및 전장 이종성 TCR-α 쇄를 코딩하는 mRNA 서열의 번역 결과로, 막횡단 도메인이 결여된 불활성 내인성 가변 영역 펩티드 (이는 예를 들어, 소포체에서 분해될 수 있거나, 또는 번역 후 분비될 수 있음), 및 전장 이종성 항원-특이적 TCR-α 쇄가 발현된다. 제2 자기-절단 펩티드 및 전장 이종성 TCR-β 쇄를 코딩하는 mRNA 서열의 번역 결과로, 막횡단 도메인이 결여된 불활성 내인성 가변 영역 펩티드 (이는 예를 들어, 소포체에서 분해될 수 있거나, 또는 번역 후 분비될 수 있음), 및 전장 이종성 항원-특이적 TCR-β 쇄가 발현된다. 전장 이종성, 항원 특이적 TCR-β 쇄 및 전장 이종성, 항원-특이적 TCR-α 쇄는 원하는 항원-특이성을 갖는 TCR을 형성한다.
본원에 제공된 방법에서, 이종성 TCR-β 쇄의 가변 영역은 가변 (V), 다양성 (D) 및 연결 (J) 대립유전자를 포함한다. 본원에 제공된 방법에서, 이종성 TCR-α 쇄의 가변 영역은 V 및 J 대립유전자를 포함한다. 예를 들어, 문헌 [Kuby, J., Immunology, 7th Ed., W.H. Freeman & Co., New York (2013)]을 참조한다.
일부 실시양태에서, 핵산 서열은 핵산을 포함하는 벡터, 예를 들어, 바이러스 벡터를 도입함으로써 T 세포의 게놈 내로 삽입된다. 바이러스 벡터의 예는 아데노 연관 바이러스 (AAV) 벡터, 레트로바이러스 벡터 또는 렌티바이러스 벡터를 포함하나, 이에 제한되지는 않는다. 일부 실시양태에서, 렌티바이러스 벡터는 인테그라제 결핍 렌티바이러스 벡터이다.
일부 실시양태에서, 핵산 서열은 비-바이러스 전달을 통해 T 세포의 게놈 내로 삽입된다. 비-바이러스 전달 방법에서, 핵산은 네이키드 DNA일 수 있거나, 또는 비-바이러스 플랏미드 또는 벡터 내에 존재할 수 있다.
일부 실시양태에서, 핵산은 T 세포 내로 (a) TRAC 유전자의 엑손 1 내의 표적 영역을 절단하여 T 세포의 게놈에 삽입 부위를 생성하는 표적화된 뉴클레아제; 및 (b) HDR에 의해 삽입 부위 내로 도입되는 핵산 서열을 도입함으로써 T 세포 내로 삽입된다. 일부 실시양태에서, 핵산은 T 세포 내로 (a) TRBC 유전자의 엑손 1 내의 표적 영역을 절단하여 T 세포의 게놈에 삽입 부위를 생성하는 표적화된 뉴클레아제; 및 (b) HDR에 의해 삽입 부위 내로 도입되는 핵산 서열을 도입함으로써 T 세포 내로 삽입된다.
일부 실시양태에서, 방법은 세포 내로, TRAC 유전자의 엑손 1의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함한다. 일부 실시양태에서, 방법은 세포 내로, TRBC 유전자의 엑손 1의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함한다.
제1 및 제2 핵산 서열을 사용하여 이종성 TCR-α 쇄 및 이종성 TCR-β 쇄를 각각 TRAC 유전자의 엑손 1 및 TRBC 유전자의 엑손 1 내로 삽입시키는 실시양태에서, 제1 및 제2 핵산은 T 세포 내로 (a) TRAC 유전자의 엑손 1 내의 제1 삽입 부위, 및 TRBC 유전자의 엑손 1 내의 제2 삽입 부위를 생성하는 하나 이상의 표적화된 뉴클레아제; (b) 제1 핵산 서열; 및 (c) 제2 핵산 서열을 도입함으로써 T 세포 내로 삽입된다. 일부 실시양태에서, 방법은 세포 내로, TRAC 유전자의 엑손 1의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA, 및 TRBC 유전자의 엑손 1의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함한다.
일부 실시양태에서, 핵산 서열의 5' 및 3' 말단은 각각 T 세포의 게놈 중 표적 영역, 예를 들어, TRAC 유전자의 엑손 1 내의 표적 영역, 또는 TRBC 유전자의 엑손 1 내의 표적 영역에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다. 일부 경우에서, 게놈 서열과 상동성인 뉴클레오티드 서열의 길이는 약 50 내지 300개의 뉴클레오티드 길이이다. 일부 경우에서, 게놈 서열과 상동성인 뉴클레오티드 서열, 또는 그의 부분은 게놈 서열과 적어도 80%, 90%, 95% 상보적이다. 일부 실시양태에서, 핵산 서열의 5' 및 3' 말단은 TRAC 유전자의 엑손 1 내의 삽입 부위에서 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태에서, 핵산 서열의 5' 및 3' 말단은 TRBC 유전자의 엑손 1 내의 삽입 부위에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함한다.
일부 경우에서, 핵산 서열은 선형 DNA 주형으로서 세포 내로 도입된다. 일부 경우에서, 핵산 서열은 이중 가닥 DNA 주형으로서 세포 내로 도입된다. 일부 경우에서, DNA 주형은 단일 가닥 DNA 주형이다. 일부 경우에서, 단일 가닥 DNA 주형은 순수한 단일 가닥 DNA 주형이다. 본원에서 사용되는 바와 같이, "순수한 단일 가닥 DNA"란, DNA의 다른 또는 반대 가닥이 실질적으로 결여된 단일 가닥 DNA를 의미한다. "실질적으로 결여된"이란, 순수한 단일 가닥 DNA에는, DNA의 하나의 가닥이 또 다른 가닥보다 적어도 100배 더 결여된다는 것을 의미한다. 일부 경우에서, DNA 주형은 이중 가닥 또는 단일 가닥 플라스미드 또는 미니-서클(mini-circle)이다.
일부 실시양태에서, 표적화된 뉴클레아제는 RNA-가이드된 뉴클레아제 도메인, 전사 활성인자-유사 이펙터 뉴클레아제 (TALEN), 아연 핑거 뉴클레아제 (ZFN) 및 메가TAL 로 이루어진 군으로부터 선택된다 (예를 들어, 문헌 [Merkert and Martin "Site-Specific Genome Engineering in Human Pluripotent Stem Cells," Int. J. Mol . Sci . 18(7): 1000 (2016)] 참조). 일부 실시양태에서, RNA-가이드된 뉴클레아제는 Cas9 뉴클레아제이고, 방법은 세포 내로 T 세포의 게놈 중 표적 영역, 예를 들어, TRAC 유전자의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함한다. 다른 실시양태에서, RNA-가이드된 뉴클레아제는 Cas9 뉴클레아제이고, 방법은 세포 내로 TRBC 유전자의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함한다.
전반에 걸쳐 사용되는 바와 같이, 가이드 RNA (gRNA) 서열은 부위-특이적 또는 표적화된 뉴클레아제와 상호작용하고, 세포의 게놈 내의 표적 핵산에 특이적으로 결합하거나, 또는 그에 하이브리드화하고, 이로써, gRNA 및 표적화된 뉴클레아제는 세포의 게놈 중 표적 핵산에 공동 국재화되는 것인 서열이다. 각 gRNA는 게놈 중의 표적 DNA 서열에 특이적으로 결합하거나, 또는 그에 하이브리드화하며, 길이가 약 10 내지 50개의 뉴클레오티드 길이인 DNA 표적화 서열 또는 프로토스페이서 서열을 포함한다. 예를 들어, DNA 표적화 서열의 길이는 약 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 또는 50개의 뉴클레오티드 길이이다. 일부 실시양태에서, gRNA는 crRNA 서열 및 트랜스활성화 crRNA (tracrRNA) 서열을 포함한다. 일부 실시양태에서, gRNA는 tracrRNA 서열을 포함하지 않는다.
일반적으로, DNA 표적화 서열은 DNA 서열에 상보성을 띠도록 (예를 들어, 완벽한 상보성을 띠도록), 또는 실질적으로 상보성을 띠도록 디자인된다. 일부 경우에서, DNA 표적화 서열은 다중 유전자 요소에 결합하기 위해 워블 또는 축중성 염기를 도입할 수 있다. 일부 경우에서, 결합 영역의 3' 또는 5' 말단의 19개의 뉴클레오티드는 표적 유전자 요소 또는 요소들에 완벽하게 상보적이다. 일부 경우에서, 결합 영역은 안정성을 증가시키도록 변경될 수 있다. 예를 들어, 비천연 뉴클레오티드는 분해에 대한 RNA 저항을 증가시키기 위해 도입될 수 있다. 일부 경우에서, 결합 영역은 결합 영역은 결합 영역에서의 2차 구조 형성을 막거나, 감소시키도록 변경 또는 디자인될 수 있다. 일부 경우에서, 결합 영역은 G-C 함량을 최적화시키도록 디자인될 수 있다. 일부 경우에서, G-C 함량은 바람직하게는 약 40% 내지 약 60% (예를 들어, 40%, 45%, 50%, 55%, 60%)이다. 일부 실시양태에서, Cas9 단백질은 활성 엔도뉴클레아제 형태일 수 있고, 이로써, 가이드 RNA와의 복합체의 일부로서, 또는 DNA 주형과의 복합체의 일부로서 표적 핵산에 결합되었을 때, 이중 가닥 파단이 표적 핵산 내로 도입된다. 본원에 제공된 방법에서, Cas9 폴리펩티드 또는 Cas9 폴리펩티드를 코딩하는 핵산은 T 세포 내로 도입될 수 있다. 이중 가닥 파단은 DNA 주형을 T 세포의 게놈 내로 삽입시키기 위해 HDR에 의해 복구될 수 있다. 다양한 Cas9 뉴클레아제가 본원에 기재된 방법에서 사용될 수 있다. 예를 들어, 가이드 RNA에 의해 표적화된 영역의 3' 바로 옆에 NGG 프로토스페이서 인접 모티프 (PAM)를 필요로 하는 Cas9 뉴클레아제가 사용될 수 있다. 상기 Cas9 뉴클레아제는 NGG 서열을 함유하는, TRAC의 엑손 1 또는 TRBC의 엑손 1 중의 영역으로 표적화될 수 있다. 또 다른 예로서, 오르토고날 PAM 모티프 요건을 갖는 Cas9 단백질을 사용하여 인접한 NGG PAM 서열을 갖지 않는 서열을 표적화할 수 있다. 오르토고날 PAM 서열 특이성을 갖는 예시적인 Cas9 단백질의 예는 문헌 [Esvelt et al., Nature Methods 10: 1116-1121 (2013)]에 기재된 것을 포함하나, 이에 제한되지는 않는다.
일부 경우에서, Cas9 단백질은 닉카제이고, 이로써, 가이드 RNA와의 복합체의 일부로서 표적 핵산에 결합되었을 때, 단일 가닥 파단 또는 닉이 표적 핵산 내로 도입된다. 각각이 구조적으로 상이한 가이드 RNA에 결합된, 한 쌍의 Cas9 닉카제는 표적 게놈 영역의 2개의 근위 부위에 표적화될 수 있는 바, 이로써, 한 쌍의 근위 단일 가닥 파단을 표적 게놈 영역, 예를 들어, TRAC 유전자의 엑손 1, 또는 TRBC 유전자의 엑손 1 내로 도입할 수 있다. 오프-타겟 효과가 단일 닉을 초래할 가능성이 있기 때문에 닉카제 쌍은 증진된 특이성을 제공할 수 있으며, 이러한 닉은 일반적으로, 염기 절제 복구 기전에 의해 병변 없이 복구된다. 예시적인 Cas9 닉카제는 D10A 또는 H840A 돌연변이를 갖는 Cas9 뉴클레아제를 포함한다 (예를 들어, 문헌 [Ran et al. "Double nicking by RNA-guided CRISPR Cas9 for enhanced genome editing specificity," Cell 154(6): 1380-1389 (2013)]).
일부 실시양태에서, Cas9 뉴클레아제, 가이드 RNA 및 핵산 서열은 세포 내로 리보핵단백질 복합체 (RNP)-DNA 주형 복합체로서 도입되며, 여기서 RNP-DNA 주형 복합체는 (i) Cas9 뉴클레아제 및 가이드 RNA를 포함하는 RNP; 및 (ii) 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄를 코딩하는 DNA 주형으로서, HDR을 통해 TRAC 유전자의 엑손 1 내로 삽입되는 DNA 주형을 포함한다. 일부 실시양태에서, Cas9 뉴클레아제, 가이드 RNA 및 핵산 서열은 세포 내로 리보핵단백질 복합체 (RNP)-DNA 주형 복합체로서 도입되며, 여기서 RNP-DNA 주형 복합체는 (i) Cas9 뉴클레아제 및 가이드 RNA를 포함하는 RNP; 및 (ii) 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄를 코딩하는 DNA 주형으로서, HDR을 통해 TRBC 유전자의 엑손 1 내로 삽입되는 DNA 주형을 포함한다.
일부 실시양태에서, 별개의 구축물을 사용하여 이종성 TCR-α 쇄를 T 세포에서 TRAC 유전자의 엑손 1 내로, 및 이종성 TCR-β 쇄를 T 세포에서 TRBC 유전자의 엑손 1 내로 삽입하는 경우, (a) 제1 RNP-DNA 주형 복합체는, (i) RNP가 Cas9 뉴클레아제, 및 TRAC 유전자의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 제1 가이드 RNA를 포함하는 제1 RNP; 및 (ii) 이종성 TCR α 서브유닛을 코딩하는 DNA 주형을 포함하는 것인 제1 (RNP)-DNA 주형 복합체; 및 (b) 제2 RNP-DNA 주형 복합체는 (i) 제2 RNP가 Cas9 뉴클레아제, 및 TRBC 유전자의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 제2 가이드 RNA를 포함하는 것인 제2 RNP; 및 (ii) 이종성 TCR β 서브유닛을 코딩하는 DNA 주형을 포함하는 것인 제2 (RNP)-DNA 주형 복합체가 세포 내로 도입된다. 일부 실시양태에서, 제1 RNP-DNA 주형 복합체 중 Cas9 뉴클레아제 및 제2 RNP-DNA 주형 복합체 중 Cas9 뉴클레아제는 동일한 것이다. 일부 실시양태에서, 제1 RNP-DNA 주형 복합체 중 Cas9 뉴클레아제 및 제2 RNP-DNA 주형 복합체 중 Cas9 뉴클레아제는 상이한 것이다.
일부 실시양태에서, RNP 대 DNA 주형의 몰비는 약 3:1 내지 약 100:1일 수 있다. 예를 들어, 몰비는 약 5:1 내지 10:1, 약 5:1 내지 약 15:1, 5:1 내지 약 20:1; 5:1 내지 약 25:1; 약 8:1 내지 약 12:1; 약 8:1 내지 약 15:1, 약 8:1 내지 약 20:1, 또는 약 8:1 내지 약 25:1일 수 있다.
일부 실시양태에서, RNP-DNA 주형 복합체 중 DNA 주형은 약 2.5 pM 내지 약 25 pM 농도로 존재한다. 일부 실시양태에서, DNA 주형의 양은 약 1 μg 내지 약 10 μg이다.
일부 경우에서, RNP-DNA 주형 복합체는 약 20℃ 내지 약 25℃의 온도에서 약 1분 미만 내지 약 30분 동안 RNP를 DNA 주형과 함께 인큐베이션함으로써 형성된다. 일부 실시양태에서, RNP-DNA 주형 복합체를 세포 내로 도입하기 전에 RNP-DNA 주형 복합체 및 세포를 혼합한다.
일부 실시양태에서, 핵산 서열 또는 RNP-DNA 주형 복합체를 전기천공에 의해 T 세포 내로 도입한다. RNP-DNA 주형 복합체를 도입하기 위해 세포를 전기천공하는 방법, 조성물, 및 장치는 본원 실시예에 기재된 것을 포함할 수 있다. RNP-DNA 주형 복합체를 도입하기 위해 세포를 전기천공하는 추가의 또는 대안적 방법, 조성물, 및 장치는 WO/2006/001614 또는 문헌 [Kim, J.A. et al. Biosens. Bioelectron. 23, 1353-1360 (2008)]에 기재된 것을 포함할 수 있다. RNP-DNA 주형 복합체를 도입하기 위해 세포를 전기천공하는 추가의 또는 대안적 방법, 조성물, 및 장치는 미국 특허 출원 공개 번호 2006/0094095; 2005/0064596; 또는 2006/0087522에 기재된 것을 포함할 수 있다. RNP-DNA 주형 복합체를 도입하기 위해 세포를 전기천공하는 추가의 또는 대안적 방법, 조성물, 및 장치는 문헌 [Li, L.H. et al. Cancer Res. Treat. 1, 341-350 (2002)]; 미국 특허 번호 6,773,669; 7,186,559; 7,771,984; 7,991,559; 6485961; 7029916; 및 미국 특허 출원 공개 번호 2014/0017213; 및 2012/0088842에 기재된 것을 포함할 수 있다. RNP-DNA 주형 복합체를 도입하기 위해 세포를 전기천공하는 추가의 또는 대안적 방법, 조성물, 및 장치는 문헌 [Geng, T. et al. J. Control Release 144, 91-100 (2010)]; 및 [Wang, J., et al. Lab. Chip 10, 2057-2061 (2010)]에 기재된 것을 포함할 수 있다.
일부 실시양태에서, 적어도 2개의 구조적으로 상이한 RNP-DNA 주형 복합체를 포함하는 복수의 RNP-DNA 주형 복합체가 세포 내로 도입된다. 전반에 걸쳐 사용되는 바와 같이, "복수"라는 어구는 2개 이상인 것을 의미한다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 RNP-DNA 주형 복합체는 구조적으로 상이한 가이드 RNA를 함유한다. 일부 실시양태에서, 적어도 2개의 구조적으로 상이한 RNP 복합체가 구조적으로 상이한 가이드 RNA를 함유하는 경우, 구조적으로 상이한 RNP 복합체는 각각 Cas9 닉카제를 포함하고, 구조적으로 상이한 가이드 RNA는 표적 영역의 반대 가닥에 하이브리드화한다.
일부 실시양태에서, 이종성 TCR-β 쇄의 가변 영역 및 이종성 TCR-α 쇄의 가변 영역을 코딩하는 적어도 2개의 구조적으로 상이한 핵산이 T 세포의 집단 중 TRAC 유전자의 엑손 1 내로 도입된다. 이러한 방식으로, 각 핵산 서열이 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 고유한 조합을 코딩하는 것인 복수의 핵산 서열이 T 세포의 집단 내로 도입될 수 있다. 각 핵산 서열은 RNP-DNA 주형 복합체의 일부로서 세포 내로 도입될 수 있다.
예를 들어, 표적화된 뉴클레아제는 복수의 (예를 들어, 2, 3, 4, 5개 또는 그 초과, 예를 들어, 2-10, 5-100, 20-100개), 이종성 TCR-β 쇄의 가변 영역 및 이종성 TCR-α 쇄의 가변 영역을 코딩하는 고유한 DNA 주형과 복합체를 형성할 수 있다. 복수의 복합체는 T 세포의 집단 내로 동시에 도입되어 이종성 TCR-β 쇄의 가변 영역 및 이종성 TCR-α 쇄의 가변 영역의 고유한 조합을 코딩하는 단일 DNA 주형을 개별 T 세포에서 TRAC 유전자의 엑손 1 내로 삽입할 수 있다. 비록 각 T 세포는 전체 세포의 집단에 걸쳐 오직 단일 DNA 주형만을 획득하겠지만, 다수의 고유한 구조적으로 상이한 DNA 주형이 T 세포 내로 통합되어 이종성 TCR 서열 라이브러리를 생성하게 될 것이다.
일부 실시양태에서, 별개의 구축물을 사용하여 이종성 TCR-α 쇄를 TRAC 유전자의 엑손 1 내로, 및 이종성 TCR-β 쇄를 TRBC 유전자의 엑손 1 내로 삽입하는 경우, 제1 표적화된 뉴클레아제는 이종성 TCR-β 쇄의 가변 영역을 코딩하는 복수의 고유한 DNA 주형과 복합체를 형성하여 복수의 제1 RNP-DNA 주형 복합체를 형성할 수 있고, 제2 표적화된 뉴클레아제는 이종성 TCR-α 쇄의 가변 영역을 코딩하는 복수의 고유한 DNA 주형과 복합체를 형성하여 복수의 제2 RNP-DNA 주형 복합체를 형성할 수 있다. 제1 및 제2 복수의 복합체는 동시에 T 세포의 집단으로 도입되어 이종성 TCR 서열 라이브러리를 생성할 수 있다.
이종성 T 세포 레퍼토리는 이전에 공지된 TCR 서열 뿐만 아니라, 관심 내인성 T 세포 집단에서 발견되는 천연 레퍼토리로부터 디자인되고, 생성될 수 있다. 예를 들어, TCR 서열은 종양 침윤 림프구로부터, 자가면역 질환의 부위에서의 자가반응성 T 세포로부터, 또는 병원체 반응성 T 세포로부터 수득된 TCR 서열일 수 있다.
일부 실시양태에서, 핵산 서열 또는 RNP-DNA 주형 복합체는 약 1 × 105 내지 약 2 × 106개 T 세포 내로 도입된다. 예를 들어, 핵산 서열 또는 RNP-DNA 주형 복합체는 약 1 × 105개 세포 내지 약 5 × 105개 세포, 약 1 × 105개 세포 내지 약 1 × 106개 세포, 1 × 105개 세포 내지 약 1.5 × 106개 세포, 1 × 105개 세포 내지 약 2 × 106개 세포, 약 1 × 106개 세포 내지 약 1.5 × 106개 세포, 또는 약 1 × 106개 세포 내지 약 2 × 106개 세포 내로 도입될 수 있다.
본원에 제공된 방법 및 조성물에서, 인간 T 세포는 1차 T 세포일 수 있다. 일부 실시양태에서, T 세포는 조절 T 세포, 이펙터 T 세포, 또는 나이브 T 세포이다. 일부 실시양태에서, 이펙터 T 세포는 CD8+ T 세포이다. 일부 실시양태에서, T 세포는 CD4+CD8+ T 세포이다. 본원에 기재된 방법 중 임의의 것에 의해 변형된 세포 중 임의의 세포의 집단을 또한 제공한다. 세포는 시험관내, 생체외, 또는 생체내 존재할 수 있다. 일부 경우에서, T 세포는 대상체로부터 제거되고, 본원에 기재된 방법 중 임의의 것을 사용하여 변형되고, 환자에게 투여된다.
일부 실시양태에서, 변형된 T 세포는 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 발현을 허용하는 조건 하에서 배양되어 이종성 항원-특이적 T 세포 수용체를 형성한다. 다른 실시양태에서, T 세포는 변형된 세포의 집단을 확장시키는데 효과적인 조건 하에서 배양된다. 일부 실시양태에서, 항원-특이적 T 세포 수용체를 발현하는 T 세포는 정제된다.
조성물
본원에 제공된 방법 중 임의의 것에 의해 제조된 인간 T 세포를 또한 제공한다. 본원에 제공된 방법 중 임의의 것에 의해 제조된 인간 T 세포의 집단을 또한 제공한다. 적어도 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 99%, 또는 그 초과의 세포의 게놈이 이종성 핵산의 표적화된 삽입을 포함하며, 여기서 핵산은 TRAC의 엑손 1 또는 TRBC의 엑손 1 내로 삽입되어 있는 것인, 복수의 인간 T 세포을 또한 추가로 제공한다. 일부 실시양태에서, T 세포는 조절 T 세포, 이펙터 T 세포, 또는 나이브 T 세포이다. 일부 실시양태에서, 이펙터 T 세포는 CD8+ T 세포이다. 일부 실시양태에서, 이펙터 T 세포는 CD4+CD8+ T 세포이다.
T 세포로서, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) TCR 서브유닛 쇄가 TCR 서브유닛 쇄의 불변 영역 및 가변 영역을 포함하는 것인 제1 이종성 TCR 서브유닛 쇄, (iii) 제2 자기-절단 펩티드 서열; (iv) 제2 이종성 TCR 서브유닛 쇄의 가변 영역; 및 (v) 내인성 TCR 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함하며, 여기서 내인성 TCR 서브유닛이 TCR-알파 (TCR-α) 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-베타 (TCR-β) 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이며, 여기서 내인성 TCR 서브유닛이 TCR-β 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-β 서브유닛 쇄인 T 세포를 또한 제공한다. 일부 실시양태에서, 핵산 서열은, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열, (ii) 이종성 TCR-β 서브유닛 쇄, (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 서브유닛 쇄의 가변 영역, 및 (v) 내인성 TCR-α 서브유닛 쇄의 N-말단 부분을 코딩한다. 일부 예에서, 핵산은, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열, (ii) 이종성 TCR-α 서브유닛 쇄, (iii) 제2 자기-절단 펩티드 서열, (iv) 이종성 TCR-β 서브유닛 쇄의 가변 영역, 및 (v) 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩한다.
변형된 T 세포로서, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-β 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역; 및 (v) 내인성 TCR-α 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함하며, 여기서 핵산 서열은 TRAC 유전자의 엑손 1 내로 통합되는 것인 변형된 T 세포를 또한 제공한다. 일부 예에서, 핵산은, N-말단에서 C-말단으로, 제1-자기-절단 펩티드 서열, 이종성 (예를 들어, 전장) TCR-β 서브유닛 쇄, 제2 자기-절단 펩티드 서열 및 이종성 TCR-α 서브유닛 쇄의 가변 영역을 코딩한다.
변형된 T 세포로서, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-α 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-β 쇄의 가변 영역; 및 (v) 내인성 TCR-β 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함하며, 여기서 핵산 서열은 TRBC 유전자의 엑손 1 내로 통합되는 것인 변형된 T 세포를 또한 제공한다. 다른 예에서, 핵산은, N-말단에서 C-말단으로, 제1 자기-절단 펩티드 서열, 이종성 (예를 들어, 전장) TCR-α 서브유닛 쇄, 제2 자기-절단 펩티드 서열 및 이종성 TCR-β 서브유닛 쇄의 가변 영역을 코딩한다.
변형된 T 세포로서, N-말단에서 C-말단으로, (i) 제1 자기-절단 펩티드 서열; (ii) 이종성 TCR-β 쇄의 가변 영역; (iii) 제2 자기-절단 펩티드 서열; (iv) 이종성 TCR-α 쇄의 가변 영역; 및 (v) 내인성 TCR-γ 서브유닛의 N-말단 부분을 코딩하는 핵산 서열을 포함하며, 여기서 핵산 서열은 TRGC 유전자의 엑손 1의 엑손 1 내로 통합되는 것인 변형된 T 세포를 또한 제공한다.
변형된 T 세포로서, a) N-말단에서 C-말단으로, (i) 제1 자기-절단 서열, (ii) 이종성 TCR-α 쇄의 가변 영역, 및 (iii) 내인성 TCR-α 쇄의 N-말단 부분을 코딩하는 제1 핵산 서열; 및 b) N-말단에서 C-말단으로, (i) 제1 자기-절단 서열, (ii) 이종성 TCR-β 쇄의 가변 영역, 및 (iii) 내인성 TCR-β 쇄의 N-말단 부분을 코딩하는 제2 핵산 서열을 포함하며, 여기서 제1 핵산 서열은 TRAC 유전자의 엑손 1 내로 통합되고, 제2 핵산 서열은 TRBC 유전자의 엑손 1 내로 통합되는 것인 변형된 T 세포를 추가로 제공한다.
치료 방법
본원에 기재된 방법 및 조성물 중 임의의 것은 질환 (예를 들어, 대상체에서의 암, 감염성 질환, 자가면역 질환, 이식 거부, 이식편 대 숙주 질환 또는 다른 염증성 장애)을 치료 또는 예방하는데 사용될 수 있다. 본원에 제공된 치료 방법에서, 예를 들어, 암, 감염성 질환, 자가면역 질환, 이식 거부를 일으킬 잠재성, 이식편 대 숙주 질환 또는 염증성 장애를 갖는 대상체에서 TCR의 TCR-α 또는 TCR-β 쇄를 포함하는 핵산 서열을 대상체에서 T 세포로부터 수득할 수 있다. 예를 들어, TCR의 TCR-α 또는 TCR-β 쇄를 포함하는 핵산 서열을 수득하기 위해, 종양 침윤 림프구, 자가면역 부위에서의, 또는 병원체 반응성 림프구로부터의 T 세포를 대상체로부터 단리할 수 있다. 일부 실시양태에서, 환자 샘플로부터 확인된 모노클로날 또는 폴리클로날 TCR 서열이 사용될 수 있다. 예를 들어, 종양 또는 염증 부위로부터의 TCR 레퍼토리를 수득할 수 있고, TCR 서열을 합성하고, 이를 DNA 주형으로서 사용함으로써 항원 특이성을 갖는 세포를 제조할 수 있다. 대안적으로, 대상체로부터의 클론/단일 세포로부터 서열을 증폭시키고, 예를 들어, PCR 증폭시킬 수 있고, 증폭된 서열을 DNA 주형으로서 사용할 수 있다. 일단 TCR의 TCR-α 및 TCR-β 쇄의 서열을 수득하고 나면, 이들 서열을 대상체 중의 또는 대상체로부터의 T 세포의 집단 내로 삽입하여 대상체 중의 T 세포의 내인성 TCR을 원하는 항원 특이성을 갖는 이종성 TCR로 대체할 수 있다. 일부 실시양태에서, 변형된 T 세포의 집단을 대상체엑 투여하여 질환을 치료할 수 있다. 예를 들어, 도 3b를 참조한다.
본원에서는 인간 대상체에서 암을 치료하는 방법으로서, 본원에 기재된 방법 중 임의의 것을 사용하여 항원-특이적 T 세포 수용체를 발현하도록 대상체의 T 세포를 변형시키는 단계를 포함하며, 여기서 T 세포 수용체는 대상체에서 종양-특이적 항원을 인식하는 것인 방법을 제공한다.
일부 실시양태에서, 치료하고자 하는 암은 B 세포 기원의 암, 유방암, 위암, 신경아세포종, 골육종, 폐암, 결장암, 만성 골수성 암, 백혈병 (예를 들어, 급성 골수성 백혈병, 만성 림프구성 백혈병 (CLL) 또는 급성 림프구성 백혈병 (ALL)), 전립선암, 결장암, 신장 세포 암종, 간암, 신장암, 난소암, 위암, 고환암, 횡문근육종, 및 호지킨 림프종으로부터 선택된다. 일부 실시양태에서, B 세포 기원의 암은 B 계통 급성 림프아구성 백혈병, B 세포 만성 림프구성 백혈병, 및 B 세포 비호지킨 림프종으로 이루어진 군으로부터 선택된다.
예를 들어, 암, 감염성 질환 또는 자가면역 장애 치료와 같은, 본원에 기재된 치료 방법의 일부 실시양태에서, T 세포는 생체내에서 변형된다. 본원에 기재된 구축물 중 임의의 것은 생체내에서 환자에게 전달된다. 예를 들어, 미국 특허 번호 9737604 및 문헌 [Zhang et al. "Lipid nanoparticle-mediated efficient delivery of CRISPR/Cas9 for tumor therapy," NPG Asia Materials Volume 9, page e441 (2017)]을 참조한다.
일부 실시양태에서, 인간 대상체에서 암을 치료하는 방법은 a) 대상체로부터 T 세포를 수득하는 단계; b) 본원에 제공된 방법 중 임의의 것을 사용하여 이종성 항원-특이적 T 세포 수용체를 발현하도록 T 세포를 변형시키는 단계로서, 여기서 T 세포 수용체는 대상체에서 종양-특이적 항원을 인식하는 것인 단계; 및 c) 변형된 T 세포를 대상체에게 투여하는 단계를 포함한다. 전반에 걸쳐 사용되는 바와 같이, "종양-특이적 항원"이라는 어구는 암 세포에 고유하거나, 또는 비암성 세포에서보다 암 세포에서 더욱 풍부하게 발현되는 항원을 의미한다.
본원에서는 인간 대상체에서 자가면역 질환을 치료하는 방법으로서, 본원에 기재된 방법 중 임의의 것을 사용하여 이종성 항원-특이적 T 세포 수용체를 발현하도록 대상체의 T 세포를 변형시키는 단계를 포함하며, 여기서 T 세포 수용체는 자가면역 장애와 연관된 항원을 인식하는 것인 방법을 추가로 제공한다.
일부 실시양태에서, 인간 대상체에서 자가면역 질환을 치료하는 방법은 a) 대상체로부터 T 세포를 수득하는 단계; b) 본원에 제공된 방법 중 임의의 것을 사용하여 이종성 항원-특이적 T 세포 수용체를 발현하도록 T 세포를 변형시키는 단계로서, 여기서 T 세포 수용체는 대상체에서 자가면역 장애와 연관된 항원을 인식하는 것인 단계; 및 c) 변형된 T 세포를 대상체에게 투여하는 단계를 포함한다. 일부 실시양태에서, T 세포는 조절 T 세포이다.
본원에서는 인간 대상체에서 감염을 치료하는 방법으로서, 본원에 기재된 방법 중 임의의 것을 사용하여 이종성 항원-특이적 T 세포 수용체를 발현하도록 대상체의 T 세포를 변형시키는 단계를 포함하며, 여기서 T 세포 수용체는 대상체에서 감염과 연관된 항원을 인식하는 것인 방법을 추가로 제공한다.
일부 실시양태에서, 인간 대상체에서 감염을 치료하는 방법은 a) 대상체로부터 T 세포를 수득하는 단계; b) 본원에 제공된 방법 중 임의의 것을 사용하여 이종성 항원-특이적 T 세포 수용체를 발현하도록 T 세포를 변형시키는 단계로서, 여기서 T 세포 수용체는 대상체에서 감염과 연관된 항원을 인식하는 것인 단계; 및 c) 변형된 T 세포를 대상체에게 투여하는 단계를 포함한다.
본원에 제공된 치료 방법 중 임의의 것은 내인성 TCR을 이종성 TCR로 대체하기 이전에 T 세포의 집단을 확장시키는 것을 추가로 포함할 수 있다. 본원에 제공된 치료 방법 중 임의의 것은 내인성 TCR을 이종성 TCR로 대체한 후, 및 대상체에게 투여하기 이전에 T 세포의 집단을 확장시키는 것을 추가로 포함할 수 있다.
개시된 방법 및 조성물의 생성물을 위해 사용될 수 있거나, 그와 함께 사용될 수 있거나, 그의 제조에서 사용될 수 있거나, 또는 그 자체인 물질, 조성물, 및 성분을 개시한다. 이들 물질 및 다른 물질을 본원에서 개시하고, 이들 물질의 조합, 서브세트, 상호작용, 그룹 등이 개시될 때, 이들 화합물의 각각의 다양한 개별적 및 집단적 조합 및 순열에 대한 구체적인 언급이 명확하게 개시되지 않을 수 있지만, 각각이 본원에 구체적으로 고려되고, 기재되는 것으로 이해된다. 예를 들어, 한 방법이 개시되고 논의되고, 상기 방법에 포함되는 하나 이상의 분자에 대해 이루어질 수 있는 다수의 변형이 논의되는 경우, 상기 방법의 각각의 및 모든 조합 및 순열, 및 가능한 변형이, 달리 반대로 구체적으로 명시되지 않는 한, 구체적으로 고려된다. 유사하게, 이들의 임의의 서브세트 또는 조합이 또한 구체적으로 고려되고, 개시된다. 이러한 개념은 개시된 조성물을 사용하는 방법에서의 단계를 포함하나, 이에 제한되지는 않는, 본 개시내용의 모든 측면에 적용된다. 따라서, 수행될 수 있는 다양한 추가 단계가 존재하는 경우, 이들 추가 단계는 각각 개시된 방법의 임의의 구체적인 방법 단계 또는 방법 단계의 조합으로 수행될 수 있고, 각각의 상기 조합 또는 조합의 서브세트가 구체적으로 고려되고, 개시된 것으로 간주되어야 하는 것으로 이해된다.
본원에 인용된 공개문헌 및 상기문헌들에 인용된 자료는 그 전문이 본원에 구체적으로 참조로 포함된다.
실시예
하기 실시예는 단지 예시를 위한 것이며 제한하려는 것이 아니다. 관련 기술분야의 통상의 기술자는 본질적으로 동일하거나 또는 유사한 결과를 산출하도록 변화되거나 또는 변형될 수 있는 다양한 비-임계 파라미터를 용이하게 인식할 것이다.
유전자
표적화를
위한 인간 1차 T 세포의 단리
1차 인간 T 세포는 신선한 전혈 샘플, 트리마 어페러시스(Trima Apheresis) (블러드 센터즈 오브 더 퍼시픽(Blood Centers of the Pacific)) 이후 백혈구 제거 챔버로부터의 잔류물, 또는 백혈구 성분 채집술 생성물 (스템셀(StemCell))로부터의 건강한 인간 공여자로부터 단리되었다. 말초 혈액 단핵구 세포 (PBMC)를 셉메이트 튜브(SepMate tube) (스템셀, 제조업체의 지시에 따름)를 사용하여 피콜(Ficoll) 원심분리에 의해 전혈 샘플로부터 단리하였다. 이지셉 인간 T 세포 단리 키트(EasySep Human T Cell Isolation Kit) (스템셀, 제조업체의 지시에 따름)를 사용하여 자기 음성 선택에 의해 모든 세포 공급원으로부터의 PBMC로부터 T 세포를 단리하였다. 달리 언급되지 않는 한, 단리된 T 세포를 자극하고, 직접 사용하였다 (신선한 세포). 동결된 세포를 사용한 경우, 제조업체의 지시에 따라 밤뱅커(Bambanker) 냉동 배지 (불독 바이오(Bulldog Bio))에서 냉동시킨 이전에 단리된 T 세포를 해동시키고, 1일 동안 자극 없이 배지에서 배양한 후, 이어서, 신선하게 단리된 샘플에 대해 기재된 바와 같이 자극하고, 취급하였다. 신선한 건강한 인간 혈액 공여자는 UCSF 인간 연구 위원회(Committee on Human Research: CHR)에 의해 승인된 프로토콜에 동의하였다. 유전자 편집을 위한 환자 샘플은 예일(Yale) 내부 검토 위원회(Internal Review Board: IRB)에 의해 승인된 프로토콜 하에서 수득되었다.
1차 T 세포 배양
달리 언급되지 않는 한, 벌크 T 세포를 5% 우태아 혈청, 50 mM 2-메르캅토 에탄올 및 10 mM N-아세틸 L-시스틴을 포함하는 XVivo™ 15 배지 (스템셀)에서 배양하였다. 첨가제를 포함하지 않는 무혈청 배지 (이뮤노컬트 XF(ImmunoCult XF) T 세포 확장 배지, 스템셀) 뿐만 아니라, RPMI + 10% FBS를 명시된 실험에 사용하였다 (도 15). 단리 직후, T 세포를 200 U/mL의 IL-2 (UCSF 파마시(UCSF Pharmacy)), 5 ng/mL의 IL-7 (써모피셔(ThermoFisher)), 및 5 ng/mL의 IL-15 (라이프 테크(Life Tech))의 시토카인 칵테일과 함께, 1:1의 비드 대 세포 농도에서 항-인간 CD3/CD28 자기 디나비드 (써모피셔)로 2일 동안 자극하였다. 전기천공 후, T 세포를 500 U/mL의 IL-2를 포함하는 배지에서 배양하였다. 배양 전 기간 동안, T 세포를 배지 1 mL당 대략 백만개의 세포 밀도로 유지시켰다. 전기천공 후, 2-3일마다 추가 배지를 추가의 신선한 IL-2와 함께 첨가하여, 최종 농도가 500 U/mL가 되도록 하였고, 필요에 따라 세포를 더 큰 배양 베쓸로 옮겨 백만개 세포/mL의 밀도를 유지시켰다.
RNP
제조
RNP는 앞서 기재된 바와 같이 ([Schumann et al. PNAS 112: 10437-10442 (2015)]; 및 [Hultquist et al. Cell Rep. 17: 1438-1452 (2016)])), 2-성분 gRNA를 Cas9로 어닐링함으로써 제조하였다. 간략하게, crRNA 및 tracrRNA를 화학적으로 합성하였고 (다르마콘(Dharmacon), IDT), 재조합 Cas9-NLS, D10A-NLS, 또는 dCas9-NLS를 재조합적으로 제조하고, 정제하였다 (QB3 마크로랩(Macrolab). 동결건조된 RNA를 160 uM 농도로 150 mM KCl을 포함하는 트리스-HCl (7.4 pH)에 재현탁시키고, -80℃에서 분취물로 보관하였다. crRNA 및 tracrRNA 분취물을 해동시키고, 부피 기준으로 1:1로 혼합하고, 37℃에서 30 min 동안 인큐베이션하여 80 uM gRNA 용액을 형성하였다. 이어서, 20 mM HEPES-KOH pH 7.5, 150 mM KCl, 10% 글리세롤, 1 mM DTT 중의 40 uM 하에 보관된 재조합 Cas9 및 변이체를 37℃에서 15 min 동안 80 uM gRNA와 부피 기준으로 1:1 (2:1 gRNA 대 Cas9 몰비)로 혼합하여 20 uM의 RNP를 형성하였다. RNP는 일반적으로 복합체 형성 직후에 전기천공하였다.
dsDNA
HDRT
제조
이중 가닥 DNA HDRT 서열은 PCR 생성물로부터 생성하였다. 깁슨 어셈블리즈(Gibson Assemblies)를 사용하여 신규 HDR 서열을 구축하여, 상동성 아암 (통상적으로 IDT로부터 gBlocks로서 합성) 및 서열 확인 및 추후 증식을 위한 클로닝 벡터 내로의 원하는 인서트 (예컨대 GFP)로 이루어진 HDR 주형 서열을 배치하였다. 이들 플라스미드를 고 처리량 PCR 증폭 (카파 핫스타트(Kapa Hotstart) 폴리머라제)을 위한 주형으로서 사용하였다. PCR 앰플리콘 (dsDNA HDRT)을 SPRI 정제하고 (1.0X), PCR 반응물 유입량 100 μL당 3 μL H2O의 최종 부피로 용출시켰다. 1:20 희석률로 나노드롭에 의해 HDRT의 농도를 분석하였다. 증폭된 HDRT의 크기는 1.0% 아가로스 겔에서 겔 전기영동에 의해 확인하였다.
엑소뉴클레아제
분해에 의한
ssDNA
HDRT
제조
HDR 공여자로서 긴 ssDNA를 제조하기 위해, 관심 DNA를 하나의 일반 비-변형된 PCR 프라이머 및 제2 인산화된 PCR 프라이머를 사용하여 PCR을 통해 증폭시켰다. 인산화된 프라이머를 사용하여 증폭되는 DNA 가닥은 이러한 방법을 사용하여 분해되는 가닥일 것이다. 이를 통해 각각의 인산화된 PCR 프라이머를 사용하여 단일 가닥 센스 또는 단일 가닥 안티센스 DNA를 제조할 수 있다. 관심 ssDNA 가닥을 제조하기 위해, PCR 생성물의 인산화된 가닥을 37℃에서 5분 동안 (1 kb 당) 각각 2개의 효소, 스트랜다제 믹스(Strandase Mix) A 및 스트랜다제 믹스 B로 후속 처리함으로써 분해시켰다. 80℃에서 5분 동안 인큐베이션하여 효소를 불활성화시켰다. 생성된 ssDNA HDR 주형을 SPRI 정제하고 (1.0X), H2O에서 용출시켰다. 가이드-잇™ 롱 ssDNA 프로덕션 시스템(Guide-it™ Long ssDNA Production System) (다카라 바이오 USA, 인크.(Takara Bio USA, Inc.) #632644)에 대한 보다 상세한 프로토콜은 제조업체의 웹사이트에서 찾아볼 수 있다.
역 합성에 의한
ssDNA
HDRT
제조
ssDNA 공여자는 문헌 [Leonetti et al. http://www.biorxiv.org/content/early/2017/08/21/178905)]에 기재된 바와 같이, RNA 중간체의 역전사에 이어, 생성된 RNA:DNA 하이브리드 생성물에서 RNA 가닥의 가수분해에 의해 합성하였다. 간략하게, 원하는 HDR 공여자를 먼저 T7 프로모터의 하류에 클로닝하고, T7-HDR 공여자 서열을 PCR에 의해 증폭시켰다. RNA는 HiScribe T7 RNA 폴리머라제 (뉴 잉글랜드 바이오랩스(New England Biolabs))를 사용하는 시험관내 전사에 의해 합성하고, TGIRT-III (인젝스(InGex))을 사용하여 역전사시켰다. 역전사 후, NaOH 및 EDTA를 각각 0.2 M 및 0.1 M에 첨가하고, RNA 가수분해를 95℃에서 10 min 동안 수행하였다. 반응물을 HCl로 켄칭하고, 최종 ssDNA 생성물을, 앰퓨어 XP(Ampure XP) 자기 비드 (베크만 쿨터(Beckman Coulter))를 사용하여 정제하고, 멸균 RNAse-무함유 H2O에서 용출시켰다. ssDNA 정질을 모세관 전기영동 (바이오애널라이저(Bioanalyzer), 애질런트(Agilent))에 의해 분석하였다.
1차 T 세포 전기천공
RNP 및 HDR 주형은 초기 T 세포 자극 후 2일 경과 시에 전기천공하였다. T 세포를 그의 배양 베쓸로부터 수거하고, 자석 위에 2분 동안 세포를 놓아둠으로써 자기 CD3/CD28 디나비드를 제거하였다. 전기천공 직전에, 비드가 제거된 세포를 90Xg에서 10분 동안 원심분리하고, 흡인하고, 백만개 세포당 20 μL 완충제로 론자(Lonza) 전기천공 완충제 P3에 재현탁시켰다. 최적의 편집을 위해, 펄스 코드 가 EH115인 론자 4D 96-웰 전기천공 시스템을 사용하여 웰당 백만개 T 세포를 전기천공하였다. 웰당 200,000개 내지 최대 2백만개 세포의 대체 세포 농도는 더 낮은 효율을 보였다. 대체 전기천공 완충제는 명시된 바와 같이 사용되었지만, 상이한 최적 펄스 설정 (OMEM 완충제의 경우, EO155)을 가졌다. 달리 명시되지 않는 한, 2.5 μL의 RNP (총 50 pmol)를 2 μg/μL에 2 μL의 HDR 주형 (총 4 μg HDR 주형)과 함께 전기천공하였다.
96-웰 실험을 위해, HDRT를 먼저 96-웰 폴리프로필렌 V-바닥 플레이트의 웰에 분취하였다. 이어서, RNP를 HDRT에 첨가하고, 적어도 30초 동안 RT에서 함께 인큐베이션하였다. 최종적으로, 전기천공 완충제에 재현탁된 세포를 첨가하고, HDRT 및 RNP로 피펫팅함으로써 간단히 혼합하고, 24 μL의 총 부피 (세포 + RNP + HDRT)을 96 웰 전기천공 큐벳 플레이트로 옮겼다. 전기천공 직후, 80 μL의 미리 가온된 배지 (시토카인 없음)를 각각의 웰에 첨가하고, 세포를 전기천공 큐벳에 잔류시키면서, 세포 배양 인큐베이터에서 37℃에서 15분 동안 휴지시켰다. 15분 후, 세포를 최종 배양 베쓸로 옮겼다.
내인성 T 세포 수용체의 단일
HDR
주형으로의 비-바이러스 대체
TCR-α 및 TCR-β 쇄 둘 다를 단일 멀티플렉스화된 라운드의 편집에서 동시에 녹인할 수 있다 (도 2). 이는 도 1a 및 도 1b의 표적화된 전략법과 유사하되, 단, 예외적으로, TCR-α 및 TCR-β 불변 로커스 둘 다에서 원하는 항원 특이적 TCR의 가변 영역만이 삽입된다. 이는 둘 다 삽입물의 총 크기를 (1개의 1.5 kbp 삽입물에서 2개의 500 bp 삽입물로) 축소시킨다는 이점을 갖고, 또한, 예를 들어, 잠재적으로 원하지 않는, 삽입된 항원 특이적 TCR-α 쇄와 내인성 TCR-β 쇄의 쌍형성을 막으면서, 원하는 항원 특이적 TCR의 쇄 둘 다를 발현하는 임의의 T 세포가 그의 앞서 재조합된 내인성 TCR-α 및 TCR-β 쇄는 녹아웃될 것이라는 것을 의미한다.
T 세포 수용체의
폴리클로날
라이브러리로의 내인성
TCR
대체
내인성 TCR을 임의의 원하는 신규 이종성 TCR 서열로 대체하는데 gRNA 및 상동성 아암은 동일한 것이기 때문에, 다양한 원하는 TCR을 함유하는 다중의 상이한 DNA 주형을 동시에 전기천공할 수 있다. 임의의 특이적 T 세포는 오직 다양한 원하는 TCR로부터 단일의 TCR만을 획득하겠지만, 다수의 TCR DNA 주형은 전기천공된 세포의 집단 전반에 걸쳐 통합될 것이며, 이로써, 원하는 서열의 합성 T 세포 레퍼토리를 생성하게 될 것이다 (도 3a).
앞서 공지된 TCR 서열로부터, 또는 관심 내인성 T 세포 집단에서 발견되는 천연 레퍼토리로부터 합성 T 세포 레퍼토리를 디자인하고, 생성할 수 있다 (도 3b). 일부 예는 (CD8+ 또는 CD4+ T 세포 이펙터의 신규 집단 내로 삽입되는) 종양 침윤 림프구에 의해 발현되는 TCR, (조절 T 세포의 집단 내로 삽입되는,) 자가면역 질환의 부위에서의 자가반응성 T 세포에 의해 발현되는 TCR, 또는 (CD8+ 또는 CD4+ T 세포 이펙터 내로 삽입된) 병원체 반응성 T 세포로부터의 TCR을 포함한다.
내인성 T 세포 수용체의 단일
HDR
주형으로의 비-바이러스 대체
T 세포 수용체의 게놈 로커스는 매우 복잡하며, 여기서 (TCR-α 쇄의 경우, V 및 J 대립유전자, 및 TCR-β 쇄의 경우, V, D 및 J 대립유전자로 명명되는) 매우 다양한 가변 대립유전자에서는 기능성 T 세포 수용체를 생성하기 위해 T 세포 발생 동안 체세포 유전자 재배열이 이루어지게 된다. TCR 레퍼토리의 다양성을 위해서는 중요하지만, (녹아웃 또는 녹인에 상관 없이) TCR 로커스에서의 표적화된 게놈 편집을 위해서는 도전과제가 되는 이들 재조합된 서열은 T 세포의 폴리클로날 집단 사이에 상이하다. 표적화 적용을 위해, TCR-α 및 TCR-β 쇄 둘 다, 비록 V-J 또는 V-D-J 세그먼트가 재배열되었다 하더라도, 단백질 C-말단의 불변 도메인은 모든 T 세포가 공유하고 있다. TCR-β 로커스는 도 1b에 제시된 바와 같이 표적화될 수 있는 2개의 불변 영역 (TRBC1 및 TRBC2)을 갖는다. 상기 불변 서열 (불변 엑손, TRAC 또는 TRBC 엑손 1, 엑손 2 등으로 표지)을 통해 게놈 표적화 시약의 단일 세트 (본 출원에서 CRISPR/Cas9 시스템, 즉, 단일 gRNA 서열)는 T 세포 그가 발현하는 TCR이 재배열되었다 하더라도, 모든 T 세포를 변형시키는데 사용될 수 있다.
상기 기재된 방법을 사용하여, 종양 항원에 특이적으로 결합하는 이종성 TCR을 코딩하는 DNA 주형을 제조하였고, 인간 T 세포에서 내인성 TCR을 대체하는데 사용하였다. 내인성 TCR을 대체하는데 사용된 상동성 지정 복구 주형 (PCR에 의해 제조된 dsDNA, 또는 본원에 기재된 다양한 방법에 의해 제조된 ssDNA)의 길이는, gRNA 커팅 부위에 플랭킹되는 게놈 서열에 상동성인 5' 및 3' 상동성 아암 (~300 bp)을 포함하여 ~2.1 kb이다 (도 1a). 이들 상동성 아암 사이에는 상동성 지정 복구에 의해 gRNA 커팅 부위에 삽입된 ~1.5 kb 서열이 존재한다. 상기 삽입된 서열은 멀티시스트론성 요소 (T2A 자기-절제 펩티드)로 시작하고, 이어서, 원하는 항원 특이적 T 세포 수용체 (본 실시예에서, NY-ESO-1 흑색종에 특이적인 TCR)의 TCR-β 쇄의 전장 서열이 이어진다. 제2 멀티시스트론성 요소 (P2A 자기 절제 펩티드)는 TCR-β 쇄 뒤로 이어지고, TCR-β 쇄를 원하는 항원 특이적 TCR-α 쇄의 가변 (재조합된 V 및 J 대립유전자) 서열로부터 분리시켰다. 오직 TCR-α 쇄로부터의 가변 영역 및 TRAC 엑손 1의 서열만이 gRNA 커팅 부위(의 5' 말단) 앞의 선행부로 삽입되었는데, 남은 TRAC 엑손은 함께 최종 mRNA 서열로 스플라이싱되었기 때문이었다. DNA 주형은 상기 기재된 바와 같이 RNP:DNA 주형 복합체의 일부로서 T 세포 내로 도입되었다.
성공적인 HDR이 이루어진 세포에서의 전사를 통해 TCR-β 및 TCR-α 둘 다를 코딩하는 폴리시스트론성 mRNA일 수득되었다. 본 표적화 전략법을 통해 3개의 펩티드 쇄를 수득하였다 - (1) 막횡단 패스를 갖지 않고 (따라서, 세포 표면 상에서 발현되지 않아야 하고), 소포체에서 분해되거나, 또는 전사 후 분비된 나머지 내인성 가변 영역 펩티드; (2) 전장의 원하는 항원-특이적 TCR-β 쇄; 및 (3) 전장의 원하는 항원-특이적 TCR-α 쇄. 결과는 내인성 TCR 프로모터의 제어 하에 원하는 항원 특이적 TCR의 쇄 둘 다를 발현한 T 세포였다. 쇄 둘 다는 T 세포에 의해 발현되었고, 이를 통해 NY-ESO-1 흑색종 신생항원을 특이적으로 인식한 이종성 TCR일 형성되었다.
도 4a에 제시된 바와 같이, 상기 기재된 구축물의 전기천공 후 4일째, 2명의 건강한 인간 혈액 공여자로부터의 CD4+ 및 CD8+ T 세포를 통합된 NY-ESO-1 특이적 TCR에 의해 인식되는 펩티드를 함유하는 형광 표지된 MHC-덱스트라머 (NYESO)로 염색하였다. 도 4b는 다른 건강한 인간 공여자에서의 유사한 결과를 보여주는 제2 실험이며, 이로써, 비-바이러스 내인성 TCR 대체의 강건성 및 재현성이 입증된다.
비록 두 불변 영역 (TRBC1 및 TRBC2)이 서로 고도로 상보적이기 때문에 β 로커스가 더 복잡하기는 하지만, TCR -α를 표적화하는 것과 유사한 전략법을 이용하여 TCR-β 로커스에서도 또한 TCR 대체를 달성하였다. HDR 주형은 TRBC1 및 TRBC2 둘 다에서 발견되는 서열을 표적화하는 gRNA를 이용하여 제1 TRBC1 엑손의 5' 말단에 신규 전장 TCR-α 및 신규 TCR-β의 VDJ 영역을 삽입하였다. TRBC1과 TRBC2 게놈 영역 사이의 서열 유사성에 기인하여, 상기 구축물의 3' 상동성 아암은 TRBC2 중 등가 영역에도 또한 거의 완벽한 상동성을 띤 반면, 5' 상동성 아암은 삽입 부위에 가장 가까운 150 bps 중 TRBC2 게놈 영역에 대하여 ~85%의 상동성을 가졌다. 따라서, 삽입은 가능하게는 TRBC1에서 지배적으로 이루어지지만, TRBC2에서도 또한 가능하거나, TRBC1과 TRBC2 사이에 개입 결실이 있을 수 있다. TRBC1 또는 TRBC2에서 특이적으로 커팅하는 gRNA가 또한 둘 다를 표적화하는 gRNA 대신 사용될 수 있다.
도 9a는 게이팅된 CD4+ 또는 CD8+ T 세포에서의 NY-ESO-1 특이적 TCR의 레트로바이러스 전달 또는 비-바이러스 TCR 대체 이후의 TCR 쌍형성오류 분석을 제시한다. TCR의 레트로바이러스 전달과 비교하였을 때, 비-바이러스 TCR 대체를 통해 TCR 쌍형성오류는 감소된다. TCR의, TRAC로 표적화된 신규 TCR-α VJ 도메인 및 TRBC1로 표적화된 신규 TRB-β VDJ 도메인을 이용한 멀티플렉스화된 대체가 또한 가능하였고, TCR 쌍형성오류를 추가로 감소시키기 위한 전략법을 제공할 수 있다 (도 9b-c).
덱스트라머를
이용한
TCR
대체 및
TCR
염색
2명의 건강한 인간 혈액 공여자로부터의 CD4+ 및 CD8+ T 세포를 상기 기재된 단일 구축물로 전기천공하였다. 전기천공 후 4일째, NYESO MHC-덱스트라머를 이용한 항원 특이적 염색 대비로 (모든 잠재적 인간 TCR에 결합하는 항체를 이용한) TCR 발현에 대한 염색을 수행하였다. 내인성 TCR의 상동성 지정 대체가 없는 대부분의 T 세포에서 (도 5), TRAC 엑손 1 gRNA에 의한 커팅 및 비-상동성 말단 연결에 의한 작은 indel의 도입에 기인하여 내인성 TCR은 녹아웃된다. 예상대로, 거의 모든 NYESO 양성 세포도 또한 TCR 발현에 대해 양성이다.
TCR
녹인 1차 인간 T 세포에 의한
시험관내
암 세포
사멸
시험관내 암 세포 사멸 검정법을 통해 TCR 녹인 세포의 기능적 표적 세포 사멸 능력을 입증하였다. 상기 기재된 바와 같이, 건강한 인간 공여자로부터의 CD3+ 1차 T 세포 중 내인성 TCR α 로커스 내로 1G4 (NYESO 특이적) TCR 서열을 삽입하였다. 전기천공 후 7일째, 세포를 형광성 NYESO 펩티드-MHC 덱스트라머로 염색하고, 형광성 활성화 세포 분류에 의해 NYESO+ 세포를 분류하여 순수한 집단을 수득하였다. 상기 집단을 추가로 5일 동안 표준 T 세포 배양 조건 (배지 및 IL-2)에서 추가로 배양하였다. 전기천공 후 12일째, 그의 내인성 TCR이 1G4 TCR에 의해 대체된 것인 분류된 T 세포를, 그의 MHC 상에 NYESO 항원을 제시하는 암 세포주 (흑색종으로부터 유래되고, NYESO 항원 뿐만 아니라, 1G4 TCR에 의해 인식되는 MHC 대립유전자인 MHC-A2를 내재적으로 발현하는 A375 세포)와 함께 공동 배양하였다. 매 12시간마다, 정량적 형광 영상화에 의해 암 세포 개수를 계수하였다 (A375 세포는 적색 형광성 단백질을 발현하는 바, 이를 통해 A375 세포를 T 세포로부터 별개로 특이적으로 계수할 수 있음). 인큐사이트(Incucyte) 자동 형광 현미경을 이용하여 형광 계수를 자동화하였다. 배양물을 3,000개의 암 세포 및 1G4+ T 세포의 명시된 비로 시딩하였다 (도 4a 참조). 2명의 건강한 인간 공여자로부터 편집된 T 세포에서, 표적 암 세포의 용량 및 시간에 의존하는 강건한 사멸이 관찰되었고, 이는 1G4 TCR 녹인 T 세포의 기능성을 시사하는 것이다. 주어진 웰 중 살아있는 암 세포의 개수를, T 세포가 존재하지 않는 대조군 웰 중의 살아있는 암 세포의 개수로 나눔으로써 암 세포의 퍼센트 사멸률을 측정하였다. T 세포 대 암 세포의 높은 비 (~10:1)의 T 세포 대 암 세포는 거의 모든 암 세포의 신속한 (<24시간) 사멸을 보였지만, 극도로 낮은 비 (~0.1:1)의 T 세포 대 암 세포도 배양 시간이 추가로 경과됨에 따라 강건한 사멸을 보였다 (도 6a 참조).
단일 시점에서의 1G4 TCR 녹인 T 세포에 의한 시험관내 암 사멸을 입증하였다 (도 6b 참조). 상기 기재된 세포 사멸 검정법에서 단일 시점으로부터 요약 데이터를 수집하였다 (공동-인큐베이션 후 36시간째). NYESO 덱스트라머+ (1G4+) T 세포를 상기 기재된 바와 같이 분류하여 100% 1G4 양성 집단을 생성하였고, 이어서, 동일 공여자로부터의 NYESO 덱스트라머- (1G4-) T 세포로 희석하여 명시된 백분율의 NYESO+ 염색 T 세포 (10%, 1%, 또는 0%)를 수득하였다. 이어서, 상기 기재된 바와 같이, 시험관내 암 사멸 검정법에서 상기 집단을 각각 암 세포와 함께 8개 T 세포 대 1개 암 세포의 비로 공동-배양하였다 (100%, 10%, 1%, 및 0% NYESO+ T 세포 집단에 대해 각각 8:1, 0.8:1, 0.08:1 및 0:1 비의 1G4+ T 세포:암 세포를 수득). 암 세포 사멸에 대한 양성 대조군으로서, T 세포의 게놈 내로 1G4 TCR 발현 카세트를 무작위로 통합하는 렌티바이러스를 추가의 건강한 공여자로부터의 세포에 형질도입하였다 (이 경우, 1G4 TCR이 내인성 TCR 로커스를 대체하는 1G4 TCR 녹인 T 세포와 달리, TCR은 무작위로 통합 및 발현되고, 이로써, 내인성 TCR 프로모터로부터 발현이 이루어지고, 동시에 내인성 TCR은 녹아웃시킨다는 점에 주의함). 상기 추가의 공여자로부터의 렌티바이러스에 의해 형질도입된 T 세포를 유사하게 분류하여 100% 1G4+ 집단을 수득하였고, 유사하게 8;1 T 세포 대 암 세포 비로 표적 A375 암 세포주와 함께 공동-배양하였다.
생체내
마우스 고형 종양 모델
모든 마우스 실험은 UCSF 동물 실험 윤리 위원회(UCSF Institutional Animal Care and Use Committee) 프로토콜 하에 완료하였다. 모든 실험을 위해 8 내지 12주령된 NOD/SCID/IL-2Rγ-널 (NSG) 수컷 마우스 (잭슨 래보러토리(Jackson Laboratory))를 사용하였다. 1x106개 A375 인간 흑색종 세포 (ATCC CRL-1619)를 면도된 우측 옆구리 내로 피하 주사하여 마우스에 종양을 시딩하였다. 종양 시딩 후 7일째, 종양 크기를 사정하고, 종양 부피가 15-30 ㎣인 마우스를 무작위로 실험 처리군 및 대조 처리군으로 배정하였다. 명시된 개수의 T 세포를 100 μl 무혈청 RPMI 중에 재현탁시키고, 안와후로 주사하였다. 종양 사이징 실험을 위해, 전자 캘리퍼스를 이용하여 종양의 길이 및 너비를 측정하였고, v = 1/6 * π * 길이 * 너비 * (길이 + 너비)/2로서 부피를 계산하였다. 사이징 측정 동안 연구원은 실험 처리군에 대해 맹검화되었다. 벌크 편집된 T 세포 집단 (5x106) 또는 분류된 NY-ESO-1 TCR+ 집단 (3x106)을 도면 및 범례에 명시된 바와 같이 전달하였다. 벌크 편집된 T 세포 전달의 경우, 렌티바이러스에 의해 편집된 세포는 일반적으로 더 높은 비로 NY-ESO-1 양성 세포를 가졌고, 이에, 총 T 세포 NY-ESO-1+의 백분율이 비-바이러스에 의해 편집된 T 세포의 벌크 집단의 백분율과 같도록 (~10% NY-ESO-1+) 정규화시키기 위해 모의 감염된 세포를 첨가하였다. 분류된 T 세포 전달의 경우, 전기천공 후 8일째 NY-ESO-1+ T 세포를 FACS 분류하고, 추가로 2일 동안 확장시키고, 냉동시켰다 (밤뱅커 냉동 배지, 불독 바이오). 이어서, 비-바이러스에 의해 또는 렌티바이러스에 의해 변형된 인간 T 세포를 해동시키고, 입양 전달 전 밤새도록 배지 중에서 휴지시켰다. 입양 전달된 T 세포의 유세포 분석법에 의한 분석을 위해, 70 ㎛ 필터를 통해 종양을 기계적으로 해리시켜 종양 및 비장으로부터의 단일 세포 현탁액을 제조하였다. 모든 실험 동물은, 어느 차원으로든 종양 크기 한계는 2.0 cm인 것을 포함하는, 승인받은 IACUC 프로토콜 (UCSF)에 따른 관련 윤리 규정에 준하여 수행하였다.
비-바이러
스
TCR
대체가 이루어진 T 세포의
생체내
기능성
인간 항원 특이적 종양 이종이식편 모델을 사용하여 (도 7a) 비-바이러스 TCR 대체가 이루어진 T 세포의 생체내 기능성을 사정하였다. 면도된 옆구리에 피하로 1x106개 A375 세포 (인간 흑색종 세포주; NY-ESO-1 항원+ 및 HLA-A*0201+)를 8 내지 12주령된 NSG 마우스에 시딩하였다. NY-ESO-1 항원 특이적 TCR을 발현하도록 편집된 1차 인간 T 세포를 (렌티바이러스 형질도입 또는 비-바이러스 TCR 대체를 통해) 생성하고, 형질도입 또는 전기천공 후 10일 동안 확장시키고, 냉동시켰다. 벌크 편집된 집단을 사용하거나 (도 7b-c), NY-ESO-1 TCR+ 분류된 집단 (도 7d-f)을 사용하였다. 종양 시딩 후 7일째, T 세포를 해동시키고, 안와후로 주사하 입양 전달하였다. 도 7b에 제시된 바와 같이, 5x106개 벌크 비-바이러스에 의해 표적화된 T 세포 전달 후 2일째 (~10% TCR+ NYESO-1+ (적색), ~10% TCR+ NYESO-1- (오렌지색), 및 ~80% TCR- NYESO-1- (녹색), 도 7b 참조), NY-ESO-1+ 비-바이러스에 의해 편집된 T 세포는 비장 대비 종양에 우선적으로 축적되었다. 4명의 인간 T 세포 공여자 각각에 대하여 마우스 n=5. 5x106개 벌크 비-바이러스에 의해 표적화된 CFSE 표지된 T 세포 전달 후 10일째, NYESO-1 TCR+ 세포는 TCR- 또는 TCR+NYESO-1- T 세포보다 더욱 큰 증식을 보였고, 비장에서보다 종양에서 더욱 큰 증식 (CFSE 낮음)을 보였다 (도 7c). 전달 후 10일째, 종양에서 TCR- 및 TCR+NYESO- T 세포를 찾기 어려웠다 (도 7d). 도 7d는 도 8f에 요약된 데이터에 대한 종축 방향 종양 부피 트랙을 제시한다. 렌티바이러스 형질도입 또는 비-바이러스 TCR 대체에 의해 생성된 3x106개 분류된 NY-ESO-1 TCR+ T 세포를 종양 시딩 후 7일째 전달하고, 종양 시딩 후 24일째까지 비히클 단독 주사인 것과 비교하였다. 렌티바이러스 전달 (상단) 및 비-바이러스 TCR 대체 (하단)와의 비교로 비히클 대조군 데이터에 대한 동일한 데이터가 각 공여자에 대하여 제시되어 있다는 것에 주의한다. 본 실험에서 (도 7e-f), T 세포 전달 후 17일째, 비-바이러스에 의해 TCR 대체된 세포는 더욱 큰 NY-ESO-1 TCR 발현 및 고갈 마커의 더 낮은 발현을 보이는 것으로 나타났다. 렌티바이러스에 의해 형질도입된 세포 및 비-바이러스 TCR 대체된 세포 전달 둘 다, 24일째 종양 부담의 유의적인 감소를 보였다. 본 실험 모델에서, 비-바이러스 TCR 대체는 렌티바이러스 형질도입과 비교하였을 때, 추가 감소를 보였다 (도 8f). 공여자 1명당 5마리의 마우스 (도 7b, 7c) 또는 7마리의 마우스 (도 7d-f)에서의 n=4 (도 7b), n=2 (도 7d-f), 또는 n=1 (도 7c) 독립된 건강한 공여자, 여기서 평균 (도 7b, 7e, 7f) 및 표준 편차 (도 7b).
종양 항원 특이적 기능
표적화된 인간 T 세포의 종양 항원-특이적 기능을 또한 사정하였다. 표적화된 T 세포를 2개의 상이한 NY-ESO-1+ 흑색종 세포주, M257 및 M407과 함께 공동-배양하였을 때, 변형된 T 세포는 강건하게 및 특이적으로 IFN-γ 및 TNF-α를 생산하였고, T 세포 탈과립화 (CD107a 표면 발현에 의해 측정)를 유도하였다 (도 8a). 시토카인 생산 및 탈과립화는 동족 NY-ESO-1 펩티드를 제시하는데 필요한 적절한 HLA-A*0201 클래스 I MHC 대립유전자를 발현하는 세포주에 NY-ESO-1 TCR T 세포가 노출되었을 때에만 발생하였다. CD8+ 및 CD4+ T 세포 반응 둘 다가 건강한 공여자 사이에는 일치하였고, NY-ESO-1 TCR이 감마 레트로바이러스에 의해 형질도입되었고, 바이러스 프로모터를 사용하여 이종 발현된 것으로, 동일한 건강한 공여자로부터의 T 세포의 반응과 유사하였다 (도 8a 및 도 9d). NY-ESO-1 TCR 녹인 T 세포는 시험관내에서 양성 대조군인 레트로바이러스에 의해 형질도입된 T 세포과 유사한 속도로 표적 M257-HLA-A*0201 암 세포를 신속하게 사멸시켰다 (도 8b). 사멸은 공여자 사이에 일관되게, NY-ESO-1 항원 및 HLA-A*0201 대립유전자를 발현하는 표적 세포에 대하여 선택적이었고, 올바른 gRNA 및 HDR 주형 둘 다를 이용하여 변형된 T 세포에 의존하였다 (도 9h-k).
마지막으로, 비-바이러스 게놈 표적화를 이용하여 NY-ESO-1 TCR 세포를 규모에 맞게 생성할 수 있고, 이들 세포는 생체내 항종양 기능을 갖는다는 것을 확인하였다 (도 8c 및 도 7a). 유사한 크기의 AAV 주형 사용시보다 비-바이러스 표적화 사용 시에 녹인 효율이 더 낮았다는 점을 고려하면, 입양 세포 요법을 위해 NY-ESO-1 양성 세포의 개수가 충분한지 여부는 보장되었다. 6명의 건강한 공여자로부터의 1억개 T 세포를 통해 10일 동안의 확장 후, 공여자 1명당 평균 3억 8,500개 NY-ESO-1 TCR T 세포를 얻었다 (도 8d). NY-ESO-1 TCR 녹인 T 세포는 양성 대조군인 렌티바이러스에 의해 형질도입된 T 세포와 유사하게, 비장보다 종양으로 우선적으로 국재화되고, 종양에 지속되고, 종양에서 증식되었다 (도 8e 및 도 7b-f). 분류된 NY-ESO-1 TCR T 세포의 입양 전달은 또한 처리된 동물에서 종양 부담을 감소시켰다 (도 8f).
Claims (74)
- 인간 T 세포의 게놈을 편집하는 방법으로서, 인간 T 세포에서 T 세포 수용체 (TCR)-서브유닛 불변 유전자의 엑손 1 내의 표적 영역 내로,
N-말단에서 C-말단으로,
(i) 제1 자기-절단 펩티드 서열;
(ii) TCR 서브유닛 쇄가 TCR 서브유닛의 가변 영역 및 불변 영역을 포함하는 것인 제1 이종성 TCR 서브유닛 쇄;
(iii) 제2 자기-절단 펩티드 서열;
(iv) 제2 이종성 TCR 서브유닛 쇄의 가변 영역; 및
(v) 내인성 TCR 서브유닛의 N-말단 부분
을 코딩하는 핵산 서열
을 삽입하는 것을 포함하며,
여기서 내인성 TCR 서브유닛이 TCR-알파 (TCR-α) 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-베타 (TCR-β) 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이며, 여기서 내인성 TCR 서브유닛이 TCR-β 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-β 서브유닛 쇄인
방법. - 제1항에 있어서, N-말단에서 C-말단으로,
(i) 제1 자기-절단 펩티드 서열;
(ii) 이종성 TCR-β 쇄;
(iii) 제2 자기-절단 펩티드 서열;
(iv) 이종성 TCR-α 쇄의 가변 영역; 및
(v) 내인성 TCR-α 서브유닛의 N-말단 부분
을 코딩하는 핵산 서열이 인간 T 세포에서 TCR-알파 서브유닛 불변 유전자 (TRAC)의 엑손 1 내로 삽입되는 것인 방법. - 제1항에 있어서, N-말단에서 C-말단으로,
(i) 제1 자기-절단 펩티드 서열;
(ii) 이종성 TCR-α 쇄;
(iii) 제2 자기-절단 펩티드 서열;
(iv) 이종성 TCR-β 쇄의 가변 영역; 및
(v) 내인성 TCR-β 서브유닛의 N-말단 부분
을 코딩하는 핵산 서열이 인간 T 세포에서 TCR-베타 서브유닛 불변 유전자 (TRBC)의 엑손 1 내로 삽입되는 것인 방법. - 제1항 내지 제3항 중 어느 한 항에 있어서, 핵산 서열이 이중 가닥 또는 단일 가닥 핵산 서열이고, 핵산 서열이 핵산 서열을 T 세포 내로 도입함으로써 삽입되는 것인 방법.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 핵산이 핵산을 포함하는 바이러스 벡터를 T 세포 내로 도입함으로써 삽입되는 것인 방법.
- 제1항, 제2항, 제4항 및 제5항 중 어느 한 항에 있어서, 핵산이, T 세포 내로,
(a) TRAC 유전자의 엑손 1 내의 표적 영역을 절단하여 T 세포의 게놈 중에 삽입 부위를 생성하는 표적화된 뉴클레아제; 및
(b) 핵산 서열로서, 상동성 지정 복구 (HDR)에 의해 삽입 부위 내로 삽입되는 핵산 서열
을 도입함으로써 T 세포 내로 삽입되는 것인 방법. - 제1항, 제3항, 제4항 및 제5항 중 어느 한 항에 있어서, 핵산이, T 세포 내로,
(a) TRBC 유전자의 엑손 1 내의 표적 영역을 절단하여 T 세포의 게놈 중에 삽입 부위를 생성하는 표적화된 뉴클레아제; 및
(b) 핵산 서열로서, 상동성 지정 복구 (HDR)에 의해 삽입 부위 내로 삽입되는 핵산 서열
을 도입함으로써 T 세포 내로 삽입되는 것인 방법. - 제1항 내지 제7항 중 어느 한 항에 있어서, 핵산 서열의 5' 말단 및 3' 말단이, 표적 영역에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함하는 것인 방법.
- 제8항에 있어서, 핵산 서열의 5' 말단 및 3' 말단이, 삽입 부위에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함하는 것인 방법.
- 제6항 내지 제9항 중 어느 한 항에 있어서, 표적화된 뉴클레아제가 삽입 부위에 이중 가닥 파단을 도입하는 것인 방법.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 핵산 서열이 단일 가닥 DNA 주형인 방법.
- 제1항 내지 제11항 중 어느 한 항에 있어서, 핵산 서열이 선형 DNA 주형인 방법.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 제1 자기-절단 펩티드 및 제2 자기-절단 펩티드가 동일하거나 또는 상이한 바이러스 2A 펩티드인 방법.
- 제6항 내지 제13항 중 어느 한 항에 있어서, 표적화된 뉴클레아제가 RNA-가이드된 뉴클레아제 도메인, 전사 활성인자-유사 이펙터 뉴클레아제 (TALEN), 아연 핑거 뉴클레아제 (ZFN) 및 메가TAL로 이루어진 군으로부터 선택되는 것인 방법.
- 제14항에 있어서, RNA-가이드된 뉴클레아제가 Cpf1 뉴클레아제 또는 Cas9 뉴클레아제이고, 방법이 세포 내로 TRAC의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함하는 것인 방법.
- 제14항에 있어서, RNA-가이드된 뉴클레아제가 Cpf1 뉴클레아제 또는 Cas9 뉴클레아제이고, 방법이 세포 내로 TRBC의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 가이드 RNA를 도입하는 것을 추가로 포함하는 것인 방법.
- 제15항 또는 제16항에 있어서, Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 가이드 RNA 및 핵산이 세포 내로 리보핵단백질 복합체 (RNP)-DNA 주형 복합체로서 도입되며, 여기서 RNP-DNA 주형 복합체는
(i) Cpf1 뉴클레아제 또는 Cas9 뉴클레아제 및 가이드 RNA를 포함하는 RNP; 및
(ii) DNA 주형
을 포함하는 것인 방법. - 제17항에 있어서, 복합체 중 RNP 대 DNA 주형의 몰비가 약 3:1 내지 약 100:1인 방법.
- 제17항 또는 제18항에 있어서, RNP-DNA 주형 복합체가 약 20℃ 내지 25℃의 온도에서 약 10 내지 약 30분 동안 RNP를 DNA 주형과 함께 인큐베이션함으로써 형성되는 것인 방법.
- 제17항 내지 제19항 중 어느 한 항에 있어서, RNP-DNA 주형 복합체 및 세포가 RNP-DNA 주형 복합체를 세포 내로 도입하기 전에 혼합되는 것인 방법.
- 제17항 내지 제20항 중 어느 한 항에 있어서, RNP-DNA 주형 복합체가 적어도 2개의 구조적으로 상이한 RNP 복합체를 포함하는 것인 방법.
- 제21항에 있어서, 적어도 2개의 구조적으로 상이한 RNP 복합체가 구조적으로 상이한 가이드 RNA를 함유하는 것인 방법.
- 제22항에 있어서, 구조적으로 상이한 RNP 복합체가 각각 Cas9 닉카제를 포함하고, 구조적으로 상이한 가이드 RNA가 표적 영역의 반대 가닥에 하이브리드화하는 것인 방법.
- 제4항 내지 제23항 중 어느 한 항에 있어서, 도입이 전기천공을 포함하는 것인 방법.
- 제4항 내지 제24항 중 어느 한 항에 있어서, 핵산 또는 RNP:DNA 주형 복합체가 약 1 × 105 내지 약 2 × 106개 T 세포의 집단 내로 도입되는 것인 방법.
- 제25항에 있어서, 적어도 2개의 구조적으로 상이한 DNA 주형이 세포 내로 도입되는 것인 방법.
- 제26항에 있어서, 적어도 2개의 구조적으로 상이한 DNA 주형이 각각 항원 특이적 T 세포 수용체의 이종성 TCR-β 쇄의 가변 영역, 및 항원 특이적 T 세포 수용체의 이종성 TCR-α 쇄의 가변 영역의 고유한 조합을 코딩하는 것인 방법.
- 제1항 내지 제27항 중 어느 한 항에 있어서, T 세포가 조절 T 세포, 이펙터 T 세포, 또는 나이브 T 세포인 방법.
- 제28항에 있어서, T 세포가 이펙터 T 세포이며, 여기서 이펙터 T 세포는 CD8+ T 세포 또는 CD4+ 세포인 방법.
- 제29항에 있어서, 이펙터 T 세포가 CD4+CD8+ T 세포인 방법.
- 제1항 내지 제30항 중 어느 한 항에 있어서, T 세포를 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 발현을 허용하는 조건 하에서 배양하여 항원-특이적 T 세포 수용체를 형성하는 것을 추가로 포함하는 방법.
- 제31항에 있어서, 변형된 T 세포를 변형된 세포의 집단을 확장시키는데 효과적인 조건 하에서 배양하는 것을 추가로 포함하는 방법.
- 제31항 또는 제32항에 있어서, 항원-특이적 T 세포 수용체를 발현하는 T 세포를 정제하는 것을 추가로 포함하는 방법.
- 제1항 내지 제33항 중 어느 한 항의 방법에 의해 제조된 변형된 T 세포.
- 변형된 T 세포로서,
N-말단에서 C-말단으로,
(i) 제1 자기-절단 펩티드 서열;
(ii) 제1 이종성 TCR 서브유닛 쇄,
(iii) 제2 자기-절단 펩티드 서열;
(iv) 제2 이종성 TCR 서브유닛 쇄의 가변 영역; 및
(v) 내인성 TCR 서브유닛의 N-말단 부분
을 코딩하는 핵산 서열을 포함하며,
여기서 내인성 TCR 서브유닛이 TCR-알파 (TCR-α) 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-베타 (TCR-β) 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이며, 여기서 내인성 TCR 서브유닛이 TCR-β 서브유닛인 경우, 제1 이종성 TCR 서브유닛 쇄는 이종성 TCR-α 서브유닛 쇄이고, 제2 이종성 TCR 서브유닛 쇄는 이종성 TCR-β 서브유닛 쇄인
변형된 T 세포. - 제35항에 있어서, 핵산 서열이, N-말단에서 C-말단으로,
(i) 제1 자기-절단 펩티드 서열;
(ii) 이종성 T 세포 수용체 (TCR)-β 쇄;
(iii) 제2 자기-절단 펩티드 서열;
(iv) 이종성 TCR-α 쇄의 가변 영역; 및
(v) 내인성 TCR 알파 서브유닛의 N-말단 부분
을 코딩하고,
핵산 서열이 TRAC 유전자의 엑손 1 내로 통합되는 것인
변형된 T 세포. - 제35항에 있어서, 핵산 서열이, N-말단에서 C-말단으로,
(i) 제1 자기-절단 펩티드 서열;
(ii) 이종성 T 세포 수용체 (TCR)-α 쇄;
(iii) 제2 자기-절단 펩티드 서열;
(iv) 내인성 TCR-β 서브유닛의 N-말단 부분
을 코딩하고,
핵산 서열이 TRBC1 또는 TRBC2 유전자의 엑손 1 내로 통합되는 것인
변형된 T 세포. - 변형된 T 세포로서,
N-말단에서 C-말단으로,
(i) 제1 자기-절단 펩티드 서열;
(ii) 이종성 T 세포 수용체 (TCR)-α 쇄의 가변 영역;
(iii) 제2 자기-절단 펩티드 서열;
(iv) 이종성 TCR-β 쇄의 가변 영역; 및
(v) 내인성 TCR 베타 서브유닛의 N-말단 부분
을 코딩하는 핵산 서열을 포함하며,
여기서 핵산 서열은 TRBC 유전자의 엑손 1 내로 통합되는 것인
변형된 T 세포. - T 세포의 게놈을 편집하는 방법으로서,
(a) 인간 T 세포에서 TCR 알파 서브유닛 불변 유전자 (TRAC)의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로,
(i) 자기-절단 펩티드 서열;
(ii) 항원 특이적 T 세포 수용체의 이종성 TCR-α 쇄; 및
(iii) 내인성 TCR 알파 서브유닛의 엑손 1의 N-말단 부분
을 코딩하는 제1 핵산 서열
을 삽입하는 것; 및
(b) 인간 T 세포에서 TCR 베타 서브유닛 불변 유전자 (TRBC)의 엑손 1 내의 표적 영역 내로, N-말단에서 C-말단으로,
(i) 제2 자기-절단 펩티드 서열;
(ii) 항원 특이적 T 세포 수용체의 이종성 TCR-β 쇄; 및
(iii) 내인성 TCR 베타 서브유닛의 엑손 1의 N-말단 부분
을 코딩하는 핵산 서열
을 삽입하는 것
을 포함하는 방법. - 제39항에 있어서, 제1 및/또는 제2 핵산 서열이 이중 가닥 또는 단일 가닥 핵산이고, 제1 및/또는 제2 핵산이 제1 및/또는 제2 핵산을 T 세포 내로 도입함으로써 삽입되는 것인 방법.
- 제40항에 있어서, 제1 및/또는 제2 핵산 서열이 제1 및/또는 제2 핵산을 포함하는 바이러스 벡터를 T 세포 내로 도입함으로써 삽입되는 것인 방법.
- 제40항 또는 제41항에 있어서, 제1 및 제2 핵산이, T 세포 내로,
(a) TRAC 유전자의 엑손 1에 제1 삽입 부위, 및 TRBC 유전자의 엑손 1에 제2 삽입 부위를 생성하는 하나 이상의 표적화된 뉴클레아제;
(b) 제1 핵산 서열; 및
(c) 제2 핵산 서열
을 도입함으로써 T 세포 내로 삽입되는 것인 방법. - 제39항 내지 제42항 중 어느 한 항에 있어서, 제1 핵산 서열의 5' 및 3' 말단이, TRAC의 엑손 1 내의 제1 표적 영역에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함하는 것인 방법.
- 제43항에 있어서, 제2 DNA 주형의 5' 및 3' 말단이, TRBC의 엑손 1 내의 제2 표적 영역에 플랭킹되는 게놈 서열과 상동성인 뉴클레오티드 서열을 포함하는 것인 방법.
- 제42항 내지 제44항 중 어느 한 항에 있어서, 하나 이상의 표적화된 뉴클레아제가 제1 및 제2 삽입 부위에 이중 가닥 파단을 도입하는 것인 방법.
- 제39항 내지 제45항 중 어느 한 항에 있어서, 제1 및/또는 제2 핵산 서열이 단일 가닥 DNA 주형인 방법.
- 제39항 내지 제46항 중 어느 한 항에 있어서, 제1 및/또는 제2 핵산이 선형 DNA 주형인 방법.
- 제39항 내지 제47항 중 어느 한 항에 있어서, 제1 자기-절단 펩티드 및 제2 자기-절단 펩티드가 동일하거나 또는 상이한 바이러스 2A 펩티드인 방법.
- 제42항 내지 제48항 중 어느 한 항에 있어서, 하나 이상의 표적화된 뉴클레아제가 RNA-가이드된 뉴클레아제 도메인, 전사 활성인자-유사 이펙터 뉴클레아제 (TALEN), 아연 핑거 뉴클레아제 (ZFN) 또는 메가TAL로 이루어진 군으로부터 선택되는 것인 방법.
- 제49항에 있어서, RNA-가이드된 뉴클레아제가 Cpf1 뉴클레아제 또는 Cas9 뉴클레아제이고, 방법이 세포 내로 TRAC의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 제1 가이드 RNA, 및 TRBC의 엑손 1 내의 표적 영역에 특이적으로 하이브리드화하는 제2 가이드 RNA를 도입하는 것을 추가로 포함하는 것인 방법.
- 제50항에 있어서, Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 제1 가이드 RNA 및 핵산 서열이 리보핵단백질 복합체 (RNP)-DNA 주형 복합체로서 세포 내로 도입되며, 여기서 RNP-DNA 주형 복합체는
(i) Cas9 뉴클레아제 또는 Cpf1 뉴클레아제, 및 제1 가이드 RNA를 포함하는 RNP; 및
(ii) 제1 DNA 주형
을 포함하는 것인 방법. - 제50항에 있어서, Cpf1 뉴클레아제 또는 Cas9 뉴클레아제, 제2 가이드 RNA 및 제2 핵산 서열이 RNP-DNA 주형 복합체로서 세포 내로 도입되며, 여기서 RNP-DNA 주형 복합체는
(i) Cpf1 뉴클레아제 또는 Cas9 뉴클레아제 및 제2 가이드 RNA를 포함하는 RNP; 및
(ii) 제2 DNA 주형
을 포함하는 것인 방법. - 제51항 또는 제52항에 있어서, 복합체 중 RNP 대 DNA 주형의 몰비가 약 3:1 내지 약 100:1인 방법.
- 제51항 내지 제53항 중 어느 한 항에 있어서, RNP-DNA 주형 복합체가 약 20℃ 내지 약 25℃의 온도에서 약 10 내지 약 30분 동안 RNP를 DNA 주형과 함께 인큐베이션함으로써 형성되는 것인 방법.
- 제51항 내지 제54항 중 어느 한 항에 있어서, RNP-DNA 주형 복합체가 적어도 2개의 구조적으로 상이한 RNP 복합체를 포함하는 것인 방법.
- 제55항에 있어서, 구조적으로 상이한 RNP 복합체가 각각 Cas9 닉카제를 포함하고, 구조적으로 상이한 가이드 RNA가 표적 영역의 반대 가닥에 하이브리드화하는 것인 방법.
- 제39항 내지 제56항 중 어느 한 항에 있어서, 도입이 전기천공을 포함하는 것인 방법.
- 제39항 내지 제57항 중 어느 한 항에 있어서, 핵산 서열(들) 또는 RNP:DNA 주형 복합체(들)가 약 1 × 105 내지 약 2 × 106개 T 세포 내로 도입되는 것인 방법.
- 제58항에 있어서, 적어도 2개의 구조적으로 상이한 제1 DNA 주형이 세포 내로 도입되는 것인 방법.
- 제59항에 있어서, 적어도 2개의 구조적으로 상이한 제1 DNA 주형이 항원 특이적 T 세포 수용체의 TCR-α 쇄의 상이한 가변 영역을 포함하는 것인 방법.
- 제60항에 있어서, 적어도 2개의 구조적으로 상이한 제2 DNA 주형이 세포 내로 도입되는 것인 방법.
- 제61항에 있어서, 적어도 2개의 구조적으로 상이한 제2 DNA 주형이 항원 특이적 T 세포 수용체의 TCR-β 쇄의 상이한 가변 영역을 포함하는 것인 방법.
- 제39항 내지 제62항 중 어느 한 항에 있어서, T 세포가 조절 T 세포, 이펙터 T 세포, 또는 나이브 T 세포인 방법.
- 제63항에 있어서, T 세포가 이펙터 T 세포이며, 여기서 이펙터 T 세포는 CD8+ T 세포 또는 CD4+ 세포인 방법.
- 제64항에 있어서, 이펙터 T 세포가 CD4+CD8+ T 세포인 방법.
- 제39항 내지 제65항 중 어느 한 항에 있어서, T 세포를 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 발현을 허용하는 조건 하에서 배양하여 항원-특이적 T 세포 수용체를 형성하는 것을 추가로 포함하는 방법.
- 제66항에 있어서, T 세포를 이종성 TCR-β 쇄 및 이종성 TCR-α 쇄의 발현을 허용하는 조건 하에서 배양하여 항원-특이적 T 세포 수용체를 형성하는 것을 추가로 포함하는 방법.
- 제67에 있어서, 변형된 T 세포를 변형된 세포의 집단을 확장시키는데 효과적인 조건 하에서 배양하는 것을 추가로 포함하는 방법.
- 제67항 또는 제68항에 있어서, 항원-특이적 T 세포 수용체를 발현하는 T 세포를 정제하는 것을 추가로 포함하는 방법.
- 제39항 내지 제69항 중 어느 한 항의 방법에 의해 제조된 변형된 T 세포.
- 변형된 T 세포로서,
a) N-말단에서 C-말단으로,
(i) 제1 자기-절단 서열;
(ii) 이종성 TCR-α 쇄의 가변 영역; 및
(iii) 내인성 TCR-α 쇄의 N-말단 부분
을 코딩하는 제1 핵산 서열; 및
b) N-말단에서 C-말단으로,
(i) 제1 자기-절단 서열;
(ii) 이종성 TCR-β 쇄의 가변 영역; 및
(iii) 내인성 TCR-β 쇄의 N-말단 부분
을 코딩하는 제2 핵산 서열
을 포함하며,
여기서 제1 핵산 서열은 TRAC 유전자의 엑손 1 내로 통합되고, 제2 핵산 서열은 TRBC 유전자의 엑손 1 내로 통합되는 것인
변형된 T 세포. - 인간 대상체에서 암을 치료하는 방법으로서,
a) 제1항 내지 제33항 및 제39항 내지 제69항 중 어느 한 항의 방법을 사용하여 항원-특이적 T 세포 수용체를 발현하도록 인간 대상체의 T 세포를 변형시키는 단계로서, 여기서 T 세포 수용체는 대상체에서 종양-특이적 항원을 인식하는 것인 단계를 포함하는 방법. - 제72항에 있어서, 대상체의 T 세포를 생체내에서 변형시키는 것인 방법.
- 제72항에 있어서, 방법이
a) 대상체로부터 T 세포를 수득하는 단계;
b) 제1항 내지 제33항 및 제39항 내지 제69항 중 어느 한 항의 방법을 사용하여 항원-특이적 T 세포 수용체를 발현하도록 T 세포를 변형시키는 단계로서, 여기서 T 세포 수용체는 대상체에서 종양-특이적 항원을 인식하는 것인 단계; 및
c) 변형된 T 세포를 대상체에게 투여하는 단계
를 포함하는 것인 방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020237005926A KR20230034416A (ko) | 2017-10-27 | 2018-10-29 | 내인성 t 세포 수용체의 표적화된 대체 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762578153P | 2017-10-27 | 2017-10-27 | |
| US62/578,153 | 2017-10-27 | ||
| PCT/US2018/058026 WO2019084552A1 (en) | 2017-10-27 | 2018-10-29 | TARGETED REPLACEMENT OF ENDOGENIC T CELL RECEPTORS |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237005926A Division KR20230034416A (ko) | 2017-10-27 | 2018-10-29 | 내인성 t 세포 수용체의 표적화된 대체 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20200088348A true KR20200088348A (ko) | 2020-07-22 |
| KR102503130B1 KR102503130B1 (ko) | 2023-02-24 |
Family
ID=66247037
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237005926A KR20230034416A (ko) | 2017-10-27 | 2018-10-29 | 내인성 t 세포 수용체의 표적화된 대체 |
| KR1020207015078A KR102503130B1 (ko) | 2017-10-27 | 2018-10-29 | 내인성 t 세포 수용체의 표적화된 대체 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020237005926A KR20230034416A (ko) | 2017-10-27 | 2018-10-29 | 내인성 t 세포 수용체의 표적화된 대체 |
Country Status (13)
| Country | Link |
|---|---|
| US (5) | US11033584B2 (ko) |
| EP (1) | EP3700924A4 (ko) |
| JP (2) | JP7101419B2 (ko) |
| KR (2) | KR20230034416A (ko) |
| CN (1) | CN111655719A (ko) |
| AU (2) | AU2018355587B2 (ko) |
| BR (1) | BR112020008201A2 (ko) |
| CA (1) | CA3080415A1 (ko) |
| EA (1) | EA202091056A1 (ko) |
| IL (2) | IL305485A (ko) |
| MX (1) | MX2020004325A (ko) |
| SG (1) | SG11202003798TA (ko) |
| WO (1) | WO2019084552A1 (ko) |
Families Citing this family (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018232356A1 (en) | 2017-06-15 | 2018-12-20 | The Regents Of The University Of California | Targeted non-viral dna insertions |
| WO2019084552A1 (en) | 2017-10-27 | 2019-05-02 | The Regents Of The University Of California | TARGETED REPLACEMENT OF ENDOGENIC T CELL RECEPTORS |
| BR112020008704A2 (pt) | 2017-10-30 | 2020-11-10 | Pact Pharma, Inc. | edição de genes de células primárias |
| JP2021520212A (ja) | 2018-04-02 | 2021-08-19 | パクト ファーマ インコーポレイテッドPact Pharma, Inc. | ペプチド−mhc compact |
| WO2019226998A1 (en) * | 2018-05-25 | 2019-11-28 | The Regents Of The University Of California | Genetic engineering of endogenous proteins |
| KR20210126073A (ko) | 2019-02-12 | 2021-10-19 | 팩트 파마, 인크. | 항원 특이적 t 세포의 식별을 위한 조성물 및 방법 |
| US20220242929A1 (en) * | 2019-08-05 | 2022-08-04 | Cartherics Pty. Ltd. | Immune cells expressing modified cell receptors and methods of making |
| EP3808765A1 (en) * | 2019-10-14 | 2021-04-21 | ETH Zurich | Cell line for tcr discovery and engineering and methods of use thereof |
| TW202124718A (zh) * | 2019-11-14 | 2021-07-01 | 國立大學法人廣島大學 | 使用環狀dna將抗原特異性受體基因導入t細胞基因組之方法 |
| CA3175106A1 (en) * | 2020-03-13 | 2021-09-16 | The Regents Of The University Of California | Compositions and methods for modifying a target nucleic acid |
| KR20230056026A (ko) * | 2020-08-27 | 2023-04-26 | 티뮤니티 테라퓨틱스 인크. | 조작된 면역 세포의 제조를 위한 벡터-비사용 공정 |
| WO2022072932A1 (en) * | 2020-10-02 | 2022-04-07 | The Regents Of The University Of California | Dna constructs for improved t cell immunotherapy of cancer |
| WO2023154968A2 (en) * | 2022-02-14 | 2023-08-17 | The Regents Of The University Of California | Dna constructs for improved t cell immunotherapy |
| WO2024059618A2 (en) | 2022-09-13 | 2024-03-21 | Arsenal Biosciences, Inc. | Immune cells having co-expressed tgfbr shrnas |
| WO2024059824A2 (en) | 2022-09-16 | 2024-03-21 | Arsenal Biosciences, Inc. | Immune cells with combination gene perturbations |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016069282A1 (en) * | 2014-10-31 | 2016-05-06 | The Trustees Of The University Of Pennsylvania | Altering gene expression in modified t cells and uses thereof |
| WO2017044661A1 (en) * | 2015-09-09 | 2017-03-16 | Immune Design Corp. | Ny-eso-1 specific tcrs and methods of use thereof |
| WO2017106528A2 (en) * | 2015-12-18 | 2017-06-22 | Sangamo Biosciences, Inc. | Targeted disruption of the t cell receptor |
| WO2017156484A1 (en) * | 2016-03-11 | 2017-09-14 | Bluebird Bio, Inc. | Genome edited immune effector cells |
Family Cites Families (91)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6534261B1 (en) | 1999-01-12 | 2003-03-18 | Sangamo Biosciences, Inc. | Regulation of endogenous gene expression in cells using zinc finger proteins |
| US20020064802A1 (en) | 2000-04-28 | 2002-05-30 | Eva Raschke | Methods for binding an exogenous molecule to cellular chromatin |
| US20050136040A1 (en) | 2001-10-11 | 2005-06-23 | Imperial College Innovations Limited | Control of gene expression using a complex of an oligonucleotide and a regulatory peptide |
| GB0124391D0 (en) | 2001-10-11 | 2001-11-28 | Gene Expression Technologies L | Control of gene expression |
| US20030232410A1 (en) | 2002-03-21 | 2003-12-18 | Monika Liljedahl | Methods and compositions for using zinc finger endonucleases to enhance homologous recombination |
| ITMI20030821A1 (it) | 2003-04-18 | 2004-10-19 | Internat Ct For Genetic En Gineering And | Polipeptidi chimerici e loro uso. |
| US20060182736A1 (en) | 2003-06-10 | 2006-08-17 | Kim Jin-Soo | Transducible dna-binding proteins |
| US8133733B2 (en) | 2003-10-24 | 2012-03-13 | Gencia Corporation | Nonviral vectors for delivering polynucleotides to target tissues |
| WO2005123962A2 (en) | 2004-06-14 | 2005-12-29 | The University Of Texas At Austin | Gene targeting in eukaryotic cells by group ii intron ribonucleoprotein particles |
| US10022457B2 (en) | 2005-08-05 | 2018-07-17 | Gholam A. Peyman | Methods to regulate polarization and enhance function of cells |
| DK2336362T3 (en) | 2005-08-26 | 2019-01-21 | Dupont Nutrition Biosci Aps | USE OF CRISPR-ASSOCIATED GENES (CAS) |
| PL2049663T3 (pl) | 2006-08-11 | 2015-08-31 | Dow Agrosciences Llc | Homologiczna rekombinacja za pośrednictwem nukleazy z palcami cynkowymi |
| US20110239315A1 (en) | 2009-01-12 | 2011-09-29 | Ulla Bonas | Modular dna-binding domains and methods of use |
| JP2012525146A (ja) | 2009-04-28 | 2012-10-22 | プレジデント アンド フェロウズ オブ ハーバード カレッジ | 細胞透過のための過剰に荷電されたタンパク質 |
| WO2011059836A2 (en) | 2009-10-29 | 2011-05-19 | Trustees Of Dartmouth College | T cell receptor-deficient t cell compositions |
| US8956828B2 (en) * | 2009-11-10 | 2015-02-17 | Sangamo Biosciences, Inc. | Targeted disruption of T cell receptor genes using engineered zinc finger protein nucleases |
| SG181601A1 (en) | 2009-12-10 | 2012-07-30 | Univ Minnesota | Tal effector-mediated dna modification |
| CA2796600C (en) | 2010-04-26 | 2019-08-13 | Sangamo Biosciences, Inc. | Genome editing of a rosa locus using zinc-finger nucleases |
| US8876458B2 (en) | 2011-01-25 | 2014-11-04 | United Technologies Corporation | Blade outer air seal assembly and support |
| WO2013074916A1 (en) | 2011-11-18 | 2013-05-23 | Board Of Regents, The University Of Texas System | Car+ t cells genetically modified to eliminate expression of t- cell receptor and/or hla |
| GB201122458D0 (en) | 2011-12-30 | 2012-02-08 | Univ Wageningen | Modified cascade ribonucleoproteins and uses thereof |
| US20130236504A1 (en) | 2012-03-06 | 2013-09-12 | Medical University Of South Carolina | Delivery System for Enhancing Drug Efficacy |
| LT3401400T (lt) | 2012-05-25 | 2019-06-10 | The Regents Of The University Of California | Būdai ir kompozicijos, skirtos rnr molekulės nukreipiamai tikslinės dnr modifikacijai ir rnr molekulės nukreipiamam transkripcijos moduliavimui |
| DE202013012597U1 (de) | 2012-10-23 | 2017-11-21 | Toolgen, Inc. | Zusammensetzung zum Spalten einer Ziel-DNA, umfassend eine für die Ziel-DNA spezifische guide-RNA und eine Cas-Protein-codierende Nukleinsäure oder ein Cas-Protein, sowie deren Verwendung |
| EP3138911B1 (en) | 2012-12-06 | 2018-12-05 | Sigma Aldrich Co. LLC | Crispr-based genome modification and regulation |
| EP4234696A3 (en) | 2012-12-12 | 2023-09-06 | The Broad Institute Inc. | Crispr-cas component systems, methods and compositions for sequence manipulation |
| EP2931899A1 (en) | 2012-12-12 | 2015-10-21 | The Broad Institute, Inc. | Functional genomics using crispr-cas systems, compositions, methods, knock out libraries and applications thereof |
| US8697359B1 (en) | 2012-12-12 | 2014-04-15 | The Broad Institute, Inc. | CRISPR-Cas systems and methods for altering expression of gene products |
| CA3081054A1 (en) | 2012-12-17 | 2014-06-26 | President And Fellows Of Harvard College | Rna-guided human genome engineering |
| CA2906553C (en) | 2013-03-15 | 2022-08-02 | The General Hospital Corporation | Rna-guided targeting of genetic and epigenomic regulatory proteins to specific genomic loci |
| US20160024493A1 (en) * | 2013-03-15 | 2016-01-28 | Adaptive Biotechnologies Corporation | Uniquely tagged rearranged adaptive immune receptor genes in a complex gene set |
| US9937207B2 (en) * | 2013-03-21 | 2018-04-10 | Sangamo Therapeutics, Inc. | Targeted disruption of T cell receptor genes using talens |
| US20160053274A1 (en) | 2013-04-02 | 2016-02-25 | Bayer Cropscience Nv | Targeted genome engineering in eukaryotes |
| ES2883131T3 (es) | 2013-05-29 | 2021-12-07 | Cellectis | Métodos para la modificación de células T para inmunoterapia utilizando el sistema de nucleasa CAS guiado por ARN |
| US9890393B2 (en) * | 2013-05-29 | 2018-02-13 | Cellectis | Methods for engineering T cells for immunotherapy by using RNA-guided CAS nuclease system |
| US9526784B2 (en) | 2013-09-06 | 2016-12-27 | President And Fellows Of Harvard College | Delivery system for functional nucleases |
| US10822606B2 (en) | 2013-09-27 | 2020-11-03 | The Regents Of The University Of California | Optimized small guide RNAs and methods of use |
| CN105899665B (zh) | 2013-10-17 | 2019-10-22 | 桑格摩生物科学股份有限公司 | 用于核酸酶介导的基因组工程改造的递送方法和组合物 |
| WO2015073867A1 (en) | 2013-11-15 | 2015-05-21 | The United States Of America, As Represented By The Secretary, Department Of Health & Human Services | Engineering neural stem cells using homologous recombination |
| KR20160089527A (ko) | 2013-12-12 | 2016-07-27 | 더 브로드 인스티튜트, 인코퍼레이티드 | 게놈 편집을 위한 crispr-cas 시스템 및 조성물의 전달, 용도 및 치료적 응용 |
| WO2015089486A2 (en) | 2013-12-12 | 2015-06-18 | The Broad Institute Inc. | Systems, methods and compositions for sequence manipulation with optimized functional crispr-cas systems |
| MX2016007327A (es) | 2013-12-12 | 2017-03-06 | Broad Inst Inc | Suministro, uso y aplicaciones terapeuticas de sistemas y composiciones crispr-cas para dirigirlos a trastornos y enfermedades usando componentes para suministro de particulas. |
| WO2015086795A1 (en) | 2013-12-13 | 2015-06-18 | Cellectis | Cas9 nuclease platform for microalgae genome engineering |
| KR20220100078A (ko) | 2014-01-31 | 2022-07-14 | 팩터 바이오사이언스 인크. | 핵산 제조 및 송달을 위한 방법 및 산물 |
| WO2015115903A1 (en) | 2014-02-03 | 2015-08-06 | Academisch Ziekenhuis Leiden H.O.D.N. Lumc | Site-specific dna break-induced genome editing using engineered nucleases |
| KR20230152175A (ko) | 2014-04-18 | 2023-11-02 | 에디타스 메디신, 인코포레이티드 | 암 면역요법을 위한 crispr-cas-관련 방법, 조성물 및 구성성분 |
| WO2016036754A1 (en) | 2014-09-02 | 2016-03-10 | The Regents Of The University Of California | Methods and compositions for rna-directed target dna modification |
| WO2016044745A1 (en) * | 2014-09-19 | 2016-03-24 | Regeneron Pharmaceuticals, Inc. | Chimeric antigen receptors |
| WO2016049251A1 (en) | 2014-09-24 | 2016-03-31 | The Broad Institute Inc. | Delivery, use and therapeutic applications of the crispr-cas systems and compositions for modeling mutations in leukocytes |
| EP3204513A2 (en) | 2014-10-09 | 2017-08-16 | Life Technologies Corporation | Crispr oligonucleotides and gene editing |
| WO2016097751A1 (en) | 2014-12-18 | 2016-06-23 | The University Of Bath | Method of cas9 mediated genome engineering |
| AU2016209295B2 (en) | 2015-01-21 | 2021-08-12 | Genevant Sciences Gmbh | Methods, compositions, and systems for delivering therapeutic and diagnostic agents into cells |
| EP3929296A1 (en) | 2015-01-30 | 2021-12-29 | The Regents of The University of California | Protein delivery in primary hematopoietic cells |
| US20180200387A1 (en) | 2015-02-23 | 2018-07-19 | Crispr Therapeutics Ag | Materials and methods for treatment of human genetic diseases including hemoglobinopathies |
| WO2016172359A2 (en) | 2015-04-24 | 2016-10-27 | The Regents Of The University Of California | Systems for detecting, monitoring or treating diseases or conditions using engineered cells and methods for making and using them |
| CA2986060A1 (en) | 2015-05-29 | 2016-12-08 | Valerie Odegard | Composition and methods for regulating inhibitory interactions in genetically engineered cells |
| AU2016278982A1 (en) | 2015-06-17 | 2018-01-18 | The Uab Research Foundation | CRISPR/Cas9 complex for genomic editing |
| EP3310931B1 (en) | 2015-06-17 | 2021-11-17 | The UAB Research Foundation | Crispr/cas9 complex for introducing a functional polypeptide into cells of blood cell lineage |
| US20170000743A1 (en) | 2015-07-02 | 2017-01-05 | Vindico NanoBio Technology Inc. | Compositions and Methods for Delivery of Gene Editing Tools Using Polymeric Vesicles |
| AU2016291778B2 (en) | 2015-07-13 | 2021-05-06 | Sangamo Therapeutics, Inc. | Delivery methods and compositions for nuclease-mediated genome engineering |
| US9512446B1 (en) | 2015-08-28 | 2016-12-06 | The General Hospital Corporation | Engineered CRISPR-Cas9 nucleases |
| US20180243446A1 (en) | 2015-09-01 | 2018-08-30 | The Hospital For Sick Children | Method and compositions for removing duplicated copy number variaions (cnvs) for genetic disorders and related uses |
| WO2017053729A1 (en) | 2015-09-25 | 2017-03-30 | The Board Of Trustees Of The Leland Stanford Junior University | Nuclease-mediated genome editing of primary cells and enrichment thereof |
| US11286480B2 (en) | 2015-09-28 | 2022-03-29 | North Carolina State University | Methods and compositions for sequence specific antimicrobials |
| EP3940070A1 (en) * | 2015-10-05 | 2022-01-19 | Precision Biosciences, Inc. | Engineered meganucleases with recognition sequences found in the human t cell receptor alpha constant region gene |
| EP4108255A1 (en) * | 2015-10-05 | 2022-12-28 | Precision Biosciences, Inc. | Genetically-modified cells comprising a modified human t cell receptor alpha constant region gene |
| WO2017070169A1 (en) | 2015-10-19 | 2017-04-27 | The Methodist Hospital | Crispr-cas9 delivery to hard-to-transfect cells via membrane deformation |
| CN108368522A (zh) | 2015-10-20 | 2018-08-03 | 10X 基因组学有限公司 | 用于高通量单细胞遗传操作的方法和系统 |
| WO2017070429A1 (en) | 2015-10-22 | 2017-04-27 | Regents Of The University Of Minnesota | Methods involving editing polynucleotides that encode t cell receptor |
| CN108368520B (zh) | 2015-11-04 | 2023-01-17 | 菲特治疗公司 | 多能细胞的基因组工程改造 |
| JP2019500899A (ja) | 2015-11-23 | 2019-01-17 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | CRISPR/Cas9の核送達を通じた細胞RNAの追跡と操作 |
| AU2016380836A1 (en) | 2015-12-30 | 2018-07-12 | Avectas Limited | Vector-free delivery of gene editing proteins and compositions to cells and tissues |
| JP2019510503A (ja) | 2016-04-07 | 2019-04-18 | ブルーバード バイオ, インコーポレイテッド | キメラ抗原受容体t細胞組成物 |
| KR20230088514A (ko) | 2016-04-14 | 2023-06-19 | 프레드 허친슨 캔서 센터 | 표적화 핵산 나노수송체를 이용하여 치료 세포를 프로그램화하기 위한 조성물 및 방법 |
| US10188749B2 (en) | 2016-04-14 | 2019-01-29 | Fred Hutchinson Cancer Research Center | Compositions and methods to program therapeutic cells using targeted nucleic acid nanocarriers |
| EP4180519A1 (en) * | 2016-04-15 | 2023-05-17 | Memorial Sloan Kettering Cancer Center | Transgenic t cell and chimeric antigen receptor t cell compositions and related methods |
| WO2017189336A1 (en) | 2016-04-25 | 2017-11-02 | The Regents Of The University Of California | Methods and compositions for genomic editing |
| WO2017186550A1 (en) | 2016-04-29 | 2017-11-02 | Basf Plant Science Company Gmbh | Improved methods for modification of target nucleic acids |
| WO2017210334A1 (en) | 2016-05-31 | 2017-12-07 | Massachusetts Institute Of Technology | Hydrodynamically controlled electric fields for high throughput transformation & high throughput parallel transformation platform |
| WO2017220527A1 (en) | 2016-06-20 | 2017-12-28 | Glycotope Gmbh | Means and methods for modifying multiple alleles |
| CN110312799A (zh) | 2016-08-17 | 2019-10-08 | 博德研究所 | 新型crispr酶和系统 |
| US20190177677A1 (en) | 2016-08-20 | 2019-06-13 | The Regents Of The University Of California | High-throughput system and method for the temporary permeablization of cells |
| CN110291100A (zh) | 2016-10-12 | 2019-09-27 | 费尔丹生物公司 | 用于将多肽负荷从细胞外空间递送至靶真核细胞的胞质溶胶和/或细胞核的合理设计的合成肽穿梭剂,其用途、与其相关的方法和试剂盒 |
| WO2018073393A2 (en) | 2016-10-19 | 2018-04-26 | Cellectis | Tal-effector nuclease (talen) -modified allogenic cells suitable for therapy |
| WO2018073391A1 (en) | 2016-10-19 | 2018-04-26 | Cellectis | Targeted gene insertion for improved immune cells therapy |
| WO2018094291A1 (en) | 2016-11-18 | 2018-05-24 | Christopher Bradley | Massively multiplexed homologous template repair for whole-genome replacement |
| US10975388B2 (en) | 2016-12-14 | 2021-04-13 | Ligandal, Inc. | Methods and compositions for nucleic acid and protein payload delivery |
| CN110546495B (zh) | 2016-12-30 | 2022-11-01 | 加利福尼亚州立大学董事会 | 用于基因组编辑t细胞的选择和传代的方法 |
| WO2018232356A1 (en) | 2017-06-15 | 2018-12-20 | The Regents Of The University Of California | Targeted non-viral dna insertions |
| WO2019084552A1 (en) | 2017-10-27 | 2019-05-02 | The Regents Of The University Of California | TARGETED REPLACEMENT OF ENDOGENIC T CELL RECEPTORS |
| BR112020008704A2 (pt) * | 2017-10-30 | 2020-11-10 | Pact Pharma, Inc. | edição de genes de células primárias |
-
2018
- 2018-10-29 WO PCT/US2018/058026 patent/WO2019084552A1/en unknown
- 2018-10-29 BR BR112020008201-5A patent/BR112020008201A2/pt not_active Application Discontinuation
- 2018-10-29 AU AU2018355587A patent/AU2018355587B2/en active Active
- 2018-10-29 KR KR1020237005926A patent/KR20230034416A/ko not_active Application Discontinuation
- 2018-10-29 MX MX2020004325A patent/MX2020004325A/es unknown
- 2018-10-29 CN CN201880084419.6A patent/CN111655719A/zh active Pending
- 2018-10-29 KR KR1020207015078A patent/KR102503130B1/ko active IP Right Grant
- 2018-10-29 SG SG11202003798TA patent/SG11202003798TA/en unknown
- 2018-10-29 JP JP2020523254A patent/JP7101419B2/ja active Active
- 2018-10-29 IL IL305485A patent/IL305485A/en unknown
- 2018-10-29 CA CA3080415A patent/CA3080415A1/en active Pending
- 2018-10-29 EP EP18871537.9A patent/EP3700924A4/en active Pending
- 2018-10-29 EA EA202091056A patent/EA202091056A1/ru unknown
- 2018-10-29 IL IL274179A patent/IL274179B2/en unknown
-
2019
- 2019-09-11 US US16/568,116 patent/US11033584B2/en active Active
-
2021
- 2021-03-12 US US17/200,301 patent/US11083753B1/en active Active
- 2021-07-30 US US17/390,673 patent/US11331346B2/en active Active
-
2022
- 2022-04-20 US US17/725,478 patent/US11590171B2/en active Active
- 2022-06-28 JP JP2022103225A patent/JP2022137112A/ja active Pending
-
2023
- 2023-01-27 US US18/160,825 patent/US20230310502A1/en active Pending
- 2023-04-28 AU AU2023202582A patent/AU2023202582A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016069282A1 (en) * | 2014-10-31 | 2016-05-06 | The Trustees Of The University Of Pennsylvania | Altering gene expression in modified t cells and uses thereof |
| WO2017044661A1 (en) * | 2015-09-09 | 2017-03-16 | Immune Design Corp. | Ny-eso-1 specific tcrs and methods of use thereof |
| WO2017106528A2 (en) * | 2015-12-18 | 2017-06-22 | Sangamo Biosciences, Inc. | Targeted disruption of the t cell receptor |
| WO2017156484A1 (en) * | 2016-03-11 | 2017-09-14 | Bluebird Bio, Inc. | Genome edited immune effector cells |
Non-Patent Citations (2)
| Title |
|---|
| Nature.,543(7643):113-117(2017.2.22.) * |
| Proc Natl Acad Sci U S A.,112(33):10437-10442(2015.8.18.) * |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2019084552A1 (en) | 2019-05-02 |
| IL305485A (en) | 2023-10-01 |
| JP7101419B2 (ja) | 2022-07-15 |
| IL274179A (en) | 2020-06-30 |
| EP3700924A1 (en) | 2020-09-02 |
| BR112020008201A2 (pt) | 2020-10-06 |
| US20200000851A1 (en) | 2020-01-02 |
| AU2018355587A1 (en) | 2020-06-18 |
| US20230310502A1 (en) | 2023-10-05 |
| CN111655719A (zh) | 2020-09-11 |
| US11033584B2 (en) | 2021-06-15 |
| US20220241336A1 (en) | 2022-08-04 |
| US11590171B2 (en) | 2023-02-28 |
| JP2021500889A (ja) | 2021-01-14 |
| IL274179B2 (en) | 2024-02-01 |
| US11331346B2 (en) | 2022-05-17 |
| KR20230034416A (ko) | 2023-03-09 |
| MX2020004325A (es) | 2020-11-09 |
| CA3080415A1 (en) | 2019-05-02 |
| US20210353678A1 (en) | 2021-11-18 |
| IL274179B1 (en) | 2023-10-01 |
| SG11202003798TA (en) | 2020-05-28 |
| AU2023202582A1 (en) | 2023-05-18 |
| KR102503130B1 (ko) | 2023-02-24 |
| JP2022137112A (ja) | 2022-09-21 |
| US11083753B1 (en) | 2021-08-10 |
| EP3700924A4 (en) | 2021-11-03 |
| US20210228631A1 (en) | 2021-07-29 |
| AU2018355587B2 (en) | 2023-02-02 |
| EA202091056A1 (ru) | 2020-09-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102503130B1 (ko) | 내인성 t 세포 수용체의 표적화된 대체 | |
| US20220143084A1 (en) | Modified natural killer (nk) cells for immunotherapy | |
| KR102528384B1 (ko) | 감소된 cd96/tigit 발현을 갖는 유전자 변형된 nk-92 세포 | |
| CN107429254B (zh) | 原代造血细胞中的蛋白递送 | |
| JP2018532426A (ja) | リンパ球における高レベル且つ安定な遺伝子移入のための方法 | |
| CN112040986A (zh) | 用于改进的免疫疗法的基因调控组合物和方法 | |
| US20230066806A1 (en) | Pooled knock-in screening and heterologous polypeptides co-expressed under the control of endogenous loci | |
| US20210207174A1 (en) | Genetic engineering of endogenous proteins | |
| CN110914431B (zh) | 经人工操纵的免疫细胞 | |
| KR20200018645A (ko) | 표적화된 비-바이러스 dna 삽입 | |
| WO2020160489A1 (en) | Gene-regulating compositions and methods for improved immunotherapy | |
| IL297881A (en) | Selection by knock-in of essential genes | |
| JP2020528046A (ja) | T細胞に基づく免疫療法の有効性増強のための組成物および方法 | |
| EP4060038A1 (en) | Method for introducing antigen-specific receptor gene into t cell genome using cyclic dna | |
| JP2023544161A (ja) | がんの改善されたt細胞免疫療法のためのdna構築物 | |
| CN116848234A (zh) | 使用修饰的自然杀伤(nk)细胞诱导抗体依赖的细胞介导的细胞毒性作用(adcc)的方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |