KR20180098235A - 비-조혈조직에 상재하는 γδ T 세포의 증식 및 이들 세포의 용도 - Google Patents
비-조혈조직에 상재하는 γδ T 세포의 증식 및 이들 세포의 용도 Download PDFInfo
- Publication number
- KR20180098235A KR20180098235A KR1020187015244A KR20187015244A KR20180098235A KR 20180098235 A KR20180098235 A KR 20180098235A KR 1020187015244 A KR1020187015244 A KR 1020187015244A KR 20187015244 A KR20187015244 A KR 20187015244A KR 20180098235 A KR20180098235 A KR 20180098235A
- Authority
- KR
- South Korea
- Prior art keywords
- cells
- cell
- rti
- human
- gamma delta
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
- C12N5/0638—Cytotoxic T lymphocytes [CTL] or lymphokine activated killer cells [LAK]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/10—Cellular immunotherapy characterised by the cell type used
- A61K40/11—T-cells, e.g. tumour infiltrating lymphocytes [TIL] or regulatory T [Treg] cells; Lymphokine-activated killer [LAK] cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/42—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
- A61P31/22—Antivirals for DNA viruses for herpes viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
- G01N33/5047—Cells of the immune system
- G01N33/505—Cells of the immune system involving T-cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2302—Interleukin-2 (IL-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2315—Interleukin-15 (IL-15)
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Virology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Cell Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Hematology (AREA)
- Epidemiology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Engineering & Computer Science (AREA)
- AIDS & HIV (AREA)
- Urology & Nephrology (AREA)
- Physics & Mathematics (AREA)
- Toxicology (AREA)
- Food Science & Technology (AREA)
- Developmental Biology & Embryology (AREA)
- Analytical Chemistry (AREA)
- General Physics & Mathematics (AREA)
Abstract
Description
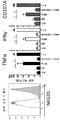
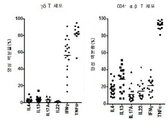
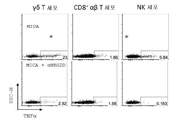
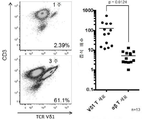
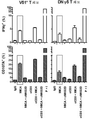
도 2a 내지 도 2d는 클라크 프로토콜을 통해 인간 피부로부터 직접적으로 유래된 피부에 상재하는 γδ T 세포가 T 세포를 활성화시키는 통상적인 수단에 의해 활성화될 때 소위 TH1에 편향된(TH1-biased) 반응을 나타내고, 마찬가지로 NKG2D 리간드 단독에 의한 활성화 시 TH1에 편향된 반응을 나타냄을 보여준다. 도 2a: 피부에 상재하는 γδ T 세포는 활성화 및 NK 세포 관련 수용체 NKG2D의 강한 발현을 보여준다(속이 채워진 히스토그램; 속이 빈 히스토그램으로 표시된 아이소타입과 대조적임). 플레이트에 결합된 NKG2D 수용체에 대한 공지된 리간드 중 하나인 재조합 MICA를 이용한 활성화 시, 피부 γδ T 세포는 임의의 다른 자극 없이 반응하고, 그 반응은 블로킹(blocking) NKG2D 항체의 존재하에 저지되므로 TCR 라이게이션과 무관하다. 브레펠딘 A(brefeldin A)와 100 단위의 IL-2/ml의 존재하에 6시간 동안 세포를 자극하였고, 그 후 CD107a에 대한 염색으로 탈과립을 분석하였다. 표면 염색 후 투과화(permeabilisation) 다음에 세포 내 사이토카인의 염색에 의해 TNFα 및 INF-γ의 생성을 분석하였다. 이오노마이신 (I)과 결합한 포르볼 12-미리스테이트 13-아세테이트 (P)를 T 세포를 활성화시키기 위한 양성 대조군으로 사용하였다. 도 2b: 피부에 상재하는 γδ T 세포는 TH1에 편향된 반응을 보여준다. 클라크 프로토콜을 이용하여 γδ T 세포를 회수하고, 브레펠딘 A의 존재하에 6시간 동안 PMA와 이오노마이신으로 자극하고, 세포 내 사이토카인에 대해 염색하였다. 인간 피부로부터 새롭게 단리된 γδ T 세포는 자극 시 TNFα와 IFN-γ를 생성하지만, 작거나 검출 불가능한 양의 TH2 또는 TH-17 세포와 관련이 있는 사이토카인, 예를 들어 IL-4, IL-17A, IL-13, IL-22만을 생성하는 반면, 통상적인 CD4+ αβ T 세포는 훨씬 더 다양한 사이토카인 생성을 보여준다. 도 2c: 인간 피부로부터 직접적으로 유래된 림프구 중에서, 다양한 수준의 NKG2D 수용체가 γδ T 세포, CD8a+ 통상적인 αβ T 세포 및 NK 세포에 의해 발현되었다. 이들 세포 가운데, NK 세포는 NKG2D 리간드 단독 노출에 반응하지만, T 세포 내에서는 임의의 TCR 자극의 부재하에서 NKG2D 리간드로 자극 시 사이토카인 반응을 보여주는 것은 γδ T 세포 집단뿐이다(유세포 분석 점 도표(dot plot)의 윗줄 참조). 반응은 가용성 블로킹 항-NKG2D 항체를 이용하여 차단될 수 있으며, 이는 반응이 NKG2D 수용체를 통해 독점적으로 매개됨을 보여준다. 도 2d: 피부에 상재하는 γδ T 세포 중에서, Vδ1 세포와 DN γδ T 세포만이 (*로 표시된) 재조합 MICA 단독에 의해서 활성화되는 선천적으로 유사한(innate-like) 잠재력을 보여준다. 피부 내에서 적은 수로 발견되는 Vδ2 발현 T 세포는 이러한 반응을 전혀 보이지 않는다.
도 3a 내지 도 3d는 피부에 상재하는 γδ T 세포가 오로지 강한 활성화 및 증식으로 인해 피부 기질로부터의 분리에 대해서만 반응함을 보여준다. 도 3a: 피부에 상재하는 림프구를 클라크 프로토콜을 이용하여 분리하였다. 3주의 기관형 배양 후, 피부 림프구를 수확하고 섬유아세포를 포함하는 임의의 잔여 피부 세포로부터 분리하여, 백만 개 림프구/ml의 밀도로 조직 배양 웰에 넣고 100 U/ml의 IL-2를 보충하였다. 3주가 더 지난 후, 상재하는 γδ T 세포가 강력하게 증식하였고, 피부 림프구 배양물 내에 농축되었다. 이러한 강력한 증식 현상은 3주 이내에 평균 127.18배로 증식된, Vδ1+ T 세포의 대다수로 대표되는 피부에 상재하는 γδ T 세포에만 존재하는 반면, 통상적인 αβ T 세포는 평균 5.21배 증식되었으며; 이는 20배가 넘지 않는다. 도 3b: 피부에 상재하는 Vδ1+ T 세포는 14일에 걸쳐 (세포 주기를 나타내는) 마커 Ki-67을 강하게 상향 조절함으로써 조직 소실에 반응한다(아이소타입 대조군은 가장자리를 점선으로 표시한 속이 빈 히스토그램으로 표시함; 0일째의 Ki-67 발현은 속이 빈 히스토그램으로 표시; 7일째의 Ki-67 발현은 옅은 회색 히스토그램으로 표시; 14일째의 Ki-67 발현은 짙은 회색 히스토그램으로 표시). 나아가, 피부 기질과 접촉 시 대부분이 IL-2 수용체 알파(CD25)에 대해 음성인, 피부에 상재하는 Vδ1 T 세포는 조직으로부터 분리 후에 CD25를 상향 조절한다(아이소타입 대조군: 점선 히스토그램, 0일째 염색: 옅은 회색 히스토그램, 7일째 염색: 짙은 회색 히스토그램).
도 3c: Ki-67의 중간 형광 강도(median fluorescence intensity, MFI)로 표시된 높은 비율의 세포 주기는 Vδ1+ T 세포로 대표되는 피부에 상재하는 γδ T 세포에서만 관찰되며, 통상적인 αβ T 세포 및 NK 세포에서는 관찰되지 않고, 이들 세포에서는 MFI가 실제로 14일에 걸쳐 감소한다. 도 3d: 기질 세포로부터 분리된 피부 림프구는 3주의 배양 후에 강하게 농축된 상재하는 γδ T 세포 집단을 보여준다. 이러한 γδ T 세포 집단은 다수의 Vδ1 양성 세포(77.49%±17.04)와 pan γδ TCR 양성 DN T 세포(21.46%±16.92)를 포함한다. 클라크 프로토콜을 이용하여 새롭게 수확된 피부 림프구에서 관찰되는 초기의 작은 Vδ2 T 세포 집단은 조직 γδ T 세포의 3주 증식 후에는 감소하고 거의 소실된다(0.6%±1.204).
도 4a 및 4b는 피부에 상재하는 γδ T 세포가 조직의 소실에 반응하며, 피부 기질세포, 특히 섬유아세포에 의한 접촉 의존성 메커니즘을 통해 억제됨을 보여준다. 도 4a: 3주 후 클라크 프로토콜에서와 같이 기관형 배양 후 혼합 피부 림프구를 수확하였다. 그런 다음, 자가 피부 섬유아세포의 전면배양 층(confluent layer)의 위에, 그리고 섬유아세포에 의해 생성된 가용성 억제제의 존재를 제어하기 위해 트랜스웰 내에 혼합 림프구를 씨딩하였다. 14일 후, 존재하는 절대 세포 수(absolute cell number)를 통해 산출된 증식 배수(fold-wise)를 γδ T 세포 및 통상적인 αβ T 세포에 대해 측정하였다. 피부에 상재하는 γδ T 세포는 조직으로부터 분리될 때 섬유아세포의 존재하에서 강한 증식 반응을 보였으나, 자가 섬유아세포와 직접적으로 세포 접촉하지 않는 경우에만 그러했다. 통상적인 αβ T 세포는 시험된 어떠한 조건에서도 이러한 반응을 보이지 않았다. 도 4b: 기관형 배양으로부터 수득된 혼합 림프구를 자가 섬유아세포의 단일층 위에 씨딩하거나(옅은 회색 히스토그램) IL-2가 보충된 빈 웰 내에 씨딩하고(짙은 회색 히스토그램), 7일 동안 배양하였다. 피부에 상재하는 Vδ1+ T 세포(왼쪽 패널)뿐만 아니라 pan γδ TCR+, DN T 세포(오른쪽 패널)도 섬유아세포의 직접적인 존재하에서는 정지 상태(quiescent)를 유지하였으나, CD25, TH 관련된 전사 인자인 T-bet, 및 세포 주기 마커 Ki-67의 상향 조절된 발현(MFI)으로 표시된 바와 같이, 섬유아세포가 존재하지 않고 피부 기관형 배양물로부터 분리될 때 강한 활성화를 보였다(점선, 속이 빈 히스토그램은 일치되는 아이소타입 대조군을 나타냄).
도 5a 및 도 5b는 증식하는 피부 γδ T 세포가 탈억제 및 강한 세포독성 잠재력 획득의 징후를 나타냄을 보여준다. 도 5a: 피부에 상재하는 γδ T 세포를 기관형 세포 배양물로부터 분리한 후 14일 동안 증식시켰다. 그런 다음, γδ T 세포는 pan αβ TCR 단일클론 항체로 염색된 모든 통상적인 T 세포를 배제함으로써 유세포 분석법에 의해 음성으로 분류되었다. 그런 다음, 150,000개의 분류된 γδ T 세포를 평판 96웰 배양 플레이트에 2중으로(in duplicate) 씨딩하고, 사이토카인의 보충 및 임의의 활성화 리간드의 보충 없이, 24시간 동안 배양하였다. 상층액을 수확하고, 애피메트릭스(Affymetrix) 루미넥스(LUMINEX®) 기반의 사이토카인 어레이를 이용하여 생성된 사이토카인을 분석하였다. 도 5b: 음성으로 분류된 γδ T 세포 또한 1일 전에 씨딩한 암 세포주 상에 웰당 10,000개 세포의 농도로 씨딩하였다. 대조군으로서, 음성으로 분류된 통상적인 피부 αβ T 세포를 이용하였다. T 세포를 100U/ml의 IL-2의 존재하에서 블로킹 NKG2D 항체의 존재 및 부재하에 지정된 이펙터:표적 비율로 씨딩하였다. 피부에 상재하는 γδ T 세포는 통상적인 αβ T 세포에 비해 악성 세포주 중에서, ELISA를 통해 측정된 카스파제 절단 상피 특이적 사이토케라틴 18(CK18) 방출에 의해 도시된 바와 같이, 우수한 살해를 보여주었다. 세포독성은, NKG2D 수용체를 차단하는 항체를 함유하는 배양물에서의 그것의 감소로 도시된 바와 같이, NKG2D 수용체를 통해 적어도 부분적으로 매개되었다.
도 6a 내지 도 6d는 인간 소화관에서 조직에 상재하는 γδ T 세포를 분석한 결과를 보여준다. 도 6a: 클라크 프로토콜의 적용은 소화관에 상재하는 림프구 분리를 가능하게 하였다. 혼합 소화관 림프구는 보통은 주로 Vδ1 세포를 포함하는 조직에 상재하는 γδ T 세포의 대규모 집단을 포함하지만, Vδ2 및 이중 음성 γδ T 세포도 포함한다. 도 6b: 소화관 기관형 배양물로부터 분리된 γδ T 세포는 일단 소화관의 기질로부터 분리되면 시간이 경과함에 따라 Ki-67을 상향 조절하므로, 피부에서 유래된 γδ T 세포와 비슷한 반응을 보여준다. 도 6c: 소화관 유래 γδ T 세포는 IFN-γ를 생성하는 것에 의해, 그리고 CD107a 상향조절에 의해 측정된 바와 같이 탈과립에 의해, 재조합 MICA와 같은 선천적으로 유사한 자극에 대해 반응한다. 도 6d: 소화관 기관형 배양물로부터 분리된 γδ T 세포는 피부 유래 γδ T 세포에 대해 비슷한 반응을 보이며, 소화관 기질과의 접촉이 결여된 림프구 배양물에서 전반적인 농축으로 관찰되는 바와 같이 세포 배양물에서 시간이 경과함에 따라 증식한다.
도 7a 및 도 7b는 증식된 피부 유래 γδ T 세포의 조직 표현형을 보여준다. 도 7a: 피부 유래 γδ T 세포는 피부 림프구 항원(cutaneous lymphocyte antigen, CLA), 피부 표적지향 케모카인 수용체(skin homing chemokine receptor)인 CCR4와 CCR8에 대해 양성 염색된다. 도 7b: 발현 수준은 각각 피부 또는 혈액으로부터 유래된 증식된 γδ T 세포 상에서 상이하다.
도 8은 임의의 TCR의 자극 없이, 피부 유래 γδ T 세포의 탈억제가 자발적인 TH-1 사이토카인 생성을 초래하며, 놀랍게도 그리고 신선한 TCR 활성화된 γδ T 세포와는 반대로, 아토피성 사이토카인 IL-13의 생성을 초래함을 보여준다. 새롭게 유래된 γδ T 세포와 일관되게, 탈억제되고 증식 중인 γδ T 세포는 무시할만한 양의 TH-2 관련 사이토카인, 예를 들어 IL-4 및 IL-5를 생성한다. 피부 유래 γδ T 세포를 14일 동안 증식시키고, 통상적인 αβ T 세포를 배제시킴으로써 음성으로 분류하였다. 150,000개의 혼합 γδ T 세포를 임의의 자극 또는 사이토카인 보충 없이 4명의 공여자에 대해 2중으로 96 플레이트 평판 웰에 1백만 개 세포/ml의 밀도로 배양하였다. 24시간 후 상층액을 수집하고, 애피메트릭스의 루미넥스 기반의 사이토카인 어레이를 이용하여 분석하였다.
도 9a 내지 도 9c는 ELISA를 이용하여 표적 세포에 의한 카스파제 절단 사이토케라틴 18의 방출로 측정된 바와 같이, 증식되어 음성으로 분류된 피부 유래 γδ T 세포가 함께 배양된 다양한 인간 종양 세포주에 대해 강한 세포독성을 나타냄을 보여준다(도 9a: HCT1954, 도 9b: HCT116, 도 9c: MD231).
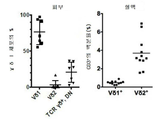
도 10a 및 도 10b는 신선한, 증식되지 않은 피부 유래 Vδ1 T 세포가 T 세포 활성화 이전의 마커를 보여준다는 점을 보여준다. 도 10a: 피부 유래 Vδ1 T 세포는 CD69, ICOS 및 TIM3을 높게 발현하고, CD28을 적게 발현한다. 나아가, 이 세포는 활성화 마커 NKG2D의 높은 발현을 보여준다. 이러한 표현형은 시험관 내에서 증식시키는 동안 피부 유래 Vδ1 T 세포에 의해 지속된다. 이와 반대로, 인간 혈액으로부터 유래된 Vδ1 T 세포는 이러한 활성화의 징후가 결여되어 있고, CD69 또는 TIM3을 발현하지 않으며, 낮은 수준의 ICOS만을 발현한다. 피부 유래 Vδ1 T 세포와 비교하여, 혈액 유래의 Vδ1 T 세포에서의 NKG2D 발현은 훨씬 낮은 반면, 혈액 유래의 Vδ1 T 세포는 공동 자극 분자 CD28을 발현한다. 도 10b: 피부 유래 Vδ1 T 세포만이 T 세포 수용체에 대한 리간드와 같은, 임의의 다른 자극의 부재하에서 재조합 MICA와 같은 NKG2D 리간드에 대해 반응성을 나타낸다. 혈액 유래 Vδ1 또는 Vδ2 T 세포는 선천적으로 유사한 자극에 대해 이러한 반응성을 보여주지 않는다. 표시된 바와 같이 재조합 MICA 또는 항-CD3 항체 또는 둘 다를 함유하는 96웰 플레이트에 세포를 씨딩하였다. 세포를 IL-2 100U/ml 중에서 6시간에 걸쳐 배양하고, 마지막 4시간 동안 BFA 중에서 배양한 후, 표면 항원 염색, 투과화 및 IFN-γ에 대한 세포 내 염색을 수행하였다.
도 11은 피부 유래 Vδ1 T 세포가 낮은 수준의 CD16을 발현하지만, 높은 친화도의 IgG 수용체 CD64의 상당한 발현을 보여준다는 점을 보여준다. 따라서, 직접적인 세포독성 활성 이외에도, 조직 유래 Vδ1 T 세포는 항체에 의해 악성 종양 및 전이 쪽으로 이끌리므로 CD20 또는 Her2 치료법과 같은 단일클론 항체요법의 효능을 증가시키고, 옵소닌화된 종양 세포를 인식하며, 그것들을 항체 의존적 세포 매개성 세포독성(ADCC)을 통해 살해하는 데 사용될 수도 있다. 도시된 결과는 (네 명 중) 한 명의 대표적인 공여자로부터 유래된 것이다.
도 12는 IL-2(왼쪽 패널), IL-15(가운데 패널) 및 IL-2 + IL-5(오른쪽 패널)에서의 Vδ1 T 세포의 증식을 보여준다. 신선하게 분리된 피부 유래 림프구를 10% FCS 및 1% Pen/Strep을 함유하는 RPMI 배지 중의 96웰 평판 플레이트에서 배양하고, 7일 동안 각각 IL-2, IL-15 또는 IL-2+IL-15를 보충하였다. IL-2와 IL-15뿐만 아니라, 이들 사이토카인의 조합은 임의의 기질 세포의 부재하에서 아이소타입(진 음성(true negative)) 염색과 비교하여 KI-67 염색에서의 변화로 표시된 바와 같이 Vδ1 T 세포의 증식을 유도하였다. Ki-67은 G0의 세포 주기를 벗어난 세포만을 염색하며, 이는 일반적으로 증식과 관련이 있다.
도 13은 21일째에 증식된 Vδ1 γδ T 세포의 표면에서의 CD9, CCR3 및 CD39의 발현을 나타내는 유세포 분석 결과를 보여준다. 증식된 피부 유래 Vδ1 T 세포는 동등한 아이소타입 염색(진 음성, 열린 히스토그램)에 비해 (짙은 색 히스토그램)으로 표시된 바와 같이 높은 수준의 세표 표면 마커 CCR3, CD39 및 CD9를 유지하였다.
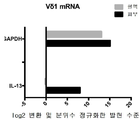
도 14는 피부 유래 Vδ1 T 세포(짙은 색 막대)와 혈액 유래 Vδ1 T 세포(옅은 색 막대)에서의 CCR3 및 CD9의 mRNA 발현을 보여준다. 피부 유래 Vδ1 T 세포를 본원에 개시된 바와 같이 증식시키고, 혈액 유래 Vδ1 T 세포를 Vδ T 세포 수용체에 대한 플레이트에 결합된 항체(20 μg/ml)를 이용하여 증식시켰다. 증식 후, Vδ1 T 세포를 형광 활성화 세포 분류법(Fluorescence Activated Cell Sorting, FACS)을 이용하여 단리하고, 양 그룹의 3명의 공여자로부터 RNA를 단리하였다(혈액=회색 대 피부=검은색). 전체 mRNA를 시퀀싱하고, 지정된 mRNA의 발현 수준을 정규화하고 로그 2 변환시켰다. 모든 발현 수준을 직접적으로 비교하여, 대부분의 인간 세포에서 높은 수준으로 발현되는 공통적인 하우스키핑(housekeeping) 유전자인 GAPDH에 대한 비율로 도시하였다.
도 15는 피부 유래 Vδ1 T 세포(짙은색 막대)와 혈액 유래 Vδ1 T 세포(옅은색 막대)에서의 IL-13의 mRNA 발현을 보여준다. 피부 유래 Vδ1 T 세포를 본원에 개시된 바와 같이 증식시키고, 혈액 유래 Vδ1 T 세포를 Vδ T 세포 수용체에 대한 플레이트에 결합된 고용량 항체(20μg/ml)를 이용하여 증식시켰다. 증식 후, Vδ1 T 세포를 FACS를 이용하여 단리하고, 양 그룹의 3명의 공여자로부터 RNA를 단리하였다(혈액=회색 대 피부=검은색). 전체 mRNA를 시퀀싱하고, IL-13에 대한 mRNA의 발현 수준을 정규화하고 로그 2 변환시켰다. 발현 수준을 직접적으로 비교하여, GAPDH에 대한 비율로 도시하였다.
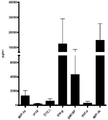
도 16a 및 16b는 PMA/이오노마이신(도 16a) 또는 항-CD3(도 16b)으로의 TCR 자극 후, 피부 유래 Vδ1 T 세포에서의 사이토카인의 생성을 보여준다. 단리 및 증식 후, 피부 유래 Vδ1 T 세포를 형광 활성화 세포 분류법(FACS)을 이용하여 정제하였다. 150,000개의 Vδ1 T 세포를 세 명의 공여자에 대해 이중으로 96웰 평판 플레이트에 씨딩하고, 24시간 동안 플레이트에 결합된 항 CD3(5μg/ml) 또는 PMA/이오노마이신으로 자극하였다. 상층액을 대상으로 루미넥스 플랫폼을 이용하여 지정된 사이토카인의 절대량을 분석하였다.
Claims (82)
- 시험관 내에서 비-조혈조직에 상재하는 γδ T 세포를 증식시키는 방법으로서,
인터루킨-2(IL-2) 및/또는 인터루킨-15(IL-15)의 존재하에 인간 또는 비인간 동물의 비-조혈조직으로부터 수득된 림프구를 배양하는 단계를 포함하며, 여기에서 림프구는 배양 중에 기질세포 또는 상피세포와 직접 접촉하지 않는 방법. - 제1항에 있어서,
림프구는 배양 중에 섬유아세포와 직접 접촉하지 않는 방법. - 제1항 또는 제2항에 있어서,
IL-2의 존재하에 인간 또는 비인간 동물의 비-조혈조직으로부터 수득된 림프구를 배양하는 단계를 포함하는 방법. - 제1항 또는 제2항에 있어서,
인터루킨-15(IL-15)의 존재하에 인간 또는 비인간 동물의 비-조혈조직으로부터 수득된 림프구를 배양하는 단계를 포함하는 방법. - 제1항 또는 제2항에 있어서,
IL-2 및 IL-15의 존재하에 인간 또는 비인간 동물의 비-조혈조직으로부터 수득된 림프구를 배양하는 단계를 포함하는 방법. - 제1항 내지 제5항 중 어느 한 항에 있어서,
TCR 활성화 또는 공동 자극 신호의 부재하에 림프구를 배양하는 단계를 포함하는 방법. - 제1항 내지 제6항 중 어느 한 항에 있어서,
T 세포 수용체 경로 작용제의 부재하에 림프구를 배양하는 단계를 포함하는 방법. - 제1항 내지 제7항 중 어느 한 항에 있어서,
림프구는 기질세포 또는 상피세포의 부재하에 배양되는 것인 방법. - 제8항에 있어서,
기질세포 또는 상피세포는 배양 전에 제거되는 것인 방법. - 제8항에 있어서,
림프구는 섬유아세포의 부재하에 배양되는 것인 방법. - 제10항에 있어서,
섬유아세포는 배양 전에 제거되는 것인 방법. - 제1항 내지 제11항 중 어느 한 항에 있어서,
림프구는 IL-2 및/또는 IL-15를 포함하는 γδ 증식 배지에서 배양되는 것인 방법. - 제12항에 있어서,
γδ 증식 배지는 T 세포 수용체를 활성화시키거나 공동 자극하지 않는 것인 방법. - 제12항 또는 제13항에 있어서,
γδ 증식 배지는 IL-2 및/또는 IL-15 이외에 성장 인자가 없는 것인 방법. - 제12항 내지 제14항 중 어느 한 항에 있어서,
γδ 증식 배지는 IL-2 및/또는 IL-15가 보충된 기본 배지로 이루어지는 것인 방법. - 제1항 내지 제15항 중 어느 한 항에 있어서,
림프구는 피부, 위장관(예를 들어, 결장), 유선 조직, 폐, 간, 췌장 또는 전립선으로부터 수득되는 것인 방법. - 제1항 내지 제16항 중 어느 한 항에 있어서,
γδ T 세포는 비 Vδ2 세포인 방법. - 제17항에 있어서,
γδ T 세포는 Vδ1 세포인 방법. - 제17항에 있어서,
γδ T 세포는 이중 음성(double negative, DN) γδ T 세포인 방법. - 제1항 내지 제19항 중 어느 한 항에 있어서,
인간 또는 비인간 동물 조직으로부터 림프구를 수득하는 단계를 포함하는 방법. - 제20항에 있어서,
림프구는 인간 또는 비인간 동물 비-조혈조직의 샘플로부터 수득되는 것인 방법. - 제20항 또는 제21항에 있어서,
조직은 비-조혈세포 및 림프구를 포함하는 것인 방법. - 제20항 내지 제22항 중 어느 한 항에 있어서,
인간 또는 비인간 동물 비-조혈조직의 샘플을 제공하는 단계 및 상기 샘플의 비-조혈세포로부터 림프구를 분리하여 기질세포를 실질적으로 포함하지 않는 림프구 집단을 생성하는 단계를 포함하는 방법. - γδ T 세포를 증식시키는 방법으로서,
(i) 비-조혈조직으로부터 수득된 γδ T 세포의 집단을 제공하는 단계; 및
(ii) γδ T 세포와 기질세포 접촉이 실질적으로 없는 조건에서 γδ T 세포를 배양하여 γδ T 세포의 증식된 집단을 생성하는 단계를 포함하는 방법. - 제24항에 있어서,
비-조혈조직으로부터 수득된 γδ T 세포의 집단은 실질적으로 순수한 γδ T 세포의 집단인 방법. - 제24항 또는 제25항에 있어서,
비-조혈조직으로부터 수득된 γδ T 세포의 집단은 비 Vδ2 세포인 방법. - 제26항에 있어서,
비 Vδ2 세포의 집단은 Vδ1 세포를 포함하는 것인 방법. - 제26항 또는 제27항에 있어서,
비 Vδ2 세포의 집단은 DN γδ T 세포를 포함하는 것인 방법. - 제24항 내지 제27항 중 어느 한 항에 있어서,
비-조혈조직으로부터 수득된 γδ T 세포의 집단은 Vδ1+CLA+CCR8+CD103+ γδ T 세포를 포함하는 것인 방법. - 제24항 내지 제29항 중 어느 한 항에 있어서,
단계 (ii)의 배양은 γδ T 세포와 기질세포 사이의 접촉 없이 수행되는 것인 방법. - 제24항 내지 제30항 중 어느 한 항에 있어서,
단계 (ii)의 γδ T 세포는 TCR 활성화 신호 또는 공동 자극 신호가 실질적으로 없는 조건에서 배양되는 것인 방법. - 제24항 내지 제31항 중 어느 한 항에 있어서,
단계 (ii)의 배양은 TCR 활성화 신호 또는 공동 자극 신호의 부재하에 수행되는 것인 방법. - 제24항 내지 제32항 중 어느 한 항에 있어서,
단계 (ii)의 배양은 기질세포 조정 배지에서 수행되는 것인 방법. - 제24항 내지 제33항 중 어느 한 항에 있어서,
단계 (ii)의 γδ T 세포 배양은 IL-2, IL-15 또는 이들의 조합의 존재하에 수행되는 것인 방법. - 제24항 내지 제34항 중 어느 한 항에 있어서,
γδ T 세포의 집단은 인간 또는 비인간 동물 비-조혈조직의 샘플로부터 수득되는 것인 방법. - 제24항 내지 제35항 중 어느 한 항에 있어서,
비-조혈조직은 비-조혈세포 및 γδ T 세포를 포함하는 것인 방법. - 제24항 내지 제36항 중 어느 한 항에 있어서,
비 조혈세포로부터 γδ T 세포를 분리하여, 기질세포를 실질적으로 포함하지 않는 γδ T 세포를 포함하는 분리된 림프구 집단을 생성하는 단계를 포함하는 방법. - 제24항 내지 제37항 중 어느 한 항에 있어서,
γδ T 세포는 IL-2 및/또는 IL-15를 포함하는 γδ 증식 배지에서 배양되는 것인 방법. - 제24항 내지 제38항 중 어느 한 항에 있어서,
γδ 증식 배지는 T 세포 수용체를 활성화시키거나 공동 자극하지 않는 것인 방법. - 제24항 내지 제39항 중 어느 한 항에 있어서,
γδ 증식 배지는 IL-2 및/또는 IL-15 이외의 성장 인자가 없는 배지인 방법. - 제24항 내지 제40항 중 어느 한 항에 있어서,
γδ 증식 배지는 IL-2 및/또는 IL-15가 보충된 기본 배지로 이루어지는 배지인 방법. - γδ T 세포를 증식시키는 방법으로서,
(i) 비-조혈조직을 제공하는 단계;
(ii) 비-조혈세포로부터 γδ T 세포를 분리하여 기질세포를 실질적으로 포함하지 않는 γδ T 세포를 포함하는 분리된 집단을 생성하는 단계; 및
(iii) TCR 활성화 신호 또는 공동 자극 신호의 부재하에 단계 (ii)의 분리된 집단을 배양하여 γδ 세포의 증식된 집단을 생성하는 단계를 포함하고,
여기에서 상기 조직은 비-조혈세포 및 γδ T 세포를 포함하는 것인 방법. - 제42항에 있어서,
단계 (ii)의 분리는 αβ T 세포로부터 γδ T 세포를 분리하는 단계를 더 포함하는 방법. - 제42항 또는 제43항에 있어서,
단계 (ii)의 분리된 집단은 실질적으로 순수한 γδ T 세포 집단인 방법. - 제42항 내지 제44항 중 어느 한 항에 있어서,
단계 (ii)의 분리된 집단은 비 Vδ2 세포인 방법. - 제45항에 있어서,
비 Vδ2 세포의 집단은 Vδ1 세포를 포함하는 것인 방법. - 제45항 또는 제46항에 있어서,
비 Vδ2 세포의 집단은 DN γδ T 세포를 포함하는 것인 방법. - 제42항 내지 제47항 중 어느 한 항에 있어서,
단계 (ii)의 분리된 집단은 Vδ1+CLA+CCR8+CD103+ γδ T 세포의 집단을 포함하는 것인 방법. - 제42항 내지 제48항 중 어느 한 항에 있어서,
단계 (iii)의 배양은 실질적으로 기질세포 접촉 없이 수행되는 것인 방법. - 제42항 내지 제48항 중 어느 한 항에 있어서,
단계 (iii)의 배양은 γδ T 세포와 기질세포 사이의 접촉 없이 수행되는 것인 방법. - 제42항 내지 제50항 중 어느 한 항에 있어서,
단계 (iii)의 배양은 TCR 활성화 신호 또는 공동 자극 신호가 실질적으로 없는 것인 방법. - 제42항 내지 제51항 중 어느 한 항에 있어서,
단계 (iii)의 배양은 TCR 활성화 신호 및 공동 자극 신호의 부재하에 수행되는 것인 방법. - 제42항 내지 제52항 중 어느 한 항에 있어서,
단계 (iii)의 배양은 기질세포 조정 배지에서 수행되는 것인 방법. - 제42항 내지 제53항 중 어느 한 항에 있어서,
단계 (iii)의 배양은 IL-2, IL-15 또는 이들의 조합의 존재하에 수행되는 것인 방법. - 제54항에 있어서,
분리된 집단은 IL-2 및/또는 IL-15를 포함하는 γδ 증식 배지에서 배양되는 것인 방법. - 제55항에 있어서,
γδ 증식 배지는 T 세포 수용체를 활성화시키거나 공동 자극하지 않는 것인 방법. - 제55항 또는 제56항에 있어서,
γδ 증식 배지는 IL-2 및/또는 IL-15 이외의 성장 인자가 없는 것인 방법. - 제55항 내지 제57항 중 어느 한 항에 있어서,
γδ 증식 배지는 IL-2 및/또는 IL-15가 보충된 기본 배지로 이루어지는 것인 방법. - 제24항 내지 제58항 중 어느 한 항에 있어서,
증식된 γδ T 세포 집단은 배양 14일 이내에 비-조혈조직으로부터 수득된 γδ T 세포로서 적어도 20배의 γδ T 세포 수를 포함하는 것인 방법. - 제59항에 있어서,
증식된 γδ T 세포 집단은 배양 7일 이내에 비-조혈조직으로부터 수득된 γδ T 세포로서 적어도 2배의 γδ T 세포 수를 포함하는 것인 방법. - 제24항 내지 제60항 중 어느 한 항에 있어서,
증식된 γδ T 세포 집단은 적어도 50% Vδ1+ 세포인 방법. - 제61항에 있어서,
증식된 γδ T 세포 집단은 적어도 70% Vδ1+ 세포인 방법. - 제62항에 있어서,
증식된 γδ T 세포 집단은 적어도 90% Vδ1+ 세포인 방법. - 제24항 내지 제63항 중 어느 한 항에 있어서,
증식된 γδ T 세포 집단은 CCR4, CCR8 및 CD103에 대해 적어도 10% 양성인 방법. - 제63항에 있어서,
증식된 γδ T 세포 집단은 CCR4 및 CCR8에 대해 적어도 30% 양성인 방법. - 제65항에 있어서,
증식된 γδ T 세포 집단은 CCR8에 대해 적어도 60% 양성인 방법. - 제24항 내지 제66항 중 어느 한 항에 있어서,
γδ T 세포는 Vδ2- 세포인 방법. - 제1항 내지 제67항 중 어느 한 항의 방법에 의해 수득된 비-조혈조직에 상재하는 γδ T 세포.
- 다음 중 하나 이상을 갖는 비-조혈조직에 상재하는 γδ T 세포:
(i) 표현형 CD69높음, ICOS높음, TIM3높음 및 CD28낮음 /없음을 나타내고,
(ii) CCR3, CD39, CD11b, 및 CD9 중 하나 이상을 상향 조절하고,
(iii) TCR 작용제의 부재하에 NKG2D 리간드에 반응하여 IFN-γ를 생성하고,
(iv) TCR 작용제의 부재하에 IL-13을 생성하고,
(v) TCR 활성화에 반응하여 IFN-γ, TNF-α 및 GM-CSF 중 하나 이상을 생성하고,
(vi) TCR 활성화에 반응하여 IL-17을 전혀 또는 실질적으로 생성하지 않고,
(vii) 추가적인 성장 인자 없이 IL-2를 함유하는 배양 배지에서 성장하고,
(viii) TCR 작용제의 부재하에 세포독성 T 세포 반응을 나타내고, 및/또는
(ix) 정상 세포보다 종양 세포에 대해 선택적인 세포독성을 나타낸다. - 체크포인트 억제제에 대한 스크리닝 방법으로서,
(i) 시험 화합물의 존재 및 부재하에 기질세포 또는 상피세포(예를 들어, 섬유아세포)와 직접적으로 접촉시켜 시험관 내(in vitro)에서 비-조혈조직에 상재하는 γδ T 세포를 배양하거나, γδ T 세포 내 및/또는 기질세포 또는 상피세포(예를 들어, 섬유아세포)에서의 시험 유전자의 발현이 변경된 기질세포 또는 상피세포(예를 들어, 섬유아세포)와 직접적으로 접촉시켜 시험관 내에서 비-조혈조직에 상재하는 γδ T 세포를 배양하는 단계; 및
(ii) 시험 화합물의 존재 및 부재하에 또는 섬유아세포 및/또는 γδ T 세포에서 시험 유전자의 발현 변경의 존재 및 부재하에 비-조혈조직에 상재하는 γδ T 세포의 증식 또는 활성화 속도를 결정하거나, 시험 화합물의 존재 및 부재하에 또는 기질세포 또는 상피세포(예를 들어, 섬유아세포) 및/또는 γδ T 세포에서 시험 유전자의 발현 변경의 존재 및 부재하에 기질세포 또는 상피세포(예를 들어, 섬유아세포)의 살해 속도를 결정하는 단계를 포함하며,
여기에서, T 세포의 증식 또는 활성화 속도가 시험 화합물의 부재하에서보다 시험 화합물의 존재하에서 더 높거나 기질세포 또는 상피세포(예를 들어, 섬유아세포) 및/또는 γδ T 세포에서의 시험 유전자의 변경의 부재하에서보다 기질세포 또는 상피세포(예를 들어, 섬유아세포) 및/또는 γδ T 세포에서 시험 유전자의 발현 변경의 존재하에서 더 높은 경우, 및/또는 기질세포 또는 상피세포(예를 들어, 섬유아세포)의 살해 속도가 시험 화합물의 부재하에서보다 시험 화합물의 존재하에서 더 높거나 섬유아세포 및/또는 γδ T 세포에서의 시험 유전자의 변경의 부재 하에서보다 기질세포 또는 상피세포(예를 들어, 섬유아세포) 및/또는 γδ T 세포에서의 시험 유전자의 발현 변경의 존재하에서 더 높은 경우, 시험 화합물은 체크포인트 조절인자이거나 시험 유전자가 체크포인트 유전자 후보일 가능성이 있는 방법. - 입양 T 세포(adoptive T cell) 치료법에 의한 인간 또는 비인간 동물의 치료 방법에 사용하기 위한, 제1항 내지 제67항 중 어느 한 항의 방법에 의해 수득된 비-조혈조직에 상재하는 γδ T 세포.
- 제71항에 있어서,
인간은 인간 암 환자 또는 CMV 감염 환자 또는 HIV 감염 환자와 같은 바이러스 감염 환자인 비-조혈조직에 상재하는 γδ T 세포. - 입양 T 세포 치료법에 의해 대상체를 치료하는 방법에 있어서,
제1항 내지 제67항 중 어느 한 항의 방법에 의해 수득된 비-조혈조직에 상재하는 γδ T 세포를 이를 필요로 하는 대상체에 투여하는 단계를 포함하는 방법. - 제73항에 있어서,
대상체는 인간 암 환자 또는 CMV35 감염 환자 또는 HIV 감염 환자와 같은 바이러스 감염 환자인 방법. - 키메라 항원 수용체 치료법에 의한 인간 또는 비인간 동물의 치료 방법에 사용하기 위한, 제1항 내지 제67항 중 어느 한 항의 방법에 의해 수득된 비-조혈조직에 상재하는 γδ T 세포.
- 제75항에 있어서,
인간은 인간 암 환자인 비-조혈조직에 상재하는 γδ T 세포. - 키메라 항원 수용체 치료법에 의해 대상체를 치료하는 방법에 있어서,
제1항 내지 제67항 중 어느 한 항의 방법에 의해 수득된 비-조혈조직에 상재하는 γδ T 세포를 이를 필요로 하는 대상체에 투여하는 단계를 포함하는 방법. - 제77항에 있어서,
대상체는 인간 암 환자인 방법. - 입양 T 세포 치료법에 의해 대상체를 치료하는 방법에 있어서,
제69항의 비-조혈조직에 상재하는 γδ T 세포를 투여하는 단계를 포함하는 방법. - 제79항에 있어서,
대상체는 인간 암 환자 또는 CMV35 감염 환자 또는 HIV 감염 환자와 같은 바이러스 감염 환자인 방법. - 키메라 항원 수용체 치료법에 의해 대상체를 치료하는 방법에 있어서,
제69항의 비-조혈조직에 상재하는 γδ T 세포를 투여하는 단계를 포함하며, 여기에서 세포는 키메라 항원 수용체를 발현하는 세포인 방법. - 제81항에 있어서,
대상체는 인간 암 환자인 방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020257019399A KR20250093576A (ko) | 2015-10-30 | 2016-10-31 | 비-조혈조직에 상재하는 γδ T 세포의 증식 및 이들 세포의 용도 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1519198.4 | 2015-10-30 | ||
| GBGB1519198.4A GB201519198D0 (en) | 2015-10-30 | 2015-10-30 | Expansion of gamma delta t cells resident in non-haematopoietic tissue and uses of these cells |
| GB1612731.8 | 2016-07-22 | ||
| GBGB1612731.8A GB201612731D0 (en) | 2016-07-22 | 2016-07-22 | Expansion of non-haematopoietic tissue-resident gamma delta t cells and uses of these cells |
| PCT/EP2016/076264 WO2017072367A1 (en) | 2015-10-30 | 2016-10-31 | EXPANSION OF NON-HAEMATOPOIETIC TISSUE-RESIDENT γδ T CELLS AND USES OF THESE CELLS |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020257019399A Division KR20250093576A (ko) | 2015-10-30 | 2016-10-31 | 비-조혈조직에 상재하는 γδ T 세포의 증식 및 이들 세포의 용도 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20180098235A true KR20180098235A (ko) | 2018-09-03 |
| KR102821381B1 KR102821381B1 (ko) | 2025-06-13 |
Family
ID=57211532
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020257019399A Pending KR20250093576A (ko) | 2015-10-30 | 2016-10-31 | 비-조혈조직에 상재하는 γδ T 세포의 증식 및 이들 세포의 용도 |
| KR1020187015244A Active KR102821381B1 (ko) | 2015-10-30 | 2016-10-31 | 비-조혈조직에 상재하는 γδ T 세포의 증식 및 이들 세포의 용도 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020257019399A Pending KR20250093576A (ko) | 2015-10-30 | 2016-10-31 | 비-조혈조직에 상재하는 γδ T 세포의 증식 및 이들 세포의 용도 |
Country Status (16)
| Country | Link |
|---|---|
| US (2) | US11618885B2 (ko) |
| EP (2) | EP3368658B1 (ko) |
| JP (3) | JP2018533373A (ko) |
| KR (2) | KR20250093576A (ko) |
| CN (1) | CN108473958A (ko) |
| AU (2) | AU2016344779B2 (ko) |
| CA (1) | CA3003077A1 (ko) |
| DK (1) | DK3368658T3 (ko) |
| ES (1) | ES2925261T3 (ko) |
| IL (3) | IL295838B2 (ko) |
| MX (2) | MX2018005207A (ko) |
| MY (1) | MY198084A (ko) |
| PH (1) | PH12018500926A1 (ko) |
| PL (1) | PL3368658T3 (ko) |
| PT (1) | PT3368658T (ko) |
| WO (1) | WO2017072367A1 (ko) |
Families Citing this family (33)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201707048D0 (en) | 2017-05-03 | 2017-06-14 | King S College London | Expansion of gamma delta cells, compositions, and methods of use thereof |
| WO2018229163A1 (en) | 2017-06-14 | 2018-12-20 | King's College London | Methods of activating v delta 2 negative gamma delta t cells |
| EP3681996B1 (en) | 2017-09-15 | 2024-08-07 | King's College London | Compositions and methods for enhancing gamma delta t cells in the gut |
| CN109777778B (zh) * | 2017-11-14 | 2023-07-18 | 中国科学院广州生物医药与健康研究院 | 一种基因改造的γδT细胞 |
| GB201804701D0 (en) | 2018-03-23 | 2018-05-09 | Gammadelta Therapeutics Ltd | Lymphocytes expressing heterologous targeting constructs |
| WO2020027193A1 (ja) * | 2018-07-31 | 2020-02-06 | 国立大学法人三重大学 | γδ型T細胞への遺伝子導入方法 |
| GB201818243D0 (en) | 2018-11-08 | 2018-12-26 | Gammadelta Therapeutics Ltd | Methods for isolating and expanding cells |
| CN113423820A (zh) * | 2018-11-08 | 2021-09-21 | 伽马三角洲疗法有限公司 | 分离和扩增细胞的方法 |
| PH12021551475A1 (en) | 2019-01-07 | 2022-05-02 | Shattuck Labs Inc | Heterodimeric proteins for modulating gamma delta t cells |
| US11098093B2 (en) | 2019-01-07 | 2021-08-24 | Shattuck Labs, Inc. | Heterodimeric proteins for modulating gamma delta T cells |
| CN112029719B (zh) * | 2019-06-04 | 2024-05-03 | 北京医明佳和生物科技有限公司 | 纯化的双阴性t细胞及其制备和应用 |
| WO2021016652A1 (en) * | 2019-07-29 | 2021-02-04 | The University Of Melbourne | METHODS AND COMPOSITIONS FOR MONITORING, TREATING AND PREVENTING CMV INFECTION OR GRAFT REJECTION USING γδ T-CELLS |
| JP2022545196A (ja) | 2019-08-16 | 2022-10-26 | ガンマデルタ セラピューティクス リミテッド | 抗tcrデルタ可変1抗体の治療的使用 |
| JP7764364B2 (ja) | 2019-08-16 | 2025-11-05 | ガンマデルタ セラピューティクス リミティッド | エクスビボγδ T細胞集団 |
| CN115151565A (zh) | 2019-10-31 | 2022-10-04 | 莫佛塞斯公司 | 包含抗CD19抗体和γδT细胞的抗肿瘤组合疗法 |
| EP4114415A1 (en) | 2020-03-06 | 2023-01-11 | Sorrento Therapeutics, Inc. | Innate immunity killer cells targeting psma positive tumor cells |
| KR20230013022A (ko) | 2020-03-20 | 2023-01-26 | 감마델타 테라퓨틱스 엘티디 | 골수성 악성종양의 치료를 위한 v 델타1+ t 세포 |
| GB202006989D0 (en) * | 2020-05-12 | 2020-06-24 | Gammadelta Therapeutics Ltd | Methods for isolating gamma delta t cells |
| PL4269444T3 (pl) | 2020-08-14 | 2025-01-13 | GammaDelta Therapeutics Limited | Wieloswoiste przeciwciała anty-tcr zmienne delta 1 |
| GB202013962D0 (en) | 2020-09-04 | 2020-10-21 | Gammadelta Therapeutics Ltd | Immunotherapy composition |
| AU2022224391A1 (en) | 2021-02-17 | 2023-08-24 | Gammadelta Therapeutics Ltd | Anti-tcr delta variable 1 antibodies |
| GB202105113D0 (en) | 2021-04-09 | 2021-05-26 | Gammadelta Therapeutics Ltd | Novel method |
| CA3228168A1 (en) | 2021-08-03 | 2023-02-09 | Gammadelta Therapeutics Ltd | Engineering of gamma delta t cells and compositions thereof |
| WO2023053994A1 (ja) * | 2021-09-29 | 2023-04-06 | アイ ピース, インコーポレイテッド | 幹細胞の製造方法 |
| CA3208653A1 (en) | 2022-02-17 | 2022-08-25 | Mihriban Tuna | Multispecific anti-tcr delta variable 1 antibodies |
| JPWO2023176896A1 (ko) * | 2022-03-18 | 2023-09-21 | ||
| EP4504247A1 (en) | 2022-04-04 | 2025-02-12 | Gammadelta Therapeutics Ltd | Novel gene armoring |
| WO2024209429A1 (en) | 2023-04-07 | 2024-10-10 | Takeda Pharmaceutical Company Limited | T cells for use in treating relapsed or refractory acute myeloid leukemia |
| CN121532496A (zh) | 2023-07-20 | 2026-02-13 | 武田药品工业株式会社 | 用于制备γδT细胞的无网格方法 |
| CN118165933B (zh) * | 2024-05-14 | 2024-07-16 | 成都美杰赛尔生物科技有限公司 | 组合物、提高cd39-cd69-t细胞比例的方法 |
| WO2026013159A1 (en) | 2024-07-10 | 2026-01-15 | Cytospire Therapeutics Limited | Antibodies binding to constant domains of gamma delta t-cell receptors |
| WO2026013158A1 (en) | 2024-07-10 | 2026-01-15 | Cytospire Therapeutics Limited | Antibodies binding to constant domains of gamma delta t-cell receptors |
| CN118853566B (zh) * | 2024-09-26 | 2025-05-09 | 青岛华赛伯曼医学细胞生物有限公司 | 一种肿瘤浸润淋巴细胞的培养方法及培养基 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE421573T1 (de) | 1998-11-04 | 2009-02-15 | Therapure Biopharma Inc | Verfahren zur herstellung von gamma delta t zellen |
| US20060246520A1 (en) * | 2003-05-23 | 2006-11-02 | Institut National De La Sante Et De La Recherche Medicale | Gamma delta t cell-mediated therapy |
| EP1777294A1 (en) | 2005-10-20 | 2007-04-25 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | IL-15Ralpha sushi domain as a selective and potent enhancer of IL-15 action through IL-15Rbeta/gamma, and hyperagonist (IL15Ralpha sushi -IL15) fusion proteins |
| WO2009131730A2 (en) * | 2008-01-31 | 2009-10-29 | University Of Iowa Research Foundation | IMMUNOGENIC COMPOSITIONS FOR ACTIVATING γδ T CELLS |
| CA2860170C (en) | 2010-12-22 | 2022-06-14 | The Board Of Trustees Of The Leland Stanford Junior University | Superagonists and antagonists of interleukin-2 |
| PT2710123T (pt) * | 2011-05-19 | 2017-10-13 | Inst De Medicina Molecular | Linha celular de linfócitos compreendendo células t gama-delta, método de composição e produção resultante dos mesmos |
| EP3060059A4 (en) | 2013-10-25 | 2017-11-01 | Board of Regents, The University of Texas System | Polyclonal gamma delta t cells for immunotherapy |
| RU2739770C2 (ru) * | 2014-06-11 | 2020-12-28 | полибайосепт ГмбХ | Экспансия лимфоцитов с использованием композиции цитокинов для активной клеточной иммунотерапии |
| CN104293734B (zh) * | 2014-09-28 | 2018-01-09 | 上海云舜生物技术有限公司 | 一种人γδT细胞的制备方法 |
| CN104711224A (zh) * | 2015-01-09 | 2015-06-17 | 天津大学 | 一种提高人Vδ2T细胞扩增效率的体外培养方法及应用 |
| AU2016274633B2 (en) * | 2015-06-09 | 2022-04-21 | Gammadelta Therapeutics Ltd | Methods for the production of TCR gamma delta+ T cells |
| WO2016198906A1 (fr) * | 2015-06-10 | 2016-12-15 | Arcelormittal | Acier a haute résistance et procédé de fabrication |
-
2016
- 2016-10-31 WO PCT/EP2016/076264 patent/WO2017072367A1/en not_active Ceased
- 2016-10-31 KR KR1020257019399A patent/KR20250093576A/ko active Pending
- 2016-10-31 IL IL295838A patent/IL295838B2/en unknown
- 2016-10-31 PT PT167885391T patent/PT3368658T/pt unknown
- 2016-10-31 US US15/771,875 patent/US11618885B2/en active Active
- 2016-10-31 IL IL315329A patent/IL315329A/en unknown
- 2016-10-31 MY MYPI2018000604A patent/MY198084A/en unknown
- 2016-10-31 CN CN201680074800.5A patent/CN108473958A/zh active Pending
- 2016-10-31 DK DK16788539.1T patent/DK3368658T3/da active
- 2016-10-31 CA CA3003077A patent/CA3003077A1/en active Pending
- 2016-10-31 KR KR1020187015244A patent/KR102821381B1/ko active Active
- 2016-10-31 PL PL16788539.1T patent/PL3368658T3/pl unknown
- 2016-10-31 MX MX2018005207A patent/MX2018005207A/es unknown
- 2016-10-31 EP EP16788539.1A patent/EP3368658B1/en active Active
- 2016-10-31 EP EP22182997.1A patent/EP4148124A1/en active Pending
- 2016-10-31 JP JP2018541524A patent/JP2018533373A/ja active Pending
- 2016-10-31 AU AU2016344779A patent/AU2016344779B2/en active Active
- 2016-10-31 ES ES16788539T patent/ES2925261T3/es active Active
-
2018
- 2018-04-26 IL IL258985A patent/IL258985B2/en unknown
- 2018-04-26 MX MX2022011003A patent/MX2022011003A/es unknown
- 2018-04-30 PH PH12018500926A patent/PH12018500926A1/en unknown
-
2021
- 2021-09-10 JP JP2021147372A patent/JP7451468B2/ja active Active
-
2022
- 2022-09-29 US US17/936,811 patent/US20230099491A1/en active Pending
- 2022-12-09 AU AU2022283768A patent/AU2022283768A1/en active Pending
-
2024
- 2024-03-06 JP JP2024033438A patent/JP2024069306A/ja active Pending
Non-Patent Citations (1)
| Title |
|---|
| European Journal of Immunology (1997) 27(11):2885-2891. 1부.* * |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7451468B2 (ja) | 非造血組織常在性γδ T細胞の増幅および該細胞の使用 | |
| JP7698672B2 (ja) | ガンマデルタt細胞の増幅、組成物およびその使用 | |
| RU2784566C2 (ru) | РАЗМНОЖЕНИЕ И ПРИМЕНЕНИЕ НЕГЕМОПОЭТИЧЕСКИХ ТКАНЕРЕЗИДЕНТНЫХ γδ Т-КЛЕТОК | |
| HK40090397A (en) | Expansion of non-haematopoietic tissue-resident gamma delta t cells and uses of these cells | |
| HK1253954B (en) | Expansion of non-haematopoietic tissue-resident gamma delta t cells and uses of these cells | |
| BR112018008293B1 (pt) | Método in vitro para a expansão de células t gama delta não hematopoiéticas | |
| EA044224B1 (ru) | ЭКСПАНСИЯ γδ-T-КЛЕТОК, КОМПОЗИЦИИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | |
| EA049808B1 (ru) | ЭКСПАНСИЯ γΔ-Т-КЛЕТОК, КОМПОЗИЦИИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | |
| BR122025001918A2 (pt) | Métodos de expansão de células t gama delta, composições, seu uso e uso de células t gama delta expandidas |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| A201 | Request for examination | ||
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PA0104 | Divisional application for international application |
St.27 status event code: A-0-1-A10-A16-div-PA0104 |
|
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| G17 | Pta granted |
Free format text: ST27 STATUS EVENT CODE: A-4-4-G10-G17-TAD-PR1102 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| PR1102 | Extension of patent period due to registration delay |
St.27 status event code: A-4-4-G10-G17-tad-PR1102 Protection beyond ip right term event data comment text: Claim Total Quantity : 0, Period Limitation Text : 99 |