KR20170010893A - 아미노 말단 면역글로불린 융합 단백질 및 이의 조성물을 구축하는 방법 - Google Patents
아미노 말단 면역글로불린 융합 단백질 및 이의 조성물을 구축하는 방법 Download PDFInfo
- Publication number
- KR20170010893A KR20170010893A KR1020177000273A KR20177000273A KR20170010893A KR 20170010893 A KR20170010893 A KR 20170010893A KR 1020177000273 A KR1020177000273 A KR 1020177000273A KR 20177000273 A KR20177000273 A KR 20177000273A KR 20170010893 A KR20170010893 A KR 20170010893A
- Authority
- KR
- South Korea
- Prior art keywords
- immunoglobulin
- amino acid
- fusion protein
- acid sequence
- seq
- Prior art date
Links
- 108060003951 Immunoglobulin Proteins 0.000 title claims abstract description 1372
- 102000018358 immunoglobulin Human genes 0.000 title claims abstract description 1372
- 108020001507 fusion proteins Proteins 0.000 title claims abstract description 437
- 102000037865 fusion proteins Human genes 0.000 title claims abstract description 437
- 238000000034 method Methods 0.000 title claims abstract description 67
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 title claims abstract description 35
- 239000000203 mixture Substances 0.000 title abstract description 15
- 108090000765 processed proteins & peptides Proteins 0.000 claims abstract description 469
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 364
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 28
- 201000010099 disease Diseases 0.000 claims abstract description 14
- 238000011282 treatment Methods 0.000 claims abstract description 9
- 150000001413 amino acids Chemical group 0.000 claims description 289
- 102000006496 Immunoglobulin Heavy Chains Human genes 0.000 claims description 115
- 108010019476 Immunoglobulin Heavy Chains Proteins 0.000 claims description 115
- 102000013463 Immunoglobulin Light Chains Human genes 0.000 claims description 113
- 108010065825 Immunoglobulin Light Chains Proteins 0.000 claims description 113
- 230000000694 effects Effects 0.000 claims description 64
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical class C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 claims description 35
- 229960000575 trastuzumab Drugs 0.000 claims description 35
- 108060003199 Glucagon Proteins 0.000 claims description 33
- 102000051325 Glucagon Human genes 0.000 claims description 31
- 229960004666 glucagon Drugs 0.000 claims description 31
- 229960001519 exenatide Drugs 0.000 claims description 29
- 108010011459 Exenatide Proteins 0.000 claims description 28
- 206010012601 diabetes mellitus Diseases 0.000 claims description 25
- 108090000623 proteins and genes Proteins 0.000 claims description 24
- 239000004606 Fillers/Extenders Substances 0.000 claims description 22
- 208000008589 Obesity Diseases 0.000 claims description 19
- 235000020824 obesity Nutrition 0.000 claims description 19
- 208000035475 disorder Diseases 0.000 claims description 13
- 208000030159 metabolic disease Diseases 0.000 claims description 13
- 229940088597 hormone Drugs 0.000 claims description 12
- 239000005556 hormone Substances 0.000 claims description 12
- 229940039781 leptin Drugs 0.000 claims description 12
- 150000007523 nucleic acids Chemical class 0.000 claims description 12
- 229960000402 palivizumab Drugs 0.000 claims description 12
- 108010092277 Leptin Proteins 0.000 claims description 11
- 102000016267 Leptin Human genes 0.000 claims description 11
- 239000013604 expression vector Substances 0.000 claims description 11
- 230000014509 gene expression Effects 0.000 claims description 9
- 108020004707 nucleic acids Proteins 0.000 claims description 8
- 102000039446 nucleic acids Human genes 0.000 claims description 8
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 claims description 7
- 208000002193 Pain Diseases 0.000 claims description 6
- 238000004113 cell culture Methods 0.000 claims description 6
- 150000001875 compounds Chemical class 0.000 claims description 6
- 206010019280 Heart failures Diseases 0.000 claims description 5
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 5
- 239000003795 chemical substances by application Substances 0.000 claims description 5
- 239000008194 pharmaceutical composition Substances 0.000 claims description 5
- 208000023275 Autoimmune disease Diseases 0.000 claims description 4
- 102000004877 Insulin Human genes 0.000 claims description 4
- 108090001061 Insulin Proteins 0.000 claims description 4
- 101710138657 Neurotoxin Proteins 0.000 claims description 4
- 230000002757 inflammatory effect Effects 0.000 claims description 4
- 229940125396 insulin Drugs 0.000 claims description 4
- 210000004962 mammalian cell Anatomy 0.000 claims description 4
- 239000002581 neurotoxin Substances 0.000 claims description 4
- 231100000618 neurotoxin Toxicity 0.000 claims description 4
- 208000011580 syndromic disease Diseases 0.000 claims description 4
- 208000007342 Diabetic Nephropathies Diseases 0.000 claims description 3
- 206010016654 Fibrosis Diseases 0.000 claims description 3
- 208000033679 diabetic kidney disease Diseases 0.000 claims description 3
- 230000004761 fibrosis Effects 0.000 claims description 3
- 210000000056 organ Anatomy 0.000 claims description 3
- 208000004476 Acute Coronary Syndrome Diseases 0.000 claims description 2
- 206010003658 Atrial Fibrillation Diseases 0.000 claims description 2
- 108010088406 Glucagon-Like Peptides Proteins 0.000 claims description 2
- 229940089838 Glucagon-like peptide 1 receptor agonist Drugs 0.000 claims description 2
- 206010020772 Hypertension Diseases 0.000 claims description 2
- 208000032382 Ischaemic stroke Diseases 0.000 claims description 2
- 102000004257 Potassium Channel Human genes 0.000 claims description 2
- 101000844197 Scolopendra subspinipes Mu-scoloptoxin(03)-Ssm2a Proteins 0.000 claims description 2
- 201000009594 Systemic Scleroderma Diseases 0.000 claims description 2
- 206010042953 Systemic sclerosis Diseases 0.000 claims description 2
- 208000029078 coronary artery disease Diseases 0.000 claims description 2
- 239000003877 glucagon like peptide 1 receptor agonist Substances 0.000 claims description 2
- 230000035876 healing Effects 0.000 claims description 2
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 2
- 208000007232 portal hypertension Diseases 0.000 claims description 2
- 108020001213 potassium channel Proteins 0.000 claims description 2
- 201000011461 pre-eclampsia Diseases 0.000 claims description 2
- 230000010410 reperfusion Effects 0.000 claims description 2
- 230000029663 wound healing Effects 0.000 claims description 2
- 208000020221 Short stature Diseases 0.000 claims 2
- 238000004519 manufacturing process Methods 0.000 claims 2
- 208000031229 Cardiomyopathies Diseases 0.000 claims 1
- 101710156545 Kappa-theraphotoxin-Tb1a Proteins 0.000 claims 1
- 206010049287 Lipodystrophy acquired Diseases 0.000 claims 1
- 102400000319 Oxyntomodulin Human genes 0.000 claims 1
- 101800001388 Oxyntomodulin Proteins 0.000 claims 1
- 108090000103 Relaxin Proteins 0.000 claims 1
- 102000003743 Relaxin Human genes 0.000 claims 1
- 230000002612 cardiopulmonary effect Effects 0.000 claims 1
- 208000006575 hypertriglyceridemia Diseases 0.000 claims 1
- 208000028867 ischemia Diseases 0.000 claims 1
- 208000006132 lipodystrophy Diseases 0.000 claims 1
- 108010002755 mokatoxin-1 Proteins 0.000 claims 1
- 230000001902 propagating effect Effects 0.000 claims 1
- 108010087851 prorelaxin Proteins 0.000 claims 1
- 230000005070 ripening Effects 0.000 claims 1
- 102000004196 processed proteins & peptides Human genes 0.000 abstract description 85
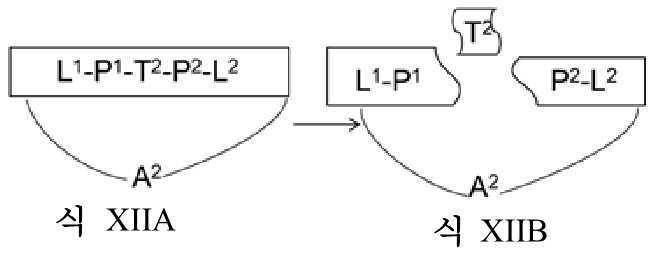
- 230000006337 proteolytic cleavage Effects 0.000 abstract description 24
- 230000002265 prevention Effects 0.000 abstract 1
- 125000003275 alpha amino acid group Chemical group 0.000 description 477
- 239000002773 nucleotide Substances 0.000 description 342
- 125000003729 nucleotide group Chemical group 0.000 description 342
- 235000001014 amino acid Nutrition 0.000 description 250
- 229940024606 amino acid Drugs 0.000 description 243
- 230000004927 fusion Effects 0.000 description 153
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 85
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 85
- 206010057190 Respiratory tract infections Diseases 0.000 description 78
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 62
- 229940027941 immunoglobulin g Drugs 0.000 description 56
- 125000005647 linker group Chemical group 0.000 description 41
- 108091028043 Nucleic acid sequence Proteins 0.000 description 33
- 239000002585 base Substances 0.000 description 32
- 229940072221 immunoglobulins Drugs 0.000 description 27
- JUFFVKRROAPVBI-PVOYSMBESA-N chembl1210015 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(=O)N[C@H]1[C@@H]([C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO[C@]3(O[C@@H](C[C@H](O)[C@H](O)CO)[C@H](NC(C)=O)[C@@H](O)C3)C(O)=O)O2)O)[C@@H](CO)O1)NC(C)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 JUFFVKRROAPVBI-PVOYSMBESA-N 0.000 description 24
- 238000006467 substitution reaction Methods 0.000 description 24
- 230000000840 anti-viral effect Effects 0.000 description 21
- 230000000844 anti-bacterial effect Effects 0.000 description 18
- 230000000843 anti-fungal effect Effects 0.000 description 18
- 230000002141 anti-parasite Effects 0.000 description 18
- 239000003096 antiparasitic agent Substances 0.000 description 18
- 102000035195 Peptidases Human genes 0.000 description 15
- 108091005804 Peptidases Proteins 0.000 description 15
- 239000004365 Protease Substances 0.000 description 15
- 230000003213 activating effect Effects 0.000 description 15
- 230000009977 dual effect Effects 0.000 description 15
- 235000019419 proteases Nutrition 0.000 description 15
- 210000004027 cell Anatomy 0.000 description 14
- 229960001521 motavizumab Drugs 0.000 description 12
- 239000003814 drug Substances 0.000 description 11
- 239000012634 fragment Substances 0.000 description 11
- 230000007062 hydrolysis Effects 0.000 description 11
- 238000006460 hydrolysis reaction Methods 0.000 description 11
- NRYBAZVQPHGZNS-ZSOCWYAHSA-N leptin Chemical compound O=C([C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](N)CC(C)C)CCSC)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](CS)C(O)=O NRYBAZVQPHGZNS-ZSOCWYAHSA-N 0.000 description 10
- 229960002915 nebacumab Drugs 0.000 description 10
- 235000018102 proteins Nutrition 0.000 description 10
- 102000004169 proteins and genes Human genes 0.000 description 10
- 102000005962 receptors Human genes 0.000 description 10
- 108020003175 receptors Proteins 0.000 description 10
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 9
- 241000700605 Viruses Species 0.000 description 9
- 239000000758 substrate Substances 0.000 description 9
- 108091008874 T cell receptors Proteins 0.000 description 8
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 8
- 239000000427 antigen Substances 0.000 description 8
- 108091007433 antigens Proteins 0.000 description 8
- 102000036639 antigens Human genes 0.000 description 8
- 241000222120 Candida <Saccharomycetales> Species 0.000 description 7
- 108010086246 Glucagon-Like Peptide-1 Receptor Proteins 0.000 description 7
- 102000007446 Glucagon-Like Peptide-1 Receptor Human genes 0.000 description 7
- 238000003776 cleavage reaction Methods 0.000 description 7
- 230000007017 scission Effects 0.000 description 7
- 108010063919 Glucagon Receptors Proteins 0.000 description 6
- 102100040890 Glucagon receptor Human genes 0.000 description 6
- 102000012745 Immunoglobulin Subunits Human genes 0.000 description 6
- 108010079585 Immunoglobulin Subunits Proteins 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 229940124597 therapeutic agent Drugs 0.000 description 6
- 241000194033 Enterococcus Species 0.000 description 5
- 102100040918 Pro-glucagon Human genes 0.000 description 5
- 241000589517 Pseudomonas aeruginosa Species 0.000 description 5
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 5
- 150000003384 small molecules Chemical class 0.000 description 5
- BXTJCSYMGFJEID-XMTADJHZSA-N (2s)-2-[[(2r,3r)-3-[(2s)-1-[(3r,4s,5s)-4-[[(2s)-2-[[(2s)-2-[6-[3-[(2r)-2-amino-2-carboxyethyl]sulfanyl-2,5-dioxopyrrolidin-1-yl]hexanoyl-methylamino]-3-methylbutanoyl]amino]-3-methylbutanoyl]-methylamino]-3-methoxy-5-methylheptanoyl]pyrrolidin-2-yl]-3-met Chemical compound C([C@H](NC(=O)[C@H](C)[C@@H](OC)[C@@H]1CCCN1C(=O)C[C@H]([C@H]([C@@H](C)CC)N(C)C(=O)[C@@H](NC(=O)[C@H](C(C)C)N(C)C(=O)CCCCCN1C(C(SC[C@H](N)C(O)=O)CC1=O)=O)C(C)C)OC)C(O)=O)C1=CC=CC=C1 BXTJCSYMGFJEID-XMTADJHZSA-N 0.000 description 4
- 108010075254 C-Peptide Proteins 0.000 description 4
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 4
- 108090000376 Fibroblast growth factor 21 Proteins 0.000 description 4
- 102000003973 Fibroblast growth factor 21 Human genes 0.000 description 4
- 102100039619 Granulocyte colony-stimulating factor Human genes 0.000 description 4
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 4
- 101000746367 Homo sapiens Granulocyte colony-stimulating factor Proteins 0.000 description 4
- 101000746373 Homo sapiens Granulocyte-macrophage colony-stimulating factor Proteins 0.000 description 4
- 101000878602 Homo sapiens Immunoglobulin alpha Fc receptor Proteins 0.000 description 4
- 102100038005 Immunoglobulin alpha Fc receptor Human genes 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 241000607626 Vibrio cholerae Species 0.000 description 4
- 125000000539 amino acid group Chemical group 0.000 description 4
- 229950011109 edobacomab Drugs 0.000 description 4
- 239000000499 gel Substances 0.000 description 4
- 210000004698 lymphocyte Anatomy 0.000 description 4
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 4
- 102000009840 Angiopoietins Human genes 0.000 description 3
- 108010009906 Angiopoietins Proteins 0.000 description 3
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 3
- 108050005493 CD3 protein, epsilon/gamma/delta subunit Proteins 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- 102000003951 Erythropoietin Human genes 0.000 description 3
- 108090000394 Erythropoietin Proteins 0.000 description 3
- HTQBXNHDCUEHJF-XWLPCZSASA-N Exenatide Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 HTQBXNHDCUEHJF-XWLPCZSASA-N 0.000 description 3
- 101710198884 GATA-type zinc finger protein 1 Proteins 0.000 description 3
- DTHNMHAUYICORS-KTKZVXAJSA-N Glucagon-like peptide 1 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 DTHNMHAUYICORS-KTKZVXAJSA-N 0.000 description 3
- 241000590002 Helicobacter pylori Species 0.000 description 3
- 102000014150 Interferons Human genes 0.000 description 3
- 108010050904 Interferons Proteins 0.000 description 3
- 102000015696 Interleukins Human genes 0.000 description 3
- 108010063738 Interleukins Proteins 0.000 description 3
- 102100029204 Low affinity immunoglobulin gamma Fc region receptor II-a Human genes 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 241001480233 Paragonimus Species 0.000 description 3
- 241000223960 Plasmodium falciparum Species 0.000 description 3
- 241000700159 Rattus Species 0.000 description 3
- 206010049416 Short-bowel syndrome Diseases 0.000 description 3
- 241000191967 Staphylococcus aureus Species 0.000 description 3
- 210000001744 T-lymphocyte Anatomy 0.000 description 3
- 108010067390 Viral Proteins Proteins 0.000 description 3
- 230000001093 anti-cancer Effects 0.000 description 3
- 229960000455 brentuximab vedotin Drugs 0.000 description 3
- 238000012217 deletion Methods 0.000 description 3
- 230000037430 deletion Effects 0.000 description 3
- 229940105423 erythropoietin Drugs 0.000 description 3
- 208000019622 heart disease Diseases 0.000 description 3
- 229950010245 ibalizumab Drugs 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- OXCMYAYHXIHQOA-UHFFFAOYSA-N potassium;[2-butyl-5-chloro-3-[[4-[2-(1,2,4-triaza-3-azanidacyclopenta-1,4-dien-5-yl)phenyl]phenyl]methyl]imidazol-4-yl]methanol Chemical compound [K+].CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C2=N[N-]N=N2)C=C1 OXCMYAYHXIHQOA-UHFFFAOYSA-N 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 239000003053 toxin Substances 0.000 description 3
- 231100000765 toxin Toxicity 0.000 description 3
- 108700012359 toxins Proteins 0.000 description 3
- 108010068327 4-hydroxyphenylpyruvate dioxygenase Proteins 0.000 description 2
- 241000589155 Agrobacterium tumefaciens Species 0.000 description 2
- 108010083359 Antigen Receptors Proteins 0.000 description 2
- 102000006306 Antigen Receptors Human genes 0.000 description 2
- 241000193738 Bacillus anthracis Species 0.000 description 2
- 241000193755 Bacillus cereus Species 0.000 description 2
- 244000063299 Bacillus subtilis Species 0.000 description 2
- 235000014469 Bacillus subtilis Nutrition 0.000 description 2
- 241000588832 Bordetella pertussis Species 0.000 description 2
- 241000193764 Brevibacillus brevis Species 0.000 description 2
- 241000222122 Candida albicans Species 0.000 description 2
- 241001327965 Clonorchis sinensis Species 0.000 description 2
- 241000193163 Clostridioides difficile Species 0.000 description 2
- 241000186227 Corynebacterium diphtheriae Species 0.000 description 2
- 241000223935 Cryptosporidium Species 0.000 description 2
- 208000032131 Diabetic Neuropathies Diseases 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- 241000194032 Enterococcus faecalis Species 0.000 description 2
- 241000588724 Escherichia coli Species 0.000 description 2
- 108010087819 Fc receptors Proteins 0.000 description 2
- 102000009109 Fc receptors Human genes 0.000 description 2
- 241000589602 Francisella tularensis Species 0.000 description 2
- 241000605986 Fusobacterium nucleatum Species 0.000 description 2
- 241000207201 Gardnerella vaginalis Species 0.000 description 2
- 102000006395 Globulins Human genes 0.000 description 2
- 108010044091 Globulins Proteins 0.000 description 2
- 241000606768 Haemophilus influenzae Species 0.000 description 2
- 101000917826 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-a Proteins 0.000 description 2
- 101000917824 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-b Proteins 0.000 description 2
- 101000917839 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-B Proteins 0.000 description 2
- 101000869643 Homo sapiens Relaxin receptor 1 Proteins 0.000 description 2
- 101000869654 Homo sapiens Relaxin receptor 2 Proteins 0.000 description 2
- 102000002265 Human Growth Hormone Human genes 0.000 description 2
- 108010000521 Human Growth Hormone Proteins 0.000 description 2
- 239000000854 Human Growth Hormone Substances 0.000 description 2
- 108010073816 IgE Receptors Proteins 0.000 description 2
- 102000009438 IgE Receptors Human genes 0.000 description 2
- 108010073807 IgG Receptors Proteins 0.000 description 2
- 102000009490 IgG Receptors Human genes 0.000 description 2
- 102000003815 Interleukin-11 Human genes 0.000 description 2
- 108090000177 Interleukin-11 Proteins 0.000 description 2
- 102100030704 Interleukin-21 Human genes 0.000 description 2
- 102000004890 Interleukin-8 Human genes 0.000 description 2
- 108090001007 Interleukin-8 Proteins 0.000 description 2
- 241000235058 Komagataella pastoris Species 0.000 description 2
- 102100029193 Low affinity immunoglobulin gamma Fc region receptor III-A Human genes 0.000 description 2
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 241000498270 Necator americanus Species 0.000 description 2
- 241000242716 Opisthorchis Species 0.000 description 2
- 241000606860 Pasteurella Species 0.000 description 2
- 241000235645 Pichia kudriavzevii Species 0.000 description 2
- 241000605862 Porphyromonas gingivalis Species 0.000 description 2
- 241001135223 Prevotella melaninogenica Species 0.000 description 2
- 102100032444 Relaxin receptor 1 Human genes 0.000 description 2
- 102100032445 Relaxin receptor 2 Human genes 0.000 description 2
- 241001473628 Sarcocystis suihominis Species 0.000 description 2
- 241000242678 Schistosoma Species 0.000 description 2
- 241000235347 Schizosaccharomyces pombe Species 0.000 description 2
- 241000191963 Staphylococcus epidermidis Species 0.000 description 2
- 241000122973 Stenotrophomonas maltophilia Species 0.000 description 2
- 241000193998 Streptococcus pneumoniae Species 0.000 description 2
- 102100021669 Stromal cell-derived factor 1 Human genes 0.000 description 2
- 241000244031 Toxocara Species 0.000 description 2
- 241000607598 Vibrio Species 0.000 description 2
- 241000222126 [Candida] glabrata Species 0.000 description 2
- 230000002159 abnormal effect Effects 0.000 description 2
- 229940049595 antibody-drug conjugate Drugs 0.000 description 2
- 210000000628 antibody-producing cell Anatomy 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 229940065181 bacillus anthracis Drugs 0.000 description 2
- 229960001212 bacterial vaccine Drugs 0.000 description 2
- 210000002798 bone marrow cell Anatomy 0.000 description 2
- 208000032343 candida glabrata infection Diseases 0.000 description 2
- 230000007910 cell fusion Effects 0.000 description 2
- 238000007385 chemical modification Methods 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 238000012258 culturing Methods 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 208000016097 disease of metabolism Diseases 0.000 description 2
- 229950002209 efungumab Drugs 0.000 description 2
- 229940032049 enterococcus faecalis Drugs 0.000 description 2
- 229960003276 erythromycin Drugs 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- 229940047650 haemophilus influenzae Drugs 0.000 description 2
- 229940037467 helicobacter pylori Drugs 0.000 description 2
- 201000001421 hyperglycemia Diseases 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 229940047124 interferons Drugs 0.000 description 2
- 229940074383 interleukin-11 Drugs 0.000 description 2
- 108010074108 interleukin-21 Proteins 0.000 description 2
- 229940096397 interleukin-8 Drugs 0.000 description 2
- XKTZWUACRZHVAN-VADRZIEHSA-N interleukin-8 Chemical compound C([C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](NC(C)=O)CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCSC)C(=O)N1[C@H](CCC1)C(=O)N1[C@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC(O)=CC=1)C(=O)N[C@H](CO)C(=O)N1[C@H](CCC1)C(N)=O)C1=CC=CC=C1 XKTZWUACRZHVAN-VADRZIEHSA-N 0.000 description 2
- 210000003041 ligament Anatomy 0.000 description 2
- 229950003526 lorvotuzumab mertansine Drugs 0.000 description 2
- 210000002540 macrophage Anatomy 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 210000000822 natural killer cell Anatomy 0.000 description 2
- 210000000440 neutrophil Anatomy 0.000 description 2
- 229950003570 panobacumab Drugs 0.000 description 2
- 229960004910 raxibacumab Drugs 0.000 description 2
- 239000000018 receptor agonist Substances 0.000 description 2
- 229940044601 receptor agonist Drugs 0.000 description 2
- 230000000241 respiratory effect Effects 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 229940031000 streptococcus pneumoniae Drugs 0.000 description 2
- 230000002889 sympathetic effect Effects 0.000 description 2
- 229950001788 tefibazumab Drugs 0.000 description 2
- 229960001612 trastuzumab emtansine Drugs 0.000 description 2
- MFZSNESUTRVBQX-XEURHVNRSA-N (2S)-2-amino-6-[4-[[3-[[(2S)-1-[[(1S,2R,3S,5S,6S,16E,18E,20R,21S)-11-chloro-21-hydroxy-12,20-dimethoxy-2,5,9,16-tetramethyl-8,23-dioxo-4,24-dioxa-9,22-diazatetracyclo[19.3.1.110,14.03,5]hexacosa-10,12,14(26),16,18-pentaen-6-yl]oxy]-1-oxopropan-2-yl]-methylamino]-3-oxopropyl]disulfanyl]pentanoylamino]hexanoic acid Chemical compound CO[C@@H]1\C=C\C=C(C)\Cc2cc(OC)c(Cl)c(c2)N(C)C(=O)C[C@H](OC(=O)[C@H](C)N(C)C(=O)CCSSC(C)CCC(=O)NCCCC[C@H](N)C(O)=O)[C@]2(C)O[C@H]2[C@H](C)[C@@H]2C[C@@]1(O)NC(=O)O2 MFZSNESUTRVBQX-XEURHVNRSA-N 0.000 description 1
- KREXTMSNGTWUJT-YWPYICTPSA-N 2-[[2-[[(2r,3s,5r)-3-[[2-(carboxymethylamino)-2-oxoethyl]carbamoyloxy]-5-[2-(2-methylpropanoylamino)-6-oxo-3h-purin-9-yl]oxolan-2-yl]methoxycarbonylamino]acetyl]amino]acetic acid Chemical compound C1=NC=2C(=O)NC(NC(=O)C(C)C)=NC=2N1[C@H]1C[C@H](OC(=O)NCC(=O)NCC(O)=O)[C@@H](COC(=O)NCC(=O)NCC(O)=O)O1 KREXTMSNGTWUJT-YWPYICTPSA-N 0.000 description 1
- GOJUJUVQIVIZAV-UHFFFAOYSA-N 2-amino-4,6-dichloropyrimidine-5-carbaldehyde Chemical group NC1=NC(Cl)=C(C=O)C(Cl)=N1 GOJUJUVQIVIZAV-UHFFFAOYSA-N 0.000 description 1
- PCFGFYKGPMQDBX-FEKONODYSA-N 78355-50-7 Chemical compound C([C@@H](C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)NCC(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC(C)C)C(O)=O)NC(=O)CNC(=O)CNC(=O)[C@@H](N)CC=1C=CC(O)=CC=1)C1=CC=CC=C1 PCFGFYKGPMQDBX-FEKONODYSA-N 0.000 description 1
- 241000224422 Acanthamoeba Species 0.000 description 1
- 241000023308 Acca Species 0.000 description 1
- 240000000073 Achillea millefolium Species 0.000 description 1
- 235000007754 Achillea millefolium Nutrition 0.000 description 1
- 241000605281 Anaplasma phagocytophilum Species 0.000 description 1
- 241000498253 Ancylostoma duodenale Species 0.000 description 1
- 241000359199 Angiostrongylus costaricensis Species 0.000 description 1
- 241000244023 Anisakis Species 0.000 description 1
- 241000700607 Archiacanthocephala Species 0.000 description 1
- 241000238888 Argasidae Species 0.000 description 1
- 241000244186 Ascaris Species 0.000 description 1
- 241000244185 Ascaris lumbricoides Species 0.000 description 1
- 206010061666 Autonomic neuropathy Diseases 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- 241000894009 Azorhizobium caulinodans Species 0.000 description 1
- 241000223836 Babesia Species 0.000 description 1
- 241000223840 Babesia bigemina Species 0.000 description 1
- 241001455947 Babesia divergens Species 0.000 description 1
- 241001648338 Babesia duncani Species 0.000 description 1
- 241000193830 Bacillus <bacterium> Species 0.000 description 1
- 241000193388 Bacillus thuringiensis Species 0.000 description 1
- 108010077805 Bacterial Proteins Proteins 0.000 description 1
- 241000606124 Bacteroides fragilis Species 0.000 description 1
- 241000934146 Balamuthia mandrillaris Species 0.000 description 1
- 241001235572 Balantioides coli Species 0.000 description 1
- 241000606108 Bartonella quintana Species 0.000 description 1
- 241000244183 Baylisascaris procyonis Species 0.000 description 1
- 241001284802 Bertiella <tapeworm> Species 0.000 description 1
- 241001284800 Bertiella studeri Species 0.000 description 1
- 241000726108 Blastocystis Species 0.000 description 1
- 241000588779 Bordetella bronchiseptica Species 0.000 description 1
- 241000589968 Borrelia Species 0.000 description 1
- 241000589969 Borreliella burgdorferi Species 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- 244000027711 Brettanomyces bruxellensis Species 0.000 description 1
- 235000000287 Brettanomyces bruxellensis Nutrition 0.000 description 1
- 241000589567 Brucella abortus Species 0.000 description 1
- 241001148106 Brucella melitensis Species 0.000 description 1
- 241001148111 Brucella suis Species 0.000 description 1
- 241000244038 Brugia malayi Species 0.000 description 1
- 241000143302 Brugia timori Species 0.000 description 1
- 241000589513 Burkholderia cepacia Species 0.000 description 1
- 241000722910 Burkholderia mallei Species 0.000 description 1
- 241001136175 Burkholderia pseudomallei Species 0.000 description 1
- 102100025221 CD70 antigen Human genes 0.000 description 1
- 229940126609 CR6261 Drugs 0.000 description 1
- 241000257161 Calliphoridae Species 0.000 description 1
- 241000589877 Campylobacter coli Species 0.000 description 1
- 241000589874 Campylobacter fetus Species 0.000 description 1
- 241000589875 Campylobacter jejuni Species 0.000 description 1
- 101100495352 Candida albicans CDR4 gene Proteins 0.000 description 1
- 244000206911 Candida holmii Species 0.000 description 1
- 235000002965 Candida holmii Nutrition 0.000 description 1
- 241000222173 Candida parapsilosis Species 0.000 description 1
- 241000222178 Candida tropicalis Species 0.000 description 1
- 241000222157 Candida viswanathii Species 0.000 description 1
- 241000282465 Canis Species 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 241000242722 Cestoda Species 0.000 description 1
- 108010008951 Chemokine CXCL12 Proteins 0.000 description 1
- 241001647372 Chlamydia pneumoniae Species 0.000 description 1
- 241001647378 Chlamydia psittaci Species 0.000 description 1
- 241000606153 Chlamydia trachomatis Species 0.000 description 1
- 101710164760 Chlorotoxin Proteins 0.000 description 1
- 241000251730 Chondrichthyes Species 0.000 description 1
- 241001327638 Cimex lectularius Species 0.000 description 1
- 241001327942 Clonorchis Species 0.000 description 1
- 241000193155 Clostridium botulinum Species 0.000 description 1
- 241000202814 Cochliomyia hominivorax Species 0.000 description 1
- 241001634499 Cola Species 0.000 description 1
- 241000606678 Coxiella burnetii Species 0.000 description 1
- 208000019736 Cranial nerve disease Diseases 0.000 description 1
- 241000938605 Crocodylia Species 0.000 description 1
- 241000270311 Crocodylus niloticus Species 0.000 description 1
- 201000007336 Cryptococcosis Diseases 0.000 description 1
- 241001522864 Cryptococcus gattii VGI Species 0.000 description 1
- 241000221204 Cryptococcus neoformans Species 0.000 description 1
- 201000003808 Cystic echinococcosis Diseases 0.000 description 1
- 241000205707 Cystoisospora belli Species 0.000 description 1
- 241000701022 Cytomegalovirus Species 0.000 description 1
- 241001218273 Demodex brevis Species 0.000 description 1
- 241000193880 Demodex folliculorum Species 0.000 description 1
- 241000202828 Dermatobia hominis Species 0.000 description 1
- 208000001380 Diabetic Ketoacidosis Diseases 0.000 description 1
- 208000032781 Diabetic cardiomyopathy Diseases 0.000 description 1
- 208000008960 Diabetic foot Diseases 0.000 description 1
- 206010012689 Diabetic retinopathy Diseases 0.000 description 1
- 241000577456 Dicrocoelium dendriticum Species 0.000 description 1
- 241000157306 Dientamoeba fragilis Species 0.000 description 1
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 1
- 241000690786 Dioctophyme renale Species 0.000 description 1
- 241000866683 Diphyllobothrium latum Species 0.000 description 1
- 241001319090 Dracunculus medinensis Species 0.000 description 1
- 101150029707 ERBB2 gene Proteins 0.000 description 1
- 241000244170 Echinococcus granulosus Species 0.000 description 1
- 241000244163 Echinococcus multilocularis Species 0.000 description 1
- 241000244162 Echinococcus oligarthrus Species 0.000 description 1
- 241000244165 Echinococcus vogeli Species 0.000 description 1
- 241001126301 Echinostoma Species 0.000 description 1
- 241000224432 Entamoeba histolytica Species 0.000 description 1
- 241000588914 Enterobacter Species 0.000 description 1
- 241000588697 Enterobacter cloacae Species 0.000 description 1
- 241000498256 Enterobius Species 0.000 description 1
- 241000498255 Enterobius vermicularis Species 0.000 description 1
- 241000194031 Enterococcus faecium Species 0.000 description 1
- 241000204939 Fasciola gigantica Species 0.000 description 1
- 241000242711 Fasciola hepatica Species 0.000 description 1
- 241001126302 Fasciolopsis buski Species 0.000 description 1
- 108010021468 Fc gamma receptor IIA Proteins 0.000 description 1
- 108010021472 Fc gamma receptor IIB Proteins 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- 241000239183 Filaria Species 0.000 description 1
- 241001621835 Frateuria aurantia Species 0.000 description 1
- 108010058643 Fungal Proteins Proteins 0.000 description 1
- 241000224467 Giardia intestinalis Species 0.000 description 1
- 101800000221 Glucagon-like peptide 2 Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 206010018429 Glucose tolerance impaired Diseases 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 241000497087 Gnathostoma hispidum Species 0.000 description 1
- 241001276383 Gnathostoma spinigerum Species 0.000 description 1
- 201000005569 Gout Diseases 0.000 description 1
- 102100040898 Growth/differentiation factor 11 Human genes 0.000 description 1
- 241000606766 Haemophilus parainfluenzae Species 0.000 description 1
- 241000196812 Halicephalobus gingivalis Species 0.000 description 1
- 206010019708 Hepatic steatosis Diseases 0.000 description 1
- 102100026122 High affinity immunoglobulin gamma Fc receptor I Human genes 0.000 description 1
- 101000934356 Homo sapiens CD70 antigen Proteins 0.000 description 1
- 101100114967 Homo sapiens CSF3 gene Proteins 0.000 description 1
- 101000737793 Homo sapiens Cerebellar degeneration-related antigen 1 Proteins 0.000 description 1
- 101000737796 Homo sapiens Cerebellar degeneration-related protein 2 Proteins 0.000 description 1
- 101000987586 Homo sapiens Eosinophil peroxidase Proteins 0.000 description 1
- 101000920686 Homo sapiens Erythropoietin Proteins 0.000 description 1
- 101000846529 Homo sapiens Fibroblast growth factor 21 Proteins 0.000 description 1
- 101000893545 Homo sapiens Growth/differentiation factor 11 Proteins 0.000 description 1
- 101000913074 Homo sapiens High affinity immunoglobulin gamma Fc receptor I Proteins 0.000 description 1
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 1
- 101001135770 Homo sapiens Parathyroid hormone Proteins 0.000 description 1
- 101001039966 Homo sapiens Pro-glucagon Proteins 0.000 description 1
- 101001135995 Homo sapiens Probable peptidyl-tRNA hydrolase Proteins 0.000 description 1
- 101000946860 Homo sapiens T-cell surface glycoprotein CD3 epsilon chain Proteins 0.000 description 1
- 241000725303 Human immunodeficiency virus Species 0.000 description 1
- 241000244166 Hymenolepis diminuta Species 0.000 description 1
- 241001464384 Hymenolepis nana Species 0.000 description 1
- 108010042653 IgA receptor Proteins 0.000 description 1
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 1
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 1
- 102000018071 Immunoglobulin Fc Fragments Human genes 0.000 description 1
- 108010091135 Immunoglobulin Fc Fragments Proteins 0.000 description 1
- 229940123993 Incretin mimetic Drugs 0.000 description 1
- 101000668058 Infectious salmon anemia virus (isolate Atlantic salmon/Norway/810/9/99) RNA-directed RNA polymerase catalytic subunit Proteins 0.000 description 1
- 241001500351 Influenzavirus A Species 0.000 description 1
- 241001500350 Influenzavirus B Species 0.000 description 1
- 241001500343 Influenzavirus C Species 0.000 description 1
- 102000006992 Interferon-alpha Human genes 0.000 description 1
- 108010047761 Interferon-alpha Proteins 0.000 description 1
- 102000003996 Interferon-beta Human genes 0.000 description 1
- 108090000467 Interferon-beta Proteins 0.000 description 1
- 241001661732 Isavirus Species 0.000 description 1
- 206010023076 Isosporiasis Diseases 0.000 description 1
- 241000238889 Ixodidae Species 0.000 description 1
- 241001534216 Klebsiella granulomatis Species 0.000 description 1
- 241000588747 Klebsiella pneumoniae Species 0.000 description 1
- 102000007330 LDL Lipoproteins Human genes 0.000 description 1
- 240000001046 Lactobacillus acidophilus Species 0.000 description 1
- 235000013956 Lactobacillus acidophilus Nutrition 0.000 description 1
- 241000194041 Lactococcus lactis subsp. lactis Species 0.000 description 1
- 241000589242 Legionella pneumophila Species 0.000 description 1
- 241000222722 Leishmania <genus> Species 0.000 description 1
- GSDSWSVVBLHKDQ-JTQLQIEISA-N Levofloxacin Chemical compound C([C@@H](N1C2=C(C(C(C(O)=O)=C1)=O)C=C1F)C)OC2=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-JTQLQIEISA-N 0.000 description 1
- 241001541122 Linguatula serrata Species 0.000 description 1
- 241000186779 Listeria monocytogenes Species 0.000 description 1
- 102100029205 Low affinity immunoglobulin gamma Fc region receptor II-b Human genes 0.000 description 1
- 101710099301 Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 1
- 208000016604 Lyme disease Diseases 0.000 description 1
- 206010054805 Macroangiopathy Diseases 0.000 description 1
- 241000022705 Mansonella streptocerca Species 0.000 description 1
- 241001660194 Metagonimus yokogawai Species 0.000 description 1
- 241000202974 Methanobacterium Species 0.000 description 1
- 241000235048 Meyerozyma guilliermondii Species 0.000 description 1
- 241001467578 Microbacterium Species 0.000 description 1
- 241000192041 Micrococcus Species 0.000 description 1
- 241000191938 Micrococcus luteus Species 0.000 description 1
- 241000700602 Moniliformis moniliformis Species 0.000 description 1
- 241000588655 Moraxella catarrhalis Species 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000187481 Mycobacterium phlei Species 0.000 description 1
- 241000187480 Mycobacterium smegmatis Species 0.000 description 1
- 241000187479 Mycobacterium tuberculosis Species 0.000 description 1
- 241000204031 Mycoplasma Species 0.000 description 1
- 241000204051 Mycoplasma genitalium Species 0.000 description 1
- 241000204048 Mycoplasma hominis Species 0.000 description 1
- 241000202944 Mycoplasma sp. Species 0.000 description 1
- 241000224438 Naegleria fowleri Species 0.000 description 1
- 241000588652 Neisseria gonorrhoeae Species 0.000 description 1
- 241000588650 Neisseria meningitidis Species 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 241000158589 Oestroidea Species 0.000 description 1
- 241000243985 Onchocerca volvulus Species 0.000 description 1
- 241001324821 Opisthorchis felineus Species 0.000 description 1
- 241000702244 Orthoreovirus Species 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 241000057252 Paragonimus africanus Species 0.000 description 1
- 241000551217 Paragonimus caliensis Species 0.000 description 1
- 241001446258 Paragonimus kellicotti Species 0.000 description 1
- 241000610664 Paragonimus skrjabini Species 0.000 description 1
- 241001480234 Paragonimus westermani Species 0.000 description 1
- 208000002606 Paramyxoviridae Infections Diseases 0.000 description 1
- 102000003982 Parathyroid hormone Human genes 0.000 description 1
- 108090000445 Parathyroid hormone Proteins 0.000 description 1
- 241000606856 Pasteurella multocida Species 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- 241000517307 Pediculus humanus Species 0.000 description 1
- 241000517306 Pediculus humanus corporis Species 0.000 description 1
- 241000191992 Peptostreptococcus Species 0.000 description 1
- 201000005702 Pertussis Diseases 0.000 description 1
- 241000709664 Picornaviridae Species 0.000 description 1
- 241000224016 Plasmodium Species 0.000 description 1
- 241000223801 Plasmodium knowlesi Species 0.000 description 1
- 241000223821 Plasmodium malariae Species 0.000 description 1
- 241001675579 Plasmodium ovale curtisi Species 0.000 description 1
- 241001675578 Plasmodium ovale wallikeri Species 0.000 description 1
- 241000223810 Plasmodium vivax Species 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- TUZYXOIXSAXUGO-UHFFFAOYSA-N Pravastatin Natural products C1=CC(C)C(CCC(O)CC(O)CC(O)=O)C2C(OC(=O)C(C)CC)CC(O)C=C21 TUZYXOIXSAXUGO-UHFFFAOYSA-N 0.000 description 1
- 208000001280 Prediabetic State Diseases 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 241000125945 Protoparvovirus Species 0.000 description 1
- 241000589516 Pseudomonas Species 0.000 description 1
- 241000517304 Pthirus pubis Species 0.000 description 1
- 241000718000 Pulex irritans Species 0.000 description 1
- 206010037742 Rabies Diseases 0.000 description 1
- 241000725643 Respiratory syncytial virus Species 0.000 description 1
- 241000293824 Rhinosporidium seeberi Species 0.000 description 1
- 241000223254 Rhodotorula mucilaginosa Species 0.000 description 1
- 241000606695 Rickettsia rickettsii Species 0.000 description 1
- 241000203719 Rothia dentocariosa Species 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 235000014680 Saccharomyces cerevisiae Nutrition 0.000 description 1
- 235000018370 Saccharomyces delbrueckii Nutrition 0.000 description 1
- 241001354013 Salmonella enterica subsp. enterica serovar Enteritidis Species 0.000 description 1
- 241000293871 Salmonella enterica subsp. enterica serovar Typhi Species 0.000 description 1
- 241000293869 Salmonella enterica subsp. enterica serovar Typhimurium Species 0.000 description 1
- 241000224003 Sarcocystis Species 0.000 description 1
- 241000257185 Sarcophagidae Species 0.000 description 1
- 241000242683 Schistosoma haematobium Species 0.000 description 1
- 241000242677 Schistosoma japonicum Species 0.000 description 1
- 241000242680 Schistosoma mansoni Species 0.000 description 1
- 241001520868 Schistosoma mekongi Species 0.000 description 1
- 241001442514 Schistosomatidae Species 0.000 description 1
- 241000607768 Shigella Species 0.000 description 1
- 241000607764 Shigella dysenteriae Species 0.000 description 1
- 102000005157 Somatostatin Human genes 0.000 description 1
- 108010056088 Somatostatin Proteins 0.000 description 1
- 241000422838 Spirometra erinaceieuropaei Species 0.000 description 1
- 241000191940 Staphylococcus Species 0.000 description 1
- 241000862969 Stella Species 0.000 description 1
- 241000194017 Streptococcus Species 0.000 description 1
- 235000014969 Streptococcus diacetilactis Nutrition 0.000 description 1
- 241000193996 Streptococcus pyogenes Species 0.000 description 1
- 208000006011 Stroke Diseases 0.000 description 1
- 101710088580 Stromal cell-derived factor 1 Proteins 0.000 description 1
- 241000244177 Strongyloides stercoralis Species 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 102100035794 T-cell surface glycoprotein CD3 epsilon chain Human genes 0.000 description 1
- 241000244155 Taenia Species 0.000 description 1
- 241000356560 Taenia multiceps Species 0.000 description 1
- 241000244159 Taenia saginata Species 0.000 description 1
- 241000244157 Taenia solium Species 0.000 description 1
- 244000309734 Thelazia californiensis Species 0.000 description 1
- 241001477955 Thelazia callipaeda Species 0.000 description 1
- 240000001068 Thogoto virus Species 0.000 description 1
- 101000844259 Thrixopelma pruriens Beta/omega-theraphotoxin-Tp2a Proteins 0.000 description 1
- 208000007536 Thrombosis Diseases 0.000 description 1
- 244000288561 Torulaspora delbrueckii Species 0.000 description 1
- 235000014681 Torulaspora delbrueckii Nutrition 0.000 description 1
- 241000244030 Toxocara canis Species 0.000 description 1
- 241000223997 Toxoplasma gondii Species 0.000 description 1
- 241000589892 Treponema denticola Species 0.000 description 1
- 241000589884 Treponema pallidum Species 0.000 description 1
- 241000243774 Trichinella Species 0.000 description 1
- 241000194297 Trichinella britovi Species 0.000 description 1
- 241000243776 Trichinella nativa Species 0.000 description 1
- 241000243779 Trichinella nelsoni Species 0.000 description 1
- 241000243777 Trichinella spiralis Species 0.000 description 1
- 241000031115 Trichobilharzia regenti Species 0.000 description 1
- 241000224527 Trichomonas vaginalis Species 0.000 description 1
- 241001489145 Trichuris trichiura Species 0.000 description 1
- 241001638368 Trichuris vulpis Species 0.000 description 1
- 241000223105 Trypanosoma brucei Species 0.000 description 1
- 241000223109 Trypanosoma cruzi Species 0.000 description 1
- 241001584775 Tunga penetrans Species 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 229940127174 UCHT1 Drugs 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 241000607272 Vibrio parahaemolyticus Species 0.000 description 1
- 241000607265 Vibrio vulnificus Species 0.000 description 1
- 241000061220 Werneckiella equi Species 0.000 description 1
- 241000244005 Wuchereria bancrofti Species 0.000 description 1
- 241000235015 Yarrowia lipolytica Species 0.000 description 1
- 241000607447 Yersinia enterocolitica Species 0.000 description 1
- 241000607477 Yersinia pseudotuberculosis Species 0.000 description 1
- -1 ZP1 Chemical compound 0.000 description 1
- 241000235029 Zygosaccharomyces bailii Species 0.000 description 1
- PNHVXXUMHKJRKJ-RPSULYRYSA-N [(Z)-[(2Z,3E)-2,3-bis(hydroxyimino)-5,5-dimethylcyclohexylidene]amino]thiourea Chemical compound CC1(C)C\C(=N/O)\C(=N/O)\C(\C1)=N/NC(N)=S PNHVXXUMHKJRKJ-RPSULYRYSA-N 0.000 description 1
- 241000192286 [Candida] stellata Species 0.000 description 1
- 229960000446 abciximab Drugs 0.000 description 1
- 230000021736 acetylation Effects 0.000 description 1
- 238000006640 acetylation reaction Methods 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 229950004283 actoxumab Drugs 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- 229960002964 adalimumab Drugs 0.000 description 1
- 229960000548 alemtuzumab Drugs 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 201000008680 babesiosis Diseases 0.000 description 1
- 229940097012 bacillus thuringiensis Drugs 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 208000007456 balantidiasis Diseases 0.000 description 1
- 229940092523 bartonella quintana Drugs 0.000 description 1
- 229960004669 basiliximab Drugs 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 229960003270 belimumab Drugs 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 229960000397 bevacizumab Drugs 0.000 description 1
- 229950008086 bezlotoxumab Drugs 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 229940056450 brucella abortus Drugs 0.000 description 1
- 229940038698 brucella melitensis Drugs 0.000 description 1
- 229940074375 burkholderia mallei Drugs 0.000 description 1
- 229960001838 canakinumab Drugs 0.000 description 1
- 229940095731 candida albicans Drugs 0.000 description 1
- 229940055022 candida parapsilosis Drugs 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 230000009787 cardiac fibrosis Effects 0.000 description 1
- 238000012832 cell culture technique Methods 0.000 description 1
- 229960003115 certolizumab pegol Drugs 0.000 description 1
- 229960005395 cetuximab Drugs 0.000 description 1
- 229940038705 chlamydia trachomatis Drugs 0.000 description 1
- QPAKKWCQMHUHNI-GQIQPHNSSA-N chlorotoxin Chemical compound C([C@H]1C(=O)NCC(=O)N2CCC[C@H]2C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H]4CSSC[C@@H](C(N[C@@H](CCSC)C(=O)N5CCC[C@H]5C(=O)N[C@@H](CSSC[C@@H](C(=O)N1)NC(=O)[C@H](CCCCN)NC(=O)CNC(=O)[C@H](CCCNC(N)=N)NC(=O)CNC(=O)[C@H](CCCCN)NC(=O)CNC(=O)CNC(=O)[C@H](CSSC[C@H](NC(=O)[C@H](CC(C)C)NC2=O)C(=O)N[C@@H](CCCNC(N)=N)C(N)=O)NC4=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N3)=O)NC(=O)[C@@H](N)CCSC)C1=CC=C(O)C=C1 QPAKKWCQMHUHNI-GQIQPHNSSA-N 0.000 description 1
- 229960005534 chlorotoxin Drugs 0.000 description 1
- 201000001883 cholelithiasis Diseases 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- 210000000078 claw Anatomy 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 208000014826 cranial nerve neuropathy Diseases 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 229960002806 daclizumab Drugs 0.000 description 1
- 229960001251 denosumab Drugs 0.000 description 1
- 229950008925 depatuxizumab mafodotin Drugs 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- RAABOESOVLLHRU-UHFFFAOYSA-N diazene Chemical compound N=N RAABOESOVLLHRU-UHFFFAOYSA-N 0.000 description 1
- 229910000071 diazene Inorganic materials 0.000 description 1
- 235000013681 dietary sucrose Nutrition 0.000 description 1
- PWWSSIYVTQUJQQ-UHFFFAOYSA-N distearyl thiodipropionate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)CCSCCC(=O)OCCCCCCCCCCCCCCCCCC PWWSSIYVTQUJQQ-UHFFFAOYSA-N 0.000 description 1
- 150000002019 disulfides Chemical class 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 229960002224 eculizumab Drugs 0.000 description 1
- 229960000284 efalizumab Drugs 0.000 description 1
- 229940096118 ella Drugs 0.000 description 1
- 229940007078 entamoeba histolytica Drugs 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 229950005562 exbivirumab Drugs 0.000 description 1
- 239000013613 expression plasmid Substances 0.000 description 1
- 229950001563 felvizumab Drugs 0.000 description 1
- 229950011078 foravirumab Drugs 0.000 description 1
- 229940118764 francisella tularensis Drugs 0.000 description 1
- 208000020694 gallbladder disease Diseases 0.000 description 1
- 208000001130 gallstones Diseases 0.000 description 1
- 229960000578 gemtuzumab Drugs 0.000 description 1
- 229960003297 gemtuzumab ozogamicin Drugs 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 208000004104 gestational diabetes Diseases 0.000 description 1
- 229940085435 giardia lamblia Drugs 0.000 description 1
- 229950009672 glembatumumab vedotin Drugs 0.000 description 1
- 102000018146 globin Human genes 0.000 description 1
- 108060003196 globin Proteins 0.000 description 1
- TWSALRJGPBVBQU-PKQQPRCHSA-N glucagon-like peptide 2 Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(O)=O)[C@@H](C)CC)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)CC)C1=CC=CC=C1 TWSALRJGPBVBQU-PKQQPRCHSA-N 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 229960001743 golimumab Drugs 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 210000003630 histaminocyte Anatomy 0.000 description 1
- 102000044890 human EPO Human genes 0.000 description 1
- 102000056713 human FGF21 Human genes 0.000 description 1
- 102000058004 human PTH Human genes 0.000 description 1
- 230000033444 hydroxylation Effects 0.000 description 1
- 238000005805 hydroxylation reaction Methods 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 229960000598 infliximab Drugs 0.000 description 1
- 229950004101 inotuzumab ozogamicin Drugs 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 229940079322 interferon Drugs 0.000 description 1
- 229950000038 interferon alfa Drugs 0.000 description 1
- 229960001388 interferon-beta Drugs 0.000 description 1
- 230000026045 iodination Effects 0.000 description 1
- 238000006192 iodination reaction Methods 0.000 description 1
- 229960005386 ipilimumab Drugs 0.000 description 1
- 230000000302 ischemic effect Effects 0.000 description 1
- 230000006122 isoprenylation Effects 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 229940039695 lactobacillus acidophilus Drugs 0.000 description 1
- 229940115932 legionella pneumophila Drugs 0.000 description 1
- 102000005861 leptin receptors Human genes 0.000 description 1
- 108010019813 leptin receptors Proteins 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 229960003376 levofloxacin Drugs 0.000 description 1
- 229950005173 libivirumab Drugs 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 230000006144 lipoylation Effects 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 230000017538 malonylation Effects 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000004630 mental health Effects 0.000 description 1
- 230000011987 methylation Effects 0.000 description 1
- 238000007069 methylation reaction Methods 0.000 description 1
- 108700008455 metreleptin Proteins 0.000 description 1
- 229960000668 metreleptin Drugs 0.000 description 1
- 229950003734 milatuzumab Drugs 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 201000005518 mononeuropathy Diseases 0.000 description 1
- 210000005087 mononuclear cell Anatomy 0.000 description 1
- 229960003816 muromonab-cd3 Drugs 0.000 description 1
- 229940055036 mycobacterium phlei Drugs 0.000 description 1
- 230000007498 myristoylation Effects 0.000 description 1
- 229960005027 natalizumab Drugs 0.000 description 1
- 201000001119 neuropathy Diseases 0.000 description 1
- 230000007823 neuropathy Effects 0.000 description 1
- 229960002450 ofatumumab Drugs 0.000 description 1
- 229960000470 omalizumab Drugs 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 229950010626 pagibaximab Drugs 0.000 description 1
- 230000026792 palmitoylation Effects 0.000 description 1
- 229960001972 panitumumab Drugs 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 230000003071 parasitic effect Effects 0.000 description 1
- 239000000199 parathyroid hormone Substances 0.000 description 1
- 229960001319 parathyroid hormone Drugs 0.000 description 1
- 229940051027 pasteurella multocida Drugs 0.000 description 1
- 108010069653 peptide E (adrenal medulla) Proteins 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 229950010074 pinatuzumab vedotin Drugs 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 229940118768 plasmodium malariae Drugs 0.000 description 1
- 108091033319 polynucleotide Proteins 0.000 description 1
- 102000040430 polynucleotide Human genes 0.000 description 1
- 239000002157 polynucleotide Substances 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- TUZYXOIXSAXUGO-PZAWKZKUSA-N pravastatin Chemical compound C1=C[C@H](C)[C@H](CC[C@@H](O)C[C@@H](O)CC(O)=O)[C@H]2[C@@H](OC(=O)[C@@H](C)CC)C[C@H](O)C=C21 TUZYXOIXSAXUGO-PZAWKZKUSA-N 0.000 description 1
- 229960002965 pravastatin Drugs 0.000 description 1
- 201000009104 prediabetes syndrome Diseases 0.000 description 1
- 229950002786 rafivirumab Drugs 0.000 description 1
- 229960003876 ranibizumab Drugs 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 229950005854 regavirumab Drugs 0.000 description 1
- 108010004459 relacin Proteins 0.000 description 1
- 229940075118 rickettsia rickettsii Drugs 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 229950004951 sevirumab Drugs 0.000 description 1
- 229940007046 shigella dysenteriae Drugs 0.000 description 1
- 201000002859 sleep apnea Diseases 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- NHXLMOGPVYXJNR-ATOGVRKGSA-N somatostatin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CSSC[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N1)[C@@H](C)O)NC(=O)CNC(=O)[C@H](C)N)C(O)=O)=O)[C@H](O)C)C1=CC=CC=C1 NHXLMOGPVYXJNR-ATOGVRKGSA-N 0.000 description 1
- 229960000553 somatostatin Drugs 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229960004793 sucrose Drugs 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 229960003989 tocilizumab Drugs 0.000 description 1
- 229960005267 tositumomab Drugs 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 229940116861 trichinella britovi Drugs 0.000 description 1
- 229940096911 trichinella spiralis Drugs 0.000 description 1
- 229950005082 tuvirumab Drugs 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- OOLLAFOLCSJHRE-ZHAKMVSLSA-N ulipristal acetate Chemical compound C1=CC(N(C)C)=CC=C1[C@@H]1C2=C3CCC(=O)C=C3CC[C@H]2[C@H](CC[C@]2(OC(C)=O)C(C)=O)[C@]2(C)C1 OOLLAFOLCSJHRE-ZHAKMVSLSA-N 0.000 description 1
- 241000701161 unidentified adenovirus Species 0.000 description 1
- 241001529453 unidentified herpesvirus Species 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 229950004362 urtoxazumab Drugs 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- BNJNAEJASPUJTO-DUOHOMBCSA-N vadastuximab talirine Chemical compound COc1ccc(cc1)C2=CN3[C@@H](C2)C=Nc4cc(OCCCOc5cc6N=C[C@@H]7CC(=CN7C(=O)c6cc5OC)c8ccc(NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)CCCCCN9C(=O)C[C@@H](SC[C@H](N)C(=O)O)C9=O)C(C)C)cc8)c(OC)cc4C3=O BNJNAEJASPUJTO-DUOHOMBCSA-N 0.000 description 1
- 229940118696 vibrio cholerae Drugs 0.000 description 1
- 229960004854 viral vaccine Drugs 0.000 description 1
- 229940098232 yersinia enterocolitica Drugs 0.000 description 1
- BPKIMPVREBSLAJ-QTBYCLKRSA-N ziconotide Chemical compound C([C@H]1C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]2C(=O)N[C@@H]3C(=O)N[C@H](C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@H](C(N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CSSC2)C(N)=O)=O)CSSC[C@H](NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)CNC(=O)[C@H](CCCCN)NC(=O)CNC(=O)[C@H](CCCCN)NC(=O)[C@@H](N)CSSC3)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C(N1)=O)CCSC)[C@@H](C)O)C1=CC=C(O)C=C1 BPKIMPVREBSLAJ-QTBYCLKRSA-N 0.000 description 1
- 229960002811 ziconotide Drugs 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/32—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against translation products of oncogenes
-
- A61K47/48438—
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/6811—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a protein or peptide, e.g. transferrin or bleomycin
- A61K47/6817—Toxins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/06—Antiarrhythmics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/605—Glucagons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from viruses from RNA viruses
- C07K16/1027—Paramyxoviridae, e.g. respiratory syncytial virus
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2869—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against hormone receptors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/02—Preparation of peptides or proteins having a known sequence of two or more amino acids, e.g. glutathione
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/55—Fusion polypeptide containing a fusion with a toxin, e.g. diphteria toxin
Abstract
본원은 면역글로불린 영역의 아미노 말단에서 치료 펩티드에 부착된 제1 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질을 개시한다. 상기 면역글로불린 융합 단백질은 제2 면역글로불린 영역을 추가로 포함할 수 있다. 상기 면역글로불린 융합 단백질은 하나 이상의 연결 펩티드, 링커, 단백질분해성 절단 부위, 내부 링커 또는 이들의 조합을 추가로 포함할 수 있다. 상기 면역글로불린 융합 단백질은 하나 이상의 추가 치료 펩티드를 추가로 포함할 수 있다. 본원은 상기 면역글로불린 융합 단백질을 포함하는 조성물, 및 대상체에서 질환 또는 병태의 치료 또는 예방을 위해 상기 면역글로불린 융합 단백질을 사용하는 방법도 개시한다.
Description
상호 참조
본원은 2014년 6월 6일자로 출원된 미국 가출원 제62/009,054호; 2014년 7월 29일자로 출원된 미국 가출원 제62/030,526호; 및 2014년 10월 15일자로 출원된 미국 가출원 제62/064,186호의 이익을 주장하며, 상기 가출원들은 모두 그 전체가 본원에 참고로 도입된다.
항체는 척추동물 면역계가 주로 감염에 대한 방어를 위해 외래 물질(항원)에 반응하여 형성하는 천연 단백질이다. 100년에 걸쳐, 항체는 인공 조건 하에 동물에서 유도되어 왔고 질환 상태의 치료 또는 진단에서의 사용, 또는 생물학적 연구를 위해 채취되어 왔다. 각각의 개별 면역글로불린 생성 세포는 화학적으로 정의된 조성을 갖는 단일 유형의 면역글로불린을 생성하나, 항원 접종에 반응하여 동물 혈청으로부터 직접적으로 수득된 항체는 사실상 개별 면역글로불린 생성 세포들의 앙상블(ensemble)로부터 만들어진 동일하지 않은 분자들(예를 들면, 폴리클론 항체들)의 앙상블을 포함한다.
본원은 면역글로불린 융합 단백질 및 이의 조성물을 제조하는 방법을 개시한다. 이 방법 및 조성물은 다수의 용도, 예를 들면, 다양한 질환들 및 병태들의 치료에 사용된다. 상기 방법 및 조성물은 표적 세포, 조직 또는 종양으로의 치료 펩티드의 전달을 개선하는 데 사용될 수도 있다.
본원은 제1 면역글로불린 영역; 면역글로불린으로부터 유래되지 않은 제1 치료 펩티드; 및 연결 펩티드를 포함하는 면역글로불린 융합 단백질로서, 상기 연결 펩티드가 상기 제1 치료 펩티드를 상기 제1 면역글로불린 영역의 아미노 말단에 연결하는 것인 면역글로불린 융합 단백질을 제공한다. 한 실시양태에서, 제1 면역글로불린 영역은 면역글로불린 경쇄의 가변 영역을 포함한다. 한 실시양태에서, 제1 면역글로불린 영역은 면역글로불린 경쇄의 불변 영역을 추가로 포함한다.
한 실시양태에서, 면역글로불린 융합 단백질은 제2 면역글로불린 영역을 추가로 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 면역글로불린 중쇄의 가변 영역을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 면역글로불린 중쇄의 불변 영역을 추가로 포함한다.
한 실시양태에서, 제1 면역글로불린 영역은 면역글로불린 중쇄의 가변 영역을 포함한다. 한 실시양태에서, 제1 면역글로불린 영역은 면역글로불린 중쇄의 불변 영역을 추가로 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 면역글로불린 경쇄의 가변 영역을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 면역글로불린 경쇄의 불변 영역을 추가로 포함한다.
한 실시양태에서, 제1 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함한다. 한 실시양태에서, 제1 면역글로불린 영역은 서열번호 5 내지 8 중 어느 하나의 아미노산 서열과 적어도 약 또는 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 서열번호 5 내지 8 중 어느 하나의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 제1 면역글로불린 영역은 트라스투주맙(trastuzumab) 면역글로불린에 기초한, 또는 트라스투주맙 면역글로불린으로부터 유래된 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 트라스투주맙 면역글로불린에 기초한, 또는 트라스투주맙 면역글로불린으로부터 유래된 아미노산 서열을 포함한다. 한 실시양태에서, 제1 면역글로불린 영역은 팔리비주맙(palivizumab) 면역글로불린에 기초한, 또는 팔리비주맙 면역글로불린으로부터 유래된 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 팔리비주맙 면역글로불린에 기초한, 또는 팔리비주맙 면역글로불린으로부터 유래된 아미노산 서열을 포함한다.
한 실시양태에서, 연결 펩티드는 약 0개 내지 약 50개의 아미노산을 포함한다. 한 실시양태에서, 연결 펩티드는 약 1개 내지 약 50개의 아미노산을 포함한다. 한 실시양태에서, 연결 펩티드는 약 1개 내지 약 20개의 아미노산, 또는 약 0개, 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개 또는 20개의 아미노산을 포함한다. 한 실시양태에서, 연결 펩티드의 아미노산들은 규칙적인 이차 구조를 형성하지 않는다. 한 실시양태에서, 연결 펩티드는 서열번호 115 내지 118 및 237 내지 239 중 어느 하나의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 연결 펩티드는 서열번호 115 내지 118 및 237 내지 239 중 어느 하나의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다.
한 실시양태에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적한다. 한 실시양태에서, 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다. 다양한 실시양태들에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적하고 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다.
본원은 제1 면역글로불린 영역; 면역글로불린으로부터 유래되지 않은 제1 치료 펩티드; 및 연결 펩티드를 포함하는 면역글로불린 융합 단백질로서, 상기 연결 펩티드가 상기 제1 치료 펩티드를 상기 제1 면역글로불린 영역의 아미노 말단에 연결하는 것인 면역글로불린 융합 단백질도 제공한다. 한 실시양태에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적한다. 한 실시양태에서, 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다. 다양한 실시양태들에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적하고, 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다. 일례에서, 면역글로불린 융합 단백질의 면역글로불린 영역의 활성은 치료 펩티드 및/또는 연결 펩티드를 갖지 않는 면역글로불린 융합 단백질의 면역글로불린 영역의 활성의 약 또는 적어도 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 100%이다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 면역글로불린 영역은 그의 동족 기질(예를 들면, 항원)에 대한 적어도 약간의 활성을 갖는다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 면역글로불린 영역은 그의 동족 기질에 대한 활성을 거의 또는 전혀 갖지 않는다. 일부 실시양태들에서, 필적하는(comparable) 활성은 면역글로불린 융합 단백질의 치료 펩티드가 면역글로불린 영역 및/또는 연결 펩티드를 갖지 않는 치료 펩티드의 활성을 갖는다는 것을 나타낸다. 일례에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 면역글로불린 영역 및/또는 연결 펩티드를 갖지 않는 면역글로불린 융합 단백질의 치료 펩티드의 활성의 약 또는 적어도 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 100%이다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 치료 펩티드는 그의 동족 기질(예를 들면, 결합 파트너)에 대한 향상된 활성을 갖는다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역 및/또는 연결 펩티드를 갖지 않는 치료 펩티드의 활성의 약 또는 적어도 약 110%, 120%, 140%, 160%, 180%, 200%, 250%, 300%, 400%, 450%, 500%, 550%, 600% 또는 800%인 활성을 갖는다. 일부 실시양태들에서, 연결 펩티드의 아미노산들은 알파 나선 및 베타 가닥을 비롯한 규칙적인 이차 구조도 형성하지 않는다.
본원은 제1 면역글로불린 영역; 면역글로불린으로부터 유래되지 않은 제1 치료 펩티드; 및 임의적으로 연결 펩티드를 포함하는 면역글로불린 융합 단백질로서, 상기 임의적 연결 펩티드가 상기 제1 치료 펩티드를 상기 제1 면역글로불린 영역의 아미노 말단에 연결하는 것인 면역글로불린 융합 단백질을 추가로 제공한다. 한 실시양태에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적한다. 한 실시양태에서, 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다. 다양한 실시양태들에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적하고 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다. 일례에서, 면역글로불린 융합 단백질의 면역글로불린 영역의 활성은 치료 펩티드 및/또는 임의적 연결 펩티드를 갖지 않는 면역글로불린 융합 단백질의 면역글로불린 영역의 활성의 약 또는 적어도 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 100%이다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 면역글로불린 영역은 그의 동족 기질(예를 들면, 항원)에 대한 적어도 약간의 활성을 갖는다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 면역글로불린 영역은 그의 동족 기질에 대한 활성을 거의 또는 전혀 갖지 않는다. 일부 실시양태들에서, 필적하는 활성은 면역글로불린 융합 단백질의 치료 펩티드가 면역글로불린 영역 및/또는 임의적 연결 펩티드를 갖지 않는 치료 펩티드의 활성을 갖는다는 것을 나타낸다. 일례에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 면역글로불린 영역 및/또는 임의적 연결 펩티드를 갖지 않는 면역글로불린 융합 단백질의 치료 펩티드의 활성의 약 또는 적어도 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 100%이다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 치료 펩티드는 그의 동족 기질(예를 들면, 결합 파트너)에 대한 향상된 활성을 갖는다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역 및/또는 임의적 연결 펩티드를 갖지 않는 치료 펩티드의 활성의 약 또는 적어도 약 110%, 120%, 140%, 160%, 180%, 200%, 250%, 300%, 400%, 450%, 500%, 550%, 600% 또는 800%인 활성을 갖는다. 일부 실시양태들에서, 임의적 연결 펩티드의 아미노산들은 알파 나선 및 베타 가닥을 비롯한 규칙적인 이차 구조도 형성하지 않는다.
본원은 제1 면역글로불린 영역; 및 면역글로불린으로부터 유래되지 않은 제1 치료 펩티드를 포함하는 면역글로불린 융합 단백질로서, 상기 제1 치료 펩티드가 상기 제1 면역글로불린 영역의 아미노 말단에 연결되어 있는 것인 면역글로불린 융합 단백질도 제공한다. 한 실시양태에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적한다. 한 실시양태에서, 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다. 다양한 실시양태들에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 표준 사용 제제의 치료 펩티드의 활성에 필적하고 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성은 천연 제1 면역글로불린 영역의 활성에 필적한다. 일부 실시양태들에서, 필적하는 활성은 면역글로불린 융합 단백질의 면역글로불린 영역이 치료 펩티드를 갖지 않는 면역글로불린 영역의 활성을 갖는다는 것을 나타낸다. 일례에서, 면역글로불린 융합 단백질의 면역글로불린 영역의 활성은 치료 펩티드를 갖지 않는 면역글로불린 융합 단백질의 면역글로불린 영역의 활성의 약 또는 적어도 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 100%이다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 면역글로불린 영역은 그의 동족 기질(예를 들면, 항원)에 대한 적어도 약간의 활성을 갖는다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 면역글로불린 영역은 그의 동족 기질에 대한 활성을 거의 또는 전혀 갖지 않는다. 일례에서, 면역글로불린 융합 단백질의 치료 펩티드의 활성은 면역글로불린 영역을 갖지 않는 면역글로불린 융합 단백질의 치료 펩티드의 활성의 약 또는 적어도 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 100%이다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 치료 펩티드는 그의 동족 기질(예를 들면, 결합 파트너)에 대한 향상된 활성을 갖는다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역을 갖지 않는 치료 펩티드의 활성의 약 또는 적어도 약 110%, 120%, 140%, 160%, 180%, 200%, 250%, 300%, 400%, 450%, 500%, 550%, 600% 또는 800%인 활성을 갖는다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 GLP-1 수용체 아고니스트 또는 이의 합성물이다. 한 실시양태에서, 치료 펩티드는 당뇨병 및/또는 당뇨병 관련 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 비만 및/또는 비만 관련 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 엑센딘(exendin)-4, 엑세나타이드(exenatide) 또는 이의 임의의 합성물의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 엑센딘-4, 엑세나타이드 또는 이의 임의의 합성물의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 95의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 95의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 95와 동일한 약 20개 내지 약 39개의 아미노산들을 포함하는 약 20개 내지 약 100개의 아미노산들을 포함한다.
한 실시양태에서, 제2 면역글로불린 영역은 식 I: A2-E1-T2-E2를 갖고, 이때 A2는 제2 면역글로불린 영역이고, E1은 제1 연장제(extender) 펩티드이고, E2는 제2 연장제 펩티드이고, T2는 제2 치료 펩티드이다. 한 실시양태에서, E1은 서열번호 119의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E1은 서열번호 119의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E1은 서열번호 119의 아미노산 서열과 동일한 약 5개 내지 약 23개의 아미노산들을 포함하는 약 5개 내지 약 50개의 아미노산들을 포함한다. 한 실시양태에서, E2는 서열번호 120의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E2는 서열번호 120의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E2는 서열번호 120의 아미노산 서열과 동일한 약 5개 내지 약 23개의 아미노산들을 포함하는 약 5개 내지 약 50개의 아미노산들을 포함한다. 한 실시양태에서, T2는 호르몬이다. 한 실시양태에서, T2는 대사 장애, 및/또는 상기 대사 장애로부터 비롯된 질환의 치료에 효과적이다. 한 실시양태에서, 대사 장애는 지방이영양증, 당뇨병 및 과트리글리세라이드혈증을 포함한다. 한 실시양태에서, T2는 렙틴(leptin), 또는 메트렐렙틴(metreleptin)을 비롯한 이의 유사체의 아미노산 서열과 적어도 50% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, T2는 서열번호 96의 아미노산 서열과 약 또는 적어도 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, T2는 서열번호 96의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, T2는 서열번호 96의 아미노산 서열과 동일한 약 5개 내지 약 167개의 아미노산들을 포함하는 약 20개 내지 약 200개의 아미노산들을 포함한다.
한 실시양태에서, 제2 면역글로불린 영역은 서열번호 43의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 서열번호 43의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 서열번호 44의 아미노산 서열과 적어도 50% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 서열번호 44의 아미노산 서열과 적어도 80% 동일한 아미노산 서열을 포함한다. 본원은 비만을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법도 제공한다. 본원은 당뇨병을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법을 추가로 제공한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 글루카곤 유사체 또는 이의 합성물이다. 한 실시양태에서, 치료 펩티드는 비만 또는 비만 관련 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 서열번호 146의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 146의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 146의 아미노산 서열과 동일한 약 5개 내지 약 29개의 아미노산들을 포함하는 약 5개 내지 약 50개의 아미노산들을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 147의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 147의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 147의 아미노산 서열과 동일한 약 5개 내지 약 39개의 아미노산들을 포함하는 약 5개 내지 약 50개의 아미노산들을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 147의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 147의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 147의 아미노산 서열과 동일한 약 5개 내지 약 39개의 아미노산들을 포함하는 약 5개 내지 약 50개의 아미노산들을 포함한다.
한 실시양태에서, 제2 면역글로불린 영역은 식 I: A2-E1-T2-E2를 갖고, 이때 A2는 제2 면역글로불린 영역이고, E1은 제1 연장제 펩티드이고, E2는 제2 연장제 펩티드이고, T2는 제2 치료 펩티드이다. 한 실시양태에서, E1은 서열번호 119의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E1은 서열번호 119의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E1은 서열번호 119의 아미노산 서열과 동일한 약 5개 내지 약 23개의 아미노산들을 포함하는 약 5개 내지 약 50개의 아미노산들을 포함한다. 한 실시양태에서, E2는 서열번호 120의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E2는 서열번호 120의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, E2는 서열번호 120의 아미노산 서열과 동일한 약 5개 내지 약 23개의 아미노산들을 포함하는 약 5개 내지 약 50개의 아미노산들을 포함한다. 한 실시양태에서, T2는 호르몬이다. 한 실시양태에서, T2는 대사 장애, 및/또는 상기 대사 장애로부터 비롯된 질환의 치료에 효과적이다. 한 실시양태에서, 대사 장애는 지방이영양증, 당뇨병 및 과트리글리세라이드혈증을 포함한다. 한 실시양태에서, T2는 렙틴, 또는 메트렐렙틴을 비롯한 이의 유사체의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, T2는 서열번호 145의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, T2는 서열번호 145의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, T2는 서열번호 145의 아미노산 서열과 약 5개 내지 약 167개의 아미노산들을 포함하는 약 20개 내지 약 200개의 아미노산들을 포함한다.
한 실시양태에서, 제2 면역글로불린 영역은 서열번호 44의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 제2 면역글로불린 영역은 서열번호 44의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 호르몬 또는 이의 합성물이다. 한 실시양태에서, 치료 펩티드는 당뇨병 및/또는 당뇨병 관련 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 비만 및/또는 비만 관련 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 인슐린의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 인슐린의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 105의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 105의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 105의 아미노산 서열과 동일한 약 20개 내지 약 57개의 아미노산들을 포함하는 약 20개 내지 약 100개의 아미노산들을 포함한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 옥신토모듈린(oxyntomodulin)의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 옥신토모듈린의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 106의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 106의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 106의 아미노산 서열과 동일한 약 15개 내지 약 37개의 아미노산들을 포함하는 약 15개 내지 약 100개의 아미노산들을 포함한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 단장 증후군 및/또는 단장 증후군 관련 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 염증성 장 질환 및/또는 염증성 장 관련 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 글루카곤의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 글루카곤의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 107의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 107의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 107의 아미노산 서열과 동일한 약 15개 내지 약 33개의 아미노산들을 포함하는 약 15개 내지 약 200개의 아미노산들을 포함한다. 본원은 단장 증후군 및/또는 단장 증후군 관련 질환을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법도 제공한다. 한 실시양태에서, 치료 펩티드는 글루카곤 유사 단백질(예를 들면, GLP2)의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 글루카곤 유사 단백질의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 156의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 본원은 염증성 장 질환 및/또는 염증성 장 관련 질환을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법을 추가로 제공한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 칼륨 채널에 결합한다. 한 실시양태에서, 치료 펩티드는 자가면역 질환을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 모카톡신(Mokatoxin)-1의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 모카톡신-1의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 108의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 108의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 108의 아미노산 서열과 동일한 약 15개 내지 약 34개의 아미노산들을 포함하는 약 15개 내지 약 100개의 아미노산들을 포함한다. 본원은 자가면역 질환을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법도 제공한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 신경독소이다. 한 실시양태에서, 치료 펩티드는 통증을 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 신경독소 mu-SLPTX-Ssm6a의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 신경독소 mu-SLPTX-Ssm6a의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 109의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 109의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 109의 아미노산 서열과 동일한 약 15개 내지 약 46개의 아미노산들을 포함하는 약 15개 내지 약 200개의 아미노산들을 포함한다. 본원은 통증을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법도 제공한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 카파-쎄라포톡신(theraphotoxin)-Tb1a의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 카파-쎄라포톡신-Tb1a의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 110의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 110의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 110의 아미노산 서열과 동일한 약 15개 내지 약 33개의 아미노산들을 포함하는 약 15개 내지 약 100개의 아미노산들을 포함한다. 본원은 통증을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법도 제공한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 맘발라인(mambalign)-1의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 맘발라인-1의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 111의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 111의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 111의 아미노산 서열과 동일한 약 15개 내지 약 57개의 아미노산들을 포함하는 약 15개 내지 약 150개의 아미노산들을 포함한다. 본원은 통증을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법도 제공한다.
본 개시의 한 양태에서, 면역글로불린 융합 단백질의 치료 펩티드는 인슐린 수퍼패밀리에 속하는 호르몬이다. 한 실시양태에서, 치료 펩티드는 심부전을 갖는 환자를 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 섬유증을 갖는 환자를 치료하도록 구성된다. 한 실시양태에서, 치료 펩티드는 프로릴랙신(prorelaxin) 또는 릴랙신(relaxin)의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 프로릴랙신 또는 릴랙신의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 99의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 99의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 99의 아미노산 서열과 동일한 약 15개 내지 약 161개의 아미노산들을 포함하는 약 15개 내지 약 200개의 아미노산들을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 100의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 100의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 100의 아미노산 서열과 동일한 약 15개 내지 약 185개의 아미노산들을 포함하는 약 15개 내지 약 300개의 아미노산들을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 101의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 101의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 101의 아미노산 서열과 동일한 약 15개 내지 약 120개의 아미노산들을 포함하는 약 15개 내지 약 200개의 아미노산들을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 102의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 102의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 102의 아미노산 서열과 동일한 약 15개 내지 약 88개의 아미노산들을 포함하는 약 15개 내지 약 200개의 아미노산들을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 103의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 103의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 103의 아미노산 서열과 동일한 약 15개 내지 약 88개의 아미노산들을 포함하는 약 15개 내지 약 200개의 아미노산들을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 104의 아미노산 서열과 약 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 104의 아미노산 서열과 적어도 약 80% 동일한 아미노산 서열을 포함한다. 한 실시양태에서, 치료 펩티드는 서열번호 104의 아미노산 서열과 동일한 약 15개 내지 약 74개의 아미노산들을 포함하는 약 15개 내지 약 200개의 아미노산들을 포함한다. 본원은 심부전을 갖는 개체를 치료하는 방법으로서, 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법을 추가로 제공한다.
본원은 제1 면역글로불린 영역, 제1 치료 펩티드 및 연결 펩티드를 코딩하는 핵산을 포함하는 제1 유전자 구축물을 추가로 제공한다. 본원은 제2 면역글로불린 영역을 코딩하는 핵산을 포함하는 제2 유전자 구축물도 제공한다. 본원은 제1 유전자 구축물을 포함하는 제1 발현 벡터를 추가로 제공한다. 본원은 제2 유전자 구축물을 포함하는 제2 발현 벡터도 제공한다. 본원은 제1 발현 벡터를 포함하는 포유동물 발현 숙주를 추가로 제공한다. 본원은 제2 발현 벡터를 포함하는 포유동물 발현 숙주도 제공한다. 본원은 포유동물 세포 배양물에서 제1 및/또는 제2 발현 벡터를 일시적으로 형질감염시키는 단계; 조절된 온도 및 CO2 비율(%)에서 발현 배지 중에서 세포 배양물을 증식시키는 단계; 및 분비된 면역글로불린 융합 단백질을 회수하는 단계를 포함하는, 면역글로불린 융합 단백질을 제조하는 방법을 추가로 제공한다. 한 실시양태에서, 상기 방법은 면역글로불린 융합 단백질을 정제하는 단계도 포함한다.
한 실시양태에서, 면역글로불린 융합 단백질은 제2 치료 펩티드를 추가로 포함한다. 한 실시양태에서, 제2 치료 펩티드는 제1 면역글로불린 영역에 부착된다. 한 실시양태에서, 면역글로불린 융합 단백질은 제2 면역글로불린 영역도 포함한다. 한 실시양태에서, 제2 치료 펩티드는 제2 면역글로불린 영역에 부착된다. 본원은 제1 면역글로불린 영역 및 제1 치료 펩티드를 코딩하는 핵산을 포함하는 유전자 구축물을 추가로 제공한다. 본원은 제1 면역글로불린 영역, 제1 치료 펩티드 및 제2 치료 펩티드를 코딩하는 핵산을 포함하는 유전자 구축물도 제공한다. 본원은 제2 면역글로불린 영역 및 제2 치료 펩티드를 코딩하는 핵산을 포함하는 유전자 구축물을 추가로 제공한다. 본원은 본원에 개시된 임의의 유전자 구축물을 포함하는 숙주 세포도 제공한다. 본원은 면역글로불린 융합 단백질을 제조하는 방법으로서, 폴리뉴클레오티드가 핵산으로부터 발현되는 조건 하에 본원에 개시된 임의의 숙주 세포를 배양함으로써, 면역글로불린 융합 단백질을 제조하는 단계를 포함하는 방법을 추가로 제공한다.
본원은 본원에 개시된 임의의 면역글로불린 융합 단백질을 포함하는 약학 조성물을 추가로 제공한다. 한 실시양태에서, 상기 약학 조성물은 약학적으로 허용 가능한 부형제도 포함한다. 본원은 질환 또는 병태의 치료를 필요로 하는 대상체에서 질환 또는 병태를 치료하는 방법으로서, 치료 유효량의 본원에 개시된 임의의 면역글로불린 융합 단백질을 상기 대상체에게 투여하는 단계를 포함하는 방법도 제공한다.
상기 요약뿐만 아니라 본 개시의 하기 상세한 설명도 첨부된 도면과 함께 판독될 때 더 잘 이해될 것이다. 그러나, 본 개시는 제시된 구체적인 예로 한정되지 않는다는 것을 이해해야 한다. 통상의 관행에 따라 도면의 다양한 특징들은 축척되어 있지 않다는 것이 강조된다. 대조적으로, 상기 다양한 특징들의 치수는 명료함을 위해 임의로 확대되거나 축소된다. 하기 도면들이 도면에 포함된다.
도 1은 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL)-엑센딘-4의 활성의 그래프를 보여준다.
도 2는 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL, GGGGS)-ZP1의 활성의 그래프를 보여준다.
도 3은 GCGR을 활성화시키는 트라스투주맙(NL)-ZP1의 활성의 그래프를 보여준다.
도 4는 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL, GGGGS)-ZPCEX의 활성의 그래프를 보여준다.
도 5는 GCGR을 활성화시키는 트라스투주맙(NL)-ZP1CEX의 활성의 그래프를 보여준다.
도 6은 렙틴 수용체를 활성화시키는 h렙틴, 트라스투주맙(CDR3H) 렙틴, 및 트라스투주맙(CDR3H) 렙틴/트라스투주맙(NL, GGGGS)-ZPCEX의 활성의 그래프를 보여준다.
도 7은 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(CDR3H) 렙틴/트라스투주맙(NL, GGGGS)-ZPCEX의 활성의 그래프를 보여준다.
도 8은 GCGR을 활성화시키는 ZP2-DA 및 트라스투주맙(NL)-ZP1CEX/트라스투주맙(CDR)-렙틴의 활성의 그래프를 보여준다.
도 9는 GLP-1R을 활성화시키는 엑센딘-4 및 팔리비주맙(NL, GGGGS)-ZP1CEX의 활성의 그래프를 보여준다.
도 10은 GCGR을 활성화시키는 ZP2-DA 및 팔리비주맙(NL)-ZP1CEX의 활성의 그래프를 보여준다.
도 11은 GLP-1R을 활성화시키는 엑센딘-4 및 팔리비주맙(NH, GGGGS)-ZP1CEX의 활성의 그래프를 보여준다.
도 12는 GCGR을 활성화시키는 ZP2-DA 및 팔리비주맙(NH)-ZP1CEX의 활성의 그래프를 보여준다.
도 13A 및 13B는 릴랙신 수용체 LGR7 및 LGR8을 활성화시키는 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일) 융합 단백질의 활성의 그래프를 보여준다.
도 14는 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL, GGGGS)-옥신토모듈린의 활성의 그래프를 보여준다.
도 15는 GCGR을 활성화시키는 트라스투주맙(NL)-옥신토모듈린의 활성의 그래프를 보여준다.
도 16A 내지 16K는 팔리비주맙 경쇄와 함께 발현된, 정제된 팔리비주맙 중쇄 릴랙신 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 17A 및 17B는 팔리비주맙 경쇄 글루카곤 융합 단백질과 함께 발현된, 정제된 팔리비주맙 중쇄 엑센딘-4 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 18은 팔리비주맙 경쇄와 함께 발현된, 정제된 팔리비주맙 중쇄 ZP1 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 19A 및 19B는 팔리비주맙 경쇄와 함께 발현된, 정제된 팔리비주맙 중쇄 GLP2 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 20은 약동학적 래트 연구에서 팔리비주맙 중쇄 릴랙신2(단일) 융합 단백질 농도 대 시간의 그래프를 제공한다.
도 21은 팔리비주맙 중쇄 릴랙신2(단일) 융합 단백질로 치료받은 마우스들에 대한 치골간 인대 길이 대 융합 단백질 용량을 제공한다.
도 22는 마우스들에서의 팔리비주맙 융합 단백질의 약력학적 연구를 위한 글루코스 측정치 대 시간의 그래프를 제공한다.
도 23A 및 도 23B는 릴랙신 수용체 LGR7 및 LGR8을 활성화시키는 팔리비주맙(NH, EAAAK)-릴랙신(이중) 융합 단백질의 활성의 그래프를 보여준다.
도 24A 및 24B는 약동학적 연구에서 피하로 치료받은 래트들 및 정맥내로 치료받은 래트들에서의 팔리비주맙 중쇄 릴랙신(이중) 융합 단백질 농도의 그래프를 제공한다.
도 25는 팔리비주맙 중쇄 릴랙신(이중) 융합 단백질로 치료받은 마우스들에 대한 치골간 인대 길이 대 융합 단백질 용량을 제공한다.
도 1은 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL)-엑센딘-4의 활성의 그래프를 보여준다.
도 2는 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL, GGGGS)-ZP1의 활성의 그래프를 보여준다.
도 3은 GCGR을 활성화시키는 트라스투주맙(NL)-ZP1의 활성의 그래프를 보여준다.
도 4는 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL, GGGGS)-ZPCEX의 활성의 그래프를 보여준다.
도 5는 GCGR을 활성화시키는 트라스투주맙(NL)-ZP1CEX의 활성의 그래프를 보여준다.
도 6은 렙틴 수용체를 활성화시키는 h렙틴, 트라스투주맙(CDR3H) 렙틴, 및 트라스투주맙(CDR3H) 렙틴/트라스투주맙(NL, GGGGS)-ZPCEX의 활성의 그래프를 보여준다.
도 7은 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(CDR3H) 렙틴/트라스투주맙(NL, GGGGS)-ZPCEX의 활성의 그래프를 보여준다.
도 8은 GCGR을 활성화시키는 ZP2-DA 및 트라스투주맙(NL)-ZP1CEX/트라스투주맙(CDR)-렙틴의 활성의 그래프를 보여준다.
도 9는 GLP-1R을 활성화시키는 엑센딘-4 및 팔리비주맙(NL, GGGGS)-ZP1CEX의 활성의 그래프를 보여준다.
도 10은 GCGR을 활성화시키는 ZP2-DA 및 팔리비주맙(NL)-ZP1CEX의 활성의 그래프를 보여준다.
도 11은 GLP-1R을 활성화시키는 엑센딘-4 및 팔리비주맙(NH, GGGGS)-ZP1CEX의 활성의 그래프를 보여준다.
도 12는 GCGR을 활성화시키는 ZP2-DA 및 팔리비주맙(NH)-ZP1CEX의 활성의 그래프를 보여준다.
도 13A 및 13B는 릴랙신 수용체 LGR7 및 LGR8을 활성화시키는 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일) 융합 단백질의 활성의 그래프를 보여준다.
도 14는 GLP-1R을 활성화시키는 엑센딘-4 및 트라스투주맙(NL, GGGGS)-옥신토모듈린의 활성의 그래프를 보여준다.
도 15는 GCGR을 활성화시키는 트라스투주맙(NL)-옥신토모듈린의 활성의 그래프를 보여준다.
도 16A 내지 16K는 팔리비주맙 경쇄와 함께 발현된, 정제된 팔리비주맙 중쇄 릴랙신 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 17A 및 17B는 팔리비주맙 경쇄 글루카곤 융합 단백질과 함께 발현된, 정제된 팔리비주맙 중쇄 엑센딘-4 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 18은 팔리비주맙 경쇄와 함께 발현된, 정제된 팔리비주맙 중쇄 ZP1 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 19A 및 19B는 팔리비주맙 경쇄와 함께 발현된, 정제된 팔리비주맙 중쇄 GLP2 융합 단백질의 SDS-PAGE 겔을 제공한다.
도 20은 약동학적 래트 연구에서 팔리비주맙 중쇄 릴랙신2(단일) 융합 단백질 농도 대 시간의 그래프를 제공한다.
도 21은 팔리비주맙 중쇄 릴랙신2(단일) 융합 단백질로 치료받은 마우스들에 대한 치골간 인대 길이 대 융합 단백질 용량을 제공한다.
도 22는 마우스들에서의 팔리비주맙 융합 단백질의 약력학적 연구를 위한 글루코스 측정치 대 시간의 그래프를 제공한다.
도 23A 및 도 23B는 릴랙신 수용체 LGR7 및 LGR8을 활성화시키는 팔리비주맙(NH, EAAAK)-릴랙신(이중) 융합 단백질의 활성의 그래프를 보여준다.
도 24A 및 24B는 약동학적 연구에서 피하로 치료받은 래트들 및 정맥내로 치료받은 래트들에서의 팔리비주맙 중쇄 릴랙신(이중) 융합 단백질 농도의 그래프를 제공한다.
도 25는 팔리비주맙 중쇄 릴랙신(이중) 융합 단백질로 치료받은 마우스들에 대한 치골간 인대 길이 대 융합 단백질 용량을 제공한다.
본원은 아미노 말단 면역글로불린 융합 단백질 및 이러한 면역글로불린 융합 단백질의 제조 방법을 개시한다. 본원은 상기 면역글로불린 융합 단백질을 사용하는 치료 방법도 제공한다. 본원에 기재된 보호대상의 한 특징에 따르면, 아미노 말단 면역글로불린 융합 단백질은 (a) 면역글로불린 영역; 및 (b) 상기 면역글로불린 영역의 아미노 말단에 연결된 치료 펩티드를 포함한다. 치료 펩티드는 연결 펩티드에 의해 면역글로불린 영역에 연결될 수 있다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 하나 이상의 링커 펩티드를 추가로 포함한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 하나 이상의 프로테아제(protease) 절단 부위도 포함한다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 내부 링커 펩티드를 포함한다.
본원에 기재된 보호대상의 또 다른 특징에 따르면, 아미노 말단 면역글로불린 융합 단백질은 제2 면역글로불린 영역을 추가로 포함한다. 제2 면역글로불린 영역은 단일 면역글로불린 도메인 또는 이의 부분, 예를 들면, 경쇄 또는 중쇄 도메인을 포함할 수 있다. 제2 면역글로불린 영역은 비면역글로불린 영역에 연결되어, 제2 면역글로불린 융합체를 형성할 수 있다. 비면역글로불린 영역은 제2 치료 펩티드를 포함할 수 있다. 일부 실시양태들에서, 제2 치료 펩티드는 내부 링커도 포함한다. 비면역글로불린 영역은 하나 이상의 연장제 펩티드, 링커 펩티드 및/또는 단백질분해성 절단 부위를 추가로 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 영역은 면역글로불린 경쇄의 아미노산을 포함한다. 일부 실시양태들에서, 제1 면역글로불린 영역은 면역글로불린 중쇄의 아미노산을 포함한다. 일부 실시양태들에서, 제2 면역글로불린 영역은 면역글로불린 경쇄의 아미노산을 포함한다. 일부 실시양태들에서, 제2 면역글로불린 영역은 면역글로불린 중쇄의 아미노산을 포함한다. 제1 면역글로불린 영역과 제2 면역글로불린 영역은 하나 이상의 다이설파이드 결합 또는 펩티드 링커에 의해 연결될 수 있다.
본원은 면역글로불린 영역에 부착된 2개 이상의 치료 펩티드들을 포함하는 이중 면역글로불린 융합 단백질로서, 적어도 하나의 치료 펩티드가 상기 면역글로불린 영역의 아미노 말단에 부착되어 있는 것인 이중 면역글로불린 융합 단백질을 추가로 개시한다. 제2 치료 펩티드는 면역글로불린 영역에 연결될 수 있거나 면역글로불린 영역 내로 삽입될 수 있다. 치료 펩티드는 면역글로불린 영역의 적어도 일부를 대체할 수 있다. 일부 실시양태들에서, 치료 펩티드는 치료 펩티드의 한 부분 및 제2 치료 펩티드의 하나 이상의 부분을 포함한다. 일부 실시양태들에서, 치료 펩티드는 치료 펩티드의 한 부분, 내부 링커 및 치료 펩티드의 제2 부분을 포함하고, 이때 상기 두 부분들은 동일한 치료 펩티드를 구성하는 아미노산들로부터 유래된다. 일부 실시양태들에서, 치료 펩티드는 내부 링커를 포함한다. 일부 실시양태들에서, 치료 펩티드는 프로테아제 절단 부위를 포함한다.
예시적인 아미노 말단 면역글로불린 융합 단백질은 식 I 내지 XXXII으로 표시되고, 이때 T는 치료 펩티드 또는 치료 펩티드의 부분이고, C는 연결 펩티드이고, A는 면역글로불린 영역이고, P는 프로테아제 부위이고, L은 링커이고, I는 내부 링커이다.
본원은 질환 또는 병태의 치료를 필요로 하는 대상체에서 질환 또는 병태를 치료하는 방법도 개시한다. 일반적으로, 상기 방법은 면역글로불린 영역의 아미노 말단에 부착된 치료 펩티드를 포함하는 아미노 말단 면역글로불린 융합 단백질을 상기 대상체에게 투여하는 단계를 포함한다. 일부 실시양태들에서, I, II, III, IV, V, VI, VII, VIII, IX, X, XI, XII, XIII, XIV, XV, XVI, XVII, XVIII, XIX, XX, XXI, XXII, XXIII, XXIV, XXV, XXVI, XXVII, XXVIII, XXIX, XXX, XXXI 또는 XXXII의 식, 또는 이의 임의의 변경, 부분 또는 추가를 갖는 면역글로불린 융합 단백질이 환자에게 투여된다. 일부 실시양태들에서, 제2 면역글로불린 영역을 추가로 포함하는 면역글로불린 융합 단백질 I, II, III, IV, V, VI, VII, VIII, IX, X, XI, XII, XIII, XIV, XV, XVI, XVII, XVIII, XIX, XX, XXI, XXII, XXIII, XXIV, XXV, XXVI, XXVII, XXVIII, XXIX, XXX, XXXI 및 XXXII 중 하나 이상이 환자에게 투여된다.
본원은 치료 펩티드의 전달을 개선하는 방법을 추가로 개시한다. 상기 방법은 유전자 구축물로부터 아미노 말단 면역글로불린 융합 단백질을 생성하는 단계를 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 면역글로불린 융합 단백질을 코딩하는 유전자 구축물로부터 재조합적으로 제조된다. 일부 실시양태들에서, 상기 구축물은 표준 포유동물 세포 배양 기법의 이용을 통해 시험관 내에서 발현된다. 일부 실시양태들에서, 제1 면역글로불린 영역의 아미노 말단에 연결된 치료 펩티드를 코딩하는 한 구축물은 제2 면역글로불린 영역을 포함하는 제2 구축물과 공발현되어, 재조합 면역글로불린 융합 단백질을 생성한다. 일부 실시양태들에서, 프로테아제를 코딩하는 구축물은 면역글로불린 융합 단백질과 공발현된다. 상기 방법은 하나 이상의 연결 펩티드, 내부 링커, 링커, 연장제 펩티드 및/또는 단백질분해성 절단 부위를 포함하는 면역글로불린 유전적 융합 구축물을 생성하는 단계를 추가로 포함할 수 있다.
본 방법 및 조성물이 기재되기 전에, 본 발명은 당연히 변경될 수 있기 때문에 기재된 특정 방법 또는 조성물로 한정되지 않는다는 것을 이해해야 한다. 본 발명의 범위가 첨부된 청구범위에 의해서만 한정될 것이기 때문에 본원에서 사용된 용어는 특정 실시양태만을 기술하기 위한 것이고 한정하기 위한 것이 아니라는 것도 이해해야 한다. 실시예는 어떻게 본 발명을 만들고 사용하는 지에 대한 완전한 개시 및 설명을 당분야에서 통상의 기술을 갖는 자에게 제공하기 위해 기재되어 있고, 본 발명자들이 그들의 발명으로서 간주하는 것의 범위를 한정하기 위한 것이 아닐 뿐만 아니라 하기 실험들이 수행된 모든 또는 유일한 실험이라는 것을 나타내기 위한 것도 아니다. 사용된 수치(예를 들면, 양, 온도 등)에 대한 정확성을 보장하기 위해 노력하였으나, 일부 실험적 오차 또는 편차가 고려되어야 한다. 달리 표시되어 있지 않은 한, 부는 중량부이고, 분자량은 중량 평균 분자량이고, 온도는 섭씨 온도이고, 압력은 대기압이거나 대기압에 가깝다.
값의 범위가 제공된 경우, 문맥이 달리 명시하지 않은 한, 그 범위의 상한과 하한 사이의 각각의 개재 값도 하한의 단위의 10분의 1까지 구체적으로 개시되어 있는 것으로 이해된다. 임의의 언급된 값 또는 언급된 범위 내의 개재 값과 임의의 다른 언급된 값 또는 그 언급된 범위 내의 개재 값 사이의 각각의 보다 더 작은 범위는 본 발명 내에 포함된다. 이들 보다 더 작은 범위들의 상한 및 하한은 그 범위에 독립적으로 포함될 수 있거나 배제될 수 있고, 상기 두 한계들 중 어느 하나가 보다 더 작은 범위에 포함되거나, 이들 중 어느 것도 보다 더 작은 범위에 포함되지 않거나, 이들 둘 다가 보다 더 작은 범위에 포함되는 경우, 언급된 범위 내의 임의의 구체적으로 배재된 한계를 조건으로, 각각의 범위도 본 발명 내에 포함된다. 언급된 범위가 상기 한계들 중 하나 또는 이들 둘 다를 포함하는 경우, 이들 포함된 한계들 중 어느 하나 또는 둘 다를 배제하는 범위도 본 발명 내에 포함된다.
달리 정의되어 있지 않은 한, 본원에서 사용된 모든 기술 용어들 및 과학 용어들은 본 발명이 속하는 분야에서 통상의 기술을 갖는 자에 의해 통상적으로 이해되는 의미와 동일한 의미를 갖는다. 본원에 기재된 방법 및 재료와 유사하거나 동등한 임의의 방법 및 재료가 본 발명의 실시 또는 시험에 사용될 수 있지만, 일부 잠재적 및 바람직한 방법들 및 재료들이 지금부터 기재되어 있다. 본원에서 언급된 모든 공개문헌들은 이 공개문헌들이 인용되는 것과 관련하여 방법 및/또는 재료를 개시하고 기술하기 위해 본원에 참고로 도입된다. 본 개시는 도입된 공개문헌의 임의의 개시를 모순이 있는 정도까지 대신하는 것으로 이해된다.
본 개시를 읽을 때 당업자에게 자명할 바와 같이, 본원에 기재되어 있고 예시되어 있는 각각의 개별 실시양태는 본 발명의 범위 또는 사상으로부터 벗어나지 않으면서 임의의 다른 여러 실시양태들의 특징으로부터 용이하게 분리될 수 있거나 이러한 특징과 용이하게 조합될 수 있는 별개의 구성요소 및 특징을 갖는다. 임의의 언급된 방법은 언급된 사건의 순서대로, 또는 논리적으로 가능한 임의의 다른 순서대로 수행될 수 있다.
본원 및 첨부된 청구범위에서 사용된 바와 같이, 문맥이 달리 명시하지 않은 한, 단수형 지시대상은 복수형 지시대상을 포함한다는 것을 인지해야 한다. 따라서, 예를 들면, "세포"의 언급은 복수의 이러한 세포들을 포함하고, "펩티드"의 언급은 당업자에게 공지되어 있는 하나 이상의 펩티드 및 이의 등가물, 예를 들면, 폴리펩티드 등의 언급을 포함한다.
아미노 말단 면역글로불린 융합 단백질
본원에 개시된 아미노 말단 면역글로불린 융합 단백질은 하나 이상의 면역글로불린 영역 및 하나 이상의 치료 펩티드를 포함하고, 이때 제1 치료 펩티드는 제1 면역글로불린 영역의 아미노 말단에 연결되어 있다. 면역글로불린 영역은 부분적으로 또는 전체적으로 면역글로불린의 임의의 부분일 수 있다. 면역글로불린은 포유동물 공급원으로부터 유래될 수 있다. 면역글로불린은 키메라 면역글로불린일 수 있다. 면역글로불린 영역은 전체적으로 또는 부분적으로 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린은 인간화된 면역글로불린, 조작된 인간 면역글로불린 또는 완전한 인간 면역글로불린으로부터 유래할 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 포유동물 면역글로불린은 비인간 영장류 면역글로불린일 수 있다. 면역글로불린은 조류 면역글로불린일 수 있다. 면역글로불린은 상어 면역글로불린일 수 있다.
면역글로불린 영역은 전체 면역글로불린 분자를 포함할 수 있거나, 중쇄, 경쇄, 가변 도메인, 불변 도메인, 상보성 결정 영역(CDR), 골격 영역, 단편 항원 결합(Fab) 영역, Fab', F(ab')2, F(ab')3, Fab', 단편 결정화가능한(Fc) 영역, 단일 쇄 가변 단편(scFV), di-scFv, 단일 도메인 면역글로불린, 삼작용성 면역글로불린, 화학적으로 연결된 F(ab')2, 및 이들의 임의의 부분 또는 조합을 포함하나 이들로 한정되지 않는 면역글로불린의 단편을 포함하는 임의의 폴리펩티드를 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 중쇄는 전체 중쇄 또는 중쇄의 부분을 포함할 수 있다. 예를 들면, 중쇄로부터 유래된 가변 도메인 또는 이의 영역은 중쇄 또는 중쇄의 영역으로서 지칭될 수 있다. 일부 실시양태들에서, 면역글로불린 경쇄는 전체 경쇄 또는 경쇄의 부분을 포함할 수 있다. 예를 들면, 경쇄로부터 유래된 가변 도메인 또는 이의 영역은 경쇄 또는 경쇄의 영역으로서 지칭될 수 있다. 면역글로불린 영역은 이중특이적일 수 있거나 삼중특이적일 수 있다. 단일 도메인 면역글로불린은 단일 단량체성 가변 면역글로불린 도메인을 포함하나 이것으로 한정되지 않는다. 단일 도메인 면역글로불린은 상어 가변 신규 항원 수용체 면역글로불린 단편(VNAR)일 수 있다. 면역글로불린은 IgA, IgD, IgE, IgG, IgM, IgY 및 IgW를 포함하나 이들로 한정되지 않는, 당업자에게 공지되어 있는 임의의 유형으로부터 유래될 수 있다. 면역글로불린 영역은 당단백질일 수 있다. 면역글로불린 영역은 1개, 2개, 3개, 4개 및 5개의 유닛을 포함하나 이들로 한정되지 않는 하나 이상의 작용 유닛을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 다이설파이드 결합에 의해 연결된 하나 이상의 유닛을 포함할 수 있다. 면역글로불린 영역은 펩티드 링커, 예를 들면, scFv 면역글로불린에 의해 연결된 하나 이상의 유닛을 포함할 수 있다. 면역글로불린은 아미노산 돌연변이, 치환 및/또는 결실을 갖는 면역글로불린을 포함하는 재조합 면역글로불린일 수 있다. 면역글로불린은 화학적 변경을 포함하는 재조합 면역글로불린일 수 있다. 면역글로불린은 면역글로불린-약물 접합체의 전부 또는 일부를 포함할 수 있다. 면역글로불린은 소분자를 포함할 수 있다. 면역글로불린은 소분자를 포함하는 면역글로불린-약물 접합체의 전부 또는 일부를 포함할 수 있다. 면역글로불린-약물 접합체의 예로는 브렌툭시맙 베도틴(Brentuximab vedotin)(SGN35), 트라스투주맙 엠탄신(emtansine)(T-DM1), 이노투주맙 오조가미신(Inotuzumab ozogamicin)(CMC-544), 겜투주맙 오조가미신(Gemtuzumab ozogamicin), SAR3419, RG-7596/DCDS4501A, 피나투주맙 베도틴(Pinatuzumab vedotin)(RG-7593/DCDT 2980S), 글렘바투무맙 베도틴(Glembatumumab vedotin)(CDX-011), 로르보투주맙 메르탄신(Lorvotuzumab mertansine)(IMGN901), PSMA-ADC, BT-062, ABT-414, 밀라투주맙 독소루비신(Milatuzumab doxorubicin)(IMMU-110), IMMU-132(hRS7-SN38), 라베투주맙(Labetuzumab)-SN-38(IMMU-130), 에프라투주맙(Epratuzumab)-SN-38, IMGN-853, RG-7458/DMUC 5754 A, RG-7636, RG-7450/DSTP 3086 S, RG-7600, RG-7598, RG-7599/DNIB 0600 A, SGN-CD19A, SGN-CD33A(EC-mAb), SGN-75, SGN CD70 A, PF-0626350, 보르세투주맙 마포도틴(Vorsetuzumab mafodotin), ASG-5ME, ASG-22ME, ASG-22CE, AGS-16M8F, ASG-15ME, MLN-0264, SAR-566658, AMG-172, AMG-595, BAY-94-9343, BAY-79-4620, SC16LD6.5, SGN-LIV1-A, MDX-1203, BIIB015, HuMax-TF-ADC 및 ARX788이 있으나 이들로 한정되지 않는다.
면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함한다.
면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개, 450개 또는 500개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열로부터 유래된 아미노산, 및 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 하나 이상의 서열로부터 유래된 아미노산, 및 서열번호 42 내지 74 및 192 내지 221 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 42 내지 74 및 192 내지 221 중 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 서열로부터 유래된 아미노산을 포함한다.
면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 50% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 70% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 80% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 50% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 70% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 80% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 100% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 600개, 650개, 700개, 750개, 800개, 850개, 900개, 950개 또는 1000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1100개, 1200개, 1300개, 1400개 또는 1500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 25 내지 44 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1,000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1,300개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 뉴클레오티드는 연속적일 수 있다. 대안적으로 또는 추가로, 뉴클레오티드는 비연속적이다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열로부터 유래된 뉴클레오티드 및 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 25 내지 44 중 하나 이상의 서열로부터 유래된 뉴클레오티드 및 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 서열번호 9 내지 41, 161 내지 191 및 265 중 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩된다.
본원은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 뉴클레오티드 서열을 포함하는 뉴클레오티드 구축물도 개시한다. 뉴클레오티드 구축물은 숙주 세포에서의 발현을 위한 플라스미드, 예를 들면, 포유동물 또는 세균 발현 플라스미드일 수 있다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 50% 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 70% 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 80% 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 50% 동일한 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 70% 동일한 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 80% 동일한 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 100% 동일한 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열을 포함한다. 일부 실시양태들에서, 상기 구축물은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열을 포함한다.
아미노 말단 면역글로불린 경쇄 융합체
본 발명의 한 특징에서, 본원은 면역글로불린 경쇄의 영역의 아미노 말단에 연결된 치료 펩티드를 포함하는 면역글로불린 융합 단백질로서, 면역글로불린 융합체가 본원에서 면역글로불린 경쇄 융합체로서 지칭되는 것인 면역글로불린 융합 단백질을 제공한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 면역글로불린 중쇄의 하나 이상의 영역을 추가로 포함하고, 이때 면역글로불린 경쇄 융합체는 디설파이드 결합 또는 연결 펩티드에 의해 면역글로불린 중쇄의 하나 이상의 영역에 연결되어 있다. 일부 실시양태들에서, 치료 펩티드는 치료 펩티드의 하나 이상의 영역을 포함한다. 일부 실시양태들에서, 치료 펩티드는 내부 링커에 의해 연결된 치료 펩티드의 2개의 영역들을 포함한다. 일부 실시양태들에서, 치료 펩티드는 프로테아제 절단 부위를 포함한다.
면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다. 일부 실시양태들에서, 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열로부터 유래된 아미노산 및 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 하나 이상의 서열로부터 유래된 아미노산 및 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 경쇄 융합체는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 서열로부터 유래된 아미노산을 포함한다.
면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 50% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 70% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 80% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 50% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 70% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 적어도 약 80% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열과 100% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다.
면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 600개, 650개, 700개, 750개, 800개, 850개, 900개, 950개 또는 1000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1100개, 1200개, 1300개, 1400개 또는 1500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1300개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 뉴클레오티드는 연속적일 수 있다. 대안적으로 또는 추가로, 뉴클레오티드는 비연속적이다. 일부 실시양태들에서, 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열로부터 유래된 뉴클레오티드, 및 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 하나 이상의 서열로부터 유래된 뉴클레오티드, 및 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 경쇄 융합체는 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 및 190 중 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩된다.
아미노 말단 면역글로불린 중쇄 융합체
본 발명의 한 특징에서, 본원은 면역글로불린 중쇄의 영역의 아미노 말단에 연결된 치료 펩티드를 포함하는 면역글로불린 융합 단백질로서, 면역글로불린 융합체가 본원에서 면역글로불린 중쇄 융합체로서 지칭되는 것인 면역글로불린 융합 단백질을 제공한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 면역글로불린 경쇄의 하나 이상의 영역을 추가로 포함하고, 이때 면역글로불린 중쇄 융합체는 디설파이드 결합 또는 연결 펩티드에 의해 면역글로불린 경쇄의 하나 이상의 영역에 연결되어 있다. 일부 실시양태들에서, 치료 펩티드는 치료 펩티드의 하나 이상의 영역을 포함한다. 일부 실시양태들에서, 치료 펩티드는 내부 링커에 의해 연결된 치료 펩티드의 2개의 영역들을 포함한다. 일부 실시양태들에서, 치료 펩티드는 프로테아제 절단 부위를 포함한다.
면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개, 450개 또는 500개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다. 일부 실시양태들에서, 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열로부터 유래된 아미노산 및 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 중쇄 융합체는 서열번호 6 및 8 중 하나 이상의 서열로부터 유래된 아미노산 및 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 중쇄 융합체는 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 1개, 2개, 3개, 4개 또는 5개의 서열로부터 유래된 아미노산을 포함한다.
면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 50% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 70% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 80% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 50% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 70% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 적어도 약 80% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열과 100% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다.
면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 600개, 650개, 700개, 750개, 800개, 850개, 900개, 950개 또는 1000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1100개, 1200개, 1300개, 1400개 또는 1500개 이상의 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1300개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 뉴클레오티드는 연속적일 수 있다. 대안적으로 또는 추가로, 뉴클레오티드는 비연속적이다. 일부 실시양태들에서, 면역글로불린 중쇄 융합체는 서열번호 2 및 4 중 어느 한 서열로부터 유래된 뉴클레오티드 및 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 하나 이상의 서열로부터 유래된 뉴클레오티드 및 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 중쇄 융합체는 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 및 265 중 1개, 2개, 3개, 4개 또는 5개의 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 융합 단백질
본 발명의 한 특징에서, 본원은 (a) 면역글로불린 경쇄 융합체, 및 (b) 면역글로불린 중쇄로부터 유래된 제2 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질로서, 상기 면역글로불린 경쇄 융합체가 하나 이상의 디설파이드 결합 또는 연결 펩티드에 의해 제2 면역글로불린 영역에 연결되어 있는 것인 면역글로불린 융합 단백질을 제공한다. 면역글로불린 경쇄 융합체는 면역글로불린 경쇄로부터 유래된 제1 면역글로불린 영역의 아미노 말단에 연결된 제1 치료 펩티드를 포함한다. 일부 실시양태들에서, 제2 면역글로불린 영역은 비면역글로불린 영역에 부착되어 제2 면역글로불린 융합체를 생성한다. 비면역글로불린 영역은 제2 치료 펩티드를 포함할 수 있다. 비면역글로불린 영역은 연장제 펩티드를 포함할 수 있다. 비면역글로불린 영역은 링커 펩티드를 포함할 수 있다. 비면역글로불린 영역은 단백질분해성 절단 부위를 포함할 수 있다. 제2 치료 펩티드는 내부 링커를 포함할 수 있다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 아미노 또는 카복실 말단에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 하나 이상의 내부 아미노산에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역 내의 루프 부분의 아미노산에 부착된다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 연장제 및/또는 링커 펩티드의 사용을 통해 제2 면역글로불린 영역에 부착된다. 면역글로불린 경쇄 융합체는 하나 이상의 추가 치료 펩티드를 추가로 포함할 수 있다.
본 발명의 한 특징에서, 본원은 (a) 면역글로불린 중쇄 융합체, 및 (b) 면역글로불린 경쇄로부터 유래된 제2 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질로서, 상기 면역글로불린 중쇄 융합체가 하나 이상의 디설파이드 결합 또는 연결 펩티드에 의해 제2 면역글로불린 영역에 연결되어 있는 것인 면역글로불린 융합 단백질을 제공한다. 면역글로불린 중쇄 융합체는 면역글로불린 중쇄로부터 유래된 제1 면역글로불린 영역의 아미노 말단에 연결된 제1 치료 펩티드를 포함한다. 일부 실시양태들에서, 제2 면역글로불린 영역은 비면역글로불린 영역에 부착되어 제2 면역글로불린 융합체를 생성한다. 비면역글로불린 영역은 제2 치료 펩티드를 포함할 수 있다. 비면역글로불린 영역은 연장제 펩티드를 포함할 수 있다. 비면역글로불린 영역은 링커 펩티드를 포함할 수 있다. 비면역글로불린 영역은 단백질분해성 절단 부위를 포함할 수 있다. 제2 치료 펩티드는 내부 링커를 포함할 수 있다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 아미노 또는 카복실 말단에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 하나 이상의 내부 아미노산에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역 내의 루프 부분의 아미노산에 부착된다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 연장제 및/또는 링커 펩티드의 사용을 통해 제2 면역글로불린 영역에 부착된다. 면역글로불린 중쇄 융합체는 하나 이상의 추가 치료 펩티드를 추가로 포함할 수 있다.
본 발명의 한 특징에서, 본원은 (a) 면역글로불린 경쇄 융합체, 및 (b) 면역글로불린 중쇄 융합체를 포함하는 면역글로불린 융합 단백질을 제공한다. 면역글로불린 경쇄 융합체는 면역글로불린 경쇄로부터 유래된 제1 면역글로불린 영역의 아미노 말단에 연결된 제1 치료 펩티드를 포함한다. 면역글로불린 중쇄 융합체는 면역글로불린 중쇄로부터 유래된 제1 면역글로불린 영역의 아미노 말단에 연결된 제1 치료 펩티드를 포함한다. 일부 실시양태들에서, 면역글로불린 경쇄 융합체는 하나 이상의 추가 치료 펩티드를 추가로 포함한다. 일부 실시양태들에서, 면역글로불린 중쇄 융합체는 하나 이상의 추가 치료 펩티드를 포함한다.
본 발명의 한 특징에서, 본원은 (a) 면역글로불린 경쇄 융합체, 및 (b) 제2 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질로서, 상기 면역글로불린 경쇄 융합체가 면역글로불린 경쇄로부터 유래된 제1 면역글로불린 영역의 아미노 말단에 연결된 제1 치료 펩티드를 포함하는 것인 면역글로불린 융합 단백질을 제공한다. 제2 면역글로불린 영역은 면역글로불린 중쇄로부터 유래될 수 있다. 제2 면역글로불린 영역은 면역글로불린 경쇄로부터 유래될 수 있다. 제2 면역글로불린 영역은 하나 이상의 비면역글로불린 영역에 연결되어 제2 면역글로불린 융합체를 생성할 수 있다. 비면역글로불린 영역은 제2 치료 펩티드를 포함할 수 있다. 비면역글로불린 영역은 연장제 펩티드를 포함할 수 있다. 비면역글로불린 영역은 링커 펩티드를 포함할 수 있다. 비면역글로불린 영역은 단백질분해성 절단 부위를 포함할 수 있다. 제2 치료 펩티드는 내부 링커를 포함할 수 있다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 아미노 또는 카복실 말단에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 하나 이상의 내부 아미노산에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역 내의 루프 부분의 아미노산에 부착된다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 연장제 및/또는 링커 펩티드의 사용을 통해 제2 면역글로불린 영역에 부착된다. 면역글로불린 경쇄 융합체는 하나 이상의 추가 치료 펩티드도 포함할 수 있다.
본 발명의 한 특징에서, 본원은 (a) 면역글로불린 중쇄 융합체, 및 (b) 제2 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질로서, 상기 면역글로불린 중쇄 융합체가 면역글로불린 중쇄로부터 유래된 제1 면역글로불린 영역의 아미노 말단에 연결된 제1 치료 펩티드를 포함하는 것인 면역글로불린 융합 단백질을 제공한다. 제2 면역글로불린 영역은 면역글로불린 중쇄로부터 유래될 수 있다. 제2 면역글로불린 영역은 면역글로불린 경쇄로부터 유래될 수 있다. 제2 면역글로불린 영역은 하나 이상의 비면역글로불린 영역에 연결되어 제2 면역글로불린 융합체를 생성할 수 있다. 비면역글로불린 영역은 제2 치료 펩티드를 포함할 수 있다. 비면역글로불린 영역은 연장제 펩티드를 포함할 수 있다. 비면역글로불린 영역은 링커 펩티드를 포함할 수 있다. 비면역글로불린 영역은 단백질분해성 절단 부위를 포함할 수 있다. 제2 치료 펩티드는 내부 링커를 포함할 수 있다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 아미노 또는 카복실 말단에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역의 하나 이상의 내부 아미노산에 부착된다. 일부 실시양태들에서, 제2 치료 펩티드는 제2 면역글로불린 영역 내의 루프 부분의 아미노산에 부착된다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 연장제 및/또는 링커 펩티드의 사용을 통해 제2 면역글로불린 영역에 부착된다. 면역글로불린 중쇄 융합체는 하나 이상의 추가 치료 펩티드도 포함할 수 있다.
면역글로불린 융합 단백질은 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 면역글로불린 중쇄 융합체를 포함할 수 있다.
면역글로불린 융합 단백질은 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 하나 이상의 서열을 포함하는 면역글로불린 중쇄로부터 유래된 제2 면역글로불린 영역을 포함할 수 있다.
면역글로불린 융합 단백질은 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 하나 이상의 서열에 기초한, 또는 이러한 서열로부터 유래된 면역글로불린 경쇄 융합체를 포함할 수 있다.
면역글로불린 융합 단백질은 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 하나 이상의 서열을 포함하는 면역글로불린 경쇄부터 유래된 제2 면역글로불린 영역을 포함할 수 있다.
면역글로불린 융합 단백질은 (a) 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 및 266 중 어느 하나 이상의 서열에 기초한, 또는 이러한 서열로부터 유래된 면역글로불린 중쇄의 영역; 및 (b) 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 및 221 중 어느 하나 이상의 서열에 기초한, 또는 이러한 서열로부터 유래된 면역글로불린 경쇄의 영역을 포함할 수 있다. 면역글로불린 융합 단백질은 (a) 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 또는 266과 적어도 약 50% 동일한 아미노산 서열을 포함하는 면역글로불린 중쇄의 영역; 및 (b) 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 적어도 약 50% 동일한 아미노산 서열을 포함하는 면역글로불린 경쇄의 영역을 포함할 수 있다. 면역글로불린 중쇄의 영역은 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 또는 266과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄의 영역은 서열번호 6, 8, 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 또는 266과 100% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄의 영역은 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄의 영역은 서열번호 5, 7, 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 100% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 융합 단백질은 (a) 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 또는 265의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 중쇄의 영역; 및 (b) 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 또는 190의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 경쇄의 영역을 포함할 수 있다. 면역글로불린 단백질은 (a) 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 또는 265의 뉴클레오티드 서열과 적어도 50% 이상 동일한 뉴클레오티드 서열에 의해 코딩된 면역글로불린 중쇄의 영역; 및 (b) 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 또는 190의 뉴클레오티드 서열과 적어도 50% 이상 동일한 뉴클레오티드 서열에 의해 코딩된 면역글로불린 경쇄의 영역을 포함할 수 있다. 면역글로불린 중쇄의 영역은 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 또는 265의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄의 영역은 서열번호 2, 4, 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 또는 265의 뉴클레오티드 서열과 100% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄의 영역은 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 또는 190의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄의 영역은 서열번호 1, 3, 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 또는 190의 뉴클레오티드 서열과 100% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다.
일부 실시양태들에서, 본원은 면역글로불린 글루카곤 융합 단백질을 제공한다. 일부 실시양태들에서, 면역글로불린 글루카곤 융합 단백질은 글루카곤 펩티드, 글루카곤 유래의 펩티드, 예컨대, ZP1, 및/또는 글루카곤 유사 펩티드, 예컨대, GLP-1 및/또는 GLP-2와 아미노 말단에서 융합된 면역글로불린 경쇄 및/또는 중쇄 영역을 포함한다. 일부 실시양태들에서, 면역글로불린 글루카곤 융합 단백질은 제2 면역글로불린 경쇄 및/또는 중쇄를 추가로 포함한다. 일부 실시양태들에서, 면역글로불린 글루카곤 융합 단백질은 아미노 말단 글루카곤 펩티드 또는 이의 유도체를 포함하는 제1 면역글로불린 쇄 및 제2 면역글로불린 쇄를 지칭한다. 일부 실시양태들에서, 제1 면역글로불린 글루카곤 융합 단백질은 제2 면역글로불린 쇄와 공발현된다. 일부 실시양태들에서, 면역글로불린 글루카곤 융합 단백질은 대사 질환, 예컨대, 비만 및/또는 당뇨병을 치료하도록 구성된다. 일부 실시양태들에서, (글루카곤 유사 융합 단백질을 포함하는) 면역글로불린 글루카곤 융합 단백질은 단장 증후군을 치료하도록 구성된다. 일부 실시양태들에서, (글루카곤 유사 융합 단백질을 포함하는) 면역글로불린 글루카곤 융합 단백질은 염증성 장 질환을 치료하도록 구성된다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 195 및 196 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 7에 기초한, 또는 서열번호 7로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 195 및 196 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 7과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 제1 면역글로불린 글루카곤 단백질은 서열번호 195 및 196 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 단백질은 서열번호 7과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 164 및 165 중 어느 한 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 3의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 164 및 165 중 어느 한 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 3의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 융합 단백질은 서열번호 164 및 165 중 어느 한 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 제2 면역글로불린 단백질은 서열번호 3의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 199 및 200 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 8에 기초한, 또는 서열번호 8로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 199 및 200 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 8과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 제1 면역글로불린 글루카곤 단백질은 서열번호 199 및 200 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 단백질은 서열번호 8과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 168 및 169 중 어느 한 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 4의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 168 및 169 중 어느 한 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 4의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 융합 단백질은 서열번호 168 및 169 중 어느 한 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 제2 면역글로불린 단백질은 서열번호 4의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 218 내지 220 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 7에 기초한, 또는 서열번호 7로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 218 내지 220 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 7과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 제1 면역글로불린 글루카곤 단백질은 서열번호 218 내지 220 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 단백질은 서열번호 7과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 187 내지 189 중 어느 한 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 3의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 187 내지 189 중 어느 한 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 3의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 융합 단백질은 서열번호 187 내지 189 중 어느 한 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 제2 면역글로불린 단백질은 서열번호 3의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 221에 기초한, 또는 서열번호 221로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 8에 기초한, 또는 서열번호 8로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 221과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 8과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 제1 면역글로불린 글루카곤 단백질은 서열번호 221과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 단백질은 서열번호 8과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 190의 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 4의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 글루카곤 융합 단백질은 (a) 서열번호 190의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 4의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 융합 단백질은 서열번호 190의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 제2 면역글로불린 단백질은 서열번호 4의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다.
일부 실시양태들에서, 본원은 면역글로불린 릴랙신 융합 단백질을 제공한다. 일부 실시양태들에서, 면역글로불린 릴랙신 융합 단백질은 내부 링커를 갖는 릴랙신을 비롯한 릴랙신 또는 릴랙신으로부터 유래된 펩티드와 아미노 말단에서 융합된 면역글로불린 경쇄 및/또는 중쇄 영역을 포함한다. 일부 실시양태들에서, 면역글로불린 릴랙신 융합 단백질은 제2 면역글로불린 경쇄 및/또는 중쇄를 추가로 포함한다. 일부 실시양태들에서, 면역글로불린 릴랙신 융합 단백질은 아미노 말단 릴랙신 펩티드 또는 이의 유도체를 포함하는 제1 면역글로불린 쇄 및 제2 면역글로불린 쇄를 지칭한다. 일부 실시양태들에서, 제1 면역글로불린 릴랙신 융합 단백질은 제2 면역글로불린 쇄와 공발현된다. 일부 실시양태들에서, 면역글로불린 릴랙신 융합 단백질은 심장 질환 또는 병태를 치료하도록 구성된다. 일부 실시양태들에서, 면역글로불린 릴랙신 융합 단백질은 심부전, 급성 관상 동맥 증후군, 심방 세동, 심장 섬유증, 관상 동맥 질환, 고형 장기(예를 들면, 폐, 신장, 간, 심장) 이식과 관련된 허혈 재관류, 장기(예를 들면, 신장) 보호를 위한 심폐 바이패스, 허혈성 뇌졸중, 각막 치유(눈 투여), 당뇨병성 신장병증, 간경변증, 문맥 고혈압, 당뇨병성 상처 치유, 전신 경화증, 분만 시 자궁경부 숙화, 자간전증, 섬유증, 및 이들의 조합을 포함하는 질환 또는 병태를 치료한다. 면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 201 내지 213 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 7에 기초한, 또는 서열번호 7로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 201 내지 213 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 7과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 제1 면역글로불린 릴랙신 단백질은 서열번호 201 내지 213 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 단백질은 서열번호 7과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 170 내지 182 중 어느 한 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 3의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 170 내지 182 중 어느 한 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 3의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 융합 단백질은 서열번호 170 내지 182 중 어느 한 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 제2 면역글로불린 단백질은 서열번호 3의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 214 및 215 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 8에 기초한, 또는 서열번호 8로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 214 및 215 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 8과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 단백질을 포함할 수 있다. 제1 면역글로불린 릴랙신 단백질은 서열번호 214 및 215 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 단백질은 서열번호 8과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 183 및 184 중 어느 한 뉴클레오티드 서열에 의해 코팅된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 4의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 면역글로불린 릴랙신 융합 단백질은 (a) 서열번호 183 및 184 중 어느 한 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 4의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 단백질을 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 융합 단백질은 서열번호 183 및 184 중 어느 한 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 제2 면역글로불린 단백질은 서열번호 4의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 이중 융합 단백질
본원은 (a) 제1 치료 펩티드에 부착된 제1 면역글로불린 영역; 및 (b) 제2 치료 펩티드를 포함하는 면역글로불린 이중 융합 단백질로서, 제1 치료 펩티드가 제1 면역글로불린 영역의 아미노 말단에 부착되어 있는 것인 면역글로불린 이중 융합 단백질도 개시한다. 제1 치료 펩티드와 제2 치료 펩티드는 동일할 수 있다. 제1 치료 펩티드와 제2 치료 펩티드는 상이할 수 있다. 면역글로불린 이중 융합 단백질은 제2 면역글로불린 영역을 추가로 포함할 수 있다. 제2 치료 펩티드는 제1 면역글로불린 영역 또는 제2 면역글로불린 영역에 연결될 수 있다. 제1 면역글로불린 영역은 면역글로불린의 경쇄 또는 중쇄에 기초한, 또는 이러한 경쇄 또는 중쇄로부터 유래된 아미노산을 포함할 수 있다. 제2 면역글로불린 영역은 면역글로불린의 경쇄 또는 중쇄에 기초한, 또는 이러한 경쇄 또는 중쇄로부터 유래된 아미노산을 포함할 수 있다. 제1 면역글로불린 영역은 경쇄를 포함할 수 있고 제2 면역글로불린은 중쇄를 포함할 수 있다. 제1 면역글로불린 영역은 중쇄를 포함할 수 있고 제2 면역글로불린은 중쇄를 포함할 수 있다. 제2 치료 펩티드는 면역글로불린 영역의 아미노 말단, 카복실 말단, CDR 또는 루프를 포함하나 이들로 한정되지 않는, 제1 또는 제2 면역글로불린 영역의 임의의 아미노산에 연결될 수 있다. 일부 실시양태들에서, 제1 면역글로불린 영역과 제2 면역글로불린 영역은 하나 이상의 디설파이드 결합을 통해 연결된다. 일부 실시양태들에서, 제1 면역글로불린 영역과 제2 면역글로불린 영역은 연결 펩티드를 통해 연결된다. 제2 치료 펩티드는 연장제 및/또는 링커 펩티드의 사용을 통해 제1 또는 제2 면역글로불린 영역에 부착될 수 있다. 제2 치료 펩티드는 프로테아제 절단 부위의 사용을 통해 제1 또는 제2 면역글로불린 영역에 부착될 수 있다.
이중 융합 단백질은 치료 펩티드로서 렙틴 및 엑센딘-4를 포함할 수 있다. 이중 융합 단백질은 치료 펩티드로서 렙틴 및 글루카곤 유사체를 포함할 수 있다.
이중 융합 단백질은 서열번호 43, 44 또는 50과 적어도 약 50% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 중쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 43, 44 또는 50과 적어도 약 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 중쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 43, 44 또는 50과 적어도 약 70% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 중쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 43, 44 또는 50과 적어도 약 80% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 중쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 43, 44 또는 50과 적어도 약 90% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 중쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 적어도 약 50% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 경쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 적어도 약 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 경쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 적어도 약 70% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 경쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 적어도 약 80% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 경쇄 융합체를 포함할 수 있다. 이중 융합 단백질은 서열번호 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221과 적어도 약 90% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 경쇄 융합체를 포함할 수 있다.
이중 융합 단백질의 적어도 부분은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 50% 상동성인 하나 이상의 핵산 서열에 의해 코딩될 수 있다. 이중 융합 단백질의 적어도 부분은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 하나 이상의 핵산 서열에 의해 코딩될 수 있다. 이중 융합 단백질의 적어도 부분은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 70% 상동성인 하나 이상의 핵산 서열에 의해 코딩될 수 있다. 이중 융합 단백질의 적어도 부분은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 80% 상동성인 하나 이상의 핵산 서열에 의해 코딩될 수 있다. 이중 융합 단백질의 적어도 부분은 서열번호 9 내지 41, 161 내지 191 및 265 중 어느 한 서열과 적어도 약 90% 상동성인 하나 이상의 핵산 서열에 의해 코딩될 수 있다.
이중 융합 단백질은 2개 이상의 치료 펩티드들을 포함할 수 있고, 이때 치료 펩티드들 중 적어도 하나는 서열번호 95 내지 114 및 230 내지 236 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열에 기초하거나 이러한 아미노산 서열로부터 유래된다. 치료 펩티드는 서열번호 95 내지 114 및 230 내지 236 중 어느 한 서열과 적어도 약 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 95 내지 114 및 230 내지 236 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 95 내지 114 및 230 내지 236 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 95 내지 114 및 230 내지 236 중 어느 한 서열과 적어도 약 90% 상동성인 아미노산 서열을 포함할 수 있다.
일부 실시양태들에서, 이중 융합 단백질은 2개 이상의 치료 펩티드들을 포함할 수 있고, 이때 치료 펩티드들 중 적어도 하나는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 50% 상동성인 뉴클레오티드 서열에 의해 코딩된다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 70% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 80% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 90% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다.
이중 융합 단백질은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 90% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 70%, 80%, 90% 또는 95% 상동성인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 면역글로불린 Fab 영역을 포함할 수 있다.
이중 융합 단백질은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 50% 상동성인 하나 이상의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 하나 이상의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 70% 상동성인 하나 이상의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 80% 상동성인 하나 이상의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 90% 상동성인 하나 이상의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 영역을 포함할 수 있다. 이중 융합 단백질은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 70%, 80%, 90% 또는 95% 상동성인 하나 이상의 뉴클레오티드 서열에 의해 코딩된 면역글로불린 Fab 영역을 포함할 수 있다.
본원은 면역글로불린 렙틴/엑센딘-4 이중 융합 단백질을 추가로 개시한다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 42에 기초한, 또는 서열번호 42로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 43 또는 44에 기초한, 또는 서열번호 43 또는 44로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 42와 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 43 또는 44와 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 42와 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 43 또는 44와 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 이중 융합 단백질은 (a) 서열번호 9의 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 10 또는 11의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 9의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 10 또는 11의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 9의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 10 또는 11의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다.
본원은 면역글로불린 렙틴/ZP1CEX 이중 융합 단백질도 개시한다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 46에 기초한, 또는 서열번호 46으로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 43 또는 44에 기초한, 또는 서열번호 43 또는 44로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 46과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 43 또는 44와 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 46과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 43 또는 44와 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 이중 융합 단백질은 (a) 서열번호 13의 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 10 또는 11의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 13의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 10 또는 11의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 13의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 10 또는 11의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다.
본원은 면역글로불린 엑센딘-4/글루카곤 이중 융합 단백질을 추가로 개시한다. 일부 실시양태들에서, 면역글로불린 엑센딘-4/글루카곤 이중 융합 단백질은 대사 질환, 예컨대, 비만 및/또는 당뇨병을 치료하도록 구성된다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 192에 기초한, 또는 서열번호 192로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 193 및 194 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 192와 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 193 및 194 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 192와 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 193 및 194 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 이중 융합 단백질은 (a) 서열번호 161의 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 162 또는 163의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 161의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 162 또는 163의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 161의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 162 또는 163의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다.
본원은 면역글로불린 엑센딘-4/ZP1 이중 융합 단백질도 개시한다. 일부 실시양태들에서, 면역글로불린 엑센딘-4/ZP1 이중 융합 단백질은 대사 질환, 예컨대, 비만 및/또는 당뇨병을 치료하도록 구성된다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 42에 기초한, 또는 서열번호 42로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 197 및 198 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 42와 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 197 및 198 중 어느 한 서열과 적어도 약 50 동일한 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 42와 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 197 및 198 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 이중 융합 단백질은 (a) 서열번호 9의 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 166 또는 167의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 이중 융합 단백질은 (a) 서열번호 9의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 166 또는 167의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 9의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 166 또는 167의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다.
본원은 면역글로불린 엑센딘-4/글루카곤 유사(예를 들면, GLP-1, GLP-2) 이중 융합 단백질도 개시한다. 일부 실시양태들에서, 면역글로불린 엑센딘-4/글루카곤 유사 이중 융합 단백질은 대사 질환, 예컨대, 비만 및/또는 당뇨병을 치료하도록 구성된다. 면역글로불린 엑센딘-4/글루카곤 유사 융합 단백질은 (a) 서열번호 216 및 217 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 42에 기초한, 또는 서열번호 42로부터 유래된 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 엑센딘-4/글루카곤 유사 융합 단백질은 (a) 서열번호 216 및 217 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함하는 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 42와 적어도 약 50% 동일한 아미노산 서열을 포함하는 제2 면역글로불린 융합 단백질을 포함할 수 있다. 제1 면역글로불린 융합 단백질은 서열번호 216 및 217 중 어느 한 서열과 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 제2 면역글로불린 융합 단백질은 서열번호 42와 적어도 약 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다.
면역글로불린 엑센딘-4/글루카곤 유사 융합 단백질은 (a) 서열번호 185 및 186 중 어느 한 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 9의 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 면역글로불린 엑센딘-4/글루카곤 유사 융합 단백질은 (a) 서열번호 185 및 186 중 어느 한 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제1 면역글로불린 융합 단백질; 및 (b) 서열번호 9의 뉴클레오티드 서열과 적어도 50% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된 제2 면역글로불린 융합 단백질을 포함할 수 있다. 일부 실시양태들에서, 제1 면역글로불린 융합 단백질은 서열번호 185 및 186 중 어느 한 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 제2 면역글로불린 융합 단백질은 서열번호 9의 뉴클레오티드 서열과 적어도 60%, 70%, 75%, 80%, 90%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩된다.
제2 면역글로불린 융합체
일부 실시양태들에서, 면역글로불린 융합 단백질은 (a) 제1 면역글로불린 영역의 아미노 말단에 부착된 제1 치료 펩티드, 및 (b) 제2 면역글로불린 영역을 포함한다. 제2 면역글로불린 영역은 하나 이상의 비면역글로불린 영역에 부착되어, 제2 면역글로불린 융합체를 생성할 수 있다. 일부 실시양태들에서, 비면역글로불린 영역은 면역글로불린의 아미노산 서열과 80% 초과 수준만큼 동일한 아미노산 서열을 포함하지 않는다. 일부 실시양태들에서, 비면역글로불린 영역은 면역글로불린의 아미노산 서열과 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 99% 초과 수준만큼 동일한 아미노산 서열을 포함하지 않는다. 일부 실시양태들에서, 면역글로불린으로부터 유래되지 않은 펩티드는 면역글로불린의 아미노산 서열과 100% 동일한 아미노산 서열을 포함하지 않는다. 일부 실시양태들에서, 비면역글로불린 영역은 치료 펩티드 및 하나 이상의 연장제 펩티드를 포함한다. 일부 실시양태들에서, 비면역글로불린 영역은 치료 펩티드 및 하나 이상의 링커 펩티드를 포함한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 프로테아제 절단 부위를 포함한다. 일부 실시양태들에서, 비면역글로불린 영역은 프로테아제 절단 부위를 포함한다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 내부 링커를 포함한다. 일부 실시양태들에서, 비면역글로불린 영역은 면역글로불린 영역에 존재하는 루프에서 면역글로불린 영역에 연결된다. 일부 실시양태들에서, 상기 루프는 상보성 결정 영역(CDR)의 아미노산을 포함한다. CDR은 CDR1, CDR2, CDR3 및 CDR4를 포함할 수 있다. 일부 실시양태들에서, 비면역글로불린 영역은 면역글로불린 영역의 기초 또는 기원인 면역글로불린 영역의 적어도 일부를 대체한다. 비면역글로불린 영역은 상보성 결정 영역의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 가변 도메인의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 불변 도메인의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 중쇄의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 경쇄의 적어도 일부를 대체할 수 있다.
예시적인 제2 면역글로불린 융합체는 식 IA 내지 XIIB로 표시된다.
식 IA는 연장제 펩티드(E1) 및 제2 치료 펩티드(T2)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체를 보여준다.
식 IIA는 제2 치료 펩티드(T2)에 부착된 2개의 연장제 펩티드들(E1 및 E2)을포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체를 보여준다.
식 IIIA는 제2 치료 펩티드(T2)에 부착된 링커(L1)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체로서, 상기 링커 및 제2 치료 펩티드가 2개의 연장제 펩티드들(E1 및 E2) 사이에 위치하는 것인 제2 면역글로불린 융합체를 보여준다.
식 IVA는 제2 치료 펩티드(T2)에 부착된 단백질분해성 절단 부위(P1)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체로서, 이때 상기 단백질분해성 절단 부위 및 제2 치료 펩티드가 2개의 연장제 펩티드들(E1 및 E2) 사이에 위치하는 것인 제2 면역글로불린 융합체를 보여준다. 식 IVB는 단백질분해성 절단 부위가 프로테아제에 의해 절단되어, 제2 치료 펩티드의 한 말단의 방출을 초래하는 것인 식 VA의 절단된 버전을 보여준다.
식 VA는 링커(L1) 및 단백질분해성 절단 부위(P1)에 부착된 제2 치료 펩티드(T2)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체로서, 제2 치료 펩티드, 상기 링커 및 상기 단백질분해성 절단 부위가 2개의 연장제 펩티드들(E1 및 E2) 사이에 위치하는 것인 제2 면역글로불린 융합체를 보여준다. 식 VB는 단백질분해성 절단 부위가 프로테아제에 의해 절단되어, 제2 치료 펩티드의 한 말단의 방출을 초래하는 것인 식 VA의 절단된 버전을 보여준다.
식 VIA는 2개의 연장제 펩티드들(E1 및 E2), 2개의 링커들(L1 및 L2), 2개의 단백질분해성 절단 부위들(P1 및 P2) 및 제2 치료 펩티드(T2)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체를 나타낸다. 식 VIB는 제2 치료 펩티드의 N 말단 및 C 말단 상에 위치한 단백질분해성 절단 부위가 프로테아제에 의해 절단되어, 제2 면역글로불린 융합체로부터의 제2 치료 펩티드의 방출을 초래하는 것인 식 VIA의 절단된 버전을 보여준다.
식 VIIA는 제2 치료 펩티드(T2)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체를 보여준다.
식 VIIIA는 제2 치료 펩티드(T2)에 부착된 링커(L1)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체를 보여준다.
식 IXA는 링커(L1), 단백질분해성 절단 부위(P1) 및 제2 치료 펩티드(T2)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체로서, 상기 단백질분해성 절단 부위가 상기 링커와 제2 치료 펩티드 사이에 위치하는 것인 제2 면역글로불린 융합체를 보여준다.
식 XA는 제2 치료 펩티드(T2)에 부착된 단백질분해성 절단 부위(P1)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합 단백질을 보여준다. 식 XB는 단백질분해성 절단 부위가 프로테아제에 의해 절단되어, 제2 치료 펩티드의 한 말단의 방출을 초래하는 것인 식 XA의 절단된 버전을 보여준다.
식 XIA는 링커(L1), 제2 치료 펩티드(T2) 및 단백질분해성 절단 부위(P1)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체로서, 제2 치료 펩티드가 상기 링커와 상기 단백질분해성 절단 부위 사이에 위치하는 것인 제2 면역글로불린 융합체를 보여준다. 식 XIB는 단백질분해성 절단 부위가 프로테아제에 의해 절단되어, 제2 치료 펩티드의 한 말단의 방출을 초래하는 것인 식 XIA의 절단된 버전을 보여준다.
식 XIIA는 2개의 링커들(L1 및 L2), 2개의 단백질분해성 절단 부위들(P1 및 P2) 및 제2 치료 펩티드(T2)를 포함하는 비면역글로불린 영역에 부착된 제2 면역글로불린 영역(A2)을 포함하는 제2 면역글로불린 융합체를 보여준다. 식 XIIB는 제2 치료 펩티드의 N 말단 및 C 말단 상에 위치한 단백질분해성 절단 부위가 프로테아제에 의해 절단되어, 제2 면역글로불린 융합체로부터의 제2 치료 펩티드의 방출을 초래하는 것인 식 XIIA의 절단된 버전을 보여준다.
면역글로불린 영역
본원에 개시된 면역글로불린 융합 단백질은 하나 이상의 면역글로불린 영역을 포함한다. 면역글로불린 영역은 면역글로불린 또는 이의 단편을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 중쇄, 면역글로불린 경쇄 또는 이들의 조합의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 2개 이상의 면역글로불린 쇄들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 3개 이상의 면역글로불린 쇄들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 4개 이상의 면역글로불린 쇄들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 5개 이상의 면역글로불린 쇄들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 2개의 면역글로불린 중쇄들 및 2개의 면역글로불린 경쇄들을 포함할 수 있다.
면역글로불린 영역은 전체 면역글로불린 분자를 포함할 수 있거나, 중쇄, 경쇄, 가변 도메인, 불변 도메인, 상보성 결정 영역(CDR), 골격 영역, 단편 항원 결합(Fab) 영역, Fab', F(ab')2, F(ab')3, Fab', 단편 결정화가능한(Fc) 영역, 단일 쇄 가변 단편(scFV), di-scFv, 단일 도메인 면역글로불린, 삼작용성 면역글로불린, 화학적으로 연결된 F(ab')2, 및 이들의 임의의 조합을 포함하나 이들로 한정되지 않는 면역글로불린의 단편을 포함하는 임의의 폴리펩티드를 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 중쇄는 전체 중쇄 또는 중쇄의 부분을 포함할 수 있다. 예를 들면, 중쇄로부터 유래된 가변 도메인 또는 이의 영역은 중쇄 또는 중쇄의 영역으로서 지칭될 수 있다. 일부 실시양태들에서, 면역글로불린 경쇄는 전체 경쇄 또는 경쇄의 부분을 포함할 수 있다. 예를 들면, 경쇄로부터 유래된 가변 도메인 또는 이의 영역은 경쇄 또는 경쇄의 영역으로서 지칭될 수 있다. 단일 도메인 면역글로불린은 단일 단량체성 가변 면역글로불린 도메인, 예를 들면, 상어 가변 신규 항원 수용체 면역글로불린 단편(VNAR)을 포함하나 이것으로 한정되지 않는다.
면역글로불린은 IgA, IgD, IgE, IgG, IgM, IgY 및 IgW를 포함하나 이들로 한정되지 않는, 당업자에게 공지되어 있는 임의의 유형으로부터 유래될 수 있다. 면역글로불린 영역은 1개, 2개, 3개, 4개 및 5개 유닛을 포함하나 이들로 한정되지 않는 하나 이상의 유닛을 포함할 수 있다. 작용성 유닛은 비면역글로불린 영역, 중쇄, 경쇄, 가변 도메인, 불변 도메인, 상보성 결정 영역(CDR), 골격 영역, 단편 항원 결합(Fab) 영역, Fab', F(ab')2, F(ab')3, Fab', 단편 결정화가능한(Fc) 영역, 단일 쇄 가변 단편(scFV), di-scFv, 단일 도메인 면역글로불린, 삼작용성 면역글로불린, 화학적으로 연결된 F(ab')2, 및 이들의 임의의 조합 또는 단편을 포함할 수 있으나 이들로 한정되지 않는다. 비면역글로불린 영역은 탄수화물, 지질, 소분자 및 치료 펩티드를 포함하나 이들로 한정되지 않는다. 면역글로불린 영역은 하나 이상의 디설파이드 결합에 의해 연결된 하나 이상의 유닛을 포함할 수 있다. 면역글로불린 영역은 펩티드 링커, 예를 들면, scFv 면역글로불린에 의해 연결된 하나 이상의 유닛을 포함할 수 있다. 면역글로불린은 아미노산 돌연변이, 치환 및/또는 결실을 갖는 면역글로불린을 포함하는 재조합 면역글로불린일 수 있다. 면역글로불린은 화학적 변경을 포함하는 재조합 면역글로불린일 수 있다. 면역글로불린은 면역글로불린-약물 접합체의 전부 또는 일부를 포함할 수 있다.
면역글로불린 영역은 면역글로불린 중쇄의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 중쇄 또는 이의 부분을 포함할 수 있다. 면역글로불린 영역은 2개 이상의 면역글로불린 중쇄들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 중쇄와 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 중쇄와 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 중쇄와 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 중쇄와 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 중쇄와 적어도 약 90% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 중쇄는 서열번호 6 또는 8을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 6 및 8 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함한다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 6 및 8 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함한다.
면역글로불린 영역은 면역글로불린 중쇄의 5개, 10개, 15개, 20개, 25개, 30개, 35개, 40개, 45개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 중쇄의 100개, 150개, 200개, 250개, 300개, 350개, 400개, 450개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다.
면역글로불린 중쇄는 서열번호 2 또는 4에 기초한, 또는 서열번호 2 또는 4로부터 유래된 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄는 서열번호 2 또는 4와 적어도 약 50% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄는 서열번호 2 또는 4와 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄는 서열번호 2 또는 4와 적어도 약 75% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 중쇄는 서열번호 2 또는 4와 적어도 약 85% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 2 및 4 중 어느 한 뉴클레오티드 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 2 및 4 중 어느 한 뉴클레오티드 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 영역은 면역글로불린 경쇄의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 경쇄 또는 이의 부분을 포함할 수 있다. 면역글로불린 영역은 2개 이상의 면역글로불린 경쇄들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 경쇄와 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 경쇄와 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 경쇄와 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 경쇄와 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 경쇄와 적어도 약 90% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 경쇄는 서열번호 5 또는 7을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 및 7 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함한다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 및 7 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함한다.
면역글로불린 영역은 면역글로불린 경쇄의 5개, 10개, 15개, 20개, 25개, 30개, 35개, 40개, 45개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 경쇄의 100개, 150개, 200개, 250개, 300개, 350개, 400개, 450개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다.
면역글로불린 경쇄는 서열번호 1 또는 3에 기초한, 또는 서열번호 1 또는 3으로부터 유래된 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄는 서열번호 1 또는 3과 적어도 약 50% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄는 서열번호 1 또는 3과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄는 서열번호 1 또는 3과 적어도 약 75% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄는 서열번호 1 또는 3과 적어도 약 85% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 1 및 3 중 어느 한 뉴클레오티드 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 1 및 3 중 어느 한 뉴클레오티드 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열에 의해 코딩된다.
면역글로불린 영역은 가변 도메인의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 하나 이상의 가변 도메인 또는 이의 부분을 포함할 수 있다. 면역글로불린 영역은 2개, 3개, 4개 또는 5개 이상의 가변 도메인들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 가변 도메인의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개, 100개, 120개, 140개, 160개, 180개, 200개, 225개, 250개, 275개, 300개, 350개, 400개 또는 500개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 아미노산은 비연속적일 수 있다.
면역글로불린 영역은 불변 도메인의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 하나 이상의 불변 도메인 또는 이의 부분을 포함할 수 있다. 면역글로불린 영역은 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 불변 도메인들 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 불변 도메인의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개, 100개, 120개, 140개, 160개, 180개, 200개, 225개, 250개, 275개, 300개, 350개, 400개, 500개, 600개, 700개, 800개, 900개, 1000개, 1200개 또는 1400개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 아미노산은 비연속적일 수 있다.
면역글로불린 영역은 상보성 결정 영역(CDR)의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 하나 이상의 상보성 결정 영역(CDR) 또는 이의 부분을 포함할 수 있다. 면역글로불린 영역은 2개, 3개, 4개 또는 5개 이상의 상보성 결정 영역들(CDR들) 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 6개, 7개 또는 8개 이상의 상보성 결정 영역들(CDR들) 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 4개 이상의 상보성 결정 영역들(CDR들) 또는 이들의 부분을 포함할 수 있다. 면역글로불린 영역은 9개, 10개 또는 11개 이상의 상보성 결정 영역들(CDR들) 또는 이들의 부분을 포함할 수 있다. 하나 이상의 CDR은 CDR1, CDR2, CDR3 또는 이들의 조합일 수 있다. 하나 이상의 CDR은 CDR1일 수 있다. 하나 이상의 CDR은 CDR2일 수 있다. 하나 이상의 CDR은 CDR3일 수 있다. CDR은 중쇄 CDR일 수 있다. 하나 이상의 CDR은 경쇄 CDR일 수 있다.
면역글로불린 영역은 CDR의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 CDR의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 3개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 CDR의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 5개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 CDR의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 아미노산은 비연속적일 수 있다.
면역글로불린 영역은 항-T 세포 수용체 면역글로불린의 적어도 부분에 기초할 수 있거나 이러한 부분으로부터 유래될 수 있다. 면역글로불린 영역은 항-B 세포 수용체 면역글로불린의 적어도 부분에 기초할 수 있거나 이러한 부분으로부터 유래될 수 있다.
면역글로불린 영역은 항-T 세포 보조수용체 면역글로불린의 적어도 부분에 기초할 수 있거나 이러한 부분으로부터 유래될 수 있다. 면역글로불린 영역은 항-CD3 면역글로불린의 적어도 부분에 기초할 수 있거나 이러한 부분으로부터 유래될 수 있다. 면역글로불린 영역은 항-CD3 면역글로불린에 기초할 수 있거나 이러한 부분으로부터 유래될 수 있다. 항-CD3 면역글로불린은 UCHT1일 수 있다. 면역글로불린 영역은 항-CD3 면역글로불린의 Fab 단편의 적어도 부분에 기초할 수 있거나 이러한 부분으로부터 유래될 수 있다. 면역글로불린 영역은 항-CD3 면역글로불린의 면역글로불린 단편에 기초할 수 있거나 이러한 단편으로부터 유래될 수 있다.
면역글로불린 영역은 세포 상의 수용체의 적어도 부분에 결합하는 면역글로불린 또는 면역글로불린 단편에 기초할 수 있거나 이러한 면역글로불린 또는 면역글로불린 단편으로부터 유래될 수 있다. 면역글로불린 영역은 세포 상의 보조수용체의 적어도 부분에 결합하는 면역글로불린 또는 면역글로불린 단편에 기초할 수 있거나 이러한 면역글로불린 또는 면역글로불린 단편으로부터 유래될 수 있다. 면역글로불린 영역은 세포 상의 항원 또는 세포 표면 마커의 적어도 부분에 결합하는 면역글로불린 또는 면역글로불린 단편에 기초할 수 있거나 이러한 면역글로불린 또는 면역글로불린 단편으로부터 유래될 수 있다. 세포는 조혈 세포일 수 있다. 조혈 세포는 골수 세포일 수 있다. 골수 세포는 적혈구, 혈전구, 호중구, 단핵구, 대식세포, 호산구, 호염기구 또는 비만 세포일 수 있다. 조혈 세포는 림프 세포일 수 있다. 림프 세포는 B 세포, T 세포 또는 NK 세포일 수 있다. 조혈 세포는 백혈구일 수 있다. 조혈 세포는 림프구일 수 있다.
면역글로불린 영역은 T 세포 상의 수용체의 적어도 부분에 결합하는 면역글로불린 또는 면역글로불린 단편에 기초할 수 있거나 이러한 면역글로불린 또는 면역글로불린 단편으로부터 유래될 수 있다. 상기 수용체는 T 세포 수용체(TCR)일 수 있다. TCR은 TCR 알파, TCR 베타, TCR 감마 및/또는 TCR 델타를 포함할 수 있다. 상기 수용체는 T 세포 수용체 제타일 수 있다.
면역글로불린 영역은 림프구, B 세포, 대식세포, 단핵구, 호중구 및/또는 NK 세포 상의 수용체의 적어도 부분에 결합하는 면역글로불린 또는 면역글로불린 단편에 기초할 수 있거나 이러한 면역글로불린 또는 면역글로불린 단편으로부터 유래될 수 있다. 상기 수용체는 Fc 수용체일 수 있다. Fc 수용체는 Fc-감마 수용체, Fc-알파 수용체 및/또는 Fc-엡실론 수용체일 수 있다. Fc-감마 수용체는 FcγRI(CD64), FcγRIIA(CD32), FcγRIIB(CD32), FcγRIIIA(CD16a) 및 FcγRIIIB(CD16b)를 포함하나 이들로 한정되지 않는다. Fc-알파 수용체는 FcαRI을 포함하나 이것으로 한정되지 않는다. Fc-엡실론 수용체는 FcεRI 및 FcεRII를 포함하나 이들로 한정되지 않는다. 상기 수용체는 CD89(IgA 수용체의 Fc 단편 또는 FCAR)일 수 있다.
면역글로불린 영역은 T 세포 상의 보조수용체의 적어도 부분에 결합하는 면역글로불린 또는 면역글로불린 단편에 기초할 수 있거나 이러한 면역글로불린 또는 면역글로불린 단편으로부터 유래될 수 있다. 상기 보조수용체는 CD3, CD4 및/또는 CD8일 수 있다. 면역글로불린 영역은 CD3 보조수용체에 결합하는 면역글로불린 단편에 기초할 수 있거나 이러한 단편으로부터 유래될 수 있다. CD3 보조수용체는 CD3-감마, CD3-델타 및/또는 CD3-엡실론을 포함할 수 있다. CD8은 CD8-알파 쇄 및/또는 CD8-베타 쇄를 포함할 수 있다.
일부 실시양태들에서, 면역글로불린 영역은 포유동물 표적에 대해 특이적이지 않다. 일부 실시양태들에서, 면역글로불린은 항-바이러스 면역글로불린이다. 일부 실시양태들에서, 면역글로불린은 항-세균 면역글로불린이다. 일부 실시양태들에서, 면역글로불린은 항-기생충 면역글로불린이다. 일부 실시양태들에서, 면역글로불린은 항-진균 면역글로불린이다. 일부 실시양태들에서, 면역글로불린 영역은 면역글로불린 백신으로부터 유래된다.
일부 실시양태들에서, 면역글로불린 영역은 악톡수맙(actoxumab), 베즐로톡수맙(bezlotoxumab), CR6261, 에도바코맙(edobacomab), 에푼구맙(efungumab), 엑스비비루맙(exbivirumab), 펠비주맙(felvizumab), 포라비루맙(foravirumab), 이발리주맙(ibalizumab)(TMB-355, TNX-355), 리비비루맙(libivirumab), 모타비주맙(motavizumab), 네바쿠맙(nebacumab), 파기박시맙(pagibaximab), 팔리비주맙(palivizumab), 파노바쿠맙(panobacumab), 라피비루맙(rafivirumab), 락시바쿠맙(raxibacumab), 레가비루맙(regavirumab), 세비루맙(sevirumab)(MSL-109), 수비주맙(suvizumab), 테피바주맙(tefibazumab), 투비루맙(tuvirumab) 및 우르톡사주맙(urtoxazumab)을 포함하나 이들로 한정되지 않는 면역글로불린에 기초하거나 이러한 면역글로불린으로부터 유래된다.
일부 실시양태들에서, 면역글로불린 영역은 클로스트리듐 디피실(Clostridium difficile), 오르토믹소바이러스(Orthomyxoviruses)(인플루엔자바이러스(Influenzavirus) A, 인플루엔자바이러스 B, 인플루엔자바이러스 C, 이사바이러스(Isavirus), 토고토바이러스(Thogotovirus)), 에스케리키아 콜라이(Escherichia coli), 칸디다(Candida), 광견병(Rabies), 인간 면역결핍 바이러스, 간염, 스타필로코커스(Staphylococcus), 호흡기 세포융합 바이러스(Respiratory Syncytial Virus), 슈도모나스 애루기노사(Pseudomonas aeruginosa), 바실러스 안쓰라시스(Bacillus anthracis), 사이토메갈로바이러스(Cytomegalovirus) 또는 스타필로코커스 아우레우스(Staphylococcus aureus)를 표적화하는 면역글로불린에 기초하거나 이러한 면역글로불린으로부터 유래된다.
면역글로불린 영역은 항-바이러스 면역글로불린에 기초할 수 있거나 이러한 면역글로불린으로부터 유래될 수 있다. 항-바이러스 면역글로불린은 바이러스 단백질의 에피토프에 대해 유도될 수 있다. 항-세균 면역글로불린은 아데노바이러스(Adenoviruses), 헤르페스바이러스(Herpesviruses), 폭스바이러스(Poxviruses), 파보바이러스(Parvoviruses), 레오바이러스(Reoviruses), 피코르나바이러스(Picornaviruses), 토가바이러스(Togaviruses), 오르토믹소바이러스(Orthomyxoviruses), 라브도바이러스(Rhabdoviruses), 레트로바이러스(Retroviruses) 및 헤파드나바이러스(Hepadnaviruses)를 포함하나 이들로 한정되지 않는 하나 이상의 바이러스를 표적화할 수 있다. 바이러스 단백질은 호흡기 세포융합 바이러스로부터 유래될 수 있다. 바이러스 단백질은 호흡기 세포융합 바이러스의 F 단백질일 수 있다. 에피토프는 F 단백질의 A 항원성 부위에 존재할 수 있다. 항-바이러스 면역글로불린은 팔리비주맙에 기초할 수 있거나 팔리비주맙으로부터 유래될 수 있다. 면역글로불린은 항-바이러스 백신에 기초할 수 있거나 이러한 백신으로부터 유래될 수 있다. 항-바이러스 면역글로불린은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙에 기초할 수 있거나 이러한 면역글로불린으로부터 유래될 수 있다.
면역글로불린 영역은 항-바이러스 면역글로불린 G에 기초할 수 있거나 항-바이러스 면역글로불린 G로부터 유래될 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 항-바이러스 면역글로불린 M에 기초한, 또는 항-바이러스 면역글로불린 M으로부터 유래된 아미노산 서열을 포함한다.
면역글로불린 영역은 항-바이러스 면역글로불린 G 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-바이러스 면역글로불린 G 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 팔리비주맙 면역글로불린에 기초할 수 있거나 팔리비주맙 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 팔리비주맙 면역글로불린 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 팔리비주맙 면역글로불린 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린에 기초할 수 있거나 이러한 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 엑스비비루맙, 포라비루맙, 리비비루맙, 라피비루맙, 레가비루맙, 세비루맙, 투비루맙, 펠비주맙, 모타비주맙, 팔리비주맙 및/또는 수비주맙 면역글로불린 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항-세균 면역글로불린에 기초할 수 있거나 항-세균 면역글로불린으로부터 유래될 수 있다. 항-세균 면역글로불린은 세균 단백질의 에피토프에 대해 유도될 수 있다. 항-세균 면역글로불린은 아세토박터 아우란티우스(Acetobacter aurantius), 아그로박테리움 라디오박터(Agrobacterium radiobacter), 아나플라스마 파고사이토필룸(Anaplasma phagocytophilum), 아조리조븀 카울리노단스(Azorhizobium caulinodans), 바실러스 안쓰라시스(Bacillus anthracis), 바실러스 브레비스(Bacillus brevis), 바실러스 세레우스(Bacillus cereus), 바실러스 서브틸리스(Bacillus subtilis), 박테로이데스 프라길리스(Bacteroides fragilis), 박테로이데스 진지발리스(Bacteroides gingivalis), 박테로이데스 멜라니노제니커스(Bacteroides melaninogenicus), 바르토넬라 퀸타나(Bartonella quintana), 보르데텔라 브론키셉티카(Bordetella bronchiseptica), 보르데텔라 퍼투시스(Bordetella pertussis), 보렐리아 부르그도르페리(Borrelia burgdorferi), 브루셀라 아보르투스(Brucella abortus), 브루셀라 멜리텐시스(Brucella melitensis), 브루셀라 수이스(Brucella suis), 부르크홀데리아 말레이(Burkholderia mallei), 부르크홀데리아 슈도말레이(Burkholderia pseudomallei), 부르크홀데리아 세파시아(Burkholderia cepacia), 칼라임마토박테리움 그라눌로마티스(Calymmatobacterium granulomatis), 캄필로박터 콜라이(Campylobacter coli), 캄필로박터 페투스(Campylobacter fetus), 캄필로박터 제주니(Campylobacter jejuni), 캄필로박터 파일로리(Campylobacter pylori), 클라마이디아 트라코마티스(Chlamydia trachomatis), 클라마이도필라 뉴모니아(Chlamydophila pneumoniae), 클라마이도필라 시타시(Chlamydophila psittaci), 클로스트리듐 보툴리눔(Clostridium botulinum), 클로스트리듐 디피실(Clostridium difficile), 코리네박테리움 디프테리아(Corynebacterium diphtheriae), 코리네박테리움 푸시포름(Corynebacterium fusiforme), 콕시엘라 부르네티이(Coxiella burnetii), 엔테로박터 클로아카(Enterobacter cloacae), 엔테로코커스 패칼리스(Enterococcus faecalis), 엔테로코커스 패시움(Enterococcus faecium), 엔테로코커스 갈리나룸(Enterococcus galllinarum), 엔테로코커스 말로라투스(Enterococcus maloratus), 에스케리키아 콜라이(Escherichia coli), 프란시셀라 툴라렌시스(Francisella tularensis), 푸소박테리움 뉴클레아툼(Fusobacterium nucleatum), 가르드네렐라 바기날리스(Gardnerella vaginalis), 해모필러스 인플루엔자(Haemophilus influenzae), 해모필러스 파라인플루엔자(Haemophilus parainfluenzae), 해모필러스 퍼투시스(Haemophilus pertussis), 해모필러스 바기날리스(Haemophilus vaginalis), 헬리코박터 파일로리(Helicobacter pylori), 클렙시엘라 뉴모니아(Klebsiella pneumoniae), 락토바실러스 악시도필러스(Lactobacillus acidophilus), 락토코커스 락티스(Lactococcus lactis), 레기오넬라 뉴모필라(Legionella pneumophila), 리스테리아 모노사이토게네스(Listeria monocytogenes), 메타노박테리움 엑스트로쿠엔스(Methanobacterium extroquens), 마이크로박테리움 멀티포름(Microbacterium multiforme), 마이크로코커스 루테우스(Micrococcus luteus), 모락셀라 카타르할리스(Moraxella catarrhalis), 마이코박테리움 플레이(Mycobacterium phlei), 마이코박테리움 스메그마티스(Mycobacterium smegmatis), 마이코박테리움 투버쿨로시스(Mycobacterium tuberculosis), 마이코플라스마 제니탈리움(Mycoplasma genitalium), 마이코플라스마 호미니스(Mycoplasma hominis), 마이코플라스마 뉴모니아(Mycoplasma pneumonie), 네이세리아 고노로에아(Neisseria gonorrhoeae), 네이세리아 메닌기티디스(Neisseria meningitidis), 파스테우렐라 멀토시다(Pasteurella multocida), 파스테우렐라 툴라렌시스(Pasteurella tularensis), 펩토스트렙토코커스(Peptostreptococcus), 포르파이로모나스 진지발리스(Porphyromonas gingivalis), 프레보텔라 멜라니노게니카(Prevotella melaninogenica), 슈도모나스 애루기노사(Pseudomonas aeruginosa), 리조븀 라디오박터(Rhizobium radiobacter), 리케치아 리케치시이(Rickettsia rickettsii), 로티아 덴토카리오사(Rothia dentocariosa), 살모넬라 엔테리티디스(Salmonella enteritidis), 살모넬라 타이피(Salmonella typhi), 살모넬라 타이피무리움(Salmonella typhimurium), 시겔라 다이센테리아(Shigella dysenteriae), 스타필로코커스 아우레우스(Staphylococcus aureus), 스타필로코커스 에피데르미디스(Staphylococcus epidermidis), 스테노트로포모나스 말토필리아(Stenotrophomonas maltophilia), 스트렙토코커스 뉴모니아(Streptococcus pneumoniae), 스트렙토코커스 파이오게네스(Streptococcus pyogenes), 트레포네마 팔리둠(Treponema pallidum), 트레포네마 덴티콜라(Treponema denticola), 비브리오 콜레라(Vibrio cholerae), 비브리오 콤마(Vibrio comma), 비브리오 파라해몰라이티커스(Vibrio parahaemolyticus), 비브리오 불니피커스(Vibrio vulnificus), 예르시니아 엔테로콜리티카(Yersinia enterocolitica) 및 예르시니아 슈도투버쿨로시스(Yersinia pseudotuberculosis)를 포함하나 이들로 한정되지 않는 세균을 표적화할 수 있다. 면역글로불린은 세균 백신에 기초할 수 있거나 세균 백신으로부터 유래될 수 있다. 항-바이러스 면역글로불린은 네바쿠맙(nebacumab), 파노바쿠맙(panobacumab), 락시바쿠맙(raxibacumab), 에도바코맙(edobacomab), 파기박시맙(pagibaximab) 및/또는 테피바주맙(tefibazumab)에 기초할 수 있거나 이러한 면역글로불린으로부터 유래될 수 있다.
면역글로불린 영역은 항-세균 면역글로불린 G에 기초할 수 있거나 항-세균 면역글로불린 G로부터 유래될 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 항-바이러스 면역글로불린 M에 기초한, 또는 항-바이러스 면역글로불린 M으로부터 유래된 아미노산 서열을 포함한다.
면역글로불린 영역은 항-세균 면역글로불린 G 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-세균 면역글로불린 G 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린에 기초할 수 있거나 이러한 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 네바쿠맙, 파노바쿠맙, 락시바쿠맙, 에도바코맙, 파기박시맙 및/또는 테피바주맙 면역글로불린 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항-기생충 면역글로불린에 기초할 수 있거나 항-기생충 면역글로불린으로부터 유래될 수 있다. 항-기생충 면역글로불린은 기생충 단백질의 에피토프에 대해 유도될 수 있다. 항-기생충 면역글로불린은 기생충 아칸타모에바(Acanthamoeba), 발라무티아 만드릴라리스(Balamuthia mandrillaris), 바베시아(Babesia)(바베시아 다이버겐스(B. divergens), 바베시아 비게미나(B. bigemina), 바베시아 에쿠이(B. equi), 바베시아 마이크로프티(B. microfti), 바베시아 던카니(B. duncani)), 발란티듐 콜라이(Balantidium coli), 블라스토사이스티스(Blastocystis), 크립토스포리듐(Cryptosporidium), 디엔타모에바 프라길리스(Dientamoeba fragilis), 엔타모에바 히스토라이티카(Entamoeba histolytica), 기아르디아 람블리아(Giardia lamblia), 이소스포라 벨리(Isospora belli), 레이쉬마니아(Leishmania), 내글레리아 파울레리(Naegleria fowleri), 플라스모듐 팔시파룸(Plasmodium falciparum), 플라스모듐 비박스(Plasmodium vivax), 플라스모듐 오발 쿠르티시(Plasmodium ovale curtisi), 플라스모듐 오발 왈리케리(Plasmodium ovale wallikeri), 플라스모듐 말라리아(Plasmodium malariae), 플라스모듐 날레시(Plasmodium knowlesi), 리노스포리듐 시이베리(Rhinosporidium seeberi), 사르코사이스티스 보비호미니스(Sarcocystis bovihominis), 사르코사이스티스 수이호미니스(Sarcocystis suihominis), 톡소플라스마 곤디이(Toxoplasma gondii), 트리코모나스 바기날리스(Trichomonas vaginalis), 트립파노소마 브루세이(Trypanosoma brucei), 트립파노소마 크루지(Trypanosoma cruzi), 세스토다(Cestoda), 태니아 멀티셉스(Taenia multiceps), 디파일로보트리움 라툼(Diphyllobothrium latum), 에키노코커스 그라눌로서스(Echinococcus granulosus), 에키노코커스 멀티로쿨라리스(Echinococcus multilocularis), 에키노코커스 보겔리(Echinococcus vogeli), 에키노코커스 올리가르트러스(Echinococcus oligarthrus), 하이메놀레피스 나나(Hymenolepis nana), 하이메놀레피스 디미누타(Hymenolepis diminuta), 태니아 사기나타(Taenia saginata), 태니아 솔리움(Taenia solium), 베르티엘라 무크로나타(Bertiella mucronata), 베르티엘라 스투데리(Bertiella studeri), 스피로메트라 에리나세이유로패이(Spirometra erinaceieuropaei), 클로노르키스 시넨시스(Clonorchis sinensis), 클로노르키스 비베리니(Clonorchis viverrini), 디크로코엘리움 덴드리티쿰(Dicrocoelium dendriticum), 파스시올라 헤파티카(Fasciola hepatica), 파스시올라 자이겐티카(Fasciola gigantica), 파스시올롭시스 부스키(Fasciolopsis buski), 그나토스토마 스피니게룸(Gnathostoma spinigerum), 그나토스토마 히스피둠(Gnathostoma hispidum), 메타고니머스 요코가와이(Metagonimus yokogawai), 오피스토르키스 비베리니(Opisthorchis viverrini), 오피스토르키스 펠리네우스(Opisthorchis felineus), 클로노르키스 시넨시스(Clonorchis sinensis), 파라고니머스 웨스터만니(Paragonimus westermani), 파라고니머스 아프리카너스(Paragonimus africanus), 파라고니머스 칼리엔시스(Paragonimus caliensis), 파라고니머스 켈리코티(Paragonimus kellicotti), 파라고니머스 스크르자비니(Paragonimus skrjabini), 파라고니머스 유테로빌라테랄리스(Paragonimus uterobilateralis), 스키스토소마(Schistosoma) 종, 스키스토소마 만소니(Schistosoma mansoni), 스키스토소마 해마토븀(Schistosoma haematobium), 스키스토소마 자포니쿰(Schistosoma japonicum), 스키스토소마 메콘기(Schistosoma mekongi), 에키노스토마 에키나툼(Echinostoma echinatum), 트리코빌하르지아 레겐티(Trichobilharzia regenti), 스키스토소마티다(Schistosomatidae), 안사이클로스토마 듀오데날(Ancylostoma duodenale), 네카토르 아메리카너스(Necator americanus), 안지오스트롱길러스 코스타리센시스(Angiostrongylus costaricensis), 아니사키스(Anisakis), 아스카리스(Ascaris) 종, 아스카리스 룸브리코이데스(Ascaris lumbricoides), 바일리사스카리스 프로사이오니스(Baylisascaris procyonis), 브루지아 말레이이(Brugia malayi), 브루지아 티모리(Brugia timori), 디옥토파임 레날(Dioctophyme renale), 드라쿤쿨러스 메디넨시스(Dracunculus medinensis), 엔테로비우스 베르미쿨라리스(Enterobius vermicularis), 엔테로비우스 그레고리이(Enterobius gregorii), 할리세팔로버스 진지발리스(Halicephalobus gingivalis), 로아 필라리아(Loa filaria), 만소넬라 스트렙토세르카(Mansonella streptocerca), 온코세르카 볼불러스(Onchocerca volvulus), 스트롱길로이데스 스테르코랄리스(Strongyloides stercoralis), 텔라지아 캘리포르니엔시스(Thelazia californiensis), 텔라지아 캘리패다(Thelazia callipaeda), 톡소카라 캐니스(Toxocara canis), 톡소카라 캐티(Toxocara cati), 트리키넬라 스피랄리스(Trichinella spiralis), 트리키넬라 브리토비(Trichinella britovi), 트리키넬라 넬소니(Trichinella nelsoni), 트리키넬라 나티바(Trichinella nativa), 트리쿠리스 트리키우라(Trichuris trichiura), 트리쿠리스 불피스(Trichuris vulpis), 부케레리아 반크로프티(Wuchereria bancrofti), 아르키아칸토세팔라(Archiacanthocephala), 모닐리포르미스 모닐리포르미스(Moniliformis moniliformis), 링구아툴라 세라타(Linguatula serrata), 오에스트로이데아(Oestroidea), 캘리포리다(Calliphoridae), 사르코파기다(Sarcophagidae), 툰가 페네트란스(Tunga penetrans), 데르마토비아 호미니스(Dermatobia hominis), 익소디다(Ixodidae), 아르가시다(Argasidae), 시멕스 렉툴라리우스(Cimex lectularius), 페디쿨러스 휴마너스(Pediculus humanus), 페디쿨러스 휴마너스 코르포리스(Pediculus humanus corporis), 프티러스 푸비스(Pthirus pubis), 데모덱스 폴리쿨로룸(Demodex folliculorum)/브레비스(brevis)/캐니스(canis), 사르콥테스 스카비에이(Sarcoptes scabiei), 코클리오마이이아 호미니보락스(Cochliomyia hominivorax) 및 풀렉스 이리탄스(Pulex irritans)를 포함하나 이들로 한정되지 않는 기생충 또는 기생충 단백질을 표적화할 수 있다.
면역글로불린 영역은 항-기생충 면역글로불린 G에 기초할 수 있거나 항-기생충 면역글로불린 G로부터 유래될 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 항-기생충 면역글로불린 M에 기초한, 또는 항-기생충 면역글로불린 M으로부터 유래된 아미노산 서열을 포함한다.
면역글로불린 영역은 항-기생충 면역글로불린 G 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-기생충 면역글로불린 G 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항-진균 면역글로불린에 기초할 수 있거나 항-진균 면역글로불린으로부터 유래될 수 있다. 항-세균 면역글로불린은 진균 단백질의 에피토프에 대해 유도될 수 있다. 항-진균 면역글로불린은 크립토코커스 네오포르만스(Cryptococcus neoformans), 크립토코커스 가티이(Cryptococcus gattii), 칸디다 알비칸스(Candida albicans), 칸디다 트로피칼리스(Candida tropicalis), 칸디다 스텔라토이데아(Candida stellatoidea), 칸디다 글라브라타(Candida glabrata), 칸디다 크루세이(Candida krusei), 칸디다 파랍실로시스(Candida parapsilosis), 칸디다 귈리에르몬디이(Candida guilliermondii), 칸디다 비스와나티이(Candida viswanathii), 칸디다 루시타니아(Candida lusitaniae), 로도토룰라 무실라기노사(Rhodotorula mucilaginosa), 쉬조사카로마이세스 폼베(Schizosaccharomyces pombe), 사카로마이세스 세레비지아(Saccharomyces cerevisiae), 브레타노마이세스 브룩셀렌시스(Brettanomyces bruxellensis), 칸디다 스텔라타(Candida stellata), 쉬조사카로마이세스 폼베(Schizosaccharomyces pombe), 토룰라스포라 델브루엑키이(Torulaspora delbrueckii), 자이고사카로마이세스 바일리이(Zygosaccharomyces bailii), 야로위아 리폴라이티카(Yarrowia lipolytica), 사카로마이세스 엑시구어스(Saccharomyces exiguus) 및 피키아 파스토리스(Pichia pastoris)를 포함하나 이들로 한정되지 않는 진균 또는 진균 단백질을 표적화할 수 있다. 항-진균 면역글로불린은 이펀구맙(efungumab)에 기초할 수 있거나 이펀구맙으로부터 유래될 수 있다.
면역글로불린 영역은 항-진균 면역글로불린 G에 기초할 수 있거나 항-진균 면역글로불린 G로부터 유래될 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 항-진균 면역글로불린 M에 기초한, 또는 항-진균 면역글로불린 M으로부터 유래된 아미노산 서열을 포함한다.
면역글로불린 영역은 항-진균 면역글로불린 G 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-진균 면역글로불린 G 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 이펀구맙 면역글로불린에 기초할 수 있거나 이펀구맙 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 이펀구맙 면역글로불린 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 이펀구맙 면역글로불린 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린에 기초할 수 있거나 트라스투주맙 면역글로불린 G 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 트라스투주맙 면역글로불린 G 면역글로불린 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항-Her2 면역글로불린에 기초할 수 있거나 항-Her2 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항-Her2 면역글로불린 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-Her2 면역글로불린 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항-CD47 면역글로불린에 기초할 수 있거나 항-CD47 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린의 적어도 부분과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린의 적어도 부분과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린의 적어도 부분과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린의 적어도 부분과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항-CD47 면역글로불린 서열의 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개 또는 90개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린 서열의 100개, 200개, 300개, 400개, 500개, 600개, 700개, 800개 또는 900개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린 서열의 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린 서열의 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 항-CD47 면역글로불린 서열의 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
면역글로불린 영역은 항암 면역글로불린에 기초할 수 있거나 항암 면역글로불린으로부터 유래될 수 있다. 항암 면역글로불린의 예로는 아브식시맙(abciximab), 아달리무맙(adalimumab), 알렘투주맙(alemtuzumab), 바실릭시맙(basiliximab), 벨리무맙(belimumab), 베바시주맙(bevacizumab), 브렌툭시맙(brentuximab), 카나키누맙(canakinumab), 세르톨리주맙(certolizumab), 세툭시맙(cetuximab), 다클리주맙(daclizumab), 데노수맙(denosumab), 에쿨리주맙(eculizumab), 에팔리주맙(efalizumab), 겜투주맙(gemtuzumab), 골리무맙(golimumab), 이브리투모맙(ibritumomab), 인플릭시맙(infliximab), 이필리무맙(ipilimumab), 무로모납(muromonab)-cd3, 나탈리주맙(natalizumab), 오파투무맙(ofatumumab), 오말리주맙(omalizumab), 팔리비주맙(palivizumab), 파니투무맙(panitumumab), 라니비주맙(ranibizumab), 리툭시맙(rituximab), 토실리주맙(tocilizumab), 토시투모맙(tositumomab) 및 트라스투주맙이 있으나 이들로 한정되지 않는다.
면역글로불린 영역은 인간 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 인간화된 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 키메라 면역글로불린의 적어도 일부를 포함할 수 있다. 면역글로불린 영역은 인간 면역글로불린에 기초할 수 있거나 인간 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 인간화된 면역글로불린에 기초할 수 있거나 인간화된 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 키메라 면역글로불린에 기초할 수 있거나 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 단일클론 면역글로불린에 기초할 수 있거나 단일클론 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 다중클론 면역글로불린에 기초할 수 있거나 다중클론 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 포유동물, 조류, 파충류, 양서류 또는 이들의 조합으로부터의 면역글로불린의 적어도 일부를 포함할 수 있다. 포유동물은 인간일 수 있다. 포유동물은 비인간 영장류일 수 있다. 포유동물은 개, 고양이, 양, 염소, 소, 토끼 또는 마우스일 수 있다.
면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편 서열에 기초한, 또는 이러한 서열로부터 유래된 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 92%, 95%, 97%, 98% 또는 99% 이상 상동성인 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 서열과 적어도 약 70% 상동성인 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 서열과 적어도 약 80% 상동성인 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 서열과 적어도 약 90% 상동성인 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 서열과 적어도 약 95% 상동성인 서열을 포함할 수 있다. 상기 서열은 펩티드 서열일 수 있다. 상기 서열은 뉴클레오티드 서열일 수 있다.
면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 200개, 150개, 100개, 90개, 80개, 70개, 60개, 50개, 40개, 30개, 20개, 17개, 15개, 12개, 10개, 8개, 6개, 5개 또는 4개 이하의 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 4개 이하의 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 3개 이하의 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 2개 이하의 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 1개 이하의 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있다. 아미노산은 연속적, 비연속적 또는 이들의 조합 상태일 수 있다. 예를 들면, 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 3개 미만의 연속적 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있다. 대안적으로 또는 추가로, 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 2개 미만의 비연속적 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있다. 또 다른 예에서, 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 펩티드 서열과 약 5개 미만의 아미노산에 의해 상이한 펩티드 서열을 포함할 수 있고, 이때 2개의 아미노산들은 연속적이고 2개의 아미노산들은 비연속적이다.
면역글로불린 영역은 하나 이상의 항체 및/또는 면역글로불린 단편에 기초한, 또는 이러한 항체 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 500개, 400개, 300개, 200개, 100개, 90개, 80개, 70개, 60개, 50개, 40개, 30개, 25개, 20개, 19개, 18개, 17개, 16개, 15개, 14개, 13개, 12개, 11개, 10개, 9개, 8개, 7개, 6개, 5개 또는 4개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 15개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 12개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 9개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 6개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 4개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 3개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 2개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 1개 이하의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 뉴클레오티드 또는 염기쌍은 연속적, 비연속적 또는 이들의 조합 상태일 수 있다. 예를 들면, 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 3개 미만의 연속적 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 대안적으로 또는 추가로, 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 2개 미만의 비연속적 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있다. 또 다른 예에서, 면역글로불린 영역은 하나 이상의 면역글로불린 및/또는 면역글로불린 단편에 기초한, 또는 이러한 면역글로불린 및/또는 면역글로불린 단편으로부터 유래된 뉴클레오티드 서열과 약 5개 미만의 뉴클레오티드 또는 염기쌍에 의해 상이한 뉴클레오티드 서열을 포함할 수 있고, 이때 2개의 뉴클레오티드들 또는 염기쌍들은 연속적이고 2개의 뉴클레오티드들 또는 염기쌍들은 비연속적이다.
면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 하나 이상의 아미노산 치환에 의해 상이할 수 있다. 면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 2개 이상의 아미노산 치환에 의해 상이할 수 있다. 면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 3개 이상의 아미노산 치환에 의해 상이할 수 있다. 면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 4개 이상의 아미노산 치환에 의해 상이할 수 있다. 면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 5개 이상의 아미노산 치환에 의해 상이할 수 있다. 면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 6개 이상의 아미노산 치환에 의해 상이할 수 있다. 면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 12개, 14개, 15개, 17개, 20개 또는 25개 이상의 아미노산 치환에 의해 상이할 수 있다. 면역글로불린 영역의 펩티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 펩티드 서열과 약 20개 내지 30개, 30개 내지 40개, 40개 내지 50개, 50개 내지 60개, 60개 내지 70개, 80개 내지 90개, 90개 내지 100개, 100개 내지 150개, 150개 내지 200개, 또는 200개 내지 300개 이상의 아미노산 치환에 의해 상이할 수 있다.
면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 하나 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 2개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 3개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 4개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 5개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 6개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 9개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 12개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 15개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 18개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 20개, 22개, 24개, 25개, 27개 또는 30개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다. 면역글로불린 영역의 뉴클레오티드 서열은 그의 기초 및/또는 기원인 면역글로불린 또는 면역글로불린 단편의 뉴클레오티드 서열과 약 30개 내지 40개, 40개 내지 50개, 50개 내지 60개, 60개 내지 70개, 70개 내지 80개, 80개 내지 90개, 90개 내지 100개, 100개 내지 200개, 200개 내지 300개, 또는 300개 내지 400개 이상의 뉴클레오티드 및/또는 염기쌍 치환에 의해 상이할 수 있다.
면역글로불린 영역은 적어도 약 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 적어도 약 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개, 500개, 525개, 550개, 575개, 600개, 625개, 650개, 675개 또는 700개 이상의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 적어도 약 100개의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 적어도 약 200개의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 적어도 약 400개의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 적어도 약 500개의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 적어도 약 600개의 아미노산들을 포함할 수 있다.
면역글로불린 영역은 약 2000개, 1900개, 1800, 1700개, 1600개, 1500개, 1400개, 1300개, 1200개 또는 1100개 미만의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 약 1000개, 950개, 900개, 850개, 800개, 750개 또는 700개 미만의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 약 1500개 미만의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 약 1000개 미만의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 약 800개 미만의 아미노산들을 포함할 수 있다. 면역글로불린 영역은 약 700개 미만의 아미노산들을 포함할 수 있다.
면역글로불린 융합 단백질은 상보성 결정 영역 3(CDR3)의 30개 이하의 연속적 아미노산을 포함하는 면역글로불린 영역을 추가로 포함할 수 있다. 면역글로불린 영역은 CDR3의 30개, 29개, 28개, 27개, 26개, 25개, 24개, 23개, 22개, 21개, 20개, 19개, 18개, 17개, 16개, 15개, 14개, 13개, 12개, 11개, 10개, 9개, 8개, 7개, 6개, 5개, 4개, 3개, 2개 또는 1개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 15개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 14개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 13개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 12개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 11개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 10개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 9개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 8개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 7개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 6개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 5개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 4개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 3개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 2개 이하의 연속적 아미노산을 포함할 수 있다. 면역글로불린 영역은 CDR3의 1개 이하의 연속적 아미노산을 포함할 수 있다. 일부 경우, 면역글로불린 영역은 CDR3을 함유하지 않는다.
면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 내지 8 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함한다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 내지 8 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함한다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 Fab 영역을 포함한다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열과 적어도 약 70%, 80%, 80%, 90%, 95% 또는 100% 동일한 서열로부터 유래된 아미노산 Fab 서열을 포함한다.
면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 내지 8 중 어느 한 서열로부터 유래된 아미노산 및 서열번호 5 내지 8 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 내지 8 중 하나 이상의 서열로부터 유래된 아미노산 및 서열번호 5 내지 8 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 5 내지 8 중 1개, 2개, 3개 또는 4개의 서열로부터 유래된 아미노산을 포함한다.
면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 50% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 70% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 80% 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 50% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 70% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 80% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 100% 동일한 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 Fab 영역을 포함한다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열과 적어도 약 70%, 80%, 85%, 90%, 95% 또는 100% 동일한 서열로부터 유래된 아미노산 Fab 서열을 포함한다.
면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 600개, 650개, 700개, 750개, 800개, 850개, 900개, 950개 또는 1000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1100개, 1200개, 1300개, 1400개 또는 1500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 500개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1000개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 1300개 이상의 뉴클레오티드들을 포함하는 뉴클레오티드 서열에 의해 코딩될 수 있다. 뉴클레오티드는 연속적일 수 있다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 1 내지 4 중 어느 한 서열로부터 유래된 뉴클레오티드 및 서열번호 1 내지 4 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 1 내지 4 중 하나 이상의 서열로부터 유래된 뉴클레오티드 및 서열번호 1 내지 4 중 어느 한 서열로부터 유래되지 않은 뉴클레오티드를 포함하는 뉴클레오티드 서열에 의해 코딩된다. 일부 실시양태들에서, 면역글로불린 영역은 서열번호 1 내지 4 중 1개, 2개, 3개 또는 4개의 서열로부터 유래된 뉴클레오티드 서열에 의해 코딩된다.
치료 펩티드
본 개시의 한 양태에서, 본원은 치료 펩티드 및 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질을 제공한다. 면역글로불린 융합 단백질은 2개 이상의 치료 펩티드들을 포함할 수 있다. 면역글로불린 융합 단백질은 3개, 4개 또는 5개 이상의 치료 펩티드들을 포함할 수 있다. 치료 펩티드는 연결 펩티드를 통해 면역글로불린 영역에 부착될 수 있다. 일부 실시양태들에서, 하나 이상의 추가 치료 펩티드는 제1 또는 제2 면역글로불린 영역에 부착된다. 하나 이상의 치료 펩티드는 하나 이상의 면역글로불린 영역에 부착될 수 있다. 2개 이상의 치료 펩티드들은 2개 이상의 면역글로불린 영역들에 부착될 수 있다. 2개 이상의 치료 펩티드들은 하나 이상의 면역글로불린 쇄에 부착될 수 있다. 2개 이상의 치료 펩티드들은 2개 이상의 면역글로불린 쇄들에 부착될 수 있다. 2개 이상의 치료 펩티드들은 하나 이상의 면역글로불린 영역 내의 하나 이상의 유닛에 부착될 수 있다. 2개 이상의 치료 펩티드들은 하나 이상의 면역글로불린 영역 내의 2개 이상의 유닛들에 부착될 수 있다. 일부 실시양태들에서, 치료 펩티드는 연결 펩티드의 도움 없이 면역글로불린 영역에 연결된다.
본원에 개시된 면역글로불린 융합 단백질은 하나 이상의 치료제를 포함할 수 있다. 치료제는 펩티드일 수 있다. 치료제는 소분자일 수 있다. 본원에 개시된 면역글로불린 융합 단백질은 2개 이상의 치료제들을 포함할 수 있다. 본원에 개시된 면역글로불린 융합 단백질은 3개, 4개, 5개 또는 6개 이상의 치료제들을 포함할 수 있다. 2개 이상의 치료제들은 동일할 수 있다. 2개 이상의 치료제들은 상이할 수 있다.
치료 펩티드는 임의의 이차 구조, 예를 들면, 알파 나선 또는 베타 가닥을 포함할 수 있거나, 규칙적인 이차 구조를 포함하지 않을 수 있다. 치료 펩티드는 미리스토일화, 팔미토일화, 이소프레닐화, 글리피화, 리포일화, 아실화, 아세틸화, 알킬화, 메틸화, 글리코실화, 말로닐화, 하이드록실화, 요오드화, 뉴클레오티드 추가, 산화, 인산화, 아데닐릴화, 프로피오닐화, 석시닐화, 황산화, 셀레노일화, 바이오티닐화, 페길화, 데이민화, 탈아미드화, 엘리미닐화 및 카바밀화를 포함하나 이들로 한정되지 않는 하나 이상의 변경을 갖는 아미노산을 포함할 수 있다. 치료 펩티드는 하나 이상의 소분자, 예를 들면, 약물에 접합된 하나 이상의 아미노산을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 비천연 아미노산을 포함한다. 일부 실시양태들에서, 치료 펩티드는 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 30개, 40개 또는 50개 이상의 비천연 아미노산을 포함한다. 일부 실시양태들에서, 치료 펩티드는 하나 이상의 치환을 포함한다. 일부 실시양태들에서, 치료 펩티드는 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 30개, 40개 또는 50개 이상의 아미노산 치환을 포함한다.
치료 펩티드는 면역글로불린 영역 내로 삽입될 수 있다. 면역글로불린 영역 내로의 치료 펩티드의 삽입은 면역글로불린 영역의 기초 또는 기원인 면역글로불린의 부분의 제거 또는 결실을 포함할 수 있다. 치료 펩티드는 중쇄의 적어도 일부를 대체할 수 있다. 치료 펩티드는 경쇄의 적어도 일부를 대체할 수 있다. 치료 펩티드는 가변 도메인의 적어도 일부를 대체할 수 있다. 치료 펩티드는 불변 도메인의 적어도 일부를 대체할 수 있다. 치료 펩티드는 상보성 결정 영역(CDR)의 적어도 일부를 대체할 수 있다. 치료 펩티드는 CDR1의 적어도 일부를 대체할 수 있다. 치료 펩티드는 CDR2의 적어도 일부를 대체할 수 있다. 치료 펩티드는 CDR3의 적어도 일부를 대체할 수 있다. 치료 펩티드는 면역글로불린 또는 이의 부분의 적어도 약 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% 또는 95% 이상을 대체할 수 있다. 예를 들면, 치료 펩티드는 가변 도메인의 적어도 약 50%를 대체할 수 있다. 치료 펩티드는 가변 도메인의 적어도 약 70%를 대체할 수 있다. 치료 펩티드는 가변 도메인의 적어도 약 80%를 대체할 수 있다. 치료 펩티드는 가변 도메인의 적어도 약 90%를 대체할 수 있다. 치료 펩티드는 가변 도메인의 적어도 약 95%를 대체할 수 있다. 예를 들면, 치료 펩티드는 면역글로불린 영역의 아미노 말단의 적어도 약 50%를 대체할 수 있다. 치료 펩티드는 면역글로불린 영역의 아미노 말단의 적어도 약 70%를 대체할 수 있다. 치료 펩티드는 면역글로불린 영역의 아미노 말단의 적어도 약 80%를 대체할 수 있다. 치료 펩티드는 면역글로불린 영역의 아미노 말단의 적어도 약 90%를 대체할 수 있다. 치료 펩티드는 면역글로불린 영역의 아미노 말단의 적어도 약 95%를 대체할 수 있다. 치료 펩티드는 CDR의 적어도 약 50%를 대체할 수 있다. 치료 펩티드는 CDR의 적어도 약 70%를 대체할 수 있다. 치료 펩티드는 CDR의 적어도 약 80%를 대체할 수 있다. 치료 펩티드는 CDR의 적어도 약 90%를 대체할 수 있다. 치료 펩티드는 CDR의 적어도 약 95%를 대체할 수 있다.
하나 이상의 치료 펩티드는 단백질에 기초할 수 있거나 단백질로부터 유래될 수 있다. 단백질은 성장 인자, 사이토카인, 호르몬 또는 독소일 수 있다. 성장 인자는 GCSF, GMCSF, GDF11 또는 FGF21일 수 있다. GCSF는 소 GCSF일 수 있다. GCSF는 인간 GCSF일 수 있다. GMCSF는 소 GMCSF 또는 인간 GMCSF일 수 있다. FGF21은 소 FGF21일 수 있다. FGF21은 인간 FGF21일 수 있다.
사이토카인은 인터페론 또는 인터류킨일 수 있다. 사이토카인은 간질 세포 유래 인자 1(SDF-1)일 수 있다. 인터페론은 인터페론-베타일 수 있다. 인터페론은 인터페론-알파일 수 있다. 인터류킨은 인터류킨 11(IL-11)일 수 있다. 인터류킨은 인터류킨 8(IL-8) 또는 인터류킨 21(IL-21)일 수 있다.
호르몬은 엑센딘-4, GLP-1, 릴랙신, 옥신토모듈린, 렙틴, 베타트로핀, 소 성장 호르몬(bGH), 인간 성장 호르몬(hGH), 에리쓰로포이에틴(EPO) 또는 부갑상선 호르몬일 수 있다. 호르몬은 소마토스타틴일 수 있다. 부갑상선 호르몬은 인간 부갑상선 호르몬일 수 있다. 에리쓰로포이에틴은 인간 에리쓰로포이에틴일 수 있다.
독소는 모카(Moka)1, VM-24, 맘바(Mamba)1, 암젠(Amgen)1, 550 펩티드 또는 프로톡신(protoxin2)일 수 있다. 독소는 지코노타이드(ziconotide) 또는 클로로톡신(chlorotoxin)일 수 있다.
단백질은 안지오포이에틴 유사 3(ANGPTL3)일 수 있다. 안지오포이에틴 유사 3은 인간 안지오포이에틴 유사 3일 수 있다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 당뇨병 및/또는 당뇨병 관련 병태를 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 당뇨병 및/또는 당뇨병 관련 병태를 치료하도록 구성된다. 당뇨병은 I형 당뇨병, 2형 당뇨병, 임신 당뇨병 및 전당뇨병을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 비만 및/또는 비만 관련 병태를 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 비만 및/또는 비만 관련 병태를 치료하도록 구성된다. 병태는 합병증 및 질환을 포함할 수 있다. 당뇨병 관련 병태의 예로는 당뇨병성 망막병증, 당뇨병성 신장병증, 당뇨병성 심장 질환, 당뇨병성 족부 장애, 당뇨병성 신경병증, 거대혈관 질환, 당뇨병성 심근병증, 감염 및 당뇨병성 케토산증이 있으나 이들로 한정되지 않는다. 당뇨병성 신경병증은 대칭적 다발신경병증, 자율 신경병증, 신경근병증, 두개 신경병증 및 단일신경병증을 포함할 수 있으나 이들로 한정되지 않는다. 비만 관련 병태는 심장 질환, 졸중, 고혈압, 당뇨병, 골관절염, 통풍, 수면 무호흡, 천식, 담낭 질환, 담석, 비정상적인 혈액 지방(예를 들면, 비정상적인 수준의 LDL 및 HDL 콜레스테롤), 비만 저호흡 증후군, 생식 문제, 간 지방증 및 정신적 건강 병태를 포함하나 이들로 한정되지 않는다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 글루카곤 유사 단백질-1(GLP-1) 수용체 아고니스트 또는 이의 제제이다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 인크레틴 미메틱(incretin mimetic)이다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 엑센딘-4, 엑세나타이드 또는 이의 합성물의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 글루카곤 유사체 또는 이의 제제이다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 인슐린의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 이중 특이적이다. 일부 실시양태들에서, 치료 펩티드는 GLP-1 수용체 및 글루카곤 수용체에 대한 특이성을 갖는다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 옥신토모듈린의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 단장 증후군 및/또는 단장 증후군 관련 병태를 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 단장 증후군 및/또는 단장 증후군 관련 병태를 치료하도록 구성된다. 단장 증후군 관련 병태는 소장에서의 세균 과다생장, 대사 산증, 담석, 신장 결석, 영양실조, 골연화증, 장 부전 및 체중 감소를 포함할 수 있으나 이들로 한정되지 않는다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 염증성 장 질환 및/또는 염증성 장 관련 병태를 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 염증성 장 질환 및/또는 염증성 장 관련 병태를 치료하도록 구성된다. 염증성 장 질환 및/또는 염증성 장 질환 관련 병태는 궤양성 결장염, 크론병, 콜라겐성 결장염, 림프구성 결장염, 허혈성 결장염, 전환(diversion) 결장염, 베체트병, 중간(intermediate) 결장염, 빈혈, 관절염, 괴저성 농피증, 원발 경화 담관염, 비갑상선 질병 증후군; 및 복부 통증, 구토, 설사, 직장 출혈, 내부 경련 또는 근육 연축, 및 염증성 장 질환을 갖는 개체에서의 체중 감소를 포함할 수 있으나 이들로 한정되지 않는다. 일부 실시양태들에서, 글루카곤 또는 글루카곤 유사 펩티드(예를 들면, GLP1, GLP2)를 포함하는 면역글로불린 융합 단백질은 염증성 장 질환 및/또는 염증성 장 질환 병태의 치료에 유용하다. 일부 실시양태들에서, 서열번호 69, 70, 193, 194, 195, 217, 218, 219, 220 및 221 중 임의의 아미노산 서열과 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함하는 면역글로불린 융합 단백질은 염증성 장 질환의 치료에 유용하다. 일부 실시양태들에서, 글루카곤 또는 글루카곤 유사 펩티드(예를 들면, GLP1, GLP2)를 포함하는 면역글로불린 융합 단백질은 단장 증후군 및/또는 단장 증후군 병태의 치료에 유용하다. 일부 실시양태들에서, 서열번호 69, 70, 193, 194, 195, 217, 218, 219, 220 및 221 중 임의의 아미노산 서열과 적어도 약 50%, 60%, 70%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% 또는 100% 동일한 아미노산 서열을 포함하는 면역글로불린 융합 단백질은 단장 증후군의 치료에 유용하다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 글루카곤, 글루카곤 유사체, 글루카곤 유사 펩티드 및/또는 글루카곤 유사 펩티드 유사체의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 글루카곤 유사 펩티드-2(GLP-2)의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 자가면역 질환 및/또는 자가면역 질환 관련 병태를 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 자가면역 질환 및/또는 자가면역 질환 관련 병태를 치료하도록 구성된다. 자가면역 질환 및/또는 자가면역 질환 관련 병태는 급성 파종 뇌척수염, 원형탈모, 항인지질 증후군, 자가면역 심근병증, 자가면역 용혈성 빈혈, 자가면역 간염, 자가면역 내이 질환, 자가면역 림프증식성 증후군, 자가면역 말초 신경병증, 자가면역 췌장염, 자가면역 다발내분비 증후군, 자가면역 프로게스테론 피부염, 자가면역 혈소판감소성 자반병, 자가면역 두드러기, 자가면역 포도막염, 베체트병, 셀리악병(Celiac disease), 한랭 응집소 질환, 크론병, 피부근염, I형 진성 당뇨병, 호산구성 근막염, 위장 유천포창, 굿파스처 증후군, 그레이브스병, 길랑-바레(Guillain-Barre) 증후군, 하시모토 뇌병증, 하시모토 갑상선염, 특발성 혈소판감소성 자반병, 홍반루푸스, 밀러-피셔(Miller-Fishe) 증후군, 혼합된 결합 조직 질환, 다발경화증, 중증근무력증, 기면증, 심상성 천포창, 악성 빈혈, 다발근염, 원발 담즙성 간경변증, 건선, 건선성 관절염, 재발 다발연골염, 류마티스성 관절염, 류마티스 열, 쇼그렌 증후군, 측두 동맥염, 횡단 척수염, 궤양성 결장염, 미분화된 결합 조직 질환, 혈관염 및 베게너 육아종증을 포함할 수 있으나 이들로 한정되지 않는다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 칼륨 채널에 결합하는 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 모카톡신(Mokatoxin)-1(모카(Moka))의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 통증을 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 통증을 치료하도록 구성된다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 신경독소인 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 신경독소 mu-SLPTX-Ssm6a(Ssam6)의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 카파-쎄라포톡신-Tb1a(550)의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 맘발라인-1의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 심부전 및/또는 섬유증을 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 심부전 및/또는 섬유증 관련 병태를 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 심부전 및/또는 섬유증을 치료하도록 구성된다. 일부 실시양태들에서, 치료 펩티드의 2개, 3개, 4개 또는 5개 이상의 영역들은 심부전 및/또는 섬유증 관련 병태를 치료하도록 구성된다. 심부전 관련 병태는 관상 심장 질환, 고혈압, 당뇨병, 심근병증, 심장 판막 질환, 부정맥, 울혈성 심장 결함, 폐쇄성 수면 무호흡, 심근염, 갑상선기능항진증, 갑상선기능저하증, 폐기종, 혈색소증 및 아밀로이드증을 포함할 수 있다. 심부전은 좌측 심부전, 우측 심부전, 수축성 심부전 및 확장성 심부전일 수 있다. 섬유증은 폐 섬유증, 특발성 폐 섬유증, 낭성 섬유증, 간경변증, 심내막심근 섬유증, 심근 경색, 심방 섬유증, 종격 섬유증, 골수섬유증, 후복막 섬유증, 진행성 괴상 섬유증, 신장발생성 전신 섬유증, 크론병, 켈로이드, 피부경화증/전신 경화증, 관절섬유증, 페이로니병, 뒤퓌트렌 구축(Dupuytren's contracture) 및 유착 관절낭염을 포함할 수 있으나 이들로 한정되지 않는다.
일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 인슐린 수퍼패밀리에 속하는 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드의 하나 이상의 영역은 인슐린의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다.
일부 실시양태들에서, 전체적으로 또는 부분적으로 치료 펩티드의 아미노산은 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열에 기초하거나 이러한 서열로부터 유래된다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함한다. 일부 실시양태들에서, 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 하나의 아미노산 서열과 100% 동일한 아미노산 서열을 포함한다.
치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다. 일부 실시양태들에서, 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열로부터 유래된 아미노산 및 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 하나 이상의 서열로부터 유래된 아미노산 및 서열번호 75 내지 94 및 223 내지 229 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 1개, 2개, 3개 또는 4개의 서열로부터 유래된 아미노산을 포함한다.
치료 펩티드는 프로테아제 절단 부위를 포함할 수 있다. 프로테아제 절단 부위는 치료 펩티드 내에 삽입될 수 있다. 일부 실시양태들에서, 치료 펩티드는 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역을 포함한다. 일부 실시양태들에서, 치료 펩티드는 제1 치료 펩티드 영역과 제2 치료 펩티드 영역 사이에 배치된 프로테아제 절단 부위를 포함한다. 일부 실시양태들에서, 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역은 동일한 단백질 또는 세트의 아미노산 서열들로부터 유래된다. 일부 실시양태들에서, 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역은 상이한 단백질 또는 세트의 아미노산 서열들로부터 유래된다. 하나 이상의 프로테아제 절단 부위는 치료 펩티드의 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착될 수 있다.
치료 펩티드는 하나 이상의 링커 펩티드를 포함할 수 있다. 치료 펩티드는 2개 이상의 링커 펩티드들을 포함할 수 있다. 치료 펩티드는 3개, 4개, 5개, 6개 또는 7개 이상의 링커 펩티드들을 포함할 수 있다. 링커 펩티드들은 상이할 수 있다. 링커 펩티드들은 동일할 수 있다. 링커 펩티드는 치료 펩티드 내에 삽입될 수 있다. 일부 실시양태들에서, 치료 펩티드는 제1 치료 영역, 제2 치료 영역, 및 제1 치료 영역과 제2 치료 영역 사이에 위치한 하나 이상의 링커 펩티드를 포함한다. 하나 이상의 링커 펩티드는 치료 펩티드의 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착될 수 있다. 일부 실시양태들에서, 링커 펩티드는 서열번호 121 및 122 중 어느 한 서열의 아미노산들로부터 유래된다.
치료 펩티드는 하나 이상의 내부 링커를 포함할 수 있다. 내부 링커는 치료 펩티드 내에 삽입될 수 있다. 일부 실시양태들에서, 치료 펩티드는 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역을 포함한다. 일부 실시양태들에서, 치료 펩티드는 제1 치료 펩티드 영역과 제2 치료 펩티드 영역 사이에 배치된 내부 링커를 포함한다. 일부 실시양태들에서, 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역은 동일한 단백질 또는 세트의 아미노산 서열들로부터 유래된다. 일부 실시양태들에서, 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역은 상이한 단백질 또는 세트의 아미노산 서열들로부터 유래된다. 일부 실시양태들에서, 내부 링커는 서열번호 123 내지 126 및 240 내지 244 중 어느 한 서열의 아미노산들로부터 유래된다. 일부 실시양태들에서, 내부 링커는 반복 서열을 갖는 아미노산들을 포함한다. 일부 실시양태들에서, 내부 링커는 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 반복 서열들을 갖는다. 일부 실시양태들에서, 내부 링커는 낮은 면역원성을 나타낸다. 일부 실시양태들에서, 내부 링커는 생체분해성이다.
비면역글로불린 영역
본원에 개시된 면역글로불린 융합 단백질은 하나 이상의 비면역글로불린 영역을 포함할 수 있다. 본원에 개시된 면역글로불린 융합 단백질은 2개 이상의 비면역글로불린 영역들을 포함할 수 있다. 본원에 개시된 면역글로불린 융합 단백질은 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 비면역글로불린 영역들을 포함할 수 있다. 일부 실시양태들에서, 비면역글로불린 영역은 본원에 개시된 면역글로불린 영역에 기초하지 않거나 이러한 영역으로부터 유래되지 않은 영역이다. 한 실시양태에서, 비면역글로불린 영역은 임의의 서열번호로 본원에 개시되어 있거나 본원에 제공되어 있는 면역글로불린 영역에 기초한, 또는 이러한 영역으로부터 유래된 아미노산을 포함하지 않는다. 한 실시양태에서, 비면역글로불린 영역은 면역글로불린 영역에 기초한, 또는 이러한 영역으로부터 유래된 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 25개, 30개, 35개, 40개, 45개, 50개, 55개, 60개, 70개, 80개, 90개, 100개, 150개, 200개, 400개 또는 500개 이상의 아미노산들을 포함하지 않는다.
2개 이상의 비면역글로불린 영역들은 하나 이상의 면역글로불린 영역에 부착될 수 있다. 2개 이상의 비면역글로불린 영역들은 2개 이상의 면역글로불린 영역들에 부착될 수 있다. 2개 이상의 비면역글로불린 영역들은 하나 이상의 면역글로불린 쇄에 부착될 수 있다. 2개 이상의 비면역글로불린 영역들은 2개 이상의 면역글로불린 쇄들에 부착될 수 있다. 2개 이상의 비면역글로불린 영역들은 하나 이상의 면역글로불린 영역 내의 하나 이상의 유닛에 부착될 수 있다. 2개 이상의 비면역글로불린 영역들은 하나 이상의 면역글로불린 영역 내의 2개 이상의 유닛들에 부착될 수 있다.
비면역글로불린 영역은 하나 이상의 치료 펩티드를 포함할 수 있다. 비면역글로불린 영역은 2개 이상의 치료 펩티드들을 포함할 수 있다. 비면역글로불린 영역은 3개, 4개, 5개, 6개 또는 7개 이상의 치료 펩티드들을 포함할 수 있다. 치료 펩티드들은 상이할 수 있다. 치료 펩티드들은 동일할 수 있다. 일부 실시양태들에서, 치료 펩티드는 서열번호 75 내지 94 및 223 내지 229 중 임의의 서열의 아미노산들로부터 유래된다. 치료 펩티드는 하나 이상의 내부 링커를 포함할 수 있다. 내부 링커는 치료 펩티드 내에 삽입될 수 있다. 일부 실시양태들에서, 치료 펩티드는 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역을 포함한다. 일부 실시양태들에서, 치료 펩티드는 제1 치료 펩티드 영역과 제2 치료 펩티드 영역 사이에 배치된 내부 링커를 포함한다. 일부 실시양태들에서, 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역은 동일한 단백질 또는 세트의 아미노산 서열들로부터 유래된다. 일부 실시양태들에서, 제1 치료 펩티드 영역 및 제2 치료 펩티드 영역은 상이한 단백질 또는 세트의 아미노산 서열들로부터 유래된다. 일부 실시양태들에서, 내부 링커는 서열번호 123 내지 126 및 240 내지 244 중 임의의 서열의 아미노산들로부터 유래된다.
비면역글로불린 영역은 하나 이상의 연장제 펩티드를 포함할 수 있다. 비면역글로불린 영역은 2개 이상의 연장제 펩티드들을 포함할 수 있다. 비면역글로불린 영역은 3개, 4개, 5개, 6개 또는 7개 이상의 연장제 펩티드들을 포함할 수 있다. 연장제 펩티드들은 상이할 수 있다. 연장제 펩티드들은 동일할 수 있다. 하나 이상의 연장제 펩티드를 포함하는 비면역글로불린 영역은 연장제 융합 영역으로서 지칭될 수 있다. 일부 실시양태들에서, 연장제 펩티드는 서열번호 119 및 120 중 임의의 서열의 아미노산들로부터 유래된다. 일부 실시양태들에서, 하나 이상의 연장제 펩티드는 면역글로불린 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다. 일부 실시양태들에서, 하나 이상의 연장제 펩티드는 치료 펩티드 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다.
비면역글로불린 영역은 프로테아제 절단 부위를 포함할 수 있다. 비면역글로불린 영역은 2개 이상의 프로테아제 절단 부위들을 포함할 수 있다. 비면역글로불린 영역은 3개, 4개, 5개, 6개 또는 7개 이상의 프로테아제 절단 부위들을 포함할 수 있다. 프로테아제 절단 부위들은 상이할 수 있다. 프로테아제 절단 부위들은 동일할 수 있다. 일부 실시양태들에서, 하나 이상의 프로테아제 절단 부위는 면역글로불린 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다. 일부 실시양태들에서, 하나 이상의 프로테아제 절단 부위는 치료 펩티드 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다.
비면역글로불린 영역은 링커 펩티드를 포함할 수 있다. 비면역글로불린 영역은 2개 이상의 링커 펩티드들을 포함할 수 있다. 비면역글로불린 영역은 3개, 4개, 5개, 6개 또는 7개 이상의 링커 펩티드들을 포함할 수 있다. 링커 펩티드들은 상이할 수 있다. 링커 펩티드들은 동일할 수 있다. 일부 실시양태들에서, 링커 펩티드는 서열번호 121 및 122 중 임의의 서열의 아미노산들로부터 유래된다. 일부 실시양태들에서, 하나 이상의 링커 펩티드는 면역글로불린 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다. 일부 실시양태들에서, 하나 이상의 링커 펩티드는 치료 펩티드 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다. 일부 실시양태들에서, 하나 이상의 링커 펩티드는 연장제 펩티드의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다.
비면역글로불린 영역은 면역글로불린 영역 내로 삽입될 수 있다. 면역글로불린 영역 내로의 비면역글로불린 영역의 삽입은 면역글로불린 영역의 기초 또는 기원인 면역글로불린의 부분의 제거 또는 결실을 포함할 수 있다. 비면역글로불린 영역은 중쇄의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 경쇄의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 V 영역의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 D 영역의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 J 영역의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 가변 영역의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 불변 영역의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 상보성 결정 영역(CDR)의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 CDR1의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 CDR2의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 CDR3의 적어도 일부를 대체할 수 있다. 비면역글로불린 영역은 면역글로불린 또는 이의 부분의 적어도 약 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% 또는 95% 이상을 대체할 수 있다. 예를 들면, 비면역글로불린 영역은 CDR의 적어도 약 50%를 대체할 수 있다. 비면역글로불린 영역은 CDR의 적어도 약 70%를 대체할 수 있다. 비면역글로불린 영역은 CDR의 적어도 약 80%를 대체할 수 있다. 비면역글로불린 영역은 CDR의 적어도 약 90%를 대체할 수 있다. 비면역글로불린 영역은 CDR의 적어도 약 95%를 대체할 수 있다.
일부 실시양태들에서, 면역글로불린 융합 단백질의 하나 이상의 비면역글로불린 영역은 렙틴의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다. 일부 실시양태들에서, 면역글로불린 융합 단백질의 비면역글로불린 영역의 치료 펩티드는 렙틴의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 아미노산 서열을 포함한다.
일부 실시양태들에서, 비면역글로불린 영역의 아미노산은 전체적으로 또는 부분적으로 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열에 기초하거나 이러한 서열로부터 유래된다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 50% 동일한 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 70% 동일한 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 적어도 약 80% 동일한 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열과 100% 동일한 아미노산 서열을 포함할 수 있다. 일부 실시양태들에서, 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 상동성인 아미노산 서열을 포함한다. 일부 실시양태들에서, 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 하나의 아미노산 서열과 적어도 약 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 동일한 아미노산 서열을 포함한다. 일부 실시양태들에서, 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 하나의 아미노산 서열과 100% 동일한 아미노산 서열을 포함한다.
비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개, 20개, 30개, 40개, 50개, 60개, 70개, 80개, 90개 또는 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 125개, 150개, 175개, 200개, 225개, 250개, 275개, 300개, 325개, 350개, 375개, 400개, 425개, 450개, 475개 또는 500개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 10개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 50개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 100개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 200개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 아미노산은 연속적일 수 있다. 대안적으로 또는 추가로, 아미노산은 비연속적이다. 일부 실시양태들에서, 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열로부터 유래된 아미노산 및 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 하나 이상의 서열로부터 유래된 아미노산 및 서열번호 144 내지 160 및 255 내지 264 중 어느 한 서열로부터 유래되지 않은 아미노산을 포함할 수 있다. 일부 실시양태들에서, 비면역글로불린 영역은 서열번호 144 내지 160 및 255 내지 264 중 1개, 2개, 3개 또는 4개의 서열로부터 유래된 아미노산을 포함한다.
연장제 펩티드
본원에 개시된 면역글로불린 융합 단백질은 하나 이상의 연장제 펩티드를 포함할 수 있다. 하나 이상의 연장제 펩티드는 치료 펩티드의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다. 하나 이상의 연장제 펩티드는 치료 펩티드의 각각의 말단에 부착될 수 있다. 하나 이상의 연장제 펩티드는 치료 펩티드의 상이한 말단들에 부착될 수 있다. 하나 이상의 연장제 펩티드는 치료 펩티드에 부착된 링커의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다. 하나 이상의 연장제 펩티드는 면역글로불린 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다. 하나 이상의 연장제 펩티드는 면역글로불린 영역의 각각의 말단에 부착될 수 있다. 하나 이상의 연장제 펩티드는 면역글로불린 영역의 상이한 말단들에 부착될 수 있다.
본원에 개시된 면역글로불린 융합 단백질의 연장제 융합 영역은 하나 이상의 연장제 펩티드를 포함할 수 있다. 연장제 융합 영역은 2개 이상의 연장제 펩티드들을 포함할 수 있다. 연장제 융합 영역은 3개 이상의 연장제 펩티드들을 포함할 수 있다. 연장제 융합 영역은 4개 이상의 연장제 펩티드들을 포함할 수 있다. 연장제 융합 영역은 5개 이상의 연장제 펩티드들을 포함할 수 있다. 연장제 융합 영역은 제1 연장제 펩티드 및 제2 연장제 펩티드를 포함할 수 있다.
연장제 펩티드는 하나 이상의 이차 구조를 포함할 수 있다. 연장제 펩티드는 2개 이상의 이차 구조들을 포함할 수 있다. 연장제 펩티드는 3개, 4개, 5개, 6개 또는 7개 이상의 이차 구조들을 포함할 수 있다. 2개 이상의 연장제 펩티드들은 하나 이상의 이차 구조를 포함할 수 있다. 2개 이상의 연장제 펩티드들은 2개 이상의 이차 구조들을 포함할 수 있다. 2개 이상의 연장제 펩티드들은 3개, 4개, 5개, 6개 또는 7개 이상의 이차 구조들을 포함할 수 있다. 각각의 연장제 펩티드는 적어도 하나의 이차 구조를 포함할 수 있다. 2개 이상의 연장제 펩티드들의 이차 구조는 동일할 수 있다. 대안적으로, 2개 이상의 연장제 펩티드들의 이차 구조는 상이할 수 있다. 일부 실시양태들에서, 연장제 펩티드는 규칙적인 이차 구조를 포함하지 않는다.
하나 이상의 이차 구조는 하나 이상의 베타 가닥을 포함할 수 있다. 연장제 펩티드는 2개 이상의 베타 가닥들을 포함할 수 있다. 예를 들면, 제1 연장제 펩티드는 제1 베타 가닥을 포함하고 제2 연장제 펩티드는 제2 베타 가닥을 포함한다. 연장제 펩티드는 3개, 4개, 5개, 6개 또는 7개 이상의 베타 가닥들을 포함할 수 있다. 2개 이상의 베타 가닥들은 역평행할 수 있다. 2개 이상의 베타 가닥들은 평행할 수 있다.
대안적으로 또는 추가로, 하나 이상의 이차 구조는 하나 이상의 알파 나선을 포함할 수 있다. 연장제 펩티드는 2개 이상의 알파 나선들을 포함할 수 있다. 예를 들면, 제1 연장제 펩티드는 제1 알파 나선을 포함하고 제2 연장제 펩티드는 제2 알파 나선을 포함한다. 연장제 펩티드는 3개, 4개, 5개, 6개 또는 7개 이상의 알파 나선들을 포함할 수 있다. 2개 이상의 알파 나선들은 역평행할 수 있다. 2개 이상의 알파 나선들은 평행할 수 있다. 2개 이상의 알파 나선들은 하나 이상의 코일드-코일(coiled-coil) 도메인을 형성할 수 있다.
하나 이상의 연장제 펩티드는 적어도 약 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 아미노산을 포함할 수 있다. 하나 이상의 연장제 펩티드는 적어도 약 10개, 11개, 12개, 13개, 14개, 15개, 16개, 17개, 18개, 19개, 20개, 21개, 22개, 23개, 24개, 25개, 26개, 27개, 28개, 29개 또는 30개 이상의 아미노산들을 포함할 수 있다. 하나 이상의 연장제 펩티드는 적어도 약 35개, 40개, 45개 또는 50개 이상의 아미노산들을 포함할 수 있다.
하나 이상의 연장제 펩티드는 약 100개 미만의 아미노산들을 포함할 수 있다. 하나 이상의 연장제 펩티드는 약 95개, 90개, 85개, 80개, 75개, 70개, 65개, 60개, 55개 또는 50개 미만의 아미노산들을 포함할 수 있다. 하나 이상의 연장제 펩티드는 약 90개 미만의 아미노산들을 포함할 수 있다. 하나 이상의 연장제 펩티드는 약 80개 미만의 아미노산들을 포함할 수 있다. 하나 이상의 연장제 펩티드는 약 70개 미만의 아미노산들을 포함할 수 있다.
2개 이상의 연장제 펩티드들은 동일한 길이를 가질 수 있다. 예를 들면, 제1 연장제 펩티드와 제2 연장제 펩티드는 동일한 길이를 갖는다. 대안적으로, 2개 이상의 연장제 펩티드들은 상이한 길이를 갖는다. 또 다른 예에서, 제1 연장제 펩티드와 제2 연장제 펩티드는 상이한 길이를 갖는다. 2개 이상의 연장제 펩티드들은 길이 면에서 적어도 약 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 아미노산에 의해 상이할 수 있다. 2개 이상의 연장제 펩티드들은 길이 면에서 적어도 약 1개 이상의 아미노산에 의해 상이할 수 있다. 2개 이상의 연장제 펩티드들은 길이 면에서 적어도 약 3개 이상의 아미노산에 의해 상이할 수 있다. 2개 이상의 연장제 펩티드들은 길이 면에서 적어도 약 5개 이상의 아미노산에 의해 상이할 수 있다.
연장제 펩티드는 면역글로불린 영역에 인접할 수 있다. 연장제 펩티드는 면역글로불린 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다. 연장제 펩티드는 비면역글로불린 영역에 인접할 수 있다. 연장제 펩티드는 비면역글로불린 영역의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다. 연장제 펩티드는 치료 펩티드에 인접할 수 있다. 연장제 펩티드는 치료 펩티드의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다. 연장제 펩티드는 링커에 인접할 수 있다. 연장제 펩티드는 링커의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다. 연장제 펩티드는 단백질분해성 절단 부위에 인접할 수 있다. 연장제 펩티드는 단백질분해성 절단 부위의 N 말단, C 말단, 또는 N 말단 및 C 말단에 부착될 수 있다.
연장제 펩티드는 치료 펩티드를 면역글로불린 영역에 연결할 수 있다. 연장제 펩티드는 면역글로불린 영역과 치료 펩티드, 링커 및/또는 단백질분해성 절단 부위 사이에 위치할 수 있다. 연장제 펩티드는 2개 이상의 면역글로불린 영역들, 치료 펩티드들, 링커들, 단백질분해성 절단 부위들 또는 이들의 조합 사이에 위치할 수 있다. 연장제 펩티드는 면역글로불린 영역, 치료 펩티드, 링커, 단백질분해성 절단 부위 또는 이들의 조합의 N 말단 방향에 존재할 수 있다. 연장제 펩티드는 면역글로불린 영역, 치료 펩티드, 링커, 단백질분해성 절단 부위 또는 이들의 조합의 C 말단 방향에 존재할 수 있다.
연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 85% 상동성인 아미노산 서열을 포함할 수 있다.
제1 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 제1 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 제1 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 제1 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 75% 상동성인 아미노산 서열을 포함할 수 있다. 제1 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
제2 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열을 포함할 수 있다. 제2 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 제2 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 이상 상동성인 아미노산 서열을 포함할 수 있다. 제2 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 제2 연장제 펩티드는 서열번호 119 및 120 중 어느 한 서열에 기초한, 또는 이러한 서열로부터 유래된 아미노산 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
면역글로불린 융합 단백질은 (a) 서열번호 119에 기초한, 또는 서열번호 119로부터 유래된 아미노산 서열을 포함하는 제1 연장제 펩티드; 및 (b) 서열번호 120에 기초한, 또는 서열번호 120으로부터 유래된 아미노산 서열을 포함하는 제2 연장제 펩티드를 포함할 수 있다. 면역글로불린 융합 단백질은 (a) 서열번호 119의 아미노산 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함하는 제1 연장제 펩티드; 및 (b) 서열번호 120의 아미노산 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함하는 제2 연장제 펩티드를 포함할 수 있다. 제1 연장제 펩티드는 서열번호 119의 아미노산 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90% 또는 95% 이상 상동성인 아미노산 서열을 포함할 수 있다. 제2 연장제 펩티드는 서열번호 120의 아미노산 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90% 또는 95% 이상 상동성인 아미노산 서열을 포함할 수 있다. 제1 연장제 펩티드는 서열번호 119의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 3개, 4개, 5개, 6개 또는 7개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 제1 연장제 펩티드는 서열번호 119의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 5개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 제2 연장제 펩티드는 서열번호 120의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 3개, 4개, 5개, 6개 또는 7개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다. 제2 연장제 펩티드는 서열번호 120의 아미노산 서열에 기초한, 또는 이러한 아미노산 서열로부터 유래된 5개 이상의 아미노산들을 포함하는 아미노산 서열을 포함할 수 있다.
본원에 개시된 연장제 펩티드는 CDR3에 기초할 수 있거나 CDR3으로부터 유래될 수 있다. CDR3은 울트라롱(ultralong) CDR3일 수 있다. 본원에서 상호교환적으로 사용된 "울트라롱 CDR3" 또는 "울트라롱 CDR3 서열"은 인간 면역글로불린 서열로부터 유래되지 않은 CDR3을 포함할 수 있다. 울트라롱 CDR3은 35개 아미노산 길이 또는 보다 더 긴 길이, 예를 들면, 40개 아미노산 길이 또는 보다 더 긴 길이, 45개 아미노산 길이 또는 보다 더 긴 길이, 50개 아미노산 길이 또는 보다 더 긴 길이, 55개 아미노산 길이 또는 보다 더 긴 길이, 또는 60개 아미노산 길이 또는 보다 더 긴 길이를 가질 수 있다. 울트라롱 CDR3은 중쇄 CDR3(CDR-H3 또는 CDRH3)일 수 있다. 울트라롱 CDR3은 반추동물(예를 들면, 소) 서열로부터 유래된 또는 이러한 서열에 기초한 서열을 포함할 수 있다. 울트라롱 CDR3은 하나 이상의 시스테인 모티프를 포함할 수 있다. 울트라롱 CDR3은 적어도 3개 이상의 시스테인 잔기들, 예를 들면, 4개 이상의 시스테인 잔기들, 6개 이상의 시스테인 잔기들 또는 8개 이상의 시스테인 잔기들을 포함할 수 있다. 울트라롱 CDR3 서열에 대한 추가 세부설명은 문헌(Saini SS, et al., Exceptionally long CDR3H region with multiple cysteine residues in functional bovine IgM antibodies, European Journal of Immunology, 1999), 문헌(Zhang Y, et al., Functional immunoglobulin CDR3 fusion proteins with enhanced pharmacological properties, Angew Chem Int Ed Engl, 2013), 문헌(Wang F, et al., Reshaping immunoglobulin diversity, Cell, 2013) 및 미국 특허 제6,740,747호에서 발견될 수 있다.
연장제 펩티드는 CDR에 기초한, 또는 CDR로부터 유래된 7개 이하의 아미노산들을 포함할 수 있다. 연장제 펩티드는 CDR에 기초한, 또는 CDR로부터 유래된 6개, 5개, 4개, 3개, 2개 또는 1개 이하의 아미노산을 포함할 수 있다. 아미노산은 연속적일 수 있다. 아미노산은 비연속적일 수 있다. CDR은 CDR1일 수 있다. CDR은 CDR2일 수 있다. CDR은 CDR3일 수 있다. CDR은 울트라롱 CDR일 수 있다.
연장제 펩티드는 울트라롱 CDR3이 아닌 CDR에 기초할 수 있거나 이러한 CDR로부터 유래될 수 있다. 연장제 펩티드는 CDR3에 기초한, 또는 CDR3으로부터 유래된 10개 이하의 아미노산을 포함할 수 있다. 연장제 펩티드는 CDR3에 기초한, 또는 CDR3으로부터 유래된 9개, 8개, 7개, 6개, 5개, 4개, 3개, 2개 또는 1개 이하의 아미노산을 포함할 수 있다. 연장제 펩티드는 CDR3에 기초한, 또는 CDR3으로부터 유래된 8개 이하의 아미노산을 포함할 수 있다. 연장제 펩티드는 CDR3에 기초한, 또는 CDR3으로부터 유래된 7개 이하의 아미노산을 포함할 수 있다. 연장제 펩티드는 CDR3에 기초한, 또는 CDR3으로부터 유래된 5개 이하의 아미노산을 포함할 수 있다.
연장제 펩티드는 울트라롱 CDR3을 포함하는 아미노산 서열과 약 50% 미만 동일한 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 울트라롱 CDR3을 포함하는 아미노산 서열과 약 45%, 40%, 35%, 30%, 25%, 20%, 15% 또는 10% 미만 동일한 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 울트라롱 CDR3을 포함하는 아미노산 서열과 약 30% 미만 동일한 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 울트라롱 CDR3을 포함하는 아미노산 서열과 약 25% 미만 동일한 아미노산 서열을 포함할 수 있다. 연장제 펩티드는 울트라롱 CDR3을 포함하는 아미노산 서열과 약 20% 미만 동일한 아미노산 서열을 포함할 수 있다.
연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개, 10개, 11개, 12개, 13개, 14개 또는 15개 이상의 아미노산을 포함할 수 있다. 연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 1개 이상의 아미노산을 포함할 수 있다. 연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 3개 이상의 아미노산들을 포함할 수 있다. 연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 5개 이상의 아미노산들을 포함할 수 있다. 울트라롱 CDR3에 부착된 또는 삽입된 2개 이상의 아미노산들은 인접할 수 있다. 대안적으로 또는 추가로, 울트라롱 CDR3에 부착된 또는 삽입된 2개 이상의 아미노산들은 인접하지 않다.
연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 30개, 25개, 20개, 19개, 18개, 17개, 16개, 15개, 14개, 13개, 12개, 11개 또는 10개 이하의 아미노산들을 포함할 수 있다. 연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 20개 이하의 아미노산들을 포함할 수 있다. 연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 15개 이하의 아미노산들을 포함할 수 있다. 연장제 펩티드는 연장제 펩티드의 울트라롱 CDR3-기초 부분에 부착된 또는 삽입된 10개 이하의 아미노산들을 포함할 수 있다. 울트라롱 CDR3에 부착된 또는 삽입된 아미노산들은 인접할 수 있다. 대안적으로 또는 추가로, 울트라롱 CDR3에 부착된 또는 삽입된 아미노산들은 인접하지 않다.
지방족 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 20%를 구성할 수 있다. 지방족 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 22%, 25%, 27%, 30%, 32%, 35%, 37%, 40%, 42% 또는 45% 이상을 구성할 수 있다. 지방족 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 22%를 구성할 수 있다. 지방족 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 27%를 구성할 수 있다.
지방족 아미노산은 연장제 펩티드의 총 아미노산들의 약 50% 미만을 구성할 수 있다. 지방족 아미노산은 연장제 펩티드의 총 아미노산들의 약 47%, 45%, 43%, 40%, 38%, 35%, 33% 또는 30% 미만을 구성할 수 있다.
지방족 아미노산은 연장제 펩티드의 총 아미노산들의 약 20% 내지 약 45%를 구성할 수 있다. 지방족 아미노산은 연장제 펩티드의 총 아미노산들의 약 23% 내지 약 45%를 구성할 수 있다. 지방족 아미노산은 연장제 펩티드의 총 아미노산들의 약 23% 내지 약 40%를 구성할 수 있다.
방향족 아미노산은 연장제 펩티드의 총 아미노산들의 약 20% 미만을 구성할 수 있다. 방향족 아미노산은 연장제 펩티드의 총 아미노산들의 약 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11% 또는 10% 미만을 구성할 수 있다. 방향족 아미노산은 연장제 펩티드의 총 아미노산들의 0% 내지 약 20%를 구성할 수 있다.
비극성 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 30%를 구성할 수 있다. 비극성 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39% 또는 40%를 구성할 수 있다. 비극성 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 32%를 구성할 수 있다.
비극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 80% 미만을 구성할 수 있다. 비극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 77%, 75%, 72%, 70%, 69% 또는 68% 미만을 구성할 수 있다.
비극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 35% 내지 약 80%를 구성할 수 있다. 비극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 38% 내지 약 80%를 구성할 수 있다. 비극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 38% 내지 약 75%를 구성할 수 있다. 비극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 35% 내지 약 70%를 구성할 수 있다.
극성 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 20%를 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30% 또는 35% 이상을 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 적어도 약 23%를 구성할 수 있다.
극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 80% 미만을 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 77%, 75%, 72%, 70%, 69% 또는 68% 미만을 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 77% 미만을 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 75% 미만을 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 72% 미만을 구성할 수 있다.
극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 25% 내지 약 70%를 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 27% 내지 약 70%를 구성할 수 있다. 극성 아미노산은 연장제 펩티드의 총 아미노산들의 약 30% 내지 약 70%를 구성할 수 있다.
대안적으로, 본원에 개시된 면역글로불린 융합 단백질은 연장제 펩티드를 포함하지 않는다.
링커
면역글로불린 융합 단백질, 면역글로불린 영역, 치료 펩티드, 비면역글로불린 영역 및/또는 연장제 융합 영역은 하나 이상의 링커를 추가로 포함할 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역, 비면역글로불린 영역 및/또는 연장제 융합 영역은 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 링커들을 추가로 포함할 수 있다. 연장제 융합 영역은 하나 이상의 링커를 추가로 포함할 수 있다. 연장제 융합 영역은 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 링커들을 추가로 포함할 수 있다.
하나 이상의 링커는 치료 펩티드의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다. 하나 이상의 링커는 연장제 펩티드의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다. 하나 이상의 링커는 단백질분해성 절단 부위의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착된다. 하나 이상의 링커는 치료 펩티드, 연장제 펩티드, 단백질분해성 절단 부위, 연장제 융합 영역, 면역글로불린 영역, 비면역글로불린 영역 또는 이들의 조합에 부착될 수 있다.
하나 이상의 링커는 서열번호 121 및 122 중 어느 한 서열로부터 선택된 아미노산 서열을 포함할 수 있다. 하나 이상의 링커는 서열번호 121 및 122 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 하나 이상의 링커는 서열번호 121 및 122 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90% 또는 95% 이상 상동성인 아미노산 서열을 포함할 수 있다. 하나 이상의 링커는 서열번호 121 및 122 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 하나 이상의 링커는 서열번호 121 및 122 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
일부 실시양태들에서, 링커는 연결 링커이다. 연결 링커는 치료 펩티드를 면역글로불린 영역에 연결할 수 있다. 연결 링커는 서열번호 115 내지 118 및 237 내지 239 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 연결 링커는 서열번호 115 내지 118 및 237 내지 239 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90% 또는 95% 이상 상동성인 아미노산 서열을 포함할 수 있다. 연결 링커는 서열번호 115 내지 118 및 237 내지 239 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 연결 링커는 서열번호 115 내지 118 및 237 내지 239 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
일부 실시양태들에서, 링커는 내부 링커이다. 내부 링커는 치료 펩티드의 부분일 수 있다. 내부 링커는 치료 펩티드의 2개의 영역들을 연결할 수 있다. 내부 링커는 2개의 상이한 펩티드들 또는 단백질들로부터 유래된 2개의 치료 펩티드들을 연결할 수 있다. 내부 링커는 동일한 펩티드 또는 단백질로부터 유래된 2개의 치료 펩티드들을 연결할 수 있다. 내부 링커는 서열번호 123 내지 126 및 240 내지 244 중 어느 한 서열과 적어도 약 50% 상동성인 아미노산 서열을 포함할 수 있다. 내부 링커는 서열번호 123 내지 126 및 240 내지 244 중 어느 한 서열과 적어도 약 60%, 65%, 70%, 75%, 80%, 85%, 90% 또는 95% 이상 상동성인 아미노산 서열을 포함할 수 있다. 내부 링커는 서열번호 123 내지 126 및 240 내지 244 중 어느 한 서열과 적어도 약 70% 상동성인 아미노산 서열을 포함할 수 있다. 내부 링커는 서열번호 123 내지 126 및 240 내지 244 중 어느 한 서열과 적어도 약 80% 상동성인 아미노산 서열을 포함할 수 있다.
단백질분해성 절단 부위
본원에 개시된 면역글로불린 융합 단백질은 하나 이상의 단백질분해성 절단 부위를 추가로 포함할 수 있다. 본원에 개시된 면역글로불린 융합 단백질은 2개 이상의 단백질분해성 절단 부위들을 추가로 포함할 수 있다. 본원에 개시된 면역글로불린 융합 단백질은 3개 이상의 단백질분해성 절단 부위들을 추가로 포함할 수 있다. 본원에 개시된 면역글로불린 융합 단백질은 4개, 5개, 6개 또는 7개 이상의 단백질분해성 절단 부위들을 추가로 포함할 수 있다. 본원에 개시된 치료 펩티드는 하나 이상의 단백질분해성 절단 부위를 추가로 포함할 수 있다.
하나 이상의 단백질분해성 절단 부위는 치료 펩티드의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착될 수 있다. 하나 이상의 단백질분해성 절단 부위는 연장제 펩티드의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착될 수 있다. 하나 이상의 단백질분해성 절단 부위는 링커의 N 말단, C 말단, 또는 N 말단 및 C 말단 둘 다에 부착될 수 있다. 하나 이상의 단백질분해성 절단 부위는 치료 펩티드, 연장제 펩티드, 링커, 연장제 융합 영역, 면역글로불린 영역, 비면역글로불린 영역 또는 이들의 조합에 부착될 수 있다.
일부 실시양태들에서, 단백질분해성 절단 부위는 치료 펩티드, 연장제 펩티드, 면역글로불린 영역 또는 이들의 조합의 아미노산 서열 내에 위치한다. 치료 펩티드는 그의 아미노산 서열 내에 하나 이상의 단백질분해성 절단 부위를 포함할 수 있다. 예를 들면, 서열번호 99 내지 101은 2개의 내부 단백질분해성 절단 부위들을 포함하는 릴랙신 단백질을 개시한다.
2개 이상의 단백질분해성 절단 부위들은 치료 펩티드, 연장제 펩티드, 링커, 면역글로불린 영역 또는 이들의 조합을 둘러쌀 수 있다. 단백질분해성 절단 부위의 분해는 2개 이상의 단백질분해성 절단 부위들 사이에 위치한 펩티드 단편의 방출을 야기할 수 있다. 예를 들면, 단백질분해성 절단 부위는 치료 펩티드-링커 펩티드를 플랭킹할 수 있다. 단백질분해성 절단 부위의 분해는 치료 펩티드-링커의 방출을 야기할 수 있다.
단백질분해성 절단 부위는 하나 이상의 프로테아제에 의해 인식될 수 있다. 하나 이상의 프로테아제는 세린 프로테아제, 쓰레오닌 프로테아제, 시스테인 프로테아제, 아스파르테이트 프로테아제, 글루탐산 프로테아제, 메탈로프로테아제, 엑소펩티다제, 엔도펩티다제 또는 이들의 조합일 수 있다. 프로테아제는 인자 VII 또는 인자 Xa를 포함하는 군으로부터 선택될 수 있다. 프로테아제의 추가 예로는 아미노펩티다제, 카복시펩티다제, 트립신, 카이모트립신, 펩신, 파파인 및 엘라스타제가 있으나 이들로 한정되지 않는다. 프로테아제는 PC2일 수 있다. 일부 실시양태들에서, 프로테아제는 아미노산 서열 KR을 인식한다. 일부 실시양태들에서, 프로테아제는 아미노산 서열 RKKR을 인식한다.
벡터, 숙주 세포 및 재조합 방법
본원에 개시된 면역글로불린 융합 단백질은 공지된 재조합 및 단백질 정제 방법에 의해 발현될 수 있고 정제될 수 있다. 일부 경우, 면역글로불린 융합 단백질의 활성은 발현 및/또는 정제 방법에 의해 영향을 받는다. 예를 들면, 치료제로서 사용되도록 구성된 면역글로불린 융합 단백질의 활성은 발현 벡터의 정체(identity), 재조합 숙주의 정체, 세포주의 정체, 발현 반응 조건, 정제 방법, 단백질 프로세싱 또는 이들의 임의의 조합을 기초로 향상되거나 약화된다. 발현 반응 조건은 온도, % CO2, 배지, 발현 시간, 보조인자 및 샤페론을 포함하나 이들로 한정되지 않는다. 정제 방법은 정제 온도, 크로마토그래피 수지, 프로테아제 억제제 및 완충제 조성물을 포함하나 이들로 한정되지 않는다.
본원에 개시된 면역글로불린 융합 단백질은 재조합 방법에 의해 발현될 수 있다. 일반적으로, 면역글로불린 융합 단백질을 코딩하는 핵산은 추가 클로닝(DNA의 증폭) 또는 발현을 위해 단리될 수 있고 복제가능한 벡터 내로 삽입될 수 있다. 면역글로불린 융합 단백질을 코딩하는 DNA는 PCR 증폭에 의해 제조될 수 있고 통상적인 절차의 사용에 의해(예를 들면, 면역글로불린 융합 단백질을 코딩하는 뉴클레오티드에 특이적으로 결합할 수 있는 올리고뉴클레오티드 프로브의 사용에 의해) 서열분석될 수 있다. 예시적인 실시양태에서, 면역글로불린 융합 단백질을 코딩하는 핵산은 PCR에 의해 증폭되고 제한효소에 의해 분해되고 겔 정제된다. 분해된 핵산은 복제가능한 벡터 내로 삽입될 수 있다. 분해된 면역글로불린 융합 단백질 삽입물을 함유하는 복제가능한 벡터는 추가 클로닝(DNA의 증폭) 또는 발현을 위해 숙주 세포 내로 형질전환될 수 있거나 형질도입될 수 있다. 숙주 세포는 원핵 또는 진핵 세포일 수 있다.
면역글로불린 융합 단백질의 폴리펩티드 성분(예를 들면, 면역글로불린 영역, 연장제 펩티드, 치료 펩티드)을 코딩하는 폴리뉴클레오티드 서열은 PCR 증폭에 의해 수득될 수 있다. 폴리뉴클레오티드 서열은 폴리펩티드 성분을 코딩하는 핵산을 함유하는 세포로부터 단리될 수 있고 서열분석될 수 있다. 대안적으로 또는 추가로, 폴리뉴클레오티드는 뉴클레오티드 합성기 또는 PCR 기법의 이용에 의해 합성될 수 있다. 폴리펩티드 성분을 코딩하는 서열은 일단 수득되면 원핵 및/또는 진핵 숙주에서 이종 폴리뉴클레오티드를 복제할 수 있고 발현할 수 있는 재조합 벡터 내로 삽입될 수 있다.
추가로, 숙주 미생물과 상용가능한 레플리콘(replicon) 및 조절 서열을 함유하는 파지 벡터는 이들 숙주들과 함께 형질전환 벡터로서 사용될 수 있다. 예를 들면, 박테리오파지, 예컨대, λGEM™-11이 민감한 숙주 세포, 예컨대, 이. 콜라이 LE392를 형질전환시키는 데 사용될 수 있는 재조합 벡터의 제조에 사용될 수 있다.
면역글로불린 융합 단백질은 세포내에서(예를 들면, 세포질) 또는 세포외에서(예를 들면, 분비) 발현될 수 있다. 세포외 발현을 위해, 벡터는 면역글로불린 융합 단백질이 세포의 외부로 전위할 수 있게 하는 분비 신호를 포함할 수 있다.
면역글로불린 융합 단백질 코딩 벡터의 클로닝 또는 발현에 적합한 숙주 세포는 원핵 또는 진핵 세포를 포함한다. 숙주 세포는 진핵 세포일 수 있다. 진핵 세포의 예로는 인간 배아 신장(HEK) 세포, 중국 햄스터 난소(CHO) 세포, 진균, 효모, 무척추동물 세포(예를 들면, 식물 세포 및 곤충 세포) 및 림프 세포(예를 들면, YO, NSO, Sp20 세포)가 있으나 이들로 한정되지 않는다. 적합한 포유동물 숙주 세포주의 다른 예는 SV40에 의해 형질전환된 원숭이 신장 CV1 세포주(COS-7); 새끼 햄스터 신장 세포(BHK); 마우스 세르톨리(sertoli) 세포; 원숭이 신장 세포(CV1); 아프리카 녹색 원숭이 신장 세포(VERO-76); 인간 자궁경부 암종 세포(HELA); 개 신장 세포(MDCK); 버팔로 래트 간 세포(BRL 3A); 인간 폐 세포(W138); 인간 간 세포(Hep G2); 마우스 유선 종양(MMT 060562); TR1 세포; MRC 5 세포; 및 FS4 세포이다. 숙주 세포는 원핵 세포(예를 들면, 이. 콜라이)일 수 있다.
숙주 세포는 면역글로불린 융합 단백질을 코딩하는 뉴클레오티드를 함유하는 벡터로 형질전환될 수 있다. 형질전환된 숙주 세포는 배지에서 배양될 수 있다. 배지는 프로모터를 유도하거나, 형질전환체를 선택하거나, 원하는 서열을 코딩하는 유전자를 증폭하거나 발현시키기 위한 하나 이상의 물질로 보충될 수 있다. 숙주 세포를 형질전환시키는 방법은 당분야에서 공지되어 있고 전기천공, 염화칼슘 또는 폴리에틸렌 글리콜/DMSO를 포함할 수 있다.
대안적으로, 숙주 세포는 면역글로불린 융합 단백질을 코딩하는 뉴클레오티드를 함유하는 벡터로 형질감염될 수 있거나 형질도입될 수 있다. 형질감염된 또는 형질도입된 숙주 세포는 배지에서 배양될 수 있다. 배지는 프로모터를 유도하거나, 형질감염된 또는 형질도입된 세포를 선택하거나, 원하는 서열을 코딩하는 유전자를 발현시키기 위한 하나 이상의 물질로 보충될 수 있다.
발현된 면역글로불린 융합 단백질은 숙주 세포의 주변세포질(periplasm) 내로 분비될 수 있고 이러한 주변세포질로부터 회수될 수 있거나, 배양 배지 내로 수송될 수 있다. 주변세포질로부터의 단백질 회수는 숙주 세포의 파괴를 수반할 수 있다. 숙주 세포의 파괴는 삼투압 쇼크, 초음파처리 또는 용해를 포함할 수 있다. 원심분리 또는 여과를 이용하여 세포 잔해(debris) 또는 전체 세포를 제거할 수 있다. 면역글로불린 융합 단백질은 예를 들면, 친화성 수지 크로마토그래피에 의해 더 정제될 수 있다.
대안적으로, 배양 배지 내로 분비되는 면역글로불린 융합 단백질은 그 배지에서 단리될 수 있다. 세포를 배양물로부터 제거할 수 있고 생성된 단백질의 추가 정제를 위해 배양 상청액을 여과할 수 있고 농축할 수 있다. 통상적으로 공지된 방법, 예컨대, 폴리아크릴아미드 겔 전기영동(PAGE) 및 웨스턴 블롯 분석을 이용하여 발현된 폴리펩티드를 더 단리할 수 있고 확인할 수 있다.
면역글로불린 융합 단백질 제조는 발효 과정에 의해 대량으로 수행될 수 있다. 다양한 대규모 유가식(fed-batch) 발효 절차가 재조합 단백질의 제조를 위해 이용될 수 있다. 대규모 발효는 적어도 1,000 리터의 용량, 바람직하게는 약 1,000 내지 100,000 리터의 용량을 갖는다. 이들 발효기들은 교반기 임펠러(agitator impellers)를 이용하여 산소 및 영양분, 특히 글루코스(바람직한 탄소/에너지 공급원)을 분배할 수 있다. 소규모 발효는 일반적으로 부피 용량이 대략 100 리터 이하이고 약 1 리터 내지 약 100 리터일 수 있는 발효기 내에서의 발효를 지칭한다.
발효 과정에서, 단백질 발현의 유도는 전형적으로 세포가 적합한 조건 하에 원하는 밀도, 예를 들면, 세포가 초기 정지기(stationary phase)에 있는 단계인 약 180 내지 220의 OD550까지 생장된 후에 시작된다. 당분야에서 공지되어 있고 본원에 기재되어 있는 바와 같이, 사용된 벡터 구축물에 따라 다양한 유도제들이 사용될 수 있다. 세포는 유도 전에 보다 더 짧은 기간 동안 생장될 수 있다. 보다 더 길거나 보다 더 짧은 유도 시간이 사용될 수 있지만, 세포는 통상적으로 약 12시간 내지 50시간 동안 유도된다.
본원에 개시된 면역글로불린 융합 단백질의 제조 수율 및 품질을 개선하기 위해, 다양한 발효 조건들이 변경될 수 있다. 예를 들면, 분비된 면역글로불린 융합 단백질 폴리펩티드의 적절한 조립 및 폴딩을 개선하기 위해, 샤페론 단백질, 예컨대, Dsb 단백질(DsbA, DsbB, DsbC, DsbD 및/또는 DsbG) 또는 FkpA(샤페론 활성을 갖는 펩티딜프롤릴 시스,트랜스-이소머라제)를 과다발현하는 추가 벡터를 사용하여 숙주 원핵 세포를 공동-형질전환시킬 수 있다. 샤페론 단백질은 세균 숙주 세포에서 생성된 이종 단백질의 적절한 폴딩 및 가용성을 용이하게 하는 것으로 입증되어 있다.
발현된 이종 단백질(특히, 단백질용해에 민감한 이종 단백질)의 단백질용해를 최소화하기 위해, 일부 단백질분해성 효소 결핍 숙주 균주들이 본 개시를 위해 사용될 수 있다. 예를 들면, 숙주 세포 균주는 공지된 세균 프로테아제, 예컨대, 프로테아제 III, OmpT, DegP, Tsp, 프로테아제 I, 프로테아제 Mi, 프로테아제 V, 프로테아제 VI 및 이들의 조합을 코딩하는 유전자에서 유전적 돌연변이(들)를 달성하도록 변경될 수 있다. 일부 이. 콜라이 프로테아제 결핍 균주들도 사용될 수 있다.
당분야에서 공지된 표준 단백질 정제 방법이 이용될 수 있다. 하기 절차들은 적합한 정제 절차의 예이다: 면역친화성 또는 이온 교환 컬럼 상에서의 분획화, 에탄올 침전, 역상 HPLC, 실리카 또는 양이온 교환 수지, 예컨대, DEAE 상에서의 크로마토그래피, 크로마토포커싱, SDS-PAGE, 황산암모늄 침전, 하이드록실아파타이트 크로마토그래피, 겔 전기영동, 투석, 및 예를 들면, 세파덱스 G-75를 사용한 친화성 크로마토그래피 및 겔 여과.
면역글로불린 융합 단백질은 상업적으로 입수가능한 단백질 농축 필터, 예를 들면, 아미콘(Amicon) 또는 밀리포어(Millipore) 펠리콘(Pellicon)® 한외여과 유닛의 이용을 통해 농축될 수 있다.
프로테아제 억제제 또는 프로테아제 억제제 칵테일이 면역글로불린 융합 단백질의 단백질용해를 억제하기 위해 상기 단계들 중 임의의 단계에 포함될 수 있다.
일부 경우, 면역글로불린 융합 단백질은 단리 시 생물학적 활성을 나타내지 않을 수 있다. 폴리펩티드를 그의 삼차 구조로 "리폴딩"하거나 전환시키고 디설파이드 연결을 생성하는 다양한 방법들을 이용하여 생물학적 활성을 복구할 수 있다. 이러한 방법들은 가용화된 폴리펩티드를 특정 농도의 카오트로프(chaotrope)의 존재 하에 통상적으로 7 초과의 pH에 노출시키는 단계를 포함한다. 카오트로프의 선택은 봉입체(inclusion body) 가용화를 위해 이용된 선택과 매우 유사하나, 통상적으로 카오트로프는 보다 더 낮은 농도에서 사용되고 상기 가용화를 위해 사용된 카오트로프와 반드시 동일할 필요는 없다. 대부분의 경우들에서, 리폴딩/산화 용액은 단백질의 시스테인 가교(들)의 형성에서 디설파이드 셔플링이 일어날 수 있게 하는 특정 산화환원 전위를 생성하도록 환원제, 또는 특정 비의 환원제 플러스 그의 산화된 형태도 함유할 것이다. 통상적으로 사용되는 산화환원 커플들의 일부는 시스테인/시스타민, 글루타티온(GSH)/디티오비스 GSH, 염화 제2구리, 디티오트레이톨(DTT)/디티안 DTT, 및 2-머캡토에탄올(bME)/디-티오-b(ME)를 포함한다. 많은 경우들에서, 리폴딩의 효율을 증가시키기 위해 보조용매가 사용될 수 있고, 이 목적을 위해 사용되는 통상의 시약은 글리세롤, 다양한 분자량의 폴리에틸렌 글리콜, 아르기닌 등을 포함한다.
조성물
본원은 본원에 개시된 면역글로불린 융합 단백질 및/또는 면역글로불린 융합 단백질의 성분을 포함하는 조성물을 개시한다. 상기 조성물은 1개, 2개, 3개, 4개, 5개, 6개, 7개, 8개, 9개 또는 10개 이상의 면역글로불린 융합 단백질들을 포함할 수 있다. 면역글로불린 융합 단백질들은 상이할 수 있다. 대안적으로, 면역글로불린 융합 단백질들은 동일할 수 있거나 유사할 수 있다. 면역글로불린 융합 단백질은 상이한 면역글로불린 영역, 연장제 융합 영역, 연장제 펩티드, 치료 펩티드 또는 이들의 조합을 포함할 수 있다.
상기 조성물은 하나 이상의 약학적으로 허용 가능한 염, 부형제 또는 비히클을 추가로 포함할 수 있다. 본 약학 조성물에서 사용될 약학적으로 허용 가능한 염, 부형제 또는 비히클은 담체, 부형제, 희석제, 항산화제, 보존제, 착색제, 풍미제, 희석제, 유화제, 현탁제, 용매, 충전제, 증량제, 완충제, 전달 비히클, 긴장성 물질, 보조용매, 습윤화제, 착물화제, 완충 물질, 항균제 및 계면활성제를 포함한다.
중성 완충된 식염수 또는 혈청 알부민과 혼합된 식염수는 예시적인 적절한 담체이다. 약학 조성물은 항산화제, 예컨대, 아스코르브산; 저분자량 폴리펩티드; 단백질, 예컨대, 혈청 알부민, 젤라틴 또는 면역글로불린; 친수성 중합체, 예컨대, 폴리비닐피롤리돈; 아미노산, 예컨대, 글리신, 글루타민, 아스파라긴, 아르기닌 또는 라이신; 당단류, 이당류, 및 글루코스, 만노스 또는 덱스트린을 포함하는 다른 탄수화물; 킬레이팅제, 예컨대, EDTA; 당 알코올, 예컨대, 만니톨 또는 소르비톨; 염 형성 반대이온, 예컨대, 나트륨; 및/또는 비이온성 계면활성제, 예컨대, 트윈, 플루로닉 또는 폴리에틸렌 글리콜(PEG)을 포함할 수 있다. 또한, 예를 들면, 적합한 긴장성 향상제는 알칼리 금속 할로겐화물(바람직하게는 염화나트륨 또는 염화칼륨), 만니톨, 소르비톨 등을 포함한다. 적합한 보존제는 염화벤즈알코늄, 티메로살, 페네틸 알코올, 메틸파라벤, 프로필파라벤, 클로르헥시딘, 소르브산 등을 포함한다. 과산화수소도 보존제로서 사용될 수 있다. 적합한 보조용매는 글리세린, 프로필렌 글리콜 및 PEG를 포함한다. 적합한 착물화제는 카페인, 폴리비닐피롤리돈, 베타-사이클로덱스트린 또는 하이드록시-프로필-베타-사이클로덱스트린을 포함한다. 적합한 계면활성제 또는 습윤화제는 소르비탄 에스테르, 폴리소르베이트, 예컨대, 폴리소르베이트 80, 트로메타민, 레시틴, 콜레스테롤, 틸록사팔 등을 포함한다. 완충제는 통상적인 완충제, 예컨대, 아세테이트, 보레이트, 시트레이트, 포스페이트, 바이카보네이트 또는 트리스-HCl일 수 있다. 아세테이트 완충제는 약 pH 4 내지 5.5일 수 있고, 트리스 완충제는 약 pH 7 내지 8.5일 수 있다. 추가 약제는 문헌(Remington's Pharmaceutical Sciences, 18th Edition, A. R. Gennaro, ed., Mack Publishing Company, 1990)에 기재되어 있다.
조성물은 액체 형태, 또는 동결건조된 또는 냉동-건조된 형태로 존재할 수 있고, 하나 이상의 동결보호제(lyoprotectant), 부형제, 계면활성제, 고분자량 구조적 첨가제 및/또는 증량제를 포함할 수 있다(예를 들면, 미국 특허 제6,685,940호, 제6,566,329호 및 제6,372,716호 참조). 한 실시양태에서, 비환원 당, 예컨대, 수크로스, 락토스 또는 트레할로스인 동결보호제가 포함된다. 일반적으로 포함되는 동결보호제의 양은 고장성 또는 다소 저장성 제제도 적합할 수 있을지라도 생성된 제제가 재구성 시 등장성을 나타낼 정도의 양이다. 또한, 동결보호제의 양은 동결건조 시 허용불가능한 양의 단백질 분해 및/또는 응집을 방해하기에 충분해야 한다. 미리 동결건조된 제제에서 당(예를 들면, 수크로스, 락토스, 트레할로스)에 대한 예시적인 동결보호제 농도는 약 10 mM 내지 약 400 mM이다. 또 다른 실시양태에서, 계면활성제, 예를 들면, 비이온성 계면활성제 및 이온성 계면활성제, 예컨대, 폴리소르베이트(예를 들면, 폴리소르베이트 20, 폴리소르베이트 80); 폴록사머(예를 들면, 폴록사머 188); 폴리(에틸렌 글리콜) 페닐 에테르(예를 들면, 트리톤); 나트륨 도데실 설페이트(SDS); 나트륨 라우렐 설페이트; 나트륨 옥틸 글리코사이드; 라우릴-, 미리스틸-, 리놀레일- 또는 스테아릴-설포베타인; 라우릴-, 미리스틸-, 리놀레일- 또는 스테아릴-사르코신; 리놀레일-, 미리스틸- 또는 세틸-베타인; 라우로아미도프로필-, 코카미도프로필-, 리놀레아미도프로필-, 미리스타미도프로필-, 팔미도프로필- 또는 이소스테아라미도프로필-베타인(예를 들면, 라우로아미도프로필); 미리스타미도프로필-, 팔미도프로필- 또는 이소스테아라미도프로필-디메틸아민; 나트륨 메틸 코코일- 또는 이나트륨 메틸 오페일-타우레이트; 및 MONAQUAT™ 시리즈(모나 인더스트리스 인코포레이티드(Mona Industries, Inc.), 뉴저지주 패터슨 소재), 폴리에틸 글리콜, 폴리프로필 글리콜, 및 에틸렌과 프로필렌 글리콜의 공중합체(예를 들면, 플루로닉, PF68 등)가 포함된다. 미리 동결건조된 제제에 존재할 수 있는 계면활성제의 예시적인 양은 약 0.001% 내지 0.5%이다. 고분자량 구조적 첨가제(예를 들면, 충전제, 결합제), 예를 들면, 아카시아, 알부민, 알긴산, 인산칼슘(이염기성), 셀룰로스, 카복시메틸셀룰로스, 카복시메틸셀룰로스 나트륨, 하이드록시에틸셀룰로스, 하이드록시프로필셀룰로스, 하이드록시프로필메틸셀룰로스, 미세결정질 셀룰로스, 덱스트란, 덱스트린, 덱스트레이트, 수크로스, 타일로스, 전호화 전분, 황산칼슘, 아밀로스, 글리신, 벤토나이트, 말토스, 소르비톨, 에틸셀룰로스, 인산수소이나트륨, 인산이나트륨, 피로아황산이나트륨, 폴리비닐 알코올, 젤라틴, 글루코스, 구아검(guar gum), 액체 글루코스, 압착가능한 당, 규산알루미늄마그네슘, 말토덱스트린, 폴리에틸렌 옥사이드, 폴리메타크릴레이트, 포비돈, 알긴산나트륨, 트라가칸쓰 미세결정질 셀룰로스, 전분 및 제인(zein)을 포함할 수 있다. 고분자량 구조적 첨가제의 예시적인 농도는 0.1 중량% 내지 10 중량%이다. 다른 실시양태에서, 증량제(예를 들면, 만니톨, 글리신)가 포함될 수 있다.
조성물은 비경구 투여에 적합할 수 있다. 예시적인 조성물은 숙련된 자에 의해 이용가능한 임의의 경로, 예컨대, 관절내, 피하, 정맥내, 근육내, 복강내, 뇌내(뇌실질내), 뇌실내, 안구내, 동맥내 또는 병변내 경로에 의해 동물 내로 주사되거나 주입되기에 적합하다. 비경구 제제는 전형적으로 약학적으로 허용 가능한 보존제를 임의적으로 함유하는 멸균 발열원 무함유 등장성 수성 용액일 것이다.
비수성 용매의 예는 프로필렌 글리콜, 폴리에틸렌 글리콜, 식물성 오일, 예컨대, 올리브유, 및 주사가능한 유기 에스테르, 예컨대, 에틸 올레에이트이다. 수성 담체는 식염수 및 완충된 매질을 비롯한 물, 알코올성/수성 용액, 에멀젼 또는 현탁액을 포함한다. 비경구 비히클은 염화나트륨 용액, 링커 덱스트로스, 덱스트로스 및 염화나트륨, 젖산 함유 링커 또는 고정유를 포함한다. 정맥내 비히클은 유체 및 영양분 보충제, 전해질 보충제, 예컨대, 링커 덱스트로스 기제의 보충제 등을 포함한다. 보존제 및 다른 첨가제, 예를 들면, 항균제, 항산화제, 킬레이팅제, 불활성 기체 등도 존재할 수 있다. 일반적으로, 문헌(Remington's Pharmaceutical Science, 16th Ed., Mack Eds., 1980)을 참조한다.
본원에 개시된 조성물은 특정 국소 환경에서 국소 농도의 생성물(예를 들면, 볼루스, 데포 효과) 및/또는 증가된 안정성 또는 반감기를 제공하는 방식으로 조절된 또는 지속된 전달을 위해 제제화될 수 있다. 상기 조성물은 본원에 개시된 면역글로불린 융합 단백질, 폴리펩티드, 핵산 또는 벡터와 중합체성 화합물, 예컨대, 폴리락트산, 폴리글리콜산 등의 미립자 제제의 배합물뿐만 아니라, 생체분해성 매트릭스, 주사가능한 미세구(microsphere), 미세캡슐 입자, 미세캡슐, 생체부식가능한 입자 비드, 리포좀, 및 데포 주사로서 전달될 수 있는 활성 물질의 조절된 또는 지속된 방출을 제공하는 이식가능한 전달 장치와 같은 물질도 포함할 수 있다. 이러한 지속된 또는 조절된 전달 수단을 제제화하는 기법은 공지되어 있고 다양한 중합체들이 약물의 조절된 방출 및 전달을 위해 개발되어 있고 사용되고 있다. 이러한 중합체들은 전형적으로 생체분해성이고 생체적합성이다. 거울상이성질체성 중합체 또는 폴리펩티드 분절과 온도 또는 pH 민감성 성질을 갖는 하이드로겔의 복합체화에 의해 형성된 중합체 하이드로겔을 비롯한 중합체 하이드로겔은 생체활성 단백질 물질의 포획에 관여하는 온화한 수성 조건 때문에 약물 데포 효과를 제공하는 데 바람직할 수 있다. 예를 들면, 국제 특허출원 공보 제WO 93/15722호에 제공된, 약학 조성물의 전달을 위한 조절 방출 다공성 중합체성 미세입자의 설명을 참조한다.
이 목적에 적합한 물질은 폴리락타이드(예를 들면, 미국 특허 제3,773,919호 참조), 폴리-(a-하이드록시카복실산)의 중합체, 예컨대, 폴리-D-(-)-3-하이드록시부티르산(유럽 특허 제133,988A호), L-글루탐산과 감마 에틸-L-글루타메이트의 공중합체(Sidman et al., Biopolymers, 22: 547-556 (1983)), 폴리(2-하이드록시에틸-메타크릴레이트)(Langer et al., J. Biomed. Mater. Res., 15: 167-277 (1981), and Langer, Chem. Tech., 12: 98-105 (1982)), 에틸렌 비닐 아세테이트 또는 폴리-D(-)-3-하이드록시부티르산을 포함한다. 다른 생체분해성 중합체는 폴리(락톤), 폴리(아세탈), 폴리(오르토에스테르) 및 폴리(오르토카보네이트)를 포함한다. 지속 방출 조성물은 당분야에서 공지된 여러 방법들 중 임의의 방법에 의해 제조될 수 있는 리포좀도 포함할 수 있다(예를 들면, 문헌(Eppstein et al., Proc. Natl. Acad. Sci. USA, 82: 3688-92 (1985)) 참조). 담체 그 자체 또는 그의 분해 생성물은 표적 조직에서 무독성이어야 하고 상태를 더 악화시키지 않아야 한다. 이것은 표적 장애의 동물 모델, 또는 이러한 모델이 입수불가능한 경우 정상 동물에서의 상용적인 스크리닝에 의해 확인될 수 있다.
본원에 개시된 면역글로불린 융합 단백질은 미세캡슐화될 수 있다.
본원에 개시된 약학 조성물은 비경구(정맥내, 피하, 복강내, 근육내, 혈관내, 경막내, 유리체내, 주입 또는 국소), 국부, 경구 또는 코 투여를 포함하나 이들로 한정되지 않는 임의의 적합한 투여 경로에 의해 대상체에게 투여될 수 있다.
근육내, 피하, 종양주위 또는 정맥내 주사에 적합한 제제는 생리학적으로 허용 가능한 멸균 수성 또는 비수성 용액, 분산액, 현탁액 또는 에멀젼, 및 멸균 주사가능한 용액 또는 분산액으로 재구성될 멸균 분말을 포함할 수 있다. 적합한 수성 담체 및 비수성 담체, 희석제, 용매 또는 비히클의 예로는 물, 에탄올, 폴리올(프로필렌글리콜, 폴리에틸렌-글리콜, 글리세롤, 크레모포르 등), 이들의 적합한 혼합물, 식물성 오일(예컨대, 올리브유) 및 주사가능한 유기 에스테르, 예컨대, 에틸 올레에이트가 있다. 적합한 유동성은 예를 들면, 코팅제, 예컨대, 레시틴의 사용에 의해, 분산액의 경우 요구된 입자 크기의 유지에 의해, 및 계면활성제의 사용에 의해 유지된다. 피하 주사에 적합한 제제는 임의적 첨가제, 예컨대, 보존제, 습윤화제, 유화제 및 분산제도 함유한다.
정맥내 주사의 경우, 활성 물질은 임의적으로 수성 용액 , 바람직하게는 생리학적으로 상용가능한 완충제, 예컨대, 행크 용액, 링커 용액 또는 생리학적 식염수 완충제에 제제화될 수 있다.
비경구 주사는 임의적으로 볼루스 주사 또는 연속 주입을 포함한다. 주사용 제제는 임의적으로 보존제가 첨가된 유닛 제형, 예를 들면, 앰플 또는 다회 용량 용기에 제공된다. 본원에 기재된 약학 조성물은 유성 또는 수성 비히클 중의 멸균 현탁액, 용액 또는 에멀젼으로서 비경구 주사에 적합한 형태로 존재할 수 있고, 제제화제, 예컨대, 현탁제, 안정화제 및/또는 분산제를 함유할 수 있다. 비경구 투여용 약학 제제는 수용성 형태로 활성 물질의 수성 용액을 포함한다. 추가로, 현탁액은 임의적으로 적절한 유성 주사 현탁액으로서 제조된다.
대안적으로 또는 추가로, 조성물은 본원에 개시된 면역글로불린 융합 단백질이 흡수되어 있거나 캡슐화되어 있는 막, 스폰지 또는 다른 적절한 물질을 영향받은 영역 내로 이식함으로써 국소적으로 투여될 수 있다. 이식 장치가 이용되는 경우, 이 장치는 임의의 적합한 조직 또는 장기 내로 이식될 수 있고, 본원에 개시된 면역글로불린 융합 단백질, 핵산 또는 벡터의 전달은 볼루스를 통해, 연속 투여를 통해, 또는 연속 주입을 이용한 카테터를 통해 상기 장치를 통해 직접적으로 달성될 수 있다.
본원에 개시된 면역글로불린 융합 단백질을 포함하는 약학 조성물은 예를 들면, 건조 분말로서 흡입용으로 제제화될 수 있다. 흡입 용액은 에어로졸 전달을 위해 액화된 추진제에 제제화될 수도 있다. 또 다른 제제에서, 용액은 분무될 수 있다. 폐 투여용 추가 약학 조성물은 예를 들면, 화학적으로 변경된 단백질의 폐 전달을 개시하는 국제 특허출원 공보 제WO 94/20069호에 기재된 약학 조성물을 포함한다. 폐 전달의 경우, 입자 크기는 멀리 떨어져 있는 폐로의 전달에 적합해야 한다. 예를 들면, 입자 크기는 1 ㎛ 내지 5 ㎛일 수 있으나; 예를 들면, 각각의 입자가 상당한 다공성을 갖는 경우 보다 더 큰 입자가 사용될 수 있다.
본원에 개시된 면역글로불린 융합 단백질을 포함하는 일부 제제들은 경구 투여될 수 있다. 이 방식으로 투여되는 제제는 고체 제형, 예컨대, 정제 및 캡슐제의 조제에서 통상적으로 사용되는 담체를 사용하거나 사용하지 않음으로써 제제화될 수 있다. 예를 들면, 캡슐제는 생체이용가능성이 최대화되고 사전 전신 분해가 최소화될 때 위장관 내의 지점에서 제제의 활성 부분을 방출시키도록 디자인될 수 있다. 선택적 결합제의 흡수를 용이하게 하기 위해 추가 물질이 포함될 수 있다. 희석제, 풍미제, 저융점 왁스, 식물성 오일, 윤활제, 현탁제, 정제 붕해제 및 결합제도 사용될 수 있다.
또 다른 제제는 정제의 제조에 적합한 무독성 부형제와의 혼합물로 유효량의 면역글로불린 융합 단백질을 포함할 수 있다. 정제를 멸균수 또는 또 다른 적절한 비히클에 용해시킴으로써 용액을 유닛 제형으로 제조할 수 있다. 적합한 부형제는 불활성 희석제, 예컨대, 탄산칼슘, 탄산나트륨 또는 중탄산나트륨, 락토스 또는 인산칼슘; 또는 결합제, 예컨대, 전분, 젤라틴 또는 아카시아; 또는 윤활제, 예컨대, 스테아르산마그네슘, 스테아르산 또는 탈크를 포함하나 이들로 한정되지 않는다.
적합한 및/또는 바람직한 약학 제제는 의도된 투여 경로, 전달 포맷 및 원하는 용량에 따라 본 개시 및 제제화 기술의 일반적인 지식을 고려함으로써 결정될 수 있다. 투여 방식과 관계없이, 유효 용량은 환자 체중, 신체 표면적 또는 장기 크기에 따라 계산될 수 있다.
본원에 기재된 제제들 각각을 수반하는 치료에 적절한 용량을 결정하기 위한 계산의 추가 개량은 당분야에서 관용적으로 이루어지고 당분야에서 관용적으로 수행되는 작업의 범위 내에 있다. 적절한 용량은 적절한 용량-반응 데이터의 사용을 통해 확인될 수 있다.
본원에 개시된 조성물은 예후의 제공 또는 진단 정보의 제공에 유용할 수 있다.
"약학적으로 허용 가능한"은 인간을 포함하는 동물에서의 사용에 대해 연방정부 또는 주정부의 규제 관청에 의해 승인되어 있거나 승인될 수 있거나, 미국 약전 또는 다른 일반적으로 인정된 약전에 나열되어 있다는 것을 의미할 수 있다.
"약학적으로 허용 가능한 염"은 약학적으로 허용가능하고 모 화합물의 원하는 약리학적 활성을 갖는 화합물의 염을 지칭할 수 있다.
"약학적으로 허용 가능한 부형제, 담체 또는 보조제"는 본 개시의 적어도 하나의 면역글로불린과 함께 대상체에게 투여될 수 있고 치료량의 화합물을 전달하기에 충분한 용량으로 투여될 때 그의 약리학적 활성을 파괴하지 않고 독성을 나타내지 않는 부형제, 담체 또는 보조제를 지칭할 수 있다.
"약학적으로 허용 가능한 비히클"은 본 개시의 적어도 하나의 면역글로불린과 함께 투여되는 희석제, 보조제, 부형제 또는 담체를 지칭할 수 있다.
키트
본원은 하나 이상의 면역글로불린 융합 단백질 또는 이의 성분을 포함하는 키트도 개시한다. 상기 면역글로불린 융합 단백질은 본 개시의 방법을 실시하기 위해 그의 사용을 용이하게 하는 방식으로 포장될 수 있다. 예를 들면, 키트는 방법을 실시하는 데 있어서 면역글로불린 융합 단백질의 용도를 기술하는, 용기에 부착된 표지 또는 포장 삽입물과 함께 용기 내에 포장된, 본원에 기재된 면역글로불린 융합 단백질을 포함한다. 적합한 용기는 예를 들면, 병, 바이알, 주사기 등을 포함한다. 용기는 다양한 재료들, 예컨대, 유리 또는 플라스틱으로부터 형성될 수 있다. 용기는 멸균 출입구를 가질 수 있다(예를 들면, 용기는 정맥내 용액 백, 또는 피하 주사 바늘에 의해 천공될 수 있는 마개를 갖는 바이알일 수 있다). 키트는 그 내부에 함유된 면역글로불린 융합 단백질을 갖는 용기를 포함할 수 있다. 키트는 (a) 면역글로불린 융합 단백질의 면역글로불린 영역; (b) 면역글로불린 융합 단백질의 연장제 융합 영역; (c) 연장제 융합 영역의 연장제 펩티드; (d) 연장제 융합 영역의 치료 펩티드; 또는 (e) 상기 (a) 내지 (d)의 조합을 갖는 용기를 포함할 수 있다. 키트는 제1 조성물 및 제2 조성물을 사용하여 특정 병태를 치료할 수 있다는 것을 표시하는 포장 삽입물을 추가로 포함할 수 있다. 대안적으로 또는 추가로, 키트는 약학적으로 허용 가능한 완충제(예를 들면, 정균 주사용수(BWFI), 포스페이트 완충 식염수, 링거 용액 및 덱스트로스 용액)를 포함하는 제2 (또는 제3) 용기도 포함할 수 있다. 상기 키트는 다른 완충제, 희석제, 필터, 바늘 및 주사기를 포함하나 이들로 한정되지 않는, 상업적 및 사용자 관점에 비추어 볼 때 바람직한 다른 물질을 추가로 포함할 수 있다. 면역글로불린 융합 단백질은 유닛 제형으로 포장될 수 있다. 키트는 특정 투여 경로에 따라 면역글로불린 융합 단백질을 투여하거나 스크리닝 분석을 실시하는 데 적합한 장치도 포함할 수 있다. 키트는 면역글로불린 융합 단백질 조성물의 용도를 기술하는 표지를 함유할 수 있다.
면역글로불린 융합 단백질을 포함하는 조성물은 포유동물, 예컨대, 인간, 소, 고양이, 개 및 뮤린에게 정맥내 투여되기에 적합한 약학 조성물로서 상용적인 절차에 따라 제제화될 수 있다. 전형적으로, 정맥내 투여용 조성물은 멸균 등장성 수성 완충제 중의 용액을 포함한다. 필요한 경우, 상기 조성물은 주사 부위에서의 통증을 완화시키기 위해 가용화제 및/또는 국소 마취제, 예컨대, 리그노카인도 포함할 수 있다. 일반적으로, 성분들은 따로 공급될 수 있거나 유닛 제형으로 함께 혼합될 수 있다. 예를 들면, 면역글로불린 융합 단백질은 면역글로불린 융합 단백질의 양을 표시하는 기밀하게 밀봉된 용기, 예컨대, 앰플 또는 사셰트(sachette) 내의 건조 동결건조된 분말 또는 무수 농축물로서 공급될 수 있다. 조성물이 주입에 의해 투여되어야 하는 경우, 상기 조성물은 멸균 약학 등급 물 또는 식염수를 함유하는 주입 병으로 분배될 수 있다. 조성물이 주사에 의해 투여되는 경우, 성분들이 투여 전에 혼합될 수 있도록 주사용 멸균수 또는 식염수의 앰플이 제공될 수 있다.
치료 펩티드의 비정상적인 발현 및/또는 활성과 관련된 질환 또는 장애의 치료, 억제 및/또는 예방에 효과적일, 본원에 기재된 조성물의 양은 표준 임상 기법에 의해 결정될 수 있다. 또한, 최적 용량 범위의 확인을 돕기 위해 임의적으로 시험관내 분석을 이용할 수 있다. 제제에서 사용될 정확한 용량은 투여 경로 및 질환 또는 장애의 심각성에 의해 좌우될 수도 있고, 의사의 판단 및 각각의 환자의 환경에 따라 결정되어야 한다. 유효 용량은 시험관내 동물 모델 시험 시스템 또는 임상 시험으로부터 유도된 용량-반응 곡선으로부터 추정될 수 있다.
치료 용도
본원은 하나 이상의 질환 및/또는 병태를 치료하고/하거나, 완화시키고/시키거나, 억제하고/하거나 예방하는 면역글로불린 융합 단백질 및 방법도 개시한다. 상기 방법은 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을, 이러한 치료, 완화, 억제 및/또는 예방을 필요로 하는 대상체에게 투여하는 단계를 포함할 수 있다. 상기 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 면역글로불린 융합 단백질은 비면역글로불린 영역에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 경우, 면역글로불린 융합 단백질은 (a) 적어도 하나의 이차 구조를 포함하는 연장제 펩티드; 및 (b) 치료 펩티드를 포함하는 연장제 융합 영역에 부착된 면역글로불린 영역을 포함한다. 연장제 융합 영역은 항체 영역 내에 삽입될 수 있다. 연장제 융합 영역은 항체 영역의 면역글로불린 중쇄 내에 삽입될 수 있다. 연장제 융합 영역은 항체 영역의 면역글로불린 경쇄 내에 삽입될 수 있다. 연장제 융합 영역은 항체 영역에 접합될 수 있다. 연장제 융합 영역은 항체 영역 내의 위치에 접합될 수 있다. 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소이다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 GCSF, 소 GCSF, 인간 GCSF, 모카1, Vm24, 맘바1, 550 펩티드, 인간 GLP-1, 엑센딘-4, 인간 EPO, 인간 FGF21, 인간 GMCSF, 인간 인터페론-베타, 인간 인터페론-알파, 릴랙신, 프로톡신2, 옥신토모듈린, 렙틴, 베타트로핀, 성장 분화 인자 11(GDF11), 부갑상선 호르몬, 안지오포이에틴 유사 3(ANGPTL3), IL-11, 인간 성장 호르몬(hGH), BCCX2, 엘라핀, ZP1, ZPCEX, 릴랙신, 인슐린, GLP-2, Ssam6, 550, 글루카곤, 또는 이들의 유도체 또는 변이체일 수 있다. 대안적으로 또는 추가로, 치료 펩티드는 인터류킨 8(IL-8), IL-21, 지코노타이드, 소마토스타틴, 클로로톡신, SDF1 알파, 또는 이들의 유도체 또는 변이체이다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 영역은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 영역은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 일부 경우, 면역글로불린 영역은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 영역은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 영역은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 영역은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역, 치료 펩티드 및/또는 연장제 융합 영역은 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 연장제 펩티드에 부착시킬 수 있다. 링커는 연장제 융합 영역을 면역글로불린 영역에 부착시킬 수 있다. 링커는 단백질분해성 절단 부위를 면역글로불린 영역, 연장제 융합 영역, 연장제 펩티드 또는 치료 펩티드에 부착시킬 수 있다. 링커는 연결 링커일 수 있다. 연결 링커는 치료 펩티드를 면역글로불린 영역의 아미노 말단에 연결할 수 있다.
질환 또는 병태는 자가면역 질환, 이종면역 질환 또는 병태, 염증성 질환, 병원성 감염, 혈전색전성 장애, 호흡기 질환 또는 병태, 대사 질환, 중추신경계(CNS) 장애, 골 질환 또는 암일 수 있다. 다른 경우, 질환 또는 병태는 혈액 장애이다. 일부 경우, 질환 또는 병태는 비만, 당뇨병, 골다공증, 빈혈 또는 통증이다. 일부 경우, 질환은 심장 관련 질환, 예를 들면, 심부전, 급성 관상 동맥 증후군, 심방 세동, 심장 섬유증 또는 관상 동맥 질환이다. 일부 실시양태들에서, 심부전은 비허혈성 급성 심부전, 만성 심부전, 급성 대상부전 심부전, 안정한 보상 심부전, 급성 심부전 또는 만성 심부전이다. 질환 및 병태의 추가 비한정적 예로는 고형 장기(예를 들면, 폐, 신장, 간, 심장) 이식과 관련된 허혈 재관류, 장기(예를 들면, 신장) 보호를 위한 심폐 바이패스, 허혈성 뇌졸중, 각막 치유(눈 투여), 당뇨병성 신장병증, 간경변증, 문맥 고혈압, 당뇨병성 상처 치유, 전신 경화증, 분만 시 자궁경부 숙화, 자간전증, 고혈압 및 섬유증이 있다.
일부 실시양태들에서, 치료 펩티드는 엑센딘-4이고, 질환 또는 병태는 비만, 비만 관련 병태, 당뇨병 및/또는 당뇨병 관련 병태이다. 일부 실시양태들에서, 치료 펩티드는 렙틴이고, 질환 또는 병태는 비만, 비만 관련 병태, 당뇨병 및/또는 당뇨병 관련 병태이다. 일부 실시양태들에서, 치료 펩티드는 글루카곤이고, 질환 또는 병태는 비만, 비만 관련 병태, 당뇨병 및/또는 당뇨병 관련 병태이다. 일부 실시양태들에서, 치료 펩티드는 글루카곤 유사체, 예를 들면, ZP1이고, 질환 또는 병태는 비만, 비만 관련 병태, 당뇨병 및/또는 당뇨병 관련 병태이다. 일부 실시양태들에서, 치료 펩티드는 인슐린이고, 질환 또는 병태는 비만, 비만 관련 병태, 당뇨병 및/또는 당뇨병 관련 병태이다. 일부 실시양태들에서, 치료 펩티드는 옥시토모듈린이고, 질환 또는 병태는 비만, 비만 관련 병태, 당뇨병 및/또는 당뇨병 관련 병태이다. 일부 실시양태들에서, 치료 펩티드는 글루카곤 유사 단백질, 예를 들면, GLP-1 또는 GLP-2이고, 질환 또는 병태는 비만, 비만 관련 병태, 당뇨병 및/또는 당뇨병 관련 병태이다.
일부 실시양태들에서, 치료 펩티드는 릴랙신이고, 질환 또는 병태는 심부전, 심부전 관련 병태, 섬유증 및/또는 섬유증 관련 병태이다. 릴랙신은 릴랙신2 및 내부 링커를 포함하는 릴랙신, 예컨대, 릴랙신2(XT100), 릴랙신2(XT35), 릴랙신2(단일), 릴랙신2(인슐린 C 펩티드), 릴랙신2(XT21), 릴랙신2(30GS), 릴랙신2(9GS) 및 릴랙신2(GGGPRR)를 포함한다. 일부 실시양태들에서, 치료 펩티드는 릴랙신이고, 질환 또는 병태는 심부전, 급성 관상 동맥 증후군, 심방 세동, 심장 섬유증 또는 관상 동맥 질환이다. 일부 실시양태들에서, 치료 펩티드는 릴랙신이고, 질환 또는 병태는 고형 장기(예를 들면, 폐, 신장, 간, 심장) 이식과 관련된 허혈 재관류, 장기(예를 들면, 신장) 보호를 위한 심폐 바이패스, 허혈성 뇌졸중, 각막 치유(눈 투여), 당뇨병성 신장병증, 간경변증, 문맥 고혈압, 당뇨병성 상처 치유, 전신 경화증, 분만 시 자궁경부 숙화, 자간전증, 고혈압 또는 섬유증이다.
일부 실시양태들에서, 치료 펩티드는 모카(Moka)이고, 질환 또는 병태는 자가면역 질환 또는 자가면역 질환 관련 병태이다. 치료 펩티드는 hGCSF일 수 있고, 질환 또는 병태는 호중구감소증일 수 있다. 치료 펩티드는 hGH일 수 있고, 질환 또는 병태는 성장 장애일 수 있다. 치료 펩티드는 IFN-알파일 수 있고, 질환 또는 병태는 바이러스 감염일 수 있다. 치료 펩티드는 550 펩티드일 수 있고, 질환 또는 병태는 통증일 수 있다. 치료 펩티드는 맘바(Mamba)1일 수 있고, 질환 또는 병태는 통증일 수 있다. 치료 펩티드는 Ssam6일 수 있고, 질환 또는 병태는 통증일 수 있다. 치료 펩티드는 BCCX2일 수 있고, 질환 또는 병태는 암일 수 있다. 치료 펩티드는 엘라핀일 수 있고, 질환 또는 병태는 염증일 수 있다.
질환 및/또는 병태는 만성 질환 또는 병태일 수 있다. 대안적으로, 질환 및/또는 병태는 급성 질환 또는 병태이다. 질환 또는 병태는 재발성, 불응성, 가속화된 또는 관해중인 질환 또는 병태일 수 있다. 질환 또는 병태는 하나 이상의 세포 유형에 영향을 미칠 수 있다. 하나 이상의 질환 및/또는 병태는 자가면역 질환, 염증성 질환, 심혈관 질환, 대사 장애, 임신 및 세포 증식성 장애일 수 있다.
질환 또는 병태는 자가면역 질환일 수 있다. 일부 경우, 자가면역 질환은 피부경화증, 미만성 피부경화증 또는 전신 피부경화증일 수 있다.
질환 또는 병태는 염증성 질환일 수 있다. 일부 경우, 염증성 질환은 간염, 섬유근육통 또는 건선일 수 있다.
질환 또는 병태는 류마티스성 질환일 수 있다. 일부 경우, 류마티스성 질환은 강직성 척추염, 등 통증, 활액낭염, 건염, 어깨 통증, 허리 통증, 이두박근 통증, 다리 통증, 무릎 통증, 발목 통증, 둔부 통증, 아킬레스 통증, 피막염, 목 통증, 골관절염, 전신 홍반루푸스, 류마티스성 관절염, 소아 관절염, 쇼그렌 증후군, 다발근염, 베체트병, 레이터 증후군, 또는 건선성 관절염일 수 있다. 류마티스성 질환은 만성일 수 있다. 대안적으로, 류마티스성 질환은 급성이다.
질환 또는 병태는 심혈관 질환일 수 있다. 일부 경우, 심혈관 질환은 급성 심부전, 울혈성 심부전, 보상 심부전, 대상부전 심부전, 고콜레스테롤혈증, 죽상동맥경화증, 관상 심장 질환 또는 허혈성 뇌졸중일 수 있다. 심혈관 질환은 심장 비대증일 수 있다.
질환 또는 병태는 대사 장애일 수 있다. 일부 경우, 대사 장애는 고콜레스테롤혈증, 저베타지단백질혈증, 과트리글리세라이드혈증, 고지질혈증, 이상지질혈증, 케톤증, 저지질혈증, 불응성 빈혈, 식욕 조절, 위 배출(gastric emptying), 비알코올성 지방간 질환, 비만, I형 진성 당뇨병, II형 진성 당뇨병, 임신 진성 당뇨병, 또는 대사 증후군일 수 있다. 대사 장애는 I형 당뇨병일 수 있다. 대사 장애는 II형 당뇨병일 수 있다.
질환 또는 병태는 임신일 수 있다. 면역글로불린 융합 단백질은 자간전증을 치료하거나 분만을 유도하는 데 사용될 수 있다.
질환 또는 병태는 세포 증식성 장애일 수 있다. 세포 증식성 장애는 백혈병, 림프종, 암종, 육종 또는 이들의 조합일 수 있다. 세포 증식성 장애는 골수원성 백혈병, 림프모구성 백혈병, 골수성 백혈병, 골수단핵세포성 백혈병, 호중구성 백혈병, 골수형성이상 증후군, B 세포 림프종, 버킷 림프종, 대세포 림프종, 혼합 세포 림프종, 소포성 림프종, 맨틀 세포 림프종, 호지킨 림프종, 재발성 소림프구성 림프종, 모발 세포 백혈병, 다발성 골수종, 호염기구성 백혈병, 호산구성 백혈병, 거핵아구성 백혈병, 단핵모구성 백혈병, 단핵구성 백혈병, 적백혈병, 적혈구성 백혈병, 간세포 암종, 고형 종양, 림프종, 백혈병, 지방육종(진행된/전이성), 골수성 악성종양, 유방암, 폐암, 난소암, 자궁암, 신장암, 췌장암 및 뇌의 악성 신경아교종일 수 있다.
본원은 질환 또는 병태의 치료를 필요로 하는 대상체에서 질환 또는 병태를 치료하는 방법으로서, 본원에 개시된 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 개시한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 면역글로불린 영역에 부착된 치료 펩티드를 포함한다. 일부 실시양태들에서, 치료 펩티드는 연결 펩티드로서 지칭된 화학적 링커를 통해 면역글로불린 영역에 부착된다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 일부 실시양태들에서, 치료 펩티드는 옥신토모듈린이다. 일부 실시양태들에서, 치료 펩티드는 인슐린이다. 일부 실시양태들에서, 치료 펩티드는 엑센딘-4이다. 일부 실시양태들에서, 치료 펩티드는 글루카곤 유사체이다. 질환 또는 병태는 대사 장애일 수 있다. 대사 장애는 당뇨병일 수 있다. 당뇨병은 II형 진성 당뇨병일 수 있다. 당뇨병은 I형 당뇨병일 수 있다. 대사 장애는 비만일 수 있다. 추가 대사 장애는 대사 증후군, 식욕 조절 또는 위 배출을 포함하나 이들로 한정되지 않는다.
본원은 질환 또는 병태의 치료를 필요로 하는 대상체에서 질환 또는 병태를 치료하는 방법으로서, 본원에 개시된 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 개시한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 면역글로불린 영역에 부착된 치료 펩티드를 포함한다. 일부 실시양태들에서, 치료 펩티드는 연결 펩티드로서 지칭된 화학적 링커를 통해 면역글로불린 영역에 부착된다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 일부 실시양태들에서, 치료 펩티드는 릴랙신이다. 질환 또는 병태는 심혈관 질환일 수 있다. 심혈관 질환은 급성 심부전일 수 있다. 추가 심혈관 질환은 울혈성 심부전, 보상 심부전 또는 대상부전 심부전을 포함하나 이들로 한정되지 않는다. 질환 또는 병태는 자가면역 장애일 수 있다. 자가면역 장애는 피부경화증, 미만성 피부경화증 또는 전신 피부경화증일 수 있다. 질환 또는 병태는 염증성 질환일 수 있다. 염증성 질환은 섬유근육통일 수 있다. 질환 또는 병태는 섬유증일 수 있다. 대안적으로, 질환 또는 병태는 임신이다. 면역글로불린 융합 단백질은 자간전증을 치료하거나 분만을 유도하는 데 사용될 수 있다.
본원은 질환 또는 병태의 치료를 필요로 하는 대상체에서 질환 또는 병태를 치료하는 방법으로서, 본원에 개시된 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법도 개시한다. 면역글로불린 융합 단백질은 비면역글로불린 영역에 부착된 면역글로불린 영역을 포함할 수 있다. 비면역글로불린 영역은 렙틴을 포함할 수 있다. 일부 경우, 면역글로불린 융합 단백질은 연장제 펩티드 및 렙틴인 치료 펩티드를 포함하는 연장제 융합 영역에 부착된 면역글로불린 영역을 포함한다. 질환 또는 병태는 대사 장애일 수 있다. 대사 장애는 비만일 수 있다. 대사 장애는 당뇨병일 수 있다. 당뇨병은 2형 진성 당뇨병, I형 진성 당뇨병 또는 임신 진성 당뇨병일 수 있다. 추가 대사 장애는 식욕 조절 및 비알코올성 지방간 질환을 포함하나 이들로 한정되지 않는다. 질환 또는 병태는 세포 증식성 장애일 수 있다. 세포 증식성 장애는 유방암일 수 있다. 병태는 선천성 범지방이영양증 또는 후천성 범지방이영양증을 갖는 개체에서 렙틴 결핍일 수 있다.
본원은 질환 또는 병태의 예방 또는 치료를 필요로 하는 대상체에서 질환 또는 병태를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 개시한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 면역글로불린 융합 단백질은 하나 이상의 면역글로불린 중쇄, 경쇄 또는 이들의 조합을 포함할 수 있다. 면역글로불린 융합 단백질 서열은 서열번호 43, 44, 50, 192, 195 내지 198, 201 내지 213, 216 내지 220, 222 또는 266에 의해 제공된 중쇄 서열과 50%, 60%, 70%, 80%, 85%, 90%, 95%, 97% 또는 99% 이상의 아미노산 서열 동일성을 공유할 수 있다. 면역글로불린 융합 단백질 서열은 서열번호 42, 45 내지 49, 51 내지 74, 193, 194, 199, 200, 214, 215 또는 221에 의해 제공된 경쇄 서열과 50%, 60%, 70%, 80%, 85%, 90%, 95%, 97% 또는 99% 이상의 아미노산 서열 동일성을 공유할 수 있다. 면역글로불린 중쇄는 서열번호 10, 11, 17, 161, 164 내지 167, 170 내지 182, 185 내지 189, 191 또는 265와 적어도 약 50%, 60%, 70%, 80%, 85%, 90%, 95%, 97% 또는 99% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 경쇄는 서열번호 9, 12 내지 16, 18 내지 41, 162, 163, 168, 169, 183, 184 또는 190과 적어도 약 50%, 60%, 70%, 80%, 85%, 90%, 95%, 97% 또는 99% 이상 상동성인 뉴클레오티드 서열에 의해 코딩될 수 있다. 면역글로불린 융합 단백질은 하나 이상의 링커를 추가로 포함할 수 있다. 면역글로불린 융합 단백질은 하나 이상의 내부 링커를 추가로 포함할 수 있다. 면역글로불린 융합 단백질은 하나 이상의 단백질분해성 절단 부위를 추가로 포함할 수 있다. 질환 또는 병태는 자가면역 질환, 이종면역 질환 또는 병태, 염증성 질환, 병원성 감염, 혈전색전성 장애, 호흡기 질환 또는 병태, 대사 질환, 중추신경계(CNS) 장애, 골 질환 또는 암일 수 있다. 질환 또는 병태는 혈액 장애일 수 있다. 일부 경우, 질환 또는 병태는 비만, 당뇨병, 골다공증, 빈혈 또는 통증일 수 있다. 일부 실시양태들에서, 질환 또는 병태는 심부전, 급성 관상 동맥 증후군, 심방 세동, 심장 섬유증 또는 관상 동맥 질환이다. 일부 실시양태들에서, 질환 또는 병태는 고형 장기(예를 들면, 폐, 신장, 간, 심장) 이식과 관련된 허혈 재관류, 장기(예를 들면, 신장) 보호를 위한 심폐 바이패스, 허혈성 뇌졸중, 각막 치유(눈 투여), 당뇨병성 신장병증, 간경변증, 문맥 고혈압, 당뇨병성 상처 치유, 전신 경화증, 분만 시 자궁경부 숙화, 자간전증, 고혈압, 또는 섬유증이다.
본원은 자가면역 질환의 예방 또는 치료를 필요로 하는 대상체에서 자가면역 질환을 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 개시한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 모카1, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 VM-24, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 베타-인터페론, 또는 이의 유도체 또는 변이체일 수 있다. 면역글로불린 융합 단백질 또는 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 또는 치료 펩티드는 링커를 추가로 포함할 수 있다. 링커는 모카1, VM-24, 베타-인터페론, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 자가면역 질환은 T 세포 매개 자가면역 질환일 수 있다. T 세포 매개 자가면역 질환은 다발경화증, 1형 당뇨병 및 건선을 포함하나 이들로 한정되지 않는다. 다른 경우, 자가면역 질환은 루푸스, 쇼그렌 증후군, 피부경화증, 류마티스성 관절염, 피부근염, 하시모토 갑상선염, 애디슨병, 셀리악병, 크론병, 악성 빈혈, 심상성 천포창, 백반증, 자가면역 용혈성 빈혈, 특발성 혈소판감소성 자반병, 중증 근무력증, 오드(Ord's) 갑상선염, 그레이브스병, 길랑-바레 증후군, 급성 파종 뇌척수염, 안구간대경련-근간대경련 증후군, 강직성 척추염, 항인지질 면역글로불린 증후군, 재생불량성 빈혈, 자가면역 간염, 굿파스처 증후군, 레이터 증후군, 다카야스 동맥염, 측두 동맥염, 베게너 육아종증, 전신 탈모증, 베체트병, 만성 피로, 자율신경기능이상, 자궁내막증, 간질성 방광염, 신경근긴장증, 피부경화증 및 외음부통을 포함한다. 루푸스는 급성 피부 홍반루푸스, 아급성 피부 홍반루푸스, 만성 피부 홍반루푸스, 원판상 홍반루푸스, 소아 원판상 홍반루푸스, 범원판상 홍반루푸스, 국소화된 원판상 홍반루푸스, 동창 홍반루푸스(허친슨(hutchinson)), 홍반루푸스-편평태선 중첩 증후군, 훙반루푸스 지방층염(심홍반루푸스), 종창 홍반루푸스, 사마귀모양 홍반루푸스(비대성 홍반루푸스), 보체 결핍 증후군, 약물-유도된 홍반루푸스, 신생아 홍반루푸스 및 전신 홍반루푸스를 포함할 수 있으나, 이들로 한정되지 않을 수 있다. 질환 또는 병태는 다발경화증일 수 있다. 질환 또는 병태는 당뇨병일 수 있다.
본원은 칼륨 전압 개폐(voltage-gated) 채널의 조절로부터 이익을 얻을 질환 또는 병태의 예방 또는 치료를 필요로 하는 대상체에서 상기 질환 또는 병태를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법도 개시한다. 상기 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 칼륨 전압 개폐 채널은 KCNA3 또는 Kv1.3 채널일 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 모카1, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 VM24, 또는 이의 유도체 또는 변이체일 수 있다. 면역글로불린 융합 단백질 또는 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 모카1, VM-24, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 상기 질환 또는 병태는 자가면역 질환일 수 있다. 자가면역 질환은 T 세포 매개 자가면역 질환일 수 있다. 상기 질환 또는 병태는 간헐적 실조증, 발작 또는 신경근긴장증일 수 있다. 칼륨 전압 개폐 채널의 조절은 칼륨 전압 개폐 채널의 억제 또는 차단을 포함할 수 있다. 칼륨 전압 개폐 채널의 조절은 칼륨 전압 개폐 채널의 활성화를 포함할 수 있다.
본원은 대사 질환 또는 병태의 예방 또는 치료를 필요로 하는 대상체에서 대사 질환 또는 병태를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 GLP-1, 엑센딘-4, FGF21, 또는 이들의 유도체 또는 변이체일 수 있다. GLP-1은 인간 GLP-1일 수 있다. FGF21은 인간 FGF21일 수 있다. 면역글로불린 또는 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 GLP-1, 엑센딘-4, FGF21, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 대사 질환 및/또는 병태는 탄수화물 대사 장애, 아미노산 대사 장애, 유기산 대사 장애(유기 산뇨), 지방산 산화 및 미토콘드리아 대사 장애, 포피린 대사 장애, 푸린 또는 피리미딘 대사 장애, 스테로이드 대사 장애, 미토콘드리아 기능 장애, 퍼록시좀 기능 장애, 우레아 주기 장애, 우레아 주기 결함 또는 라이소좀 저장 장애를 포함할 수 있다. 대사 질환 또는 병태는 당뇨병일 수 있다. 다른 경우, 대사 질환 또는 병태는 글리코겐 저장 질환, 페닐케톤뇨증, 단풍시럽뇨 질환, 글루타르산혈증 1형, 카바모일 포스페이트 합성효소(synthetase) I 결핍, 알캅톤뇨증, 중간-쇄 아실-보조효소 A 데하이드로게나제(dehydrogenase) 결핍(MCADD), 급성 간헐성 포르피린증(porphyria), 레쉬-니한(Lesch-Nyhan) 증후군, 유지질 선천성 부신 과다형성, 선천성 부신 과다형성, 컨스-세이어(Kearns-Sayre) 증후군, 젤웨거(Zellweger) 증후군, 고셔병(Gaucher's disease) 또는 니만 픽병(Niemann Pick disease)일 수 있다.
본원은 중추신경계(CNS) 장애의 예방 또는 치료를 필요로 하는 대상체에서 CNS 장애를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 GLP-1, 엑센딘-4, 또는 이들의 유도체 또는 변이체일 수 있다. GLP-1은 인간 GLP-1일 수 있다. 면역글로불린은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 GLP-1, 엑센딘-4, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. CNS 장애는 알츠하이머병(AD)일 수 있다. 추가 CNS 장애는 뇌염, 뇌수막염, 열대 경련성 대부전마비, 지주막낭종, 헌팅톤병, 락트-인(locked-in) 증후군, 파킨슨병, 뚜렛 및 다발경화증을 포함하나 이들로 한정되지 않는다.
본원은 GLP-1R 및/또는 글루카곤 수용체(GCGR) 아고니스트로부터 이익을 얻는 질환 또는 병태의 예방 또는 치료를 필요로 하는 대상체에서 상기 질환 또는 병태를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 GLP-1, 엑센딘-4, 또는 이들의 유도체 또는 변이체일 수 있다. GLP-1은 인간 GLP-1일 수 있다. 면역글로불린 융합 단백질 또는 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 GLP-1, 엑센딘-4, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 상기 질환 또는 병태는 대사 질환 또는 장애일 수 있다. 상기 질환 또는 병태는 당뇨병일 수 있다. 다른 경우, 상기 질환 또는 병태는 비만일 수 있다. GLP-1R 및/또는 GCGR 아고니스트로부터 이익을 얻는 추가 질환 및/또는 병태는 이상지질혈증, 심혈관 질환 및 지방간 질환을 포함하나 이들로 한정되지 않는다.
본원은 혈액 장애의 예방 또는 치료를 필요로 하는 대상체에서 혈액 장애를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 에리쓰로포이에틴, GMCSF, 또는 이들의 유도체 또는 변이체일 수 있다. 에리쓰로포이에틴은 인간 에리쓰로포이에틴일 수 있다. GMCSF는 인간 GMCSF일 수 있다. 면역글로불린은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 에리쓰로포이에틴, GMCSF, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 혈액 장애는 빈혈일 수 있다. 빈혈의 예로는 유전성 제로사이토시스(xerocytosis), 선천성 적혈구생성이상 빈혈, Rh 널(null) 질환, 감염성 단핵구증 관련 빈혈, 약물 관련 빈혈, 재생불량성 빈혈, 소적혈구성 빈혈, 대적혈구성 빈혈, 정상적혈구성 빈혈, 용혈성 빈혈, 변형적혈구성 빈혈, 구상적혈구성 빈혈, 겸상적혈구성 빈혈, 정상색소성 빈혈, 고색소성 빈혈, 저색소성 빈혈, 대적혈구성-정상색소성 빈혈, 소적혈구성-저색소성 빈혈, 정상적혈구성-정상색소성 빈혈, 철 결핍 빈혈, 악성 빈혈, 폴레이트 결핍 빈혈, 지중해빈혈, 철적혈모구성 빈혈, 출혈 후 빈혈, 겸상 세포 빈혈, 만성 빈혈, 이용불능성 빈혈, 자가면역 용혈성 빈혈, 쿨리(Cooley's) 빈혈, 약물 유도된 면역 용혈성 빈혈, 적혈모구성 빈혈, 저형성 빈혈, 다이아몬드-블랙판(Diamond-Blackfan) 빈혈, 피어슨(Pearson's) 빈혈, 일시적 빈혈, 판코니(Fanconi's) 빈혈, 레더러(Lederer's) 빈혈, 척수병증성 빈혈, 영양 빈혈, 돌기 세포(spur-cell) 빈혈, 폰 야크쉬(Von Jaksh's) 빈혈, 철적혈모구성 빈혈, 철결핍성 빈혈, 알파 지중해빈혈, 베타 지중해빈혈, 헤모글로빈 h 질환, 급성 후천성 용혈성 빈혈, 온난 자가면역 용혈성 빈혈, 한랭 자가면역 용혈성 빈혈, 일차 한랭 자가면역 용혈성 빈혈, 이차 한랭 자가면역 용혈성 빈혈, 이차 자가면역 용혈성 빈혈, 일차 자가면역 용혈성 빈혈, x-연관 철적혈모구성 빈혈, 피리독신 반응성 빈혈, 영양 철적혈모구성 빈혈, 피리독신 결핍 유도된 철적혈모구성 빈혈, 구리 결핍 유도된 철적혈모구성 빈혈, 사이클로세린 유도된 철적혈모구성 빈혈, 클로람페니콜 유도된 철적혈모구성 빈혈, 에탄올 유도된 철적혈모구성 빈혈, 이소니아지드 유도된 철적혈모구성 빈혈, 약물 유도된 철적혈모구성 빈혈, 독소 유도된 철적혈모구성 빈혈, 소적혈구성 고색소성 빈혈, 대적혈구성 고색소성 빈혈, 거대적혈구성-정상색소성 빈혈, 약물 유도된 면역 용혈성 빈혈, 비유전성 구상적혈구성 빈혈, 유전성 구상적혈구성 빈혈 및 선천성 구상적혈구성 빈혈이 있으나 이들로 한정되지 않는다. 다른 경우, 혈액 장애는 말라리아일 수 있다. 대안적으로, 혈액 장애는 림프종, 백혈병, 다발성 골수종 또는 골수형성이상 증후군일 수 있다. 혈액 장애는 호중구감소증, 슈와크만-다이몬드(shwachman-daimond syndrome) 증후군, 코스트만(Kostmann) 증후군, 만성 육아종증 질환, 백혈구 부착 결핍, 미엘로퍼록시다제 결핍 또는 체디악 히가시(Chediak Higashi) 증후군일 수 있다.
본원은 백혈구 생성의 자극 또는 증가로부터 이익을 얻는 질환 또는 장애의 예방 또는 치료를 필요로 하는 대상체에서 이러한 질환 또는 장애를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 GMCSF, 또는 이의 유도체 또는 변이체일 수 있다. GMCSF는 인간 GMCSF일 수 있다. 면역글로불린 융합 단백질 또는 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 면역글로불린 영역을 면역글로불린 영역에 부착시킬 수 있다. 상기 질환 또는 장애는 호중구감소증, 슈와크만-다이아몬드 증후군, 코스트만 증후군, 만성 육아종증 질환, 백혈구 부착 결핍, 미엘로퍼록시다제 결핍 또는 체디악 히가시 증후군일 수 있다.
본원은 적혈구 생성의 자극 또는 증가로부터 이익을 얻는 질환 또는 장애의 예방 또는 치료를 필요로 하는 대상체에서 이러한 질환 또는 장애를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 에리쓰로포이에틴, 또는 이의 유도체 또는 변이체일 수 있다. 에리쓰로포이에틴은 인간 에리쓰로포이에틴일 수 있다. 면역글로불린은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 에리쓰로포이에틴, 또는 이의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 상기 질환 또는 장애는 빈혈일 수 있다.
본원은 비만의 예방 또는 치료를 필요로 하는 대상체에서 비만을 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 GLP-1, 또는 이의 유도체 또는 변이체일 수 있다. GLP-1은 인간 GLP-1일 수 있다. 치료 펩티드는 FGF21, 또는 이의 유도체 또는 변이체일 수 있다. FGF21은 인간 FGF21일 수 있다. 치료 펩티드는 엑센딘-4, 또는 이의 유도체 또는 변이체일 수 있다. 면역글로불린은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 GLP-1, 엑센딘-4, FGF21, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다.
본원은 통증의 예방 또는 치료를 필요로 하는 대상체에서 통증을 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 대상체는 포유동물일 수 있다. 일부 경우, 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 프로톡신2, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 550 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 맘바1, 또는 이의 유도체 또는 변이체일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 프로톡신2, 550 펩티드 또는 맘바1, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다.
본원은 나트륨 이온 채널의 조절로부터 이익을 얻는 질환 또는 병태의 예방 또는 치료를 필요로 하는 대상체에서 이러한 질환 또는 병태를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 대상체는 포유동물일 수 있다. 일부 경우, 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 프로톡신2, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 550 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 하나 이상의 항체, 면역글로불린 단편 또는 면역글로불린 구축물은 링커를 추가로 포함한다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 나트륨 이온 채널은 Nav 채널일 수 있다. Nav 채널은 Nav1.7 채널일 수 있다. 나트륨 이온 채널의 조절은 나트륨 이온 채널의 억제 또는 차단을 포함할 수 있다. 나트륨 이온 채널의 조절은 나트륨 이온 채널의 활성화를 포함할 수 있다. 상기 질환 또는 병태는 드라벳(Dravet) 증후군, 열성 발작 플러스를 동반하는 범간질(GEFS+), 선천성 이상근긴장증 또는 홍색사지통증일 수 있다. 상기 질환 또는 병태는 통증일 수 있다.
본원은 산 감지 이온 채널(ASIC)의 조절로부터 이익을 얻는 질환 또는 병태의 예방 또는 치료를 필요로 하는 대상체에서 이러한 질환 또는 병태를 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 대상체는 포유동물일 수 있다. 일부 경우, 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 프로톡신2, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 맘바1, 또는 이의 유도체 또는 변이체일 수 있다. 하나 이상의 항체, 면역글로불린 단편 또는 면역글로불린 구축물은 링커를 추가로 포함한다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. ASIC의 조절은 ASIC의 억제 또는 차단을 포함할 수 있다. ASIC의 조절은 ASIC의 활성화를 포함할 수 있다. 상기 질환 또는 병태는 중추신경계 장애일 수 있다. 다른 경우, 상기 질환 또는 병태는 통증이다.
본원은 병원성 감염의 예방 또는 치료를 필요로 하는 대상체에서 병원성 감염을 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 알파-인터페론, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 베타-인터페론, 또는 이의 유도체 또는 변이체일 수 있다. 면역글로불린은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 알파-인터페론, 베타-인터페론, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 병원성 감염은 세균 감염일 수 있다. 병원성 감염은 진균 감염일 수 있다. 병원성 감염은 기생충 감염일 수 있다. 병원성 감염은 바이러스 감염일 수 있다. 바이러스 감염은 헤르페스 바이러스 감염일 수 있다.
본원은 암의 예방 또는 치료를 필요로 하는 대상체에서 암을 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 상기 조성물은 약학적으로 허용 가능한 담체를 추가로 포함할 수 있다. 대상체는 포유동물일 수 있다. 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 베타-인터페론, 또는 이의 유도체 또는 변이체일 수 있다. 치료 펩티드는 BCCX2, 또는 이의 유도체 또는 변이체일 수 있다. 면역글로불린은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래될 수 있다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린일 수 있다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 베타-인터페론, BCCX2, 또는 이들의 유도체 또는 변이체를 면역글로불린 영역에 부착시킬 수 있다. 암은 혈액 악성종양일 수 있다. 혈액 악성종양은 백혈병 또는 림프종일 수 있다. 혈액 악성종양은 B 세포 림프종, T 세포 림프종, 소포성 림프종, 변연부 림프종, 모발 세포 백혈병, 만성 골수성 백혈병, 맨틀 세포 림프종, 결절성 림프종, 버킷 림프종, 피부 T 세포 림프종, 만성 림프구성 백혈병 또는 소림프구성 백혈병일 수 있다.
본원은 수용체의 조절로부터 이익을 얻을 질환 또는 병태의 예방 또는 치료를 필요로 하는 대상체에서 이러한 질환 또는 병태를 예방하거나 치료하는 방법으로서, 본원에 개시된 조성물을 상기 대상체에게 투여하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 일부 경우, 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함하는 하나 이상의 면역글로불린 융합 단백질을 포함한다. 대상체는 포유동물일 수 있다. 일부 경우, 포유동물은 인간일 수 있다. 대안적으로, 포유동물은 소일 수 있다. 치료 펩티드는 hGCSF, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 GCSFR일 수 있다. 치료 펩티드는 에리쓰로포이에틴, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 EPOR일 수 있다. 치료 펩티드는 엑센딘-4, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 GLP1R일 수 있다. 치료 펩티드는 GLP-1, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 GLP1R일 수 있다. 치료 펩티드는 렙틴, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 LepR일 수 있다. 치료 펩티드는 hGH, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 GHR일 수 있다. 치료 펩티드는 인터페론-알파, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 IFNR일 수 있다. 치료 펩티드는 인터페론-베타, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 IFNR일 수 있다. 치료 펩티드는 릴랙신, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 LGR7일 수 있다. 치료 펩티드는 BCCX2, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 CXCR4일 수 있다. 치료 펩티드는 GMCSF, 또는 이의 유도체 또는 변이체일 수 있고, 수용체는 GMCSFR일 수 있다. 하나 이상의 면역글로불린 융합 단백질, 치료 펩티드 또는 면역글로불린 영역은 링커를 추가로 포함한다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 상기 질환 또는 병태는 자가면역 질환일 수 있다. 자가면역 질환은 T 세포 매개 자가면역 질환일 수 있다. 상기 질환 또는 병태는 대사 장애일 수 있다. 대사 장애는 당뇨병일 수 있다. 상기 질환 또는 병태는 염증성 장애일 수 있다. 염증성 장애는 다발경화증일 수 있다. 상기 질환 또는 병태는 세포 증식성 장애일 수 있다. 상기 질환 또는 병태는 혈액 장애일 수 있다. 혈액 장애는 호중구감소증일 수 있다. 혈액 장애는 빈혈일 수 있다. 상기 질환 또는 병태는 병원성 감염일 수 있다. 병원성 감염은 바이러스 감염일 수 있다. 상기 질환 또는 병태는 성장 장애일 수 있다. 상기 질환 또는 병태는 심혈관 병태일 수 있다. 심혈관 병태는 급성 심부전일 수 있다. 수용체의 조절은 수용체의 억제 또는 차단을 포함할 수 있다. 수용체의 조절은 수용체의 활성화를 포함할 수 있다. 치료 펩티드는 수용체 아고니스트로서 작용할 수 있다. 치료 펩티드는 수용체 길항제로서 작용할 수 있다.
본원은 질환의 예방 또는 치료를 필요로 하는 포유동물에서 질환을 예방하거나 치료하는 방법으로서, 본원에 기재된 약학 조성물을 상기 포유동물에게 투여하는 단계를 포함하는 방법을 제공한다. 일부 실시양태들에서, 질환은 감염성 질환일 수 있다. 일부 실시양태들에서, 감염성 질환은 유방염일 수 있다. 일부 실시양태들에서, 감염성 질환은 호흡기 질환일 수 있다. 일부 실시양태들에서, 호흡기 질환은 수송열의 소 호흡기 질환일 수 있다. 일부 실시양태들에서, 필요로 하는 포유동물은 소, 낙타, 당나귀, 염소, 말, 순록, 양, 물소, 무스(moose) 및 야크를 포함하는 목록으로부터 선택된 낙농 동물일 수 있다. 일부 실시양태들에서, 포유동물은 소일 수 있다.
본원은 낙농 동물에서 유방염을 예방하거나 치료하는 방법으로서, 본원에 개시된 하나 이상의 면역글로불린 융합 단백질을 포함하는 조성물 유효량을 상기 낙농 동물에게 제공하는 단계를 포함하는 방법을 제공한다. 면역글로불린 융합 단백질은 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 치료 펩티드는 GCSF일 수 있다. GCSF는 소 GCSF일 수 있다. GCSF는 인간 GCSF일 수 있다. 일부 실시양태들에서, 낙농 동물은 소 또는 물소일 수 있다.
본원은 본원에 기재된 면역글로불린 융합 단백질 또는 약학 조성물 유효량을, 질환 또는 병태의 치료, 억제 또는 예방을 필요로 하는 대상체에게 투여함으로써 상기 대상체에서 질환 또는 병태를 치료하거나, 억제하거나 예방하는 방법을 제공한다. 면역글로불린 융합 단백질은 실질적으로 정제될 수 있다(예를 들면, 그의 효과를 한정하거나 원치 않는 부작용을 생성하는 물질을 실질적으로 함유하지 않을 수 있다). 대상체는 동물, 예컨대, 소, 돼지, 양, 염소, 토끼, 말, 닭, 고양이, 개, 마우스 등을 포함하나 이들로 한정되지 않는 동물일 수 있다. 대상체는 포유동물일 수 있다. 대상체는 인간일 수 있다. 대상체는 비인간 영장류일 수 있다. 대안적으로, 대상체는 소일 수 있다. 대상체는 조류, 파충류 또는 양서류일 수 있다.
추가 용도
본원은 질환 또는 병태의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 추가로 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 본원은 질환 또는 병태의 치료용 약제의 제조에 있어서 치료 펩티드에 부착된 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질의 용도를 개시한다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 본원은 질환 또는 병태의 치료용 약제의 제조에 있어서 치료 펩티드에 부착된 면역글로불린 영역을 포함하는 면역글로불린 융합 단백질의 용도를 추가로 개시한다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 면역글로불린 융합 단백질은 하나 이상의 내부 링커, 하나 이상의 프로테아제 절단 부위, 하나 이상의 연결 펩티드, 하나 이상의 연장제 펩티드 및 이들의 임의의 조합을 포함할 수 있다. 하나 이상의 내부 링커, 하나 이상의 프로테아제 절단 부위, 하나 이상의 연결 펩티드 및/또는 하나 이상의 연장제 펩티드는 면역글로불린 영역 내에 삽입될 수 있다. 하나 이상의 내부 링커, 하나 이상의 프로테아제 절단 부위, 하나 이상의 연결 펩티드 및/또는 하나 이상의 연장제 펩티드는 치료 펩티드 내에 삽입될 수 있다. 하나 이상의 내부 링커, 하나 이상의 프로테아제 절단 부위, 하나 이상의 연결 펩티드 및/또는 하나 이상의 연장제 펩티드는 면역글로불린 영역의 아미노 말단에 연결될 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 GCSF를 포함할 수 있다. GCSF는 인간 GCSF를 포함할 수 있다. 치료 펩티드는 모카1을 포함할 수 있다. 치료 펩티드는 VM24를 포함할 수 있다. 치료 펩티드는 엑센딘-4를 포함할 수 있다. 치료 펩티드는 에리쓰로포이에틴을 포함할 수 있다. 에리쓰로포이에틴은 인간 에리쓰로포이에틴을 포함할 수 있다. 치료 펩티드는 렙틴을 포함할 수 있다. 치료 펩티드는 인슐린을 포함할 수 있다. 치료 펩티드는 Ssam6을 포함할 수 있다. 치료 펩티드는 옥신토모듈린을 포함할 수 있다. 치료 펩티드는 성장 호르몬(GH)을 포함할 수 있다. 성장 호르몬은 인간 성장 호르몬(hGH)일 수 있다. 치료 펩티드는 인터페론-알파를 포함할 수 있다. 치료 펩티드는 글루카곤 유사체를 포함할 수 있다. 치료 펩티드는 인터페론-베타를 포함할 수 있다. 치료 펩티드는 GLP-1을 포함할 수 있다. 치료 펩티드는 GLP-2를 포함할 수 있다. 치료 펩티드는 릴랙신을 포함할 수 있다. 치료 펩티드는 550 펩티드를 포함할 수 있다. 치료 펩티드는 맘바1을 포함할 수 있다. 치료 펩티드는 BCCX2를 포함할 수 있다. 치료 펩티드는 엘라핀을 포함할 수 있다. 치료 펩티드는 베타트로핀을 포함할 수 있다. 치료 펩티드는 GDF11을 포함할 수 있다. 치료 펩티드는 GMCSF를 포함할 수 있다. 치료 펩티드는 글루카곤을 포함할 수 있다. 질환 또는 병태는 자가면역 질환, 이종면역 질환 또는 병태, 염증성 질환, 병원성 감염, 혈전색전성 장애, 호흡기 질환 또는 병태, 대사 질환, 중추신경계(CNS) 장애, 골 질환 또는 암일 수 있다. 다른 경우, 질환 또는 병태는 혈액 장애이다. 일부 경우, 질환 또는 병태는 비만, 당뇨병, 골다공증, 빈혈 또는 통증이다. 질환 또는 병태는 성장 장애일 수 있다. 일부 실시양태들에서, 질환 또는 병태는 심부전, 급성 관상 동맥 증후군, 심방 세동, 심장 섬유증 또는 관상 동맥 질환이다. 일부 실시양태들에서, 질환 또는 병태는 고형 장기(예를 들면, 폐, 신장, 간, 심장) 이식과 관련된 허혈 재관류, 장기(예를 들면, 신장) 보호를 위한 심폐 바이패스, 허혈성 뇌졸중, 각막 치유(눈 투여), 당뇨병성 신장병증, 간경변증, 문맥 고혈압, 당뇨병성 상처 치유, 전신 경화증, 분만 시 자궁경부 숙화, 자간전증, 고혈압, 또는 섬유증이다.
본원은 세포 증식성 장애의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 세포 증식성 장애는 암일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 BCCX2일 수 있다.
본원은 대사 장애의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 대사 장애는 당뇨병일 수 있다. 당뇨병은 I형 당뇨병일 수 있다. 당뇨병은 II형 당뇨병일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 엑센딘-4일 수 있다. 치료 펩티드는 GLP-1일 수 있다. 치료 펩티드는 렙틴일 수 있다. 치료 펩티드는 베타트로핀일 수 있다.
본원은 자가면역 질환 또는 병태의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 모카1일 수 있다. 치료 펩티드는 VM24일 수 있다.
본원은 염증성 질환 또는 병태의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 염증성 질환 또는 병태는 다발경화증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 엘라핀일 수 있다. 치료 펩티드는 인터페론-베타일 수 있다.
본원은 중추신경계의 질환 또는 병태의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 중추신경계의 질환 또는 병태는 통증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 영역은 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 550 펩티드일 수 있다. 치료 펩티드는 맘바1일 수 있다.
본원은 심혈관 질환 또는 병태의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 심혈관 질환 또는 병태는 급성 심부전일 수 있다. 심혈관 질환 또는 병태는 심장 비대증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 릴랙신일 수 있다. 치료 펩티드는 GDF11일 수 있다.
본원은 혈액 질환 또는 병태의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 혈액 질환 또는 병태는 빈혈일 수 있다. 혈액 질환 또는 병태는 호중구감소증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 GCSF일 수 있다. GCSF는 인간 GCSF일 수 있다. 치료 펩티드는 에리쓰로포이에틴일 수 있다. 에리쓰로포이에틴은 인간 에리쓰로포이에틴일 수 있다. 치료 펩티드는 GMCSF일 수 있다.
본원은 병원성 감염의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 병원성 감염은 바이러스 감염일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 인터페론-알파일 수 있다.
본원은 성장 장애의 치료용 약제의 제조에 있어서 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 성장 장애의 예로는 연골무형성증, 소아의 연골무형성증, 말단비대증, 지방생식기이영양증, 왜소증, 거인증, 브룩 그린버그(Brooke Greenberg), 편측비대증, 연골형성저하증, 얀센(Jansen's) 골간단부 연골이형성증, 코와르스키(Kowarski) 증후군, 레리-웨일(Leri-Weill) 연골뼈형성이상증, 국소 거인증, 지방종성 거대증, 마쥬스키(Majewski's) 다지증 증후군, 소두 골형성이상 원발성 왜소증 II형, 난쟁이, 과다성장 증후군, 파라스트렘매틱(parastremmatic) 왜소증, 원발성 왜소증, 가성연골무형성증, 심리사회적 저신장(psychosocial short stature), 시클(Seckel) 증후군, 짧은 늑골 - 다지증 증후군 및 실버-러셀(Silver-Russell) 증후군이 있으나 이들로 한정되지 않는다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 성장 호르몬일 수 있다. 성장 호르몬은 인간 성장 호르몬(hGH)일 수 있다.
본원은 질환 또는 병태의 치료용 면역글로불린 융합 단백질의 용도도 개시한다. 본원은 질환 또는 병태의 치료를 필요로 하는 대상체에서 질환 또는 병태를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 GCSF를 포함할 수 있다. GCSF는 인간 GCSF일 수 있다. 치료 펩티드는 모카1일 수 있다. 치료 펩티드는 VM24일 수 있다. 치료 펩티드는 엑센딘-4일 수 있다. 치료 펩티드는 에리쓰로포이에틴일 수 있다. 에리쓰로포이에틴은 인간 에리쓰로포이에틴일 수 있다. 치료 펩티드는 렙틴일 수 있다. 치료 펩티드는 성장 호르몬(GH)일 수 있다. 성장 호르몬은 인간 성장 호르몬(hGH)일 수 있다. 치료 펩티드는 인터페론-알파일 수 있다. 치료 펩티드는 인터페론-베타일 수 있다. 치료 펩티드는 GLP-1일 수 있다. 치료 펩티드는 릴랙신일 수 있다 .치료 펩티드는 550 펩티드일 수 있다. 치료 펩티드는 맘바1일 수 있다. 치료 펩티드는 BCCX2일 수 있다. 치료 펩티드는 엘라핀일 수 있다. 치료 펩티드는 베타트로핀일 수 있다. 치료 펩티드는 GDF11일 수 있다. 치료 펩티드는 GMCSF일 수 있다. 질환 또는 병태는 자가면역 질환, 이종면역 질환 또는 병태, 염증성 질환, 병원성 감염, 혈전색전성 장애, 호흡기 질환 또는 병태, 대사 질환, 중추신경계(CNS) 장애, 골 질환 또는 암일 수 있다. 다른 경우, 질환 또는 병태는 혈액 장애이다. 일부 경우, 질환 또는 병태는 비만, 당뇨병, 골다공증, 빈혈 또는 통증이다. 질환 또는 병태는 성장 장애일 수 있다.
본원은 세포 증식성 장애의 치료를 필요로 하는 대상체에서 세포 증식성 장애를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 BCCX2일 수 있다.
본원은 대사 장애의 치료를 필요로 하는 대상체에서 대사 장애를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 대사 장애는 당뇨병일 수 있다. 당뇨병은 I형 당뇨병일 수 있다. 당뇨병은 II형 당뇨병일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 엑센딘-4일 수 있다. 치료 펩티드는 GLP-1일 수 있다. 치료 펩티드는 렙틴일 수 있다. 치료 펩티드는 베타트로핀일 수 있다.
본원은 자가면역 질환 또는 병태의 치료를 필요료 하는 대상체에서 자가면역 질환 또는 병태를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 모카1일 수 있다. 치료 펩티드는 VM24일 수 있다.
본원은 염증성 질환 또는 병태의 치료를 필요로 하는 대상체에서 염증성 질환 또는 병태를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 염증성 질환 또는 병태는 다발경화증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 엘라핀일 수 있다. 치료 펩티드는 인터페론-베타일 수 있다.
본원은 중추신경계의 질환 또는 병태의 치료를 필요로 하는 대상체에서 중추신경계의 질환 또는 병태를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 중추신경계의 질환 또는 병태는 통증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 550 펩티드일 수 있다. 치료 펩티드는 맘바1일 수 있다.
본원은 심혈관 질환 또는 병태의 치료를 필요로 하는 대상체에서 심혈관 질환 또는 병태를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 일부 실시양태들에서, 면역글로불린 융합 단백질은 심부전, 급성 관상 동맥 증후군, 심방 세동, 심장 섬유증 및 관상 동맥 질환으로부터 선택된 질환 또는 병태를 치료한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 심혈관 질환 또는 병태는 급성 심부전일 수 있다. 심혈관 질환 또는 병태는 심장 비대증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 릴랙신일 수 있다. 치료 펩티드는 GDF11일 수 있다.
본원은 혈액 질환 또는 병태의 치료를 필요로 하는 대상체에서 혈액 질환 또는 병태를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 혈액 질환 또는 병태는 빈혈일 수 있다. 혈액 질환 또는 병태는 호중구감소증일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 GCSF일 수 있다. GCSF는 인간 GCSF일 수 있다. 치료 펩티드는 에리쓰로포이에틴일 수 있다. 에리쓰로포이에틴은 인간 에리쓰로포이에틴일 수 있다. 치료 펩티드는 GMCSF일 수 있다.
본원은 병원성 감염의 치료를 필요로 하는 대상체에서 병원성 감염을 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 병원성 감염은 바이러스 감염일 수 있다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 인터페론-알파일 수 있다.
본원은 성장 장애의 치료를 필요로 하는 대상체에서 성장 장애를 치료하기 위한 면역글로불린 융합 단백질의 용도를 개시한다. 면역글로불린 융합 단백질은 본원에 개시된 면역글로불린 융합 단백질들 중 임의의 면역글로불린 융합 단백질일 수 있다. 면역글로불린 융합 단백질은 하나 이상의 치료 펩티드에 부착된 면역글로불린 영역을 포함할 수 있다. 일부 실시양태들에서, 치료 펩티드는 면역글로불린 영역의 아미노 말단에 부착된다. 성장 장애의 예로는 연골무형성증, 소아의 연골무형성증, 말단비대증, 지방생식기이영양증, 왜소증, 거인증, 브룩 그린버그, 편측비대증, 연골형성저하증, 얀센 골간단부 연골이형성증, 코와르스키 증후군, 레리-웨일 연골뼈형성이상증, 국소 거인증, 지방종성 거대증, 마쥬스키 다지증 증후군, 소두 골형성이상 원발성 왜소증 II형, 난쟁이, 과다성장 증후군, 소두 골형성이상 원발성 왜소증 II형, 난쟁이, 과다성장 증후군, 파라스트렘매틱 왜소증, 원발성 왜소증, 가성연골무형성증, 심리사회적 저신장, 시클 증후군, 짧은 늑골 - 다지증 증후군 및 실버-러셀 증후군이 있으나 이들로 한정되지 않는다. 면역글로불린 영역은 하나 이상의 면역글로불린 도메인을 포함할 수 있다. 면역글로불린 도메인은 면역글로불린 A, 면역글로불린 D, 면역글로불린 E, 면역글로불린 G 또는 면역글로불린 M일 수 있다. 면역글로불린 도메인은 면역글로불린 중쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 면역글로불린 경쇄 영역 또는 이의 단편일 수 있다. 면역글로불린 도메인은 항바이러스 면역글로불린, 항균 면역글로불린, 항기생충 면역글로불린 및/또는 항진균 면역글로불린으로부터 유래될 수 있다. 일부 경우, 면역글로불린 도메인은 포유동물 면역글로불린으로부터 유래된다. 대안적으로, 면역글로불린 도메인은 키메라 면역글로불린으로부터 유래된다. 면역글로불린 도메인은 조작된 면역글로불린 또는 재조합 면역글로불린으로부터 유래될 수 있다. 면역글로불린 도메인은 인간화된, 조작된 인간 또는 완전한 인간 면역글로불린으로부터 유래될 수 있다. 포유동물 면역글로불린은 소 면역글로불린일 수 있다. 포유동물 면역글로불린은 인간 면역글로불린일 수 있다. 다른 경우, 포유동물 면역글로불린은 뮤린 면역글로불린이다. 면역글로불린 융합 단백질, 면역글로불린 영역 및/또는 치료 펩티드는 하나 이상의 링커를 추가로 포함할 수 있다. 링커는 치료 펩티드를 면역글로불린 영역에 부착시킬 수 있다. 치료 펩티드는 펩티드, 또는 이의 유도체 또는 변이체일 수 있다. 대안적으로, 치료 펩티드는 소분자이다. 치료 펩티드는 성장 호르몬일 수 있다. 성장 호르몬은 인간 성장 호르몬(hGH)일 수 있다.
약리학적 특성
본원은 치료 펩티드의 하나 이상의 약리학적 특성을 개선하는 방법을 개시한다. 상기 방법은 본원에 개시된 면역글로불린 융합 단백질을 생성하는 단계를 포함할 수 있다. 약리학적 특성의 예로는 반감기, 안정성, 가용성, 면역원성, 독성, 생체이용가능성, 흡수, 유리, 분포, 대사 및 배출이 있을 수 있으나 이들로 한정되지 않는다. 유리는 치료 펩티드를 약학 제제로부터 방출시키는 과정을 지칭할 수 있다. 흡수는 물질이 혈액 순환계로 들어가는 과정을 지칭할 수 있다. 분포는 신체의 체액 및 조직 전체에 걸친 물질의 분산 또는 살포를 지칭할 수 있다. 대사(또는 생체내변환 또는 불활성화)는 외래 물질이 존재한다는 것이 유기체에 의해 인식되는 것 및 모 화합물이 자손 대사물질로 비가역적으로 변환되는 것을 지칭할 수 있다. 배출은 신체로부터의 물질의 제거를 지칭할 수 있다.
치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 더 클 수 있다. 치료 펩티드의 반감기는 대상체에게 투여될 때 4시간 초과, 6시간 초과, 12시간 초과, 24시간 초과, 36시간 초과, 2일 초과, 3일 초과, 4일 초과, 5일 초과, 6일 초과, 7일 초과, 8일 초과, 9일 초과, 10일 초과, 11일 초과, 12일 초과, 13일 초과 또는 14일 초과의 시간일 수 있다. 치료 펩티드의 반감기는 대상체에게 투여될 때 4시간 초과의 시간일 수 있다. 치료 펩티드의 반감기는 대상체에게 투여될 때 6시간 초과의 시간일 수 있다.
치료 펩티드의 반감기는 적어도 약 2시간, 4시간, 6시간, 8시간, 10시간, 12시간, 14시간, 16시간, 18시간 또는 20시간 이상까지 증가할 수 있다. 치료 펩티드의 반감기는 적어도 약 2시간까지 증가할 수 있다. 치료 펩티드의 반감기는 적어도 약 4시간까지 증가할 수 있다. 치료 펩티드의 반감기는 적어도 약 6시간까지 증가할 수 있다. 치료 펩티드의 반감기는 적어도 약 8시간까지 증가할 수 있다.
치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 1.5배, 2배, 2.5배, 3배, 3.5배, 4배, 4.5배, 5배, 5.5배, 6배, 6.5배, 7배, 7.5배, 8배, 8.5배, 9배, 9.5배 또는 10배 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 15배, 16배, 17배, 18배, 19배, 20배, 25배, 30배, 35배, 40배, 45배 또는 50배 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 2배 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 5배 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 10배 더 클 수 있다.
본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 5%, 10%, 15%, 20%, 25%, 30%, 35%, 40%, 45%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95% 또는 97% 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 10% 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 20% 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 30% 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 40% 더 클 수 있다. 본원에 기재된 면역글로불린의 치료 펩티드의 반감기는 접합되지 않은 치료 펩티드의 반감기보다 적어도 약 50% 더 클 수 있다.
실시예
하기 실시예에서 제공된 활성 데이터는 일반적으로 실시예에서 정의되어 있고 제공된 서열번호로 예시되어 있는 면역글로불린 융합 단백질의 사용을 통해 수득된다. 본원에 개시된 임의의 면역글로불린 융합 단백질의 활성은 면역글로불린 융합 단백질 서열과 관련되지 않은 조건, 예를 들면, 발현 및 정제 조건에 따라 향상될 수 있거나 약화될 수 있다.
실시예 1: 포유동물 세포에서의 발현을 위한 트라스투주맙-엑센딘-4 융합 단백질의 구축
엑센딘-4(EX4) 유전자는 IDT(미국 아이오와주 소재)에 의해 합성되었고 중합효소 연쇄 반응(PCR)에 의해 증폭되었다. 오버랩 PCR로 아미노산 서열 GGGGS(서열번호 115)를 코딩하는 링커를 사용하여 엑센딘-4 유전자(서열번호 75)를, 트라스투주맙 경쇄를 코딩하는 핵산(서열번호 1)에 유전적으로 융합시켰다. 증폭된 트라스투주맙-EX4 융합체(서열번호 9)를 pFuse 골격 벡터(인비보겐(InvivoGen), 캘리포니아주 소재)에 인-프레임(in-frame) 라이게이션시킴으로써, 트라스투주맙-EX4 경쇄를 코딩하는 p트라스투주맙(NL)-EX4 포유동물 발현 벡터를 생성하였다. 트라스투주맙 중쇄를 코딩하는 유전자(서열번호 2)를 증폭하고 pFuse 벡터 내로 클로닝하여 p트라스투주맙(H) 포유동물 발현 벡터를 생성하였다. 생성된 포유동물 발현 벡터를 DNA 서열분석으로 검증하였다.
실시예
2: 트라스투주맙-
엑센딘
-4 융합 단백질의 발현 및 정제
트라스투주맙(NL)-EX4 및 트라스투주맙(H)을 코딩하는 벡터들을 사용한 프리스타일 HEK293 세포의 공동-형질감염을 통해 트라스투주맙-EX4 융합 단백질을 발현시켰다. 5% CO2 하에 37℃에서 프리스타일 293 발현 배지(라이프 테크놀로지스(Life Technologies))를 사용하여 세포를 125 rpm의 진탕기 플라스크에서 증식시켰다. 발현된 단백질은 배양 배지 내로 분비되었고, 이 발현된 단백질을 형질감염 후 48시간마다 2회 수거하였다. 융합 단백질을 단백질 A/G 크로마토그래피(써모 피셔 사이언티픽(Thermo Fisher Scientific), 일리노이주 소재)로 정제하였고 SDS-PAGE 겔로 분석하였다.
실시예 3: GLP-1 수용체를 활성화시키는 트라스투주맙 융합 단백질의 활성
GLP-1 수용체 활성화에 대한 트라스투주맙 융합 단백질의 활성을 루시퍼라제 분석으로 조사하였다. 표면 GLP-1 수용체(GLP-1R) 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 웰당 5,000개 세포의 밀도로 384웰 플레이트에 시딩하고 5% CO2 하에 37℃에서 24시간 동안 다양한 농도의 EX4 펩티드, 렙틴, 트라스투주맙, 트라스투주맙(H)(서열번호 6)을 갖는 트라스투주맙(NL, GGGGS)-ZP1(서열번호 45), 트라스투주맙(H)(서열번호 6)을 갖는 트라스투주맙(NL, GGGGS)-ZPCEX(서열번호 46), 트라스투주맙(NL, GGGGS)-ZPCEX(서열번호 46)를 갖는 트라스투주맙(CDR3H) 렙틴(서열번호 44), 트라스투주맙(H)(서열번호 6)을 갖는 트라스투주맙(NL, GGGGS)-옥신토모듈린(서열번호 68), 및 트라스투주맙-EX4 융합체로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(One-Glo)(프로메가(Promega)) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 곡선은 도면들에 제시되어 있다: 도 1: EX4 EC50 = 61 pM, 트라스투주맙-EX4 EC50 = 551.3 pM; 도 2: EX4 EC50 = 41.41 ± 2.1 pM, 트라스투주맙(H)(서열번호 6)을 갖는 트라스투주맙(NL, GGGGS)-ZP1(서열번호 45); 도 4: EX4 EC50 = 41.41 ± 2.1 pM, 트라스투주맙(H)(서열번호 6)을 갖는 트라스투주맙(NL, GGGGS)-ZPCEX(서열번호 46) EC50 = 38.6 ± 2.19 pM; 도 6: 렙틴 EC50 = 55.02 ± 13.62 pM, 트라스투주맙(CDR3H) 렙틴(서열번호 44) EC50 = 44.84 ± 8.89 pM, 트라스투주맙(NL, GGGGS)-ZPCEX(서열번호 46)를 갖는 트라스투주맙(CDR3H) 렙틴(서열번호 44) EC50 = 117 ± 28.51 pM; 도 7: EX4 EC50 = 43.25 ± 2.92 pM, 트라스투주맙(NL, GGGGS)-ZPCEX(서열번호 46)를 갖는 트라스투주맙(CDR3H) 렙틴(서열번호 44) EC50 = 114.6 ± 5.36 pM; 및 도 14: 트라스투주맙(H)(서열번호 6)을 갖는 트라스투주맙(NL, GGGGS)-옥신토모듈린(서열번호 68).
실시예 4: 글루카곤 수용체를 활성화시키는 트라스투주맙 기반 융합 단백질 팔리비주맙 기반 융합 단백질의 활성
트라스투주맙 포함 융합 단백질 및 팔리비주맙 포함 융합 단백질의 활성을 루시퍼라제 분석으로 조사하였다. 표면 글루카곤 수용체(GCGR) 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 웰당 5,000개 세포의 밀도로 384웰 플레이트에 시딩하고 5% CO2 하에 37℃에서 24시간 동안 다양한 농도의 글루카곤, 트라스투주맙(NL)-ZP1, ZP2-DA(HsQGTFTSDY SKYLDECAAK EFICWLLRA, 이때 s는 D-세린임), 트라스투주맙(NL, GGGGS)-ZP1CEX(서열번호 46) 및 트라스투주맙(CDR3H)-렙틴, 팔리비주맙(NL, GGGGS)-ZP1CEX(서열번호 48), 팔리비주맙(NH, GGGGS)-ZP1CEX(서열번호 50), 팔리비주맙(NL, GGGGS)-ZPCEX(서열번호 48), 팔리비주맙(NH, GGGGS)-ZPCEX(서열번호 50) 및 트라스투주맙(NL)-옥신토모듈린(서열번호 68) 단백질로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(프로메가) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 곡선은 도 3(트라스투주맙(NL) - ZP1: EC50 = 2.283 ± 0.294 nM), 도 5(트라스투주맙(NL) - ZP1CEX: EC50 = 92.16 ± 14.35 pM), 도 8(트라스투주맙(NL) - ZP1CEX 및 트라스투주맙(CDR) - 렙틴: EC50 = 410.3 ± 106.77 pM; ZP2-DA: EC50 = 36.81 ± 7.45 pM), 도 10(팔리비주맙(NL) - ZP1CEX: EC50 = 63.5 ± 7.84 pM; ZP2-DA: EC50 = 33.73 ± 6.92 pM), 도 12(팔리비주맙(NH) - ZP1CEX: EC50 = 14.89 ± 5.24 pM; ZP2-DA: EC50 = 33.73 ± 6.92 pM), 도 9(EX4: EC50 = 40.5 ± 3.24 pM; 팔리비주맙(NL, GGGGS)-ZPCEX: EC50 = 58.77 ± 8.14 pM), 도 11(EX4: EC50 = 40.5 ± 3.24 pM; 팔리비주맙(NH, GGGGS)-ZPCEX(서열번호 50): EC50 = 27.42 ± 1.75 pM), 및 도 15(트라스투주맙(NL)-옥신토모듈린)에 제시되어 있다.
실시예 5: 릴랙신 수용체를 활성화시키는 팔리비주맙-릴랙신 융합 단백질의 활성
팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)(서열번호 201)의 활성을 루시퍼라제 분석으로 조사하였다. 릴랙신 수용체(LGR7 또는 LGR8), 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 과다발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 24시간 동안 384웰 플레이트에 시딩한 후, 추가 24시간 동안 다양한 농도의 릴랙신-2 및 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일) 융합 단백질(서열번호 201)로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(프로메가) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 곡선은 도 13A 및 13B에 제시되어 있다. LGR7 발현 세포의 경우, 릴랙신-2에 대한 EC50은 0.012 nM이었고 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)에 대한 EC50은 2.5 nM이었다. LGR8 발현 세포의 경우, 릴랙신-2에 대한 EC50은 11.2 nM이었고 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)에 대한 EC50은 552.7 nM이었다. 이들 데이터는 아미노 말단 릴랙신 융합 단백질들이 릴랙신 수용체에 대한 그들의 선택성에 있어서 야생형 릴랙신에 필적한다는 것을 보여준다.
실시예 6: 포유동물 세포에서의 발현을 위한 팔리비주맙-릴랙신 융합 단백질 벡터의 구축
릴랙신 핵산 서열은 IDT(미국 아이오와주 소재)에 의해 합성되었고 중합효소 연쇄 반응(PCR)에 의해 증폭되었다.
오버랩 PCR로 연결 펩티드 GGGGG(서열번호 116)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2(GGGPRR)(서열번호 227)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, GGGGG)-릴랙신2(GGGPRR)(서열번호 180)를 생성하였다. 증폭된 팔리비주맙(NH, GGGGG)-릴랙신2(GGGPRR)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, GGGGG)-릴랙신2(GGGPRR)를 코딩하는 p팔리비주맙(NH, GGGGG)-릴랙신2(GGGPRR) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 CEXGGGGG(서열번호 118)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2(GGGPRR)(서열번호 227)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, CEXGGGGG)-릴랙신2(GGGPRR)(서열번호 181)를 생성하였다. 증폭된 팔리비주맙(NH, CEXGGGGG)-릴랙신2(GGGPRR)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, CEXGGGGG)-릴랙신2(GGGPRR)를 코딩하는 p팔리비주맙(NH, CEXGGGGG)-릴랙신2(GGGPRR) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 EAAAK(서열번호 237)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2(GGGPRR)(서열번호 227)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, EAAAK)-릴랙신2(GGGPRR)(서열번호 182)를 생성하였다. 증폭된 팔리비주맙(NH, EAAAK)-릴랙신2(GGGPRR)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, EAAAK)-릴랙신2(GGGPRR)를 코딩하는 p팔리비주맙(NH, EAAAK)-릴랙신2(GGGPRR) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 CEXGGGGS(서열번호 238)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2(단일)(서열번호 82)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)(서열번호 170)를 생성하였다. 증폭된 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)를 코딩하는 p팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 CEXGGGGG(서열번호 118)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2(30GS)(서열번호 223)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, CEXGGGGG)-릴랙신2(30GS)(서열번호 173)를 생성하였다. 증폭된 팔리비주맙(NH, CEXGGGGG)-릴랙신2(30GS)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, CEXGGGGG)-릴랙신2(30GS)를 코딩하는 p팔리비주맙(NH, CEXGGGGG)-릴랙신2(30GS) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 CEXGGGGS(서열번호 238)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2((단일)(서열번호 82)를, 팔리비주맙 중쇄 fab를 코딩하는 핵산(서열번호 4의 부분)에 유전적으로 융합시켜, 팔리비주맙 fab(NH, CEXGGGGS)-릴랙신2(단일)(서열번호 172)를 생성하였다. 증폭된 팔리비주맙 fab(NH, CEXGGGGS)-릴랙신2(단일)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙 fab(NH, CEXGGGGS)-릴랙신2(단일)를 코딩하는 p팔리비주맙 fab(NH, CEXGGGGS)-릴랙신2(단일) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 GGGGS3(서열번호 115)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2c(9GS)(서열번호 226)를, 팔리비주맙 중쇄 fab를 코딩하는 핵산(서열번호 4의 부분)에 유전적으로 융합시켜, 팔리비주맙 fab(NH, GGGGS3)-릴랙신2c(9GS)(서열번호 178)를 생성하였다. 증폭된 팔리비주맙 fab(NH, GGGGS3)-릴랙신2(9GS)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙 fab(NH, GGGGS3)-릴랙신2(9GS)를 코딩하는 p팔리비주맙 fab(NH, GGGGS3)-릴랙신2(9GS) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 GGGGS3(서열번호 115)을 코딩하는 연결 핵산 서열을 사용하여 릴랙신2c(9GS)(서열번호 226)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, GGGGS3)-릴랙신2c(9GS)(서열번호 176)를 생성하였다. 증폭된 팔리비주맙(NH, GGGGS3)-릴랙신2(9GS)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, GGGGS3)-릴랙신2(9GS)를 코딩하는 p팔리비주맙(NH, GGGGS3)-릴랙신2(9GS) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 CEXGGGGG(서열번호 118)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2c(9GS)(서열번호 226)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, CEXGGGGG)-릴랙신2c(9GS)(서열번호 175)를 생성하였다. 증폭된 팔리비주맙(NH, CEXGGGGG)-릴랙신2(9GS)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, CEXGGGGG)-릴랙신2(9GS)를 코딩하는 p팔리비주맙(NH, CEXGGGGG)-릴랙신2(9GS) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 GGGGS3(서열번호 115)을 코딩하는 연결 핵산 서열을 사용하여 릴랙신2(18GS)(서열번호 228)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, GGGGS3)-릴랙신2(18GS)(서열번호 179)를 생성하였다. 증폭된 팔리비주맙(NH, GGGGS3)-릴랙신(18GS)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, GGGGS3)-릴랙신(18GS)을 코딩하는 p팔리비주맙(NH, GGGGS3)-릴랙신(18GS) 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 EAAAK(서열번호 237)를 코딩하는 연결 핵산 서열을 사용하여 릴랙신2(단일)(서열번호 82)를, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, EAAAK)-릴랙신2(단일)(서열번호 266)를 생성하였다. 증폭된 팔리비주맙(NH, EAAAK)-릴랙신2(단일)를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, EAAAK)-릴랙신2(단일)를 코딩하는 p팔리비주맙(NH, EAAAK)-릴랙신2(단일) 포유동물 발현 벡터를 생성하였다.
팔리비주맙 경쇄를 코딩하는 유전자(서열번호 3)를 증폭하고 pFuse 벡터 내로 클로닝하여 p팔리비주맙(L) 포유동물 발현 벡터를 생성하였다. 생성된 포유동물 발현 벡터를 DNA 서열분석으로 검증하였다.
실시예 7: 팔리비주맙-릴랙신 융합 단백질의 발현 및 정제
실시예 7에 기재된 팔리비주맙-릴랙신 중쇄 포유동물 발현 벡터 및 팔리비주맙 경쇄 포유동물 발현 벡터를 사용한 프리스타일 HEK293 세포의 공동-형질감염을 통해 팔리비주맙-릴랙신 중쇄 융합 단백질들을 각각 발현시켰다. 5% CO2 하에 37℃에서 프리스타일 293 발현 배지(라이프 테크놀로지스)를 사용하여 세포를 125 rpm의 진탕기 플라스크에서 증식시켰다. 발현된 단백질은 배양 배지 내로 분비되었고, 이 발현된 단백질을 형질감염 후 48시간마다 2회 수거하였다. 융합 단백질을 단백질 A/G 크로마토그래피(써모 피셔 사이언티픽, 일리노이주 소재)로 정제하였고 SDS-PAGE 겔로 분석하였다. 팔리비주맙 경쇄와 함께 발현된 정제된 중쇄 융합 단백질은 도 16의 SDS-PAGE 겔에서 표시되어 있다. 각각의 겔의 경우, 제1 레인은 분자 마커에 상응하고, 제2 레인은 정제된 단백질에 상응하고, 제3 레인은 환원제 DTT로 처리된 정제된 단백질에 상응한다. 중쇄는 별모양으로 표시되어 있다. 경쇄는 삼각형으로 표시되어 있다. 도 16A는 정제된 팔리비주맙(NH, GGGGG)-릴랙신2(GGGPRR)(서열번호 211)를 보여준다. 도 16B는 정제된 팔리비주맙(NH, CEXGGGGG)-릴랙신2(GGGPRR)(서열번호 212)를 보여준다. 도 16C는 정제된 팔리비주맙(NH, EAAAK)-릴랙신2(GGGPRR)(서열번호 213)를 보여준다. 도 16D는 정제된 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)(서열번호 201)를 보여준다. 도 16E는 정제된 팔리비주맙(NH, CEXGGGGG)-릴랙신2(30GS)(서열번호 204)를 보여준다. 도 16F는 정제된 팔리비주맙 fab(NH, CEXGGGGS)-릴랙신2(단일)(서열번호 203)를 보여준다. 도 16G는 정제된 팔리비주맙 fab(NH, GGGGS3)-릴랙신2(9GS)(서열번호 209)를 보여준다. 도 16H는 정제된 팔리비주맙(NH, GGGGS3)-릴랙신2(9GS)(서열번호 207)를 보여준다. 도 16I는 정제된 팔리비주맙(NH, CEXGGGGG)-릴랙신2(9GS)(서열번호 206)를 보여준다. 도 16J는 정제된 팔리비주맙(NH, GGGGS3)-릴랙신(18GS)(서열번호 210)를 보여준다. 도 16K는 정제된 팔리비주맙(NH, EAAAK)-릴랙신2(단일)(서열번호 265)를 보여준다.
실시예 8: 릴랙신 수용체를 활성화시키는 팔리비주맙-릴랙신 융합 단백질의 활성
실시예 8에서 정제된 팔리비주맙-릴랙신 융합 단백질들의 활성을 루시퍼라제 분석으로 조사하였다. 릴랙신 수용체(LGR7) 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 과다발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 24시간 동안 384웰 플레이트에 시딩한 후, 추가 24시간 동안 다양한 농도의, 실시예 7로부터 정제된 팔리비주맙-릴랙신 융합 단백질들 또는 릴랙신2 펩티드로 독립적으로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(프로메가) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 릴랙신-2에 대한 EC50은 12.1 pM이었다.
팔리비주맙(NH, CEXGGGGG)-릴랙신2(GGGPRR)(서열번호 212) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 2,000 pM이었다. 팔리비주맙(NH, EAAAK)-릴랙신2(GGGPRR)(서열번호 213) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 3,400 pM이었다. 팔리비주맙(NH, CEXGGGGS)-릴랙신2(단일)(서열번호 201) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 2,500 pM이었다. 팔리비주맙(NH, CEXGGGGG)-릴랙신2(30GS)(서열번호 204) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 208 pM이었다. 팔리비주맙 fab(NH, CEXGGGGS)-릴랙신2(단일)(서열번호 203) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 47,300 pM이었다. 팔리비주맙 fab(NH, GGGGS3)-릴랙신2(9GS)(서열번호 209) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 5,800 pM이었다. 팔리비주맙(NH, GGGGS3)-릴랙신2(9GS)(서열번호 207) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 240 pM이었다. 팔리비주맙(NH, CEXGGGGG)-릴랙신2(9GS)(서열번호 206) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 480 pM이었다. 팔리비주맙(NH, GGGGS3)-릴랙신(18GS)(서열번호 210) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 1,300 pM이었다. 팔리비주맙(NH, EAAAK)-릴랙신2(단일)(서열번호 266) 및 팔리비주맙 경쇄(서열번호 7)에 대한 EC50은 4,290 pM이었다.
실시예 9: 포유동물 세포에서의 발현을 위한 팔리비주맙-글루카곤 융합 단백질 벡터의 구축
글루카곤 핵산 서열은 IDT(미국 아이오와주 소재)에 의해 합성되었고 중합효소 연쇄 반응(PCR)에 의해 증폭되었다.
오버랩 PCR로 연결 펩티드 EAAAK(서열번호 237)를 코딩하는 연결 핵산 서열을 사용하여 글루카곤 핵산 서열(서열번호 92)을, 팔리비주맙 경쇄를 코딩하는 핵산(서열번호 3)에 유전적으로 융합시켜, 팔리비주맙(NL, EAAAK)-글루카곤(서열번호 162)을 생성하였다. 증폭된 팔리비주맙(NL, EAAAK)-글루카곤을 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NL, EAAAK)-글루카곤을 코딩하는 p팔리비주맙(NL, EAAAK)-글루카곤 포유동물 발현 벡터를 생성하였다.
생성된 포유동물 발현 벡터를 DNA 서열분석으로 검증하였다.
실시예 10: 포유동물 세포에서의 발현을 위한 팔리비주맙-엑센딘-4 융합 단백질 벡터의 구축
엑센딘-4 핵산 서열은 IDT(미국 아이오와주 소재)에 의해 합성되었고 중합효소 연쇄 반응(PCR)에 의해 증폭되었다.
오버랩 PCR로 연결 펩티드 GGGGS1(서열번호 115)를 코딩하는 연결 핵산 서열을 사용하여 엑센딘-4 핵산 서열(서열번호 75)을, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, GGGGS1)-엑센딘-4(서열번호 161)를 생성하였다. 증폭된 팔리비주맙(NH, GGGGS1)-엑센딘-4를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, GGGGS1)-엑센딘-4를 코딩하는 p팔리비주맙(NH, GGGGS1)-엑센딘-4 포유동물 발현 벡터를 생성하였다.
생성된 포유동물 발현 벡터를 DNA 서열분석으로 검증하였다.
실시예 11: 팔리비주맙-글루카곤 융합 단백질 및 팔리비주맙-엑센딘-4 융합 단백질의 발현 및 정제
실시예 10 및 11에 기재된 p팔리비주맙(NL, EAAAK)-글루카곤 포유동물 발현 벡터 및 p팔리비주맙(NH, GGGGS1)-엑센딘-4 포유동물 발현 벡터를 사용한 프리스타일 HEK293 세포의 공동-형질감염을 통해 팔리비주맙-글루카곤 경쇄 융합 단백질 및 팔리비주맙-엑센딘-4 중쇄 융합 단백질을 공발현시켰다. 5% CO2 하에 37℃에서 프리스타일 293 발현 배지(라이프 테크놀로지스)를 사용하여 세포를 125 rpm의 진탕기 플라스크에서 증식시켰다. 발현된 단백질은 배양 배지 내로 분비되었고, 이 발현된 단백질을 형질감염 후 48시간마다 2회 수거하였다. 융합 단백질을 단백질 A/G 크로마토그래피(써모 피셔 사이언티픽, 일리노이주 소재)로 정제하였고 SDS-PAGE 겔로 분석하였다. 정제된 융합 단백질은 도 17의 SDS-PAGE 겔에서 표시되어 있다. 각각의 겔의 경우, 제1 레인은 분자 마커에 상응하고, 제2 레인은 정제된 단백질에 상응하고, 제3 레인은 환원제 DTT로 처리된 정제된 단백질에 상응한다. 중쇄는 별모양으로 표시되어 있다. 경쇄는 삼각형으로 표시되어 있다. 도 17A는 정제된 팔리비주맙(NL, EAAAK)-글루카곤(2S) 및 p팔리비주맙(NH, GGGGS1)-엑센딘-4를 보여준다. 도 17B는 정제된 팔리비주맙(NL, EAAAK)-글루카곤(2G) 및 p팔리비주맙(NH, GGGGS1)-엑센딘-4를 보여준다.
실시예 12: 글루카곤 수용체를 활성화시키는 팔리비주맙 융합 단백질의 활성
팔리비주맙 융합 단백질의 활성을 루시퍼라제 분석으로 조사하였다. 표면 글루카곤 수용체 또는 GLP-1 수용체(GCGR 또는 GLP-1R) 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 웰당 5,000개 세포의 밀도로 384웰 플레이트에 시딩하고, 5% CO2 하에 37℃에서 24시간 동안 다양한 농도의 엑센딘-4, 글루카곤, 및 팔리비주맙-글루카곤 경쇄 및 팔리비주맙-엑센딘-4 중쇄 융합 단백질(실시예 11로부터 수득됨)로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(프로메가) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 그래프패드 프리즘(GraphPad Prism) 6 소프트웨어를 이용하여 데이터를 분석하였다. GLP-1R을 발현하는 세포의 경우, 엑센딘-4에 대한 EC50은 57 pM이었다. GLP-1R을 발현하는 세포의 경우, 팔리비주맙(NL, EAAAK)-글루카곤(2S) 및 p팔리비주맙(NH, GGGGS1)-엑센딘-4에 대한 EC50은 13 pM이었다. GLP-1R을 발현하는 세포의 경우, 팔리비주맙(NL, EAAAK)-글루카곤(2G) 및 p팔리비주맙(NH, GGGGS1)-엑센딘-4에 대한 EC50은 9 pM이었다. GCGR을 발현하는 세포의 경우, 글루카곤에 대한 EC50은 95 pM이었다. GCGR을 발현하는 세포의 경우, 팔리비주맙(NL, EAAAK)-글루카곤(2G) 및 p팔리비주맙(NH, GGGGS1)-엑센딘-4에 대한 EC50은 26 pM이었다. GCGR을 발현하는 세포의 경우, 팔리비주맙(NL, EAAAK)-글루카곤(2S) 및 p팔리비주맙(NH, GGGGS1)-엑센딘-4에 대한 EC50은 33 pM이었다.
실시예 13: 포유동물 세포에서의 발현을 위한 팔리비주맙-ZP1 융합 단백질 벡터의 구축
ZP1 핵산 서열은 IDT(미국 아이오와주 소재)에 의해 합성되었고 중합효소 연쇄 반응(PCR)에 의해 증폭되었다.
오버랩 PCR로 연결 펩티드 EAAAK(서열번호 237)를 코딩하는 연결 핵산 서열을 사용하여 ZP1 핵산 서열(서열번호 77)을, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, EAAAK)-ZP1(서열번호 165)을 생성하였다. 증폭된 팔리비주맙(NH, EAAAK)-ZP1을 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, EAAAK)-ZP1을 코딩하는 p팔리비주맙(NH, EAAAK)-ZP1 포유동물 발현 벡터를 생성하였다.
팔리비주맙 경쇄를 코딩하는 유전자(서열번호 3)를 증폭하고 pFuse 벡터 내로 클로닝하여 p팔리비주맙(L) 포유동물 발현 벡터를 생성하였다. 생성된 포유동물 발현 벡터를 DNA 서열분석으로 검증하였다.
실시예 14: 팔리비주맙-ZP1 융합 단백질의 발현 및 정제
팔리비주맙-ZP1 중쇄 포유동물 발현 벡터(실시예 14) 및 팔리비주맙 경쇄 포유동물 발현 벡터를 사용한 프리스타일 HEK293 세포의 공동-형질감염을 통해 팔리비주맙-ZP1 중쇄 융합 단백질을 발현시켰다. 5% CO2 하에 37℃에서 프리스타일 293 발현 배지(라이프 테크놀로지스)를 사용하여 세포를 125 rpm의 진탕기 플라스크에서 증식시켰다. 발현된 단백질은 배양 배지 내로 분비되었고, 이 발현된 단백질을 형질감염 후 48시간마다 2회 수거하였다. 융합 단백질을 단백질 A/G 크로마토그래피(써모 피셔 사이언티픽, 일리노이주 소재)로 정제하였고 SDS-PAGE 겔로 분석하였다. 팔리비주맙 경쇄와 함께 발현된 정제된 중쇄 융합 단백질은 도 18의 SDS-PAGE 겔에서 표시되어 있다. 제1 레인은 분자 마커에 상응하고, 제2 레인은 정제된 단백질에 상응하고, 제3 레인은 환원제 DTT로 처리된 정제된 단백질에 상응한다. 중쇄는 별모양으로 표시되어 있다. 경쇄는 삼각형으로 표시되어 있다. 도 18은 정제된 팔리비주맙(NH, EAAAK)-ZP1(서열번호 196) 및 팔리비주맙(L)(서열번호 7)을 보여준다.
실시예 15: 글루카곤 수용체를 활성화시키는 팔리비주맙-ZP1 융합 단백질의 활성
팔리비주맙-ZP1 중쇄 융합체 및 팔리비주맙 경쇄의 활성을 루시퍼라제 분석으로 조사하였다. 표면 글루카곤 수용체 또는 GLP-1 수용체(GCGR 또는 GLP-1R) 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 웰당 5,000개 세포의 밀도로 384웰 플레이트에 시딩하고, 5% CO2 하에 37℃에서 24시간 동안 다양한 농도의 엑센딘-4, 글루카곤, 및 팔리비주맙-ZP1 중쇄 및 팔리비주맙 경쇄(실시예 15)로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(프로메가) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 그래프패드 프리즘 6 소프트웨어를 이용하여 데이터를 분석하였다. GLP-1R을 발현하는 세포의 경우, 엑센딘-4에 대한 EC50은 17 pM이었다. GLP-1R을 발현하는 세포의 경우, 팔리비주맙(NH, EAAAK)-ZP1(서열번호 196) 및 팔리비주맙(L)(서열번호 7)에 대한 EC50은 3 pM이었다. GCGR을 발현하는 세포의 경우, 글루카곤에 대한 EC50은 95 pM이었다. GCGR을 발현하는 세포의 경우, 팔리비주맙(NH, EAAAK)-ZP1(서열번호 196) 및 팔리비주맙(L)(서열번호 7)에 대한 EC50은 14 pM이었다.
실시예 16: 포유동물 세포에서의 발현을 위한 팔리비주맙-GLP2 융합 단백질 벡터의 구축
GLP2 핵산 서열은 IDT(미국 아이오와주 소재)에 의해 합성되었고 중합효소 연쇄 반응(PCR)에 의해 증폭되었다.
오버랩 PCR로 연결 펩티드 EAAAK(서열번호 237)를 코딩하는 연결 핵산 서열을 사용하여 GLP2 핵산 서열(서열번호 87)을, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, EAAAK)-GLP2(서열번호 189)를 생성하였다. 증폭된 팔리비주맙(NH, EAAAK)-GLP2를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, EAAAK)-GLP2를 코딩하는 p팔리비주맙(NH, EAAAK)-GLP2 포유동물 발현 벡터를 생성하였다.
오버랩 PCR로 연결 펩티드 CEXGGGGS(서열번호 238)를 코딩하는 연결 핵산 서열을 사용하여 GLP2 핵산 서열(서열번호 87)을, 팔리비주맙 중쇄를 코딩하는 핵산(서열번호 4)에 유전적으로 융합시켜, 팔리비주맙(NH, CEXGGGGS)-GLP2(서열번호 187)를 생성하였다. 증폭된 팔리비주맙(NH, CEXGGGGS)-GLP2를 pFuse 골격 벡터(인비보겐, 캘리포니아주 소재)에 인-프레임 라이게이션시킴으로써, 팔리비주맙(NH, CEXGGGGS)-GLP2를 코딩하는 p팔리비주맙(NH, CEXGGGGS)-GLP2 포유동물 발현 벡터를 생성하였다.
팔리비주맙 경쇄를 코딩하는 유전자(서열번호 3)를 증폭하고 pFuse 벡터 내로 클로닝하여 p팔리비주맙(L) 포유동물 발현 벡터를 생성하였다. 생성된 포유동물 발현 벡터를 DNA 서열분석으로 검증하였다.
실시예 17: 팔리비주맙-GLP2 융합 단백질의 발현 및 정제
팔리비주맙-GLP2 중쇄 포유동물 발현 벡터(실시예 17) 및 팔리비주맙 경쇄 포유동물 발현 벡터를 사용한 프리스타일 HEK293 세포의 공동-형질감염을 통해 팔리비주맙-GLP2 중쇄 융합 단백질을 발현시켰다. 5% CO2 하에 37℃에서 프리스타일 293 발현 배지(라이프 테크놀로지스)를 사용하여 세포를 125 rpm의 진탕기 플라스크에서 증식시켰다. 발현된 단백질은 배양 배지 내로 분비되었고, 이 발현된 단백질을 형질감염 후 48시간마다 2회 수거하였다. 융합 단백질을 단백질 A/G 크로마토그래피(써모 피셔 사이언티픽, 일리노이주 소재)로 정제하였고 SDS-PAGE 겔로 분석하였다. 팔리비주맙 경쇄와 함께 발현된 정제된 중쇄 융합 단백질은 도 19의 SDS-PAGE 겔에서 표시되어 있다. 각각의 겔의 경우, 제1 레인은 분자 마커에 상응하고, 제2 레인은 정제된 단백질에 상응하고, 제3 레인은 환원제 DTT로 처리된 정제된 단백질에 상응한다. 중쇄는 별모양으로 표시되어 있다. 경쇄는 삼각형으로 표시되어 있다. 도 19A는 정제된 팔리비주맙(NH, EAAAK)-GLP2(서열번호 220) 및 팔리비주맙(L)(서열번호 7)을 보여준다. 도 19B는 정제된 팔리비주맙(NH, CEXGGGGS)-GLP2(서열번호 218) 및 팔리비주맙(L)(서열번호 7)을 보여준다.
실시예 18: 글루카곤 수용체를 활성화시키는 팔리비주맙-GLP2 융합 단백질의 활성
팔리비주맙-GLP2 중쇄 융합체 및 팔리비주맙 경쇄의 활성을 루시퍼라제 분석으로 조사하였다. 표면 GLP-2 수용체(GLP-2R) 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 웰당 5,000개 세포의 밀도로 384웰 플레이트에 시딩하고, 5% CO2 하에 37℃에서 24시간 동안 다양한 농도의 GLP2, 및 팔리비주맙-GLP2 중쇄 및 팔리비주맙 경쇄(실시예 18)로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(프로메가) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 그래프패드 프리즘 6 소프트웨어를 이용하여 데이터를 분석하였다. GLP2에 대한 EC50은 46 pM이었다. 팔리비주맙(NH, EAAAK)-GLP2(서열번호 220) 및 팔리비주맙(L)(서열번호 7)에 대한 EC50은 69 pM이었다. 팔리비주맙(NH, CEXGGGGS)-GLP2(서열번호 218) 및 팔리비주맙(L)(서열번호 7)에 대한 EC50은 133 pM이었다.
실시예 19: 팔리비주맙-릴랙신 융합 단백질의 약동학 연구
팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일)(서열번호 201)를 투여 모드 둘 다에 대해 2.4 nmol/kg의 용량으로 2개의 분리된 실험군들 내의 SD 암컷 래트 내로 정맥내(i.v.) 또는 피하(s.c.) 주사하였다. 350시간의 경과에 걸쳐 혈장 샘플을 채취하였다. 샌드위치 ELISA 분석을 이용하여 팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일) 수준을 정량하였다. 요약하건대, 96웰 플레이트를 4℃에서 항-hFc(애브캄(abcam) 98616, 1:100 희석, PBS)와 함께 하룻밤 동안 항온처리하였다. 이 코팅 용액을 따라내고 플레이트를 1시간 동안 실온에서 차단 완충제(0.5% 트윈-20/PBS 중의 2% 밀크)로 차단하였다. 차단 용액을 따라내고 플레이트를 2시간 동안 실온에서 (차단 완충제 중의) 혈청 희석물과 함께 항온처리하였는데, 이때 혈청은 10배 내지 106배 희석되었다. 혈청을 따라내고 플레이트를 0.5% 트윈-20/PBS로 광범위하게 세척한 후, 1시간 동안 실온에서 항-릴랙신(밀리포어(Millipore), 553850, 1:1000 희석, 차단 완충제)과 함께 항온처리하였다. 용액을 따라내고 플레이트를 0.5% 트윈-20/PBS로 광범위하게 세척한 후, 30분 동안 실온에서 항-토끼-HRP(라이프 테크놀로지스, A16023, 1:3000 희석, 차단 완충제)와 함께 항온처리하였다. 용액을 따라내고 플레이트를 0.5% 트윈-20/PBS로 광범위하게 세척하고 퀀타블루(QuantaBlu) 형광발생성 퍼록시다제 기질(라이프 테크놀로지스, 15169)로 현상하고 스펙트라맥스(Spectramax) 형광 플레이트 판독기를 이용하여 정량하였다. 신호를 표준 곡선의 직선 범위 내로 외삽함으로써(신호 대 농도) 혈장 샘플 중의 팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일) 융합 단백질의 양을 정량하였다. 윈놀린(WinNonlin)(파사이트(Pharsight))을 이용하여 약동학 파라미터를 모델링하였다. 각각의 채취 시점에서의 융합 단백질의 농도가 작도되었고 도 20에 표시되어 있다. 팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일) 융합 단백질은 0.5시간 미만의 반감기를 갖는 야생형 릴랙신에 비해 연장된 반감기를 가졌다. 팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일) 융합 단백질의 반감기는 s.c. 투여의 경우 79시간이었고 i.v. 투여의 경우 115시간이었다. s.c. 경로에 대한 Cmax는 27.75 nM이었고 i.v. 투여 경로에 대한 Cmax는 38.06 nM이었다. s.c. 경로에 대한 AUC∞는 5231.51(hr*nM)이었고 i.v. 투여 경로에 대한 AUC∞는 6298.81(hr*nM)이었다.
실시예 20: 마우스 치골간 인대 모델에서의 팔리비주맙-릴랙신 융합 단백질의 용량-반응 효능
체중이 18 g 내지 20 g인 교미 무경험 암컷 CD1 마우스들을 할란(Harlan)으로부터 구입하였다. 마우스들을 실온(23℃ 내지 25℃) 및 광 조절된 실내(12시간 암주기, 12시간 명주기)에서 유지하였고 설치류 정규식 및 물에 자유롭게 접근하게 하였다. 치료 1주 전, 0.1 ㎖ 참깨유 중의 5 ㎍ 에스트라디올 사이피오네이트를 피하 주사함으로써 마우스들을 에스트로겐 프라이밍하였다. 에스트로겐 프라이밍으로부터 1주 후, 마우스들을 s.c. 용량의 릴랙신(40 nmol/kg), 또는 팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일) 융합 단백질(1.5, 3.0, 7.5 또는 15 nmol/kg)로 치료하였다. 투약으로부터 24시간 후, 캘리퍼를 이용하여 치골간 인대 길이를 측정하였다. 팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일) 융합체는 40 nmol/kg의 릴랙신과 유사한 효능을 갖는 1.5 nmol/kg까지 용량-반응 효능 하향을 보였다. 도 21은 치골간 인대 길이(mm) 대 릴랙신 또는 팔리비주맙(NH, CEXGGGGG)-릴랙신2(단일) 융합 단백질의 용량을 제공한다.
실시예 21: 마우스들에서의 팔리비주맙 융합 단백질의 약력학
단회 용량의 팔리비주맙 융합 단백질(8 mg/kg) 또는 PBS를 s.c. 주사로 CD1 마우스들(N=5)에게 투여하였다. 단회 용량 치료로부터 30분, 24시간, 48시간, 72시간, 96시간, 120시간, 144시간, 168시간 및 216시간 후, 글루코스(3 g/kg, p.o.)를 제공한 후, 글루코스 적재 직전 및 글루코스 적재로부터 15분, 30분, 45분, 60분 및 120분 후 혈액 글루코스를 측정하였다. 투여된 융합 단백질들은 다음과 같았다: 팔리비주맙(NH, GGGGS)-GLP1(서열번호 217); 팔리비주맙(NL, GGGGG)-글루카곤(서열번호 194)과 함께 팔리비주맙(NH, GGGGS)-GLP1(서열번호 217); 및 팔리비주맙(NH, GGGGS)-엑센딘-4(서열번호 192). 각각의 융합 단백질에 대한 글루코스 측정치 대 시간의 곡선은 도 22의 그래프에 표시되어 있다.
실시예 22: 팔리비주맙-릴랙신(이중) 융합 단백질의 발현 및 정제
팔리비주맙(NH, EAAAK)-릴랙신(이중)(서열번호 222)을 코딩하는 플라스미드(0.4 mg) 및 팔리비주맙(LC)(서열번호 7)을 코딩하는 플라스미드(0.2 mg)를 PC2 플라스미드(0.4 mg)와 함께 600 ㎖의 HEK293 세포에 형질감염시켰다. 배양물을 37℃에서 진탕하면서 생장시킨 후 72시간 내지 96시간 동안 배양하였다. 세포 배양물을 원심분리하였고 상청액(600 ㎖)을 DPBS로 평형화된 3 ㎖의 단백질 A 비드 상에 적재하였다. 상기 비드를 25 ㎖의 DPBS로 세척하였고 결합된 단백질을 나중에 1 ㎖의 1 M 트리스-HCL(pH 8.9)로 보충된 10 ㎖의 0.1 M 글리신(pH 2.7)으로 용출하였다. 용출된 단백질을 3 ㎖의 DPBS 평형화된 Ni-NTA 비드에 적용하였고 팔리비주맙(NH, EAAAK)-릴랙신(이중)(0.4 mg) 및 팔리비주맙(LC)을 포함하는 비결합된 분획을 수집하였다.
실시예 23: 릴랙신 수용체를 활성화시키는 팔리비주맙-릴랙신 융합(이중) 단백질의 활성
실시예 22에서 정제된, 팔리비주맙(LC)(서열번호 7)을 갖는 팔리비주맙(NH, EAAAK)-릴랙신(이중)(서열번호 222)의 활성을 루시퍼라제 분석으로 조사하였다. 릴랙신 수용체(LGR7 또는 LGR8) 및 cAMP 반응 요소(CRE)-루시퍼라제(Luc) 레포터 유전자를 과다발현하는 HEK293 세포를, 5% CO2 하에 37℃에서 10% FBS로 보충된 DMEM에서 증식시켰다. 세포를 24시간 동안 384웰 플레이트에 시딩한 후, 추가 24시간 동안 다양한 농도의 릴랙신-2, 및 팔리비주맙(LC)을 갖는 팔리비주맙(NH, EAAAK)-릴랙신(이중)으로 처리하였다. 그 다음, 제조자의 지시에 따라 원-글로(프로메가) 루시퍼라제 시약을 사용하여 발광 강도를 측정하였다. 데이터를 로지스틱 S자형 함수 y = A2 + (A1-A2)/(1 + (x/x0)p)(이때, A1은 초기 값이고, A2는 최종 값이고, x0은 곡선의 변곡점이고, p는 거듭제곱임)에 피팅함으로써 EC50 값을 결정하였다. 곡선은 도 23A 및 23B에 표시되어 있다. LGR7 발현 세포의 경우, 릴랙신-2에 대한 EC50은 0.014 nM이었고, 팔리비주맙(LC)을 갖는 팔리비주맙(NH, EAAAK)-릴랙신(이중)에 대한 EC50은 0.079 nM이었다. LGR8 발현 세포의 경우, 릴랙신-2에 대한 EC50은 11.2 nM이었고, 팔리비주맙(LC)을 갖는 팔리비주맙(NH, EAAAK)-릴랙신(이중)에 대한 EC50은 6766 nM이었다. 이들 데이터는 아미노 말단 릴랙신 융합 단백질들이 릴랙신 수용체에 대한 그들의 선택성에 있어서 야생형 릴랙신에 필적한다는 것을 보여준다.
실시예 24: 팔리비주맙-릴랙신(이중) 융합 단백질의 약동학 연구
실시예 22에서 정제된, 팔리비주맙(LC)(서열번호 7)을 갖는 팔리비주맙(NH, EAAAK)-릴랙신(이중)(서열번호 222)을 투여 모드 둘 다에 대해 20 nmol/kg의 용량으로 2개의 분리된 실험군들 내의 SD 암컷 래트 내로 정맥내(i.v.) 또는 피하(s.c.) 주사하였다. 150시간의 경과에 걸쳐 혈장 샘플을 채취하였다. 샌드위치 ELISA 분석을 이용하여 팔리비주맙(LC)을 갖는 팔리비주맙(NH, EAAAK)-릴랙신(이중) 수준을 정량하였다. 요약하건대, 96웰 플레이트를 4℃에서 항-hFc(애브캄 98616, 1:100 희석, PBS)와 함께 하룻밤 동안 항온처리하였다. 이 코팅 용액을 따라내고 플레이트를 1시간 동안 실온에서 차단 완충제(0.5% 트윈-20/PBS 중의 2% 밀크)로 차단하였다. 차단 용액을 따라내고 플레이트를 2시간 동안 실온에서 (차단 완충제 중의) 혈청 희석물과 함께 항온처리하였는데, 이때 혈청은 10배 내지 106배 희석되었다. 혈청을 따라내고 플레이트를 0.5% 트윈-20/PBS로 광범위하게 세척한 후, 1시간 동안 실온에서 항-릴랙신(밀리포어, 553850, 1:1000 희석, 차단 완충제)과 함께 항온처리하였다. 용액을 따라내고 플레이트를 0.5% 트윈-20/PBS로 광범위하게 세척한 후, 30분 동안 실온에서 항-토끼-HRP(라이프 테크놀로지스, A16023, 1:3000 희석, 차단 완충제)와 함께 항온처리하였다. 용액을 따라내고 플레이트를 0.5% 트윈-20/PBS로 광범위하게 세척하고 퀀타블루 형광발생성 퍼록시다제 기질(라이프 테크놀로지스, 15169)로 현상하고 스펙트라맥스 형광 플레이트 판독기를 이용하여 정량하였다. 신호를 표준 곡선의 직선 범위 내로 외삽함으로써(신호 대 농도) 혈장 샘플 중의 융합 단백질의 양을 정량하였다. 윈놀린(파사이트)을 이용하여 약동학 파라미터를 모델링하였다. 각각의 채취 시점에서의 융합 단백질의 농도가 작도되었고 도 24A(s.c. 투여) 및 24B(i.v. 투여)에 표시되어 있다. 팔리비주맙(NH, EAAAK)-릴랙신(이중) 융합 단백질은 0.5시간 미만의 반감기를 갖는 야생형 릴랙신에 비해 연장된 반감기를 가졌다. 팔리비주맙(NH, EAAAK)-릴랙신(이중) 융합 단백질의 반감기는 s.c. 투여의 경우 14시간이었고 i.v. 투여의 경우 17시간이었다. s.c. 경로에 대한 Cmax는 170.24 nM이었고 i.v. 투여 경로에 대한 Cmax는 660.99 nM이었다. s.c. 경로에 대한 AUC∞는 4223.08(hr*nM)이었고 i.v. 투여 경로에 대한 AUC∞는 3624.51(hr*nM)이었다.
실시예 25: 마우스 치골간 인대 모델에서의 팔리비주맙-릴랙신(이중) 융합 단백질의 용량-반응 효능
체중이 18 g 내지 20 g인 교미 무경험 암컷 CD1 마우스들을 할란으로부터 구입하였다. 마우스들을 실온(23℃ 내지 25℃) 및 광 조절된 실내(12시간 암주기, 12시간 명주기)에서 유지하였고 설치류 정규식 및 물에 자유롭게 접근하게 하였다. 치료 1주 전, 0.1 ㎖ 참깨유 중의 5 ㎍ 에스트라디올 사이피오네이트를 피하 주사함으로써 마우스들을 에스트로겐 프라이밍하였다. 에스트로겐 프라이밍으로부터 1주 후, 마우스들을 s.c. 용량의, 팔리비주맙(LC)(서열번호 7)을 갖는 팔리비주맙(NH, EAAAK)-릴랙신(이중)(서열번호 222)(실시예 22에서 정제됨)(1.5, 3.0, 7.5 또는 15 nmol/kg)으로 치료하였다. 투약으로부터 24시간 후, 캘리퍼를 이용하여 치골간 인대 길이를 측정하였다. 상기 융합 단백질은 3.0 nmol/kg까지 용량-반응 효능 하향을 보였다. 도 25는 치골간 인대 길이(mm) 대 팔리비주맙(NH, EAAAK)-릴랙신(이중) 융합 단백질의 용량을 제공한다.
전술된 내용은 단지 본 발명의 원리를 보여준다. 당업자는 본원에 명확히 기재되어 있거나 제시되어 있지 않더라도 본 발명의 원리를 구현하고 본 발명의 사상 및 범위 내에 포함되는 다양한 배열들을 고안할 수 있다는 것이 인식될 것이다. 나아가, 본원에서 언급된 모든 예들 및 조건부 표현은 원칙적으로 본 설명을 읽은 자가 당분야를 더 발전시키기 위해 본 발명자들에 의해 제공된 본 발명의 원리 및 개념을 이해하는 데 도움을 주기 위한 것이고, 이러한 구체적으로 언급된 예 및 조건으로 한정되지 않는 것으로서 해석되어야 한다. 뿐만 아니라, 본 발명의 원리, 양태 및 실시양태뿐만 아니라 이의 구체적인 예도 언급하는 본원의 모든 문장들은 그의 구조적 균등물 및 기능적 균등물 둘 다를 포괄하기 위한 것이다. 추가로, 이러한 균등물들은 현재 공지된 균등물 및 향후 개발된 균등물, 즉 동일한 기능을 수행하는 개발된 임의의 요소 둘 다를 구조와 관계없이 포함하고자 한다. 따라서, 본 발명의 범위는 본원에 제시되어 있고 기재되어 있는 예시적인 실시양태들로 한정되지 않는다. 오히려, 본 발명의 범위 및 사상은 첨부된 청구범위에 의해 구현된다.
본 발명의 바람직한 실시양태들이 본원에 제시되어 있고 기재되어 있지만, 이러한 실시양태들이 예로서만 제공되는 것임은 당업자에게 자명할 것이다. 본 발명으로부터 벗어나지 않으면서 다수의 변이들, 변화들 및 치환들이 당업자에게 도출될 것이다. 본원에 기재되어 있는 본 발명의 실시양태들에 대한 다양한 대안들이 본 발명을 실시하는 데 사용될 수 있다는 것이 이해되어야 한다. 하기 청구범위는 본 발명의 범위를 정의하고 이 청구범위 내의 방법들 및 구조들, 및 이들의 균등물들은 그에 의해 커버된다.
본원에서 인용된 모든 참고문헌들은 마치 각각의 개별 공개문헌, 특허 또는 특허출원이 모든 목적들을 위해 전체로서 참고로 도입되는 것으로 구체적으로 및 개별적으로 표시되어 있는 것처럼 동일한 정도로 모든 목적들을 위해 전체로서 참고로 도입된다.
Claims (73)
- a. 제1 면역글로불린 영역;
b. 면역글로불린으로부터 유래되지 않은 제1 치료 펩티드; 및
c. 연결 펩티드
를 포함하는 면역글로불린 융합 단백질로서, 상기 연결 펩티드가 제1 치료 펩티드를 제1 면역글로불린 영역의 아미노 말단에 연결시키는 것인 면역글로불린 융합 단백질. - 제1항에 있어서, 제2 면역글로불린 영역을 추가로 포함하는 면역글로불린 융합 단백질.
- 제1항 또는 제2항에 있어서, 제1 면역글로불린 영역이 면역글로불린 경쇄의 가변 영역, 면역글로불린 중쇄의 가변 영역, 또는 면역글로불린 경쇄의 가변 영역 및 면역글로불린 중쇄의 가변 영역 둘 다를 포함하는 것인 면역글로불린 융합 단백질.
- 제2항에 있어서, 제2 면역글로불린 영역이 면역글로불린 중쇄의 가변 영역, 면역글로불린 경쇄의 가변 영역, 또는 면역글로불린 경쇄의 가변 영역 및 면역글로불린 중쇄의 가변 영역 둘 다를 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제4항 중 어느 한 항에 있어서, 제1 면역글로불린 영역이 서열번호 5 내지 8 중 어느 하나의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제2항에 있어서, 제2 면역글로불린 영역이 서열번호 5 내지 8 중 어느 하나의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제6항 중 어느 한 항에 있어서, 제1 면역글로불린 영역이 트라스투주맙(trastuzumab), 팔리비주맙(palivizumab), 또는 트라스투주맙 및 팔리비주맙 둘 다의 면역글로불린 서열에 기초한, 또는 이러한 면역글로불린 서열로부터 유래된 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제2항에 있어서, 제2 면역글로불린 영역이 트라스투주맙, 팔리비주맙, 또는 트라스투주맙 및 팔리비주맙 둘 다의 면역글로불린 서열에 기초한, 또는 이러한 면역글로불린 서열로부터 유래된 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제8항 중 어느 한 항에 있어서, 연결 펩티드가 약 1개 내지 약 50개의 아미노산을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 연결 펩티드의 아미노산들이 규칙적인 이차 구조를 형성하지 않는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 연결 펩티드가 서열번호 115 내지 118 및 237 내지 239 중 어느 하나의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제11항 중 어느 한 항에 있어서, 면역글로불린 융합 단백질의 제1 치료 펩티드의 활성이 표준 사용 제제의 제1 치료 펩티드의 활성에 필적하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 면역글로불린 융합 단백질의 제1 면역글로불린 영역의 활성이 천연(native) 제1 면역글로불린 영역의 활성에 필적하는 것인 면역글로불린 융합 단백질.
- 제2항에 있어서, 제2 면역글로불린 영역이 하기 식 I을 갖는 것인 면역글로불린 융합 단백질:
A2-E1-T2-E2 I
상기 식에서, A2는 제2 면역글로불린 영역이고, E1은 제1 연장제(extender) 펩티드이고, E2는 제2 연장제 펩티드이고, T2는 제2 치료 펩티드이다. - 제14항에 있어서, E1이 서열번호 119의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제14항 또는 제15항에 있어서, E2가 서열번호 120의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제14항 내지 제16항 중 어느 한 항에 있어서, T2가 호르몬인 면역글로불린 융합 단백질.
- 제14항 내지 제17항 중 어느 한 항에 있어서, T2가 대사 장애, 및/또는 상기 대사 장애로부터 비롯된 질환의 치료에 효과적인 것인 면역글로불린 융합 단백질.
- 제18항에 있어서, 대사 장애가 지방이영양증, 당뇨병, 과트리글리세라이드혈증, 또는 이들의 조합인 면역글로불린 융합 단백질.
- 제14항 내지 제19항 중 어느 한 항에 있어서, T2가 렙틴(leptin) 아미노산 서열 및/또는 서열번호 96의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제2항 및 제14항 내지 제20항 중 어느 한 항에 있어서, 제2 면역글로불린 영역이 서열번호 43의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제2항 및 제14항 내지 제20항 중 어느 한 항에 있어서, 제2 면역글로불린 영역이 서열번호 44의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제22항 중 어느 한 항에 있어서, 추가 치료 펩티드를 추가로 포함하는 면역글로불린 융합 단백질.
- 제23항에 있어서, 추가 치료 펩티드가 제1 면역글로불린 영역에 부착되어 있는 것인 면역글로불린 융합 단백질.
- 제2항에 있어서, 제2 면역글로불린 영역이 추가 치료 펩티드에 부착되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 GLP-1 수용체 아고니스트 또는 이의 합성물인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 글루카곤 유사체 또는 이의 합성물인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 호르몬 또는 이의 합성물인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 칼륨 채널에 결합하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 신경독소인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 인슐린 수퍼패밀리에 속하는 호르몬인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 엑센딘(exendin)-4 아미노산 서열 및/또는 서열번호 95의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 서열번호 97의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 서열번호 98의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 인슐린 아미노산 서열 및/또는 서열번호 105의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 옥신토모듈린(oxyntomodulin) 아미노산 서열 및/또는 서열번호 106의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 a) 글루카곤 아미노산 서열 또는 b) 글루카곤 유사 펩티드 아미노산 서열 및/또는 서열번호 107의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 모카톡신(mokatoxin)-1 아미노산 서열 및/또는 서열번호 108의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 신경독소 mu-SLPTX-Ssm6a 아미노산 서열 및/또는 서열번호 109의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 카파-쎄라포톡신(kappa-theraphotoxin)-Tb1a 아미노산 서열 및/또는 서열번호 110의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 맘발라인(mambalign)-1 아미노산 서열 및/또는 서열번호 111의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 제1 치료 펩티드가 a) 프로릴랙신(prorelaxin) 또는 릴랙신(relaxin) 아미노산 서열 또는 이로부터 유래된 아미노산 서열 및/또는 b) 서열번호 99, 104, 112, 113 및 230 내지 235로부터 선택된 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제25항 중 어느 한 항에 있어서, 서열번호 42 내지 74 및 192 내지 221 중 어느 하나의 아미노산 서열과 약 또는 적어도 약 80%, 85%, 90%, 95% 또는 100% 동일한 아미노산 서열을 포함하는 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 심부전을 갖는 환자를 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 섬유증을 갖는 환자를 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 당뇨병 및/또는 당뇨병 관련 질환을 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 비만 및/또는 비만 관련 질환을 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 단장 증후군 및/또는 단장 증후군 관련 질환을 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 염증성 장 질환 및/또는 염증성 장 관련 질환을 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 자가면역 질환을 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 통증을 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 급성 관상 동맥 증후군, 심방 세동, 심장 섬유증 및 관상 동맥 질환으로부터 선택된 질환 또는 병태를 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 제1 치료 펩티드 및/또는 면역글로불린 융합 단백질이 허혈 재관류, 장기 보호를 위한 심폐 바이패스, 허혈성 뇌졸중, 각막 치유, 당뇨병성 신장병증, 간경변증, 문맥 고혈압, 당뇨병성 상처 치유, 전신 경화증, 분만 시 자궁경부 숙화, 자간전증 및 고혈압으로부터 선택된 질환 또는 병태를 치료하도록 구성되어 있는 것인 면역글로불린 융합 단백질.
- 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 포함하는 약학 조성물.
- 제54항에 있어서, 약학적으로 허용 가능한 부형제를 추가로 포함하는 약학 조성물.
- 질환 또는 병태의 치료를 필요로 하는 대상체에서 질환 또는 병태를 치료하는 방법으로서, 치료 유효량의 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 상기 대상체에게 투여하는 단계를 포함하는 방법.
- 비만을 갖는 개체를 치료하는 방법으로서, 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법.
- 당뇨병을 갖는 개체를 치료하는 방법으로서, 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법.
- 단장 증후군 및/또는 단장 증후군 관련 질환을 갖는 개체를 치료하는 방법으로서, 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법.
- 염증성 장 질환 및/또는 염증성 장 관련 질환을 갖는 개체를 치료하는 방법으로서, 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법.
- 자가면역 질환을 갖는 개체를 치료하는 방법으로서, 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법.
- 통증을 갖는 개체를 치료하는 방법으로서, 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법.
- 심부전을 갖는 개체를 치료하는 방법으로서, 제1항 내지 제53항 중 어느 한 항의 면역글로불린 융합 단백질을 투여하는 단계를 포함하는 방법.
- 제1항 내지 제53항 중 어느 한 항의 제1 면역글로불린 영역, 제1 치료 펩티드 및 연결 펩티드를 코딩하는 핵산을 포함하는 제1 유전자 구축물.
- 제2항 및 제14항 내지 제22항 중 어느 한 항의 제2 면역글로불린 영역을 코딩하는 핵산을 포함하는 제2 유전자 구축물.
- 제64항의 유전자 구축물을 포함하는 제1 발현 벡터.
- 제65항의 유전자 구축물을 포함하는 제2 발현 벡터.
- 제66항의 제1 발현 벡터를 포함하는 포유동물 발현 숙주.
- 제67항의 제2 발현 벡터를 포함하는 포유동물 발현 숙주.
- 면역글로불린 융합 단백질을 제조하는 방법으로서,
a. 제66항의 발현 벡터를 포유동물 세포 배양물에서 일시적으로 형질감염시키는 단계;
b. 조절된 온도 및 CO2 비율(%)에서 발현 배지 중에서 세포 배양물을 증식시키는 단계; 및
c. 분비된 면역글로불린 융합 단백질을 회수하는 단계
를 포함하는 방법. - 제70항에 있어서, 면역글로불린 융합 단백질을 정제하는 단계를 추가로 포함하는 방법.
- 제2 면역글로불린 영역을 제조하는 방법으로서,
a. 제67항의 발현 벡터를 포유동물 세포 배양물에서 일시적으로 형질감염시키는 단계;
b. 조절된 온도 및 백분율 CO2에서 발현 배지 중에서 세포 배양물을 증식시키는 단계; 및
c. 분비된 제2 면역글로불린 영역을 회수하는 단계
를 포함하는 방법. - 제72항에 있어서, 제2 면역글로불린 영역을 정제하는 단계를 추가로 포함하는 방법.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201462009054P | 2014-06-06 | 2014-06-06 | |
| US62/009,054 | 2014-06-06 | ||
| US201462030526P | 2014-07-29 | 2014-07-29 | |
| US62/030,526 | 2014-07-29 | ||
| US201462064186P | 2014-10-15 | 2014-10-15 | |
| US62/064,186 | 2014-10-15 | ||
| PCT/US2015/034533 WO2015188132A1 (en) | 2014-06-06 | 2015-06-05 | Methods of constructing amino terminal immunoglobulin fusion proteins and compositions thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170010893A true KR20170010893A (ko) | 2017-02-01 |
Family
ID=54767470
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177000273A KR20170010893A (ko) | 2014-06-06 | 2015-06-05 | 아미노 말단 면역글로불린 융합 단백질 및 이의 조성물을 구축하는 방법 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20170327577A1 (ko) |
| EP (1) | EP3152238A4 (ko) |
| JP (1) | JP2017518049A (ko) |
| KR (1) | KR20170010893A (ko) |
| CN (1) | CN106661128A (ko) |
| AU (1) | AU2015269210A1 (ko) |
| CA (1) | CA2950178A1 (ko) |
| WO (1) | WO2015188132A1 (ko) |
Families Citing this family (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6261500B2 (ja) | 2011-07-22 | 2018-01-17 | プレジデント アンド フェローズ オブ ハーバード カレッジ | ヌクレアーゼ切断特異性の評価および改善 |
| US9163284B2 (en) | 2013-08-09 | 2015-10-20 | President And Fellows Of Harvard College | Methods for identifying a target site of a Cas9 nuclease |
| US9359599B2 (en) | 2013-08-22 | 2016-06-07 | President And Fellows Of Harvard College | Engineered transcription activator-like effector (TALE) domains and uses thereof |
| US9737604B2 (en) | 2013-09-06 | 2017-08-22 | President And Fellows Of Harvard College | Use of cationic lipids to deliver CAS9 |
| US9322037B2 (en) | 2013-09-06 | 2016-04-26 | President And Fellows Of Harvard College | Cas9-FokI fusion proteins and uses thereof |
| US9340800B2 (en) | 2013-09-06 | 2016-05-17 | President And Fellows Of Harvard College | Extended DNA-sensing GRNAS |
| US11053481B2 (en) | 2013-12-12 | 2021-07-06 | President And Fellows Of Harvard College | Fusions of Cas9 domains and nucleic acid-editing domains |
| US10077453B2 (en) | 2014-07-30 | 2018-09-18 | President And Fellows Of Harvard College | CAS9 proteins including ligand-dependent inteins |
| WO2017070632A2 (en) | 2015-10-23 | 2017-04-27 | President And Fellows Of Harvard College | Nucleobase editors and uses thereof |
| ES2903257T3 (es) | 2015-12-09 | 2022-03-31 | Scripps Research Inst | Proteínas de fusión de inmunoglobulina de relaxina y métodos de uso |
| WO2017112889A1 (en) | 2015-12-23 | 2017-06-29 | The Johns Hopkins University | Long-acting glp-1r agonist as a therapy of neurological and neurodegenerative conditions |
| BR112018073683A2 (pt) * | 2016-05-18 | 2019-02-26 | Modernatx, Inc. | polinucleotídeos codificadores de relaxina |
| WO2018027078A1 (en) | 2016-08-03 | 2018-02-08 | President And Fellows Of Harard College | Adenosine nucleobase editors and uses thereof |
| CA3033327A1 (en) | 2016-08-09 | 2018-02-15 | President And Fellows Of Harvard College | Programmable cas9-recombinase fusion proteins and uses thereof |
| WO2018039438A1 (en) | 2016-08-24 | 2018-03-01 | President And Fellows Of Harvard College | Incorporation of unnatural amino acids into proteins using base editing |
| GB2573062A (en) | 2016-10-14 | 2019-10-23 | Harvard College | AAV delivery of nucleobase editors |
| WO2018119359A1 (en) | 2016-12-23 | 2018-06-28 | President And Fellows Of Harvard College | Editing of ccr5 receptor gene to protect against hiv infection |
| AU2018219283B2 (en) | 2017-02-08 | 2022-05-19 | Bristol-Myers Squibb Company | Modified relaxin polypeptides comprising a pharmacokinetic enhancer and uses thereof |
| US11898179B2 (en) | 2017-03-09 | 2024-02-13 | President And Fellows Of Harvard College | Suppression of pain by gene editing |
| WO2018165629A1 (en) | 2017-03-10 | 2018-09-13 | President And Fellows Of Harvard College | Cytosine to guanine base editor |
| KR20190130613A (ko) | 2017-03-23 | 2019-11-22 | 프레지던트 앤드 펠로우즈 오브 하바드 칼리지 | 핵산 프로그램가능한 dna 결합 단백질을 포함하는 핵염기 편집제 |
| US11560566B2 (en) | 2017-05-12 | 2023-01-24 | President And Fellows Of Harvard College | Aptazyme-embedded guide RNAs for use with CRISPR-Cas9 in genome editing and transcriptional activation |
| CN111801345A (zh) | 2017-07-28 | 2020-10-20 | 哈佛大学的校长及成员们 | 使用噬菌体辅助连续进化(pace)的进化碱基编辑器的方法和组合物 |
| WO2019139645A2 (en) | 2017-08-30 | 2019-07-18 | President And Fellows Of Harvard College | High efficiency base editors comprising gam |
| WO2019079347A1 (en) | 2017-10-16 | 2019-04-25 | The Broad Institute, Inc. | USES OF BASIC EDITORS ADENOSINE |
| KR20210143230A (ko) | 2019-03-19 | 2021-11-26 | 더 브로드 인스티튜트, 인코퍼레이티드 | 뉴클레오티드 서열을 편집하기 위한 방법 및 조성물 |
| RU2750267C1 (ru) * | 2020-02-07 | 2021-06-25 | Общество с ограниченной ответственностью «НАУЧНО-ПРОИЗВОДСТВЕННОЕ ОБЪЕДИНЕНИЕ ИН-ВЕТ» | Рекомбинантный ростовой дифференцировочный фактор роста 11 (GDF11), способ его получения, инъекционный препарат для повышения мышечной массы млекопитающих животных и птицы, а также способ использования препарата |
| CN116096873A (zh) | 2020-05-08 | 2023-05-09 | 布罗德研究所股份有限公司 | 同时编辑靶标双链核苷酸序列的两条链的方法和组合物 |
| WO2024026418A1 (en) * | 2022-07-28 | 2024-02-01 | New York University | Targeting long non-coding rna chromr in interferon-mediated inflammation in humans |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4944324B2 (ja) * | 1999-07-13 | 2012-05-30 | ボルダー バイオテクノロジー, インコーポレイテッド | 免疫グロブリン融合タンパク質 |
| AU2001275246B2 (en) * | 2000-06-05 | 2006-06-29 | Altor Bioscience Corporation | T cell receptor fusions and conjugates and methods of use thereof |
| AU2001283496A1 (en) * | 2000-07-25 | 2002-02-05 | Immunomedics, Inc. | Multivalent target binding protein |
| US6992174B2 (en) * | 2001-03-30 | 2006-01-31 | Emd Lexigen Research Center Corp. | Reducing the immunogenicity of fusion proteins |
| US20080260731A1 (en) * | 2002-03-01 | 2008-10-23 | Bernett Matthew J | Optimized antibodies that target cd19 |
| PT1636261E (pt) * | 2003-06-26 | 2007-11-08 | Merck Patent Gmbh | Proteínas trombopoietina com propriedades melhoradas |
| JP2012521197A (ja) * | 2009-03-20 | 2012-09-13 | アムジエン・インコーポレーテツド | 担体免疫グロブリンおよびその使用 |
| EA201290123A1 (ru) * | 2009-09-30 | 2012-10-30 | Глаксо Груп Лимитед | Продукты слияния и конъюгаты лекарственных средств с увеличенным периодом полувыведения |
| WO2012169822A2 (ko) * | 2011-06-10 | 2012-12-13 | 강원대학교산학협력단 | 암세포 증식 억제와 혈관신생 억제를 위한 융합 단백질 및 이를 포함한 항암 조성물 |
-
2015
- 2015-06-05 CN CN201580042157.3A patent/CN106661128A/zh active Pending
- 2015-06-05 WO PCT/US2015/034533 patent/WO2015188132A1/en active Application Filing
- 2015-06-05 KR KR1020177000273A patent/KR20170010893A/ko unknown
- 2015-06-05 CA CA2950178A patent/CA2950178A1/en not_active Abandoned
- 2015-06-05 AU AU2015269210A patent/AU2015269210A1/en not_active Abandoned
- 2015-06-05 EP EP15803905.7A patent/EP3152238A4/en not_active Withdrawn
- 2015-06-05 US US15/315,645 patent/US20170327577A1/en not_active Abandoned
- 2015-06-05 JP JP2016569796A patent/JP2017518049A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| WO2015188132A1 (en) | 2015-12-10 |
| AU2015269210A8 (en) | 2017-01-05 |
| WO2015188132A8 (en) | 2017-01-12 |
| EP3152238A1 (en) | 2017-04-12 |
| CN106661128A (zh) | 2017-05-10 |
| US20170327577A1 (en) | 2017-11-16 |
| CA2950178A1 (en) | 2015-12-10 |
| EP3152238A4 (en) | 2018-01-03 |
| JP2017518049A (ja) | 2017-07-06 |
| AU2015269210A1 (en) | 2016-12-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11673959B2 (en) | Coiled coil immunoglobulin fusion proteins and compositions thereof | |
| KR20170010893A (ko) | 아미노 말단 면역글로불린 융합 단백질 및 이의 조성물을 구축하는 방법 | |
| US11421033B2 (en) | Insulin immunoglobulin fusion proteins | |
| JP6346189B2 (ja) | Gm−csf中和化合物を含む液体製剤 | |
| JP6339578B2 (ja) | Gm−csf中和化合物を含む凍結乾燥製剤 | |
| JP6769879B2 (ja) | Gm−csf中和化合物を含む液体製剤 | |
| US20220048969A1 (en) | Relaxin immunoglobulin fusion proteins and methods of use | |
| WO2018013483A1 (en) | Kv1.3 channel blocking peptides and uses thereof |