KR20150132375A - 비-중공, 다공성 입자의 제조를 위한 분무 열분해시 슬러리의 사용 방법 - Google Patents
비-중공, 다공성 입자의 제조를 위한 분무 열분해시 슬러리의 사용 방법 Download PDFInfo
- Publication number
- KR20150132375A KR20150132375A KR1020157029101A KR20157029101A KR20150132375A KR 20150132375 A KR20150132375 A KR 20150132375A KR 1020157029101 A KR1020157029101 A KR 1020157029101A KR 20157029101 A KR20157029101 A KR 20157029101A KR 20150132375 A KR20150132375 A KR 20150132375A
- Authority
- KR
- South Korea
- Prior art keywords
- particles
- solid phase
- metal oxide
- average
- product
- Prior art date
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/485—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of mixed oxides or hydroxides for inserting or intercalating light metals, e.g. LiTi2O4 or LiTi2OxFy
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2/00—Processes or devices for granulating materials, e.g. fertilisers in general; Rendering particulate materials free flowing in general, e.g. making them hydrophobic
- B01J2/02—Processes or devices for granulating materials, e.g. fertilisers in general; Rendering particulate materials free flowing in general, e.g. making them hydrophobic by dividing the liquid material into drops, e.g. by spraying, and solidifying the drops
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B29—WORKING OF PLASTICS; WORKING OF SUBSTANCES IN A PLASTIC STATE IN GENERAL
- B29B—PREPARATION OR PRETREATMENT OF THE MATERIAL TO BE SHAPED; MAKING GRANULES OR PREFORMS; RECOVERY OF PLASTICS OR OTHER CONSTITUENTS OF WASTE MATERIAL CONTAINING PLASTICS
- B29B9/00—Making granules
- B29B9/16—Auxiliary treatment of granules
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01D—COMPOUNDS OF ALKALI METALS, i.e. LITHIUM, SODIUM, POTASSIUM, RUBIDIUM, CAESIUM, OR FRANCIUM
- C01D15/00—Lithium compounds
- C01D15/02—Oxides; Hydroxides
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G1/00—Methods of preparing compounds of metals not covered by subclasses C01B, C01C, C01D, or C01F, in general
- C01G1/02—Oxides
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
- C01G53/40—Nickelates
- C01G53/42—Nickelates containing alkali metals, e.g. LiNiO2
- C01G53/44—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese
- C01G53/50—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese of the type [MnO2]n-, e.g. Li(NixMn1-x)O2, Li(MyNixMn1-x-y)O2
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/58—Selection of substances as active materials, active masses, active liquids of inorganic compounds other than oxides or hydroxides, e.g. sulfides, selenides, tellurides, halogenides or LiCoFy; of polyanionic structures, e.g. phosphates, silicates or borates
- H01M4/5825—Oxygenated metallic salts or polyanionic structures, e.g. borates, phosphates, silicates, olivines
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G45/00—Compounds of manganese
- C01G45/12—Manganates manganites or permanganates
- C01G45/1221—Manganates or manganites with a manganese oxidation state of Mn(III), Mn(IV) or mixtures thereof
- C01G45/1228—Manganates or manganites with a manganese oxidation state of Mn(III), Mn(IV) or mixtures thereof of the type [MnO2]n-, e.g. LiMnO2, Li[MxMn1-x]O2
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G45/00—Compounds of manganese
- C01G45/12—Manganates manganites or permanganates
- C01G45/1221—Manganates or manganites with a manganese oxidation state of Mn(III), Mn(IV) or mixtures thereof
- C01G45/125—Manganates or manganites with a manganese oxidation state of Mn(III), Mn(IV) or mixtures thereof of the type[MnO3]n-, e.g. Li2MnO3, Li2[MxMn1-xO3], (La,Sr)MnO3
- C01G45/1257—Manganates or manganites with a manganese oxidation state of Mn(III), Mn(IV) or mixtures thereof of the type[MnO3]n-, e.g. Li2MnO3, Li2[MxMn1-xO3], (La,Sr)MnO3 containing lithium, e.g. Li2MnO3, Li2[MxMn1-xO3
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G51/00—Compounds of cobalt
- C01G51/40—Cobaltates
- C01G51/42—Cobaltates containing alkali metals, e.g. LiCoO2
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G51/00—Compounds of cobalt
- C01G51/40—Cobaltates
- C01G51/42—Cobaltates containing alkali metals, e.g. LiCoO2
- C01G51/44—Cobaltates containing alkali metals, e.g. LiCoO2 containing manganese
- C01G51/50—Cobaltates containing alkali metals, e.g. LiCoO2 containing manganese of the type [MnO2]n-, e.g. Li(CoxMn1-x)O2, Li(MyCoxMn1-x-y)O2
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G51/00—Compounds of cobalt
- C01G51/40—Cobaltates
- C01G51/42—Cobaltates containing alkali metals, e.g. LiCoO2
- C01G51/44—Cobaltates containing alkali metals, e.g. LiCoO2 containing manganese
- C01G51/56—Cobaltates containing alkali metals, e.g. LiCoO2 containing manganese of the type [MnO3]2-, e.g. Li2[CoxMn1-xO3], Li2[MyCoxMn1-x-yO3
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
- C01G53/40—Nickelates
- C01G53/42—Nickelates containing alkali metals, e.g. LiNiO2
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
- C01G53/40—Nickelates
- C01G53/42—Nickelates containing alkali metals, e.g. LiNiO2
- C01G53/44—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese
- C01G53/56—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese of the type [MnO3]2-, e.g. Li2[NixMn1-xO3], Li2[MyNixMn1-x-yO3
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/30—Three-dimensional structures
- C01P2002/32—Three-dimensional structures spinel-type (AB2O4)
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2002/00—Crystal-structural characteristics
- C01P2002/50—Solid solutions
- C01P2002/52—Solid solutions containing elements as dopants
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/01—Particle morphology depicted by an image
- C01P2004/03—Particle morphology depicted by an image obtained by SEM
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/30—Particle morphology extending in three dimensions
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/30—Particle morphology extending in three dimensions
- C01P2004/45—Aggregated particles or particles with an intergrown morphology
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/61—Micrometer sized, i.e. from 1-100 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/62—Submicrometer sized, i.e. from 0.1-1 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/80—Particles consisting of a mixture of two or more inorganic phases
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/80—Particles consisting of a mixture of two or more inorganic phases
- C01P2004/82—Particles consisting of a mixture of two or more inorganic phases two phases having the same anion, e.g. both oxidic phases
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/11—Powder tap density
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/12—Surface area
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/16—Pore diameter
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/40—Electric properties
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Materials Engineering (AREA)
- Crystallography & Structural Chemistry (AREA)
- Manufacturing & Machinery (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
- Glanulating (AREA)
- Mechanical Engineering (AREA)
Abstract
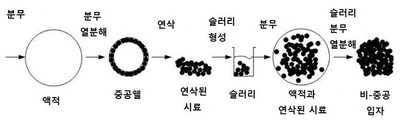
슬러리의 액적을 형성하기 위한 하나 이상의 금속 산화물의 하나 또는 그 이상의 금속 원소를 포함하는, 하나 이상의 전구체 화합물을 포함하는 액체 내에 고체상 입자를 포함하는 슬러리를 에어로졸화하는 것을 포함하는 분무 열분해를 수행하는 단계, 및 최소한 부분적으로 하나 이상의 전구체 화합물을 분해하고 비-중공 형태를 갖는 금속 산화물을 포함하는 분말을 형성하기 위해 액적을 소성하는 단계를 포함하는 금속 산화물을 포함하는 분말을 제조하는 방법.
Description
관련 출원의 상호-참조
본 출원은 그 전체가 참조로서 인용되는, 2013년 03월 13일자로 출원된 미국 가출원 61/780,059의 이익을 주장하는 비-가출원이다.
연방정부로부터 후원 받은 연구 또는 개발에 대한 언급
본 발명은 국립 과학 재단(National Science Foundation)으로부터 승인(부여번호. 0928964)된 정부의 지원으로 이루어졌다. 정부는 본 발명에 대한 특정 권한을 가진다.
본 발명의 기술분야
본 발명은 일반적으로 분말의 제조를 위한 분무 열분해 방법에 관한 것이다. 보다 구체적으로, 본 발명은 조절된 또는 감소된 중공 또는 비-중공 형태를 갖는 입자를 제조하기 위한 고체 물질 및 액체의 혼합물을 포함하는 슬러리의 분무 열분해에 관한 것이다.
분무 열분해는 미크론(micron) 및 나노스케일 분말을 제조하는 강력하고 가장 비용 효율이 높은 방법이다. 그러나, 생성되는 입자의 형태의 조절 정도는 제한적이었다. 특히, 일반적으로 다공성 및 미세 구조의 쉘을 가지는 중공구체(hollow spheres)가 제조되며, 특히 원하는 입자가 어느 정도 미크론 크기 또는 그 이상인 경우 그러하다. "Morphology of single-component particles produced by spray pyrolysis," S. Jain, D. J. Skamser, T. T. Kodas, Aerosol Sci. Technol., 27, 575 (1997); "Ceramic powder synthesis by spray pyrolysis," G.L. Messing, S.C. Zhang, G.V. Jayanthi, J. Am. Ceram. Soc., 76, 2707 (1993). 이러한 구조는 물질의 충전 밀도(packing density)가 주요 성능 파라미터(performance parameter)인 에너지 저장과 같은 적용에 바람직하지 않다. 여러 방법들이 중공구체의 문제를 해결하기 위하여 개발되었으나, 각각은 자체의 결점과 제한을 갖는다.
예를 들어, 특정 방법은 "소성된(fired)" 생성물, 또는 열분해된 물질을 증발시키고 기체상으로부터 고체 입자를 재구성하는 최종물질의 하나 이상의 구성 성분 또는 화합물의 녹는점을 초과하는 온도를 활용하고 있다. "Ceramic powder synthesis by spray pyrolysis," G.L. Messing, S.C. Zhang, G.V. Jayanthi, J. Am. Ceram. Soc., 76, 2707 (1993); "Flame spray pyrolysis: An enabling technology for nanoparticles design and fabrication," W. Y. Teoh, R. Amal, L. Maedler, Nanoscale, 2 (8), 1324 (2010); "Flame aerosol synthesis of smart nanostructured materials," R. Stroble, S. E. Pratsinis, J. Mater. Chem., 17 (45), 4743 (2007). 중공도(hollowness)를 해결하지만, 최소한 부분적으로, 이들 공정은 비-다공성 또는 낮은 다공성 입자가 발생하는 경향이 있으며 제조하는 동안 사용되는 높은 온도로 인하여 원치않는 상(phases) 및/또는 화합물을 갖는 경향이 있다.
또다른 방법은 건조 조절 화학적 첨가제(DCCA)의 사용을 포함한다. "Effects of amide types DCCAs on the properties of Y2O3: Euphosphor powders with spherical shape and fine size," H. Y. Koo, S. H. Lee, C. Y. Kang, J. Ceram. Soc. Jpn., 116 (1357), 955 (2008); "Effects of types of drying control chemical additives on the morphologies and electrochemical properties of Li4Ti5O12 anode powders prepared by spray pyrolysis," S. H. Ju, C. Y. Kang, J. Alloys Compd ., 506 (2), 913 (2010). 전구체를 가진 이러한 첨가제의 포함은 입자의 형태에 영향을 미치며 1 또는 2 미크론까지의 입자에 대하여 중공구조를 막아주나, 더 큰 입자 크기에 효과적이지 않다고 보고되었다. 또한, 이들 첨가제는 일반적으로 비싸며 최종 생성물을 오염시킬 위험이 있다.
또한 또다른 방법은 분쇄된 생성물의 분무 건조를 포함한다. "Synthesis of spherical LiMn2O4 microparticles by a combination of spray pyrolysis and drying method," I. Taniguchi, N. Fukuda, M. Konarova, Powder Technol., 181 (3), 228 (2008). 이 다단계 경로는 상대적으로 큰 이차 입자의 이점을 제공하나, 상기 입자는 결합 연결 또는 구조적 강도가 없는 여러 단편으로 구성된다. 이 문제는 분무된 용액에 결합제를 첨가함으로써 극복될 수 있으나, 결합제 자체가 생성물 내에서 오염물질로서 역할을 할 수 있으며 단편 사이의 밀접한 접촉을 방해할 수 있다.
또한, 제한된 양의 나노입자는 열분해 단계 동안 이종 핵생성을 촉진하는 시드로서 역할을 하도록 전구체 용액 내에 포함되어 있다. "Photoluminescence optimization of luminescent nanocomposites fabricated by spray pyrolysis of a colloid-solution precursor," W. Wang, W. Widiyastuti, T. Ogi, I. W. Lenggoro, K. Okuyama, Chem. Mater., 19 (7), 1723 (2007). 이 방법으로 제조된 비-중공 입자는 오직 서브미크론 크기 범위 내에 있다. 또한, 이 방법은 최종 생성물에 큰 부피의 비-활성 콜로이드를 포함시키며, 이는 대부분의 적용에 있어 바람직하지 않은 특징이다.
전술한 관점에서, 바람직하지 않은 불순물 또는 상의 도입 없이 상대적으로 큰 크기(예를 들어, 1 미크론 초과)의 비-중공, 다공성 입자의 제조 방법의 필요성은 여전히 존재한다.
일 구현예에서, 본 발명은 금속 산화물을 포함하는 분말을 제조하는 공정에 관한 것이다. 상기 공정은 하기를 포함하는 분무 열분해를 수행하는 단계를 포함한다:
(a) 전구체 용액 및 하나 또는 그 이상의 고체상 입자를 포함하는 액적(droplets)을 형성하기 위하여, 전구체 용액 내 고체상 입자를 포함하는 슬러리를 에어로졸화하는 단계, 여기서 (i) 고체상 입자는 약 10 nm 및 50 ㎛ 범위의 평균 크기를 가지며, (ii) 전구체 용액은 용매 내에 용해되거나 현탁된 하나 이상의 전구체 화합물을 포함하고, 여기서 하나 이상의 전구체 화합물은 하나 이상의 금속 산화물의 하나 또는 그 이상의 금속 원소를 포함하며, (iii) 슬러리는 약 2% 내지 약 75% 범위 내인 금속 산화물을 포함하는 분말에 대한 고체상 입자의 총 질량비를 갖는다;
(b) 하나 이상의 전구체 화합물 및 하나 또는 그 이상의 고체상 입자를 포함하는 건조된 액적을 형성하기 위한 액적 내 용매를 증발시키는 단계; 및
(c) 최소한 부분적으로 하나 이상의 전구체 화합물을 분해하고 금속 산화물을 포함하는 분말을 형성하기 위해 건조된 액적을 소성(calcining)하는 단계, 여기서 금속 산화물을 포함하는 분말은 하나 이상의 금속 산화물을 포함하는 생성물 입자를 포함하고, 여기서 생성물 입자는 (i) 약 100 nm 내지 약 500 ㎛ 범위 내인 평균 크기 및 (ii) 에어로졸 내 시드(seed) 입자의 부재를 제외하고 동일하게 수행되는 다른 분무 열분해 공정에 의해 제조된 거의 동일한 평균 크기 입자의 평균 중공도(hollowness) 미만인 평균 중공도를 갖는다.
또다른 구현예에서, 본 발명은 복수의 메조다공성, 비-중공 형태 및 약 1 ㎛ 내지 약 15 ㎛ 의 범위 내인 평균 크기를 갖는 이차 입자를 함유하는 금속 산화물을 포함하는 물질에 관한 것이며, 여기서 이차 입자는 약 50 nm 내지 약 500 nm의 범위 내인 평균 크기를 갖는 일차 입자를 포함한다.
또다른 구현예에서, 본 발명은 분말을 제조하는 공정에 관한 것으로, 상기 공정은 하기를 포함하는 분무 열분해를 수행하는 단계를 포함한다:
(a) 액체 및 하나 또는 그 이상의 고체상 입자를 포함하는 액적을 형성하기 위한 하나 이상의 전구체 화합물을 포함하는 액체 내 고체상 입자를 포함하는 슬러리를 에어로졸화하는 단계, 여기서 (i) 고체상 입자는 약 10 nm 및 50 ㎛ 범위 내인 평균 크기를 가지며, 및 (ii) 슬러리는 약 2% 내지 약 75%의 범위 내인 금속 산화물을 포함하는 분말에 대한 고체상 입자의 총 질량비를 갖는다; 및
(b) 최소한 부분적으로 하나 이상의 전구체 화합물을 분해하고 분말을 형성하도록 액적을 소성하는 단계, 여기서 분말은 하나 이상의 전구체 화합물의 분해 생성물(들)을 포함하는 생성물 입자를 포함하며, 여기서 생성물 입자는 (i) 약 100 nm 내지 약 500 ㎛ 범위 내인 평균 크기 및 (ii) 에어로졸 내 시드 입자의 부재를 제외하고 동일하게 수행되는 다른 분무 열분해 공정에 의해 제조된 거의 동일한 평균 크기 입자의 평균 중공도 미만인 평균 중공도를 갖는다.
또다른 구현예에서, 본 발명은 비-중공 형태 및 약 1 ㎛ 내지 약 15 ㎛ 범위 내인 평균 크기를 갖는 복수의 메조다공성 이차 입자를 포함하며, 여기서 이차 입자는 약 50 nm 내지 약 500 nm 범위 내인 평균 크기를 갖는 일차 입자를 포함하는 물질에 관한 것이다.
도 1은 비-슬러리 방법으로 생성된, 900℃에서 어닐링 후 분무 열분해를 이용하여 만들어진 0.5Li2MnO3·0.5LiNi0 .333Mn0 .333Co0 .333O2의 입자의 주사 전자 현미경 이미지를 포함한다. 상기 입자는 내부 중공도에 의해 변형된 구/깨진 쉘을 강조하는 원으로 가리킨 바와 같이 중공구체의 현저한 존재를 나타낸다.
도 2는 중공구체 형태를 나타내는 미크로톰(microtom)에 의해 만들어진 입자 단면의 주사 전자 현미경 이미지이다.
도 3은 본 발명의 일 구현예에 따른 물질의 공정을 도시하는 도면이다.
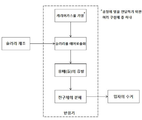
도 4는 본 발명의 일 구현예의 공정 흐름 블록도이다.
도 5는 본 발명의 구현예를 수행하는데 사용될 수 있는 "역화(back flame)" 분무 열분해 반응기를 도시하는 개략도이다.
도 6은 900℃에서 어닐링 후 슬러리 분무 열분해를 이용하여 만들어진 0.5Li2MnO3·0.5LiNi0.333Mn0.333Co0.333O2의 생성 분말의 주사 전자 현미경 이미지를 포함한다.
도 7은 수지 내 내포된 900℃에서 슬러리 분무 열분해 어닐링를 이용하여 만들어진 0.5Li2MnO3·0.5LiNi0.333Mn0.333Co0.333O2의 생성 분말의 단면의 주사 전자 현미경 이미지이다.
도 8은 2012-12-14 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 사이클 시험 결과를 나타내는 그래프이다.
도 9는 2012-12-14 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 속도 능력 시험 결과를 나타내는 그래프이다.
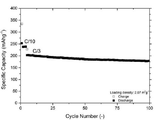
도 10은 2013-02-06 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 사이클 시험 결과를 나타내는 그래프이다.
도 11은 2013-02-06 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 속도 능력 시험 결과를 나타내는 그래프이다.
도 2는 중공구체 형태를 나타내는 미크로톰(microtom)에 의해 만들어진 입자 단면의 주사 전자 현미경 이미지이다.
도 3은 본 발명의 일 구현예에 따른 물질의 공정을 도시하는 도면이다.
도 4는 본 발명의 일 구현예의 공정 흐름 블록도이다.
도 5는 본 발명의 구현예를 수행하는데 사용될 수 있는 "역화(back flame)" 분무 열분해 반응기를 도시하는 개략도이다.
도 6은 900℃에서 어닐링 후 슬러리 분무 열분해를 이용하여 만들어진 0.5Li2MnO3·0.5LiNi0.333Mn0.333Co0.333O2의 생성 분말의 주사 전자 현미경 이미지를 포함한다.
도 7은 수지 내 내포된 900℃에서 슬러리 분무 열분해 어닐링를 이용하여 만들어진 0.5Li2MnO3·0.5LiNi0.333Mn0.333Co0.333O2의 생성 분말의 단면의 주사 전자 현미경 이미지이다.
도 8은 2012-12-14 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 사이클 시험 결과를 나타내는 그래프이다.
도 9는 2012-12-14 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 속도 능력 시험 결과를 나타내는 그래프이다.
도 10은 2013-02-06 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 사이클 시험 결과를 나타내는 그래프이다.
도 11은 2013-02-06 배치로부터 반전지 성능 대 슬러리 생성물의 리튬 애노드를 속도 능력 시험 결과를 나타내는 그래프이다.
A.
슬러리
분무 열분해를 이용하여 제조된 입자
본 발명은 슬러리의 분무 열분해를 통해 분말을 생성하는 방법 및 그 결과로 생성된 분말에 관한 것이다. 본원에서 사용된, 용어 "분무 열분해(spray pyrolysis)"는 기본적으로 물질을 포함하는 액체 내 하나 또는 그 이상의 화합물의 열분해와 함께 물질을 포함하는 액체를 분무하는 단계를 포함하는 물질 제조 방법을 포함하도록 한다. 예로서, 용어 분무 열분해는 흔히 분무 건조 설비로 지칭되는 설비를 활용하는, 상대적으로 낮은 온도(예를 들어, 450℃ 또는 그 미만)에서 일어나는 공정을 포함할 수 있다. 유사하게, 분무 열분해는 또한 분무 배소(spray roasting)로 지칭되는 공정을 포함할 수 있다.
1. 비-중공 생성물 입자
유리하게도, 본 발명의 슬러리 분무 열분해 방법은 비-중공, 다공성 입자 또는 분말을 제조하는데 사용될 수 있다. 상대적으로 작은 비-중공 입자가 제조될 수 있지만, 이의 특정 이점은 크기가 상대적으로 큰(예를 들어, > 약 1 미크론) 비-중공 입자를 제조하는 능력이다. 상기에 개시된 바와 같이, 중공 형태는 특히 약 1 미크론을 초과하여 입자 크기가 증가하는 것처럼 종래의 분무 열분해 기술을 이용해 만들어진 입자/분말의 흔한 특성이다. 중공 형태를 가진 입자의 SEM 이미지는 도 1 및 2에서 제공된다. 도 1에서 움푹 들어간 구는 중공 입자의 전형적인 형태이며, 도 2의 미크로톰은 중공 내부를 나타낸다. 반면, 도 6 및 7은 비-중공 형태를 가진 본 발명의 입자의 SEM 이미지이다. 본원에서 사용된 용어 "크기(size)"는 입자의 가장 큰 단면 치수를 의미한다. 따라서, 만일 입자가 구형이라면, 그 크기는 입자의 지름에 해당할 것이다.
생성물 입자(들)에 대한 용어 "중공도(hollowness)"는 입자의 중공 또는 비어있는 부위/공간/부피(종래에 다공성으로 간주되던 것을 제외하고)와 입자가 고체 입자인 것을 가정하고 입자의 총 부피 사이의 관계이다. 일반적으로, 입자는 중앙에 공극을 갖지 않는다면(즉, "쉘-유사(shell-like)" 형태) 비-중공이거나 또는 비-중공 형태를 갖는 것으로 간주되며, 또는 공극이 존재한다면, 공극은 입자 총 부피의 10% 미만을 구성한다. 본 발명의 특정 구현예에서, 공정은 약 60%, 약 40%, 약 20%, 약 10%, 약 5%, 약 2%, 또는 약 1% 미만인 중공도를 갖는 입자를 생성하도록 조절된다.
입자 또는 상당수의 입자(즉, 분말 시료)의 중공도의 정도는 상기와 유사한 방법에 따라 결정될 수 있다. 구체적으로, 입자 또는 분말 시료는 수지, 미크로톰으로 잘린 단면, 및 SEM/TEM 현미경으로 관찰된 절단면에 내포될 수 있다. 입자는 만일 공극을 가진다면, 또는 분말인 경우, 입자의 거의 대부분(예를 들어, 입자의 75% 또는 그 이상)이 약 1.5 ㎛ 초과의 입자 크기(또는 평균 입자 크기를 갖는 입자)에 대하여 크기가 300 nm를 초과하는 공극을 갖는다면, 중공인 것으로 간주될 수 있다(예를 들어, 도 2 참고).
분말에 대하여 상기보다 빠르고 쉬운 입자의 중공도의 정도를 판단 및/또는 근사치를 내기 위한 방법을 활용하는 것이 바람직할 수 있다. 특히, 분말을 만드는 입자의 중공도는 물질의 탭(tap) 또는 부피 밀도와 같은 분말의 특정 거시적 특성에 영향을 미치므로 매우 중요할 수 있다. 물질의 부피 밀도는 이차 입자 크기, 일차 입자 크기, 계면 화학 및 표면 형태와 같은 다른 다양한 물리적 및 화학적 특성에 영향을 받는다고 이. 그럼에도 불구하고, 중공도가 부피 밀도에 매우 상당히 영향을 미치며 어떠한 다른 특징의 영향은 무시될 수 있다고 믿어지고 있다. 따라서, 일인은 중공 입자를 포함하는 특정 조성물의 분말에 대한 부피 밀도 또는 부피 밀도의 범위를 경험적으로 결정할 수 있으며 비-중공인 본 발명의 입자의 그것과 비교할 수 있다. 예를 들어, 중공 입자 형태의 xLi2MnO3·(1-x)LiMn0.33Ni0.33Co0.33O2가 약 0.4 내지 약 0.6 g/cm3 범위의 탭 밀도(tap density)를 갖는다는 것이 결정될 수 있다. 따라서, 만일 이러한 조성물의 분말의 탭 밀도가 임의의 추가적 사후-분무 열분해 공정(예를 들어, 연삭(grinding), 제트 분쇄(jet milling), 압축(pressing)) 없이 약 0.6 g/cm3을 초과한다면, 이는 거의 대부분의 입자가 비-중공 형태를 갖는 분말로 간주된다.
명확하게 하기 위하여, 만일 입자 또는 분말이 여기에 명시된 방법 중 어느 하나를 이용하여 중공인 것으로 결정되었다면, 이는 중공인 것이거나 또는 중공 형태를 갖는 것으로 간주되어야 한다.
2. 다공성 생성물 입자
상기에 나타낸 바와 같이, 또한 비-중공인 것 또는 조절된 또는 감소된 양의 중공도를 갖는 것뿐만 아니라, 본 발명의 입자는 다공성인 것으로 간주될 수 있고, 일반적으로 다공성인 것으로 간주되도록 하는 방식으로 제조된다. 명확하게 하기 위하여, 본 발명의 공정은 비-다공성인, 비-중공 또는 조절된 또는 감소된 중공도를 제조하도록 수행될 수 있다(예를 들어, 그 중에서도, 특정 조성물을 선택함으로써). 다공성은 중공도와 구별된다. 용어 "다공성(porosity)"은 입자 내에서 발견되는 구별가능한 기공 크기를 말한다. 기공 크기 분포는 입자 내 공극 또는 기공의 빈도의 확률 밀도 함수로서 나타내었으며, 대부분의 기공은 가우시안(Gaussian) 유형 평균 기공 크기를 중심으로 할 것이다. 따라서, 만일 입자(들)이 중공이라면 판단하기 위한 또다른 방법은 하나 또는 그 이상의 평균 기공 크기보다 명백하게 큰 공극(예를 들어, 공극 > 2σ 더 큰)이 존재하는지 여부로 판단하는 것이다. 예로서, xLi2MnO3·(1-x)LiMn0.33Ni0.33Co0.33O2 물질 내 평균 입자 내 기공의 공극의 크기는 일반적으로 약 50 nm 내지 약 150 nm의 범위 내이다. 따라서, 만일 평균보다 상당히 더 큰(예를 들어, 평균 기공 크기보다 50 nm 더 큰) 입자 내 공극의 크기가 있다면, 이는 입자(들)이 중공임을 나타내는 것이다. 공극의 크기 분포는 SEM 이미지 또는 BET 기공 크기 분포 측정을 이용하여 측정할 수 있다.
특정 구현예에서, 입자 내 기공 구조는 나노기공(2 nm 미만), 메조기공(2 nm 및 50 nm 사이), 및 매크로기공(50 nm 초과)을 포함한다. 입자 내 기공 공간(일차 입자 사이의 공간, 하기 참조)은 몇 나노미터(예를 들어, 2 nm)에서 수십 나노미터(예를 들어, 100 nm)의 범위 내이며 다공성은 입자 내에 균일하게 분포된다. 이 유형의 다공성은 "메조다공성"이라 할 수 있다.
3. 이차 입자 및 일차 입자
일부 구현예에서, 생성물 입자는 더 큰(미크론-규모) "이차" 입자(즉, 생성물 입자)를 형성하기 위해 단단하게 서로 연결된 더 작은(서브-미크론) "일차" 입자로 만들어진다. 유리하게도, 비-중공 생성물 또는 이차 입자를 제조하기 위한 이 방법은 더 낮은 작동 온도를 허용하며, 이는 생성물 입자의 하나 이상의 구성 성분 또는 화합물의 녹는점을 초과하는 온도를 활용하는 것보다 더 나은 상 및 일차 입자 크기 조절을 허용한다(상기에, 이전에 공지된 바와 같이). 물질이 오직 전구체 분해에 충분한 온도를 필요로 하므로 더 낮은 작동 온도가 사용될 수 있다. 예를 들어, 공정은 일차 입자의 크기가 약 1 나노미터 내지 약 2 마이크로미터 범위 내이고 이차 입자의 크기가 약 10 nm 내지 약 100 ㎛의 범위 내이도록 조절될 수 있다(예를 들어, 도 2 참조). 또한, 공정은 일차 입자의 평균 크기가 약 1 nm 내지 약 500 nm의 범위 내이고 이차 입자의 평균 크기가 서브미크론(예를 들어, 약 0.1 ㎛) 내지 미크론(예를 들어, 20 ㎛)의 범위 내이도록 조절될 수 있다. 또다른 구현예에서, 일차 입자의 평균 크기는 500 nm 내지 약 2 ㎛의 범위 내이며 이차 입자의 평균 크기는 약 1 ㎛ 내지 약 100 ㎛의 범위 내이다. 또한, 공정은 이차 입자 크기에 대한 평균 값의 표준 편차가 0.5 내지 약 10 ㎛의 범위 내가 되도록 조절될 수 있다.
D. 슬러리 분무 열분해 방법
도 3 및 4를 참조하여, 본 발명의 방법은 하기를 포함한다: 슬러리를 액적으로 에어로졸화하는 단계, 여기서 슬러리는 전구체 용액 내 고체 입자를 포함하며, 액적으로부터 용매(들)를 증발하는 단계, 및 생성물 입자를 형성하기 위한 전구체 화합물을 열분해 생성물로 분해하기 위하여 건조된 액적을 소성하는 단계. 입자의 형성시 이들은 일반적으로 열분해 기체 스트림으로부터 수거된다.
1.
슬러리
제조
공정시 사용되는 슬러리는 전구체 액체 또는 전구체 용액 내 고체 입자를 포함하며, 여기서 전구체 액체 또는 용액은 열분해 공정 동안 분해될 하나 이상의 전구체 화합물을 함유한다. 본원에서 사용된 용어 "슬러리(slurry)"는 액체 내 입자가 안정한 및/또는 진한 또는 점성의 현탁액이거나 이를 형성하는 것을 의미하나, 그것은 다른 것을 제외하는 것을 의도하지 않는다. 슬러리 또는 입자-액체 혼합물 또는 현탁액은 안정하거나(즉, 이는 교반 없이 중력의 영향 하에서 침전되지 않는 경향이 있다) 또는 안정하지 않을 수 있다(즉, 이는 교반 없이 중력의 영향 하에서 침전되는 경향이 있다). 용어 "전구체 액체(precursor liquid)"는 전구체 화합물 자체가 액체이고, 액체 용매 내에 용해된 고체가 아닐 때 슬러리 성분을 구별하기 위하여 본원에서 사용된다.
a. 고체상 입자
슬러리는 액체 전구체 또는 전구체 용액 내 고체상 입자를 포함하며, 여기서 액체 부분은 분무 열분해시 분해될 전구체 화합물을 포함한다. 본원에서 사용된 용어 "시드 입자(seed particles)" 및 "고체상 입자(solid-phase particles)"는 전구체 액체 또는 전구체 용액 또는 슬러리 또는 현탁액을 제조하는 임의의 다른 액체에 추가된 입자를 말한다. 상기 입자는 일반적으로 고체로 간주되는 것, 일반적으로 중공으로 간주되는 것, 또는 고체 및 중공 입자의 조합일 수 있다. 명확하게 하기 위하여, 고체상 또는 시드 입자에 대한 상기 용어 "고체(solid)" 및 "중공(hollow)"의 사용은 입자의 다공성을 설명하는 것으로 의도되지 않는다. 그러나, 만일 중공 입자가 사용된다면, 생성된 입자가 60%, 약 40%, 약 20%, 약 10%, 약 5%, 약 2%, 또는 약 1% 미만이도록 이들의 양 및/또는 중공도 및/또는 공정이 조절되는 것이 선호된다. 또한, 수식어 "시드(seed)"는 입자가 공정 내 임의의 시점에 핵생성을 촉진하도록 작용하는 것을 의미하나 다른 것을 제외하지 않는다.
고체상 입자는 액체 전구체의 그것과 동일한 또는 다른 조성을 가질 수 있다. 특정 구현예에서, 고체상 입자의 장점은 이들이, 특히 상대적으로 좁은 크기 분포(예를 들어, 250 nm의 표준편차)를 갖는 2 ㎛ 미만인 평균 이차 입자 크기를 갖는 생성물 입자에 대하여, 입자 내 공극을 채우는 경향이 있다는 것이다. 일반적으로 이들은 시드 핵(seeding nuclei)으로서 작용하지 않기 때문에, 일반적으로 고체상 입자가 특정 또는 선호되는 형태 또는 결정형을 갖는 것이 필요하지 않다. 이와 같이, 핵생성 기능이 요구되지 않는 한, 고체상 입자는 임의의 결정학적 구조를 가질 수 있다. 고체상 입자는 분무 열분해를 포함하는 임의의 적합한 방법(들)에 따라 제조될 수 있으며, 바람직한 경우, 바람직한 평균 크기 및/또는 크기 분포를 얻기 위한 분쇄(milling) 또는 연삭(grinding) 및/또는 선별(screening)과 같은 다양한 공정 작업을 실시할 수 있다. 상기에 나타낸 바와 같이, 만일 분말의 부피 밀도를 증가시키기 위해 필요한 경우, 일반적으로 입자 내 공극을 채우는 것을 용이하게 하기 위하여 고체상 입자가 생성물 입자의 이차 입자의 대략적인 평균 크기 미만인 평균 크기를 가지도록 하는 것이 도움이 될 수 있다.
예시적인 고체상 입자는 하기를 포함한다: 실리콘 나노입자; 티타늄 나노입자; 리튬 전이 금속 산화물(예를 들어, 리튬, 니켈, 망간의 코발트 산화물); 및 탄소. 더욱 일반적으로, 고체상 입자는 본 발명의 방법에 적용할 수 있는 온도(들)(예를 들어 실온 내지 약 1500℃)에서 고체인, 산화물(예를 들어, 인광물질인 Y3Al5O12, Y2O3, Gd2O3; Y-Ba-Cu-O, Bi-Sr-Ca-Cu-O, Ba-Ca-Ti-O와 같은 체계 내 산화 조성물; 및 ZrO2, SrTiO3; Ba0 .86Ca0 .14TiO3; Al2O3; Fe2O3; Ta2O5; La2O3; Y2O3; CeO2; Sm2O3; TiO2; Ba2O3; CuO; MgO; NiO; Mn3O4; SnO2; V2O5; PdO; PbO2, 및 Co3O4와 같은 다양한 산화물); 인산염(phosphates); 질화물(nitrides)(예를 들어, BN); 할로겐화물(halides), 및 금속(예를 들어, Ag, Cu, Ni)과 같은 임의의 금속 또는 비금속 고체 물질 또는 화합물을 포함할 수 있다.
b. 전구체 용액
전구체 용액에서, 고체 전구체 화합물은 용매 내에 용해되거나 현탁된다. 용매 또는 용매 혼합물은 물, 알코올(에탄올, 메탄올, 등), 및 이들의 혼합물을 포함하나, 이에 제한되지 않는다. 일 구현예에서, 전구체 화합물은 열분해 생성물로 분해되도록 선택되며 이는 슬러리 내 고체 입자로서 꽤 유사한 조성을 갖고, 균일한 화학적 조성의 생성물 분말을 생성한다. 또다른 구현예에서, 전구체 화합물은 슬러리 내 고체 입자로서 다른 조성을 갖는 열분해 생성물로 분해되도록 선택되며(즉, 원소 및/또는 화합물, 및/또는 다른 원소 및/또는 화합물의 상대적인 양의 측면에서) 이로써 비-균일한 화학적 조성을 갖는 생성물 분말(일반적으로 "코어-쉘(core-shell)" 입자라 한다)을 생성한다. 전구체 화합물의 예시는 하기를 포함하나, 이에 제한되지 않는다: 질산염 및 아세트산염. 하기는 더욱 구체적이지만 불완전한, 용매 내 용해되거나 현탁될 수 있는 예시적 전구체 화합물의 목록이다: 질산 리튬, 질산 니켈, 질산 망간, 질산 코발트, 질산 나트륨, 질산 알루미늄, 질산 칼슘, 질산 칼륨, 질산 루비듐, 질산 세슘, 질산 크롬, 질산 철, 염화 티타늄, 염화 주석, 질산 아연, 질산 카드뮴, 질산 구리, 질산 바륨, 수산화 나트륨, 브롬화 마그네슘, 아세트산 리튬, 아세트산 망간. 더욱 일반적으로, 전구체 화합물(들)은 임의의 금속 또는 비-금속 황산염, 탄산염, 수산화물, 인산염, 칼코겐화물, 할로겐화물, 규산염, 또는 용매 내 침전물 형성 없이 유기(양성자성 또는 비양성자성) 또는 무기 용매(예를 들어, 물, 에탄올, 아세톤, 테트라히드로퓨란, 벤젠, 톨루엔, 등.)에 용해될 수 있고 분산되지 않는 유기화합물일 수 있다. 특정 용매 내 특정 금속(예를 들어, 알루미늄)의 용해도는 수성 용액의 pH에 의존할 수 있다고 이해된다.
c. 예시적 균일한 조성 입자
균일한 조성 입자의 예시는 LixMOy, 여기서 M은 Al, Ni, Co, Mn, Mg, Fe, Cu, Zn, Cr, Ag, Ca, Na, K, In, Ga, Ge, V, Mo, Nb, Si, Ti, Zr로부터 선택되며 x 및 y는 포함된 금속의 산화수에 따른다; MnuOv 및 CouOv, 여기서 u 및 v는 Mn의 산화수에 따른다,를 포함하나 이에 제한되지 않는다. 보다 구체적으로, 현재 발명의 적용을 이에 제한되지 않는, 추가적 예시는 하기를 포함한다: LiFePO4; LiMn1/3Ni1/3Co1/3O2; zLi2MnO3·(1-z)LiNi1/3Mn1/3Co1/3O2(여기서 z=0-1); zLi2MnO3·(1-z)LiNi1/2Mn1/2O2(여기서 z=0-1); Li4Ti5O12; LiMnO2; LiNi0.5Mn1.5O4; Li2MnO3; LiNiPO4. 더욱 일반적으로, 생성물 입자는 하기를 포함할 수 있다,
임의의 금속 또는 비-금속 고체 물질 또는 산화물(예를 들어, 인광물질인 Y3Al5O12, Y2O3, Gd2O3; Y-Ba-Cu-O, Bi-Sr-Ca-Cu-O, Ba-Ca-Ti-O와 같은 체계 내 산화 조성물; 및 ZrO2, SrTiO3; Ba0 .86Ca0 .14TiO3; Al2O3; Fe2O3; Ta2O5; La2O3; Y2O3; CeO2; Sm2O3; TiO2; Ba2O3; CuO; MgO; NiO; Mn3O4; SnO2; V2O5; PdO; PbO2, 및 Co3O4와 같은 다양한 다른 산화물); 인산염; 질산염(예를 들어, BN); 할로겐화물, 및 금속(예를 들어, Ag, Cu, Ni)과 같은 화합물.
일 구현예에서, 고체상 입자 및 전구체 용액은 균일한 조성의 리튬 삽입 금속 산화물을 제조하도록 선택된다. 보다 구체적으로, 상기 물질은 리튬-함유 금속 산화물을 포함하며, 이는 미국 특허 출원 공개 번호 2009/0297947, Deng 외, "Nano-sized Structured Layered Positive Electrode Materials to Enable High Energy Density and High Rate Capability Lithium Batteries"에서 개시된 일반 화학식ㅡLi1 +α(NixCoyMnz)1- tMtO2 - dRd에 따라 설명될 수 있고, 여기서 M은 Al, Mg, Fe, Cu, Zn, Cr, Ag, Ca, Na, K, In, Ga, Ge, V, Mo, Nb, Si, Ti, Zr, 또는 이들의 2 이상의 혼합물로부터 선택되며, R은 F, Cl, Br, I, H, S, N, 또는 이들의 2 이상의 혼합물로부터 선택되고, 0 ≤α≤ 0.50; 0 < x ≤ 1; 0 ≤ y ≤ 1; 0 < z ≤ 1; 0 ≤ t ≤ 1; 및 0 ≤ d ≤ 0.5이다. 일 구현예에서, M은 Al, Mg, Fe, Cu, Zn, Cr, Ag, Ca, Na, K, Si, Ti, V, 및 이들의 조합으로 구성되는 군으로부터 선택되고, R은 F, Cl, Br, I, 및 이들의 조합으로 구성되는 군으로부터 선택된다. 불소는 순환 안정성(cycling stability)에 기여할 수 있는 도펀트로 보고되어 있다. 또다른 구현예에서, 상기 화학식이 Li1 +αNixMnzO2로 감소되도록 t=0, y=0, 및 d=0이며, 여기서 0 ≤ α ≤ 0.2, 0.1 ≤ x ≤ 0.6, 0.2 ≤ z ≤ 0.6이다. 또다른 구현예에서, 상기 화학식이 Li1 +αNixCoyMnzO2로 감소되도록 t = 0 및 d = 0이며, 여기서 0 ≤ α ≤ 0.2, 0.1 ≤ x ≤ 0.6, 0.1 ≤ y ≤ 0.6, 0.2 ≤ z ≤ 0.6이다.
본 발명의 일부 구현예에서 금속 산화물 조성은 복합 결정 구조를 가질 수 있다. 복합 결정 구조를 갖는 금속 산화물은 두개의 성분 화학식 xLi2MO3·(1-x)LiM'O2에 의해 나타낼 수 있으며, 여기서: M은 +4의 평균 산화수를 갖는 하나 또는 그 이상의 금속 이온이고, M'는 +3의 평균 산화수를 갖는 하나 또는 그 이상의 금속 이온이며, 0 ≤ x ≤ 1이다. 본 발명의 구현예에서, M은 Mn이고 M'는 Mn, Ni, Co, Cr, 및 이들의 조합으로 구성된 군으로부터 선택된다. 또다른 구현예에서, M은 Mn이고 M'는 Mn 및 Ni 중 하나 이상을 포함한다. 또다른 구현예에서, M은 Mn이고 M'는 Mn 및 Ni이다. 또다른 구현예에서, M은 Mn이고 M'는 Mn, Ni, 및 Co이다. 구체적인 예는 xLi2MnO3·(1-x)LiMn0.5Ni0.5O2, xLi2MnO3·(1-x)LiCoO2, 및 xLi2MnO3·(1-x)LiMn1/3Ni1/3Co1/3O2를 포함한다. 추가 구현예에서, 임의의 상기 화학식에 대하여 x는 하기 범위 0.3 ≤ x ≤ 0.7 내일 수 있다.
금속 산화물 조성의 선택뿐만 아니라, 본 발명의 공정은 본 발명의 금속 산화물의 결정 구조에 영향을 미치도록 조절될 수 있다. 예를 들어, 공정은 조절될 수 있으며 상기 조성은 금속 산화물이 층상-층상 조성 복합 결정 구조를 갖도록 선택된다. 사실상, 현재까지 실험 결과는 층상-층상 구조를 갖는 금속 산화물이 용량 및 가역성(cyclability)의 바람직한 조합을 갖는다고 제시한다. 예를 들어, 높은 온도에서 합성된 Li[Li(1/3-2a/3)NiaMn(2/3-a/3)]O2 (0 < a < ½)가 1/10C만큼 높은 현재 밀도에서 200 mAhg-1 넘게 전달하였으며 여기서 1C = 250 mAg-1이다.
d. 예시적 코어-쉘 입자
이러한 비-균일한 조성 입자의 예시는 유리-금속(glass-metal) 나노복합재료 입자(예를 들어, 일본 특허번호 JP 2005001978 참조) 및 구형(spheroidal) 탄소-코팅된 실리콘 나노 복합 재료 입자(예를 들어, "Highly Reversible Lithium Storage in Spheroidal Carbon-Coated Silicon Nanocomposites as Anodes for Lithium-Ion Batteries," See-How Ng, Jiazhao Wang, David Wexler, Konstantin Konstantinov, Zai-Ping Guo, and Hua-Kun Liu, Angew. Chem. Int. Ed., 45, 6896-6899 (2006) 참조)를 포함한다.
e. 고체상 및 전구체 사이의 화학 반응
또다른 구현예에서, 슬러리는 분무 열분해 공정 중 고체상 입자 및 전구체 용액 또는 화합물 사이에서 화학반응이 발생하도록 선택된 것 중 최소한 일부의 고체상 입자 및 전구체 화합물을 함유한다. 이 화학 반응은 고체상 입자 및 전구체 용액의 분해 생성물 모두와 다른 조성을 갖는 최종 생성물을 생산한다(만일 분리하여 분해된 경우). 이 유형의 열분해는 반응물 중 하나가 용액 내에서 불용성인 경우 생성 조성물을 합성하는데 사용된다. "Spray pyrolysis method for in situ production of graphene oxide based composites," Konstantinov, International publication No. WO 2012/155196 A1; "Preparation of ultrafine barium titanate powder by slurry spray pyrolysis," Jonk Ho Lee, Kang Heon Hur, and Jung Soo Lee, Journal of the Korean Ceramic Society, Vol. 46, No. 2, pp. 137-145 (2009).
f.
슬러리
내 고체상 입자의 질량비
슬러리 내 고체상 입자의 질량비는 일반적으로 형태, 일차 입자 크기, 생성물 입자의 충전 밀도에 영향을 미친다. 이 질량비는 하기 식에 따라 계산될 수 있다:
M
sp
=M
ss
/(M
ss
+
V
p
·ρ
p
·A)
여기서 M sp 는 생성물 질량에 대한 슬러리 내 고체상 입자의 질량비이고, M ss 는 슬러리에 넣은 고체상 입자의 질량이고, V p 는 슬러리를 제조하기 위해 사용되는 전구체 용액의 부피이고, ρ p 는 상기 전구체 용액의 밀도이며, A는 전구체 용액에서 충분히 분해된 물질로의 질량 환산 계수이다. 만일 전구체가 열분해 공정 중 충분히 분해되지 않는다면, 분해의 정도는 A의 값에 대해 설명할 필요가 있다. 만일 슬러리 내 고체상 입자가 열분해 상 중 이들의 질량 비율만큼을 잃는다면(예를 들어, 만일 슬러리 내 고체상 입자가 오직 부분적으로 분해될 때 첨가되고 그 후 슬러리의 분무 열분해 중 더 분해된다면) 추가적 계산이 필요하다. 이 특정 경우에 대하여 상기 식은 하기와 같이 변경될 수 있다:
M
sp
=M
ss
·A'/(M
ss
·A'+
V
p
·ρ
p
·A)
여기서 A'는 개별 생성물 및 슬러리에 첨가된 고체 입자에 기반하여 추정된다. 부분적으로 분해된 시료에 대하여 A'는 1 미만인 반면, 충분히 분해된 고체 시드 입자에 대하여 A'=1이다.
예를 들어, 형태는 생성물 분말의 총 칠량에 대한 슬러리 내 고체상 입자의 질량의 비율(즉, "질량비")이 증가하는 만큼 중공구체에서 비-중공 구체로, 비-구형의 응집체로 변화할 수 있다. 예를 들어, 전구체 화합물, 용매, 에어로졸 가열 프로파일, 체류 시간, 및 특정 무화(atomization) 장치를 포함하는 다양한 기타 요인 또한 형태에 영향을 미칠 수 있다. 예를 들어, 전구체 조성물은 결정화도(crystallinity) 및 크기에 영향을 미침으로써 생성물에 영향을 미칠 것이다. 무화 장치는 또한 입자 형태에 상당히 영향을 미치는 경향이 있다. 구체적으로, 만일 무화기(atomizers)가 상대적으로 작은 액적(크기가 1 미크론 미만인)를 제조하기 위하여 선택된다면, 입자는 중공이 적은 경향이 있다. 반면 액적의 크기(1 미크론 초과)가 증가하는 만큼, 생성물 입자 내부 공극의 크기가 증가하는 경향이 있다. 따라서, 주어진 형태를 달성하기 위해 요구되는, 생성물 분말의 총 질량에 대한 슬러리 내 고체상 입자의 질량의 비율은 모든 공정 변화에 걸쳐 일정하지 않다.
구현예에서 n개의 개별 화합물 또는 화학적 혼합물(즉, n은 고체 및 하나 이상의 고체 성분을 갖는 액체 전구체 화합물의 수와 일치하며, 이는 고체상 내 또는 물 또는 유기 용매와 같은 용매 내에서 용해된 단일 화학 원소 또는 많은 화학 원소들을 포함할 수 있다)로 구성된 단일 또는 다중 성분 슬러리에 대하여, 고체 성분의 특정 최소 수준은 비-중공 형태를 갖는 입자를 제조하기 위하여 유지/추가되어야 한다. 단순화하기 위해, 논의를 두개-성분 혼합물, A 및 B로 제한하며, 이는 임의의 화학적 화합물일 수 있으나, 이 예시는 본 발명의 적용 및 성분의 수를 제한하는 것이 아니라고 이해된다. A는 현탁액 또는 고체 모두일 수 있으나 현재 예시에서 A는 용액 내에 있고 B는 고체이다. 이러한 혼합물에 대하여, 입자의 비-중공 내부 형태를 얻기 위해 필요한 최소의 고체 농도가 존재한다. 슬러리 내 최소의 고체 농도는 생성물 입자의 분말이 비-중공이거나 또는 비-중공 형태를 갖는 결과를 보장하기 위하여 필요하다고 믿어지고 있다. 일반적으로, 용액 기반 성분의 m의 수 및 고체상 성분의 p의 수에 대하여, 만약, 오직 ≥α라면, 화합물의 혼합물은 비-중공일 것이며, 여기서 x j 는 성분 j의 질량비이고, a는 경험적으로 얻은 비-중공 생성물 입자를 제조하기 위해 필요한 고체상 입자의 최소의 총 질량비를 나타내는 수이다. 예를 들어, xLi2MnO3·(1-x)LiMn0.33Ni0.33Co0.33O2에 대하여 a = 10 %이다. 균일한 조성 및 다중 성분 물질에 대하여도 이것은 사실이다. 하기 식은 시드 입자의 조성이 전구체 입자의 조성과 다른 경우 물질에 대한 조성을 판단하는데 사용될 수 있다. 혼합물 내 1 이상의 유형의 고체상 입자 및 1 이상의 유형의 전구체 성분을 갖는 것은 가능하며 하기 식은 이 가능성을 허용한다:
여기서 x h 는 각각의 액체 성분의 질량비이고, ρ i 는 액체 전구체의 밀도이고, V i 는 용매가 증발한 이후 액체 전구체 내 성분의 부피이고, m은 액체 성분의 수이고, p는 고체 성분의 수이고, m k 는 전구체 내 고체 성분의 질량이며 m h 및 m k 는 고체 및 액체 성분으로부터 유도된 생성물의 질량이다. 상기 식에 기반한 질량비는 하기와 같다:
만일 첨가된 시드 입자가 오직 부분적으로 분해되었다면, 상기에 나타낸 바와 같이 유사한 조정이 행해질 수 있다.
상기 식에 구체화하여,
여기서 A 및 B는 이원 혼합물(binary mixture) 내 각각의 성분이고, x 및 (1-x)는 각각의 질량비이며, 만일 이들이 최소 고체 비율 기준을 충족하지 못한다면 중공 형태로 이어질 것이다. 만일 최소 기준을 충족한다면, 충분한 양의 고체가 액적 내에 제공되어, 일부 중공 쉘이 형성될지라도, 충분한 고체 입자가 형성될 것이며 이로써 최종 생성물이 비-중공으로 간주될 것이다. m A 및 m B 의 비율은 생성물의 내부 중공 또는 비-중공 형태에 관계 없이 최종 생성물의 조성을 정의한다. 고체상 입자의 총 질량비, a는 약 2% 만큼 작을 수 있으며 여전히 약 5% 이상을 갖는 비-중공 생성물 입자가 생성되는 것이 선호된다고 생각되어 진다. 유사하게, 75% 만큼 큰 고체상 입자의 총 질량비, a는 비-중공 생성물 입자를 제조하기 위해 사용될 수 있다. 특정 구현예에서, 고체상 입자의 총 질량비는 약 70%, 65%, 60%, 55%, 또는 50%만큼 크다. 그렇긴 하지만, 현재까지 실험 결과는 슬러리 내 고체상 입자의 총 질량비가 약 10% 및 약 70% 사이가 되도록 선택하는 것이, 조성이 균일 또는 비-균일한지 또는 다중 조성을 갖는지 여부와 관계없는 것을 포함하여 어떤 조성이 생성되는지 여부와 관계없이 일관되게 비-중공 형태(즉, a ≒ 10-70%)를 갖는 입자로 이어질 것이라 이해된다. 또다른 구현예에서, 고체상 입자의 총 질량비는 약 20% 및 약 60%(즉, a ≒ 20-60%) 사이가 되도록 선택된다.
본 발명의 일 구현예에서, 고체 입자는 0.5Li2MnO3·0.5LiNi0.333Mn0.333Co0.333O2 의 혼합된 금속 산화물이고 전구체 용액 내 전구체 화합물은 물에 용해된 질산 리튬, 질산 니켈, 질산 망간, 및 질산 코발트이다. 전구체 화합물의 비율은 이들의 열분해 생성물이 고체 입자로서 동일한 화학 조성을 갖도록 하며, 단일 화학 조성을 갖는 최종 생성물 분말(0.5Li2MnO3·0.5LiNi0.333Mn0.333 Co0.333O2)을 생성한다. 슬러리 내 고체 입자의 질량은 최종 생성물에 대한 고체상 입자의 질량비가 약 0.5가 되도록 선택되었다.
2.
슬러리의
액적으로의
에어로졸화
슬러리는 캐리어 기체(carrier gas)에 현탁된 슬러리 혼합물을 포함하는 액적을 제조하기 위해 에어로졸화된다. 많은 에어로졸화 방법/설비가 사용될 수 있으며, 하기를 포함하나 이에 제한되지 않는다: 이-유체 노즐(two-fluid nozzles), 초음파 분무기(ultrasonic nebulizers), 회전 무화기(rotary atomizers) 및 고압 노즐(high-pressure nozzles). 많은 캐리어 기체가 사용될 수 있으며, 화학적 특성 또는 생성되는 물질에 의존한다. 캐리어 기체는 하기를 포함하나 이에 제한되지 않는다: 공기(air), 아르곤(argon), 질소(nitrogen), 및 공기 및 연소 생성물(combustion products)의 혼합물.
본 발명의 일 구현예에서, 슬러리는 이-유체 노즐을 이용하여 에어로졸화된다. 슬러리는 노즐로 압송(pressure-fed)된 후 고속 기류에 의해 에어로졸화된다. 액적은 공기 및 연소 생성물의 혼합물을 포함하는 가열된 캐리어 기체로 분무된다.
3.
액적으로부터
용매(들)의 증발
슬러리의 액적으로부터 전구체 용액의 용매 또는 용매의 혼합물을 증발시키며, 고체 입자 및 전구체 화합물로 구성되는 액적 또는 입자(전구체 화합물의 상에 의존하며 이후 "액적(droplet)"이라 함)을 생성한다. 명확하게 하기 위하여, 전구체 액체(상기에 설명한 바와 같이 전구체 용액과 구별되는)를 포함하는 구현예에서, 용매는 이 단계에서 전개(evolved)되지 않는다.
본 발명의 일 구현예에서, 물은 고온의 기류로 분무시 슬러리 액적으로부터 증발하며, 간단히 질산 금속염(질산 리튬, 질산 니켈, 질산 망간, 및 질산 코발트)에 의해 결합된 혼합된-금속 산화물의 입자를 생성한다.
4. 열분해 생성물로 전구체 화합물의 분해
전구체 화합물을 열분해 생성물로 분해(열분해)를 유도하기에 충분한 온도로 액적을 가열하였다. 요구되는 온도 및 온도의 지속 시간은 사용되는 전구체 물질과 전구체 분해의 원하는 수준에 따라 달라질 것이다. 일부 슬러리 및 온도 프로파일에 있어서, 증발 및 분해는 매우 긴밀하게 진행될 것이므로 공정-관리 관점에서 단일 단계로 처리될 수 있다. 열분해를 촉진시키기 위한 가열은 당업자에게 명백한 많은 수단에 의해 제공될 수 있으며, 하기를 포함하나 이에 제한되지 않는다: 1) 액적에 도달하기 전, "역화(back flame)"의 생성물과 함께 캐리어 기체를 가열, 여기서 화염(flame)이 에어로졸의 제조시 공정 내 상류가 되도록, 캐리어 기체/연소 생성물 혼합물 (일반적으로 간단히 "캐리어 기체"라 함)이 에어로졸에 도달하기 전 화염의 고온의 연소 생성물을 캐리어 기체와 혼합한다; 2) 액적에 도달하기 전 열 교환기 내 캐리어 기체 또는 이들의 변형을 가열(예를 들어, 고온-벽 반응기를 통해 에어로졸을 이동); 3) 에어로졸화한 후 측화(side flames) 또는 가열된 기체로 액적을 가열(예를 들어, 알코올이 전구체 용액 내 용매로서 사용된 경우 슬러리 분무를 연소); 및/또는 4) 화염을 통해 에어로졸을 통과.
본 발명의 일 구현예에서, 역화(back flame)는 노즐 주위 공간에 도달하기 전 공기를 가열하기 위해 사용된다. 역화에서, 정적 혼합기(static mixers)(노즐의 상류)는 노즐을 통과하는 가열된 캐리어 기체를 제공하기 위해 공기 및 연소 생성물을 혼합한다. 슬러리 액적의 에어로졸은 이 고온의 캐리어 기체로 분무되며, 용매가 증발되고 전구체의 질산 금속염이 새롭게 혼합된-금속 산화물을 형성하기 위해 충분히 또는 부분적으로 분해된다. 새로운 산화물은 슬러리의 산화물의 고체 입자 사이 및 주변에 형성되고, 균일한 화학적 조성을 갖는 다공성, 비-중공 물질을 생성하기 위해 공극을 채운다. 특정 구현예에서, 생성물 분말은 0.5Li2MnO3·0.5LiNi0.333Mn0.333Co0.333O2로 구성된다.
또다른 구현예에서, 공기-과잉 가열기(burner)(예를 들어, Eclipse ThermJet Burners Model TJ0200)는 공정시 열원(heat source)으로서 사용될 수 있다. 공기-과잉 가열기는 온도 유연성을 가진 고속 화염을 제공한다. 특히, 연로로서 프로판의 사용은 화염을, 예를 들어, 400 % 과잉 공기에서 600℃의 표적 온도에 도달하도록 한다.
또한, 전체 분무 열분해 시스템은 증발 및 분해를 조절하기 위해 열 관리를 위한 성분 또는 설비를 포함할 수 있다. 예를 들어, 하나는 냉각수 코일 및 세라믹 절연 물질 및 주위 허니콤(honeycomb)을 사용할 수 있으며, 이로써 액적이 균일한 열 흐름 하에 증발 및 분해될 것이다.
5. 기체
스트림으로부터
생성물 입자의 수거
생성물 입자는 임의의 적절한 방법에 의해 캐리어 기체로부터 수거된다. 본 발명의 일 구현예에서, 여과 집진 필터(bag house filter)는 기체 스트림으로부터 생성물을 분리하는데 사용된다. 분말 수거 방법에 있어서 당업자들은 입자를 수거하기 위해 사이클론(cyclones) 또는 다른 공기-입자 분리 장치와 같은 기구를 사용할 수 있음이 이해된다.
D. 분무 열분해 장치 구현예
분무 열분해 장치의 일 구현예는 도 5에서 도시된다. 상기 장치는 4개의 구획을 포함한다. 맨 아래 구획은 가로질러 대략 18 인치(45 cm)로 측정되며, 여기서 열은 장치의 맨 아래에 있는 서로 반대편에 인접하여 위치한 두개의 공기-프로판 가열기에 의해 생성된다. 이 구획의 예로서, 기류는 시스템 벽에 부착된 세라믹 블록에 의해 혼합되며 균일한 기체 온도를 형성하기 위한 정적 혼합기로서의 역할을 한다. 이 구획의 중심을 통과하는 노즐 집합체에 있어 재료 투입 튜브(Feed tubes)는 3-인치 지름의 세라믹 튜브, 여러 층의 절연, 및 공기-냉각 퍼지(purge)에 의해 가열된 환경으로부터 보호된다. 제1 구획의 열린 단면 구획은 연돌 효과(stack effect)를 활용하여 분당 대략 60 입방피트의 기류를 허용하도록 설계된다. 제2 구획은 위쪽을 향하며 제1 구획에서 상승하는 기체의 높은 온도로부터 노즐을 보호하는 쉬라우드(shroud) 기류와 결합한 2개의 유체 노즐(Delavan siphon type SNA)을 특징으로 한다. 제3 구획은 대략 60 인치(152 cm) 길이로 측정되는 8 인치(20 cm) 지름 튜브이다. 에어로졸은 고온의 기체와 혼합되는 동안 물질 건조(용매의 증발) 및 분해가 발생하도록 이 구획을 통해 흐른다. 시스템의 마지막 구획은 생성물을 수거하고 응축을 방지하기 위해 대략 100℃에서 유지되는 여과 집진 필터이다. 필터의 주입구는 제3 구획 출구 위에 위치하나 연결되어 있지 않다. 여과 집진 필터는 여과막을 가로질러 압력 차를 생성하기 위해 분당 100 입방피트(2.8 m3/min)의 최대 유체 용량을 가진 송풍기(air blower)를 활용한다. 기체 온도는 제2 구획(노즐 높이에서) 내 및 제3 구획의 출구 내 유형 K 열전대(thermocouples)로 측정된다. 가열기에 대한 연료 유량은 구획 2 내 대략 600℃ 및 구획 3의 출구 내 400℃의 기체 온도를 만들기 위해 조정된다. 슬러리는 약간 가압된 삼각플라스크로부터 노즐로 공급된다.
실시예
슬러리의
제조시 사용하기 위한 분무 열분해에 의한 금속 산화물의 제조
2.5 mole L-1 전구체를 탈이온수 내 충분히 용해시킨 LiNO3, Mn(NO3)2·4H2O, Ni(NO3)2·6H2O, Co(NO3)2·6H2O에 의해 제조하였다. LiNO3, Mn(NO3)2, Ni(NO3)2 및 Co(NO3)2의 농도는 각각 1.5 mole L-1, 0.67 mole L-1, 0.17 mole L-1 및 0.17 mole L-1이었다.
금속 산화물(슬러리 내 고체상 입자로서 사용하기 위한)의 제조시, 전구체를 건조하기 위한 열을 생성하기 위해 화염을 활용하고 무화된 물질을 분해하는 분무 열분해 장치 내에서 분무하였다. 상기 장치는 4개의 구획을 포함한다. 맨 아래 구획은 대략 18 인치로 측정되며, 여기서 열은 위쪽을 향하는 6개의 공기-프로판 가열기에 의해 생성된다. 노즐에서 기체 및 액체를 베어링하는 재료 투입 튜브는 이 구획의 중심에 위치하며 여러 층의 절연에 의해 가열된 환경으로부터 보호된다. 이 구획의 맨 윗부분 12 인치가 구획 3의 좁은 끝부분에 연결되어 있는 콘(cone)에 의해 차폐되는 반면, 처음 6 인치는 대기에 열려있다. 제2 구획은 위쪽을 향하며 제1 구획에서 상승하는 기체의 높은 온도로부터 노즐을 보호하는 쉬라우드(shroud) 기류와 결합한 2개의 유체 노즐(Delavan siphon type SNA)을 특징으로 한다. 제조하는 동안, 쉬라우드를 연속 분무가 가능하도록 충분한 기류로 설정하고, 노즐 공기 압력을 9.5psi로 조정하였다. 제3 구획은 대략 36 인치 길이로 측정되는 4 인치 너비의 튜브이다. 에어로졸은 고온의 기체와 혼합되는 동안 물질 건조(용매의 증발) 및 분해가 발생하도록 이 구획을 통해 흐른다. 이 구획의 열린 단면 구획은 연돌 효과를 활용하여 분당 대략 60 입방피트의 기류를 허용한다. 시스템의 마지막 구획은 생성물을 수거하기 위한 여과 집진 필터이다. 이는 액체 응축을 방지하기 위해 대략 100℃에서 유지된다. 필터의 주입구는 제3 구획 출구 위에 위치하나 연결되어 있지 않다. 여과 집진 필터는 여과막을 가로질러 압력 차를 생성하기 위해 분당 100 입방피트의 최대 유체 용량을 가진 송풍기를 활용한다. 유량 온도는 제3 구획의 출구 내 유형 K 열전대로 측정하였다. 가열기에 대한 연료 유량은 구획 3 출구 내에 대략 415℃ 내지 445℃ 범위의 온도를 유지하도록 조정하였다. 전구체 용액을 약간 가압된 탱크로부터 노즐로 공급하고 유량은 유량계(flow meter)로 측정하였으며 니들 밸브(needle valve)를 이용하여 5sccm로 조정하였다.
체류 시간 및 온도를 조절함으로써, 본 발명자들은 분해 수준을 조절하고 최종 생성물의 특성(일차 입자 크기 및 기계적 특성을 포함)에 영향을 미칠 수 있다. 이 구획에서 설명된 방법에 의해 제조된 물질은 충분히 분해되지 않았다.
참조용으로 5 g 시료를 이 물질 밖으로 꺼내어 900℃에서 2시간 동안 어닐링하였다. 어닐링 후 시료의 무게는 3.13 g이었다. 시료를 메쉬(mesh) 수 70(212 미크론 구멍 크기)에서 걸렀다. 3.12 g의 걸러진 물질을 탭 밀도 분석기(Quantachrome instruments Autotap)로 분석하고 0.69 g/cc의 탭 밀도를 산출하였다.
대부분의 입자가 내부 중공을 갖는 구형인 이 물질의 SEM 이미지(SEM FEI Nova 2300 Field Emission)를 나타내었다(도 1 참조). 일부 입자는 깨지거나 및/또는 변형되었다.
슬러리 제조
추가적 공정 전 분해의 정도를 바람직한 수준으로 조정하기 위해, 80 g의 물질을 알루미나 도가니(alumina crucible)에 적재하고 열을 처리하였다. 물질을 45 분 안에 450℃까지 올리고, 30 분 동안 450℃에서 유지한 후 실온으로 다시 자연적으로 냉각하였다. 시료는 열처리 공정 중 이의 무게를 대략 10% 잃었다. 만일 물질이 이의 제조된 형태 자체가 이미 원하는 분해 수준이라면 열처리는 생략할 수 있다.
67 g의 열 처리된 물질을 막자 및 막자사발로 분쇄하였다. 상기 물질을 5개의 배치에서 배치당 대략 12 분 동안 분쇄하였다.
54 g의 분쇄된 물질을 상기 "금속 산화물의 제조" 구획에서 설명한 것과 동일한 조성의 270 ml의 전구체 용액과 혼합하였다. 슬러리는 고속 균질화 혼합기(homogenizing mixer)로 대략 1000 rpm에서 대략 3 분 동안 균질화 하였다. 슬러리로 넣을 고체 입자의 질량은 최종 생성물 내 기존 물질의 질량비가 0.65가 되도록 선택하였다.
슬러리의 분무 열분해
슬러리 물질은 원료 물질의 제조시 사용되는 것 및 실시예 1의 상기 "금속 산화물의 제조" 섹션에서 설명한 것과 유사한 분무 열분해 장치에서 제조하였으나, 하기와 같은 변화가 수반되었다: 슬러리는 자기 교반되는 삼각플라스크로부터 노즐로 공급하였다. 삼각플라스크 내 슬러리는 대략 20sccm의 평균 슬러리 공급 속도를 허용하는 공기 압력 하에서 유지하였다. 가열기에 대한 연료 유량은 구획 3의 출구 내 대략 400℃의 온도를 유지하기 위해 조정되었다.
5g 시료를 이 물질로부터 꺼내어 900℃에서 2시간 동안 어닐링하였다. 어닐링 후 시료의 무게는 3.07 g이었다. 시료를 메쉬(mesh) 수 70(212 미크론 구멍 크기)에서 걸렀다. 3.06 g의 걸러진 물질을 탭 밀도 분석기(Quantachrome instruments Autotap)로 분석하고 0.93 g/cc의 탭 밀도를 나타내었다.
또 다른 증명으로서, 이 어닐링된 물질의 부분은 어닐링 공정 중 발생할 수 있는 응집을 방해하기 위해 수압기(hydraulic press) 내에 1.57 g/cc의 퍽(puck) 밀도로 압축하였다. 다시 거른 후, 압축된 물질은 1.06 g/cc의 탭 밀도를 나타내었다. 이 어닐링되고 걸러진 물질의 SEM 이미지(SEM FEI Nova 2300 Field Emission)는 대부분의 입자의 모양이 구형이 아니지만 대략 등축성(equiaxed)을 나타내었다. 오직 소수의 입자만이 변형되거나 또는 중공인 임의의 표면 표시를 가지는 것으로 보였다. 입자는 종종 2 미크론을 초과하였다(도 6 참조).
생성물의 내부 구조를 분석하기 위하여, 입자를 에폭시계 수지(Ted Pella)에 넣었다. 다음날, Leica 초미크로톰(ultramicrotome)을 이용하여 건조 수지로부터 구획을 잘라냈다. 입자의 내부는 SEM(SEM FEI Nova 2300 Field Emission)으로 관찰하였다. 이들 이미지는 거의 대부분의 입자가 비-중공 내부 형태를 갖는다는 것을 확인하였다(도 7 참조).
전기화학 시험
캐소드(cathode) 필름 제조는 다른 곳에서 보고된 절차에 따라 수행하였다. "Spray Pyrolysis Synthesis of Mesoporous Lithium-Nickel-Manganese-Oxides for High Energy Li-Ion Batteries," X. Zhang, R. L. Axelbaum, J. Electrochem. Soc., 159 (6), A834 (2012). 캐소드 슬러리는 폴리비닐리덴 플로라이드(polyvinylidene fluoride, PVdF) 결합제 용액(Kureha Corp. Japan) 및 1-메틸-2-피롤리디논(1-Methyl-2-pyrrolidinone, NMP) 내 현탁된 Super-P 전도성 카본 블랙(carbon black)(Timcal)을 이용하여 제조하였다. 순수 리튬 애노드 및 2500 Celgard 상표 막(Celgard LLC)을 이용하여 전기화학 시험을 위한 반전지를 제조하였다. 전해질 용액은 에틸렌 카보네이트(ethylene carbonate)/에틸-메틸-카보네이트(ethyl-methyl-carbonate) 용액(EC:EMC = 3:7 중량비)(Tomiyama High Purity Chemicals, provided by Argonne National Laboratory) 내 1.2 M LiPF6 이었다.
분말의 전기화학적 성능은 아르곤-충진 글러브 박스(glove box)에서 제조된 2032-유형 코인 셀(coin cells)(Hohsen Corporation)에서 평가하였다. 사이클 시험 및 속도 능력 시험은 표 1에 나열된 절차에 따라 수행하였다. 사이클링 및 속도 능력 시험 모두 MTI-BST8-WA-유형 전지 시험기(battery tester)를 이용하여 수행하였다. 모든 전기화학 시험은 실온, 22 ℃에서 수행하였다. 사이클 시험 프로토콜의 결과는 도 8에 포함된다. 특히, 제1 방전(discharge)은 20 mAg-1의 속도로 방전될 때 254 mAh/g의 용량을 나타낸다. 66.67 mAg-1 방전율을 나타내는 제5 사이클은, 200 mAhg-1의 방전 용량을 가졌다. 사이클 시험 프로토콜의 결과는 도 9에 포함된다.
또한, 본 발명에서 설명된 방법을 이용하여 2013-02-06에 제조된 동일한 화학적 조성물의 캐소드 물질의 배치에 대한 예비 사이클링 및 속도 시험 데이터는 각각 도 10 및 11에 포함된다. 동일한 시험 프로토콜 하에서, 이들 물질은 300 mAh/g가 넘는 높은 초기 충전 용량 및 C/3(66.67 mAg-1) 속도에서 225 mAhg-1가 넘는 방전 용량을 나타낸다.
|
사이클 시험 프로토콜
(1C=200 mAhg -1 ) |
속도 능력 시험 프로토콜
(1C=200mAhg -1 ) |
|
| 활성화 | C/10 (20mAg-1)에서 1 사이클 2.0-4.8 V | C/10 (20mAg-1)에서 1 사이클 2.0-4.8V |
| 이후 사이클 |
C/10 (20mAg-1)에서 3 사이클 2.0-4.6 V C/3 (66.67mAg-1)에서 96 사이클 2.0-4.6 V |
C/10 (20mAg-1)에서 4 사이클 2.0-4.6V C/5 (40mAg-1)에서 10 사이클 2.0-4.6V C/2 (100mAg-1)에서 20 사이클 2.0-4.6V 1C (200mAg-1)에서 40 사이클 2.0-4.6V C/10 (20mAg-1)에서 25 사이클 2.0-4.6V |
본원에서 사용된, "약(about)"은 당업자에게 이해될 것이며, 그것이 사용되는 문맥에 따라 어느 정도 달라질 것이다. 만일 당업자에게 자명하지 않은 용어의 사용이 있다면, 사용된 문맥을 고려하여, "약(about)"은 특정 용어의 더하기 또는 빼기 10 %까지를 의미할 것이다.
논의된 모든 범위는 또한 모든 목적을 위해 그 안의 모든 하위 범위를 반드시 설명할 수 있고 설명하며, 모든 이러한 하위 범위는 본 발명의 일부이다. 임의의 나열된 범위는 충분히 설명되고 적어도 동일한 반쪽(예를 들어, 아래쪽 절반 및 위쪽 절반), 1/3, 1/4, 1/10, 등으로 나눠지는 동일한 범위가 가능한 것으로 쉽게 인식될 수 있다.
본 발명의 원리를 도시하고 설명하였으나, 본 발명이 이러한 원리로부터 벗어나지 않는 방식 및 세부사항에서 변경될 수 있다는 것은 당업자에게 명백할 것이다.
본 발명의 물질 및 방법을 다양한 구현예 및 실례의 관점에서 설명하였으나, 본 발명의 개념, 사상 및 범위를 벗어나지 않는, 여기에 설명된 물질 및 방법에 변경이 적용될 수 있다는 것은 당업자에게 명백할 것이다. 당업자에게 명백한 모든 이러한 유사한 대체물 및 변경은 첨부된 청구범위에 의해 정의되는 본 발명의 사상, 범위 및 개념 내에 속하는 것으로 간주한다.
Claims (59)
- 금속 산화물을 포함하는 분말을 제조하는 방법에 있어서, 하기를 포함하는 분무 열분해를 수행하는 단계를 포함하는 것을 특징으로 하는 방법:
(a) 전구체 용액 및 하나 또는 그 이상의 고체상 입자를 포함하는 액적(droplets)을 형성하기 위하여, 전구체 용액 내 고체상 입자를 포함하는 슬러리를 에어로졸화하는 단계, 여기서 (i) 고체상 입자는 약 10 nm 및 50 ㎛ 범위의 평균 크기를 가지며, (ii) 전구체 용액은 용매 내에 용해되거나 현탁된 하나 이상의 전구체 화합물을 포함하고, 여기서 하나 이상의 전구체 화합물은 하나 이상의 금속 산화물의 하나 또는 그 이상의 금속 원소를 포함하며, (iii) 슬러리는 약 2% 내지 약 75% 범위 내인 금속 산화물을 포함하는 분말에 대한 고체상 입자의 총 질량비를 갖는다;
(b) 하나 이상의 전구체 화합물 및 하나 또는 그 이상의 고체상 입자를 포함하는 건조된 액적을 형성하도록 액적 내 용매를 증발시키는 단계; 및
(c) 최소한 부분적으로 하나 이상의 전구체 화합물을 분해하고 금속 산화물을 포함하는 분말을 형성하기 위해 건조된 액적을 소성(calcining)하는 단계, 여기서 금속 산화물을 포함하는 분말은 하나 이상의 금속 산화물을 포함하는 생성물 입자를 포함하고, 여기서 생성물 입자는 (i) 약 100 nm 내지 약 500 ㎛ 범위 내인 평균 크기 및 (ii) 에어로졸 내 시드(seed) 입자의 부재를 제외하고 동일하게 수행되는 다른 분무 열분해 방법에 의해 제조된 거의 동일한 평균 크기 입자의 평균 중공도(hollowness) 미만인 평균 중공도를 갖는다. - 제1항에 있어서, 상기 고체상 입자의 평균 크기는 약 100 nm 내지 약 15 ㎛ 범위 내이고, 생성물 입자의 평균 크기는 약 500 nm 내지 약 50 ㎛ 범위 내인 것인 방법.
- 제1항에 있어서, 상기 생성물 입자의 평균 크기는 1 ㎛ 초과인 것인 방법.
- 제1항에 있어서, 상기 생성물 입자의 평균 크기는 2 ㎛ 초과인 것인 방법.
- 제1항에 있어서, 상기 생성물 입자의 평균 크기는 4 ㎛ 초과인 것인 방법.
- 제1항에 있어서, 상기 생성물 입자의 평균 중공도는 약 60% 미만인 것인 방법.
- 제1항에 있어서, 상기 생성물 입자의 평균 중공도는 약 40% 미만인 것인 방법.
- 제1항에 있어서, 상기 생성물 입자의 평균 중공도는 약 20% 미만인 것인 방법.
- 제1항에 있어서, 상기 생성물 입자의 평균 중공도는 약 10% 미만인 것인 방법.
- 제1항에 있어서, 상기 고체상 입자는 (i) 소성 중 분해되는 조성을 갖는 분해성 고체상 입자, (ii) 고체상 입자를 소성 중 대체로 분해되지 않는 조성을 갖는 안정한 고체상 입자, (iii) 소성 중 분해되는 하나 이상의 화합물 및 소성 중 대체로 분해되지 않는 하나 이상의 다른 화합물을 포함하는 조성을 갖는 부분적으로 안정한 고체상 입자, 및 (iv) 이들의 조합으로 구성되는 군으로부터 선택된 것인 방법.
- 제1항에 있어서, 상기 소성은 하나 이상의 금속 산화물의 녹는점을 초과하지 않는 온도에서 수행되는 것인 방법.
- 제1항에 있어서, 상기 고체상 입자는 분무 열분해에 의해 제조되는 것인 방법.
- 제12항에 있어서, 상기 고체상 입자는 비-중공 형태를 갖는 것인 방법.
- 제12항에 있어서, 상기 고체상 입자는 고체상 입자의 크기 분포를 변경하도록 분무 열분해에 의해 제조된 후 연삭되어진 것인 방법.
- 제1항에 있어서, 상기 생성물 입자는 (iii) 다공성 형태를 더 갖는 것인 방법.
- 제1항에 있어서, 하나 이상의 전구체 화합물을 더 분해하기 위하여, 결정 성장을 유발하기 위하여, 또는 그 모두를 위하여 생성물 입자를 어닐링하는 단계를 더 포함하는 방법.
- 제16항에 있어서, 하나 이상의 금속 산화물 내 결함의 형성을 억제하기 위하여 충분히 느린 속도로 어닐링된 생성물 입자를 냉각시키는 단계를 더 포함하는 방법.
- 제1항에 있어서, 상기 대체로 모든 생성물 입자는 대체로 균일한 조성을 갖는 것인 방법.
- 제1항에 있어서, 상기 대체로 모든 생성물 입자는 비-균일한 조성을 가지는 것인 방법으로서, 여기서 이들의 고체상 입자 부분(들)은 이들의 하나 이상의 금속 산화물 부분과 다른 조성인 것인 방법.
- 제1항에 있어서, 상기 고체상 입자는 하나 이상의 금속 산화물의 핵생성을 촉진하기 위하여 선택된 것인 방법.
- 제1항에 있어서,
고체상 입자는 금속 산화물, 식별번호 45-46에서 언급된 것들 및 이들의 조합을 포함하는 질산 금속염(metal nitrates)으로 구성된 군으로부터 선택된 조성을 가지고;
하나 이상의 전구체 화합물은 식별번호 45-46에서 언급된 것들 및 이들의 조합을 포함하는 질산 금속염으로 구성된 군으로부터 선택된 조성을 가지며;
금속 산화물은 이들의 금속 산화물과 혼합된 식별번호 45-46에서 언급된 것들, 및 이들의 조합을 포함하는 것으로 구성된 군으로부터 선택되며; 및 질산 금속염은 식별번호 45-46에서 언급된 것들 및 이들의 조합을 포함하는 것으로 구성된 군으로부터 선택되는 것을 특징으로 하는 방법. - 제1항에 있어서, 상기 고체상 입자 및 하나 이상의 금속 산화물은 일반 화학식 Li1 +α(NixCoyMnz)1- tMtO2 - dRd을 갖도록 독립적으로 선택된 방법으로서, 여기서:
M은 Al, Mg, Fe, Cu, Zn, Cr, Ag, Ca, Na, K, In, Ga, Ge, V, Mo, Nb, Si, Ti, Zr, 및 이들의 혼합물로 구성된 군으로부터 선택되고;
R은 F, Cl, Br, I, H, S, N, 및 이들의 혼합물로 구성된 군으로부터 선택되며; 및
0 ≤ α ≤ 0.50; 0 < x ≤ 1; 0 ≤ y ≤ 1; 0 < z ≤ 1; 0 ≤ t ≤ 1; 및 0 ≤ d ≤ 0.5인 방법. - 제1항에 있어서, 상기 고체상 입자 및 하나 이상의 금속 산화물은 복합 화학식 xLi2MO3*(1-x)LiM'O2을 갖도록 독립적으로 선택된 방법으로서, 여기서:
M은 +4의 평균 산화수를 갖는 하나 또는 그 이상의 금속 이온이고;
M'는 +3의 평균 산화수를 갖는 하나 또는 그 이상의 금속 이온이며; 및
0 < x < 1인 방법. - 제23항에 있어서, 상기 M은 Mn이고 M'는 Mn, Ni, Co, 및 이들의 조합으로 구성되는 군으로부터 선택된 것인 방법.
- 제22항 내지 제24항 중 어느 한 항에 있어서, 상기 생성물 입자는 0.6 g/cm3 초과의 탭 밀도(tap density)를 갖는 것인 방법.
- 제22항 내지 제25항 중 어느 한 항에 있어서, 상기 고체상 입자 및 하나 이상의 금속 산화물은 다른 조성인 것인 방법.
- 제22항 내지 제25항 중 어느 한 항에 있어서, 상기 고체상 입자 및 하나 이상의 금속 산화물은 대체로 동일한 조성인 것인 방법.
- 제22항 내지 제25항 중 어느 한 항에 있어서, 상기 전구체 용액은 둘 이상의 전구체 화합물을 포함하며, 이들이 전구체 용액 내에서 결합되었을 때 이들은 약 300 ℃ 이내의 온도에서 서로 분해하며 이 금속 산화물의 금속 원소에 대해서는 증발 온도 이하가 되도록 선택되는 것인 방법.
- 제28항에 있어서, 상기 전구체 용액은 LiNO3, Mn(NO3)2, 및 Ni(NO3)2 및/또는 이들의 수화물을 포함하는 것인 방법.
- 제28항에 있어서, 상기 전구체 용액은 LiNO3, Mn(NO3)2, Ni(NO3)2, 및 Co(NO3)2 및/또는 이들의 수화물을 포함하는 것인 방법.
- 제22항 내지 제30항 중 어느 한 항에 있어서, 상기 생성물 입자는 약 50 nm 내지 약 500 nm 범위의 평균 크기를 갖는 금속 산화물 일차 입자를 포함하는 약 1 ㎛ 내지 약 15 ㎛ 범위의 평균 크기를 갖는 메조다공성 이차 입자인 것인 방법.
- 제22항 내지 제31항 중 어느 한 항에 있어서, 약 30 분 내지 약 48 시간 범위 내인 기간 동안 약 300 ℃ 내지 약 1000 ℃의 범위 내 온도에서 생성물 입자를 어닐링하는 단계를 더 포함하는 방법.
- 제32항에 있어서, 상기 어닐링 온도는 약 700℃ 내지 약 900℃의 범위 내이고 상기 어닐링 기간은 약 2 시간 내지 약 10 시간의 범위 내인 것인 방법.
- 제32항 또는 제33항에 있어서, 약 5 ℃/min를 초과하지 않는 냉각 속도에서 어닐링된 생성물 입자를 냉각시키는 단계를 더 포함하는 방법.
- 복수의 메조다공성, 비-중공 형태 및 약 1 ㎛ 내지 약 15 ㎛의 범위 내인 평균 크기를 갖는 이차 입자를 함유하는 금속 산화물을 포함하고, 여기서 이차 입자는 약 50 nm 내지 약 500 nm의 범위 내인 평균 크기를 갖는 일차 입자를 포함하는 것인 물질.
- 제35항에 있어서, 상기 이차 입자의 평균 크기는 약 4 ㎛ 내지 약 10 ㎛ 범위 내인 것인 물질.
- 제35항에 있어서, 상기 이차 입자의 중간 크기에 대한 표준 편차는 약 0 내지 약 10의 범위 내인 것인 물질.
- 제35항에 있어서, 상기 이차 입자는 약 2 nm 내지 약 100 nm의 범위 내인 일차 입자간 간격을 갖는 것인 물질.
- 제35항에 있어서, 상기 이차 입자는 약 1 m2/g 내지 약 100 m2/g의 범위 내인 Brunnauer-Emmett-Teller 표면적을 갖는 것인 물질.
- 제35항에 있어서, 상기 물질의 임의의 1 마이크로미터 부위 내 각 원소의 상대 농도가 평균으로부터 약 4% 이상으로 변화하지 않으며 물질 전체에서 표준 편차가 약 4%를 초과하지 않는 것인 물질.
- 제35항에 있어서, 상기 물질의 임의의 1 마이크로미터 부위 내 각 원소의 상대 농도가 평균으로부터 약 1% 이상으로 변화하지 않으며 물질 전체에서 표준 편차가 약 1%를 초과하지 않는 것인 물질.
- 제35항에 있어서, 상기 금속 산화물은 일반 화학식 Li1 +α(NixCoyMnz)1- tMtO2 - dRd를 갖는 것인 물질로서, 여기서:
M은 Al, Mg, Fe, Cu, Zn, Cr, Ag, Ca, Na, K, In, Ga, Ge, V, Mo, Nb, Si, Ti, Zr, 및 이들의 혼합물로 구성되는 군으로부터 선택되고;
R은 F, Cl, Br, I, H, S, N, O 및 이들의 혼합물로 구성되는 군으로부터 선택되며; 및
0 ≤ α ≤ 0.50; 0 < x ≤ 1; 0 ≤ y ≤ 1; 0 < z ≤ 1; 0 ≤ t ≤ 1; 및 0 ≤ d ≤ 0.5인 물질. - 제35항에 따른 물질로서, 여기서:
M은 Al, Mg, Fe, Cu, Zn, Cr, Ag, Ca, Na, K, Si, Ti, V, 및 이들의 혼합물로 구성되는 군으로부터 선택되며; 및
R은 F, Cl, Br, I, 및 이들의 혼합물로 구성되는 군으로부터 선택된 물질. - 제35항에 있어서, 상기 일차 입자는 Li1 +αixMnzO2를 포함하는 것인 물질로서, 여기서 0 ≤ α ≤ 0.2, 0.1 ≤ x ≤ 0.6, 및 0.2 ≤ z ≤ 0.6인 물질.
- 제35항에 있어서, 상기 금속 산화물은 복합화학식 xLi2MO3·(1-x)LiM'O2을 갖는 것인 물질로서, 여기서:
M은 +4의 평균 산화수를 갖는 하나 또는 그 이상의 금속 이온이며; 및
M'는 +3의 평균 산화수를 갖는 하나 또는 그 이상의 금속 이온이며; 및
0 < x <1인 물질. - 제45항에 있어서, 상기 M은 Mn이고 M'는 Mn, Ni, Co, Cr, 및 이들의 조합으로 구성되는 군으로부터 선택된 것인 물질.
- 제45항에 있어서, 상기 M은 Mn이고 M'는 하나 이상의 Mn 및 Ni를 포함하는 것인 물질.
- 제45항에 있어서, 상기 M은 Mn이고 M'는 Mn 및 Ni인 것인 물질.
- 제45항에 있어서, 상기 M은 Mn이고 M'는 Mn0 .25-0.75 및 Ni0 .25-0.75인 것인 물질.
- 제45항에 있어서, 상기 금속 산화물 복합식은 xLi2MnO3·(1-x)LiMn0.5Ni0.5O2이고 0.3 ≤ x ≤ 0.7인 것인 물질.
- 제50항에 있어서, 상기 x = 0.3이고 금속 산화물은 층상-층상(layered-layered) 복합 구조를 갖는 것인 물질.
- 제45항에 있어서, 상기 금속 산화물 복합식은 xLi2MnO3·(1-x)LiCoO2이고 0.3 ≤ x ≤ 0.7인 것인 물질.
- 제45항에 있어서, 상기 금속 산화물 복합식은 xLi2MnO3·(1-x)LiMn1/3Ni1/3Co1/3O2이고 0.3 ≤ x ≤ 0.7인 것인 물질.
- 제45항에 있어서, 상기 금속 산화물은 층상-층상 복합 결정 구조를 갖는 것인 물질.
- 제45항에 있어서, 상기 금속 산화물은 층상-스피넬(layered-spinel) 복합 결정 구조를 포함하는 것인 물질.
- 제45항에 있어서, 상기 금속 산화물은 스피넬-유형 (LT-LiCoO2-유형) 결정 구조를 포함하는 것인 물질.
- 제45항에 있어서, 상기 금속 산화물은 단사정계(monoclinic) Li2MnO3-유형 결정 구조를 포함하는 것인 물질.
- 하기를 포함하는 분무 열분해를 수행하는 단계를 포함하는, 분말을 제조하는 방법:
(a) 액체 및 하나 또는 그 이상의 고체상 입자를 포함하는 액적을 형성하기 위하여, 하나 이상의 전구체 화합물을 포함하는 액체 내 고체상 입자를 포함하는 슬러리를 에어로졸화 하는 단계, 여기서 (i) 고체상 입자는 약 10 nm 및 50 ㎛ 범위 내인 평균 크기를 가지며, (ii) 슬러리는 약 2% 내지 약 75% 범위 내인 금속 산화물을 포함하는 분말에 대한 고체상 입자의 총 질량비를 갖는다; 및
(b) 최소한 부분적으로 하나 이상의 전구체 화합물을 분해하고 분말을 형성하기 위해 액적을 소성하는 단계, 여기서 분말은 하나 이상의 전구체 화합물의 분해 생성물(들)을 포함하는 생성물 입자를 포함하고, 여기서 생성물 입자는 (i) 약 100 nm 내지 약 500 ㎛ 범위 내인 평균 크기 및 (ii) 에어로졸 내 시드 입자의 부재를 제외하고 동일하게 수행되는 다른 분무 열분해 방법에 의해 제조된 거의 동일한 평균 크기 입자의 평균 중공도 미만인 평균 중공도를 갖는다. - 비-중공 형태 및 약 1 ㎛ 내지 약 15 ㎛ 범위 내인 평균 크기를 갖는 복수의 메조다공성 이차 입자를 포함하며, 여기서 이차 입자는 약 50 nm 내지 약 500 nm 범위 내인 평균 크기를 갖는 일차 입자를 포함하는 물질.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361780059P | 2013-03-13 | 2013-03-13 | |
| US61/780,059 | 2013-03-13 | ||
| PCT/US2014/026641 WO2014160445A1 (en) | 2013-03-13 | 2014-03-13 | Method for the use of slurries in spray pyrolysis for the production of non-hollow, porous particles |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150132375A true KR20150132375A (ko) | 2015-11-25 |
Family
ID=51625427
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157029101A KR20150132375A (ko) | 2013-03-13 | 2014-03-13 | 비-중공, 다공성 입자의 제조를 위한 분무 열분해시 슬러리의 사용 방법 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US9748567B2 (ko) |
| EP (1) | EP2969170A4 (ko) |
| JP (1) | JP2016520411A (ko) |
| KR (1) | KR20150132375A (ko) |
| WO (1) | WO2014160445A1 (ko) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6043321B2 (ja) * | 2014-07-07 | 2016-12-14 | 大陽日酸株式会社 | リチウムイオン二次電池用正極材及びその製造方法 |
| US20180237314A1 (en) * | 2015-08-07 | 2018-08-23 | Yangchuan Xing | Synthesis of deep eutectic solvent chemical precursors and their use in the production of metal oxides |
| FR3043572B1 (fr) | 2015-11-12 | 2020-05-15 | Pylote | Materiaux thermiquement isolants integrant des particules inorganiques spheriques et creuses |
| KR102413464B1 (ko) * | 2016-04-01 | 2022-06-24 | 덴카 주식회사 | 티탄산바륨질 분말 및 그 제조 방법, 용도 |
| JP7101681B2 (ja) | 2017-01-09 | 2022-07-15 | エボニック オペレーションズ ゲーエムベーハー | 噴霧熱分解による金属酸化物の製造方法 |
| JP2020507193A (ja) * | 2017-02-09 | 2020-03-05 | ワッカー ケミー アクチエンゲゼルシャフトWacker Chemie AG | リチウムイオン電池のアノード材料用シリコン粒子 |
| EP3495321A1 (de) | 2017-12-07 | 2019-06-12 | Evonik Degussa GmbH | Herstellung von pulverförmigen, porösen kristallinen metallsilikaten mittels flammensprühpyrolyse |
| CN110918047B (zh) * | 2018-09-20 | 2021-04-20 | 比亚迪股份有限公司 | 一种锂铝复合材料及其制备方法和从含锂卤水中富集锂离子的方法 |
| KR101993149B1 (ko) * | 2018-10-31 | 2019-09-30 | 주황윤 | 제강분진으로부터 황산아연분말을 제조하는 방법 |
| JP2022514405A (ja) * | 2018-12-19 | 2022-02-10 | ハルドール・トプサー・アクチエゼルスカベット | リチウム正極活物質 |
| GB201901061D0 (en) * | 2019-01-25 | 2019-03-13 | Ceramic Powder Tech As | Process |
| CN110935394B (zh) * | 2019-11-05 | 2021-07-30 | 南京清大迈特新材料有限公司 | 一种微纳粉体精细加工方法及装置 |
| CN112520792A (zh) * | 2021-01-30 | 2021-03-19 | 浙江博瓦德新材料科技有限公司 | 一种镍沉淀物回用制备氧化亚镍的方法 |
| CN116351419A (zh) * | 2023-03-02 | 2023-06-30 | 中科合成油技术股份有限公司 | 一种重质含碳原料浆态床加氢铁基催化剂及其制备方法 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5128291A (en) * | 1990-12-11 | 1992-07-07 | Wax Michael J | Porous titania or zirconia spheres |
| US5958361A (en) * | 1993-03-19 | 1999-09-28 | Regents Of The University Of Michigan | Ultrafine metal oxide powders by flame spray pyrolysis |
| US6338809B1 (en) * | 1997-02-24 | 2002-01-15 | Superior Micropowders Llc | Aerosol method and apparatus, particulate products, and electronic devices made therefrom |
| US6268014B1 (en) | 1997-10-02 | 2001-07-31 | Chris Eberspacher | Method for forming solar cell materials from particulars |
| JP2000340226A (ja) * | 1999-05-26 | 2000-12-08 | Kawasaki Steel Corp | リチウムマンガン複合酸化物粒子およびその製造方法 |
| US7704483B2 (en) | 2005-04-29 | 2010-04-27 | Cabot Corporation | High surface area tetragonal zirconia and processes for synthesizing same |
| US20120128577A1 (en) * | 2010-10-06 | 2012-05-24 | Blue Juice, Inc. | Metal oxide synthesis |
| TW201311545A (zh) * | 2011-05-02 | 2013-03-16 | Univ Washington | 用於高能量鋰離子電池之介孔性正電極材料的噴霧熱製解合成法 |
| WO2012155196A1 (en) | 2011-05-13 | 2012-11-22 | University Of Wollongong | Spray pyrolysis method for in situ production of graphene oxide based composites |
-
2014
- 2014-03-13 US US14/775,231 patent/US9748567B2/en active Active
- 2014-03-13 WO PCT/US2014/026641 patent/WO2014160445A1/en active Application Filing
- 2014-03-13 KR KR1020157029101A patent/KR20150132375A/ko not_active Application Discontinuation
- 2014-03-13 JP JP2016502203A patent/JP2016520411A/ja active Pending
- 2014-03-13 EP EP14773759.7A patent/EP2969170A4/en not_active Withdrawn
-
2017
- 2017-07-24 US US15/658,014 patent/US10490814B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2016520411A (ja) | 2016-07-14 |
| EP2969170A4 (en) | 2016-09-07 |
| WO2014160445A1 (en) | 2014-10-02 |
| US20160049652A1 (en) | 2016-02-18 |
| EP2969170A1 (en) | 2016-01-20 |
| US10490814B2 (en) | 2019-11-26 |
| US9748567B2 (en) | 2017-08-29 |
| US20170324088A1 (en) | 2017-11-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10490814B2 (en) | Method for the use of slurries in spray pyrolysis for the production of non-hollow, porous particles | |
| US10507446B2 (en) | Method of preparing a material of a battery cell | |
| Oh et al. | Effect of calcination temperature on morphology, crystallinity and electrochemical properties of nano-crystalline metal oxides (Co3O4, CuO, and NiO) prepared via ultrasonic spray pyrolysis | |
| JP4894969B1 (ja) | ニッケルマンガン複合水酸化物粒子とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、ならびに、非水系電解質二次電池 | |
| WO2012131881A1 (ja) | ニッケルマンガン複合水酸化物粒子とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、および非水系電解質二次電池 | |
| US20120282522A1 (en) | Spray Pyrolysis Synthesis of Mesoporous Positive Electrode Materials for High Energy Lithium-Ion Batteries | |
| JP2009302044A (ja) | 無機物粒子の製造方法、及びそれを用いた二次電池正極並びに二次電池 | |
| JPWO2016068263A1 (ja) | ニッケル含有複合水酸化物とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、および非水系電解質二次電池 | |
| JP2009062256A (ja) | 無機物粒子の製造方法 | |
| JP2005347134A (ja) | リチウムイオン二次電池用正極活物質の製造方法 | |
| JP2020177860A (ja) | ニッケルマンガンコバルト含有複合水酸化物およびその製造方法、リチウムニッケルマンガンコバルト含有複合酸化物およびその製造方法、リチウムイオン二次電池用正極活物質およびその製造方法、並びに、リチウムイオン二次電池 | |
| JP7452569B2 (ja) | 非水系電解質二次電池用正極活物質 | |
| KR101510528B1 (ko) | 분무건조 공정에 의한 응집체 구조의 리튬 이차 전지용 전극활물질 분말의 제조방법 및 이로부터 제조된 전극활물질 분말 | |
| JP2008044836A (ja) | リチウム遷移金属複合酸化物の製造方法 | |
| JP7452570B2 (ja) | 非水系電解質二次電池用正極活物質 | |
| JP2002260656A (ja) | 電池材料の製造方法 | |
| JP2022542788A (ja) | パワージェットモジュールを伴うシステム及びその方法 | |
| US20230163350A1 (en) | Large-scale synthesis of powders of solid-state electrolyte material particles for solid-state batteries, systems and methods thereof | |
| JP7119302B2 (ja) | 非水系電解質二次電池用正極活物質前駆体、非水系電解質二次電池用正極活物質前駆体の製造方法、非水系電解質二次電池用正極活物質の製造方法 | |
| Fauteux et al. | Flexible synthesis of mixed metal oxides illustrated for LiMn2O4 and LiCoO2 | |
| JP4032784B2 (ja) | リチウム遷移金属複合酸化物の製造方法 | |
| JP2019021426A (ja) | 非水系電解質二次電池用正極活物質前駆体、非水系電解質二次電池用正極活物質、非水系電解質二次電池用正極活物質前駆体の製造方法、非水系電解質二次電池用正極活物質の製造方法 | |
| JP2021005475A (ja) | リチウムイオン二次電池用正極活物質およびその製造方法、並びに、リチウムイオン二次電池 | |
| JPH10114528A (ja) | リチウムニッケル複合酸化物の製造方法 | |
| JP2007290885A (ja) | 無機物粒子の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| N231 | Notification of change of applicant | ||
| WITN | Withdrawal due to no request for examination |