KR20140001996A - Hdl 소분획 중의 콜레스테롤의 측정 방법, 측정용 시약 및 측정용 키트 - Google Patents
Hdl 소분획 중의 콜레스테롤의 측정 방법, 측정용 시약 및 측정용 키트 Download PDFInfo
- Publication number
- KR20140001996A KR20140001996A KR20137023141A KR20137023141A KR20140001996A KR 20140001996 A KR20140001996 A KR 20140001996A KR 20137023141 A KR20137023141 A KR 20137023141A KR 20137023141 A KR20137023141 A KR 20137023141A KR 20140001996 A KR20140001996 A KR 20140001996A
- Authority
- KR
- South Korea
- Prior art keywords
- reagent
- cholesterol
- measuring
- hdl3
- metal salt
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/60—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving cholesterol
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/26—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving oxidoreductase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/26—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving oxidoreductase
- C12Q1/32—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving oxidoreductase involving dehydrogenase
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/34—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving hydrolase
- C12Q1/44—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving hydrolase involving esterase
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/92—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving lipids, e.g. cholesterol, lipoproteins, or their receptors
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- Biotechnology (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Analytical Chemistry (AREA)
- Physics & Mathematics (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Urology & Nephrology (AREA)
- Biomedical Technology (AREA)
- Hematology (AREA)
- Cell Biology (AREA)
- Endocrinology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
본 발명은 간편하고 정확하게 검체 중의 HDL 소분획 중의 콜레스테롤을 측정하는 방법을 제공한다. 검체와, (1) 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 조합, 또는 (2) 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소 및 콜레스테롤 탈수소 효소의 조합을 (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 수성 매체 중에서 반응시켜, HDL3 이외의 리포 단백질을 분리 제거하지 않고, 생성되는 물질 또는 소비되는 물질을 측정하는 것을 특징으로 하는 검체 중의 HDL3 중의 콜레스테롤의 측정 방법이다.
Description
본 발명은 검체 중의 HDL 소분획 중의 콜레스테롤의 측정 방법, 측정용 시약, 및 측정용 키트에 관한 것이다.
고밀도 리포 단백질 (HDL) 은 리포 단백질의 하나로, 1.063 ∼ 1.210 의 비중을 갖는다. HDL 중의 콜레스테롤 (HDL-C) 은 관동맥 질환 (CHD) 의 부 (負) 의 위험 인자로 알려져 있다. 최근, HDL 의 소분획인 HDL2 와 HDL3 에 대해 그 임상적 의의에 관심이 높아지고 있다. HDL2 는 비중 1.063 ∼ 1.125, HDL3 은 비중 1.125 ∼ 1.210 의 리포 단백질이다.
간장 또는 장관에서 분비된 원시형 HDL 은, 말초 세포막에 접착하여, 거기로부터 유리형 콜레스테롤을 취입하고, 취입된 유리형 콜레스테롤은, HDL 표면 상에 존재하는 LCAT (레시틴콜레스테롤아실트랜스페라아제) 의 작용에 의해 에스테르형 콜레스테롤로 변환되고, 이 에스테르형 콜레스테롤을 심으로 한 구상의 HDL3 이 된다. HDL3 은 또한, LCAT 의 작용에 의해 에스테르형 콜레스테롤이 증가하여 HDL2 가 된다.
HDL2 중의 콜레스테롤은 2 개의 경로에 의해 대사된다. 하나는, HDL2 마다 간장에 직접 취입되어 담즙산으로 배출되는 경로이고, 또 다른 하나는, HDL2 중의 에스테르형 콜레스테롤이 CETP (콜레스테롤 에스테르 전송 단백) 의 작용에 의해 초저밀도 리포 단백질 (VLDL), 중간 밀도 리포 단백질 (IDL), 저밀도 리포 단백질 (LDL) 등의 중성 지방이 풍부한 리포 단백질 내의 중성 지방과 교환되어, 당해 중성 지방이 풍부한 리포 단백질으로 전송되는 경로 (콜레스테롤 역전송계) 이다.
HDL 소분획 중의 콜레스테롤의 측정 방법에 대하여, 지금까지 HDL3 과 HDL2 의 분리 공정을 수반하는 침전법, HDL3 과 HDL2 의 분리 공정을 수반하지 않는 호모지니어스법이 알려져 있다.
침전법으로는, 헤파린, 2 가 금속 이온 및 덱스트란황산을 사용하는, 1 단계의 분리 조작에 의한 검체 중의 HDL3 중의 콜레스테롤의 측정 방법 (예를 들어, 특허문헌 1, 비특허문헌 1), 2 단계의 분리 조작에 의한 검체 중의 HDL3 중의 콜레스테롤의 측정 방법 (예를 들어, 비특허문헌 2 ∼ 4) 등이 알려져 있다. 1 단계의 분리 조작에 의한 검체 중의 HDL3 중의 콜레스테롤의 측정 방법은, 검체 중의 HDL3 이외의 리포 단백질을 응집시켜 분리 제거하고, 얻어진 HDL3 중의 콜레스테롤을 측정하는 방법이다. 2 단계의 분리 조작에 의한 검체 중의 HDL3 중의 콜레스테롤의 측정 방법은, 먼저, 검체 중의 HDL 이외의 리포 단백질을 응집시켜, 원심분리에 의해 HDL 이외의 리포 단백질을 제거하고, 이어서, 얻어진 HDL 을 함유하는 상청 중의 HDL2 를 응집시켜, 원심분리에 의해 HDL2 를 제거하고, 상청에 함유되는 HDL3 을 회수하여, 얻어진 HDL3 중의 콜레스테롤을 측정하는 방법이다.
호모지니어스법으로는, HDL 에 대해 높은 특이성을 나타내는 효소, 및 HLB 값이 17 이상인 비이온성 계면활성제를 사용하는 방법이 알려져 있다 (예를 들어, 특허문헌 2).
원심분리 등의 번잡한 조작을 수반하지 않는 간편하고 정확한, 검체 중의 HDL 소분획 중의 콜레스테롤의 측정 방법이 요구되고 있다.
저널 오브 리피드 리서치 (Journal of Lipid Research), 49권, 5호, 1130-1136페이지 (2008년)
클리니컬 케미스트리 (Clinical Chemistry), 34권, 11호, 2322-2327페이지 (1998년)
클리니컬 케미스트리 (Clinical Chemistry), 36권, 2호, 265-270페이지 (1999년)
저널 오브 리피드 리서치 (Journal of Lipid Research), 23권, 8호, 1206-1223페이지 (1982년)
본 발명의 목적은 간편하고 정확하게 검체 중의 HDL 소분획 중의 콜레스테롤을 측정하는 방법, 시약, 및 키트를 제공하는 것에 있다.
본 발명자들은 본 과제를 해결하기 위해 예의 검토를 거듭한 결과, 콜레스테롤 측정용 효소, 2 가의 금속염, 특정한 알칼리 금속염, 및 덱스트란황산 또는 그 염을 사용함으로써, HDL3 이외의 리포 단백질을 분리 제거하지 않고, HDL3 중의 콜레스테롤을 측정할 수 있다는 지견을 알아내어 본 발명을 완성시켰다. 즉, 본 발명은 이하의 [1] ∼ [19] 에 관한 것이다.
[1] 검체와, (1) 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 조합, 또는 (2) 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소 및 콜레스테롤 탈수소 효소의 조합을 (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 수성 매체 중에서 반응시켜, HDL3 이외의 리포 단백질을 분리 제거하지 않고, 생성되는 물질 또는 소비되는 물질을 측정하는 것을 특징으로 하는 검체 중의 HDL3 중의 콜레스테롤의 측정 방법,
[2] 2 가의 금속염이 마그네슘염 또는 칼슘염인 상기 [1] 에 기재된 방법,
[3] 덱스트란황산 또는 그 염의 반응액 중의 농도가 0.75 ∼ 2.6 g/ℓ 인 상기 [1] 또는 [2] 에 기재된 방법,
[4] 반응액 중의 2 가의 금속염 유래의 2 가의 금속 이온의 농도가 12 ∼ 20 m㏖/ℓ 이고, 반응액 중의 알칼리 금속염 유래의 알칼리 금속 이온의 농도가 5 ∼ 21 m㏖/ℓ 인 상기 [1] ∼ [3] 중 어느 하나에 기재된 방법,
[5] 이하의 공정을 포함하는 것을 특징으로 하는 검체 중의 HDL2 중의 콜레스테롤의 측정 방법
(1) 검체 중의 고밀도 리포 단백질 (HDL) 중의 콜레스테롤을 측정하는 공정 ;
(2) 상기 [1] ∼ [4] 중 어느 하나에 기재된 측정 방법에 의해 검체 중의 HDL3 중의 콜레스테롤을 측정하는 공정 ;
(3) 상기 (1) 공정에서 측정한 측정값에서 (2) 공정에서 측정한 측정값을 빼는 공정,
[6] 상기 [1] ∼ [4] 중 어느 하나에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 시약으로서, 콜레스테롤 에스테르 가수분해 효소, 콜레스테롤 산화 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, (c) 덱스트란황산 또는 그 염, 및 과산화수소 측정용 시약을 함유하는 것을 특징으로 하는 검체 중의 HDL3 중의 콜레스테롤의 측정용 시약,
[7] 상기 [1] ∼ [4] 중 어느 하나에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 시약으로서, 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소, 콜레스테롤 탈수소 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 것을 특징으로 하는 검체 중의 HDL3 중의 콜레스테롤의 측정용 시약,
[8] 추가로, 환원형 보조 효소 측정용 시약을 포함하는 상기 [7] 에 기재된 시약,
[9] 2 가의 금속염이 마그네슘염 또는 칼슘염인 상기 [6] ∼ [8] 중 어느 하나에 기재된 시약,
[10] 덱스트란황산 또는 그 염이 반응액 중에서의 농도가 0.75 ∼ 2.6 g/ℓ 가 되는 함량으로 함유되는 상기 [6] ∼ [9] 중 어느 하나에 기재된 시약,
[11] 2 가의 금속염이, 반응액 중에서의 2 가의 금속염 유래의 2 가의 금속 이온의 농도가 12 ∼ 20 m㏖/ℓ 가 되는 함량으로 함유되고, 알칼리 금속염이, 반응액 중에서의 알칼리 금속염 유래의 알칼리 금속 이온의 농도가 5 ∼ 21 m㏖/ℓ 가 되는 함량으로 함유되는 상기 [6] ∼ [10] 중 어느 하나에 기재된 시약,
[12] 제 1 시약 및 제 2 시약을 함유하는 상기 [1] ∼ [4] 중 어느 하나에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 키트로서, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 제 1 시약에 함유하고, 콜레스테롤 산화 효소를 제 2 시약에 함유하고, 과산화수소 측정용 시약을 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하고, 콜레스테롤 에스테르 가수분해 효소를 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하는 것을 특징으로 하는 키트,
[13] 제 1 시약 및 제 2 시약을 함유하는 상기 [1] ∼ [4] 중 어느 하나에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 키트로서, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 제 1 시약에 함유하고, 콜레스테롤 탈수소 효소를 제 2 시약에 함유하고, 산화형 보조 효소를 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하고, 콜레스테롤 에스테르 가수분해 효소를 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하는 것을 특징으로 하는 키트,
[14] 추가로, 환원형 보조 효소 측정용 시약을 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하는 상기 [13] 에 기재된 키트,
[15] 2 가의 금속염이 마그네슘염 또는 칼슘염인 상기 [12] ∼ [14] 중 어느 하나에 기재된 키트,
[16] 덱스트란황산 또는 그 염이 반응액 중에서의 농도가 0.75 ∼ 2.6 g/ℓ 가 되는 함량으로 함유되는 상기 [12] ∼ [15] 중 어느 하나에 기재된 키트,
[17] 2 가의 금속염이, 반응액 중에서의 2 가의 금속염 유래의 2 가의 금속 이온의 농도가 12 ∼ 20 m㏖/ℓ 가 되는 함량으로 함유되고, 알칼리 금속염이, 반응액 중에서의 알칼리 금속염 유래의 알칼리 금속 이온의 농도가 5 ∼ 21 m㏖/ℓ 가 되는 함량으로 함유되는 상기 [12] ∼ [16] 중 어느 하나에 기재된 키트,
[18] 상기 [6] ∼ [11] 중 어느 하나에 기재된 HDL3 중의 콜레스테롤 측정용 시약과, HDL 콜레스테롤 측정용 시약을 포함하는 것을 특징으로 하는 검체 중의 HDL2 중의 콜레스테롤의 측정용 키트,
[19] 상기 [12] ∼ [17] 중 어느 하나에 기재된 HDL3 중의 콜레스테롤 측정용 키트의 제 1 시약 및 제 2 시약과, HDL 콜레스테롤 측정용 시약을 포함하는 것을 특징으로 하는 검체 중의 HDL2 중의 콜레스테롤의 측정용 키트.
본 발명에 의해 간편하고 정확하게 검체 중의 HDL 소분획 중의 콜레스테롤을 측정하는 방법, 시약, 및 키트가 제공된다.
<HDL3 중의 콜레스테롤의 측정 방법>
본 발명의 검체 중의 HDL3 중의 콜레스테롤 (이하, HDL3-C 라고 기재한다) 의 측정 방법은, 원심분리 등의 물리적 방법에 의한 리포 단백질의 분리 제거를 필요로 하지 않는 방법이며, 또, HDL3-C 의 측정에 앞서, 검체 중의 HDL3 이외의 리포 단백질 중의 콜레스테롤을 소거하지 않고, 검체 중의 HDL3-C 를 측정하는 방법이다.
본 발명의 HDL3-C 측정 방법은, 검체와 콜레스테롤 측정용 효소를 (a) 마그네슘염 또는 칼슘염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 수성 매체 중에서 반응시켜, HDL3 이외의 리포 단백질을 분리 제거하지 않고, 생성되는 물질 또는 소비되는 물질을 측정하는 것을 특징으로 하는 방법이다. 콜레스테롤 측정용 효소로는, 예를 들어 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 조합, 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소 및 콜레스테롤 탈수소 효소의 조합 등을 들 수 있다.
본 발명의 측정 방법은,
(1) 검체와, 콜레스테롤 측정용 효소의 반응을 (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 수성 매체 중에서 반응시키는 공정 ;
(2) HDL3 이외의 리포 단백질을 분리 제거하지 않고, 공정 (1) 의 반응에 의해 생성되는 물질 또는 소비되는 물질을 측정하는 공정 ;
(3) 미리 공지된 농도의 HDL3-C 를 이용하여 작성된 HDL3-C 농도와, 그 생성되는 물질 또는 그 소비되는 물질 유래의 정보량의 관계를 나타내는 검량선과, 상기 (2) 에서의 측정값을 상관짓는 공정 ; 및
(4) 검체 중의 HDL3-C 농도를 결정하는 공정
을 포함한다. 여기서, 공정 (1) 에 있어서의 콜레스테롤 측정용 효소로는, 전술한 콜레스테롤 측정용 효소 등을 들 수 있다.
공정 (2) 에 있어서의 공정 (1) 의 반응에 의해 생성되는 물질로는, 콜레스테롤 측정용 효소로서, 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 조합을 사용하는 경우에는 과산화수소 등을 들 수 있고, 콜레스테롤 측정용 효소로서, 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소 및 콜레스테롤 탈수소 효소의 조합을 사용하는 경우에는 환원형 보조 효소 등을 들 수 있다.
공정 (2) 에 있어서의 공정 (1) 의 반응에 의해 소비되는 물질로는, 콜레스테롤 측정용 효소로서, 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 조합을 사용하는 경우에는 산소 분자 등을 들 수 있다.
본 발명의 측정 방법에 있어서, 검체와, 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 반응에 의해 생성되는 과산화수소는, 예를 들어 과산화수소 전극이나 후술하는 과산화수소 측정용 시약을 사용하여 측정할 수 있다.
본 발명의 측정 방법에 있어서, 검체와, 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소 및 콜레스테롤 탈수소 효소의 반응에 의해 생성되는 환원형 보조 효소는, 예를 들어 흡광도법이나 후술하는 환원형 보조 효소 측정용 시약을 사용하여 측정할 수 있다. 흡광도법으로는, 흡광도를 이용하여 환원형 보조 효소를 측정할 수 있는 방법이면 특별히 제한은 없으며, 예를 들어 환원형 보조 효소의 흡광도를 환원형 보조 효소의 최대 흡수 파장 (λmax = 340 ㎚) 부근의 파장으로 측정하는 방법 등을 들 수 있다.
소비되는 산소 분자는, 예를 들어 산소 전극을 이용하여 측정할 수 있다.
본 발명의 측정 방법에 있어서 사용되는 검체로는, 예를 들어 전혈, 혈장, 혈청 등을 들 수 있으며, 혈장 및 혈청이 바람직하다.
본 발명에 있어서의 콜레스테롤 에스테르 가수분해 효소로는, 콜레스테롤 에스테르를 가수분해하는 능력을 갖는 효소이면 특별히 제한은 없으며, 예를 들어 동물, 식물 또는 미생물 유래의 콜레스테롤 에스테라아제, 리포프로테인리파아제 이외에, 유전자 공학적 수법에 의해 제조되는 콜레스테롤 에스테라아제, 리포프로테인리파아제 등도 사용할 수 있다.
콜레스테롤 에스테르 가수분해 효소로는, 무수식의 콜레스테롤 에스테르 가수분해 효소 이외에, 화학적으로 수식된 콜레스테롤 에스테르 가수분해 효소도 사용할 수 있다. 또, 콜레스테롤 에스테르 가수분해 효소로는 시판품을 사용할 수도 있다.
시판되고 있는 콜레스테롤 에스테르 가수분해 효소로는, 콜레스테롤 에스테라아제 (COE-311 ; 토요 방적사 제조), 리포프로테인리파아제 (LPL-311 ; 토요 방적사 제조), 콜레스테롤 에스테라아제 (CHE“Amano”3 ; 아마노 엔자임 주식회사 제조), 콜레스테롤 에스테라아제 (EST“Amano”2 ; 아마노 엔자임 주식회사 제조) 등을 들 수 있다. 또, 본 발명에 있어서는, 2 종류 이상의 콜레스테롤 에스테르 가수분해 효소를 조합하여 사용할 수도 있다.
콜레스테롤 에스테르 가수분해 효소의 화학 수식에 있어서 당해 효소를 수식하는 기 (화학 수식기) 로는, 예를 들어 폴리에틸렌글리콜을 주성분으로 하는 기, 폴리프로필렌글리콜을 주성분으로 하는 기, 폴리프로필렌글리콜과 폴리에틸렌글리콜의 공중합체를 갖는 기, 수용성 다당류를 함유하는 기, 술포프로필기, 술포부틸기, 폴리우레탄기, 킬레이트 기능을 갖는 기 등을 들 수 있지만, 폴리에틸렌글리콜을 주성분으로 하는 기가 바람직하다. 수용성 다당류로는, 예를 들어 덱스트란, 풀루란, 가용성 전분 등을 들 수 있다.
콜레스테롤 에스테르 가수분해 효소를 화학적으로 수식하기 위한 시약 (화학 수식제) 으로는, 상기 화학 수식기와, 효소의 아미노기, 카르복실기, 술프하이드릴기 등과 반응할 수 있는 관능기 또는 구조를 함께 갖는 화합물 등을 들 수 있다. 효소 중의 아미노기와 반응할 수 있는 관능기 또는 구조로는, 예를 들어 카르복실기, 활성 에스테르기 (N-하이드록시숙신이미드기 등), 산무수물, 산염화물, 알데히드, 에폭사이드기, 1,3-프로판술톤, 1,4-부탄술톤 등을 들 수 있다. 효소 중의 카르복실기와 반응할 수 있는 관능기 또는 구조로는, 예를 들어 아미노기 등을 들 수 있다. 효소 중의 술프하이드릴기와 반응성이 있는 기 또는 구조로는, 예를 들어 말레이미드기, 디술파이드, α-할로에스테르 (α-요드에스테르 등) 등을 들 수 있다.
화학 수식제로서 시판품을 사용할 수도 있다. 시판되고 있는 화학 수식제로는, 폴리에틸렌글리콜을 주성분으로 하는 기와 N-하이드록시숙신이미드기를 갖는 선브라이트 VFM-4101, 선브라이트 ME-050AS, 선브라이트 DE-030AS (모두 니치유사 제조), 폴리알킬렌글리콜을 주성분으로 하는 기와 산무수물 구조를 갖는 선브라이트 AKM 시리즈 (예를 들어, 선브라이트 AKM-1510 등), 선브라이트 ADM 시리즈, 선브라이트 ACM 시리즈 (모두 니치유사 제조), 폴리에틸렌글리콜을 주성분으로 하는 기와 에폭사이드기를 갖는 EPOX-3400, M-EPOX-5000 (모두 Sheawater Polymers 사 제조), 킬레이트 기능을 갖는 기와 산무수물 구조를 갖는 디에틸렌트리아민-N,N,N',N", N"-펜타 무수 이아세트산 (DTPA anhydride ; 도진 화학 연구소사 제조) 등을 들 수 있다.
콜레스테롤 에스테르 가수분해 효소의 화학 수식은, 예를 들어 이하의 방법에 의해 실시할 수 있지만, 본 방법에 한정되는 것은 아니다. 먼저, 콜레스테롤 에스테르 가수분해 효소를 pH 8.0 이상의 완충액 (예를 들어 HEPES 완충액) 에 용해시키고, 0 ∼ 55 ℃ 에서 0.01 ∼ 500 배 몰량의 화학 수식제를 첨가하여, 5 분간 ∼ 5 시간 교반한다. 효소 반응에 있어서는, 화학적으로 수식된 콜레스테롤 에스테르 가수분해 효소로서, 이 반응액 그 자체뿐만 아니라, 필요에 따라 한외 여과막 등에 의해 미반응의 화학 수식제 등을 제거한 것도 사용할 수도 있다.
본 발명의 측정 방법에 있어서의 콜레스테롤 에스테르 가수분해 효소의 농도로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없으며, 반응액 중의 농도는 통상적으로 0.001 ∼ 800 kU/ℓ 이고, 0.01 ∼ 300 kU/ℓ 가 바람직하다.
본 발명에 있어서의 콜레스테롤 산화 효소로는, 콜레스테롤을 산화시켜 과산화수소를 생성하는 능력을 갖는 효소이면 특별히 제한은 없으며, 예를 들어 동물, 식물 또는 미생물 유래의 콜레스테롤옥시다아제 이외에, 유전자 공학적 수법에 의해 제조되는 콜레스테롤옥시다아제 등도 사용할 수 있고, 콜레스테롤옥시다아제 (CHODI ; 쿄와 발효 공업사 제조), 콜레스테롤옥시다아제 (CHODI ; 키코망사 제조), 콜레스테롤옥시다아제 (CHO-CE ; 키코망사 제조), 콜레스테롤옥시다아제 (COO321 ; 토요 방적사 제조), 콜레스테롤옥시다아제 (COO322 ; 토요 방적사 제조) 등의 시판품을 사용할 수도 있다. 또, 본 발명에 있어서는, 2 종류 이상의 콜레스테롤 산화 효소를 조합하여 사용할 수도 있다.
콜레스테롤 산화 효소는 무수식의 효소이어도 되고, 화학적으로 수식된 효소이어도 된다. 화학적으로 수식된 콜레스테롤 산화 효소는, 예를 들어 전술한 화학 수식제를 이용하여 전술한 화학 수식 방법에 의해 제조할 수 있다.
본 발명의 측정 방법에 있어서의 콜레스테롤 산화 효소의 농도로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없으며, 반응액 중의 농도는 통상적으로 0.001 ∼ 800 kU/ℓ 이고, 0.01 ∼ 300 kU/ℓ 가 바람직하다.
본 발명에 있어서의 콜레스테롤 탈수소 효소로는, 산화형 보조 효소의 존재하에 콜레스테롤을 산화시켜 환원형 보조 효소를 생성하는 능력을 갖는 효소이면 특별히 제한은 없으며, 예를 들어 동물, 식물 또는 미생물 유래의 콜레스테롤 데하이드로게나아제 이외에, 유전자 공학적 수법에 의해 제조되는 콜레스테롤 데하이드로게나아제 등도 사용할 수 있다. 콜레스테롤 데하이드로게나아제 (CHDH“Amano”5 ; 아마노 엔자임사 제조) 등의 시판품을 사용할 수도 있다. 또, 본 발명에 있어서는, 2 종류 이상의 콜레스테롤 탈수소 효소를 조합하여 사용할 수도 있다. 콜레스테롤 탈수소 효소는 무수식의 효소이어도 되고, 화학적으로 수식된 효소이어도 된다. 화학적으로 수식된 콜레스테롤 탈수소 효소는, 예를 들어 전술한 화학 수식제를 이용하여 전술한 화학 수식 방법에 의해 제조할 수 있다.
본 발명의 측정 방법에 있어서의 콜레스테롤 탈수소 효소의 농도로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없으며, 반응액 중의 농도는 통상적으로 0.001 ∼ 800 kU/ℓ 이고, 0.01 ∼ 300 kU/ℓ 가 바람직하다.
본 발명의 콜레스테롤 탈수소 효소를 사용한 측정법에 있어서는, 산화형 보조 효소가 사용된다. 산화형 보조 효소로는, 예를 들어 NAD, NADP, 티오 (thio)-NAD, 티오 (thio)-NADP 등을 들 수 있다.
본 발명의 측정 방법에 있어서의 산화형 보조 효소의 농도로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없으며, 반응액 중의 농도는 통상적으로 0.01 ∼ 400 m㏖/ℓ 이고, 0.1 ∼ 100 m㏖/ℓ 가 바람직하다.
본 발명에 있어서의 환원형 보조 효소로는, 예를 들어 NADH, NADPH, 티오 (thio)-NADH, 티오 (thio)-NADPH 등을 들 수 있다.
본 발명에 있어서 사용되는 2 가의 금속염으로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 2 가의 금속염이면 특별히 제한은 없으며, 예를 들어, 마그네슘염, 칼슘염, 망간염 등을 들 수 있지만, 마그네슘염 또는 칼슘염이 바람직하다. 또, 본 발명에 있어서는, 2 가의 금속염의 수화물 등도 사용할 수 있다. 마그네슘염으로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 마그네슘염이면 특별히 제한은 없으며, 예를 들어 염화마그네슘, 질산마그네슘, 황산마그네슘 등을 들 수 있다. 칼슘염으로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 칼슘염이면 특별히 제한은 없으며, 예를 들어 염화칼슘, 질산칼슘, 황산칼슘 등을 들 수 있다.
본 발명의 측정 방법에 있어서의 2 가의 금속염의 반응액 중의 농도로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없지만, 통상적으로 12 ∼ 20 m㏖/ℓ 이고, 13 ∼ 19 m㏖/ℓ 가 바람직하다.
본 발명의 측정 방법에 있어서의 알칼리 금속염은, 황산염, 질산염, 탄산염, 아세트산염 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염이며, 예를 들어 황산리튬, 질산리튬, 탄산리튬, 아세트산리튬, 불화리튬, 염화리튬, 브롬화리튬, 요오드화리튬, 황산나트륨, 질산나트륨, 탄산나트륨, 아세트산나트륨, 불화나트륨, 염화나트륨, 브롬화나트륨, 요오드화나트륨, 황산칼륨, 질산칼륨, 탄산칼륨, 아세트산칼륨, 불화칼륨, 염화칼륨, 브롬화칼륨, 요오드화칼륨 등을 들 수 있다.
본 발명의 측정 방법에 있어서의 황산염, 질산염, 탄산염, 아세트산염 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염의 반응액 중의 농도로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없지만, 통상적으로 5 ∼ 21 m㏖/ℓ 이고, 6 ∼ 18 m㏖/ℓ 가 바람직하다.
본 발명의 측정 방법에 있어서의 덱스트란황산 또는 그 염은, 본 발명의 HDL3-C 의 측정을 가능하게 하는 덱스트란황산 또는 그 염이면 특별히 제한은 없지만, 분자량이 4 만 ∼ 50 만인 덱스트란황산 또는 그 염이 바람직하다. 염으로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 염이면 특별히 제한은 없으며, 예를 들어 나트륨염 등을 들 수 있다. 본 발명의 측정 방법에 있어서의 덱스트란황산 또는 그 염의 반응액 중의 농도로는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없지만, 통상적으로 0.75 ∼ 2.6 g/ℓ 이고, 1.0 ∼ 2.3 g/ℓ 가 바람직하다.
본 발명에 있어서 사용되는 수성 매체는, 본 발명의 HDL3-C 의 측정 방법을 가능하게 하는 수성 매체이면 특별히 제한은 없으며, 예를 들어 탈이온수, 증류수, 완충액 등을 들 수 있고, 완충액이 바람직하다.
본 발명의 HDL3-C 의 측정 방법에 있어서의 pH 는, 본 발명의 HDL3-C 의 측정 방법을 가능하게 하는 pH 이면 어느 것이어도 되지만, 예를 들어 pH 4 ∼ 10 을 들 수 있다. 수성 매체로서 완충액을 사용하는 경우에는, 설정하는 pH 에 따른 완충제를 사용하는 것이 바람직하다. 완충액에 사용하는 완충제로는, 예를 들어 트리스(하이드록시메틸)아미노메탄 완충제, 인산 완충제, 붕산 완충제, 굿 완충제 등을 들 수 있다.
굿 완충제로는, 예를 들어 2-모르폴리노에탄술폰산 (MES), 비스(2-하이드록시에틸)이미노트리스(하이드록시메틸)메탄 (Bis-Tris), N-(2-아세트아미드)이미노이아세트산 (ADA), 피페라진-N,N'-비스(2-에탄술폰산) (PIPES), N-(2-아세트아미드)-2-아미노에탄술폰산 (ACES), 3-모르폴리노-2-하이드록시프로판술폰산 (MOPSO), N,N-비스(2-하이드록시에틸)-2-아미노에탄술폰산 (BES), 3-모르폴리노프로판술폰산 (MOPS), N-[트리스(하이드록시메틸)메틸]-2-아미노에탄술폰산 (TES), 2-[4-(2-하이드록시에틸)-1-피페라지닐]에탄술폰산 (HEPES), 3-[N,N-비스(2-하이드록시에틸)아미노]-2-하이드록시프로판술폰산 (DIPSO), N-[트리스(하이드록시메틸)메틸]-2-하이드록시-3-아미노프로판술폰산 (TAPSO), 피페라진-N,N'-비스(2-하이드록시프로판술폰산) (POPSO), 3-[4-(2-하이드록시에틸)-1-피페라지닐]-2-하이드록시프로판술폰산 (HEPPSO), 3-[4-(2-하이드록시에틸)-1-피페라지닐]프로판술폰산 [(H) EPPS], N-[트리스(하이드록시메틸)메틸]글리신 (Tricine), N,N-비스(2-하이드록시에틸)글리신 (Bicine), N-트리스(하이드록시메틸)메틸-3-아미노프로판술폰산 (TAPS), N-시클로헥실-2-아미노에탄술폰산 (CHES), N-시클로헥실-3-아미노-2-하이드록시프로판술폰산 (CAPSO), N-시클로헥실-3-아미노프로판술폰산 (CAPS) 등을 들 수 있다.
완충액의 농도는 측정에 적합한 농도이면 특별히 제한되지는 않지만, 0.001 ∼ 2.0 ㏖/ℓ 가 바람직하고, 0.005 ∼ 1.0 ㏖/ℓ 가 보다 바람직하다.
본 발명의 HDL3-C 의 측정 방법에 있어서의 반응 온도는, 본 발명의 HDL3-C 의 측정 방법을 가능하게 하는 온도이면 특별히 제한은 없지만, 10 ∼ 50 ℃ 가 바람직하고, 30 ∼ 40 ℃ 가 보다 바람직하다. 범용의 자동 분석 장치에서 설정되는 반응 온도는 통상적으로 37 ℃ 이다.
본 발명의 HDL3-C 의 측정 방법에 있어서의 반응 시간은, 본 발명의 HDL3-C 의 측정 방법을 가능하게 하는 반응 시간이면 특별히 제한은 없지만, 1 ∼ 60 분간이 바람직하고, 2 ∼ 30 분간이 보다 바람직하다.
본 발명의 HDL3-C 의 측정 방법에 있어서, 콜레스테롤 측정용 효소로서, 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 조합을 사용하는 경우에는, HDL3-C 의 측정은, 반응에 의해 생성된 과산화수소의 양을 측정함으로써 실시할 수 있다.
생성된 과산화수소의 양은, 예를 들어 과산화수소 전극이나 과산화수소 측정용 시약을 사용하여 측정할 수 있다. 과산화수소 측정용 시약은, 생성된 과산화수소를 검출 가능한 물질로 변환시키기 위한 시약이다. 검출 가능한 물질로는, 예를 들어 색소, 발광 등을 들 수 있지만, 색소가 바람직하다. 검출 가능한 물질이 색소인 경우에는, 과산화수소 측정용 시약은, 산화 발색형 색원체 및 퍼옥시다아제 등의 과산화 활성 물질을 함유한다. 산화 발색형 색원체로는, 예를 들어 후술하는 산화 발색형 색원체를 들 수 있다. 검출 가능한 물질이 발광인 경우에는, 과산화수소 측정용 시약은 화학 발광 물질을 함유한다. 화학 발광 물질로는, 예를 들어 루미놀, 이소루미놀, 루시게닌, 아크리디늄에스테르 등을 들 수 있다.
과산화수소 측정용 시약으로서, 산화 발색형 색원체 및 퍼옥시다아제 등의 과산화 활성 물질을 함유하는 시약을 사용하는 경우에는, 과산화수소는, 과산화 활성 물질의 존재하에 산화 발색형 색원체와 반응하여 색소를 생성하고, 생성된 색소를 측정함으로써 측정할 수 있다. 또, 화학 발광 물질을 함유하는 과산화수소 측정용 시약을 사용하는 경우에는, 과산화수소는, 화학 발광 물질과 반응하여 포톤을 발생시키고, 생성된 포톤을 측정함으로써 측정할 수 있다.
산화 발색형 색원체로는, 예를 들어 로이코형 색원체, 산화 커플링 발색형 색원체 등을 들 수 있다. 로이코형 색원체는, 과산화수소 및 퍼옥시다아제 등의 과산화 활성 물질의 존재하, 단독으로 색소로 변환되는 물질이다. 구체적으로는, 테트라메틸벤지딘, o-페닐렌디아민, 10-N-카르복시메틸카르바모일-3,7-비스(디메틸아미노)-10H-페노티아진 (CCAP), 10-N-메틸카르바모일-3,7-비스(디메틸아미노)-10H-페노티아진 (MCDP), N-(카르복시메틸아미노카르보닐)-4,4'-비스(디메틸아미노)디페닐아민나트륨염 (DA-64), 10-N-(카르복시메틸아미노카르보닐)-3,7-비스(디메틸아미노)-10H-페노티아진나트륨염 (DA-67), 4,4'-비스(디메틸아미노)디페닐아민, 비스[3-비스(4-클로로페닐)메틸-4-디메틸아미노페닐]아민 (BCMA) 등을 들 수 있다.
산화 커플링 발색형 색원체는, 과산화수소 및 퍼옥시다아제 등의 과산화 활성 물질의 존재하, 2 개의 화합물이 산화적 커플링되어 색소를 생성하는 물질이다. 2 개의 화합물의 조합으로는, 커플러와 아닐린류의 조합, 커플러와 페놀류의 조합 등을 들 수 있다.
커플러로는, 예를 들어 4-아미노안티피린 (4-AA), 3-메틸-2-벤조티아졸리논하이드라존 등을 들 수 있다.
아닐린류로는, N-(3-술포프로필)아닐린, N-에틸-N-(2-하이드록시-3-술포프로필)-3-메틸아닐린 (TOOS), N-에틸-N-(2-하이드록시-3-술포프로필)-3,5-디메틸아닐린 (MAOS), N-에틸-N-(2-하이드록시-3-술포프로필)-3,5-디메톡시아닐린 (DAOS), N-에틸-N-(3-술포프로필)-3-메틸아닐린 (TOPS), N-(2-하이드록시-3-술포프로필)-3,5-디메톡시아닐린 (HDAOS), N,N-디메틸-3-메틸아닐린, N,N-디(3-술포프로필)-3,5-디메톡시아닐린, N-에틸-N-(3-술포프로필)-3-메톡시아닐린, N-에틸-N-(3-술포프로필)아닐린, N-에틸-N-(3-술포프로필)-3,5-디메톡시아닐린, N-(3-술포프로필)-3,5-디메톡시아닐린, N-에틸-N-(3-술포프로필)-3,5-디메틸아닐린, N-에틸-N-(2-하이드록시-3-술포프로필)-3-메톡시아닐린, N-에틸-N-(2-하이드록시-3-술포프로필)아닐린, N-에틸-N-(3-메틸페닐)-N'-숙시닐에틸렌디아민 (EMSE), N-(3,5-디메톡시페닐)-N'-숙시닐에틸렌디아민 (DOSE), N-에틸-N-(3-메틸페닐)-N'-아세틸에틸렌디아민, N-에틸-N-(2-하이드록시-3-술포프로필)-4-플루오로-3,5-디메톡시아닐린 (F-DAOS), N-[2-(숙시닐아미노)에틸]-2-메톡시-5-메틸아닐린 (MASE), N-에틸-N-[2-(숙시닐아미노)에틸]-2-메톡시-5-메틸아닐린 (Et-MASE) 등을 들 수 있다.
페놀류로는, 페놀, 4-클로로페놀, 3-메틸페놀, 3-하이드록시-2,4,6-트리요드벤조산 (HTIB) 등을 들 수 있다.
과산화수소의 측정에 있어서, 과산화 활성 물질의 농도는, 측정에 적합한 농도이면 특별히 제한은 없지만, 과산화 활성 물질로서 퍼옥시다아제를 사용하는 경우에는 1 ∼ 100 kU/ℓ 가 바람직하다. 또, 산화 발색형 색원체의 농도는, 과산화수소의 측정에 적합한 농도이면 특별히 제한은 없지만, 0.01 ∼ 10 g/ℓ 가 바람직하다.
본 발명의 HDL3-C 의 측정 방법에 있어서, 콜레스테롤 측정용 효소로서, 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소 및 콜레스테롤 탈수소 효소의 조합을 사용하는 경우에는, HDL3-C 의 측정은 반응에 의해 생성된 환원형 보조 효소의 양을 측정함으로써 실시할 수 있다.
생성된 환원형 보조 효소의 양은, 예를 들어 흡광도법이나 환원형 보조 효소 측정용 시약을 사용하여 측정할 수 있다. 흡광도법으로는, 예를 들어 전술한 흡광도법 등을 들 수 있다. 환원형 보조 효소 측정용 시약은, 생성된 환원형 보조 효소를 검출 가능한 물질로 변환시키기 위한 시약이다. 검출 가능한 물질로는, 예를 들어 색소 등을 들 수 있다.
환원형 보조 효소 측정용 시약으로는, 예를 들어 디아포라아제, 전자 캐리어 및 환원 발색형 색원체를 함유하는 시약, 환원형 보조 효소 산화 효소를 함유하는 시약, 환원형 보조 효소 산화 효소 및 과산화수소 측정용 시약을 함유하는 시약 등을 들 수 있다.
환원형 보조 효소 측정용 시약으로서, 디아포라아제, 전자 캐리어 및 환원 발색형 색원체를 함유하는 시약을 사용하는 경우에는, 환원 발색형 색원체가 변환되어 생성된 색소를 정량함으로써, 환원형 보조 효소를 정량할 수 있다. 전자 캐리어로는, 예를 들어 1-메톡시-5-메틸페나듐메틸설페이트 등을 들 수 있다.
환원 발색형 색원체로는, 예를 들어 3-(4,5-디메틸-2-티아졸릴)-2,5-디페닐-2H-테트라졸륨브로마이드 (MTT), 2-(4-요드페닐)-3-(4-니트로페닐)-5-(2,4-디술포페닐)-2H-테트라졸륨모노나트륨염 (WST-1), 2-(4-요드페닐)-3-(2,4-디니트로페닐)-5-(2,4-디술포페닐)-2H-테트라졸륨모노나트륨염 (WST-3) 등을 들 수 있다.
환원형 보조 효소 측정용 시약으로서, 환원형 보조 효소 산화 효소를 함유하는 시약을 사용하는 경우에는, 환원 발색형 색원체와 환원형 보조 효소 산화 효소의 반응에 의해 생성되는 과산화수소를 측정함으로써, 환원형 보조 효소를 측정할 수 있다. 생성된 과산화수소는, 예를 들어 전술한 과산화수소 전극을 사용하는 방법이나, 전술한 과산화수소 측정용 시약을 사용하는 방법 등에 의해 측정할 수 있다. 과산화수소 측정용 시약을 사용하는 방법을 이용하여 환원형 보조 효소를 측정하는 경우에는, 환원형 보조 효소 측정용 시약은, 환원형 보조 효소 산화 효소 및 과산화수소 측정용 시약을 함유한다.
<HDL2 중의 콜레스테롤의 측정 방법>
HDL 는, HDL2 와 HDL3 의 2 개의 소분획으로 이루어지는 리포 단백질이므로, 검체 중의 HDL 콜레스테롤 (총 HDL 콜레스테롤) 을 측정하여, 당해 총 HDL 콜레스테롤 농도에서, 본 발명의 HDL3-C 의 측정 방법에 의해 측정되는 검체 중의 HDL3-C농도를 뺌으로써, 당해 검체 중의 HDL2 콜레스테롤 (이하, HDL2-C 라고 기재한다) 농도를 측정할 수 있다.
즉, 본 발명의 검체 중의 HDL2-C 의 측정 방법은, 이하의 공정을 포함하는 방법이다.
(1) 검체 중의 HDL 중의 콜레스테롤을 측정하는 공정 ;
(2) 본 발명의 HDL3-C 의 측정 방법에 의해 검체 중의 HDL3-C 를 측정하는 공정 ;
(3) 상기 (1) 공정에서 측정한 측정값에서 (2) 공정에서 측정한 측정값을 빼는 공정.
공정 (1) 에 있어서의 HDL 중의 콜레스테롤 (이하, HDL-C 라고 기재한다) 의 측정은, 검체 중의 총 HDL 중의 콜레스테롤의 측정을 가능하게 하는 방법이면, 특별히 제한은 없으며, 예를 들어 일본 공개특허공보 평8-131197호, WO2004/035816호 팜플렛, WO2006/118199호 팜플렛 등에 기재된 방법에 의해 실시할 수 있다. 또, HDL-C 의 측정은, 시판되는 HDL-C 측정용 시약, 및 HDL-C 측정용 키트를 사용하여 실시할 수도 있다. 시판되는 HDL-C 측정용 시약, 및 HDL-C 측정 키트로는, 예를 들어 「메타보리드 HDL-C」(쿄와 메덱스사 제조), 「데타미나 L HDL-C」(쿄와 메덱스사 제조) 등을 들 수 있다.
공정 (2) 에 있어서의 HDL3-C 의 측정은, 전술한 HDL3-C 측정 방법에 의해 실시할 수 있다.
<HDL3-C 측정용 시약>
본 발명의 HDL3-C 측정용 시약은, 본 발명의 HDL3-C 측정 방법에 사용되는 시약이다.
본 발명의 HDL3-C 측정용 시약의 양태를 이하에 기재한다.
·측정용 시약 1
콜레스테롤 에스테르 가수분해 효소, 콜레스테롤 산화 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 시약
·측정용 시약 2
콜레스테롤 에스테르 가수분해 효소, 콜레스테롤 산화 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, (c) 덱스트란황산 또는 그 염, 및 과산화수소 측정용 시약을 함유하는 시약
·측정용 시약 3
콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소, 콜레스테롤 탈수소 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 시약
·측정용 시약 4
콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소, 콜레스테롤 탈수소 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, (c) 덱스트란황산 또는 그 염, 및 환원형 보조 효소 측정용 시약을 함유하는 시약
본 발명의 HDL3-C 측정용 시약은, 동결 건조된 상태이어도 되고, 수성 매체에 용해된 상태이어도 된다. 동결 건조된 상태의 시약을 사용하여 검체 중의 HDL3-C 를 측정하는 경우에는, 당해 시약은 수성 매체에 용해시켜 사용된다.
본 발명의 HDL3-C 측정용 시약이 수성 매체에 용해된 상태인 경우, 시약 중의 각 요소의 농도는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없으며, 예를 들어, 반응액 중의 농도가 이하에 나타내는 농도가 되는 농도이다.
·콜레스테롤 에스테르 가수분해 효소 : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 산화 효소 : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 탈수소 효소 : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·산화형 보조 효소 : 통상적으로 0.01 ∼ 400 m㏖/ℓ, 바람직하게는 0.1 ∼ 100 m㏖/ℓ.
·2 가의 금속염 : 통상적으로 12 ∼ 20 m㏖/ℓ, 바람직하게는 13 ∼ 19 m㏖/ℓ.
·황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염 : 통상적으로 5 ∼ 21 m㏖/ℓ, 바람직하게는 6 ∼ 18 m㏖/ℓ.
·덱스트란황산 또는 그 염 : 통상적으로 0.75 ∼ 2.6 g/ℓ, 바람직하게는 1.0 ∼ 2.3 g/ℓ.
본 발명의 HDL3-C 측정용 시약이 동결 건조 상태인 경우, 시약 중의 각 요소의 함량은, 본 발명의 HDL3-C 의 측정을 가능하게 하는 함량이면 특별히 제한은 없으며, 예를 들어 반응액 중에서의 농도가 상기의 농도가 되는 함량이다.
본 발명의 HDL3-C 측정용 시약 중의 각 요소의 함량으로는, 수성 매체에 의해 용해된 상태에서의 각 요소의 농도가, 예를 들어 이하의 농도가 되는 함량이다.
·콜레스테롤 에스테르 가수분해 효소 : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 산화 효소 : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 탈수소 효소 : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·산화형 보조 효소 : 통상적으로 0.01 ∼ 400 m㏖/ℓ, 바람직하게는 0.1 ∼ 100 m㏖/ℓ.
·2 가의 금속염 : 통상적으로 12 ∼ 20 m㏖/ℓ, 바람직하게는 13 ∼ 19 m㏖/ℓ.
·황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염 : 통상적으로 5 ∼ 21 m㏖/ℓ, 바람직하게는 6 ∼ 18 m㏖/ℓ.
·덱스트란황산 또는 그 염 : 통상적으로 0.75 ∼ 2.6 g/ℓ, 바람직하게는 1.0 ∼ 2.3 g/ℓ.
<HDL3-C 측정용 키트>
본 발명의 HDL3-C 측정용 시약은, 본 발명의 HDL3-C 측정 방법에 이용되며, 보존, 유통 및 사용에 적합한 키트의 형태를 취할 수 있다. 본 발명의 HDL3-C 측정용 키트로는, 예를 들어 2 시약계의 키트, 3 시약계의 키트 등을 들 수 있지만, 제 1 시약과 제 2 시약으로 이루어지는 2 시약계의 키트가 바람직하다.
제 1 시약과 제 2 시약으로 이루어지는 2 시약계의 HDL3-C 측정용 키트에 있어서는, 콜레스테롤 에스테르 가수분해 효소는, 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유된다. 콜레스테롤 산화 효소는, 제 2 시약에 함유되는 것이 바람직하다. 산화형 보조 효소는, 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유된다. 콜레스테롤 탈수소 효소는, 제 2 시약에 함유되는 것이 바람직하다. 2 가의 금속염은, 제 1 시약에 함유되는 것이 바람직하다. 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염은, 제 1 시약에 함유되는 것이 바람직하다. 덱스트란황산 또는 그 염은, 제 1 시약에 함유되는 것이 바람직하다.
과산화수소 측정용 시약은, 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유되어도 되지만, 당해 시약이 산화 커플링형 색원체를 함유하는 경우에는, 산화 커플링형 색원체의 2 개의 화합물, 즉, 커플러와 아닐린류, 또는 커플러와 페놀류는 각각 다른 시약에 함유되는 양태가 바람직하다.
환원형 보조 효소 측정용 시약은, 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유된다.
본 발명의 HDL3-C 측정용 키트의 양태를 이하에 기재한다.
·측정용 키트 1
제 1 시약
(a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 시약
제 2 시약
콜레스테롤 에스테르 가수분해 효소, 및 콜레스테롤 산화 효소를 함유하는 시약
·측정용 키트 2
제 1 시약
(a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, (c) 덱스트란황산 또는 그 염, 및 과산화수소 측정용 시약을 함유하는 시약
제 2 시약
콜레스테롤 에스테르 가수분해 효소, 콜레스테롤 산화 효소를 함유하는 시약, 및 과산화수소 측정용 시약을 함유하는 시약
·측정용 키트 3
제 1 시약
(a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 시약
제 2 시약
콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소, 및 콜레스테롤 탈수소 효소를 함유하는 시약
·측정용 키트 4
제 1 시약
(a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, (c) 덱스트란황산 또는 그 염, 및 환원형 보조 효소 측정용 시약을 함유하는 시약
제 2 시약
콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소, 콜레스테롤 탈수소 효소, 및 환원형 보조 효소 측정용 시약을 함유하는 시약
본 발명의 HDL3-C 측정용 키트는, 동결 건조된 상태이어도 되고, 수성 매체에 용해된 상태에서도 된다. 동결 건조된 상태의 키트를 사용하여 검체 중의 HDL3-C 를 측정하는 경우에는, 당해 키트는 수성 매체에 용해시켜 사용된다. 그 수성 매체로는, 예를 들어 전술한 수성 매체 등을 들 수 있다.
본 발명의 HDL3-C 측정용 키트가 수성 매체에 용해된 상태인 경우, 키트의 제 1 시약 또는 제 2 시약 중의 각 요소의 농도는, 본 발명의 HDL3-C 의 측정을 가능하게 하는 농도이면 특별히 제한은 없으며, 예를 들어 반응액 중의 농도가 이하에 나타내는 농도가 되는 농도이다.
·콜레스테롤 에스테르 가수분해 효소 (제 1 시약 또는 제 2 시약) : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 산화 효소 (제 2 시약) : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 탈수소 효소 (제 2 시약) : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·산화형 보조 효소 (제 1 시약 또는 제 2 시약) : 통상적으로 0.01 ∼ 400 m㏖/ℓ, 바람직하게는 0.1 ∼ 100 m㏖/ℓ.
·2 가의 금속염 (제 1 시약) : 통상적으로 12 ∼ 20 m㏖/ℓ, 바람직하게는 13 ∼ 19 m㏖/ℓ.
·황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염 (제 1 시약) : 통상적으로 5 ∼ 21 m㏖/ℓ, 바람직하게는 6 ∼ 18 m㏖/ℓ.
·덱스트란황산 또는 그 염 (제 1 시약) : 통상적으로 0.75 ∼ 2.6 g/ℓ, 바람직하게는 1.0 ∼ 2.3 g/ℓ.
본 발명의 HDL3-C 측정용 키트가 동결 건조 상태인 경우, 키트의 제 1 시약 또는 제 2 시약 중의 각 요소의 함량은, 본 발명의 HDL3-C 의 측정을 가능하게 하는 함량이면 특별히 제한은 없으며, 예를 들어 반응액 중의 농도가 상기의 농도가 되는 함량이다.
본 발명의 HDL3-C 측정용 키트의 제 1 시약 또는 제 2 시약 중의 각 요소의 함량으로는, 수성 매체에 의해 용해된 상태에서의 각 요소의 농도가, 예를 들어 이하의 농도가 되는 함량이다.
·콜레스테롤 에스테르 가수분해 효소 (제 1 시약 또는 제 2 시약) : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 산화 효소 (제 2 시약) : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·콜레스테롤 탈수소 효소 (제 2 시약) : 통상적으로 0.001 ∼ 800 kU/ℓ, 바람직하게는 0.01 ∼ 300 kU/ℓ.
·산화형 보조 효소 (제 1 시약 또는 제 2 시약) : 통상적으로 0.01 ∼ 400 m㏖/ℓ, 바람직하게는 0.1 ∼ 100 m㏖/ℓ.
·2 가의 금속염 (제 1 시약) : 통상적으로 16 ∼ 27 m㏖/ℓ, 바람직하게는 17 ∼ 25 m㏖/ℓ.
·황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염 (제 1 시약) : 통상적으로 7 ∼ 28 m㏖/ℓ, 바람직하게는 8 ∼ 25 m㏖/ℓ.
·덱스트란황산 또는 그 염 (제 1 시약) : 통상적으로 1.0 ∼ 3.5 g/ℓ, 바람직하게는 1.3 ∼ 3.1 g/ℓ.
본 발명의 HDL3-C 측정용 시약 및 측정용 키트에는, 필요에 따라 수성 매체, 안정화제, 방부제, 영향 물질 소거제, 반응 촉진제 등이 함유되어도 된다. 수성 매체로는, 예를 들어 전술한 수성 매체 등을 들 수 있다. 안정화제로는, 예를 들어 에틸렌디아민4아세트산 (EDTA), 수쿠로오스, 염화칼슘, 콜산 또는 그 염 등을 들 수 있다. 방부제로는, 예를 들어 아지화나트륨, 항생 물질 등을 들 수 있다. 영향 물질 소거제로는, 예를 들어 아스코르브산의 영향을 소거하기 위한 아스코르브산옥시다아제 등을 들 수 있다. 반응 촉진제로는, 예를 들어 코리파아제, 포스포리파아제 등을 들 수 있다.
본 발명의 HDL3-C 측정용 시약 및 측정용 키트에 있어서는, 전술한 콜레스테롤 에스테르 가수분해 효소, 콜레스테롤 산화 효소, 산화형 보조 효소, 콜레스테롤 탈수소 효소, 2 가의 금속염, 알칼리 금속염 (황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염), 덱스트란황산 또는 그 염, 과산화수소 측정용 시약, 환원형 보조 효소 측정용 시약을 사용할 수 있다.
<HDL2-C 측정용 키트>
본 발명의 HDL2-C 측정용 키트는, 본 발명의 HDL2-C 의 측정 방법에 사용되는 키트이다. 본 발명의 HDL2-C 측정용 키트로는, 예를 들어 본 발명의 HDL3-C 측정용 시약과, HDL-C 측정용 시약을 포함하는 키트, 본 발명의 HDL3-C 측정용 키트의 제 1 시약 및 제 2 시약과, HDL-C 측정용 시약을 포함하는 키트 등을 들 수 있다. 본 발명의 HDL2-C 측정용 키트에 있어서의 본 발명의 HDL3-C 측정용 시약으로는, 본 발명의 HDL3-C 측정용 키트이어도 된다.
본 발명의 HDL2-C 측정용 키트에 있어서의 HDL-C 측정용 시약은, HDL-C 측정용 키트이어도 된다. HDL-C 측정용 시약, 및 HDL-C 측정용 키트는, HDL-C 의 측정을 가능하게 하는 시약, 및 키트이면 특별히 제한은 없으며, 예를 들어 일본 공개특허공보 평8-131197호, WO2004/035816호 팜플렛, WO2006/118199호 팜플렛 등에 기재된 HDL-C 측정용 시약, 및 HDL-C 측정용 키트 등을 들 수 있다. 또, HDL-C 측정용 시약, 및 HDL-C 측정용 키트로서, 시판되는 HDL-C 측정용 시약, 및 측정용 키트를 사용할 수도 있다. 시판되는 HDL-C 측정용 시약, 및 측정용 키트로는, 예를 들어 전술한 시판되는 HDL-C 측정용 시약, 및 HDL-C 측정용 키트 등을 들 수 있다.
이하, 실시예에 의해 본 발명을 보다 상세하게 설명하지만, 이들은 본 발명의 범위를 전혀 한정하는 것은 아니다. 또한, 본 실시예 및 비교예에 있어서는, 하기 메이커의 시약 및 효소를 사용하였다.
HEPES (VWR 사 제조), HSDA (도진 화학 연구소사 제조), PIPES (도진 화학 연구소사 제조), 콜산나트륨 (아크로스사 제조), 소 혈청 알부민 (BSA ; 셀라이언스사 제조), 4-아미노안티피린 (사이쿄 화성사 제조), 덱스트란황산나트륨 분자량 50 만 (메이토 산업사 제조), 덱스트란황산나트륨 분자량 4 만 (ICN 사 제조), 질산마그네슘 6 수화물 (칸토 화학사 제조), 염화칼슘 2 수화물 (와코 쥰야쿠사 제조), 황산나트륨 (칸토 화학사 제조), 염화나트륨 (와코 쥰야쿠사 제조), 염화칼륨 (와코 쥰야쿠사 제조), 염화리튬 (와코 쥰야쿠사 제조), 질산나트륨 (나카라이테스크사 제조), 탄산나트륨 (칸토 화학사 제조), 브롬화나트륨 (와코 쥰야쿠사 제조), 아세트산나트륨 3 수화물 (칸토 화학사 제조), 불화나트륨 (와코 쥰야쿠사 제조)
COO322 (콜레스테롤 산화 효소 ; 토요 방적사 제조), LPL311 (콜레스테롤 에스테르 가수분해 효소 ; 토요 방적사 제조), 퍼옥시다아제 (토요 방적사 제조)
또, 화학 수식 LPL311 은, 이하와 같이 조제한 것을 사용하였다.
HEPES 완충액 (pH 8.5, 0.15 ㏖/ℓ) 에 LPL311 을 33 g/ℓ 가 되도록 첨가하여 5 ℃ 로 냉각시킨 후, 선브라이트 VFM-4101 (니치유사 제조) 을 330 g/ℓ 가 되도록 첨가하여 다시 3 시간 반응시켰다. 얻어진 수식 효소 용액을 정제 분리하지 않고 그대로 화학 수식 LPL311 로서 사용하였다.
화학 수식 COO322 는, 이하와 같이 조제한 것을 사용하였다.
HEPES 완충액 (pH 8.0, 0.1 ㏖/ℓ) 에 COO322 를 50 g/ℓ 가 되도록 첨가하여 15 ℃ 로 냉각시킨 후, 선브라이트 VFM-4101 (니치유사 제조) 을 6.25 g/ℓ 가 되도록 첨가하여 다시 2 시간 반응시켰다. 얻어진 수식 효소 용액을 정제 분리하지 않고 그대로 화학 수식 COO322 로서 사용하였다.
실시예 1
·2 가의 금속염과 황산나트륨의 조합에 의한 HDL3-C 의 측정
이하의 제 1 시약 및 제 2 시약으로 이루어지는 HDL3-C 측정용 키트를 조제하였다. 표 1 에 나타내는 농도의 2 가의 금속염 (질산마그네슘 6 수화물 또는 염화칼슘 2 수화물), 및 황산나트륨을 함유하는 키트를 실시예 1(1) ∼ 1(11) 의 키트로 하였다.
제 1 시약
HEPES (pH 7.0) 10 m㏖/ℓ
HSDA 0.3 g/ℓ
콜산나트륨 0.75 g/ℓ
퍼옥시다아제 10 kU/ℓ
덱스트란황산나트륨 x g/ℓ (표 1 참조)
2 가의 금속염 y m㏖/ℓ (표 1 참조)
황산나트륨 z m㏖/ℓ (표 1 참조)
제 2 시약
PIPES (pH 7.0) 10 m㏖/ℓ
4-아미노안티피린 0.3 g/ℓ
콜산나트륨 6 g/ℓ
퍼옥시다아제 20 kU/ℓ
화학 수식 LPL311 0.2 kU/ℓ
화학 수식 COO322 7.6 kU/ℓ
[비교예 1]
이하의 제 1 시약 및 제 2 시약으로 이루어지는 HDL3-C 측정용 키트를 조제하였다. 표 1 에 나타내는 농도의 질산마그네슘 6 수화물을 함유하는 키트를 비교예 1(1) ∼ 1(3) 의 키트로 하였다.
제 1 시약
HEPES (pH 7.0) 10 m㏖/ℓ
HSDA 0.3 g/ℓ
콜산나트륨 0.75 g/ℓ
퍼옥시다아제 10 kU/ℓ
덱스트란황산나트륨 x g/ℓ (표 1 참조)
질산마그네슘 6 수화물 y m㏖/ℓ (표 1 참조)
제 2 시약
PIPES (pH 7.0) 10 m㏖/ℓ
4-아미노안티피린 0.3 g/ℓ
콜산나트륨 6 g/ℓ
퍼옥시다아제 20 kU/ℓ
화학 수식 LPL311 0.2 kU/ℓ
화학 수식 CHOD322 7.6 kU/ℓ
실시예 2
실시예 1(a) 의 키트를 사용해 이하와 같이 하여, 트리글리세리드가 200 ㎎/㎗ 이하인 인간 혈청 42 검체에 대하여, 각각의 검체 중의 HDL3-C 를 측정하여, 분획법과의 상관 계수를 산출하였다.
(1) 인간 혈청 검체와 실시예 1(a) 의 키트의 반응에 의한 당해 검체에 있어서의 「반응 흡광도」의 산출
히타치 7170S 형 자동 분석 장치를 이용하여 이하의 조작에 의해 「반응 흡광도」를 산출하였다.
인간 혈청을 검체로 하여 반응 셀에 (2 ㎕) 첨가하고, 이어서 각각 실시예 1(a) 의 키트의 제 1 시약 (0.15 ㎖) 을 첨가하여 반응 (제 1 반응) 을 개시시키고, 37 ℃ 에서 5 분간 가온하여, 반응 5 분 후의 반응액의 흡광도 (E1) 를 주파장 600 ㎚, 부파장 700 ㎚ 로 측정하였다. 이어서, 이 반응액에 각각 실시예 1(a) 의 키트의 제 2 시약 (0.05 ㎖) 을 첨가하여 다시 37 ℃ 에서 5 분간 가온하여 반응 (제 2 반응) 을 실시하고, 제 2 반응 5 분 후의 반응액의 흡광도 (E2) 를 주파장 600 ㎚, 부파장 700 ㎚ 로 측정하고, E2 에서 E1 을 빼, 흡광도 변화 (ΔE 혈청검 체) 를 산출하였다. 또, 인간 혈청 대신에 생리 식염수를 검체로 사용하여 동일한 측정을 실시하여, 흡광도 변화 (ΔE 블랭크) 를 산출하였다. 마지막으로, 하기 (식 1) 에 의해 각 인간 혈청 검체에 있어서의 「반응 흡광도」를 산출하였다.
[수학식 1]
반응 흡광도 = ΔE면적검체 - ΔE블랭크 (식 1)
(2) 분획법에 의한 인간 혈청 검체 중의 HDL3-C 의 측정
상기 (1) 과 동일한 인간 혈청 검체를 이용하여, Journal of Lipid Research vol.49, p.1130-1136(2008) 에 기재된 방법 (분획법) 에 의해 각 검체 중의 HDL3 을 분리하고, 얻어진 HDL3 분획 중의 콜레스테롤량을 데타미나 L TCⅡ (쿄와 메덱스사 제조) 를 이용하여 측정하였다.
또, 참고로, 동일한 인간 혈청 검체를 이용하여, Clinical Chemistry, Vol.45, No.10, pp.1803-1812(1999) 에 기재된 DCM (Designated Comparison Method) 에 의해 각 검체 중의 HDL 을 분리하고, 얻어진 HDL 분획 중의 콜레스테롤을 데타미나 L TCⅡ (쿄와 메덱스사 제조) 를 이용하여 측정하였다.
(3) 본 발명의 측정 방법과 분획법의 상관
실시예 1(1) 의 키트를 사용한 측정에 있어서의 「반응 흡광도」와, (2) 의 분획법에 의한 측정값 사이의 상관 계수를 표 1 에 기재한다.
마찬가지로, 실시예 1(1) 의 키트 대신에 실시예 1(2) ∼ 1(11) 의 키트를 사용하여 분획법에 의한 측정값 사이의 상관 계수를 결정하였다. 상관 관계를 표 1 에 기재한다.
[비교예 2]
실시예 1(1) 대신에 비교예 1(1) ∼ 1(3) 의 각 키트를 사용한 것 이외에는 실시예 2 의 방법과 동일한 방법에 의해 비교예 1(1) ∼ 1(3) 의 각 키트를 사용한 측정에 있어서의 「반응 흡광도」와, 분획법에 의한 측정값 사이의 상관 계수를 결정하였다. 상관 계수를 표 1 에 기재한다.
표 1 로부터, 제 1 시약 중에 알칼리 금속염인 황산나트륨을 함유하지 않는 비교예 1(1) ∼ 1(3) 의 키트를 사용한 측정에 있어서는, 분획법에 의한 HDL3-C 측정과의 사이에 양호한 상관 관계는 보이지 않고, 오히려 HDL-C 측정과의 사이에 양호한 상관 관계를 보이는 것이 판명되었다.
한편, 제 1 시약에 황산나트륨 및 2 가의 금속염을 함유하는 실시예 1(1) ∼ 1(11) 의 키트를 사용한 측정에 있어서는, 분획법에 의한 HDL3-C 측정과의 사이에 양호한 상관 관계를 보이는 것이 판명되었다.
실시예 3
·마그네슘염 농도와 황산나트륨 농도의 검토
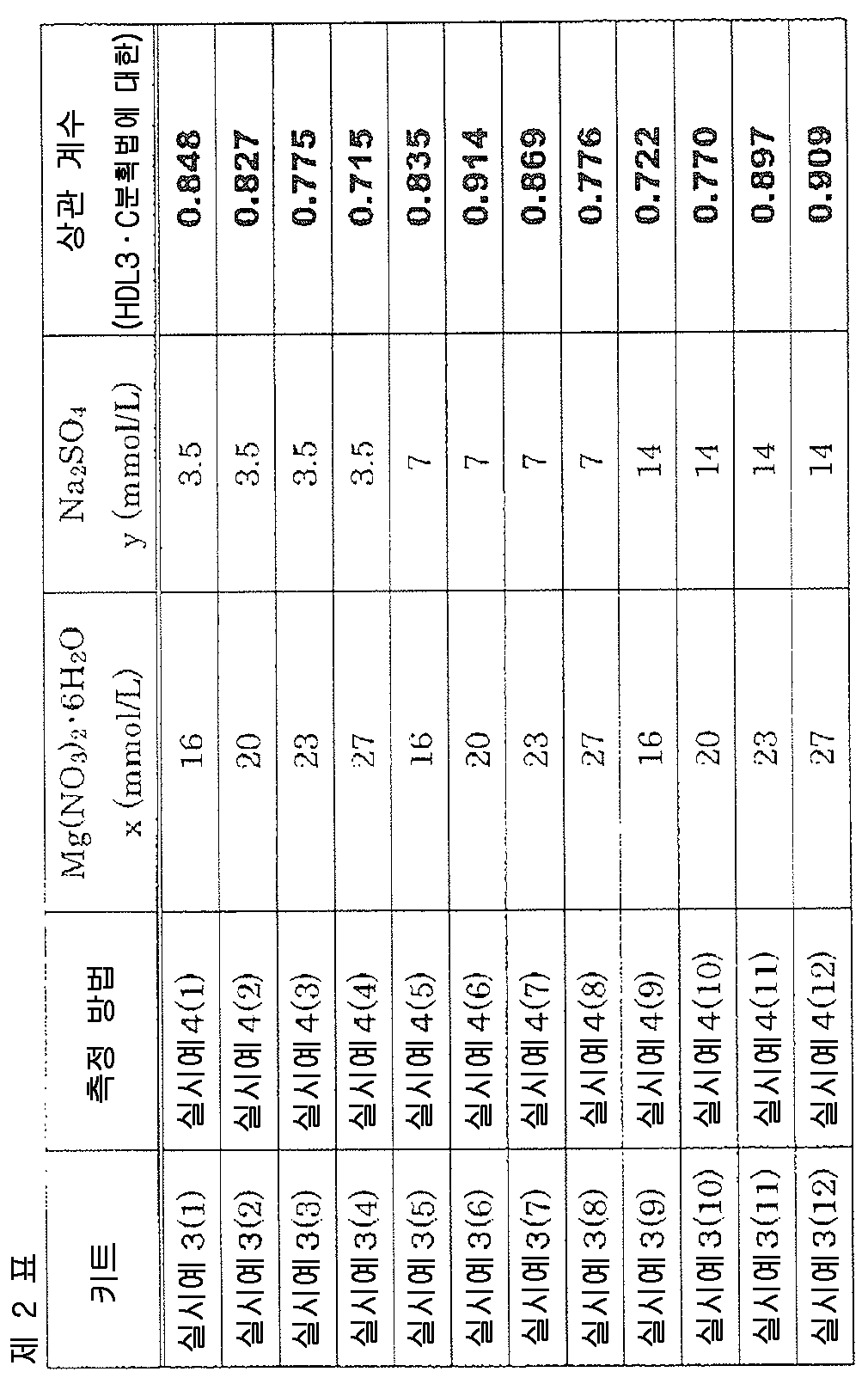
이하의 제 1 시약 및 제 2 시약으로 이루어지는 HDL3-C 측정용 키트를 조제하였다. 표 2 에 나타내는 농도의 질산마그네슘 6 수화물, 및 황산나트륨을 함유하는 키트를 실시예 3(1) ∼ 3(12) 의 키트로 하였다.
제 1 시약
HEPES (pH 7.0) 10 m㏖/ℓ
HSDA 0.3 g/ℓ
콜산나트륨 0.75 g/ℓ
퍼옥시다아제 10 kU/ℓ
덱스트란황산나트륨 (분자량 50 만) 2 g/ℓ
질산마그네슘 6 수화물 x m㏖/ℓ (표 2 참조)
황산나트륨 y m㏖/ℓ (표 2 참조)
제 2 시약
PIPES (pH 7.0) 10 m㏖/ℓ
4-아미노안티피린 0.3 g/ℓ
콜산나트륨 6 g/ℓ
퍼옥시다아제 20 kU/ℓ
화학 수식 LPL311 0.2 kU/ℓ
화학 수식 COO322 7.6 kU/ℓ
실시예 4
실시예 1(1) 대신에 실시예 3(1) ∼ 3(12) 의 각 키트를 사용한 것 이외에는 실시예 2 의 방법과 동일한 방법에 의해 실시예 3(1) ∼ 3(12) 의 각 키트를 사용한 측정에 있어서의 반응 흡광도와, 분획법에 의한 측정값 사이의 상관 계수를 결정하였다. 상관 계수를 표 2 에 기재한다.
표 2 로부터, 제 1 시약 중에 마그네슘염, 및 황산나트륨을 함유하는 실시예 3(1) ∼ 3(12) 의 키트를 사용한 측정에 있어서는, 분획법에 의한 HDL3-C 측정과의 사이에 양호한 상관 관계를 보이는 것이 판명되었다.
실시예 5
·알칼리 금속염의 검토
이하의 제 1 시약 및 제 2 시약으로 이루어지는 HDL3-C 측정용 키트를 조제하였다. 표 3 에 나타내는 알칼리 금속염 및 그 농도를 사용한 키트를 실시예 5(1a) ∼ 5(9c) 의 키트로 하였다.
제 1 시약
HEPES (pH 7.0) 10 m㏖/ℓ
HSDA 0.3 g/ℓ
콜산나트륨 0.75 g/ℓ
퍼옥시다아제 10 kU/ℓ
덱스트란황산나트륨 (분자량 50 만) 2 g/ℓ
질산마그네슘 6 수화물 20 m㏖/ℓ
알칼리 금속염 (표 3 참조)
제 2 시약
PIPES (pH 7.0) 10 m㏖/ℓ
4-아미노안티피린 0.3 g/ℓ
콜산나트륨 6 g/ℓ
퍼옥시다아제 20 kU/ℓ
화학 수식 LPL311 0.2 kU/ℓ
화학 수식 COO322 7.6 kU/ℓ
실시예 6
실시예 1(1) 대신에 실시예 5(1a) ∼ 5(9c) 의 각 키트를 사용한 것 이외에는 실시예 2 의 방법과 동일한 방법에 의해 실시예 5(1a) ∼ 5(9c) 의 각 키트를 사용한 측정에 있어서의 반응 흡광도와, 분획법에 의한 측정값 사이의 상관 계수를 결정하였다. 상관 계수를 표 3 에 기재한다.
표 3 으로부터, 제 1 시약 중에 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염을 함유하는 키트를 사용한 측정에 있어서는, 분획법에 의한 HDL3-C 측정과의 사이에 양호한 상관 관계를 보이는 것이 판명되었다.
실시예 7
·검체 중의 HDL3-C 의 정량
사람의 신선한 혈청 5 검체에 대하여, 각 검체 중의 HDL3-C 농도를 분획법, 및 본 발명의 실시예 3(6) 및 실시예 3(11) 의 키트를 사용하는 방법에 의해 이하의 순서에 따라 결정하였다.
(1) 분획법을 사용한 HDL3-C 의 정량
Journal of Lipid Research vol.49, p.1130-1136(2008) 에 기재된 방법 (분획법) 에 의해 각 검체 중의 HDL3 를 분리하고, 얻어진 HDL3 분획 중의 콜레스테롤을 데타미나 L TCⅡ (쿄와 메덱스사 제조) 를 이용하여 측정하여, 각 검체 중의 HDL3-C 농도를 결정하였다.
(2) 실시예 3(6) 및 실시예 3(11) 의 키트를 사용한 HDL3-C 의 정량
분획법에 의한 측정에 의해 HDL3-C 농도가 16.1 ㎎/㎗ 인 것이 판명된 혈청 표준액을 검량선 작성용 샘플로 하였다. 실시예 2 의 (1) 에 기재된 측정 방법과 동일하게 하여 히타치 7170S 자동 분석 장치에 의해 실시예 3(6) 의 키트를 사용하여 검량선 작성용 샘플 검체의 반응 흡광도를 측정하여, HDL3-C 농도와 반응 흡광도 사이의 관계를 나타내는 검량선을 작성하였다.
상기 검량선 작성용 샘플 대신에 인간 혈청 5 검체를 이용하여 실시예 2 의 (1) 에 기재된 방법과 동일한 방법에 의해 측정을 실시하여, 얻어진 측정값과 먼저 작성된 검량선으로부터 각 검체 중의 HDL3-C 농도를 결정하였다.
실시예 3(6) 의 키트 대신에 실시예 3(11) 의 키트를 사용하여 동일한 방법에 의해 동일한 인간 혈청 5 검체 중의 HDL3-C 농도를 결정하였다.
분획법을 이용하여 결정된 HDL3-C 농도, 실시예 3(6) 및 실시예 3(11) 의 키트를 사용하여 결정된 HDL3-C 농도를 표 4 에 나타낸다.
표 4 로부터, 본 발명의 키트를 사용하는 측정 방법에 의해 결정된 HDL3-C 농도가, 분획법에 의해 결정된 HDL3-C 농도와 거의 일치하는 것이 판명되었다. 따라서, 본 발명의 키트를 사용하는 측정 방법에 의해 인간 혈청 중의 HDL3-C 를 정확하게 측정할 수 있는 것이 판명되었다.
산업상 이용가능성
본 발명에 의해 관동맥 질환 등의 진단에 유효한 HDL 소분획 중의 콜레스테롤의 측정 방법, 측정용 시약 및 측정용 키트가 제공된다.
Claims (19)
- 검체와, (1) 콜레스테롤 에스테르 가수분해 효소 및 콜레스테롤 산화 효소의 조합, 또는 (2) 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소 및 콜레스테롤 탈수소 효소의 조합을 (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 수성 매체 중에서 반응시켜, HDL3 이외의 리포 단백질을 분리 제거하지 않고, 생성되는 물질 또는 소비되는 물질을 측정하는 것을 특징으로 하는 검체 중의 HDL3 중의 콜레스테롤의 측정 방법.
- 제 1 항에 있어서,
2 가의 금속염이 마그네슘염 또는 칼슘염인 방법. - 제 1 항 또는 제 2 항에 있어서,
덱스트란황산 또는 그 염의 반응액 중의 농도가 0.75 ∼ 2.6 g/ℓ 인 방법. - 제 1 항 내지 제 3 항 중 어느 한 항에 있어서,
반응액 중의 2 가의 금속염 유래의 2 가의 금속 이온의 농도가 12 ∼ 20 m㏖/ℓ 이고, 반응액 중의 알칼리 금속염 유래의 알칼리 금속 이온의 농도가 5 ∼ 21 m㏖/ℓ 인 방법. - 이하의 공정을 포함하는 것을 특징으로 하는 검체 중의 HDL2 중의 콜레스테롤의 측정 방법.
(1) 검체 중의 고밀도 리포 단백질 (HDL) 중의 콜레스테롤을 측정하는 공정 ;
(2) 제 1 항 내지 제 4 항 중 어느 한 항에 기재된 측정 방법에 의해 검체 중의 HDL3 중의 콜레스테롤을 측정하는 공정 ;
(3) 상기 (1) 공정에서 측정한 측정값에서 (2) 공정에서 측정한 측정값을 빼는 공정 ; - 제 1 항 내지 제 4 항 중 어느 한 항에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 시약으로서, 콜레스테롤 에스테르 가수분해 효소, 콜레스테롤 산화 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, (c) 덱스트란황산 또는 그 염, 및 과산화수소 측정용 시약을 함유하는 것을 특징으로 하는 검체 중의 HDL3 중의 콜레스테롤의 측정용 시약.
- 제 1 항 내지 제 4 항 중 어느 한 항에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 시약으로서, 콜레스테롤 에스테르 가수분해 효소, 산화형 보조 효소, 콜레스테롤 탈수소 효소, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 함유하는 것을 특징으로 하는 검체 중의 HDL3 중의 콜레스테롤의 측정용 시약.
- 제 7 항에 있어서,
추가로, 환원형 보조 효소 측정용 시약을 포함하는 시약. - 제 6 항 내지 제 8 항 중 어느 한 항에 있어서,
2 가의 금속염이 마그네슘염 또는 칼슘염인 시약. - 제 6 항 내지 제 9 항 중 어느 한 항에 있어서,
덱스트란황산 또는 그 염이 반응액 중에서의 농도가 0.75 ∼ 2.6 g/ℓ 가 되는 함량으로 함유되는 시약. - 제 6 항 내지 제 10 항 중 어느 한 항에 있어서,
2 가의 금속염이, 반응액 중에서의 2 가의 금속염 유래의 2 가의 금속 이온의 농도가 12 ∼ 20 m㏖/ℓ 가 되는 함량으로 함유되고, 알칼리 금속염이, 반응액 중에서의 알칼리 금속염 유래의 알칼리 금속 이온의 농도가 5 ∼ 21 m㏖/ℓ 가 되는 함량으로 함유되는 시약. - 제 1 시약 및 제 2 시약을 함유하는, 제 1 항 내지 제 4 항 중 어느 한 항에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 키트로서, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 제 1 시약에 함유하고, 콜레스테롤 산화 효소를 제 2 시약에 함유하고, 과산화수소 측정용 시약을 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하고, 콜레스테롤 에스테르 가수분해 효소를 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하는 것을 특징으로 하는 키트.
- 제 1 시약 및 제 2 시약을 함유하는, 제 1 항 내지 제 4 항 중 어느 한 항에 기재된 측정 방법에 의해 HDL3 이외의 리포 단백질을 분리 제거하지 않고, 검체 중의 HDL3 중의 콜레스테롤을 측정하기 위한 키트로서, (a) 2 가의 금속염, (b) 황산염, 질산염, 탄산염, 아세트산염, 및 할로겐화물로 이루어지는 군에서 선택되는 알칼리 금속염, 및 (c) 덱스트란황산 또는 그 염을 제 1 시약에 함유하고, 콜레스테롤 탈수소 효소를 제 2 시약에 함유하고, 산화형 보조 효소를 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하고, 콜레스테롤 에스테르 가수분해 효소를 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하는 것을 특징으로 하는 키트.
- 제 13 항에 있어서,
추가로, 환원형 보조 효소 측정용 시약을 제 1 시약, 제 2 시약 중 어느 하나 또는 양방에 함유하는 키트. - 제 12 항 내지 제 14 항 중 어느 한 항에 있어서,
2 가의 금속염이 마그네슘염 또는 칼슘염인 키트. - 제 12 항 내지 제 15 항 중 어느 한 항에 있어서,
덱스트란황산 또는 그 염이 반응액 중에서의 농도가 0.75 ∼ 2.6 g/ℓ 가 되는 함량으로 함유되는 키트. - 제 12 항 내지 제 16 항 중 어느 한 항에 있어서,
2 가의 금속염이 반응액 중에서의 2 가의 금속염 유래의 2 가의 금속 이온의 농도가 12 ∼ 20 m㏖/ℓ 가 되는 함량으로 함유되고, 알칼리 금속염이, 반응액 중에서의 알칼리 금속염 유래의 알칼리 금속 이온의 농도가 5 ∼ 21 m㏖/ℓ 가 되는 함량으로 함유되는 키트. - 제 6 항 내지 제 11 항 중 어느 한 항에 기재된 HDL3 중의 콜레스테롤 측정용 시약과, HDL 콜레스테롤 측정용 시약을 포함하는 것을 특징으로 하는 검체 중의 HDL2 중의 콜레스테롤의 측정용 키트.
- 제 12 항 내지 제 17 항 중 어느 한 항에 기재된 HDL3 중의 콜레스테롤 측정용 키트의 제 1 시약 및 제 2 시약과, HDL 콜레스테롤 측정용 시약을 포함하는 것을 특징으로 하는 검체 중의 HDL2 중의 콜레스테롤의 측정용 키트.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2011-057959 | 2011-03-16 | ||
| JP2011057959 | 2011-03-16 | ||
| PCT/JP2012/001820 WO2012124340A1 (ja) | 2011-03-16 | 2012-03-15 | Hdl亜分画中のコレステロールの測定方法、測定用試薬及び測定用キット |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20140001996A true KR20140001996A (ko) | 2014-01-07 |
| KR101924663B1 KR101924663B1 (ko) | 2018-12-03 |
Family
ID=46830423
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020137023141A KR101924663B1 (ko) | 2011-03-16 | 2012-03-15 | Hdl 소분획 중의 콜레스테롤의 측정 방법, 측정용 시약 및 측정용 키트 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9080201B2 (ko) |
| EP (1) | EP2687606B1 (ko) |
| JP (1) | JP5969978B2 (ko) |
| KR (1) | KR101924663B1 (ko) |
| CN (1) | CN103415623B9 (ko) |
| CA (1) | CA2828934C (ko) |
| WO (1) | WO2012124340A1 (ko) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015030236A1 (ja) * | 2013-08-30 | 2015-03-05 | 積水メディカル株式会社 | 高比重リポ蛋白中のコレステロール測定方法および該方法に用いる試薬 |
| CN109813921B (zh) * | 2019-02-25 | 2022-04-19 | 安徽大千生物工程有限公司 | 基于多克隆抗体制备的hdl3免疫比浊法检测试剂盒及其制备使用方法 |
| CN111534568B (zh) * | 2020-05-11 | 2021-08-31 | 中拓生物有限公司 | 一种血清高密度脂蛋白胆固醇测定试剂盒 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2600065B2 (ja) * | 1994-03-08 | 1997-04-16 | 協和メデックス株式会社 | 高密度リポ蛋白中のコレステロールの定量法 |
| JP2799835B2 (ja) | 1995-01-31 | 1998-09-21 | 第一化学薬品株式会社 | コレステロールの定量方法 |
| JP4708531B2 (ja) | 2000-06-07 | 2011-06-22 | シスメックス株式会社 | Hdl亜画分中のコレステロールの測定法 |
| JP4498143B2 (ja) | 2002-10-16 | 2010-07-07 | 協和メデックス株式会社 | 高密度リポ蛋白中のコレステロールの測定方法および試薬 |
| AU2003301324A1 (en) * | 2002-10-16 | 2004-05-04 | Kyowa Medex Co., Ltd. | Method and reagent for measuring cholesterol in high-density lipoproteins |
| TWI372783B (en) | 2005-04-27 | 2012-09-21 | Kyowa Medex Co Ltd | A process for measuring the cholesterol in high density lipoprotein |
| US20090181413A1 (en) * | 2005-09-30 | 2009-07-16 | Denka Seiken Co., Ltd. | Simultaneous and differential quantification of two target analytes in biological sample |
| JP5500777B2 (ja) * | 2008-03-06 | 2014-05-21 | デンカ生研株式会社 | Hdl3−cの測定方法及びhdl3−c測定用試薬 |
| US8932865B2 (en) * | 2010-07-23 | 2015-01-13 | Denka Seiken Co., Ltd. | Method for quantifying the amount of cholesterol in high-density lipoprotein 3 |
-
2012
- 2012-03-15 WO PCT/JP2012/001820 patent/WO2012124340A1/ja active Application Filing
- 2012-03-15 CA CA2828934A patent/CA2828934C/en active Active
- 2012-03-15 JP JP2013504575A patent/JP5969978B2/ja active Active
- 2012-03-15 KR KR1020137023141A patent/KR101924663B1/ko active IP Right Grant
- 2012-03-15 US US14/002,816 patent/US9080201B2/en active Active
- 2012-03-15 EP EP12757569.4A patent/EP2687606B1/en not_active Not-in-force
- 2012-03-15 CN CN201280012906.4A patent/CN103415623B9/zh active Active
Also Published As
| Publication number | Publication date |
|---|---|
| KR101924663B1 (ko) | 2018-12-03 |
| US20130344518A1 (en) | 2013-12-26 |
| CN103415623B9 (zh) | 2017-09-22 |
| CA2828934C (en) | 2018-12-04 |
| CA2828934A1 (en) | 2012-09-20 |
| EP2687606B1 (en) | 2017-05-03 |
| CN103415623A (zh) | 2013-11-27 |
| EP2687606A1 (en) | 2014-01-22 |
| JPWO2012124340A1 (ja) | 2014-07-17 |
| WO2012124340A1 (ja) | 2012-09-20 |
| EP2687606A4 (en) | 2014-11-12 |
| US9080201B2 (en) | 2015-07-14 |
| JP5969978B2 (ja) | 2016-08-17 |
| CN103415623B (zh) | 2017-06-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101046898B1 (ko) | 고밀도 리포 단백질 중의 콜레스테롤의 측정 방법 및 시약 | |
| JP5111389B2 (ja) | 小粒子低密度リポ蛋白中のコレステロールの定量方法 | |
| KR101326476B1 (ko) | 렘난트형 리포단백질 (rlp) 중의 콜레스테롤의 정량방법, 시약 및 키트 | |
| JP5112861B2 (ja) | 高密度リポ蛋白中のコレステロールの測定方法 | |
| CN111032880B (zh) | 低密度脂蛋白中的胆固醇的测定方法、测定用试剂和测定用试剂盒 | |
| WO2005100591A1 (ja) | 高密度リポ蛋白中のコレステロールの測定方法 | |
| WO2010055916A1 (ja) | 低密度リポ蛋白中のコレステロールの測定方法、測定用試薬及び測定用キット | |
| KR101924663B1 (ko) | Hdl 소분획 중의 콜레스테롤의 측정 방법, 측정용 시약 및 측정용 키트 | |
| EP2740801B1 (en) | Sphingomyelin measurement method and measurement kit | |
| JP5534809B2 (ja) | 低密度リポ蛋白中のコレステロールの測定方法及び測定用キット | |
| CN107267594B (zh) | 高密度脂蛋白中的胆固醇的测定方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant |