KR20120051663A - 알칼리형 연료전지를 이용한 발전 시스템 및 상기 시스템을 이용하는 알칼리형 연료 전지용 연료가스 - Google Patents
알칼리형 연료전지를 이용한 발전 시스템 및 상기 시스템을 이용하는 알칼리형 연료 전지용 연료가스 Download PDFInfo
- Publication number
- KR20120051663A KR20120051663A KR1020127002647A KR20127002647A KR20120051663A KR 20120051663 A KR20120051663 A KR 20120051663A KR 1020127002647 A KR1020127002647 A KR 1020127002647A KR 20127002647 A KR20127002647 A KR 20127002647A KR 20120051663 A KR20120051663 A KR 20120051663A
- Authority
- KR
- South Korea
- Prior art keywords
- basic compound
- anion exchange
- fuel cell
- exchange membrane
- anode
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 239000000446 fuel Substances 0.000 title claims abstract description 78
- 238000010248 power generation Methods 0.000 title claims abstract description 28
- 239000002737 fuel gas Substances 0.000 title claims abstract description 17
- 239000003011 anion exchange membrane Substances 0.000 claims abstract description 70
- 150000007514 bases Chemical class 0.000 claims abstract description 67
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims abstract description 50
- 239000012528 membrane Substances 0.000 claims abstract description 47
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 claims abstract description 34
- 239000007789 gas Substances 0.000 claims abstract description 27
- 238000000034 method Methods 0.000 claims abstract description 24
- 239000007800 oxidant agent Substances 0.000 claims abstract description 24
- 230000001590 oxidative effect Effects 0.000 claims abstract description 24
- 239000003792 electrolyte Substances 0.000 claims abstract description 19
- 229910021529 ammonia Inorganic materials 0.000 claims abstract description 17
- 230000005611 electricity Effects 0.000 claims abstract description 4
- 150000001875 compounds Chemical class 0.000 claims 1
- 239000003054 catalyst Substances 0.000 description 48
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 32
- 150000002500 ions Chemical class 0.000 description 22
- 150000001450 anions Chemical class 0.000 description 19
- -1 hydrogen ions Chemical class 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 17
- 239000001569 carbon dioxide Substances 0.000 description 16
- 229910002092 carbon dioxide Inorganic materials 0.000 description 16
- 229920000554 ionomer Polymers 0.000 description 16
- 238000005349 anion exchange Methods 0.000 description 15
- 239000000463 material Substances 0.000 description 14
- 239000000203 mixture Substances 0.000 description 14
- 239000005518 polymer electrolyte Substances 0.000 description 14
- 239000007787 solid Substances 0.000 description 14
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 12
- 239000000243 solution Substances 0.000 description 11
- 239000001257 hydrogen Substances 0.000 description 10
- 229910052739 hydrogen Inorganic materials 0.000 description 10
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 9
- 230000000694 effects Effects 0.000 description 9
- 239000001301 oxygen Substances 0.000 description 9
- 229910052760 oxygen Inorganic materials 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 8
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 8
- 229920000642 polymer Polymers 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 239000004215 Carbon black (E152) Substances 0.000 description 7
- 241000220259 Raphanus Species 0.000 description 7
- 235000006140 Raphanus sativus var sativus Nutrition 0.000 description 7
- 229930195733 hydrocarbon Natural products 0.000 description 7
- 150000002430 hydrocarbons Chemical class 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 239000002245 particle Substances 0.000 description 7
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- 239000007864 aqueous solution Substances 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 239000011230 binding agent Substances 0.000 description 6
- 238000005342 ion exchange Methods 0.000 description 6
- 229920005989 resin Polymers 0.000 description 6
- 239000011347 resin Substances 0.000 description 6
- 238000005341 cation exchange Methods 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 238000001035 drying Methods 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- ROSDSFDQCJNGOL-UHFFFAOYSA-N Dimethylamine Chemical compound CNC ROSDSFDQCJNGOL-UHFFFAOYSA-N 0.000 description 4
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 4
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 4
- 239000002250 absorbent Substances 0.000 description 4
- 230000002745 absorbent Effects 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 229910052799 carbon Inorganic materials 0.000 description 4
- 230000003197 catalytic effect Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 238000003411 electrode reaction Methods 0.000 description 4
- 229910052697 platinum Inorganic materials 0.000 description 4
- 125000001453 quaternary ammonium group Chemical group 0.000 description 4
- 238000006722 reduction reaction Methods 0.000 description 4
- 229920005992 thermoplastic resin Polymers 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 239000003513 alkali Substances 0.000 description 3
- 239000003957 anion exchange resin Substances 0.000 description 3
- 239000006258 conductive agent Substances 0.000 description 3
- 229920001577 copolymer Polymers 0.000 description 3
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 3
- 239000011630 iodine Substances 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 3
- 239000004810 polytetrafluoroethylene Substances 0.000 description 3
- 239000011148 porous material Substances 0.000 description 3
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 239000007784 solid electrolyte Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- IWTYTFSSTWXZFU-UHFFFAOYSA-N 3-chloroprop-1-enylbenzene Chemical compound ClCC=CC1=CC=CC=C1 IWTYTFSSTWXZFU-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 2
- 239000002033 PVDF binder Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 239000004696 Poly ether ether ketone Substances 0.000 description 2
- 239000004693 Polybenzimidazole Substances 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- 239000004721 Polyphenylene oxide Substances 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- HQABUPZFAYXKJW-UHFFFAOYSA-N butan-1-amine Chemical compound CCCCN HQABUPZFAYXKJW-UHFFFAOYSA-N 0.000 description 2
- 239000006229 carbon black Substances 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000000151 deposition Methods 0.000 description 2
- JQVDAXLFBXTEQA-UHFFFAOYSA-N dibutylamine Chemical compound CCCCNCCCC JQVDAXLFBXTEQA-UHFFFAOYSA-N 0.000 description 2
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 2
- 239000002612 dispersion medium Substances 0.000 description 2
- 238000010494 dissociation reaction Methods 0.000 description 2
- 230000005593 dissociations Effects 0.000 description 2
- 239000003480 eluent Substances 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 229910052736 halogen Inorganic materials 0.000 description 2
- 150000002367 halogens Chemical class 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 229910052763 palladium Inorganic materials 0.000 description 2
- 230000035699 permeability Effects 0.000 description 2
- 229920002492 poly(sulfone) Polymers 0.000 description 2
- 229920002480 polybenzimidazole Polymers 0.000 description 2
- 229920002530 polyetherether ketone Polymers 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 2
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 2
- 239000002759 woven fabric Substances 0.000 description 2
- NWUYHJFMYQTDRP-UHFFFAOYSA-N 1,2-bis(ethenyl)benzene;1-ethenyl-2-ethylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.CCC1=CC=CC=C1C=C.C=CC1=CC=CC=C1C=C NWUYHJFMYQTDRP-UHFFFAOYSA-N 0.000 description 1
- HNSDLXPSAYFUHK-UHFFFAOYSA-N 1,4-bis(2-ethylhexyl) sulfosuccinate Chemical compound CCCCC(CC)COC(=O)CC(S(O)(=O)=O)C(=O)OCC(CC)CCCC HNSDLXPSAYFUHK-UHFFFAOYSA-N 0.000 description 1
- UWFRVQVNYNPBEF-UHFFFAOYSA-N 1-(2,4-dimethylphenyl)propan-1-one Chemical compound CCC(=O)C1=CC=C(C)C=C1C UWFRVQVNYNPBEF-UHFFFAOYSA-N 0.000 description 1
- DQRXJTQZENKXNW-UHFFFAOYSA-N 3-chloroprop-1-enylbenzene;styrene Chemical compound C=CC1=CC=CC=C1.ClCC=CC1=CC=CC=C1 DQRXJTQZENKXNW-UHFFFAOYSA-N 0.000 description 1
- KFDVPJUYSDEJTH-UHFFFAOYSA-N 4-ethenylpyridine Chemical compound C=CC1=CC=NC=C1 KFDVPJUYSDEJTH-UHFFFAOYSA-N 0.000 description 1
- HXQXSNNOGXXMLU-UHFFFAOYSA-N 6-bromohex-1-enylbenzene Chemical compound BrCCCCC=CC1=CC=CC=C1 HXQXSNNOGXXMLU-UHFFFAOYSA-N 0.000 description 1
- 229920000049 Carbon (fiber) Polymers 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 229910017563 LaCrO Inorganic materials 0.000 description 1
- 229910017771 LaFeO Inorganic materials 0.000 description 1
- 241000877463 Lanio Species 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- 230000010718 Oxidation Activity Effects 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- 239000012670 alkaline solution Substances 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 238000005576 amination reaction Methods 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 125000005998 bromoethyl group Chemical group 0.000 description 1
- 125000005997 bromomethyl group Chemical group 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000004917 carbon fiber Substances 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 125000002603 chloroethyl group Chemical group [H]C([*])([H])C([H])([H])Cl 0.000 description 1
- 125000004218 chloromethyl group Chemical group [H]C([H])(Cl)* 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 239000004020 conductor Substances 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 229940043279 diisopropylamine Drugs 0.000 description 1
- 229910001882 dioxygen Inorganic materials 0.000 description 1
- WEHWNAOGRSTTBQ-UHFFFAOYSA-N dipropylamine Chemical compound CCCNCCC WEHWNAOGRSTTBQ-UHFFFAOYSA-N 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- 229920006351 engineering plastic Polymers 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 239000006232 furnace black Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910002804 graphite Inorganic materials 0.000 description 1
- 239000010439 graphite Substances 0.000 description 1
- 125000001188 haloalkyl group Chemical group 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 150000004693 imidazolium salts Chemical group 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 239000002923 metal particle Substances 0.000 description 1
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- GNVRJGIVDSQCOP-UHFFFAOYSA-N n-ethyl-n-methylethanamine Chemical compound CCN(C)CC GNVRJGIVDSQCOP-UHFFFAOYSA-N 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 229910000510 noble metal Inorganic materials 0.000 description 1
- 239000004745 nonwoven fabric Substances 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- 229920000885 poly(2-vinylpyridine) Polymers 0.000 description 1
- 229920000075 poly(4-vinylpyridine) Polymers 0.000 description 1
- 229920002006 poly(N-vinylimidazole) polymer Polymers 0.000 description 1
- 229920001643 poly(ether ketone) Polymers 0.000 description 1
- 229920006267 polyester film Polymers 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 229920006393 polyether sulfone Polymers 0.000 description 1
- 229920000306 polymethylpentene Polymers 0.000 description 1
- 239000011116 polymethylpentene Substances 0.000 description 1
- 229920005672 polyolefin resin Polymers 0.000 description 1
- 229920006380 polyphenylene oxide Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920005996 polystyrene-poly(ethylene-butylene)-polystyrene Polymers 0.000 description 1
- 239000010970 precious metal Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- JUJWROOIHBZHMG-UHFFFAOYSA-O pyridinium Chemical group C1=CC=[NH+]C=C1 JUJWROOIHBZHMG-UHFFFAOYSA-O 0.000 description 1
- 230000003014 reinforcing effect Effects 0.000 description 1
- 230000002940 repellent Effects 0.000 description 1
- 239000005871 repellent Substances 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 229910052703 rhodium Inorganic materials 0.000 description 1
- 239000010948 rhodium Substances 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 229910052707 ruthenium Inorganic materials 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M sodium chloride Inorganic materials [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229910052712 strontium Inorganic materials 0.000 description 1
- 229920003048 styrene butadiene rubber Polymers 0.000 description 1
- 125000001302 tertiary amino group Chemical group 0.000 description 1
- 238000012719 thermal polymerization Methods 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 239000011135 tin Substances 0.000 description 1
- 229920000428 triblock copolymer Polymers 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- RKBCYCFRFCNLTO-UHFFFAOYSA-N triisopropylamine Chemical compound CC(C)N(C(C)C)C(C)C RKBCYCFRFCNLTO-UHFFFAOYSA-N 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- LEONUFNNVUYDNQ-UHFFFAOYSA-N vanadium atom Chemical compound [V] LEONUFNNVUYDNQ-UHFFFAOYSA-N 0.000 description 1
- 239000011800 void material Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/08—Fuel cells with aqueous electrolytes
- H01M8/083—Alkaline fuel cells
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/06—Combination of fuel cells with means for production of reactants or for treatment of residues
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/02—Details
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/10—Fuel cells with solid electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/22—Fuel cells in which the fuel is based on materials comprising carbon or oxygen or hydrogen and other elements; Fuel cells in which the fuel is based on materials comprising only elements other than carbon, oxygen or hydrogen
- H01M8/222—Fuel cells in which the fuel is based on compounds containing nitrogen, e.g. hydrazine, ammonia
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Sustainable Development (AREA)
- Sustainable Energy (AREA)
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Fuel Cell (AREA)
- Manufacture Of Macromolecular Shaped Articles (AREA)
Abstract
본 발명은, 음이온 교환막으로 이루어지는 전해질막을 이용하는 알칼리형 연료전지에 있어서, 종래보다 높은 출력을 얻는 방법을 개발하는 것을 목적으로 한다. 음이온 교환막으로 이루어지는 전해질막과, 그 양측에 배치된 한 쌍의 전극인 애노드 및 캐소드를 포함하고, 애노드 측에 연료 가스가 공급되고, 타측인 캐소드 측에 산화제 가스가 각각 공급되어 발전하는 알칼리형 연료 전지를 이용한 발전 시스템에 있어서, 상기 애노드 측에 공급되는 연료 가스로서, 암모니아 등의 염기성 화합물을 함유하는 수소 가스를 이용하는 것을 특징으로 하는 알칼리형 연료 전지를 이용한 발전 시스템.
Description
본 발명은, 음이온 교환막으로 이루어지는 전해질막을 이용하는 알칼리형 연료 전지를 이용한 발전 시스템 및 이를 이용하는 연료가스에 관한 것이다.
연료전지는, 화학 에너지를 전력으로 이용하는 발전 시스템이다. 이러한 작동 기구(메커니즘) 또는 이용하는 재료로부터 알칼리형, 인산형, 용융 탄산염형, 고체 전해질형, 고체 고분자형 등으로 분류되고, 각종 형식의 연료 전지가 제안, 검토되고 있다. 이 중에서도, 알칼리형 연료 전지나 고체 고분자형 연료 전지는, 작동 온도가 200℃ 이하의 온도이기 때문에, 휴대 전원 이외에도 고정형 전원이나 차량 탑재용도 등의 중소형 저온 작동형 연료 전지로써의 사용이 기대되고 있다.
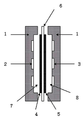
고체 고분자형 연료전지는 이온 교환 수지 등의 고체 고분자를 전해질로서 이용한 연료 전지이고, 작동 온도가 비교적 낮다고 하는 특징을 갖는다. 당해 고체 고분자형 연료전지는, 도 1에 도시하는 바와 같이, 각각 외부와 연통하는 연료 유통공(2) 및 산화제 가스 유통공(3)을 가지는 전지 격벽(1) 내의 공간을, 고체 고분자 전해질막(6)의 양면에 각각 애노드(anode)(4) 및 캐소드(cathode)(5)가 접합한 접합체로 구획하고, 연료 유통공(2)을 통하여 외부와 연통하는 애노드실(7) 및 산화제 가스 유통공(3)을 통하여 외부로 연통하는 캐소드실(8)이 형성된 기본 구조를 가진다. 또한, 이러한 기본 구조의 고체 고분자형 연료 전지에서는, 상기 애노드실(7)에 연료 유통공(2)을 통해 수소 가스 혹은 메탄올 등의 액체로 이루어지는 연료를 공급함과 동시에 캐소드실(8)에 산화제 가스 유통공(3)을 통해 산화제인 산소나 공기 등의 산소 함유 가스를 공급하고, 또한 양 전극 간에 외부 부하 회로를 접속함으로써 다음과 같은 메커니즘에 의한 전기 에너지를 발생시킨다.
고체 고분자 전해질막(6)으로서 양이온 교환막을 사용한 경우에는, 애노드(4)에서 당해 전극 내에 포함되는 촉매와 연료가 접촉함으로써 생성된 프로톤(수소 이온)이 고체 고분자 전해질막(6) 내를 전도하여 캐소드실(8)로 이동하고, 캐소드(5)에서 산화제 가스 중의 산소와 반응하여 물을 생성한다. 한편, 애노드(4)에서 프로톤과 동시에 생성한 전자는 외부 부하 회로를 통해 캐소드(5)로 이동하므로 상기 반응 에너지를 전기 에너지로 이용할 수 있다.
이와 같은 고체 전해질막으로서 양이온 교환막을 사용한 고체 고분자형 연료 전지에서는 반응장소(reactive site)가 강산성이기 때문에, 전극 중의 촉매로서 고가의 귀금속 촉매를 사용할 수 밖에 없다.
따라서, 양이온 교환막 대신에 음이온 교환막을 이용하는 것이 검토되고 있다. 음이온 교환막을 이용한 연료 전지에서는 반응장소가 염기성이기 때문에, 귀금속 이외의 촉매도 사용할 수 있다. 그러나, 이러한 경우, 고체 고분자형 연료 전지에서, 전기 에너지가 발생하기 위한 메커니즘은, 다음과 같은 고체 고분자 전해질막(6) 내를 이동하는 이온의 종류가 달라지게 된다. 즉, 애노드실에 수소 혹은 메탄올 등을 공급하고, 캐소드실에 산소 및 물을 공급함으로써, 캐소드(5)에서 당해 전극 내에 포함되는 촉매와 산소 및 물이 접촉하여 수산화물 이온이 생성된다. 이러한 수산화물 이온은, 상기 음이온 교환막으로 이루어지는 고체 고분자 전해질막(6) 내를 전도하여 애노드실(7)로 이동하고, 애노드(4)에서 연료와 반응하여 물을 생성하게 되는데, 이에 수반하여 당해 애노드(4)에서 생성된 전자를 외부 부하 회로를 통하여 캐소드(5)로 이동시켜서, 이러한 반응 에너지를 전기 에너지로서 이용한다.
상기와 같이, 막 내를 수산화물 이온이 이동하는 메커니즘의 연료 전지를 알칼리형 연료 전지라고 한다. 따라서, 음이온 교환막을 고체 고분자형 전해질막으로서 이용하는 고체 고분자형 연료전지도 알칼리형 연료전지로서 분류된다.
알칼리형 연료 전지에서는 양 전극의 분위기가 염기성으로 되고, 또한 사용 가능하게 되는 촉매 종류의 선택 범위가 넓어짐으로써, 이하와 같은 이점이 있다. 예를 들면, 산소 환원의 과전압이 저감되고, 또한, 막을 투과한 연료에 대하여 불활성 캐소드 촉매를 선택함으로써 전압 향상도 기대되고 있다.
음이온 교환막을 이용한 알칼리형 연료 전지로는, 수소를 애노드 측에, 산소 또는 공기를 캐소드 측에 공급하여 발전시킨 예가 있다(특허 문헌 1, 비특허 문헌 1).
[특허문헌1] 일본 특허 공개2007-042617공보
[비특허문헌1] 저널 오브 파워 소소(Journal of Power Sources) 2008년, 178권, 620페이지
음이온 교환막으로 이루어지는 전해질막을 이용하는 알칼리형 연료전지에서, 연료가스는 확산성이 높고, 고활성의 촉매가 사용될 수 있는 것을 이용하면 높은 출력을 얻기 쉽다는 점에서, 수소 가스가 유리하다. 그러나, 이렇게 수소 가스를 사용하였다고 해도, 당해 음이온 교환막으로 이루어지는 전해질막을 이용하는 알칼리형 연료전지는, 양이온 교환막을 이용하는 것에 비해 전술한 여러 가지 이점이 있음에도 불구하고, 실제의 출력은 기대하는 것만큼 높은 값을 얻지 못하고 있다.
따라서, 본 발명은 음이온 교환막으로 이루어지는 전해질막을 이용하는 알칼리형 연료전지에 있어서, 종래보다 높은 출력을 얻는 방법을 개발하는 것을 목적으로 한다.
본 발명자들은, 알칼리형 연료전지에서 고출력을 달성하기 위하여 여러 가지를 검토하였다. 그 결과, 애노드에서의 전압 손실을 억제하면 높은 출력이 얻어진다는 것을 깨달았다. 그 구체적인 수단으로서, 애노드 측에 염기성 화합물을 함유하는 수소를 연료로 공급함으로써 출력이 향상된다는 사실을 알아내어, 본 발명을 완성하기에 이르렀다.
즉, 본 발명은, 음이온 교환막으로 이루어지는 전해질막과, 그 양측에 배치된 한 쌍의 전극인 애노드와 캐소드를 포함하고, 애노드 측에 연료가스가 공급되고, 타측인 캐소드 측에 산화제 가스가 각각 공급되어 발전하는 알칼리형 연료 전지를 이용한 발전 시스템, 또는 발전 방법에 있어서, 당해 애노드 측에 공급되는 연료가스로서, 염기성 화합물을 함유하는 수소가스를 이용하는 것을 특징으로 하는 알칼리형 연료 전지를 이용한 발전 시스템 또는 발전 방법에 관한 것이다.
또한, 다른 발명은, 염기성 화합물이 암모니아인 상기 발전 시스템 또는 발전 방법에 관한 것이다
한편, 또 다른 발명은, 염기성 화합물을 함유하는 수소 가스 중에서, 상기 염기성 화합물의 함유량이 0.1 내지 10 mol/m3 인 발전 시스템 또는 발전 방법에 관한 것이다.
또 다른 발명은, 산화제 가스가 대기인 발전 시스템 또는 발전 방법에 관한 것이다.
또 다른 발명은, 염기성 화합물을 함유하는 수소가스로 이루어지는 전해질막으로서 음이온 교환막을 이용한 알칼리형 연료전지용 연료가스에 관한 것이다.
본 발명의 알칼리형 연료 전지를 이용한 발전 시스템 또는 발전 방법에 의하면, 종래 이용되어 온 연료 가스로서 수소 가스를 이용하는 연료 전지보다도, 높은 출력을 얻을 수 있다. 따라서, 상기의 다양한 이점을 갖는 알칼리형 연료 전지의 실용화에 있어서 매우 유용하다.
본 발명의 시스템에서, 이와 같은 높은 출력이 얻어지는 이유가 반드시 명확하지는 않지만, 본 발명자들은 다음과 같이 추정하고 있다. 즉, 알칼리형 연료 전지에 있어서 애노드 및 캐소드는, 후술하는 바와 같이, 전극 촉매와 음이온 전도성 아이오노머를 포함하고, 또한 당해 전극 촉매가 도전제의 입자에 담지되어 있는 경우, 이러한 전극에는 당해 입자 사이에 공극이 형성되어 있다. 애노드에서의 전극 반응에서는 물이 생성되기 때문에, 당해 애노드에서, 상기 음이온 전도성 아이오노머는 수분을 함유하여, 입자 사이의 공극에도 물이 흡수된다. 따라서, 연료의 수소 가스에 염기성 화합물이 함유되어 있으면, 애노드에서는, 상기 함유된 물에 이러한 염기성 화합물이 용해하여 수산화물 이온의 농도가 높아지고, 이온 전도도가 향상된다. 그 결과, 애노드에서의 옴 손실(Ohmic loss)이나 애노드 반응 과전압이 작아져서, 높은 출력을 얻을 수 있는 것으로 생각된다.
도 1은 고체 고분자형 연료 전지의 기본 구조를 나타내는 개념도이다.
본 발명의 알칼리형 연료전지를 이용한 발전 시스템에서는, 음이온 교환막으로 이루어지는 전해질막과, 그 양측에 배치된 한 쌍의 전극인 애노드와 캐소드를 포함하고, 애노드 측에 연료가스가 공급되는 한편, 타측인 캐소드 측에 산화제 가스가 각각 공급되어 발전하는 알칼리형 연료 전지에 있어서, 연료가스로서, 염기성 화합물을 함유하는 수소가스를 이용한다. 여기서, 염기성 화합물로서는, 수소 가스와 혼합하는 것이 가능하며, 연료 전지의 애노드에 공급되었을 때 가스 상태를 유지하고, 물에 용해되었을 때 염기성을 나타내는 것을 제한 없이 이용할 수 있다. 보다 높은 출력을 얻는 관점에서는, 수용성이 높고, 염기성의 지표인 산 해리 상수(pKa)가 8이상, 보다 바람직하게는 9~12, 더 바람직하게는 9~11인 것이 좋다. 산 해리 상수가 지나치게 큰 경우에는 애노드에 포함되는 음이온 전도성 아이오노머나 음이온 교환막이 열화(deterioration)되는 경우가 있다.
본 발명에서 사용할 수 있는 염기성 화합물을 구체적으로 예시하면, 암모니아, 메틸아민, 디메틸아민, 트리메틸아민, 에틸아민, 디에틸아민, 트리에틸아민, 디에틸메틸아민, 프로필아민, 디프로필아민, 트리프로필아민, 이소프로필아민, 디이소프로필아민, 트리이소프로필아민, 부틸아민, 디부틸아민, 트리부틸아민 등의 알킬아민류, 아닐린, 피리딘 등을 들 수 있다. 이 중에서, 상온(25℃)에서 용이하게 기체 상태로 되는 암모니아, 메틸아민, 디메틸아민, 트리메틸아민이 바람직하며, 더욱 수용성이 높은 암모니아가 가장 바람직하다.
수소 가스에 함유되는 염기성 화합물의 농도는, 특히 제한되는 것은 아니나, 낮은 경우에는, 알칼리형 연료전지의 출력을 향상시키는 효과가 낮다. 또한, 수소에 함유된 염기성 화합물의 농도가 지나치게 높으면, 상대적으로 연료가 되는 수소가스 농도가 낮아지기 때문에, 애노드 전위가 상승한다거나 애노드로의 공급 부족이 발생할 수 있다. 따라서, 수소 가스에 함유되는 염기성 화합물의 농도는, 0.1 ~ 10 mol/m3 인 것이 바람직하며, 0.2 내지 8 mol/m3 인 것이 더 바람직하다.
또한, 염기성 화합물은, 애노드의 촉매에 흡착되어 활성을 저하시키는 것으로 알려져 있다. 따라서, 수소 가스에 함유되는 염기성 화합물의 농도가 높은 경우에는, 상기와 같은 이유뿐만 아니라, 염기성 화합물에 의한 촉매 활성의 저감효과도 더해진다. 이러한 촉매 활성의 저감 효과는, 상기 염기성 화합물의 바람직한 범위 내라도 고농도 영역에서는 영향을 미친다. 따라서, 이러한 촉매 활성의 저감을 억제하면서, 염기성 화합물에 의한 이온 전도도의 향상 효과를 최대한으로 발휘시키고, 특히 높은 출력을 얻는 관점에서 보면, 상기 수소 가스에 함유되는 염기성 화합물의 농도는, 0.4 ~ 4 mol/m3 인 것이 최적이다.
염기성 화합물을 함유하는 수소가스를 얻는 방법에는 특히 제한이 없으며, 공지의 방법을 이용할 수 있다. 구체적인 예를 들면, 다음과 같다. 즉, 염기성 화합물 또는 염기성 화합물의 용액에 수소 가스를 통과시킴으로써 함유시키는 방법, 수소 가스 내에 염기성 화합물 또는 염기성 화합물의 용액을 분무하여 함유시키는 방법 등이 있다. 염기성 화합물이, 염기성 화합물을 함유하는 수소 가스를 공급하는 온도에서 기체인 경우는 그대로, 혹은 질소나 아르곤과 같은 불활성 가스와의 혼합가스로서 수소가스와 기체 상태로 혼합하여 함유시켜도 무방하다. 이렇게 하여 얻은 염기성 화합물을 함유하는 수소 가스는, 전해질막으로서 음이온 교환막을 이용한 알칼리형 연료전지용의 연료가스로서 이용할 수 있다.
염기성 화합물을 함유하는 수소 가스의 애노드에 대한 공급량은, 특히 제한되는 것은 아니지만, 바람직하게는, 사용하는 음이온 교환막의 면적과 발전시의 전류밀도로부터 연료 사용량을 산출하여, 그 2배 이상의 값이 이용된다. 일반적으로, 음이온 교환막 1cm2당 5~100ml/분의 범위에서 선택된다.
본 발명의 발전 시스템에서는, 상술한 염기성 화합물을 함유하는 수소 가스를 연료 가스로서 공급하는 점 이외에는, 종래 공지된 음이온 교환막으로 이루어지는 전해질막을 이용한 알칼리형 연료전지의 운전 조건이나 구성을 아무런 제한 없이 채택할 수 있다
즉, 애노드에 공급될 수 있는 산화제로는, 산소, 공기가 공급되지만, 공기는 상대습도가 30~100%RH인 것이 바람직하며, 50~100%RH인 것이 더욱 바람직하다. 30%RH 미만의 경우, 음이온 교환막이 건조하여 저항이 높아져 출력이 낮아지는 경우가 있다. 연료 전지의 운전 환경에서 대기 습도가 상기 범위의 경우에는, 습도를 조절하지 않고 공급해도 좋고, 또한 가습기에 의해 가습하여 공급해도 무방하다.
또한, 산화제에는, 특별한 정제 장치나 봄베 등의 보존 장치가 불필요 한 이유에서 보면, 대기를, 상기 필요에 따라 습도 조절만으로 직접 공급하는 것이 실용적으로 바람직하다.
알칼리형 연료전지에서는, 공기에 함유된 이산화탄소가 발전 성능에 영향을 미치는 것으로 알려져 있다. 일반적으로, 대기에는 380ppm정도의 농도를 가지는 이산화탄소가 함유되어 있다. 본 발명의 알칼리형 연료전지에 전해질막으로 이용되는 음이온 교환막은, 미리 음이온 교환기의 반대 이온을 OH-로 이온 교환한 것이라도, 연료전지로서 사용하기 전에 대기에 노출시키는 등으로, 대기 중의 이산화탄소를 흡수하여, 당해 반대 이온은 급속하게 OH-로부터 CO3 2 -로 치환되고, 연이어 당해 CO3 2-도 HCO3 -로 변화한다. 반대 이온이 CO3 2 -나 HCO3 -로 된 음이온 교환막은 그 이온 전도성이, 반대 이온 전부가 OH-인 음이온 교환막에 비해 낮고, 또한 전극 반응종인 OH-의 농도나 전극 반응장소의 염기성이 낮다. 따라서, 반응 과전압이, 반대 이온 전부가 OH-인 음이온 교환막에 비해 높아지고, 그 결과로서 반대 이온 전부가 OH-인 음이온 교환막을 이용한 연료 전지인 것에 비해 그 출력이 낮다.
본 발명의, 수소 가스에 염기성 화합물을 함유시키는 효과는, 이산화탄소의 농도를 저감시킨 공기를 산화제 가스로 이용하는 경우에 비하여, 대기를 필요에 따라 습도 조절만을 하여 산화제 가스로 이용하는 경우에 현저하다. 즉, 대기를 직접 이용한 경우가, 산소 가스에 염기성 화합물을 함유시킨 경우와 함유시키지 않은 경우의 출력차가 크다. 그 이유에 대하여, 자세히는 명확하지 않으나, 이하와 같이 추정된다.
상술한 바와 같이, 알칼리형 연료 전지의 음이온 교환막은, 발전 전에는 대기 중의 이산화탄소를 흡수하여 HCO3 -형으로 되어 있으나, 당해 HCO3 - 등은 발전시에는 캐소드에서 생성하는 OH-로 재차 치환되어 애노드로부터 이산화탄소로서 방출된다. 그러나, 이산화탄소를 함유하는 공기를 산화제 가스로서 이용한 경우에는, 캐소드로부터 항상 이산화탄소가 흡수되기 때문에 반대 이온 전부가 OH-로 되는 일은 없다. 즉, 잔존하는 CO3 2 -나 HCO3 -에 의해 음이온 교환막의 이온 전도성이 낮아지고, 또한 애노드 촉매 주위의 염기성이 낮아진다. 이산화탄소를 제거한 공기를 이용한 경우에는 이러한 이온 전도성이나 염기성의 저하가 발생하지 않는다. 수소 가스에 염기성 화합물이 포함되어 있는 경우에는, 염기성 화합물에 의해 음이온 교환막이나 애노드 내에서 전극 촉매 주위의 CO3 2 -나 HCO3 -가 중화되어, 더욱 이들 영역의 염기성을 높이기 때문에, 산화제 가스가 이산화 탄소를 포함하고 있어도 출력이 높아지는 것으로 생각된다.
산화제 가스의 캐소드에 대한 공급량은, 특히 제한되는 것은 아니나, 바람직하게는, 사용하는 음이온 교환막의 면적과 발전시의 전류 밀도로부터 산화제 가스 사용량을 산출하고, 그 2배 이상의 값이 이용된다. 일반적으로는, 음이온 교환막 1cm2당 10~200ml/분의 범위로부터 채택된다.
본 발명의 발전 시스템에서의 알칼리형 연료전지의 운전온도로는, 일반적으로, -30℃~120℃이고, 출력의 높이나 사용하는 재료의 내구성을 감안하면 20℃~90℃가 바람직하다. 연료 가스나 산화제 가스도, 상기 온도 범위에서 공급하는 것이 바람직하다.
본 발명의 시스템에서 사용하는 알칼리형 연료 전지는, 음이온 교환막으로 이루어지는 전해질막과 그 양측에 배치된 한 쌍의 전극인 애노드와 캐소드를 포함한다(이하, 그 구조를 “음이온 교환막-전극 접합체”라고 칭한다). 여기서, 상기 음이온 교환막-전극 접합체에 이용되는 각종 재료나 당해 접합체의 제조방법에는 제한이 없고, 종래의 고분자 전해질형 연료 전지에서 채택되고 있는 재료나 제조 방법이 아무런 제한 없이 사용될 수 있다.
예를 들면, 음이온 교환막에는 고분자 전해질형 연료 전지용의 고체 고분자 전해질막으로서 사용될 수 있는 것으로 알려져 있는 공지의 음이온 교환막이 제한 없이 사용될 수 있다. 그 중에도, 연료인 수소 가스의 투과성을 억제할 수 있고, 값싸게 제조할 수 있는 등의 관점에서 보면, 상기 음이온 교환막으로는 탄화 수소계를 사용하는 것이 바람직하다. 탄화수소계 음이온 교환수지를 포함하는 음이온 교환막으로는, 예를 들면, 폴리술폰, 폴리에테르케톤, 폴리에테르에테르케톤, 폴리벤즈이미다졸계 폴리머 등으로 대표되는 엔지니어링 플라스틱 재료에 필요에 따라 여러 관능기를 도입한 탄화 수소계 음이온 교환수지를 캐스트 필름 성형한 음이온 교환막 등이어도 좋다.
바람직하게는, 탄화 수소계 음이온 교환막으로서는, 다공질막을 모재료로하고, 당해 다공질막의 공극부에 가교된 탄화 수소계 음이온 교환막 수지가 충진되어 이루어지는 음이온 교환막으로 구성되는 것이 바람직하다. 이러한 다공질막 중에 가교된 탄화 수소계 음이온 교환수지가 불균질하게 분산된 음이온 교환막은, 당해 다공질막이 보강부분으로서 역할을 하기 때문에 전기 저항을 희생시키지 않고 음이온 교환막의 물리적 강도를 높이는 것이 가능하고, 또한 화학적 내구성도 높일 수 있다는 이점을 갖는다. 이러한 음이온 교환막으로서는, 예를 들면, 일본 특허 공개 2007-42617호 공보에 기재되어 있는 바와 같이, 다공질막의 공극에 클로로메틸스틸렌과 디비닐벤젠, 4-비닐피리딘과 디비닐벤젠 등의 중합성 단량체 조성물을 함침시키고, 당해 중합성 조성물을 열중합시켜, 또한 아미노화, 알킬화 등의 처리에 의해 원하는 음이온 교환기를 도입한 막 등을 들 수 있다.
상술한 다공질막으로는, 일반적으로는, 열가소성 수지제의 직포, 부직포, 다공질 필름 등이 사용되는데, 가스 투과성이 낮고, 박막화가 가능한 점으로부터 당해 다공질막으로서는, 폴리에틸렌, 폴리프로필렌, 폴리메틸펜텐 등의 폴리올레핀수지, 폴리테트라플로오르에틸렌, 폴리(테트라플루오르에틸렌-헥사플루오르프로필렌), 폴리불화비닐리덴 등의 불소계 수지 등의 열가소성 수지제 다공질 필름으로 이루어진 것을 이용하는 것이 바람직하다.
이와 같은 음이온 교환막 내에 존재하는 음이온 교환기로서는, 1~3급 아미노기, 4급 암모늄염기, 필리딜기, 이미다졸기, 4급 피리디늄염기, 4급 이미다졸리움염기 등을 들 수 있다. 음이온 전도성이 뛰어난 점에서, 강염기성기인 4급 암모늄염기가 바람직하다.
본 발명에서 전해질막에 이용되는 음이온 교환막은, 어떠한 반대 이온을 갖는 것이어도 좋으나, 일반적으로, 당해 반대이온은 할로겐형으로 제조된다. 반대이온이 할로겐형인 음이온 교환막은, 이온 전도성이 낮고 막의 고출력을 얻기 힘들기 때문에, 이와 같은 반대 이온형의 경우에는, 막의 이온 전도성을 높이고, 전극 반응종류인 OH-의 농도를 높이고, 또한 전극 반응장소의 염기성도 높이기 쉽다는 점에서, 반대 이온의 OH-형으로의 이온 교환 처리가 된 것이 바람직하다. OH-형으로의 이온 교환은, 종래의 공지된 방법, 즉, 음이온 교환막을 수산화 나트륨이나 수산화 칼륨의 수용액 등의 알칼리 용액에 침적시켜 행할 수 있다. 일반적으로, 상기 이온 교환은, 알칼리 농도 0.01~5mol/L의 농도에서, 0.5~10시간 침적함으로써 행하여진다. 이온 교환의 조작을 여러 차례 반복하여 행하는 것도 가능하다. 또한, 일반적으로 이온 교환 후의 음이온 교환막은 필요에 따라 물로 세정, 건조 등을 시행한 후 사용된다.
또한, 전술한 음이온 교환막의 반대이온을, HCO3나 CO3 2 -, 혹은 이들의 혼합물로 하는 것도 바람직하다. 이와 같은 반대 이온형으로 함으로써, 대기 중의 이산화 탄소의 흡수도에 관계없이 안정된 특성을 갖는 음이온 교환막으로 할 수 있을 뿐만 아니라, 4급 암모늄염기 등의 음이온 교환기의 안정성을 향상시키는 것도 가능하게 된다. 이들 반대 이온으로의 교환도, OH-형으로의 이온교환과 마찬가지로, 예를 들면, 탄산 나트륨, 탄산수소 나트륨 등의 수용액에 음이온 교환막을 침적함으로써 행할 수 있다.
본 발명에서 전해질막에 이용되는 음이온 교환막은, 통상 0.2~3mmol?g-1, 바람직하게는, 0.5~2.5mmol?g- 1 의 음이온 교환 용량을 갖고, 또한 건조에 의한 음이온의 전도성의 저하가 발생하기 어렵도록, 25℃에서의 함수율이 7질량% 이상, 바람직하게는 10~90질량%로 되도록 조제하는 것이 바람직하다. 또한, 막 두께는, 전기 저항을 낮게 억제할 수 있는 관점 및 지지막으로서 필요한 기계적 강도를 부여하는 관점에서, 통상 5~200μm의 두께를 갖는 것이 바람직하고, 보다 바람직하게는 10~100μm을 갖는 것이 바람직하다. 이러한 특성을 가짐으로써, 본 발명의 전해질에 이용되는 음이온 교환막은 25℃, 0.5mol/L-염화 나트륨 내의 막 저항이 통상 0.05~1.5Ω?cm2이고, 바람직하게는 0.1~0.5 Ω?cm2이다.
음이온 교환막-전극 접합체를 구성하는 애노드 및 캐소드는, 전극 촉매와 음이온 전도성 아이오노머를 포함하여 이루어지는, 고체 고분자 전해질형 연료전지에서 사용되는 종래 공지된 촉매 전극층이 제한없이 사용될 수 있다. 음이온 교환막에 대하여, 이들 애노드 및 캐소드를 형성하는 구체적인 방법은, (I)전극 촉매에 필요에 따라서 결착제나 분산매를 첨가하여 페이스트 형태의 조성물로하고, 이를 그대로 롤 성형하거나 또는 카본 페이퍼 등의 지지층 재료 위에 도포한 후에 열처리하여 층상물을 얻고, 음이온 교환막과의 접합면이 되는 표면에 음이온 전도성 아이오노머 용액을 도포 함침시킨 후에 필요에 따라 건조하고, 음이온 교환막과 열 압착하는 방법; 또는 (II)전극 촉매에 음이온 전도성 아이오노머 및 필요에 따라서 결착제나 분산매를 첨가하여 페이스트 형태의 조성물로 하고, 이를 카본 페이퍼 등의 지지층 재료 상에 도포하거나, 박리 필름 상에 도포하여 음이온 교환막 상에 전사하거나, 또는 음이온 교환막 상에 직접 도포하거나 한 후에 건조시켜, 그 후 필요에 따라 음이온 교환막과 열압착하는 방법 등을 들 수 있다. 촉매 전극층의 전극 촉매의 이용률을 높이는 관점에서는, 상기 (II)의 방법이 보다 바람직하다.
상기 음이온 전도성 아이오노머로는, 분자 내에 음이온 교환기를 갖고, 음이온의 전도성을 나타내는 재료라면, 종래의 공지 재료를 제한 없이 사용할 수 있다. 염기성 화합물을 용해시켜 본 발명의 효과를 충분히 발휘시킨다는 관점에서, 25℃에서 함수율이 5질량% 이상, 바람직하게는 10~200질량%인 것을 이용하는 것이 바람직하다.
예를 들면, 클로로메틸기, 클로로에틸기, 클로로프로필기, 클로로부틸기, 클로로펜틸기, 클로로헥실기, 브로모메틸기, 브로모에틸기, 브로모프로필기, 브로모부틸기, 브로모펜틸기, 브로모헥실기, 요오드메틸기, 요오드에틸기, 요오드부틸기 등의 할로겐알킬기를 갖는 수지, 구체적으로는, 폴리클로로메틸스틸렌, 폴리(스틸렌-클로로메틸스틸렌)공중합체, 폴리브로모에틸스틸렌, 브로모부틸스틸렌, 클로로메틸화폴리술폰, 클로로메틸화폴리페닐렌옥시드, 클로로메틸화폴리에테르에테르케톤 등을 아미노화하여, 대응하는 음이온 교환기를 도입한 수지 등을 들 수 있다.
혹은, 폴리-(4-비닐피리딘), 폴리-(2-비닐피리딘)나, 폴리비닐이미다졸, 폴리벤즈이미다졸 등에, 아이오딘화메틸 등의 알킬화제를 작용시켜, 대응하는 음이온 교환기를 도입한 수지도 사용할 수 있다.
특히, 애노드 및 캐소드로 되는 각 촉매 전극층의, 상기 음이온 교환막으로의 접합성이나 액체 연료로의 내용제성, 게다가 전술한 촉매 전극층 제조시의 조작성 등을 고려하면, 일본 특허 공개 2002-367626호 공보에 개시된 바와 같이, 분자 내에 음이온 교환기를 포함하고, 물과 메탄올에 용해되기 어려운 탄화 수소계 고분자 탄성 중합체가 바람직하게 사용된다.
촉매 전극층의 전극 촉매도 공지된 것이 특별한 제한없이 사용될 수 있다. 즉, 수소의 산화 반응 및 산소의 환원 반응을 촉진하는 백금, 금, 은, 팔라듐, 이리듐, 로듐, 루테늄, 주석, 철, 코발트, 니켈, 몰리브덴, 텅스텐, 바나듐, 혹은 이들의 합금 등의 금속 입자가 제한 없이 사용될 수 있으나, 촉매 활성이 뛰어나다는 점에서 백금족 촉매를 이용하는 것이 바람직하다.
또한, 음이온 교환막을 이용하기 때문에, 종래의 강산성의 양이온 교환막에서는 사용될 수 없었던 각종 금속 산화물을 전극촉매로서 이용하는 것이 가능하다. 예를 들면, 산화 활성이 뛰어난 ABO3로 표현되는 페로브스카이트형 산화물 등도 바람직하게 사용될 수 있다. 구체적으로는, LaMnO3, LaFeO3, LaCrO3, LaCoO3, LaNiO3 등 혹은 상기 A 위치의 일부를 Sr, Ca, Ba, Ce, Ag 등으로 부분 치환한 것, 또한, B 위치의 일부를 Pd, Pt, Ru, Ag 등으로 부분 치환한 페로브스카이트형 산화물 등도 전해 촉매로서 바람직하게 사용될 수 있다.
한편, 이들 전해 촉매의 입경은 일반적으로 0.1~100nm, 보다 바람직하게는, 0.5~10nm이다. 입경이 작을수록 촉매성능은 높아지나, 0.5nm미만인 경우는, 제작이 곤란하고, 100nm보다 크면 충분한 촉매 성능을 얻기 힘들다. 또한, 이들 촉매는, 미리 도전제에 담지시키고 나서 사용해도 좋다. 도전제로서는, 전자 도전성 물질이라면 특히 한정되지 않으나, 예를 들면, 퍼네스 블랙, 아세틸렌 블랙 등의 카본 블랙, 활성탄, 흑연 등을 단독으로 또는 혼합하여 사용하는 것이 일반적이다.
이들 전극 촉매의 함유량은, 애노드 및 캐소드로 되는 촉매 전극층을 시트 형상으로 한 상태에서 단위 면적당의 전극 촉매 질량으로, 통상 0.01~10mg/cm2, 보다 바람직하게는 0.1~5.0mg/cm2다.
또한, 애노드 및 캐소드로 되는 촉매 전극층에는, 필요에 따라 결착제를 첨가하는 것도 가능하다. 이러한 결착제로서는, 각종 열가소성 수지가 일반적으로 이용되는데, 바람직하게 사용할 수 있는 열가소성 수지를 예시하면, 폴리테트라플루오르에틸렌, 폴리불화비닐리덴, 테트라플루오르에틸렌-퍼플루오르알킬비닐에테르공중합체, 폴리에테르에테르케톤, 폴리에테르술폰, 스틸렌?부타디엔공중합체, 아크릴로니트릴?부타디엔공중합체 등을 들 수 있다. 당해 결착제의 함유량은, 상기 촉매 전극층의 5~25중량%인 것이 바람직하다. 또한, 결착제는, 단독으로 사용해도 좋으며, 2종류 이상을 혼합하여 사용해도 좋다.
또한, 촉매 전극층에 대하여, 필요에 따라 사용되는 지지층 재료로서는, 일반적으로 카본 섬유 직포, 카본 페이퍼 등의 다공질 탄소 재료가 사용된다. 이들 지지층 재료의 두께는, 50~300μm가 바람직하고, 그 공극율은 50~90%가 바람직하다. 일반적으로, 이와 같은 지지층 재료의 공극내 및 표면상에 상기 전극촉매를 포함하는 페이스트 형상의 조성물을, 얻을 수 있는 촉매 전극층이 5~50μm의 두께가 되도록 충진 및 부착시켜 촉매 전극층이 구성된다.
또한, 상기(I) 및 (II)의 애노드 및 캐소드의 형성 방법에서, 상술한 음이온 전도성 아이오노머의 사용량은 특히 한정되지 않으나, 상기 (I)의 방법에서는, 이온 전도성 부여 효과의 관점에서, 접합면으로부터 전체 두께의 1~50% 범위의 촉매 전극층에 대하여, 음이온 전도성 아이오노머의 함유량이 5~60질량%, 특히 10~40질량%로 되도록 사용하는 것이 바람직하다. 또한, 상기(II)의 방법에서는 촉매 전극층의 전체 질량에 대하여 음이온 전도성 아이오노머의 함유량이 5~60질량%, 특히 10~40질량%로 되도록 사용하는 것이 바람직하다.
또한, 상기 (I) 및 (II)의 방법에서, 애노드 및 캐소드를 음이온 교환막에 열압착하는 경우에는, 당해 열압착은 가압, 가온할 수 있는 장치, 일반적으로는, 핫 프레스기, 롤 프레스기 등에 의해 행하여진다. 프레스 온도는 일반적으로 80℃~200℃이다. 프레스 압력은 사용하는 각 촉매 전극층의 두께, 경도에 의존하지만, 일반적으로 0.5~20MPa이다.
이와 같이 제조된 음이온 교환막-전극 접합체는 상술한 도1에 도시한 바와 같은 기본구조의 고체 전해질용 연료 전지에 장착되어 사용된다.
[실시예]
이하, 본 발명을 더욱 상세하게 설명하기 위하여 실시예를 들어 설명하지만, 본 발명은 이들의 실시예에 한정되는 것은 아니다. 한편, 실시예, 비교예에서 연료 전지의 운전 특성을 이하에서 설명한다.
1)수소가스 연료에 함유되는 염기성 화합물 농도의 측정
염기성 화합물을 함유하는 수소가스를 10mM 황산수용액 100ml(흡수액) 중에 통과시키고, 통과시킨 수소가스의 체적이 1L(25℃에서)가 될 때까지 이를 수행하였다. 이 흡수액 중의 염기성 화합물의 농도를 이온 크로마토그래피로 분리 분석하였다. 함유되는 염기성 화합물 농도의 산출은, 이하의 계산식과 이미 알고 있는 농도(단위:mol/L)의 염기성 화합물 수용액(표준 농도 용액이라고 칭함)을 측정했을 때의 크로마토 피크의 피크면적을 이용하여 행하였다.
흡수액 중의 염기성 화합물의 양(mol)= Asoln / Astd x Cstd x Vsoln
여기서, 각 기호는 이하의 것을 나타낸다.
Asoln : 흡수액을 측정했을 때의 크로마토 피크의 면적
Astd : 표준 농도 용액을 측정했을 때의 크로마토 피크의 면적
Cstd : 상기 표준 농도 용액의 농도(mol/L)
Vsoln : 흡수액의 체적(L)
수소가스에 함유되는 염기성 화합물의 농도(mol/m3)=흡수액 중의 염기 화합물의 양(mol) ÷ 0.001(m3)
측정조건은 이하와 같다.
측정장치 다이오넥스사 ICS-2000
분리컬럼 IONPAC CS-14
측정시료체적 25μl
검출기 전도도검출기
용리액 조성 25mM 메탄술폰산/아세토니트릴(9/1) 혼합용액
용리액 유속 1ml/min
2)알칼리형 연료전지의 평가
(음이온 교환막의 작성)
폴리에틸렌으로 이루어진 다공질막(막 두께 25μm, 평균 공경 0.03μm, 공극율 37%)에, 클로로메틸스틸렌 97질량부, 디비닐벤젠 3질량부, 에틸렌글리콜디글리시딜에테르 5질량부, t-부틸퍼옥시에틸헥사노에이트 5질량부로 이루어지는 중합성 단량체 조성물을 함침시키고, 100μm 폴리에스테르필름을 박리재로 다공질막의 양측을 피복한 후, 0.3MPa의 질소 가압 하에, 80℃에서 5시간 가열 중합하였다. 얻어진 막상물을 6질량%의 트리메틸아민과 25질량%의 아세톤을 포함하는 수용액 내에 실온에서 16시간 침적시키고, 4급 암모늄염기를 음이온 교환기로 갖는 연료 전지용 음이온 교환막을 얻었다.
얻어진 음이온 교환막의 음이온 교환 용량은 1.8mmol/g, 25℃에서 함수율은 25%, 건조 막 두께는 28μm이었다.
음이온 교환막은 0.5mol/L의 수산화나트륨 수용액에 함침시키고, 음이온 교환기의 반대 이온을 OH-로 이온 교환하였다.
그 후, 대기 중에서 12시간 이상 방치한 후, 그 막을 연료 전지 출력 평가에 사용하였다.
(음이온 교환막-촉매 전극 접합체의 작성)
{폴리스틸렌-폴리(에틸렌-부틸렌)-폴리스틸렌}트리블럭 공중합체(아사히 카세이 케미칼 제조, '터프테크H1031')을 클로로메틸화한 것을 6질량%의 트리메틸아민과 25질량%의 아세톤을 포함하는 수용액 중에 실온에서 16시간 침적시키고, 또한 0.5mol/L-NaOH 수용액에 10시간 이상 침적하여 촉매 전극층용의 음이온 전도성 아이오노머(OH-형)를 합성하였다. 당해 아이오노머는 중량 평균 분자량 30000이고, 음이온 교환용량은 1.5mmol/g- 건조수지, 25℃에서 함수율은 120질량%이었다.
이 음이온 전도성 아이오노머를 130℃의 오토 클레이브 내에 1-프로판올에 3시간 걸쳐 용해시켜, 농도 5질량%의 아이오노머 용액을 얻었다.
이어서, 상기 아이오노머 용액과 평균 입자직경 2nm의 백금촉매를 50질량% 담지시킨 카본블랙을 혼합하여 촉매 전극층 형성용 조성물을 작성하였다. 그 다음에, 당해 조성물을 음이온 교환막의 한쪽 면에 인쇄하고, 대기 중 25℃에서 12시간 이상 건조하여 애노드를 형성하였다. 또한, 음이온 교환막의 다른 한쪽의 면에도 마찬가지로 하여 캐소드를 형성하고, 음이온 교환막-촉매 전극접합체를 얻었다. 애노드 면 및 캐소드 면 모두, 백금 양은 0.4mg/cm2이 되도록 하고, 이들 촉매 전극층의 아이오노머 함유량은 모두 30질량%이었다. 또한, 촉매 전극층의 면적은 각각 5cm2이다.
(연료 전지 출력 시험)
얻어진 음이온 교환막-촉매 전극 접합체의 양면에 폴리테트라플루오르에틸렌에서 발수화 처리한 두께가 300μm의 카본 크로스(일렉트로켐사 제조 EC-CC1-060T)를 겹쳐, 이를 도1에 나타난 연료 전지 셀에 장착시켰다. 이어서, 연료 전지 셀 온도를 50℃로 설정하고, 애노드 실에는, 50℃로 가온한 염기성 화합물 수용액을 통과시킨 수소를 50ml/min으로 공급하고, 캐소드 실에는, 봄베로부터 공기를 50℃에서 95%RH로 가습하여 200ml/min로 공급하여 발전 시험을 수행하였다. 염기성 화합물 수용액의 농도에 의해, 수소 가스에 함유된 염기성 화합물의 농도를 제어하였다. 함유되는 염기성 화합물의 농도는 상기 방법에 의해 별도로 측정하였다. 셀 전압 0.2V에서 2시간 발전을 행한 후에, 전류 밀도 0A/cm2에서 셀 전압(개회로 전압) 및 0.2A/cm2에서 셀 전압을 측정하여 출력을 평가하였다.
[실시예 1~9]
각종 농도의 염기성 화합물을 함유하는 수소 가스를 애노드에 공급하고, 출력 시험을 수행하였다. 산화제 가스로서는 이산화탄소를 380ppm 함유하는 공기를 사용하였다. 결과를 표1에 나타냈다. 또한, 함유된 염기성 화합물의 수소에 대한 농도를 측정하였다. 결과를 표1에 함께 나타냈다.
[비교예 1]
실시예 1에서, 염기성 화합물을 함유하지 않는 수소 가스를 이용하는 것을 제외하고는 실시예 1과 마찬가지로 하여 출력 시험을 수행하였다. 출력 시험 결과를 표1에 나타냈다.
염기성 화합물이 포함된 수소가스를 이용하면, 셀 전압이 높아지고, 출력이 향상되는 것이 나타났다.
[실시예 10~15]
실시예 1에서, 산화제 가스로써 이산화탄소를 함유하지 않는 공기를 사용한 것을 제외하고는 실시예 1과 마찬가지로 하여 출력 시험을 행하였다. 결과를 표2에 나타냈다.
[비교예 2]
실시예 10에서, 염기성 화합물을 함유하지 않는 수소 가스를 이용하는 것을 제외하고는, 실시예 10과 마찬가지로 하여 출력 시험을 행하였다. 출력 시험 결과를 표2에 나타냈다.
이산화탄소를 함유하지 않는 공기를 이용한 경우에는, 염기성 화합물을 함유하지 않는 수소를 이용한 경우에도, 이산화탄소를 380ppm함유하는 수소를 이용한 실시예 1~9에 비하여, 셀 전압은 높은 값이 되었다. 그러나, 실시예 10~15에 나타내는 바와 같이 염기성 화합물이 포함된 수소 가스를 이용하면, 더욱 셀 전압이 높아지고, 출력이 향상된 것이 나타났다.
|
|
염기성화합물 |
염기성화합물의 농도(mol/m3) | 산화제가스(공기)의 이산화탄소 함유의 유무 | 셀 전압(V) | |
| 0A/cm2 | 0.2A/cm2 | ||||
| 실시예 1 | 암모니아 | 3 | 유 | 0.94 | 0.37 |
| 실시예 2 | 암모니아 | 0.2 | 유 | 1.01 | 0.31 |
| 실시예 3 | 암모니아 | 1 | 유 | 0.98 | 0.35 |
| 실시예 4 | 암모니아 | 2 | 유 | 0.96 | 0.35 |
| 실시예 5 | 암모니아 | 4 | 유 | 0.92 | 0.36 |
| 실시예 6 | 암모니아 | 9 | 유 | 0.90 | 0.23 |
| 실시예 7 | 트리메틸아민 | 4 | 유 | 0.96 | 0.35 |
| 실시예 8 | 트리메틸아민 | 9 | 유 | 0.94 | 0.27 |
| 실시예 9 | 디에틸아민 | 8 | 유 | 0.95 | 0.33 |
| 비교예 1 | --- | --- | 유 | 1.03 | 0.21 |
|
|
염기성 화합물 |
염기성 화합물의 농도(mol/m3) | 산화제 가스(공기)의 이산화탄소 함유의 유무 |
셀 전압(V) |
|
| 0A/cm2 | 0.2A/cm2 | ||||
| 실시예 10 | 암모니아 | 3 | 무 | 1.02 | 0.45 |
| 실시예 11 | 암모니아 | 0.2 | 무 | 1.03 | 0.37 |
| 실시예 12 | 암모니아 | 1 | 무 | 1.03 | 0.40 |
| 실시예 13 | 암모니아 | 2 | 무 | 1.02 | 0.40 |
| 실시예 14 | 암모니아 | 4 | 무 | 1.01 | 0.41 |
| 실시예 15 | 트리에틸아민 | 8 | 무 | 1.01 | 0.36 |
| 비교예 2 | --- | --- | 무 | 1.02 | 0.34 |
1 전지 격벽
2 연료 유통공
3 산화제 가스 유통공
4 애노드
5 캐소드
6 고체 고분자 전해질(음이온 교환막)
7 애노드 실
8 캐소드 실
2 연료 유통공
3 산화제 가스 유통공
4 애노드
5 캐소드
6 고체 고분자 전해질(음이온 교환막)
7 애노드 실
8 캐소드 실
Claims (5)
- 음이온 교환막으로 이루어지는 전해질막과, 그 양측에 배치된 한 쌍의 전극인 애노드와 캐소드를 포함하고, 애노드 측에 연료가스가 공급되고, 타측인 캐소드 측에 산화제 가스가 각각 공급되어 발전하는 알칼리형 연료 전지를 이용한 발전 시스템이며, 상기 애노드 측에 공급되는 연료가스로서, 염기성 화합물을 함유하는 수소가스를 이용하고,
상기 염기성 화합물은 상온에서 기체 상태의 화합물이고,
염기성 화합물을 함유하는 수소 가스 중에서, 상기 염기성 화합물의 함유량이 0.1~10mol/m3이고,
산화제 가스는 대기인 것을 특징으로 하는 알칼리형 연료전지를 이용한 발전 시스템. - 제 1 항에 있어서,
상기 염기성 화합물은 암모니아인 것을 특징으로 하는 발전 시스템. - 제 1 항 또는 제 2 항에 있어서,
상기 염기성 화합물을 함유하는 수소가스 중에서, 상기 염기성 화합물의 함유량이 0.1 내지 10 mol/m3 인 것을 특징으로 하는 발전 시스템. - 제 1 항 또는 제 2 항에 있어서,
상기 산화제 가스는 대기인 것을 특징으로 하는 발전 시스템. - 염기성 화합물을 함유하는 수소가스로 이루어지는 전해질막으로서 음이온 교환막을 이용한 알칼리형 연료전지용 연료가스.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2009-177642 | 2009-07-30 | ||
| JP2009177642A JP5404233B2 (ja) | 2009-07-30 | 2009-07-30 | アルカリ型燃料電池を用いた発電システムおよび該システムで用いるアルカリ型燃料電池用燃料ガス |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20120051663A true KR20120051663A (ko) | 2012-05-22 |
Family
ID=43529223
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020127002647A Withdrawn KR20120051663A (ko) | 2009-07-30 | 2010-07-22 | 알칼리형 연료전지를 이용한 발전 시스템 및 상기 시스템을 이용하는 알칼리형 연료 전지용 연료가스 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US8974984B2 (ko) |
| EP (1) | EP2461411A1 (ko) |
| JP (1) | JP5404233B2 (ko) |
| KR (1) | KR20120051663A (ko) |
| IL (1) | IL217817A0 (ko) |
| TW (1) | TW201121137A (ko) |
| WO (1) | WO2011013565A1 (ko) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20130130136A1 (en) * | 2011-06-24 | 2013-05-23 | Miles Page | Use of Ammonia as Source of Hydrogen Fuel and as a Getter for Air-CO2 in Alkaline Membrane Fuel Cells |
| JP5860636B2 (ja) * | 2011-08-25 | 2016-02-16 | シャープ株式会社 | アニオン交換膜型燃料電池システム |
| EP2940765A4 (en) * | 2012-12-28 | 2016-08-17 | Nitto Denko Corp | METHOD FOR PRODUCING AN ANION EXCHANGE MEMBRANE, MEMBRANE ELECTRODE ARRANGEMENT FOR FUEL CELLS AND FUEL CELL |
| US20150349368A1 (en) * | 2014-05-29 | 2015-12-03 | Christopher G. ARGES | Reversible alkaline membrane hydrogen fuel cell-water electrolyzer |
| JP6474242B2 (ja) * | 2014-11-25 | 2019-02-27 | 株式会社三共 | 遊技機 |
| JP6420682B2 (ja) * | 2015-02-06 | 2018-11-07 | 株式会社トクヤマ | 燃料電池システム |
| JP2018063748A (ja) * | 2015-02-27 | 2018-04-19 | 株式会社トクヤマ | 陰イオン交換膜型燃料電池の運転方法及び燃料電池システム |
| IL260880B (en) * | 2018-07-30 | 2019-11-28 | Pocell Tech Ltd | Alkaline fuel cell with a membrane directly fed with ammonia and a method for operating it |
| JP7234663B2 (ja) * | 2018-12-17 | 2023-03-08 | 株式会社Ihi | 燃料電池システムおよび燃料電池システムの運転方法 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4749604B2 (ja) | 2001-06-12 | 2011-08-17 | 株式会社トクヤマ | ガス拡散電極用イオン伝導性付与剤 |
| JP5004525B2 (ja) | 2005-07-01 | 2012-08-22 | 株式会社トクヤマ | 燃料電池用隔膜 |
| JP2008218397A (ja) | 2007-02-08 | 2008-09-18 | Toyota Motor Corp | 燃料電池 |
| JP2008204647A (ja) * | 2007-02-16 | 2008-09-04 | Nippon Synthetic Chem Ind Co Ltd:The | アニオン交換膜型燃料電池用の電解質膜および接着剤 |
| US20100035111A1 (en) | 2007-03-27 | 2010-02-11 | Daihatsu Motor Co., Ltd. | Fuel cell |
| JP5194569B2 (ja) * | 2007-05-31 | 2013-05-08 | トヨタ自動車株式会社 | 燃料電池 |
| JP5219121B2 (ja) * | 2007-10-10 | 2013-06-26 | 独立行政法人産業技術総合研究所 | 直接型燃料電池 |
-
2009
- 2009-07-30 JP JP2009177642A patent/JP5404233B2/ja not_active Expired - Fee Related
-
2010
- 2010-07-14 TW TW099123081A patent/TW201121137A/zh unknown
- 2010-07-22 KR KR1020127002647A patent/KR20120051663A/ko not_active Withdrawn
- 2010-07-22 EP EP10804311A patent/EP2461411A1/en not_active Withdrawn
- 2010-07-22 US US13/387,130 patent/US8974984B2/en not_active Expired - Fee Related
- 2010-07-22 WO PCT/JP2010/062304 patent/WO2011013565A1/ja not_active Ceased
-
2012
- 2012-01-29 IL IL217817A patent/IL217817A0/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| EP2461411A1 (en) | 2012-06-06 |
| US8974984B2 (en) | 2015-03-10 |
| WO2011013565A1 (ja) | 2011-02-03 |
| IL217817A0 (en) | 2012-03-29 |
| TW201121137A (en) | 2011-06-16 |
| EP2461411A9 (en) | 2012-08-15 |
| JP2011034710A (ja) | 2011-02-17 |
| US20120122006A1 (en) | 2012-05-17 |
| JP5404233B2 (ja) | 2014-01-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4606487B2 (ja) | 固体高分子電解質型燃料電池用陰イオン交換膜の製造方法 | |
| TWI474549B (zh) | Operation method of anion exchange membrane fuel cell | |
| JP5055116B2 (ja) | イオン交換膜を含む固体アルカリ型燃料電池 | |
| KR20120051663A (ko) | 알칼리형 연료전지를 이용한 발전 시스템 및 상기 시스템을 이용하는 알칼리형 연료 전지용 연료가스 | |
| JP6077774B2 (ja) | イオン伝導性付与剤並びにカソード触媒層並びに該触媒層を用いて形成する膜−電極接合体並びに陰イオン交換膜型燃料電池及びその運転方法 | |
| US8440366B2 (en) | Solid polymer electrolyte fuel cell membrane with anion exchange membrane | |
| KR102296050B1 (ko) | 연료 전지용 전해질 막 및 이의 제조 방법 | |
| US20110104590A1 (en) | Method for Producing Ion Conductivity Providing Agent for Catalyst Electrode Layer in Anion-Exchange Membrane Type Fuel Cell | |
| JP5618584B2 (ja) | 固体高分子型燃料電池用燃料 | |
| WO2022157757A1 (en) | Membrane assemblies and separation layers for fuel cells and electrolyzers | |
| JP2003142124A (ja) | 電解質膜およびそれを用いた固体高分子型燃料電池 | |
| JP5355178B2 (ja) | 低温作動型燃料電池の運転方法 | |
| JP2013045670A (ja) | 燃料電池装置 | |
| Field et al. | Exploring Operating Conditions and Nafion Membranes for the Direct Methanol Fuel Cell (DMFC) |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20120130 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |