KR20110117841A - Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 - Google Patents
Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 Download PDFInfo
- Publication number
- KR20110117841A KR20110117841A KR1020100037299A KR20100037299A KR20110117841A KR 20110117841 A KR20110117841 A KR 20110117841A KR 1020100037299 A KR1020100037299 A KR 1020100037299A KR 20100037299 A KR20100037299 A KR 20100037299A KR 20110117841 A KR20110117841 A KR 20110117841A
- Authority
- KR
- South Korea
- Prior art keywords
- pepck
- canine
- egg
- nuclear transfer
- promoter
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/8509—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells for producing genetically modified animals, e.g. transgenic
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/027—New or modified breeds of vertebrates
- A01K67/0273—Cloned vertebrates
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K67/00—Rearing or breeding animals, not otherwise provided for; New or modified breeds of animals
- A01K67/027—New or modified breeds of vertebrates
- A01K67/0275—Genetically modified vertebrates, e.g. transgenic
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2217/00—Genetically modified animals
- A01K2217/05—Animals comprising random inserted nucleic acids (transgenic)
- A01K2217/052—Animals comprising random inserted nucleic acids (transgenic) inducing gain of function
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2267/00—Animals characterised by purpose
- A01K2267/03—Animal model, e.g. for test or diseases
- A01K2267/035—Animal model for multifactorial diseases
- A01K2267/0362—Animal model for lipid/glucose metabolism, e.g. obesity, type-2 diabetes
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Environmental Sciences (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Animal Husbandry (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- General Engineering & Computer Science (AREA)
- Biodiversity & Conservation Biology (AREA)
- Wood Science & Technology (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Plant Pathology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Physics & Mathematics (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
본 발명에 따른 PEPCK 유전자를 과발현하는 형질전환 복제 개과 동물은 당뇨병 동물 모델로서, 제2형 당뇨병의 유전적 원인 규명과 진단 시약 및 치료제 개발에 이용될 수 있다.
Description
도 2는 H41IIE 세포에서 개의 PEPCK 프로모터의 활성을 웨스턴 블롯 분석으로 나타낸 것이다.
도 3은 본 발명에 따른 재조합 발현 벡터 pGL3_dPEPCK의 모식도를 나타낸 것이다.
도 4는 형질전환 공여핵원세포와 형질전환된 복제견의 유전체 DNA에 대한 PCR 분석 결과를 나타낸 것이다.
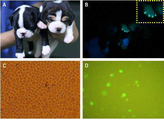
도 5는 일반광(a)과 형광(b)하에서 EGFP의 발현 유무를 확인한 결과를 나타낸 것이다(좌측견: 일반 복제견 보스턴 테이러, 우측견: 형질전환 복제견 비글).
도 6은 공여핵원, 복제자견과 대리모의 Microsatellite 분석 결과를 나타낸 것으로, 공여핵원과 DMP-108. DMP110 피크값이 같음을 알 수 있고, 이를 통해 공여핵원과 복제산자가 유전적으로 일치함을 밝혔다.
| S-D-Ta |
No. of oocytes transferred | No. of recipients | No. of pregnancy (%) | No. of puppies born (%) |
| 1.9-30-2 | 66 | 6 | 1 (16.7) | 1 (1.5) |
| 2.0-30-2 | 94 | 9 | 3 (33.3) | 3 (3.2) |
| 2.1-30-2 | 51 | 5 | 3 (60.0) | 3 (5.9) |
| 2.2-30-2 | 32 | 2 | 1 (50.0) | 1 (3.2) |
| 세포의 종류 | No. and (%) of oocytes | No. of recipients | Pregnancy status (%) of recipients | No. of puppies born | ||
| Used for NT | Successfully fused | Day 30 pregnancy | Full term | |||
| 성체 섬유아세포 | 152 | 147 (96.7) | 9 | 1 (11.1) | 1 (11.1) | 1 |
| 재복제된 태아 섬유아세포 | 118 | 115 (97.5) | 10 | 3 (30.0) | 2 (20.0) | 2 |
| 일반 태아 섬유 아세포 | 66 | 51 (77.3) | 4 | 2(50.0) | 2 (50.0) | 2 |
| Offspring identification | Karyoplast passage no. | Gestation length | Birth weight (g) | Delivery method | GFP expressionc |
| DFN59 | 5 | 44 | N/Aa | Natural | - |
| DFN60 | 5 | 65 | 380b | Cesarean section | - |
| DFN64 | 5 | 63 | 340 | Cesarean section | - |
| DMP108 | 6 | 62 | 380 | Cesarean section | + |
| DMP110 | 6 | 63 | 360 | Cesarean section | + |
Claims (13)
- PEPCK (Phosphoenol Pyruvate Carboxykinase)를 코딩하는 핵산으로 형질전환된 개과 동물 유래 체세포 핵을 탈핵된 난자에 이식하여 형성된 개과 동물의 핵 이식란.
- 제 1항에 있어서, 상기 핵 이식란은 수탁번호 제 KCTC11360BP 호로 기탁된 것을 특징으로 하는 핵 이식란.
- 제 1항에 있어서, 상기 PEPCK 코딩 핵산은 (1) 개의 PEPCK 유전자에 천연적으로 존재하는 전장의 프로모터, (2) 상기 전장의 프로모터로부터 -2349 염기까지 제거된 프로모터, (3) 상기 전장의 프로모터로부터 -1018 염기까지 제거된 프로모터, (4) 상기 전장의 프로모터로부터 -746 염기까지 제거된 프로모터로 이루어진 그룹으로부터 선택된 프로모터의 조절하에 위치하는 것을 특징으로 하는 핵 이식란.
- 제 1항에 있어서, 상기 PEPCK 코딩 핵산은 개과 동물로부터 유래된 것을 특징으로 하는 핵 이식란.
- 제 1항에 있어서, 상기 개과 동물의 체세포는 태아의 섬유아세포인 것을 특징으로 하는 핵 이식란.
- 제 1항에 있어서, 상기 개과 동물은 개임을 특징으로 하는 핵 이식란.
- (a) 개과 동물에서 유래한 체세포주를 PEPCK 코딩 핵산으로 형질전환시키는 단계를 포함하여 공여핵원세포를 준비하는 단계; (b) 개과 동물의 성숙난자로부터 핵을 제거하는 단계; (c) 상기 (b) 단계의 탈핵 난자에 (a) 단계의 공여핵원세포를 미세주입하고 전기 융합시키는 단계를 포함하는 PEPCK 유전자로 형질전환된 개과 동물의 핵 이식란의 생산방법.
- 제 7항에 있어서, 상기 핵 이식란은 수탁번호 제 KCTC11360BP 호로 기탁된 것을 특징으로 하는 생산방법.
- 제 7항에 있어서, 상기 (b) 단계의 개과 동물의 성숙난자는 개과 동물의 배란일로부터 70 ~ 90 시간에 회수된 것임을 특징으로 하는 생산방법.
- 제 7항에 있어서, 상기 (c) 단계에서 전기융합은 직류 전압 1.9~2.2kV/cm로, 시간은 15~45㎲동안, 회수는 1~3회 수행하는 것을 특징으로 하는 생산방법.
- 제 1항에 따른 핵 이식란을 대리모의 난관에 이식하여 산자를 출생하는 단계를 포함하는 PEPCK를 과발현하는 형질전환 복제 개과 동물의 생산방법.
- 제 11항에 있어서, 상기 핵 이식란은 수탁번호 제 KCTC11360BP 호로 기탁된 것을 특징으로 하는 생산방법.
- 제 11항에 따른 방법에 의하여 생산된 PEPCK를 과발현하는 형질전환 복제 개과 동물.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020100037299A KR20110117841A (ko) | 2010-04-22 | 2010-04-22 | Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 |
| PCT/KR2011/002944 WO2011132990A2 (ko) | 2010-04-22 | 2011-04-22 | Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020100037299A KR20110117841A (ko) | 2010-04-22 | 2010-04-22 | Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020120065716A Division KR20120092534A (ko) | 2012-06-19 | 2012-06-19 | Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20110117841A true KR20110117841A (ko) | 2011-10-28 |
Family
ID=44834689
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020100037299A Ceased KR20110117841A (ko) | 2010-04-22 | 2010-04-22 | Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR20110117841A (ko) |
| WO (1) | WO2011132990A2 (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4342476A4 (en) * | 2021-05-21 | 2025-05-07 | Daewoong Pharmaceutical Co., Ltd. | Pharmaceutical composition for the prevention or treatment of diabetes mellitus in animals of the family Canidae containing enavogliflozin |
| CN116098122A (zh) * | 2022-10-25 | 2023-05-12 | 中国科学院深圳先进技术研究院 | 一种癫痫动物模型的制备方法及应用 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100733012B1 (ko) * | 2005-07-26 | 2007-06-28 | 재단법인서울대학교산학협력재단 | 복제된 개과 동물 및 이의 생산 방법 |
| KR20090115025A (ko) * | 2008-04-30 | 2009-11-04 | 황우석 | 개과 동물의 복제 생산 방법 |
-
2010
- 2010-04-22 KR KR1020100037299A patent/KR20110117841A/ko not_active Ceased
-
2011
- 2011-04-22 WO PCT/KR2011/002944 patent/WO2011132990A2/ko not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| WO2011132990A3 (ko) | 2012-03-08 |
| WO2011132990A2 (ko) | 2011-10-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20080060089A1 (en) | Process for producing exogenous protein in the milk of transgenic mammals and a process for purifying proteins therefrom | |
| WO1988001648A1 (en) | Expression of heterologous proteins by transgenic lactating mammals | |
| KR20110117841A (ko) | Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 | |
| KR101890978B1 (ko) | 알츠하이머 질환 모델용 형질전환 돼지 및 이의 용도 | |
| CN115322993B (zh) | 一种用于猪基因组定点整合外源基因的安全位点及用其构建猪育种群方法 | |
| KR101431783B1 (ko) | 알츠하이머 모델용 형질전환 개과 동물 및 이의 제조방법 | |
| CN111073900B (zh) | 一种提高猪克隆胚胎发育效率的方法 | |
| KR20120092534A (ko) | Pepck 과발현 형질전환 복제 개과 동물 및 이의 생산방법 | |
| KR101832485B1 (ko) | 목적유전자를 조건적으로 발현하는 복제된 개과동물의 생산방법 | |
| KR100790514B1 (ko) | Csf를 유선에서 발현하는 형질전환 복제 돼지 및 그의제조 방법 | |
| KR100905709B1 (ko) | hGM―CSF를 생산하는 형질전환된 복제 산양 및 이의제조방법 | |
| RU2390562C2 (ru) | Способ получения трансгенных млекопитающих, которые продуцируют экзогенные белки в молоке, и трансгенные млекопитающие, полученные таким способом | |
| KR20090115081A (ko) | 개과 동물의 복제 생산 방법 | |
| US10036041B2 (en) | Method for positioning and integrating transgene and use thereof | |
| CN102558343A (zh) | 突变型生长激素受体及其应用 | |
| KR20230009140A (ko) | Human mutant Presenilin-1 발현 인지장애 모델 개의 생산 | |
| KR20050022811A (ko) | 여윈 표현형을 갖는 유전자 이식 생쥐 | |
| MXPA06003480A (en) | A process of making transgenic mammals that produce exogenous proteins in milk and transgenic mammals produced thereby | |
| JP2007082446A (ja) | トランスジェニック動物、その作出方法及びそのための核酸 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20100422 |
|
| PA0201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20110919 Patent event code: PE09021S01D |
|
| PG1501 | Laying open of application | ||
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20120520 Comment text: Decision to Refuse Application Patent event code: PE06012S01D Patent event date: 20110919 Comment text: Notification of reason for refusal Patent event code: PE06011S01I |
|
| A107 | Divisional application of patent | ||
| PA0107 | Divisional application |
Comment text: Divisional Application of Patent Patent event date: 20120619 Patent event code: PA01071R01D |