KR100729887B1 - 알로에로부터 유래된 다당류를 포함하는 조성물 - Google Patents
알로에로부터 유래된 다당류를 포함하는 조성물 Download PDFInfo
- Publication number
- KR100729887B1 KR100729887B1 KR1020067017809A KR20067017809A KR100729887B1 KR 100729887 B1 KR100729887 B1 KR 100729887B1 KR 1020067017809 A KR1020067017809 A KR 1020067017809A KR 20067017809 A KR20067017809 A KR 20067017809A KR 100729887 B1 KR100729887 B1 KR 100729887B1
- Authority
- KR
- South Korea
- Prior art keywords
- immuno
- aloe
- polysaccharides
- polysaccharide
- composition
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/14—Preparation of compounds containing saccharide radicals produced by the action of a carbohydrase (EC 3.2.x), e.g. by alpha-amylase, e.g. by cellulase, hemicellulase
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/88—Liliopsida (monocotyledons)
- A61K36/886—Aloeaceae (Aloe family), e.g. aloe vera
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B37/00—Preparation of polysaccharides not provided for in groups C08B1/00 - C08B35/00; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/04—Polysaccharides, i.e. compounds containing more than five saccharide radicals attached to each other by glycosidic bonds
Abstract
본 발명은 알로에로부터 유래된 다당류를 포함하는 조성물을 제공한다. 본 발명은, 다당류의 활성화된 혼합물(본원에서는 "면역-10"으로 언급됨)을 포함한다. 본 발명은 또한 면역 촉진제, 면역 조절제, 상처 치유제로서의 상기 다당류의 용도를 포함한다. 생성되는 면역 조절 복합체는, 종래기술의 알콜 침전 체계(scheme)를 사용하여 분리된 벌크(bulk) 탄수화물보다 더 안정하며 더 높은 활성을 갖는다.
알로에, 다당류 혼합물, 면역-10, 면역 촉진제, 면역 조절제
Description
도 1은, 알로에로부터 면역-10을 제조하기 위한 본 발명의 일반적인 방법을 개략적으로 예시(illustrate)한 것이다.
도 2는, 한정된 효소 가수분해, 탈색 및 여과 후의 면역-10의 크로마토그램(실시예 1)을 나타낸 것이다. 페놀 황산 방법을 사용하여 490 nm 에서 흡수도(absorbance)를 모니터하면서 크로마토그래피를 세파로오즈 CL-4B 칼럼상에서 수행하였다.
도 3은, 실시예 3의 방법에 따라 제조된, 부분적으로 정제된 면역-10의 크로마토그램을 나타낸 것이다. 크로마토그래피는, 490 nm 에서 흡수도를 모니터하면서 세파덱스 G-100 칼럼상에서 수행되었다.
도 5는 세개의 다른 방법에 의해 분리된 알로에 다당류의 크로마토그램을 도시한 것이다. 여기서 세개의 다른 방법에 의해 얻은 다당류는 첫째, 공지의 방법을 사용하여 신선한 추출물로부터 정제된 다당류(▲), 둘째, 동결건조된 알로에 겔로 부터 유래된 다당류(■), 셋째, 알로에 전체 잎에서 유래된 다당류(●)이다. 크로마토그래피는, 490nm에서 흡수도를 모니터하면서 세파로오스 CL-4B 칼럼상에서 수행되었다.
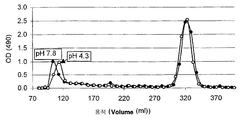
도 6은 실온에서 pH 4.3(○) 및 pH 7.8(●)의 H2O내에 3개월간 방치한 후 세파덱스 G-100 칼럼상에서의 면역-10의 크로마토그램을 도시한 것이다.
도 7은 실온에서 pH 4.3(○) 및 pH 7.8(●)의 H2O내에 3개월간 방치한 후 세파덱스 G-100 칼럼상에서의 정제된 천연 알로에 다당류의 크로마토그램을 도시한 것이다.
도 8은 피부 면역 기능을 복원시키는 면역-10의 능력을 그래프로 예시한 것이다(접촉 과민성 UVB 분석).
도 9는 UVB 조사에 의해 유도된 종양괴사인자-α(TNF-α)의 방출이 면역-10에 의해 억제되는 것을 그래프로 예시한 것이다.
도 10은 마우스 복막(peritoneal)의 마크로파지로부터의 TNF-α방출을 면역-10이 촉진하는 것을 그래프로 예시한 것이다.
도 11은 면역-10에 의한 세포 증식의 촉진을 그래프로 예시한 것이다.
본 발명은 알로에로부터 유래된 다당류(polysaccharide)를 포함하는 조성물에 관한 것이다. 본 발명은, 본 발명의 방법에 의해 생산된, 다당류의 활성화된 혼합물(본원에서는 "면역-10" 또는 "면역-10 다당류"로 언급함)을 포함한다. 본 발명은 또한 면역 촉진제, 면역 조절제 및 상처 치유제로서의 다당류의 용도를 포함한다.
알로에는 많은 생물학적 활성 물질들을 함유하는 복잡한 식물이다(코헨 외 다수의 문헌, 상처 치유/생화학적 및 임상적인 면, 제1판, WB 사운더스, 필라델피아(1992)). 알로에의 종은 300 개 이상 알려져 있으며, 그 중 대부분은 아프리카의 토착종이다. 그 생물학적 활성 물질들은, 알로에 잎의 3개의 별도 영역 - 잎의 피층(cortex), 잎 껍질(rind) 또는 잎 중앙내에 위치한 투명한(clear) 겔 필릿(fillet) 및 잎 껍질과 내부 겔 필릿 사이에 위치한 관다발의 내초(pericyclic) 세포에 함유된 황색 유체(라텍스로 호칭됨) 내에 존재한다고 연구에 의해 밝혀졌다. 역사적으로, 알로에 제품은 화상, 미란(sore) 및 기타 상처의 치료를 위한 피부과 용도로 사용되었다. 이 용도들로 인해, 임상적 효능을 지닌 화합물들, 특히 항염증 활성을 지닌 화합물들을 알로에로부터 동정(identify)하기 위한 연구들이 많이 행해졌다.(예를들면 그린드레이(Grindlay) 및 레이놀즈(Reynolds)(1986) J. of Ethnopharmacology 16:117-151; 하트(Hart) 외 다수.(1988) J. of Ethnopharmacology 23: 61-71 참조). 이들 연구의 결과로서, 항-종양 활성, 항-산(acid) 활성(히라타(Hirata) 및 슈거(Suga)(1977) Z. Naturforsch 32c:731-734), 항-당뇨 활성, 타이로시나아제(tyrosinase) 억제 활성(야기(Yagi) 외 다수. (1987) Planta Medica 515-517) 및 항산화제 활성(국제 특허 출원 PCT/US95/07404, 1996년 12월 19일 공개, 국제 공개 번호 WO 96/40182)을 비롯하여, 다양한 생물학적 활성을 지니는 알로에 화합물에 대한 보고서가 많이 있다.
알로에 제품이 면역계를 자극할 수 있다는 것이 또한 보고되어 있다. 면역계를 자극하는 알로에의 능력은, 겔 내에 존재하는 다당류에 기인한 것이다.(예를들면 데이(Day) 외 다수.(1922) J. Am. Pharm. Assoc. 11: 462-463; 플라그(Flagg)(1959) American Perfumes and Aromatics 74:27-28, 61; 왈러(Waller) 외 다수.(1978) Proc. Okla.Acad.Sci. 58:69-76; 스처부킨(Shcherbukhin) 외 다수.(1979) Applied Biochemistry & Microbiology 15:892-896; 만달(Mandal) 외 다수.(1980) Carbohydrate Research 86:247-257; 만달 외 다수.(1980) Carbohydrate Research 87:249-256; 윈터스(Winters) 외 다수.(1981) Eco. Botany 35:89-95; 롭손(Robson) 외 다수.(1982) J.Burn Care Rehab. 3:157-163; 이반(Ivan) 외 다수.(1983) Drug & Cosmetic Ind. 52-54,105-106; 스모더스(Smothers) (1983) Drug & Cosmetic Ind. 40:77-80; 만달 외 다수.(1983) Indian J. of Chem. 22B:890-893; 빌카스(Vilkas) 외 다수(1986) Biochimie 68:1123-1127; 왈러 외 다수 (1994) Cosmetic Toiletries Manufacturing Worldwide 64-80; 맥카널리(McAnally) 외 다수의 미국 특허 제5,308,838호)
알로에 제품은 또한 자외선 조사의 유해한 영향에 대해서 피부를 보호하기 위해 향장(cosmetic) 산업에서도 광범위하게 사용된다(그롤리어(Grollier)외 다수. 미국 특허 4,656,029, 1987년 4월 7일 특허됨). 사람 및 실험 동물에 있어서 피부 가 만성적으로 자외선 조사에 노출되면, 피부암이 유발된다. 실험 동물의 피부를 자외선 B (UVB) 조사(280-320 nm)에 노출시키면 피부 면역계의 억제가 유발되어, UV(자외선)-유도된 피부 암, 접촉-감작성 합텐(hapten) 및 다양한 전염성 미생물에 대한 면역 반응을 전개하는 피부 면역계의 능력이 손상된다(스트릭랜드(Strickland)(1994) J.Invest.Dermatol. 102:197-204, 및 여기에 삽입된 참고문헌 참조). 스트릭랜드 외 다수의 연구에서, 알로에 베라 겔(Aloe vera gel)을 국소 적용하면, UVB 노출에 의해 야기되는 면역계의 억제가 감소된다는 것이 밝혀졌다(스트릭랜드(1994) J.Invest.Dermatol. 102:197-204).
면역계의 억제를 감소시키는 천연(native) 겔의 능력은, 매우 낮고 불규칙하며 또한 시간이 지나면서 감소된다. 이에 대한 한가지 가설은, 알로에 식물 내에 천연적으로 존재하는 효소 및/또는 박테리아 분해에 의해, UV-B 에 대한 차단(protective) 인자가 가수분해된다는 것이다. 그러므로, 알로에로부터 다당류를 분리하는 것이 이 면역조절 활성을 보존하는 데 도움이 될 것이다. 그러나, 알로에로부터 다당류를 벌크(bulk) 분리하기 위한 선행기술 방법들은, 그 면역조절 활성을 효과적으로 보존하지 않는다. 이들 방법은, 예를들면 미국 특허 출원 제4,957,907호, 제4,966,892호 및 제5,356,811호에 기재되어 있는데, 장시간(4 ~ 24시간)의 알콜 침전 및 원심분리 단계를 사용한다. 선행기술 방법들이 알로에 겔의 면역조절 활성을 효과적으로 보존하지 못하는 것을 고려해 볼 때, 면역조절 활성이 보유 및 안정화될 수 있는, 알로에로부터의 다당류의 분리 방법을 갖는 것이 유용하다.
따라서, 본 발명에서는 이러한 점을 감안하여 이루어진 것으로, 다당류의 활성화된 혼합물을 포함하고 면역 촉진제, 면역 조절제 및 상처 치유제로서 면역 조절 복합체는 종래 알콜 침전 체계(scheme)를 사용하여 분리된 벌크(bulk) 탄수화물보다 더 안정하며 더 높은 활성을 갖는, 알로에로부터 유래된 다당류를 포함하는 조성물을 제공하고자 한다.
본원은 알로에로부터 유래된 다당류를 포함하는 조성물에 관한 것이다. 상기 조성물의 면역 촉진제, 면역 조절제 및 상처 치유제로서의 용도도 본 발명에 포함된다. 본 발명의 방법에 의해 분리된 다당류의 활성은, 천연 알로에 겔 추출물의 활성보다 훨씬 높고 훨씬 더 안정하며 재현성도 매우 크다.
본 발명의 방법은 (a) 알로에로부터 알로에 겔 즙(juice)을 추출하는 단계; (b) 한정된 탄수화물 가수분해에 적합한 시간동안 및 온도에서 상기 알로에 겔 즙내에 있는 전체 다당류의 제어되고 한정된 효소적 가수분해를 수행하는 단계; (c) 상기 가수분해를 종결시키는 단계; 및 (d) 상기 가수분해된 생성물을 탈색 및 여과시키는 임의의(optional) 단계를 포함한다. 바람직한 구체예에서는, 25℃ ±1℃ 에서 2 ~ 2.5 시간동안 셀룰라아제를 첨가하는데 216 L 의 겔 추출물에 대해 0.5 g ~ 2.5 g 의 셀룰라아제의 비율로 첨가하여 한정된 가수분해를 수행한다. 도 1에 본 발명의 방법의 개략도가 제시되어 있다.
본 발명은, 본 발명의 방법에 의해 분리 및 제조된 다당류의 혼합물(본원에서는 "면역-10" 또는 "면역-10 다당류"로 언급되어 있음)을 포함한다. 상기 조성물(composition of matter)의 특징이 하기에 상세히 기재되었다.
본 발명은 또한, 면역 촉진제, 면역 조절제 및 상처 치유제로서의 면역-10의 용도를 포함한다. 면역-10은, UVB 조사에 노출된 마우스내에서 접촉 과민성(contact hypersensitivity: CH)의 억제를 방지하고 또 사람 표피모양암종(epidermoid carcinoma) 세포주내에서 UVB 조사에 의해 유발된 종양괴사인자(TNF-α) 방출을 억제한다. 본 발명의 방법에 의해 분리된 면역-10은, 면역 결핍 또는 면역-억제 질병을 지니고 있는 사람들을 위해 또는 HIV와 같은 질병의 치료를 위해, 사람 면역계의 복원(restoration) 또는 촉진을 위한 경구용 또는 국소용 제제로 사용될 수 있다. 본 발명의 방법에 의해 분리된 면역-10은 또한 상처 치유제로서도 유용하다. 본 발명의 방법에 의해 분리된 다당류는, 천연 알로에 겔보다 활성이 높고 더 안정하다.
본원에 기재된 방법은 알로에 다당류의 한정되고 제어된 가수분해를 포함하는데, 이 가수분해는 알로에 다당류의 안정성과 면역 조절 활성을 증가시키는 것으로 작용한다. 이 방법은, 선행기술의 방법보다 더 빠르고 더 간단하며 생산규모의 확대가 더 용이하고, 유기용매의 사용을 포함하지 않는다. 더우기, 본원에 기재된 방법은 알로에 다당류의 면역 조절 활성에 손실을 주지 않으면서 알로에 다당류의 용해도를 높이고 그 용액의 점도를 감소시킨다. 본 발명의 방법에 의해 분리된 면 역-10은, 동일한 알로에 겔 추출물로부터 정제된, 활성화된 벌크 다당류와 정성적으로(qualitatively) 유사한 UVB-차단(protective) 활성을 나타내지만, 벌크 다당류보다는 높은 고유 활성도(specific activity)를 가진다. 부가적으로, 정제된 면역-10은 천연 알로에 겔보다 2배 이상 높은 UVB CH(접촉 과민성) 복원 활성을 나타낸다.
상기의 일반적인 설명과 하기의 상세한 설명은 단지 본원 발명을 예시 및 설명하기 위한 것일 뿐, 본원 발명의 청구범위를 제한하는 것은 아니다.
본원은, 정의되고(defined) 생물학적으로 활성인 다당류 혼합물을 알로에로부터 분리 및 활성화시키는 방법에 관한 것이다. "알로에"라는 용어는 릴리아시(Liliaceae)과에서 세계적으로 발견되는 식물의 속명(genus)을 의미하며, Aloe barbadensis 식물은 릴리아시(Liliaceae)과에 속하는 종이다. 본 발명의 방법은, (a) 알로에로부터 알로에 겔 즙(juice)을 추출하는 단계; (b) 한정된(limited) 탄수화물 가수분해에 적합한 시간동안 및 온도에서 상기 알로에 겔 즙내에 있는 전체 다당류의 제어되고 한정된 가수분해를 수행하는 단계; (c) 상기 가수분해를 종결시키는 단계; 및 (d) 상기 가수분해된 생성물을 탈색 및 여과하는 임의의 단계를 포함한다.
본 발명의 방법의 개략도가 도 1에 제시되어 있다. 도 1을 참고로 살펴보면, 알로에 겔 즙(AGJ)은 신선한 겔 필릿(fillet)으로부터 당해분야에서 공지된 방법으로 생산되며, 이 공지 방법은 분쇄(grinding)를 포함하지만 이에 한정되지는 않는데, 이 공지의 분쇄 방법은 "톰프슨 알로에 즙 추출기"(텍사스주 할링겐에 소재하 는 Thompson Manufacturing Co.)를 사용하거나 압력(pressure) 롤러를 사용한다. 그후, 알로에 겔 즙은 가수분해제와 혼합된다. 가수분해제의 예는, 효소, 예를들면 셀룰라아제(cellulase), 펙티나아제(pectinase) 또는 만나나아제(mannanase)와, 비효소성 가수분해제, 예를들면 염산(hydrochloric acid) 및 트리플루오로아세트 산(trifluoroacetic acid)을 포함하나, 이에 한정되는 것은 아니다. 바람직한 구체예에서, 가수분해제는 효소이다. 가장 바람직하게는 가수분해제는 셀룰라아제, 예를 들어 셀룰라아제 4000 (Valley Research Inc.)이다. 생성되는 혼합물은, 한정된 탄수화물 가수분해에 적합한 시간동안 및 온도에서 인큐베이트된다(실시예 1 참조). 예를들어, 가수분해제가 셀룰라아제인 경우는, 이것은 216 L 의 겔 추출물에 대해 0.5 g ~ 2.5 g 의 셀룰라아제의 비율을 사용하여 25℃ ±1℃ 에서 2 ~ 2.5 시간동안이 바람직하다(실시예 4 참조).
그 후 적절한 시간이 지난 후에 탄수화물의 가수분해를 종결시킨다. 셀룰라아제가 사용된 경우에는, 이것은 바람직하게는 상기의 소화(digestion) 혼합물을 고온으로 가열시킴으로써 행해진다. 그 결과 생성된 면역-10은 이 단계에서 적색인데, 이 색은, 면역-10과 샤르콜(charcoal) 입자를 혼합하여 슬러리(slurry)를 형성시킴에 의해(실시예 1 참조) 또는 칼럼 크로마토그래피(column chromatography)에 의해 임의로 제거될 수 있다. 적합한 크로마토그래피 수지(resin)의 예로는 역상(reverse-phase) 수지를 들 수 있으나, 이에 한정되는 것은 아니다. 역상 수지의 예는, 방향족(aromatic) 수지, 예를들면 XAD 계열의 수지 및 CG-161 과, 비방향족 수지, 예를들면 C-4, C-8 및 C-18 를 포함하나, 이에 한정되는 것은 아니다. 바람 직한 구체예에서, 샤르콜 입자를 제거하기 위해 이러한 면역-10의 슬러리(slurry)를 여과시킨다. 이것은 당해 기술분야에 공지된 방법에 의해 수행될 수 있다. 본 발명의 바람직한 구체예는 다단계 여과 체계(scheme)를 사용하는데, 이 다단계 여과 체계에서 슬러리는 기공(pore)의 크기가 점차적으로 작아지는 일련의 필터를 통과한다(실시예 1과 표 1 및 2 참조). 예를들어 일부 구체예에서 슬러리는 30 ㎛의 필터 종이를 통해 여과된 다음, 1.0 ㎛의 필터 종이를 통해 여과되고 최종적으로 0.7 ㎛의 필터 종이를 통해 여과된다. 일부 구체예에서는 셀라이트(celite), FW12 또는 FW14와 같은 여과보조제(filtration aid)가, 여과될 혼합물내에 포함된다. 이 방법을 사용한 여과 후에, 여과액(filtrate)은 탈색되고 미세한 샤르콜 입자가 존재하지 않는다.
임의의(optional) 탈색 및 여과 후에, 면역-10은 저장을 위해서, 동결건조(lyophilization) 또는 스프레이-건조(spray-drying)에 의해 건조될 수 있다. 본 발명의 방법을 사용한 전형적인 수율(yield)은, 1L의 알로에 겔 즙당 대략 6g의 동결건조된 고체이다. 세파로오스(Sepharose) CL-4B 칼럼상에서의 면역-10의 크로마토그래피는, 490㎚에서의 2개의 탄수화물 피크(peak)의 존재(도 2)에 의해서 증명된 바와 같이, 면역-10이 다당류 및 단당류 분획 둘다를 함유하는 것을 보여준다. 면역 조절 활성이 다당류 피크내에 포함되어 있긴 하지만 상기 단당류들이 이 활성에 영향을 미치지 않는다(데이타는 도시되지 않음). 단당류는 한정된 효소적 소화(digestion) 전에 알로에 겔 즙의 다이아필트레이션(diafiltration)/투석에 의해 제거될 수 있다.
실시예 2 및 3에서는 약제 등급의 면역-10를 제조하는 방법을 설명하고 있는데, 약제 등급의 면역-10은 더 큰 생물학적인 활성과 안정성을 갖는 보다 순수한 형태의 면역-10이다.
본 발명은, 본 발명의 방법에 의해 생산된, 활성화된 다당류(본원에서는 "면역-10" 또는 "면역-10 다당류"로 언급됨)를 포함한다.
면역-10 내의 활성화된 다당류의 조성과 화학 구조를, 95% 이상의 순도를 갖는 약제 등급의 면역-10을 사용하여 결정하였다. 이는 하기와 같다.
크기 배제(size exclusion) 크로마토그래피 분석은, 50 ~ 200 kDa 의 범위와 함께 면역-10 내의 다당류의 평균 분자량이 70 ~ 80 kDa 이라는 것을 보여준다. 세파덱스 G-100 칼럼(Sephadex G-100 column)상에서의 크기 배제 크로마토그래피 및 슈퍼로우스(Superose) 12 칼럼(H10/30 Pharmacia)상에서의 HPLC 겔 투과(permeation)를 사용하여, 분자량을 측정했다.
단당류 조성의 분석에 의하면, 면역-10내의 다당류는 D-갈락토오스(D-galactose)(대략 5% 이하), D-글루코오스(D-glucose)(대략 5% 이하) 및 D-만노오스(D-mannose)(대략 90%)를 함유한다. 면역-10내의 다당류는 또한 미량(trace amount)의 자일로오스(xylose) 및 아라비노오스(arabinose)를 함유할 수도 있다.
더 고도로 정제된(실시예 2 및 3 참조) 약제 등급의 면역-10은, 1 대 9.6 ±2.2 의 비율로 D-갈락토오스 및 D-만노오스를 주로 함유하고 있다.
양자(proton) 및 13C NMR-스펙트로스코피(spectroscopy) 분석은, 상기 단당 류의 결합(linkage)이 주로 β-1,4 결합이라는 것을 나타낸다. 양자(proton) 및 13C NMR 스펙트럼은, 바리안(Varian) XL-300 분광계 상에서 분석되었다. 면역-10 다당류의 주된 구조는 β-1,4 글루코만난(glucomannan)이다. 더우기 다당류는 고도로 아세틸화(acetylated)되어 있다( 평균적으로 당(sugar) 잔기 1개당 대략 1개의 아세틸기). 단당류 유니트의 2, 3 및 6 위치는 -OH 또는 -OAc로 독립적으로 치환될 수 있다.
면역-10의 크로마토그래피는, 면역-10 이 다당류 및 단당류 분획 둘다를 함유하는 것을 나타낸다(도 2 참조). 활성화된 다당류의 단당류 조성은, 디오넥스(Dionex) 바이오-Lc 시스템을 사용하는 펄스(pulsed) 전류측정분석(amperometric) 검출기(HPAEC-PAD)와 함께 디오넥스 카보팩(CarboPac) PA1 칼럼상에서의 고성능 음이온-교환 크로마토그래피에 의해, 측정되었다. 면역 조절 활성이 다당류 피크(peak)내에 포함되어 있긴 하지만 상기 단당류들이 이 활성에 영향을 미치지 않는다(데이터는 도시되지 않음). 면역-10은 또한, 그 활성에 영향을 미치지 않는 다양한 염을 함유할 수도 있다.
면역-10은 열 및 단백질분해효소(protease)의 처리에도 그 생물학적 활성을 잃지 않고 안정하다. 이것은, 면역-10의 생물학적 활성이 활성화된 다당류에서 유래하는 것일 수 있다는 것을 추가로 나타낸다.
본 발명의 방법에 의해 분리된 면역-10은, 종래의 공지된 방법에 의해 분리된 알로에 다당류보다 훨씬 더 안정하다. 실시예 5 및 6 (도 5 ~ 8)은 다당류의 가 공방법과 그 안정성 사이의 관계를 나타낸다.
본 발명은 또한 면역 촉진제, 면역 조절제 및 상처 치유제로서의 면역-10의 용도를 포함한다.
면역조절 활성.
면역-10은, UVB 에 의해 억제된 면역반응(접촉 과민성:CH)을 복원시켜 주고, 또한 케라티노사이트(keratinocyte)(사람 표피모양암종 세포, KB 세포)로부터의 UVB-유도된 종양 괴사 인자-α(TNF-α) 방출을 억제한다.
실시예 7 에 개략적으로 기재된 바와 같이, UVB에 의해 억제된 피부 면역 기능을 반전시키는 면역-10의 능력을 측정하기 위해 국소 억제(suppression) 모델을 사용하였으며, 본원에서는 이러한 면역-10의 능력을 면역-10의 복원 활성(restorative activity)으로 언급했다. (본원에 참고로서 삽입된, 스트릭랜드(1994) J.Invest.Dermatol. 102:197-204 및 빈섹(Vincek) 외 다수 (1994) Cancer Research 53:728 참조). 국소 억제 모델에 있어서 C3H/HeN 마우스가 저용량의 UVB 조사에 노출되면, 조사된 위치에 도포된 합텐(hapten)에 대한 접촉 과민성(CH) 반응의 유도가 억제된다. 간단히 말해서, 마우스의 복부의 털을 제거하고 2000 J/m2으로 UVB 조사에 노출시킨 후 공지의 비이클(vehicle)인 아쿠아퍼(Aquaphor)내에 있는 면역-10 (0.25mg/mL)을 조사된 부위에 도포하였다. 3일 후에, 조사된 부위에 2,4-디니트로벤젠(DNFB)(0.3%, 50㎕)을 도포함으로써 마우스를 감작(sensitize)시켰다. 6일 후에, 마우스의 귀의 두께를 측정한 후 DNFB(0.2%, 5㎕)를 마우스 귀의 양면에 도포하여 마우스를 챌린지(challenge)시켰다. 24시간 후에 마우스 귀의 두께를 다시 측정하였다. 그 결과가 도 8에 도시되었다.
수행한 실험의 대부분에서, UVB 노출은, 접촉 과민성(CH) 반응을 80~100% 억제시켰다. 도 8를 참조해 보면, 이 군이 음성(억제) 대조군(0%의 접촉 과민성 반응)으로 사용되었다. 마우스의 양성 대조군은 UVB의 조사를 받지 않았고 면역-10으로 처리되지도 않았으나(비이클만 존재), 감작되었고 챌린지되었다(100%의 접촉 과민성 반응). 마우스의 비이클(블랭크(blank)) 대조군은 UVB의 조사를 받지 않았고 면역-10으로 처리되지도 않았으며(비이클만 존재) 감작되지도 않았으나, 챌린지되었다. 이 군은, 챌린지 화학물질 자극에 의하여 유발된 마우스 귀의 순수(net) 팽윤(swelling)을 빼는 데 사용되었다. 면역-10으로 처리된 마우스 군은, 비이클만 사용하는 대신에 비이클내의 면역-10으로 마우스를 처리했다는 점을 제외하고는, 억제 대조군과 동일한 방법으로 처리되었다. 면역-10에 의한 회복(recovery) 백분율은 하기의 식을 사용하여 계산했다.
회복% (% Recovery) = (A-B)/(C-B) X 100
여기서,
A = 면역-10으로 처리된 군의 귀의 순수(net) 팽윤 - 블랭크군의 귀의 순수 팽윤;
B = 억제군의 귀의 순수 팽윤 - 블랭크군의 귀의 순수 팽윤; 및
C = 양성군의 귀의 순수 팽윤 - 블랭크군의 귀의 순수 팽윤.
회복% 가 높을수록 면역-10의 활성이 높다. 도 8에서 볼 수 있듯이, 면역-10 의 활성은 30~80% 사이이며, 평균은 약 60% 이다. 면역조절 활성은, 면역-10이 4℃에서 용액내에 저장될 때는 3개월동안, 또는 실온에서 고체 상태로 저장될 때는 일년동안 안정하다.
UVB-유도된 종양 괴사 인자-α(TNF-α) 방출이, 표피내의 국소적인 면역 억제의 매개(mediation)와 관련된다는 것이 보고되어 왔다. 면역-10에 의한, UVB -유도된 종양 괴사 인자-α(TNF-α) 방출의 억제를 측정하기 위하여 시험관내(in vitro) 모델이 개발되었다. 이 방법은 실시예 8에 기재되어 있다. 사람 표피모양암종(epidermoid carcinoma) 세포주(KB 세포)가 사용되었다(정상 세포는 ELISA에 의해 측정될 만큼의 충분한 TNF-α를 생산하지 않는다). 그 결과가 도 9에 제시되었다. 도 9에서 X축은 면역-10의 용량(mg/ml,세포배지에서의 최종 농도)을 나타내고, Y축은 면역-10에 의한 억제 백분율을 나타낸다. 면역-10에 의한 억제%은 하기 식을 사용하여 계산되었다.
억제% (%Inhibition) = 1 - (A-B)/(C-B) X 100
A = UVB로 조사되고 면역-10으로 처리된 세포들로부터의 배지내 TNF-α의 양;
B = UVB로 조사되지 않은 세포들로부터의 배지내 TNF-α의 양; 및
C = UVB로 조사되었지만 면역-10으로 처리되지 않은 세포들로부터의 배지내 TNF-α의 양.
도 9에서 볼 수 있듯이, 면역-10은, KB 세포로부터의 UVB-유도된 종양 괴사 인자-α(TNF-α) 방출을 용량-의존적(dose-dependent)으로 억제하는 것을 나타냈 다. 1 mg/ml의 농도에서 면역-10은 거의 100%에 가깝게 상기 방출을 억제했다.
면역 촉진 활성.
면역-10은 종양 괴사 인자-α(TNF-α) 방출을 촉진함으로써 마크로파지(macrophage)를 활성화시킨다.
악성 종양에 대한 숙주의 방어(defense)는 몇개의 상이한 메카니즘으로 이루어지는데, 면역 방어의 실패 또는 손상은 악성 질병의 발생 또는 진전을 초래할 수 있다. 마크로파지는 항원-처리 세포이고, 세포독성 작용과 식세포(phagocytic) 작용이 둘다 있음이 밝혀졌다. 마크로파지가 활성화되었을 때 상기 기능들 각각은 유의성있게(significantly) 증가된다. 이 세포 집단의 선별적 촉진은, 치료적 용도의 개발에 기여한다는 점에서 중요할 수 있다. 활성화된 마크로파지는 신체의 상처 치유 능력에 있어서도 매우 중요하다. 마크로파지에 의해서 방출되는 사이토카인(cytokine)중 하나인 종양 괴사 인자-α(TNF-α)는 방어 시스템에서의 신호전달을 매개(mediate)하는 데에 중요한 역할을 한다. 실시예 9는 면역-10에 의해 촉진된 마크로파지의 활성화를 측정하는 데에 사용되는 방법을 기재하고 있다. 그 결과가 도 10에 제시되어 있다. 도 10에서 보여지듯이, 마우스 복막의 마크로파지로부터의 종양 괴사 인자-α(TNF-α)의 방출이 면역-10에 의해 용량-의존적으로 촉진된다는 것이 검출되었다. 1ml당 0.5㎍의 면역-10의 농도에서, 면역-10에 의해 촉진된 마크로파지는, 촉진되지 않은 세포보다 종양 괴사 인자-α(TNF-α)를 500배 이상 더 방출했다. 도 10 에서 또한 볼 수 있듯이, 동일한 실험조건하에서, 천연 알로에 겔은 마크로파지로부터 종양 괴사 인자-α(TNF-α)의 방출을 유도하지 않았다. 이 결과는, 면역-10이 면역계의 비특이적(non-specific) 촉진제로서 그리고 상처 치유제로서 사용될 수 있음을 나타낸다.
상처치유활성.
면역-10은 섬유아세포(어린 햄스터의 신장 세포, BHK-21 세포)의 증식을 자극한다.
실시예 10은 면역-10에 의한 세포 증식을 측정하기 위해 사용된 방법을 기재하고 있다. 촉진된 세포 증식을 측정하기 위해 MTT 방법이 사용되었다. 그 결과가 도 11에 제시되어 있다. 도 11에서 볼 수 있듯이, 면역-10이 BHK-21 세포의 성장을용량-의존적으로 촉진한다.
실시예
다음의 실시예들은 예시만을 위한 것이며, 본 발명의 범위를 한정하는 것이 아니다.
실시예
1. 면역-10의 분리 및 정제
면역-10은 도 1에 대략 제시된 바와 같이 분리되고 정제되었다. 간단히 말해서, 신선한 Aloe barbadensis 겔 추출물을, 탄수화물의 한정된 가수분해에 적합한 시간동안 및 온도에서 한정되게 효소 소화(digest)시켰다. 이것은, 효소로서 셀룰라아제(cellulase)를 사용하여, 통상적으로 25℃에서 2시간이다. 활성화된 알로에 겔을, 활성탄 및 여과를 사용하여 부분적으로 정제하였다(I-10). 그 후, 활성화된 다당류는 투석, 에탄올 침전 및 크기 배제 크로마토그래피에 의해서 더 정제되었 다.
한정 효소 소화(digestion)
신선한 겔 필릿(fillets)(텍사스주 할링겐에 소재하는 Aloecorp에 의해 제공됨)으로부터 생산된 알로에 겔 즙(AGJ)(10 L)을 열 교환기로 25℃까지 가열했다. 이 열교환기는 마린 프로펠러 블레이드(marine propeller blade)(A100)가 장착된 기계적 교반기로 부드럽게(gently) 혼합되면서 1/4" 316 스테인레스 강 코일을 통해 순환하는 60℃의 물로 이루어졌다. pH 6의 50mM의 구연산염(citrate) 수용액 10mL내에 있는 116mg의 셀룰라아제 4000(밸리 리서치 회사)의 용액을 첨가하고, 혼합물을 2시간동안 부드럽게 교반했다.
효소 불활성화
2 시간 후에, 최소 30분동안 이 반응 혼합물을 약 90℃ 로 가열했다. 그 다음 이 반응 혼합물을 얼음과 물이 혼합된 배쓰(ice-water bath)에 침지(immerse)시켜 이 물질을 실온으로 냉각시켰다.
탈색 및 여과
효소를 불활성화시키는 동안 생긴 적색을 제거하기 위해 샤르콜(charcoal)을 사용했다. 상기 물질을 두개의 5.0 L 뱃치(batch)로 나누었다. 각각의 5.0 L 뱃치에 거친(coarse) 샤르콜(charcoal)(Norit 으로부터 구입한 Darco 20 X 40) 100.0g을 첨가하고 이 혼합물을 실온에서 1 시간동안 부드럽게 교반시켰다. 그 후에, 50.0 g의 셀라이트(celite) 545(알드리히 케미컬 회사)를 첨가한 다음 이 슬러 리(slurry)를 추가로 10분동안 교반시켰다.
그 후, 상기 슬러리(slurry)를 30㎛ 필터 종이(왓트만(Whatman) 등급 113)가 장착된 압력 필터로 펌프시켜 고체를 제거했다. 이 여과액(filtrate)은 필터를 통과한 소량의 미세한 샤르콜 입자를 함유했다. 상기 물질은 포개놓은(superimposed) 2개의 필터상에서 여과되었을 때 정화되며, 100g의 셀라이트(celite) 545로 코팅된 0.7 ㎛ 필터 종이(왓트만 GF/F)의 위에 1.0 ㎛ 기공 크기의 필터 종이(왓트만 #1)가 포개져 있다. 여과액(filtrate)은 탈색되고 미세한 샤르콜 입자가 없는 상태로 되었다. 그 활성화된 다당류는 투석, 에탄올 침전 및 크기 배제 크로마토그래피에 의해 더 정제되었다. 여과 데이터가 표 1과 표 2에 요약되어 있다.
| 매개변수(parameter) | 수치(value) |
| 슬러리(slurry) 부피 | 5 L |
| 필터 종이 | 왓트만 #113 |
| 기공크기 | 30 ㎛ |
| 여과 보조제 | 없음 |
| 여과 면적 | 113 cm2 |
| 최대 압력 | <1 psi |
| 평균 여과 속도 | 7.0 ml/min/cm2 |
| 액체 회수 | 정량적 |
| 물질 외관(material appearance) | 미세한 샤르콜 입자 함유함 |
| 매개변수 | 수치 |
| 슬러리 부피 | 5 L |
| 필터 종이 (조합) | 왓트만 GF/F의 위에 왓트만 #1 |
| 기공크기 | 0.7㎛위에 1.0㎛ |
| 여과 보조제 | 100g의 셀라이트 545 |
| 여과 면적 | 113 cm2 |
| 최대 압력 | 2 psi |
| 평균여과속도 | 0.74 ml/min/cm2 |
| 액체 회수 | 정량적 |
| 물질 외관 | 투명 |
동결건조(
lyophilization
)
여과 후에 두 뱃치(batch)가 혼합되고 상기 물질이 동결건조 트레이(tray)에 이송된 후 20L 비르티스(VirTis) 동결건조기(Freeze Dryer)내에서 동결 및 동결건조(lyophilize)되어 57.14g의 면역-10을 생산하는데, 이것은 알로에 겔 즙(AGJ) 1리터당 5.71g의 면역-10 과 등가(equivalent)이다.
실시예 2. 중공(Hollow)-섬유 카트리지(Cartridge)를 사용한 약제 등급의 면역-10의 제조
동결건조된 알로에 겔 10g을, 2 L의 비이커내에 있는 1.8 L의 증류수에 용해시켰다. 그 슬러리는 4℃에서 하룻밤동안 교반되어 균질한(homogenous) 혼합물을 생산했다. 상기 혼합물을 필터 종이(왓트만 #3)를 통해 여과하여 미립자들(particulates)을 제거한 다음, 그 여과액의 부피를 2L가 되도록 조정했다. 상기 혼합물의 온도를 실온으로 하고, pH 6의 50 mM의 구연산염(citrate) 수용액 5 mL내에 있는 4.63 mg의 셀룰라아제 4000(밸리 리서치 회사)의 용액을 첨가했다. 그 후, 상기 여과액을 유입구 압력이 10 내지 15psi사이인 중공-섬유 카트리지(UFP-5-E-6, 분자량 컷오프(cutoff) : 5000 Da, A/G 테크놀로지 회사)를 통해 펌프시켰다. 5000 Da 미만의 분자량을 가진 투과물(permeate)을 별도의 2 L의 비이커에 모았다. 5000 Da 보다 큰 분자량을 갖는 농축물(concentrate)을, 출발 여과액과 동일한 비이커에 모았다. 이 혼합물을 연속적으로 교반시키고, 출발 여과액의 부피가 1 L로 감소되었을 때 증류수(1 L)를 첨가하여 이 부피가 다시 2 L가 되게 했다. 이 과정을 다섯 번 반복했다. 투과물(permeate)의 세개의 2 L 분획물 전체를 모았다. 최종 농축물(concentrate)은 보유된(retained) 분획으로서 모아졌다. 각각의 2 L 투과물(permeate) 분획을 모으는데 평균적으로 대략 2.5시간이 걸렸다. 이 분획들을 동결건조 트랩(trap)으로 이송시킨 후 20 L 비르티스(VirTis) 동결건조기내에서 동결 및 동결건조(lyophilize)시켰다. 투과물(permeate) 분획 Ⅰ,Ⅱ,Ⅲ 및 상기 보유된 분획의 수율(yield)은 각각 4.88g, 1.77g, 0.56g 및 0.37g이었다. 상기 보유된 분획은, UVB에 의해 억제된 접촉 과민성(CH)을 복원시키는 데 가장 높은 활성을 가졌다. 투과물의 분획 Ⅲ는 UVB에 의해 억제된 접촉 과민성(CH)을 복원시키는 데 중간 정도의 활성을 가졌다. 투과물의 분획 Ⅰ및 Ⅱ은 활성이 없었다.
실시예
3. 약제 등급의 면역-10의 제조 방법
실시예 1에 기재된 방법으로 제조된 면역-10 (50g)을, 증류수(diH2O)에 용해시켜 최종 부피가 200ml가 되게 했다. 그 후, 에탄올(66.7ml,25%의 최종 농도)을 이 용액에 첨가했다. 에탄올의 첨가는 교반되면서 서서히 행해졌다. 그 후 이 용액을 추가로 30분 동안 교반시키는데, 이 동안 침전물이 형성되었다. 이 혼합물을 10분동안 2500rpm(Jouan CR412)으로 원심분리시키고, 이 침전물을 25%의 에탄올로 1회 세정하고 원심분리시킨 후 diH2O에 다시 용해시켰다. 그 결과 생성된 용액을 건조상태로 동결건조시켰다(ppt/25%). 상기 상청액(supernatant)에 추가의 133.3ml의 에탄올(25%~50%)을 첨가하고, 전술한 바와 같이, 이 용액을 다시 30분동안 교반시킨 다음 침전물을 모으고, 50%의 에탄올로 세정한 후 동결건조시켰다(ppt/25%~50%). 이 과정을, 50~75%의 에탄올(ppt/50%~75%) 및 75~80%의 에탄올(ppt/75%~80%)로 재결정시키면서 2회 더(two more times) 반복했다. ppt/25%, ppt/25%~50%, ppt/50%~75% 및 ppt/75%~80%에 대하여 침전물의 고체 회수율은 각각 0.3%, 20.5%, 10.3% 및 1.5%이었다. ppt/50%~75%의 생성물은 세파덱스(Sephadex) G-100 칼럼(2.5 x 68cm)상에서 더 분별(fractionate)되었다. 다당류 피크(좌측 피크, 도 3)의 분획을 혼합(combine)시키고 동결건조시켜, 약제 등급의 면역-10을 생산했다. ppt/50%~75%로부터 약제 등급의 면역-10의 회수율은 15.8%이었다.
실시예
4. 알로에 베라(Vera) 겔(
AJG
) 다당류의 시간-의존적 분해
신선한 알로에 베라 겔 추출물을 실온에서 3분, 10분, 30분, 60분, 120분, 24시간 및 48시간동안 셀룰라아제(겔 추출물 1리터당 11.57mg의 셀룰라아제)로 처리했다. 처리의 끝 단계에서, 겔 추출물을 워터 배쓰(water bath)내에서 30분동안 95℃로 가열시킨 후 10분동안 2500rpm으로 원심분리시켰다. 상청액을 건조상태로 동결건조시켰다. 처리된 겔 추출물내의 다당류의 분자량 분포를, 세파덱스(Sephadex) G-75 칼럼(2.5 x 68 cm, 177 ~ 179 mg의 샘플이 이 칼럼에 적용되었음) 상에서 크기 배제 크로마토그래피에 의해 분석했다. 75,000 Da 이상의 분자량을 가진 다당류는 공극 용적(void volume)에서 용출한 반면 단당류와 일부 올리고당류(oligosaccharide)는 칼럼 용적(column volume)에서 용출했다(도 4 참조). 그 결과의 생성물의 생물학적 활성에 기초하여, 바람직한 가수분해 반응 시간은 120분으로 측정되었다. 도 4에서 볼 수 있듯이, 120분동안 셀룰라아제로 처리하면, 쇼울더(shoulder)가 없이 날카로운(sharp) 다당류 피크가 만들어졌다(). 24시간() 또는 48시간()동안 셀룰라아제로 처리하면, 다당류 피크의 흡수도(absorbance)는 상당히 감소한 반면 단당류 피크와 올리고당류 피크의 흡수도는 증가하였다. 3분(◇), 10분(○) 및 30분(△)동안 처리하여 수득한 생성물은, 쇼울더가 있는 다당류 피크를 만들었다.
실시예
5. 상이한 알로에
제제들내의
알로에 다당류의 안정성
신선한 알로에 겔 추출물(표준 정제방법, 즉 투석과 에탄올 침전을 사용하여 정제됨), 동결건조된 알로에 겔 및 동결건조된 알로에 전체(whole) 잎 내의 다당류의 안정성을, 세파로오스 CL-4B 칼럼상에서의 크기 배제 크로마토그래피에 의해 연구했다(도 5참조). 도 5에서 볼 수 있듯이, 신선한 알로에 겔 추출물로부터 분리된 알로에 다당류는 ~2백만 Da의 분자량을 가진다. 동결건조된 알로에 전체 잎내의 다당류의 분자량은 신선한 알로에 겔 추출물로부터 분리된 다당류의 분자량보다 낮고, 동결건조된 알로에 겔내의 다당류는 ~500,000 Da의 분자량을 가진다. 이 결과는 알로에 다당류의 안정성과 다당류의 가공방법 사이의 관계를 나타내준다.
실시예
6. 면역-10 다당류의 안정성
면역-10은 다당류 외에 몇몇의 염들과 기타 작은 분자들을 함유하고 있다. 증류수(diH2O)내에서 면역-10의 pH는 약 4.3이다. 면역-10 다당류의 안정성을 연구하기 위하여, pH 4.3 또는 pH 7.8의 정제된 천연(native) 알로에 다당류 및 면역-10의 용액을 실온에서 3개월동안 방치해 두었다. 최종 농도가 0.02%인 나트륨 아자이드(sodium azide)를 면역-10 또는 다당류 용액에 첨가하여 미생물의 성장을 억제시켰다. 이 샘플들에서 다당류의 분해(degradation)를 세파덱스(Sephadex) G-100 칼럼상에서 분석하였다. 도 6은, 490nm에서의 면역-10의 다당류 흡수도(absorbance)가 pH 4.3과 pH 7.8 둘다에서 매우 유사했다는 것을 보여주는 크로마토그램을 도시하고 있다. 다당류 피크가 pH 4.3에서 오른쪽으로 약간 이동(shift)하긴 했지만, 이것은 출발물질과 비교했을 때 양 pH 조건하에서 여전히 매우 안정했다. 동일한 조건하에서, 정제된 천연 다당류는 pH 7.8에서 부분적으로 분해되었다(도 7). 다당류 피크의 약간의 이동은, 세파덱스 G-100 칼럼의 리팩킹(repacking) 때문일 수도 있다.
실시예
7. 면역-10에 의한,
UVB
-억제된 접촉 과민성의 복원의 측정
특이적 병원균이 없는 암컷 C3H/HeN 마우스를 할란 스프라그 다울리(Harlan Sprague Dawley)로부터 얻고, 이를 실험 동물 관리(care)의 내쇼날 리서치 카운슬(National Research Council)의 지침에 따른 병원균-부재의 시설내에 놓아 두었다. 각각의 실험은, 9~10주 된 연령이 맞추어진 마우스를 가지고 수행되었다.
마우스의 복부의 털을 전기 가위(clipper)로 제거하였다. 그 후 알루미늄 호일로 귀를 덮은 마우스를, 일렬의 4개의 여과되지 않은(unfiltered) FS40 태양등(sunlamp)(National Biological Corp.)에 2000J/m2의 용량으로 노출시켰다. 이들 태양등으로부터 방출(emit)되는 에너지의 약 65%가 UVB의 범위(280-320)내에 있으며 피크 방출(emission)은 313 nm 이었다. UVB에 노출시킨 직후에, 아쿠아퍼(Aquaphor)(비이클) 단독을, 또는 1:1 비율의 아쿠아퍼(Aquaphor)내 테스트 화합물을 마우스 복부의 피부에 도포하였다. UVB에 노출시키고 3일 후에, 0.3% 디니트로플루오로벤젠(DNFB) 50㎕을 마우스의 털을 깍아낸 복부 피부상에 도포하여 마우스를 감작(sensitize)시켰다. 감작시키고 6일 후에, 0.2% 디니트로플루오로벤젠(DNFB) 5㎕을 마우스의 각각의 귀의 귓등(dorsal)표면과 그 반대쪽의 전면(ventral surface) 둘다의 위에 도포하여 마우스를 챌린지(challenge)시켰다. 챌린지 직전에 및 24시간 후에, 엔지니어의 마이크로미터(engineers, micrometer)로 귀의 두께를 측정하였다. 챌린지되었지만 감작되지 않은 마우스(블랭크 군)에서 얻은 수치를 빼줌으로써, 귀의 고유(specific) 팽윤을 측정했다. 각각의 처리군은 5개의 마우스를 포함하고 있다. 2개의 추가의 대조군, 즉 양성 대조군과 억제 대조군이 각각의 실험에 포함되었다. 양성 대조군은 UVB의 조사를 받지 않고 어떤 처리도 되지 않았지만, 감작 및 챌린지되었다(100% 반응). 마우스의 억제 대조군은 UVB 조사를 받고 어떤 처리도 되지 않았지만, 감작 및 챌린지되었다(0% 반응). 그 결과가 도 8에 제시되어 있다.
실시예
8. 면역-10에 의한,
UVB
-유도된
TNF
-α방출의 억제의 측정
사람 표피모양암종(epidermoid carcinoma) 세포(KB)가 100mm의 접시당 2 x 106의 세포 비율로 플레이트(plate)되었다. 이 세포들이 합류점(confluence)에 도달한 후(약 2일 후)에, 이 세포들을 PBS로 3회 세정하고, 300 J/m2의 UVB 조사에 노출시켰다. 그후 이 세포들을 한번 더 PBS로 세정한 다음, 5ml의 DMEM/0.2% FBS내에서 면역-10과 함께 또는 면역-10이 없이 한시간동안 인큐베이트(incubate)시켰다. 이 세포들을 다시 한번 PBS로 세정한 후 성장배지내에서 하룻밤동안 인큐베이트시켰다. 다음 날 그 배지를 모으고 4 ℃에서 2500rpm으로 10분간 원심분리시켰다. 상청액으로 방출된 TNF-α를 ELISA에 의해 측정했다. 그 결과가 도 9에 제시되어 있다.
실시예
9. 면역-10에 의한
마크로파지
활성화의 촉진의 측정
마우스 복막에 거주하는 마크로파지를 ICR 마우스로부터 분리시킨 후, 웰(well)당 200,000 세포의 비율로 96-웰(well) 판(plate)에 플레이트시켰다. 2시간 동안 인큐베이트시킨 후에 세포들을 3회 세정하여 부착되지 않은 세포들을 제거하였다. 그 후 마크로파지는 면역-10과 함께 또는 면역-10이 없이 하룻밤동안 인큐베이트되었다. 배지로 방출된 TNF-α는 ELISA에 의해서 측정되었다. 리포다당류(Lipopolysaccharide:LPS)가 양성 대조군으로서 사용되었다. 그 결과가 도 10에 제시되었다.
실시예
10. 면역-10에 의한 세포증식 촉진의 측정(
MTT
)
어린 햄스터 신장 세포주(BHK 세포)가 웰당 5000세포의 비율로 96-웰 판에 플레이트되었다. 이 세포들은 면역-10이 없이 또는 면역-10과 함께 3일간 조직 배양 인큐베이터(incubator)내에서 인큐베이트되었다. 그 후 이 세포들은 4.5시간동안 1mg/ml의 MTT(3-(4,5-dimethylthiazol-2-yl)-2,3-diphenyltetrazolium bromide, Thiazolyl blue)와 함께 인큐베이트되었다. 0.01N의 HCl내의 10% SD 100㎕로 이 세포들을 추출한 다음, 570~630nm에서의 흡수도를 측정하였다. 섬유아세포 성장 인자(FGF)가 양성 대조군으로서 포함되었다. 그 결과가 도 11에 제시되었다.
이상 설명한 바와 같이, 본 발명의 알로에로부터 유래된 다당류를 포함하는 조성물에서는, 다당류의 활성화된 혼합물을 포함하고 면역 촉진제, 면역 조절제 및 상처 치유제로서 면역 조절 복합체는 종래 알콜 침전 체계(scheme)를 사용하여 분리된 벌크(bulk) 탄수화물보다 더 안정하며 더 높은 활성을 갖는 것이다.
Claims (5)
- 하기 (a)~(d)의 특징을 지니는, 알로에로부터 유래된 다당류를 포함하는 조성물(composition of matter):(a) 상기 조성물내 상기 다당류는 50 ~ 200 kDa 의 범위와 함께 70 ~ 80 kDa 의 평균 분자량을 가지며;(b) 상기 조성물내 상기 다당류는 D-갈락토오스(D-galactose)(5% 이하), D-글루코오스(D-glucose)(5% 이하) 및 D-만노오스(D-mannose)(90% 이하)를 포함하고;(c) 상기 조성물내 상기 다당류는 β-1,4 결합(linkage)을 갖는 단당류(monosaccharide)를 포함하고 있으며; 그리고(d) 상기 조성물내 상기 다당류는, 단당류당 1 이하의 아세틸기를 지녀서 고도로 아세틸화되어 있고, 여기서 상기 아세틸기는 단당류 유니트의 2, 3 또는 6 위치상에 존재한다.
- 제1항에 있어서, 상기 다당류가 또한 미량(trace amount)의 자일로오스(xylose) 및 아라비노오스(arabinose)를 포함하는 조성물.
- 제1항에 있어서, 상기 다당류가 1 대 9.6 ±2.2의 비율로 D-갈락토오스(D-galactose) 및 D-만노오스(D-mannose)를 포함하는 조성물.
- 제1항의 조성물을 포함하는 면역 촉진, 면역 조절 또는 상처 치유용 약제학적 조성물.
- 제1항의 조성물을 포함하는 면역 결핍 또는 면역-억제 질환 치료용 약제학적 조성물.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US6168197P | 1997-10-10 | 1997-10-10 | |
| US60/061,681 | 1997-10-10 | ||
| US9827198P | 1998-08-28 | 1998-08-28 | |
| US60/098,271 | 1998-08-28 | ||
| KR1020007003894A KR100678238B1 (ko) | 1997-10-10 | 1998-10-09 | 알로에로부터 면역조절성 다당류를 제조하는 방법 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020007003894A Division KR100678238B1 (ko) | 1997-10-10 | 1998-10-09 | 알로에로부터 면역조절성 다당류를 제조하는 방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20060103285A KR20060103285A (ko) | 2006-09-28 |
| KR100729887B1 true KR100729887B1 (ko) | 2007-06-18 |
Family
ID=26741367
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020067017809A KR100729887B1 (ko) | 1997-10-10 | 1998-10-09 | 알로에로부터 유래된 다당류를 포함하는 조성물 |
| KR1020007003894A KR100678238B1 (ko) | 1997-10-10 | 1998-10-09 | 알로에로부터 면역조절성 다당류를 제조하는 방법 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020007003894A KR100678238B1 (ko) | 1997-10-10 | 1998-10-09 | 알로에로부터 면역조절성 다당류를 제조하는 방법 |
Country Status (5)
| Country | Link |
|---|---|
| US (3) | US6133440A (ko) |
| EP (1) | EP1036187A4 (ko) |
| JP (1) | JP4542262B2 (ko) |
| KR (2) | KR100729887B1 (ko) |
| WO (1) | WO1999019505A1 (ko) |
Families Citing this family (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20030096378A1 (en) * | 1997-10-10 | 2003-05-22 | Univera Pharmaceuticals, Inc. | Process for the preparation of immunomodulatory polysaccharides from aloe |
| US7022683B1 (en) | 1998-05-13 | 2006-04-04 | Carrington Laboratories, Inc. | Pharmacological compositions comprising pectins having high molecular weights and low degrees of methoxylation |
| US7196072B2 (en) * | 2000-07-10 | 2007-03-27 | University Of Mississippi | High molecular weight polysaccharide fraction from Aloe vera with immunostimulatory activity |
| US6777000B2 (en) | 2001-02-28 | 2004-08-17 | Carrington Laboratories, Inc. | In-situ gel formation of pectin |
| EP1323738A1 (en) * | 2001-12-27 | 2003-07-02 | 2QR Research BV | Negatively charged polysaccharide derivable form Aloe Vera |
| US20050004211A1 (en) * | 2003-06-30 | 2005-01-06 | Kaohsiung Medical University | Pharmaceutical compositions comprising aryl-substituted acyclic enediyne compounds |
| KR100743852B1 (ko) | 2004-03-31 | 2007-08-02 | 모리나가 뉴교 가부시키가이샤 | 4-메틸에르고스트-7-엔-3-올 골격을 갖는 글리코사이드 및고혈당 개선제 |
| WO2005094838A1 (ja) | 2004-03-31 | 2005-10-13 | Morinaga Milk Industry Co., Ltd. | 高血糖改善のための医薬及び飲食品 |
| US7507424B2 (en) * | 2004-04-26 | 2009-03-24 | Mmi Corporation | Natural immunostimulant compositions, methods for obtaining the same and pharmaceutical formulations thereof |
| US7410661B2 (en) * | 2004-08-02 | 2008-08-12 | Weston Haskell | Enhanced wound healing method, product and composition |
| US7175860B2 (en) * | 2004-08-02 | 2007-02-13 | Haskell Pharmaceuticals, Inc. | Enhanced wound healing method and composition |
| CA2542780C (en) | 2004-09-29 | 2010-04-27 | Morinaga Milk Industry Co., Ltd. | Drug and food or drink for improving hyperglycemia |
| US20060084629A1 (en) * | 2004-10-15 | 2006-04-20 | Alvin Needleman | Immune system activating formula composed of selected long chain polysaccharides from natural sources |
| CN101098702B (zh) | 2005-05-17 | 2010-12-29 | 森永乳业株式会社 | 改善胰腺功能的药物和食品或饮料 |
| US7531520B2 (en) | 2005-05-17 | 2009-05-12 | Morinaga Milk Industry Co., Ltd. | Drug and food or drink for improving pancreatic functions |
| KR20070063574A (ko) | 2005-05-17 | 2007-06-19 | 모리나가 뉴교 가부시키가이샤 | 췌장 기능 개선을 위한 의약 또는 음식품 |
| US20070036840A1 (en) * | 2005-07-27 | 2007-02-15 | Jose Antonio Matji Tuduri | Phosphorylated glucomannan polysaccharides containing 1-6 and 1-2 linkages increase weight gain in swine |
| JP4954523B2 (ja) * | 2005-09-26 | 2012-06-20 | 長谷川香料株式会社 | 高濃度のs−アルケニル(またはアルキル)システインスルフォキサイド類を含有する抽出物の製造方法 |
| US8158152B2 (en) * | 2005-11-18 | 2012-04-17 | Scidose Llc | Lyophilization process and products obtained thereby |
| CN101720226B (zh) | 2007-05-11 | 2013-01-30 | 芦荟研究实验室公司 | 用于皮肤增强的芦荟制剂 |
| CN101980695B (zh) * | 2008-05-16 | 2013-05-22 | 株式会社日冷生物科学 | 由兰科植物得到的提取物、生产所述提取物的方法和包含所述提取物的皮肤外用剂 |
| CN102186487B (zh) * | 2008-10-14 | 2013-05-15 | 奈瑞姆生物技术公司 | 提取强心苷的方法和组合物 |
| US7833829B2 (en) * | 2008-10-28 | 2010-11-16 | Honeywell International Inc. | MEMS devices and methods of assembling micro electromechanical systems (MEMS) |
| JP4761584B2 (ja) * | 2008-11-07 | 2011-08-31 | 長谷川香料株式会社 | 粘性物質の除去されたアロエ葉肉加工品の製造方法 |
| US8604187B2 (en) | 2010-01-14 | 2013-12-10 | North Texas Medical Associates | Compositions and methods of aloe polysaccharides |
| RU2587784C2 (ru) * | 2011-01-06 | 2016-06-20 | Биспоук Баиосаиенс, ЛЛСи | Композиции и способы полисахаридов алоэ |
| KR101502219B1 (ko) * | 2013-07-03 | 2015-03-13 | 제주알로에영농조합법인 | 알로에 효소 추출물 또는 이의 분획물을 함유하는 항산화 조성물 |
| MX2016011427A (es) * | 2014-03-20 | 2016-12-02 | Morinaga Milk Industry Co Ltd | Metodo para fabricar extracto de aloe, y extracto de aloe. |
| EP3131529B1 (en) | 2014-04-17 | 2018-01-24 | Unilever N.V. | Aloe vera extract for personal care compositions |
| CN106456524B (zh) * | 2014-04-17 | 2019-12-10 | 荷兰联合利华有限公司 | 个人护理组合物 |
| KR101772894B1 (ko) * | 2015-07-14 | 2017-08-31 | 코스맥스 주식회사 | 스팀 처리를 이용한 알로에 다당체의 제조방법 |
| JP6129947B2 (ja) * | 2015-12-28 | 2017-05-17 | ビスポーク バイオサイエンス,エルエルシー | アロエ多糖体の組成物及び方法 |
| US10076552B2 (en) | 2016-08-09 | 2018-09-18 | DATT MEDIPRODUCTS LIMITED and DATT LIFE SCIENCE PVT. LTD. | Multifunctional formulation comprised of natural ingredients and method of preparation/manufacturing thereof |
| CN112533614A (zh) | 2018-03-28 | 2021-03-19 | 美国康宝莱国际公司 | 多糖的乙酰化 |
| WO2022250313A1 (ko) * | 2021-05-27 | 2022-12-01 | 주식회사 유니베라 | 알로에 베라 꽃 추출물, 또는 알로에 베라 꽃 추출물 및 알로에 베라 다당체를 유효성분으로 함유하는 피부 보습, 재생 촉진 및 상처 치료용 조성물 |
| KR102517668B1 (ko) * | 2022-10-25 | 2023-04-05 | (주)바이텍 | 효소처리 알로에 베라를 포함하는 유산균 동결건조 보호용 조성물 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4735935A (en) * | 1985-12-17 | 1988-04-05 | Carrington Laboratories, Inc. | Process for preparation of aloe products products, produced thereby and compositions thereof |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3892853A (en) * | 1967-05-22 | 1975-07-01 | Aloe 99 & 0 Inc | Stabilized aloe vera gel and preparation of same |
| US3470109A (en) * | 1968-01-31 | 1969-09-30 | Aloe Creme Lab Inc | Method of making reconstitutable aloe gel in crystalline form |
| US4178372A (en) * | 1978-03-06 | 1979-12-11 | Coats Billy C | Hypoallergenic stabilized aloe vera gel |
| US5443830A (en) * | 1982-05-07 | 1995-08-22 | Carrington Laboratories, Inc. | Drink containing mucilaginous polysaccharides and its preparation |
| US4917890A (en) * | 1985-06-28 | 1990-04-17 | Carrington Laboratories, Inc. | Processes for preparation of aloe products, products produced thereby and compositions thereof |
| US5118673A (en) * | 1982-05-07 | 1992-06-02 | Carrington Laboratories, Inc. | Uses of aloe products |
| US5106616A (en) * | 1988-01-14 | 1992-04-21 | Carrington Laboratories, Inc. | Administration of acemannan |
| US5468737A (en) * | 1982-05-07 | 1995-11-21 | Carrington Laboratories, Inc. | Wound healing accelerated by systemic administration of polysaccharide from aloe |
| US4851224A (en) * | 1986-06-05 | 1989-07-25 | Carrington Laboratories, Inc. | Process for preparation of aloe products |
| US5308838A (en) * | 1982-05-07 | 1994-05-03 | Carrington Laboratories, Inc. | Uses of aloe products |
| US4966892A (en) * | 1982-05-07 | 1990-10-30 | Carrington Laboratories, Inc. | Processes for preparation of aloe products products produced thereby and compositions thereof |
| US4555987A (en) * | 1983-07-22 | 1985-12-03 | Tumlinson Larry N | Method and apparatus for extraction of aloe vera gel |
| US4959214A (en) * | 1985-06-28 | 1990-09-25 | Carrington Laboratories Inc. | Processes for preparation of aloe products products produced thereby and compositions thereof |
| US4957907A (en) * | 1985-06-28 | 1990-09-18 | Carrington Laboratories Inc. | Process for preparation of aloe products |
| JPS62263193A (ja) * | 1986-05-09 | 1987-11-16 | Ichimaru Pharcos Co Ltd | アロエ由来水溶性抽出物 |
| US5562906A (en) * | 1989-09-12 | 1996-10-08 | Terry; James M. | Method for the treatment of vascular disorders |
| CA2112123A1 (en) * | 1991-06-24 | 1993-01-07 | Bill H. Mcanalley | Wound cleanser |
| US5356811A (en) * | 1992-04-21 | 1994-10-18 | Coats Billy C | Method of processing stabilized aloe vera gel obtained from the whole aloe vera leaf |
| US5512488A (en) * | 1994-05-05 | 1996-04-30 | Carrington Laboratories, Inc. | Colorimetric assay for bioactive polysaccharide |
| US5824659A (en) * | 1996-09-04 | 1998-10-20 | Board Of Regents, The University Of Texas System | Cytoprotective oligosaccharide from Aloe preventing damage to the skin immune system by UV radiation |
-
1998
- 1998-10-09 JP JP2000516056A patent/JP4542262B2/ja not_active Expired - Fee Related
- 1998-10-09 KR KR1020067017809A patent/KR100729887B1/ko not_active IP Right Cessation
- 1998-10-09 US US09/169,449 patent/US6133440A/en not_active Expired - Lifetime
- 1998-10-09 KR KR1020007003894A patent/KR100678238B1/ko not_active IP Right Cessation
- 1998-10-09 EP EP98953354A patent/EP1036187A4/en not_active Withdrawn
- 1998-10-09 WO PCT/US1998/021361 patent/WO1999019505A1/en not_active Application Discontinuation
-
1999
- 1999-04-21 US US09/295,648 patent/US6271214B1/en not_active Expired - Lifetime
- 1999-04-21 US US09/295,907 patent/US6436679B1/en not_active Expired - Lifetime
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4735935A (en) * | 1985-12-17 | 1988-04-05 | Carrington Laboratories, Inc. | Process for preparation of aloe products products, produced thereby and compositions thereof |
Also Published As
| Publication number | Publication date |
|---|---|
| US6436679B1 (en) | 2002-08-20 |
| KR20060103285A (ko) | 2006-09-28 |
| WO1999019505A1 (en) | 1999-04-22 |
| US6271214B1 (en) | 2001-08-07 |
| EP1036187A1 (en) | 2000-09-20 |
| JP2001520019A (ja) | 2001-10-30 |
| US6133440A (en) | 2000-10-17 |
| EP1036187A4 (en) | 2002-03-27 |
| KR20010015736A (ko) | 2001-02-26 |
| JP4542262B2 (ja) | 2010-09-08 |
| KR100678238B1 (ko) | 2007-02-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100729887B1 (ko) | 알로에로부터 유래된 다당류를 포함하는 조성물 | |
| EP0328775B1 (en) | Processes for preparation of aloe products, products produced thereby and compositions thereof | |
| EP0356484B1 (en) | Process for preparation of aloe products | |
| EP0212595B1 (de) | Calcium- und Magnesiumkomplexe von Phytohaemagglutinin-polyheteroglykanen, ihre Herstellung und pharmazeutische Zubereitungen | |
| US20030096378A1 (en) | Process for the preparation of immunomodulatory polysaccharides from aloe | |
| KR20070002409A (ko) | 문형 추출물을 유효성분으로 함유하는 화장료 조성물 | |
| KR20170124976A (ko) | 피부보습 및 재생 촉진활성을 갖는 녹차유래의 다당체를 함유하는 화장료 조성물 및 그 제조방법 | |
| DE2919132A1 (de) | Substanz ks-2-b, verfahren zu deren herstellung und diese substanz enthaltende mittel | |
| US4762825A (en) | Polysaccharide RON substance | |
| JPH0539305A (ja) | アストラガルス・メンブラナセウスから抽出した免疫 変調性多糖類及びこれらを含有する薬剤組成物 | |
| KR102477052B1 (ko) | 선복화 단백다당체 또는 선복화 올리고당/펩타이드 복합체를 유효성분으로 함유하는 피부 외용제 조성물 및 이의 제조방법 | |
| DE3409029C2 (ko) | ||
| KR20180124443A (ko) | 흰목이버섯 자실체 추출물을 포함하는 피부장벽강화용 화장료 조성물 | |
| KR100549662B1 (ko) | 러시아산 무미 추출물 또는 분획물을 함유하는면역활성증강용 조성물 | |
| US4442087A (en) | Interferon inducer, a process for producing the same and pharmaceutical composition containing the same | |
| AU2001218789B2 (en) | Polysaccharide compound having immune stimulating activity | |
| EP0173228A2 (en) | Polysaccharide rin substance, production of the same and use of the same | |
| JPS5899498A (ja) | フラボノ−ル配糖体 | |
| JPH11130690A (ja) | 免疫調節薬及び抗炎症薬 | |
| JPH06256205A (ja) | 植物組織からの生理活性物質の製造方法及びこの物質を含有する組成物 | |
| EP2305280A1 (en) | Bcl-2 protein expressor, apoptosis inhibitor and preventive for uv-dna damage in epidermal cells | |
| AU2001218789A1 (en) | Polysaccharide compound having immune stimulating activity | |
| JPS63233921A (ja) | 抗腫瘍活性物質及びその製造法 | |
| JPS6152806B2 (ko) | ||
| KR20050050072A (ko) | 러시아산 무미 추출물 또는 분획물을 함유하는면역활성증강용 조성물 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| G170 | Re-publication after modification of scope of protection [patent] | ||
| FPAY | Annual fee payment |
Payment date: 20130527 Year of fee payment: 7 |
|
| FPAY | Annual fee payment |
Payment date: 20140528 Year of fee payment: 8 |
|
| FPAY | Annual fee payment |
Payment date: 20150527 Year of fee payment: 9 |
|
| FPAY | Annual fee payment |
Payment date: 20170530 Year of fee payment: 11 |
|
| FPAY | Annual fee payment |
Payment date: 20180529 Year of fee payment: 12 |
|
| EXPY | Expiration of term |