JP7689416B2 - かご状シロキサン含有高分子、かご状シロキサン及びその製造方法 - Google Patents
かご状シロキサン含有高分子、かご状シロキサン及びその製造方法 Download PDFInfo
- Publication number
- JP7689416B2 JP7689416B2 JP2020063794A JP2020063794A JP7689416B2 JP 7689416 B2 JP7689416 B2 JP 7689416B2 JP 2020063794 A JP2020063794 A JP 2020063794A JP 2020063794 A JP2020063794 A JP 2020063794A JP 7689416 B2 JP7689416 B2 JP 7689416B2
- Authority
- JP
- Japan
- Prior art keywords
- cage
- siloxane
- carbon atoms
- alkyl group
- phenyl group
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Landscapes
- Compositions Of Macromolecular Compounds (AREA)
- Silicon Polymers (AREA)
Description
[1]
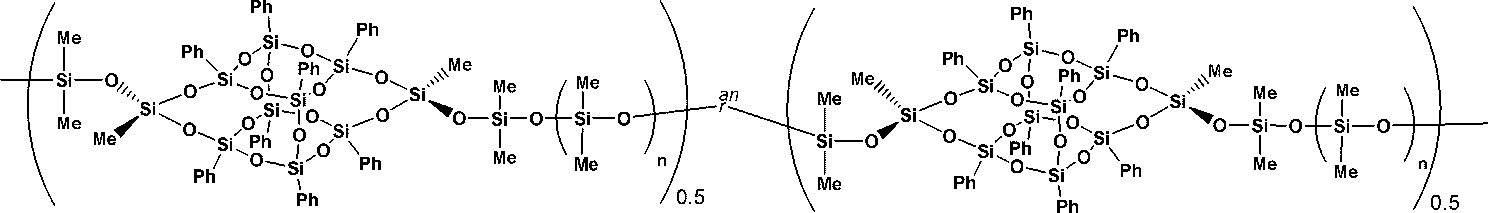
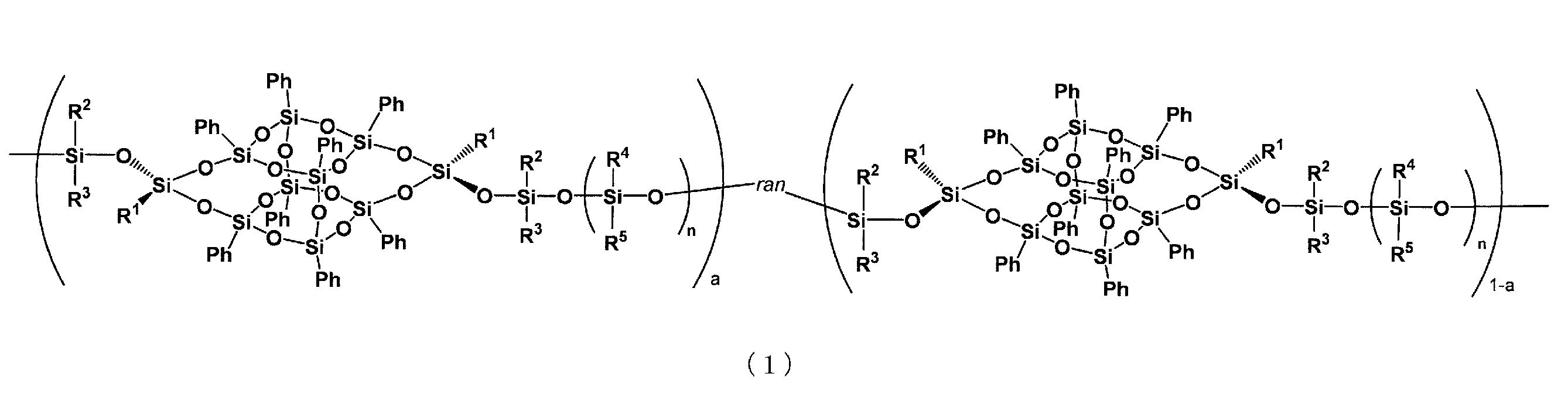
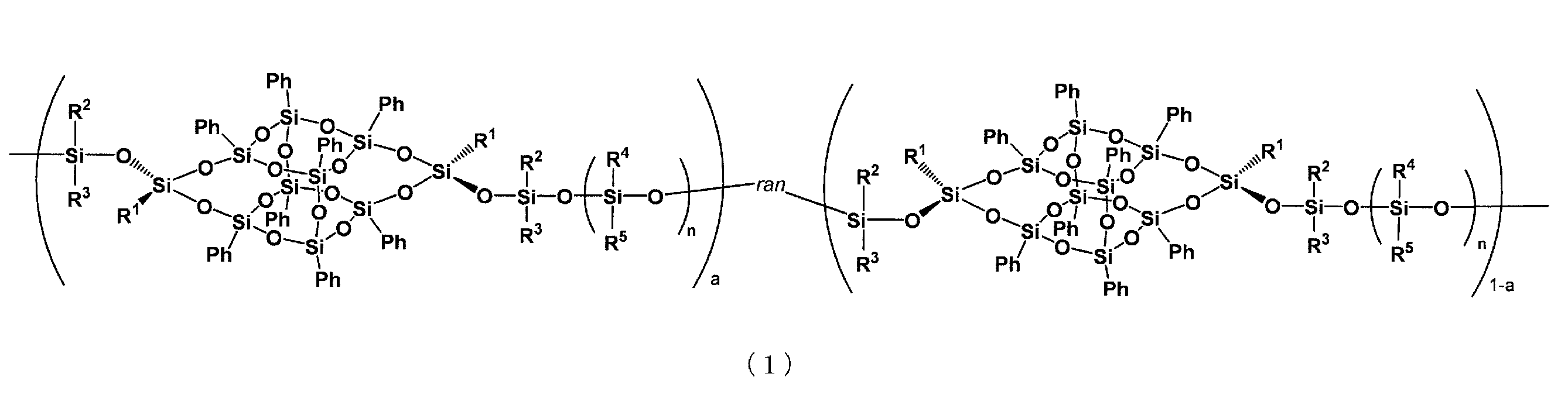
一般式(1)
かご状シロキサン含有高分子。
なお、本明細書中で「ハロゲン原子で置換されていてもよい」とは、当該アルキル基またはフェニル基の任意の水素原子がハロゲン原子で置換されても良いことを意味し、置換される水素原子の数は複数であってもよい。
[2]
[1]に記載のかご状シロキサン含有高分子、架橋剤、及び架橋触媒を含んでなる硬化膜。
[3]
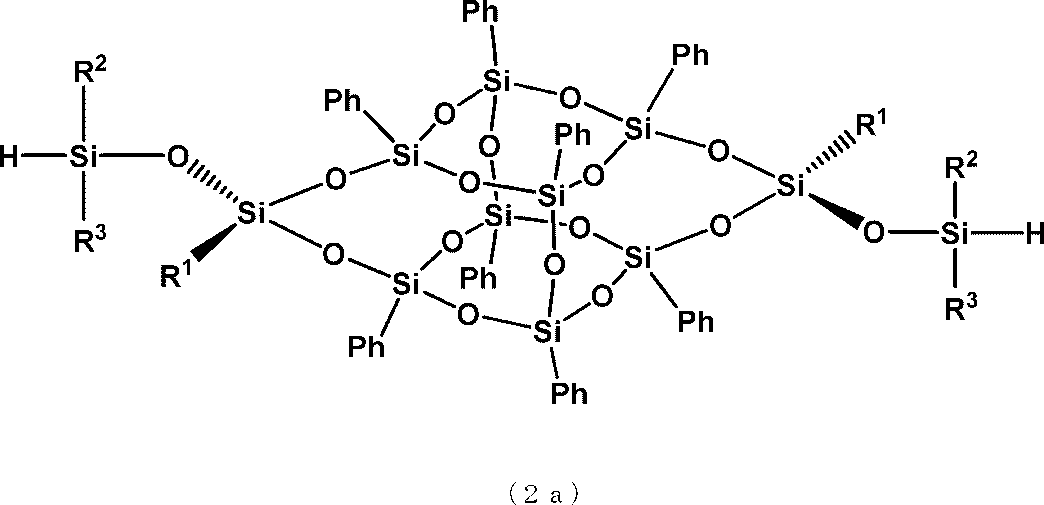
一般式(2a)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサン化合物、および、一般式(2b)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサン化合物、の一方または両方を含むかご状シロキサン化合物であって、前記シス型かご状シロキサン化合物または前記トランス型かご状シロキサン化合物のいずれかを70モル%以上含むかご状シロキサン化合物と、
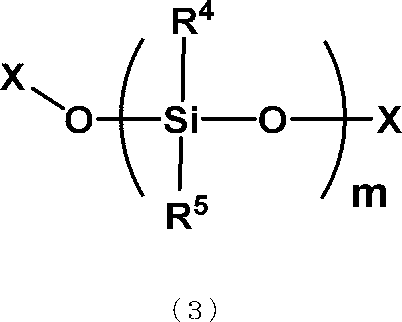
一般式(3)
(式中、R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。Xは水素原子、メチル基又はエチル基を表す。mは2から10の整数を表す。)で示される直鎖
シロキサン化合物、または
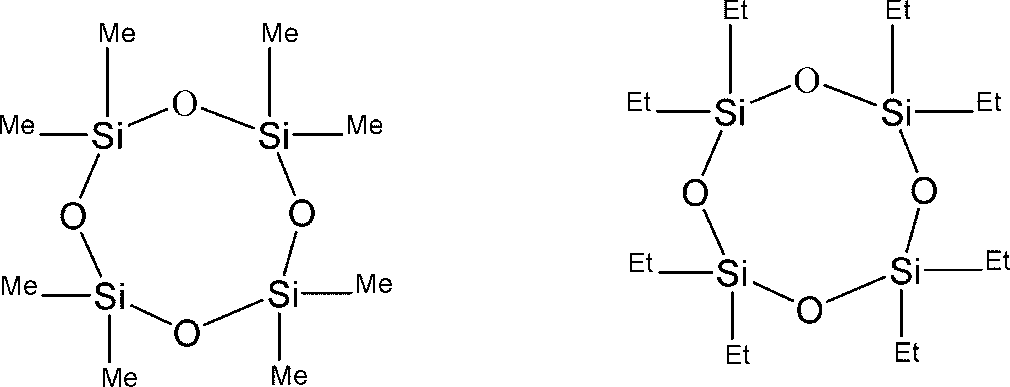
一般式(3’)
(式中、R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。)で示される環状シロキサン化合物、
とを、酸触媒存在下で反応させることを特徴とする、一般式(1)で示されるかご状シロキサン含有高分子の製造方法。
[4]
一般式(1)で示されるかご状シロキサン含有高分子を製造する方法であって、一般式(4)
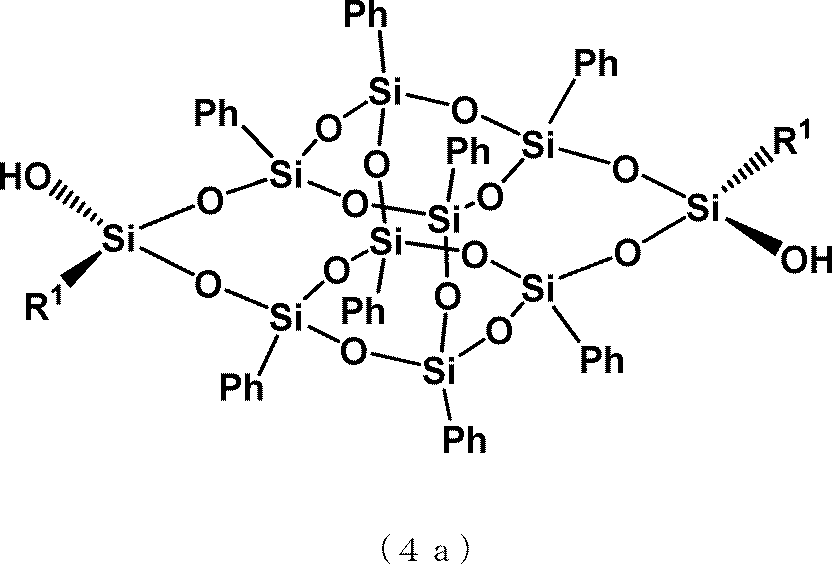
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるかご状シロキサンジオールを晶析し、一般式(4a)
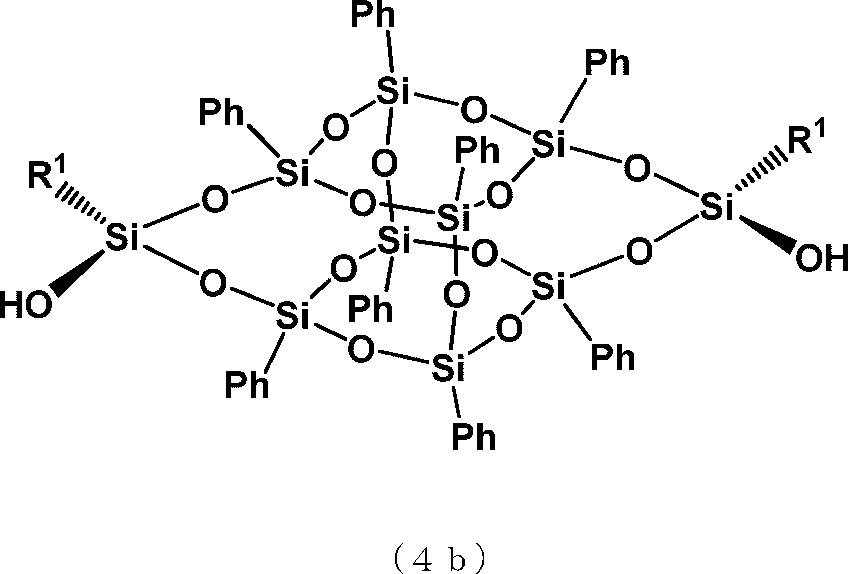
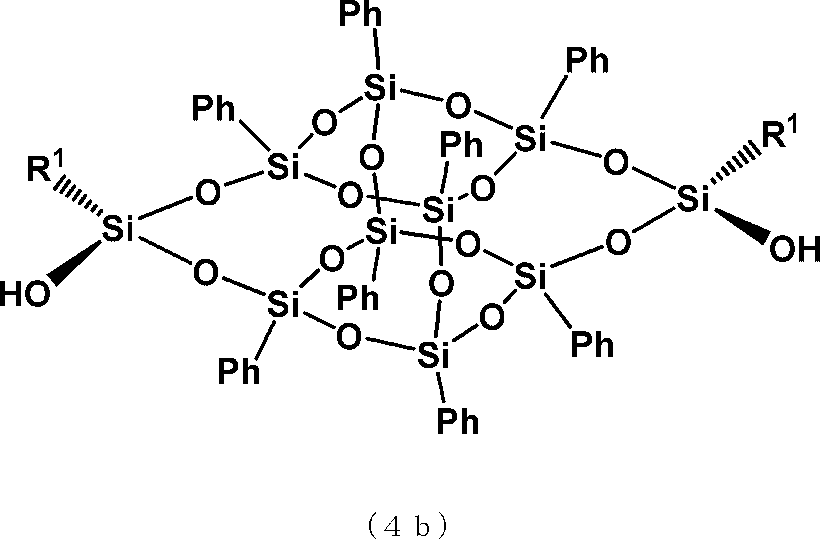
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサンジオール、又は一般式(4b)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサンジオールのいずれかを70モル%以上に富化する工程、
得られた一般式(4a)又は(4b)で示されるかご状シロキサンジオールのいずれかを70モル%以上含むかご状シロキサンジオールと、クロロヒドロシランR2R3HSiCl(式中、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)とを反応させ、一般式(2a)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサン化合物、又は、一般式(2b)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサン化合物のいずれかを70モル%以上含むかご状シロキサン化合物を得る工程、および
得られた一般式(2a)又は(2b)で示されるかご状シロキサン化合物のいずれかを70モル%以上含むかご状シロキサン化合物と、一般式(3)
(式中、R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。Xは水素原子、メチル基又はエチル基を表す。mは2から10の整数を表す。)で示される直鎖シロキサン化合物、または
一般式(3’)
(式中、R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。)で示される環状シロキサン化合物、
とを酸触媒存在下で反応させる工程、
を含むことを特徴とする、製造方法。
[5]
一般式(4)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるかご状シロキサンジオールを極性有機溶媒から晶析し、一般式(4a)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサンジオール、又は一般式(4b)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサンジオールのいずれかを70モル%以上に富化する方法。
[6]
極性有機溶媒が、テトラヒドロフラン、アセトン及びシクロペンチルメチルエーテルからなる群から選ばれる少なくとも一つを含むことを特徴とする、[5]に記載のかご状シロキサンジオールのいずれかを70モル%以上に富化する方法。
[7]
一般式(4a)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサンジオール、および一般式(4b)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサンジオール、の一方または両方を含むかご状シロキサンジオールであって、前記シス型かご状シロキサンジオールまたは前記トランス型かご状シロキサンジオールのいずれかを70モル%以上含有することを特徴とするかご状シロキサンジオール。
ラン、テトラエトキシシラン又はパーメトキシオリゴシロキサンが好ましく、パーメトキシオリゴシロキサンが更に好ましい。架橋剤の含有率は、かご状シロキサン含有高分子(1)に対して0.01重量%から20重量%の範囲にあることが好ましく、より好ましくは0.1重量%から10重量%である。
(式中、Phはフェニル基を表す。R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。Xは水素原子、メチル基又はエチル基を表す。nは0から20の範囲をとる実数を表し、0から6の範囲をとる実数であることが好ましい。nは整数でもよいが、平衡重合の場合は複数の整数の平均数となるので、整数でなくともよい。mは2から10の整数を表す。)
、(2a-1)、(2b-1)、(2a-2)又は(2b-2)が更に好ましい。
ましく、(3-2)又は(3-8)が殊更好ましい。これらの直鎖シロキサン化合物は、市販品を用いることも、既知の製造方法に従って合成して用いることも出来る。
また原料としてシス型かご状シロキサン化合物一般式(2b)の割合が70モル%以上であるかご状シロキサン化合物(2)を用いることによって、シス型かご状シロキサン含有高分子(1b)を70%以上含むかご状シロキサン含有高分子(1)を製造することが出来る。
好ましく、(2a-1)、(2b-1)、(2a-2)又は(2b-2)が更に好ましい。
本発明では、トランス型かご状シロキサンジオール(4a)及びシス型かご状シロキサンジオール(4b)の混合物に対し、晶析により(4a)又は(4b)のいずれか一方を70モル%以上含む異性体の富化を行う工程(以下、異性体富化工程ともいう)を行い、これを製造原料としてシリル化工程を行い、かご状シロキサン化合物(2a)又は(2b)を70%以上含むかご状シロキサン化合物(2)を得る工程を含むことを特徴とする。異性体富化工程については後述する。
当業者が有機ケイ素化合物や有機化合物の晶析に通常用いる方法を適用することが出来、溶媒の沸点以下の温度に加熱後冷却して過飽和とする熱結晶化法、かご状シロキサンジオール(4)の極性有機溶媒溶液に貧溶媒を加える方法、又はゆっくりと溶媒を蒸発させる蒸発法等が例示できる。該貧溶媒としては、極性有機溶媒に混和しかご状シロキサンジオール化合物(4)の溶解度が低いものであれば特に制約はなく、ペンタン、ヘキサン、オクタン等の炭化水素溶媒;メタノール、エタノール等のアルコール溶媒が例示できる。晶析温度は特に限定されないが、通常は-80℃から80℃の範囲が好ましく、0℃から50℃がより好ましい。
アルゴン雰囲気下、25mgのトリス(ペンタフルオロフェニル)ボランをジクロロメタン54.2gに溶解し、ここにトランス型かご状シロキサン化合物(2a-1)/シス型かご状シロキサン化合物(2b-1)比が9/1のかご状シロキサン化合物7.0g、1,3-ジメトキシ-1,1,3,3-テトラメチルジシロキサン0.91gのジクロロメタン24.1g溶液をゆっくり滴下した。滴下終了30分後、溶液は発泡した。3時間半後、トリエチルアミン少量を加え反応を停止した。反応混合物を多量のメタノールにゆっくりと加え、沈殿をろ取して粗高分子を得た。これを再度THFに溶解し、多量のメタノール中にゆっくりと加え、再沈殿した高分子をろ取し、減圧下で乾燥させることによりかご状シロキサン含有高分子(1a-1)を白色粉末として6.6g得た。PMMA換算のゲルパーミエーションクロマトグラフィーによる分子量測定では、かご状シロキサン含有高分子(1a-1)(1a-1/1b-1=9/1)は重量平均分子量 161000
、数平均分子量53000であった。
アルゴン雰囲気下、25mgのトリス(ペンタフルオロフェニル)ボランをジクロロメタン54.2gに溶解し、ここにトランス異性体(2a-1)/シス異性体(2b-1)比が2/8のかご状シロキサン化合物7.0g、1,3-ジメトキシ-1,1,3,3-テトラメチルジシロキサン0.91gのジクロロメタン24.1g溶液をゆっくり滴下した。滴下終了30分後、溶液は発泡した。3時間半後、トリエチルアミン少量を加え反応を停止した。反応混合物を多量のメタノールにゆっくりと加え、沈殿をろ取して粗高分子を得た。これを再度THFに溶解し、多量のメタノール中にゆっくりと加え、再沈殿した高分子をろ取し、減圧下で乾燥させることによりかご状シロキサン含有高分子(1b-1)(1a-1/1b-1=2/8)を白色粉末として6.6gを得た。PMMA換算のゲルパーミエーションクロマトグラフィーによる分子量測定では、かご状シロキサン含有高分子(1b-1)は重量平均分子量 345000、数平均分子量175000であった
。
アルゴン雰囲気下、25mgのトリス(ペンタフルオロフェニル)ボランをジクロロメタン54.2gに溶解し、ここにトランス異性体(2a-1)/シス異性体(2b-1)比が5/5のかご状シロキサン化合物(2-1)7.0g、1,3-ジメトキシ-1,1,3,3-テトラメチルジシロキサン0.91gのジクロロメタン24.1g溶液をゆっくり滴下した。滴下終了30分後、溶液は発泡した。3時間半後、トリエチルアミン少量を加え反応を停止した。反応混合物を多量のメタノールにゆっくりと加え、沈殿をろ取して粗高分子を得た。これを再度THFに溶解し、多量のメタノール中にゆっくりと加え、再沈殿した高分子をろ取し、減圧下で乾燥させることによりかご状シロキサン含有高分子(1c)(1a-1/1b-1=5/5)を白色粉末として6.6g得た。PMMA換算のゲルパーミエーションクロマトグラフィーによる分子量測定では、この高分子は重量平均分子量 188000、数平均分子量66000であった。
ケーターを用いてテフロンコートしたステンレス板上に塗布製膜した。これを、40℃で30分、70℃で30分、100℃で1時間、200℃で2時間加熱乾燥させ、ステンレス板から剥がし透明薄膜を調製した。この薄膜の1%重量減少温度は438℃、5%重量減少温度は485℃であった。薄膜のガラス転移点をDMAにより求めたところ32℃であった。この薄膜を切り出し、室温で引張強度試験を行ったところ、塑性変形による応力伸びを示し、破断点での応力は13MPaであった。
アルゴン雰囲気下、25mgのトリス(ペンタフルオロフェニル)ボランをジクロロメタン54.2gに溶解し、ここにトランス異性体(2a-2)/シス異性体(2b-2)比が9/1のかご状シロキサン化合物7.0g、1,3-ジメトキシ-1,1,3,3-テトラメチルジシロキサン0.91gのジクロロメタン24.1g溶液をゆっくり滴下した。滴下終了30分後、溶液は発泡した。3時間半後、トリエチルアミン少量を加え反応を停止した。反応混合物を多量のメタノールにゆっくりと加え、沈殿をろ取して粗高分子を得た。これを再度THFに溶解し、多量のメタノール中にゆっくりと加え、再沈殿した高分子をろ取し、減圧下で乾燥させることによりかご状シロキサン含有高分子(1a-5)(1a-5/1b-5=9/1)を白色粉末として6.6g得た。PMMA換算のゲルパーミエーションクロマトグラフィーによる分子量測定では、この高分子は重量平均分子量32000、数平均分子量18000であった。
特許4379120号公報記載の方法に従い調製したかご状シロキサンジオール(4-1)((4a-1)および(4b-1)の1:1比の異性体混合物)20.0gを177mLの沸騰THFに完全溶解させた。これを室温まで降温し、14時間静置し、晶析させた。析出した結晶をろ取することにより、トランス型かご状シロキサンジオールを6.8g得た。これは、トランス異性体(4a-1)/シス異性体(4b-1)比が9.5/0.5であることがケイ素NMRにより決定された。
溶液を濃縮後、さらに同様の操作を繰り返し、トランス異性体(4a-1)/シス異性体(4b-1)比が9/1のトランス型かご状シロキサンジオール(2a-1)1.1gを白色結晶性粉末として得た。
この母液を濃縮することにより、トランス異性体(4a-1)/シス異性体(4b-1)比が2/8のシス型かご状シロキサンジオールを結晶性粉末として11.5g得た。
磁気撹拌子、ジムロート冷却器および三方コックを備えた200mL三口フラスコに、トランス型かご状シロキサンジオール(4a-1)/シス型かご状シロキサンジオール(4b-1)比が9/1のかご状シロキサンジオール42.6g(35.9mmol)を収め、装置をアルゴンで置換した。このフラスコにピリジン11.36g(143.7mmol)および脱水THF360mLを収め、クロロジメチルシラン13.6g(144mmol)を注射器より30分かけて滴下した。滴下後、1時間加熱還流させた。反応混合物を分液ロートに移し、ヘキサン300mLで抽出し、蒸留水200mLで3回洗浄した。有機層を硫酸マグネシウムで乾燥し、ろ過により硫酸マグネシウムを除いた。ろ液をロータリーエバポレーターで濃縮し、減圧乾燥することによりかご状シロキサン化合物(2a-1)(2a-1/2b-1=9/1)を白色固体として46.0g(収率98%)得た。
.8Hz,12H),0.2706(s,6H),4.7056(sep,J=2.8Hz,2H),7.1780(t,J=7.54Hz,9H),7.2534(t,J=7.5Hz,オーバーラップ),7.30-7.45(18H、オーバーラップ),7.52-7.58(m,9H、オーバーラップ).13C-NMR(101MHz,CDCl3),δ(ppm):-3.53,-0.41,127.17,127.35,129.
90,129.97,130.55,131.42,133.58,133.68.29
Si-NMR(79MHz,CDCl3),δ(ppm):-79.52,-79.21,-63.39,-4.48.IRスペクトル(固体,cm-1):3072,3053,3006,2960,2133,1595,1429,1275,1250,1109,1065,1053,1030,997,904,833,814,783,737,729,719,694,671,627,619,613.
磁気撹拌子、ジムロート冷却器および三方コックを備えた200mL三口フラスコに、トランス型かご状シロキサンジオール(4a-1)/シス型かご状シロキサンジオール(4b-1)比が9/1のかご状シロキサンジオール10.0g(8.43mmol)を収め、装置をアルゴンで置換した。このフラスコにピリジン2.68g(33.9mmol)および脱水THF80mLを収め、クロロフェニルメチルシラン3.15 g(20.
1 mmol)を注射器より10分かけて滴下した。滴下後、1時間加熱還流させた。反
応混合物を分液ロートに移し、クロロホルム100mLで抽出し、蒸留水150mLで3回洗浄した。有機層を硫酸マグネシウムで乾燥し、ろ過により硫酸マグネシウムを除いた。ろ液をロータリーエバポレーターで濃縮し、減圧乾燥して結晶性固体を13.4g得た。これを最少量のTHFに溶解し、メタノールをゆっくりとTHF量の三倍加え、トランス型かご状シロキサン化合物(2a-2)(2a-2/2b-2=9/1)を粉末状白色固体として11.1g(収率92.7%)得た。
磁気撹拌子、10mL滴下ロート、ジムロート冷却器および三方コックを備えた100mL三口フラスコに、トランス型かご状シロキサンジオール(4a-1)/シス型かご状シロキサンジオール(4b-1)比が9/1のかご状シロキサンジオール5.00g(3.84mmol)を収め、アルゴンで置換した。三口フラスコにトリエチルアミン1.54g(15.2mmol)および脱水THF40mLを収めた。滴下ロートにクロロジフェニルシラン2.83g(9.22mmol)を収め、10分かけて滴下した。滴下後、1時間加熱還流させた。反応混合物を分液ロートに移し、ジエチルエーテル150mLを加え、蒸留水100mLで3回洗浄した。有機層を硫酸マグネシウムで乾燥させ、ろ過により硫酸マグネシウムを除いた。ろ液をロータリーエバポレーターで濃縮することで淡黄色の固体を得た。これをヘキサンで洗い、吸引ろ過し、減圧乾燥することで白色固体を5.57g得た。得られた白色固体を最少量のTHFに溶解し、5倍量のメタノールを加え
再結晶することでトランス型かご状シロキサン化合物(2a-3)(2a-3/2b-3=9/1)を無色の結晶として3.71g(収率62.2%)得た。
磁気撹拌子、ジムロート冷却器および三方コックを備えた500mL三口フラスコに、トランス型かご状シロキサンジオール(4a-1)/シス型かご状シロキサンジオール(4b-1)比が2/8のかご状シロキサンジオール30.0g(25.3mmol)を収め、装置をアルゴンで置換した。このフラスコにピリジン8.03g(102mmol)および脱水THF250mLを収め、クロロジメチルシラン9.61g(102mmol)を注射器より30分かけて滴下した。滴下後、1時間加熱還流させた。反応混合物を分液ロートに移し、ヘキサン300mLで抽出し、蒸留水200mLで3回洗浄した。有機層を硫酸マグネシウムで乾燥し、ろ過により硫酸マグネシウムを除いた。ろ液をロータリーエバポレーターで濃縮し、減圧乾燥してシス型かご状シロキサン化合物(2b-1)(2a-1/2b-1=2/8)を粉末状白色固体として31.1g(収率94.4%)得た。
m),7.30‐7.46(m,19.6H),7.53‐7.58(m,9.7H).
13C-NMR(101MHz,CDCl3),δ(ppm):-3.5291(SiMe2),-0.4094(SiMe),127.0726(ortho),127.2616(ortho),127.3486(ortho),129.8418(para),129.9634(para,overlap),130.5359(ipso),130.5777(ipso),131.4261(ipso),133.5760(meta),133.6049(meta),133.7439(meta).29Si-NMR(79MHz,CDCl3),δ(ppm):-79.67,-79.38,-79.21,-63.41,-4.46.
かご状シロキサンジオール異性体混合物((4a-1)/ (4b-1) = 92/ 8) を10 g、 オクタメチルシクロテトラシロキサン(D4)を2.3 g, トルエン(16.8
g)を100 mLの4つ口丸底フラスコに加え、還流管、マグネチックスターラー、オイルバスをセットし、窒素をフローした。撹拌しながら、硫酸 0.31 g、トルエン2.0 gを加え、1時間還流させた。その後80℃で5時間熟成した。加熱を停止し、水を
加え、分液後、水層を除去した。さらに数回水洗後、有機層を濃縮し、ヘプタンで再沈殿させ、沈殿をヘプタンで数回洗浄後、80℃で減圧乾燥し、白色固体8.6gを得た。PMMA換算のゲルパーミエーションクロマトグラフィーによる分子量測定では、かご状シロキサン含有高分子(1a-2)((1a-2/1b-2=11.5/1))は重量平均分子量 142000、数平均分子量57000であった。1H-NMRよりnは平均3.0であった。
かご状シロキサンジオール異性体混合物((4a-1)/ (4b-1) = 25/ 75) を1
0 g、 オクタメチルシクロテトラシロキサン(D4)を2.3 g, トルエン(18.
8 g)を100 mLの4つ口丸底フラスコに加え、還流管、マグネチックスターラー、
オイルバスをセットし、窒素をフローした。撹拌しながら、硫酸 0.31 g、トルエン2.0 gを加え、1時間還流させた。その後80℃で5時間熟成した。加熱を停止し、
水を加え、分液後、水層を除去した。さらに数回水洗後、有機層を濃縮し、ヘプタンで再沈殿させ、沈殿をヘプタンで数回洗浄後、80℃で減圧乾燥し、白色固体8.6gを得た。PMMA換算のゲルパーミエーションクロマトグラフィーによる分子量測定では、かご状シロキサン含有高分子(1b-2)((1a-2/1b-2=1/3))は重量平均分子量 146000、数平均分子量45000であった。1H-NMRよりnは平均3.2であった。
かご状シロキサンジオール異性体混合物((4a-1)/ (4b-1) = 50/ 50) を1
0 g、 オクタメチルシクロテトラシロキサン(D4)を2.3 g, トルエン(16.
8 g)を100 mLの4つ口丸底フラスコに加え、還流管、マグネチックスターラー、
オイルバスをセットし、窒素をフローした。撹拌しながら、硫酸 0.31 g、トルエン2.0 gを加え、1時間還流させた。その後80℃で7時間熟成した。加熱を停止し、
水を加え、分液後、水層を除去した。さらに数回水洗後、有機層を濃縮し、ヘプタンで再沈殿させ、沈殿をヘプタンで数回洗浄後、80℃で減圧乾燥し、白色固体8.3gを得た。PMMA換算のゲルパーミエーションクロマトグラフィーによる分子量測定では、かご状シロキサン含有高分子(1C’)は重量平均分子量 73000、数平均分子量310
00であった。1H-NMRよりnは平均3.2であった。
Claims (6)
- 請求項1に記載のかご状シロキサン含有高分子、架橋剤、及び架橋触媒を含んでなる組成物を熱硬化してなる硬化膜であって、
前記架橋剤が、アルコキシ置換モノシラン又はパーアルコキシオリゴシロキサンである、硬化膜。 - 一般式(2a)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサン化合物、および、一般式(2b)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサン化合物、の一方または両方を含むかご状シロキサン化合物であって、前記シス型かご状シロキサン化合物または前記トランス型かご状シロキサン化合物のいずれかを70モル%以上含むかご状シロキサン化合物と、一般式(3)
(式中、R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。Xは水素原子、メチル基又はエチル基を表す。mは2から10の整数を表す。)で示される直鎖シロキサン化合物、または一般式(3’)
(式中、R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。)で示される環状シロキサン化合物、
とを、酸触媒存在下で反応させることを特徴とする、一般式(1)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。R4及びR5はそれぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。aは1から0.7の範囲をとる実数、又は0から0.3の範囲をとる実数を表す。nは2から20の範囲をとる実数を表す。ranは、不規則共重合体であることを表す。)で示される
かご状シロキサン含有高分子の製造方法。 - 一般式(1)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。R4及びR5はそれぞれ独立にハロゲン原子で置換されていてもよい炭素数1
から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。aは1から0.7の範囲をとる実数、又は0から0.3の範囲をとる実数を表す。nは2から20の範囲をとる実数を表す。ranは、不規則共重合体であることを表す。)で示される
かご状シロキサン含有高分子を製造する方法であって、一般式(4)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるかご状シロキサンジオールを晶析し、一般式(4a)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサンジオール、又は一般式(4b)
(式中、R1は炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサンジオールのいずれかを70モル%以上に富化する工程、
前記工程で得られた一般式(4a)又は(4b)で示されるかご状シロキサンジオールのいずれかを70モル%以上含むかご状シロキサンジオールと、クロロヒドロシランR2R3HSiCl(式中、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)とを反応させ、一般式(2a)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるトランス型かご状シロキサン化合物、又は、一般式(2b)
(式中、R1、R2及びR3はそれぞれ独立に炭素数1から3のアルキル基又はフェニル基を表す。)で示されるシス型かご状シロキサン化合物のいずれかを70モル%以上含むかご状シロキサン化合物を得る工程、および
前記工程で得られた一般式(2a)又は(2b)で示されるかご状シロキサン化合物のいずれかを70モル%以上含むかご状シロキサン化合物と、一般式(3)
(式中、R4及びR5は、それぞれ独立にハロゲン原子で置換されていてもよい炭素数1から3のアルキル基又はハロゲン原子で置換されていてもよいフェニル基を表す。Xは水素原子、メチル基又はエチル基を表す。mは2から10の整数を表す。)で示される直鎖シロキサン化合物、または
一般式(3’)
とを酸触媒存在下で反応させる工程、
を含むことを特徴とする、方法。 - 前記ケトンが、アセトンであり、前記エーテル溶媒が、テトラヒドロフラン又はシクロペンチルメチルエーテルであることを特徴とする、請求項5に記載のかご状シロキサンジオールのいずれかを70モル%以上に富化する方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020063794A JP7689416B2 (ja) | 2020-03-31 | 2020-03-31 | かご状シロキサン含有高分子、かご状シロキサン及びその製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020063794A JP7689416B2 (ja) | 2020-03-31 | 2020-03-31 | かご状シロキサン含有高分子、かご状シロキサン及びその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021161226A JP2021161226A (ja) | 2021-10-11 |
| JP7689416B2 true JP7689416B2 (ja) | 2025-06-06 |
Family
ID=78004425
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020063794A Active JP7689416B2 (ja) | 2020-03-31 | 2020-03-31 | かご状シロキサン含有高分子、かご状シロキサン及びその製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP7689416B2 (ja) |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010120901A (ja) | 2008-11-21 | 2010-06-03 | Konishi Kagaku Ind Co Ltd | 完全縮合オリゴシルセスキオキサン立体異性体、それを用いた重合体及びそれらの製造方法 |
-
2020
- 2020-03-31 JP JP2020063794A patent/JP7689416B2/ja active Active
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010120901A (ja) | 2008-11-21 | 2010-06-03 | Konishi Kagaku Ind Co Ltd | 完全縮合オリゴシルセスキオキサン立体異性体、それを用いた重合体及びそれらの製造方法 |
Non-Patent Citations (1)
| Title |
|---|
| Industrial & Engineering Chemistry Research,2019年,Vol.58,No.1,p.403-410 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021161226A (ja) | 2021-10-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4470738B2 (ja) | シルセスキオキサン誘導体 | |
| JPH08311205A (ja) | カルボシラン−デンドリマー類、カルボシラン−ハイブリツド材料、これらの製造方法およびこのカルボシラン−デンドリマー類から被覆材を製造する方法 | |
| CN107108663A (zh) | 使用衍生自锗烯的有机催化剂的氢化硅烷化方法 | |
| JP6702616B2 (ja) | 高純度のアミノシロキサン | |
| JP2006022207A (ja) | ケイ素化合物 | |
| US20180201734A1 (en) | Method for preparing polyhedral oligomeric silsesquioxane | |
| EP0728793A1 (fr) | Procédé de préparation de résine polyorganosiloxane, éventuellement alcoxylée, par condensation non hydrolytique | |
| JP5990909B2 (ja) | 片末端官能基含有オルガノポリシロキサン及びその製造方法 | |
| WO2003091186A2 (en) | Azasilanes and methods for making and using the same | |
| JP2010120901A (ja) | 完全縮合オリゴシルセスキオキサン立体異性体、それを用いた重合体及びそれらの製造方法 | |
| EP1539861A1 (en) | Process for the preparation of polyorganosilylated carboxylate monomers or polymers thereof | |
| JP3652151B2 (ja) | 硬化性ポリメチルシルセスキオキサンの製造方法 | |
| TW201925144A (zh) | 矽氧烷化合物及其製造方法、聚合體、共聚體及眼科設備 | |
| JP3801208B2 (ja) | 硬化性ポリメチルシルセスキオキサン組成物 | |
| CN107922442B (zh) | 具有(甲基)丙烯酸酯基团的有机硅化合物及用于制备其的方法 | |
| JP7689416B2 (ja) | かご状シロキサン含有高分子、かご状シロキサン及びその製造方法 | |
| US20060041098A1 (en) | Synthesis and characterization of novel cyclosiloxanes and their self- and co-condensation with silanol-terminated polydimethylsiloxane | |
| JP2013216895A (ja) | シリコーン樹脂を製造する方法 | |
| JPH0275635A (ja) | チオアルキルアクリレート官能基を含有するジオルガノポリシロキサン | |
| JP5601270B2 (ja) | フルオロアルキル基を有するシラザン化合物及びその製造方法 | |
| KR101208460B1 (ko) | Poss 단량체의 어셈블리 방법 | |
| JP2014101458A (ja) | オルガノポリシロキサン及びその製造方法 | |
| CN115916793A (zh) | 用于制备硅氧烷的方法 | |
| KR20100099322A (ko) | 니켈 함유 막 형성 재료 및 그 제조 방법 | |
| JP5079245B2 (ja) | 3位に置換基を有するオキセタン誘導体の重合方法および重合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A80 | Written request to apply exceptions to lack of novelty of invention |
Free format text: JAPANESE INTERMEDIATE CODE: A80 Effective date: 20200430 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20221012 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20230719 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230905 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231024 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240130 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240313 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240702 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240821 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241203 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250128 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250507 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250527 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7689416 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |