JP7586810B2 - ダノン病治療用遺伝子療法ベクター - Google Patents
ダノン病治療用遺伝子療法ベクター Download PDFInfo
- Publication number
- JP7586810B2 JP7586810B2 JP2021500664A JP2021500664A JP7586810B2 JP 7586810 B2 JP7586810 B2 JP 7586810B2 JP 2021500664 A JP2021500664 A JP 2021500664A JP 2021500664 A JP2021500664 A JP 2021500664A JP 7586810 B2 JP7586810 B2 JP 7586810B2
- Authority
- JP
- Japan
- Prior art keywords
- fold
- lamp
- vector
- seq
- identity
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/177—Receptors; Cell surface antigens; Cell surface determinants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
- A61K48/0066—Manipulation of the nucleic acid to modify its expression pattern, e.g. enhance its duration of expression, achieved by the presence of particular introns in the delivered nucleic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70596—Molecules with a "CD"-designation not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/021—Uses of viruses as vector for the expression of a heterologous nucleic acid
- C12N2799/022—Uses of viruses as vector for the expression of a heterologous nucleic acid where the vector is derived from an adenovirus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2799/00—Uses of viruses
- C12N2799/02—Uses of viruses as vector
- C12N2799/04—Uses of viruses as vector in vivo
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2810/00—Vectors comprising a targeting moiety
- C12N2810/50—Vectors comprising as targeting moiety peptide derived from defined protein
- C12N2810/80—Vectors comprising as targeting moiety peptide derived from defined protein from vertebrates
- C12N2810/85—Vectors comprising as targeting moiety peptide derived from defined protein from vertebrates mammalian
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/001—Vector systems having a special element relevant for transcription controllable enhancer/promoter combination
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2830/00—Vector systems having a special element relevant for transcription
- C12N2830/008—Vector systems having a special element relevant for transcription cell type or tissue specific enhancer/promoter combination
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Wood Science & Technology (AREA)
- Biomedical Technology (AREA)
- General Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Cardiology (AREA)
- Gastroenterology & Hepatology (AREA)
- Cell Biology (AREA)
- Diabetes (AREA)
- Heart & Thoracic Surgery (AREA)
- Physics & Mathematics (AREA)
- Virology (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Toxicology (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Obesity (AREA)
Description
本願は、その全体が参照により本明細書中に組み込まれる、2018年7月12日に出願された米国特許仮出願番号62/697,302の優先権を主張する。
本願は、EFS-Webを介して電子的に提出され、テキスト形式で電子的に提出された配列表が含まれている。テキストファイルは、2019年7月11日に作成された、「ROPA_011_01WO_SeqList_ST25.txt」という表題の、約62キロバイトのサイズを有する配列表を含む。このテキストファイルに含まれる配列表は、本明細書の一部であり、その全体が参照により本明細書中に組み込まれる。
本発明は、概して、リソソーム関連膜タンパク質2(LAMP-2、CD107bとしても知られる)における変異に関連する疾患の遺伝子療法に関する。
リソソーム関連膜タンパク質2(LAMP-2、CD107bとしても知られる)は、リソソーム関連膜糖タンパク質をコードする遺伝子である。遺伝子の選択的スプライシングによって、3つのアイソフォーム:LAMP-2A、LAMP-2B、及びLAMP-2Cが生成される。LAMP-2における機能欠失変異は、オートファジー障害に関連する家族性心筋症であるダノン病をはじめとするヒトの疾患と関連する。
リソソーム関連膜タンパク質2(LAMP-2)のアイソフォーム又はその機能的変異体をコードする導入遺伝子を含む発現カセットを含む遺伝子療法ベクターであって、前記導入遺伝子がヒト宿主細胞における発現のために最適化されている、遺伝子療法ベクター。
[本発明1002]
前記導入遺伝子が、ヒト宿主細胞における発現のためにコドン最適化されている、本発明1001の遺伝子療法ベクター。
[本発明1003]
前記発現カセットが、配列番号2よりも少ないCpG部位を含む、本発明1001又は本発明1002の遺伝子療法ベクター。
[本発明1004]
前記発現カセットが、配列番号2よりも少ないクリプティックスプライス部位を含む、本発明1001~1003のいずれかの遺伝子療法ベクター。
[本発明1005]
前記発現カセットが、配列番号2よりも少ない代替オープンリーディングフレームをコードする、本発明1001~1004のいずれかの遺伝子療法ベクター。
[本発明1006]
前記導入遺伝子が、配列番号3~5から選択される配列に対して少なくとも95%の同一性又は少なくとも99%の同一性を共有する、本発明1001~1004のいずれかの遺伝子療法ベクター。
[本発明1007]
前記導入遺伝子が、配列番号3~5から選択される配列を含む、本発明1006の遺伝子療法ベクター。
[本発明1008]
前記導入遺伝子が、配列番号3と少なくとも95%の同一性を共有するか、又は配列番号3と同一である、本発明1007の遺伝子療法ベクター。
[本発明1009]
前記発現カセットがコンセンサス最適化Kozak配列を含み、任意選択的に、前記コンセンサス最適化Kozak配列が配列番号6を含む、本発明1001~1008のいずれかの遺伝子療法ベクター。
[本発明1010]
前記発現カセットが完全長ポリA配列を含み、任意選択的に、前記完全長ポリA配列が配列番号7を含む、本発明1001~1009のいずれかの遺伝子療法ベクター。
[本発明1011]
前記発現カセットが、代替mRNAを生成することができる前記導入遺伝子に対して5’の開始部位を含まない、本発明1001~1010のいずれかの遺伝子療法ベクター。
[本発明1012]
前記発現カセットが、5’から3’の方向で、第一の逆方向末端反復、エンハンサ/プロモータ領域、イントロン、コンセンサス最適化Kozak配列、前記導入遺伝子、完全長ポリA配列を含む3’未翻訳領域、及び第二の逆方向末端反復を含む、本発明1001~1011のいずれかの遺伝子療法ベクター。
[本発明1013]
前記エンハンサ/プロモータ領域が、5’から3’の方向で、CMV IEエンハンサとニワトリβアクチンプロモータとを含み、任意選択的に、前記エンハンサ/プロモータ領域が、ニワトリβアクチン遺伝子の第一エクソン及び第一イントロンと、ウサギβグロビン遺伝子のスプライスアクセプタとをさらに含む、本発明1012の遺伝子療法ベクター。
[本発明1014]
前記発現カセットが、配列番号8~10から選択される配列に対して少なくとも95%の同一性を共有する、本発明1001~1013のいずれかの遺伝子療法ベクター。
[本発明1015]
前記発現カセットが、配列番号8~10から選択される配列に対して完全同一性を共有する、本発明1014の遺伝子療法ベクター。
[本発明1016]
前記発現カセットが、配列番号3に対して少なくとも95%の同一性を共有するか、又は配列番号8と同一である、本発明1014の遺伝子療法ベクター。
[本発明1017]
前記ベクターが、アデノ随伴ウイルス(AAV)ベクターである、本発明1001~1016のいずれかの遺伝子療法ベクター。
[本発明1018]
本発明1001~1017のいずれかの遺伝子療法ベクターを含む、医薬組成物。
[本発明1019]
それを必要とする対象においてダノン病又は別のオートファジー障害を治療又は防止する方法であって、
前記対象に対して、本発明1001~1017のいずれかの遺伝子療法ベクター又は本発明1018の医薬組成物を投与すること
を含む、方法。
[本発明1020]
前記ベクター又は医薬組成物が、静脈内、動脈内、心臓内、冠動脈内、心筋内、腎内、尿道内、硬膜外、及び筋肉内からなる群から選択される経路を介して投与される、本発明1019の方法。
[本発明1021]
前記オートファジー障害が、末期心不全、心筋梗塞、薬物中毒、糖尿病、末期腎不全、及び老化からなる群から選択される、本発明1019又は本発明1020の方法。
[本発明1022]
前記対象がヒトである、本発明1019~1021のいずれかの方法。
[本発明1023]
前記対象が、ダノン病又は別のオートファジー障害の症状を示している、本発明1019~1022のいずれかの方法。
[本発明1024]
前記対象が、減少しているか又は検出不能なLAMP-2発現を有すると特定されている、本発明1019~1023のいずれかの方法。
[本発明1025]
前記対象が、変異LAMP-2遺伝子を有すると特定されている、本発明1019~1024のいずれかの方法。
[本発明1026]
前記遺伝子療法ベクターを投与すると、未処置の対象と比較して、心臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が増加する、本発明1019~1025のいずれかの方法。
[本発明1027]
前記遺伝子療法ベクターを投与すると、未処置の対象と比較して、心臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が、少なくとも約1.2倍、少なくとも約1.3倍、少なくとも約1.4倍、少なくとも約1.5倍、少なくとも約1.6倍、少なくとも約1.7倍、少なくとも約1.8倍、少なくとも約1.9倍、少なくとも約2.0倍、少なくとも約2.2倍、少なくとも約2.3倍、少なくとも約2.4倍、少なくとも約2.5倍、少なくとも約3倍、又は少なくとも約4倍増加する、本発明1019~1026のいずれかの方法。
[本発明1028]
前記遺伝子療法ベクターを投与すると、未処置の対象の肝臓における発現と比較して、肝臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が、最大で約1.1倍、最大で約1.2倍、最大で約1.3倍、最大で約1.4倍、又は最大で約1.5倍増加する、本発明1019~1027のいずれかの方法。
[本発明1029]
対象においてLAMP-2Bを発現する方法であって、
アデノ随伴ウイルス(AAV)ベクターを前記対象に対して全身投与すること
を含み、
前記AAVベクターが、配列番号3と少なくとも95%の同一性を共有する導入遺伝子を含む発現カセットを含むか、又は配列番号3と同一であり、
前記導入遺伝子が、エンハンサ/プロモータ領域に機能的に連結され、
前記AAVベクターを前記対象に対して全身投与すると、前記AAVベクターの投与前のLAMP-2Bの発現又は未処置の対照対象におけるLAMP-2Bの発現と比較して、LAMP-2Bの発現が増加する、方法。
[本発明1030]
前記全身投与が静脈内投与を含む、本発明1029の方法。
[本発明1031]
前記AAVベクターを、前記対象の全体重1キログラム(vg)あたり、約1×10 12 ~5×10 14 ベクターゲノム(vg)の前記AAVベクター(vg/kg)の用量で投与する、本発明1029又は本発明1030の方法。
[本発明1032]
前記AAVベクターを、約1×10 13 ~5×10 14 vg/kgの用量で投与する、本発明1031の方法。
[本発明1033]
前記AAVベクターを、約5×10 13 ~3×10 14 vg/kgの用量で投与する、本発明1031の方法。
[本発明1034]
前記AAVベクターを、約5×10 13 ~1×10 14 vg/kgの用量で投与する、本発明1031の方法。
[本発明1035]
前記エンハンサ/プロモータ領域が、5’から3’の方向で、CMV IEエンハンサとニワトリβアクチンプロモータとを含み、任意選択的に、前記エンハンサ/プロモータ領域が、ニワトリβアクチン遺伝子の第一エクソン及び第一イントロンと、ウサギβグロビン遺伝子のスプライスアクセプタとをさらに含む、本発明1029~1034のいずれかの方法。
[本発明1036]
前記発現カセットが、前記導入遺伝子に機能的に連結されたコンセンサス最適化Kozak配列を含み、任意選択的に、前記コンセンサス最適化Kozak配列が配列番号6を含む、本発明1029~1035のいずれかの方法。
[本発明1037]
前記発現カセットが、前記導入遺伝子に機能的に連結された完全長ポリA配列を含み、任意選択的に、前記完全長ポリA配列が配列番号7を含む、本発明1029~1036のいずれかの方法。
[本発明1038]
前記発現カセットが、代替mRNAを生成することができる前記導入遺伝子に対して5’の開始部位を含まない、本発明1029~1037のいずれかの方法。
[本発明1039]
前記発現カセットが、5’から3’の方向で、機能的に連結された、第一の逆方向末端反復、エンハンサ/プロモータ領域、イントロン、コンセンサス最適化Kozak配列、前記導入遺伝子、完全長ポリA配列を含む3’未翻訳領域、及び第二の逆方向末端反復を含み、前記発現カセットが、前記導入遺伝子の開始コドンに対して5’の開始コドンを含まない、本発明1029~1038のいずれかの方法。
[本発明1040]
前記対象が霊長類である、本発明1029~1039のいずれかの方法。
[本発明1041]
前記対象が、減少しているか若しくは検出不能なLAMP-2発現を有すると特定されているか、又は有する疑いがある、本発明1029~1040のいずれかの方法。
[本発明1042]
前記対象が変異LAMP-2遺伝子を有する、本発明1029~1041のいずれかの方法。
[本発明1043]
前記対象がダノン病の症状を示している、本発明1029~1042のいずれかの方法。
[本発明1044]
前記対象が、ダノン病にかかっているか、またはダノン病のリスクがある、本発明1029~1043のいずれかの方法。
[本発明1045]
前記遺伝子療法ベクターを投与すると、未処置の対象と比較して、心臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が増加する、本発明1029~1044のいずれかの方法。
[本発明1046]
前記遺伝子療法ベクターを投与すると、未処置の対象と比較して、心臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が、少なくとも約1.2倍、少なくとも約1.3倍、少なくとも約1.4倍、少なくとも約1.5倍、少なくとも約1.6倍、少なくとも約1.7倍、少なくとも約1.8倍、少なくとも約1.9倍、少なくとも約2.0倍、少なくとも約2.2倍、少なくとも約2.3倍、少なくとも約2.4倍、少なくとも約2.5倍、少なくとも約3倍、又は少なくとも約4倍増加する、本発明1029~1045のいずれかの方法。
[本発明1047]
前記遺伝子療法ベクターを投与すると、未処置の対象の肝臓における発現と比較して、肝臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が、最大で約1.1倍、最大で約1.2倍、最大で約1.3倍、最大で約1.4倍、又は最大で約1.5倍増加する、本発明1029~1047のいずれかの方法。
[本発明1048]
配列番号3~5又はその機能的変異体のいずれか一つに対して少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%、又は少なくとも100%の同一性を共有するポリヌクレオチド配列を含む、ポリヌクレオチド。
[本発明1049]
前記ポリヌクレオチド配列が、配列番号3又はその機能的変異体に対して少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%、又は少なくとも100%の同一性を共有する、本発明1048のポリヌクレオチド。
[本発明1050]
前記ポリヌクレオチド配列が、配列番号3に対して少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%、又は少なくとも100%の同一性を共有する、本発明1049のポリヌクレオチド。
[本発明1051]
前記ポリヌクレオチド配列が、配列番号3からなる、本発明1050のポリヌクレオチド。
[本発明1052]
LAMP-2B又はその機能的変異体をコードする導入遺伝子である、本発明1048~1051のいずれかのポリヌクレオチド。
[本発明1053]
本発明1048~1052のいずれかのポリヌクレオチドを含む、発現カセット。
[本発明1054]
CAGプロモータ(配列番号22)に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有するエンハンサ/プロモータ領域を含む、本発明1053の発現カセット。
[本発明1055]
CMVプロモータ(配列番号23)、SV40プロモータ(配列番号24)、PGKプロモータ(配列番号25)、及び/又はヒトβアクチンプロモータ(配列番号26)から選択される配列に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有するエンハンサ/プロモータ領域を含む、本発明1053の発現カセット。
[本発明1056]
配列番号27に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有する3’UTRを含む、本発明1053~1055のいずれかの発現カセット。
[本発明1057]
CAGプロモータ(配列番号7)に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有するポリアデニル化配列を含む、本発明1053~1056のいずれかの発現カセット。
[本発明1058]
5’から3’の順で:
(a)CAGプロモータ(配列番号22)に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有する、エンハンサ/プロモータ領域;
(b)配列番号3に対して少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%、又は少なくとも100%の同一性を共有する、LAMP-2Bタンパク質をコードするポリヌクレオチド配列;
(c)配列番号27に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有する、3’UTR;及び
(d)CAGプロモータ(配列番号7)に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有する、ポリアデニル化配列
を含む、発現カセット。
[本発明1059]
前記機能的LAMP-2Bが、配列番号1に対して少なくとも少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%、又は少なくとも100%の同一性を共有する、本発明1058の発現カセット。
[本発明1060]
LAMP-2Bタンパク質をコードする前記ポリヌクレオチド配列が、配列番号2に対して最大で90%、最大で91%、最大で92%、最大で93%、最大で94%、最大で95%、最大で96%、最大で97%、最大で98%、最大で99%、又は最大で100%の同一性を共有する、本発明1058又は本発明1059の発現カセット。
[本発明1061]
(i)配列番号11に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有する5’ITRと、(ii)配列番号12に対して少なくとも80%の同一性、90%の同一性、95%の同一性、又は100%の同一性を共有する5’ITRと、に隣接している本発明1053~1069のいずれかの発現カセットを含む、AAVベクター。
[本発明1062]
AAV9カプシドを含む、本発明1061のAAVベクター。
[本発明1063]
前記AAV9カプシドが、配列番号27のアミノ酸1~736、配列番号27のアミノ酸138~736、及び/又は配列番号27のアミノ酸203~736に対して少なくとも95%の同一性を共有する、本発明1062のAAVベクター。
[本発明1064]
配列番号8~10のいずれか一つに対して少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%、又は少なくとも100%の同一性を共有するポリヌクレオチド配列を含む、ポリヌクレオチド。
[本発明1065]
前記ポリヌクレオチド配列が、配列番号8に対して少なくとも90%、少なくとも91%、少なくとも92%、少なくとも93%、少なくとも94%、少なくとも95%、少なくとも96%、少なくとも97%、少なくとも98%、少なくとも99%、又は少なくとも100%の同一性を共有する、本発明1064のポリヌクレオチド。
[本発明1066]
前記ポリヌクレオチド配列が、配列番号8からなる、本発明1065のポリヌクレオチド。
[本発明1067]
LAMP-2B又はその機能的変異体をコードする発現カセットを含む、本発明1065~1066のいずれかのポリヌクレオチド。
[本発明1068]
(i)配列番号11に対して少なくとも80%の同一性、90%の同一性、95%の同一性、若しくは100%の同一性を共有する5’ITRと、(ii)配列番号12に対して少なくとも80%の同一性、90%の同一性、95%の同一性、若しくは100%の同一性を共有する5’ITRと、のいずれか又は両方を含む、本発明1065~1067のいずれかのポリヌクレオチド。
[本発明1069]
本発明1065~1068のいずれかのポリヌクレオチドを含む、AAVベクター。
[本発明1070]
前記AAVベクターが、AAV9カプシドを含む、本発明1069のAAVベクター。
[本発明1071]
前記AAV9カプシドが、配列番号27のアミノ酸1~736、配列番号27のアミノ酸138~736、及び/又は配列番号27のアミノ酸203~736に対して少なくとも95%の同一性を共有する、本発明1071のAAVベクター。
[本発明1072]
それを必要とする対象においてダノン病を治療する方法であって、
本発明1061~1063又は本発明1069~1071のいずれかのAAVベクターを前記対象に静脈内投与すること
を含む、方法。
[本発明1073]
前記遺伝子療法ベクターを投与すると、未処置の対象と比較して、心臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が、少なくとも約1.2倍、少なくとも約1.3倍、少なくとも約1.4倍、少なくとも約1.5倍、少なくとも約1.6倍、少なくとも約1.7倍、少なくとも約1.8倍、少なくとも約1.9倍、少なくとも約2.0倍、少なくとも約2.2倍、少なくとも約2.3倍、少なくとも約2.4倍、少なくとも約2.5倍、少なくとも約3倍、又は少なくとも約4倍増加する、本発明1072の方法。
[本発明1074]
前記遺伝子療法ベクターを投与すると、未処置の対象の肝臓における発現と比較して、肝臓におけるLAMP-2Bポリヌクレオチド及び/又はLAMP-2Bタンパク質の発現が、最大で約1.1倍、最大で約1.2倍、最大で約1.3倍、最大で約1.4倍、又は最大で約1.5倍増加する、本発明1072又は本発明1073の方法。
発明の他の特徴及び利点は、以下の詳細な説明及び特許請求の範囲から明らかであり、これに含まれる。
本開示は、LAMP-2のアイソフォーム(例えば、LAMP-2B)をコードする、改善されたポリヌクレオチド配列、発現カセット、及びベクター、並びに関連する医薬組成物、及びLAMP-2欠乏又は変異に関連する疾患及び障害を治療するためのそれらの使用を提供する。本発明者らは、LAMP-2Bの遺伝子配列に対する修飾の結果、導入遺伝子発現が増大することを見出した。加えて、LAMP-2Bを発現する遺伝子療法ベクターの発現カセット中に特定配列要素が存在することで、導入遺伝子発現が改善される。したがって、本明細書中で開示されているLAMP-2ポリヌクレオチド配列、発現カセット、及びベクターは、以前の遺伝子療法ベクターよりも高レベルのLAMP-2発現を治療上関連する組織において達成できることをはじめとする利点を提供する。
「リソソーム関連膜タンパク質2」及び「LAMP-2」という語は、同義的に:(1)LAMP-2核酸によってコードされるアミノ酸配列(例えば、GenBank受入番号NM_002294.2(アイソフォームA).NM_013995.2(アイソフォームB)、NM_001122606.1(アイソフォームC)を参照)又はLAMP-2ポリペプチドのアミノ酸配列(例えば、GenBank受入番号NP_002285.1(アイソフォームA)、NP_054701.1(アイソフォームB)、NP_001116078.1(アイソフォームC)を参照)に対して、好ましくは、少なくとも約25、50、100、200、300、400、又はそれ以上のアミノ酸の領域にわたって、あるいは全長にわたって、約90%を超えるアミノ酸配列同一性、例えば、91%、92%、93%、94%、95%、96%、97%、98%若しくは99%又はそれ以上のアミノ酸配列同一性を有するアミノ酸配列を有する;(2)LAMP-2ポリペプチド(例えば、本明細書中で記載するLAMP-2ポリペプチド)のアミノ酸配列;又はLAMP-2核酸(例えば、本明細書中で記載するLAMP-2ポリヌクレオチド)によってコードされるアミノ酸配列、及びそれらの保存的に修飾された変異体を含む免疫源に対する抗体、例えば、ポリクローナル抗体と結合する;(3)LAMP-2タンパク質をコードする核酸配列、及びそれらの保存的に修飾された変異体に対応するアンチセンス鎖に対してストリンジェントなハイブリダイゼーション条件下で特異的にハイブリダイズする;(4)LAMP-2核酸(例えば、本明細書中で記載するようなLAMP-2ポリヌクレオチド、及び本明細書中で記載するようなLAMP-2ポリペプチドをコードするLAMP-2ポリヌクレオチド)に対して、好ましくは、少なくとも約25、50、100、200、500、1000、2000若しくはそれ以上のヌクレオチドの領域にわたって、又は全長にわたって、約90%超、好ましくは、約91%超、92%超、93%超、94%超、95%超、96%超、97%超、98%超、99%超、又はそれ以上のヌクレオチド配列同一性を有する核酸配列を有する、核酸及びポリペプチド多型変異体、対立遺伝子、突然変異体、及び種間相同体を指す。
図2に示す遺伝子発現カセットを、LAMP-2B導入遺伝子発現用のプラスミドベースの緑色蛍光タンパク質(GFP)レポータ系中で構築した。プラスミドは、LAMP-2B導入遺伝子、2Aペプチド、及び強化緑色蛍光タンパク質(eGFP)をコードする単一のオープンリーディングフレームを含んでいた。2Aペプチドの翻訳後自己切断の結果、LAMP-2B及びeGFPが当モル量で同時発現された。野生型LAMP-2Bコーディング配列(配列番号2)及びLAMP-2Bコーディング配列の3つのコドン変異体(コドン変異体1、2及び3;それぞれ配列番号3~5)を導入遺伝子として試験した。三つのコドン変異体は、野生型LAMP-2Bコーディング配列と比較して、CpGの数が減少し、クリプティック部位が除去され、オープンリーディングフレームの数が減少していた。
最適化AAV遺伝子療法ベクターは、実施例1で記載したLAMP-2B最適化変異体、CO1配列を組換えAAVベクターの発現カセットに挿入することによって、産生した。AAV調節カセットは、上流クリプティックATG配列の除去、最適化コンセンサスKozak配列、及び/又は完全長ポリアデニル化配列の使用によって修飾する。ベクターを、導入遺伝子の上流の一つ以上のさらなるATG部位、非最適化Kozak配列、及び/又は非完全長ポリアデニル化配列を含む対照組換えAAVベクターと比較して試験する。ベクターを、ダノン患者iPSC由来の心筋細胞においてインビトロで、及びダノン病のLAMP-2-/-ノックアウトマウスモデルにおいて試験する。最適化AAV遺伝子療法カセット及びベクターは、対照組換えAAVベクターと比較して、より高レベルの発現及び/又はより高いパーセンテージの細胞における発現をもたらすと予想される。
AAV遺伝子療法カセット及びベクターは、LAMP-2B変異体配列CO1(配列番号3)を、導入遺伝子の上流にクリプティック開始部位を有さず、最適化コンセンサスKozak配列、及びウサギグロビンからの完全長ポリアデニル化(ポリA)配列を有する組換えAAVプラスミドベクターに挿入することによって産生した(「LAMP-2B.v.1.2”;発現カセット:配列番号8)。LAMP-2B.v1.2を、最適化Kozak配列及びミニ-ポリAを含まず、野生型LAMP-2B導入遺伝子(導入遺伝子配列:配列番号2)を有する調節カセットである、LAMP-2B v1.0と比較した。
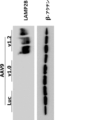
LAMP-2欠損マウスに、1×1013vg/kgの、元のヒトLAMP-2B(AAV9-LAMP-2B.v1.0)、最適化ヒトLAMP-2B(AAV9-LAMP-2B.v1.2、コドン変異体1-配列番号3)又はビヒクル単独を含むAAV9ウイルスベクターを静脈内注射した。治療後6週に、マウスを処分し、LAMP-2B発現について分析するために心筋組織を収集した。
ベクターコピー数の定量分析のために、DNA全体を、DNeasy Blood及び組織キットを製造業者のガイドラインにしたがって使用して凍結組織から単離した。DNA濃度及び完全性を分光光度法により評価した。qPCRを実施して、WPRE遺伝子についてTaqPath ProAmpマスターミックス(Applied Biosystems)と、
順:
及び、逆:
プライマー、並びにプローブ:
を使用してDNA1μgあたりのウイルスゲノムコピーを計算した。RNase Pを内在性対照(Thermofisher、#4403328)として使用した。ウイルス産生のために使用したベクターゲノム(WPRE)を含む直線化プラスミドを使用して標準曲線を作成した。サンプル当たりのDNAの定量化を、TaqManコピー数基準アッセイを使用して計算し、二倍体核あたりのベクターコピー数(VCN/二倍体核)として表した。
順:
及び、逆:
プライマー、並びにプローブ:
を使用してcDNAに関してqRT-PCRを実施した。
定量PCRをAAV9で処置されたLAMP-2欠損マウスの心臓組織に関して実施した。同様のウイルスコピー数が野生型及び最適化LAMP-2B含有ベクターで処置されたマウスの心臓組織において観察されたが(図9A)、AAV9最適化LAMP-2B.v1.2の転写は、AAV9-野生型LAMP-2B.v1.0と比較してほぼ7倍増加した(図9B)。心臓組織におけるv1.0及びv1.2ウイルスベクターの同様の形質導入にかかわらず、ヒトLAMP-2BmRNA発現の誘導は、v1.2を用いて有意に増強された。
ヒト以外の霊長類に、1×1013vg/kgの、実施例2に記載するコドン変異体LAMP-2B(v1.2、コドン変異体1-配列番号3)を含むAAV9ウイルスベクター、又はビヒクル対照のいずれかを静脈内注射した。治療後8週間に、ヒト以外の霊長類を人道的に処分し、心臓、筋肉、肝臓及び脳組織をLAMP-2B発現の分析のために収集した。
ベクターコピー数の定量分析のために、凍結組織から、Qiagen DNeasyキットを製造業者のガイドラインにしたがって使用して、DNA全体を単離した。DNA濃度及び完全性を分光光度法により評価した。単離されたDNAに対する定量PCRを、WPRE遺伝子についてTaqMan UniversalマスターミックスII(Applied Biosystems)と、
順:
及び、逆:
プライマー、並びにプローブ:
を使用して実施した。RNasePを内在性対照(#4403328、ThermoFisher)として使用した。ウイルス産生のために使用したベクターゲノムを含む直線化プラスミドを使用して標準曲線を作成した。サンプルごとのDNAの定量化を、TaqManコピー数基準アッセイを使用して計算し、二倍体核あたりのベクターコピー数(VCN/二倍体核)として表した。
WPRE遺伝子の、順:
及び、逆:
プライマー、並びにプローブ:
を使用してcDNAに対して実施した。ヒトHPRT-1を内在性対照として使用した。ウイルス産生のために使用したベクターゲノムを含む直線化プラスミドを使用して標準曲線を作成した。
定量PCRをAAV9処置霊長類の様々な組織に関して実施した。ウイルスコピー数は、ビヒクル対照と比較して、AAV9-LAMP-2B.v1.2ベクターを1×1013vg/kgで注射した霊長類の心臓、筋肉及び肝臓組織で増加した(図10A)。ベクターゲノムは、左及び右心室並びに左及び右心房を含む、調べたすべての心室で検出された(図10B)。ベクターmRNAは、未処置ビヒクル対照と比較して、処置された霊長類の心臓、骨格筋及び肝臓組織において有意なレベルで検出された(図10C及び図10D)。インサイチュRNA分析は、心臓及び肝臓組織の約25~75%がベクターmRNAを発現することを示した(図10E及び図10F)。これらのデータは、1×1013vg/kgのAAV9最適化LAMP-2B.v1.2を霊長類に全身投与すると、インビボで心臓組織において効率的な形質導入及び発現が得られることを示す。
Claims (19)
- リソソーム関連膜タンパク質2(LAMP-2)のアイソフォーム又はその機能的変異体をコードする導入遺伝子を含む発現カセットを含む遺伝子療法ベクターであって、前記導入遺伝子が配列番号3~5から選択される配列を含む、遺伝子療法ベクター。
- 前記導入遺伝子が、
(a)ヒト宿主細胞における発現のためにコドン最適化されている、
(b)配列番号2よりも少ないCpG部位を含む、
(c)配列番号2よりも少ないクリプティックスプライス部位を含む、かつ/又は
(d)配列番号2よりも少ない代替オープンリーディングフレームを含む、
請求項1に記載の遺伝子療法ベクター。 - 前記発現カセットが、配列番号6を含むコンセンサス最適化Kozak配列、配列番号7を含む完全長ポリA配列、又はそれらの組み合わせを含む、請求項1~2のいずれか一項に記載の遺伝子療法ベクター。
- 前記発現カセットが、5’から3’の方向で、第一の逆方向末端反復、エンハンサ/プロモータ領域、イントロン、コンセンサス最適化Kozak配列、前記導入遺伝子、完全長ポリA配列を含む3’未翻訳領域、及び第二の逆方向末端反復を含む、請求項1~3のいずれか一項に記載の遺伝子療法ベクター。
- 前記エンハンサ/プロモータ領域が、5’から3’の方向で、CMV IEエンハンサとニワトリβアクチンプロモータとを含み、任意選択的に、前記エンハンサ/プロモータ領域が、ニワトリβアクチン遺伝子の第一エクソン及び第一イントロンと、ウサギβグロビン遺伝子のスプライスアクセプタとをさらに含む、請求項4に記載の遺伝子療法ベクター。
- 前記発現カセットが、配列番号8~10から選択される配列に対して少なくとも95%の同一性を共有するか、又は配列番号8~10から選択される配列と同一である、請求項1~5のいずれか一項に記載の遺伝子療法ベクター。
- 前記ベクターが、アデノ随伴ウイルス(AAV)ベクター、任意選択的にAAV9ベクター又はAAVrh.74ベクターである、請求項1~6のいずれか一項に記載の遺伝子療法ベクター。
- 請求項1~7のいずれか一項に記載の遺伝子療法ベクターを含む、医薬組成物。
- それを必要とする対象においてダノン病又は別のオートファジー障害を治療又は防止するための、請求項1~7のいずれか一項に記載の遺伝子療法ベクターを含む医薬組成物であって、任意選択的に、静脈内、動脈内、心臓内、冠動脈内、心筋内、腎内、尿道内、硬膜外、及び筋肉内から選択される経路を介して投与される、医薬組成物。
- 前記オートファジー障害が、末期心不全、心筋梗塞、薬物中毒、糖尿病、末期腎不全、及び老化から選択される、請求項9に記載の医薬組成物。
- アデノ随伴ウイルス(AAV)ベクターを含む、対象においてLAMP-2Bを発現するための医薬組成物であって、
前記AAVベクターが前記対象に対して全身投与されることを特徴とし、
前記AAVベクターが、リソソーム関連膜タンパク質2(LAMP-2)のアイソフォームをコードする導入遺伝子を含む発現カセットを含み、
前記導入遺伝子が配列番号3を含み、
前記導入遺伝子が、エンハンサ/プロモータ領域に機能的に連結され、かつ
前記AAVベクターを前記対象に対して全身投与すると、前記AAVベクターの投与前のLAMP-2Bの発現又は未処置の対照対象におけるLAMP-2Bの発現と比較して、LAMP-2Bの発現が増加する、医薬組成物。 - 前記ベクターが、静脈内投与を介して投与され、任意選択的に、
(a)前記ベクターが、前記対象の全体重1キログラム(vg)あたり、約1×1012~5×1014ベクターゲノム(vg)の前記ベクター(vg/kg)の用量で投与される、
(b)前記ベクターが、約1×1013~5×1014vg/kgの用量で投与される、
(c)前記ベクターが、約5×1013~3×1014vg/kgの用量で投与される、又は
(d)前記ベクターが、約5×1013~1×1014vg/kgの用量で投与される、
請求項9~11のいずれか一項に記載の医薬組成物。 - 前記対象がヒトであり、任意選択的に、
(a)前記対象がダノン病若しくは別のオートファジー障害の症状を示している、
(b)前記対象が、減少しているか若しくは検出不能なLAMP-2発現を有するとして同定されている、かつ/又は
(c)前記対象が変異LAMP-2遺伝子を有するとして同定されている、
請求項9~12のいずれか一項に記載の医薬組成物。 - 前記医薬組成物の投与により、
(a)未処置の対象と比較して、心臓におけるLAMP-2Bポリヌクレオチド及び/若しくはLAMP-2Bタンパク質の発現が増加する、
(b)未処置の対象と比較して、心臓におけるLAMP-2Bポリヌクレオチド及び/若しくはLAMP-2Bタンパク質の発現が、少なくとも約1.2倍、少なくとも約1.3倍、少なくとも約1.4倍、少なくとも約1.5倍、少なくとも約1.6倍、少なくとも約1.7倍、少なくとも約1.8倍、少なくとも約1.9倍、少なくとも約2.0倍、少なくとも約2.2倍、少なくとも約2.3倍、少なくとも約2.4倍、少なくとも約2.5倍、少なくとも約3倍、若しくは少なくとも約4倍増加する、かつ/又は
(c)未処置の対象の肝臓における発現と比較して、肝臓におけるLAMP-2Bポリヌクレオチド及び/若しくはLAMP-2Bタンパク質の発現が、最大で約1.1倍、最大で約1.2倍、最大で約1.3倍、最大で約1.4倍、若しくは最大で約1.5倍増加する、
請求項9~13のいずれか一項に記載の医薬組成物。 - 前記発現カセットが、
(a)5’から3’の方向で、CMV IEエンハンサとニワトリβアクチンプロモータとを含み、任意選択的に、ニワトリβアクチン遺伝子の第一エクソン及び第一イントロンと、ウサギβグロビン遺伝子のスプライスアクセプタとをさらに含む、エンハンサ/プロモータ領域を含む、
(b)配列番号6を含むKozak配列を含む、
(c)配列番号7を含む完全長ポリA配列を含む、
(d)5’から3’の方向で、機能的に連結された、第一の逆方向末端反復、エンハンサ/プロモータ領域、イントロン、コンセンサス最適化Kozak配列、前記導入遺伝子、完全長ポリA配列を含む3’未翻訳領域、及び第二の逆方向末端反復を含み、前記発現カセットが、前記導入遺伝子の開始コドンに対して5’の開始コドンを含まない、
請求項9~14のいずれか一項に記載の医薬組成物。 - リソソーム関連膜タンパク質2(LAMP-2)のアイソフォーム又はその機能的変異体をコードするポリヌクレオチドであって、
(a)配列番号3~5のいずれか一つ、又は
(b)配列番号3
を含むポリヌクレオチド配列を含む、ポリヌクレオチド。 - 請求項16に記載のポリヌクレオチドを含む、発現カセット。
- (a)配列番号22に対して少なくとも90%の同一性、95%の同一性、若しくは100%の同一性を共有するエンハンサ/プロモータ領域、
(b)配列番号23~26から選択される配列に対して少なくとも90%の同一性、95%の同一性、若しくは100%の同一性を共有するエンハンサ/プロモータ領域、
(c)配列番号27に対して少なくとも90%の同一性、95%の同一性、若しくは100%の同一性を共有する3’UTR、
(d)配列番号7に対して少なくとも90%の同一性、95%の同一性、若しくは100%の同一性を共有するポリアデニル化配列、
(e)5’から3’の順で:
(i)配列番号22に対して少なくとも90%の同一性、95%の同一性、若しくは100%の同一性を共有する、エンハンサ/プロモータ領域;
(ii)配列番号3を含む、LAMP-2Bタンパク質をコードするポリヌクレオチド配列;
(iii)配列番号27に対して少なくとも90%の同一性、95%の同一性、若しくは100%の同一性を共有する、3’UTR;及び
(iv)配列番号7に対して少なくとも90%の同一性、95%の同一性、若しくは100%の同一性を共有する、ポリアデニル化配列
を含む、請求項17に記載の発現カセット。 - (i)配列番号11に対して少なくとも90%の同一性、95%の同一性、又は100%の同一性を共有する5’ITRと、
(ii)配列番号12に対して少なくとも90%の同一性、95%の同一性、又は100%の同一性を共有する3’ITRと、
に隣接している請求項17又は18に記載の発現カセットを含む、AAVベクターであって、任意選択的にAAV9カプシド又はAAVrh.74カプシドを含み、任意選択的に、前記AAV9カプシドが、配列番号27のアミノ酸1~736、配列番号27のアミノ酸138~736、及び/又は配列番号27のアミノ酸203~736に対して少なくとも95%の同一性を共有する、AAVベクター。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024114749A JP2024150588A (ja) | 2018-07-12 | 2024-07-18 | ダノン病治療用遺伝子療法ベクター |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201862697302P | 2018-07-12 | 2018-07-12 | |
| US62/697,302 | 2018-07-12 | ||
| PCT/US2019/041465 WO2020014523A1 (en) | 2018-07-12 | 2019-07-11 | Gene therapy vectors for treatment of danon disease |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024114749A Division JP2024150588A (ja) | 2018-07-12 | 2024-07-18 | ダノン病治療用遺伝子療法ベクター |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2021531752A JP2021531752A (ja) | 2021-11-25 |
| JPWO2020014523A5 JPWO2020014523A5 (ja) | 2022-07-14 |
| JP7586810B2 true JP7586810B2 (ja) | 2024-11-19 |
Family
ID=69141704
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021500664A Active JP7586810B2 (ja) | 2018-07-12 | 2019-07-11 | ダノン病治療用遺伝子療法ベクター |
| JP2024114749A Pending JP2024150588A (ja) | 2018-07-12 | 2024-07-18 | ダノン病治療用遺伝子療法ベクター |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024114749A Pending JP2024150588A (ja) | 2018-07-12 | 2024-07-18 | ダノン病治療用遺伝子療法ベクター |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US10703797B2 (ja) |
| EP (1) | EP3820537A4 (ja) |
| JP (2) | JP7586810B2 (ja) |
| KR (1) | KR102918544B1 (ja) |
| CN (1) | CN112512596B (ja) |
| AU (1) | AU2019299970B2 (ja) |
| BR (1) | BR112021000509A2 (ja) |
| CA (1) | CA3106010A1 (ja) |
| IL (1) | IL279918A (ja) |
| MX (1) | MX2021000443A (ja) |
| SG (1) | SG11202100022SA (ja) |
| WO (1) | WO2020014523A1 (ja) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109641063B (zh) | 2016-04-20 | 2022-11-15 | 能源环境和技术研究中心O.A., M.P. | 用于增强pklr的基因表达的组合物和方法 |
| CN111163810B (zh) | 2017-10-16 | 2024-09-10 | 能源环境和技术研究中心O.A.,M.P. | 用于递送pklr以治疗丙酮酸激酶缺乏症的慢病毒载体 |
| SG11202008400SA (en) | 2018-04-11 | 2020-09-29 | Rocket Pharmaceuticals Ltd | Compositions and methods for stem cell transplant |
| CA3096293A1 (en) | 2018-04-27 | 2019-10-31 | Rocket Pharmaceuticals, Ltd. | Gene therapy for cns degeneration |
| KR20210125999A (ko) * | 2019-02-12 | 2021-10-19 | 스페이스크래프트 세븐, 엘엘씨 | 다논병 치료를 위한 유전자 요법 벡터 |
| EP4087489B1 (en) | 2020-01-08 | 2025-05-14 | Vitruvia Holdings Inc. | Methods and computing system for processing ultrasound image to determine health of subdermal tissue |
| WO2022017630A1 (en) * | 2020-07-23 | 2022-01-27 | Ucl Business Ltd | GENE THERAPY VECTOR FOR eEF1A2 AND USES THEREOF |
| WO2022026516A1 (en) * | 2020-07-29 | 2022-02-03 | The Board Of Regents Of The University Of Texas System | Transgene cassettes, aav vectors, and aav viral vectors for expression of human codon-optimized cstb |
| CA3185267A1 (en) | 2020-08-07 | 2022-02-10 | Spacecraft Seven, Llc | Plakophilin-2 (pkp2) gene therapy using aav vector |
| EP4217010A4 (en) * | 2020-09-28 | 2025-01-08 | Tacit Therapeutics, Inc. | TRANS-SPLICING SYSTEM FOR TISSUE-SPECIFIC REPLACEMENT OF RNA SEQUENCES |
| EP4228610A1 (en) * | 2020-10-13 | 2023-08-23 | Kriya Therapeutics, Inc. | Viral vector constructs for delivery of nucleic acids encoding cytokines and uses thereof for treating cancer |
| IL303012A (en) * | 2020-11-20 | 2023-07-01 | Baylor College Medicine | Suppressing hippo signaling in the stem cell niche promotes skeletal muscle regeneration |
| AU2021396150A1 (en) * | 2020-12-07 | 2023-07-06 | Spacecraft Seven, Llc | Treatment of danon disease |
| JP2024523707A (ja) * | 2021-07-08 | 2024-06-28 | テナヤ セラピューティクス, インコーポレイテッド | 遺伝子治療のための最適化された発現カセット |
| KR20240052034A (ko) | 2021-09-03 | 2024-04-22 | 태시트 테라퓨틱스, 인코포레이티드 | 스플라이세오솜 구성요소의 동원을 통한 rna 편집 |
| JP7772920B2 (ja) * | 2021-09-08 | 2025-11-18 | ククムラボ インコーポレーテッド | 生体分子の安定的発現および伝達のためのプラスミドプラットフォーム |
| CN117916379A (zh) * | 2021-09-08 | 2024-04-19 | 株式会社梦想实验室 | 用于生物分子的稳定表达及递送的质粒平台 |
| WO2025217543A1 (en) * | 2024-04-12 | 2025-10-16 | AskBio Inc. | Therapeutic adeno-associated virus using codon optimized nucleic acid encoding lamp2b |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017127565A1 (en) | 2016-01-19 | 2017-07-27 | The Regents Of The University Of California | Methods for the treatment of danon disease and other disorders of autophagy |
Family Cites Families (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5139941A (en) | 1985-10-31 | 1992-08-18 | University Of Florida Research Foundation, Inc. | AAV transduction vectors |
| US4861719A (en) | 1986-04-25 | 1989-08-29 | Fred Hutchinson Cancer Research Center | DNA constructs for retrovirus packaging cell lines |
| US5278056A (en) | 1988-02-05 | 1994-01-11 | The Trustees Of Columbia University In The City Of New York | Retroviral packaging cell lines and process of using same |
| US5670488A (en) | 1992-12-03 | 1997-09-23 | Genzyme Corporation | Adenovirus vector for gene therapy |
| WO1992001070A1 (en) | 1990-07-09 | 1992-01-23 | The United States Of America, As Represented By The Secretary, U.S. Department Of Commerce | High efficiency packaging of mutant adeno-associated virus using amber suppressions |
| US5173414A (en) | 1990-10-30 | 1992-12-22 | Applied Immune Sciences, Inc. | Production of recombinant adeno-associated virus vectors |
| AU663725B2 (en) | 1991-08-20 | 1995-10-19 | United States Of America, Represented By The Secretary, Department Of Health And Human Services, The | Adenovirus mediated transfer of genes to the gastrointestinal tract |
| CA2156725A1 (en) | 1993-02-22 | 1994-09-01 | Warren S. Pear | Production of high titer helper-free retroviruses by transient transfection |
| FR2712812B1 (fr) | 1993-11-23 | 1996-02-09 | Centre Nat Rech Scient | Composition pour la production de produits thérapeutiques in vivo. |
| IL116816A (en) | 1995-01-20 | 2003-05-29 | Rhone Poulenc Rorer Sa | Cell for the production of a defective recombinant adenovirus or an adeno-associated virus and the various uses thereof |
| US6013516A (en) | 1995-10-06 | 2000-01-11 | The Salk Institute For Biological Studies | Vector and method of use for nucleic acid delivery to non-dividing cells |
| US6004797A (en) | 1995-11-09 | 1999-12-21 | Avigen, Inc. | Adenovirus helper-free recombinant AAV Virion production |
| US6346415B1 (en) | 1997-10-21 | 2002-02-12 | Targeted Genetics Corporation | Transcriptionally-activated AAV inverted terminal repeats (ITRS) for use with recombinant AAV vectors |
| US5994136A (en) | 1997-12-12 | 1999-11-30 | Cell Genesys, Inc. | Method and means for producing high titer, safe, recombinant lentivirus vectors |
| US20020065236A1 (en) * | 1998-09-09 | 2002-05-30 | Yew Nelson S. | CpG reduced plasmids and viral vectors |
| CN103555677B (zh) | 2001-11-13 | 2018-01-30 | 宾夕法尼亚大学托管会 | 检测和/或鉴定腺伴随病毒(aav)序列以及分离所鉴定的新型序列的方法 |
| WO2003052051A2 (en) | 2001-12-17 | 2003-06-26 | The Trustees Of The University Of Pennsylvania | Adeno-associated virus (aav) serotype 8 sequences |
| US7858367B2 (en) | 2002-04-30 | 2010-12-28 | Duke University | Viral vectors and methods for producing and using the same |
| AU2003274397A1 (en) | 2002-06-05 | 2003-12-22 | University Of Florida | Production of pseudotyped recombinant aav virions |
| EP1529105B1 (en) | 2002-08-12 | 2012-10-03 | Société de commercialisation des produits de la recherche appliquée SOCPRA Sciences Santé et Humaines s.e.c. | Methods to reprogram splice site selection in pre-messenger rnas |
| AU2003295881A1 (en) * | 2002-11-25 | 2004-06-18 | Exelixis, Inc. | Lamps as modifiers of the p53 pathway and methods of use |
| DK3211085T3 (da) | 2003-09-30 | 2021-06-21 | Univ Pennsylvania | Klader af adeno-associeret virus (aav), sekvenser, vektorer indeholdende disse og anvendelser deraf |
| EP1981546B1 (en) | 2006-02-06 | 2014-06-04 | The Medical Research and Infrastructure Fund of the Tel-Aviv Sourasky Medical Center | Enzyme replacement therapy for treating lysosomal storage diseases |
| US7588772B2 (en) | 2006-03-30 | 2009-09-15 | Board Of Trustees Of The Leland Stamford Junior University | AAV capsid library and AAV capsid proteins |
| US8324367B2 (en) | 2006-11-03 | 2012-12-04 | Medtronic, Inc. | Compositions and methods for making therapies delivered by viral vectors reversible for safety and allele-specificity |
| PT3252161T (pt) | 2007-06-06 | 2022-02-01 | Genzyme Corp | Terapia genética para doenças do armazenamento lisossomal |
| US9169494B2 (en) | 2010-01-12 | 2015-10-27 | The University Of North Carolina At Chapel Hill | Restrictive inverted terminal repeats for viral vectors |
| EP2571530A4 (en) * | 2010-05-20 | 2014-03-05 | Univ Rochester | METHOD AND COMPOSITIONS FOR AUTOPHAGIA MODULATION |
| US9434928B2 (en) | 2011-11-23 | 2016-09-06 | Nationwide Children's Hospital, Inc. | Recombinant adeno-associated virus delivery of alpha-sarcoglycan polynucleotides |
| US10648001B2 (en) * | 2012-07-11 | 2020-05-12 | Sangamo Therapeutics, Inc. | Method of treating mucopolysaccharidosis type I or II |
| HUE051612T2 (hu) | 2012-07-11 | 2021-03-01 | Sangamo Therapeutics Inc | Eljárások és készítmények lizoszomális tárolási betegségek kezelésére |
| CN104936606A (zh) | 2012-10-17 | 2015-09-23 | 泰莱托恩基金会 | 糖原贮积病的基因疗法 |
| WO2015196179A1 (en) | 2014-06-20 | 2015-12-23 | University Of Florida Research Foundation, Inc. | Methods of packaging multiple adeno-associated virus vectors |
| US11535665B2 (en) * | 2015-05-13 | 2022-12-27 | The Trustees Of The University Of Pennsylvania | AAV-mediated expression of anti-influenza antibodies and methods of use thereof |
| CN110536966A (zh) * | 2016-09-08 | 2019-12-03 | 能源环境和技术研究中心O.A.,M.P. | 用于范可尼贫血患者的基因疗法 |
| JP7059285B2 (ja) * | 2016-09-30 | 2022-04-25 | エステベ プアルマセウティカルス, エッセ.ア. | ムコ多糖症の治療のためのアデノ随伴ウイルスベクター |
| AU2018236353B2 (en) | 2017-03-15 | 2023-12-21 | The Regents Of The University Of California | Methods of treating lysosomal disorders |
| KR20210125999A (ko) * | 2019-02-12 | 2021-10-19 | 스페이스크래프트 세븐, 엘엘씨 | 다논병 치료를 위한 유전자 요법 벡터 |
-
2019
- 2019-07-11 CN CN201980049274.0A patent/CN112512596B/zh active Active
- 2019-07-11 CA CA3106010A patent/CA3106010A1/en active Pending
- 2019-07-11 JP JP2021500664A patent/JP7586810B2/ja active Active
- 2019-07-11 BR BR112021000509-9A patent/BR112021000509A2/pt unknown
- 2019-07-11 WO PCT/US2019/041465 patent/WO2020014523A1/en not_active Ceased
- 2019-07-11 SG SG11202100022SA patent/SG11202100022SA/en unknown
- 2019-07-11 KR KR1020217003946A patent/KR102918544B1/ko active Active
- 2019-07-11 MX MX2021000443A patent/MX2021000443A/es unknown
- 2019-07-11 EP EP19835189.2A patent/EP3820537A4/en active Pending
- 2019-07-11 AU AU2019299970A patent/AU2019299970B2/en active Active
- 2019-12-27 US US16/729,002 patent/US10703797B2/en active Active
-
2021
- 2021-01-03 IL IL279918A patent/IL279918A/en unknown
- 2021-01-08 US US17/144,933 patent/US20210381003A1/en not_active Abandoned
-
2024
- 2024-07-18 JP JP2024114749A patent/JP2024150588A/ja active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017127565A1 (en) | 2016-01-19 | 2017-07-27 | The Regents Of The University Of California | Methods for the treatment of danon disease and other disorders of autophagy |
Also Published As
| Publication number | Publication date |
|---|---|
| SG11202100022SA (en) | 2021-01-28 |
| IL279918A (en) | 2021-03-01 |
| KR20210030965A (ko) | 2021-03-18 |
| EP3820537A1 (en) | 2021-05-19 |
| JP2021531752A (ja) | 2021-11-25 |
| US20210381003A1 (en) | 2021-12-09 |
| EP3820537A4 (en) | 2022-04-13 |
| AU2019299970B2 (en) | 2025-12-11 |
| CA3106010A1 (en) | 2020-01-16 |
| WO2020014523A1 (en) | 2020-01-16 |
| BR112021000509A2 (pt) | 2021-04-06 |
| JP2024150588A (ja) | 2024-10-23 |
| AU2019299970A1 (en) | 2021-01-28 |
| US10703797B2 (en) | 2020-07-07 |
| CN112512596A (zh) | 2021-03-16 |
| KR102918544B1 (ko) | 2026-01-27 |
| US20200148745A1 (en) | 2020-05-14 |
| CN112512596B (zh) | 2025-12-12 |
| MX2021000443A (es) | 2021-05-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7586810B2 (ja) | ダノン病治療用遺伝子療法ベクター | |
| JP7807825B2 (ja) | 医薬組成物 | |
| US20220143215A1 (en) | Gene therapy vectors for treatment of danon disease | |
| JP7623299B2 (ja) | 乳児性悪性大理石骨病に対する遺伝子療法ベクター | |
| RU2808459C2 (ru) | Геннотерапевтические векторы для лечения болезни данона | |
| JP2026050416A (ja) | ダノン病およびオートファジーの他の障害の治療のための方法 | |
| RU2777571C2 (ru) | Способы лечения болезни данона и других нарушений аутофагии | |
| CA3011731C (en) | Methods for the treatment of danon disease and other disorders of autophagy | |
| HK40096493A (zh) | Danon病和其它自噬障碍的治疗方法 | |
| BR112018014633B1 (pt) | Vetor de terapia gênica e usos de vetores | |
| HK40000046B (en) | Methods for the treatment of danon disease and other disorders of autophagy | |
| HK40000046A (en) | Methods for the treatment of danon disease and other disorders of autophagy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220706 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220706 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20230704 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230814 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20231110 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240214 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20240319 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240718 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20240726 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241010 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241107 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7586810 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S111 | Request for change of ownership or part of ownership |
Free format text: JAPANESE INTERMEDIATE CODE: R313113 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |