JP7399514B2 - 分離装置、検出装置、保存装置及びセンサ - Google Patents
分離装置、検出装置、保存装置及びセンサ Download PDFInfo
- Publication number
- JP7399514B2 JP7399514B2 JP2022502621A JP2022502621A JP7399514B2 JP 7399514 B2 JP7399514 B2 JP 7399514B2 JP 2022502621 A JP2022502621 A JP 2022502621A JP 2022502621 A JP2022502621 A JP 2022502621A JP 7399514 B2 JP7399514 B2 JP 7399514B2
- Authority
- JP
- Japan
- Prior art keywords
- hydrophilic
- plasma
- serum
- separation filter
- separation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000926 separation method Methods 0.000 title claims description 330
- 238000001514 detection method Methods 0.000 title claims description 48
- 210000002966 serum Anatomy 0.000 claims description 206
- 239000000463 material Substances 0.000 claims description 199
- 238000006243 chemical reaction Methods 0.000 claims description 165
- 239000007788 liquid Substances 0.000 claims description 110
- 239000000126 substance Substances 0.000 claims description 71
- 238000002347 injection Methods 0.000 claims description 63
- 239000007924 injection Substances 0.000 claims description 63
- 239000002250 absorbent Substances 0.000 claims description 33
- 230000002745 absorbent Effects 0.000 claims description 33
- 238000011084 recovery Methods 0.000 claims description 22
- 239000011148 porous material Substances 0.000 claims description 21
- 230000002209 hydrophobic effect Effects 0.000 claims description 19
- 238000005259 measurement Methods 0.000 claims description 16
- 239000012510 hollow fiber Substances 0.000 claims description 14
- 239000002689 soil Substances 0.000 claims description 14
- 239000000243 solution Substances 0.000 claims description 11
- 210000000078 claw Anatomy 0.000 claims description 8
- 238000001125 extrusion Methods 0.000 claims description 6
- 210000002381 plasma Anatomy 0.000 description 193
- 210000004369 blood Anatomy 0.000 description 75
- 239000008280 blood Substances 0.000 description 75
- 238000000034 method Methods 0.000 description 44
- 238000010586 diagram Methods 0.000 description 41
- 150000007523 nucleic acids Chemical class 0.000 description 15
- 239000003153 chemical reaction reagent Substances 0.000 description 13
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 12
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 12
- 108020004707 nucleic acids Proteins 0.000 description 12
- 102000039446 nucleic acids Human genes 0.000 description 12
- 239000012528 membrane Substances 0.000 description 11
- 229910052751 metal Inorganic materials 0.000 description 11
- 239000002184 metal Substances 0.000 description 11
- 239000000872 buffer Substances 0.000 description 9
- 238000004040 coloring Methods 0.000 description 9
- 239000004033 plastic Substances 0.000 description 9
- 229920003023 plastic Polymers 0.000 description 9
- 238000004321 preservation Methods 0.000 description 9
- 125000006850 spacer group Chemical group 0.000 description 9
- 238000003780 insertion Methods 0.000 description 8
- 230000037431 insertion Effects 0.000 description 8
- -1 abixaban Chemical compound 0.000 description 7
- 239000003146 anticoagulant agent Substances 0.000 description 7
- 229940127219 anticoagulant drug Drugs 0.000 description 7
- 239000000427 antigen Substances 0.000 description 7
- 102000036639 antigens Human genes 0.000 description 7
- 108091007433 antigens Proteins 0.000 description 7
- 239000012620 biological material Substances 0.000 description 7
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- 108091028043 Nucleic acid sequence Proteins 0.000 description 6
- LSNNMFCWUKXFEE-UHFFFAOYSA-N Sulfurous acid Chemical compound OS(O)=O LSNNMFCWUKXFEE-UHFFFAOYSA-N 0.000 description 6
- 229940088598 enzyme Drugs 0.000 description 6
- 238000010438 heat treatment Methods 0.000 description 6
- 230000003287 optical effect Effects 0.000 description 6
- 238000003752 polymerase chain reaction Methods 0.000 description 6
- 239000002904 solvent Substances 0.000 description 6
- 239000010457 zeolite Substances 0.000 description 6
- 108010049003 Fibrinogen Proteins 0.000 description 5
- 102000008946 Fibrinogen Human genes 0.000 description 5
- 230000005540 biological transmission Effects 0.000 description 5
- 230000017531 blood circulation Effects 0.000 description 5
- 229940012952 fibrinogen Drugs 0.000 description 5
- 239000000376 reactant Substances 0.000 description 5
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 4
- 102100034343 Integrase Human genes 0.000 description 4
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 4
- 229910021536 Zeolite Inorganic materials 0.000 description 4
- 230000003321 amplification Effects 0.000 description 4
- 239000012491 analyte Substances 0.000 description 4
- 238000003776 cleavage reaction Methods 0.000 description 4
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 4
- 239000011521 glass Substances 0.000 description 4
- 238000003199 nucleic acid amplification method Methods 0.000 description 4
- 239000002245 particle Substances 0.000 description 4
- 229920000728 polyester Polymers 0.000 description 4
- 229920001223 polyethylene glycol Polymers 0.000 description 4
- 210000003296 saliva Anatomy 0.000 description 4
- 230000007017 scission Effects 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 108091033409 CRISPR Proteins 0.000 description 3
- 229920000742 Cotton Polymers 0.000 description 3
- 108010053770 Deoxyribonucleases Proteins 0.000 description 3
- 102000016911 Deoxyribonucleases Human genes 0.000 description 3
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 3
- 229920001046 Nanocellulose Polymers 0.000 description 3
- 239000000020 Nitrocellulose Substances 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- 102000006382 Ribonucleases Human genes 0.000 description 3
- 108010083644 Ribonucleases Proteins 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- 229930006000 Sucrose Natural products 0.000 description 3
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 3
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 3
- 241000700605 Viruses Species 0.000 description 3
- 210000004027 cell Anatomy 0.000 description 3
- 210000003608 fece Anatomy 0.000 description 3
- 239000000835 fiber Substances 0.000 description 3
- 238000000691 measurement method Methods 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 239000000178 monomer Substances 0.000 description 3
- 229920001220 nitrocellulos Polymers 0.000 description 3
- 239000012466 permeate Substances 0.000 description 3
- 239000003761 preservation solution Substances 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 239000008107 starch Substances 0.000 description 3
- 239000005720 sucrose Substances 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- OGIDPMRJRNCKJF-UHFFFAOYSA-N titanium oxide Inorganic materials [Ti]=O OGIDPMRJRNCKJF-UHFFFAOYSA-N 0.000 description 3
- HDTRYLNUVZCQOY-UHFFFAOYSA-N α-D-glucopyranosyl-α-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OC1C(O)C(O)C(O)C(CO)O1 HDTRYLNUVZCQOY-UHFFFAOYSA-N 0.000 description 2
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 2
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 2
- 230000005653 Brownian motion process Effects 0.000 description 2
- 102000008186 Collagen Human genes 0.000 description 2
- 108010035532 Collagen Proteins 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 108010015776 Glucose oxidase Proteins 0.000 description 2
- 239000004366 Glucose oxidase Substances 0.000 description 2
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 2
- 102000003992 Peroxidases Human genes 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 229920001486 SU-8 photoresist Polymers 0.000 description 2
- HDTRYLNUVZCQOY-WSWWMNSNSA-N Trehalose Natural products O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-WSWWMNSNSA-N 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- HDTRYLNUVZCQOY-LIZSDCNHSA-N alpha,alpha-trehalose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 HDTRYLNUVZCQOY-LIZSDCNHSA-N 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 2
- 230000023555 blood coagulation Effects 0.000 description 2
- 238000005537 brownian motion Methods 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 229920001436 collagen Polymers 0.000 description 2
- 239000002299 complementary DNA Substances 0.000 description 2
- 150000004696 coordination complex Chemical class 0.000 description 2
- 238000002484 cyclic voltammetry Methods 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 239000000428 dust Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 239000010419 fine particle Substances 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 229940116332 glucose oxidase Drugs 0.000 description 2
- 235000019420 glucose oxidase Nutrition 0.000 description 2
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 2
- 229910052737 gold Inorganic materials 0.000 description 2
- 239000010931 gold Substances 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- 239000008363 phosphate buffer Substances 0.000 description 2
- 239000002953 phosphate buffered saline Substances 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 229920000139 polyethylene terephthalate Polymers 0.000 description 2
- 239000005020 polyethylene terephthalate Substances 0.000 description 2
- 229920001721 polyimide Polymers 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 229920002635 polyurethane Polymers 0.000 description 2
- 239000004814 polyurethane Substances 0.000 description 2
- JLKDVMWYMMLWTI-UHFFFAOYSA-M potassium iodate Chemical compound [K+].[O-]I(=O)=O JLKDVMWYMMLWTI-UHFFFAOYSA-M 0.000 description 2
- 239000001230 potassium iodate Substances 0.000 description 2
- 235000006666 potassium iodate Nutrition 0.000 description 2
- 229940093930 potassium iodate Drugs 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 239000001509 sodium citrate Substances 0.000 description 2
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 2
- PUZPDOWCWNUUKD-UHFFFAOYSA-M sodium fluoride Chemical compound [F-].[Na+] PUZPDOWCWNUUKD-UHFFFAOYSA-M 0.000 description 2
- 239000001488 sodium phosphate Substances 0.000 description 2
- 229910000162 sodium phosphate Inorganic materials 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 210000004243 sweat Anatomy 0.000 description 2
- 229920003002 synthetic resin Polymers 0.000 description 2
- 239000000057 synthetic resin Substances 0.000 description 2
- 210000001138 tear Anatomy 0.000 description 2
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- PSBDWGZCVUAZQS-UHFFFAOYSA-N (dimethylsulfonio)acetate Chemical compound C[S+](C)CC([O-])=O PSBDWGZCVUAZQS-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N 2-Propenoic acid Natural products OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- GHCZTIFQWKKGSB-UHFFFAOYSA-N 2-hydroxypropane-1,2,3-tricarboxylic acid;phosphoric acid Chemical compound OP(O)(O)=O.OC(=O)CC(O)(C(O)=O)CC(O)=O GHCZTIFQWKKGSB-UHFFFAOYSA-N 0.000 description 1
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- 229940122295 Clotting factor inhibitor Drugs 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- HGVDHZBSSITLCT-JLJPHGGASA-N Edoxaban Chemical compound N([C@H]1CC[C@@H](C[C@H]1NC(=O)C=1SC=2CN(C)CCC=2N=1)C(=O)N(C)C)C(=O)C(=O)NC1=CC=C(Cl)C=N1 HGVDHZBSSITLCT-JLJPHGGASA-N 0.000 description 1
- 102000002494 Endoribonucleases Human genes 0.000 description 1
- 108010093099 Endoribonucleases Proteins 0.000 description 1
- 102000004678 Exoribonucleases Human genes 0.000 description 1
- 108010002700 Exoribonucleases Proteins 0.000 description 1
- 108020005004 Guide RNA Proteins 0.000 description 1
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 1
- 108700011259 MicroRNAs Proteins 0.000 description 1
- 102000015728 Mucins Human genes 0.000 description 1
- 108010063954 Mucins Proteins 0.000 description 1
- CNCOEDDPFOAUMB-UHFFFAOYSA-N N-Methylolacrylamide Chemical compound OCNC(=O)C=C CNCOEDDPFOAUMB-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 108010001014 Plasminogen Activators Proteins 0.000 description 1
- 102000001938 Plasminogen Activators Human genes 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 229920001328 Polyvinylidene chloride Polymers 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- 229940122388 Thrombin inhibitor Drugs 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 239000004699 Ultra-high molecular weight polyethylene Substances 0.000 description 1
- 229940127508 Vitamin K Inhibitors Drugs 0.000 description 1
- URLYGBGJPQYXBN-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methyl prop-2-enoate Chemical compound OCC1CCC(COC(=O)C=C)CC1 URLYGBGJPQYXBN-UHFFFAOYSA-N 0.000 description 1
- VABCILAOYCMVPS-UHFFFAOYSA-N acenocoumarol Chemical compound OC=1C2=CC=CC=C2OC(=O)C=1C(CC(=O)C)C1=CC=C([N+]([O-])=O)C=C1 VABCILAOYCMVPS-UHFFFAOYSA-N 0.000 description 1
- 229960002054 acenocoumarol Drugs 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000002390 adhesive tape Substances 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 239000003698 antivitamin K Substances 0.000 description 1
- 229910052586 apatite Inorganic materials 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- KXNPVXPOPUZYGB-XYVMCAHJSA-N argatroban Chemical compound OC(=O)[C@H]1C[C@H](C)CCN1C(=O)[C@H](CCCN=C(N)N)NS(=O)(=O)C1=CC=CC2=C1NC[C@H](C)C2 KXNPVXPOPUZYGB-XYVMCAHJSA-N 0.000 description 1
- 229960003856 argatroban Drugs 0.000 description 1
- 230000003592 biomimetic effect Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 230000001112 coagulating effect Effects 0.000 description 1
- 230000015271 coagulation Effects 0.000 description 1
- 238000005345 coagulation Methods 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 150000004775 coumarins Chemical class 0.000 description 1
- 229960003850 dabigatran Drugs 0.000 description 1
- YBSJFWOBGCMAKL-UHFFFAOYSA-N dabigatran Chemical compound N=1C2=CC(C(=O)N(CCC(O)=O)C=3N=CC=CC=3)=CC=C2N(C)C=1CNC1=CC=C(C(N)=N)C=C1 YBSJFWOBGCMAKL-UHFFFAOYSA-N 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 235000013325 dietary fiber Nutrition 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 238000012674 dispersion polymerization Methods 0.000 description 1
- 229960000622 edoxaban Drugs 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 238000005530 etching Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 210000001808 exosome Anatomy 0.000 description 1
- KANJSNBRCNMZMV-ABRZTLGGSA-N fondaparinux Chemical compound O[C@@H]1[C@@H](NS(O)(=O)=O)[C@@H](OC)O[C@H](COS(O)(=O)=O)[C@H]1O[C@H]1[C@H](OS(O)(=O)=O)[C@@H](O)[C@H](O[C@@H]2[C@@H]([C@@H](OS(O)(=O)=O)[C@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O[C@@H]4[C@@H]([C@@H](O)[C@H](O)[C@@H](COS(O)(=O)=O)O4)NS(O)(=O)=O)[C@H](O3)C(O)=O)O)[C@@H](COS(O)(=O)=O)O2)NS(O)(=O)=O)[C@H](C(O)=O)O1 KANJSNBRCNMZMV-ABRZTLGGSA-N 0.000 description 1
- 229960001318 fondaparinux Drugs 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 108010046301 glucose peroxidase Proteins 0.000 description 1
- RBTKNAXYKSUFRK-UHFFFAOYSA-N heliogen blue Chemical compound [Cu].[N-]1C2=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=NC([N-]1)=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=N2 RBTKNAXYKSUFRK-UHFFFAOYSA-N 0.000 description 1
- ZFGMDIBRIDKWMY-PASTXAENSA-N heparin Chemical compound CC(O)=N[C@@H]1[C@@H](O)[C@H](O)[C@@H](COS(O)(=O)=O)O[C@@H]1O[C@@H]1[C@@H](C(O)=O)O[C@@H](O[C@H]2[C@@H]([C@@H](OS(O)(=O)=O)[C@@H](O[C@@H]3[C@@H](OC(O)[C@H](OS(O)(=O)=O)[C@H]3O)C(O)=O)O[C@@H]2O)CS(O)(=O)=O)[C@H](O)[C@H]1O ZFGMDIBRIDKWMY-PASTXAENSA-N 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 229960001008 heparin sodium Drugs 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 239000010954 inorganic particle Substances 0.000 description 1
- 239000000138 intercalating agent Substances 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 239000002082 metal nanoparticle Substances 0.000 description 1
- 239000002679 microRNA Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- 238000010979 pH adjustment Methods 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- VSIIXMUUUJUKCM-UHFFFAOYSA-D pentacalcium;fluoride;triphosphate Chemical compound [F-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O VSIIXMUUUJUKCM-UHFFFAOYSA-D 0.000 description 1
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical compound [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- NFBAXHOPROOJAW-UHFFFAOYSA-N phenindione Chemical compound O=C1C2=CC=CC=C2C(=O)C1C1=CC=CC=C1 NFBAXHOPROOJAW-UHFFFAOYSA-N 0.000 description 1
- 229960000280 phenindione Drugs 0.000 description 1
- 238000009832 plasma treatment Methods 0.000 description 1
- 229940127126 plasminogen activator Drugs 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 239000005033 polyvinylidene chloride Substances 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 239000011535 reaction buffer Substances 0.000 description 1
- 239000005871 repellent Substances 0.000 description 1
- 239000003161 ribonuclease inhibitor Substances 0.000 description 1
- 229960001148 rivaroxaban Drugs 0.000 description 1
- KGFYHTZWPPHNLQ-AWEZNQCLSA-N rivaroxaban Chemical compound S1C(Cl)=CC=C1C(=O)NC[C@@H]1OC(=O)N(C=2C=CC(=CC=2)N2C(COCC2)=O)C1 KGFYHTZWPPHNLQ-AWEZNQCLSA-N 0.000 description 1
- 239000004576 sand Substances 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 239000011775 sodium fluoride Substances 0.000 description 1
- 235000013024 sodium fluoride Nutrition 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 229940117986 sulfobetaine Drugs 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 239000003868 thrombin inhibitor Substances 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229920000785 ultra high molecular weight polyethylene Polymers 0.000 description 1
- 210000002700 urine Anatomy 0.000 description 1
- PJVWKTKQMONHTI-UHFFFAOYSA-N warfarin Chemical compound OC=1C2=CC=CC=C2OC(=O)C=1C(CC(=O)C)C1=CC=CC=C1 PJVWKTKQMONHTI-UHFFFAOYSA-N 0.000 description 1
- 229960005080 warfarin Drugs 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N1/00—Sampling; Preparing specimens for investigation
- G01N1/02—Devices for withdrawing samples
- G01N1/10—Devices for withdrawing samples in the liquid or fluent state
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/52—Use of compounds or compositions for colorimetric, spectrophotometric or fluorometric investigation, e.g. use of reagent paper and including single- and multilayer analytical elements
Description
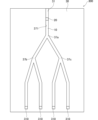
図1を参照して、実施形態における分離装置1の第1例について説明する。図1は、実施形態における分離装置1の第1例を示す斜視図である。図2は、実施形態における分離装置1の第1例を示す側面図である。また、各図において、共通する部分については、共通する参照符号を付し、重複する説明は適宜省略する。
図19を参照して、実施形態における検出装置100の第1例について説明する。図19は、実施形態における検出装置100の第1例を示す図である。
図21を参照して、実施形態における保存装置200の第1例について説明する。図21は、実施形態における保存装置200の第1例を示す図である。
図25を参照して、実施形態におけるセンサ300の第1例について説明する。図25は、実施形態におけるセンサ300の第1例を示す図である。
10 :親水部
11 :第1主面
12 :第2主面
13 :端面
14 :溝
14a :底面
14b :側面
15 :収集部
16 :嵌合部
16a :拡径部
16b :開口部
20 :分離用フィルタ
21 :第1主面
22 :第2主面
23 :端面
25 :吸収材
30 :基材
30a :内面
31 :注入口
32 :回収口
34 :鉤爪部
36 :弁部
37 :流路
391 :上壁
392 :下壁
393 :第1側壁
394 :第2側壁
40 :疎水部
50 :吸引部
51 :透過フィルタ
59 :容器
60 :送気部
61 :透過フィルタ
70 :蓋部
71 :押出機構
80 :スペーサー
90 :支持部材
91 :突起部
92 :挟持部
100 :検出装置
110 :検出部
120 :浸透層
130 :反射防止層
140 :反応層
150 :透明層
200 :保存装置
210 :収容器
220 :挿入部
230 :保存液
240 :温度センサ
250 :温度制御部
260 :バッテリー
300 :センサ
310 :測定部
320 :反応部
330 :変換部
340 :制御電極
350 :温度制御部
8 :保管容器
9 :回収装置
93 :先端部
Claims (17)
- 生体又は土壌から採取される採取物を含む液体状の検体から少なくとも血清または血漿を分離するための分離装置であって、
親水性材料で構成される親水部と、
前記親水部の一部の領域に設けられるとともに、中空糸又は多孔質材料で構成される分離用フィルタと、
前記分離用フィルタを前記親水部に支持する支持部材と、を備え、
前記支持部材は、前記分離用フィルタに挿通する複数の突起部を有すること
を特徴とする分離装置。 - 前記親水部は、板状に形成され、前記分離用フィルタから離間する方向に向けて下方に傾斜されて形成されること
を特徴とする請求項1記載の分離装置。 - 前記親水部は、前記分離用フィルタから離間する方向に向けて延びる溝が形成されること
を特徴とする請求項1記載の分離装置。 - 前記親水部は、親水性フィルムからなること
を特徴とする請求項1記載の分離装置。 - 前記親水部は、分離した血清又は血漿を収集するための収集部を有すること
を特徴とする請求項1記載の分離装置。 - 前記親水部は、分離した血清又は血漿を回収する回収装置を嵌合するための嵌合部を有すること
を特徴とする請求項1記載の分離装置。 - 筒状に形成される基材を更に備え、
前記基材は、一方側の端部に形成される注入口と、前記注入口とは反対側に形成される回収口と、を有し、
前記親水部は、前記基材の内面に設けられ、
前記分離用フィルタは、前記回収口から離間して前記基材の内部に配置されること
を特徴とする請求項1記載の分離装置。 - 前記回収口側の前記基材の内面の端部に疎水性材料で構成される疎水部を更に備えること
を特徴とする請求項7記載の分離装置。 - 前記回収口側から前記基材の内部の空気を吸引するための吸引部を更に備えること
を特徴とする請求項7記載の分離装置。 - 前記注入口側から前記基材の内部に空気を送る送気部を更に備えること
を特徴とする請求項7記載の分離装置。 - 開口された注入口を有するとともに、前記分離用フィルタが設けられる基材と、
前記注入口に設けられる蓋部と、を備え、
前記基材は、前記注入口に嵌め込まれるとともに液体状の検体を吸収するための吸収材と、前記吸収材と前記分離用フィルタとの間に設けられる鉤爪部と、を有し、
前記蓋部は、前記吸収材を前記基材の内部に押し出すための押出機構を有すること
を特徴とする請求項1記載の分離装置。 - 生体物質を検出するための検出装置であって、
生体又は土壌から採取される採取物を含む液体状の検体から血清又は血漿を分離するための分離装置と、前記分離装置から分離した血清又は血漿から生体物質を検出する検出部とを備え、
前記分離装置は、
親水性材料で構成される親水部と、
前記親水部の一部の領域に設けられるとともに、中空糸又は多孔質材料で構成される分離用フィルタと、
前記分離用フィルタを前記親水部に支持する支持部材と、を有し、
前記支持部材は、前記分離用フィルタに挿通する複数の突起部を有し、
前記検出部は、
前記親水部に設けられる、分離した血清又は血漿を浸透させるための浸透層と、
前記浸透層を挟んで前記親水部とは反対側に設けられる、分離した血清又は血漿と発色反応させるための反応層と、を有すること
を特徴とする検出装置。 - 前記検出部は、前記反応層を挟んで前記浸透層の反対側に設けられる、透明性フィルムで構成される透明層を有すること
を特徴とする請求項12記載の検出装置。 - 前記親水部は、前記分離用フィルタが設けられる第1主面と、前記第1主面とは反対側の第2主面とを有し、
前記反応層は、前記親水部の前記第1主面側に配置されること
を特徴とする請求項12記載の検出装置。 - 前記親水部は、前記分離用フィルタが設けられる第1主面と、前記第1主面とは反対側の第2主面とを有し、
前記反応層は、前記親水部の前記第2主面側に配置されること
を特徴とする請求項12記載の検出装置。 - 血清又は血漿を保存するための保存装置であって、
生体又は土壌から採取される採取物を含む液体状の検体から血清又は血漿を分離するための分離装置と、前記分離装置を収容可能な収容器とを備え、
前記分離装置は、
親水性材料で構成される親水部と、
前記親水部の一部の領域に設けられるとともに、中空糸又は多孔質材料で構成される分離用フィルタと、
前記分離用フィルタを前記親水部に支持する支持部材と、を有し、
前記支持部材は、前記分離用フィルタに挿通する複数の突起部を有し、
前記収容器は、分離した血清又は血漿を保存するための保存液が収容されること
を特徴とする保存装置。 - 生体物質を測定するためのセンサであって、
生体又は土壌から採取される採取物を含む液体状の検体から血清又は血漿を分離するための分離装置と、前記分離装置により分離した血清又は血漿から生体物質を測定する測定部とを備え、
前記分離装置は、
親水性材料で構成される親水部と、
前記親水部の一部の領域に設けられるとともに、中空糸又は多孔質材料で構成される分離用フィルタと、
前記分離用フィルタを前記親水部に支持する支持部材と、を有し、
前記支持部材は、前記分離用フィルタに挿通する複数の突起部を有し、
前記測定部は、分離した血清又は血漿と化学反応させるための反応部と、血清又は血漿と前記反応部との化学反応に基づいて発生する電子又は光を信号に変換する変換部と、有すること
を特徴とするセンサ。
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2020/007516 WO2021171378A1 (ja) | 2020-02-25 | 2020-02-25 | 分離装置、検出装置、保存装置及びセンサ |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JPWO2021171378A1 JPWO2021171378A1 (ja) | 2021-09-02 |
| JPWO2021171378A5 JPWO2021171378A5 (ja) | 2023-02-03 |
| JP7399514B2 true JP7399514B2 (ja) | 2023-12-18 |
Family
ID=77489985
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022502621A Active JP7399514B2 (ja) | 2020-02-25 | 2020-02-25 | 分離装置、検出装置、保存装置及びセンサ |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP7399514B2 (ja) |
| WO (1) | WO2021171378A1 (ja) |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5916521A (en) | 1995-01-04 | 1999-06-29 | Spectral Diagnostics, Inc. | Lateral flow filter devices for separation of body fluids from particulate materials |
| JP2000502451A (ja) | 1995-12-22 | 2000-02-29 | ユニバーサル ヘルスウォッチ,インコーポレーテッド | 血漿分離をもたらす診断分析 |
| JP2003135435A (ja) | 2001-08-22 | 2003-05-13 | Kyowa Medex Co Ltd | 採血用具、これを用いた定量用溶液調製方法、定量用溶液調製器具及びその使用方法並びに定量用溶液を用いた定量方法 |
| JP2003194806A (ja) | 2001-12-27 | 2003-07-09 | Minolta Co Ltd | 血球分離用チップ |
| JP2003254934A (ja) | 2002-03-01 | 2003-09-10 | Matsushita Electric Ind Co Ltd | バイオセンサ |
| JP2011133235A (ja) | 2009-12-22 | 2011-07-07 | Physical Screening Inc | 検査対象液保存器具 |
| JP2012529039A (ja) | 2009-06-04 | 2012-11-15 | インフォピア カンパニー,リミテッド | 生体データ測定用のストリップ及び生体データ測定方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE118615T1 (de) * | 1989-04-07 | 1995-03-15 | Abbott Lab | Verfahren und vorrichtung zur trennung von plasma oder von serum aus blut. |
| JP3186106B2 (ja) * | 1991-07-30 | 2001-07-11 | テルモ株式会社 | 血液成分分離保存装置 |
| EP2910944B1 (en) * | 2012-10-22 | 2018-09-26 | Panasonic Intellectual Property Management Co., Ltd. | Filter device |
| JP6539935B2 (ja) * | 2017-10-12 | 2019-07-10 | Blue Industries株式会社 | 分離フィルタ、遺伝子解析用前処理キット |
-
2020
- 2020-02-25 WO PCT/JP2020/007516 patent/WO2021171378A1/ja active Application Filing
- 2020-02-25 JP JP2022502621A patent/JP7399514B2/ja active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5916521A (en) | 1995-01-04 | 1999-06-29 | Spectral Diagnostics, Inc. | Lateral flow filter devices for separation of body fluids from particulate materials |
| JP2000502451A (ja) | 1995-12-22 | 2000-02-29 | ユニバーサル ヘルスウォッチ,インコーポレーテッド | 血漿分離をもたらす診断分析 |
| JP2003135435A (ja) | 2001-08-22 | 2003-05-13 | Kyowa Medex Co Ltd | 採血用具、これを用いた定量用溶液調製方法、定量用溶液調製器具及びその使用方法並びに定量用溶液を用いた定量方法 |
| JP2003194806A (ja) | 2001-12-27 | 2003-07-09 | Minolta Co Ltd | 血球分離用チップ |
| JP2003254934A (ja) | 2002-03-01 | 2003-09-10 | Matsushita Electric Ind Co Ltd | バイオセンサ |
| JP2012529039A (ja) | 2009-06-04 | 2012-11-15 | インフォピア カンパニー,リミテッド | 生体データ測定用のストリップ及び生体データ測定方法 |
| JP2011133235A (ja) | 2009-12-22 | 2011-07-07 | Physical Screening Inc | 検査対象液保存器具 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2021171378A1 (ja) | 2021-09-02 |
| JPWO2021171378A1 (ja) | 2021-09-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4513085B2 (ja) | 試料の容器 | |
| EP1387170B1 (en) | Specimen analyzing implement | |
| JP4627395B2 (ja) | 分析用カートリッジ及び送液制御装置 | |
| JP2020024220A (ja) | 流体の処理および制御 | |
| JP3325018B2 (ja) | 狭窄化された毛管チャネルを有する分析試験エレメント | |
| US10463290B2 (en) | Biological sample collection and storage assembly | |
| RO119751B1 (ro) | Disc optic, aparat pentru efectuarea unui control optic, metodă pentru detectarea prezenţei sau absenţei unui analit într-o probă şi metodă de control al unei probe bioligice, chimice sau biochimice | |
| US10350592B2 (en) | Sample collection and transfer device | |
| BR112015022738B1 (pt) | Dispositivo para utilização com um componente de amostra líquida formado | |
| JP2012523571A (ja) | マイクロ流体臨床分析器 | |
| WO2003064046A1 (en) | Sample collection and testing system | |
| US20060016747A1 (en) | Glass-fiber filter for blood filtration, blood filtration device and blood analysis element | |
| US10675622B2 (en) | Sample collection and transfer device | |
| EP3495824A1 (en) | Analysis cell, analysis device, analysis equipment, and analysis system | |
| JP5444632B2 (ja) | 核酸増幅方法およびそれに用いる容器 | |
| JPH10132800A (ja) | 体液分離シートと一体型の検体保護容器 | |
| JP7399514B2 (ja) | 分離装置、検出装置、保存装置及びセンサ | |
| US20090260458A1 (en) | High throughput dispenser | |
| CN111644216B (zh) | 用于血浆分离和检测的微流控结构 | |
| US20220276238A1 (en) | Poc test system and method | |
| KR20150101316A (ko) | 유체 분석 카트리지 | |
| JP5953128B2 (ja) | アッセイ用キャピラリアレイの製造方法 | |
| US11857966B1 (en) | Methods and devices for sample collection and sample separation | |
| CN114018835A (zh) | 微量全血预处理和血浆自动定量分配装置及分析方法 | |
| WO1998010283A1 (fr) | Recipient de protection d'echantillon solidaire d'une feuille de separation de fluides corporels |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230125 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230125 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20231128 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20231129 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7399514 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |