JP7360170B2 - 虚血病変部位特異的な遺伝子治療法 - Google Patents
虚血病変部位特異的な遺伝子治療法 Download PDFInfo
- Publication number
- JP7360170B2 JP7360170B2 JP2020503551A JP2020503551A JP7360170B2 JP 7360170 B2 JP7360170 B2 JP 7360170B2 JP 2020503551 A JP2020503551 A JP 2020503551A JP 2020503551 A JP2020503551 A JP 2020503551A JP 7360170 B2 JP7360170 B2 JP 7360170B2
- Authority
- JP
- Japan
- Prior art keywords
- nucleic acid
- acid strand
- ischemic
- region
- bases
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/111—General methods applicable to biologically active non-coding nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/543—Lipids, e.g. triglycerides; Polyamines, e.g. spermine or spermidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/549—Sugars, nucleosides, nucleotides or nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/55—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound the modifying agent being also a pharmacologically or therapeutically active agent, i.e. the entire conjugate being a codrug, i.e. a dimer, oligomer or polymer of pharmacologically or therapeutically active compounds
- A61K47/551—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound the modifying agent being also a pharmacologically or therapeutically active agent, i.e. the entire conjugate being a codrug, i.e. a dimer, oligomer or polymer of pharmacologically or therapeutically active compounds one of the codrug's components being a vitamin, e.g. niacinamide, vitamin B3, cobalamin, vitamin B12, folate, vitamin A or retinoic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/554—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound the modifying agent being a steroid plant sterol, glycyrrhetic acid, enoxolone or bile acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/323—Chemical structure of the sugar modified ring structure
- C12N2310/3231—Chemical structure of the sugar modified ring structure having an additional ring, e.g. LNA, ENA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/33—Chemical structure of the base
- C12N2310/334—Modified C
- C12N2310/3341—5-Methylcytosine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/341—Gapmers, i.e. of the type ===---===
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3515—Lipophilic moiety, e.g. cholesterol
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3519—Fusion with another nucleic acid
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/50—Physical structure
- C12N2310/53—Physical structure partially self-complementary or closed
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/32—Special delivery means, e.g. tissue-specific
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/50—Methods for regulating/modulating their activity
- C12N2320/52—Methods for regulating/modulating their activity modulating the physical stability, e.g. GC-content
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/50—Methods for regulating/modulating their activity
- C12N2320/53—Methods for regulating/modulating their activity reducing unwanted side-effects
Description
[1]標的転写産物に対するアンチセンスオリゴヌクレオチド領域を含む第1核酸鎖と、第1核酸鎖の少なくとも一部に相補的な相補的領域を含み、脂質が結合している第2核酸鎖とが互いにアニールしてなる核酸複合体を含む、被験体の虚血部位において標的転写産物の発現を調節するための組成物。
[2]第1核酸鎖が、9~50塩基長である、[1]に記載の組成物。
[3]第1核酸鎖中の前記アンチセンスオリゴヌクレオチド領域が、9~20塩基長である、[1]または[2]に記載の組成物。
[4]第2核酸鎖が、9~50塩基長である、[1]~[3]のいずれかに記載の組成物。
[5]第2核酸鎖中の前記相補的領域が、第1核酸鎖中の前記アンチセンスオリゴヌクレオチド領域の少なくとも一部に相補的である、[1]~[4]のいずれかに記載の組成物。
[6]アンチセンスオリゴヌクレオチド領域が、ギャップマー型またはミックスマー型アンチセンスオリゴヌクレオチド領域である、[1]~[5]のいずれかに記載の組成物。
[7]脂質が、トコフェロールもしくはその類縁体、またはコレステロールもしくはその類縁体である、[1]~[6]のいずれかに記載の組成物。
[8]脂質が、コレステロールもしくはその類縁体である、[7]に記載の組成物。
[9]虚血部位が、脳、脊髄、心筋、骨格筋(上肢骨格筋および下肢骨格筋を含む)、血管、肺、腎臓、肝臓、腸管、脾臓、眼、網膜、皮膚、末梢神経、または四肢に存在する、[1]~[8]のいずれかに記載の組成物。
[10]虚血部位が、脳、心筋、または下肢骨格筋に存在する、[1]~[8]のいずれかに記載の組成物。
[11]静脈内投与するための、[1]~[10]のいずれかに記載の組成物。
[12]標的転写産物の発現調節が、標的転写産物量の低下である、[1]~[11]のいずれかに記載の組成物。
[13]虚血急性期に投与するための、[1]~[12]のいずれかに記載の組成物。
[14]虚血性疾患を治療するための、[1]~[13]のいずれかに記載の組成物。
[15]虚血性疾患が、脳梗塞、心筋梗塞または下肢閉塞性動脈硬化症である、[14]に記載の組成物。
本明細書は本願の優先権の基礎となる日本国特許出願番号2018-035538号、2018-136625号の開示内容を包含する。
本発明は、第1核酸鎖と、第1核酸鎖の少なくとも一部に相補的な相補的領域を含む(またはそれからなる)第2核酸鎖が、相補的塩基対の水素結合を介してアニールしている核酸複合体を用いる。核酸複合体は、第1核酸鎖と第2核酸鎖のアニーリングにより生じた二本鎖構造を有する。第1核酸鎖の全部と第2核酸鎖の全部とがアニールしていることは必要ではなく、第1核酸鎖の一部と第2核酸鎖の全部がアニールしていてもよいし、第1核酸鎖の全部と第2核酸鎖の一部がアニールしていてもよい。または第1核酸鎖の一部と第2核酸鎖の一部がアニールしていてもよい。
上記の核酸複合体を含む、虚血を有する被験体の虚血部位において標的転写産物の発現を調節するための組成物が提供される。本組成物は医薬組成物であってもよい。
(脳梗塞部位への脂質リガンド結合型二本鎖オリゴヌクレオチドの送達)
脂質リガンドが結合したヘテロ二本鎖オリゴヌクレオチド(heteroduplex oligonucleotide、HDO;ヘテロ核酸ともいう;国際公開第2013/089283号、Nishina K, et. al., Nature Communication, 2015, 6:7969、およびAsami Y, et al., Drug Discoveries & Therapeutics. 2016; 10(5):256-262を参照)の脳梗塞部位(虚血病変)への送達性を、従来のアンセンスオリゴヌクレオチド(ASO)と比較した。
蛍光色素であるAlexaFluor568が5'末端に共有結合したLNA/DNAギャップマーASO(Alexa-ASO)を用意した(図6A)。このASOはMalat-1ノンコーディングRNA(配列番号1)の1317~1332位に相補的な塩基配列を有し、Malat-1遺伝子を標的とする。このASOは、5'末端から3個のLNAヌクレオシド、3'末端から3個のLNAヌクレオシド、およびそれらの間の10個のDNAヌクレオシドを含む、16塩基長のオリゴヌクレオチドである。
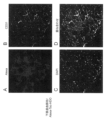
Alexa-Toc-HDO投与群では、脳梗塞部位に非常に強いAlexaシグナルが見られた(図7Aおよび8A~C)のに対し、非虚血部位には主に脳血管内皮細胞にわずかなAlexaシグナルを認めるのみであった(図7B)。また、Alexa-ASO投与群では、脳梗塞大脳半球であっても脳血管内皮細胞の一部に弱いAlexaシグナルを認めるのみであった(図7Cおよび8D~F)。PBSを投与した陰性対照群では、脳梗塞大脳半球および非虚血大脳半球ともに脳切片上に明らかなAlexaシグナルは検出されなかった。
(脳梗塞部位への脂質リガンド結合型二本鎖オリゴヌクレオチドの送達のさらなる解析)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドが送達される脳梗塞部位を、血管内皮細胞マーカーおよび神経細胞マーカーを用いてより詳細に観察した。
実施例1に記載したように脳梗塞モデルマウスを作製し、脂質リガンド(トコフェロール)結合型ヘテロ二本鎖オリゴヌクレオチド(Alexa-Toc-HDO)を脳梗塞モデルマウスに投与し、脳を摘出し、薄切切片を作製した。血管内皮細胞マーカーとして抗CD31抗体(rat anti-mouse CD31 antibody (1:50希釈、BD Pharmingen(商標)、BD Biosciences)もしくはrat anti-mouse CD31 antibody(1:50希釈、Santa Cruz Biotechnology))、神経細胞マーカーとして抗NeuN抗体(mouse anti-NeuN antibody(1:100希釈、EMD Millipore))を用いて切片に免疫染色を行った。それぞれの一次抗体に対応する、蛍光標識二次抗体(FITCまたはローダミン標識ヤギ抗体)はEMD millipore社から入手した。また、切片をDAPIで処理し、核を染色した。切片を蛍光顕微鏡にてAlexaシグナル、CD31もしくはNeuNシグナル、ならびに核について観察した。
Alexa-Toc-HDOを投与した脳梗塞モデルマウスの脳梗塞部位において、AlexaシグナルはCD31陽性の脳血管内皮細胞に観察され(図10A~C)、さらに中枢神経細胞である神経細胞(NeuN陽性細胞)にも観察された(図10D~F)。
(脳梗塞モデルマウスにおける標的遺伝子発現の抑制)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドによる脳梗塞モデルマウスにおける標的遺伝子発現抑制効果を、アンセンスオリゴヌクレオチド(ASO)と比較して調べた。
蛍光色素であるAlexaFluor568が結合していないことを除いて実施例1で用いたものと同じLNA/DNAギャップマーASOを用意した。このASOを、実施例1で用いたToc-cRNA(トコフェロールが共有結合した相補的RNA鎖)にアニーリングさせることにより、脂質リガンド(トコフェロール)結合型ヘテロ二本鎖オリゴヌクレオチド(Toc-HDO)を作製した。
図11(相対的Malat-1レベル)の白棒に示すように、非虚血大脳半球では、PBS投与群と比較して、ASO投与群およびToc-HDO投与群においてともに、Malat-1遺伝子発現の有意な低下を認めなかった(それぞれの群は5匹で検討)。一方で、図11(相対的Malat-1レベル)の黒棒に示すように、脳梗塞大脳半球では、Toc-HDO投与群のみで、PBS投与群と比較してMalat-1遺伝子発現が有意に低下した(*p<0.01)。
(脳梗塞の病態の変化)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドによって、脳梗塞の病態を変化させることができるかどうかを検討した。
実施例3と同様に脳梗塞モデルマウスを作製し、動脈閉塞3時間後に、50mg/kgの用量のToc-HDOを尾静脈から静脈内注射した。また、陰性対照群としてPBSのみ、またはシャッフルToc-HDOを脳梗塞モデルマウスに投与した。
脳梗塞体積はPBS投与群およびシャッフルToc-HDO投与群(陰性対照)と比較して、Toc-HDO投与群で有意に増加した(図13A、**p<0.01)。
(心筋梗塞部位への脂質リガンド結合型二本鎖オリゴヌクレオチドの送達)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドの心筋梗塞部位への送達性を、従来のアンセンスオリゴヌクレオチド(ASO)と比較した。
8~10週齢のマウス(C57BL/6、雄、三協ラボサービス株式会社)を用いて次のように心筋梗塞モデルを作製した。イソフルラン3~4%吸入により麻酔後、マウスの気管に経口挿管カニューレを挿入し、カニューレを小動物人工呼吸器に接続して呼吸管理を行った。マウスの前胸部を1cm程度切開し、肋間スペースから開創器により胸腔および心臓を露呈させた。冠動脈左前下行枝上の中枢部にシリコンチューブを留置し、同血管(冠動脈左前下行枝)およびシリコンチューブを縫合糸で結紮し、心電図でのST異常(ST部分の異常)を確認しながら左前下行枝の虚血状態を維持した。60分間の虚血後、シリコンチューブを抜去し再灌流を施行した。止血を確認し、皮膚縫合を行った後、自発呼吸を確認後に抜管した。
Alexa-Toc-HDO投与群の心筋梗塞部位では全域にわたって非常に強いAlexaシグナルが検出された(図14A)。一方、Alexa-ASO投与群の心筋梗塞部位では弱いAlexaシグナルが認められるのみであったが(図14B)。また、正常心筋では、Alexa-ASO投与群およびAlexa-Toc-HDO投与群(図14C)ともに弱い点状のAlexaシグナルが見られるのみであった。
(心筋梗塞部位への脂質リガンド結合型二本鎖オリゴヌクレオチドの送達のさらなる解析) 脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドが送達される心筋梗塞部位を、血管内皮細胞マーカーを用いてより詳細に観察した。
実施例5に記載したように心筋梗塞モデルマウスを作製し、Alexa標識した脂質リガンド(トコフェロール)結合型ヘテロ二本鎖オリゴヌクレオチド(Alexa-Toc-HDO)を心筋梗塞モデルマウスに投与し、心臓を摘出し、薄切切片を作製した。
Alexa-Toc-HDOを投与した心筋梗塞モデルマウスの非梗塞部位では、一部の血管内皮細胞のみにAlexaシグナルが見られた(図15A~C)。一方、Alexa-Toc-HDOを投与した心筋梗塞モデルマウスの心筋梗塞部位では、血管内皮細胞だけでなく心筋内にも強いAlexaシグナルが見られた(図15D~F)。また、Alexa-Toc-HDOを投与した心筋梗塞モデルマウスの心筋梗塞部位では、心拍を司る特殊心筋(図16A~C)、ならびに、血管内皮細胞だけでなく冠動脈などの太い動脈の内皮細胞(冠動脈内皮細胞)および平滑筋細胞にも強いAlexaシグナルが見られた(図16D~F)。
(下肢閉塞性動脈硬化症モデルの下肢虚血部位への脂質リガンド結合型二本鎖オリゴヌクレオチドの送達)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドが下肢閉塞性動脈硬化症モデルの下肢虚血部位へ送達されるかどうかを、従来のアンセンスオリゴヌクレオチド(ASO)と比較して調べた。
8~10週齢のマウス(BALB/c、雄、三協ラボサービス株式会社)を用いて、次のように下肢閉塞性動脈硬化症モデルを作製した。イソフルラン3~4%吸入により麻酔導入後、イソフルラン2~2.5%で麻酔を維持し、右大腿部を約1cm切開し、鼠経靭帯直下において大腿動脈を大腿静脈および大腿神経から分離し、大腿動脈の近位と遠位の2カ所ならびにその間の分枝を2カ所の合計4カ所を結紮し、大腿動脈を切除した。その後、止血を確認して皮膚縫合を行い、下肢閉塞性動脈硬化症モデルマウスを作製した。
図17AおよびBのHE染色標本に示されるように、健常下肢骨格筋(図17A)と比べて、虚血下肢骨格筋(図17B)では、軽度の筋繊維の円形化や核成分の増加が見られ、大腿動脈の結紮術により下肢閉塞性動脈硬化症モデルが作製できたことが確認された。
(下肢虚血部位への脂質リガンド結合型二本鎖オリゴヌクレオチドの送達のさらなる解析) 脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドが送達される下肢虚血部位を、血管内皮細胞マーカーを用いてより詳細に観察した。
実施例7に記載したように下肢閉塞性動脈硬化症モデルマウスを作製し、Alexa標識した脂質リガンド(トコフェロール)結合型ヘテロ二本鎖オリゴヌクレオチド(Alexa-Toc-HDO)を下肢閉塞性動脈硬化症モデルマウスに投与し、虚血下肢骨格筋を摘出し、薄切切片を作製した。
Alexa-Toc-HDOを投与した下肢閉塞性動脈硬化症モデルマウスの虚血下肢骨格筋では、血管内皮細胞にAlexaシグナルが観察され、さらには骨格筋にもAlexaシグナルが観察された(図19A~D)。この結果から、脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドは、下肢虚血部位の血管内皮細胞、さらに血管を超えた骨格筋へも効率的に送達されることが示された。
(下肢閉塞性動脈硬化症モデルマウスにおける標的遺伝子発現の抑制)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドによる下肢閉塞性動脈硬化症モデルマウスにおける標的遺伝子発現抑制効果を、アンセンスオリゴヌクレオチド(ASO)と比較して調べた。
実施例3で用いた蛍光色素が結合していないLNA/DNAギャップマーASO、および脂質リガンド(トコフェロール)結合型ヘテロ二本鎖オリゴヌクレオチド(Toc-HDO)を本実施例で用いた。
虚血下肢骨格筋において、Toc-HDO投与群では、ASO投与群と比較してMalat-1遺伝子発現が大きく低下した(図20)。この結果から、脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドにより、一本鎖アンセンスオリゴヌクレオチドと比べて下肢虚血部位において強い遺伝子抑制効果が実現できることが示された。
(脂質受容体の脳梗塞急性期における増加)
脂質が結合する受容体が虚血病態(特に脳梗塞急性期)で増加するかどうかを調べた。
実施例1に記載したように脳梗塞モデルマウスを作製し、血管閉塞3、6、9および15時間後、ならびに1日後(各群n=4)に、マウスをPBSにて灌流した後に、解剖して虚血側(脳梗塞)大脳半球を摘出した。虚血側大脳半球において、生体内で主要な脂質受容体(LDLR(low density lipoprotein receptor)、SRBI(scavenger receptor class B type I)、およびLRP1(LDL receptor-related protein-1))のmRNA発現量およびタンパク質量を測定した。
図21A~Cに示すように、LDLR、SRBIおよびLRP1はいずれも、虚血24時間以内の超急性期の脳において、正常脳(偽手術)と比較してmRNAレベルで顕著に増加した(図21、*p<0.05、**p<0.01、***p<0.001)。また、図22に示すように、LDLRおよびSRBIはいずれも、虚血6時間後の脳において、非虚血大脳半球(偽手術)と比較して、タンパク質レベルでも顕著に増加した。血液脳関門の物理的な破綻が見られないタイミングである脳梗塞超急性期(特に、発症から12時間以内)に脂質受容体発現が増加することは、これまでに報告がなく、初めての発見である。
(脂質受容体の発現が増加する細胞種の同定)
実施例10に示されたように脂質受容体の発現が増加する細胞種を、血管内皮細胞マーカーおよび神経細胞マーカーを用いて同定した。
実施例1に記載したように脳梗塞モデルマウスを作製し、6時間後にマウスをPBSにて灌流した後に、解剖して大脳を摘出した。非虚血マウス(偽手術マウス)からも同様に大脳を摘出した。摘出した大脳を4%PFAで固定し20μmの薄切切片を作製した。一次抗体として抗LDLR抗体、抗SRBI抗体または抗LRP1抗体と、抗CD31抗体(血管内皮細胞マーカー)または抗NeuN抗体(神経細胞マーカー)との組み合わせを用いて切片を免疫組織染色し、蛍光顕微鏡にて観察した。抗LDLR抗体、抗SRBI抗体および抗LRP1抗体は実施例10に記載されている。抗CD31抗体および抗NeuN抗体は実施例2に記載されている。
LDL受容体(LDLR)の免疫染色の結果、非虚血脳(偽手術)ではLDL受容体の発現はほとんど見られないが(図23A)、脳梗塞6時間後(脳梗塞超急性期)の脳ではLDL受容体の発現が亢進していた(図23D)。LDL受容体の発現増加は、主にCD31陽性の血管内皮細胞(図23D~F)、および脳実質内の神経細胞で目立って見られた。
(LDL受容体ノックアウトマウスを用いた脳梗塞超急性期の血管透過性の検討)
LDL受容体(LDLR)ノックアウトマウスで脳梗塞を生じさせ、脳梗塞超急性期の血管透過性を検討した。
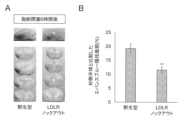
LDL受容体ノックアウトマウス(C57BL/6J; B6.129S7-Ldlr (tm1Her)/J (Ldlr-/-) mice (Jackson Laboratory, ME, USA); Ishibashi S, et al., Hypercholesterolemia in low density lipoprotein receptor knockout mice and its reversal by adenovirus-mediated gene delivery. J Clin Invest. 1993;92(2):883-93を参照)および正常C57BL6Jマウス(野生型)を用いて、実施例1に記載したように脳梗塞モデルを作製した。脳梗塞モデル作製3時間後に、エバンスブルー(和光純薬工業株式会社、054-04062)を生理的食塩水で希釈した2%エバンスブルー溶液を尾静脈よりマウスに注射(4ml/kg)した。注射後3時間(脳梗塞6時間後)に4%PFAでマウスを灌流固定し、脳を摘出した。脳の側面の写真を撮影した。その後、摘出脳を2mmの厚さで薄切し実体顕微鏡で撮像後にエバンスブルー陽性の領域を定量した。
脳のエバンスブルー陽性領域は、血管透過性が亢進している領域を示す。図26Aの写真およ図26Bのグラフに示すように、正常マウスでは、エバンスブルー陽性領域は閉塞した中大脳動脈領域全域に広く分布していたが、LDL受容体ノックアウトマウスでは、同領域は顕著に縮小していた(図26B、**p<0.01)。
(下肢閉塞性動脈硬化症モデルにおける脂質受容体の増加)
実施例10~12に示された脳梗塞以外の虚血病態での脂質受容体の発現変化を、下肢閉塞性動脈硬化症モデルで検討した。
実施例7に記載したように下肢閉塞性動脈硬化症モデルマウスを作製し、3時間後にマウスをPBSにて灌流した後に、解剖して虚血側骨格筋を摘出した。非虚血マウス(偽手術マウス)からも同様に骨格筋を摘出した。実施例10に記載したように、LDLR、SRBIおよびLRP1のmRNA発現量を定量的RT-PCRで測定し、非虚血群(偽手術群)と比較した。
LDL受容体(LDLR)、SRBI、およびLRP1のmRNA発現量は、下肢閉塞性動脈硬化症モデルでも実施例10の脳梗塞モデルと同様に顕著に増加した(図27、***p<0.001)。このことから、脂質受容体の増加は虚血病態に特徴的な変化であることが示された。よって、実施例12に記載した、脂質結合型ヘテロ二本鎖オリゴヌクレオチドの脂質受容体を介した虚血部位への送達メカニズムは、下肢閉塞性動脈硬化症モデルにも該当することが示唆された。
(脳梗塞部位へのコレステロール結合型二本鎖オリゴヌクレオチドの送達)
コレステロールが結合したヘテロ二本鎖オリゴヌクレオチドの脳梗塞部位(虚血病変)への送達性を、従来のアンセンスオリゴヌクレオチド(ASO)等と比較した。
実施例1に記載したように脳梗塞モデルマウスを作製し、動脈閉塞3時間後に5つの群(各群n=4)に無作為に分けて、それぞれPBS、または50mg/kgのASO、HDO、Toc-HDO、またはCho-HDOを尾静脈より投与した。
PBSの虚血側大脳半球を対象とした場合の遺伝子抑制効果を図28に示す(**p<0.01)。図28に示される通り、ASOおよび脂質リガンドのないHDOでは、優位な遺伝子抑制効果を示さなかった。これに対し、Toc-HDOおよびCho-HDOは優位な遺伝子抑制効果を示し、特にコレステロールを用いた場合に、最も高い効果が認められた。
この結果は、脂質リガンドのないHDOは、ASOと同様に中枢神経系での遺伝子抑制効果が乏しいが、TocやChoなどの脂質リガンドを結合させると、その抑制効果が著しく上昇することを示している。
(LDL受容体ノックアウトマウスを用いた脳梗塞超急性期の遺伝子抑制効果の検討)
脂質リガンド結合HDOの虚血側大脳半球へのデリバリーにLDL受容体が介しているか否かを、LDL受容体ノックアウトマウスを用いて調べた。
実施例12に従って、LDL受容体ノックアウトマウス(C57BL/6J)および正常C57BL6Jマウス(WT)を用いて、脳梗塞モデルを作製した。動脈閉塞3時間後に、実施例14で作製したToc-HDO 50mg/kg投与を尾静脈より投与し、動脈閉塞3日後に、Malat-1 RNAの発現量を実施例3に記載の方法に従って定量的RT-PCRで測定し、遺伝子抑制効果を比較した(各群n=4)。
図29に示す通り、虚血側大脳半球ではToc-HDOによるMalat-1遺伝子の抑制効果が認められるが、LDL受容体ノックアウト(LDLR KO)マウスでは、その遺伝子抑制効果が優位に減弱していた(*p<0.05)。
この結果は、脂質リガンド結合HDOの虚血側大脳半球へのデリバリーに、LDL受容体が関与していることを示唆している。
(心筋梗塞モデルにおけるトコフェロール結合HDOのデリバリー効果の検討)
トコフェロール結合型ヘテロ二本鎖オリゴヌクレオチドが心筋梗塞モデルの虚血部位へ送達されるかどうかを、従来のアンセンスオリゴヌクレオチド(ASO)と比較して調べた。
実施例5に記載したように心筋梗塞モデルを作製し、1時間後に実施例1に従って調製したAlexa-ASO 10mg/kg、またはAlexa-Toc-HDO 10mg/kgを尾静脈より投与し、その3時間後に組織へのデリバリー効率を、実施例1に記載の方法に従ってAlexaの蛍光強度で定量的に比較した(各群n=3)。
図30に示す通り、心筋梗塞モデルマウスの非梗塞部位では、ASOと比較してToc-HDOでデリバリー効率が若干の改善が認められた(*p<0.05、***p<0.001)。虚血部位では、ASOと比較してToc-HDOで5倍以上のデリバリー効率の改善を認められた。肝臓では、Toc-HDOのデリバリー効率は、ASOと比較して2倍程度改善していた。
この結果は、脂質リガンド結合型HDOでは、虚血部位選択的、特異的に送達されることを示している。これは、実施例6で示したAlexa-Toc-HDOの心筋梗塞への効率的な送達を示す組織学的な検討結果と一致する。
(心筋梗塞モデルマウスでのMalat-1 RNA発現抑制効果の比較)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドによる心筋梗塞モデルマウスにおける標的遺伝子発現抑制効果を、アンセンスオリゴヌクレオチド(ASO)と比較して調べた。
実施例5に記載したように心筋梗塞モデルを作成し、1時間後に5つの群(各群n=4)に無作為に分けて、それぞれPBS、または10mg/kgのASO、HDO、Toc-HDO、またはCho-HDOを尾静脈より投与した。ASO、HDO、Toc-HDO、およびCho-HDOの作製方法は実施例14に従った。心筋梗塞モデルマウス作製3日後に、Malat-1 RNAの発現量を実施例3に記載の方法に従って定量的RT-PCRで測定し、遺伝子抑制効果を比較した。
図31に示す通り、心筋梗塞モデルマウスにおいても、ASOと比較しToc-HDO、Cho-HDOで強い遺伝子抑制効果を認めたが、その抑制効果は特にCho-HDOで優れていた(*p<0.05、**p<0.01)。中枢神経と異なり、10mg/kgの投与量(脳は50mg/kg)で十分な抑制効果を示した。
(脂質受容体の心筋梗塞における増加)
脂質が結合する受容体が心筋梗塞で増加するかどうかを調べた。
実施例5に記載したように心筋梗塞モデルマウスを作製し、3日後にLDLR、LRP1、およびSRBIのmRNAを実施例10に記載の方法に従って定量的RT-PCRで解析した。虚血のない部位、梗塞周辺部位、梗塞部位の3箇所で解析した。
図32に示す通り、非虚血部位と比較して、梗塞周辺部位、梗塞部位ではそれぞれ有意にすべての脂質受容体の発現が増加していた(*p<0.05、**p<0.01)。
脳梗塞モデルと同様に、心筋梗塞モデルの虚血部位では脂質受容体の高い発現が認められ、これは脂質結合型HDOのデリバリー効率が虚血部位で増加することと関連している可能性がある。
(下肢閉塞性動脈硬化症モデルでのMalat-1 RNA発現抑制効果の比較)
脂質リガンド結合型ヘテロ二本鎖オリゴヌクレオチドによる下肢閉塞性動脈硬化症モデルマウスにおける標的遺伝子発現抑制効果を、アンセンスオリゴヌクレオチド(ASO)と比較して調べた。
実施例7に記載したように下肢閉塞性動脈硬化症モデルを作製し、3時間後に5つの群(各群n=4)に無作為に分けて、それぞれPBS、または10mg/kgのASO、HDO、Toc-HDO、またはCho-HDOを尾静脈より投与した。ASO、HDO、Toc-HDO、およびCho-HDOの作製方法は実施例14に従った。下肢閉塞性動脈硬化症モデルマウス作製3日後に、Malat-1 RNAの発現量を実施例3に記載の方法に従って定量的RT-PCRで測定し、遺伝子抑制効果を比較した。
図33に示す通り、下肢閉塞性動脈硬化症モデルマウスにおいても、ASOと比較しToc-HDO、Cho-HDOで強い遺伝子抑制効果を認めたが、その抑制効果は特にCho-HDOで優れていた(*p<0.05、**p<0.01)。中枢神経と異なり、10mg/kgの投与量(脳は50mg/kg)で十分な抑制効果を示した。
(脂質受容体の下肢閉塞性動脈硬化症モデルにおける発現)
下肢閉塞性動脈硬化症モデルにおける脂質受容体の発現増加を、免疫蛍光染色によって確認した。
実施例7に記載したように下肢閉塞性動脈硬化症モデルを作製し、本モデルにおけるLDLRSRBI発現を実施例11に記載の方法に従って免疫蛍光染色によって確認した。
図34に示す通り、虚血部位(A)では、正常部位(B)に対し、特にCD31陽性の血管内皮細胞でLDLRおよびSRBIの発現が上昇していた。これは脂質結合型HDOのデリバリー効率が虚血部位で増加することと関連している可能性がある。
本明細書で引用した全ての刊行物、特許および特許出願はそのまま引用により本明細書に組み入れられるものとする。
Claims (12)
- 被験体の虚血部位において標的転写産物の発現を調節するための組成物であって、
標的転写産物の少なくとも一部に対して相補的な塩基配列を含むアンチセンスオリゴヌクレオチド領域を含む第1核酸鎖と、第1核酸鎖の少なくとも一部に相補的な相補的領域を含み、脂質が結合している第2核酸鎖とが互いにアニールしてなる核酸複合体を含み、
前記脂質は、トコフェロールもしくはその類縁体、またはコレステロールもしくはその類縁体であり、
トコフェロールの前記類縁体は、α-トコトリエノール、β-トコトリエノール、γ-トコトリエノール、およびδ-トコトリエノールからなる群から選択され、
コレステロールの前記類縁体は、コレスタノール、ラノステロール、セレブロステロール、デヒドロコレステロール、およびコプロスタノールからなる群から選択され、
前記標的転写産物の発現調節が、標的転写産物量の低下、標的転写産物の翻訳の阻害、またはスプライシング機能改変である、前記組成物。 - 第1核酸鎖が、9~50塩基長である、請求項1に記載の組成物。
- 第1核酸鎖中の前記アンチセンスオリゴヌクレオチド領域が、9~20塩基長である、請求項1または2に記載の組成物。
- 第2核酸鎖が、9~50塩基長である、請求項1~3のいずれか一項に記載の組成物。
- 第2核酸鎖中の前記相補的領域が、第1核酸鎖中の前記アンチセンスオリゴヌクレオチド領域の少なくとも一部に相補的である、請求項1~4のいずれか一項に記載の組成物。
- アンチセンスオリゴヌクレオチド領域が、ギャップマー型またはミックスマー型アンチセンスオリゴヌクレオチド領域である、請求項1~5のいずれか一項に記載の組成物。
- 虚血部位が、脳、心筋、または下肢骨格筋に存在する、請求項1~6のいずれか一項に記載の組成物。
- 静脈内投与するための、請求項1~7のいずれか一項に記載の組成物。
- 虚血急性期に投与するための、請求項1~8のいずれか一項に記載の組成物。
- 虚血性疾患を治療するための、請求項1~9のいずれか一項に記載の組成物。
- 虚血性疾患が、脳梗塞、心筋梗塞または下肢閉塞性動脈硬化症である、請求項10に記載の組成物。
- 前記スプライシング機能改変が、エクソンスキッピングまたは標的転写産物の分解である、請求項1~11のいずれか一項に記載の組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018035538 | 2018-02-28 | ||
| JP2018035538 | 2018-02-28 | ||
| JP2018136625 | 2018-07-20 | ||
| JP2018136625 | 2018-07-20 | ||
| PCT/JP2019/007458 WO2019167995A1 (ja) | 2018-02-28 | 2019-02-27 | 虚血病変部位特異的な遺伝子治療法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2019167995A1 JPWO2019167995A1 (ja) | 2021-02-12 |
| JP7360170B2 true JP7360170B2 (ja) | 2023-10-12 |
Family
ID=67806260
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020503551A Active JP7360170B2 (ja) | 2018-02-28 | 2019-02-27 | 虚血病変部位特異的な遺伝子治療法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US11674141B2 (ja) |
| EP (1) | EP3760209B1 (ja) |
| JP (1) | JP7360170B2 (ja) |
| WO (1) | WO2019167995A1 (ja) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008519596A (ja) | 2004-11-14 | 2008-06-12 | ヴァスキュラー バイオジェニックス リミテッド | 内皮細胞特異性を示すプロモーター及びそのプロモーターを使って血管形成を制御する方法 |
| JP2011500858A (ja) | 2007-10-30 | 2011-01-06 | テー2キュア ゲーエムベーハー | 血管新生、血管形成、若しくは血管修復を促進するか、又は腫瘍血管新生を阻害する方法 |
| US20140220038A1 (en) | 2011-06-29 | 2014-08-07 | Concepción Vicenta Llorente Cortés | Lrp1 as key receptor for the transfer of sterified cholesterol from very-low-density lipoproteins (vldl) to ischaemic cardiac muscle |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2669377A3 (en) | 2003-04-17 | 2015-10-14 | Alnylam Pharmaceuticals Inc. | Modified iRNA agents |
| WO2006053430A1 (en) | 2004-11-17 | 2006-05-26 | Protiva Biotherapeutics, Inc. | Sirna silencing of apolipoprotein b |
| US20090326042A1 (en) | 2006-05-05 | 2009-12-31 | Isis Pharmaceuticals, Inc | Compounds and methods for modulating expression of crp |
| CA2666191C (en) | 2006-10-09 | 2017-07-11 | Santaris Pharma A/S | Rna antagonist compounds for the modulation of pcsk9 |
| EP2410053B2 (en) | 2006-10-18 | 2020-07-15 | Ionis Pharmaceuticals, Inc. | Antisense compounds |
| WO2010083615A1 (en) | 2009-01-26 | 2010-07-29 | Protiva Biotherapeutics, Inc. | Compositions and methods for silencing apolipoprotein c-iii expression |
| EP2545173A2 (en) * | 2010-03-12 | 2013-01-16 | Sarepta Therapeutics, Inc. | Antisense modulation of nuclear hormone receptors |
| EP3210611B1 (en) | 2010-03-12 | 2019-08-21 | The Brigham and Women's Hospital, Inc. | Methods of treating vascular inflammatory disorders |
| WO2013089283A1 (en) | 2011-12-16 | 2013-06-20 | National University Corporation Tokyo Medical And Dental University | Chimeric double-stranded nucleic acid |
| US20160108395A1 (en) | 2013-03-01 | 2016-04-21 | National University Corporation Tokyo Medical And Dental University | Chimeric single-stranded antisense polynucleotides and double-stranded antisense agent |
| EP3004347B1 (en) | 2013-05-30 | 2018-09-26 | National University Corporation Tokyo Medical and Dental University | Double-stranded agents for delivering therapeutic oligonucleotides |
| JP6604544B2 (ja) | 2013-06-16 | 2019-11-13 | 国立大学法人 東京医科歯科大学 | エクソンスキッピング効果を有する二本鎖アンチセンス核酸 |
| EP3517610A4 (en) | 2016-09-23 | 2020-05-27 | National University Corporation Tokyo Medical and Dental University | THROUGH HETERODUPLEX NUCLEIC ACID THROUGH BLOOD BRAIN CABINET |
| JP7129702B2 (ja) | 2016-09-29 | 2022-09-02 | 国立大学法人 東京医科歯科大学 | オーバーハングを有する二本鎖核酸複合体 |
| JP2018136625A (ja) | 2017-02-20 | 2018-08-30 | Kddi株式会社 | 識別装置、識別方法及び識別プログラム |
| JP6583647B2 (ja) | 2017-11-22 | 2019-10-02 | 株式会社ユピテル | ゴルフ支援装置およびプログラム |
-
2019
- 2019-02-27 WO PCT/JP2019/007458 patent/WO2019167995A1/ja unknown
- 2019-02-27 US US16/975,441 patent/US11674141B2/en active Active
- 2019-02-27 EP EP19760346.7A patent/EP3760209B1/en active Active
- 2019-02-27 JP JP2020503551A patent/JP7360170B2/ja active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008519596A (ja) | 2004-11-14 | 2008-06-12 | ヴァスキュラー バイオジェニックス リミテッド | 内皮細胞特異性を示すプロモーター及びそのプロモーターを使って血管形成を制御する方法 |
| JP2011500858A (ja) | 2007-10-30 | 2011-01-06 | テー2キュア ゲーエムベーハー | 血管新生、血管形成、若しくは血管修復を促進するか、又は腫瘍血管新生を阻害する方法 |
| US20140220038A1 (en) | 2011-06-29 | 2014-08-07 | Concepción Vicenta Llorente Cortés | Lrp1 as key receptor for the transfer of sterified cholesterol from very-low-density lipoproteins (vldl) to ischaemic cardiac muscle |
Non-Patent Citations (1)
| Title |
|---|
| Drug Discoveries and Therapeutics,2016年,Vol.10,pp.256-262 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3760209C0 (en) | 2023-11-22 |
| US11674141B2 (en) | 2023-06-13 |
| EP3760209A1 (en) | 2021-01-06 |
| JPWO2019167995A1 (ja) | 2021-02-12 |
| US20210130825A1 (en) | 2021-05-06 |
| WO2019167995A1 (ja) | 2019-09-06 |
| EP3760209A4 (en) | 2021-11-17 |
| EP3760209B1 (en) | 2023-11-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6638923B2 (ja) | キメラ2重鎖核酸 | |
| WO2018062510A1 (ja) | オーバーハングを有する二本鎖核酸複合体 | |
| KR20240036132A (ko) | 대상에게서 smn2 스플라이싱을 조정하기 위한 조성물 및 방법 | |
| IL194419A (en) | Dsrna to inhibit the expression of a 5eg gene in a human cell, a pharmaceutical compound containing it, a vector method | |
| WO2018056442A1 (ja) | 血液脳関門通過型ヘテロ2本鎖核酸 | |
| US20180282728A1 (en) | Organic compositions to treat beta-catenin-related diseases | |
| JP2016533751A (ja) | プレカリクレイン(pkk)発現の調節 | |
| JP7333079B2 (ja) | 毒性が軽減した核酸 | |
| CN113677374A (zh) | 肌疾病治疗用药物组合物 | |
| JP7360170B2 (ja) | 虚血病変部位特異的な遺伝子治療法 | |
| JP2023544385A (ja) | Snca関連神経変性疾患を治療又は予防するためのsnca irna組成物及びその使用方法 | |
| JPWO2021002359A1 (ja) | 核酸医薬とその使用 | |
| KR101667384B1 (ko) | miR-551b-3p 를 이용한 허혈성 뇌중풍의 예방 또는 치료 | |
| WO2021070959A1 (ja) | 修飾ヘテロ核酸 | |
| WO2024005156A1 (ja) | 核酸医薬の毒性軽減剤 | |
| JP2024002985A (ja) | 膜貫通型セリンプロテアーゼ6(tmprss6)発現を阻害するための組成物および方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220225 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230404 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230602 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230905 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230922 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7360170 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |