JP7229467B2 - トランス-スプライシングRNA(tsRNA) - Google Patents
トランス-スプライシングRNA(tsRNA) Download PDFInfo
- Publication number
- JP7229467B2 JP7229467B2 JP2018551404A JP2018551404A JP7229467B2 JP 7229467 B2 JP7229467 B2 JP 7229467B2 JP 2018551404 A JP2018551404 A JP 2018551404A JP 2018551404 A JP2018551404 A JP 2018551404A JP 7229467 B2 JP7229467 B2 JP 7229467B2
- Authority
- JP
- Japan
- Prior art keywords
- trans
- splicing
- tsrna
- vector
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/7105—Natural ribonucleic acids, i.e. containing only riboses attached to adenine, guanine, cytosine or uracil and having 3'-5' phosphodiester links
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/14—Prodigestives, e.g. acids, enzymes, appetite stimulants, antidyspeptics, tonics, antiflatulents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
- A61P21/04—Drugs for disorders of the muscular or neuromuscular system for myasthenia gravis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/14—Drugs for disorders of the nervous system for treating abnormal movements, e.g. chorea, dyskinesia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
- A61P31/06—Antibacterial agents for tuberculosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
- A61P31/22—Antivirals for DNA viruses for herpes viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/64—General methods for preparing the vector, for introducing it into the cell or for selecting the vector-containing host
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/67—General methods for enhancing the expression
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Molecular Biology (AREA)
- Virology (AREA)
- Oncology (AREA)
- General Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Communicable Diseases (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Plant Pathology (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Hematology (AREA)
- Diabetes (AREA)
- Epidemiology (AREA)
- Psychology (AREA)
- Hospice & Palliative Care (AREA)
- Psychiatry (AREA)
- Pulmonology (AREA)
- Cell Biology (AREA)
Description
治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである遺伝子の少なくとも一部分に特異的な少なくとも1つの結合ドメイン;
少なくとも1つの自殺タンパク質または自殺系の成分であるタンパク質をコードする核酸;および
少なくとも1つのスプライスシグナル;
ここで、前記結合ドメインは、内部結合および/または自己相補的配列を有しない少なくとも25個、より好ましくは35個、より一層好ましくは45個、最も好ましくは55個またはそれ以上の連続的な非構造化ヌクレオチド(nt)を含む結合部位を含み、そして;前記結合ドメインが44ntまたはそれより長い場合、前記結合ドメインは、前記結合部位内にまたは当該部位の外に、少なくとも1つの、または複数の、前記遺伝子に対するミスマッチヌクレオチド(単数または複数)を有する。
図1 HepG2組織培養細胞における標的AFPへの5’ERおよび3’ERによる細胞死シグナルのトランス-スプライシングの検出。(a)5’エキソン置換(5’ER)または3’エキソン置換(3’ER)のいずれかによる、アルファフェトプロテイン(AFP)へのHSVtk死シグナルでのエキソン置換のために設計された2種のトランス-スプライシング分子を示す図。5’ERコンストラクトは、コーディングドメインHSVtk遺伝子、それに続く5’ドナースプライス部位を有する5’スプライシングドメイン、およびAFP遺伝子のイントロン3を認識する50塩基対の結合ドメインを含む。自己切断HH Rzが、ポリAシグナルからBDを切り離すために取り付けられる。3’ERコンストラクトは、AFPイントロン5を標的にする50塩基対のBD、それに続く3’スプライスシグナル、P2AおよびHSVtkコーディング領域を含む。タンパク質分解的切断部位P2Aが、トランス-スプライシングの成功後にAFP-HSVtk融合タンパク質からのHSVtkの切断のために取り付けられる。HSVtk,単純ヘルペスウイルスチミジンキナーゼ;ISE,イントロニック・スプライス・エンハンサー;BD,結合ドメイン;HH Rz,ハンマーヘッド型リボザイム;BP,分岐点;Ppy,ポリピリミジントラクト。(b)5’ER(上のパネル)および3’ER(下のパネル)を用いた、過剰発現されたAFP_E3-E6ミニ遺伝子の状況においてトランス-スプライシングコンストラクトを導入した際のシス-スプライシングおよびトランス-スプライシングの生の閾値サイクル(Ct)を示す定量的リアルタイムRT-PCR。AFP(5’ERに関してはエキソン4、3’ERに関してはエキソン6に結合、左のパネル)およびHSVtk(5’ERに関しては遠位部で、3’ERについては近位部で結合、右のパネル)の2セットのTaqManプローブを検出のために使用した。ベータ-アクチンを内部コントロールとして使用した。n=3、平均±SEM。(c)慣用の30+30サイクルの2ステップPCRを実施して、過剰発現させたAFPとの5’(上)および3’(下)スプライシング事象を1%アガロースゲル上で観察し、スプライスジャンクションを配列決定により確認した。C,シス; T,トランス。(b)および(c)Mock_HepG2は、AFPシス-スプライシング検出の内因性レベルを示す(b,左のパネル、およびc,上および下の最後のレーン)。(d)および(e)は、活性な5’(d)および3’(e)トランス-スプライシングコンストラクトをAFPミニ遺伝子とともに導入した場合の、シス-スプライシングレベルの低下を示す。シスおよびトランス-スプライシングの生Ct値は、スプライシング事象の二分子反応の結果を表す。n=3、平均±SEM。(f)Ct値として表された内因性標的AFPにおけるスプライシング事象。n=3、平均±SEM。(g)活性3’ER(上のパネル)および5’ER(下)における内因性CおよびTのレベルを示す、35+35サイクルの慣用のPCR。
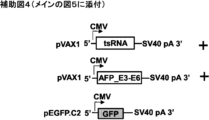
RNA設計:活性および標的特異性を改善するために種々の報告されたおよび新規の分子の特徴を組み合わせて、トランス-スプライシングコンストラクトを設計した。3’ER tsコンストラクトは、CMVプロモーター(pEGFP-N1,Clontech acc no.U55762)、それに続く標的AFPイントロン5に相補的な50塩基の結合ドメイン(BD)からなっていた。前記BDは、細胞の核内においてより長いdsRNAによって誘発され得る潜在的なアンチセンス(as)効果を抑制するために、18番目および19番目に2つのミスマッチを含んでいた。AFPイントロン5に指向され得る完全なアンチセンスRNA構造スペース内の短い非構造化BDを選択するために、ソフトウェア「foldanalyze」(HUSAR,DKFZ)を使用した。選択したBDの構造を、ソフトウェアツールmfoldおよびRNAfoldを用いるRNA 2°構造(最小自由エネルギーおよびセントロイド)予測により確認した。そのような選択されたBDをその後、トランス-スプライシングRNAの残部と融合し、BDが融合時に非構造化されたままであってトランスースプライシングまたはコーディングドメインの塩基対形成に関与しないことを確実にし、これは適切なスペーサーを付与することにより達成された。選択された3’スプライスシグナル(3’ss)は、機能的に細胞のシス-スプライス部位と競合するように設計され、イントロニック・スプライス・エンハンサー(intronic splice enhancer:ISE)(McCarthy, et al., 1998; Konczak, et al., 2000; Yeo et al., 2004)、分岐点(BP)(Eul, 2006)およびポリピリミジントラクト(Ppt)(Nobel, et al., 1998; Taggart, et al, 2012)によって支持された。トランス-スプライシングプロセスから最初に得られるAFP-HSVtk融合タンパク質からの天然のHSV-tkの内因性の切り離しを保証するために、タンパク質分解的切断部位P2A(Kim, et al, 2011)をコードする配列をHSVtk cdsの前に置いた。前記HSVtk遺伝子は開始コドンを欠いており、トランス-スプライシング後にのみ、標的メッセージの翻訳開始を用いて翻訳され得る。HSV-tk遺伝子は、HSV-tkアミノ酸配列を変化させない縮重した選択的コドンを使用することにより生成したA/Gリッチ・エキソニック・スプライス・エンハンサー(ESE)を備えていた(Fairbrother, et al, 2002; Jin et al., 2003) (補助図1a)。133塩基のベータ-グロビン・ミニイントロン((pCMVTNTTM, acc num. AF477200.1)をHSVtk遺伝子に、スプライス部位コンセンサスモチーフ(3’ss CAG/Gおよび5’ss MAG)で導入した。転写終結のために、SV40ポリA配列(pcDNA3.1,Life Technologies)を使用した。
(a)ステムループプライマーのリン酸化
個別のRE部位からなるステムループはAIT Biotech(シンガポール)によって合成し、それを表1に示す以下の反応を用いてリン酸化した:
(b) ELAN法
ELANループ-ライゲーション法において、遺伝子発現カセットを、親プラスミドから直接切り出した。遺伝子発現カセットの大部分がキャップされることを確実にするために、50倍のさらなるステムループをライゲーション反応に添加した。ループダイマーのような副生成物を制限酵素により切断し、エクソヌクレアーゼ処理の間に破壊した。反応の詳細なセットアップを表2に示す。
生成したダンベルを、それらの完全性を確認するために1%アガロースゲルで泳動した。
5’および3’エキソン置換(ER)のために新規に設計したトランス-スプライシングRNAは、過剰発現されたまたは内因性pre-mRNA標的に対して標的化されたトランス-スプライシングを誘発する
この発明は、より高いトランス-スプライシング活性および特異性を達成するために設計された新規の最適化されたRNA配列および構造に向けられている。我々は、下記の分子的特徴を含む、5’ERまたは3’ER両方のための親トランス-スプライシングRNA(tsRNA)分子を設計した(図1a):第1に、AFPのpre-mRNAのイントロン3または5に相補的なコンピューターにより選択された約50ntの長さの非構造化結合ドメイン(BD)およびtsRNA分子の状況下で選択されたBD構造を保存するスペーサー;第2に、5’ERに関して、イントロニック・スプライス・エンハンサー(ISE)およびコンセンサス・スプライスドナー(SD)部位(CAG/GT)から、または3’ERに関して、ISE、コンセンサスYNYURAC (R プリン, Y ピリミジン, N 任意のヌクレオチド)分岐点(BP)配列、広範囲のポリピリミジントラクト(PPT)およびコンセンサススプライスアクセプター(SA)部位(AG/G)から構成されるスプライシングドメイン;および第3に、新規の強化されたエキソニック・スプライス・エンハンサー(ESE)ならびにα-グロビンミニイントロンを有する、最適化HSVtk遺伝子を含むコーディングドメイン。
我々は、RNAトランス-スプライシングにおけるBD RNA二次の役割を調べた。我々の以前に記載したソフトウェアツール(Senger, et al. 1995)を用いて、我々は、AFP pre-mRNAに対して標的化できる約50ntの長さの最も構造化されていないBDを同定した:それぞれイントロン5またはイントロン3に結合する3’または5’ERのための3ER_BD-optまたは5ER_BD-opt(図2、補助図1b,2a)。コントロールとして、我々は同等の長さの高度に構造化したドメイン(3ER_BD-struc1、3ER_BD-struc2および5ER_BD-struc1)(これらの各々は非構造化ドメインと重複していた)を同定した(補助図1,2)。最後に我々は、有利なBD、すなわち3ER_BD-optおよび5ER_BD-optを完全に包含する内部逆方向反復を使用し、それらを構造化された不利なBDに変えるが、標的スプライス部位への距離を維持することにより、別の2つのBD、すなわち3ER_BD-opt-invおよび5ER_BD-opt-invを設計した。選択された結合ドメインを、リンカーまたはスペーサー配列を介してtsRNAの他のドメインと融合し、これにより選択されたBD構造が融合の際に変化しないことが確保された(補助図1a)。RNA編集を抑制するために、これらの全てのBDは、中央に2ntの標的ミスマッチを有する不完全な標的結合ドメイン(ΔBD)として生成した。これらのミスマッチによって生じる効果を調べるために、我々はまた、それぞれ非構造化BDもしくは最も構造化されたBDの完全に相補的なアナログ、3ER_BD-optおよび5ER_BD-opt、または3ER_BD-opt-invおよび5ER_BD-opt-invを生成した(図2a,2b)。全てのBDおよびΔBDを、親のトランス-スプライシングベクター中にクローニングした。HepG2細胞を、トランス-スプライシングプラスミドおよびAFPミニ遺伝子ベクターでコトランスフェクトし、トランス-スプライシング活性をトランスフェクションの24時間後にモニタリングした。3’ERの場合、3ER_ΔBD-optを有するtsRNAは、3ER_BD-opt、3ER_ΔBD-opt-invまたは3ER_BD-opt-invを有するそのアナログと比較して、4倍(p=0,04)、3倍または30倍(p=0.04)強いトランス-スプライシングを誘発した(図2c)。さらに、3ER_ΔBD-optは、4倍または6倍(p=0.04)、3ER_BD-struc1または3ER_BD-struc2より強力であった。これらのデータは、(i)ミスマッチΔBDが相補的なBDよりも強力であること、および(ii)非構造化BDまたはΔBDが構造化されたものより効果的であることを示す。反対に、結合ドメイン内のRNA二次構造形成および標的相補性の程度は、5’ER活性に影響を与えなかった(図2d)。しかしながら、スプライス部位突然変異は、全てのコンストラクトの3’および5’ER活性を低下させた(図2a,b)。5’エキソン置換は、tsRNA 3’末端の熱力学的安定性と相関する。
選択的オンターゲットトランス-スプライシングを抑制するため、およびトランス-スプライシング特異性を改善するために、我々は、複数の標的および/または自己結合ドメインを有する3’ERのための新規RNAを設計した(図4c)。迅速な標的への結合のために最適化されたBD-optを補足して、我々は、 (i)BD-Eに、意図するトランス-スプライス部位D2およびAを互いにより近接させ、(ii)BD-Fを結合させ、機能的に選択的ドナースプライス部位D1をブロックし、(iii)BD-optのすぐ上流に位置していた自己結合ドメインBD-Dに、標的結合不在下でトランス-スプライシングRNAのアクセプタースプライス部位AのPPTを保護させた。さらに我々は、BD-opに加えそれぞれBD EおよびFまたはBD D、EおよびFを有する、マルチプルBD、すなわちp3ER_ΔBD-opt_EFまたはp3ER_ΔBD-opt_DEFを生成した。全てのコンストラクトに関して、我々は、特異的(TSspec)および選択的オンターゲットトランス-スプライシング(TSalt)の相対活性を測定し、式(1)を用いて特異性係数Sを計算した(図4d):
S = TSspec/TSalt*100% (1)
全ての二次BDは、特異性係数の増加に反映されるように、トランス-スプライシングの特異性を増加させた。BD-Fおよびより顕著なBD-Dは、特異的および選択的オンターゲットトランス-スプライシングの両方を抑制した一方で、BD-EならびにBD-Eおよび-Fの組み合わせは、特異的なトランス-スプライシングは増加させたが、選択的オンターゲットトランス-スプライシングは抑制した。しかしながら、最も成功したのは3つ全ての追加的なBD、すなわちD、EおよびFの組み合わせであり、これは、特異的なトランス-スプライシングを約2倍増加させ、選択的スプライシングを約5倍減少させ、従って、親コンストラクトと比較して、10倍高いトランス-スプライシングの特異性を示した。標的結合ドメインのないコンストラクトにおいて、内部BD-Dは 強力なスプライスドナーD1またはやや強力なドナーD2に向けたトランス-スプライシングを20倍または130倍抑制し、他の細胞のオフターゲットに対するトランス-スプライシングが同程度抑制されたと考えられる。特に、トランス-スプライシングの同等の減少が、突然変異誘発により弱められたスプライス部位を有するBD(-)コンストラクトで観察された。
自殺遺伝子系として、我々は単純ヘルペスウイルスチミジンキナーゼ(HSVtk)およびプロドラッグのガンシクロビル(GCV)を選択した。トランス-スプライシングは、標的RNAに依存する様式でHSVtk発現を誘発し、これはその後 GCVのそのモノホスフェートへのリン酸化に触媒作用を及ぼし、それは引き続きそのジ-およびトリ-ホスフェート誘導体に細胞キナーゼにより変換される。毒性のGCV-トリホスフェートはその後、デオキシグアノシントリホスフェート(dGTP)アナログとして作用し、従って、複製の間にDNA鎖上に留まり、鎖の終結および細胞死を引き起こす。我々は、過剰発現させたまたは内因性AFP pre-mRNAに向けられた5’または3’ERによって誘発されたヒト肝がん細胞HepG2の死を3つの異なるアッセイを用いて調べた。第1に、alamar blue細胞生存性アッセイ。細胞をトランスフェクトし、トランスフェクションの24時間後に10もしくは100μM GCVを培地に添加し、薬剤処理の24時間後にalamar色素を添加し、90分のインキュベーション時間後に蛍光を測定した。alamar測定後に、培地および薬剤を補充し、6日間連続でプロセスを繰り返した。ポジティブコントロールのレベルに達する、最も高いレベルの細胞死、すなわち、100μM GCVで最大80%(図5a,b)または10μM GCVで60~70%(補助図3)が、過剰発現AFPメッセージに対する親コンストラクトのトランス-スプライシングにより処理の6日目に誘発された。同様に、高レベルの細胞死が、4つ全てのBDを含む3’ERコンストラクトで、および突然変異を有するHHRz切断モチーフを有する5’ERに関して観察された。内因性AFP RNAでの3’ERは、わずかに効果が低かった。予測されたように、より低いレベルの細胞死が、部分的に不活性なHSVtk突然変異体、スプライス部位突然変異体およびAFP特異的BDを欠くRNAにより誘発された。GCVの非存在下においてAFPミニ遺伝子またはトランス-スプライシングコンストラクトにより細胞毒性は誘発されなかった。第2に、我々の系によって誘発される細胞死の特定の様式をモニターするために、我々は、アネキシンV/ヨウ化プロピジウム(PI)アポトーシスアッセイを利用した。従って、HepG2細胞をトランスフェクトし、100μM GCVで48時間処理し、フローサイトメトリーを用いて解析した。トランスフェクトした細胞のみを分析するために、我々は最初にトランス-スプライシングベクターおよびAFPミニ遺伝子と一緒にEGFP発現ベクターをコトランスフェクトした(補助図4)。活性なトランス-スプライシングコンストラクトが、部分的に不活性なコンストラクトまたはコントロールと比較して高いレベルのアポトーシス(最大50%)を誘発することが見出されたが、相当の割合(30%)のアポトーシス細胞がEGFP陽性であった(補助図8d)。複数のプラスミドのコトランスフェクトに伴う欠点を回避するために、我々は、SV40プロモーター駆動性のEGFP遺伝子を、トランス-スプライシングベクター、AFPミニ遺伝子ベクターおよびHSVtkベクターに挿入し、その結果、細胞を1つのプラスミドだけ(内因性標的)または2つのプラスミド(過剰発現標的)でトランスフェクトすることができた(図5c,d,e)。最適化されたBDまたはマルチプルBDを有する最も活性な3’ERコンストラクト、および活性もしくは不活性切断モチーフを有するHHRzを持つ最良の5’ERコンストラクトは、AFP過剰発現細胞の40%超でアポトーシスを誘発した。半分のアポトーシス細胞は、内因性AFPのみを発現する細胞で検出された。例外は、突然変異を有するHHRz切断部位を有する5’ERコンストラクトであり、これは、内因性および過剰発現AFPの両方と同等の高レベルのアポトーシスを誘発した。このtsRNAは、標的に対するトランス-スプライシングを受けなくとも、5’キャップおよび3’ポリA尾部を有する完全に損傷されていない安定なmRNAを示す。従って、このtsRNAの高い細胞死活性は、トランス-スプライシングの非存在下での核輸出およびHSVtk翻訳のどちらかによるものであるか、および/または代替として高い内因性の安定性および後続の高率のトランス-スプライシング(これらはまさにこのRNAに関して測定された)によるものであるかもしれない(図3d)。HSVtk/GCV誘発細胞死の様式は、主に、DNA二本鎖破壊を伴うアポトーシスとして報告されてきた。大部分の割合の細胞がアポトーシスにより殺されたことを確認するために、我々は第3に、単細胞ゲル電気泳動後に部分的に分解したDNAを可視化できるコメットアッセイを実施した。従って、HepG2細胞を、トランス-スプライシングコンストラクトおよびAFPミニ遺伝子でコトランスフェクトし、100μM GCVでインキュベートし、24時間後にDNA破壊をテイルモーメントとして記録した。結果は、alamar blueおよびアネキシンV/PIアッセイで得られたものと一致し:大部分のDNAの破壊が、マルチプルBDまたは親3’ER RNAにより、5’ERの場合は突然変異を有するHHRz切断部位および親配列を持つRNAにより誘発された(図5f)。
他の多くのヒト疾患のように、肝細胞がん(HCC)の発がんは、多因子性の、多段階の複雑なプロセスであり、単一のバイオマーカーは疾患およびそのステージを正確に示さない。我々のアプローチのHCC特異性および感受性の両方を増加させるために、我々は、別個のBDを用いて2つのHCCバイオマーカーを同時に標的化する二重特異性(二重標的化)tsRNAを調べた。マルチプルHCCバイオマーカーは文献に報告されており、我々は、10種の異なる細胞株または細胞において12個の対応するpre-mRNAおよびmRNAの量を測定した(補助図5a)。我々の試験細胞株における量、HCC特異性および臨床的意義に基づいて、我々は3つの遺伝子を選択した:第1にHCCA2(YY1AP1)であり、肝がん患者においてアップレギュレートされているHCC関連タンパク質;第2にCD24であり、表面マーカー糖タンパク質であって、末期HCCにおける細胞の高い侵襲性および転移可能性に関するマーカー;および第3にVEGFであって、腫瘍の血管新生に重要な役割を果たすサイトカインであり、HCCにおけるリンパ節転移のバイオマーカーである。我々は、AFPおよびBDをスペーサー配列で分離する1つの二次標的BDの6つ全ての組み合わせを考慮して二重標的化トランス-スプライシングRNAを設計し、alamar blue細胞生存性アッセイを用いて、内因性のpre-mRNAのみを標的とするHepG2細胞のトランス-スプライシング介在性死を調べた(図5g,h)。10μM GCVで、全ての二重標的化コンストラクトは、AFPのみを標的とするコンストラクトと比較して有意に高いレベルの細胞死を誘発したが(図5h);100μM GCVでは、単一および二重標的化コンストラクトは同等の効果を示した(補助図5b)。
我々のtsRNAの普遍的な設計は、関心のある任意のpre-mRNAを標的とするための、スペーサーと一緒のBDの置換を促進する。第2の臨床的に関連する標的として、我々はヒトパピローマウイルス16型(HPV-16)を選択した。HPVは、皮膚および粘膜のケラチノサイトにおいて増殖的に感染し、良性の乳頭腫、前がん病変および癌を引き起こす。HPV感染は、世界中で最も高頻度な性感染疾患であり、2つの高リスク型HPV-16およびHPV-18は、子宮頸がん全症例の約70%を引き起こす。細胞形質転換の前に、HPV-16ゲノムが宿主細胞ゲノムに組み込まれ、ウイルスDNAを感染した個体から排除する方法はない。しかしながら、自殺遺伝子治療による感染細胞の選択的な破壊は、この問題を解決するためのアプローチを提示し得る。HPV感染において、選択的スプライシングは、ウイルスmRNAの多様なアイソフォームを生成する。我々は、コンピューターにより5つの最も有利な非構造化アンチセンスBD(opt_E6、_E1a、_E1b、_E2および_E5)を選択し、これらは初期ウイルス遺伝子E6、E1、E2およびE5を標的としてHPV-16転写物に対して向けられることができる(図6a)。46~82ntの長さの選択したBDを適切な構造保存スペーサーと一緒に親トランス-スプライシングベクターにクローニングして、3’ERのために4つのコンストラクトおよび5’ERに関して2つのコンストラクトを生成した。得られた5’ERまたは3’ER tsRNAの各々は、多様な選択的ウイルススプライスアクセプターまたはドナー部位を採用することができ、これらは、発表されているか、またはスプライス部位予測者アルゴリズムASSPを用いて我々により予測された。我々は、HPV-16形質転換細胞株SiHa(ヒト、2つのウイルスゲノムコピー)およびC3(マウス、多重切断および完全ウイルスゲノムコピー)におけるトランス-スプライシング用のこれらのスプライス部位の使用を、rtRT-PCRを用いてモニターした(図6b)。両細胞株において、HPV-16転写物は非常に多量であった。5’ERベクターおよび2つの最も活性な3’ERコンストラクトE1およびE6をその後、alamar blue細胞生存性アッセイおよび100μMのGCV濃度を用いて、HSVtk発現ベクター(ポジティブコントロール)と比較して、細胞死を誘発するためのそれらの可能性に関して試験した。HPV-16形質転換細胞株SiHaおよびC3において細胞死が選択的に誘発されたが、HPV-18形質転換HeLa細胞においてまたはHPV陰性細胞株HepG2においては誘発されなかった(図6c、補助図6)。SiHa細胞では、全てのtsRNAはポジティブコントロールと同程度に細胞死を誘発し;C3細胞では3’ERが5’ERより効率的であった。
なお、本願は、特許請求の範囲に記載の発明に関するものであるが、他の態様として以下も包含し得る。
1.治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである遺伝子の少なくとも一部分に特異的な少なくとも1つの結合ドメイン;
少なくとも1つの発現可能な自殺タンパク質または自殺系の成分であるタンパク質をコードする核酸;および
少なくとも1つのスプライスシグナル、
を含むトランス-スプライシングRNA(tsRNA)分子であって、
前記結合ドメインは、内部結合および/または自己相補的配列を有しない少なくとも25個の連続的な非構造化されたヌクレオチド(nt)を含む結合部位を含み、そして前記結合部位内にまたは当該部位の外に、前記結合ドメインは、44ntまたはそれより長い場合、少なくとも1つのまたは複数の、前記遺伝子に対するミスマッチヌクレオチドを有する、
トランス-スプライシングRNA(tsRNA)分子。
2.前記結合部位が、次の個数のヌクレオチドを含むかまたは次の個数のヌクレオチドからなるリストから選択されるヌクレオチドの配列を含む、上記1に記載のトランス-スプライシングRNA分子:25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、69,70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、153、154、155、156、157、158、159、160、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、177、178、179、180、181、182、183、184、185、186、187、188、189、190、191、192、193、194、195、196、197、198、199、200、201、202、203、204、205、206、207、208、209、210、211、212、213、214、215、216、217、218、219、220、221、222、223、224、225、226、227、228、229、230、231、232、233、234、235、236、237、238、239、240、241、242、243、244、245、246、247、248、249、250、251、252、253、254、255、256、257、258、259、260、261、262、263、264、265、266、267、268、269、270、271、272、273、274、275、276、277、278、279、280、281、282、283、284、285、286、287、288、289、290、291、292、293、294、295、296、297、298、299、300個またはそれを超えるヌクレオチド。
3.前記結合ドメインが、治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである遺伝子の前記一部分に対して少なくとも50%、55%、60%、65%、70%、75%、80%、85%、90%、91、92、93、94、95、96、97、98、99%または100%相補的であるヌクレオチドの配列を含む、上記1または2に記載のトランス-スプライシングRNA分子。
4.前記結合ドメインにおけるミスマッチが、前記結合部位を含めるかまたは当該結合部位を除いて、標的に対して完全に相補的な45ntのまたはそれより長い区間を回避するように位置する、上記1~3のいずれか1つに記載のトランス-スプライシングRNA分子。
5.前記ミスマッチが、5’または3’末端から少なくとも5ヌクレオチドである、上記4に記載のトランス-スプライシングRNA分子。
6.前記の少なくとも1つの発現可能な自殺タンパク質が単純ヘルペスウイルスチミジンキナーゼ(HSVtk)である、上記1~5のいずれか1つに記載のトランス-スプライシングRNA分子。
7.前記核酸が複数の発現可能な自殺タンパク質または自殺系の成分である複数のタンパク質をコードする、上記1~6のいずれか1つに記載のトランス-スプライシングRNA分子。
8.前記tsRNAが3’ERを誘発する、上記7に記載のトランス-スプライシングRNA分子。
9.前記tsRNAが前記結合ドメインに隣接するスペーサー配列も含む、上記1~8のいずれか1つに記載のトランス-スプライシングRNA分子。
10.前記のトランス-スプライシングRNA分子が、治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである遺伝子の同一のもしくは異なる部分に対して相補的である前記結合ドメインを複数含む、上記1~9のいずれか1つに記載のトランス-スプライシングRNA分子。
11.前記結合ドメインが、治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである異なる遺伝子に相補的である、上記1~9のいずれか1つに記載のトランス-スプライシングRNA分子。
12.前記tsRNAが、結合ドメインの外側に、少なくとも1つのシス結合もしくは自己結合ドメインを含む、上記1~11のいずれか1つに記載のトランス-スプライシングRNA分子。
13.前記tsRNAが、結合ドメインの外側かつ前記分子の3’に、自己相補的な配列の存在のために折りたたまれるかまたは自身と対を形成するRNAの高度に構造化された配列を含む、上記1~12のいずれか1つに記載のトランス-スプライシングRNA分子。
14.高度に構造化されたRNAが、それとポリA部位の間に位置したスペーサーに隣接する、上記13に記載のトランス-スプライシングRNA分子。
15.高度に構造化されたRNAが、活性もしくは不活性リボザイムである、上記14に記載のトランス-スプライシングRNA分子。
16.前記tsRNAが5’ERを誘発する、上記14または15に記載のトランス-スプライシングRNA分子。
17.前記tsRNAが5’または3’ERを誘発する、上記1~7または9~15のいずれか1つに記載のトランス-スプライシングRNA分子。
18.前記疾患が、癌またはウイルス感染または細菌感染または転位因子、放射線、化学物質もしくは未知の誘因により誘発された突然変異により引き起こされる後天性遺伝疾患である、上記1~17のいずれか1つに記載のトランス-スプライシングRNA分子。
19.前記癌が、肝細胞がん(HCC)、子宮頸がん、膣癌、外陰癌、陰茎癌、皮膚癌、悪性黒色腫を含む黒色腫、扁平上皮癌、基底細胞癌、メルケル細胞癌、肺癌、細胞膀胱癌(cell bladder cancer)、乳癌、結腸または直腸癌、肛門癌、子宮内膜癌、腎癌、白血病、急性骨髄性白血病(AML)、急性リンパ性白血病(ALL)、慢性リンパ性白血病(CML)、慢性骨髄性白血病(CML)、有毛細胞白血病(HCL)、T細胞前リンパ球性白血病(P-TLL)、大顆粒リンパ球性白血病、成人T細胞白血病、リンパ腫、骨髄腫、非ホジキンリンパ腫、膵臓癌、前立腺癌、甲状腺癌、鼻咽頭癌、口腔または咽頭癌、口腔咽頭癌、胃癌、脳腫瘍、骨の癌および幹細胞の癌である、上記18に記載のトランス-スプライシングRNA分子。
20.前記ウイルス感染が、ヒトT細胞白血病ウイルス(HTLV)を含むレトロウイルス、ヒト免疫不全ウイルス1型および2型(HIV-1およびHIV-2)を含むレンチウイルス、16型および18型(HPV-16およびHPV-18)を含むヒトパピローマウイルス、HAV、HBV、HCV、HDVおよびHEVを含む肝炎ウイルス、単純ヘルペス(HSV)、エプスタイン・バーウイルス(EBV)、サイトメガロウイルス(CMV)を含むヘルペスウイルス、アデノウイルス、アデノ随伴ウイルス、インフルエンザウイルスまたは他の任意の組み込みウイルスによる感染である、上記18に記載のトランス-スプライシングRNA分子。
21.前記細菌感染が、細菌、例えばバントネラ・ヘンセラ(Bartonella henselae)、フランシセラ・ツラレンシス(Francisella tularensis)、リステリア・モノサイトゲネス(Listeria monocytogenes)、サルモネラ種、サルモネラ・チフス(Salmonella typhi)、ブルセラ種、レジオネラ種、マイコバクテリア種、マイコバクテリウム・ツベルクローシス(Mycobacterium tunberculosis)、ノカルジア種、ロドコッカス種、エルシニア種、ナイセリア・メニンギティディス(Neisseria meningitides)等による感染である、上記18に記載のトランス-スプライシングRNA分子。
22.前記の後天性遺伝疾患が、神経線維腫症1型および2型、マッキューン・オルブライト、デュシェンヌ型筋ジストロフィー(DMD)、表皮水疱症、ファンコニAおよびC、フィラデルフィア染色体、血友病AおよびB、嚢胞性線維症、マックル・ウェルズ症候群、リポタンパク質リパーゼ欠損症、B-サラセミア、ピルビン酸脱水素酵素複合体欠損症等である、上記18に記載のトランス-スプライシングRNA分子。
23.上記1~22のいずれか1つに記載の前記tsRNAを含む細胞。
24.上記1~22のいずれか1つに記載の前記tsRNAを含むベクター。
25.前記ベクターが、裸の核酸をベースとするベクター、非ウイルスベクターまたはウイルスベクターである、上記24に記載のベクター。
26.前記の裸の核酸をベースとするベクターが、RNA分子、プラスミド、DNAミニサークルまたはダンベル型DNA最小ベクターを含む、上記25に記載のベクター。
27.前記の非ウイルスベクターが、リポソーム小胞、ナノ粒子、ポリマーコンジュゲート、抗体コンジュゲート、細胞貫通ペプチドまたはポリマーカプセルを含む、上記25に記載のベクター。
28.前記ウイルスベクターが、レトロウイルスベクター、レンチウイルスベクター、アデノウイルスベクター、アデノ随伴ウイルスベクター、単純ヘルペスウイルスベクター、ワクシニアウイルスベクター、キメラウイルスベクター、シンドビス・ウイルスベクターまたはアルファウイルスベクター、セムリキ森林ウイルスベクターおよびベネズエラウマ脳炎ウイルスベクターである、上記25に記載のベクター。
29.異常細胞を標的化する方法であって、上記1~22のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクターでの、in vivoにおける、腫瘍中への、局所適用;経鼻適用;肺胞適用;全身適用;経口適用;静脈内適用;筋肉適用;皮下適用;皮膚適用;腹腔内適用または注射、および、任意選択的に、前記細胞を、前記細胞を殺すために有効な前記自殺系の他の成分(単数または複数)に曝露することを含む方法。
30.細胞を殺す方法であって、前記細胞を、上記1~22のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクターで、ex vivoまたはin vivoにおいて、トランスフェクション、リポフェクション、形質導入、エレクトロポレーション、ヌクレオフェクションまたは形質転換すること、および任意選択的に、前記細胞を殺すために有効な前記自殺系の他の成分(単数または複数)に前記細胞を曝露することを含む方法。
31.疾患を治療する方法であって、異常細胞を、上記1~22のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクターで、ex vivoまたはin vivoにおいて、トランスフェクション、リポフェクション、形質導入、エレクトロポレーション、ヌクレオフェクションまたは形質転換すること、および任意選択的に、前記細胞を殺すために有効な前記自殺系の他の成分(単数または複数)に前記細胞を曝露することを含む方法。
32.前記自殺系の前記成分(単数または複数)が、ガンシクロビル、シトシンデアミナーゼ-5-フルオロシトシン、シトクロムP450-イホスファミド、シトクロムP450-シクロホスファミドおよびニトロレダクダーゼ-5-[アジリジン-1-イル]-2,4-ジニトロベンズアミドを含むかまたはこれらからなる群から選択される、上記29~31のいずれか1つに記載の方法。
33.前記細胞が哺乳類である、上記19~22のいずれか1つに記載のトランス-スプライシングRNA分子または上記23に記載の細胞または上記29~32のいずれか1つに記載の方法。
34.前記細胞がヒトである、上記19~22のいずれか1つに記載のトランス-スプライシングRNA分子または上記23に記載の細胞または上記29~32のいずれか1つに記載の方法。
35.上記1~22のいずれか1つに記載の前記tsRNAまたは上記24~28のいずれか1つに記載のベクターおよび、任意選択的に、前記トランス-スプライスされたRNAを発現する細胞の死を誘発するために有効な前記自殺系の少なくとも1つのさらに別の成分を含む薬剤。
36.上記1~22のいずれか1つに記載の前記tsRNAまたは上記24~28のいずれか1つに記載のベクター;任意選択的に、前記トランス-スプライスされたRNAを発現する細胞の死を誘発するために有効な前記自殺系の少なくとも1つのさらに別の成分;およびヒトまたは獣医学的用途に適したキャリアーを含む医薬組成物。
37.前記自殺系の前記1つのさらに別の成分が、ガンシクロビル、シトシンデアミナーゼ-5-フルオロシトシン、シトクロムP450-イホスファミド、シトクロムP450-シクロホスファミドおよびニトロレダクターゼ-5-[アジリジン-1-イル]-2,4-ジニトロベンズアミドを含むかまたはこれらからなる群から選択される、上記36に記載の医薬組成物。
Claims (36)
- 治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである異なる遺伝子におけるそれぞれの少なくとも一部分に対して特異的な複数の結合ドメイン;
少なくとも1つの発現可能な自殺タンパク質または自殺系の成分であるタンパク質をコードする核酸;および
少なくとも1つのスプライスシグナル、
を含むトランス-スプライシングRNA(tsRNA)分子であって、
前記結合ドメインは、内部結合および/または自己相補的配列を有しない少なくとも25個の連続的な非構造化されたヌクレオチド(nt)を含む結合部位を含み、そして前記結合部位内にまたは当該部位の外に、前記結合ドメインは、44ntまたはそれより長い場合、少なくとも1つのまたは複数の、前記遺伝子に対するミスマッチヌクレオチドを有する、
トランス-スプライシングRNA(tsRNA)分子。 - 前記結合部位が、次の個数のヌクレオチドを含むかまたは次の個数のヌクレオチドからなるリストから選択されるヌクレオチドの配列を含む、請求項1に記載のトランス-スプライシングRNA分子:25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、69,70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、153、154、155、156、157、158、159、160、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、177、178、179、180、181、182、183、184、185、186、187、188、189、190、191、192、193、194、195、196、197、198、199、200、201、202、203、204、205、206、207、208、209、210、211、212、213、214、215、216、217、218、219、220、221、222、223、224、225、226、227、228、229、230、231、232、233、234、235、236、237、238、239、240、241、242、243、244、245、246、247、248、249、250、251、252、253、254、255、256、257、258、259、260、261、262、263、264、265、266、267、268、269、270、271、272、273、274、275、276、277、278、279、280、281、282、283、284、285、286、287、288、289、290、291、292、293、294、295、296、297、298、299、300個またはそれを超えるヌクレオチド。
- 前記結合ドメインが、治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである遺伝子の前記一部分に対して少なくとも50%、55%、60%、65%、70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%または100%相補的であるヌクレオチドの配列を含む、請求項1または2に記載のトランス-スプライシングRNA分子。
- 前記結合ドメインにおけるミスマッチが、前記結合部位を含めるかまたは当該結合部位を除いて、標的に対して完全に相補的な45ntのまたはそれより長い区間を回避するように位置する、請求項1~3のいずれか1つに記載のトランス-スプライシングRNA分子。
- 前記ミスマッチが、5’または3’末端から少なくとも5ヌクレオチドである、請求項4に記載のトランス-スプライシングRNA分子。
- 前記核酸が複数の発現可能な自殺タンパク質または自殺系の成分である複数のタンパク質をコードする、請求項1~5のいずれか1つに記載のトランス-スプライシングRNA分子。
- 少なくとも1つの発現可能な自殺タンパク質をコードする前記核酸が、アミノ酸配列を変化させない縮重した選択的コドンを使用することにより生成した2つのA/Gリッチ・エキソニック・スプライス・エンハンサー(ESE)を含む、請求項1~6のいずれか1つに記載のトランス-スプライシングRNA分子。
- 前記tsRNAが3’ERを誘発する、請求項6または7に記載のトランス-スプライシングRNA分子。
- 前記tsRNAが前記結合ドメインに隣接するスペーサー配列も含む、請求項1~8のいずれか1つに記載のトランス-スプライシングRNA分子。
- 前記結合ドメインが、治療すべき疾患に関連するかまたは治療すべき疾患のためのバイオマーカーである遺伝子の同一のもしくは異なる一部分に対して相補的である、請求項1~9のいずれか1つに記載のトランス-スプライシングRNA分子。
- 前記tsRNAが、結合ドメインの外側に、少なくとも1つのシス結合もしくは自己結合ドメインを含む、請求項1~10のいずれか1つに記載のトランス-スプライシングRNA分子。
- 前記tsRNAが、結合ドメインの外側かつ前記分子の3’に、自己相補的な配列の存在のために折りたたまれるかまたは自身と対を形成するRNAの高度に構造化された配列を含む、請求項1~11のいずれか1つに記載のトランス-スプライシングRNA分子。
- 高度に構造化されたRNAが、それとポリA部位の間に位置したスペーサーに隣接する、請求項12に記載のトランス-スプライシングRNA分子。
- 高度に構造化されたRNAが、活性もしくは不活性リボザイムである、請求項13に記載のトランス-スプライシングRNA分子。
- 前記tsRNAが5’ERを誘発する、請求項13または14に記載のトランス-スプライシングRNA分子。
- 前記tsRNAが5’または3’ERを誘発する、請求項1~6または9~14のいずれか1つに記載のトランス-スプライシングRNA分子。
- 前記疾患が、癌またはウイルス感染または細菌感染または転位因子、放射線、化学物質もしくは未知の誘因により誘発された突然変異により引き起こされる後天性遺伝疾患である、請求項1~16のいずれか1つに記載のトランス-スプライシングRNA分子。
- 前記癌が、肝細胞がん(HCC)、子宮頸がん、膣癌、外陰癌、陰茎癌、皮膚癌、悪性黒色腫を含む黒色腫、扁平上皮癌、基底細胞癌、メルケル細胞癌、肺癌、細胞膀胱癌(cell bladder cancer)、乳癌、結腸または直腸癌、肛門癌、子宮内膜癌、腎癌、白血病、急性骨髄性白血病(AML)、急性リンパ性白血病(ALL)、慢性リンパ性白血病(CML)、慢性骨髄性白血病(CML)、有毛細胞白血病(HCL)、T細胞前リンパ球性白血病(P-TLL)、大顆粒リンパ球性白血病、成人T細胞白血病、リンパ腫、骨髄腫、非ホジキンリンパ腫、膵臓癌、前立腺癌、甲状腺癌、鼻咽頭癌、口腔または咽頭癌、口腔咽頭癌、胃癌、脳腫瘍、骨の癌および幹細胞の癌である、請求項17に記載のトランス-スプライシングRNA分子。
- 前記ウイルス感染が、ヒトT細胞白血病ウイルス(HTLV)を含むレトロウイルス、ヒト免疫不全ウイルス1型および2型(HIV-1およびHIV-2)を含むレンチウイルス、16型および18型(HPV-16およびHPV-18)を含むヒトパピローマウイルス、HAV、HBV、HCV、HDVおよびHEVを含む肝炎ウイルス、単純ヘルペス(HSV)、エプスタイン・バーウイルス(EBV)、サイトメガロウイルス(CMV)を含むヘルペスウイルス、アデノウイルス、アデノ随伴ウイルス、インフルエンザウイルスまたは他の任意の組み込みウイルスによる感染である、請求項17に記載のトランス-スプライシングRNA分子。
- 前記細菌感染が、細菌、例えばバントネラ・ヘンセラ(Bartonella henselae)、フランシセラ・ツラレンシス(Francisella tularensis)、リステリア・モノサイトゲネス(Listeria monocytogenes)、サルモネラ種、サルモネラ・チフス(Salmonella typhi)、ブルセラ種、レジオネラ種、マイコバクテリア種、マイコバクテリウム・ツベルクローシス(Mycobacterium tunberculosis)、ノカルジア種、ロドコッカス種、エルシニア種またはナイセリア・メニンギティディス(Neisseria meningitides)による感染である、請求項17に記載のトランス-スプライシングRNA分子。
- 前記の後天性遺伝疾患が、神経線維腫症1型および2型、マッキューン・オルブライト、デュシェンヌ型筋ジストロフィー(DMD)、表皮水疱症、ファンコニAおよびC、フィラデルフィア染色体、血友病AおよびB、嚢胞性線維症、マックル・ウェルズ症候群、リポタンパク質リパーゼ欠損症、B-サラセミアまたはピルビン酸脱水素酵素複合体欠損症である、請求項17に記載のトランス-スプライシングRNA分子。
- 請求項1~21のいずれか1つに記載の前記tsRNAを含む細胞。
- 請求項1~21のいずれか1つに記載の前記tsRNAを含むベクター。
- 前記ベクターが、裸の核酸をベースとするベクター、非ウイルスベクターまたはウイルスベクターである、請求項23に記載のベクター。
- 前記の裸の核酸をベースとするベクターが、RNA分子、プラスミド、DNAミニサークルまたはダンベル型DNA最小ベクターを含む、請求項24に記載のベクター。
- 前記の非ウイルスベクターが、リポソーム小胞、ナノ粒子、ポリマーコンジュゲート、抗体コンジュゲート、細胞貫通ペプチドまたはポリマーカプセルを含む、請求項24に記載のベクター。
- 前記ウイルスベクターが、レトロウイルスベクター、レンチウイルスベクター、アデノウイルスベクター、アデノ随伴ウイルスベクター、単純ヘルペスウイルスベクター、ワクシニアウイルスベクター、キメラウイルスベクター、シンドビス・ウイルスベクターまたはアルファウイルスベクター、セムリキ森林ウイルスベクターおよびベネズエラウマ脳炎ウイルスベクターである、請求項24に記載のベクター。
- 異常細胞を標的化する方法に使用するための請求項1~21のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクターであって、前記方法が、前記tsRNAまたは前記tsRNAを含むベクターでの、in vivoにおける、腫瘍中への、局所適用;経鼻適用;肺胞適用;全身適用;経口適用;静脈内適用;筋肉適用;皮下適用;皮膚適用;腹腔内適用または注射、および、任意選択的に、前記細胞を、前記細胞を殺すために有効な前記自殺系の他の成分(単数または複数)に曝露することを含む、前記tsRNAまたは前記tsRNAを含むベクター。
- 細胞を殺す方法に使用するための請求項1~21のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクターであって、前記方法が、前記細胞を、前記tsRNAまたは前記tsRNAを含むベクターで、ex vivoにおいて、トランスフェクション、リポフェクション、形質導入、エレクトロポレーション、ヌクレオフェクションまたは形質転換すること、および任意選択的に、前記細胞を殺すために有効な前記自殺系の他の成分(単数または複数)に前記細胞を曝露することを含む、前記tsRNAまたは前記tsRNAを含むベクター。
- 疾患を治療する方法に使用するための請求項1~21のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクターであって、前記方法が、異常細胞を、前記tsRNAまたは前記tsRNAを含むベクターで、ex vivoまたはin vivoにおいて、トランスフェクション、リポフェクション、形質導入、エレクトロポレーション、ヌクレオフェクションまたは形質転換すること、および任意選択的に、前記細胞を殺すために有効な前記自殺系の他の成分(単数または複数)に前記細胞を曝露することを含む、前記tsRNAまたは前記tsRNAを含むベクター。
- 前記自殺系の前記成分(単数または複数)が、ガンシクロビル、シトシンデアミナーゼ-5-フルオロシトシン、シトクロムP450-イホスファミド、シトクロムP450-シクロホスファミドおよびニトロレダクダーゼ-5-[アジリジン-1-イル]-2,4-ジニトロベンズアミドを含むかまたはこれらからなる群から選択される、請求項28~30のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクター。
- 前記細胞が哺乳類である、請求項18~21のいずれか1つに記載のトランス-スプライシングRNA分子または請求項22に記載の細胞または請求項28~31のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクター。
- 前記細胞がヒトである、請求項18~21のいずれか1つに記載のトランス-スプライシングRNA分子または請求項22に記載の細胞または請求項28~31のいずれか1つに記載のtsRNAまたは前記tsRNAを含むベクター。
- 請求項1~21のいずれか1つに記載の前記tsRNAまたは請求項23~27のいずれか1つに記載のベクターおよび、任意選択的に、前記トランス-スプライスされたRNAを発現する細胞の死を誘発するために有効な前記自殺系の少なくとも1つのさらに別の成分を含む薬剤。
- 請求項1~21のいずれか1つに記載の前記tsRNAまたは請求項23~27のいずれか1つに記載のベクター;任意選択的に、前記トランス-スプライスされたRNAを発現する細胞の死を誘発するために有効な前記自殺系の少なくとも1つのさらに別の成分;およびヒトまたは獣医学的用途に適したキャリアーを含む医薬組成物。
- 前記自殺系の前記1つのさらに別の成分が、ガンシクロビル、シトシンデアミナーゼ-5-フルオロシトシン、シトクロムP450-イホスファミド、シトクロムP450-シクロホスファミドおよびニトロレダクターゼ-5-[アジリジン-1-イル]-2,4-ジニトロベンズアミドを含むかまたはこれらからなる群から選択される、請求項35に記載の医薬組成物。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023011523A JP2023055809A (ja) | 2016-04-01 | 2023-01-30 | トランス-スプライシングRNA(tsRNA) |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB1605586.5 | 2016-04-01 | ||
| GB201605586 | 2016-04-01 | ||
| PCT/SG2017/050183 WO2017171654A1 (en) | 2016-04-01 | 2017-03-31 | Trans-splicing rna (tsrna) |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023011523A Division JP2023055809A (ja) | 2016-04-01 | 2023-01-30 | トランス-スプライシングRNA(tsRNA) |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2019509756A JP2019509756A (ja) | 2019-04-11 |
| JP2019509756A5 JP2019509756A5 (ja) | 2020-05-14 |
| JP7229467B2 true JP7229467B2 (ja) | 2023-02-28 |
Family
ID=59966148
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018551404A Active JP7229467B2 (ja) | 2016-04-01 | 2017-03-31 | トランス-スプライシングRNA(tsRNA) |
| JP2023011523A Pending JP2023055809A (ja) | 2016-04-01 | 2023-01-30 | トランス-スプライシングRNA(tsRNA) |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023011523A Pending JP2023055809A (ja) | 2016-04-01 | 2023-01-30 | トランス-スプライシングRNA(tsRNA) |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US11517583B2 (ja) |
| EP (1) | EP3436590A4 (ja) |
| JP (2) | JP7229467B2 (ja) |
| CN (1) | CN109642241B (ja) |
| AU (1) | AU2017240703B2 (ja) |
| SG (1) | SG11201808538QA (ja) |
| WO (1) | WO2017171654A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP4045665A4 (en) * | 2019-10-15 | 2023-11-15 | University of Massachusetts | RNA EDITOR ENHANCED RNA TRANS-SPLICING |
| KR20220141829A (ko) * | 2020-02-07 | 2022-10-20 | 유니버시티 오브 로체스터 | 리보자임-매개 rna 조립 및 발현 |
| GB202102118D0 (en) | 2021-02-15 | 2021-03-31 | Cambridge Entpr Ltd | RNA Trans-Splicing molecule |
| GB202108855D0 (en) | 2021-06-21 | 2021-08-04 | Cambridge Entpr Ltd | Methods of eukaryotic gene expression |
| CN113584169A (zh) * | 2021-07-28 | 2021-11-02 | 南京大学 | 一种与肝癌相关的血清tsRNA标志物、探针及其应用 |
| AU2022337146A1 (en) * | 2021-09-03 | 2024-03-14 | Tacit Therapeutics, Inc. | Rna editing via recruitment of spliceosome components |
| WO2023140792A2 (en) * | 2022-01-18 | 2023-07-27 | National University Of Singapore | TRANS-SPLICING RNA (tsRNA) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050202448A1 (en) | 2004-03-15 | 2005-09-15 | Digigenomics Co., Ltd. | Methods for identification, assessment, prevention, and therapy of cancer |
| JP2015534811A (ja) | 2012-11-02 | 2015-12-07 | バウアー,ヨハン | 癌の治療に使用されるrnaトランススプライシング分子(rtm) |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0883344B2 (en) * | 1995-12-15 | 2010-06-09 | VIRxSYS Corporation | Therapeutic molecules generated by trans-splicing |
| US6280978B1 (en) | 1995-12-15 | 2001-08-28 | Intronn Holdings, Llc | Methods and compositions for use in spliceosome mediated RNA trans-splicing |
| DE10139492B4 (de) * | 2001-08-13 | 2004-06-09 | Eul, Joachim, Dr. | Verfahren zur Reparatur einer mutierten RNA aus einer gendefekten DNA und zum gezielten Abtöten von Tumorzellen durch RNA-Transspleißen sowie Verfahren zum Nachweis von natürlich-transgespleißter zellulärer RNA |
| US8003381B2 (en) * | 2002-04-30 | 2011-08-23 | Icon Genetics Gmbh | Amplification vectors based on trans-splicing |
| JP2005528911A (ja) * | 2002-06-05 | 2005-09-29 | イントロン,インコーポレーテッド | スプライセオソーム媒介型rnaトランススプライシング、及びスプライセオソーム媒介型rnaトランススプライシングを利用した第viii因子の遺伝的欠陥の修正 |
| WO2004038380A2 (en) * | 2002-10-23 | 2004-05-06 | Intronn, Inc. | Screening methods for identification of efficient pre-trans-splicing molecules |
| KR100958293B1 (ko) * | 2008-03-27 | 2010-05-19 | 단국대학교 산학협력단 | 테오필린에 의해 표적 특이적 rna 치환 활성이 조절되는알로스테릭 트랜스―스플라이싱 그룹 i 리보자임 |
| KR20110036996A (ko) | 2009-10-05 | 2011-04-13 | 전남대학교산학협력단 | 편평세포암 진단 마커인 ho-1 및 이의 용도 |
| WO2012056441A1 (en) * | 2010-10-28 | 2012-05-03 | Nanodoc Ltd. | Compositions and methods for specific cleavage of exogenous rna in a cell |
| US20150025127A1 (en) * | 2011-08-12 | 2015-01-22 | Virxsys Corporation | Compositions and methods for inducing apoptosis |
| KR101293620B1 (ko) | 2011-08-19 | 2013-08-13 | 국립암센터 | 트랜스-스플라이싱 라이보자임 및 암치료 유전자를 포함하는 재조합 아데노바이러스 및 이의 용도 |
| KR101429696B1 (ko) * | 2012-11-21 | 2014-08-13 | 국립암센터 | 안전성 및 항암활성이 증가된 재조합 아데노바이러스 및 이의 용도 |
| US20140283156A1 (en) * | 2013-03-14 | 2014-09-18 | Cold Spring Harbor Laboratory | Trans-splicing ribozymes and silent recombinases |
-
2017
- 2017-03-31 SG SG11201808538QA patent/SG11201808538QA/en unknown
- 2017-03-31 EP EP17776008.9A patent/EP3436590A4/en active Pending
- 2017-03-31 JP JP2018551404A patent/JP7229467B2/ja active Active
- 2017-03-31 US US16/090,226 patent/US11517583B2/en active Active
- 2017-03-31 AU AU2017240703A patent/AU2017240703B2/en active Active
- 2017-03-31 WO PCT/SG2017/050183 patent/WO2017171654A1/en active Application Filing
- 2017-03-31 CN CN201780034177.5A patent/CN109642241B/zh active Active
-
2022
- 2022-11-10 US US17/984,846 patent/US20240075051A1/en active Pending
-
2023
- 2023-01-30 JP JP2023011523A patent/JP2023055809A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050202448A1 (en) | 2004-03-15 | 2005-09-15 | Digigenomics Co., Ltd. | Methods for identification, assessment, prevention, and therapy of cancer |
| JP2015534811A (ja) | 2012-11-02 | 2015-12-07 | バウアー,ヨハン | 癌の治療に使用されるrnaトランススプライシング分子(rtm) |
Non-Patent Citations (4)
| Title |
|---|
| BMC Cancer,2013年,Vol.13, article No.137,p.1-10 |
| Molecular Oncology,2013年,Vol.7,p.1056-1068 |
| SUSHMITA PODDAR,Chapter4 Results Trans-splicing RNA molecules for 3’and 5’exon labelling (EL) targeting alpha-fetoprotein (AFP), Chapter5 Results Selective killing of AFP positive cells triggered by trans-splicing,RNA trans-splicing for selective killing of virus-transduced or cancer cells,2016年01月,p.67-141 |
| SUSHMITA PODDAR,Chapter4 Results Trans-splicing RNA molecules for 3’and 5’exon labelling (EL) targeting alpha-fetoprotein (AFP),RNA trans-splicing for selective killing of virus-transduced or cancer cells,2016年01月,p.67-110 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20240075051A1 (en) | 2024-03-07 |
| CN109642241A (zh) | 2019-04-16 |
| JP2023055809A (ja) | 2023-04-18 |
| AU2017240703A1 (en) | 2018-10-18 |
| WO2017171654A1 (en) | 2017-10-05 |
| AU2017240703B2 (en) | 2020-05-21 |
| SG11201808538QA (en) | 2018-10-30 |
| EP3436590A1 (en) | 2019-02-06 |
| JP2019509756A (ja) | 2019-04-11 |
| CN109642241B (zh) | 2023-06-27 |
| US20190111072A1 (en) | 2019-04-18 |
| US11517583B2 (en) | 2022-12-06 |
| EP3436590A4 (en) | 2019-12-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7229467B2 (ja) | トランス-スプライシングRNA(tsRNA) | |
| EP3230460B2 (en) | Methods and compositions for selectively eliminating cells of interest | |
| Chappell et al. | Homologous recombination repair factors Rad51 and BRCA1 are necessary for productive replication of human papillomavirus 31 | |
| EP2871239B1 (en) | Cell capable of producing adeno-associated virus vector | |
| JP2021526792A (ja) | 真核細胞における翻訳のための環状rna | |
| KR20200093635A (ko) | 변형된 폐쇄된 말단 dna (cedna)를 사용한 유전자 편집 | |
| CN110177578B (zh) | modRNA的细胞特异性表达 | |
| JP2017506893A (ja) | ウイルス複製不活化組成物並びにその製造方法及び使用 | |
| EP3054993A1 (en) | Permanent gene correction by means of nucleotide-modified messenger rna | |
| US11939575B2 (en) | Modified tracrRNAs gRNAs, and uses thereof | |
| JP2012080889A (ja) | 多コンパートメント真核生物発現系 | |
| Zhitnyuk et al. | Efficient mRNA delivery system utilizing chimeric VSVG-L7Ae virus-like particles | |
| Fechner et al. | Coxsackievirus B3 and adenovirus infections of cardiac cells are efficiently inhibited by vector-mediated RNA interference targeting their common receptor | |
| KR101478869B1 (ko) | 마이크로rna를 이용한 조절을 통한 암 특이적 유전자 치료제 | |
| Painter et al. | Conditional expression of a suicide gene by the telomere reverse transcriptase promoter for potential post‐therapeutic deletion of tumorigenesis | |
| TW202323524A (zh) | Hbb—調節組合物及方法 | |
| JP6483019B2 (ja) | 新規アデノウイルス及びその増殖促進方法 | |
| KR20220018410A (ko) | 세포질에서 자가전사가 가능하고 유전체 편집을 제공하는 rna/dna 시스템 | |
| Berthault et al. | Highly efficient ex-vivo correction of COL7A1 through RNP-based CRISPR/Cas9 and Homology-Directed Repair to treat recessive dystrophic epidermolysis bullosa | |
| Cordelier et al. | Replication-deficient rSV40 mediate pancreatic gene transfer and long-term inhibition of tumor growth | |
| Rahimi et al. | Molecular Approach for HIV-1 Replication Inhibition: Assessment of Different siRNAs Targeting Tat and Nef Genes to Effectively Suppress their Expression. | |
| RU2811724C2 (ru) | РЕДАКТИРОВАНИЕ ГЕНОВ С ИСПОЛЬЗОВАНИЕМ МОДИФИЦИРОВАННОЙ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (зкДНК) | |
| EP4342986A1 (en) | Composition and method for treatment of lca10 using rna-guided nuclease | |
| JP4505566B2 (ja) | 肺癌治療剤 | |
| Kim et al. | Selective regression of cells expressing mouse cytoskeleton-associated protein 2 transcript by trans-splicing ribozyme |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190903 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200330 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20200330 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200330 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210512 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210721 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210924 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211104 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220330 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220621 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20221214 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230106 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230131 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7229467 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |