JP7170642B2 - Adam9を標的とする免疫コンジュゲート及びその使用 - Google Patents
Adam9を標的とする免疫コンジュゲート及びその使用 Download PDFInfo
- Publication number
- JP7170642B2 JP7170642B2 JP2019533514A JP2019533514A JP7170642B2 JP 7170642 B2 JP7170642 B2 JP 7170642B2 JP 2019533514 A JP2019533514 A JP 2019533514A JP 2019533514 A JP2019533514 A JP 2019533514A JP 7170642 B2 JP7170642 B2 JP 7170642B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- adam9
- domain
- cdr
- antibody
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 229940127121 immunoconjugate Drugs 0.000 title claims description 297
- 101000832769 Homo sapiens Disintegrin and metalloproteinase domain-containing protein 9 Proteins 0.000 title claims description 249
- 102100024361 Disintegrin and metalloproteinase domain-containing protein 9 Human genes 0.000 title claims description 210
- 230000008685 targeting Effects 0.000 title description 5
- 230000027455 binding Effects 0.000 claims description 252
- 206010028980 Neoplasm Diseases 0.000 claims description 133
- 239000012634 fragment Substances 0.000 claims description 126
- 150000003839 salts Chemical class 0.000 claims description 126
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 114
- 150000001875 compounds Chemical class 0.000 claims description 78
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 76
- -1 pyrrolobenzodiazepine compound Chemical class 0.000 claims description 67
- 235000001014 amino acid Nutrition 0.000 claims description 57
- 125000000539 amino acid group Chemical group 0.000 claims description 56
- 229910052757 nitrogen Inorganic materials 0.000 claims description 52
- 201000011510 cancer Diseases 0.000 claims description 51
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 claims description 48
- 150000001413 amino acids Chemical class 0.000 claims description 45
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 claims description 44
- 102000054116 human ADAM9 Human genes 0.000 claims description 43
- 229910052799 carbon Inorganic materials 0.000 claims description 40
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 claims description 34
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 30
- 239000008177 pharmaceutical agent Substances 0.000 claims description 29
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 28
- 230000004048 modification Effects 0.000 claims description 28
- 238000012986 modification Methods 0.000 claims description 28
- 239000008194 pharmaceutical composition Substances 0.000 claims description 27
- 201000010099 disease Diseases 0.000 claims description 26
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 claims description 25
- 206010009944 Colon cancer Diseases 0.000 claims description 22
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 20
- 125000001424 substituent group Chemical group 0.000 claims description 20
- 239000011734 sodium Substances 0.000 claims description 19
- 150000001412 amines Chemical class 0.000 claims description 18
- 208000029742 colonic neoplasm Diseases 0.000 claims description 18
- 230000014509 gene expression Effects 0.000 claims description 17
- 230000002633 protecting effect Effects 0.000 claims description 17
- 208000005718 Stomach Neoplasms Diseases 0.000 claims description 14
- 206010017758 gastric cancer Diseases 0.000 claims description 14
- 208000002154 non-small cell lung carcinoma Diseases 0.000 claims description 14
- 201000011549 stomach cancer Diseases 0.000 claims description 14
- 208000029729 tumor suppressor gene on chromosome 11 Diseases 0.000 claims description 14
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 claims description 13
- 210000002966 serum Anatomy 0.000 claims description 13
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical group C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 claims description 12
- 229910052708 sodium Inorganic materials 0.000 claims description 12
- 230000001965 increasing effect Effects 0.000 claims description 11
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 claims description 11
- 206010060862 Prostate cancer Diseases 0.000 claims description 10
- 208000000236 Prostatic Neoplasms Diseases 0.000 claims description 10
- 201000001441 melanoma Diseases 0.000 claims description 10
- 206010006187 Breast cancer Diseases 0.000 claims description 9
- 208000026310 Breast neoplasm Diseases 0.000 claims description 9
- 206010061902 Pancreatic neoplasm Diseases 0.000 claims description 7
- 239000003937 drug carrier Substances 0.000 claims description 7
- 201000002528 pancreatic cancer Diseases 0.000 claims description 7
- 208000006265 Renal cell carcinoma Diseases 0.000 claims description 6
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 claims description 6
- 208000008443 pancreatic carcinoma Diseases 0.000 claims description 6
- 206010008342 Cervix carcinoma Diseases 0.000 claims description 5
- 208000000461 Esophageal Neoplasms Diseases 0.000 claims description 5
- 206010030155 Oesophageal carcinoma Diseases 0.000 claims description 5
- 206010033128 Ovarian cancer Diseases 0.000 claims description 5
- 206010061535 Ovarian neoplasm Diseases 0.000 claims description 5
- 208000024313 Testicular Neoplasms Diseases 0.000 claims description 5
- 206010057644 Testis cancer Diseases 0.000 claims description 5
- 208000024770 Thyroid neoplasm Diseases 0.000 claims description 5
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 claims description 5
- 230000004075 alteration Effects 0.000 claims description 5
- 201000006491 bone marrow cancer Diseases 0.000 claims description 5
- 201000010881 cervical cancer Diseases 0.000 claims description 5
- 201000004101 esophageal cancer Diseases 0.000 claims description 5
- 201000010536 head and neck cancer Diseases 0.000 claims description 5
- 208000014829 head and neck neoplasm Diseases 0.000 claims description 5
- 201000007270 liver cancer Diseases 0.000 claims description 5
- 208000014018 liver neoplasm Diseases 0.000 claims description 5
- 230000001926 lymphatic effect Effects 0.000 claims description 5
- 201000003120 testicular cancer Diseases 0.000 claims description 5
- 201000002510 thyroid cancer Diseases 0.000 claims description 5
- 206010005003 Bladder cancer Diseases 0.000 claims description 4
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 claims description 4
- 208000002495 Uterine Neoplasms Diseases 0.000 claims description 4
- 239000003085 diluting agent Substances 0.000 claims description 4
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 4
- 201000005112 urinary bladder cancer Diseases 0.000 claims description 4
- 206010046766 uterine cancer Diseases 0.000 claims description 4
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 348
- 239000000562 conjugate Substances 0.000 description 143
- 210000004027 cell Anatomy 0.000 description 138
- 241000282414 Homo sapiens Species 0.000 description 108
- 238000000034 method Methods 0.000 description 84
- 241000699670 Mus sp. Species 0.000 description 72
- 238000006467 substitution reaction Methods 0.000 description 69
- 238000006243 chemical reaction Methods 0.000 description 54
- 239000000203 mixture Substances 0.000 description 52
- 239000003814 drug Substances 0.000 description 50
- 229940127089 cytotoxic agent Drugs 0.000 description 45
- 102000004196 processed proteins & peptides Human genes 0.000 description 44
- 239000002254 cytotoxic agent Substances 0.000 description 43
- 229940024606 amino acid Drugs 0.000 description 41
- 229920001184 polypeptide Polymers 0.000 description 40
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 38
- 231100000599 cytotoxic agent Toxicity 0.000 description 37
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 37
- 238000011282 treatment Methods 0.000 description 36
- 239000004472 Lysine Substances 0.000 description 35
- 229940079593 drug Drugs 0.000 description 34
- 108010056243 alanylalanine Proteins 0.000 description 32
- XKUKSGPZAADMRA-UHFFFAOYSA-N glycyl-glycyl-glycine Chemical compound NCC(=O)NCC(=O)NCC(O)=O XKUKSGPZAADMRA-UHFFFAOYSA-N 0.000 description 32
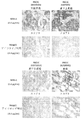
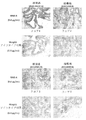
- 238000010186 staining Methods 0.000 description 31
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 29
- 230000037396 body weight Effects 0.000 description 29
- 229910052739 hydrogen Inorganic materials 0.000 description 29
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 29
- 108090000623 proteins and genes Proteins 0.000 description 28
- 239000011347 resin Substances 0.000 description 26
- 229920005989 resin Polymers 0.000 description 26
- 241000282567 Macaca fascicularis Species 0.000 description 25
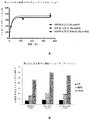
- 230000000259 anti-tumor effect Effects 0.000 description 25
- 235000018102 proteins Nutrition 0.000 description 25
- 102000004169 proteins and genes Human genes 0.000 description 25
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 24
- 230000006870 function Effects 0.000 description 23
- 229910052727 yttrium Inorganic materials 0.000 description 23
- 210000001519 tissue Anatomy 0.000 description 22
- 230000000694 effects Effects 0.000 description 21
- 125000005647 linker group Chemical group 0.000 description 21
- 241001465754 Metazoa Species 0.000 description 20
- 239000000427 antigen Substances 0.000 description 20
- 229910052731 fluorine Inorganic materials 0.000 description 20
- 230000002829 reductive effect Effects 0.000 description 20
- 108091007433 antigens Proteins 0.000 description 19
- 102000036639 antigens Human genes 0.000 description 19
- 239000012636 effector Substances 0.000 description 19
- 150000002466 imines Chemical class 0.000 description 18
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 18
- 230000035772 mutation Effects 0.000 description 18
- 239000003960 organic solvent Substances 0.000 description 17
- 238000012360 testing method Methods 0.000 description 17
- LIWMQSWFLXEGMA-WDSKDSINSA-N Ala-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@H](C)N LIWMQSWFLXEGMA-WDSKDSINSA-N 0.000 description 16
- DEFJQIDDEAULHB-QWWZWVQMSA-N D-alanyl-D-alanine Chemical compound C[C@@H]([NH3+])C(=O)N[C@H](C)C([O-])=O DEFJQIDDEAULHB-QWWZWVQMSA-N 0.000 description 16
- 101800001224 Disintegrin Proteins 0.000 description 16
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 16
- 108060003951 Immunoglobulin Proteins 0.000 description 16
- DEFJQIDDEAULHB-IMJSIDKUSA-N L-alanyl-L-alanine Chemical compound C[C@H](N)C(=O)N[C@@H](C)C(O)=O DEFJQIDDEAULHB-IMJSIDKUSA-N 0.000 description 16
- DEFJQIDDEAULHB-UHFFFAOYSA-N N-D-alanyl-D-alanine Natural products CC(N)C(=O)NC(C)C(O)=O DEFJQIDDEAULHB-UHFFFAOYSA-N 0.000 description 16
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 16
- 231100000433 cytotoxic Toxicity 0.000 description 16
- 230000001472 cytotoxic effect Effects 0.000 description 16
- 108010067216 glycyl-glycyl-glycine Proteins 0.000 description 16
- 102000018358 immunoglobulin Human genes 0.000 description 16
- 238000003364 immunohistochemistry Methods 0.000 description 16
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 15
- 241001529936 Murinae Species 0.000 description 15
- 208000009956 adenocarcinoma Diseases 0.000 description 15
- 150000001768 cations Chemical class 0.000 description 15
- 241000699666 Mus <mouse, genus> Species 0.000 description 14
- 230000036961 partial effect Effects 0.000 description 14
- YUOCYTRGANSSRY-UHFFFAOYSA-N pyrrolo[2,3-i][1,2]benzodiazepine Chemical compound C1=CN=NC2=C3C=CN=C3C=CC2=C1 YUOCYTRGANSSRY-UHFFFAOYSA-N 0.000 description 14
- 210000004881 tumor cell Anatomy 0.000 description 14
- 229910052721 tungsten Inorganic materials 0.000 description 14
- 239000003981 vehicle Substances 0.000 description 14
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 13
- 229940049595 antibody-drug conjugate Drugs 0.000 description 13
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 13
- 239000012528 membrane Substances 0.000 description 13
- 239000002953 phosphate buffered saline Substances 0.000 description 13
- 238000002360 preparation method Methods 0.000 description 13
- 229940124597 therapeutic agent Drugs 0.000 description 13
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 12
- 102100029205 Low affinity immunoglobulin gamma Fc region receptor II-b Human genes 0.000 description 12
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 12
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 12
- 239000000872 buffer Substances 0.000 description 12
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 12
- 238000004519 manufacturing process Methods 0.000 description 12
- FUHCFUVCWLZEDQ-UHFFFAOYSA-N 1-(2,5-dioxopyrrolidin-1-yl)oxy-1-oxo-4-(pyridin-2-yldisulfanyl)butane-2-sulfonic acid Chemical compound O=C1CCC(=O)N1OC(=O)C(S(=O)(=O)O)CCSSC1=CC=CC=N1 FUHCFUVCWLZEDQ-UHFFFAOYSA-N 0.000 description 11
- 102100026120 IgG receptor FcRn large subunit p51 Human genes 0.000 description 11
- 125000000217 alkyl group Chemical group 0.000 description 11
- 238000004458 analytical method Methods 0.000 description 11
- 239000011230 binding agent Substances 0.000 description 11
- 238000000746 purification Methods 0.000 description 11
- 102000029791 ADAM Human genes 0.000 description 10
- 108091022885 ADAM Proteins 0.000 description 10
- 239000004971 Cross linker Substances 0.000 description 10
- 101710177940 IgG receptor FcRn large subunit p51 Proteins 0.000 description 10
- 230000000274 adsorptive effect Effects 0.000 description 10
- 230000001588 bifunctional effect Effects 0.000 description 10
- 125000004432 carbon atom Chemical group C* 0.000 description 10
- 230000001419 dependent effect Effects 0.000 description 10
- 125000000879 imine group Chemical group 0.000 description 10
- 230000001976 improved effect Effects 0.000 description 10
- 230000005764 inhibitory process Effects 0.000 description 10
- 230000003993 interaction Effects 0.000 description 10
- 108091033319 polynucleotide Proteins 0.000 description 10
- 102000040430 polynucleotide Human genes 0.000 description 10
- 239000002157 polynucleotide Substances 0.000 description 10
- 230000001225 therapeutic effect Effects 0.000 description 10
- 230000004614 tumor growth Effects 0.000 description 10
- 108010073969 valyllysine Proteins 0.000 description 10
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- 108010021472 Fc gamma receptor IIB Proteins 0.000 description 9
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 9
- 102100029204 Low affinity immunoglobulin gamma Fc region receptor II-a Human genes 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 229920002684 Sepharose Polymers 0.000 description 9
- 239000002253 acid Substances 0.000 description 9
- 239000000611 antibody drug conjugate Substances 0.000 description 9
- 210000004899 c-terminal region Anatomy 0.000 description 9
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 9
- 210000000981 epithelium Anatomy 0.000 description 9
- 150000002148 esters Chemical class 0.000 description 9
- 239000000178 monomer Substances 0.000 description 9
- 239000000047 product Substances 0.000 description 9
- 102000005962 receptors Human genes 0.000 description 9
- 108020003175 receptors Proteins 0.000 description 9
- 239000011780 sodium chloride Substances 0.000 description 9
- 206010041823 squamous cell carcinoma Diseases 0.000 description 9
- 239000000126 substance Substances 0.000 description 9
- ZJAVYEURWFEFIB-RUUJEGCPSA-N (2,5-dioxopyrrolidin-1-yl) 6-[[(2S)-1-[[(2S)-1-[3-[[(12aS)-8-methoxy-6-oxo-12a,13-dihydroindolo[2,1-c][1,4]benzodiazepin-9-yl]oxymethyl]-5-[[(12aS)-8-methoxy-6-oxo-11,12,12a,13-tetrahydroindolo[2,1-c][1,4]benzodiazepin-9-yl]oxymethyl]anilino]-1-oxopropan-2-yl]amino]-1-oxopropan-2-yl]amino]-6-oxohexanoate Chemical compound COc1cc2c(NC[C@@H]3Cc4ccccc4N3C2=O)cc1OCc1cc(COc2cc3N=C[C@@H]4Cc5ccccc5N4C(=O)c3cc2OC)cc(NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)CCCCC(=O)ON2C(=O)CCC2=O)c1 ZJAVYEURWFEFIB-RUUJEGCPSA-N 0.000 description 8
- KQRHTCDQWJLLME-XUXIUFHCSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-aminopropanoyl]amino]-4-methylpentanoyl]amino]propanoyl]amino]-4-methylpentanoic acid Chemical compound CC(C)C[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)N KQRHTCDQWJLLME-XUXIUFHCSA-N 0.000 description 8
- AGGWFDNPHKLBBV-YUMQZZPRSA-N (2s)-2-[[(2s)-2-amino-3-methylbutanoyl]amino]-5-(carbamoylamino)pentanoic acid Chemical compound CC(C)[C@H](N)C(=O)N[C@H](C(O)=O)CCCNC(N)=O AGGWFDNPHKLBBV-YUMQZZPRSA-N 0.000 description 8
- WEZDRVHTDXTVLT-GJZGRUSLSA-N 2-[[(2s)-2-[[(2s)-2-[(2-aminoacetyl)amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]acetic acid Chemical compound OC(=O)CNC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)CN)CC1=CC=CC=C1 WEZDRVHTDXTVLT-GJZGRUSLSA-N 0.000 description 8
- QXRNAOYBCYVZCD-BQBZGAKWSA-N Ala-Lys Chemical compound C[C@H](N)C(=O)N[C@H](C(O)=O)CCCCN QXRNAOYBCYVZCD-BQBZGAKWSA-N 0.000 description 8
- FSHURBQASBLAPO-WDSKDSINSA-N Ala-Met Chemical compound CSCC[C@@H](C(O)=O)NC(=O)[C@H](C)N FSHURBQASBLAPO-WDSKDSINSA-N 0.000 description 8
- OMLWNBVRVJYMBQ-YUMQZZPRSA-N Arg-Arg Chemical compound NC(N)=NCCC[C@H](N)C(=O)N[C@@H](CCCN=C(N)N)C(O)=O OMLWNBVRVJYMBQ-YUMQZZPRSA-N 0.000 description 8
- DAQIJMOLTMGJLO-YUMQZZPRSA-N Arg-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@@H](N)CCCNC(N)=N DAQIJMOLTMGJLO-YUMQZZPRSA-N 0.000 description 8
- SJUXYGVRSGTPMC-IMJSIDKUSA-N Asn-Ala Chemical compound OC(=O)[C@H](C)NC(=O)[C@@H](N)CC(N)=O SJUXYGVRSGTPMC-IMJSIDKUSA-N 0.000 description 8
- FAQVCWVVIYYWRR-WHFBIAKZSA-N Gln-Ala Chemical compound OC(=O)[C@H](C)NC(=O)[C@@H](N)CCC(N)=O FAQVCWVVIYYWRR-WHFBIAKZSA-N 0.000 description 8
- VHLZDSUANXBJHW-QWRGUYRKSA-N Gln-Phe Chemical compound NC(=O)CC[C@H](N)C(=O)N[C@H](C(O)=O)CC1=CC=CC=C1 VHLZDSUANXBJHW-QWRGUYRKSA-N 0.000 description 8
- MRVYVEQPNDSWLH-XPUUQOCRSA-N Gln-Val Chemical compound CC(C)[C@@H](C(O)=O)NC(=O)[C@@H](N)CCC(N)=O MRVYVEQPNDSWLH-XPUUQOCRSA-N 0.000 description 8
- 108010009504 Gly-Phe-Leu-Gly Proteins 0.000 description 8
- YLEIWGJJBFBFHC-KBPBESRZSA-N Gly-Phe-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@@H](NC(=O)CN)CC1=CC=CC=C1 YLEIWGJJBFBFHC-KBPBESRZSA-N 0.000 description 8
- VAXBXNPRXPHGHG-BJDJZHNGSA-N Ile-Ala-Leu Chemical compound CC[C@H](C)[C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)O)N VAXBXNPRXPHGHG-BJDJZHNGSA-N 0.000 description 8
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 8
- FADYJNXDPBKVCA-UHFFFAOYSA-N L-Phenylalanyl-L-lysin Natural products NCCCCC(C(O)=O)NC(=O)C(N)CC1=CC=CC=C1 FADYJNXDPBKVCA-UHFFFAOYSA-N 0.000 description 8
- LSPYFSHXDAYVDI-SRVKXCTJSA-N Leu-Ala-Leu Chemical compound CC(C)C[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@H](C(O)=O)CC(C)C LSPYFSHXDAYVDI-SRVKXCTJSA-N 0.000 description 8
- NVGBPTNZLWRQSY-UWVGGRQHSA-N Lys-Lys Chemical compound NCCCC[C@H](N)C(=O)N[C@H](C(O)=O)CCCCN NVGBPTNZLWRQSY-UWVGGRQHSA-N 0.000 description 8
- JHKXZYLNVJRAAJ-WDSKDSINSA-N Met-Ala Chemical compound CSCC[C@H](N)C(=O)N[C@@H](C)C(O)=O JHKXZYLNVJRAAJ-WDSKDSINSA-N 0.000 description 8
- MIDZLCFIAINOQN-WPRPVWTQSA-N Phe-Ala Chemical compound OC(=O)[C@H](C)NC(=O)[C@@H](N)CC1=CC=CC=C1 MIDZLCFIAINOQN-WPRPVWTQSA-N 0.000 description 8
- FADYJNXDPBKVCA-STQMWFEESA-N Phe-Lys Chemical compound NCCCC[C@@H](C(O)=O)NC(=O)[C@@H](N)CC1=CC=CC=C1 FADYJNXDPBKVCA-STQMWFEESA-N 0.000 description 8
- RBRNEFJTEHPDSL-ACRUOGEOSA-N Phe-Phe-Lys Chemical compound C([C@@H](C(=O)N[C@@H](CCCCN)C(O)=O)NC(=O)[C@@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 RBRNEFJTEHPDSL-ACRUOGEOSA-N 0.000 description 8
- 229920001213 Polysorbate 20 Polymers 0.000 description 8
- 229930006000 Sucrose Natural products 0.000 description 8
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 8
- HSRXSKHRSXRCFC-WDSKDSINSA-N Val-Ala Chemical compound CC(C)[C@H](N)C(=O)N[C@@H](C)C(O)=O HSRXSKHRSXRCFC-WDSKDSINSA-N 0.000 description 8
- QRZVUAAKNRHEOP-GUBZILKMSA-N Val-Ala-Val Chemical compound [H]N[C@@H](C(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](C(C)C)C(O)=O QRZVUAAKNRHEOP-GUBZILKMSA-N 0.000 description 8
- IBIDRSSEHFLGSD-YUMQZZPRSA-N Val-Arg Chemical compound CC(C)[C@H](N)C(=O)N[C@H](C(O)=O)CCCN=C(N)N IBIDRSSEHFLGSD-YUMQZZPRSA-N 0.000 description 8
- JKHXYJKMNSSFFL-IUCAKERBSA-N Val-Lys Chemical compound CC(C)[C@H](N)C(=O)N[C@H](C(O)=O)CCCCN JKHXYJKMNSSFFL-IUCAKERBSA-N 0.000 description 8
- 108010054982 alanyl-leucyl-alanyl-leucine Proteins 0.000 description 8
- 108010068380 arginylarginine Proteins 0.000 description 8
- 108010036533 arginylvaline Proteins 0.000 description 8
- 238000003556 assay Methods 0.000 description 8
- 239000007853 buffer solution Substances 0.000 description 8
- 239000003795 chemical substances by application Substances 0.000 description 8
- 238000004587 chromatography analysis Methods 0.000 description 8
- 102000006495 integrins Human genes 0.000 description 8
- 108010044426 integrins Proteins 0.000 description 8
- 108010054155 lysyllysine Proteins 0.000 description 8
- 239000013642 negative control Substances 0.000 description 8
- 210000000440 neutrophil Anatomy 0.000 description 8
- 108010024607 phenylalanylalanine Proteins 0.000 description 8
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 8
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 8
- 239000012070 reactive reagent Substances 0.000 description 8
- 239000005720 sucrose Substances 0.000 description 8
- 210000005239 tubule Anatomy 0.000 description 8
- IBIDRSSEHFLGSD-UHFFFAOYSA-N valinyl-arginine Natural products CC(C)C(N)C(=O)NC(C(O)=O)CCCN=C(N)N IBIDRSSEHFLGSD-UHFFFAOYSA-N 0.000 description 8
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 7
- 108010021468 Fc gamma receptor IIA Proteins 0.000 description 7
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 7
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 7
- 102100029193 Low affinity immunoglobulin gamma Fc region receptor III-A Human genes 0.000 description 7
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 7
- 102000005741 Metalloproteases Human genes 0.000 description 7
- 108010006035 Metalloproteases Proteins 0.000 description 7
- 241000283984 Rodentia Species 0.000 description 7
- 238000011579 SCID mouse model Methods 0.000 description 7
- 230000003213 activating effect Effects 0.000 description 7
- 238000003776 cleavage reaction Methods 0.000 description 7
- 125000004185 ester group Chemical group 0.000 description 7
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 7
- 229940072221 immunoglobulins Drugs 0.000 description 7
- 230000000977 initiatory effect Effects 0.000 description 7
- 238000011081 inoculation Methods 0.000 description 7
- 230000007017 scission Effects 0.000 description 7
- 239000012453 solvate Substances 0.000 description 7
- 238000003786 synthesis reaction Methods 0.000 description 7
- 230000004580 weight loss Effects 0.000 description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 6
- 101710116121 Disintegrin and metalloproteinase domain-containing protein 9 Proteins 0.000 description 6
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 6
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 6
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 6
- 241000699660 Mus musculus Species 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 239000002671 adjuvant Substances 0.000 description 6
- 230000008859 change Effects 0.000 description 6
- 238000009295 crossflow filtration Methods 0.000 description 6
- 230000003013 cytotoxicity Effects 0.000 description 6
- 231100000135 cytotoxicity Toxicity 0.000 description 6
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 6
- 210000000987 immune system Anatomy 0.000 description 6
- 238000002513 implantation Methods 0.000 description 6
- 230000006872 improvement Effects 0.000 description 6
- 238000000338 in vitro Methods 0.000 description 6
- 229910052740 iodine Inorganic materials 0.000 description 6
- 210000000265 leukocyte Anatomy 0.000 description 6
- 239000002207 metabolite Substances 0.000 description 6
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 6
- 238000005457 optimization Methods 0.000 description 6
- 229910052698 phosphorus Inorganic materials 0.000 description 6
- 238000004007 reversed phase HPLC Methods 0.000 description 6
- WBHQBSYUUJJSRZ-UHFFFAOYSA-M sodium bisulfate Chemical compound [Na+].OS([O-])(=O)=O WBHQBSYUUJJSRZ-UHFFFAOYSA-M 0.000 description 6
- 229910000342 sodium bisulfate Inorganic materials 0.000 description 6
- 235000010267 sodium hydrogen sulphite Nutrition 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 239000002904 solvent Substances 0.000 description 6
- 239000007929 subcutaneous injection Substances 0.000 description 6
- 238000010254 subcutaneous injection Methods 0.000 description 6
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 6
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 6
- 239000013598 vector Substances 0.000 description 6
- 230000035899 viability Effects 0.000 description 6
- DOKWDOLZCMETIJ-ZAQUEYBZSA-N (12as)-9-[[3-[[(12as)-8-methoxy-6-oxo-11,12,12a,13-tetrahydroindolo[2,1-c][1,4]benzodiazepin-9-yl]oxymethyl]-5-[2-[2-(2-methoxyethoxy)ethoxy]ethyl-(2-methyl-2-sulfanylpropyl)amino]phenyl]methoxy]-8-methoxy-12a,13-dihydroindolo[2,1-c][1,4]benzodiazepin-6-o Chemical compound N1=C[C@@H]2CC3=CC=CC=C3N2C(=O)C(C=C2OC)=C1C=C2OCC1=CC(N(CC(C)(C)S)CCOCCOCCOC)=CC(COC=2C(=CC=3C(=O)N4C5=CC=CC=C5C[C@H]4CNC=3C=2)OC)=C1 DOKWDOLZCMETIJ-ZAQUEYBZSA-N 0.000 description 5
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 5
- 239000004475 Arginine Substances 0.000 description 5
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 5
- 239000004471 Glycine Substances 0.000 description 5
- 101000917824 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-b Proteins 0.000 description 5
- 108010073807 IgG Receptors Proteins 0.000 description 5
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 5
- 241000209094 Oryza Species 0.000 description 5
- 235000007164 Oryza sativa Nutrition 0.000 description 5
- 229910006069 SO3H Inorganic materials 0.000 description 5
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 5
- DWAQJAXMDSEUJJ-UHFFFAOYSA-M Sodium bisulfite Chemical group [Na+].OS([O-])=O DWAQJAXMDSEUJJ-UHFFFAOYSA-M 0.000 description 5
- GLNADSQYFUSGOU-GPTZEZBUSA-J Trypan blue Chemical compound [Na+].[Na+].[Na+].[Na+].C1=C(S([O-])(=O)=O)C=C2C=C(S([O-])(=O)=O)C(/N=N/C3=CC=C(C=C3C)C=3C=C(C(=CC=3)\N=N\C=3C(=CC4=CC(=CC(N)=C4C=3O)S([O-])(=O)=O)S([O-])(=O)=O)C)=C(O)C2=C1N GLNADSQYFUSGOU-GPTZEZBUSA-J 0.000 description 5
- 230000004913 activation Effects 0.000 description 5
- 239000007864 aqueous solution Substances 0.000 description 5
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 5
- 230000003305 autocrine Effects 0.000 description 5
- 210000004369 blood Anatomy 0.000 description 5
- 239000008280 blood Substances 0.000 description 5
- 230000030833 cell death Effects 0.000 description 5
- 230000000875 corresponding effect Effects 0.000 description 5
- 230000006240 deamidation Effects 0.000 description 5
- 230000007717 exclusion Effects 0.000 description 5
- 230000004927 fusion Effects 0.000 description 5
- 108020001507 fusion proteins Proteins 0.000 description 5
- 102000037865 fusion proteins Human genes 0.000 description 5
- 210000003494 hepatocyte Anatomy 0.000 description 5
- 238000004128 high performance liquid chromatography Methods 0.000 description 5
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 5
- 239000002502 liposome Substances 0.000 description 5
- 125000005439 maleimidyl group Chemical group C1(C=CC(N1*)=O)=O 0.000 description 5
- 108010082117 matrigel Proteins 0.000 description 5
- 238000011580 nude mouse model Methods 0.000 description 5
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical compound [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 description 5
- 239000008363 phosphate buffer Substances 0.000 description 5
- 229910052700 potassium Inorganic materials 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 208000015347 renal cell adenocarcinoma Diseases 0.000 description 5
- 235000009566 rice Nutrition 0.000 description 5
- 239000012679 serum free medium Substances 0.000 description 5
- 241000894007 species Species 0.000 description 5
- 238000002560 therapeutic procedure Methods 0.000 description 5
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 5
- 230000003612 virological effect Effects 0.000 description 5
- NJQOCRDPGFWEKA-UHFFFAOYSA-N 1-(2-aminoethyl)pyrrole-2,5-dione;hydrochloride Chemical compound Cl.NCCN1C(=O)C=CC1=O NJQOCRDPGFWEKA-UHFFFAOYSA-N 0.000 description 4
- 125000001433 C-terminal amino-acid group Chemical group 0.000 description 4
- 206010007279 Carcinoid tumour of the gastrointestinal tract Diseases 0.000 description 4
- 201000009030 Carcinoma Diseases 0.000 description 4
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- 241000196324 Embryophyta Species 0.000 description 4
- 206010051066 Gastrointestinal stromal tumour Diseases 0.000 description 4
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 4
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 4
- 101000917839 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-B Proteins 0.000 description 4
- 102000002791 Interleukin-8B Receptors Human genes 0.000 description 4
- 108010018951 Interleukin-8B Receptors Proteins 0.000 description 4
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 206010027476 Metastases Diseases 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 4
- 108010029485 Protein Isoforms Proteins 0.000 description 4
- 102000001708 Protein Isoforms Human genes 0.000 description 4
- 229920005654 Sephadex Polymers 0.000 description 4
- 239000012507 Sephadex™ Substances 0.000 description 4
- RAHZWNYVWXNFOC-UHFFFAOYSA-N Sulphur dioxide Chemical compound O=S=O RAHZWNYVWXNFOC-UHFFFAOYSA-N 0.000 description 4
- 208000034841 Thrombotic Microangiopathies Diseases 0.000 description 4
- 125000004429 atom Chemical group 0.000 description 4
- 210000003719 b-lymphocyte Anatomy 0.000 description 4
- 229940049706 benzodiazepine Drugs 0.000 description 4
- 125000003310 benzodiazepinyl group Chemical group N1N=C(C=CC2=C1C=CC=C2)* 0.000 description 4
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 235000018417 cysteine Nutrition 0.000 description 4
- 238000012217 deletion Methods 0.000 description 4
- 230000037430 deletion Effects 0.000 description 4
- 238000011033 desalting Methods 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 201000011243 gastrointestinal stromal tumor Diseases 0.000 description 4
- 235000013922 glutamic acid Nutrition 0.000 description 4
- 239000004220 glutamic acid Substances 0.000 description 4
- 210000004408 hybridoma Anatomy 0.000 description 4
- 238000001597 immobilized metal affinity chromatography Methods 0.000 description 4
- 230000028993 immune response Effects 0.000 description 4
- 230000002163 immunogen Effects 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 238000001802 infusion Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 238000006317 isomerization reaction Methods 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- 239000007788 liquid Substances 0.000 description 4
- 210000004072 lung Anatomy 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 230000001338 necrotic effect Effects 0.000 description 4
- 102000039446 nucleic acids Human genes 0.000 description 4
- 108020004707 nucleic acids Proteins 0.000 description 4
- 150000007523 nucleic acids Chemical class 0.000 description 4
- NMHMNPHRMNGLLB-UHFFFAOYSA-N phloretic acid Chemical compound OC(=O)CCC1=CC=C(O)C=C1 NMHMNPHRMNGLLB-UHFFFAOYSA-N 0.000 description 4
- 239000013641 positive control Substances 0.000 description 4
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 4
- 235000021251 pulses Nutrition 0.000 description 4
- 239000011541 reaction mixture Substances 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 239000011550 stock solution Substances 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 150000003573 thiols Chemical class 0.000 description 4
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 4
- GHCZTIFQWKKGSB-UHFFFAOYSA-N 2-hydroxypropane-1,2,3-tricarboxylic acid;phosphoric acid Chemical group OP(O)(O)=O.OC(=O)CC(O)(C(O)=O)CC(O)=O GHCZTIFQWKKGSB-UHFFFAOYSA-N 0.000 description 3
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 3
- 108091035707 Consensus sequence Proteins 0.000 description 3
- 238000012286 ELISA Assay Methods 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- 108010087819 Fc receptors Proteins 0.000 description 3
- 102000009109 Fc receptors Human genes 0.000 description 3
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 3
- 208000032612 Glial tumor Diseases 0.000 description 3
- 206010018338 Glioma Diseases 0.000 description 3
- 102100026122 High affinity immunoglobulin gamma Fc receptor I Human genes 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 101000913074 Homo sapiens High affinity immunoglobulin gamma Fc receptor I Proteins 0.000 description 3
- 101000917826 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-a Proteins 0.000 description 3
- 102000009490 IgG Receptors Human genes 0.000 description 3
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 3
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 3
- 101710099301 Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 3
- 102000035195 Peptidases Human genes 0.000 description 3
- 108091005804 Peptidases Proteins 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- 108010076504 Protein Sorting Signals Proteins 0.000 description 3
- 208000000102 Squamous Cell Carcinoma of Head and Neck Diseases 0.000 description 3
- LSNNMFCWUKXFEE-UHFFFAOYSA-N Sulfurous acid Chemical group OS(O)=O LSNNMFCWUKXFEE-UHFFFAOYSA-N 0.000 description 3
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 3
- 239000004473 Threonine Substances 0.000 description 3
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 3
- 238000007792 addition Methods 0.000 description 3
- 125000003277 amino group Chemical group 0.000 description 3
- 239000003708 ampul Substances 0.000 description 3
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 3
- 239000002246 antineoplastic agent Substances 0.000 description 3
- 125000003118 aryl group Chemical group 0.000 description 3
- 235000003704 aspartic acid Nutrition 0.000 description 3
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 230000015556 catabolic process Effects 0.000 description 3
- 230000010261 cell growth Effects 0.000 description 3
- 230000012292 cell migration Effects 0.000 description 3
- 230000036755 cellular response Effects 0.000 description 3
- 235000015165 citric acid Nutrition 0.000 description 3
- 201000002690 colon leiomyosarcoma Diseases 0.000 description 3
- 201000003970 colon lymphoma Diseases 0.000 description 3
- 201000007750 congenital bile acid synthesis defect Diseases 0.000 description 3
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 3
- 238000012303 cytoplasmic staining Methods 0.000 description 3
- 230000001086 cytosolic effect Effects 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 238000006731 degradation reaction Methods 0.000 description 3
- 210000001163 endosome Anatomy 0.000 description 3
- 210000002950 fibroblast Anatomy 0.000 description 3
- 238000000684 flow cytometry Methods 0.000 description 3
- 238000009472 formulation Methods 0.000 description 3
- 210000004602 germ cell Anatomy 0.000 description 3
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 3
- 235000004554 glutamine Nutrition 0.000 description 3
- 201000000459 head and neck squamous cell carcinoma Diseases 0.000 description 3
- 125000000623 heterocyclic group Chemical group 0.000 description 3
- 238000004191 hydrophobic interaction chromatography Methods 0.000 description 3
- 230000005847 immunogenicity Effects 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 108091008042 inhibitory receptors Proteins 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 229960000310 isoleucine Drugs 0.000 description 3
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 3
- 201000005249 lung adenocarcinoma Diseases 0.000 description 3
- 239000008176 lyophilized powder Substances 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 230000009401 metastasis Effects 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 3
- 230000026731 phosphorylation Effects 0.000 description 3
- 238000006366 phosphorylation reaction Methods 0.000 description 3
- 159000000001 potassium salts Chemical class 0.000 description 3
- 238000012545 processing Methods 0.000 description 3
- 230000035755 proliferation Effects 0.000 description 3
- 230000000069 prophylactic effect Effects 0.000 description 3
- 210000002307 prostate Anatomy 0.000 description 3
- 125000006239 protecting group Chemical group 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 230000000717 retained effect Effects 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 238000010532 solid phase synthesis reaction Methods 0.000 description 3
- 208000012972 squamous cell carcinoma of colon Diseases 0.000 description 3
- JJAHTWIKCUJRDK-UHFFFAOYSA-N succinimidyl 4-(N-maleimidomethyl)cyclohexane-1-carboxylate Chemical compound C1CC(CN2C(C=CC2=O)=O)CCC1C(=O)ON1C(=O)CCC1=O JJAHTWIKCUJRDK-UHFFFAOYSA-N 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 3
- 238000002054 transplantation Methods 0.000 description 3
- 238000013414 tumor xenograft model Methods 0.000 description 3
- 208000010576 undifferentiated carcinoma Diseases 0.000 description 3
- 230000003442 weekly effect Effects 0.000 description 3
- VRDGQQTWSGDXCU-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 2-iodoacetate Chemical compound ICC(=O)ON1C(=O)CCC1=O VRDGQQTWSGDXCU-UHFFFAOYSA-N 0.000 description 2
- LLXVXPPXELIDGQ-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(2,5-dioxopyrrol-1-yl)benzoate Chemical compound C=1C=CC(N2C(C=CC2=O)=O)=CC=1C(=O)ON1C(=O)CCC1=O LLXVXPPXELIDGQ-UHFFFAOYSA-N 0.000 description 2
- WGMMKWFUXPMTRW-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-[(2-bromoacetyl)amino]propanoate Chemical compound BrCC(=O)NCCC(=O)ON1C(=O)CCC1=O WGMMKWFUXPMTRW-UHFFFAOYSA-N 0.000 description 2
- PVGATNRYUYNBHO-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-(2,5-dioxopyrrol-1-yl)butanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCN1C(=O)C=CC1=O PVGATNRYUYNBHO-UHFFFAOYSA-N 0.000 description 2
- JSHOVKSMJRQOGY-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-(pyridin-2-yldisulfanyl)butanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCSSC1=CC=CC=N1 JSHOVKSMJRQOGY-UHFFFAOYSA-N 0.000 description 2
- GTBCXYYVWHFQRS-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-(pyridin-2-yldisulfanyl)pentanoate Chemical compound C=1C=CC=NC=1SSC(C)CCC(=O)ON1C(=O)CCC1=O GTBCXYYVWHFQRS-UHFFFAOYSA-N 0.000 description 2
- PMJWDPGOWBRILU-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-[4-(2,5-dioxopyrrol-1-yl)phenyl]butanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCC(C=C1)=CC=C1N1C(=O)C=CC1=O PMJWDPGOWBRILU-UHFFFAOYSA-N 0.000 description 2
- VHYRHFNOWKMCHQ-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 4-formylbenzoate Chemical compound C1=CC(C=O)=CC=C1C(=O)ON1C(=O)CCC1=O VHYRHFNOWKMCHQ-UHFFFAOYSA-N 0.000 description 2
- WCMOHMXWOOBVMZ-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 6-[3-(2,5-dioxopyrrol-1-yl)propanoylamino]hexanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCCCCNC(=O)CCN1C(=O)C=CC1=O WCMOHMXWOOBVMZ-UHFFFAOYSA-N 0.000 description 2
- KVYDWWCHNVBFJG-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 6-hydrazinylpyridine-3-carboxylate;hydrochloride Chemical compound Cl.C1=NC(NN)=CC=C1C(=O)ON1C(=O)CCC1=O KVYDWWCHNVBFJG-UHFFFAOYSA-N 0.000 description 2
- IGVKWAAPMVVTFX-BUHFOSPRSA-N (e)-octadec-5-en-7,9-diynoic acid Chemical compound CCCCCCCCC#CC#C\C=C\CCCC(O)=O IGVKWAAPMVVTFX-BUHFOSPRSA-N 0.000 description 2
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 2
- RVRLFABOQXZUJX-UHFFFAOYSA-N 1-[1-(2,5-dioxopyrrol-1-yl)ethyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1C(C)N1C(=O)C=CC1=O RVRLFABOQXZUJX-UHFFFAOYSA-N 0.000 description 2
- AASYSXRGODIQGY-UHFFFAOYSA-N 1-[1-(2,5-dioxopyrrol-1-yl)hexyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1C(CCCCC)N1C(=O)C=CC1=O AASYSXRGODIQGY-UHFFFAOYSA-N 0.000 description 2
- SGVWDRVQIYUSRA-UHFFFAOYSA-N 1-[2-[2-(2,5-dioxopyrrol-1-yl)ethyldisulfanyl]ethyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1CCSSCCN1C(=O)C=CC1=O SGVWDRVQIYUSRA-UHFFFAOYSA-N 0.000 description 2
- DIYPCWKHSODVAP-UHFFFAOYSA-N 1-[3-(2,5-dioxopyrrol-1-yl)benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)C1=CC=CC(N2C(C=CC2=O)=O)=C1 DIYPCWKHSODVAP-UHFFFAOYSA-N 0.000 description 2
- FPKVOQKZMBDBKP-UHFFFAOYSA-N 1-[4-[(2,5-dioxopyrrol-1-yl)methyl]cyclohexanecarbonyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)C1CCC(CN2C(C=CC2=O)=O)CC1 FPKVOQKZMBDBKP-UHFFFAOYSA-N 0.000 description 2
- VHYRLCJMMJQUBY-UHFFFAOYSA-N 1-[4-[4-(2,5-dioxopyrrol-1-yl)phenyl]butanoyloxy]-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCCC1=CC=C(N2C(C=CC2=O)=O)C=C1 VHYRLCJMMJQUBY-UHFFFAOYSA-N 0.000 description 2
- SVUOLADPCWQTTE-UHFFFAOYSA-N 1h-1,2-benzodiazepine Chemical compound N1N=CC=CC2=CC=CC=C12 SVUOLADPCWQTTE-UHFFFAOYSA-N 0.000 description 2
- WXTMDXOMEHJXQO-UHFFFAOYSA-N 2,5-dihydroxybenzoic acid Chemical compound OC(=O)C1=CC(O)=CC=C1O WXTMDXOMEHJXQO-UHFFFAOYSA-N 0.000 description 2
- ZMRMMAOBSFSXLN-UHFFFAOYSA-N 4-[4-(2,5-dioxopyrrol-1-yl)phenyl]butanehydrazide Chemical compound C1=CC(CCCC(=O)NN)=CC=C1N1C(=O)C=CC1=O ZMRMMAOBSFSXLN-UHFFFAOYSA-N 0.000 description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- ORILYTVJVMAKLC-UHFFFAOYSA-N Adamantane Natural products C1C(C2)CC3CC1CC2C3 ORILYTVJVMAKLC-UHFFFAOYSA-N 0.000 description 2
- 239000012103 Alexa Fluor 488 Substances 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 2
- 208000035473 Communicable disease Diseases 0.000 description 2
- AEMOLEFTQBMNLQ-AQKNRBDQSA-N D-glucopyranuronic acid Chemical compound OC1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@H]1O AEMOLEFTQBMNLQ-AQKNRBDQSA-N 0.000 description 2
- KZSNJWFQEVHDMF-SCSAIBSYSA-N D-valine Chemical compound CC(C)[C@@H](N)C(O)=O KZSNJWFQEVHDMF-SCSAIBSYSA-N 0.000 description 2
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 2
- 102100031113 Disintegrin and metalloproteinase domain-containing protein 15 Human genes 0.000 description 2
- 101800000620 Disintegrin-like Proteins 0.000 description 2
- 208000030453 Drug-Related Side Effects and Adverse reaction Diseases 0.000 description 2
- 108090000371 Esterases Proteins 0.000 description 2
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical class CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 2
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 2
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 208000012766 Growth delay Diseases 0.000 description 2
- 101100334515 Homo sapiens FCGR3A gene Proteins 0.000 description 2
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 2
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 2
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 2
- 108090001090 Lectins Proteins 0.000 description 2
- 102000004856 Lectins Human genes 0.000 description 2
- 241000735235 Ligustrum vulgare Species 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- NQTADLQHYWFPDB-UHFFFAOYSA-N N-Hydroxysuccinimide Chemical group ON1C(=O)CCC1=O NQTADLQHYWFPDB-UHFFFAOYSA-N 0.000 description 2
- 241000283973 Oryctolagus cuniculus Species 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 206010035226 Plasma cell myeloma Diseases 0.000 description 2
- 241000288906 Primates Species 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 2
- 102000006437 Proprotein Convertases Human genes 0.000 description 2
- 108010044159 Proprotein Convertases Proteins 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 2
- 206010070863 Toxicity to various agents Diseases 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- 101710204001 Zinc metalloprotease Proteins 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 230000002411 adverse Effects 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 125000000304 alkynyl group Chemical group 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 230000001130 anti-lysozyme effect Effects 0.000 description 2
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 2
- 235000009582 asparagine Nutrition 0.000 description 2
- 229960001230 asparagine Drugs 0.000 description 2
- 210000003651 basophil Anatomy 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 210000004419 bladder transitional cell Anatomy 0.000 description 2
- 201000007983 brain glioma Diseases 0.000 description 2
- 210000000481 breast Anatomy 0.000 description 2
- 230000036952 cancer formation Effects 0.000 description 2
- 235000013877 carbamide Nutrition 0.000 description 2
- 208000025188 carcinoma of pharynx Diseases 0.000 description 2
- 230000021164 cell adhesion Effects 0.000 description 2
- 210000000170 cell membrane Anatomy 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 239000000919 ceramic Substances 0.000 description 2
- 238000012512 characterization method Methods 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 2
- 239000012539 chromatography resin Substances 0.000 description 2
- 229940001468 citrate Drugs 0.000 description 2
- 201000000493 colon squamous cell carcinoma Diseases 0.000 description 2
- 230000000052 comparative effect Effects 0.000 description 2
- 239000012141 concentrate Substances 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- 230000009260 cross reactivity Effects 0.000 description 2
- 239000002619 cytotoxin Substances 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 238000000502 dialysis Methods 0.000 description 2
- 125000002228 disulfide group Chemical group 0.000 description 2
- 239000002552 dosage form Substances 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- 238000010353 genetic engineering Methods 0.000 description 2
- 102000054766 genetic haplotypes Human genes 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- 210000003630 histaminocyte Anatomy 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 230000003053 immunization Effects 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 239000007928 intraperitoneal injection Substances 0.000 description 2
- 230000009545 invasion Effects 0.000 description 2
- 238000004255 ion exchange chromatography Methods 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- 238000002372 labelling Methods 0.000 description 2
- 239000002523 lectin Substances 0.000 description 2
- 238000012417 linear regression Methods 0.000 description 2
- 230000004807 localization Effects 0.000 description 2
- 208000020816 lung neoplasm Diseases 0.000 description 2
- 201000005243 lung squamous cell carcinoma Diseases 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000002493 microarray Methods 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 235000013336 milk Nutrition 0.000 description 2
- 239000008267 milk Substances 0.000 description 2
- 210000004080 milk Anatomy 0.000 description 2
- 210000001616 monocyte Anatomy 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- 108010068617 neonatal Fc receptor Proteins 0.000 description 2
- 125000006501 nitrophenyl group Chemical group 0.000 description 2
- 239000002773 nucleotide Substances 0.000 description 2
- 125000003729 nucleotide group Chemical group 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 230000002018 overexpression Effects 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 238000002823 phage display Methods 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 230000004481 post-translational protein modification Effects 0.000 description 2
- 235000010259 potassium hydrogen sulphite Nutrition 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 238000002203 pretreatment Methods 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 229940080818 propionamide Drugs 0.000 description 2
- 235000019833 protease Nutrition 0.000 description 2
- 230000020978 protein processing Effects 0.000 description 2
- 230000002285 radioactive effect Effects 0.000 description 2
- 229910052705 radium Inorganic materials 0.000 description 2
- 238000003259 recombinant expression Methods 0.000 description 2
- 238000010188 recombinant method Methods 0.000 description 2
- 238000004064 recycling Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 229910052701 rubidium Inorganic materials 0.000 description 2
- FGDZQCVHDSGLHJ-UHFFFAOYSA-M rubidium chloride Chemical compound [Cl-].[Rb+] FGDZQCVHDSGLHJ-UHFFFAOYSA-M 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- 238000013207 serial dilution Methods 0.000 description 2
- 238000009097 single-agent therapy Methods 0.000 description 2
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical group [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 2
- 235000010262 sodium metabisulphite Nutrition 0.000 description 2
- HHSGWIABCIVPJT-UHFFFAOYSA-M sodium;1-[4-[(2-iodoacetyl)amino]benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)C1=CC=C(NC(=O)CI)C=C1 HHSGWIABCIVPJT-UHFFFAOYSA-M 0.000 description 2
- 230000009870 specific binding Effects 0.000 description 2
- 230000000087 stabilizing effect Effects 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 239000008362 succinate buffer Substances 0.000 description 2
- 238000006277 sulfonation reaction Methods 0.000 description 2
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 2
- 125000003396 thiol group Chemical group [H]S* 0.000 description 2
- 230000009261 transgenic effect Effects 0.000 description 2
- ZDPHROOEEOARMN-UHFFFAOYSA-N undecanoic acid Chemical compound CCCCCCCCCCC(O)=O ZDPHROOEEOARMN-UHFFFAOYSA-N 0.000 description 2
- 238000011144 upstream manufacturing Methods 0.000 description 2
- 239000004474 valine Substances 0.000 description 2
- JKHVDAUOODACDU-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(2,5-dioxopyrrol-1-yl)propanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCN1C(=O)C=CC1=O JKHVDAUOODACDU-UHFFFAOYSA-N 0.000 description 1
- JWDFQMWEFLOOED-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(pyridin-2-yldisulfanyl)propanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCSSC1=CC=CC=N1 JWDFQMWEFLOOED-UHFFFAOYSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- SHAHPWSYJFYMRX-GDLCADMTSA-N (2S)-2-(4-{[(1R,2S)-2-hydroxycyclopentyl]methyl}phenyl)propanoic acid Chemical compound C1=CC([C@@H](C(O)=O)C)=CC=C1C[C@@H]1[C@@H](O)CCC1 SHAHPWSYJFYMRX-GDLCADMTSA-N 0.000 description 1
- LTDQGCFMTVHZKP-UHFFFAOYSA-N (4-bromophenyl)-(4,6-dimethoxy-3-methyl-1-benzofuran-2-yl)methanone Chemical compound O1C2=CC(OC)=CC(OC)=C2C(C)=C1C(=O)C1=CC=C(Br)C=C1 LTDQGCFMTVHZKP-UHFFFAOYSA-N 0.000 description 1
- GHOKWGTUZJEAQD-ZETCQYMHSA-N (D)-(+)-Pantothenic acid Chemical compound OCC(C)(C)[C@@H](O)C(=O)NCCC(O)=O GHOKWGTUZJEAQD-ZETCQYMHSA-N 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-M 1,1-dioxo-1,2-benzothiazol-3-olate Chemical compound C1=CC=C2C([O-])=NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-M 0.000 description 1
- VNJBTKQBKFMEHH-UHFFFAOYSA-N 1-[4-(2,5-dioxopyrrol-1-yl)-2,3-dihydroxybutyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1CC(O)C(O)CN1C(=O)C=CC1=O VNJBTKQBKFMEHH-UHFFFAOYSA-N 0.000 description 1
- WXXSHAKLDCERGU-UHFFFAOYSA-N 1-[4-(2,5-dioxopyrrol-1-yl)butyl]pyrrole-2,5-dione Chemical compound O=C1C=CC(=O)N1CCCCN1C(=O)C=CC1=O WXXSHAKLDCERGU-UHFFFAOYSA-N 0.000 description 1
- NWHAVGHJSKQCHH-UHFFFAOYSA-N 1-[6-(2,5-dioxopyrrol-1-yl)hexanoyloxy]-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCCCCN1C(=O)C=CC1=O NWHAVGHJSKQCHH-UHFFFAOYSA-N 0.000 description 1
- 125000001917 2,4-dinitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C(=C1*)[N+]([O-])=O)[N+]([O-])=O 0.000 description 1
- GVJXGCIPWAVXJP-UHFFFAOYSA-N 2,5-dioxo-1-oxoniopyrrolidine-3-sulfonate Chemical class ON1C(=O)CC(S(O)(=O)=O)C1=O GVJXGCIPWAVXJP-UHFFFAOYSA-N 0.000 description 1
- YVJSYWFYCJWIKW-UHFFFAOYSA-N 2-(2,5-dioxopyrrolidin-1-yl)-2-(4-formylphenoxy)acetic acid Chemical compound O=C1CCC(=O)N1C(C(=O)O)OC1=CC=C(C=O)C=C1 YVJSYWFYCJWIKW-UHFFFAOYSA-N 0.000 description 1
- OWDQCSBZQVISPN-UHFFFAOYSA-N 2-[(2,5-dioxopyrrolidin-1-yl)amino]-4-(2-iodoacetyl)benzoic acid Chemical compound OC(=O)C1=CC=C(C(=O)CI)C=C1NN1C(=O)CCC1=O OWDQCSBZQVISPN-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- ODIAMVWPUHIALN-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperidin-1-yl]ethanesulfonic acid Chemical compound OCCC1CCN(CCS(O)(=O)=O)CC1 ODIAMVWPUHIALN-UHFFFAOYSA-N 0.000 description 1
- XHEYLBRFUKIQMM-UHFFFAOYSA-N 2-aminoethanol;dichloromethane Chemical compound ClCCl.NCCO XHEYLBRFUKIQMM-UHFFFAOYSA-N 0.000 description 1
- NEAQRZUHTPSBBM-UHFFFAOYSA-N 2-hydroxy-3,3-dimethyl-7-nitro-4h-isoquinolin-1-one Chemical class C1=C([N+]([O-])=O)C=C2C(=O)N(O)C(C)(C)CC2=C1 NEAQRZUHTPSBBM-UHFFFAOYSA-N 0.000 description 1
- 125000004398 2-methyl-2-butyl group Chemical group CC(C)(CC)* 0.000 description 1
- 125000004918 2-methyl-2-pentyl group Chemical group CC(C)(CCC)* 0.000 description 1
- 125000004922 2-methyl-3-pentyl group Chemical group CC(C)C(CC)* 0.000 description 1
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 description 1
- UEIZUEWXLJOVLD-UHFFFAOYSA-N 3-(1-methylpyrrolidin-3-yl)pyridine Chemical compound C1N(C)CCC1C1=CC=CN=C1 UEIZUEWXLJOVLD-UHFFFAOYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-M 3-carboxy-2,3-dihydroxypropanoate Chemical compound OC(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-M 0.000 description 1
- 125000004917 3-methyl-2-butyl group Chemical group CC(C(C)*)C 0.000 description 1
- 125000004919 3-methyl-2-pentyl group Chemical group CC(C(C)*)CC 0.000 description 1
- 125000004921 3-methyl-3-pentyl group Chemical group CC(CC)(CC)* 0.000 description 1
- GUPXYSSGJWIURR-UHFFFAOYSA-N 3-octoxypropane-1,2-diol Chemical compound CCCCCCCCOCC(O)CO GUPXYSSGJWIURR-UHFFFAOYSA-N 0.000 description 1
- SLMVEZKWNOGJPD-UHFFFAOYSA-N 4-(pyridin-2-yldisulfanyl)butanoic acid Chemical compound OC(=O)CCCSSC1=CC=CC=N1 SLMVEZKWNOGJPD-UHFFFAOYSA-N 0.000 description 1
- GWEVSJHKQHAKNW-UHFFFAOYSA-N 4-[[1-(2,5-dioxopyrrolidin-1-yl)-2h-pyridin-2-yl]disulfanyl]-2-sulfobutanoic acid Chemical compound OC(=O)C(S(O)(=O)=O)CCSSC1C=CC=CN1N1C(=O)CCC1=O GWEVSJHKQHAKNW-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- 125000004920 4-methyl-2-pentyl group Chemical group CC(CC(C)*)C 0.000 description 1
- 101150017816 40 gene Proteins 0.000 description 1
- ACVAAFHNDGTZLL-UHFFFAOYSA-N 5-(2,5-dioxopyrrol-1-yl)pentanoic acid Chemical compound OC(=O)CCCCN1C(=O)C=CC1=O ACVAAFHNDGTZLL-UHFFFAOYSA-N 0.000 description 1
- HBEDKBRARKFPIC-UHFFFAOYSA-N 6-(2,5-dioxopyrrol-1-yl)hexanoic acid;1-hydroxypyrrolidine-2,5-dione Chemical compound ON1C(=O)CCC1=O.OC(=O)CCCCCN1C(=O)C=CC1=O HBEDKBRARKFPIC-UHFFFAOYSA-N 0.000 description 1
- 108091007505 ADAM17 Proteins 0.000 description 1
- 102000043279 ADAM17 Human genes 0.000 description 1
- 208000010507 Adenocarcinoma of Lung Diseases 0.000 description 1
- GVNWZKBFMFUVNX-UHFFFAOYSA-N Adipamide Chemical compound NC(=O)CCCCC(N)=O GVNWZKBFMFUVNX-UHFFFAOYSA-N 0.000 description 1
- 241000024188 Andala Species 0.000 description 1
- 102220465452 Angiogenin_K64Q_mutation Human genes 0.000 description 1
- 102100022014 Angiopoietin-1 receptor Human genes 0.000 description 1
- 208000037260 Atherosclerotic Plaque Diseases 0.000 description 1
- 230000003844 B-cell-activation Effects 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 108030001720 Bontoxilysin Proteins 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 208000011691 Burkitt lymphomas Diseases 0.000 description 1
- 239000012619 Butyl Sepharose® Substances 0.000 description 1
- FERIUCNNQQJTOY-UHFFFAOYSA-N Butyric acid Natural products CCCC(O)=O FERIUCNNQQJTOY-UHFFFAOYSA-N 0.000 description 1
- 108010075254 C-Peptide Proteins 0.000 description 1
- 101150013553 CD40 gene Proteins 0.000 description 1
- 102100029761 Cadherin-5 Human genes 0.000 description 1
- 101100028791 Caenorhabditis elegans pbs-5 gene Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 241000282465 Canis Species 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- 102000000844 Cell Surface Receptors Human genes 0.000 description 1
- 108010001857 Cell Surface Receptors Proteins 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- 102000012422 Collagen Type I Human genes 0.000 description 1
- 108010022452 Collagen Type I Proteins 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 102220553771 Cyclic GMP-AMP synthase_K62R_mutation Human genes 0.000 description 1
- 108091000069 Cystinyl Aminopeptidase Proteins 0.000 description 1
- 102000030900 Cystinyl aminopeptidase Human genes 0.000 description 1
- 101710112752 Cytotoxin Proteins 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 108010016626 Dipeptides Proteins 0.000 description 1
- 108010053187 Diphtheria Toxin Proteins 0.000 description 1
- 102000016607 Diphtheria Toxin Human genes 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 108700021041 Disintegrin Proteins 0.000 description 1
- 101710121363 Disintegrin and metalloproteinase domain-containing protein 15 Proteins 0.000 description 1
- 102000012545 EGF-like domains Human genes 0.000 description 1
- 108050002150 EGF-like domains Proteins 0.000 description 1
- 108010055323 EphB4 Receptor Proteins 0.000 description 1
- 102100031983 Ephrin type-B receptor 4 Human genes 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 241000282324 Felis Species 0.000 description 1
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 1
- BDAGIHXWWSANSR-UHFFFAOYSA-M Formate Chemical compound [O-]C=O BDAGIHXWWSANSR-UHFFFAOYSA-M 0.000 description 1
- 102100035233 Furin Human genes 0.000 description 1
- 108090001126 Furin Proteins 0.000 description 1
- MVMSCBBUIHUTGJ-GDJBGNAASA-N GDP-alpha-D-mannose Chemical compound C([C@H]1O[C@H]([C@@H]([C@@H]1O)O)N1C=2N=C(NC(=O)C=2N=C1)N)OP(O)(=O)OP(O)(=O)O[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@@H]1O MVMSCBBUIHUTGJ-GDJBGNAASA-N 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- OWXMKDGYPWMGEB-UHFFFAOYSA-N HEPPS Chemical compound OCCN1CCN(CCCS(O)(=O)=O)CC1 OWXMKDGYPWMGEB-UHFFFAOYSA-N 0.000 description 1
- 241001622557 Hesperia Species 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 101000753291 Homo sapiens Angiopoietin-1 receptor Proteins 0.000 description 1
- 101000794587 Homo sapiens Cadherin-5 Proteins 0.000 description 1
- 101000777455 Homo sapiens Disintegrin and metalloproteinase domain-containing protein 15 Proteins 0.000 description 1
- 101000935040 Homo sapiens Integrin beta-2 Proteins 0.000 description 1
- 101000622304 Homo sapiens Vascular cell adhesion protein 1 Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 description 1
- 102000009786 Immunoglobulin Constant Regions Human genes 0.000 description 1
- 108010009817 Immunoglobulin Constant Regions Proteins 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 108700005091 Immunoglobulin Genes Proteins 0.000 description 1
- 102100025390 Integrin beta-2 Human genes 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-N L-arginine Chemical compound OC(=O)[C@@H](N)CCCN=C(N)N ODKSFYDXXFIFQN-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- 125000000510 L-tryptophano group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C(C([H])([H])[C@@]([H])(C(O[H])=O)N([H])[*])C2=C1[H] 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 208000018142 Leiomyosarcoma Diseases 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 208000019693 Lung disease Diseases 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 101000913098 Macaca fascicularis IgG receptor FcRn large subunit p51 Proteins 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 241000699667 Mus spretus Species 0.000 description 1
- KWYHDKDOAIKMQN-UHFFFAOYSA-N N,N,N',N'-tetramethylethylenediamine Chemical compound CN(C)CCN(C)C KWYHDKDOAIKMQN-UHFFFAOYSA-N 0.000 description 1
- LMSMREVZQWXONY-UHFFFAOYSA-N N-(2,5-dioxopyrrolidin-1-yl)-6-hydrazinylpyridine-3-carboxamide propan-2-ylidenehydrazine Chemical compound CC(C)=NN.C1=NC(NN)=CC=C1C(=O)NN1C(=O)CCC1=O LMSMREVZQWXONY-UHFFFAOYSA-N 0.000 description 1
- 125000000729 N-terminal amino-acid group Chemical group 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 206010061309 Neoplasm progression Diseases 0.000 description 1
- 244000061176 Nicotiana tabacum Species 0.000 description 1
- 235000002637 Nicotiana tabacum Nutrition 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 208000015914 Non-Hodgkin lymphomas Diseases 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 206010057249 Phagocytosis Diseases 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 1
- 101000762949 Pseudomonas aeruginosa (strain ATCC 15692 / DSM 22644 / CIP 104116 / JCM 14847 / LMG 12228 / 1C / PRS 101 / PAO1) Exotoxin A Proteins 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- 239000012614 Q-Sepharose Substances 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- 108091030071 RNAI Proteins 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- JQYMGXZJTCOARG-UHFFFAOYSA-N Reactive blue 2 Chemical compound C1=2C(=O)C3=CC=CC=C3C(=O)C=2C(N)=C(S(O)(=O)=O)C=C1NC(C=C1S(O)(=O)=O)=CC=C1NC(N=1)=NC(Cl)=NC=1NC1=CC=CC(S(O)(=O)=O)=C1 JQYMGXZJTCOARG-UHFFFAOYSA-N 0.000 description 1
- 102220485514 Rhodopsin_M33L_mutation Human genes 0.000 description 1
- 102000014400 SH2 domains Human genes 0.000 description 1
- 108050003452 SH2 domains Proteins 0.000 description 1
- 101150099493 STAT3 gene Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 108010084592 Saporins Proteins 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- 108010029180 Sialic Acid Binding Ig-like Lectin 3 Proteins 0.000 description 1
- 102000001555 Sialic Acid Binding Ig-like Lectin 3 Human genes 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 102000000551 Syk Kinase Human genes 0.000 description 1
- 108010016672 Syk Kinase Proteins 0.000 description 1
- 229920002253 Tannate Polymers 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- RYYWUUFWQRZTIU-UHFFFAOYSA-N Thiophosphoric acid Chemical class OP(O)(S)=O RYYWUUFWQRZTIU-UHFFFAOYSA-N 0.000 description 1
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 description 1
- 241000700618 Vaccinia virus Species 0.000 description 1
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 1
- 102100023543 Vascular cell adhesion protein 1 Human genes 0.000 description 1
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000011481 absorbance measurement Methods 0.000 description 1
- 239000008351 acetate buffer Substances 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 230000021736 acetylation Effects 0.000 description 1
- 238000006640 acetylation reaction Methods 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 150000001266 acyl halides Chemical class 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- IAJILQKETJEXLJ-RSJOWCBRSA-N aldehydo-D-galacturonic acid Chemical compound O=C[C@H](O)[C@@H](O)[C@@H](O)[C@H](O)C(O)=O IAJILQKETJEXLJ-RSJOWCBRSA-N 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 229910001860 alkaline earth metal hydroxide Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 229940061720 alpha hydroxy acid Drugs 0.000 description 1
- 150000001280 alpha hydroxy acids Chemical class 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- INJRKJPEYSAMPD-UHFFFAOYSA-N aluminum;silicic acid;hydrate Chemical compound O.[Al].[Al].O[Si](O)(O)O INJRKJPEYSAMPD-UHFFFAOYSA-N 0.000 description 1
- 230000009435 amidation Effects 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- 125000006242 amine protecting group Chemical group 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 239000004037 angiogenesis inhibitor Substances 0.000 description 1
- 150000008064 anhydrides Chemical class 0.000 description 1
- 230000008485 antagonism Effects 0.000 description 1
- 230000000840 anti-viral effect Effects 0.000 description 1
- 230000009830 antibody antigen interaction Effects 0.000 description 1
- 238000011319 anticancer therapy Methods 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 239000003080 antimitotic agent Substances 0.000 description 1
- 210000000709 aorta Anatomy 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 159000000032 aromatic acids Chemical class 0.000 description 1
- 229940072107 ascorbate Drugs 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 229940009098 aspartate Drugs 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229940077388 benzenesulfonate Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 1
- 229940053197 benzodiazepine derivative antiepileptics Drugs 0.000 description 1
- 150000001557 benzodiazepines Chemical class 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 238000007068 beta-elimination reaction Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 230000008512 biological response Effects 0.000 description 1
- 239000000090 biomarker Substances 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 238000010504 bond cleavage reaction Methods 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000012267 brine Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 239000001506 calcium phosphate Substances 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 230000009702 cancer cell proliferation Effects 0.000 description 1
- ZSCYJHGJGRSPAB-UHFFFAOYSA-N carbamic acid Chemical class NC(O)=O.NC(O)=O ZSCYJHGJGRSPAB-UHFFFAOYSA-N 0.000 description 1
- 150000004657 carbamic acid derivatives Chemical class 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 210000001715 carotid artery Anatomy 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 230000020411 cell activation Effects 0.000 description 1
- 238000010609 cell counting kit-8 assay Methods 0.000 description 1
- 230000003306 cell dissemination Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000009920 chelation Effects 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 239000007979 citrate buffer Substances 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 208000022136 colorectal lymphoma Diseases 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 238000009109 curative therapy Methods 0.000 description 1
- 208000030381 cutaneous melanoma Diseases 0.000 description 1
- 231100000409 cytocidal Toxicity 0.000 description 1
- 230000000445 cytocidal effect Effects 0.000 description 1
- 239000000824 cytostatic agent Substances 0.000 description 1
- 230000001085 cytostatic effect Effects 0.000 description 1
- 238000007257 deesterification reaction Methods 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- NAGJZTKCGNOGPW-UHFFFAOYSA-N dithiophosphoric acid Chemical class OP(O)(S)=S NAGJZTKCGNOGPW-UHFFFAOYSA-N 0.000 description 1
- 125000005414 dithiopyridyl group Chemical group 0.000 description 1
- AFOSIXZFDONLBT-UHFFFAOYSA-N divinyl sulfone Chemical compound C=CS(=O)(=O)C=C AFOSIXZFDONLBT-UHFFFAOYSA-N 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 238000012377 drug delivery Methods 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 238000004520 electroporation Methods 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- JOXWSDNHLSQKCC-UHFFFAOYSA-N ethenesulfonamide Chemical compound NS(=O)(=O)C=C JOXWSDNHLSQKCC-UHFFFAOYSA-N 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 238000010195 expression analysis Methods 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 210000001105 femoral artery Anatomy 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 229960000390 fludarabine Drugs 0.000 description 1
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 229910052587 fluorapatite Inorganic materials 0.000 description 1
- 210000000285 follicular dendritic cell Anatomy 0.000 description 1
- 229940017705 formaldehyde sulfoxylate Drugs 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 230000005714 functional activity Effects 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 229940083124 ganglion-blocking antiadrenergic secondary and tertiary amines Drugs 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 229940114119 gentisate Drugs 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229940050410 gluconate Drugs 0.000 description 1
- 229940097042 glucuronate Drugs 0.000 description 1
- 229940097043 glucuronic acid Drugs 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- 125000000404 glutamine group Chemical group N[C@@H](CCC(N)=O)C(=O)* 0.000 description 1
- 239000007973 glycine-HCl buffer Substances 0.000 description 1
- 229960004275 glycolic acid Drugs 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 125000005179 haloacetyl group Chemical group 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical group 0.000 description 1
- 230000002489 hematologic effect Effects 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- KIWQWJKWBHZMDT-UHFFFAOYSA-N homocysteine thiolactone Chemical compound NC1CCSC1=O KIWQWJKWBHZMDT-UHFFFAOYSA-N 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 150000002429 hydrazines Chemical class 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 150000003840 hydrochlorides Chemical class 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- XMBWDFGMSWQBCA-UHFFFAOYSA-N hydrogen iodide Chemical compound I XMBWDFGMSWQBCA-UHFFFAOYSA-N 0.000 description 1
- 229940079826 hydrogen sulfite Drugs 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 150000002443 hydroxylamines Chemical class 0.000 description 1
- 230000033444 hydroxylation Effects 0.000 description 1
- 238000005805 hydroxylation reaction Methods 0.000 description 1
- SBGKURINHGJRFN-UHFFFAOYSA-N hydroxymethanesulfinic acid Chemical compound OCS(O)=O SBGKURINHGJRFN-UHFFFAOYSA-N 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 150000002463 imidates Chemical class 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 230000036737 immune function Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 230000002055 immunohistochemical effect Effects 0.000 description 1
- 238000011532 immunohistochemical staining Methods 0.000 description 1
- 230000004957 immunoregulator effect Effects 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 239000012678 infectious agent Substances 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 108010021518 integrin beta5 Proteins 0.000 description 1
- 230000017306 interleukin-6 production Effects 0.000 description 1
- 230000010039 intracellular degradation Effects 0.000 description 1
- 230000010189 intracellular transport Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 210000004153 islets of langerhan Anatomy 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 150000002519 isoleucine derivatives Chemical group 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 208000003849 large cell carcinoma Diseases 0.000 description 1
- 108010034897 lentil lectin Proteins 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000029226 lipidation Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 210000004185 liver Anatomy 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000037841 lung tumor Diseases 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 239000012931 lyophilized formulation Substances 0.000 description 1
- 239000012516 mab select resin Substances 0.000 description 1
- 150000002680 magnesium Chemical class 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- SVVGCFZPFZGWRG-OTKBOCOUSA-N maytansinoid dm4 Chemical compound CO[C@@H]([C@@]1(O)C[C@H](OC(=O)N1)C(C)(C)[C@@H]1O[C@@]1(C)[C@@H](OC(=O)[C@H](C)N(C)C(=O)CCC(C)(C)S)CC(=O)N1C)\C=C\C=C(C)\CC2=CC(OC)=C(Cl)C1=C2 SVVGCFZPFZGWRG-OTKBOCOUSA-N 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- 239000003094 microcapsule Substances 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 238000007479 molecular analysis Methods 0.000 description 1
- 238000003032 molecular docking Methods 0.000 description 1
- 230000009456 molecular mechanism Effects 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- 229940049964 oleate Drugs 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-M oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC([O-])=O ZQPPMHVWECSIRJ-KTKRTIGZSA-M 0.000 description 1
- 231100000590 oncogenic Toxicity 0.000 description 1
- 230000002246 oncogenic effect Effects 0.000 description 1
- 238000011275 oncology therapy Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 210000000963 osteoblast Anatomy 0.000 description 1
- 229940116315 oxalic acid Drugs 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 125000000636 p-nitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)[N+]([O-])=O 0.000 description 1
- WLJNZVDCPSBLRP-UHFFFAOYSA-N pamoic acid Chemical class C1=CC=C2C(CC=3C4=CC=CC=C4C=C(C=3O)C(=O)O)=C(O)C(C(O)=O)=CC2=C1 WLJNZVDCPSBLRP-UHFFFAOYSA-N 0.000 description 1
- 229940014662 pantothenate Drugs 0.000 description 1
- 235000019161 pantothenic acid Nutrition 0.000 description 1
- 239000011713 pantothenic acid Substances 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- 230000035699 permeability Effects 0.000 description 1
- 230000008782 phagocytosis Effects 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- XNGIFLGASWRNHJ-UHFFFAOYSA-L phthalate(2-) Chemical compound [O-]C(=O)C1=CC=CC=C1C([O-])=O XNGIFLGASWRNHJ-UHFFFAOYSA-L 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 235000002949 phytic acid Nutrition 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 238000003752 polymerase chain reaction Methods 0.000 description 1
- 102000054765 polymorphisms of proteins Human genes 0.000 description 1
- 229920001296 polysiloxane Polymers 0.000 description 1
- 150000003109 potassium Chemical class 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- DJEHXEMURTVAOE-UHFFFAOYSA-M potassium bisulfite Chemical compound [K+].OS([O-])=O DJEHXEMURTVAOE-UHFFFAOYSA-M 0.000 description 1
- IWZKICVEHNUQTL-UHFFFAOYSA-M potassium hydrogen phthalate Chemical compound [K+].OC(=O)C1=CC=CC=C1C([O-])=O IWZKICVEHNUQTL-UHFFFAOYSA-M 0.000 description 1
- RWPGFSMJFRPDDP-UHFFFAOYSA-L potassium metabisulfite Chemical compound [K+].[K+].[O-]S(=O)S([O-])(=O)=O RWPGFSMJFRPDDP-UHFFFAOYSA-L 0.000 description 1
- 235000010263 potassium metabisulphite Nutrition 0.000 description 1
- 230000003334 potential effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- QLNJFJADRCOGBJ-UHFFFAOYSA-N propionamide Chemical compound CCC(N)=O QLNJFJADRCOGBJ-UHFFFAOYSA-N 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 208000023958 prostate neoplasm Diseases 0.000 description 1
- 230000001012 protector Effects 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 230000002797 proteolythic effect Effects 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- WQGWDDDVZFFDIG-UHFFFAOYSA-N pyrogallol Chemical compound OC1=CC=CC(O)=C1O WQGWDDDVZFFDIG-UHFFFAOYSA-N 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000003127 radioimmunoassay Methods 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 238000002708 random mutagenesis Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000010837 receptor-mediated endocytosis Effects 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 238000006722 reduction reaction Methods 0.000 description 1
- 230000008521 reorganization Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 208000030925 respiratory syncytial virus infectious disease Diseases 0.000 description 1
- 230000001177 retroviral effect Effects 0.000 description 1
- 238000004366 reverse phase liquid chromatography Methods 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 102200153431 rs1060501000 Human genes 0.000 description 1
- 102220148488 rs201147592 Human genes 0.000 description 1
- 102200158818 rs35103459 Human genes 0.000 description 1
- 102200081693 rs397514719 Human genes 0.000 description 1
- 229940102127 rubidium chloride Drugs 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000009738 saturating Methods 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000002864 sequence alignment Methods 0.000 description 1
- 125000003607 serino group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(O[H])([H])[H] 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 201000003708 skin melanoma Diseases 0.000 description 1
- 239000003998 snake venom Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- GEHJYWRUCIMESM-UHFFFAOYSA-L sodium sulfite Chemical group [Na+].[Na+].[O-]S([O-])=O GEHJYWRUCIMESM-UHFFFAOYSA-L 0.000 description 1
- MKNJJMHQBYVHRS-UHFFFAOYSA-M sodium;1-[11-(2,5-dioxopyrrol-1-yl)undecanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCCCCCCCCN1C(=O)C=CC1=O MKNJJMHQBYVHRS-UHFFFAOYSA-M 0.000 description 1
- ULARYIUTHAWJMU-UHFFFAOYSA-M sodium;1-[4-(2,5-dioxopyrrol-1-yl)butanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCN1C(=O)C=CC1=O ULARYIUTHAWJMU-UHFFFAOYSA-M 0.000 description 1
- VSIVTUIKYVGDCX-UHFFFAOYSA-M sodium;4-[2-(2-methoxy-4-nitrophenyl)-3-(4-nitrophenyl)tetrazol-2-ium-5-yl]benzene-1,3-disulfonate Chemical compound [Na+].COC1=CC([N+]([O-])=O)=CC=C1[N+]1=NC(C=2C(=CC(=CC=2)S([O-])(=O)=O)S([O-])(=O)=O)=NN1C1=CC=C([N+]([O-])=O)C=C1 VSIVTUIKYVGDCX-UHFFFAOYSA-M 0.000 description 1
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 1
- IZUPJOYPPLEPGM-UHFFFAOYSA-M sodium;hydron;phthalate Chemical compound [Na+].OC(=O)C1=CC=CC=C1C([O-])=O IZUPJOYPPLEPGM-UHFFFAOYSA-M 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000012289 standard assay Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008227 sterile water for injection Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-L sulfite Chemical class [O-]S([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-L 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 150000003461 sulfonyl halides Chemical class 0.000 description 1
- DHCDFWKWKRSZHF-UHFFFAOYSA-N sulfurothioic S-acid Chemical compound OS(O)(=O)=S DHCDFWKWKRSZHF-UHFFFAOYSA-N 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- GFKSKVCFBACPGK-UHFFFAOYSA-N terephthalic acid;hydrochloride Chemical compound Cl.OC(=O)C1=CC=C(C(O)=O)C=C1 GFKSKVCFBACPGK-UHFFFAOYSA-N 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000007970 thio esters Chemical group 0.000 description 1
- 125000000101 thioether group Chemical group 0.000 description 1
- CNHYKKNIIGEXAY-UHFFFAOYSA-N thiolan-2-imine Chemical compound N=C1CCCS1 CNHYKKNIIGEXAY-UHFFFAOYSA-N 0.000 description 1
- 125000000341 threoninyl group Chemical group [H]OC([H])(C([H])([H])[H])C([H])(N([H])[H])C(*)=O 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000011830 transgenic mouse model Methods 0.000 description 1
- 102000035160 transmembrane proteins Human genes 0.000 description 1
- 108091005703 transmembrane proteins Proteins 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- 125000004044 trifluoroacetyl group Chemical group FC(C(=O)*)(F)F 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- 230000005751 tumor progression Effects 0.000 description 1
- 150000003672 ureas Chemical class 0.000 description 1
- 229960005486 vaccine Drugs 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 210000004509 vascular smooth muscle cell Anatomy 0.000 description 1
- 230000003313 weakening effect Effects 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- 230000034365 zymogen activation Effects 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2896—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against molecules with a "CD"-designation, not provided for elsewhere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/68033—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a maytansine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6801—Drug-antibody or immunoglobulin conjugates defined by the pharmacologically or therapeutically active agent
- A61K47/6803—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates
- A61K47/68035—Drugs conjugated to an antibody or immunoglobulin, e.g. cisplatin-antibody conjugates the drug being a pyrrolobenzodiazepine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6835—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site
- A61K47/6871—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment the modifying agent being an antibody or an immunoglobulin bearing at least one antigen-binding site the antibody targeting an enzyme
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/30—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants from tumour cells
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/524—CH2 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/526—CH3 domain
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/71—Decreased effector function due to an Fc-modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/72—Increased effector function due to an Fc-modification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/77—Internalization into the cell
Description
本出願は、2016年12月23日に出願された米国特許出願番号第62/438,488号、2017年3月31日に出願された米国特許出願第62/480,201号に対する優先権を主張し、これらの出願は、その全体が本明細書に参考として組み込まれる。
(I)抗ADAM9抗体またはそのADAM9結合フラグメントは、医薬薬剤に結合されており、
(II)抗ADAM9抗体またはそのADAM9結合フラグメントは、軽鎖可変(VL)ドメインと重鎖可変(VH)ドメインとを含み、前記重鎖可変ドメインは、CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインを含み、前記軽鎖可変ドメインは、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインを含み、
(A)前記CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインは、MAB-Aの最適化された変異体の重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインのアミノ酸配列を有し、前記CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインは、MAB-Aの軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインのアミノ酸配列を有するか、または
(B)前記CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインは、MAB-Aの重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインのアミノ酸配列を有し、前記CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインは、MAB-Aの最適化された変異体の軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインのアミノ酸配列を有するか、または
(C)前記CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインは、MAB-Aの最適化された変異体の重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインのアミノ酸配列を有し、前記CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインは、MAB-Aの最適化された変異体の軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインのアミノ酸配列を有する、免疫コンジュゲートを提供する。
(A)(1)MAB-Aの重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメイン、及び
(2)MAB-Aのヒト化変異体のVHドメインのFR1、FR2、FR3及びFR4、または
(B)(1)MAB-Aの軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメイン、及び
(2)MAB-Aのヒト化変異体のVLドメインのFR1、FR2、FR3及びFR4、または
(C)(1)MAB-Aの最適化された変異体の重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメイン、及び
(2)MAB-Aのヒト化変異体のVHドメインのFR1、FR2、FR3及びFR4、または
(D)(1)MAB-Aの最適化された変異体の軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメイン、及び
(2)MAB-Aのヒト化変異体のVLドメインのFR1、FR2、FR3及びFR4、または
(E)(1)MAB-Aのヒト化/最適化された変異体の重鎖可変(VH)ドメイン、及び
(2)MAB-Aのヒト化/最適化された変異体のVL軽重鎖可変(VL)ドメイン
を含む。
(1)配列番号47(SYWX1H)
(ここで、X1は、MまたはIである)、
(2)配列番号48(EIIPIX2GHTNYNEX3FX4X5)
(ここで、X2、X3、X4及びX5は、独立して選択され、
X2は、NまたはFであり;X3は、KまたはRであり;
X4は、KまたはQであり、
X5は、SまたはGである)、
(3)配列番号49(GGYYYYX6X7X8X9X10X11DY)
(ここで、X6は、P、F、Y、W、I、L、V、T、GまたはDであり、X7、X8、X9、X10及びX11は、
(A)X6がPである場合、
X7は、KまたはRであり;X8は、FまたはMであり;X9は、Gであり;
X10は、WまたはFであり;X11は、M、LまたはKであり;
(B)X6が、F、YまたはWである場合、
X7は、NまたはHであり;X8は、SまたはKであり;X9は、GまたはAであり;
X10は、TまたはVであり;X11は、M、LまたはKであり;
(C)X6が、I、LまたはVである場合、
X7は、Gであり;X8は、Kであり;X9は、GまたはAであり;
X10は、Vであり;X11は、M、LまたはKであり;
(D)X6がTである場合、
X7は、Gであり;X8は、K、MまたはNであり;X9は、Gであり;
X10は、VまたはTであり;X11は、LまたはMであり;
(E)X6がGである場合、
X7は、Gであり;X8は、Sであり;X9は、Gであり;
X10は、Vであり;X11は、Lであり、
(F)X6がDである場合、
X7は、Sであり;X8は、Nであり;X9は、Aであり;
X10は、Vであり;X11は、Lであるように選択される)を有する。
X1は、MまたはIであり;X2は、NまたはFであり;
X3は、KまたはRであり;X4は、KまたはQであり;
X5は、SまたはGであり、X6は、P、F、Y、W、I、L、V、T、GまたはDであり;
X7、X8、X9、X10及びX11は、
X6がPである場合、X7は、KまたはRであり;X8は、FまたはMであり;X9は、Gであり;X10は、WまたはFであり;X11は、M、LまたはKであり;
X6が、F、YまたはWである場合、X7は、NまたはHであり;X8は、SまたはKであり;X9は、GまたはAであり;X10は、TまたはVであり;X11は、M、LまたはKであり;
X6が、I、LまたはVである場合、X7は、Gであり;X8は、Kであり;X9は、GまたはAであり;X10は、Vであり;X11は、M、LまたはKであり;
X6がTである場合、X7は、Gであり;X8は、K、MまたはNであり;X9は、Gであり;X10は、VまたはTであり;X11は、LまたはMであり;
X6がGである場合、X7は、Gであり;X8は、Sであり;X9は、Gであり;X10は、Vであり;X11は、Lであり;
X6がDである場合、X7は、Sであり;X8は、Nであり;X9は、Aであり;X10は、Vであり;X11は、Lであるように選択される。
(1)hMAB-A VH(1)(配列番号16);
(2)hMAB-A VH(2)(配列番号17);
(3)hMAB-A VH(3)(配列番号18);
(4)hMAB-A VH(4)(配列番号19);
(5)hMAB-A VH(2A)(配列番号20);
(6)hMAB-A VH(2B)(配列番号21);
(7)hMAB-A VH(2C)(配列番号22);
(8)hMAB-A VH(2D)(配列番号23);
(9)hMAB-A VH(2E)(配列番号24);
(10)hMAB-A VH(2F)(配列番号25);
(11)hMAB-A VH(2G)(配列番号26);
(12)hMAB-A VH(2H)(配列番号27);
(13)hMAB-A VH(2I)(配列番号28);及び
(14)hMAB-A VH(2J)(配列番号29)からなる群から選択される。
(1)配列番号66(X12ASQSVDYX13GDSYX14N)
(ここで、X12、X13、X14は、独立して選択され、
X12は、KまたはRであり;X13は、DまたはSであり;X14は、MまたはLである);
(2)配列番号13(AASDLES);及び
(3)配列番号67(QQSX15X16X17PFT)
(ここで、X15、X16及びX17は独立して選択され、
X15は、HまたはYであり;X16は、EまたはSであり;X17は、DまたはTである)
のアミノ酸配列を有する。
X12は、KまたはRであり;X13は、DまたはSであり;
X14は、MまたはLであり;X15は、HまたはYであり;
X16は、EまたはSであり;X17は、DまたはTである。
(1)hMAB-A VL(1)(配列番号54);
(2)hMAB-A VL(2)(配列番号55);
(3)hMAB-A VL(3)(配列番号56);
(4)hMAB-A VL(4)(配列番号57);
(5)hMAB-A VL(2A)(配列番号20)からなる群から選択される。
(A)hMAB-A(2I.2)の重鎖可変(VH)ドメイン(配列番号28);または
(B)hMAB-A(2I.2)の軽鎖可変(VL)ドメイン(配列番号55);または
(C)hMAB-A(2I.2)の重鎖可変(VH)ドメイン(配列番号28)及びhMAB-A(2I.2)の軽鎖可変(VL)ドメイン(配列番号55)
を含む。
(a)FcγRに対する変異体Fc領域のアフィニティを下げる1つ以上のアミノ酸改変、及び/または
(b)システイン残基を導入する1つ以上のアミノ酸改変
を含む変異体Fc領域である。いくつかの実施形態では、FcγRに対する変異体Fc領域のアフィニティを下げる1つ以上のアミノ酸改変は、
(A)L234A;
(B)L235A;または
(C)L234A及びL235A
を含み、前記番号付けが、KabatにあるEUインデックスの番号付けである。いくつかの実施形態では、システイン残基を導入する1つ以上のアミノ酸改変は、S442Cを含み、前記番号付けが、KabatにあるEUインデックスの番号付けである。
(a)それぞれ、配列番号8、35及び10及び配列番号62、13、14;
(b)それぞれ、配列番号8、35及び10及び配列番号63、13、14;
(c)それぞれ、配列番号8、36及び10及び配列番号63、13、14
(d)それぞれ、配列番号34、36及び10及び配列番号64、13、65
からなる群から選択される配列を有する、CDRH1ドメイン、CDRH2ドメイン及びCDRH3と、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む。
(a)それぞれ、配列番号17及び配列番号55;
(b)それぞれ、配列番号17及び配列番号56;
(c)それぞれ、配列番号18及び配列番号56;及び
(d)それぞれ、配列番号19及び配列番号57
からなる群から選択される配列に対して少なくとも90%、少なくとも95%または少なくとも99%の同一性を有する配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む。
(a)それぞれ、配列番号17及び配列番号55;
(b)それぞれ、配列番号17及び配列番号56;
(c)それぞれ、配列番号18及び配列番号56;及び
(d)それぞれ、配列番号19及び配列番号57
からなる群から選択される配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む。
(a)それぞれ、配列番号8、35及び37及び配列番号62、13、14;
(b)それぞれ、配列番号8、35及び38及び配列番号62、13、14;
(c)それぞれ、配列番号8、35及び39及び配列番号62、13、14;
(d)それぞれ、配列番号8、35及び40及び配列番号62、13、14;
(e)それぞれ、配列番号8、35及び41及び配列番号62、13、14;
(f)それぞれ、配列番号8、35及び42及び配列番号62、13、14;
(g)それぞれ、配列番号8、35及び43及び配列番号62、13、14;
(h)それぞれ、配列番号8、35及び44及び配列番号62、13、14;
(i)それぞれ、配列番号8、35及び45及び配列番号62、13、14;及び
(j)それぞれ、配列番号8、35及び46及び配列番号62、13、14
からなる群から選択される配列を有する、CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインを含む。
(a)それぞれ、配列番号20及び配列番号55;
(b)それぞれ、配列番号21及び配列番号55;
(c)それぞれ、配列番号22及び配列番号55;
(d)それぞれ、配列番号23及び配列番号55;
(e)それぞれ、配列番号24及び配列番号55;
(f)それぞれ、配列番号25及び配列番号55;
(g)それぞれ、配列番号26及び配列番号55;
(h)それぞれ、配列番号27及び配列番号55;
(i)それぞれ、配列番号28及び配列番号55;及び
(j)それぞれ、配列番号29及び配列番号55
からなる群から選択される配列に対して少なくとも90%、少なくとも95%または少なくとも99%の同一性を有する配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む。
(a)それぞれ、配列番号20及び配列番号55;
(b)それぞれ、配列番号21及び配列番号55;
(c)それぞれ、配列番号22及び配列番号55;
(d)それぞれ、配列番号23及び配列番号55;
(e)それぞれ、配列番号24及び配列番号55;
(f)それぞれ、配列番号25及び配列番号55;
(g)それぞれ、配列番号26及び配列番号55;
(h)それぞれ、配列番号27及び配列番号55;
(i)それぞれ、配列番号28及び配列番号55;及び
(j)それぞれ、配列番号29及び配列番号55
からなる群から選択される配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む。
(a)それぞれ、配列番号50及び配列番号68;
(b)それぞれ、配列番号51及び配列番号68;及び
(c)それぞれ、配列番号52及び配列番号68からなる群から選択される配列を有する重鎖と軽鎖とを含む。
(a)それぞれ、配列番号141及び配列番号68;
(b)それぞれ、配列番号142及び配列番号68;
(c)それぞれ、配列番号143及び配列番号68;
(d)それぞれ、配列番号151及び配列番号68;
(e)それぞれ、配列番号152及び配列番号68;
(f)それぞれ、配列番号153及び配列番号68;及び
(g)それぞれ、配列番号154及び配列番号68
からなる群から選択される配列を有する重鎖と軽鎖とを含む。
CBAは、リシン残基を介してCyL1に共有結合する、本明細書に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL1は、以下の式
NとCとの間の二重線
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は、(C1-C6)アルキルであり;
L’は、以下の式
-NR5-P-C(=O)-(CRaRb)m-C(=O)-(B1’);または
-NR5-P-C(=O)-(CRaRb)m-S-Zs1-(B2’)
によって表され、
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、それぞれ独立して、-H、(C1-C3)アルキル、または帯電した置換基またはイオン化可能な基Qであり;
mは、1~6の整数であり、
Zs1は、以下の式
qは、1~5の整数である。
CBAは、リシン残基を介してCyL2に共有結合する、本明細書に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL2は、以下の式
NとCとの間の二重線
Rx1及びRx2は、独立して、(C1-C6)アルキルであり;
Reは、-Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Zs1は、以下の式
qは、1~5の整数である。
CBAは、リシン残基を介してCyL3に共有結合する、本明細書に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL3は、以下の式
m’は、1または2であり;
R1及びR2は、それぞれ独立して、Hまたは(C1-C3)アルキルであり;
Zs1は、以下の式
qは、1~5の整数である。
CBAは、システイン残基を介してCyC1に共有結合する、本明細書に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC1は、以下の式
NとCとの間の二重線
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、独立して、-H、(C1-C3)アルキルまたは帯電した置換基またはイオン化可能な基Qであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は、(C1-C6)アルキルであり;
LCは、
R19及びR20は、それぞれの場合に、独立して、-Hまたは(C1-C3)アルキルであり;
m”は、1~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルである。
NとCとの間の二重線
CBAは、システイン残基を介してCyC2に共有結合する、本明細書に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC2は、以下の式
NとCとの間の二重線
Rx1は、(C1-C6)アルキルであり;
Reは、Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx2は、(C1-C6)アルキルであり;
Lc’は、以下の式
ここで、
s1は、CBAに共有結合した部位であり、s2は、CyC2上の-S-基に共有結合した部位であり;
Zは、C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドである。
CBAは、システイン残基を介してCyC3に共有結合する、本明細書に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC3は、以下の式
ここで、
m’は、1または2であり;
R1及びR2は、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
LCは、以下の式
ここで、
s1は、CBAに共有結合した部位であり、s2は、CyC3上の-S-基に共有結合した部位であり;
Zは、C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドである。
ここで、
DMは、以下の式
WCは、1または2である。
ここで、
DMは、以下の式
CBAは、それぞれ配列番号8、35及び45及び配列番号62、13、14の配列を有するCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントである。特定の実施形態では、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントは、それぞれ配列番号28及び配列番号55の配列を有する重鎖可変ドメイン(VH)と軽鎖可変ドメイン(VL)とを含む。いくつかの実施形態では、ヒト化抗ADAM9抗体は、それぞれ配列番号142及び配列番号68の配列を有する重鎖と軽鎖とを含む。いくつかの実施形態では、ヒト化抗ADAM9抗体は、それぞれ配列番号152及び配列番号68の配列を有する重鎖と軽鎖とを含み、
WCは、1または2である。いくつかの実施形態では、WCは、2である。
I.抗体及びその結合ドメイン
A.抗体可変ドメインの特性決定
B.抗体定常ドメインの特性決定
1.軽鎖の定常領域
EPKSCDKTHTCPPCP
ERKCCVECPPCP
ESKYGPPCPSCP上述のとおり、IgG4ヒンジ領域は、安定化する突然変異、例えば、S228P置換を含んでいてもよい。例示的な安定化されたヒトIgG4ヒンジ領域のアミノ酸配列は、(配列番号77)である。
ESKYGPPCPPCP
b.Fcγ受容体(FcγR)
FcγRI(CD64)、FcγRIIA(CD32A)及びFcγRIII(CD16)は、活性化する(すなわち、免疫系を向上させる)受容体であり、FcγRIIB(CD32B)は、阻害(すなわち、免疫系を弱める)受容体である。加えて、新生児Fc受容体(FcRn)との相互作用が、エンドソームから細胞表面へのIgG分子の再循環及び血中への放出を媒介する。例示的な野生型IgG1(配列番号1)、IgG2(配列番号2)、IgG3(配列番号3)及びIgG4(配列番号4)のアミノ酸配列を上に提示している。
c.変異体Fc領域
エフェクター機能を減少させるか、または失わせるL234A/L235A置換(下線で示される)と、2つのCH3ドメインが互いにジスルフィド結合によって共有結合するのが可能になるか、または医薬薬剤の結合が可能になるS442C置換(下線で示される)とを含む。このような分子のアミノ酸配列は、(配列番号80)であり、
特に、T250Q、M252Y、S254T、T256E、K288D、T307Q、V308P、A378V、M428L、N434A、H435K及びY436Iから選択される2つ以上の置換。番号付けは、KabatにあるEUインデックスの番号付けである。
(A)M252Y、S254T及びT256E;
(B)M252Y及びS254T;
(C)M252Y及びT256E;
(D)T250Q及びM428L;
(E)T307Q及びN434A;
(F)A378V及びN434A;
(G)N434A及びY436I;
(H)V308P及びN434A;または
(I)K288D及びH435K
の置換を含む変異体IgG Fc領域を有する。
(A)エフェクター機能及び/またはFcγRを変える1つ以上の突然変異と、
(B)血清半減期を延ばす1つ以上の突然変異とを含む変異体Fc領域を有する免疫コンジュゲートを包含する。
II.例示的な抗ADAM9抗体
(1)がん細胞表面で内因性発現する場合に、ヒトADAM9に免疫特異的に結合する能力;
(2)同様の結合アフィニティで、ヒト及び非ヒト霊長類ADAM9(例えば、カニクイザルADAM9)に特異的に結合する;
(3)4nM以下の平衡結合定数(KD)で、ヒトADAM9に特異的に結合する;
(4)4nM以下の平衡結合定数(KD)で、非ヒト霊長類ADAM9に特異的に結合する;
(5)5×105M-1分-1以上のオンレート(ka)で、ヒトADAM9に特異的に結合する;
(6)1×106M-1分-1以上のオンレート(ka)で、非ヒト霊長類ADAM9に特異的に結合する;
(7)1×10-3分-1以下のオフレート(kd)でヒトADAM9に特異的に結合する;
(8)9×10-4分-1以下のオフレート(kd)で非ヒト霊長類ADAM9に特異的に結合する。
(9)キメラまたはマウス親抗体と比較して、cyno ADAM9に対する結合アフィニティ(例えば、BIACORE(登録商標)分析によって決定されるような)において、少なくとも100倍の向上(例えば、少なくとも100倍、少なくとも150倍、少なくとも200倍、少なくとも250倍、少なくとも300倍、少なくとも350倍、少なくとも400倍、少なくとも450倍、少なくとも500倍、少なくとも550倍、または少なくとも600倍の向上)を有し、ヒトADAM9に対する高アフィニティ結合(例えば、BIACORE(登録商標)分析)を保持するように最適化される。
A.マウス抗ヒトADAM9抗体
(A)(1)MAB-AのVHドメインの3個のCDRH;及び
(2)MAB-Aのヒト化変異体のVHドメインの4個のFR;または
(B)(1)MAB-AのVLドメインの3個のCDRL;及び
(2)MAB-Aのヒト化変異体のVLドメインの4個のFR;または
(C)MAB-Aの最適化された変異体のVHドメインの3個のCDRH;及び
MAB-AのVLドメインの3個のCDRL;または
(D)MAB-AのVHドメインの3個のCDRH;及び最適化された変異体MAB-AのVLドメインの3個のCDRL;または
(E)MAB-Aの最適化された変異体のVHドメインの3個のCDRH;及び最適化されたMAB-AのVLドメインの3個のCDRL;または
(F)(1)MAB-Aの最適化された変異体のVHドメインの3個のCDRH;及び
(2)MAB-Aのヒト化変異体のVHドメインの4個のFR;または
(G)(1)MAB-Aの最適化された変異体のVLドメインの3個のCDRL;及び
(2)MAB-Aのヒト化変異体のVLドメインの4個のFR;または
(H)(1)MAB-Aのヒト化/最適化された変異体のVHドメイン;及び
(2)MAB-Aのヒト化/最適化された変異体のVLドメイン
を含む免疫コンジュゲートに関する。マウス抗体「MAB-A」
B.例示的なヒト化/最適化された抗ADAM9-VHドメイン及びVLドメイン
1.MAB-Aの変異体VHドメイン
X1は、MまたはIであり;X2は、NまたはFであり;
X3は、KまたはRであり;X4は、KまたはQであり;
X5は、SまたはGであり、及びX6は、P、F、Y、W、I、L、V、T、GまたはDであり;
X7、X8、X9、X10及びX11は、以下になるように選択される。
hMAB-A VH(2)(配列番号17) hMAB-A VH(2D)(配列番号23)
hMAB-A VH(3)(配列番号18) hMAB-A VH(2E)(配列番号24)
hMAB-A VH(4)(配列番号19) hMAB-A VH(2F)(配列番号25)
hMAB-A VH(2A)(配列番号20) hMAB-A VH(2G)(配列番号26)
hMAB-A VH(2B)(配列番号21) hMAB-A VH(2H)(配列番号27)
hMAB-A VH(2C)(配列番号22) hMAB-A VH(2I)(配列番号28)
及びhMAB-A VH(2J)(配列番号29)
を以下に示す(CDRH残基は、1本の下線が引かれた状態で示されている。hMAB-A VH(1)(配列番号7)に関する差は、二重下線で示されている)。
FRH1ドメイン(配列番号30):EVQLVESGGGLVKPGGSLRLSCAASGFTFS
FRH2ドメイン(配列番号31):WVRQAPGKGLEWVG
FRH3ドメイン(配列番号32):RFTISLDNSKNTLYLQMGSLRAEDTAVYYCAR
FRH4ドメイン(配列番号33):WGQGTTVTVSS
配列番号8:SYWMH
配列番号34:SYWIH
配列番号9:EIIPINGHTNYNEKFKS
配列番号35:EIIPIFGHTNYNEKFKS
配列番号36:EIIPIFGHTNYNERFQG
配列番号10:GGYYYYGSRDYFDY
配列番号37:GGYYYYFNSGTLDY
配列番号38:GGYYYYIGKGVLDY
配列番号39:GGYYYYPRFGWLDY
配列番号40:GGYYYYTGKGVLDY
配列番号41:GGYYYYDSNAVLDY
配列番号42:GGYYYYFHSGTLDY
配列番号43:GGYYYYFNKAVLDY
配列番号44:GGYYYYGGSGVLDY
配列番号45:GGYYYYPRQGFLDY
配列番号46:GGYYYYYNSGTLDY
(1)以下のアミノ酸配列を有するCDRH1ドメイン
配列番号47:SYWX1H
ここで、X1は、MまたはIであり;
(2)以下のアミノ酸配列を有するCDRH2ドメイン
配列番号48:EIIPIX2GHTNYNEX3FX4X5
X2、X3、X4及びX5は、独立して選択され、
X2は、NまたはFであり;X3は、KまたはRであり;
X4は、KまたはQであり;X5は、SまたはGである。
及び
(3)以下のアミノ酸配列を有するCDRH3ドメイン
配列番号49:GGYYYYX6X7X8X9X10X11DY
ここで、X6は、P、F、Y、W、I、L、V、T、GまたはDであり、X7、X8、X9、X10は、以下になるように選択される。
2.MAB-Aの変異体VLドメイン
X12は、KまたはRであり;X13は、DまたはSであり;
X14は、MまたはLであり;X15は、HまたはYであり;
X16は、EまたはSであり;X17は、DまたはTである。
FRL1ドメイン(配列番号58):DIVMTQSPDSLAVSLGERATISC
FRL2ドメイン(配列番号59):WYQQKPGQPPKLLIY
FRL3ドメイン(配列番号60):GIPARFSGSGSGTDFTLTISSLEPEDFATYYC
FRL4ドメイン(配列番号61):FGQGTKLEIK
配列番号12:KASQSVDYDGDSYMN
配列番号62:KASQSVDYSGDSYMN
配列番号63:RASQSVDYSGDSYMN
配列番号64:RASQSVDYSGDSYLN
配列番号14:QQSHEDPFT
配列番号65:QQSYSTPFT
(1)以下のアミノ酸配列を有するCDRL1ドメイン
配列番号66:X12ASQSVDYX13GDSYX14N
ここで、X12、X13、X14は、独立して選択され、
X12は、KまたはRであり;X13は、DまたはSであり;X14は、MまたはLであり;
(2)以下のアミノ酸配列を有するCDRL2ドメイン
配列番号13:AASDLES
及び
(3)以下のアミノ酸配列を有するCDRL3ドメイン
配列番号67:QQSX15X16X17PFT
ここで、X15、X16,及びX17は、独立して選択され、
X15は、HまたはYであり;X16は、EまたはSであり;X17は、DまたはTである。
(a)それぞれ、配列番号8、35及び10及び配列番号62、13、14;
(b)それぞれ、配列番号8、35及び10及び配列番号63、13、14;
(c)それぞれ、配列番号8、36及び10及び配列番号63、13、14;
(d)それぞれ、配列番号34、36及び10及び配列番号64、13、65;
(e)それぞれ、配列番号8、35及び37及び配列番号62、13、14;
(f)それぞれ、配列番号8、35及び38及び配列番号62、13、14;
(g)それぞれ、配列番号8、35及び39及び配列番号62、13、14;
(h)それぞれ、配列番号8、35及び40及び配列番号62、13、14;
(i)それぞれ、配列番号8、35及び41及び配列番号62、13、14;
(j)それぞれ、配列番号8、35及び42及び配列番号62、13、14;
(k)それぞれ、配列番号8、35及び43及び配列番号62、13、14;
(l)それぞれ、配列番号8、35及び44及び配列番号62、13、14;
(m)それぞれ、配列番号8、35及び45及び配列番号62、13、14;及び
(n)それぞれ、配列番号8、35及び46及び配列番号62、13、14
からなる群から選択される配列を有する、CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインを含む。
(a)それぞれ、配列番号17及び配列番号55;
(b)それぞれ、配列番号17及び配列番号56;
(c)それぞれ、配列番号18及び配列番号56;
(d)それぞれ、配列番号19及び配列番号57;
(e)それぞれ、配列番号20及び配列番号55;
(f)それぞれ、配列番号21及び配列番号55;
(g)それぞれ、配列番号22及び配列番号55;
(h)それぞれ、配列番号23及び配列番号55;
(i)それぞれ、配列番号24及び配列番号55;
(j)それぞれ、配列番号25及び配列番号55;
(k)それぞれ、配列番号26及び配列番号55;
(l)それぞれ、配列番号27及び配列番号55;
(m)それぞれ、配列番号28及び配列番号55;及び
(n)それぞれ、配列番号29及び配列番号55
の配列に対して少なくとも90%、少なくとも95%、少なくとも99%または100%の同一性を有する配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む。
(a)それぞれ、配列番号50及び配列番号68;
(b)それぞれ、配列番号51及び配列番号68;
(c)それぞれ、配列番号52及び配列番号68;
(d)それぞれ、配列番号141及び配列番号68;
(e)それぞれ、配列番号142及び配列番号68;
(f)それぞれ、配列番号143及び配列番号68;
(g)それぞれ、配列番号151及び配列番号68;
(h)それぞれ、配列番号152及び配列番号68;
(i)それぞれ、配列番号153及び配列番号68;及び
(j)それぞれ、配列番号154及び配列番号68。
III.抗体薬物コンジュゲート
定義
A.例示的な免疫コンジュゲート
CBAは、リシン残基を介してCyL1に共有結合する、本明細書で上に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL1は、以下の式
NとCとの間の二重線
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は、(C1-C6)アルキルであり;
L’は、以下の式
-NR5-P-C(=O)-(CRaRb)m-C(=O)-(B1’);または
-NR5-P-C(=O)-(CRaRb)m-S-Zs1-(B2’)
によって表され、
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、それぞれ独立して、-H、(C1-C3)アルキル、または帯電した置換基またはイオン化可能な基Qであり;
mは、1~6の整数であり、
Zs1は、以下の式
qは、1~5の整数である。
Xは存在せず、Yは-Hである。別のより具体的な実施形態では、NとCとの間の二重線
CBAは、リシン残基を介してCyL2に共有結合する、本明細書で上に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL2は、以下の式
NとCとの間の二重線
Rx1及びRx2は、独立して、(C1-C6)アルキルであり;
Reは、-Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Zs1は、以下の式
qは、1~5の整数である。
CBAは、リシン残基を介してCyL3に共有結合する、本明細書で上に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL3は、以下の式
m’は、1または2であり;
R1及びR2は、それぞれ独立して、Hまたは(C1-C3)アルキルであり;
Zs1は、以下の式
qは、1~5の整数である。
CBAは、システイン残基を介してCyC1に共有結合する、本明細書に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC1は、以下の式
NとCとの間の二重線
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、独立して、-H、(C1-C3)アルキルまたは帯電した置換基またはイオン化可能な基Qであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は、(C1-C6)アルキルであり;
LCは、
R19及びR20は、それぞれの場合に、独立して、-Hまたは(C1-C3)アルキルであり;
m”は、1~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルである。
Xは存在せず、Yは-Hである。別のより具体的な実施形態では、NとCとの間の二重線
CBAは、システイン残基を介してCyC2に共有結合する、本明細書で上に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC2は、以下の式
NとCとの間の二重線
Rx1は、(C1-C6)アルキルであり;
Reは、Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx2は、(C1-C6)アルキルであり;
LC’は、以下の式
ここで、
s1は、CBAに共有結合した部位であり、s2は、CyC2上の-S-基に共有結合した部位であり;
Zは、C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、-H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドである。
Xは存在せず、Yは-Hである。別の具体的な実施形態では、NとCとの間の二重線
CBAは、システイン残基を介してCyC3に共有結合する、本明細書で上に記載の本発明の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC3は、以下の式
ここで、
m’は、1または2であり;
R1及びR2は、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
LC’は、以下の式
ここで、
s1は、CBAに共有結合した部位であり、s2は、CyC3上の-S-基に共有結合した部位であり;
Zは、C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドである。
C.例示的なリンカー分子
特定の実施形態では、二官能リンカーは、以下に記載する式(a1L)~(a10L)のいずれか1つによって表される。
D.例示的な医薬薬剤
1.メイタンシノイド
Lc’は、以下の式
-NR5-P-C(=O)-(CRaRb)m-C(=O)E (B1);または
-NR5-P-C(=O)-(CRaRb)m-S-Zs (B2)
によって表され、
C(=O)Eは、反応性エステル基、例えば、N-ヒドロキシスクシンイミドエステル、N-ヒドロキシスルホスクシンイミドエステル、ニトロフェニル(例えば、2または4-ニトロフェニル)エステル、ジニトロフェニル(例えば、2,4-ジニトロフェニル)エステル、スルホ-テトラフルオロフェニル(例えば、4-スルホ-2,3,5,6-テトラフルオロフェニル)エステル、またはペンタフルオロフェニルエステル、好ましくはN-ヒドロキシスクシンイミドエステルであり;
Zsは、以下の式
ここで、
qは、1~5の整数であり;
Uは、-HまたはSO3H、またはその医薬的に許容される塩であり、残りの可変部分は、第1の実施形態の第1~12及び第17の具体的な実施形態のいずれか1つまたはそこに記載される任意のより具体的な実施形態において上に記載したとおりである。
式(C1a’)、(C1a’1)、(C1b’)及び(C1b’1)の-LC Cは、以下の式
式(C2a”)、(C2a”1)、(C2b””)及び(C2b”1)の-LC C’は、以下の式
好ましくは、アミノ酸置換は、保存的であろう(すなわち、置換アミノ酸が、元々のアミノ酸と同様の化学特性を有している)。このような保存的置換は、当該技術分野で知られており、例を上に提示している。アミノ酸改変は、領域(例えば可変ドメイン)の完全な再設計のために、1つ以上のアミノ酸を交換するか、または改変するものまでの範囲であってもよい。可変ドメインを交換すると、結合アフィニティ及び/または特異性が変化する場合がある。他の改変方法は、当該技術分野で既知のカップリング技術、限定されないが、酵素手段、酸化置換及びキレート化を含む技術を用いることを含む。例えば、イムノアッセイのための標識の接続、例えば、ラジオイムノアッセイのための放射性部分の接続に、改変を使用してもよい。改変ポリペプチドは、当該技術分野で確立された手順を用いて作られ、当該技術分野で既知の標準的なアッセイを用いてスクリーニングすることができる。
V.薬物の結合
(a)細胞毒性薬と、アミン反応性基及びチオール反応性基を有するリンカー化合物とを反応させ、アミン反応性基が結合した細胞毒性薬-リンカー化合物を形成する工程と、
(b)CBAと、細胞毒性薬-リンカー化合物とを反応させる工程とを含む、第2の方法によって調製することができる。
(a)CBAと、アミン反応性基及びチオール反応性基を有するリンカー化合物とを反応させ、チオール反応性基が結合した改変CBAを形成する工程と、
(b)改変CBAと、細胞毒性薬とを反応させる工程とを含む、第3の方法によって調製することができる。
ここで、Xはハロゲン;JD-SH、-SSRd、または-SC(=O)Rgであり;Rdは、フェニル、ニトロフェニル、ジニトロフェニル、カルボキシニトロフェニル、ピリジルまたはニトロピリジルであり;Rgは、アルキルであり;残りの可変部分は、式(a1)~(a10)について上に記載したとおりであり、細胞毒性薬は、以下の式
ここで、NとCとの間の
二重線
Xは存在せず、Yは-Hである。別のより具体的な実施形態では、NとCとの間の二重線
(a)上述のチオール反応性基を有するイミン含有細胞毒性薬のイミン部分(すなわち、式(C1a’)、(C1a’1)、(C1b’)、(C1b’1)、(C2a”)、(C2a”1)、(C2b”)または(C2b”1)、ここで、NとCとの間の二重線
(b)改変細胞毒性薬と、本明細書に記載の抗ADAM9抗体またはそのADAM9結合フラグメントとを反応させ、免疫コンジュゲートを形成することによって調製することができる。
VI.本発明の免疫コンジュゲートの使用
VII.医薬組成物
VIII.投与方法
抗ADAM9抗体MAB-Aの腫瘍細胞特異性
マウス抗ADAM9抗体(本明細書でMAB-Aと呼ばれる)は、(1)ADAM9の標的タンパク質処理活性をブロックし、(2)内部移行し、(3)抗腫瘍活性を有することが同定された(例えば、米国特許第8,361,475号を参照)。MAB-Aの腫瘍細胞特異性を、IHCによって観察した。腫瘍組織をMAB-A(0.4μg/mL)と接触させるか、またはアイソタイプ対照(0.4μg/mL)と接触させ、染色の程度を視覚化した。MAB-Aは、種々の大細胞癌、扁平上皮癌及び腺癌非小細胞肺癌細胞型(図1A)、乳癌細胞、前立腺癌細胞、胃癌細胞(図1B)及び結腸癌サンプル(図1C)を強く標識することがわかった。正常組織をMAB-A(1.25μg/mL)と接触させ、染色の程度を視覚化した。上の表2にまとめたように、MAB-Aは、多種多様な正常組織の染色をほとんど示さないか、または全く示さなかった。これらの試験に使用したMAB-Aの濃度は、腫瘍細胞の染色に使用したもののほぼ3倍であったことを注記しておく。これらのIHC試験の結果は、MAB-Aが、正常細胞よりも腫瘍細胞に対して、強い優先的な結合を示すことを示している。
種の交差反応性
ヒトADAM9(huADAM9)及びカニクイザルADAM9(cynoADAM9)に対するMAB-Aの結合を試験した。簡単に言うと、huADAM9、cynoADAM9、無関係の抗原を一次的に発現する293-FT細胞及びCHO-K細胞、またはトランスフェクトしていない親細胞をMAB-Aと共にインキュベートし、その後、ヤギ抗マウスPE二次抗体と共にインキュベートし、FACSによって分析した。図2に示されるように、MAB-Aは、両方の細胞型を一時的に発現するhuADAM9に対して強い結合を示す。MAB-Aは、cynoADAM9に対する良好な結合を示さない。MAB-Aは、親細胞または無関係な抗原を発現する細胞に結合しなかった。ELISAアッセイにおいて、cynoADAMに対する同様の低レベルの結合がみとめられた。
ヒト化及び初期最適化
MAB-Aのヒト化によって、ヒト化VHドメイン(本明細書で「hMAB-A VH(1)」と呼ばれる)及びヒト化VLドメイン(本明細書で「hMAB-A VL(1)」と呼ばれる)が得られた。次いで、結合活性を高め、及び/または以下に更に詳細に記載する、潜在的に不安定なアミノ酸残基を除去するために、ヒト化可変ドメインを最適化した。この1回目の最適化によって、本明細書で「hMAB-A VH(2)」、「hMAB-A VH(3)」及び「hMAB-A VH(4)」と呼ぶ3つの更なるヒト化VHドメインと、本明細書で「hMAB-A VL(2)」、「hMAB-A VL(3)」及び「hMAB-A VL(4)」と呼ぶ3つの更なるヒト化VLドメインが得られた。これに加え、マウスVHドメイン及びVLドメインとヒト定常領域とを有するMAB-Aのキメラ態様(「chMAB-A」)を作成した。マウス及びヒト化/最適化されたVH及びVLドメインのアミノ酸配列を上に提示しており、アラインメントを図3A及び3Bに提示している。これらのヒト化/最適化されたVH及びVLドメインのコンセンサス配列を上に提示している。複数のヒト化可変ドメインが作成される場合、特定の抗ADAM9抗体(例えば、MAB-A)のヒト化重鎖及び軽鎖可変ドメインを、任意の組み合わせで使用してもよく、ヒト化鎖の特定の組み合わせは、特定のVH/VLドメインを参照することによって言及され、例えば、hMAB-A VH(1)及びhMAB-A VL(2)を含む抗体は、具体的に「hMAB-A(1.2)」と呼ばれる。
これらの試験は、アフィニティを下げることなく、CDRからリシン残基を除去するために導入し得る更なる置換も特定した。アフィニティに対する影響を最小限にしつつ、他の潜在的に不安定な残基を除去するために、更なる置換を同定した。
非ヒト霊長類ADAM9に対する結合の最適化
ランダム突然変異を使用し、hMAB-A(2.2)の重鎖CDRH2(Kabat位置53-58)及びCDRH3(Kabat位置95-100及び100a-100f)ドメイン内に置換を導入した。この変異体をスクリーニングし、非ヒト霊長類ADAM9(例えば、cynoADAM9)への結合が向上し、huADAM9に対する高アフィニティ結合を保持するクローンを同定した。CDRH3(Kabat位置100a-100f)内の突然変異の2種類の独立したスクリーニングから、48種類のクローンを選択した。表4は、2つの独立したスクリーニングからcynoADAM9に対する結合の向上について選択したhMAB-A(2.2)クローンからのCDRH3 Kabat残基100a-fのアミノ酸配列のアラインメントを提示する。更なるクローンアラインメントを表5に提示している。このような表で示されるように、各実験で、別個の置換パターンに含まれる同様のクローンが発生した。
抗体hMAB-A(2I.2)の免疫組織化学試験
hMAB-A(2I.2)の細胞特異性をIHCによって観察した。陽性対照及び陰性対照細胞及び正常なヒト及びカニクイザル組織を、hMAB-A(2I.2)(2.5μg/mL)またはアイソタイプ参照(2.5μg/mL)と接触させ、染色の程度を視覚化した。この試験の結果を表7にまとめている。
変異体Fc領域を含むhMAB-A(2I.2)
hMAB-A(2I.2)は、κ軽鎖定常領域を有する軽鎖(配列番号68)と、野生型IgG重鎖定常領域を有する重鎖(配列番号52)とを含む。以下の置換をFc領域に導入することによってFc変異体を作成した。L234A/L235A(例えば、配列番号78を参照)、hMAB-A(2I.2)(AA)と呼ばれる;S442C(例えば、配列番号79を参照)、hMAB-A(2I.2)(C)と呼ばれる;及びL234A/L235A/S442C(例えば、配列番号80を参照)、hMAB-A(2I.2)(AA/C)と呼ばれる。huADAM9-His及びcynoADAM9-Hisに対する各Fc変異体の結合をELISAアッセイによって試験した。簡単に言うと、ヒスチジン含有ペプチドに結合し、マイクロタイタープレート上にコーティングされた抗体を使用し、Hisペプチドタグ化可溶性cynoADAM9またはHisペプチドタグ化可溶性huADAM9(0.5μg/mL)を捕捉し、親hMAB-A(2.2)及びFc変異体の段階的希釈物の結合を試験した。結合曲線huADAM9及びcynoADAM9は、図5A及び図5Bに提示されており、それぞれ、Fc変異体が、野生型Fc領域を有するhMAB-A(2I.2)の結合アフィニティを保持していたことを示している。
標的発現分析
異なる適応症間でADAM9発現を評価するために、20種類の異なる腫瘍型を用いた組織マイクロアレイ(TMA)を、まず、予備研究使用のためにImmunoGenで開発されたADAM9 IHCアッセイを用いて評価した。
1*(1+強度で染色する細胞の割合)
+2*(2+強度で染色する細胞の割合)
+3*(3+強度で染色する細胞の割合)
=Hスコア。
抗ADAM9抗体インターナリゼーション試験
本発明の抗ADAM9抗体のインターナリゼーションを評価するためにフローサイトメトリーに基づくインターナリゼーション実験を、Alexa Fluor 488に結合されたhMAB-A(2.2)、hMAB-A(2I.2)及びhMAB-A(2I.2)-S442C抗体で行った。
抗ADAM9抗体細胞処理試験
細胞上での標的結合、chMAB-Aの取り込み、リポソーム分解を評価するために、既に記載した3H-プロピオンアミド標識された抗体を処理する方法を使用した(Lai et al.、Pharm Res.2015年11月;32(11):3593-603)。この方法を用い、ADAM9を標的とするchMAB-A抗体を、リシン残基を介したトリチウム化プロピオネートを用いてわずかに標識した。細胞結合、取り込み、リポソームへのトラフィッキングの時に、[3H]プロピオネート標識されたAb(3H-Ab)が分解し、リシン-[3H]プロピオンアミドが、細胞成長培地に放出されることが以前示されている。有機溶媒を加えると、インタクトな標識された抗体が沈殿し、リシン-[3H]プロピノアミド溶液が残り、これは、抗体処理の程度の簡便かつ正確な指標となる。
製造プロトコルあたり、1mLのSOLVABLE(Perkin Elmer)を各ウェルサンプルに加え、50℃の水浴で一晩インキュベートした。サンプルを水浴から取り出し、20mLのガラスシンチレーションバイアルに移し、EDTA及びH2O2をサンプルに加え、次いで、さらに50℃で1時間インキュベートした。サンプルをHClでクエンチし、15mLのOptima Gold液体シンチレーション液(Perkin Elmer)を加え、サンプルを十分にボルテックス撹拌した。LSCで計測する前に、サンプルを暗室に最短で4時間保持した。タンパク質を含まないアセトン抽出物サンプルを、高減圧下、体積が1mL未満になるまで乾燥させ、LSC前に、上述のようなSolvableを用いて処理した。得られたサンプルのCPM値から、結合し、分解し、インタクトな標識された抗体の量を計算した。
ヒト化/最適化された抗ADAM9抗体及び薬物コンジュゲートの結合アフィニティ試験
抗原結合に対する結合の結果を評価するために、ADAM9に対する各抗ADAM9免疫コンジュゲート及びそのそれぞれの結合していない抗体の相対結合アフィニティを、FACS分析によって、ヒトADAM9またはカニクイザルADAM9のいずれかを異所的に発現する300-19細胞で決定した。簡単に言うと、ADAM9を発現する300-19細胞を、段階希釈した抗ADAM9抗体または免疫コンジュゲートと共に、FACSバッファー(PBS、0.1% BSA、0.01% NaN3)中、4℃で30分間インキュベートした。次いで、サンプルを洗浄し、蛍光標識した二次抗体と共に4℃で30分間インキュベートした。各濃度での蛍光強度の正規化された平均値をプロットし、結合のEC50を、非線形回帰分析を用いて計算した(GraphPad Prims 4.0)。この試験から得た結果を表14にまとめている。
N-(2-(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)エチル)-11-(3-((((S)-8-メトキシ-6-オキソ-11,12,12a,13-テトラヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)-5-((((S)-8-メトキシ-6-オキソ-12a,13-ジヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)フェニル)-13,13-ジメチル-2,5,8-トリオキサ-14,15-ジチア-11-アザノナデカン-19-アミド(化合物D6)の合成
N1-(2-(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)エチル)-N6-((S)-1-(((S)-1-((3-((((S)-8-メトキシ-6-オキソ-11,12,12a,13-テトラヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)-5-((((S)-8-メトキシ-6-オキソ-12a,13-ジヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)フェニル)アミノ)-1-オキソプロパン-2-イル)アミノ)-1-オキソプロパン-2-イル)アジパミド(化合物D5)の合成
1-((2-(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)エチル)アミノ)-4-((5-((3-((((S)-8-メトキシ-6-オキソ-11,12,12a,13-テトラヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)-5-((((S)-8-メトキシ-6-オキソ-12a,13-ジヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)フェニル)アミノ)-2-メチル-5-オキソペンタン-2-イル)1スルファニル)-1-オキソブタン-2-スルホン酸(化合物D4)の合成
遊離チオールD1(88mg、0.105mmol)及び1-((2,5-ジオキソピロリジン-1-イル)オキシ)-1-オキソ-4-(ピリジン-2-イルジスルファニル)ブタン-2-スルホン酸(スルホ-SPDB)(64.0mg、0.158mmol)の無水ジクロロメタン(2.10mL)懸濁物に、DIPEA(55.0μL、0.315mmol)を窒素下、室温で加えた。混合物を16時間撹拌し、次いで、1-(2-アミノエチル)-1H-ピロール-2,5-ジオン塩酸塩(55.6mg、0.315mmol)、無水ジクロロメタン(1.0mL)及びDIPEA(0.055mL、0.315mmol)を加えた。混合物を室温で更に5時間撹拌し、その時点で、反応物を高減圧下で濃縮した。得られた残渣をRP-HPLC(C18、CH3CN/H2O)によって精製した。所望の生成物を含有するフラクションを凍結させ、凍結乾燥し、マレイミドD4(20mg、収率16%)を白色固体として得た。LCMS=4.92分(8分法)。MS(m/z):1158.6(M+1)+。
N-(2-(2,5-ジオキソ-2,5-ジヒドロ-1H-ピロール-1-イル)エチル)-11-(3-((((S)-8-メトキシ-6-オキソ-11,12,12a,13-テトラヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)-5-((((S)-8-メトキシ-6-オキソ-12a,13-ジヒドロ-6H-ベンゾ[5,6][1,4]ジアゼピノ[1,2-a]インドール-9-イル)オキシ)メチル)フェニル)-2,5,8-トリオキサ-11-アザペンタデカン-15-アミド(化合物D7)の合成
抗ADAM9抗体hMAB-A(2I.2)-S442C-DGN549のシステイン部位特異的コンジュゲートの調製
hMAB-A(2I.2)-S442Cは、配列番号68の軽鎖配列(配列番号55のVL配列を含む)と、配列番号142の重鎖配列(配列番号28のVH配列を含む)とを含む、ヒト化/最適化された抗体であり、Xがリシンである場合、配列番号142の6番目から最後の残基に対応する操作されたCysを含み、またはXが存在しない場合、配列番号142の5番目から最後の残基に対応する操作されたCysを含む。
抗ADAM9抗体のリシンが結合したIGNコンジュゲートの調製
a.hMAB-A(2I.2)-DGN549の調製
hMAB-A(2I.2)は、配列番号68の軽鎖配列と、配列番号52の重鎖配列とを含むヒト化/最適化された抗体である。15mMの2-[4-(ヒドロキシエチル)ピペリジン-1-イル]エタンスルホン酸(HEPES)、N,N-ジメチルアセトアミド(DMA)を用いてpH8.5で緩衝化したhMAB-A(2I.2)抗体を含有する溶液に、4.8当量のDGN549-L(化合物D2)をDMAのストック溶液として加え、最終溶媒組成を10%(v/v)DMA及び90%(v/v)バッファー水溶液とした。反応を25℃で4時間進めた。
b.hMAB-A(2.2)-DGN549の調製
c.hMAB-A(2C.2)-DGN549の調製
d.chMAB-A-DGN549、chMAB-A-sSPDB-IGN137、chMAB-A-IGN23及びchMAB-A-sSPDB-DGN462の調製
抗ADAM9抗体のリシンが結合したDMコンジュゲートの調製
a.hMAB-A(2I.2)-sSPDB-DM4の調製
hMAB-A(2I.2)は、配列番号68の軽鎖配列と、配列番号52の重鎖配列とを含むヒト化/最適化された抗体である。
b.hMAB-A(2C.2)-sSPDB-DM4の調製
c.hMAB-A(2.2)-sSPDB-DM4の調製
d.chMAB-A-sSPDB-DM4及びchMAB-A-SMCC-DMlの調製
抗ADAM9抗体薬物コンジュゲートのインビトロ細胞毒性
ADAM9を発現する細胞株のパネルに対する種々の抗ADAM9抗体免疫コンジュゲートのインビトロ細胞毒性を、標的ではないIgG1コンジュゲートと比較した。具体的には、治療の24時間前に、500~2000細胞/ウェルを96ウェルプレートに接種した。コンジュゲートを、段階的な3倍希釈を用い、培地で希釈し、ウェルあたり100μLを加えた。細胞を含むが、コンジュゲートを含まない対照ウェルと、培地のみを含むウェルが、各アッセイプレートに含まれていた。各データ点について、アッセイを3個ずつ実施した。プレートを加湿した5%CO2インキュベータ中、37℃で4~5日間インキュベートした。次いで、WST-8に基づくCell Counting Kit-8(Dojindo Molecular Technologies)を用い、各ウェル中の生存可能な細胞の相対数を決定した。まず、培地バックグラウンド吸光度で補正し、次いで、それぞれの値を、対照ウェル(未処理細胞)の値の平均で割り算することによって、各ウェル中の細胞の生存している分率を計算した。生存している細胞の割合を、コンジュゲート濃度に対してプロットし、活性のEC50を、非線形回帰分析(GraphPad Prims 4.0)を用いて計算した。
Calu3ヒト非小細胞肺腺癌異種移植片を有するSCIDマウスにおける抗ADAM9抗体薬物コンジュゲートの抗腫瘍活性
種々の投薬量のhMAB-A(2.2)-sSPDB-DM4及び1種類の投薬量のchMAB-A-DGN549コンジュゲートの抗腫瘍活性を、ヒト肺腺癌皮下異種移植モデルであるCalu3細胞を含む雌SCIDマウスで評価した。
H1703ヒト非小細胞肺扁平上皮癌異種移植片を有するSCIDマウスにおける抗ADAM9抗体薬物コンジュゲートの抗腫瘍活性
種々の投薬量のhMAB-A(2.2)-sSPDB-DM4コンジュゲートの抗腫瘍活性を、NSCLC扁平上皮細胞癌異種移植片モデルである、H1703細胞を有する雌SCIDマウスで評価した。
48匹のマウスを、腫瘍体積によって、8グループ(1グループあたり6匹のマウス)に無作為に分けた。腫瘍体積は、76.18~159.00(115.19±22.08、平均±SD)mm3の範囲であった。マウスを測定し、移植から19日後の腫瘍体積に基づき、無作為に分けた。移植(4/21/16)から20日目に、マウスに投薬した。マウスの体重は、20.20~29.15(23.88±1.95、平均±SD)グラムであった。各グループ中のマウスは、パンチ法によって特定した。試験薬剤及びビヒクルの投与は、27ゲージ、1/2インチ針を取り付けた1.0mLのシリンジを用いることによって、静脈内で行われた。グループは、以下が含まれていた。ビヒクル(PBS)を150μL/マウスで投薬した対照グループ、qdx1、chKTI-sSPDB-DM4を5mg/kgで、qdxl、hMAB-A(2.2)-sSPDB-DM4を1.25mg/kgで、qdxl、hMAB-A(2.2)-sSPDB-DM4を2.5mg/kgで、qdxl、hMAB-A(2.2)-sSPDB-DM4を5mg/kgで、qdxl。
頭頸部異種移植片のDetroit562扁平上皮癌を有するSCIDマウスにおける抗ADAM9抗体薬物コンジュゲートの抗腫瘍活性
種々の投薬量のchMAB-A-sSPDB-DM4コンジュゲートの抗腫瘍活性を、咽頭癌異種移植片モデルである、Detroit562を含む雌CD-I免疫欠損マウスで評価した。
グループには、以下が含まれていた。ビヒクル(PBS)を投薬された対照グループ、chMAB-A-sSPDB-DM4を5mg/kg、qdxl及びchMAB-A-sSPDB-DM4を1.25mg/kg、qdxl。
SNU-5胃癌異種移植片を有するNudeマウスにおける抗ADAM9抗体薬物コンジュゲートの抗腫瘍活性
種々の投薬量のhuMAB-A(2.2)-sSPDB-DM4及び1種類の投薬量のhuMAB-A(2I.2)-S442C-DGN549コンジュゲートの抗腫瘍活性を、ヒト胃癌異種移植モデルであるSnu-5細胞を含む雌Nudeマウスで評価した。
SW48大腸癌細胞株異種移植片を有するマウスにおける抗ADAM9抗体薬物コンジュゲートの抗腫瘍活性
種々の投薬量のhMAB-A(2.2)-sSPDB-DM4及びhuMAB-A(2I.2)-S442C-DGN649コンジュゲートの抗腫瘍活性を、大腸癌細胞株異種移植モデルであるSW48細胞を含む雌Nudeマウスで評価した。
FcRn結合を向上させることによって、抗ADAM9抗体メイタンシノイドコンジュゲートの曝露を延ばす
抗ADAM9抗体メイタンシノイドコンジュゲートが、効力を発揮する潜在能力を最大にするために、FcRn結合を向上させることによって抗体薬物コンジュゲートの曝露時間を延ばすために、置換M252Y、S254T及びT256E(「YTE突然変異」)を抗ADAM9抗体であるhMAB-A(2I.2)及びhMAB-A(2I.2)-S442CのFc領域に導入した。FcRnは、血清IgGレベルの維持において、主要な役割を果たす。非特異的に取り込まれるIgGは、pH依存性の相互作用に起因して、エンドソーム中のFcRnに結合する。次いで、FcRnが結合したIgGは、再循環するエンドソーム内に選別され、細胞表面に再び運ばれ、その場所で、中性pHに起因して、IgGが放出される。FcRn結合の向上は、選別を向上させ、薬物動態を向上させることができる。
[1]
抗ADAM9抗体またはそのADAM9結合フラグメントを含む免疫コンジュゲートであって、
(I)前記抗ADAM9抗体またはそのADAM9結合フラグメントは、医薬薬剤に結合されており、
(II)前記抗ADAM9抗体またはそのADAM9結合フラグメントは、軽鎖可変(VL)ドメインと重鎖可変(VH)ドメインとを含み、前記重鎖可変ドメインは、CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインを含み、前記軽鎖可変ドメインは、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインを含み、
(A)前記CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインは、MAB-Aの最適化された変異体の重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインのアミノ酸配列を有し、前記CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインは、MAB-Aの軽鎖可変(VL)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインのアミノ酸配列を有するか、または
(B)前記CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインは、MAB-Aの重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインのアミノ酸配列を有し、前記CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインは、MAB-Aの最適化された変異体の軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインのアミノ酸配列を有するか、または
(C)前記CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインは、MAB-Aの最適化された変異体の重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインのアミノ酸配列を有し、前記CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインは、MAB-Aの最適化された変異体の軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインのアミノ酸配列を有する、前記免疫コンジュゲート。
[2]
前記抗ADAM9抗体またはそのADAM9結合フラグメントが、
(A)(1)MAB-Aの重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメイン、及び
(2)MAB-Aのヒト化変異体のVHドメインのFR1、FR2、FR3及びFR4、または
(B)(1)MAB-Aの軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメイン、及び
(2)MAB-Aのヒト化変異体のVLドメインのFR1、FR2、FR3及びFR4、または
(C)(1)MAB-Aの最適化された変異体の重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメイン、及び
(2)MAB-Aのヒト化変異体のVHドメインのFR1、FR2、FR3及びFR4、または
(D)(1)MAB-Aの最適化された変異体の軽鎖可変(VL)ドメインのCDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメイン、及び
(2)MAB-Aのヒト化変異体のVLドメインのFR1、FR2、FR3及びFR4、または
(E)(1)MAB-Aのヒト化/最適化された変異体の重鎖可変(VH)ドメイン、
(2)MAB-Aのヒト化/最適化された変異体のVL軽重鎖可変(VL)ドメイン
を含む、[1]に記載の免疫コンジュゲート。
[3]
MAB-Aの前記最適化された変異体の前記重鎖可変(VH)ドメインのCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインは、それぞれ、以下のアミノ酸配列:
(1)配列番号47(SYWX1H)
(ここで、X1は、MまたはIである)、
(2)配列番号48(EIIPIX2GHTNYNEX3FX4X5)
(ここで、X2、X3、X4及びX5は、独立して選択され、
X2は、NまたはFであり;X3は、KまたはRであり;
X4は、KまたはQであり、
X5は、SまたはGである)、
(3)配列番号49(GGYYYYX6X7X8X9X10X11DY)
(ここで、X6は、P、F、Y、W、I、L、V、T、GまたはDであり、X7、X8、X9、X10及びX11は、
(A)X6がPである場合、
X7は、KまたはRであり;X8は、FまたはMであり;X9は、Gであり;
X10は、WまたはFであり;X11は、M、LまたはKであり;
(B)X6が、F、YまたはWである場合、
X7は、NまたはHであり;X8は、SまたはKであり;X9は、GまたはAであり;
X10は、TまたはVであり;X11は、M、LまたはKであり;
(C)X6が、I、LまたはVである場合、
X7は、Gであり;X8は、Kであり;X9は、GまたはAであり;
X10は、Vであり;X11は、M、LまたはKであり;
(D)X6がTである場合、
X7は、Gであり;X8は、K、MまたはNであり;X9は、Gであり;
X10は、VまたはTであり;X11は、LまたはMであり;
(E)X6がGである場合、
X7は、Gであり;X8は、Sであり;X9は、Gであり;
X10は、Vであり;X11は、Lであり、
(F)X6がDである場合、
X7は、Sであり;X8は、Nであり;X9は、Aであり;
X10は、Vであり;X11は、Lであるように選択される)を有する、[1]または[2]のいずれか一項に記載の免疫コンジュゲート。
[4]
[1]~[3]のいずれか一項に記載の免疫コンジュゲートであって、MAB-Aの前記最適化された変異体の前記重鎖可変(VH)ドメインは、配列番号15のアミノ酸配列を含み、
X1は、MまたはIであり;X2は、NまたはFであり;
X3は、KまたはRであり;X4は、KまたはQであり;
X5は、SまたはGであり、X6は、P、F、Y、W、I、L、V、T、GまたはDであり;
X7、X8、X9、X10及びX11は、
X6がPである場合、X7は、KまたはRであり;X8は、FまたはMであり;X9は、Gであり;X10は、WまたはFであり;X11は、M、LまたはKであり;
X6が、F、YまたはWである場合、X7は、NまたはHであり;X8は、SまたはKであり;X9は、GまたはAであり;X10は、TまたはVであり;X11は、M、LまたはKであり;
X6が、I、LまたはVである場合、X7は、Gであり;X8は、Kであり;X9は、GまたはAであり;X10は、Vであり;X11は、M、LまたはKであり;
X6がTである場合、X7は、Gであり;X8は、K、MまたはNであり;X9は、Gであり;X10は、VまたはTであり;X11は、LまたはMであり;
X6がGである場合、X7は、Gであり;X8は、Sであり;X9は、Gであり;X10は、Vであり;X11は、Lであり;
X6がDである場合、X7は、Sであり;X8は、Nであり;X9は、Aであり;X10は、Vであり;X11は、Lであるように選択される、前記免疫コンジュゲート。
[5]
MAB-Aの前記最適化された変異体の前記重鎖可変(VH)ドメインは、
(1)hMAB-A VH(1)(配列番号16);
(2)hMAB-A VH(2)(配列番号17);
(3)hMAB-A VH(3)(配列番号18);
(4)hMAB-A VH(4)(配列番号19);
(5)hMAB-A VH(2A)(配列番号20);
(6)hMAB-A VH(2B)(配列番号21);
(7)hMAB-A VH(2C)(配列番号22);
(8)hMAB-A VH(2D)(配列番号23);
(9)hMAB-A VH(2E)(配列番号24);
(10)hMAB-A VH(2F)(配列番号25);
(11)hMAB-A VH(2G)(配列番号26);
(12)hMAB-A VH(2H)(配列番号27);
(13)hMAB-A VH(2I)(配列番号28);及び
(14)hMAB-A VH(2J)(配列番号29)からなる群から選択される、[4]に記載の免疫コンジュゲート。
[6]
MAB-Aの前記最適化された変異体の前記軽鎖可変(VL)ドメインの前記CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインは、それぞれ、
(1)配列番号66(X12ASQSVDYX13GDSYX14N)
(ここで、X12、X13、X14は、独立して選択され、
X12は、KまたはRであり;X13は、DまたはSであり;X14は、MまたはLである);
(2)配列番号13(AASDLES);及び
(3)配列番号67(QQSX15X16X17PFT)
(ここで、X15、X16及びX17は独立して選択され、
X15は、HまたはYであり;X16は、EまたはSであり;X17は、DまたはTである)
のアミノ酸配列を有する、[1]~[5]のいずれか一項に記載の免疫コンジュゲート。
[7]
[1]~[6]のいずれか一項に記載の免疫コンジュゲートであって、前記軽鎖可変(VL)ドメインは、配列番号53のアミノ酸配列を含む、
X12は、KまたはRであり;X13は、DまたはSであり;
X14は、MまたはLであり;X15は、HまたはYであり;
X16は、EまたはSであり;X17は、DまたはTである)
前記免疫コンジュゲート。
[8]
MAB-Aの前記最適化された変異体の前記軽鎖可変(VL)ドメインが、
(1)hMAB-A VL(1)(配列番号54);
(2)hMAB-A VL(2)(配列番号55);
(3)hMAB-A VL(3)(配列番号56);
(4)hMAB-A VL(4)(配列番号57);
(5)hMAB-A VL(2A)(配列番号20)からなる群から選択される、[7]に記載の免疫コンジュゲート。
[9]
前記CDRH1ドメインが、アミノ酸配列SYWMH(配列番号8)を含み、前記CDRH2ドメインが、アミノ酸配列EIIPIFGHTNYNEKFKS(配列番号35)を含み、前記CDRH3ドメインが、アミノ酸配列GGYYYYPRQGFLDY(配列番号45)を含む、[1]に記載の免疫コンジュゲート。
[10]
前記CDRL1ドメインが、アミノ酸配列KASQSVDYSGDSYMN(配列番号62)を含み、前記CDRL2ドメインが、アミノ酸配列AASDLES(配列番号13)を含み、前記CDRL3ドメインが、アミノ酸配列QQSHEDPFT(配列番号14)を含む、[1]または[9]のいずれか一項に記載の免疫コンジュゲート。
[11]
前記免疫コンジュゲートが、
(A)hMAB-A(2I.2)の重鎖可変(VH)ドメイン(配列番号28);または
(B)hMAB-A(2I.2)の軽鎖可変(VL)ドメイン(配列番号55);または
(C)hMAB-A(2I.2)の重鎖可変(VH)ドメイン(配列番号28)及びhMAB-A(2I.2)の軽鎖可変(VL)ドメイン(配列番号55)
を含む、[9]または[10]のいずれか一項に記載の免疫コンジュゲート。
[12]
前記免疫コンジュゲートが、Fc領域を含む、[1]~[11]のいずれか一項に記載の免疫コンジュゲート。
[13]
前記Fc領域が、
(a)FcγRに対する変異体Fc領域のアフィニティを下げる1つ以上のアミノ酸改変、及び/または
(b)システイン残基を導入する1つ以上のアミノ酸改変
を含む変異体Fc領域である、[12]に記載の免疫コンジュゲート。
[14]
FcγRに対する変異体Fc領域のアフィニティを下げる前記1つ以上のアミノ酸改変が、
(A)L234A;
(B)L235A;または
(C)L234A及びL235A
を含み、前記番号付けが、KabatにあるEUインデックスの番号付けである、[13]に記載の免疫コンジュゲート。
[15]
システイン残基を導入する前記1つ以上のアミノ酸改変が、S442Cを含み、前記番号付けが、KabatにあるEUインデックスの番号付けである、[13]または[14]のいずれか一項に記載の免疫コンジュゲート。
[16]
前記免疫コンジュゲートが、ヒトADAM9及びcynoADAM9に特異的に結合するヒト化抗ADAM9抗体またはそのADAM9結合フラグメントを含み、前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、前記医薬薬剤に結合される、[1]に記載の免疫コンジュゲート。
[17]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、
(a)それぞれ、配列番号8、35及び10及び配列番号62、13、14;
(b)それぞれ、配列番号8、35及び10及び配列番号63、13、14;
(c)それぞれ、配列番号8、36及び10及び配列番号63、13、14
(d)それぞれ、配列番号34、36及び10及び配列番号64、13、65
からなる群から選択される配列を有する、CDRH1ドメイン、CDRH2ドメイン及びCDRH3と、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、[16]に記載の免疫コンジュゲート。
[18]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、
(a)それぞれ、配列番号17及び配列番号55;
(b)それぞれ、配列番号17及び配列番号56;
(c)それぞれ、配列番号18及び配列番号56;及び
(d)それぞれ、配列番号19及び配列番号57
からなる群から選択される配列に対して少なくとも90%、少なくとも95%または少なくとも99%の同一性を有する配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む、[16]または[17]に記載の免疫コンジュゲート。
[19]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、
(a)それぞれ、配列番号17及び配列番号55;
(b)それぞれ、配列番号17及び配列番号56;
(c)それぞれ、配列番号18及び配列番号56;及び
(d)それぞれ、配列番号19及び配列番号57
からなる群から選択される配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む、[18]に記載の免疫コンジュゲート。
[20]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントは、キメラまたはマウス親抗体と比較して、cynoADAM9に対する結合アフィニティが少なくとも100倍向上し、ヒトADAM9に対する高いアフィニティを保持しているように最適化される、[16]に記載の免疫コンジュゲート。
[21]
前記抗ADAM9抗体またはそのADAM9結合フラグメントが、
(a)それぞれ、配列番号8、35及び37及び配列番号62、13、14;
(b)それぞれ、配列番号8、35及び38及び配列番号62、13、14;
(c)それぞれ、配列番号8、35及び39及び配列番号62、13、14;
(d)それぞれ、配列番号8、35及び40及び配列番号62、13、14;
(e)それぞれ、配列番号8、35及び41及び配列番号62、13、14;
(f)それぞれ、配列番号8、35及び42及び配列番号62、13、14;
(g)それぞれ、配列番号8、35及び43及び配列番号62、13、14;
(h)それぞれ、配列番号8、35及び44及び配列番号62、13、14;
(i)それぞれ、配列番号8、35及び45及び配列番号62、13、14;及び
(j)それぞれ、配列番号8、35及び46及び配列番号62、13、14
からなる群から選択される配列を有する、CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインを含む、[20]に記載の免疫コンジュゲート。
[22]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、
(a)それぞれ、配列番号20及び配列番号55;
(b)それぞれ、配列番号21及び配列番号55;
(c)それぞれ、配列番号22及び配列番号55;
(d)それぞれ、配列番号23及び配列番号55;
(e)それぞれ、配列番号24及び配列番号55;
(f)それぞれ、配列番号25及び配列番号55;
(g)それぞれ、配列番号26及び配列番号55;
(h)それぞれ、配列番号27及び配列番号55;
(i)それぞれ、配列番号28及び配列番号55;及び
(j)それぞれ、配列番号29及び配列番号55
からなる群から選択される配列に対して少なくとも90%、少なくとも95%または少なくとも99%の同一性を有する配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む、[21]に記載の免疫コンジュゲート。
[23]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、
(a)それぞれ、配列番号20及び配列番号55;
(b)それぞれ、配列番号21及び配列番号55;
(c)それぞれ、配列番号22及び配列番号55;
(d)それぞれ、配列番号23及び配列番号55;
(e)それぞれ、配列番号24及び配列番号55;
(f)それぞれ、配列番号25及び配列番号55;
(g)それぞれ、配列番号26及び配列番号55;
(h)それぞれ、配列番号27及び配列番号55;
(i)それぞれ、配列番号28及び配列番号55;及び
(j)それぞれ、配列番号29及び配列番号55
からなる群から選択される配列を有する重鎖可変ドメイン(VH)及び軽鎖可変ドメイン(VL)を含む、[22]に記載の免疫コンジュゲート。
[24]
前記ヒト化抗ADAM9抗体が、Fc領域を含む全長抗体である、[16]~[23]のいずれか一項に記載の免疫コンジュゲート。
[25]
前記ヒト化抗ADAM9抗体が、
(a)それぞれ、配列番号50及び配列番号68;
(b)それぞれ、配列番号51及び配列番号68;及び
(c)それぞれ、配列番号52及び配列番号68からなる群から選択される配列を有する重鎖と軽鎖とを含む、[24]に記載の免疫コンジュゲート。
[26]
前記Fc領域が、以下を含む変異体Fc領域である、[16]~[25]のいずれか一項に記載の免疫コンジュゲート:
(a)L234A、L235A並びにL234A及びL235Aからなる群から選択される、FcγRに対する前記変異体Fc領域のアフィニティを下げる1つ以上のアミノ酸改変;及び/または
(b)S442にシステイン残基を導入するアミノ酸改変を含む変異体Fc領域(前記番号付けは、KabatにあるEUインデックスの番号付けである)及び/または
(c)M252Y、S254T及びT256Eからなる群から選択されるFcRnに対する前記変異体Fc領域の半減期を延ばす1つ以上のアミノ酸置換。
[27]
前記ヒト化抗ADAM9抗体が、
(a)それぞれ、配列番号141及び配列番号68;
(b)それぞれ、配列番号142及び配列番号68;
(c)それぞれ、配列番号143及び配列番号68;
(d)それぞれ、配列番号151及び配列番号68;
(e)それぞれ、配列番号152及び配列番号68;
(f)それぞれ、配列番号153及び配列番号68;及び
(g)それぞれ、配列番号154及び配列番号68
からなる群から選択される配列を有する重鎖と軽鎖とを含む、[21]に記載の免疫コンジュゲート。
[28]
配列番号141、配列番号142、配列番号143、配列番号151、配列番号152、配列番号153または配列番号154のXがリシンである、[27]に記載の免疫コンジュゲート。
[29]
配列番号141、配列番号142、配列番号143、配列番号151、配列番号152、配列番号153または配列番号154のXが存在しない、[27]に記載の免疫コンジュゲート。
[30]
前記免疫コンジュゲートは、以下の式によって表され、
CBAは、リシン残基を介してCyL1に共有結合する、[1]~[14]及び[16]~[29]のいずれか一項に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL1は、以下の式
NとCとの間の二重線
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は、(C1-C6)アルキルであり;
L’は、以下の式
-NR5-P-C(=O)-(CRaRb)m-C(=O)- (B1’);または
-NR5-P-C(=O)-(CRaRb)m-S-Zs1- (B2’)
によって表され、
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、それぞれ独立して、-H、(C1-C3)アルキル、または帯電した置換基またはイオン化可能な基Qであり;
mは、1~6の整数であり、
Zs1は、以下の式
qは、1~5の整数である、[1]~[14]及び[16]~[29]のいずれか一項に記載の免疫コンジュゲート。
[31]
Ra及びRbが両方ともHであり;R5が、HまたはMeである、[30]に記載の免疫コンジュゲート。
[32]
Pが、2~5個のアミノ酸残基を含むペプチドである、[30]または[31]に記載の免疫コンジュゲート。
[33]
Pが、Gly-Gly-Gly、Ala-Val、Val-Ala、Val-Cit、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp、Cit、Phe-Ala、Phe-N9-トシル-Arg、Phe-N9-ニトロ-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu(配列番号144)、β-Ala-Leu-Ala-Leu(配列番号145)、Gly-Phe-Leu-Gly(配列番号146)、Val-Arg、Arg-Val、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala、Ala-Met、Met-Ala、Gln-Val、Asn-Ala、Gln-Phe及びGln-Alaから選択される、[30]~[32]のいずれか一項に記載の免疫コンジュゲート。
[34]
Pが、Gly-Gly-Gly、Ala-Val、Ala-Ala、Ala-D-Ala、D-Ala-AlaまたはD-Ala-D-Alaである、[33]に記載の免疫コンジュゲート。
[35]
Qが、-SO3Hまたはその医薬的に許容される塩である、[30]~[34]のいずれか一項に記載の免疫コンジュゲート。
[36]
前記免疫コンジュゲートが、以下の式
[37]
前記免疫コンジュゲートが、以下の式によって表され
CBAは、リシン残基を介してCyL2に共有結合する、請求項1~14及び16~29のいずれか一項に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL2は、以下の式
NとCとの間の二重線
Rx1及びRx2は、独立して、(C1-C6)アルキルであり;
Reは、-Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Zs1は、以下の式
qは、1~5の整数である、[1]~[14]及び[16]~[29]のいずれか一項に記載の免疫コンジュゲート。
[38]
Reが、HまたはMeであり;Rx1及びRx2が、独立して、-(CH2)p-(CRfRg)-であり、Rf及びRgは、それぞれ独立して、-Hまたは(C1-C4)アルキルであり;pが、0、1、2または3である、[37]に記載の免疫コンジュゲート。
[39]
Rf及びRgが同じであるか、または異なっており、-H及び-Meから選択される、[38]に記載の免疫コンジュゲート。
[40]
前記免疫コンジュゲートが、以下の式
[41]
NとCとの間の二重線
[42]
NとCとの間の二重線
[43]
Yが、-SO3H、-SO3Naまたは-SO3Kである、[42]に記載の免疫コンジュゲート。
[44]
Yが、-SO3Naである、[42]に記載の免疫コンジュゲート。
[45]
前記免疫コンジュゲートが、以下の式によって表され、
CBAは、リシン残基を介してCyL3に共有結合する、請求項1~14及び16~29のいずれか一項に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり、
CyL3は、以下の式
m’は、1または2であり;
R1及びR2は、それぞれ独立して、Hまたは(C1-C3)アルキルであり;
Zs1は、以下の式
qは、1~5の整数である、[1]~[14]及び[16]~[29]のいずれか一項に記載の免疫コンジュゲート。
[46]
m’が1であり、R1及びR2が両方ともHである、[45]に記載の免疫コンジュゲート。
[47]
m’が2であり、R1及びR2が両方ともMeである、[45]に記載の免疫コンジュゲート。
[48]
前記免疫コンジュゲートが、以下の式
[49]
前記免疫コンジュゲートが、以下の式
ここで、
WLは、1~10の整数であり、
CBAは、それぞれ配列番号8、35及び45及び配列番号62、13、14の配列を有するCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントである、[45]に記載の免疫コンジュゲート。
[50]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、それぞれ配列番号28及び配列番号55の配列を有する重鎖可変ドメイン(VH)と軽鎖可変ドメイン(VL)とを含む、[49]に記載の免疫コンジュゲート。
[51]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号52及び配列番号68の配列を有する重鎖と軽鎖とを含む、[50]に記載の免疫コンジュゲート。
[52]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号151及び配列番号68の配列を有する重鎖と軽鎖とを含む、[49]に記載の免疫コンジュゲート。
[53]
前記免疫コンジュゲートが、以下の式によって表され、
CBAは、システイン残基を介してCyC1に共有結合する、請求項1~24及び26~29のいずれか一項に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC1は、以下の式
NとCとの間の二重線
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、独立して、-H、(C1-C3)アルキルまたは帯電した置換基またはイオン化可能な基Qであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は、(C1-C6)アルキルであり;
LCは、
R19及びR20は、それぞれの場合に、独立して、-Hまたは(C1-C3)アルキルであり;
m”は、1~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルである、[1]~[24]及び[26]~[29]のいずれか一項に記載の免疫コンジュゲート。
[54]
Ra及びRbが両方ともHであり;R5が、HまたはMeである、[53]に記載の免疫コンジュゲート。
[55]
Pが、2~5個のアミノ酸残基を含むペプチドである、[53]または[54]に記載の免疫コンジュゲート。
[56]
Pが、Gly-Gly-Gly、Ala-Val、Val-Ala、Val-Cit、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp、Cit、Phe-Ala、Phe-N9-トシル-Arg、Phe-N9-ニトロ-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu(配列番号144)、β-Ala-Leu-Ala-Leu(配列番号145)、Gly-Phe-Leu-Gly(配列番号146)、Val-Arg、Arg-Val、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala、Ala-Met、Met-Ala、Gln-Val、Asn-Ala、Gln-Phe及びGln-Alaから選択される、[53]~[55]のいずれか一項に記載の免疫コンジュゲート。
[57]
Pが、Gly-Gly-Gly、Ala-Val、Ala-Ala、Ala-D-Ala、D-Ala-AlaまたはD-Ala-D-Alaである、[56]に記載の免疫コンジュゲート。
[58]
Qが、-SO3Hまたはその医薬的に許容される塩である、[53]~[57]のいずれか一項に記載の免疫コンジュゲート。
[59]
R19及びR20が、両方ともHであり、m”が、1~6の整数である、[53]~[58]のいずれか一項に記載の免疫コンジュゲート。
[60]
-LC-は、以下の式
[61]
以下の式
[62]
以下の式
ここで、
NとCとの間の二重線
CBAは、それぞれ配列番号8、35及び45及び配列番号62、13、14の配列を有するCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントである、[53]に記載の免疫コンジュゲート。
[63]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、それぞれ配列番号28及び配列番号55の配列を有する重鎖可変ドメイン(VH)と軽鎖可変ドメイン(VL)とを含む、[62]に記載の免疫コンジュゲート。
[64]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号142及び配列番号68の配列を有する重鎖と軽鎖とを含む、[63]に記載の免疫コンジュゲート。
[65]
前記免疫コンジュゲートが、以下の式によって表され、
CBAは、システイン残基を介してCyC2に共有結合する、請求項1~24及び26~29のいずれか一項に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC2は、以下の式
NとCとの間の二重線
Rx1は、(C1-C6)アルキルであり;
Re’は、-Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx2は、(C1-C6)アルキルであり;
LC’は、以下の式
ここで、
s1は、CBAに共有結合した部位であり、s2は、CyC2上の-S-基に共有結合した部位であり;
Zは、C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、-H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドである、[1]~[24]及び[26]~[29]のいずれか一項に記載の免疫コンジュゲート。
[66]
P’が、2~5個のアミノ酸残基を含むペプチドである、[65]に記載の免疫コンジュゲート。
[67]
P’が、Gly-Gly-Gly、Ala-Val、Val-Ala、Val-Cit、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp、Cit、Phe-Ala、Phe-N9-トシル-Arg、Phe-N9-ニトロ-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu(配列番号144)、β-Ala-Leu-Ala-Leu(配列番号145)、Gly-Phe-Leu-Gly(配列番号146)、Val-Arg、Arg-Val、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala、Ala-Met、Met-Ala、Gln-Val、Asn-Ala、Gln-Phe及びGln-Alaから選択される、[65]または[66]のいずれか一項に記載の免疫コンジュゲート。
[68]
P’が、Gly-Gly-Gly、Ala-Val、Ala-Ala、Ala-D-Ala、D-Ala-AlaまたはD-Ala-D-Alaである、[67]に記載の免疫コンジュゲート。
[69]
-LC’-は、以下の式
[70]
Reが、HまたはMeであり;Rx1が、-(CH2)p-(CRfRg)-であり、Rx2が、-(CH2)p-(CRfRg)-であり、Rf及びRgは、それぞれ独立して、-Hまたは(C1-C4)アルキルであり;pが、0、1、2または3である、[65]~[69]のいずれか一項に記載の免疫コンジュゲート。
[71]
Rf及びRgが同じであるか、または異なっており、-H及び-Meから選択される、[70]に記載の免疫コンジュゲート。
[72]
以下の式
[73]
NとCとの間の二重線
[74]
NとCとの間の二重線
[75]
Yが、-SO3H、-SO3Naまたは-SO3Kである、[74]に記載の免疫コンジュゲート。
[76]
Yが、-SO3Naである、[74]に記載の免疫コンジュゲート。
[77]
前記免疫コンジュゲートが、以下の式によって表され、
CBAは、システイン残基を介してCyC3に共有結合する、請求項1~24及び26~29のいずれか一項に記載の抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり、
CyC3は、以下の式
ここで、
m’は、1または2であり;
R1及びR2は、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
LC’は、以下の式
ここで、
s1は、CBAに共有結合した部位であり、s2は、CyC3上の-S-基に共有結合した部位であり;
Zは、-C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドである、[1]~[24]及び[26]~[29]のいずれか一項に記載の免疫コンジュゲート。
[78]
P’が、2~5個のアミノ酸残基を含むペプチドである、[77]に記載の免疫コンジュゲート。
[79]
P’が、Gly-Gly-Gly、Ala-Val、Val-Ala、Val-Cit、Val-Lys、Phe-Lys、Lys-Lys、Ala-Lys、Phe-Cit、Leu-Cit、Ile-Cit、Trp、Cit、Phe-Ala、Phe-N9-トシル-Arg、Phe-N9-ニトロ-Arg、Phe-Phe-Lys、D-Phe-Phe-Lys、Gly-Phe-Lys、Leu-Ala-Leu、Ile-Ala-Leu、Val-Ala-Val、Ala-Leu-Ala-Leu(配列番号144)、β-Ala-Leu-Ala-Leu(配列番号145)、Gly-Phe-Leu-Gly(配列番号146)、Val-Arg、Arg-Val、Arg-Arg、Val-D-Cit、Val-D-Lys、Val-D-Arg、D-Val-Cit、D-Val-Lys、D-Val-Arg、D-Val-D-Cit、D-Val-D-Lys、D-Val-D-Arg、D-Arg-D-Arg、Ala-Ala、Ala-D-Ala、D-Ala-Ala、D-Ala-D-Ala、Ala-Met、Met-Ala、Gln-Val、Asn-Ala、Gln-Phe及びGln-Alaから選択される、[77]または[78]のいずれか一項に記載の免疫コンジュゲート。
[80]
P’が、Gly-Gly-Gly、Ala-Val、Ala-Ala、Ala-D-Ala、D-Ala-AlaまたはD-Ala-D-Alaである、[79]に記載の免疫コンジュゲート。
[81]
-LC’-は、以下の式
[82]
m’が1であり、R1及びR2が両方ともHである、[77]~[81]のいずれか一項に記載の免疫コンジュゲート。
[83]
m’が2であり、R1及びR2が両方ともMeである、[77]~[81]のいずれか一項に記載の免疫コンジュゲート。
[84]
前記免疫コンジュゲートが、以下の式
[85]
以下の式
ここで、
WLは、1~10の整数であり、
CBAは、それぞれ配列番号8、35及び45及び配列番号62、13、14の配列を有するCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントである、免疫コンジュゲート。
[86]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、それぞれ配列番号28及び配列番号55の配列を有する重鎖可変ドメイン(VH)と軽鎖可変ドメイン(VL)とを含む、[85]に記載の免疫コンジュゲート。
[87]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号52及び配列番号68の配列を有する重鎖と軽鎖とを含む、[86]に記載の免疫コンジュゲート。
[88]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号151及び配列番号68の配列を有する重鎖と軽鎖とを含む、[86]に記載の免疫コンジュゲート。
[89]
配列番号52または配列番号151のXがリシンである、[87]または[88]に記載の免疫コンジュゲート。
[90]
配列番号52または配列番号151のXが存在しない、[87]または[88]に記載の免疫コンジュゲート。
[91]
以下の式
ここで、
NとCとの間の二重線
CBAは、それぞれ配列番号8、35及び45及び配列番号62、13、14の配列を有するCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントである、免疫コンジュゲート。
[92]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、それぞれ配列番号28及び配列番号55の配列を有する重鎖可変ドメイン(VH)と軽鎖可変ドメイン(VL)とを含む、[91]に記載の免疫コンジュゲート。
[93]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号142及び配列番号68の配列を有する重鎖と軽鎖とを含む、[92]に記載の免疫コンジュゲート。
[94]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号152及び配列番号68の配列を有する重鎖と軽鎖とを含む、[92]に記載の免疫コンジュゲート。
[95]
配列番号142または配列番号152のXがリシンである、[93]または[94]に記載の免疫コンジュゲート。
[96]
配列番号142または配列番号152のXが存在しない、[93]または[94]に記載の免疫コンジュゲート。
[97]
以下の式
ここで、
wCが、1または2であり;
DMは、以下の式
CBAは、それぞれ配列番号8、35及び45及び配列番号62、13、14の配列を有するCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントである、免疫コンジュゲート。
[98]
以下の式
ここで、
wCが、1または2であり;
DMは、以下の式
CBAは、それぞれ配列番号8、35及び45及び配列番号62、13、14の配列を有するCDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインと、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインとを含む、ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントである、免疫コンジュゲート。
[99]
前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントが、それぞれ配列番号28及び配列番号55の配列を有する重鎖可変ドメイン(VH)と軽鎖可変ドメイン(VL)とを含む、[97]または[98]に記載の免疫コンジュゲート。
[100]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号142及び配列番号68の配列を有する重鎖と軽鎖とを含む、[97]または[98]に記載の免疫コンジュゲート。
[101]
前記ヒト化抗ADAM9抗体が、それぞれ配列番号152及び配列番号68の配列を有する重鎖と軽鎖とを含む、[97]または[98]に記載の免疫コンジュゲート。
[102]
配列番号142または配列番号152のXがリシンである、[100]または[101]に記載の免疫コンジュゲート。
[103]
配列番号142または配列番号152のXが存在しない、[100]または[101]に記載の免疫コンジュゲート。
[104]
前記医薬的に許容される塩が、ナトリウム塩またはカリウム塩である、[30]~[103]のいずれか一項に記載の免疫コンジュゲート。
[105]
有効量の[1]~[104]のいずれか一項に記載の免疫コンジュゲートと、医薬的に許容される担体、賦形剤または希釈剤とを含む、医薬組成物。
[106]
ADAM9の発現と関連するか、またはADAM9の発現によって特徴付けられる疾患または状態の治療における、[1]~[104]のいずれか一項に記載の免疫コンジュゲートまたは請求項105に記載の医薬組成物の使用。
[107]
ADAM9と関連するか、またはADAM9によって特徴付けられる前記疾患または状態が、がんである、[106]に記載の使用。
[108]
前記がんが、非小細胞肺癌、大腸癌、膀胱癌、胃癌、膵臓癌、腎細胞癌、前立腺癌、食道癌、乳癌、頭頸部癌、子宮癌、卵巣癌、肝臓癌、子宮頸癌、甲状腺癌、精巣癌、骨髄がん、黒色腫及びリンパがんからなる群から選択される、[107]に記載の使用。
[109]
前記非小細胞肺癌が、扁平上皮癌、腺癌または大細胞未分化癌である、[108]に記載の使用。
[110]
前記大腸癌が、腺癌、消化管カルチノイド腫瘍、消化管間質腫瘍、原発性大腸リンパ腫、平滑筋肉腫または扁平上皮癌である、[108]に記載の使用。
[111]
対象において、ADAM9の発現と関連するか、またはADAM9の発現によって特徴付けられる疾患または状態を治療するための方法であって、前記対象に、有効量の[1]~[104]のいずれか一項に記載の免疫コンジュゲートまたは[105]に記載の医薬組成物を投与することを含む、前記方法。
[112]
ADAM9と関連するか、またはADAM9によって特徴付けられる前記疾患または状態が、がんである、[111]に記載の方法。
[113]
前記がんが、非小細胞肺癌、大腸癌、膀胱癌、胃癌、膵臓癌、腎細胞癌、前立腺癌、食道癌、乳癌、頭頸部癌、子宮癌、卵巣癌、肝臓癌、子宮頸癌、甲状腺癌、精巣癌、骨髄がん、黒色腫及びリンパがんからなる群から選択される、[112]に記載の方法。
[114]
前記非小細胞肺癌が、扁平上皮癌、腺癌または大細胞未分化癌である、[113]に記載の方法。
[115]
前記大腸癌が、腺癌、消化管カルチノイド腫瘍、消化管間質腫瘍、原発性大腸リンパ腫、平滑筋肉腫または扁平上皮癌である、[113]に記載の方法。
Claims (15)
- ヒトADAM9及びcynoADAM9に特異的に結合するヒト化抗ADAM9抗体またはそのADAM9結合フラグメントを含む免疫コンジュゲートであって、
(I)前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントは、医薬薬剤に結合されており、
(II)前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントは、軽鎖可変(VL)ドメインと重鎖可変(VH)ドメインとを含み、前記重鎖可変ドメインは、CDRH1ドメイン、CDRH2ドメイン及びCDRH3ドメインを含み、前記軽鎖可変ドメインは、CDRL1ドメイン、CDRL2ドメイン及びCDRL3ドメインを含み、
前記CDR H 1ドメイン、前記CDR H 2ドメイン及び前記CDR H 3ドメインと、前記CDR L 1ドメイン、前記CDR L 2ドメイン及び前記CDR L 3ドメインが、以下からなる群から選択される配列:
(a)それぞれ、配列番号8、35及び45配列番号62、13、14;
(b)それぞれ、配列番号8、35及び38及び配列番号62、13、14;
(c)それぞれ、配列番号8、35及び39及び配列番号62、13、14;
(d)それぞれ、配列番号8、35及び40及び配列番号62、13、14;
(e)それぞれ、配列番号8、35及び41及び配列番号62、13、14;
(f)それぞれ、配列番号8、35及び42及び配列番号62、13、14;
(g)それぞれ、配列番号8、35及び43及び配列番号62、13、14;
(h)それぞれ、配列番号8、35及び44及び配列番号62、13、14;
(i)それぞれ、配列番号8、35及び37及び配列番号62、13、14;並びに
(j)それぞれ、配列番号8、35及び46及び配列番号62、13、14
を含む、前記免疫コンジュゲート。 - (A)前記VHドメインが、配列番号20、配列番号21、配列番号22、配列番号23、配列番号24、配列番号25、配列番号26、配列番号27、配列番号28又は配列番号29を含み;かつ
(B)前記VLドメインが、配列番号54、配列番号55、配列番号56又は配列番号57を含む、請求項1に記載の免疫コンジュゲート。 - 前記CDRH1ドメインが、アミノ酸配列SYWMH(配列番号8)を含み、前記CDRH2ドメインが、アミノ酸配列EIIPIFGHTNYNEKFKS(配列番号35)を含み、前記CDRH3ドメインが、アミノ酸配列GGYYYYPRQGFLDY(配列番号45)を含み、前記CDRL1ドメインが、アミノ酸配列KASQSVDYSGDSYMN(配列番号62)を含み、前記CDRL2ドメインが、アミノ酸配列AASDLES(配列番号13)を含み、前記CDRL3ドメインが、アミノ酸配列QQSHEDPFT(配列番号14)を含む、請求項1に記載の免疫コンジュゲート。
- 前記免疫コンジュゲートが、
(A)hMAB-A(2I.2)の重鎖可変(VH)ドメイン(配列番号28);および/または
(B)hMAB-A(2I.2)の軽鎖可変(VL)ドメイン(配列番号55);および/または
(C)hMAB-A(2I.2)の重鎖可変(VH)ドメイン(配列番号28)及びhMAB-A(2I.2)の軽鎖可変(VL)ドメイン(配列番号55)
を含む、請求項3に記載の免疫コンジュゲート。 - 前記免疫コンジュゲートがFc領域を含み、任意選択で、前記Fc領域が、
(a)FcγRに対する変異体Fc領域のアフィニティを下げる1つ以上のアミノ酸改変;及び/または
(b)システイン残基を導入する1つ以上のアミノ酸改変;及び/または
(c)血清半減期を延ばす1つ以上のアミノ酸改変
を含む変異体Fc領域である、請求項1~4のいずれか一項に記載の免疫コンジュゲート。 - (I)FcγRに対する変異体Fc領域のアフィニティを下げる前記1つ以上のアミノ酸改変が、
(A)L234A;
(B)L235A;または
(C)L234A及びL235A
を含み;および/または
(II)システイン残基を導入する前記1つ以上のアミノ酸改変が、S442Cを含み;および/または
(III)血清半減期を延ばす前記1つ以上のアミノ酸改変が:
(A)M252Y;
(B)M252Y及びS254T;
(C)M252Y及びT256E;
(D)M252Y、S254T及びT256E;又は
(E)K288D及びH435K
を含み、前記番号付けが、KabatにあるEUインデックスの番号付けである、請求項5に記載の免疫コンジュゲート。 - 前記ヒト化抗ADAM9抗体が、
(a)それぞれ、配列番号152及び配列番号68;
(b)それぞれ、配列番号141及び配列番号68;
(c)それぞれ、配列番号142及び配列番号68;
(d)それぞれ、配列番号143及び配列番号68;
(e)それぞれ、配列番号151及び配列番号68;
(f)それぞれ、配列番号52及び配列番号68;
(g)それぞれ、配列番号153及び配列番号68;及び
(h)それぞれ、配列番号154及び配列番号68
からなる群から選択される配列を有する重鎖と軽鎖とを含む、請求項1~6のいずれか一項に記載の免疫コンジュゲート。 - 配列番号141、配列番号142、配列番号143、配列番号151、配列番号152、配列番号153または配列番号154のXが存在しない、請求項7に記載の免疫コンジュゲート。
- 前記ヒト化抗ADAM9抗体が、配列番号152及び配列番号68の配列をそれぞれ有する重鎖及び軽鎖を含む、請求項1~8のいずれか一項に記載の免疫コンジュゲート。
- 前記医薬薬剤が、メイタンシノイド化合物、ピロロベンゾジアゼピン化合物、又はインドリノベンゾジアゼピン化合物である、請求項1~9のいずれか一項に記載の免疫コンジュゲート。
- 前記医薬薬剤が、メイタンシノイド化合物である、請求項10に記載の免疫コンジュゲート。
- 前記免疫コンジュゲートが、以下からなる群から選択される式:
(I)
CBAは、リシン残基を介してCyL1に共有結合する、前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり;
CyL1は、以下の式
NとCとの間の二重線
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は、(C1-C6)アルキルであり;
L’は、以下の式
-NR5-P-C(=O)-(CRaRb)m-C(=O)- (B1’);または
-NR5-P-C(=O)-(CRaRb)m-S-Zs1- (B2’)
によって表され、
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、それぞれ独立して、-H、(C1-C3)アルキル、または帯電した置換基またはイオン化可能な基Qであり;
mは、1~6の整数であり;
Zs1は、以下の式
qは、1~5の整数であり、そして任意選択で、前記医薬的に許容される塩はナトリウム塩またはカリウム塩である;
(II)
CBAは、リシン残基を介してCyL2に共有結合する、前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり;
CyL2は、以下の式
NとCとの間の二重線
Rx1及びRX2は、独立に(C1-C6)アルキルであり;
Reは、-Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Zs1は、以下の式
qは、1~5の整数であり、そして任意選択で、前記医薬的に許容される塩はナトリウム塩またはカリウム塩である;
(III)
CBAは、リシン残基を介してCyL3に共有結合する、前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WLは、1~20の整数であり;
CyL3は、以下の式
m’は1または2であり;
R1およびR2は,それぞれ独立に、Hまたは(C1-C3)アルキルであり;
Zs1は、以下の式
qは、1~5の整数であり、そして任意選択で、前記医薬的に許容される塩はナトリウム塩またはカリウム塩である;
(IV)
CBAは、システイン残基を介してCyC1に共有結合する、前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり;
CyC1は、以下の式
NとCとの間の二重線
R5は、-Hまたは(C1-C3)アルキルであり;
Pは、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり;
Ra及びRbは、それぞれの場合に、それぞれ独立して、-H、(C1-C3)アルキル、または帯電した置換基またはイオン化可能な基Qであり;
W’は、-NRe’であり、
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx3は(C1-C6)アルキルであり;
LCは
R19及びR20は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
m”は、1~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり、そして任意選択で、前記医薬的に許容される塩はナトリウム塩またはカリウム塩である;
(V)
CBAは、システイン残基を介してCyC2に共有結合する、前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり;
CyC2は、以下の式
NとCとの間の二重線
Rx1は、(C1-C6)アルキルであり;
Reは、-Hまたは(C1-C6)アルキルであり;
W’は、-NRe’であり;
Re’は、-(CH2-CH2-O)n-Rkであり;
nは、2~6の整数であり;
Rkは、-Hまたは-Meであり;
Rx2は(C1-C6)アルキルであり;
LC ’は
Zは、C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、-H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、それぞれ独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり、そして任意選択で、前記医薬的に許容される塩はナトリウム塩またはカリウム塩である;および
(VI)
CBAは、システイン残基を介してCyC3に共有結合する、前記ヒト化抗ADAM9抗体またはそのADAM9結合フラグメントであり;
WCは、1または2であり;
CyC3は、以下の式
m’は、1または2であり;
R1およびR2は、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
LC ’は
Zは、-C(=O)-NR9-または-NR9-C(=O)-であり;
Qは、-H、帯電した置換基またはイオン化可能な基であり;
R9、R10、R11、R12、R13、R19、R20、R21及びR22は、それぞれの場合に、それぞれ独立して、-Hまたは(C1-C3)アルキルであり;
q及びrは、それぞれの場合に、それぞれ独立して、0~10の整数であり;
m及びnは、それぞれ独立して、0~10の整数であり;
Rhは、-Hまたは(C1-C3)アルキルであり;
P’は、アミノ酸残基または2~20個のアミノ酸残基を含有するペプチドであり、そして任意選択で、前記医薬的に許容される塩はナトリウム塩またはカリウム塩である;
によって表される、請求項1~11のいずれか一項に記載の免疫コンジュゲート。 - 有効量の請求項1~12のいずれか一項に記載の免疫コンジュゲートと、医薬的に許容される担体、賦形剤または希釈剤とを含む、医薬組成物。
- ADAM9の発現と関連するか、またはADAM9の発現によって特徴付けられる疾患または状態の治療における使用のための医薬組成物であって、請求項1~12のいずれか一項に記載の免疫コンジュゲートを含む、前記医薬組成物。
- ADAM9と関連するか、またはADAM9によって特徴付けられる前記疾患または状態が、がんであり、任意選択で、前記がんが、非小細胞肺癌、大腸癌、膀胱癌、胃癌、膵臓癌、腎細胞癌、前立腺癌、食道癌、乳癌、頭頸部癌、子宮癌、卵巣癌、肝臓癌、子宮頸癌、甲状腺癌、精巣癌、骨髄がん、黒色腫及びリンパがんからなる群から選択される、請求項14に記載の医薬組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662438488P | 2016-12-23 | 2016-12-23 | |
| US62/438,488 | 2016-12-23 | ||
| US201762480201P | 2017-03-31 | 2017-03-31 | |
| US62/480,201 | 2017-03-31 | ||
| PCT/US2017/067823 WO2018119196A1 (en) | 2016-12-23 | 2017-12-21 | Immunoconjugates targeting adam9 and methods of use thereof |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020504607A JP2020504607A (ja) | 2020-02-13 |
| JP2020504607A5 JP2020504607A5 (ja) | 2021-02-04 |
| JP7170642B2 true JP7170642B2 (ja) | 2022-11-14 |
Family
ID=61025051
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019533514A Active JP7170642B2 (ja) | 2016-12-23 | 2017-12-21 | Adam9を標的とする免疫コンジュゲート及びその使用 |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US20210388102A1 (ja) |
| EP (1) | EP3558391B1 (ja) |
| JP (1) | JP7170642B2 (ja) |
| CN (1) | CN110267685B (ja) |
| DK (1) | DK3558391T3 (ja) |
| ES (1) | ES2912266T3 (ja) |
| HR (1) | HRP20220550T1 (ja) |
| HU (1) | HUE058664T2 (ja) |
| LT (1) | LT3558391T (ja) |
| MD (1) | MD3558391T2 (ja) |
| PL (1) | PL3558391T3 (ja) |
| PT (1) | PT3558391T (ja) |
| RS (1) | RS63154B1 (ja) |
| SI (1) | SI3558391T1 (ja) |
| TW (1) | TWI783957B (ja) |
| WO (1) | WO2018119196A1 (ja) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20200108843A (ko) | 2018-01-12 | 2020-09-21 | 이뮤노젠 아이엔씨 | 항체 약물 접합, 정제, 및 제제화 방법 |
| WO2020005945A1 (en) * | 2018-06-26 | 2020-01-02 | Immunogen, Inc. | Immunoconjugates targeting adam9 and methods of use thereof |
| WO2020191306A1 (en) | 2019-03-21 | 2020-09-24 | Immunogen, Inc. | Methods of preparing cell-binding agent-drug conjugates |
| WO2020205564A1 (en) | 2019-03-29 | 2020-10-08 | Immunogen, Inc. | Cytotoxic bis-benzodiazepine derivatives and conjugates thereof with cell-binding agents for inhibiting abnormal cell growth or for treating proliferative diseases |
| TW202106691A (zh) | 2019-04-26 | 2021-02-16 | 美商伊繆諾金公司 | 喜樹鹼衍生物 |
| CN110713983B (zh) * | 2019-11-04 | 2022-06-10 | 深圳市体内生物医药科技有限公司 | 一种表达透明质酸酶的免疫细胞及其应用 |
| EP4304660A1 (en) | 2021-03-08 | 2024-01-17 | ImmunoGen, Inc. | Methods for increasing efficacy of immunoconjugates targeting adam9 for the treatment of cancer |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10337368A1 (de) | 2003-08-08 | 2005-03-03 | Technische Universität Dresden | Verfahren und Mittel zur Diagnose und Behandlung von Pankreastumoren |
| US20090285840A1 (en) | 2008-04-29 | 2009-11-19 | New York Society For The Ruptured And Crippled Maintaining The Hospital For Special Surgery | Methods for treating pathological neovascularization |
Family Cites Families (68)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US5807715A (en) | 1984-08-27 | 1998-09-15 | The Board Of Trustees Of The Leland Stanford Junior University | Methods and transformed mammalian lymphocyte cells for producing functional antigen-binding protein including chimeric immunoglobulin |
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| DE69233482T2 (de) | 1991-05-17 | 2006-01-12 | Merck & Co., Inc. | Verfahren zur Verminderung der Immunogenität der variablen Antikörperdomänen |
| WO1994004679A1 (en) | 1991-06-14 | 1994-03-03 | Genentech, Inc. | Method for making humanized antibodies |
| GB9115364D0 (en) | 1991-07-16 | 1991-08-28 | Wellcome Found | Antibody |
| CA2078539C (en) | 1991-09-18 | 2005-08-02 | Kenya Shitara | Process for producing humanized chimera antibody |
| ES2136092T3 (es) | 1991-09-23 | 1999-11-16 | Medical Res Council | Procedimientos para la produccion de anticuerpos humanizados. |
| US5733743A (en) | 1992-03-24 | 1998-03-31 | Cambridge Antibody Technology Limited | Methods for producing members of specific binding pairs |
| US6180377B1 (en) | 1993-06-16 | 2001-01-30 | Celltech Therapeutics Limited | Humanized antibodies |
| US6265150B1 (en) | 1995-06-07 | 2001-07-24 | Becton Dickinson & Company | Phage antibodies |
| WO1998023289A1 (en) | 1996-11-27 | 1998-06-04 | The General Hospital Corporation | MODULATION OF IgG BINDING TO FcRn |
| US6277375B1 (en) | 1997-03-03 | 2001-08-21 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| JP5179689B2 (ja) | 2000-02-11 | 2013-04-10 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | 抗体ベース融合タンパク質の循環系内半減期の増強 |
| US20030091568A1 (en) | 2000-04-07 | 2003-05-15 | Jurgen Frey | Inhibitors for the formation of soluble human CD23 |
| EP1142910A1 (en) | 2000-04-07 | 2001-10-10 | Jürgen Prof. Dr. Frey | Inhibitors for the formation of soluble human CD23 |
| PT1355919E (pt) | 2000-12-12 | 2011-03-02 | Medimmune Llc | Moléculas com semivida longa, composições que as contêm e suas utilizações |
| CN1620309A (zh) | 2001-12-18 | 2005-05-25 | 蒙多生物技术实验室 | 用于结合分子诊断法改进间质性肺疾病的治疗的干扰素γ或甲苯吡啶酮的新型药物组合物 |
| US6716821B2 (en) | 2001-12-21 | 2004-04-06 | Immunogen Inc. | Cytotoxic agents bearing a reactive polyethylene glycol moiety, cytotoxic conjugates comprising polyethylene glycol linking groups, and methods of making and using the same |
| US20040092466A1 (en) | 2002-11-11 | 2004-05-13 | Isis Pharmaceuticals Inc. | Modulation of ADAM9 expression |
| AU2003259163B2 (en) | 2002-08-16 | 2008-07-03 | Immunogen, Inc. | Cross-linkers with high reactivity and solubility and their use in the preparation of conjugates for targeted delivery of small molecule drugs |
| US7217797B2 (en) | 2002-10-15 | 2007-05-15 | Pdl Biopharma, Inc. | Alteration of FcRn binding affinities or serum half-lives of antibodies by mutagenesis |
| US8088387B2 (en) | 2003-10-10 | 2012-01-03 | Immunogen Inc. | Method of targeting specific cell populations using cell-binding agent maytansinoid conjugates linked via a non-cleavable linker, said conjugates, and methods of making said conjugates |
| US7276497B2 (en) | 2003-05-20 | 2007-10-02 | Immunogen Inc. | Cytotoxic agents comprising new maytansinoids |
| EP1697415A1 (en) | 2003-11-12 | 2006-09-06 | Biogen Idec MA Inc. | NEONATAL Fc RECEPTOR (FcRn)-BINDING POLYPEPTIDE VARIANTS, DIMERIC Fc BINDING PROTEINS AND METHODS RELATED THERETO |
| US7829277B2 (en) | 2004-03-01 | 2010-11-09 | The Regents Of The University Of California | Methods for identifying compounds that suppress chemically-induced carcinogenesis |
| US8802820B2 (en) | 2004-11-12 | 2014-08-12 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| US8367805B2 (en) | 2004-11-12 | 2013-02-05 | Xencor, Inc. | Fc variants with altered binding to FcRn |
| CN101142236B (zh) | 2005-02-02 | 2013-03-20 | 雷文生物技术公司 | Adam-9调节剂 |
| US8445198B2 (en) | 2005-12-01 | 2013-05-21 | Medical Prognosis Institute | Methods, kits and devices for identifying biomarkers of treatment response and use thereof to predict treatment efficacy |
| US8524865B2 (en) | 2006-05-30 | 2013-09-03 | Genentech, Inc. | Antibodies and immunoconjugates and uses therefor |
| WO2007143752A2 (en) | 2006-06-09 | 2007-12-13 | The Regents Of The University Of California | Targets in breast cancer for prognosis or therapy |
| KR101443214B1 (ko) | 2007-01-09 | 2014-09-24 | 삼성전자주식회사 | 폐암 환자 또는 폐암 치료를 받은 폐암 환자의 폐암 재발 위험을 진단하기 위한 조성물, 키트 및 마이크로어레이 |
| PT2019104E (pt) | 2007-07-19 | 2013-12-03 | Sanofi Sa | Agentes citotóxicos compreendendo novos derivados de tomaimicina e sua utilização terapêutica |
| GB2453589A (en) | 2007-10-12 | 2009-04-15 | King S College London | Protease inhibition |
| WO2009114532A2 (en) | 2008-03-10 | 2009-09-17 | National Jewish Health | Markers for diagnosis of pulmonary inflammation and methods related thereto |
| AU2009233899A1 (en) | 2008-04-07 | 2009-10-15 | Zymogenetics, Inc. | Thrombin activator compostions and methods of making and using the same |
| SG189817A1 (en) | 2008-04-30 | 2013-05-31 | Immunogen Inc | Potent conjugates and hydrophilic linkers |
| DK2281006T3 (da) | 2008-04-30 | 2017-11-06 | Immunogen Inc | Tværbindingsmidler og anvendelser deraf |
| ES2675730T3 (es) | 2008-06-04 | 2018-07-12 | Macrogenics, Inc. | Anticuerpos con unión alterada a FcRn y métodos de uso de los mismos |
| WO2010014990A2 (en) | 2008-08-01 | 2010-02-04 | The Board Of Trustees Of The University Of Illinois | Method of promoting neurogenesis by modulating secretase activities |
| GB0819095D0 (en) | 2008-10-17 | 2008-11-26 | Spirogen Ltd | Pyrrolobenzodiazepines |
| US20100112713A1 (en) | 2008-11-05 | 2010-05-06 | The Texas A&M University System | Methods For Detecting Colorectal Diseases And Disorders |
| EP2373692A4 (en) | 2008-12-04 | 2013-11-20 | Abbvie Inc | IMMUNOGLOBULINE WITH DOUBLE VARIABLE DOMAIN AND ITS USE |
| MX368362B (es) | 2009-02-05 | 2019-09-30 | Immunogen Inc | Derivados novedosos de benzodiacepina. |
| RU2765240C2 (ru) | 2009-06-03 | 2022-01-27 | Иммьюноджен, Инк. | Способы конъюгации |
| EP2910565A3 (en) | 2010-02-11 | 2015-11-04 | University of Southern California | Modified ADAM disintegrin domain polypeptides and uses |
| GEP20166442B (en) | 2010-03-04 | 2016-03-10 | Macrogenics Inc | Antibodies reactive with b7-h3, immunologically active fragments thereof and uses thereof |
| MX339185B (es) | 2010-04-15 | 2016-05-16 | Seattle Genetics Inc | Pirrolobenzodiazepinas usadas para tratar enfermedades proliferativas. |
| EP3666289A1 (en) | 2011-02-15 | 2020-06-17 | ImmunoGen, Inc. | Cytotoxic benzodiazepine derivatives |
| UA116189C2 (uk) * | 2011-05-02 | 2018-02-26 | Мілленніум Фармасьютікалз, Інк. | КОМПОЗИЦІЯ АНТИ-α4β7 АНТИТІЛА |
| US20130058947A1 (en) | 2011-09-02 | 2013-03-07 | Stem Centrx, Inc | Novel Modulators and Methods of Use |
| US20130130355A1 (en) | 2011-09-28 | 2013-05-23 | Armune Biosciences, Inc. | Method and system of particle-phage epitope complex |
| IN2014CN04935A (ja) | 2011-12-31 | 2015-09-18 | Moni Abraham Kuriakose | |
| US9534058B2 (en) | 2012-02-08 | 2017-01-03 | Abbvie Stemcentrx Llc | Anti-CD324 monoclonal antibodies and uses thereof |
| WO2013177481A1 (en) | 2012-05-25 | 2013-11-28 | Immunogen, Inc. | Benzodiazepines and conjugates thereof |
| US10851402B2 (en) | 2013-01-09 | 2020-12-01 | Friedrich-Alexander-Universitaet Erlangen-Nuernberg | Method for in vitro detection and monitoring of a disease by measuring disease-associated protease activity in extracellular vesicles |
| EP2954056A4 (en) | 2013-02-08 | 2016-09-21 | Stemcentrx Inc | NEW MULTISPECIFIC CONSTRUCTIONS |
| US20160024582A1 (en) | 2013-04-08 | 2016-01-28 | Mitsubishi Rayon Co., Ltd. | Microarray for evaluating eye disease, and evaluation method of eye disease |
| CA2912542A1 (en) | 2013-05-13 | 2014-11-20 | Tufts University | Methods and compositions for prognosis, diagnosis and treatment of adam8-expressing cancer |
| CA2915823A1 (en) | 2013-06-19 | 2014-12-24 | Memorial Sloan-Kettering Cancer Center | Methods and compositions for the diagnosis, prognosis and treatment of brain metastasis |
| US9567641B2 (en) | 2013-07-03 | 2017-02-14 | Samsung Electronics Co., Ltd. | Combination therapy for the treatment of cancer using an anti-C-met antibody |
| CN116514903A (zh) | 2014-09-03 | 2023-08-01 | 伊缪诺金公司 | 细胞毒性苯并二氮杂䓬衍生物 |
| CN107580604A (zh) * | 2014-09-03 | 2018-01-12 | 伊缪诺金公司 | 包含细胞结合剂和细胞毒性剂的缀合物 |
| JP2017527562A (ja) | 2014-09-03 | 2017-09-21 | イミュノジェン・インコーポレーテッド | 細胞毒性ベンゾジアゼピン誘導体 |
| JP2018500049A (ja) | 2014-11-11 | 2018-01-11 | アムニクス オペレーティング インコーポレイテッド | ターゲティングxtenコンジュゲート組成物およびそれを作製する方法 |
| DK3313845T3 (da) | 2015-06-29 | 2020-11-16 | Immunogen Inc | Konjugater af cysteinmanipulerede antistoffer |
-
2017
- 2017-12-21 MD MDE20191243T patent/MD3558391T2/ro unknown
- 2017-12-21 DK DK17835533.5T patent/DK3558391T3/da active
- 2017-12-21 ES ES17835533T patent/ES2912266T3/es active Active
- 2017-12-21 HR HRP20220550TT patent/HRP20220550T1/hr unknown
- 2017-12-21 SI SI201731135T patent/SI3558391T1/sl unknown
- 2017-12-21 HU HUE17835533A patent/HUE058664T2/hu unknown
- 2017-12-21 CN CN201780079982.XA patent/CN110267685B/zh active Active
- 2017-12-21 JP JP2019533514A patent/JP7170642B2/ja active Active
- 2017-12-21 WO PCT/US2017/067823 patent/WO2018119196A1/en unknown
- 2017-12-21 EP EP17835533.5A patent/EP3558391B1/en active Active
- 2017-12-21 TW TW106145085A patent/TWI783957B/zh active
- 2017-12-21 PT PT178355335T patent/PT3558391T/pt unknown
- 2017-12-21 US US16/469,494 patent/US20210388102A1/en active Pending
- 2017-12-21 RS RS20220395A patent/RS63154B1/sr unknown
- 2017-12-21 PL PL17835533T patent/PL3558391T3/pl unknown
- 2017-12-21 LT LTEPPCT/US2017/067823T patent/LT3558391T/lt unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10337368A1 (de) | 2003-08-08 | 2005-03-03 | Technische Universität Dresden | Verfahren und Mittel zur Diagnose und Behandlung von Pankreastumoren |
| US20090285840A1 (en) | 2008-04-29 | 2009-11-19 | New York Society For The Ruptured And Crippled Maintaining The Hospital For Special Surgery | Methods for treating pathological neovascularization |
Non-Patent Citations (2)
| Title |
|---|
| Bioconjugate Chem.,2010年,Vol. 21,p. 84-92 |
| Blood,2016年12月02日,Volume 128, Issue 22: 2832 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3558391A1 (en) | 2019-10-30 |
| PL3558391T3 (pl) | 2022-05-16 |
| MD3558391T2 (ro) | 2022-05-31 |
| US20210388102A1 (en) | 2021-12-16 |
| HUE058664T2 (hu) | 2022-09-28 |
| WO2018119196A1 (en) | 2018-06-28 |
| WO2018119196A8 (en) | 2019-06-20 |
| CN110267685A (zh) | 2019-09-20 |
| SI3558391T1 (sl) | 2022-06-30 |
| TW201822821A (zh) | 2018-07-01 |
| ES2912266T3 (es) | 2022-05-25 |
| CN110267685B (zh) | 2023-06-20 |
| JP2020504607A (ja) | 2020-02-13 |
| HRP20220550T1 (hr) | 2022-06-10 |
| PT3558391T (pt) | 2022-05-05 |
| RS63154B1 (sr) | 2022-05-31 |
| DK3558391T3 (da) | 2022-05-09 |
| TWI783957B (zh) | 2022-11-21 |
| EP3558391B1 (en) | 2022-02-02 |
| LT3558391T (lt) | 2022-07-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7170642B2 (ja) | Adam9を標的とする免疫コンジュゲート及びその使用 | |
| US20210171637A1 (en) | Anti-b7-h3 antibodies and antibody drug conjugates | |
| JP7203497B2 (ja) | 抗cd123抗体、ならびにその複合体及び誘導体 | |
| KR102419766B1 (ko) | 항체에 대한 링커 약물의 부위 특이적 접합 및 그 결과로 얻어지는 adc | |
| US20210403594A1 (en) | Epcam antibodies, activatable antibodies, and immunoconjugates, and uses thereof | |
| US11834498B2 (en) | Biparatopic FR-alpha antibodies and immunoconjugates | |
| US20210275685A1 (en) | Immunoconjugates targeting adam9 and methods of use thereof | |
| US20180230218A1 (en) | Met antibodies and immunoconjugates and uses thereof | |
| TWI831797B (zh) | 靶向adam9之免疫接合物及其使用方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201218 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20201218 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220131 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220427 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220630 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20221014 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20221101 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7170642 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |