JP7019727B2 - インフルエンザの治療方法 - Google Patents
インフルエンザの治療方法 Download PDFInfo
- Publication number
- JP7019727B2 JP7019727B2 JP2019563650A JP2019563650A JP7019727B2 JP 7019727 B2 JP7019727 B2 JP 7019727B2 JP 2019563650 A JP2019563650 A JP 2019563650A JP 2019563650 A JP2019563650 A JP 2019563650A JP 7019727 B2 JP7019727 B2 JP 7019727B2
- Authority
- JP
- Japan
- Prior art keywords
- influenza
- virus
- influenza virus
- pharmaceutical composition
- pharmaceutically acceptable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- WVROWPPEIMRGAB-UHFFFAOYSA-N C[n]1ncc(-c2cccc3c2ccc(C(NC(N)=N)=O)c3)c1 Chemical compound C[n]1ncc(-c2cccc3c2ccc(C(NC(N)=N)=O)c3)c1 WVROWPPEIMRGAB-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/196—Carboxylic acids, e.g. valproic acid having an amino group the amino group being directly attached to a ring, e.g. anthranilic acid, mefenamic acid, diclofenac, chlorambucil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/351—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom not condensed with another ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7012—Compounds having a free or esterified carboxyl group attached, directly or through a carbon chain, to a carbon atom of the saccharide radical, e.g. glucuronic acid, neuraminic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/16—Antivirals for RNA viruses for influenza or rhinoviruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Virology (AREA)
- Molecular Biology (AREA)
- Oncology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Communicable Diseases (AREA)
- Pulmonology (AREA)
- Emergency Medicine (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Description
●ノイラミニダーゼ阻害剤-オセルタミビル(oseltamivir)、ザナミビル(zanamivir)、及びペラミビル(peramivir)を含む。
●M2イオンチャネル阻害剤-アマンタジン(amantadine)及びリマンタジン(rimantadine)を含む。これらの薬物は、構造的に異なるM2チャネルのため、A型インフルエンザウイルスに対しては有効であるが、B型インフルエンザウイルスに対しては有効ではない。
以前は、N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド(BIT225)は、A型インフルエンザのM2ビロポリンに対して限られた活性しか有しないことが示されており、インフルエンザを治療するのに適切であるとは考えられていなかった(Jalily et al., MolPharm, 2016. 90: 80-95)。しかし、本出願は、驚くべきことに、BIT225が、インフルエンザウイルスの複数の亜型及び株に対して活性を有することを示す。重要なことに、BIT225は、アマンタジン(amantadine)に耐性のある亜型及び株に対して活性を有することが見出されている。
本発明の説明及び特許請求の範囲において、以下の用語は、以下に記載される定義に従って使用されている。また、本明細書で使用される用語は、本発明の特定の実施形態を説明することのみを目的としており、限定することを意図するものではないことも理解されたい。他に定義されない限り、本明細書で使用される全ての技術用語及び科学用語は、本発明が関係する当業者によって一般に理解されるのと同じ意味を有する。
本明細書に詳述される特定の実施形態を参照して本発明を説明しているが、他の実施形態は同じ又は同様の結果を達成することができる。本発明のバリエーション及び変更は当業者には明らかであり、本発明は全てのそのような変更及び均等物に及ぶことが意図される。
250mLの丸底フラスコ中の5-ブロモ-2-ナフトエ酸(2.12g、8.44mmol)、1-メチル-4-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)-1H-ピラゾール(1.84g、8.86mmol)、及びテトラキス(トリフェニルホスフィン)パラジウム(0)(502mg、0.435mmol)の混合物を、排気し、窒素でパージした(3回のサイクルにおいて)。アセトニトリル(40mL)及び2M炭酸ナトリウム水溶液(10mL)をシリンジにより混合物に添加し、混合物を還流下で窒素下で22時間加熱した。反応混合物を冷まし、その後、1M塩酸水溶液(30mL)を添加し、次いで、それを酢酸エチル(3×50mL)で抽出した。合わせた有機層を乾燥させ(MgSO4)、ろ過し、真空中で濃縮し、粗生成物(空気乾燥後2.98g)を得た。この粗材料を熱エタノール(150mL)に溶解し、熱いうちにろ過して、黄色不純物(120mg)を除去した。ろ液を真空中で濃縮し、残渣をジクロロメタン(30mL)から再結晶化し、5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトエ酸を白色固体(724mg、34%)として得た。2回目の収穫の5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトエ酸(527mg、25%)は、ジクロロメタン(20mL)からの再結晶化により濃縮母液から得られた。
BIT225の活性は、次のウイルス株に対して測定した:
●A型インフルエンザ/ニューカレドニア(New Caledonia)/20/99(H1N1)。最新のワクチン(CDC)に使用される最近の臨床分離株;
●A型インフルエンザ/パナマ(Panama)/2007/99(H3N2)。最新のワクチン(CDC)に使用される最近の臨床分離株;
●B型インフルエンザ/香港(Hong Kong)/330/02。最新のワクチン(CDC)に使用される最近の臨床分離株;
●A型インフルエンザ/NWS/33(H1N1)。よく認識されている実験室株(KW. Cochran, Univ. Michigan)。
迅速スクリーニングアッセイ
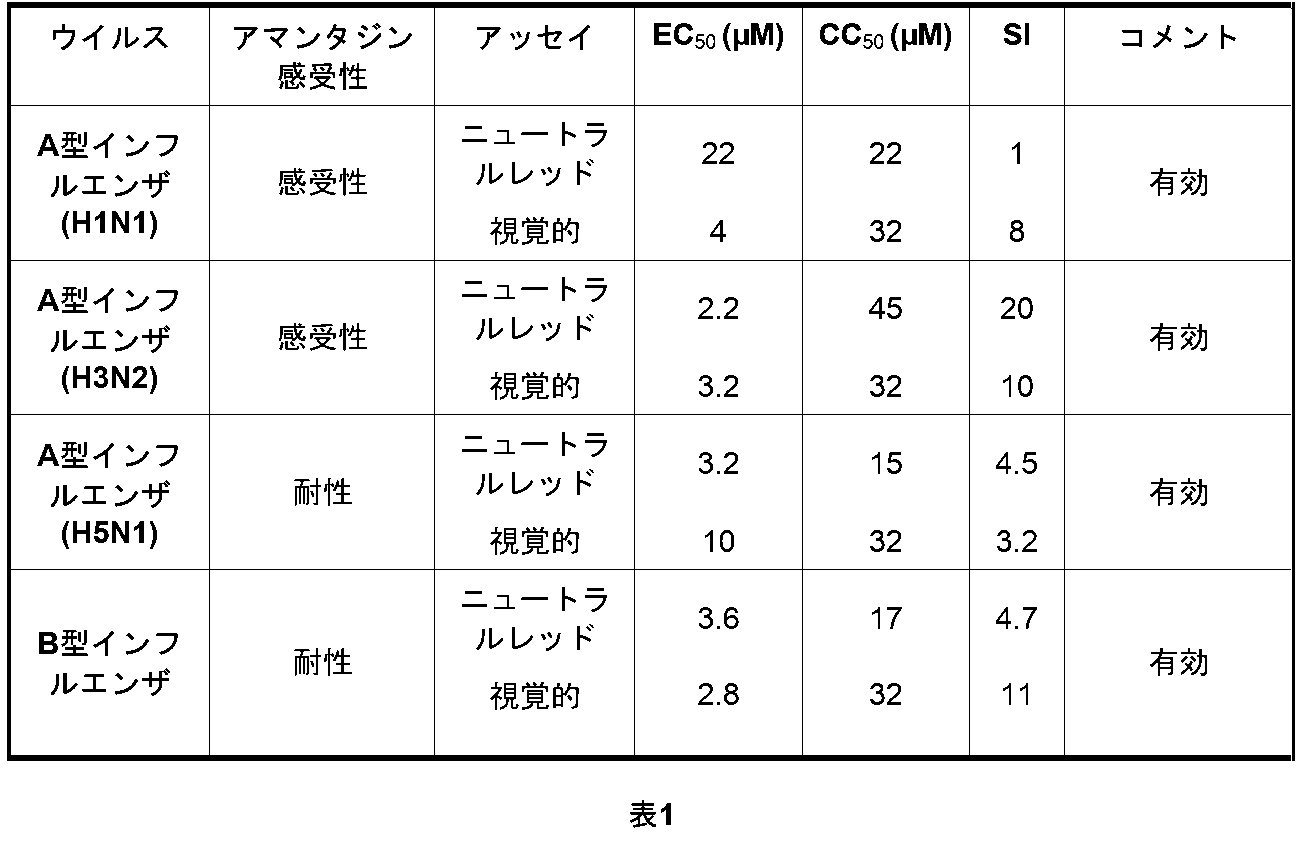
標準的な細胞変性効果(CPE)アッセイは、適切な細胞の18時間単層(80~100%コンフルエント)を使用し、培地を除去し、各濃度の試験化合物又はプラセボを添加し、その後15分以内にウイルス又はウイルス希釈液を添加する。抗ウイルス試験及び細胞毒性試験の両方について、化合物の各濃度について2つのウェルを使用する。プレートを密封し、ほぼ最大のウイルスCPEを誘導するのに必要な標準時間インキュベートする。次いで、以下に説明する方法でプレートをニュートラルレッドで染色し、生細胞を示す取り込みの割合を405及び540nmの二重波長でマイクロプレートオートリーダーで読み取り、バックグラウンドを除去するために差を取る。おおよそのウイルス阻害濃度、50%エンドポイント(EC50)及び細胞阻害濃度、50%エンドポイント(CC50)を決定し、これらから一般的な選択性指数を計算する: SI=(CC50)/(EC50)。3以上のSIは、確認試験を誘発する。
このアッセイは、96ウェルの平底マイクロプレートで実行され、全ての新しい試験化合物の最初の抗ウイルス評価に使用される。このCPE阻害試験では、各試験化合物の4個のlog10希釈液(例えば、1000、100、10、1μg/mL)を、細胞単層を含有する3個のウェルに添加し、5分以内にウイルスを添加し、プレートを密封し、37℃でインキュベートする。CPEは、未処理の感染対照が3~4+のCPEを生じるとき(約72~120時間)に顕微鏡で読み取る。公知の陽性対照薬物を、各アッセイ実行で試験薬物と並行して評価する。最初のスクリーニング試験で有効であることが見出された化合物を使用したフォローアップ試験を、各化合物の8個の1/2log10希釈液を、1つの希釈液あたり細胞単層を含有する4個のウェルに使用することを除いて、同じ方法で実行する。
このアッセイは、最初の試験で観察されたCPE阻害を検証するために実行され、CPEが評価された後に同じ96ウェルマイクロプレートを利用する。ニュートラルレッドを培地に添加する; ウイルスによって損傷を受けていない細胞は、より大量の色素を取り込み、これをコンピュータ化されたマイクロプレートオートリーダーで読み取る。McManus(McManus, App Environ Microbiol, 1976. 31(1): 35-38)によって記載された方法を使用する。EC50を色素取り込みから決定する。
BIT225の抗A型インフルエンザウイルス活性を、メイディン・ダービー(Madin Darby)イヌ腎臓(MDCK)細胞におけるin vitro用量反応プラーク低減アッセイによって確認した。実験室株PR8をこれらの実験で使用し、アマンタジン(amantadine)耐性バリアントウイルスを、アラニンの代わりに30位の配列トレオニンをコードするようにM2遺伝子を変異させることによって作成した。[A30T]変異体ウイルスはPR8 4Cとして公知である。
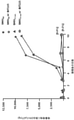
それぞれA型インフルエンザM2又はHIV-1 Vpuのイオンチャネル配列を発現するキメラウイルスSHIV-1M2及びSHIV-1SCVpuのT細胞株(C8166)中での複製に対するBIT225の効果を調べるために、実験を行った。10μM BIT225で処理すると、ウイルスp27タンパク質によって測定される培養上清に放出されるウイルスが低減した(図2)。担体溶媒単独(DMSO)で処理した対照を比較のために示す。
(付記)
(付記1)
対象におけるインフルエンザウイルス感染の治療又は予防方法であって、対象に、有効量のN-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩を投与するステップを含む、方法。
(付記2)
インフルエンザウイルスの複製が阻害される、付記1に記載の方法。
(付記3)
インフルエンザウイルス感染に関連する合併症又は症状の重症度、強度、又は期間が低減する、付記1又は付記2に記載の方法。
(付記4)
インフルエンザウイルスの力価が低減する、付記1~3のいずれか一つに記載の方法。
(付記5)
インフルエンザウイルスが、A型インフルエンザウイルス、B型インフルエンザウイルス、及びC型インフルエンザウイルスから選択される、付記1~4のいずれか一つに記載の方法。
(付記6)
インフルエンザウイルスが、A型インフルエンザウイルスである、付記1~5のいずれか一つに記載の方法。
(付記7)
A型インフルエンザウイルスが、H1N1、H1N2、H2N2、H3N2、H3N8、H5N1、H5N2、H5N3、H5N6、H5N8、H5N9、H7N1、H7N2、H7N3、H7N4、H7N7、H7N9、H9N2、及びH10N7亜型から選択される、付記6に記載の方法。
(付記8)
A型インフルエンザウイルスが、H1N1、H3N2及びH5N1亜型から選択される、付記6又は付記7に記載の方法。
(付記9)
インフルエンザウイルスが、B型インフルエンザウイルスである、付記1~5のいずれか一つに記載の方法。
(付記10)
N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口、経鼻、静脈内、腹腔内、吸入及び局所から選択される経路により投与される、付記1~9のいずれか一つに記載の方法。
(付記11)
N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口的に投与される、付記1~10のいずれか一つに記載の方法。
(付記12)
N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、約100mg~約600mgの投与量で投与される、付記1~11のいずれか一つに記載の方法。
(付記13)
N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口的に、1日1回、約100mg~約200mgの投与量で投与される、付記1~12のいずれか一つに記載の方法。
(付記14)
N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口的に、1日2回、約100mg~約200mgの投与量で投与される、付記1~12のいずれか一つに記載の方法。
(付記15)
N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、好ましくはザナミビル、オセルタミビル及びペラミビルから選択される、1つ以上の追加の抗ウイルス剤と組み合わせて投与される、付記1~14のいずれか一つに記載の方法。
(付記16)
インフルエンザウイルス感染の治療又は予防のための医薬の製造のための、N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩の使用。
(付記17)
インフルエンザウイルスの複製が阻害される、付記16に記載の使用。
(付記18)
インフルエンザウイルス感染に関連する合併症又は症状の重症度、強度、又は期間が低減する、付記16又は付記17に記載の使用。
(付記19)
インフルエンザウイルスの力価が低減する、付記16~18のいずれか一つに記載の使用。
Claims (20)
- 対象におけるインフルエンザウイルス感染の治療又は予防のための医薬組成物であって、有効量のN-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩を含む、医薬組成物。
- インフルエンザウイルスの複製を阻害する、請求項1に記載の医薬組成物。
- インフルエンザウイルス感染に関連する合併症又は症状の重症度、強度、又は期間を低減させる、請求項1又は請求項2に記載の医薬組成物。
- インフルエンザウイルスの力価を低減する、請求項1~3のいずれか一項に記載の医薬組成物。
- インフルエンザウイルスが、A型インフルエンザウイルス、B型インフルエンザウイルス、及びC型インフルエンザウイルスから選択される、請求項1~4のいずれか一項に記載の医薬組成物。
- インフルエンザウイルスが、A型インフルエンザウイルスである、請求項1~5のいずれか一項に記載の医薬組成物。
- A型インフルエンザウイルスが、H1N1、H1N2、H2N2、H3N2、H3N8、H5N1、H5N2、H5N3、H5N6、H5N8、H5N9、H7N1、H7N2、H7N3、H7N4、H7N7、H7N9、H9N2、及びH10N7亜型から選択される、請求項6に記載の医薬組成物。
- A型インフルエンザウイルスが、H1N1、H3N2及びH5N1亜型から選択される、請求項6又は請求項7に記載の医薬組成物。
- インフルエンザウイルスが、B型インフルエンザウイルスである、請求項1~5のいずれか一項に記載の医薬組成物。
- N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口、経鼻、静脈内、腹腔内、吸入及び局所から選択される経路により投与される、請求項1~9のいずれか一項に記載の医薬組成物。
- N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口的に投与される、請求項1~10のいずれか一項に記載の医薬組成物。
- N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、約100mg~約600mgの投与量で投与される、請求項1~11のいずれか一項に記載の医薬組成物。
- N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口的に、1日1回、約100mg~約200mgの投与量で投与される、請求項1~12のいずれか一項に記載の医薬組成物。
- N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、経口的に、1日2回、約100mg~約200mgの投与量で投与される、請求項1~12のいずれか一項に記載の医薬組成物。
- N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩が、1つ以上の追加の抗ウイルス剤と組み合わせて投与される、請求項1~14のいずれか一項に記載の医薬組成物。
- 1つ以上の追加の抗ウイルス剤が、ザナミビル、オセルタミビル及びペラミビルから選択される、請求項15に記載の医薬組成物。
- インフルエンザウイルス感染の治療又は予防のための医薬の製造のための、N-カルバムイミドイル-5-(1-メチル-1H-ピラゾール-4-イル)-2-ナフトアミド又はその薬学的に許容される塩の使用。
- インフルエンザウイルスの複製が阻害される、請求項17に記載の使用。
- インフルエンザウイルス感染に関連する合併症又は症状の重症度、強度、又は期間が低減する、請求項17又は請求項18に記載の使用。
- インフルエンザウイルスの力価が低減する、請求項17~19のいずれか一項に記載の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2017900385A AU2017900385A0 (en) | 2017-02-08 | Methods of treating influenza | |
| AU2017900385 | 2017-02-08 | ||
| PCT/AU2018/050085 WO2018145148A1 (en) | 2017-02-08 | 2018-02-07 | Methods of treating influenza |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020506243A JP2020506243A (ja) | 2020-02-27 |
| JP2020506243A5 JP2020506243A5 (ja) | 2021-03-11 |
| JP7019727B2 true JP7019727B2 (ja) | 2022-02-15 |
Family
ID=63106827
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019563650A Active JP7019727B2 (ja) | 2017-02-08 | 2018-02-07 | インフルエンザの治療方法 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US10918623B2 (ja) |
| EP (1) | EP3579833B1 (ja) |
| JP (1) | JP7019727B2 (ja) |
| KR (1) | KR102607599B1 (ja) |
| CN (1) | CN110325187B (ja) |
| AU (1) | AU2018218179B2 (ja) |
| BR (1) | BR112019016316A2 (ja) |
| ES (1) | ES2910136T3 (ja) |
| MX (1) | MX387115B (ja) |
| RU (1) | RU2769317C2 (ja) |
| SG (1) | SG11201907034PA (ja) |
| WO (1) | WO2018145148A1 (ja) |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CR20170278A (es) | 2010-07-22 | 2017-09-29 | Gilead Sciences Inc | Métodos y compuestos para tratar infecciones virales por paramyxoviridae |
| TWI767201B (zh) | 2014-10-29 | 2022-06-11 | 美商基利科學股份有限公司 | 絲狀病毒科病毒感染之治療 |
| PL3349758T3 (pl) | 2015-09-16 | 2022-09-12 | Gilead Sciences, Inc. | Sposoby leczenia zakażeń wirusami arenaviridae |
| CN110869028B (zh) | 2017-03-14 | 2023-01-20 | 吉利德科学公司 | 治疗猫冠状病毒感染的方法 |
| US10836787B2 (en) | 2017-05-01 | 2020-11-17 | Gilead Sciences, Inc. | Crystalline forms of (S)-2-ethylbutyl 2-(((S)-(((2R,3S,4R,5R)-5- (4-aminopyrrolo[2,1-f] [1,2,4]triazin-7-yl)-5-cyano-3,4-dihydroxytetrahydrofuran-2-yl)methoxy)(phenoxy) phosphoryl)amino)propanoate |
| ES3000461T3 (en) | 2017-07-11 | 2025-02-28 | Gilead Sciences Inc | Compositions comprising an rna polymerase inhibitor and cyclodextrin for treating viral infections |
| CN114641299A (zh) | 2020-01-27 | 2022-06-17 | 吉利德科学公司 | 用于治疗SARS CoV-2感染的方法 |
| CA3169340A1 (en) | 2020-03-12 | 2021-09-16 | Pavel R. Badalov | Methods of preparing 1'-cyano nucleosides |
| EP4132651B1 (en) | 2020-04-06 | 2026-03-18 | Gilead Sciences, Inc. | Inhalation formulations of 1'-cyano substituted carbanucleoside analogs |
| ES3041698T3 (en) | 2020-05-29 | 2025-11-13 | Gilead Sciences Inc | Remdesivir for the treatment of viral infections |
| US11939347B2 (en) | 2020-06-24 | 2024-03-26 | Gilead Sciences, Inc. | 1′-cyano nucleoside analogs and uses thereof |
| PE20231847A1 (es) | 2020-08-24 | 2023-11-21 | Gilead Sciences Inc | Compuestos fosfolipidos y usos de los mismos |
| DK4204421T3 (da) | 2020-08-27 | 2024-05-27 | Gilead Sciences Inc | Forbindelser og fremgangsmåder til behandling af virale infektioner |
| TW202344257A (zh) | 2020-10-16 | 2023-11-16 | 美商基利科學股份有限公司 | 磷脂化合物及其用途 |
| US12427150B2 (en) | 2021-05-26 | 2025-09-30 | Gilead Sciences, Inc. | Phospholipid formulations of 1′-cyano substituted carba-nucleoside analogs |
| JP7719954B2 (ja) | 2021-08-18 | 2025-08-06 | ギリアード サイエンシーズ, インコーポレイテッド | リン脂質化合物並びにその製造方法及び使用方法 |
| CA3238183A1 (en) * | 2021-11-24 | 2023-06-01 | Michelle Miller | Methods of treating sars-cov-2 infection |
| WO2023167938A1 (en) | 2022-03-02 | 2023-09-07 | Gilead Sciences, Inc. | Compounds and methods for treatment of viral infections |
| MX2024010591A (es) | 2022-03-02 | 2024-09-06 | Gilead Sciences Inc | Compuestos y metodos para el tratamiento de infecciones virales. |
| IL314961A (en) | 2022-03-03 | 2024-10-01 | Gilead Sciences Inc | Antiviral compounds and methods of making and using the same |
| CN118900839A (zh) | 2022-03-03 | 2024-11-05 | 吉利德科学公司 | 抗病毒化合物及其制备和使用方法 |
| AU2023283718A1 (en) | 2022-06-06 | 2024-12-12 | Gilead Sciences, Inc. | Methods for treatment of viral infections including sars-cov-2 |
| WO2024006376A1 (en) | 2022-06-29 | 2024-01-04 | Gilead Sciences, Inc. | Solid forms of a nucleoside analogue and uses thereof |
| US20240043466A1 (en) | 2022-06-30 | 2024-02-08 | Gilead Sciences, Inc. | Solid forms of a nucleoside analogue and uses thereof |
| US12357577B1 (en) | 2024-02-02 | 2025-07-15 | Gilead Sciences, Inc. | Pharmaceutical formulations and uses thereof |
| EP4665737A1 (en) | 2023-02-16 | 2025-12-24 | Gilead Sciences, Inc. | Phospholipid compounds and methods of making and using the same |
| WO2025049699A1 (en) | 2023-08-31 | 2025-03-06 | Gilead Sciences, Inc. | Antiviral compounds and methods of making and using the same |
| CN121693506A (zh) | 2023-08-31 | 2026-03-17 | 吉利德科学公司 | 抗病毒化合物及其制备和使用方法 |
| WO2025054278A1 (en) | 2023-09-06 | 2025-03-13 | Gilead Sciences, Inc. | Solid forms of a nucleoside analogue and uses thereof |
| US20250109157A1 (en) | 2023-09-28 | 2025-04-03 | Gilead Sciences, Inc. | Compounds and methods for treatment of viral infections |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008543886A (ja) | 2005-06-24 | 2008-12-04 | バイオトロン リミテッド | 抗ウイルス化合物および方法 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BRPI0814737B8 (pt) * | 2007-08-03 | 2021-05-25 | Biotron Ltd | composição para o tratamento de hcv, e, uso de uma composição |
| KR101369584B1 (ko) * | 2011-04-19 | 2014-03-06 | 일양약품주식회사 | 페닐-이속사졸 유도체 및 그의 제조방법 |
| MX392650B (es) * | 2014-07-07 | 2025-03-24 | Elian Llc | Metodos de tratamiento profilactico antivirales y kits de profilaxis previa a la exposicion |
| CN110870864B (zh) * | 2018-08-29 | 2021-09-24 | 复旦大学 | 马来酸卡比沙明在制备抗流感病毒药物中的应用 |
-
2018
- 2018-02-07 RU RU2019126746A patent/RU2769317C2/ru active
- 2018-02-07 EP EP18751710.7A patent/EP3579833B1/en active Active
- 2018-02-07 KR KR1020197024919A patent/KR102607599B1/ko active Active
- 2018-02-07 SG SG11201907034PA patent/SG11201907034PA/en unknown
- 2018-02-07 JP JP2019563650A patent/JP7019727B2/ja active Active
- 2018-02-07 US US16/483,958 patent/US10918623B2/en active Active
- 2018-02-07 AU AU2018218179A patent/AU2018218179B2/en active Active
- 2018-02-07 ES ES18751710T patent/ES2910136T3/es active Active
- 2018-02-07 MX MX2019009443A patent/MX387115B/es unknown
- 2018-02-07 WO PCT/AU2018/050085 patent/WO2018145148A1/en not_active Ceased
- 2018-02-07 CN CN201880010492.9A patent/CN110325187B/zh active Active
- 2018-02-07 BR BR112019016316-6A patent/BR112019016316A2/pt not_active Application Discontinuation
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008543886A (ja) | 2005-06-24 | 2008-12-04 | バイオトロン リミテッド | 抗ウイルス化合物および方法 |
Non-Patent Citations (4)
| Title |
|---|
| A. D. Balgi et al.,Inhibitors of the Influenza A Virus M2 Proton Channel Discovered Using a High-Throughput Yeast Growth Restoration Assay,PLOS One,2013年02月01日,8 (2),e55271 |
| J. L. Nieva et al.,Viroporins: structure and biological functions,Nature Reviews Microbiology,2012年08月,10,563-574 |
| J. Wilkinson et al.,A Phase 1b/2a study of the safety, pharmacokinetics and antiviral activity of BIT225 in patients with HIV-1 infection,J. of Antimicrobial Chemotherapy,2016年,71,731-738 |
| P. H. Jalily et al.,Mechanisms of Action of Novel Influenza A/M2 Viroporin Inhibitors Derived from Hexamethylene Amiloride,Molecular Pharmacology,2016年08月,90 (2),80-95 |
Also Published As
| Publication number | Publication date |
|---|---|
| RU2019126746A3 (ja) | 2021-05-28 |
| KR20190112051A (ko) | 2019-10-02 |
| EP3579833A4 (en) | 2021-01-13 |
| MX2019009443A (es) | 2019-12-16 |
| JP2020506243A (ja) | 2020-02-27 |
| EP3579833A1 (en) | 2019-12-18 |
| AU2018218179A1 (en) | 2019-08-22 |
| RU2769317C2 (ru) | 2022-03-30 |
| ES2910136T3 (es) | 2022-05-11 |
| BR112019016316A2 (pt) | 2020-03-31 |
| EP3579833B1 (en) | 2022-01-05 |
| CN110325187B (zh) | 2022-09-30 |
| US10918623B2 (en) | 2021-02-16 |
| MX387115B (es) | 2025-03-19 |
| CA3052503A1 (en) | 2018-08-16 |
| US20200093796A1 (en) | 2020-03-26 |
| WO2018145148A1 (en) | 2018-08-16 |
| CN110325187A (zh) | 2019-10-11 |
| SG11201907034PA (en) | 2019-08-27 |
| AU2018218179B2 (en) | 2023-05-04 |
| KR102607599B1 (ko) | 2023-11-28 |
| RU2019126746A (ru) | 2021-03-09 |
| NZ755900A (en) | 2025-03-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7019727B2 (ja) | インフルエンザの治療方法 | |
| WO2020241759A1 (ja) | インフルエンザウイルス感染症またはコロナウイルス感染症の予防および/または治療剤 | |
| US11433080B2 (en) | Antiviral treatment | |
| US10221152B2 (en) | Usage of mycophenolate mofetil or salt thereof in preparing drug for resisting against influenza virus | |
| CN118574614A (zh) | 治疗sars-cov-2感染的方法 | |
| CA3052503C (en) | Methods of treating influenza | |
| US20230225988A1 (en) | Antiviral use of calixarenes | |
| HK40017310A (en) | Methods of treating influenza | |
| HK40017310B (en) | Methods of treating influenza | |
| CN114377009A (zh) | Sb216763在制备抗流感病毒药物中的应用 | |
| RU2842052C1 (ru) | Азеластин в качестве противовирусного лечения | |
| CN102526086A (zh) | 女贞苷的提取方法及其制备药物用途 | |
| WO2019089734A1 (en) | Methods and compositions for the treatment of influenza | |
| TWI530284B (zh) | 馬替麥考酚酯或其鹽類用於製備抗流感病毒之藥物的用途 | |
| CN115414370A (zh) | 牛磺胆酸钠在制备治疗或预防流感病毒感染的药物中的应用 | |
| HK40087524A (zh) | 氮卓斯汀用作抗病毒治疗 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210201 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210201 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20211117 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220104 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220202 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7019727 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |