JP6920694B2 - ヒトパピローマウイルスタイプ11のl1タンパク質の突然変異 - Google Patents
ヒトパピローマウイルスタイプ11のl1タンパク質の突然変異 Download PDFInfo
- Publication number
- JP6920694B2 JP6920694B2 JP2018548264A JP2018548264A JP6920694B2 JP 6920694 B2 JP6920694 B2 JP 6920694B2 JP 2018548264 A JP2018548264 A JP 2018548264A JP 2018548264 A JP2018548264 A JP 2018548264A JP 6920694 B2 JP6920694 B2 JP 6920694B2
- Authority
- JP
- Japan
- Prior art keywords
- protein
- hpv11
- mutant
- amino acid
- vlp
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 102000004169 proteins and genes Human genes 0.000 title claims description 135
- 108090000623 proteins and genes Proteins 0.000 title claims description 135
- 230000035772 mutation Effects 0.000 title claims description 5
- 241000701828 Human papillomavirus type 11 Species 0.000 title description 130
- 125000000539 amino acid group Chemical group 0.000 claims description 56
- 239000002245 particle Substances 0.000 claims description 41
- 108700025391 Human papillomavirus type 6 L1 Proteins 0.000 claims description 28
- 208000009608 Papillomavirus Infections Diseases 0.000 claims description 25
- 208000015181 infectious disease Diseases 0.000 claims description 25
- 150000001413 amino acids Chemical class 0.000 claims description 24
- 238000006467 substitution reaction Methods 0.000 claims description 23
- 229960005486 vaccine Drugs 0.000 claims description 23
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 22
- 238000000034 method Methods 0.000 claims description 22
- 241000588724 Escherichia coli Species 0.000 claims description 19
- 201000010099 disease Diseases 0.000 claims description 17
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 17
- 239000013598 vector Substances 0.000 claims description 13
- 239000000203 mixture Substances 0.000 claims description 12
- 108020004707 nucleic acids Proteins 0.000 claims description 12
- 102000039446 nucleic acids Human genes 0.000 claims description 12
- 150000007523 nucleic acids Chemical class 0.000 claims description 12
- 206010008342 Cervix carcinoma Diseases 0.000 claims description 11
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 claims description 11
- 201000010881 cervical cancer Diseases 0.000 claims description 11
- 206010059313 Anogenital warts Diseases 0.000 claims description 10
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 9
- 239000008194 pharmaceutical composition Substances 0.000 claims description 9
- 208000022361 Human papillomavirus infectious disease Diseases 0.000 claims description 7
- 238000003776 cleavage reaction Methods 0.000 claims description 6
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 6
- 230000007017 scission Effects 0.000 claims description 6
- 239000003937 drug carrier Substances 0.000 claims description 5
- 239000003814 drug Substances 0.000 claims 1
- 235000018102 proteins Nutrition 0.000 description 110
- 241000701806 Human papillomavirus Species 0.000 description 74
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 34
- 230000003472 neutralizing effect Effects 0.000 description 28
- 235000001014 amino acid Nutrition 0.000 description 26
- 229940024606 amino acid Drugs 0.000 description 25
- 241000699670 Mus sp. Species 0.000 description 24
- 239000012634 fragment Substances 0.000 description 22
- 238000004519 manufacturing process Methods 0.000 description 21
- 239000002671 adjuvant Substances 0.000 description 20
- 210000004027 cell Anatomy 0.000 description 18
- 239000011780 sodium chloride Substances 0.000 description 17
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 16
- 229910052782 aluminium Inorganic materials 0.000 description 16
- 230000001681 protective effect Effects 0.000 description 15
- 239000013612 plasmid Substances 0.000 description 14
- 108010021466 Mutant Proteins Proteins 0.000 description 12
- 102000008300 Mutant Proteins Human genes 0.000 description 12
- 239000000872 buffer Substances 0.000 description 12
- 238000004587 chromatography analysis Methods 0.000 description 11
- 238000002255 vaccination Methods 0.000 description 10
- 238000011156 evaluation Methods 0.000 description 9
- 210000002966 serum Anatomy 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 241000894006 Bacteria Species 0.000 description 8
- 239000006228 supernatant Substances 0.000 description 8
- 241000282567 Macaca fascicularis Species 0.000 description 7
- 239000013604 expression vector Substances 0.000 description 7
- 239000002609 medium Substances 0.000 description 7
- 229960002566 papillomavirus vaccine Drugs 0.000 description 7
- 238000004062 sedimentation Methods 0.000 description 7
- 230000001580 bacterial effect Effects 0.000 description 6
- 238000004925 denaturation Methods 0.000 description 6
- 230000036425 denaturation Effects 0.000 description 6
- 241000282693 Cercopithecidae Species 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 230000001939 inductive effect Effects 0.000 description 5
- 229930027917 kanamycin Natural products 0.000 description 5
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 5
- 229960000318 kanamycin Drugs 0.000 description 5
- 229930182823 kanamycin A Natural products 0.000 description 5
- 229920001184 polypeptide Polymers 0.000 description 5
- 102000004196 processed proteins & peptides Human genes 0.000 description 5
- 108090000765 processed proteins & peptides Proteins 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 230000000694 effects Effects 0.000 description 4
- 230000006870 function Effects 0.000 description 4
- 238000004191 hydrophobic interaction chromatography Methods 0.000 description 4
- 230000007124 immune defense Effects 0.000 description 4
- 239000006166 lysate Substances 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 239000002773 nucleotide Substances 0.000 description 4
- 125000003729 nucleotide group Chemical group 0.000 description 4
- 239000008363 phosphate buffer Substances 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 101001065501 Escherichia phage MS2 Lysis protein Proteins 0.000 description 3
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 3
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 108091028043 Nucleic acid sequence Proteins 0.000 description 3
- 238000012408 PCR amplification Methods 0.000 description 3
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 3
- 241000700605 Viruses Species 0.000 description 3
- 238000000137 annealing Methods 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000005540 biological transmission Effects 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 238000001493 electron microscopy Methods 0.000 description 3
- 238000001962 electrophoresis Methods 0.000 description 3
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 3
- 229960000310 isoleucine Drugs 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000012139 lysis buffer Substances 0.000 description 3
- 239000002808 molecular sieve Substances 0.000 description 3
- 230000000877 morphologic effect Effects 0.000 description 3
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical compound [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 description 3
- 108091033319 polynucleotide Proteins 0.000 description 3
- 102000040430 polynucleotide Human genes 0.000 description 3
- 239000002157 polynucleotide Substances 0.000 description 3
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 3
- 239000012064 sodium phosphate buffer Substances 0.000 description 3
- 239000004474 valine Substances 0.000 description 3
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 2
- 108090000565 Capsid Proteins Proteins 0.000 description 2
- 102100023321 Ceruloplasmin Human genes 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- 229940124897 Gardasil Drugs 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- HNDVDQJCIGZPNO-YFKPBYRVSA-N L-histidine Chemical compound OC(=O)[C@@H](N)CC1=CN=CN1 HNDVDQJCIGZPNO-YFKPBYRVSA-N 0.000 description 2
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 2
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 2
- AYFVYJQAPQTCCC-GBXIJSLDSA-N L-threonine Chemical compound C[C@@H](O)[C@H](N)C(O)=O AYFVYJQAPQTCCC-GBXIJSLDSA-N 0.000 description 2
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 2
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 2
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 2
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 2
- 239000004472 Lysine Substances 0.000 description 2
- 101710135729 Major capsid protein L1 Proteins 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 2
- 229920002684 Sepharose Polymers 0.000 description 2
- 108091081024 Start codon Proteins 0.000 description 2
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 2
- 239000004473 Threonine Substances 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 2
- 238000007792 addition Methods 0.000 description 2
- 235000004279 alanine Nutrition 0.000 description 2
- 230000003321 amplification Effects 0.000 description 2
- 230000008827 biological function Effects 0.000 description 2
- 239000001110 calcium chloride Substances 0.000 description 2
- 229910001628 calcium chloride Inorganic materials 0.000 description 2
- 238000005277 cation exchange chromatography Methods 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 238000011097 chromatography purification Methods 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 238000012217 deletion Methods 0.000 description 2
- 230000037430 deletion Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000001914 filtration Methods 0.000 description 2
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 239000007928 intraperitoneal injection Substances 0.000 description 2
- 239000011159 matrix material Substances 0.000 description 2
- 125000001360 methionine group Chemical group N[C@@H](CCSC)C(=O)* 0.000 description 2
- 238000002703 mutagenesis Methods 0.000 description 2
- 231100000350 mutagenesis Toxicity 0.000 description 2
- 238000003199 nucleic acid amplification method Methods 0.000 description 2
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 2
- 108091008146 restriction endonucleases Proteins 0.000 description 2
- 238000012163 sequencing technique Methods 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000012536 storage buffer Substances 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 2
- MTCFGRXMJLQNBG-REOHCLBHSA-N (2S)-2-Amino-3-hydroxypropansäure Chemical compound OC[C@H](N)C(O)=O MTCFGRXMJLQNBG-REOHCLBHSA-N 0.000 description 1
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 241000340969 Alphapapillomavirus 10 Species 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 241001057184 Axion Species 0.000 description 1
- 239000012617 Butyl Sepharose™ 4 Fast Flow Substances 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- 229940124957 Cervarix Drugs 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 102000012410 DNA Ligases Human genes 0.000 description 1
- 108010061982 DNA Ligases Proteins 0.000 description 1
- 238000007400 DNA extraction Methods 0.000 description 1
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 1
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 1
- 108060002716 Exonuclease Proteins 0.000 description 1
- 208000031969 Eye Hemorrhage Diseases 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- XUJNEKJLAYXESH-REOHCLBHSA-N L-Cysteine Chemical compound SC[C@H](N)C(O)=O XUJNEKJLAYXESH-REOHCLBHSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 239000007993 MOPS buffer Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102000016943 Muramidase Human genes 0.000 description 1
- 108010014251 Muramidase Proteins 0.000 description 1
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 239000001888 Peptone Substances 0.000 description 1
- 108010080698 Peptones Proteins 0.000 description 1
- 231100000645 Reed–Muench method Toxicity 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 101150100563 VLP4 gene Proteins 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 230000036952 cancer formation Effects 0.000 description 1
- 210000000234 capsid Anatomy 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 238000005341 cation exchange Methods 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000012501 chromatography medium Substances 0.000 description 1
- 238000010367 cloning Methods 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- NKLPQNGYXWVELD-UHFFFAOYSA-M coomassie brilliant blue Chemical compound [Na+].C1=CC(OCC)=CC=C1NC1=CC=C(C(=C2C=CC(C=C2)=[N+](CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=2C=CC(=CC=2)N(CC)CC=2C=C(C=CC=2)S([O-])(=O)=O)C=C1 NKLPQNGYXWVELD-UHFFFAOYSA-M 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 235000018417 cysteine Nutrition 0.000 description 1
- 238000000502 dialysis Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 210000003527 eukaryotic cell Anatomy 0.000 description 1
- 238000002270 exclusion chromatography Methods 0.000 description 1
- 102000013165 exonuclease Human genes 0.000 description 1
- 238000001125 extrusion Methods 0.000 description 1
- 210000004392 genitalia Anatomy 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 230000008696 hypoxemic pulmonary vasoconstriction Effects 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000003053 immunization Effects 0.000 description 1
- 238000002649 immunization Methods 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 238000010324 immunological assay Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000002198 insoluble material Substances 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 1
- 229960000274 lysozyme Drugs 0.000 description 1
- 235000010335 lysozyme Nutrition 0.000 description 1
- 239000004325 lysozyme Substances 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000010369 molecular cloning Methods 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000003002 pH adjusting agent Substances 0.000 description 1
- 235000019319 peptone Nutrition 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- IYDGMDWEHDFVQI-UHFFFAOYSA-N phosphoric acid;trioxotungsten Chemical compound O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.O=[W](=O)=O.OP(O)(O)=O IYDGMDWEHDFVQI-UHFFFAOYSA-N 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000004262 preparative liquid chromatography Methods 0.000 description 1
- 210000001236 prokaryotic cell Anatomy 0.000 description 1
- 238000010298 pulverizing process Methods 0.000 description 1
- 239000012557 regeneration buffer Substances 0.000 description 1
- 238000001338 self-assembly Methods 0.000 description 1
- 238000002741 site-directed mutagenesis Methods 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 210000005253 yeast cell Anatomy 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
- C07K14/01—DNA viruses
- C07K14/025—Papovaviridae, e.g. papillomavirus, polyomavirus, SV40, BK virus, JC virus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P21/00—Preparation of peptides or proteins
- C12P21/02—Preparation of peptides or proteins having a known sequence of two or more amino acids, e.g. glutathione
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5258—Virus-like particles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55505—Inorganic adjuvants
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/20011—Papillomaviridae
- C12N2710/20022—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/20011—Papillomaviridae
- C12N2710/20023—Virus like particles [VLP]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/20011—Papillomaviridae
- C12N2710/20034—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/20011—Papillomaviridae
- C12N2710/20041—Use of virus, viral particle or viral elements as a vector
- C12N2710/20043—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/20011—Papillomaviridae
- C12N2710/20071—Demonstrated in vivo effect
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Virology (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Genetics & Genomics (AREA)
- Microbiology (AREA)
- Gastroenterology & Hepatology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Immunology (AREA)
- Mycology (AREA)
- Epidemiology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- General Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Description
本発明は、少なくとも部分的には、本発明者らの驚くべき発見に基づいている:ヒトパピローマウイルス(HPV)タイプ11のL1タンパク質の特定のセグメントを第2のHPVタイプ(HPV6など)のL1タンパク質の対応するセグメントで置換した後、このようにして得られた突然変異型HPV11 L1タンパク質は、生物におけるHPV11及び第2のHPV型(例えばHPV6)に対する高力価中和抗体の生成を誘導することができ、その保護効果は、HPV11 VLP及び第2のHPVタイプのVLPの混合物のものに匹敵し、HPV11に対するその保護効果は、HPV11 VLP単独のものに匹敵し、第2のHPVタイプ(HPV6など)に対するその保護効果は、第2のHPVタイプ単独のVLPのものに匹敵する。
(1)3〜6アミノ酸、例えば3、4、5又は6アミノ酸のN末端切断;及び
(2)(a)第2のタイプの野生型HPVのL1タンパク質の対応する位置のアミノ酸残基による、野生型HPV11 L1タンパク質の170〜179位のアミノ酸残基の置換;又は
(b)第2のタイプの野生型HPVのL1タンパク質の対応する位置のアミノ酸残基による、野生型のHPV11 L1タンパク質の346〜351位のアミノ酸残基の置換;又は
(c)第2のタイプの野生型HPVのL1タンパク質の対応する位置のアミノ酸残基による、野生型HPV11 L1タンパク質の119〜140位のアミノ酸残基の置換;
ならびに、改変体は、1つ又は複数(例えば、1、2、3、4、5、6、7、8又は9個)のアミノ酸の置換(好ましくは保存的置換)、付加又は欠失のみによる突然変異型HPV11 L1タンパク質とは異なるが、突然変異型HPV11 L1タンパク質の機能、すなわち少なくとも2つのHPVタイプ(例えば、HPV11及びHPV6)に対する中和抗体の生成を誘導する能力を保持する。
本発明において、他に特定しない限り、本明細書で使用される科学用語及び技術用語は、当業者によって一般に理解される意味を有する。さらに、本明細書で使用される細胞培養、分子遺伝学、核酸化学及び免疫学の実験室操作は、対応する分野で広く使用されているルーチン操作である。一方、本発明をよりよく理解するために、関連用語の定義及び説明は以下のように提供される。
研究は、HPV11と他のHPVタイプ(HPV6など)との間に一定の交差防御があるが、そのような交差防御は非常に低く、一般的に、同HPVタイプのVLPの保護レベルの1%より低く、さらには1000分の1、さらには1000分の1であることを示す。したがって、HPV11ワクチンでワクチン接種された対象は、他のHPVタイプ(HPV6など)に感染するリスクがなおも高い。
本発明に関与する配列のいくつかを以下の表1に提供する。
MWRPSDSTVYVPPPNPVSKVVATDAYVKRTNIFYHASSSRLLAVGHPYYSIKKVNKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPLLNKYDDVENSGGYGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGTQCSNTSVQNGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPLDICGTVCKYPDYLQMAADPYGDRLFFYLRKEQMFARHFFNRAGTVGEPVPDDLLVKGGNNRSSVASSIYVHTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNHLFVTVVDTTRSTNMTLCASVSKSATYTNSDYKEYMRHVEEFDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKQDPYKDMSFWEVNLKEKFSSELDQFPLGRKFLLQSGYRGRTSARTGIKRPAVSKPSTAPKRKRTKTKK
MWRPSDSTVYVPPPNPVSKVVATDAYVTRTNIFYHASSSRLLAVGHPYFSIKRANKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPFLNKYDDVENSGSGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGKQCTNTPVQAGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPIDICGTTCKYPDYLQMAADPYGDRLFFFLRKEQMFARHFFNRAGEVGEPVPDTLIIKGSGNRTSVGSSIYVNTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNQLFVTVVDTTRSTNMTLCASVTTSSTYTNSDYKEYMRHVEEYDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKPDPYKNLSFWEVNLKEKFSSELDQYPLGRKFLLQSGYRGRSSIRTGVKRPAVSKASAAPKRKRAKTKR
MSDSTVYVPPPNPVSKVVATDAYVKRTNIFYHASSSRLLAVGHPYYSIKKVNKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPLLNKYDDVENSGGYGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGTQCSNTSVQNGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPLDICGTVCKYPDYLQMAADPYGDRLFFYLRKEQMFARHFFNRAGTVGEPVPDDLLVKGGNNRSSVASSIYVHTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNHLFVTVVDTTRSTNMTLCASVSKSATYTNSDYKEYMRHVEEFDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKQDPYKDMSFWEVNLKEKFSSELDQFPLGRKFLLQSGYRGRTSARTGIKRPAVSKPSTAPKRKRTKTKK
MDSTVYVPPPNPVSKVVATDAYVTRTNIFYHASSSRLLAVGHPYFSIKRANKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPFLNKYDDVENSGSGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGKQCTNTPVQAGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPIDICGTTCKYPDYLQMAADPYGDRLFFFLRKEQMFARHFFNRAGEVGEPVPDTLIIKGSGNRTSVGSSIYVNTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNQLFVTVVDTTRSTNMTLCASVTTSSTYTNSDYKEYMRHVEEYDLQFIFQLCSITLSAEVVAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKQKPDPYKNLSFWEVNLKEKFSSELDQYPLGRKFLLQSGYRGRSSIRTGVKRPAVSKASAAPKRKRAKTKR
MSDSTVYVPPPNPVSKVVATDAYVKRTNIFYHASSSRLLAVGHPYFSIKRANKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPLLNKYDDVENSGGYGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGTQCSNTSVQNGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPLDICGTVCKYPDYLQMAADPYGDRLFFYLRKEQMFARHFFNRAGTVGEPVPDDLLVKGGNNRSSVASSIYVHTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNHLFVTVVDTTRSTNMTLCASVSKSATYTNSDYKEYMRHVEEFDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKQDPYKDMSFWEVNLKEKFSSELDQFPLGRKFLLQSGYRGRTSARTGIKRPAVSKPSTAPKRKRTKTKK
MSDSTVYVPPPNPVSKVVATDAYVKRTNIFYHASSSRLLAVGHPYYSIKKVNKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPFLNKYDDVENSGSGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGTQCSNTSVQNGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPLDICGTVCKYPDYLQMAADPYGDRLFFYLRKEQMFARHFFNRAGTVGEPVPDDLLVKGGNNRSSVASSIYVHTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNHLFVTVVDTTRSTNMTLCASVSKSATYTNSDYKEYMRHVEEFDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKQDPYKDMSFWEVNLKEKFSSELDQFPLGRKFLLQSGYRGRTSARTGIKRPAVSKPSTAPKRKRTKTKK
Sequence 7 (SEQ ID NO: 7):
MSDSTVYVPPPNPVSKVVATDAYVKRTNIFYHASSSRLLAVGHPYYSIKKVNKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPLLNKYDDVENSGGYGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGKQCTNTPVQAGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPLDICGTVCKYPDYLQMAADPYGDRLFFYLRKEQMFARHFFNRAGTVGEPVPDDLLVKGGNNRSSVASSIYVHTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNHLFVTVVDTTRSTNMTLCASVSKSATYTNSDYKEYMRHVEEFDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKQDPYKDMSFWEVNLKEKFSSELDQFPLGRKFLLQSGYRGRTSARTGIKRPAVSKPSTAPKRKRTKTKK
MSDSTVYVPPPNPVSKVVATDAYVKRTNIFYHASSSRLLAVGHPYYSIKKVNKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPLLNKYDDVENSGGYGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGTQCSNTSVQNGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPLDICGTVCKYPDYLQMAADPYGDRLFFYLRKEQMFARHFFNRAGEVGEPVPDTLIIKGSGNRTSVGSSIYVHTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNHLFVTVVDTTRSTNMTLCASVSKSATYTNSDYKEYMRHVEEFDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKQDPYKDMSFWEVNLKEKFSSELDQFPLGRKFLLQSGYRGRTSARTGIKRPAVSKPSTAPKRKRTKTKK
MSDSTVYVPPPNPVSKVVATDAYVKRTNIFYHASSSRLLAVGHPYYSIKKVNKTVVPKVSGYQYRVFKVVLPDPNKFALPDSSLFDPTTQRLVWACTGLEVGRGQPLGVGVSGHPLLNKYDDVENSGGYGGNPGQDNRVNVGMDYKQTQLCMVGCAPPLGEHWGKGTQCSNTSVQNGDCPPLELITSVIQDGDMVDTGFGAMNFADLQTNKSDVPLDICGTVCKYPDYLQMAADPYGDRLFFYLRKEQMFARHFFNRAGTVGEPVPDDLLVKGGNNRSSVASSIYVHTPSGSLVSSEAQLFNKPYWLQKAQGHNNGICWGNHLFVTVVDTTRSTNMTLCASVTTSSTYTNSDYKEYMRHVEEFDLQFIFQLCSITLSAEVMAYIHTMNPSVLEDWNFGLSPPPNGTLEDTYRYVQSQAITCQKPTPEKEKQDPYKDMSFWEVNLKEKFSSELDQFPLGRKFLLQSGYRGRTSARTGIKRPAVSKPSTAPKRKRTKTKK
ATGAGCGACAGCACAGTATATGTGCCTCCTCCCAACCCTGTATCCAAGGTTGTTGCCACGGATGCGTATGTTAAACGCACCAACATATTTTATCACGCCAGCAGTTCTAGACTCCTTGCTGTGGGACATCCATATTACTCTATCAAAAAAGTTAACAAAACAGTTGTACCAAAGGTGTCTGGATATCAATATAGAGTGTTTAAGGTAGTGTTGCCAGATCCTAACAAGTTTGCATTACCTGATTCATCTCTGTTTGACCCCACTACACAGCGTTTAGTATGGGCGTGCACAGGGTTGGAGGTAGGCAGGGGTCAACCTTTAGGCGTTGGTGTTAGTGGGCATCCATTGCTAAACAAATATGATGATGTAGAAAATAGTGGTGGGTATGGTGGTAATCCTGGTCAGGATAATAGGGTTAATGTAGGTATGGATTATAAACAAACCCAGCTATGTATGGTGGGCTGTGCTCCACCGTTAGGTGAACATTGGGGTAAGGGTACACAATGTTCAAATACCTCTGTACAAAATGGTGACTGCCCCCCGTTGGAACTTATTACCAGTGTTATACAGGATGGGGACATGGTTGATACAGGCTTTGGTGCTATGAATTTTGCAGACTTACAAACCAATAAATCGGATGTTCCCCTTGATATTTGTGGAACTGTCTGCAAATATCCTGATTATTTGCAAATGGCAGCAGACCCTTATGGTGATAGGTTGTTTTTTTATTTGCGAAAGGAACAAATGTTTGCTAGACACTTTTTTAATAGGGCCGGTACTGTGGGGGAACCTGTGCCTGATGACCTGTTGGTAAAAGGGGGTAATAATAGGTCATCTGTAGCTAGTAGTATTTATGTACATACACCTAGTGGATCCTTGGTGTCTTCAGAGGCTCAATTATTTAATAAACCATATTGGCTTCAAAAGGCTCAGGGACATAACAATGGTATTTGCTGGGGAAACCACTTGTTTGTTACTGTGGTAGATACCACACGCAGTACAAATATGACACTATGTGCATCTGTGTCTAAATCTGCTACATACACTAATTCAGATTATAAGGAATATATGCGCCATGTGGAGGAGTTTGATTTACAGTTTATTTTTCAATTGTGTAGCATTACATTATCTGCAGAAGTCATGGCCTATATACACACAATGAATCCTTCTGTTTTGGAGGACTGGAACTTTGGTTTATCGCCTCCACCAAATGGTACACTGGAGGATACTTATAGATATGTACAGTCACAGGCCATTACCTGTCAGAAACCCACACCCGAAAAAGAAAAACAGGACCCCTATAAGGATATGAGTTTTTGGGAGGTTAACTTAAAAGAAAAGTTTTCTTCTGAATTAGATCAGTTTCCCCTTGGACGTAAGTTTTTATTGCAAAGTGGATATCGAGGACGGACGTCTGCTCGTACAGGTATAAAGCGCCCAGCTGTGTCTAAGCCCTCTACAGCCCCCAAACGAAAACGTACCAAAACCAAAAAGTAA
ATGGACAGCACAGTATATGTGCCTCCTCCTAACCCTGTATCCAAAGTTGTTGCCACGGATGCTTATGTTACTCGCACCAACATATTTTATCATGCCAGCAGTTCTAGACTTCTTGCAGTGGGTCATCCTTATTTTTCCATAAAACGGGCTAACAAAACTGTTGTGCCAAAGGTGTCAGGATATCAATACAGGGTATTTAAGGTGGTGTTACCAGATCCTAACAAATTTGCATTGCCTGACTCGTCTCTTTTTGATCCCACAACACAACGTTTGGTATGGGCATGCACAGGCCTAGAGGTGGGCAGGGGACAGCCATTAGGTGTGGGTGTAAGTGGACATCCTTTCCTAAATAAATATGATGATGTTGAAAATTCAGGGAGTGGTGGTAACCCTGGACAGGATAACAGGGTTAATGTTGGTATGGATTATAAACAAACACAATTATGCATGGTTGGATGTGCCCCCCCTTTGGGCGAGCATTGGGGTAAAGGTAAACAGTGTACTAATACACCTGTACAGGCTGGTGACTGCCCGCCCTTAGAACTTATTACCAGTGTTATACAGGATGGCGATATGGTTGACACAGGCTTTGGTGCTATGAATTTTGCTGATTTGCAGACCAATAAATCAGATGTTCCTATTGATATATGTGGCACTACATGTAAATATCCAGATTATTTACAAATGGCTGCAGACCCTTATGGTGATAGATTATTTTTTTTTCTACGGAAGGAACAAATGTTTGCCAGACATTTTTTTAACAGGGCTGGCGAGGTGGGGGAACCTGTGCCTGATACTCTTATAATTAAGGGTAGTGGAAATCGAACGTCTGTAGGGAGTAGTATATATGTTAACACCCCAAGCGGCTCTTTGGTGTCCTCTGAGGCACAATTGTTTAATAAGCCATATTGGCTACAAAAAGCCCAGGGACATAACAATGGTATTTGTTGGGGTAATCAACTGTTTGTTACTGTGGTAGATACCACACGCAGTACCAACATGACATTATGTGCATCCGTAACTACATCTTCCACATACACCAATTCTGATTATAAAGAGTACATGCGTCATGTGGAAGAGTATGATTTACAATTTATTTTTCAATTATGTAGCATTACATTGTCTGCTGAAGTAGTGGCCTATATTCACACAATGAATCCCTCTGTTTTGGAAGACTGGAACTTTGGGTTATCGCCTCCCCCAAATGGTACATTAGAAGATACCTATAGGTATGTGCAGTCACAGGCCATTACCTGTCAAAAGCCCACTCCTGAAAAGCAAAAGCCAGATCCCTATAAGAACCTTAGTTTTTGGGAGGTTAATTTAAAAGAAAAGTTTTCTAGTGAATTGGATCAGTATCCTTTGGGACGCAAGTTTTTGTTACAAAGTGGATATAGGGGACGGTCCTCTATTCGTACCGGTGTTAAGCGCCCTGCTGTTTCCAAAGCCTCTGCTGCCCCTAAACGTAAGCGCGCCAAAACTAAAAGGTAA
ATGAGCGACAGCACAGTATATGTGCCTCCTCCCAACCCTGTATCCAAGGTTGTTGCCACGGATGCGTATGTTAAACGCACCAACATATTTTATCACGCCAGCAGTTCTAGACTCCTTGCTGTGGGACATCCATATTTTTCCATAAAACGGGCTAACAAAACTGTTGTGCCAAAGGTGTCAGGATATCAATATAGAGTGTTTAAGGTAGTGTTGCCAGATCCTAACAAGTTTGCATTACCTGATTCATCTCTGTTTGACCCCACTACACAGCGTTTAGTATGGGCGTGCACAGGGTTGGAGGTAGGCAGGGGTCAACCTTTAGGCGTTGGTGTTAGTGGGCATCCATTGCTAAACAAATATGATGATGTAGAAAATAGTGGTGGGTATGGTGGTAATCCTGGTCAGGATAATAGGGTTAATGTAGGTATGGATTATAAACAAACCCAGCTATGTATGGTGGGCTGTGCTCCACCGTTAGGTGAACATTGGGGTAAGGGTACACAATGTTCAAATACCTCTGTACAAAATGGTGACTGCCCCCCGTTGGAACTTATTACCAGTGTTATACAGGATGGGGACATGGTTGATACAGGCTTTGGTGCTATGAATTTTGCAGACTTACAAACCAATAAATCGGATGTTCCCCTTGATATTTGTGGAACTGTCTGCAAATATCCTGATTATTTGCAAATGGCAGCAGACCCTTATGGTGATAGGTTGTTTTTTTATTTGCGAAAGGAACAAATGTTTGCTAGACACTTTTTTAATAGGGCCGGTACTGTGGGGGAACCTGTGCCTGATGACCTGTTGGTAAAAGGGGGTAATAATAGGTCATCTGTAGCTAGTAGTATTTATGTACATACACCTAGTGGATCCTTGGTGTCTTCAGAGGCTCAATTATTTAATAAACCATATTGGCTTCAAAAGGCTCAGGGACATAACAATGGTATTTGCTGGGGAAACCACTTGTTTGTTACTGTGGTAGATACCACACGCAGTACAAATATGACACTATGTGCATCTGTGTCTAAATCTGCTACATACACTAATTCAGATTATAAGGAATATATGCGCCATGTGGAGGAGTTTGATTTACAGTTTATTTTTCAATTGTGTAGCATTACATTATCTGCAGAAGTCATGGCCTATATACACACAATGAATCCTTCTGTTTTGGAGGACTGGAACTTTGGTTTATCGCCTCCACCAAATGGTACACTGGAGGATACTTATAGATATGTACAGTCACAGGCCATTACCTGTCAGAAACCCACACCCGAAAAAGAAAAACAGGACCCCTATAAGGATATGAGTTTTTGGGAGGTTAACTTAAAAGAAAAGTTTTCTTCTGAATTAGATCAGTTTCCCCTTGGACGTAAGTTTTTATTGCAAAGTGGATATCGAGGACGGACGTCTGCTCGTACAGGTATAAAGCGCCCAGCTGTGTCTAAGCCCTCTACAGCCCCCAAACGAAAACGTACCAAAACCAAAAAGTAA
ATGAGCGACAGCACAGTATATGTGCCTCCTCCCAACCCTGTATCCAAGGTTGTTGCCACGGATGCGTATGTTAAACGCACCAACATATTTTATCACGCCAGCAGTTCTAGACTCCTTGCTGTGGGACATCCATATTACTCTATCAAAAAAGTTAACAAAACAGTTGTACCAAAGGTGTCTGGATATCAATATAGAGTGTTTAAGGTAGTGTTGCCAGATCCTAACAAGTTTGCATTACCTGATTCATCTCTGTTTGACCCCACTACACAGCGTTTAGTATGGGCGTGCACAGGGTTGGAGGTAGGCAGGGGACAGCCATTAGGTGTGGGTGTAAGTGGACATCCTTTCCTAAATAAATATGATGATGTTGAAAATTCAGGGAGTGGTGGTAACCCTGGACAGGATAACAGGGTTAATGTTGGTATGGATTATAAACAAACCCAGCTATGTATGGTGGGCTGTGCTCCACCGTTAGGTGAACATTGGGGTAAGGGTACACAATGTTCAAATACCTCTGTACAAAATGGTGACTGCCCCCCGTTGGAACTTATTACCAGTGTTATACAGGATGGGGACATGGTTGATACAGGCTTTGGTGCTATGAATTTTGCAGACTTACAAACCAATAAATCGGATGTTCCCCTTGATATTTGTGGAACTGTCTGCAAATATCCTGATTATTTGCAAATGGCAGCAGACCCTTATGGTGATAGGTTGTTTTTTTATTTGCGAAAGGAACAAATGTTTGCTAGACACTTTTTTAATAGGGCCGGTACTGTGGGGGAACCTGTGCCTGATGACCTGTTGGTAAAAGGGGGTAATAATAGGTCATCTGTAGCTAGTAGTATTTATGTACATACACCTAGTGGATCCTTGGTGTCTTCAGAGGCTCAATTATTTAATAAACCATATTGGCTTCAAAAGGCTCAGGGACATAACAATGGTATTTGCTGGGGAAACCACTTGTTTGTTACTGTGGTAGATACCACACGCAGTACAAATATGACACTATGTGCATCTGTGTCTAAATCTGCTACATACACTAATTCAGATTATAAGGAATATATGCGCCATGTGGAGGAGTTTGATTTACAGTTTATTTTTCAATTGTGTAGCATTACATTATCTGCAGAAGTCATGGCCTATATACACACAATGAATCCTTCTGTTTTGGAGGACTGGAACTTTGGTTTATCGCCTCCACCAAATGGTACACTGGAGGATACTTATAGATATGTACAGTCACAGGCCATTACCTGTCAGAAACCCACACCCGAAAAAGAAAAACAGGACCCCTATAAGGATATGAGTTTTTGGGAGGTTAACTTAAAAGAAAAGTTTTCTTCTGAATTAGATCAGTTTCCCCTTGGACGTAAGTTTTTATTGCAAAGTGGATATCGAGGACGGACGTCTGCTCGTACAGGTATAAAGCGCCCAGCTGTGTCTAAGCCCTCTACAGCCCCCAAACGAAAACGTACCAAAACCAAAAAGTAA
ATGAGCGACAGCACAGTATATGTGCCTCCTCCCAACCCTGTATCCAAGGTTGTTGCCACGGATGCGTATGTTAAACGCACCAACATATTTTATCACGCCAGCAGTTCTAGACTCCTTGCTGTGGGACATCCATATTACTCTATCAAAAAAGTTAACAAAACAGTTGTACCAAAGGTGTCTGGATATCAATATAGAGTGTTTAAGGTAGTGTTGCCAGATCCTAACAAGTTTGCATTACCTGATTCATCTCTGTTTGACCCCACTACACAGCGTTTAGTATGGGCGTGCACAGGGTTGGAGGTAGGCAGGGGTCAACCTTTAGGCGTTGGTGTTAGTGGGCATCCATTGCTAAACAAATATGATGATGTAGAAAATAGTGGTGGGTATGGTGGTAATCCTGGTCAGGATAATAGGGTTAATGTAGGTATGGATTATAAACAAACCCAGCTATGTATGGTGGGCTGTGCTCCACCGTTAGGTGAACATTGGGGTAAAGGTAAACAGTGTACTAATACACCTGTACAGGCTGGTGACTGCCCGCCCTTGGAACTTATTACCAGTGTTATACAGGATGGGGACATGGTTGATACAGGCTTTGGTGCTATGAATTTTGCAGACTTACAAACCAATAAATCGGATGTTCCCCTTGATATTTGTGGAACTGTCTGCAAATATCCTGATTATTTGCAAATGGCAGCAGACCCTTATGGTGATAGGTTGTTTTTTTATTTGCGAAAGGAACAAATGTTTGCTAGACACTTTTTTAATAGGGCCGGTACTGTGGGGGAACCTGTGCCTGATGACCTGTTGGTAAAAGGGGGTAATAATAGGTCATCTGTAGCTAGTAGTATTTATGTACATACACCTAGTGGATCCTTGGTGTCTTCAGAGGCTCAATTATTTAATAAACCATATTGGCTTCAAAAGGCTCAGGGACATAACAATGGTATTTGCTGGGGAAACCACTTGTTTGTTACTGTGGTAGATACCACACGCAGTACAAATATGACACTATGTGCATCTGTGTCTAAATCTGCTACATACACTAATTCAGATTATAAGGAATATATGCGCCATGTGGAGGAGTTTGATTTACAGTTTATTTTTCAATTGTGTAGCATTACATTATCTGCAGAAGTCATGGCCTATATACACACAATGAATCCTTCTGTTTTGGAGGACTGGAACTTTGGTTTATCGCCTCCACCAAATGGTACACTGGAGGATACTTATAGATATGTACAGTCACAGGCCATTACCTGTCAGAAACCCACACCCGAAAAAGAAAAACAGGACCCCTATAAGGATATGAGTTTTTGGGAGGTTAACTTAAAAGAAAAGTTTTCTTCTGAATTAGATCAGTTTCCCCTTGGACGTAAGTTTTTATTGCAAAGTGGATATCGAGGACGGACGTCTGCTCGTACAGGTATAAAGCGCCCAGCTGTGTCTAAGCCCTCTACAGCCCCCAAACGAAAACGTACCAAAACCAAAAAGTAA
ATGAGCGACAGCACAGTATATGTGCCTCCTCCCAACCCTGTATCCAAGGTTGTTGCCACGGATGCGTATGTTAAACGCACCAACATATTTTATCACGCCAGCAGTTCTAGACTCCTTGCTGTGGGACATCCATATTACTCTATCAAAAAAGTTAACAAAACAGTTGTACCAAAGGTGTCTGGATATCAATATAGAGTGTTTAAGGTAGTGTTGCCAGATCCTAACAAGTTTGCATTACCTGATTCATCTCTGTTTGACCCCACTACACAGCGTTTAGTATGGGCGTGCACAGGGTTGGAGGTAGGCAGGGGTCAACCTTTAGGCGTTGGTGTTAGTGGGCATCCATTGCTAAACAAATATGATGATGTAGAAAATAGTGGTGGGTATGGTGGTAATCCTGGTCAGGATAATAGGGTTAATGTAGGTATGGATTATAAACAAACCCAGCTATGTATGGTGGGCTGTGCTCCACCGTTAGGTGAACATTGGGGTAAGGGTACACAATGTTCAAATACCTCTGTACAAAATGGTGACTGCCCCCCGTTGGAACTTATTACCAGTGTTATACAGGATGGGGACATGGTTGATACAGGCTTTGGTGCTATGAATTTTGCAGACTTACAAACCAATAAATCGGATGTTCCCCTTGATATTTGTGGAACTGTCTGCAAATATCCTGATTATTTGCAAATGGCAGCAGACCCTTATGGTGATAGGTTGTTTTTTTATTTGCGAAAGGAACAAATGTTTGCTAGACACTTTTTTAACAGGGCTGGCGAGGTGGGGGAACCTGTGCCTGATACTCTTATAATTAAGGGTAGTGGAAATCGAACGTCTGTAGGGAGTAGTATATATGTACATACACCTAGTGGATCCTTGGTGTCTTCAGAGGCTCAATTATTTAATAAACCATATTGGCTTCAAAAGGCTCAGGGACATAACAATGGTATTTGCTGGGGAAACCACTTGTTTGTTACTGTGGTAGATACCACACGCAGTACAAATATGACACTATGTGCATCTGTGTCTAAATCTGCTACATACACTAATTCAGATTATAAGGAATATATGCGCCATGTGGAGGAGTTTGATTTACAGTTTATTTTTCAATTGTGTAGCATTACATTATCTGCAGAAGTCATGGCCTATATACACACAATGAATCCTTCTGTTTTGGAGGACTGGAACTTTGGTTTATCGCCTCCACCAAATGGTACACTGGAGGATACTTATAGATATGTACAGTCACAGGCCATTACCTGTCAGAAACCCACACCCGAAAAAGAAAAACAGGACCCCTATAAGGATATGAGTTTTTGGGAGGTTAACTTAAAAGAAAAGTTTTCTTCTGAATTAGATCAGTTTCCCCTTGGACGTAAGTTTTTATTGCAAAGTGGATATCGAGGACGGACGTCTGCTCGTACAGGTATAAAGCGCCCAGCTGTGTCTAAGCCCTCTACAGCCCCCAAACGAAAACGTACCAAAACCAAAAAGTAA
ATGAGCGACAGCACAGTATATGTGCCTCCTCCCAACCCTGTATCCAAGGTTGTTGCCACGGATGCGTATGTTAAACGCACCAACATATTTTATCACGCCAGCAGTTCTAGACTCCTTGCTGTGGGACATCCATATTACTCTATCAAAAAAGTTAACAAAACAGTTGTACCAAAGGTGTCTGGATATCAATATAGAGTGTTTAAGGTAGTGTTGCCAGATCCTAACAAGTTTGCATTACCTGATTCATCTCTGTTTGACCCCACTACACAGCGTTTAGTATGGGCGTGCACAGGGTTGGAGGTAGGCAGGGGTCAACCTTTAGGCGTTGGTGTTAGTGGGCATCCATTGCTAAACAAATATGATGATGTAGAAAATAGTGGTGGGTATGGTGGTAATCCTGGTCAGGATAATAGGGTTAATGTAGGTATGGATTATAAACAAACCCAGCTATGTATGGTGGGCTGTGCTCCACCGTTAGGTGAACATTGGGGTAAGGGTACACAATGTTCAAATACCTCTGTACAAAATGGTGACTGCCCCCCGTTGGAACTTATTACCAGTGTTATACAGGATGGGGACATGGTTGATACAGGCTTTGGTGCTATGAATTTTGCAGACTTACAAACCAATAAATCGGATGTTCCCCTTGATATTTGTGGAACTGTCTGCAAATATCCTGATTATTTGCAAATGGCAGCAGACCCTTATGGTGATAGGTTGTTTTTTTATTTGCGAAAGGAACAAATGTTTGCTAGACACTTTTTTAATAGGGCCGGTACTGTGGGGGAACCTGTGCCTGATGACCTGTTGGTAAAAGGGGGTAATAATAGGTCATCTGTAGCTAGTAGTATTTATGTACATACACCTAGTGGATCCTTGGTGTCTTCAGAGGCTCAATTATTTAATAAACCATATTGGCTTCAAAAGGCTCAGGGACATAACAATGGTATTTGCTGGGGAAACCACTTGTTTGTTACTGTGGTAGATACCACACGCAGTACAAATATGACACTATGTGCATCTGTAACTACATCTTCCACATACACCAATTCTGATTATAAGGAATATATGCGCCATGTGGAGGAGTTTGATTTACAGTTTATTTTTCAATTGTGTAGCATTACATTATCTGCAGAAGTCATGGCCTATATACACACAATGAATCCTTCTGTTTTGGAGGACTGGAACTTTGGTTTATCGCCTCCACCAAATGGTACACTGGAGGATACTTATAGATATGTACAGTCACAGGCCATTACCTGTCAGAAACCCACACCCGAAAAAGAAAAACAGGACCCCTATAAGGATATGAGTTTTTGGGAGGTTAACTTAAAAGAAAAGTTTTCTTCTGAATTAGATCAGTTTCCCCTTGGACGTAAGTTTTTATTGCAAAGTGGATATCGAGGACGGACGTCTGCTCGTACAGGTATAAAGCGCCCAGCTGTGTCTAAGCCCTCTACAGCCCCCAAACGAAAACGTACCAAAACCAAAAAGTAA
KQCTNTPVQA
TTSSTY
FLNKYDDVENSGSGGNPGQDN
本発明は、以下の実施例を参照してさらに説明されるが、これらの実施例は、本発明を限定するのではなく、本発明を説明する目的でのみ使用される。
発現ベクターの構築
HPV6 L1タンパク質由来の特定のセグメントを含む突然変異型HPV11 L1タンパク質(H11N4−6T1)をコードする発現ベクターは、マルチサイト突然変異誘発のためのPCRによって構築した。使用した初期鋳型は、プラスミドpTO−T7−HPV11N4C(N末端で切断された4アミノ酸を有するHPV11 L1タンパク質をコードする;表2に11L1N4と略記する)であった。各PCRの鋳型及びプライマーを表2に示し、PCRの増幅条件を以下のようにした:94℃で10分間の変性;25サイクル(94℃で50秒間の変性、一定温度で一定時間のアニーリング、72℃で7.5分間の伸長);最後に72℃で10分間伸長する。使用したPCRプライマーの配列を表3に列挙した。
組換えプラスミドpTO−T7−H11N4−6T1、pTO−T7−H11N4−6T2、pTO−T7−H11N4−6T3、pTO−T7−H11N4−6T4、及びpTO−T7−H11N4−6T5をそれぞれ含む大腸菌を−70℃の冷蔵庫から取り出し、カナマイシンを含有する100mLのLB液体培地に播種し、200rpm及び37℃で約8時間インキュベートした。次に、培養物をカナマイシンを含む500mLのLB培地に移し(1mlの細菌溶液を移した)、さらにインキュベートした。細菌の濃度が約0.6のOD600に達したとき、培養温度を25℃に下げ、各培養ボトルに500μLのIPTGを添加した。インキュベーションをさらに8時間行った。インキュベーションが終了した後、細菌を遠心分離によって回収した。H11N4−6T1、H11N4−6T2、H11N4−6T3、H11N4−6T4及びH11N4−6T5タンパク質を発現する細菌をそれぞれ得た。
得られた細菌は、1gの細菌1g/10mLの溶解緩衝液(20mM Tris緩衝液、pH7.2、300mM NaCl)の比で再懸濁された。細菌は、超音波装置を用いて30分間破砕された。破砕された細菌を含む溶解溶液を13500rpm(30000g)で15分間遠心分離し、上清(すなわち、破砕された細菌の上清)を得た。
装置:GE Healthcare(すなわち、元のAmershan Pharmacia Co.)によって製造されたAKTA Explorer 100分取液体クロマトグラフィーシステム
クロマトグラフィー媒体:SP Sepharose 4 Fast Flow(GE Healthcare Co.)、CHT−II(Bio−RADから購入)及びButyl Sepharose 4 Fast Flow(GE Healthcare Co.)
緩衝液:20mMリン酸緩衝液、pH8.0、20mM DTT;20mMリン酸緩衝液、pH8.0、20mM DTT、2M NaCl
試料:上記で得られたそれぞれH11N4−6T1、H11N4−6T2、H11N4−6T3、H11N4−6T4及びH11N4−6T5を含む破砕された細菌の上清。
(1)SP Sepharose 4 Fast Flowによる破砕した細菌の上清の陽イオン交換精製:試料をカラムに装填し、次に、400mM NaClを含む緩衝液で不要なタンパク質を溶出し、続いて、800mM NaClを含む緩衝液で目的のタンパク質を溶出した。800mM NaClを含む緩衝液で溶出された画分を回収した;
(2)CHT−II(ハイドロキシアパタイトクロマトグラフィー)による、工程(1)で得られた溶出画分のクロマトグラフィーによる精製:工程(1)で得られた溶出画分は、NaCl濃度が0.5Mになるように希釈されるように希釈され;試料をカラムに装填し、500mMのNaClを含む緩衝液で溶出した後、1000mMのNaClを含む緩衝液で目的のタンパク質を溶出し、1000mMのNaClを含む緩衝液で溶出した画分を回収した;
(3)HIC(疎水性相互作用クロマトグラフィー)による、工程(2)で得られた溶出画分の精製:試料をカラムに装填し、次に、不要なタンパク質を1000mM NaClを含む緩衝液で溶出した後、200mMのNaClを含む緩衝液で目的のタンパク質を溶出し、200mMのNaClを含む緩衝液で溶出された画分を回収した。
HPBウイルス様粒子のアセンブリ
所定体積(約2ml)のタンパク質H11N4−6T1、H11N4−6T2、H11N4−6T3、H11N4−6T4又はH11N4−6T5は、(1)2L保存緩衝液(20mMリン酸ナトリウム緩衝液pH6.5、0.5M NaCl);(2)2L再生緩衝液(50mMリン酸ナトリウム緩衝液pH6.0、2mM CaCl2、2mM MgCl2、0.5M NaCl);及び(3)20mMリン酸ナトリウム緩衝液pH7.0、0.5M NaClに対して連続的に透析した。透析は3つの緩衝液のそれぞれで12時間行った。
透析した試料を、1120コンパクトLC高速液体クロマトグラフィーシステム(Agilent Technologies)によるモレキュラーシーブクロマトグラフィー分析に供し、分析カラムは、TSK Gel PW5000xl 7.8x300mmであった。分析結果を図2A〜2Fに示した。結果は、タンパク質H11N4−6T1、H11N4−6T2、H11N4−6T3、H11N4−6T4及びH11N4−6T5をそれぞれ含む試料の最初のタンパク質ピークは約12分で現れたことを、これはHPV11N4 VLPのそれに匹敵することを示した。これは、上記で調製したタンパク質がVLPにアセンブルすることができたことを示した。
沈降速度分析のための装置は、光学検査システム及びAn−50Ti及びAn−60Tiローターを備えたBeckman XL−A Analytical Ultracentrifugeであった。HPV11N4 VLP、H11N4−6T1 VLP、H11N4−6T2 VLP、H11N4−6T3 VLP、H11N4−6T4 VLP及びH11N4−6T5 VLPの沈降係数を沈降速度法により分析した。結果を図3A〜3Fに示した。結果は、H11N4−6T1 VLP、H11N4−6T2 VLP、H11N4−6T3 VLP、H11N4−6T4 VLP及びH11N4−6T5 VLPの沈降係数はそれぞれ140S、138S、111S、139S及び139Sであることを示した。これは、5つの突然変異型HPV11 L1タンパク質が、サイズ及び形態に関して野生型VLP(HPV11N4 VLP、136.3S)に類似したウイルス様粒子にアセンブルすることができることを示した。
VLPを含む試料100μLを透過型電子顕微鏡(TEM)で観察した。使用した装置は、JEOL Ltd.によって供給された100kV透過電子顕微鏡(倍率100,000倍)であった。要するに、13.5μLの試料を2%リンタングステン酸(pH7.0)で陰性に染色し、炭素被覆した銅グリッドに固定し、次いでTEMで観察した。結果を図4A〜4Fに示した。結果は、H11N4−6T1、H11N4−6T2、H11N4−6T3、H11N4−6T4及びH11N4−6T5がウイルス様粒子にアセンブルし得ることを示した。さらに、これらの結果はまた、これらの突然変異型タンパク質によってアセンブルした粒子が約25nmの半径を有し、サイズが均一であることを示した。これは、これらの突然変異型タンパク質がHPV11 L1タンパク質(HPV11N4 VLP)に類似しており、均一なサイズのVLPにアセンブルすることができたことを示した。
HPV11N4、H11N4−6T1、H11N4−6T2、H11N4−6T3、H11N4−6T4及びH11N4−6T5により形成されたVLPは、GE Company(すなわち、もともとはMicroCal Co.)から購入した示差走査熱量計VPキャピラリーDSCを用いてそれらの熱安定性について評価した。タンパク質の保存緩衝液を対照として使用し、タンパク質を10℃〜90℃の温度範囲内で1.5℃/分の加熱速度で走査した。検出結果を図5A〜5Fに示した。結果は、タンパク質によって形成されたこれらのVLPのすべてが非常に高い熱安定性を有することを示した。
以前に報告された方法(Wolf M, Garcea RL, Grigorieff N. et al. Proc Natl Acad Sci U S A. (2010), 107(14): 6298-303)に従って、H11N4−6T3 VLP及びH11N4−6T5 VLPの3次元構造は、低温電子顕微鏡法(cryoEM)を用いて再構築された。簡単に述べると、低温電子顕微鏡(cryoEM)を用いて、H11N4−6T3 VLP及びH11N4−6T5 VLPを観察し、次に、H11N4−6T3 VLP及びH11N4−6T5 VLPの低温電子顕微鏡(cryoEM)写真(図6A及び6C)では、コンピュータの重なり及び構造の再構成のために、均一なサイズ及び50nmより大きい直径を有する、それぞれ300個の粒子及び360個の粒子を選択し、H11N4−6T3 VLP及びH11N4−6T5 VLPの三次元構造を得た。得られた三次元構造を図6B及び6D(それぞれ17.38Å及び20.48Åの解像度にて)に示した。結果は、H11N4−6T3 VLP及びH11N4−6T5 VLPの両方が、72個のキャプソマー(形態学的サブユニット、ペンタマー)からなるT=7の二十面体構造(h=1、k=2)を有することを示した。準同値原理に一致する従来の二十面体ウイルスキャプシドとは異なり、H11N4−6T3 VLP及びH11N4−6T5 VLPの構造における構成的サブユニットはすべて、六量体を含まず、五量体であった。さらに、前記VLPは、約60nmの外径を有していた。これらは、以前報告された天然のHPVウイルス粒子及び真核生物発現系によって調製されたHPV VLP(例えば、ポックスウイルス発現系)の三次元構造と同様であった(Baker TS, Newcomb WW, Olson NH. et al. Biophys J. (1991), 60(6): 1445-1456. Hagensee ME, Olson NH, Baker TS, et al. J Virol. (1994), 68(7):4503-4505. Buck CB, Cheng N, Thompson CD. et al. J Virol. (2008), 82(11): 5190-7)。
H11N4−6T1、H11N4−6T2、H11N4−6T3、H11N4−6T4及びH11N4−6T5によって形成されたVLPの免疫防御をマウスで評価した。ワクチン接種のための動物は、5〜6週齢のBALB/cマウス(正常な等級)(Shanghai SLAC Laboratory Animal Co.LTDから購入)であった。
この実験において、ワクチン接種スケジュールを表5に示した。全てのマウス(6週齢のBalB/c雌性マウス)を3群に分けた:アルミニウムアジュバントグループ1(10μgの免疫化用量で、アルミニウムアジュバントを使用する)、アルミニウムアジュバントグループ2(1μgの免疫化用量で、アルミニウムアジュバントを使用する)、アルミニウムアジュバントグループ3(0.1μgの免疫化用量で、アルミニウムアジュバントを使用する)。各グループをさらに5つのサブグループに分けた。対照サブグループ1〜3は、それぞれHPV11N4 VLP単独、HPV6N5 VLP単独、及び混合したHPV11/HPV6 VLPでワクチン接種され、実験サブグループ1〜2は、H11N4−6T3 VLP及びH11N4−6T5 VLPでそれぞれワクチン接種された。
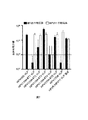
6週齢のBalB/c雌性マウス(8匹のマウス)に単回腹腔内注射によりアルミニウムアジュバントを接種した。実験群にH11N4−6T3 VLP又はH11N4−6T5 VLP(0.300μg、0.100μg、0.033μg又は0.011μgの免疫化用量で)を用いた。対照群にHPV6N5 VLP単独又はHPV11N4 VLP単独(0.300μg、0.100μg、0.033μg又は0.011μgの免疫化用量で)、又は混合したHPV11/HPV6 VLP(すなわち、HPV6N5 VLPとHPV11N4 VLPの混合物)、各VLPについて免疫化用量は0.300μg、0.100μg、0.033μg又は0.011μgであった)を用いた。免疫容量は1mLであった。さらに、ワクチンを希釈するための希釈剤をブランク対照として使用した。8匹のマススを各グループにおいてワクチン接種し、ワクチン接種から5週後に血清を回収した。その後、血清の中和抗体力価を中和化試験によって、及びReed−Muench法(Reed LJ MH. A simple method of estimating fifty percent endpoints. Am J Hyg. 1938; 27:493-7)によって決定し、セロコンバージョンを誘導する(すなわち、マウスにおける抗体の生成を誘導する)ためのED50を各試料について計算した。結果を表6.1〜6.5に示す。
同体重のカニクイザル18匹を無作為に3グループ(各グループあたり6匹のサル)に分け、グループ1のサルに5μgのH11N4−6T3 VLPをワクチン接種した。グループ2のサルに、5μgのH11N4−6T5 VLPをワクチン接種した;グループ3のサルに10μgの混合したHPV11/HPV6 VLP(5μgのHPV6N5 VLP+5μgのHPV11N4 VLP)をワクチン接種した。使用したアジュバントはアルミニウムアジュバントであり、注入量は1mlであり、サルは筋肉内注射によってワクチン接種された。ワクチン接種スケジュールを表7に示した。
Claims (17)
- 突然変異型HPV11 L1タンパク質であって、野生型HPV11 L1タンパク質と比較すると、突然変異型HPV11 L1タンパク質は、以下の突然変異を有する:
(1)3、4、5又は6アミノ酸のN末端切断;そして
(2)(a)野生型HPV6のL1タンパク質の対応する位置の全てのアミノ酸残基による、野生型HPV11 L1タンパク質の346〜351位のアミノ酸残基の置換;又は
(b)野生型HPV6のL1タンパク質の対応する位置の全てのアミノ酸残基による、野生型HPV11 L1タンパク質の119〜140位のアミノ酸残基の置換;
を有する、上記突然変異型HPV11 L1タンパク質。 - (2)(a)に記載の対応する位置のアミノ酸残基が、野生型HPV6 L1タンパク質の345〜350位のアミノ酸残基であり;及び/又は、(2)(a)に記載の対応する位置のアミノ酸残基が、野生型HPV6 L1タンパク質の119〜139位のアミノ酸残基である、請求項1に記載の突然変異型HPV11 L1タンパク質。
- 野生型HPV11 L1タンパク質が、配列番号1に記載のアミノ酸配列を有し;及び/又は、野生型HPV6 L1タンパク質が、配列番号2に示されるアミノ酸配列を有する、請求項1又は2に記載の突然変異型HPV11 L1タンパク質。
- 突然変異型HPV11 L1タンパク質が、配列番号6及び9からなる群から選択されるアミノ酸配列を有する、請求項1〜3のいずれか1項に記載の突然変異型HPV11 L1タンパク質。
- 請求項1〜4のいずれか1項に記載の突然変異型HPV11 L1タンパク質をコードする単離された核酸。
- 請求項5に記載の単離された核酸を含むベクター。
- 請求項5に記載の単離された核酸及び/又は請求項6に記載のベクターを含む宿主細胞。
- 請求項1〜4のいずれか1項に記載の突然変異型HPV11 L1タンパク質を含む又はそれからなるHPVウイルス様粒子。
- 請求項1〜4のいずれか1項に記載の突然変異型HPV11 L1タンパク質、又は請求項5に記載の単離された核酸、又は請求項6に記載のベクター、又は請求項7に記載の宿主細胞、又は請求項8に記載のHPVウイルス様粒子を含む組成物。
- 請求項8に記載のHPVウイルス様粒子、及び場合により医薬として許容される担体及び/又は賦形剤を含む医薬組成物又はワクチン。
- HPVウイルス様粒子が、HPV感染又はHPV感染によって引き起こされる疾患の予防に有効な量で存在する、請求項10に記載の医薬組成物又はワクチン。
- HPV感染が、HPV11感染及び/又はHPV6感染であり;及び/又は、HPV感染によって引き起こされる疾患が、子宮頸癌及び尖圭コンジロームからなる群から選択される、請求項10又は11に記載の医薬組成物又はワクチン。
- 請求項1〜4のいずれか1項に記載の突然変異型HPV11 L1タンパク質を調製する方法であって、該方法は、突然変異型HPV11 L1タンパク質を宿主細胞で発現させ、次に、突然変異型HPV11 L1タンパク質を宿主細胞の培養物から回収することを含む、上記方法。
- 宿主細胞が大腸菌である、請求項13に記載の方法。
- 請求項8に記載のHPVウイルス様粒子を医薬として許容される担体及び/又は賦形剤と組み合わせることを含む、ワクチンを調製する方法。
- HPV感染又はHPV感染によって引き起こされる疾患に使用するための、請求項1〜4のいずれか1項に記載の突然変異型HPV11 L1タンパク質、又は請求項8に記載のHPVウイルス様粒子。
- HPV感染が、HPV11感染及び/又はHPV6感染であり;及び/又は、HPV感染によって引き起こされる疾患が、子宮頸癌及び尖圭コンジロームからなる群から選択される、請求項16に記載の突然変異型HPV11 L1タンパク質。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201510887801 | 2015-12-04 | ||
| CN201510887801.9 | 2015-12-04 | ||
| PCT/CN2016/108349 WO2017092711A1 (zh) | 2015-12-04 | 2016-12-02 | 一种人乳头瘤病毒11型l1蛋白的突变体 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2019502404A JP2019502404A (ja) | 2019-01-31 |
| JP2019502404A5 JP2019502404A5 (ja) | 2019-08-08 |
| JP6920694B2 true JP6920694B2 (ja) | 2021-08-18 |
Family
ID=58796324
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018548264A Active JP6920694B2 (ja) | 2015-12-04 | 2016-12-02 | ヒトパピローマウイルスタイプ11のl1タンパク質の突然変異 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US10513541B2 (ja) |
| EP (1) | EP3385274B1 (ja) |
| JP (1) | JP6920694B2 (ja) |
| KR (1) | KR20180084139A (ja) |
| CN (1) | CN106831958B (ja) |
| BR (1) | BR112018011331A2 (ja) |
| WO (1) | WO2017092711A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN114127095B (zh) * | 2019-07-19 | 2024-04-09 | 神州细胞工程有限公司 | 嵌合的人乳头瘤病毒11型l1蛋白 |
| CN114127099B (zh) * | 2019-07-19 | 2024-04-19 | 神州细胞工程有限公司 | 嵌合的人乳头瘤病毒6型l1蛋白 |
| BR112022022719A2 (pt) * | 2020-05-14 | 2023-02-14 | Inovio Pharmaceuticals Inc | Vacinas para papilomatose respiratória recorrente e métodos de usar a mesma |
| CN114539363B (zh) * | 2020-11-26 | 2023-12-01 | 中国医学科学院基础医学研究所 | 一种c端改造的人乳头瘤病毒11型l1蛋白及其用途 |
| KR20230126566A (ko) | 2022-02-23 | 2023-08-30 | 충남대학교산학협력단 | 핵수송 신호 펩타이드가 접합된 핵산 전달용 2세대 폴리아미도아민 덴드리머 고분자 유도체 |
| CN116041445B (zh) * | 2023-01-06 | 2023-09-05 | 北京康乐卫士生物技术股份有限公司 | 一种人乳头瘤病毒51型l1蛋白突变体及减少重组蛋白降解的方法及应用 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL117591A0 (en) * | 1995-03-30 | 1996-07-23 | Merck & Co Inc | Synthetic DNA encoding human papillomavirus type 11 L1 protein |
| US5795754A (en) * | 1995-07-19 | 1998-08-18 | Merck & Co., Inc. | Synthetic HPV11 virus-like particles |
| EP0863982B1 (en) * | 1995-11-15 | 2004-01-21 | Merck & Co., Inc. | Synthetic hpv11 virus-like particles |
| US5738853A (en) * | 1995-11-15 | 1998-04-14 | Merck & Co., Inc. | Synthetic HPV11 virus-like particles |
| AUPP765398A0 (en) * | 1998-12-11 | 1999-01-14 | University Of Queensland, The | Treatment of papillomavirus infections |
| US6689366B1 (en) * | 1998-12-17 | 2004-02-10 | Merck & Co., Inc. | Synthetic virus like particles with heterologous epitopes |
| US8748127B2 (en) * | 2007-05-29 | 2014-06-10 | Xiamen University | Truncated L1 protein of human papillomavirus type 6 |
| EP2910566B1 (en) * | 2007-05-29 | 2016-07-13 | Xiamen University | A truncated L1 protein of human papillomavirus 11 |
| CN101518647A (zh) * | 2008-02-29 | 2009-09-02 | 江阴艾托金生物技术有限公司 | 人乳头瘤病毒预防性疫苗、构建方法及应用 |
| CN104911154A (zh) * | 2008-08-08 | 2015-09-16 | 武田疫苗股份有限公司 | 交叉反应性增强的包含复合衣壳氨基酸序列的病毒样颗粒 |
| CN102229660B (zh) * | 2011-05-25 | 2015-04-22 | 厦门大学 | 截短的人乳头瘤病毒33型l1蛋白 |
| CN102747047B (zh) * | 2012-02-28 | 2016-03-23 | 厦门大学 | 人乳头瘤病毒型别杂合病毒样颗粒及其制备方法 |
| CN104211782B (zh) * | 2013-06-04 | 2017-11-17 | 厦门大学 | 截短的人乳头瘤病毒45型l1蛋白 |
-
2016
- 2016-12-02 BR BR112018011331-0A patent/BR112018011331A2/pt active Search and Examination
- 2016-12-02 WO PCT/CN2016/108349 patent/WO2017092711A1/zh active Application Filing
- 2016-12-02 CN CN201611095116.3A patent/CN106831958B/zh active Active
- 2016-12-02 KR KR1020187018923A patent/KR20180084139A/ko not_active Application Discontinuation
- 2016-12-02 JP JP2018548264A patent/JP6920694B2/ja active Active
- 2016-12-02 EP EP16870021.9A patent/EP3385274B1/en active Active
- 2016-12-02 US US15/781,328 patent/US10513541B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3385274A4 (en) | 2019-08-14 |
| EP3385274B1 (en) | 2021-09-22 |
| JP2019502404A (ja) | 2019-01-31 |
| BR112018011331A2 (pt) | 2019-04-30 |
| CN106831958A (zh) | 2017-06-13 |
| CN106831958B (zh) | 2020-12-29 |
| EP3385274A1 (en) | 2018-10-10 |
| US10513541B2 (en) | 2019-12-24 |
| KR20180084139A (ko) | 2018-07-24 |
| US20190062379A1 (en) | 2019-02-28 |
| WO2017092711A1 (zh) | 2017-06-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6958818B2 (ja) | ヒトパピローマウイルスタイプ58のl1タンパク質の突然変異 | |
| JP6920694B2 (ja) | ヒトパピローマウイルスタイプ11のl1タンパク質の突然変異 | |
| US11427618B2 (en) | Mutant of L1 protein of human papillomavirus type 39 | |
| JP7290258B2 (ja) | ヒトパピローマウイルス51型のl1タンパク質の変異型 | |
| US11213580B2 (en) | Mutant of L1 protein of human papillomavirus type 16 | |
| JP7265563B2 (ja) | ヒトパピローマウイルス18型のl1タンパク質の変異体 | |
| US11464846B2 (en) | Mutant of L1 protein of human papillomavirus type 66 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190701 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190701 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200424 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200602 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200901 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210209 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210405 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210629 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210714 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6920694 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |