JP6906542B2 - 試料の特性評価のためのデバイス及び方法 - Google Patents
試料の特性評価のためのデバイス及び方法 Download PDFInfo
- Publication number
- JP6906542B2 JP6906542B2 JP2018547858A JP2018547858A JP6906542B2 JP 6906542 B2 JP6906542 B2 JP 6906542B2 JP 2018547858 A JP2018547858 A JP 2018547858A JP 2018547858 A JP2018547858 A JP 2018547858A JP 6906542 B2 JP6906542 B2 JP 6906542B2
- Authority
- JP
- Japan
- Prior art keywords
- channel
- sample
- separation channel
- separation
- enriched
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502715—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by interfacing components, e.g. fluidic, electrical, optical or mechanical interfaces
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502761—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip specially adapted for handling suspended solids or molecules independently from the bulk fluid flow, e.g. for trapping or sorting beads, for physically stretching molecules
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
- G01N27/447—Systems using electrophoresis
- G01N27/44704—Details; Accessories
- G01N27/44717—Arrangements for investigating the separated zones, e.g. localising zones
- G01N27/44721—Arrangements for investigating the separated zones, e.g. localising zones by optical means
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
- G01N27/447—Systems using electrophoresis
- G01N27/44756—Apparatus specially adapted therefor
- G01N27/44773—Multi-stage electrophoresis, e.g. two-dimensional electrophoresis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
- G01N27/447—Systems using electrophoresis
- G01N27/44756—Apparatus specially adapted therefor
- G01N27/44791—Microapparatus
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N27/00—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means
- G01N27/26—Investigating or analysing materials by the use of electric, electrochemical, or magnetic means by investigating electrochemical variables; by using electrolysis or electrophoresis
- G01N27/416—Systems
- G01N27/447—Systems using electrophoresis
- G01N27/44756—Apparatus specially adapted therefor
- G01N27/44795—Isoelectric focusing
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/60—Construction of the column
- G01N30/6095—Micromachined or nanomachined, e.g. micro- or nanosize
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N30/00—Investigating or analysing materials by separation into components using adsorption, absorption or similar phenomena or using ion-exchange, e.g. chromatography or field flow fractionation
- G01N30/02—Column chromatography
- G01N30/62—Detectors specially adapted therefor
- G01N30/72—Mass spectrometers
- G01N30/7233—Mass spectrometers interfaced to liquid or supercritical fluid chromatograph
- G01N30/724—Nebulising, aerosol formation or ionisation
- G01N30/7266—Nebulising, aerosol formation or ionisation by electric field, e.g. electrospray
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J49/00—Particle spectrometers or separator tubes
- H01J49/02—Details
- H01J49/04—Arrangements for introducing or extracting samples to be analysed, e.g. vacuum locks; Arrangements for external adjustment of electron- or ion-optical components
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J49/00—Particle spectrometers or separator tubes
- H01J49/02—Details
- H01J49/04—Arrangements for introducing or extracting samples to be analysed, e.g. vacuum locks; Arrangements for external adjustment of electron- or ion-optical components
- H01J49/0431—Arrangements for introducing or extracting samples to be analysed, e.g. vacuum locks; Arrangements for external adjustment of electron- or ion-optical components for liquid samples
- H01J49/0445—Arrangements for introducing or extracting samples to be analysed, e.g. vacuum locks; Arrangements for external adjustment of electron- or ion-optical components for liquid samples with means for introducing as a spray, a jet or an aerosol
- H01J49/045—Arrangements for introducing or extracting samples to be analysed, e.g. vacuum locks; Arrangements for external adjustment of electron- or ion-optical components for liquid samples with means for introducing as a spray, a jet or an aerosol with means for using a nebulising gas, i.e. pneumatically assisted
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01J—ELECTRIC DISCHARGE TUBES OR DISCHARGE LAMPS
- H01J49/00—Particle spectrometers or separator tubes
- H01J49/02—Details
- H01J49/10—Ion sources; Ion guns
- H01J49/16—Ion sources; Ion guns using surface ionisation, e.g. field-, thermionic- or photo-emission
- H01J49/165—Electrospray ionisation
- H01J49/167—Capillaries and nozzles specially adapted therefor
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/06—Fluid handling related problems
- B01L2200/0647—Handling flowable solids, e.g. microscopic beads, cells, particles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/14—Process control and prevention of errors
- B01L2200/143—Quality control, feedback systems
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/16—Reagents, handling or storing thereof
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0627—Sensor or part of a sensor is integrated
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0627—Sensor or part of a sensor is integrated
- B01L2300/0645—Electrodes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/06—Auxiliary integrated devices, integrated components
- B01L2300/0627—Sensor or part of a sensor is integrated
- B01L2300/0654—Lenses; Optical fibres
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0816—Cards, e.g. flat sample carriers usually with flow in two horizontal directions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
- B01L2300/0877—Flow chambers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0403—Moving fluids with specific forces or mechanical means specific forces
- B01L2400/0415—Moving fluids with specific forces or mechanical means specific forces electrical forces, e.g. electrokinetic
- B01L2400/0421—Moving fluids with specific forces or mechanical means specific forces electrical forces, e.g. electrokinetic electrophoretic flow
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/02—Burettes; Pipettes
- B01L3/0241—Drop counters; Drop formers
- B01L3/0268—Drop counters; Drop formers using pulse dispensing or spraying, eg. inkjet type, piezo actuated ejection of droplets from capillaries
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2223/00—Investigating materials by wave or particle radiation
- G01N2223/40—Imaging
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2223/00—Investigating materials by wave or particle radiation
- G01N2223/50—Detectors
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2550/00—Electrophoretic profiling, e.g. for proteome analysis
Description
本出願は、それぞれ「Devices,Methods,and Kits for Sample Characterization」と題する、2015年11月30日に出願された米国仮特許出願第62/260,944号、及び2016年5月18日に出願された米国仮特許出願第62/338,074号の非仮出願であって、これらの利益を主張するものであり、これらの各々の開示は、その全体が参照として本明細書に組み込まれる。
(デバイス)
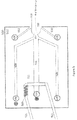
図1は、一実施形態による、自動的に装填された試料の2次元分離及びESIのためのデバイスの概略図である。マイクロ流体ネットワーク100は、基板102によって画定される。基板は、実施される富化ステップと適合する材料から製造される。例えば、材料の選択に関連して、化学的適合性、pH安定性、温度、光の様々な波長における透明性、機械的強度等が考慮される。
チャネル124は、クロマトグラフィ富化ステップ又は電気泳動富化ステップのいずれかを行うために使用することができる。
図6は、一実施形態による、検体混合物富化の方法を示す。この方法は、20において、検体混合物をマイクロ流体デバイスに装填及び/又は導入することを含む。マイクロ流体デバイスは、図1〜図3を参照して上述したマイクロ流体デバイスと同様であり得る。幾つかの実施形態において、検体混合物は、例えば、グリカン、炭水化物、DNA、RNA、インタクトタンパク質、消化されたタンパク質、ペプチド、代謝産物、ワクチン、ウイルス及び小分子であり得る。幾つかの実施形態では、検体混合物は、培養細胞の溶解物、体細胞由来の治療剤、又は腫瘍もしくは他の組織由来の細胞などのタンパク質の混合物、バイオ医薬品を含む組み換えタンパク質、血液由来細胞、灌流又は任意の他のソースからのタンパク質混合物であり得る検体混合物は、デバイスに直接装填することができ、又は複数の混合物の連続分析のためにオートサンプラに装填することができる。
実施形態の態様は、以下の実施例に照らして更に理解することができるが、これらは決して限定するものと解釈すべきではない。
この例では、図4に示すチャネルネットワークは、標準フォトリソグラフィーエッチング技術を用いて、ソーダ石灰ガラスのプレートから作製され、280nmの光に対する非常に低い透過率を有する。富化チャネル418の深さは、ガラス層402の厚みと同じであり、すなわち富化チャネル418は、このガラス板402の上部から底部まで全体を通過している。デバイス400は、デバイス400の一方の側に配置された光源によって照射され、デバイス400の反対側に配置された検出器によって画像化することができる。基板402は不透明であるが、富化チャネル418が光学スリットを画定するので、基板402は、富化チャネル418を通過しない光を遮断し、迷光を遮断し、画像化プロセスの分解能を向上させることができる。
実施例2は実施例1と同様であり得るが、図1を参照して説明する。チャネル116は、C18で誘導体化されたゾルゲルが充填された第1の富化ゾーンであり得る。タンパク質を装填した後、一定量の溶出液(IEF両性電解質及び標準を有するMeCN/H2O)がチャネル116の中に充填されて、ゾルゲルに捕捉された最も疎水性の低いタンパク質を溶出することができる。溶出液は、実施例1に記載したように、IEF、UV吸光度モニタリング及び最後にESIが行われる第2の富化ゾーンであり得るチャネル124に向けられる。第1の溶出液のESIがいったん完了すると、次に一定量のより高い濃度のMeCNが使用され、2番目に低い疎水性を有するタンパク質画分が溶出される。
実施例3は実施例2に類似であり得るが、生物学的薬物標的誘導体化ビーズをチャネル116の中に充填し、タンパク質を捕捉するために使用することができる。反応の親和性は、溶液相標的(競合的)、塩、pH等による溶出を通して特性評価される。
実施例4は実施例2と同様であり得るが、図5を参照して説明する。タンパク質混合物は、入口521を通って充填され移動し富化ゾーン510に至ることができ、タンパク質混合物は、逆相クロマトグラフィのためにC18で誘導体化されたビーズを含有することができる。装填の間、流体はゾーン510を通過し、視認領域511を通って出口522から出て廃棄物となる。視認領域510は、280nmのUV光に対して不透明なソーダ石灰ガラスでできている内部層を横断し、上部層及び底部層は280nmの光に対して透明な溶融シリカからできている。
噴霧窒素ガスラインは、ポート508及び528でデバイスに接続され、チャネル512及び530を通って移動し、エレクトロスプレーからの材料がオリフィス520を介してデバイスから出る際に、その材料に隣接(flank)する。
この例では、図7のレイアウトによって表されるマイクロ流体チャネル層は、環状オレフィンコポリマーから作製される。同様に述べると、マイクロ流体デバイス800の基板802はチャネルネットワークを画定する。多くの用途、例えば、蛍光検出が使用される用途では、この材料が検体を検出するために必要な波長範囲の光を透過するならば、単一の材料を用いてマイクロ流体デバイス800を製造することができる。
場合によっては、質量分析計インタフェースの有無によって異なるマイクロ流体層の2つの設計を有することが有利である。いったん検体の特性評価がなされると、確認の特性評価は質量分析データなしで行うことができる。確認の特性評価を、ほとんど同じ設計のマイクロ流体で行うことにより、異常が認識されたとき、質量同定のために質量分析計インタフェースを用いてアッセイをチップに戻すことが簡単になる。これにより、さもなければ、確認データの異常が質量分析データで分析されていることを示すために必要な作業を省略することができる。
Claims (14)
- (a)検体混合物を、分離チャネルを含むマイクロ流体デバイスに導入する段階と、
(b)前記分離チャネルの間に電界を印加して、等電点電気泳動により、前記検体混合物を富化された検体のフラクションに分離する段階と、
(c)前記検体混合物の分離、及び、この後の前記分離チャネルの内部における前記富化された検体のフラクションの移動を、前記マイクロ流体デバイスの透明な部分を介して、画像化する段階と、
(d)分離された検体混合物にシース流体電解質を導入して、前記富化された検体のフラクションの実質的にすべてを、移動させ、前記分離チャネルと直線状に並ぶ単一のオリフィスからエレクトロスプレーイオン化を介して質量分析計に排出する段階と、
(e)前記(c)における前記分離チャネルの画像化により検出された特定の富化された検体のフラクションに対する吸収ピークと、該特定の富化された検体のフラクションに対する質量分析計のデータと、を関連付ける段階と、
を含む、
ことを特徴とする方法。 - 前記マイクロ流体デバイスが、第1の分離チャネル及び第2の分離チャネルを含む、請求項1に記載の方法。
- 前記電界を印加して前記第2の分離チャネルにおいて等電点電気泳動による前記検体混合物の分離を実行する前に、前記第1の分離チャネルにおいて前記検体混合物をクロマトグラフィにより分離する段階、をさらに含む、請求項2に記載の方法。
- 前記富化された検体のフラクションの実質的にすべてが連続した流れとなって前記オリフィスから排出される、請求項1に記載の方法。
- 両性電解質及び等電点(pI)マーカを、前記分離チャネルに導入して該分離チャネルにおけるpH勾配を生成しかつ該分離チャネルにおけるpI範囲をマッピングする前に、前記検体混合物と混合する段階、をさらに含む、請求項1に記載の方法。
- 前記検体混合物がインタクトタンパク質を含む、請求項1に記載の方法。
- 前記シース流体電解質の導入は、前記分離チャネルの下流にある合流領域に流体結合された電解質チャネルから、シース流体電解質溶液を流すことにより、実行される、請求項1に記載の方法。
- イオンポテンシャルの補充が、前記シース流体電解質の導入によって前記マイクロ流体デバイスに生ずる、請求項1に記載の方法。
- 前記マイクロ流体デバイスが、前記分離チャネル、前記オリフィス及び前記シース流体電解質のチャネルを含む、請求項7に記載の方法。
- 前記分離チャネルと前記シース流体電解質のチャネルとが前記合流領域において交差する、請求項9に記載の方法。
- 前記合流領域が、前記分離チャネルに印加される前記電界の内部に含まれる、請求項10に記載の方法。
- 前記合流領域が、前記分離チャネル及び前記オリフィスと直線状に並ぶ、請求項10に記載の方法。
- 前記マイクロ流体デバイスが、シース流体電解質のチャネルに沿って電界を発生させる2つの電極を含む、請求項1に記載の方法。
- 前記マイクロ流体デバイスが、検体を導入するチャネルとイオン化のための噴霧ガス搬送チャネルとをさらに含む、請求項9に記載の方法。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021107723A JP7323576B2 (ja) | 2015-11-30 | 2021-06-29 | 試料の特性評価のためのデバイス及び方法 |
| JP2023122384A JP2023139239A (ja) | 2015-11-30 | 2023-07-27 | 試料の特性評価のためのデバイス及び方法 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562260944P | 2015-11-30 | 2015-11-30 | |
| US62/260,944 | 2015-11-30 | ||
| US201662338074P | 2016-05-18 | 2016-05-18 | |
| US62/338,074 | 2016-05-18 | ||
| PCT/US2016/064013 WO2017095813A1 (en) | 2015-11-30 | 2016-11-29 | Devices and methods for sample characterization |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021107723A Division JP7323576B2 (ja) | 2015-11-30 | 2021-06-29 | 試料の特性評価のためのデバイス及び方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2019503493A JP2019503493A (ja) | 2019-02-07 |
| JP2019503493A5 JP2019503493A5 (ja) | 2020-01-16 |
| JP6906542B2 true JP6906542B2 (ja) | 2021-07-21 |
Family
ID=58798061
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018547858A Active JP6906542B2 (ja) | 2015-11-30 | 2016-11-29 | 試料の特性評価のためのデバイス及び方法 |
| JP2021107723A Active JP7323576B2 (ja) | 2015-11-30 | 2021-06-29 | 試料の特性評価のためのデバイス及び方法 |
| JP2023122384A Pending JP2023139239A (ja) | 2015-11-30 | 2023-07-27 | 試料の特性評価のためのデバイス及び方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021107723A Active JP7323576B2 (ja) | 2015-11-30 | 2021-06-29 | 試料の特性評価のためのデバイス及び方法 |
| JP2023122384A Pending JP2023139239A (ja) | 2015-11-30 | 2023-07-27 | 試料の特性評価のためのデバイス及び方法 |
Country Status (10)
| Country | Link |
|---|---|
| US (6) | US20170176386A1 (ja) |
| EP (2) | EP3957986A1 (ja) |
| JP (3) | JP6906542B2 (ja) |
| KR (1) | KR20180101350A (ja) |
| CN (1) | CN108603828A (ja) |
| AU (2) | AU2016365121B2 (ja) |
| CA (1) | CA3006200A1 (ja) |
| DE (1) | DE202016008838U1 (ja) |
| DK (1) | DK3384274T3 (ja) |
| WO (1) | WO2017095813A1 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017095813A1 (en) | 2015-11-30 | 2017-06-08 | Intabio, Inc. | Devices and methods for sample characterization |
| JP6943860B2 (ja) * | 2015-12-31 | 2021-10-06 | ユニバーシティ・オブ・ノートル・ダム・デュ・ラック | 電気運動的にポンピングされる界面を介したesi−ms |
| CA3011620A1 (en) | 2016-02-01 | 2017-08-10 | Li-Cor, Inc. | Capillary electrophoresis inkjet dispensing |
| US10737268B2 (en) * | 2016-08-08 | 2020-08-11 | Li-Cor, Inc. | Multi-sheath flow and on-chip terminating electrode for microfluidic direct-blotting |
| CN109564188A (zh) * | 2016-08-08 | 2019-04-02 | 利康公司 | 微芯片电泳喷墨式分配 |
| SG11202007188RA (en) * | 2018-01-29 | 2020-08-28 | Intabio Inc | Devices, methods and kits for sample characterization |
| CN112534549A (zh) * | 2018-05-31 | 2021-03-19 | 因塔生物公司 | 用于微流体系统与质谱联用的软件 |
| US20210341422A1 (en) * | 2018-10-03 | 2021-11-04 | The Regents Of The University Of Michigan | Integrated micro-photoionization detector with an ultrathin ultraviolet transmission window |
| CA3125040A1 (en) * | 2019-01-25 | 2020-07-30 | Regeneron Pharmaceuticals, Inc. | Online chromatography and electrospray ionization mass spectrometer |
| US11285484B2 (en) | 2019-08-12 | 2022-03-29 | Intabio, Llc | Multichannel isoelectric focusing devices and high voltage power supplies |
| WO2021072262A1 (en) * | 2019-10-09 | 2021-04-15 | ProteinSimple | Method for single-channel free-flow electrophoresis with sequential ph adjustment |
| US20230010104A1 (en) * | 2019-11-25 | 2023-01-12 | Intabio, Llc | Software for microfluidic systems interfacing with mass spectrometry |
| GB202103194D0 (en) * | 2020-06-23 | 2021-04-21 | Micromass Ltd | Nebuliser outlet |
| CN113838738A (zh) * | 2021-09-14 | 2021-12-24 | 清华大学深圳国际研究生院 | 一种质谱联用多通道电喷雾微流控芯片离子源 |
Family Cites Families (107)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5395502A (en) | 1988-11-14 | 1995-03-07 | Anthony R. Torres | Apparatus for performing and universally detecting capillary isoelectric focusing without mobilization using concentration gradient imaging systems |
| DE69117875T2 (de) | 1990-11-08 | 1996-07-25 | Alcatel Fibres Optiques | Herstellungsverfahren von Multisteckerstiften mit einer Reihe von Kanälen mit parallelen Achsen und so hergestellter Multisteckerstift |
| US5110434A (en) | 1990-12-20 | 1992-05-05 | Bio-Rad Laboratories, Inc. | Use of zwitterions to mobilize isoelectrically focused ampholyte zones |
| US5259939A (en) | 1991-08-30 | 1993-11-09 | Beckman Instruments, Inc. | Capillary electrophoresis buffer |
| US5784154A (en) | 1992-01-13 | 1998-07-21 | Anthony R. Torres | Electrophoresis separation in a capillary passage |
| US5423964A (en) | 1993-08-02 | 1995-06-13 | Battelle Memorial Institute | Combined electrophoresis-electrospray interface and method |
| US6001229A (en) | 1994-08-01 | 1999-12-14 | Lockheed Martin Energy Systems, Inc. | Apparatus and method for performing microfluidic manipulations for chemical analysis |
| GB9509905D0 (en) | 1995-05-11 | 1995-07-12 | Watson Arthur H | Fast sample device for capillary isoelectric focusing |
| US5942443A (en) | 1996-06-28 | 1999-08-24 | Caliper Technologies Corporation | High throughput screening assay systems in microscale fluidic devices |
| US5779868A (en) | 1996-06-28 | 1998-07-14 | Caliper Technologies Corporation | Electropipettor and compensation means for electrophoretic bias |
| WO1998000705A1 (en) | 1996-06-28 | 1998-01-08 | Caliper Technologies Corporation | Electropipettor and compensation means for electrophoretic bias |
| US5800690A (en) | 1996-07-03 | 1998-09-01 | Caliper Technologies Corporation | Variable control of electroosmotic and/or electrophoretic forces within a fluid-containing structure via electrical forces |
| US6110343A (en) | 1996-10-04 | 2000-08-29 | Lockheed Martin Energy Research Corporation | Material transport method and apparatus |
| US5876675A (en) | 1997-08-05 | 1999-03-02 | Caliper Technologies Corp. | Microfluidic devices and systems |
| US5842787A (en) | 1997-10-09 | 1998-12-01 | Caliper Technologies Corporation | Microfluidic systems incorporating varied channel dimensions |
| EP1044370B1 (en) | 1997-12-30 | 2017-08-23 | Caliper Life Sciences, Inc. | Software for the display of chromatographic separation data |
| US6167910B1 (en) | 1998-01-20 | 2001-01-02 | Caliper Technologies Corp. | Multi-layer microfluidic devices |
| JP3887963B2 (ja) | 1998-08-07 | 2007-02-28 | 株式会社島津製作所 | 等電点電気泳動装置 |
| EP1876442A3 (en) | 1998-09-17 | 2008-03-05 | Advion BioSciences, Inc. | Integrated monolithic microfabricated liquid chromatography system and method |
| US6149787A (en) | 1998-10-14 | 2000-11-21 | Caliper Technologies Corp. | External material accession systems and methods |
| JP2000162184A (ja) | 1998-11-30 | 2000-06-16 | Hitachi Ltd | 小型電気泳動装置及びこれを用いた質量分析装置 |
| WO2000043131A2 (en) | 1999-01-22 | 2000-07-27 | Lord Corporation | Autodepositable adhesive |
| AU3372800A (en) | 1999-02-23 | 2000-09-14 | Caliper Technologies Corporation | Manipulation of microparticles in microfluidic systems |
| US6764817B1 (en) * | 1999-04-20 | 2004-07-20 | Target Discovery, Inc. | Methods for conducting metabolic analyses |
| US7329388B2 (en) | 1999-11-08 | 2008-02-12 | Princeton Biochemicals, Inc. | Electrophoresis apparatus having staggered passage configuration |
| US6974527B2 (en) | 2000-06-06 | 2005-12-13 | Spectrumedix Llc | Multidimensional separations employing an array of electrophoresis channels |
| US20020079220A1 (en) | 2000-11-09 | 2002-06-27 | Pawliszyn Janusz B. | Micromachining using printing technology |
| US20020166592A1 (en) | 2001-02-09 | 2002-11-14 | Shaorong Liu | Apparatus and method for small-volume fluid manipulation and transportation |
| US20050189225A1 (en) | 2001-02-09 | 2005-09-01 | Shaorong Liu | Apparatus and method for small-volume fluid manipulation and transportation |
| JP2004532392A (ja) * | 2001-02-20 | 2004-10-21 | アドヴィオン バイオサイエンシィズ インコーポレイテッド | 親和性吸着剤を有するマイクロチップ電子噴霧装置およびカラムならびにそれらの使用法 |
| US6974526B2 (en) * | 2001-05-01 | 2005-12-13 | Calibrant Biosystems, Inc. | Plastic microfluidics enabling two-dimensional protein separations in proteome analysis |
| US7601251B2 (en) | 2001-05-10 | 2009-10-13 | Life Technologies Corporation | Methods and apparatus for low resistance electrophoresis of prior-cast, hydratable separation media |
| JP4080893B2 (ja) | 2001-05-24 | 2008-04-23 | ニューオブジェクティブ,インク. | エレクトロスプレーをフィードバック制御するための方法と装置 |
| EP1270073B1 (de) | 2001-06-28 | 2005-02-16 | Agilent Technologies, Inc. (a Delaware corporation) | Mikrofluid-System mit Regler |
| EP1410029B1 (en) | 2001-07-16 | 2007-09-12 | Protein Forest, Inc. | Arrays of buffers for analysing biomolecules by their isoelectric point |
| US6803568B2 (en) * | 2001-09-19 | 2004-10-12 | Predicant Biosciences, Inc. | Multi-channel microfluidic chip for electrospray ionization |
| JP2005509872A (ja) * | 2001-10-19 | 2005-04-14 | ウエスト バージニア ユニバーシティ リサーチ コーポレーション | プロテオーム解析のための微小流体システム |
| US6831274B2 (en) | 2002-03-05 | 2004-12-14 | Battelle Memorial Institute | Method and apparatus for multispray emitter for mass spectrometry |
| JP2004031757A (ja) | 2002-06-27 | 2004-01-29 | Matsushita Electric Ind Co Ltd | 半導体素子の実装方法 |
| JP2004069430A (ja) | 2002-08-05 | 2004-03-04 | Mitsubishi Kagaku Iatron Inc | 電気泳動用チップ、その製造方法、及び物質の分離方法 |
| US7381317B2 (en) | 2002-08-12 | 2008-06-03 | Beckman Coulter, Inc. | Methods and compositions for capillary electrophoresis (CE) |
| US20040112751A1 (en) * | 2002-08-26 | 2004-06-17 | Jongyoon Han | Multidimensional electrophoresis and methods of making and using thereof |
| AU2003261957A1 (en) * | 2002-09-05 | 2004-04-23 | Katayanagi Institute | Method for separating substances |
| GB0226160D0 (en) * | 2002-11-08 | 2002-12-18 | Diagnoswiss Sa | Apparatus for dispensing a sample in electrospray mass spectrometers |
| WO2004065937A2 (en) | 2003-01-15 | 2004-08-05 | Protasis Corporation | Method and apparatus determining the isoelectric point of charged analyte |
| US20040202994A1 (en) * | 2003-02-21 | 2004-10-14 | West Virginia University Research Corporation | Apparatus and method for on-chip concentration using a microfluidic device with an integrated ultrafiltration membrane structure |
| US7655477B1 (en) | 2003-02-26 | 2010-02-02 | Science Applications International Corporation | System and method for the separation of analytes |
| JP3969654B2 (ja) | 2003-03-07 | 2007-09-05 | インターナショナル・ビジネス・マシーンズ・コーポレーション | Soapメッセージ作成方法並びに処理方法、情報処理方法、情報処理装置及びプログラム |
| US7425700B2 (en) | 2003-05-22 | 2008-09-16 | Stults John T | Systems and methods for discovery and analysis of markers |
| US20050072915A1 (en) | 2003-10-07 | 2005-04-07 | Biospect Inc. | Methods and apparatus for self-optimization of electrospray ionization devices |
| US8267914B1 (en) | 2003-10-16 | 2012-09-18 | University Of Notre Dame Du Lac | Method and apparatus for AC electrospray |
| CN1616958A (zh) * | 2003-11-11 | 2005-05-18 | 中国科学院大连化学物理研究所 | 一种基于微流控芯片的细胞定性分析方法 |
| US7022214B2 (en) | 2004-01-21 | 2006-04-04 | Bio-Rad Laboratories, Inc. | Carrier ampholytes of high pH range |
| US20060060769A1 (en) | 2004-09-21 | 2006-03-23 | Predicant Biosciences, Inc. | Electrospray apparatus with an integrated electrode |
| JP2006220551A (ja) * | 2005-02-10 | 2006-08-24 | Toray Ind Inc | マイクロチップ |
| US8021611B2 (en) | 2005-04-09 | 2011-09-20 | ProteinSimple | Automated micro-volume assay system |
| EP1715348B2 (en) | 2005-07-15 | 2019-05-08 | Agilent Technologies, Inc. | Handling unit for microfluidic devices with clamping means |
| US7329865B2 (en) | 2005-11-14 | 2008-02-12 | Agilent Technologies, Inc. | Mass spectrometry system and method with window assembly |
| WO2007055293A1 (ja) | 2005-11-14 | 2007-05-18 | Nec Corporation | マイクロチップおよびその使用方法、ならびに質量分析システム |
| US7339166B2 (en) | 2006-02-24 | 2008-03-04 | Battelle Memorial Institute | Interface and process for enhanced transmission of non-circular ion beams between stages at unequal pressure |
| US7495210B2 (en) | 2006-05-04 | 2009-02-24 | Agilent Technologies, Inc. | Micro fluidic gas assisted ionization device and method |
| US20080035484A1 (en) * | 2006-07-10 | 2008-02-14 | Jiaqi Wu | Method and apparatus for precise selection and extraction of a focused component in isoelectric focusing performed in micro-channels |
| WO2008052138A2 (en) | 2006-10-25 | 2008-05-02 | The Regents Of The University Of California | Inline-injection microdevice and microfabricated integrated dna analysis system using same |
| US20080318334A1 (en) * | 2007-06-20 | 2008-12-25 | Robotti Karla M | Microfluidic devices comprising fluid flow paths having a monolithic chromatographic material |
| US8329016B1 (en) | 2007-07-30 | 2012-12-11 | Sandia Corporation | Microfluidic device having an immobilized pH gradient and PAGE gels for protein separation and analysis |
| US10107782B2 (en) * | 2008-01-25 | 2018-10-23 | ProteinSimple | Method to perform limited two dimensional separation of proteins and other biologicals |
| US8173080B2 (en) | 2008-02-14 | 2012-05-08 | Illumina, Inc. | Flow cells and manifolds having an electroosmotic pump |
| WO2009109037A1 (en) | 2008-03-07 | 2009-09-11 | The University Of British Colu | Self-contained capillary electrophoresis system for interfacing with mass spectrometry |
| FR2934179B1 (fr) * | 2008-07-24 | 2010-09-17 | Commissariat Energie Atomique | Laboratoire sur puce comprenant un reseau micro-fluidique et un nez d'electronebulisation coplanaires. |
| CN101344518B (zh) * | 2008-08-15 | 2012-04-11 | 东南大学 | 微纳生物粒子的多模式集成化介电表征装置及方法 |
| CN201247242Y (zh) * | 2008-08-15 | 2009-05-27 | 东南大学 | 微纳生物粒子介电表征装置 |
| JP5164163B2 (ja) * | 2008-10-20 | 2013-03-13 | 独立行政法人産業技術総合研究所 | 等電点マーカー蛋白質 |
| US7939798B2 (en) * | 2009-01-30 | 2011-05-10 | Agilent Technologies, Inc. | Tandem ionizer ion source for mass spectrometer and method of use |
| GB0905575D0 (en) * | 2009-03-31 | 2009-05-13 | Stfc Science & Technology | Electrospinning nozzle |
| CN101692048B (zh) * | 2009-10-27 | 2012-04-25 | 浙江大学 | 毛细管电泳分离和化学发光检测的微芯片分析系统 |
| US20110243813A1 (en) * | 2010-03-30 | 2011-10-06 | Jackinsky Steve W | Diagnostic card with micro-fluidic channels and method of construction thereof |
| US20160084805A1 (en) | 2010-09-23 | 2016-03-24 | Battelle Memorial Institute | System and method of preconcentrating analytes in a microfluidic device |
| WO2012125318A2 (en) | 2011-03-11 | 2012-09-20 | The University Of North Carolina At Chapel Hill | Microchips with integrated multiple electrospray ionization emitters and related methods, systems and devices |
| US9234880B2 (en) | 2011-06-03 | 2016-01-12 | University Of Washington Through Its Center For Commercialization | Sheath-flow electrospray interface |
| GB201112726D0 (en) * | 2011-07-22 | 2011-09-07 | Molecular Vision Ltd | An optical device |
| CN103998394B (zh) * | 2011-08-01 | 2016-08-17 | 德诺弗科学公司 | 细胞捕获系统和使用方法 |
| US9989515B2 (en) | 2012-02-10 | 2018-06-05 | The University Of North Carolina At Chapel Hill | Devices with fluidic nanofunnels, associated methods, fabrication and analysis systems |
| EP2839276B1 (en) | 2012-04-19 | 2018-06-27 | ProteinSimple | Dual wavelength isoelectric focusing for determining drug load in antibody drug conjugates |
| AU2013256229A1 (en) * | 2012-05-03 | 2014-10-30 | Medimmune, Llc | Method for analyzing sample components |
| US9500621B2 (en) | 2012-06-04 | 2016-11-22 | Beckman Coulter, Inc. | Leakage current sense circuit for error detection in an improved capillary electrophoresis-electrospray ionization-mass spectrometry system |
| US9502225B2 (en) | 2012-06-20 | 2016-11-22 | The University Of North Carolina At Chapel Hill | Integrated sample processing for electrospray ionization devices |
| US10105702B2 (en) | 2013-03-15 | 2018-10-23 | Lariat Biosciences, Inc. | Microfluidic methods for manipulating DNA |
| CN105723213B (zh) | 2013-08-29 | 2019-09-13 | 圣母大学 | 高灵敏度电喷射接口 |
| US20150093757A1 (en) | 2013-09-27 | 2015-04-02 | Protein Simple | Methods. apparatus and systems for detection of total protein using capillary electrophoresis |
| US9766206B2 (en) | 2013-09-27 | 2017-09-19 | ProteinSimple | Apparatus, systems, and methods for capillary electrophoresis |
| US10031104B2 (en) | 2014-06-13 | 2018-07-24 | Yes Way Intellectual Holdings, Llc | Mobile micro-lab for chemical analysis of fluids |
| WO2016090064A1 (en) | 2014-12-05 | 2016-06-09 | Advanced Electrophoresis Solutions Ltd | Apparatus and method for separating molecules |
| US9606082B2 (en) | 2015-05-11 | 2017-03-28 | The University Of North Carolina At Chapel Hill | Pressure driven microfluidic injection for chemical separations |
| US9255905B1 (en) | 2015-05-11 | 2016-02-09 | The University Of North Carolina At Chapel Hill | Pressure driven microfluidic injection for chemical separations |
| MA56416A (fr) | 2015-05-12 | 2022-05-04 | Regeneron Pharma | Détermination de la pureté de protéines multimériques |
| CN107636455B (zh) | 2015-05-20 | 2021-01-22 | 普诺森公司 | 用于分析物的电泳分离和分析的系统和方法 |
| CN106374981B (zh) | 2015-07-20 | 2021-01-08 | 索尼公司 | 无线通信系统中的电子设备和无线通信方法 |
| US9728387B2 (en) | 2015-10-20 | 2017-08-08 | The University Of North Carolina At Chapel Hill | Solid phase extraction with capillary electrophoresis |
| WO2017095813A1 (en) | 2015-11-30 | 2017-06-08 | Intabio, Inc. | Devices and methods for sample characterization |
| EP3403082A4 (en) | 2016-01-13 | 2019-08-28 | ProteinSimple | SYSTEMS AND METHODS FOR CAPILLARY ELECTROPHORESIS, ISOELECTRIC POINT AND MOLECULAR WEIGHT ANALYSIS |
| US10737268B2 (en) | 2016-08-08 | 2020-08-11 | Li-Cor, Inc. | Multi-sheath flow and on-chip terminating electrode for microfluidic direct-blotting |
| CN109564188A (zh) | 2016-08-08 | 2019-04-02 | 利康公司 | 微芯片电泳喷墨式分配 |
| CN109791132A (zh) | 2016-09-26 | 2019-05-21 | 圣母大学 | 用于缓解毛细管区电泳-电喷雾装置中电流反转的方法和装置 |
| US10209218B2 (en) | 2017-03-30 | 2019-02-19 | 908 Devices Inc. | Microfluidic analysis of biological samples |
| SG11202007188RA (en) * | 2018-01-29 | 2020-08-28 | Intabio Inc | Devices, methods and kits for sample characterization |
| CN112534549A (zh) | 2018-05-31 | 2021-03-19 | 因塔生物公司 | 用于微流体系统与质谱联用的软件 |
| US11285484B2 (en) | 2019-08-12 | 2022-03-29 | Intabio, Llc | Multichannel isoelectric focusing devices and high voltage power supplies |
-
2016
- 2016-11-29 WO PCT/US2016/064013 patent/WO2017095813A1/en active Application Filing
- 2016-11-29 EP EP21200433.7A patent/EP3957986A1/en active Pending
- 2016-11-29 DK DK16871360.0T patent/DK3384274T3/da active
- 2016-11-29 CN CN201680080047.0A patent/CN108603828A/zh active Pending
- 2016-11-29 CA CA3006200A patent/CA3006200A1/en active Pending
- 2016-11-29 KR KR1020187018180A patent/KR20180101350A/ko not_active Application Discontinuation
- 2016-11-29 AU AU2016365121A patent/AU2016365121B2/en active Active
- 2016-11-29 US US15/363,908 patent/US20170176386A1/en not_active Abandoned
- 2016-11-29 DE DE202016008838.7U patent/DE202016008838U1/de active Active
- 2016-11-29 EP EP16871360.0A patent/EP3384274B1/en active Active
- 2016-11-29 JP JP2018547858A patent/JP6906542B2/ja active Active
-
2017
- 2017-09-19 US US15/709,158 patent/US10209217B2/en active Active
-
2018
- 2018-12-18 US US16/224,558 patent/US10401324B2/en active Active
-
2019
- 2019-11-19 US US16/688,141 patent/US10782264B2/en active Active
-
2020
- 2020-08-03 US US16/983,293 patent/US11573200B2/en active Active
-
2021
- 2021-06-29 JP JP2021107723A patent/JP7323576B2/ja active Active
-
2022
- 2022-02-11 AU AU2022200939A patent/AU2022200939B2/en active Active
- 2022-12-30 US US18/091,651 patent/US20230213478A1/en active Pending
-
2023
- 2023-07-27 JP JP2023122384A patent/JP2023139239A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| EP3957986A1 (en) | 2022-02-23 |
| US20170176386A1 (en) | 2017-06-22 |
| JP2023139239A (ja) | 2023-10-03 |
| JP2019503493A (ja) | 2019-02-07 |
| US10209217B2 (en) | 2019-02-19 |
| US20230213478A1 (en) | 2023-07-06 |
| AU2022200939B2 (en) | 2023-08-17 |
| US20180003674A1 (en) | 2018-01-04 |
| CA3006200A1 (en) | 2017-06-08 |
| DK3384274T3 (da) | 2021-12-13 |
| US11573200B2 (en) | 2023-02-07 |
| JP7323576B2 (ja) | 2023-08-08 |
| BR112018011132A2 (pt) | 2018-11-21 |
| US20200110055A1 (en) | 2020-04-09 |
| US20190128843A1 (en) | 2019-05-02 |
| JP2021170013A (ja) | 2021-10-28 |
| US10401324B2 (en) | 2019-09-03 |
| US20210181148A1 (en) | 2021-06-17 |
| AU2016365121A1 (en) | 2018-06-07 |
| WO2017095813A1 (en) | 2017-06-08 |
| EP3384274A1 (en) | 2018-10-10 |
| AU2016365121B2 (en) | 2022-03-03 |
| EP3384274B1 (en) | 2021-11-10 |
| CN108603828A (zh) | 2018-09-28 |
| DE202016008838U1 (de) | 2020-01-20 |
| AU2022200939A1 (en) | 2022-03-10 |
| US10782264B2 (en) | 2020-09-22 |
| KR20180101350A (ko) | 2018-09-12 |
| EP3384274A4 (en) | 2019-07-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6906542B2 (ja) | 試料の特性評価のためのデバイス及び方法 | |
| US10866246B2 (en) | Devices, methods and kits for sample characterization | |
| Zhou et al. | Advances in capillary electrophoresis-mass spectrometry for cell analysis | |
| Buszewski et al. | Electromigration techniques | |
| Chen et al. | Construction of discontinuous capillary isoelectric focusing system and its application in pre-fractionation of exosomal proteins | |
| BR112018011132B1 (pt) | Método para caracterização de amostra | |
| JP2007040816A (ja) | 分析方法、及び該分析方法に用いる装置 | |
| US20040163961A1 (en) | Apparatus and method for using bi-directional capillary electrophoresis | |
| Risley | Analysis of human erythropoietin and erythropoietin N-linked glycans using capillary electrophoresis and mass spectrometry | |
| Beutner | Selectivity enhancement in capillary electrophoresis–development of a two-dimensional separation and a dual detection system | |
| Black | Development and Application of Microfluidic Capillary Electrophoresis-Electrospray Ionization Devices for the Analysis of Biological Samples |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A529 | Written submission of copy of amendment under article 34 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A529 Effective date: 20180704 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20191126 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20191126 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200929 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201006 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20201216 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210325 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210601 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210629 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6906542 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| RD02 | Notification of acceptance of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: R3D02 |