JP6535483B2 - 幼若ホルモンセンサー - Google Patents
幼若ホルモンセンサー Download PDFInfo
- Publication number
- JP6535483B2 JP6535483B2 JP2015040712A JP2015040712A JP6535483B2 JP 6535483 B2 JP6535483 B2 JP 6535483B2 JP 2015040712 A JP2015040712 A JP 2015040712A JP 2015040712 A JP2015040712 A JP 2015040712A JP 6535483 B2 JP6535483 B2 JP 6535483B2
- Authority
- JP
- Japan
- Prior art keywords
- amino acid
- jhbp
- sensor
- juvenile hormone
- acid sequence
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Description
(2)前記共鳴エネルギー供与型物質が発光若しくは蛍光共鳴エネルギー供与型物質である、(1)に記載のJHセンサー。
(3)チョウ目昆虫におけるJHBPのシグナルペプチドを除いた切端アミノ酸配列において、該切端アミノ酸配列のアミノ末端におけるアミノ酸残基を1位としたときに、10〜15位の範囲内の連続する2つのアミノ酸残基間に共鳴エネルギー供与型物質及び該共鳴エネルギー供与型物質の励起エネルギーを受容する共鳴エネルギー受容型物質のいずれか一方を連結し、かつ前記切端アミノ酸配列のカルボキシル末端に前記共鳴エネルギー供与型物質及び前記共鳴エネルギー受容型物質の他方を連結した融合ポリペプチドからなるJHセンサー。
(4)前記共鳴エネルギー供与型物質及び/又は共鳴エネルギー受容型物質がペプチドである、(3)に記載のJHセンサー。
(5)前記ペプチドが発光若しくは蛍光ペプチドである、(4)に記載のJHセンサー。
(6)チョウ目昆虫における幼若ホルモン結合タンパク質のシグナルペプチドを除いた切端アミノ酸配列において、該切端アミノ酸配列のアミノ末端におけるアミノ酸残基を1位としたときに、10〜15位の範囲内の連続する2つのアミノ酸残基間に2分割された発光又は蛍光タンパク質断片のアミノ末端側のアミノ酸配列を連結し、かつ前記切端アミノ酸配列のカルボキシル末端に2分割された発光又は蛍光タンパク質断片のカルボキシル末端側のアミノ酸配列を連結した融合ポリペプチドからなるJHセンサー。
(7)前記連続する2つのアミノ酸残基間が11位と12位のアミノ酸残基間である、(3)〜(6)のいずれかに記載のJHセンサー。
(8)前記切端アミノ酸配列が(a)〜(c)で示すいずれかのアミノ酸配列である、(3)〜(7)のいずれかに記載のJHセンサー。
(a)配列番号2、3、6又は8で示すアミノ酸配列、
(b)(a)に記載のいずれか一のアミノ酸配列において1若しくは複数個のアミノ酸残基が欠失、置換若しくは付加されたアミノ酸配列、又は
(c)(a)に記載のいずれか一のアミノ酸配列に対して90%以上のアミノ酸同一性を有するアミノ酸配列
(9)(4)〜(8)のいずれかに記載のJHセンサーを構成する融合ポリペプチドをコードするDNA。
(10)(9)のDNAを発現可能な状態で包含するJHセンサー発現ベクター。
(11)(10)に記載のJHセンサー発現ベクターを宿主細胞又は宿主生物に導入した形質転換体又はその後代。
(12)節足動物の生体内におけるJHの動態をモニタリングする方法であって、被験体の節足動物に(1)〜(8)のいずれかに記載のJHセンサーを導入する工程、前記被験体において共鳴エネルギー移動により変動するエネルギー変異又は発光若しくは蛍光タンパク質の再構築により発生する発光若しくは蛍光を測定する工程、及び前記測定工程で測定された測定値に基づいてJHを検出する工程を含む前記方法。
(13)前記変動するエネルギー変異が発光若しくは蛍光である、(12)に記載の方法。
(14)節足動物の生体内におけるJHの動態をモニタリングする方法であって、被験体の節足動物に(10)に記載のJHセンサー発現ベクターを導入し、形質転換体を作製する工程、前記形質転換体においてJHセンサー発現ベクターから発現したJHセンサーに由来する発光若しくは蛍光共鳴エネルギー移動により変動するエネルギー変異又は蛍光タンパク質の再構築により発生する発光若しくは蛍光を測定する工程、及び前記測定工程で測定された測定値に基づいてJHを検出する工程を含む前記方法。
(15)前記変動するエネルギー変異が発光若しくは蛍光である、(14)に記載の方法。
(16)節足動物のJHに構造的に類似するJH類似体の探索方法であって、(1)〜(8)のいずれかに記載のJHセンサーと候補物質とを混合する工程、JHセンサーの共鳴エネルギー移動によるエネルギー変異又は発光若しくは蛍光タンパク質の再構築により発生する蛍光を測定する工程、及び前記測定工程で得られた測定値に基づいて候補物質をJH類似体として選択する工程を含む前記方法。
(17)前記変動するエネルギー変異が発光若しくは蛍光である、(16)に記載の方法。
(18)前記選択工程が、前記混合工程において候補物質を混合しない陰性対照の測定値との有意差、又は候補物質の濃度依存的な測定値の増加に基づく、(16)又は(17)に記載の方法。
1.幼若ホルモンセンサー
1−1.概要
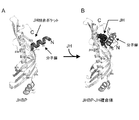
本発明の第1の態様は、幼若ホルモンセンサー(JHセンサー)である。本態様のJHセンサーは、幼若ホルモンの結合によるチョウ目昆虫由来の幼若ホルモン結合タンパク質(JHBP)の立体構造変化を利用したバイオセンサーであり、FRETの共鳴エネルギー移動の原理に基づいて、又は蛍光又は発光タンパク質の再構築に基づいて、節足動物のJHをインビトロ及びインビボにおいて高感度に検出及び定量することを特徴とする。
本発明のJHセンサーは、(1)チョウ目昆虫由来のJHBPの異なる2つの特定の位置のアミノ酸残基に、共鳴エネルギー移動を生じ得る共鳴エネルギー供与型物質及び共鳴エネルギー受容型物質を修飾してなる修飾タンパク質、又は、(2)チョウ目昆虫由来のJHBPの異なる2つの特定の位置に共鳴エネルギー供与型物質及び共鳴エネルギー受容型物質を連結してなる融合ポリペプチド、あるいは(3)チョウ目昆虫由来のJHBPの異なる2つの特定の位置に、2分割した発光又は蛍光タンパク質断片のアミノ末端側断片とカルボキシル末端側断片をそれぞれ連結してなる融合ポリペプチド、で構成される。
成熟型JHBPのアミノ末端のアミノ酸残基を1位としたときに、10〜15位のいずれか一のアミノ酸残基、及びカルボキシル末端のアミノ酸残基がJHBPの特定の位置に該当する。
成熟型JHBPのアミノ末端のアミノ酸残基を1位としたときに、10〜15位の範囲内の連続する2つのアミノ酸残基間、及びJHBPのカルボキシル末端がJHBPの特定の位置に該当する。
(2)と同様に、成熟型JHBPのアミノ末端のアミノ酸残基を1位としたときに、10〜15位の範囲内の連続する2つのアミノ酸残基間、及びJHBPのカルボキシル末端がJHBPの特定の位置に該当する。
本発明のJHセンサーは、JHに対して高い特異性を有することから、JHを高感度に検出及び定量することができる。特に甲殻生物のJHであるMFは、エポキシ環を持たないためイオン化し難く、質量分析による定量は極めて困難であったが、本発明のJHセンサーによれば、微量MFの高感度検出や定量化も可能となる。
2−1.概要
本発明の第2の態様は、第1態様のJHセンサーをコードするDNA(本明細書では、しばしば「JHセンサーDNA」と表記する)である。本態様のJHセンサーDNAは、第1態様のJHセンサーにおいて、該センサーがドナー型ペプチド及びアクセプター型ペプチドを含むJHBPの融合ポリペプチドの場合に該当する。
JHセンサーDNAにおいて、JHBPをコードするDNA(本明細書では、しばしば「JHBP遺伝子」と表記する)の塩基配列には、配列番号2で示すアミノ酸配列からなるカイコJHBPをコードするJHBP遺伝子、具体的には、例えば、配列番号3で示す塩基配列からなるカイコJHBP遺伝子、配列番号4で示すアミノ酸配列からなるタバコスズメガJHBPをコードするJHBP遺伝子、具体的には、例えば、配列番号5で示す塩基配列からなるタバコスズメガJHBP遺伝子、配列番号6で示すアミノ酸配列からなるオオタバコガJHBPをコードするJHBP遺伝子、具体的には、例えば、配列番号7で示す塩基配列からなるオオタバコガJHBP遺伝子、そして配列番号8で示すアミノ酸配列からなるハチノスツヅリガJHBPをコードするJHBP遺伝子、具体的には、例えば、配列番号9で示す塩基配列からなるハチノスツヅリガJHBP遺伝子が挙げられる。JHBP遺伝子は、上記の野生型JHBP遺伝子の他にも第1態様に記載した各生物種の変異型JHBPをコードする変異型JHBP遺伝子であってもよい。
本発明のJHセンサーDNAは、JHBP、及びドナー型ペプチド及びアクセプター型ペプチドとしての発光若しくは蛍光タンパク質、又は2分割タンパク質断片のN末側断片及びC末側断片のそれぞれをコードするDNAを当該分野で公知の分子遺伝学的手法に基づいて連結することで調製できる。
3−1.概要
本発明の第3の態様は、第2態様のJHセンサーDNAを発現可能な状態で包含する幼若ホルモンセンサー発現ベクター(本明細書では、しばしば「JHセンサー発現ベクター」と表記する)である。本発明のJHセンサー発現ベクターは、JHセンサーの発現を制御することができる。また宿主である節足動物に導入することによって、その形質転換体を得て後述する第5態様のJHの生体内動態モニタリング方法によりJHの生体内動態モニタリングシステムを構築することが可能となる。
本明細書において「JHセンサー発現ベクター」とは、ベクター内部にコードされたJHセンサーDNAを発現可能な状態で包含し、その発現を誘導できる発現系単位をいう。
母核ベクターは、JHセンサー発現ベクターの骨格部分を構成する。母核ベクターには、様々なベクターを利用することができる。例えば、プラスミド若しくはバクミド(Bacmid)のような自律複製可能なベクター、ウイルスベクター、又は染色体中に相同組換え可能なベクターが挙げられる。母核ベクターとして、一般には導入する宿主生物の細胞内で複製可能なベクターが選択される。また、母核ベクターは、大腸菌等の他の細菌と節足動物間で複製可能なシャトルベクターであってもよい。さらに、ライフサイエンスメーカーの各社から、母核ベクター中に後述するプロモーター、ターミネーター、マルチクローニングサイト、選抜マーカー等が既に挿入されたタンパク質発現用ベクターが市販されており、それらをJHセンサー発現ベクターに利用することもできる。
このJHセンサーDNAは、前記第2態様に記載したJHセンサーDNAである。JHセンサーを分泌タンパク質として発現させる場合には、5’末端にシグナルDNAを連結したJHセンサーDNAとすればよい。例えば、本発明のJHセンサー発現ベクターを後述する第4態様のJHの生体内動態モニタリング用として、宿主である節足動物に導入する場合には、シグナルDNAが連結されたJHセンサーDNAにする必要がある。
JHセンサー発現ベクターに含まれるプロモーターは、本発明のJHセンサー発現ベクターにおいてJHセンサーの発現を制御する必須構成エレメントである。プロモーターは、宿主細胞内で転写制御機能を有するプロモーターであれば、その種類は特に限定はしない。当該分野で公知のプロモーターを用いればよい。一般的には、例えば、宿主内で目的の遺伝子を、過剰に発現可能な過剰発現型プロモーター、恒常的に発現可能な構成的活性型プロモーター、宿主の発生段階に応じて発現制御できる時期特異的活性型プロモーター、発現を自由に制御できる発現誘導型プロモーター、そして宿主の特定組織や特定部位で選択的に発現することができる部位特異的プロモーター等が知られている。いずれのプロモーターを用いてもよく、本発明のJHセンサー発現ベクターの使用用途を勘案して適宜定めればよい。
ターミネーターは、本発明のJHセンサー発現ベクターにおいてJHセンサーDNAの発現時にその転写を終結できる塩基配列で構成される選択構成エレメントである。プロモーターにより転写されたJHセンサーDNAの転写を終結できる配列であれば特に限定はしない。
エンハンサーは、プロモーターを制御する調節因子であり、本発明のJHセンサー発現ベクターにおける選択構成エレメントである。
マルチクローニングサイトは、クローニング用制限酵素部位を多数包含するクラスター領域で、本発明のJHセンサー発現ベクターにおける選択構成エレメントである。マルチクローニングサイトを構成する塩基配列や包含する制限酵素部位の種類及び数については特に制限はしない。また、JHセンサー発現ベクターにおけるマルチクローニングサイトの数や配置される位置についても制限はしないが、JHセンサーDNAを発現可能な状態でJHセンサー発現ベクターには、少なくともプロモーターの制御領域範囲内に配置しておくことが好ましい。
5’UTR及び3’UTRは、それ自身がタンパク質やその断片、又は機能性核酸をコードしない非翻訳領域からなる核酸領域である。3’UTRは、ポリAシグナルを含むことができる。本発明のJHセンサー発現ベクターにおける選択構成エレメントである。5’UTRはJHセンサーDNAの開始コドン上流に、また3’UTRはJHセンサーDNAの終止コドン下流に配置される。
選抜マーカーは、宿主が本発明のJHセンサー発現ベクターを保持していることを示す確認用マーカーとして機能し得る。本発明のJHセンサー発現ベクターの選択構成エレメントである。選抜マーカーには、一般に、酵素、蛍光タンパク質、色素合成タンパク質又は発光タンパク質等をコードする遺伝子が利用される。例えば、薬剤耐性遺伝子(例えば、テトラサイクリン耐性遺伝子、アンピシリン耐性遺伝子、カナマイシン耐性遺伝子、ハイグロマイシン耐性遺伝子、スペクチノマイシン耐性遺伝子、クロラムフェニコール耐性遺伝子又はネオマイシン耐性遺伝子)、栄養素遺伝子(例えば、ロイシン、ウラシル、アデニン、ヒスチジン、リジン又はトリプトファンの生合成遺伝子)、蛍光又は発光レポーター遺伝子(例えば、ルシフェラーゼ、β-ガラクトシダーゼ、β-グルクロニターゼ(GUS)、又はGFP)、酵素遺伝子(ネオマイシンホスホトランスフェラーゼII(NPT II)、ジヒドロ葉酸還元酵素等)、ブラストサイジンS耐性遺伝子等の酵素遺伝子が挙げられる。ただし、蛍光又は発光レポーター遺伝子を選抜マーカーとする場合には、共鳴エネルギー移動に関与する発色団の活性を阻害しない蛍光又は発光スペクトルを選択する。JHセンサーの共鳴エネルギー移動供与型又は受容型物質が蛍光又は発光タンパク質の場合、それを選抜マーカーとして利用してもよい。必要に応じて、一つのJHセンサー発現ベクターに同一の又は異なる複数の選抜マーカーを包含することができる。
インスレーターは、本発明のJHセンサー発現ベクターにおける選択構成エレメントであって、周囲の染色体のクロマチンによる影響を受けることなく、その配列に挟まれた遺伝子の転写を、安定的に制御できる塩基配列である。例えば、ショウジョウバエのgypsy配列などが挙げられる。
「トランスポゾンの逆位末端反復配列(Inverted terminal repeat sequence)」は、本発明のJHセンサー発現ベクターが相同組換え可能な発現ベクターの場合に含まれ得る選択構成エレメントである。逆位末端反復配列は、通常は2個1組で使用され、例えば、昆虫のトランスポゾンとしては、piggyBac、mariner、minos等を用いることができる(Shimizu,K. et al., 2000, Insect Mol. Biol., 9, 277-281;Wang W. et al.,2000, Insect Mol Biol 9(2):145-55)。
本発明のJHセンサー発現ベクターの調製方法も前記第2態様のJHセンサーDNAの調製方法と同様に、当該分野の公知技術で達成し得る。例えば、Green, M.R. and Sambrook, J., 2012(前述)に記載の方法に従って行えばよい。本明細書では後述する実施例1で、JHセンサー発現ベクターの具体的な調製方法を一例として、記載している。
4−1.概要
本発明の第4の態様は形質転換体又はその後代である。本発明の形質転換体は、第3態様のJHセンサー発現ベクターを包含することを特徴とする。本発明の形質転換体が、大腸菌や酵母等の単細胞生物であればJHセンサー発現系として利用することができる。また、節足動物門生物の形質転換体であれば、第5態様に記載のJHの生体内動態モニタリング用形質転換体として利用することができる。
本発明の形質転換体は、第3態様のJHセンサー発現ベクターを細胞内に包含する。すなわち、第3態様のJHセンサー発現ベクターの導入によって形質転換された宿主が本態様の形質転換体となる。したがって、本態様の形質転換体は、宿主及び第3態様のJHセンサー発現ベクターで構成されている。以下、具体的に説明をする。
本発明の形質転換体を構成する宿主は、JHセンサー発現ベクターに包含されたJHセンサーDNAを発現することができる細胞又は個体であれば、特に制限はされない。宿主が原核細胞であれば、例えば、大腸菌(Escherichia coli)、枯草菌(Bacillus subtilis)等が挙げられる。また、宿主が真核細胞であれば、出芽酵母(Saccharomyces cerevisiae)、分裂酵母(Schizosaccharomyces pombe)、昆虫細胞(例えば、Sf9、Sf21、SF+、High-Five、BmN4)等の培養細胞が挙げられる。さらに、宿主が個体であれば、節足動物、例えば、前述の昆虫、甲殻生物、又は蛛形綱生物等が挙げられる。個体として特に好ましい宿主は、昆虫である。
本発明の形質転換体に包含されるJHセンサー発現ベクターは、第3態様に記載のJHセンサー発現ベクターである。宿主が大腸菌、枯草菌、出芽酵母、分裂酵母、又は培養細胞の場合、JHセンサー発現ベクターに包含されるJHセンサーDNAは、シグナルDNAを連結していても、いなくてもよい。一方、宿主が多細胞生物個体の場合には、JHセンサー発現ベクターに包含されるJHセンサーDNAは、シグナルDNAを連結していることが好ましい。JHセンサー発現ベクターは、宿主ゲノム内に組み込まれていても構わない。
本明細書で「後代」とは、形質転換体第1世代の子孫個体であって、第3態様のJHセンサー発現ベクターをその細胞内に保持している個体をいう。後代は、第3態様のJHセンサー発現ベクター保持する限りにおいてその世代数を問わない。
本発明の形質転換体の作製は、宿主へのJHセンサー発現ベクターの導入によって行われる。JHセンサー発現ベクターの導入方法は、導入する宿主に応じた公知の導入方法を用いればよい。細菌や酵母に該ベクターを導入する方法であれば、例えば、ヒートショック法、カルシウムイオンを用いる方法、エレクトロポレーション法等が挙げられる。これらの技術は、いずれも当該分野で公知であり、様々な文献に記載されている。例えば、Green, M.R. and Sambrook, J., 2012(前述)に記載の方法を参照にすればよい。また、細胞に該ベクターを導入する方法であれば、例えば、リポフェクチン法(PNAS,1989,86: 6077;PNAS, 1987,84: 7413)、エレクトロポレーション法、リン酸カルシウム法(Virology, 1973, 52: 456-467)、リポソーム法、DEAE-Dextran法等が好適に用いられる。また、個体に導入する方法も公知技術を用いればよい。例えば、昆虫の個体にJHセンサー発現ベクターを導入する方法としては、遺伝子発現ベクターをカイコに導入するTamuraらの方法(Tamura T. et al., 2000, Nature Biotechnology, 18, 81-84)を利用することができる。
5−1.概要
本発明の第5の態様は、JHの生体内動態モニタリング方法である。本発明の方法は、第1態様に記載のJHセンサーを導入した個体又は第4態様に記載の形質転換体を用いて、FRETに基づく生体内の蛍光スペクトルの変化を検出する。当該方法によって、従来のJH検出及び定量方法では成し得なかった生体内におけるJHの動態をモニタリングすることができる。
本明細書において「生体」とは、個体が生存している状態をいう。
本発明の方法は、第1実施形態と第2実施形態からなる。以下、それぞれの実施形態について説明をする。
第1実施形態は、第1態様に記載のJHセンサーを個体に導入し、その個体を用いて生体内動態モニタリングを行う形態である。本実施形態は、導入工程、測定工程、及びJH検出工程を含む。以下、各工程について説明をする。
「導入工程」は、被験体の節足動物に第1態様に記載のJHセンサーを導入する工程である。
本工程の「被験体」は、本発明のJHの生体内動態モニタリング方法に供される節足動物個体をいう。節足動物は、昆虫、甲殻生物又は蛛形綱生物が好ましく、昆虫はより好ましい。
「測定工程」は、導入工程後の被験体からJHセンサーに由来するFRET又はタンパク質再構築により発生する蛍光又は発光を測定する工程である。前述のように、本発明のJHセンサーは、JHの結合によるJHBPの立体構造変化をFRET又はタンパク質再構築による発光若しくは蛍光として捉えることを原理とする。その発光又は蛍光スペクトルの変化を測定することによって、生体内におけるJHの存在やその量を間接的に検出し、定量化することができる。
「JH検出工程」は、前記測定工程で測定された測定値に基づいてJHを検出する工程である。「測定値」とは、前記測定工程における発光又は蛍光の測定方法に基づいて得られた数値である。数値単位は、測定方法によって異なる。例えば、蛍光を検出し、測定する方法であれば、数値単位として、蛍光強度(Fluorescence intensity)(単位:arbitrary unit)等となる。
第2実施形態は、第4態様に記載の形質転換体を用いて生体内動態モニタリングを行う形態である。本実施形態は、形質転換体作製工程、測定工程、及びJH検出工程を含む。以下、各工程について説明をする。
「形質転換体作製工程」は、被験体である節足動物に第3態様のJHセンサー発現ベクターを導入し、形質転換体を作製する工程である。本工程は、第4形態の形質転換体又はその後代が入手可能な場合には不要な工程である。その場合、次の測定工程から行えばよい。
「測定工程」は、前記形質転換体のJHセンサー発現ベクターから発現したJHセンサーに由来するFRET、又は発光若しくは蛍光タンパク質の再構築により発生する蛍光又は発光を測定する工程である。基本的には、第1実施形態の測定工程に準じて行えばよい。そこで、ここでは、第1実施形態とは異なる点について説明をする。
「JH検出工程」は、前記測定工程で測定された測定値に基づいてJHを検出する工程である。基本的には、第1実施形態のJH検出工程に準じて行えばよい。ここでは、第1実施形態とは異なる点について説明をする。
従来のJH検出及び定量方法は、いずれの方法もJHの検出にあたっては、細胞や組織を破壊する必要があり、生体内におけるJHの動態を観察することはできなかった。本発明のJHの生体内動態モニタリング方法によれば、従来方法では成し得なかった生体内におけるJHの動態をモニタリングすることができる。
6−1.概要
本発明の第6の態様は、JH類似体の探索方法である。本発明の方法は、JH類似体をハイスループットでスクリーニングする方法である。本方法によれば、昆虫等の変態を効果的に阻害する薬剤としてのJH類似体を簡便かつ迅速に探索し、得ることができる。
本発明の方法は、混合工程、測定工程、及び選択工程を含む。
(1)混合工程
「混合工程」とは、前記第1態様に記載のJHセンサーと候補物質とを混合する工程である。
本発明の方法をインビトロ系で行う場合には、予めJHセンサーを調製しておく。JHセンサーは、公知のタンパク質発現方法により本発明のJHセンサー発現ベクターを包含する大腸菌や酵母等の単細胞生物か昆虫細胞等の培養細胞の形質転換体から抽出することができる。大腸菌、酵母、培養細胞等の培養方法、タンパク質発現方法及びタンパク質抽出方法の具体的な方法については、Green, M.R. and Sambrook, J., 2012(前述)に記載の方法を参考にすればよい。なお、形質転換体がシグナルDNAを有するJHセンサー遺伝子を含んだJHセンサー発現ベクターを包含しているのであれば、発現したJHセンサーは、培養液中に分泌されることから、培養上清を回収することでJHセンサーを得ることができる。JHセンサーを含む培養上清は、必要に応じて公知のタンパク質分離精製技術、例えば、ゲルろ過、イオン交換クロマトグラフィー、アフィニティークロマトグラフィーを用いて回収することができる。
「測定工程」とは、JHセンサーの発光若しくは蛍光共鳴エネルギー移動又は蛍光タンパク質の再構築により発生する蛍光又は発光を測定する工程である。
「選択工程」とは、前記測定工程で得られた測定値に基づいた候補物質をJH類似体として選択する工程である。
本発明のJHセンサー発現ベクターを構築した。
(1)mTFPmVenus_pRSET-A(Kpn)_ver1.2の構築
大腸菌タンパク質発現用ベクターであるpRSET-A-BFP(Life technologies)を母核として、そのベクターに含まれるBFP ORF(open reading frame:読取枠)をFRET発色団ORFと置換した「mTFPmVenus_pRSET-A(Kpn)_ver1.2」を構築した。FRETの発色団ORFには、配列番号11で示される塩基配列からなるシアン蛍光タンパク質mTFP1 ORFと配列番号13で示される塩基配列からなる黄蛍光タンパク質mVenus ORFを用いた。
mTFPmVenus_pRSET-A(Kpn)_ver1.2においてmTFPm ORFとVenus ORF間の制限酵素認識配列はKpnIのみである(図3A参照)。それ故、JHセンサーを構築する上で、JHBP遺伝子挿入時における利便性が低い。そこで、Inverse PCR法により制限酵素認識配列(XhoI、EcoRV、KpnI)を付加したmTFPmVenus_pRSET-A(RV)_ver1.2を構築した。核酸増幅用プライマーとして配列番号20と配列番号21で示すプライマーペアを用いた。完成したmTFPmVenus_pRSET-A(RV)_ver1.2のプラスミドマップを図3Bに示す。
FRET-JHBP-TypeA〜TypeCを含むFRET-JHBPキメラタンパク発現ベクターを構築した。FRET-JHBP-TypeA〜TypeC(図4)は、それぞれmTFP及びmVenusのJHBPへの挿入位置が異なるキメラタンパク質をコードする。このうちFRET-JHBP-TypeAが本発明のJHセンサーの構成を有する。
成熟型JHBP ORFには、配列番号3で示す塩基配列からなるカイコ成熟型JHBP II ORF(BmJHBP II)を用いた(Vermunt et al., 2001. Insect Mol. Biol. 10: 147)。JHBPII-pGEX2Tを鋳型として、5’末端側にXho Iを付加したプライマーJHBP_f1(配列番号22)と3’ 末端側にKpn Iを付加したプライマーJHBP_r1(配列番号23)でPCRを行い、得られたPCR産物を精製後、XhoI及びKpnIで切断処理してBmJHBP II DNA断片(XhoI/KpnI)を得た。続いて、mTFPmVenus_pRSET-A(RV)_ver1.2をXhoI及びKpnIで切断し、BmJHBP II DNA断片(XhoI/KpnI)を組み込んだ。PCR条件やライゲーション反応条件は、(1)の方法に準じて行った。その結果、BmJHBP II ORFの5’末端側にmTFP ORFが、また3’末端側にmVenus ORFが連結されたFRET-JHBP-TypeCを得た(図4)。
JHの結合及び乖離時のJHBPの立体構造情報(Suzuki et al., 2011)から、蛍光タンパク質をJHBP内に挿入することで、FRET効率が大きくなるアミノ酸領域を推定した。その候補領域の一つを成熟JHBPにおける10〜15位のアミノ酸として、BmJHBPの11位のリジンコドン(L11)と12位のグリシンコドン(G12)間にmTFP ORFを挿入し、またmVenus ORFをJHBP ORFの3’末端に連結したFRET-JHBP-TypeA(図4)を構築した。
続いて、N末端領域とC末端領域を鋳型として、N末端領域の5’末端側GeneArt認識配列に結合するフォワードプライマーAJH-Ff3(配列番号26)とN末端領域の3’末端側GeneArt認識配列に結合するリバースプライマーAJH-Fr1(配列番号27)、C末端領域の5’末端側GeneArt認識配列に結合するフォワードプライマーAJH-Rf1(配列番号28)とC末端領域の3’末端側GeneArt認識配列に結合するリバースプライマーAJH_Rf1(配列番号29)を用いてPCRを行い、GeneArt Seamless cloning(Life technologies)によりFRET-JHBP-TypeAの全長断片を調製した。全長断片を含むPCR産物をpBluescript II (sk)に直接クローニングした後、BigDye Terminator v3.1 cycle sequencing kit(Life technologies)を用いてPCR産物の塩基配列を決定し、JHBP ORF内の特定の位置にmTFP1 ORFがシームレスに挿入されていることを確認した。Bam HIとHind IIIによる切断処理によってpBluescript II (sk)からFRET-JHBP-TypeAの全長断片を切り出した後、その断片をBam HIとHind IIIによる切断処理によってBFP ORFを除いたpRSET-A-BFP(Life technologies)のBam HI/Hind III制限酵素認識配列中に挿入した。得られたFRET-JHBP-TypeAキメラタンパク質発現ベクターを「FRET-JHBP-TypeA_pRSE Ta」とした。FRET-JHBP-TypeA_pRSE Taの塩基配列を配列番号30に示す。前述のように、この発現ベクターは、本発明のJHセンサー発現ベクターの構成を有する。
FRET効率が大きくなる他の推定アミノ酸領域として、成熟BmJHBPの137位のアスパラギンコドン(N137)と138位のグリシンコドン(G12)を選択し、それらのアミノ酸残基間にmVenus ORFを挿入し、またmTFP ORFをBmJHBPの5’末端に連結したFRET-JHBP-TypeB(図4)を構築した。
実施例1で調製した3種類の遺伝子発現ベクターを宿主に導入した形質転換体を作製し、各遺伝子発現ベクターにコードされたFRET-JHBPキメラタンパク質の発現誘導とその精製を行った。
実施例2で調製し、単一精製した各FRET-JHBPキメラタンパク質によるJH存在下での蛍光強度を測定した。
実施例3の結果から、FRET-JHBP-TypeAは、JHセンサーとして機能することが明らかとなった。しかし、FRET-JHBP-TypeAは、FRETが不安定という問題があった。そこで、TypeAの配列を基に、高い安定性を保持したJHセンサーの開発を行った。
結果を表1に示す。
実施例3及び4では、JHとしてJH IIIを用いた。本発明のJHセンサーがJH III以外のJH又はJH類似体を検出可能なことを検証する。
本発明のJHセンサーにより試料中のJH又はJH類似体を定量化できることを確認した。
96wellマイクロプレート(Falcon #3072)に、実施例4で調製したJHセンサー(FRET-JHBP-TypeAd5)を最終濃度が1 μMとなるように150mM NaCLを含む198μLの10mM Tris-HCl buffer(pH 7.5)に加え、その後、リガンドとして0.1nM〜1×107nMのJH(JH I (SciTech)、JH II (SciTech)、JH III (Sigma-Aldrich)、MF (Echelon Biosciences))又はJH類似体(メトプレン酸 (Sigma-Aldrich))のエタノール溶液2 μLを濃度ごとに各wellに添加して、室温(約25℃)にて暗所で1時間静置した。反応後、各wellにおける励起波長450nm、測定波長480、及び535nmの蛍光強度を蛍光プレートリーダー(Perkin-Elmer ARVO MX ;1420 Multilabel Counter)で測定した。535nm/480nmの蛍光強度比を算出した。
Claims (18)
- チョウ目昆虫における幼若ホルモン結合タンパク質のシグナルペプチドを除いた切端アミノ酸配列において、
該切端アミノ酸配列のアミノ末端におけるアミノ酸残基を1位としたときに、10〜15位のいずれか一のアミノ酸残基が共鳴エネルギー供与型物質及び該共鳴エネルギー供与型物質の励起エネルギーを受容する共鳴エネルギー受容型物質のいずれか一方で修飾され、かつ
前記切端アミノ酸配列のカルボキシル末端のアミノ酸残基が前記共鳴エネルギー供与型物質及び前記共鳴エネルギー受容型物質の他方で修飾されている
タンパク質からなる幼若ホルモンセンサー。 - 前記共鳴エネルギー供与型物質が発光若しくは蛍光共鳴エネルギー供与型物質である、請求項1に記載の幼若ホルモンセンサー。
- チョウ目昆虫における幼若ホルモン結合タンパク質のシグナルペプチドを除いた切端アミノ酸配列において、
該切端アミノ酸配列のアミノ末端におけるアミノ酸残基を1位としたときに、10〜15位の範囲内の連続する2つのアミノ酸残基間に共鳴エネルギー供与型物質及び該共鳴エネルギー供与型物質の励起エネルギーを受容する共鳴エネルギー受容型物質のいずれか一方を連結し、かつ
前記切端アミノ酸配列のカルボキシル末端に前記共鳴エネルギー供与型物質及び前記共鳴エネルギー受容型物質の他方を連結した
融合ポリペプチドからなる幼若ホルモンセンサー。 - 前記共鳴エネルギー供与型物質及び/又は共鳴エネルギー受容型物質がペプチドである、請求項3に記載の幼若ホルモンセンサー。
- 前記ペプチドが発光若しくは蛍光ペプチドである、請求項4に記載の幼若ホルモンセンサー。
- チョウ目昆虫における幼若ホルモン結合タンパク質のシグナルペプチドを除いた切端アミノ酸配列において、
該切端アミノ酸配列のアミノ末端におけるアミノ酸残基を1位としたときに、10〜15位の範囲内の連続する2つのアミノ酸残基間に2分割された発光又は蛍光タンパク質断片のアミノ末端側のアミノ酸配列を連結し、かつ
前記切端アミノ酸配列のカルボキシル末端に2分割された発光又は蛍光タンパク質断片のカルボキシル末端側のアミノ酸配列を連結した
融合ポリペプチドからなる幼若ホルモンセンサー。 - 前記連続する2つのアミノ酸残基間が11位と12位のアミノ酸残基間である、請求項3〜6のいずれか一項に記載の幼若ホルモンセンサー。
- 前記切端アミノ酸配列が(a)〜(c)で示すいずれかのアミノ酸配列である、請求項3〜7のいずれか一項に記載の幼若ホルモンセンサー。
(a)配列番号2、4、6又は8で示すアミノ酸配列、
(b)(a)に記載のいずれか一のアミノ酸配列において1若しくは2〜20個のアミノ酸残基が欠失、置換若しくは付加されたアミノ酸配列、又は
(c)(a)に記載のいずれか一のアミノ酸配列に対して90%以上のアミノ酸同一性を有するアミノ酸配列 - 請求項4〜8のいずれか一項に記載の幼若ホルモンセンサーを構成する融合ポリペプチドをコードするDNA。
- 請求項9に記載のDNAを発現可能な状態で包含する幼若ホルモンセンサー発現ベクター。
- 請求項10に記載の幼若ホルモンセンサー発現ベクターを宿主細胞又は宿主生物に導入した形質転換体又はその後代。
- 節足動物の生体内における幼若ホルモンの動態をモニタリングする方法であって、
被験体の節足動物に請求項1〜8のいずれか一項に記載の幼若ホルモンセンサーを導入する工程、
前記被験体において共鳴エネルギー移動により変動するエネルギー変異又は発光若しくは蛍光タンパク質の再構築により発生する発光若しくは蛍光を測定する工程、及び
前記測定工程で測定された測定値に基づいて幼若ホルモンを検出する工程
を含む前記方法。 - 前記変動するエネルギー変異が発光若しくは蛍光である、請求項12に記載の方法。
- 節足動物の生体内における幼若ホルモンの動態をモニタリングする方法であって、
被験体の節足動物に請求項10に記載の幼若ホルモンセンサー発現ベクターを導入し、形質転換体を作製する工程、
前記形質転換体において幼若ホルモンセンサー発現ベクターから発現した幼若ホルモンセンサーに由来する発光若しくは蛍光共鳴エネルギー移動により変動するエネルギー変異又は発光若しくは蛍光タンパク質の再構築により発生する発光若しくは蛍光を測定する工程、及び
前記測定工程で測定された測定値に基づいて幼若ホルモンを検出する工程
を含む前記方法。 - 前記変動するエネルギー変異が発光若しくは蛍光である、請求項14に記載の方法。
- 節足動物の幼若ホルモンに構造的に類似する幼若ホルモン類似体の探索方法であって、 前記請求項1〜8のいずれか一項に記載の幼若ホルモンセンサーと候補物質とを混合する工程、
前記幼若ホルモンセンサーの共鳴エネルギー移動によるエネルギー変異又は発光若しくは蛍光タンパク質の再構築により発生する蛍光を測定する工程、及び
前記測定工程で得られた測定値に基づいて候補物質を幼若ホルモン類似体として選択する工程
を含む前記方法。 - 前記変動するエネルギー変異が発光若しくは蛍光である、請求項16に記載の方法。
- 前記選択工程が、前記混合工程において候補物質を混合しない陰性対照の測定値との有意差、又は候補物質の濃度依存的な測定値の増加に基づく、請求項16又は17に記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015040712A JP6535483B2 (ja) | 2015-03-02 | 2015-03-02 | 幼若ホルモンセンサー |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015040712A JP6535483B2 (ja) | 2015-03-02 | 2015-03-02 | 幼若ホルモンセンサー |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016161420A JP2016161420A (ja) | 2016-09-05 |
| JP6535483B2 true JP6535483B2 (ja) | 2019-06-26 |
Family
ID=56844749
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015040712A Active JP6535483B2 (ja) | 2015-03-02 | 2015-03-02 | 幼若ホルモンセンサー |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6535483B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11360104B2 (en) | 2017-12-04 | 2022-06-14 | Trustees Of Boston University | Microbial-based biosensors |
| JP7142351B2 (ja) * | 2018-09-26 | 2022-09-27 | 国立研究開発法人農業・食品産業技術総合研究機構 | チョウ目昆虫の幼虫における脱皮個体判別方法 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003025220A2 (en) * | 2001-09-18 | 2003-03-27 | Carnegie Institution Of Washington | Fusion proteins useful for detecting analytes |
| US8178654B2 (en) * | 2006-05-23 | 2012-05-15 | Stanford University | Estrogen receptor intramolecular folding systems, estrogen receptor intramolecular folding sensors, methods of use thereof, methods of detecting ER ligands, and methods of detecting ER agonists and antagonists |
-
2015
- 2015-03-02 JP JP2015040712A patent/JP6535483B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2016161420A (ja) | 2016-09-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Kim et al. | Superluminescent variants of marine luciferases for bioassays | |
| Fukuda et al. | Folding of green fluorescent protein and the cycle3 mutant | |
| US9945860B2 (en) | Nicotinamide adenine dinucleotide indicators, methods of preparation and application thereof | |
| US20170247769A1 (en) | Biosensors and methods of use | |
| JP4505439B2 (ja) | 糖濃度に対するシグナル強度の向上した蛍光標識蛋白質及びその用途 | |
| US20240027344A1 (en) | Fluorescent Probe for Branched Chain Amino Acids and Use Thereof | |
| JP2010517543A (ja) | 分泌型MLuc7ルシフェラーゼおよびその使用 | |
| JP7278634B2 (ja) | pH応答性のタンパク質分解プローブ | |
| JP6535483B2 (ja) | 幼若ホルモンセンサー | |
| EP3037534B1 (en) | Polypeptide exhibiting fluorescent properties, and utilization of same | |
| JP5793921B2 (ja) | 低カルシウム感受性発光蛋白質の変異アポ蛋白質 | |
| WO2015106067A2 (en) | Lucigen yellow (lucy), a yellow fluorescent protein | |
| KR20070029630A (ko) | 단리된 광단백질 엠티클리틴 및 그의 용도 | |
| JP5283105B2 (ja) | 高いエネルギー移動効率を有するbret発現系 | |
| CA3062431A1 (en) | Genetically encoded potassium ion indicators | |
| KR20220023985A (ko) | 효율적인 피피알 단백질의 작제방법 및 그의 이용 | |
| US10787650B2 (en) | Artificial bioluminescent enzymes | |
| Nagamine et al. | Electrochemical screening of recombinant protein solubility in Escherichia coli using scanning electrochemical microscopy (SECM) | |
| US10907134B2 (en) | Mutated genes for the catalytic protein of oplophorus luciferase and use thereof | |
| JPWO2004022600A1 (ja) | 分泌型又は膜結合型キメラ蛋白質 | |
| Krauspe et al. | Discovery of a novel small protein factor involved in the coordinated degradation of phycobilisomes in cyanobacteria | |
| Zhang et al. | Identification of the structural determinants for efficient glucose transport via segment swapping between two fungal glucose transporters | |
| JP6441534B2 (ja) | 発光酵素タンパク質 | |
| KR20080021018A (ko) | 단리된 광단백질 aq디케이 및 그의 용도 | |
| KR20110026965A (ko) | 리포터로 사용 가능한 베타 클루코시다아제와 이를 인디케이터로 이용한 클로닝 벡터의 제조방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20160824 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20180215 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20180215 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20180215 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20180817 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180925 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181122 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20190508 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190603 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6535483 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |