JP6252949B2 - 統合失調症マーカーセット及びその利用 - Google Patents
統合失調症マーカーセット及びその利用 Download PDFInfo
- Publication number
- JP6252949B2 JP6252949B2 JP2014542025A JP2014542025A JP6252949B2 JP 6252949 B2 JP6252949 B2 JP 6252949B2 JP 2014542025 A JP2014542025 A JP 2014542025A JP 2014542025 A JP2014542025 A JP 2014542025A JP 6252949 B2 JP6252949 B2 JP 6252949B2
- Authority
- JP
- Japan
- Prior art keywords
- schizophrenia
- protein
- gart
- combination
- biomarker
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 201000000980 schizophrenia Diseases 0.000 title claims description 115
- 239000003550 marker Substances 0.000 title claims description 25
- 108010064209 Phosphoribosylglycinamide formyltransferase Proteins 0.000 claims description 79
- 108090000623 proteins and genes Proteins 0.000 claims description 73
- 102100031802 Interferon-induced GTP-binding protein Mx1 Human genes 0.000 claims description 68
- 102000004169 proteins and genes Human genes 0.000 claims description 68
- 238000000034 method Methods 0.000 claims description 56
- 102100026482 Tubulin-folding cofactor B Human genes 0.000 claims description 40
- 238000001514 detection method Methods 0.000 claims description 20
- 238000012360 testing method Methods 0.000 claims description 19
- 239000003153 chemical reaction reagent Substances 0.000 claims description 16
- 210000004027 cell Anatomy 0.000 claims description 13
- 102100039654 Phosphoribosylglycinamide formyltransferase Human genes 0.000 claims description 12
- 102000017278 Glutaredoxin Human genes 0.000 claims description 9
- 108050005205 Glutaredoxin Proteins 0.000 claims description 9
- 102000015437 Uroporphyrinogen decarboxylase Human genes 0.000 claims description 9
- 108010064762 Uroporphyrinogen decarboxylase Proteins 0.000 claims description 9
- 101710202180 Interferon-induced GTP-binding protein Mx1 Proteins 0.000 claims description 7
- 210000004369 blood Anatomy 0.000 claims description 7
- 239000008280 blood Substances 0.000 claims description 7
- 210000004698 lymphocyte Anatomy 0.000 claims description 7
- 102000030782 GTP binding Human genes 0.000 claims description 6
- 108091000058 GTP-Binding Proteins 0.000 claims description 6
- 210000002966 serum Anatomy 0.000 claims description 6
- 102000029749 Microtubule Human genes 0.000 claims description 5
- 108091022875 Microtubule Proteins 0.000 claims description 5
- 101710087831 Tubulin-folding cofactor B Proteins 0.000 claims description 5
- 101710194664 Tubulin-specific chaperone B Proteins 0.000 claims description 5
- 210000000601 blood cell Anatomy 0.000 claims description 5
- 210000004688 microtubule Anatomy 0.000 claims description 5
- 210000002381 plasma Anatomy 0.000 claims description 5
- 102000014150 Interferons Human genes 0.000 claims description 4
- 108010050904 Interferons Proteins 0.000 claims description 4
- 229940079322 interferon Drugs 0.000 claims description 4
- 210000002200 mouth mucosa Anatomy 0.000 claims description 3
- 210000002850 nasal mucosa Anatomy 0.000 claims description 3
- 210000003491 skin Anatomy 0.000 claims description 3
- KDCGOANMDULRCW-UHFFFAOYSA-N 7H-purine Chemical compound N1=CNC2=NC=NC2=C1 KDCGOANMDULRCW-UHFFFAOYSA-N 0.000 claims 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 claims 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 claims 1
- 239000000090 biomarker Substances 0.000 description 82
- 102000019448 GART Human genes 0.000 description 67
- 101001128393 Homo sapiens Interferon-induced GTP-binding protein Mx1 Proteins 0.000 description 48
- 101000910482 Homo sapiens Uroporphyrinogen decarboxylase Proteins 0.000 description 48
- 102100024118 Uroporphyrinogen decarboxylase Human genes 0.000 description 48
- 102100036424 Glutaredoxin-3 Human genes 0.000 description 44
- 101001071851 Homo sapiens Glutaredoxin-3 Proteins 0.000 description 44
- 102100039560 Microtubule-associated protein RP/EB family member 1 Human genes 0.000 description 36
- 101000835634 Homo sapiens Tubulin-folding cofactor B Proteins 0.000 description 35
- 101000962664 Homo sapiens Microtubule-associated protein RP/EB family member 1 Proteins 0.000 description 34
- 102100028829 Heat shock 70 kDa protein 4L Human genes 0.000 description 31
- 101001078634 Homo sapiens Heat shock 70 kDa protein 4L Proteins 0.000 description 28
- 101100125778 Homo sapiens IGHM gene Proteins 0.000 description 21
- 102100039352 Immunoglobulin heavy constant mu Human genes 0.000 description 21
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 18
- 201000010099 disease Diseases 0.000 description 17
- 238000010998 test method Methods 0.000 description 17
- 238000010200 validation analysis Methods 0.000 description 17
- 239000000126 substance Substances 0.000 description 12
- 238000012795 verification Methods 0.000 description 12
- 239000000427 antigen Substances 0.000 description 11
- 108091007433 antigens Proteins 0.000 description 11
- 102000036639 antigens Human genes 0.000 description 11
- 238000012216 screening Methods 0.000 description 11
- 238000011161 development Methods 0.000 description 10
- 239000000523 sample Substances 0.000 description 9
- 238000003745 diagnosis Methods 0.000 description 8
- 230000009870 specific binding Effects 0.000 description 8
- 238000013179 statistical model Methods 0.000 description 8
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- 229940088598 enzyme Drugs 0.000 description 6
- 230000001900 immune effect Effects 0.000 description 6
- 238000007619 statistical method Methods 0.000 description 6
- 230000027455 binding Effects 0.000 description 5
- 238000011156 evaluation Methods 0.000 description 5
- 238000007689 inspection Methods 0.000 description 5
- 230000000698 schizophrenic effect Effects 0.000 description 5
- 208000024891 symptom Diseases 0.000 description 5
- 238000001262 western blot Methods 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 210000004556 brain Anatomy 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 230000003053 immunization Effects 0.000 description 4
- 238000002649 immunization Methods 0.000 description 4
- 230000006872 improvement Effects 0.000 description 4
- 238000002372 labelling Methods 0.000 description 4
- 206010003445 Ascites Diseases 0.000 description 3
- 102000014914 Carrier Proteins Human genes 0.000 description 3
- 108010078791 Carrier Proteins Proteins 0.000 description 3
- 101710093355 Heat shock 70 kDa protein 4L Proteins 0.000 description 3
- 108060003951 Immunoglobulin Proteins 0.000 description 3
- 241000283973 Oryctolagus cuniculus Species 0.000 description 3
- 238000000692 Student's t-test Methods 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 230000002596 correlated effect Effects 0.000 description 3
- 230000000875 corresponding effect Effects 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 238000002405 diagnostic procedure Methods 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 210000004408 hybridoma Anatomy 0.000 description 3
- 102000018358 immunoglobulin Human genes 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 230000008506 pathogenesis Effects 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 230000035945 sensitivity Effects 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- OBYNJKLOYWCXEP-UHFFFAOYSA-N 2-[3-(dimethylamino)-6-dimethylazaniumylidenexanthen-9-yl]-4-isothiocyanatobenzoate Chemical compound C=12C=CC(=[N+](C)C)C=C2OC2=CC(N(C)C)=CC=C2C=1C1=CC(N=C=S)=CC=C1C([O-])=O OBYNJKLOYWCXEP-UHFFFAOYSA-N 0.000 description 2
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 2
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 2
- 101710099411 Microtubule-associated protein RP/EB family member 1 Proteins 0.000 description 2
- 108010058846 Ovalbumin Proteins 0.000 description 2
- 208000028017 Psychotic disease Diseases 0.000 description 2
- 102000004243 Tubulin Human genes 0.000 description 2
- 108090000704 Tubulin Proteins 0.000 description 2
- 238000001042 affinity chromatography Methods 0.000 description 2
- 238000013103 analytical ultracentrifugation Methods 0.000 description 2
- 210000000628 antibody-producing cell Anatomy 0.000 description 2
- 102000005936 beta-Galactosidase Human genes 0.000 description 2
- 108010005774 beta-Galactosidase Proteins 0.000 description 2
- 238000010876 biochemical test Methods 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 238000010195 expression analysis Methods 0.000 description 2
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 238000003018 immunoassay Methods 0.000 description 2
- 108010045069 keyhole-limpet hemocyanin Proteins 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 238000000691 measurement method Methods 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 238000000491 multivariate analysis Methods 0.000 description 2
- 229940092253 ovalbumin Drugs 0.000 description 2
- 238000002823 phage display Methods 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 208000020016 psychiatric disease Diseases 0.000 description 2
- 238000003127 radioimmunoassay Methods 0.000 description 2
- 238000002702 ribosome display Methods 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 230000002123 temporal effect Effects 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- HUDPLKWXRLNSPC-UHFFFAOYSA-N 4-aminophthalhydrazide Chemical compound O=C1NNC(=O)C=2C1=CC(N)=CC=2 HUDPLKWXRLNSPC-UHFFFAOYSA-N 0.000 description 1
- 102100031126 6-phosphogluconolactonase Human genes 0.000 description 1
- 108010029731 6-phosphogluconolactonase Proteins 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 208000028698 Cognitive impairment Diseases 0.000 description 1
- 235000005956 Cosmos caudatus Nutrition 0.000 description 1
- 206010012239 Delusion Diseases 0.000 description 1
- 229910052693 Europium Inorganic materials 0.000 description 1
- 206010070246 Executive dysfunction Diseases 0.000 description 1
- 108010015776 Glucose oxidase Proteins 0.000 description 1
- 239000004366 Glucose oxidase Substances 0.000 description 1
- 108010018962 Glucosephosphate Dehydrogenase Proteins 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 108010027992 HSP70 Heat-Shock Proteins Proteins 0.000 description 1
- 102000018932 HSP70 Heat-Shock Proteins Human genes 0.000 description 1
- 208000004547 Hallucinations Diseases 0.000 description 1
- 101000617823 Homo sapiens Solute carrier organic anion transporter family member 6A1 Proteins 0.000 description 1
- 241000701044 Human gammaherpesvirus 4 Species 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 101710175625 Maltose/maltodextrin-binding periplasmic protein Proteins 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 108010079855 Peptide Aptamers Proteins 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 206010035226 Plasma cell myeloma Diseases 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 210000001744 T-lymphocyte Anatomy 0.000 description 1
- 101710120037 Toxin CcdB Proteins 0.000 description 1
- 210000000683 abdominal cavity Anatomy 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- DZBUGLKDJFMEHC-UHFFFAOYSA-N acridine Chemical class C1=CC=CC2=CC3=CC=CC=C3N=C21 DZBUGLKDJFMEHC-UHFFFAOYSA-N 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- 230000004520 agglutination Effects 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 1
- 235000011130 ammonium sulphate Nutrition 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000007321 biological mechanism Effects 0.000 description 1
- 239000012472 biological sample Substances 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 239000005515 coenzyme Substances 0.000 description 1
- 208000010877 cognitive disease Diseases 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000012937 correction Methods 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000002790 cross-validation Methods 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 231100000868 delusion Toxicity 0.000 description 1
- 230000001066 destructive effect Effects 0.000 description 1
- 125000000664 diazo group Chemical group [N-]=[N+]=[*] 0.000 description 1
- 238000002349 difference gel electrophoresis Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 230000008451 emotion Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- OGPBJKLSAFTDLK-UHFFFAOYSA-N europium atom Chemical compound [Eu] OGPBJKLSAFTDLK-UHFFFAOYSA-N 0.000 description 1
- 238000005194 fractionation Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000001641 gel filtration chromatography Methods 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 238000012252 genetic analysis Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229940116332 glucose oxidase Drugs 0.000 description 1
- 235000019420 glucose oxidase Nutrition 0.000 description 1
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 1
- 230000036039 immunity Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 238000004255 ion exchange chromatography Methods 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- HWYHZTIRURJOHG-UHFFFAOYSA-N luminol Chemical compound O=C1NNC(=O)C2=C1C(N)=CC=C2 HWYHZTIRURJOHG-UHFFFAOYSA-N 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 230000003340 mental effect Effects 0.000 description 1
- 108010029942 microperoxidase Proteins 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 230000009456 molecular mechanism Effects 0.000 description 1
- 201000000050 myeloid neoplasm Diseases 0.000 description 1
- 238000002610 neuroimaging Methods 0.000 description 1
- 230000036963 noncompetitive effect Effects 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 108091008104 nucleic acid aptamers Proteins 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 230000008520 organization Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000007310 pathophysiology Effects 0.000 description 1
- 210000005259 peripheral blood Anatomy 0.000 description 1
- 239000011886 peripheral blood Substances 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 238000001050 pharmacotherapy Methods 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- 229920005668 polycarbonate resin Polymers 0.000 description 1
- 239000004431 polycarbonate resin Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920005990 polystyrene resin Polymers 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 230000002250 progressing effect Effects 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 238000003498 protein array Methods 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000012857 radioactive material Substances 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000010187 selection method Methods 0.000 description 1
- 238000011896 sensitive detection Methods 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 238000000551 statistical hypothesis test Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 230000003936 working memory Effects 0.000 description 1
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
- G01N33/6896—Neurological disorders, e.g. Alzheimer's disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/30—Psychoses; Psychiatry
- G01N2800/302—Schizophrenia
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/50—Determining the risk of developing a disease
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/60—Complex ways of combining multiple protein biomarkers for diagnosis
Landscapes
- Life Sciences & Earth Sciences (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Chemical & Material Sciences (AREA)
- Urology & Nephrology (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Analytical Chemistry (AREA)
- Biotechnology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Pathology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Description
[1]三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、インターフェロン誘導GTP結合タンパク質Mx1、グルタレドキシン-3、微小管関連タンパク質RP/EBファミリー・メンバー1、チューブリン・フォールディング・コファクターB、免疫グロブリンmu鎖C領域及び熱ショック70kDaタンパク質4Lからなる群より選択される、2個以上のタンパク質分子の組合せからなる、統合失調症マーカーセット。
[2]三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、インターフェロン誘導GTP結合タンパク質Mx1及びグルタレドキシン-3を少なくとも含む、[1]に記載の統合失調症マーカーセット。
[3]微小管関連タンパク質RP/EBファミリー・メンバー1及び/又はチューブリン・フォールディング・コファクターBを更に含む、[2]に記載の統合失調症マーカーセット。
[4]三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、インターフェロン誘導GTP結合タンパク質Mx1、グルタレドキシン-3、微小管関連タンパク質RP/EBファミリー・メンバー1及びチューブリン・フォールディング・コファクターBの組合せからなる、[1]に記載の統合失調症マーカーセット。
[5]三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、インターフェロン誘導GTP結合タンパク質Mx1及びグルタレドキシン-3の組合せからなる、[1]に記載の統合失調症マーカーセット。
[6]三官能基プリン生合成タンパク質アデノシン-3及びインターフェロン誘導GTP結合タンパク質Mx1を少なくとも含む、[1]に記載の統合失調症マーカーセット。
[7]三官能基プリン生合成タンパク質アデノシン-3及びインターフェロン誘導GTP結合タンパク質Mx1の組合せからなる、[1]に記載の統合失調症マーカーセット。
[8]三官能基プリン生合成タンパク質アデノシン-3、インターフェロン誘導GTP結合タンパク質Mx1及び熱ショック70kDaタンパク質4Lからなる群より選択される1個以上のタンパク分子を含む、[1]に記載の統合失調症マーカーセット。
[9][1]〜[8]のいずれか一項に記載の統合失調症マーカーセットの検体中レベルを指標とした統合失調症検査法。
[10]以下のステップ(1)〜(3)を含む、[9]に記載の統合失調症検査法:
(1)被検者由来の検体を用意するステップ;
(2)前記検体中の、前記マーカーセットを構成する各タンパク質分子を検出するステップ;及び
(3)検出結果に基づいて、統合失調症の現在又は将来の発症可能性を判定するステップ。
[11]三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、グルタレドキシン-3、微小管関連タンパク質RP/EBファミリー・メンバー1、チューブリン・フォールディング・コファクターB及び熱ショック70kDaタンパク質4Lについては、検出値が低いことが統合失調症の発症可能性が高いことを示し、
インターフェロン誘導GTP結合タンパク質Mx1及び免疫グロブリンmu鎖C領域については、検出値が高いことが統合失調症の発症可能性が高いことを示す、[10]に記載の統合失調症検査法。
[12]ロジスティックモデルを用いてステップ(3)の判定を行う、[10]又は[11]に記載の統合失調症検査法。
[13]前記検体が血液、血漿、血清、口腔粘膜、鼻粘膜、皮膚、血液細胞、又は被検者から採取した血液リンパ球を不死化したリンパ球芽様細胞である、[9]〜[12]のいずれか一項に記載の統合失調症検査法。
[14][1]に記載の統合失調症マーカーセットを構成する各タンパク質分子を検出するための試薬と、取り扱い説明と、を含む、統合失調症検査キット。
[15]前記試薬が、各々、その標的であるタンパク質分子に対する抗体からなる、[14]に記載の統合失調症検査キット。
本発明の第1の局面は、統合失調症に特異的なタンパク質分子(バイオマーカー)の組合せである統合失調症マーカーセット(以下、「本発明のバイオマーカーセット」とも呼ぶ)に関する。本発明のバイオマーカーセットは統合失調症の現在又は将来の発症可能性を判定・評価する上で有用である。「現在の発症可能性」は、検査時において統合失調症を罹患ないし発症しているか否か(統合失調症であるか否か)又は罹患ないし発症している確率を表すことになる。他方、「将来の発症可能性」は統合失調症を将来発症する可能性(リスク)を表す。「統合失調症」とは精神機能の分裂を基本とする精神疾患群の総称である。世界保健機構(WHO)の疾病及び関連保健問題の国際統計分類(ICD)によれば妄想型、破瓜型、緊張型、鑑別不能型、統合失調症後抑うつ、残遺型、単純型に分類されている。
三官能基プリン生合成タンパク質アデノシン-3(以下、「GART」と称する。配列番号1);
ウロポルフィリノーゲン脱炭酸酵素(以下、「UROD」と称する。配列番号2);
インターフェロン誘導GTP結合タンパク質Mx1(以下、「MX1」と称する。配列番号3);
グルタレドキシン-3(以下、「GLRX3」と称する。配列番号4);
微小管関連タンパク質RP/EBファミリー・メンバー1(以下、「MAPRE1」と称する。配列番号5);
チューブリン・フォールディング・コファクターB(以下、「TBCB」と称する。配列番号6);
免疫グロブリンmu鎖C領域(以下、「IGHM」と称する。配列番号7);
熱ショック70kDaタンパク質4L(以下、「HSPA4L」と称する。配列番号8)
GART、UROD、MX1、GLRX3、MAPRE1、TBCBの組合せ
GART、UROD、MX1、GLRX3、MAPRE1、TBCB、IGHMの組合せ
GART、UROD、MX1、GLRX3、MAPRE1、TBCB、HSPA4Lの組合せ
GART、UROD、GLRX3、MAPRE1、TBCBの組合せ
GART、UROD、MX1、GLRX3、MAPRE1、TBCB、IGHM、HSPA4Lの組合せ
GART、UROD、MX1、MAPRE1、TBCBの組合せ
GART、UROD、MX1、GLRX3、TBCB、IGHMの組合せ
GART、UROD、MX1、GLRX3、MAPRE1、HSPA4Lの組合せ
GART、UROD、MX1、MAPRE1、TBCB、HSPA4Lの組合せ
GART、UROD、GLRX3、MAPRE1、TBCB、HSPA4Lの組合せ
GART、UROD、MX1、GLRX3、MAPRE1、IGHM、HSPA4Lの組合せ
GART、MX1、GLRX3、MAPRE1、TBCB、IGHM、HSPA4Lの組合せ
GART、UROD、MX1、GLRX3、TBCB、HSPA4Lの組合せ
GART、UROD、GLRX3、MAPRE1、TBCBの組合せ
GART、UROD、MX1、GLRX3の組合せ
GART、UROD、MX1、GLRX3、TBCB、IGHM、HSPA4Lの組合せ
GART、UROD、MX1、MAPRE1、IGHMの組合せ
GART、UROD、MX1、MAPRE1、TBCB、IGHMの組合せ
GART、UROD、MX1、GLRX3、MAPRE1、IGHMの組合せ
GART、UROD、GLRX3、MAPRE1、TBCB、IGHM、HSPA4Lの組合せ
GART、UROD、MX1、GLRX3、TBCB、HSPA4Lの組合せ
GART、UROD、MX1、MAPRE1、TBCB、IGHMの組合せ
GART、UROD、MX1、GLRX3、HSPA4Lの組合せの組合せ
GART、MX1、GLRX3、MAPRE1、IGHM、HSPA4Lの組合せ
GART、UROD、MX1、GLRX3、IGHM、HSPA4Lの組合せ
GART、UROD、MX1、GLRX3、IGHMの組合せ
GART、MX1、GLRX3、MAPRE1、TBCB、IGHM、HSPA4Lの組合せ
GART、UROD、MX1、GLRX3、MAPRE1、IGHMの組合せ
GART、UROD、MX1、TBCB、IGHMの組合せ
GART、UROD、MX1、TBCB、IGHM、HSPA4Lの組合せ
本発明の第2の局面は上記本発明のバイオマーカーセットの用途に関し、統合失調症の現在又は将来の発症可能性を検査する方法(以下、「本発明の検査法」とも呼ぶ)を提供する。本発明の検査法は、統合失調症を罹患ないし発症しているか否かを判定するための手段として、或いは統合失調症を将来発症する可能性を判定するための手段として有用である。本発明の検査法は統合失調症を診断するために有用な情報を与える。本発明の検査法によれば統合失調症の発症可能性を簡便且つ客観的に判定することが可能となる。
(1)被検者由来の検体を用意するステップ
(2)前記検体中の、マーカーセット(即ち、GART、UROD、MX1、GLRX3、MAPRE1、TBCB、IGHM、HSPA4Lからなる群より選択される、2個以上(好ましくは3個以上、更に好ましくは4個以上)のタンパク質分子の組合せ)を構成する各タンパク質分子を検出するステップ
(3)検出結果に基づいて、統合失調症の現在又は将来の発症可能性を判定するステップ
以下のロジスティックモデルにおいて、pを算出する。具体的には、各タンパク質分子のレベル(検出値)を以下の式に代入し、統合失調症の発症可能性(統合失調症有病確率)を求める。
(a)バイオマーカーセットに含まれるバイオマーカーの全てに関して陽性(カットオフ値以上)である場合を陽性(例えば発症可能性50%以上)と判定し、それ以外の場合を陰性(例えば発症可能性50%未満)と判定する。
(b)バイオマーカーセットに含まれるバイオマーカーの一つでも陽性(カットオフ値以上)の場合を陽性(例えば発症可能性50%以上)と判定し、それ以外の場合を陰性(例えば発症可能性50%未満)と判定する。
本発明はさらに、統合失調症の発症可能性を検査するためのキットも提供する。本発明のキットは、統合失調症マーカーセットを構成する各タンパク質分子を検出するための試薬を含む。バイオマーカー(タンパク質分子)毎に試薬が用意される。各試薬は、対応するバイオマーカーに特異的結合性を示す物質(以下、「結合分子」と呼ぶ)からなる。例えば、GART用の試薬であれば、GARTに特異的結合性を示す物質を試薬として用いる。結合分子の例として、バイオマーカーを特異的に認識する抗体、核酸アプタマー及びペプチドアプタマーを挙げることができる。結合分子は、採用するバイオマーカーに対する特異的結合性を有する限り、その種類や由来などは特に限定されない。また、抗体の場合、ポリクローナル抗体、オリゴクローナル抗体(数種〜数十種の抗体の混合物)、及びモノクローナル抗体のいずれでもよい。ポリクローナル抗体又はオリゴクローナル抗体としては、動物免疫して得た抗血清由来のIgG画分のほか、抗原によるアフィニティー精製抗体を使用できる。抗バイオマーカー抗体が、Fab、Fab'、F(ab')2、scFv、dsFv抗体などの抗体断片であってもよい。
(1)方法
統合失調症患者30名(男性15名:43.7±12.6歳、女性15名:43.1±8.9歳)と健常者30名(男性15名:44.4±12.9歳、女性15名:43.2±9.6歳)を対象として、同定された22種類のタンパク質について、ウエスタンブロット法により発現量の再確認を行った。
22種類のタンパク質中、発現量の有意な差異(Student’s t-test, p < 0.05)を認めたタンパク質は8種類であった。統合失調症患者群において発現上昇を認めたタンパク質が2個(MX1、IGHM)、発現低下を認めたタンパク質が6個(MAPRE1、TBCB、GLRX3、UROD、HSPA4L、GART)であった(図1)。
統合失調症患者群と健常者群のタンパク発現量の平均値の差を、統計的仮説検定を用いて比較した結果、有意な差異を認めたタンパク質は8種類であった(Student's t-test, p < 0.05)(上記結果に同じ)。この8種の中から、統合失調症患者群と健常者群の判別に有用なタンパク質を同定し、高精度で疾患を判別できる統計モデル(ロジスティックモデル)を作製した。ロジスティックモデルは、下式(式(1))で表される二値応答(ここでは、統合失調症患者者と健常者)を判別するための統計モデルである。
255のタンパク質の組合せについて、バイアス補正型area under the curve (AUC)、leave one out cross validation (LOOCV)に基づく予測誤差をそれぞれ算出した。補正型AUCが1.0に近い程、LOOCVに基づく予測誤差が小さい程、その組合せの判別精度が高いことを意味する。なお、両指標とも統計学の教科書及び論文で推奨されている評価指標である。図2は、補正型AUCが大きい上位30のタンパク質の組合せを示している。図2の表からは、GART、UROD、MX1、GLRX3、MAPRE1、TBCBを用いたモデル(以下、判別モデル1)の判別精度が最も高いことが分かる(補正型AUC:0.877、予測誤差:0.164)。判別モデル1のロジスティックモデルは、以下のとおり(式(2))である。
統計学には、オッカムの剃刀(Occam's razor)という考え方がある。これは、「ある事象を同様に説明できるのであれば、仮定の数は少ないほうが良い」という考え方である。具体的には、統計モデルを用いて、従属変数(統合失調症の有無)を複数の説明変数(タンパク質)の測定データで説明する場合、統計モデルに含める説明変数の数を増やし、モデルを複雑にすればするほど、「その測定データ」に対する適合度は良くなる。しかし、この統計モデルは「その測定データ(過去のデータ)」に過剰に適合してしまい、新たに測定したデータに対する適合が悪くなる。すなわち、統計モデルが既存のデータに過剰適合(Overfitting)してしまう。この問題を回避するためにも、統計モデルに含める説明変数は少ないほうが良い。この考え方に基づけば、判別精度が同程度であれば、判別に用いるタンパク質の数は少ない方が良いことになる。図2の表からは、GART、UROD、MX1、GLRX3を用いたモデル(以下、判別モデル2)がこの考えに適したモデルであることが分かる(補正型AUC:0.860、予測誤差:0.178)。判別モデル2のロジスティックモデル(式(3))は、以下のとおりである。
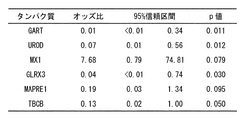
判別モデル1及び2に含まれるタンパク質のオッズ比をそれぞれ図3及び図4に示した。両モデルに含まれるタンパク質が統合失調症有病確率に与える影響は統計学的に有意(p < 0.05)又は限界的有意(p < 0.10)であり、判別に適したタンパク質であることが示唆されている。また、ステップワイズ変数選択法という統計手法を用いて、判別に適したタンパク質の組合せを選定した。その結果、GART、UROD、MX1、GLRX3が選択され、判別モデル2の有用性が異なる統計手法からも支持された。さらに、図2の表からは、GART、UROD、MX1、GLRX3、MAPRE1、TBCB、IGHM、HSPA4Lの順でモデルに含まれている回数が多いことが分かる。
・判別モデル1及び2の統合失調症判別精度は、統計学的にはほぼ同じである。
・統合失調症の判別には、図2の殆どのモデルに含まれていたGART、UROD、MX1、GLRX3が特に重要である。
・判別モデル1に含まれるMARPRE1とTBCBも判別における有用性が高い。
判別モデル1又は2を用いて、統合失調症であるか否かを判定する場合、統合失調症有病確率(式(2)又は(3)におけるp)を算出することになる。例えば、判別モデル1を用いる場合、患者のGART、UROD、MX1、GLRX3、MAPRE1、TBCBを測定し、その値を式(2)に代入して、統合失調症有病確率を求める。
選択された8種類のバイオマーカーの有効性を別の臨床検体を用いて検証した。ウエスタンブロットによる検証の結果を図5、6に示す。MX1、GART及びHSPA4Lについて、スクリーニングデータ(上記1.で使用した30検体のデータ)とバリデーションデータ(別の30検体のデータ)が同方向への変化(統計的有意性あり)を示し、再現性が認められた。
・MX1及びGARTの再現性はよく、優れたバイオマーカーである。
・HSPA4Lも比較的再現性がよく、利用価値が高い。
・MX1及びGARTの二つで判別すると最も精度の高い結果が得られる。
Claims (9)
- 三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、インターフェロン誘導GTP結合タンパク質Mx1、グルタレドキシン-3、微小管関連タンパク質RP/EBファミリー・メンバー1及びチューブリン・フォールディング・コファクターBの組合せからなる、統合失調症マーカーセット。
- 三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、インターフェロン誘導GTP結合タンパク質Mx1及びグルタレドキシン-3の組合せからなる、統合失調症マーカーセット。
- 三官能基プリン生合成タンパク質アデノシン-3及びインターフェロン誘導GTP結合タンパク質Mx1の組合せからなる、統合失調症マーカーセット。
- 統合失調症を検出するために、請求項1〜3のいずれか一項に記載の統合失調症マーカーセットの検体中レベルを測定する方法。
- 以下のステップ(1)及び(2)を含む、請求項4に記載の方法:
(1)被検者由来の検体を用意するステップ;
(2)前記検体中の、前記マーカーセットを構成する各タンパク質分子を検出するステップ。 - 三官能基プリン生合成タンパク質アデノシン-3、ウロポルフィリノーゲン脱炭酸酵素、グルタレドキシン-3、微小管関連タンパク質RP/EBファミリー・メンバー1、及びチューブリン・フォールディング・コファクターBについては、検出値が低いことが統合失調症の発症可能性が高いことを示し、
インターフェロン誘導GTP結合タンパク質Mx1については、検出値が高いことが統合失調症の発症可能性が高いことを示す、請求項5に記載の方法。 - 前記検体が血液、血漿、血清、口腔粘膜、鼻粘膜、皮膚、血液細胞、又は被検者から採取した血液リンパ球を不死化したリンパ球芽様細胞である、請求項5又は6に記載の方法。
- 請求項1〜3のいずれか一項に記載の統合失調症マーカーセットを構成する各タンパク質分子を検出するための試薬と、取り扱い説明と、を含む、統合失調症検査キット。
- 前記試薬が、各々、その標的であるタンパク質分子に対する抗体からなる、請求項8に記載の統合失調症検査キット。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012228417 | 2012-10-15 | ||
| JP2012228417 | 2012-10-15 | ||
| PCT/JP2013/076918 WO2014061456A1 (ja) | 2012-10-15 | 2013-10-03 | 統合失調症マーカーセット及びその利用 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2014061456A1 JPWO2014061456A1 (ja) | 2016-09-05 |
| JP6252949B2 true JP6252949B2 (ja) | 2017-12-27 |
Family
ID=50488027
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2014542025A Expired - Fee Related JP6252949B2 (ja) | 2012-10-15 | 2013-10-03 | 統合失調症マーカーセット及びその利用 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20150260729A1 (ja) |
| EP (1) | EP2908134A4 (ja) |
| JP (1) | JP6252949B2 (ja) |
| CN (1) | CN104704365B (ja) |
| WO (1) | WO2014061456A1 (ja) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2018028538A (ja) * | 2016-08-12 | 2018-02-22 | 公立大学法人名古屋市立大学 | 統合失調症とその関連疾患の診断用マーカー及びその使用 |
| JP6466548B1 (ja) * | 2017-11-27 | 2019-02-06 | 由紀子 濱崎 | 子供の精神病リスク早期スクリーニングシステム |
| CN110618276A (zh) * | 2019-06-21 | 2019-12-27 | 厦门大学 | 用于检测睡眠剥夺引发型干眼的分子标记物组及其应用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1565753A2 (en) * | 2002-11-21 | 2005-08-24 | The University Of Leicester | Bodily fluid markers of tissue hypoxia |
| AU2006290222A1 (en) * | 2005-09-14 | 2007-03-22 | The Regents Of The University Of California | Salivary protein and RNA for breast cancer detection |
| CA2713156A1 (en) * | 2008-02-04 | 2009-08-13 | Bipar Sciences, Inc. | Methods of diagnosing and treating parp-mediated diseases |
| EP2542696B1 (en) * | 2010-03-01 | 2016-09-28 | Caris Life Sciences Switzerland Holdings GmbH | Biomarkers for theranostics |
| JP5641471B2 (ja) * | 2010-06-29 | 2014-12-17 | 国立大学法人名古屋大学 | 統合失調症マーカー及びその利用 |
| GB201018056D0 (en) * | 2010-10-26 | 2010-12-08 | Cambridge Entpr Ltd | Biomarkers |
-
2013
- 2013-10-03 US US14/434,207 patent/US20150260729A1/en not_active Abandoned
- 2013-10-03 CN CN201380053407.4A patent/CN104704365B/zh not_active Expired - Fee Related
- 2013-10-03 WO PCT/JP2013/076918 patent/WO2014061456A1/ja active Application Filing
- 2013-10-03 EP EP13846893.9A patent/EP2908134A4/en not_active Withdrawn
- 2013-10-03 JP JP2014542025A patent/JP6252949B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| CN104704365A (zh) | 2015-06-10 |
| JPWO2014061456A1 (ja) | 2016-09-05 |
| US20150260729A1 (en) | 2015-09-17 |
| CN104704365B (zh) | 2016-07-27 |
| EP2908134A1 (en) | 2015-08-19 |
| WO2014061456A1 (ja) | 2014-04-24 |
| EP2908134A4 (en) | 2016-06-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI788704B (zh) | 分析個體樣品之方法 | |
| CN105164536B (zh) | 阿尔兹海默症诊断的组合物和方法 | |
| JP7457337B2 (ja) | アルツハイマー病バイオマーカー | |
| US20120178637A1 (en) | Biomarkers and methods for detecting alzheimer's disease | |
| CN107709991B (zh) | 用于诊断眼表炎症和干眼病的方法和装置 | |
| WO2012033999A2 (en) | Biomarkers for predicting kidney and glomerular pathologies | |
| JP6252949B2 (ja) | 統合失調症マーカーセット及びその利用 | |
| JP5924502B2 (ja) | リンパ球性漏斗下垂体後葉炎のバイオマーカー及びその用途 | |
| JP5641471B2 (ja) | 統合失調症マーカー及びその利用 | |
| CN113358881B (zh) | 用于nmosd预测或复发监测的生物标志物及其应用 | |
| KR101788404B1 (ko) | 활동성 루푸스신염 검출용 바이오마커 및 그 용도 | |
| US20150323529A1 (en) | Marker sequences for neuromyelitis optica (nmo) and use thereof | |
| KR102254053B1 (ko) | 인지기능 정상군 또는 경도 인지장애에서 아밀로이드 베타의 뇌 침착 검출용 혈액 바이오 마커 | |
| JP5653725B2 (ja) | 筋萎縮性側索硬化症マーカー及びその利用 | |
| JP5787895B2 (ja) | 筋萎縮性側索硬化症マーカー及びその利用 | |
| JP6618107B2 (ja) | リンパ球性漏斗下垂体後葉炎検査試薬及びその用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20160922 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170704 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170811 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20171107 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20171117 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6252949 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| S533 | Written request for registration of change of name |
Free format text: JAPANESE INTERMEDIATE CODE: R313533 |
|
| R350 | Written notification of registration of transfer |
Free format text: JAPANESE INTERMEDIATE CODE: R350 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |