JP5967092B2 - 光学異方体の波長分散調整方法及び重合性組成物 - Google Patents
光学異方体の波長分散調整方法及び重合性組成物 Download PDFInfo
- Publication number
- JP5967092B2 JP5967092B2 JP2013526802A JP2013526802A JP5967092B2 JP 5967092 B2 JP5967092 B2 JP 5967092B2 JP 2013526802 A JP2013526802 A JP 2013526802A JP 2013526802 A JP2013526802 A JP 2013526802A JP 5967092 B2 JP5967092 B2 JP 5967092B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- ring group
- carbon atoms
- ring
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B5/00—Optical elements other than lenses
- G02B5/30—Polarising elements
- G02B5/3083—Birefringent or phase retarding elements
Description
位相差板としては、方解石、雲母、水晶などの無機材料から構成される薄板や、固有複屈折性の高い高分子の延伸フィルムなどが知られている。これら位相差板の種類には、直線偏光を円偏光に変換する1/4波長板や直線偏光の偏光振動面を90度変換する1/2波長板等がある。
しかし、従来の位相差板は、ある特定の単色光に対しては正確に光線波長の1/4λあるいは1/2λの位相差に変換可能であるが、可視光域の光線が混在する合成波である白色光に対しては、各波長ごとでの偏光状態に分布が生じることから、全ての波長領域において正確な1/4λあるいは1/2λの位相差に調整することが困難であるという問題があった。その結果、位相差板を通過して出力される偏光は有色の偏光に変換されてしまう場合があった。これは、位相差板を構成する材料が、位相差について波長分散性を有することに起因する。
薄層化に対しては、フィルム基材に低分子重合性化合物を含有する液晶組成物を塗布することにより位相差板を作成する方法が最も有効な方法の一つである。
そこで、逆波長分散性を有する低分子重合性化合物あるいはそれを用いた液晶組成物の開発が行われている(特許文献1〜18)。
このような逆波長分散を有するフィルムは、タッチパネルや有機電界発光素子の反射防止や液晶ディスプレイの位相差フィルムとして好適に用いることができる。
反射防止用途では、広い波長域において正確に一様の偏光変換を実現するためにフィルムの波長分散を調整することが求められている。また、液晶ディスプレイの位相差フィルムにおいては、パネルを構成する部材の組み合わせにより、フィルムに求められる最適な波長分散が異なってくる。
そこで、フィルムの波長分散を調整する方法が種々検討されている(例えば、特許文献19〜23)。
(1)下記式(I)で表される重合性化合物(I)と、他の重合性化合物とを含有する重合性組成物を用いて光学異方体を製造するにあたり、前記重合性組成物における、前記重合性化合物(I)と他の重合性化合物との配合割合を調整することにより、所望の波長分散特性を有する光学異方体を得る、光学異方体の波長分散調整方法。
G1、G2はそれぞれ独立して、置換基を有していてもよい炭素数1〜20の2価の脂肪族基を表す〔該脂肪族基には、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR2−C(=O)−、−C(=O)−NR2−、−NR2−、又は、−C(=O)−が介在していてもよい。ただし、−O−又は−S−がそれぞれ2以上隣接して介在する場合を除く。ここで、R2は、水素原子又は炭素数1〜6のアルキル基を表す。〕。
Z1、Z2はそれぞれ独立して、ハロゲン原子で置換されていてもよい炭素数2〜10のアルケニル基を表す。
Axは芳香族炭化水素環及び芳香族複素環からなる群から選ばれる少なくとも一つの芳香環を有する、炭素数2〜30の有機基を表し、Ayは水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は、芳香族炭化水素環及び芳香族複素環からなる群から選ばれる少なくとも一つの芳香環を有する、炭素数2〜30の有機基を表す。前記Ax及びAyが有する芳香環は置換基を有していてもよい。また、前記AxとAyは一緒になって、環を形成していてもよい。
A1は、置換基を有していてもよい三価の芳香族基を表す。
A2、A3はそれぞれ独立して、置換基を有していてもよい炭素数4〜30の二価の芳香族基を表す。
Q1は、水素原子、又は、置換基を有していてもよい炭素数1〜6のアルキル基を表す。〕
(3)前記重合性化合物(I)が、前記式(I)中、A1が、置換基を有していてもよい、三価のベンゼン環基又は三価のナフタレン環基であり、A2、A3が、それぞれ独立して、置換基を有していてもよい、フェニレン基又はナフチレン基の化合物である、(1)又は(2)に記載の光学異方体の波長分散調整方法。
(4)前記重合性化合物(I)が、前記式(I)中、Y1〜Y6が、それぞれ独立して、化学的な単結合、−O−、−O−C(=O)−、−C(=O)−O−、又は、−O−C(=O)−O−の化合物である、(1)〜(3)のいずれかに記載の光学異方体の波長分散調整方法。
(6)前記重合性化合物(I)が、前記式(I)中、G1、G2がそれぞれ独立して、置換基を有していてもよい炭素数1〜12の2価の脂肪族基〔該脂肪族基には、−O−、−O−C(=O)−、−C(=O)−O−又は−C(=O)−が介在していてもよい。ただし、−O−が2以上隣接して介在する場合を除く。〕の化合物である、(1)〜(5)のいずれかに記載の光学異方体の波長分散調整方法。
(7)前記重合性化合物(I)が、前記式(I)中、G1、G2がそれぞれ独立して、炭素数1〜12の2価のアルキレン基の化合物である、(1)〜(5)のいずれかに記載の光学異方体の波長分散調整方法。
G11、G12はそれぞれ独立して、置換基を有していてもよい炭素数1〜20の2価の脂肪族基を表す〔該脂肪族基には、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR12−C(=O)−、−C(=O)−NR12−、−NR12−、又は、−C(=O)−が介在していてもよい。ただし、−O−又は−S−がそれぞれ2以上隣接して介在する場合を除く。ここで、R12は、水素原子又は炭素数1〜6のアルキル基を表す。〕。
Z11、Z12はそれぞれ独立して、ハロゲン原子で置換されていてもよい炭素数2〜10のアルケニル基を表す。
Aaは芳香族炭化水素環及び芳香族複素環からなる群から選ばれる少なくとも一つの芳香環を有する、炭素数2〜30の有機基を表し、Abは水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は、芳香族炭化水素環及び芳香族複素環からなる群から選ばれる少なくとも一つの芳香環を有する、炭素数2〜30の有機基を表す。前記Aa及びAbが有する芳香環は置換基を有していてもよい。また、前記AaとAbは一緒になって、環を形成していてもよい。
A11は、置換基を有していてもよい三価の芳香族基を表す。
A12、A13はそれぞれ独立して、置換基を有していてもよい炭素数4〜30の二価の芳香族基を表す。
Q11は、水素原子、又は、置換基を有していてもよい炭素数1〜6のアルキル基を表す。〕
本発明の重合性組成物は、本発明の波長分散調整方法に用いるこができ、特に逆波長分散調整方法に好適に用いることができる。
本発明の波長分散調整方法によって、広い波長域において一様の偏光変換が可能な、性能面で満足のいく光学フィルムを簡便に形成することができる。その具体的な実用例としては、偏光板と組み合わせることで反射防止フィルムを作製することができ、産業上例えばタッチパネルや有機電界発光素子の反射防止に好適に使用することができる。
1)光学異方体の波長分散調整方法
本発明は、前記式(I)で表される重合性化合物(I)〔以下、「重合性化合物(I)」という。〕と他の重合性化合物とを含有する重合性組成物を用いて光学異方体を製造するにあたり、前記重合性組成物における、重合性化合物(I)と他の重合性化合物との配合割合を調整することにより、所望の波長分散特性を有する光学異方体を得る、光学異方体の波長分散調整方法である。
ここで、「波長分散特性」とは、光学異方体における位相差の光線波長の依存特性をいう。
「正の波長分散性」とは、(波長450nmにおける位相差)>(波長550nmにおける位相差)>(波長650nmにおける位相差)の関係を満たす波長分散特性を意味する。
また、「フラットな波長分散性」とは、(波長450nmにおける位相差)≒(波長550nmにおける位相差)≒(波長650nmにおける位相差)の関係を満たす波長分散特性を意味する。
図1中、横軸は測定波長(nm)、縦軸は測定波長における位相差(Re(nm))を示す。
図1に示すグラフについては、後述する実施例の項において詳細に説明する。
本発明に用いる重合性化合物(I)は、前記式(I)で表される化合物である。
前記式(I)中、Y1〜Y6はそれぞれ独立して、化学的な単結合、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR1−C(=O)−、−C(=O)−NR1−、−O−C(=O)−NR1−、−NR1−C(=O)−O−、−NR1−C(=O)−NR1−、−O−NR1−、又は、−NR1−O−を表す。
R1の炭素数1〜6のアルキル基としては、メチル基、エチル基、n−プロピル基、イソプロピル基、n−ブチル基、sec−ブチル基、t−ブチル基、n−ペンチル基、n−へキシル基等が挙げられる。
炭素数1〜20の2価の脂肪族基としては、鎖状構造を有する炭素数1〜20の2価の脂肪族基;脂環式構造を有する炭素数3〜20の2価の脂肪族基;及び、鎖状構造を有する炭素数1〜20の2価の脂肪族基と、脂環式構造を有する炭素数3〜20の2価の脂肪族基の組合せ;等が挙げられる。
炭素数7〜20の2価の脂環式縮合環基としては、ビシクロ[2.2.1]ヘプタンジイル基、アダマンタンジイル基、デカリンジイル基等が挙げられる。
これらの中では、−O−、−O−C(=O)−、−C(=O)−O−、又は、−C(=O)−が好ましい。
該アルケニル基の炭素数としては、2〜6が好ましい。Z1及びZ2のアルケニル基の置換基であるハロゲン原子としては、フッ素原子、塩素原子、臭素原子等が挙げられ、塩素原子が好ましい。
本発明において、「芳香環」は、Huckel則に従う広義の芳香族性を有する環状構造、すなわち、π電子を(4n+2)個有する環状共役構造、及びチオフェン、フラン等に代表される硫黄、酸素等のヘテロ原子の孤立電子対がπ電子系に関与して芳香族性を示すものを意味する。
なお、Axの炭素数2〜30の有機基の「炭素数」は、置換基の炭素原子を含まない有機基全体の総炭素数を意味する(後述するAyにて同じである。)。
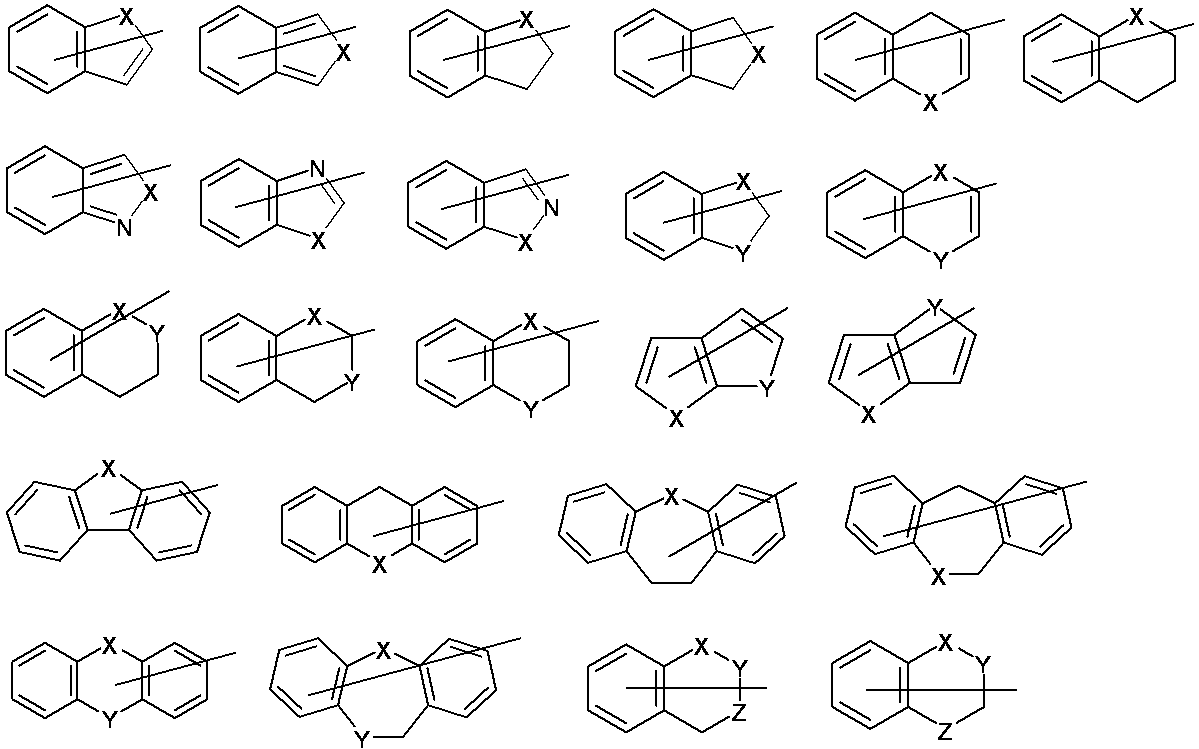
炭素数4〜30の不飽和複素環、炭素数6〜30の不飽和炭素環としては、特に制約はなく、芳香族性を有していても有していなくてもよい。例えば、下記に示す環が挙げられる。なお、下記に示す環は、式(I)中の
また、これらの環は置換基を有していてもよい。
置換基としては、ハロゲン原子、シアノ基、炭素数1〜6のアルキル基、炭素数1〜6のアルコキシ基、ニトロ基、−C(=O)−OR基、−SO2R基等が挙げられる。ここで、Rは前記と同じ意味を表す。
式中、X、Yは、前記と同じ意味を表す。前記Ayの置換基を有していてもよいアルキル基の置換基としては、シクロアルキル基;シアノ基;フッ素原子等のハロゲン原子;であるのが好ましい。
A2、A3の芳香族基は単環のものであっても、多環のものであってもよい。
A2、A3の具体例としては、下記のものが挙げられる。
置換基を有していてもよい炭素数1〜6のアルキルとしては、前記Axで例示したのと同様のものが挙げられる。
これらの中でも、Q1は、水素原子又は炭素数1〜6のアルキル基が好ましく、水素原子がより好ましい。
また、本発明においては、重合性化合物(I)としては、重合性化合物(I)のみで(他の重合性化合物を用いないで)光学異方体を製造した場合に、その光学異方体が逆波長分散特性を示すものを用いるのが好ましい。
重合性化合物(I)は、例えば、下記に示す反応により製造することができる。
すなわち、式(3)で表されるヒドラジン化合物(ヒドラジン化合物(3))を、式(4)で表されるカルボニル化合物(カルボニル化合物(4))と、〔ヒドラジン化合物(3):カルボニル化合物(4)〕のモル比で、1:2〜2:1、好ましくは1:1.5〜1.5:1の割合で反応させることにより、高選択的かつ高収率で目的とする本発明の式(I)で示される重合性化合物を製造することができる。
これらの中でも、アルコール系溶媒、エーテル系溶媒、及びアルコール系溶媒とエーテル系溶媒の混合溶媒が好ましい。
この反応に用いる溶媒としては、反応に不活性なものであれば特に限定されない。例えば、メチルアルコール、エチルアルコール、n−プロピルアルコール、イソプロピルアルコール、n−ブチルアルコール、イソブチルルコール、sec−ブチルアルコール、t−ブチルアルコール、n−ペンチルアルコール、アミルアルコール等のアルコール系溶媒;ジエチルエーテル、テトラヒドロフラン、1,2−ジメトキシエタン、1,4−ジオキサン、シクロペンチルメチルエーテル等のエーテル系溶媒;ベンゼン、トルエン、キシレン等の芳香族炭化水素系溶媒;n−ペンタン、n−ヘキサン、n−ヘプタン等の脂肪族炭化水素系溶媒;N,N−ジメチルホルムアミド、N−メチルピロリドン、ヘキサメチルリン酸トリアミド等のアミド系溶媒;ジメチルスルホキシド、スルホラン等の含硫黄系溶媒;及びこれらの2種以上からなる混合溶媒;等が挙げられる。
これらの中でも、アルコール系溶媒、エーテル系溶媒、及びアルコール系溶媒とエーテル系溶媒の混合溶媒が好ましい。
反応は、−10℃から用いる溶媒の沸点までの温度範囲で円滑に進行する。各反応の反応時間は、反応規模にもよるが、通常、数分から数時間である。
金属塩還元剤とは一般に低原子価金属を含む化合物、もしくは金属イオンとヒドリド源からなる化合物である(「有機合成実験法ハンドブック」1990年社団法人有機合成化学協会編 丸善株式会社発行810ページを参照)。
金属塩還元剤としては、例えば、NaAlHn(OR15)m、LiAlH4、iBu2AlH、LiBH4、NaBH4、SnCl2、CrCl2、TiCl3等が挙げられる。ここで、R15は炭素数1〜6のアルキル基を表し、nは1〜4の整数を表し、mはn+m=4を満たす整数を表す。
また、ジアゾニウム塩(5)は、アニリン等の化合物から常法により製造することができる。
(i)式:D1−hal(halはハロゲン原子を表す。以下にて同じ。)で表される化合物と、式:D2−OMet(Metはアルカリ金属(主にナトリウム)を表す。以下にて同じ。)で表される化合物とを混合して縮合させる(ウイリアムソン合成)。なお、式中、D1及びD2は任意の有機基を表す(以下にて同じ。)
(ii)式:D1−halで表される化合物と、式:D2−OHで表される化合物とを水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して縮合させる。
(iii)式:D1−J(Jはエポキシ基を表す。)で表される化合物と、式:D2−OHで表される化合物とを水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して縮合させる。
(iv)式:D1−OFN(OFNは不飽和結合を有する基を表す。)で表される化合物と、式:D2−OMetで表される化合物を、水酸化ナトリウム、水酸化カリウム等の塩基存在下、混合して付加反応させる。
(v)式:D1−halで表される化合物と、式:D2−OMetで表される化合物とを、銅あるいは塩化第一銅存在下、混合して縮合させる(ウルマン縮合)。
(vi)式:D1−COOHで表される化合物と、式:D2−OH又はD2−NH2で表される化合物とを、脱水縮合剤(N,N−ジシクロヘキシルカルボジイミド等)の存在下に脱水縮合させる。
(vii)式:D1−COOHで表される化合物にハロゲン化剤を作用させることにより、式:D1−CO−halで表される化合物を得、このものと式:D2−OH又はD2−NH2で表される化合物とを、塩基の存在下に反応させる。
(viii)式:D1−COOHで表される化合物に酸無水物を作用させることにより、混合酸無水物を得た後、このものに、式:D2−OH又はD2−NH2で表される化合物を反応させる。
(ix)式:D1−COOHで表される化合物と、式:D2−OH又はD2−NH2で表される化合物とを、酸触媒あるいは塩基触媒の存在下に脱水縮合させる。
脱水縮合剤の使用量は、化合物(7)1モルに対し、通常1〜3モルである。
用いる塩基としては、トリエチルアミン、ピリジン等の有機塩基;水酸化ナトリウム、炭酸ナトリウム、炭酸水素ナトリウム等の無機塩基が挙げられる。
塩基の使用量は、化合物(7)1モルに対し、通常1〜3モルである。
化合物(7)が、式(7)中、Lがメタンスルホニルオキシ基、又はp−トルエンスルホニルオキシ基の化合物(混合酸無水物)である場合もハロゲン原子の場合と同様である。
溶媒の使用量は、特に限定されず、用いる化合物の種類や反応規模等を考慮して適宜定めることができるが、ヒドロキシ化合物(6)1gに対し、通常1〜50gである。
目的とする化合物の構造は、NMRスペクトル、IRスペクトル、マススペクトル等の測定、元素分析等により、同定することができる。
本発明においては、重合性化合物(I)と共に、他の重合性化合物を用いる。他の重合性化合物は、一種単独で、或いは二種以上を組み合わせて用いることができる。
これらの中でも、本発明においては、重合性化合物(II)を用いるのが好ましい。
式(II)中、Y11〜Y16はそれぞれ独立して、前記Y1〜Y6と同様の、化学的な単結合、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR11−C(=O)−、−C(=O)−NR11−、−O−C(=O)−NR11−、−NR11−C(=O)−O−、−NR11−C(=O)−NR11−、−O−NR11−、又は、−NR11−O−を表す。ここで、R11は、前記R1と同様の、水素原子又は炭素数1〜6のアルキル基を表す。
Aaは、前記Axと同様の、芳香族炭化水素環及び芳香族複素環からなる群から選ばれる少なくとも一つの芳香環を有する、炭素数2〜30の有機基を表し、Abは、前記Ayと同様の、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は、芳香族炭化水素環及び芳香族複素環からなる群から選ばれる少なくとも一つの芳香環を有する、炭素数2〜30の有機基を表す。前記Aa及びAbが有する芳香環は置換基を有していてもよい。
ここで、「芳香環」は、Huckel則に従う広義の芳香族性を有する環状構造、すなわち、π電子を(4n+2)個有する環状共役構造及びチオフェン、フラン等に代表される硫黄、酸素等のヘテロ原子の孤立電子対がπ電子系に関与して芳香族性を示すものを意味する。
なお、Aaの炭素数2〜30の有機基の「炭素数」は、置換基の炭素原子を含まない有機基全体の総炭素数を意味する(後述するAbにて同じである。)。
炭素数4〜30の不飽和複素環、炭素数6〜30の不飽和炭素環としては、特に制約はなく、芳香族性を有していても有していなくてもよい。なかでも、下記に示す環が好ましい。なお、式中には、便宜上、環と窒素原子を結ぶ二重結合を示している(以下にて同じ)。
また、これらの環は置換基を有していてもよい。
置換基としては、ハロゲン原子、シアノ基、炭素数1〜6のアルキル基、炭素数1〜6のアルコキシ基、ニトロ基、−C(=O)−OR基、−SO2R基等が挙げられる。ここで、Rは前記と同じ意味を表す。
これらの中でも、AaとAbが一緒になって形成する環としては、下記に示すものが特に好ましい。
AaとAbが一緒になって下記に示す環を形成しているものがより好ましい。
A11は、前記A1と同様の、置換基を有していてもよい三価の芳香族基を表す。
A12、A13はそれぞれ独立して、前記A2、A3と同様の、置換基を有していてもよい炭素数4〜30の二価の芳香族基を表す。
Q11は、前記Q1と同様の、水素原子、又は、置換基を有していてもよい炭素数1〜6のアルキル基を表す。
重合性化合物(II)は、例えば、下記に示す製造方法1、2により製造することができる。
反応は、前記ヒドラゾン化合物(3)とカルボニル化合物(4)との反応と同様にして行うことができる。
前記式(II)で示される本発明の重合性化合物のうち、前記式(II)中、式:Z12−Y16−G12−Y14−A13−Y12−で表される基が、式:Z11−Y15−G11−Y13−A12−Y11−で表される基と同一であり、Y11が、Y22−C(=O)−O−で表される基である化合物(II’)は、以下に示す、工程1、工程2により製造することができる。
用いる溶媒としては、前記重合性化合物(I)の製造方法において化合物(3)と化合物(4)の反応で用いることができるとして例示したのと同様のものが挙げられる。溶媒の使用量は、特に限定されず、用いる化合物の種類や反応規模等を考慮して適宜定めることができるが、ヒドラゾン化合物(13)1gに対し、通常1〜100gである。
なお、ヒドラゾン化合物(13)は、次のようにして製造することができる。
本発明に用いる重合性組成物は、前記重合性化合物(I)の少なくとも一種、前記他の重合性化合物の少なくとも一種を含有する。
本発明に用いる重合性組成物としては、前記重合性化合物(I)の少なくとも一種、前記重合性化合物(II)の少なくとも一種を含有するものが特に好ましい。
用いる重合開始剤としては、重合性化合物(I)及び他の重合性化合物が有する重合性基の種類に応じて適宜なものを選択して使用すればよい。例えば、重合性基がラジカル重合性であればラジカル重合開始剤を、アニオン重合性の基であればアニオン重合開始剤を、カチオン重合性の基であればカチオン重合開始剤を、それぞれ使用すればよい。ラジカル重合開始剤としては、熱ラジカル発生剤と光ラジカル発生剤のいずれも使用可能であるが、光ラジカル発生剤を使用するのが好適である。
「水素供与体」とは、露光によりビイミダゾール系化合物から発生したラジカルに対して、水素原子を供与することができる化合物を意味する。水素供与体としては、下記で定義するメルカプタン系化合物、アミン系化合物等が好ましい。
アミン系化合物としては、4,4’−ビス(ジメチルアミノ)ベンゾフェノン、4,4’−ビス(ジエチルアミノ)ベンゾフェノン、4−ジエチルアミノアセトフェノン、4−ジメチルアミノプロピオフェノン、エチル−4−ジメチルアミノベンゾエート、4−ジメチルアミノ安息香酸、4−ジメチルアミノベンゾニトリル等を挙げることができる。
これらの重合開始剤は一種単独で、又は二種以上を組み合わせて用いることができる。
本発明の重合性組成物において、重合開始剤の配合割合は、重合性化合物100重量部(重合性化合物(I)及び他の重合性化合物との合計が100重量部、以下同じ)に対し、通常、0.1〜30重量部、好ましくは0.5〜10重量部である。
光学異方体は、前記重合性組成物を重合して得られる高分子からなる成形体である。
ここで、「重合」とは、通常の重合反応のほか、架橋反応を含む広い意味での化学反応を意味するものとする。
フィルム状又はシート状の光学異方体は、(A)適当な有機溶媒中で、前記重合性組成物の重合反応を行った後、目的とする高分子を単離し、得られる高分子を適当な有機溶媒に溶解して溶液を調製し、この溶液を適当な基板上に塗工して得られた塗膜を乾燥後、所望により加熱することにより得る方法、(B)前記重合性組成物を所望により適当な有機溶媒で希釈した溶液を、公知の塗工法により基板上に塗布した後、脱溶媒し、次いで加熱又は活性エネルギー線を照射することにより重合反応を行う方法等により好適に製造することができる。
また、用いる基板は、単層のものであっても、積層体であってもよい。
基板としては、有機材料が好ましく、この有機材料をフィルムとした樹脂フィルムが更に好ましい。
配向膜は、例えば、ポリイミド、ポリビニルアルコール、ポリエステル、ポリアリレート、ポリアミドイミド、ポリエーテルイミド等のポリマーを含有するものである。配向膜は、このようなポリマーを含有する溶液(配向膜用組成物)を基板上に膜状に塗布し、乾燥し、そして一方向にラビング処理等することで、得ることができる。
配向膜の厚さは0.001〜5μmであることが好ましく、0.001〜1μmであることがさらに好ましい。
また、ラビング処理する方法以外に、配向膜の表面に偏光紫外線を照射する方法によっても、配向膜にコレステリック規則性を持つコレステリック液晶層を面内で一方向に配向規制する機能を持たせることができる。
本発明にかかる光学異方体としては、位相差板、液晶表示素子用配向膜、偏光板、視野角拡大板、カラーフィルター、ローパスフィルター、光偏光プリズム、各種光フィルター等が挙げられる。
目的物の構造は1H−NMRで同定した。
温度計を備えた4つ口反応器に、窒素気流中、先のステップ1で合成した中間体A 10.5g(15.3mmol)、2−ヒドラジノベンゾチアゾール3.0g(18.3mmol)、及びテトラヒドロフラン(THF)80mlを加えた。さらに、(±)−10−カンファースルホン酸 18mg(0.08mmol)を加え、全容を25℃にて3時間撹拌した。反応終了後、反応液を10%重曹水800mlに投入し、酢酸エチル100mlで2回抽出した。酢酸エチル層を集め、無水硫酸ナトリウムで乾燥し、硫酸ナトリウムをろ別した。ろ液からロータリーエバポレーターにて酢酸エチルを減圧留去して、淡黄色固体を得た。この淡黄色固体をシリカゲルカラムクロマトグラフィー(トルエン:酢酸エチル=8:2(体積比))により精製し、淡黄色固体として化合物1を8.0g得た(収率:62.7%)。
目的物の構造は1H−NMR、マススペクトルで同定した。
LCMS(APCI):calcd for C46H47N3O10S:833[M+];Found:833
温度計を備えた4つ口反応器に、窒素気流中、化合物1合成におけるステップ1で合成した中間体A 3.0g(4.37mmol)、先のステップ1で合成した中間体B 1.0g(5.24mmol)、THF30ml、及びエタノール15mlを加えた。さらに、(±)−10−カンファースルホン酸0.1g(0.44mmol)をTHF3mlに溶解させた溶液をゆっくりと加え、全容を25℃にて2時間攪拌した。反応終了後、反応液を飽和重曹水200mlに投入し、酢酸エチル100mlで2回抽出した。得られた酢酸エチル層を飽和食塩水200mlで洗浄した後、無水硫酸ナトリウムで乾燥し、硫酸ナトリウムをろ別した。ろ液からロータリーエバポレーターにて酢酸エチルを減圧留去して、黄色固体を得た。この黄色固体をシリカゲルカラムクロマトグラフィー(トルエン:酢酸エチル=95:5(体積比))により精製して、黄色固体として化合物2を2.2g得た(収率:58.6%)。
目的物の構造は1H−NMRで同定した。
(i)液晶組成物の調製
製造例1、2で得た化合物1及び化合物2を、下記表1に示す割合で合計1gとなるように混合した。混合物それぞれに、光重合開始剤(商品名:イルガキュアー907、BASF社製)を30mg、界面活性剤(商品名:KH−40、AGCセイミケミカル社製)の1%シクロペンタノン溶液100mgを2.3gのシクロペンタノンに溶解させた。この溶液を0.45μmの細孔径を有するディスポーサブルフィルターでろ過し、液晶組成物1〜3を得た。
厚み100μmの脂環式オレフィンポリマーからなるフィルム(商品名:ゼオノアフィルムZF16-100、日本ゼオン社製)の両面をコロナ放電処理した。5%のポリビニルアルコールの水溶液を当該フィルムの片面に♯2のワイヤーバーを使用して塗布し、塗膜を乾燥し、膜厚0.1μmの配向膜を形成した。次いで当該配向膜をラビング処理し、配向膜を有する透明樹脂基材を調製した。
前記液晶組成物1〜3を、♯4のワイヤーバーを使用して、(ii)で調製した配向膜を有する透明樹脂基材の、配向膜を有する面に塗布した。塗膜を110℃で30秒間乾燥し、下記表1に記載する膜厚の液晶層を形成した。その後、液晶層の塗布面側から2000mJ/cm2の紫外線を照射して波長分散測定用の試料(フィルム)とした。
(iii)で作製した液晶層を有するフィルムの400nmから800nm間の位相差(Re)をエリプソメーター(XLS−100型、J.A.Woollam社製)を用いて測定した。測定結果を、図1のグラフに示す。縦軸は位相差(Re(nm))を、横軸は波長(nm)を示す。
さらに、測定結果から、下記の計算式を用いてα、β値を算出した。算出結果を下記表1にまとめて示す。
(v)で測定した、波長548.5nmにおける位相差の値(Re)と液晶層の膜厚(d)から、下記式によりΔnを算出した。
実施例1〜3において、化合物1と2の混合物の代わりに、化合物1のみ(参考例1)、化合物2のみ(参考例2)を用いて、実施例1〜3と同様に、液晶組成物1r、2rを調製し、このものを用いて、液晶層を形成し、位相差の測定等を行った。測定結果等を、下記表1に、実施例1〜3の結果と併せて示す。
表1中、波長548.5nmにおける位相差の値(Re)と液晶層の膜厚(d)から算出したΔnを「Δn @550nm」と記載する。
また、Δnの値は、その割合によって化合物1単独の数値から、化合物2単独の数値まで徐々に大きくなっていることが確認できる。
本発明によれば、位相差の波長分散を高度に制御することができ、目的に合った、品質の高い光学異方体を提供することができる。
Claims (9)
- 下記式(I)で表される重合性化合物(I)と、他の重合性化合物とを含有する重合性組成物を用いて光学異方体を製造するに際し、前記重合性組成物における、前記重合性化合物(I)と他の重合性化合物との配合割合を調整することにより、所望の波長分散特性を有する光学異方体を得る、光学異方体の波長分散調整方法。
G1、G2はそれぞれ独立して、置換基を有していてもよい炭素数1〜20の2価の脂肪族基を表す〔該脂肪族基には、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR2−C(=O)−、−C(=O)−NR2−、−NR2−、又は、−C(=O)−が介在していてもよい。ただし、−O−又は−S−がそれぞれ2以上隣接して介在する場合を除く。ここで、R2は、水素原子又は炭素数1〜6のアルキル基を表す。〕。
Z1、Z2はそれぞれ独立して、ハロゲン原子で置換されていてもよい炭素数2〜10のアルケニル基を表す。
Axは、置換基を有していてもよい、ベンゼン環基、ナフタレン環基、アントラセン環基、フルオレン環基、ピロール環基、フラン環基、チオフェン環基、ピラゾール環基、イミダゾール環基、オキサゾール環基、チアゾール環基、ピリジン環基、ピリダジン環基、ピリミジン環基、ピラジン環基、ベンズイミダゾール環基、ベンゾチオフェン環基、ベンゾオキサゾール環基、ベンゾチアゾール環基、カルバゾール環基からなる群から選ばれる芳香環基であり、前記芳香環基が有する置換基は、ハロゲン原子、シアノ基、炭素数1〜6のアルキル基、炭素数2〜6のアルケニル基、炭素数1〜6のハロゲン化アルキル基、置換アミノ基、炭素数1〜6のアルコキシ基、ニトロ基、アリール基、−C(=O)−OR基又は−SO 2 R基である。ここで、Rは炭素数1〜6のアルキル基または炭素数6〜14のアリール基を表す。
Ayは、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は、置換基を有していてもよい、ベンゼン環基、ナフタレン環基、アントラセン環基、フルオレン環基、ピロール環基、フラン環基、チオフェン環基、ピラゾール環基、イミダゾール環基、オキサゾール環基、チアゾール環基、ピリジン環基、ピリダジン環基、ピリミジン環基、ピラジン環基、ベンズイミダゾール環基、ベンゾチオフェン環基、ベンゾオキサゾール環基、ベンゾチアゾール環基、カルバゾール環基からなる群から選ばれる芳香環基であり、前記芳香環基が有する置換基は、ハロゲン原子、シアノ基、炭素数1〜6のアルキル基、炭素数2〜6のアルケニル基、炭素数1〜6のハロゲン化アルキル基、置換アミノ基、炭素数1〜6のアルコキシ基、ニトロ基、アリール基、−C(=O)−OR基又は−SO 2 R基である。Rは前記と同じ意味を表す。
A1は、置換基を有していてもよい三価の芳香族基を表す。
A2、A3はそれぞれ独立して、置換基を有していてもよい炭素数4〜30の二価の芳香族基を表す。
Q1は、水素原子、又は、置換基を有していてもよい炭素数1〜6のアルキル基を表す。} - 前記重合性化合物(I)が、前記式(I)中、AxとAyに含まれるπ電子の総数が4以上24以下の化合物である、請求項1に記載の光学異方体の波長分散調整方法。
- 前記重合性化合物(I)が、前記式(I)中、A1が、置換基を有していてもよい、三価のベンゼン環基又は三価のナフタレン環基であり、A2、A3が、それぞれ独立して、置換基を有していてもよい、フェニレン基又はナフチレン基の化合物である、請求項1又は2に記載の光学異方体の波長分散調整方法。
- 前記重合性化合物(I)が、前記式(I)中、Y1〜Y6が、それぞれ独立して、化学的な単結合、−O−、−O−C(=O)−、−C(=O)−O−、又は、−O−C(=O)−O−の化合物である、請求項1〜3のいずれかに記載の光学異方体の波長分散調整方法。
- 前記重合性化合物(I)が、前記式(I)中、Z1、Z2が、それぞれ独立して、CH2=CH−、CH2=C(CH3)−、又は、CH2=C(Cl)−の化合物である、請求項1〜4のいずれかに記載の光学異方体の波長分散調整方法。
- 前記重合性化合物(I)が、前記式(I)中、G1、G2がそれぞれ独立して、置換基を有していてもよい炭素数1〜12の2価の脂肪族基〔該脂肪族基には、−O−、−O−C(=O)−、−C(=O)−O−又は−C(=O)−が介在していてもよい。ただし、−O−が2以上隣接して介在する場合を除く。〕の化合物である、請求項1〜5のいずれかに記載の光学異方体の波長分散調整方法。
- 前記重合性化合物(I)が、前記式(I)中、G1、G2がそれぞれ独立して、炭素数1〜12の2価のアルキレン基の化合物である、請求項1〜5のいずれかに記載の光学異方体の波長分散調整方法。
- 前記他の重合性化合物が、下記式(II)で表される重合性化合物(II)である、請求項1〜7のいずれかに記載の光学異方体の波長分散調整方法。
G11、G12はそれぞれ独立して、置換基を有していてもよい炭素数1〜20の2価の脂肪族基を表す〔該脂肪族基には、−O−、−S−、−O−C(=O)−、−C(=O)−O−、−O−C(=O)−O−、−NR12−C(=O)−、−C(=O)−NR12−、−NR12−、又は、−C(=O)−が介在していてもよい。ただし、−O−又は−S−がそれぞれ2以上隣接して介在する場合を除く。ここで、R12は、水素原子又は炭素数1〜6のアルキル基を表す。〕。
Z11、Z12はそれぞれ独立して、ハロゲン原子で置換されていてもよい炭素数2〜10のアルケニル基を表す。
Aaは、置換基を有していてもよい、ベンゼン環基、ナフタレン環基、アントラセン環基、フルオレン環基、ピロール環基、フラン環基、チオフェン環基、ピラゾール環基、イミダゾール環基、オキサゾール環基、チアゾール環基、ピリジン環基、ピリダジン環基、ピリミジン環基、ピラジン環基、ベンズイミダゾール環基、ベンゾチオフェン環基、ベンゾオキサゾール環基、ベンゾチアゾール環基、カルバゾール環基からなる群から選ばれる芳香環基であり、前記芳香環基が有する置換基は、ハロゲン原子、シアノ基、炭素数1〜6のアルキル基、炭素数2〜6のアルケニル基、炭素数1〜6のハロゲン化アルキル基、置換アミノ基、炭素数1〜6のアルコキシ基、ニトロ基、アリール基、−C(=O)−OR基又は−SO 2 R基である。ここで、Rは炭素数1〜6のアルキル基または炭素数6〜14のアリール基を表す。Abは、水素原子、置換基を有していてもよい炭素数1〜6のアルキル基、又は、置換基を有していてもよい、ベンゼン環基、ナフタレン環基、アントラセン環基、フルオレン環基、ピロール環基、フラン環基、チオフェン環基、ピラゾール環基、イミダゾール環基、オキサゾール環基、チアゾール環基、ピリジン環基、ピリダジン環基、ピリミジン環基、ピラジン環基、ベンズイミダゾール環基、ベンゾチオフェン環基、ベンゾオキサゾール環基、ベンゾチアゾール環基、カルバゾール環基からなる群から選ばれる芳香環基であり、前記芳香環基が有する置換基は、ハロゲン原子、シアノ基、炭素数1〜6のアルキル基、炭素数2〜6のアルケニル基、炭素数1〜6のハロゲン化アルキル基、置換アミノ基、炭素数1〜6のアルコキシ基、ニトロ基、アリール基、−C(=O)−OR基又は−SO 2 R基である。Rは前記と同じ意味を表す。
A11は、置換基を有していてもよい三価の芳香族基を表す。
A12、A13はそれぞれ独立して、置換基を有していてもよい炭素数4〜30の二価の芳香族基を表す。
Q11は、水素原子、又は、置換基を有していてもよい炭素数1〜6のアルキル基を表す。} - 請求項1に記載の重合性化合物(I)の少なくとも一種と、請求項8に記載の重合性化合物(II)の少なくとも一種とを含有することを特徴とする重合性組成物。
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011166929 | 2011-07-29 | ||
| JP2011166929 | 2011-07-29 | ||
| JP2011263047 | 2011-11-30 | ||
| JP2011263047 | 2011-11-30 | ||
| PCT/JP2012/067906 WO2013018526A1 (ja) | 2011-07-29 | 2012-07-13 | 光学異方体の波長分散調整方法及び重合性組成物 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2013018526A1 JPWO2013018526A1 (ja) | 2015-03-05 |
| JP5967092B2 true JP5967092B2 (ja) | 2016-08-10 |
Family
ID=47629057
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013526802A Active JP5967092B2 (ja) | 2011-07-29 | 2012-07-13 | 光学異方体の波長分散調整方法及び重合性組成物 |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JP5967092B2 (ja) |
| WO (1) | WO2013018526A1 (ja) |
Families Citing this family (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013146633A1 (ja) * | 2012-03-30 | 2013-10-03 | 日本ゼオン株式会社 | 位相差フィルム積層体およびその製造方法、ならびに液晶表示装置 |
| JP5880226B2 (ja) * | 2012-04-03 | 2016-03-08 | 日本ゼオン株式会社 | 重合性化合物の製造方法 |
| CN107253935B (zh) * | 2012-07-09 | 2020-10-09 | 日本瑞翁株式会社 | 肼化合物、聚合性化合物的制备方法及将肼化合物作为聚合性化合物的制造原料使用的方法 |
| CN104755512B (zh) * | 2012-10-19 | 2016-05-18 | 日本瑞翁株式会社 | 聚合性化合物、聚合性组合物、高分子以及光学各向异性体 |
| US9777096B2 (en) | 2012-10-23 | 2017-10-03 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optical anisotropic body |
| US10227292B2 (en) * | 2013-02-15 | 2019-03-12 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optically anisotropic body |
| TW201444798A (zh) | 2013-02-28 | 2014-12-01 | 必治妥美雅史谷比公司 | 作爲強效rock1及rock2抑制劑之苯基吡唑衍生物 |
| EP2961746B1 (en) | 2013-02-28 | 2018-01-03 | Bristol-Myers Squibb Company | Phenylpyrazole derivatives as potent rock1 and rock2 inhibitors |
| US10273322B2 (en) * | 2013-08-22 | 2019-04-30 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optical anisotropic body |
| JP6641683B2 (ja) * | 2013-10-28 | 2020-02-05 | 日本ゼオン株式会社 | 樹脂フィルム、λ/4板、円偏光板、有機エレクトロルミネッセンス表示装置、及び製造方法 |
| KR102315630B1 (ko) | 2013-10-31 | 2021-10-20 | 제온 코포레이션 | 중합성 화합물, 중합성 조성물, 고분자, 및 광학 이방체 |
| EP3106456B1 (en) | 2014-02-12 | 2018-10-24 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optical isomer |
| EP3106478B1 (en) | 2014-02-14 | 2019-12-25 | Zeon Corporation | Polymerizable compound, polymerizable composition, polymer, and optically anisotropic body |
| US20180016502A1 (en) * | 2015-01-16 | 2018-01-18 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| US11186669B2 (en) | 2015-01-16 | 2021-11-30 | Dic Corporation | Polymerizable composition and optically anisotropic body using same |
| CN107108775B (zh) | 2015-01-16 | 2019-12-13 | Dic株式会社 | 聚合性组合物和使用该聚合性组合物的光学各向异性体 |
| JP6669160B2 (ja) * | 2015-03-19 | 2020-03-18 | 日本ゼオン株式会社 | 液晶性組成物、位相差層の製造方法及び円偏光板 |
| KR20170139535A (ko) * | 2015-04-24 | 2017-12-19 | 니폰 제온 가부시키가이샤 | 복층 필름의 제조 방법 및 복층 필름 |
| WO2017038265A1 (ja) * | 2015-09-01 | 2017-03-09 | Dic株式会社 | 粉体混合物 |
| US10647920B2 (en) * | 2015-12-22 | 2020-05-12 | Zeon Corporation | Liquid crystalline composition, liquid crystal cured layer, method for producing same, and optical film |
| KR20180118133A (ko) * | 2016-03-08 | 2018-10-30 | 니폰 제온 가부시키가이샤 | 액정성 조성물, 액정 경화층 및 그 액정 경화층의 제조 방법 |
| JP6146526B1 (ja) * | 2016-10-06 | 2017-06-14 | 日本ゼオン株式会社 | 混合物、重合性組成物、高分子、光学フィルム、光学異方体、偏光板、フラットパネル表示装置、有機エレクトロルミネッセンス表示装置および反射防止フィルム、並びに重合性化合物の使用方法 |
| CN110431454B (zh) * | 2017-03-28 | 2021-07-16 | 日本瑞翁株式会社 | 相位差片、多层相位差片、偏振片、图像显示装置以及聚合性化合物 |
| WO2019044863A1 (ja) | 2017-08-30 | 2019-03-07 | 富士フイルム株式会社 | 硬化物、光学部材、レンズ、化合物、及び硬化性組成物 |
| WO2019131572A1 (ja) * | 2017-12-26 | 2019-07-04 | 富士フイルム株式会社 | レンズ用接着剤、接合レンズ、および撮像モジュール |
| WO2020009053A1 (ja) | 2018-07-02 | 2020-01-09 | 富士フイルム株式会社 | 硬化性組成物、硬化物、光学部材、レンズ、及び化合物 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006201502A (ja) * | 2005-01-20 | 2006-08-03 | Fuji Photo Film Co Ltd | 位相差フィルム、偏光板、および液晶表示装置 |
| JP2007052079A (ja) * | 2005-08-15 | 2007-03-01 | Kaneka Corp | 位相差フィルムの波長分散調整方法およびそれを用いたフィルムの製造方法 |
| JP5391682B2 (ja) * | 2007-12-28 | 2014-01-15 | 住友化学株式会社 | 化合物、光学フィルム及び光学フィルムの製造方法 |
| JP5396815B2 (ja) * | 2008-10-29 | 2014-01-22 | 日本ゼオン株式会社 | 重合性化合物、重合性液晶化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
| JP5624393B2 (ja) * | 2010-07-13 | 2014-11-12 | 住友化学株式会社 | 組成物及び光学フィルム |
| JP5621584B2 (ja) * | 2010-12-27 | 2014-11-12 | 日本ゼオン株式会社 | 重合性キラル化合物、重合性液晶組成物、液晶性高分子及び光学異方体 |
-
2012
- 2012-07-13 WO PCT/JP2012/067906 patent/WO2013018526A1/ja active Application Filing
- 2012-07-13 JP JP2013526802A patent/JP5967092B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2013018526A1 (ja) | 2015-03-05 |
| WO2013018526A1 (ja) | 2013-02-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5967092B2 (ja) | 光学異方体の波長分散調整方法及び重合性組成物 | |
| JP5892158B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6485354B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6206413B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP5994777B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6206481B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6183514B2 (ja) | 光学フィルム | |
| JP6206414B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6428637B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6575360B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP6015655B2 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 | |
| JP2018039811A (ja) | ヒドラジン化合物、光学異方体の製造方法、およびヒドラジン化合物の使用方法 | |
| JPWO2015122384A1 (ja) | 重合性化合物、重合性組成物、高分子、及び光学異方体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150303 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20151104 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151225 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160607 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160620 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5967092 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |