JP5904153B2 - 核酸増幅反応用試料の調製方法、核酸増幅方法、固相状核酸増幅反応用試薬及びマイクロチップ - Google Patents
核酸増幅反応用試料の調製方法、核酸増幅方法、固相状核酸増幅反応用試薬及びマイクロチップ Download PDFInfo
- Publication number
- JP5904153B2 JP5904153B2 JP2013075428A JP2013075428A JP5904153B2 JP 5904153 B2 JP5904153 B2 JP 5904153B2 JP 2013075428 A JP2013075428 A JP 2013075428A JP 2013075428 A JP2013075428 A JP 2013075428A JP 5904153 B2 JP5904153 B2 JP 5904153B2
- Authority
- JP
- Japan
- Prior art keywords
- nucleic acid
- acid amplification
- amplification reaction
- reagent
- solid phase
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6806—Preparing nucleic acids for analysis, e.g. for polymerase chain reaction [PCR] assay
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Analytical Chemistry (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biophysics (AREA)
- Immunology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
Description
核酸増幅反応用試料の調製方法を提供する。
前記溶解させる手順の前に、前記液体をイオン性界面活性剤を含む溶液で希釈する手順、を含んでいてもよい。
前記イオン性界面活性剤は、陰イオン性界面活性剤であってもよく、前記陰イオン性界面活性剤は、ドデシル硫酸ナトリウムとすることができる。
前記シクロデキストリンは、前記ドデシル硫酸ナトリウムの濃度の8倍以上の濃度で含まれていてもよい。
また、前記溶解させる手順の前に、前記液体の希釈液を超音波処理する手順を含むこともでき、前記溶解させる手順の前に、前記液体の希釈液を加熱する手順を含むこともできる。
前記核酸の増幅を等温で行ってもよい。また、前記核酸がリボ核酸であり、前記増幅する手順の前に前記リボ核酸を鋳型として逆転写反応を行う手順、を含んでいてもよい。
前記シクロデキストリンは、ヒドロキシプロピル基を有するものでもよい。
前記固相状核酸増幅反応用試薬は、鋳型核酸鎖とイオン性界面活性剤とを含む液体に混合されてもよい。
前記シクロデキストリンは、前記イオン性界面活性剤の濃度の8倍以上の濃度で含まれていてもよい。
また、前記固相状核酸増幅反応用試薬は、リボヌクレアーゼHを含有していてもよい。
前記固相状核酸増幅反応用試薬は、前記マイクロチップに配設された複数の核酸増幅反応の反応場の各々に備えられ、該反応場は、流路を介して前記マイクロチップ内へ液体を導入する導入部と連通していてもよい。
本技術に係る固相状核酸増幅反応用試薬(以下、単に「固相状試薬」とも称す)はDNAポリメラーゼとシクロデキストリンとバインダーとを少なくとも含有する。固相状試薬に含まれる各成分について順に説明する。
固相状試薬に含まれるDNAポリメラーゼは、核酸増幅反応において、鋳型核酸に対して相補的な核酸鎖を合成するための成分である。DNAポリメラーゼは、任意の核酸増幅法に合わせて適宜選択することができる。DNAポリメラーゼとしては、例えば、TaqDNAポリメラーゼ、Tth DNAポリメラーゼ、KODDNAポリメラーゼ、Pfu DNAポリメラーゼなどが挙げられる。また、鎖置換型DNAポリメラーゼなどであってもよい。
固相状試薬に含まれるシクロデキストリンは、固相状試薬に含まれるDNAポリメラーゼ等の酵素の活性低下を抑制するための成分である(実験例1参照)。固相状の試薬は、所定の成分に調製された後に乾燥、あるいは凍結乾燥させて作製される。このような製造工程やその後の乾燥状態によって、固相状試薬に含まれる酵素は失活するおそれがある。本技術に係る固相状試薬では、シクロデキストリンが含まれていることによって、酵素の活性低下を抑制することができる(実験例1参照)。
固相状試薬に含まれるバインダーは、固相状である試薬の形状の安定性を高めるための成分である。特に上記のHPβCDなど、吸湿性の高いシクロデキストリンが固相状試薬に含まれている場合には、固相状試薬の形状を保つことが困難となる。そこで、本技術に係る固相状試薬は、バインダーが添加されることによって、その形状が保持される。
本技術に係る固相状試薬には、リボヌクレアーゼH(RNaseH)を含有していてもよい。RNaseHはRNA/DNAハイブリッド鎖のRNA鎖を特異的に加水分解する酵素である。リボヌクレアーゼH(RNaseH)を含む固相状試薬は、逆転写反応を伴う核酸増幅反応に好適であり、等温核酸増幅法に好適である。逆転写反応を伴う核酸増幅反応は、逆転写反応と核酸増幅反応を連続して行うことで、これらの反応を2段階に分けた場合に比べ、迅速にRNAを検出できる手法である。
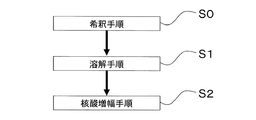
上述した固相状核酸増幅反応試薬は、本技術に係る核酸増幅反応用試料の調製方法(以下、単に「試料の調製方法」とも称す)に好適に用いられ得る。図1は、本技術に係る試料の調製方法を示すフローチャートである。試料の調製方法には、固相状の試薬(固相状核酸増幅反応用試薬)を、核酸を含む液体に溶解させる手順(溶解手順S1)を含む。また、試料の調製方法には、溶解させる手順(溶解手順S1)の前に、液体をイオン性界面活性剤を含む溶液で希釈する手順(希釈手順S0)を含んでいてもよい。さらに、本技術は、上記の手順に加え、核酸を増幅する手順(増幅手順S2)を含む核酸増幅方法とすることもできる。図1に示す各手順について説明する。
溶解手順S1では、核酸増幅反応において鋳型核酸となる核酸を含む液体に上述した固相状試薬を溶解させる。本技術に係る試料の調製方法において、核酸とは、動物由来、植物由来、菌類由来、細菌類由来、あるいはウイルス由来などの核酸である。核酸は、一本鎖、二本鎖の何れでもよく、DNA、RNAの何れでもよい。また、核酸の分子量についても特に限定されない。なお、試料に含まれる核酸は、細菌の細胞内に存在する細菌ゲノムなどのように、直接試料中に分散されず、細胞膜などの膜に囲まれた状態や粒子内に存在する状態であってもよい。
図1に示す希釈手順S0では、上記の核酸を含む液体をイオン性界面活性剤を含む溶液で希釈する。イオン性界面活性剤としては、ヘキサデシルトリメチルアンモニウムブロミド、ミリスチルトリメチルアンモニウムブロミド等の陽イオン性界面活性剤や、ドデシル硫酸ナトリウム(SDS)、デオキシコール酸ナトリウム等の陰イオン性界面活性剤が挙げられる。イオン性界面活性剤としては、陰イオン性界面活性剤が好ましく、SDSがより好ましい。
本手順S2では、上述した溶解手順S1によって固相状試薬が溶解された液体を用いて、液体に含まれる核酸を増幅する。本手順S2では、核酸増幅反応を行うために公知の核酸増幅法の中から適宜選択することができる。核酸増幅法としては、例えば、温度サイクルを実施するポリメラーゼ連鎖反応(PCR)法が挙げられる。また、温度サイクルを伴わない各種等温増幅法であってもよい。等温増幅法としては、例えば、LAMP(Loop-Mediated Isothermal Amplification)法やTRC(Transcription-Reverse transcription Concerted)法等が挙げられる。本技術に係る核酸増幅方法では、核酸の増幅を等温で行う等温増幅法が好ましく、等温増幅法としては、例えば、LAMP法が好ましい。
液体に含まれる核酸がリボ核酸(RNA)の場合には、増幅手順S2の前にリボ核酸を鋳型として逆転写反応を行う手順を含んでいてもよい。逆転写反応と核酸増幅反応は、各々を分けて行ってもよく、また、例えば、逆転写反応−ポリメラーゼ連鎖反応(RT−PCR)や、逆転写反応−LAMP(RT−LAMP)などのように、一つの反応場で連続的に行ってもよい。なお、2つの反応を連続的に行う場合には、固相状試薬には、DNAポリメラーゼに加えて、逆転写酵素が含まれていることが好ましい。
本技術に係る試料の調製方法では、溶解手順S1の前に、液体の希釈液を超音波処理する手順を含んでいてもよい。本手順は、本技術に係る試料の調製方法において必須ではない。しかし、例えば、鋳型となる核酸が、細菌のゲノムなどのように細胞の中に存在する場合には、超音波処理を行うことによって細胞膜を破砕し、核酸を希釈液中へ放出され易くすることができる。このため、細胞内に留まっている場合に比べ、核酸がプライマーや他の試薬の成分と接触しやすくなり、核酸増幅反応がより効率的となる。
本技術に係る試料の調製方法では、溶解手順S1の前に、液体の希釈液を加熱する手順を含んでいてもよい。本手順は、本技術に係る試料の調製方法において必須ではない。しかし、例えば、鋳型となる核酸が、細菌のゲノムなどのように細胞の中に存在する場合には、超音波処理と同様に、希釈液の加熱を行うことによって溶菌をすることができる。また、鋳型となる核酸がウイルスである場合にも、例えば、ウイルスがエンベロープを有している場合には、本手順によって、ウイルスゲノムとエンベローブとを分離させ、ウイルスゲノムを液体中に拡散させることができる。
上述した本技術に係る固相状試薬は、マイクロチップを用いた核酸増幅反応に好適である。図2に、本技術の第1実施形態に係るマイクロチップを示す。図2Aは、マイクロチップMの上面図であり、図2Bは図2AのP−P線の矢視断面図である。マイクロチップMは、3枚の基板層11,12,13から構成されている(図2B参照)。また、マイクロチップMには、複数の核酸増幅反応の反応場であるウェル21〜25が配設されている。なお、図2においては、一つの流路に連通する5つウェルを全て同じ符号で示す。
(1)DNAポリメラーゼとシクロデキストリンとバインダーとを少なくとも含有する固相状の試薬を、核酸を含む液体に溶解させる手順、を含む核酸増幅反応用試料の調製方法。
(2)前記溶解させる手順の前に、前記液体をイオン性界面活性剤を含む溶液で希釈する手順、を含む上記(1)記載の核酸増幅反応用試料の調製方法。
(3)前記イオン性界面活性剤は、陰イオン性界面活性剤である上記(2)記載の核酸増幅反応用試料の調製方法。
(4)前記陰イオン性界面活性剤は、ドデシル硫酸ナトリウムである上記(3)記載の核酸増幅反応用試料の調製方法。
(5)前記シクロデキストリンが、前記ドデシル硫酸ナトリウムの濃度の8倍以上の濃度で含まれている上記(4)記載の核酸増幅反応用試料の調製方法。
(6)前記溶解させる手順の前に、前記液体の希釈液を超音波処理する手順を含む上記(2)〜(5)の何れかに記載の核酸増幅反応用試料の調製方法。
(7)前記溶解させる手順の前に、前記液体の希釈液を加熱する手順を含む上記(2)〜(5)の何れかに記載の核酸増幅反応用試料の調製方法。
(8)DNAポリメラーゼとシクロデキストリンとバインダーとを少なくとも含有する固相状の試薬を、核酸を含む液体に溶解させる手順と、前記核酸を増幅する手順と、を含む核酸増幅方法。
(9)前記核酸の増幅を等温で行う上記(8)記載の核酸増幅方法。
(10)前記核酸がリボ核酸であり、前記増幅する手順の前に前記リボ核酸を鋳型として逆転写反応を行う手順、を含む上記(8)又は(9)記載の核酸増幅方法。
(11)DNAポリメラーゼとシクロデキストリンとバインダーとを少なくとも含有する固相状核酸増幅反応用試薬。
(12)前記シクロデキストリンは、ヒドロキシプロピル基を有する上記(11)記載の固相状核酸増幅反応用試薬。
(13)鋳型核酸鎖とイオン性界面活性剤とを含む液体に混合される上記(11)又は(12)記載の固相状核酸増幅反応用試薬。
(14)前記シクロデキストリンが、前記イオン性界面活性剤の濃度の8倍以上の濃度で含まれている上記(12)〜(13)の何れかに記載の固相状核酸増幅反応用試薬。
(15)リボヌクレアーゼHを含有する上記(11)〜(14)の何れかに記載の固相状核酸増幅反応用試薬。
(16)DNAポリメラーゼとシクロデキストリンとバインダーとを少なくとも含有する固相状核酸増幅反応用試薬が備えられたマイクロチップ。
(17)前記固相状核酸増幅反応用試薬は、前記マイクロチップに配設された複数の核酸増幅反応の反応場の各々に備えられ、該反応場は、流路を介して前記マイクロチップ内へ液体を導入する導入部と連通している上記(16)記載のマイクロチップ。
1.シクロデキストリンによる核酸増幅反応用試薬の活性の保持についての検証
シクロデキストリンのDNAポリメラーゼを含む核酸増幅反応用試薬への添加によって、核酸増幅反応用試薬の活性が保持されるか検証した。
本実験例で用いた固相状試薬の組成を表1に示す。シクロデキストリンとして、本実験例では、ヒドロキシプロピルシクロデキストリン(HPβCD)を用いた。また、バインダーとしては、スクロース、デキストラン、ポリエチレングリコール(PEG)、トレハロース、コラーゲンペプチド、ゼラチン、BSA、FICOLL、ポリビニルピロリドンうち、何れか1種類以上が溶解されたバインダー溶液を用いた。DNAポリメラーゼとしては、Bst DNA polymerase Lg Frag(NEW ENGLAND BIOLABS)を用いた。HPβCDとバインダー溶液とDNAポリメラーゼを含む試薬液を表1に示す所定の濃度となるように混合し、容器に分注して凍結乾燥させ、試験例1〜6の固相状の試薬を得た。また、HPβCDもバインダーも含まない試薬液も用意し、凍結乾燥させ、比較例1とした。さらにバインダーを含まず、HPβCDと試薬液とを混合させてものについても凍結乾燥させ、これを比較例2とした。
本実験例の結果を表1に示す。表1において、反応開始までの時間とは、核酸増幅反応が開始されるまでの時間であり、Tt値 (分)に相当し、蛍光物質の消光シグナルの変曲点に基づく。加熱を開始してから、LAMP法による核酸増幅反応が開始されたと判断した時間までに要した時間について、同じ組成からなる凍結乾燥されていない試薬を用いて核酸増幅反応を行ってた場合のTt値を基準として、その時間(Tt値)に対する増加を割合(%)で示す。また、固相状態とは、凍結乾燥後の試薬の状態を表す。「×」は、固相状態にならなかったことを表し、「△」は、固相状態となったことを表し、「○」は、固相状態が、長期間に渡って保たれていたことを表す。
2.SDSが添加された核酸増幅反応液におけるシクロデキストリンの効果についての検証
本実験例では、シクロデキストリンの添加によって、SDSの核酸増幅反応への影響が低減するか検証した。
本実験例で用いた試薬の組成を表2に示す。シクロデキストリンとして、本実験例では、ヒドロキシプロピルシクロデキストリン(HPβCD)を用いた。RT−LAMP反応試薬にSDSとシクロデキストリンが所定の濃度で添加されたものを試験例1〜3とした。また、比較例1としてRT−LAMP反応試薬のみのものを用意した。さらに、LAMP反応試薬にSDSを0.4%の濃度で含むものを比較例2とした。上記の比較例1〜2及び試験例1〜3と鋳型核酸とを混合し、LAMP法によって核酸増幅反応を行った。増幅核酸鎖の検出は、実験例1と同様にQプローブを用いて行った。
本実験例の結果を表2に示す。表2において、反応開始までの時間は、実験例1と同様である。表2に示すように、核酸増幅反応液にSDSが添加されると、核酸増幅反応が阻害されることが確認された(比較例2)。また、SDS濃度の5倍の濃度でHPβCDが添加されているでも、核酸増幅反応が阻害されることが確認された(試験例1)。一方、HPβCDがSDS濃度の10倍含まれる試験例2と、15倍含まれている試験例3では、核酸の増幅が見られた。以上の結果から、SDSの存在下であっても、シクロデキストリンを、例えばSDS濃度の10倍程度核酸増幅反応液に添加することによって、核酸増幅反応が阻害されないことが確認された。
3.SDSによるRNaseAの活性抑制についての検証
溶液へのSDSの添加によって、溶液に含まれるRNaseAの活性が抑制されるか、検証した。
RNaseAの活性測定にはRNaseAlert QC test Kit(Ambion)を用いた。RNaseAlert substrateを含む溶液 に、RNaseA を終濃度で0.003U/mL となるように添加した。このRNaseA溶液に、SDSを終濃度で0.1%又は1.0%となるように添加し、各々、試験例1及び試験例2とした。また、RNaseAもSDSも含んでいない溶液を比較例1とし、RNaseAを含みSDSを含んでいない溶液を比較例2とした。試験例1〜2及び比較例1〜2を37℃で60分間保温した。RNaseAlert substrateには、蛍光物質(FAM)とクエンチャーが結合していて、RNaseAによって分解されると、蛍光物質がクエンチャーから離れ、発光する。この蛍光をChromo4 (Bio-rad)を用いて、励起光:490nm /発光:520nmで測定した。
本実験例の結果を図3に示す。図3の縦軸は、蛍光強度(相対蛍光単位、relative fluorescence units)を示し、横軸は時間を示す。図3に示すように、RNaseAが添加され、SDSが添加されていない比較例2では、蛍光強度の増加が確認され、RNaseAの活性が阻害されていないことが示された。一方、RNaseAもSDSも添加していない比較例1では、蛍光強度の増加は確認されず、RNaseAの活性がないことが示された。
4.生体由来のサンプルに含まれるRNaseAに対するSDSの活性抑制効果についての検証
本実験例では、生体由来のサンプルに含まれるRNaseAに対してSDSによる活性の抑制が有効であるか検証した。
本実験理例では、生体由来サンプルとしてウシ血漿を用いた。ウシ血漿は、予め10倍又は20倍に希釈してから用いた。RNaseA活性の測定には実験例3と同様に、RNaseAlert QC test Kit(Ambion)を用いた。10倍希釈のウシ血漿にRNaseAlert substrate と、終濃度が 各々0.05%、0.1%、0.2%、0.3%、0.4%、0.5%となるようにSDSを添加し、これを試験例1〜6とした。また、 20倍希釈のウシ血漿にRNaseAlert substrate と終濃度が 0.05%、0.1%、0.2%、0.3%、0.4%、0.5%の各々となるようにSDSを添加し、これを試験例7〜12とした。さらに、SDSが添加されていない10倍希釈のウシ血漿を比較例1とし、SDSが添加されていない20倍希釈のウシ血漿を比較例2とした。試験例1〜12及び比較例1〜2については、37℃で60分間保温し、この間のRNaseA活性を実験例3同じ方法で測定した。
本実験例の結果を図4と図5に示す。図4及び図5の縦軸は、蛍光強度(相対蛍光単位、relative fluorescence units)を示し、横軸は時間を示す。図4は、比較例1と試験例1〜6の結果を示す。また、図5は、比較例2と試験例7〜12の結果を示す。
[SDS濃度%]≧ −0.02x[生体試料の希釈倍率]+0.6
5.細菌からの核酸抽出に必要なSDS濃度の検討
本試験例では、核酸増幅反応のための菌体からの核酸抽出に必要なSDSの濃度を検討した。
本実験例では、核酸抽出が比較的困難なビフィズス菌を細菌として用いた。ビフィズス菌(Bifidobacterium bifidum、NBRC番号:100015 )は、製品評価技術基盤機構(NITE)のBiological Resource Center (NBRC)より入手した。また、ビフィズス菌ゲノムの核酸増幅反応は、LAMP法で行い、核酸増幅反応用試薬として、LAMP反応試薬(栄研化学、LoopAmp DNA増幅試薬キット)を用いた。また、表3に示す5種類のプライマーを用いた。
本実験例の結果を図6に示す。図6は、試験例1〜5と比較例1のTt値(分)を示す。比較例1のTt値は、18.0であった。また、超音波処理をおこなった試験例2のTt値は、13.7であった。これは、比較例1と比べTt値が低下しており、鋳型核酸となるビフィズス菌ゲノムがより多く核酸増幅反応液に存在していることを示している。即ち、菌体からゲノムが抽出されていることを示している。
6.核酸増幅反応におけるSDSによる反応阻害の抑制に必要なシクロデキストリン濃度の検討
本実験例では、SDSによる核酸増幅反応の阻害を抑制可能なシクロデキストリンの濃度を検討した。
本実験例では、ビフィズス菌ゲノムを鋳型核酸として、LAMP法によって核酸増幅反応を行った。また、核酸増幅反応に用いた核酸増幅反応用試薬、プライマー及びQProbeは、実験例5と同様である。核酸増幅反応液におけるHPβCDの終濃度が2.5%となるように調製し、さらに、SDS濃度が0%、0.05%、0.1%、0.2%、0.3%、0.4%、0.5%又は1.0%となるように添加し、各々、試験例1〜8とした。また、核酸増幅反応液におけるHPβCDの終濃度が5.0%となるように調製し、さらに、SDS濃度が0%、0.05%、0.1%、0.2%、0.3%、0.4%、0.5%、又は1.0%なるように添加し、各々、試験例9〜16とした。また、HPβCDの濃度を0% とし、SDS濃度が0%、0.01%、0.1%となるように調製した核酸増幅反応液を、各々比較例1〜3とした。
図7に本実験例の結果を示す。核酸増幅反応時におけるHPβCD濃度が2.5%の時には、0.0〜0.3%のSDS濃度に対して、核酸増幅反応に対するSDSの阻害効果を抑制することができた(試験例1〜5)。また、核酸増幅反応時におけるHPβCD濃度が5.0%の時には、0.0〜0.5%のSDS濃度に対して、核酸増幅反応に対するSDSの阻害効果を抑制することができた(試験例9〜15)。
7.ウイルス由来の核酸を鋳型核酸とした核酸増幅反応の検証
本実験例では、インフルエンザウイルス感染患者由来の鼻腔スワブを用いて、核酸増幅反応を行い、核酸の増幅を試みた。
インフルエンザウイルス感染患者6人から得た鼻腔スワブサンプルをサンプル希釈液(20mMTris−HCl、0.2% SDS)4mlに溶解させた。鼻腔スワブサンプル溶解後のサンプル希釈液10μlをRT−LAMP核酸増幅試薬(Loopamp RNA増幅試薬キット(栄研化学))と混合して、核酸増幅反応液(25μl)を調製し、これを試験例1〜6とした。また、本実験例で用いたインフルエンザウイルスTypeAに対するLAMP反応用のプライマーは、公知のプライマーを用いた(J Med Virol. 2011 Jan;83(1):10-15.参照)。核酸増幅反応の反応条件及び増幅核酸鎖の検出方法は、実験例5と同様である。
本実験例の結果を表5に示す。表5は、試験例1〜6のTt値(分)を示す。表5に示すように、試験例1〜6の何れについても核酸の増幅を確認することができた。以上の結果から、核酸を含む液体を、イオン性界面活性剤であるSDSを含む溶液で希釈することによって、エンベローブを有するインフルエンザウイルスを鋳型として核酸増幅反応を行うことができることが確認された。
8.固相状の試薬を用いた核酸増幅反応によるウイルス由来の核酸の増幅の検証
本実験例では、固相状の試薬を用いても、液状の試薬と同様にウイルス由来の核酸の増幅が可能であるか検証した。
本実験例では、実験例7における核酸増幅反応試薬を、固相状のものに置き換え、LAMP法による核酸増幅反応を行った。本実験例で用いた固相状の核酸増幅反応試薬には、DNAポリメラーゼとして、Bst DNA polymerase Lg Frag(NEW ENGLAND BIOLABS)が含まれている。また、この固相状試薬には、RNaseH活性が抑制されている逆転写酵素として、ThermoScript(Life technologies)を含む。RNaseHとして、Hybridase Thermostable RNaseH(EPICENTRE)を含む。さらに固相状試薬には、HPβCDと実験例1に記載したバインダーを用いた。検体については、実験例7と同様に、6人のインフルエンザウイルス感染患者由来の鼻腔スワブを用いた。鼻腔スワブは、10mlのサンプル希釈液(20mMTris HCl、0.2% SDS)に溶解させ、これを試験例1〜6とした。このサンプル溶解液、上記の固相状試薬、プライマーとQプローブを混合させ、RT−LAMP法により核酸増幅反応を行った。なお、本実験例では、固相状試薬を用いたため、試薬液によるサンプル溶解液の希釈を生じさせることなく、RT−LAMP反応を行った。核酸増幅反応の反応条件及び増幅核酸鎖の検出方法は、実験例5と同様である。
9.逆転写反応を含む核酸増幅反応におけるRNaseHの効果の検証
本実験例では、RNAを鋳型とする逆転写反応を含む核酸増幅反応におけるRNaseHの影響を検証した。
本実験例では、RNaseH 活性が抑制されている逆転写酵素として、ThermoScript(Life technologies)を用いた。また、DNAポリメラーゼとして、Bst DNA polymerase Lg Frag(NEW ENGLAND BIOLABS)を用いた。さらに、RNaseHとして、Hybridase Thermostable RNaseH(EPICENTRE)を用いた。前記の逆転写酵素(3.75U/25μl)、DNAポリメラーゼ(16U/25μl)とプライマー、QProbe及び鋳型核酸(RNA)を混合した。この混合液にRNaseHを0.63U/25μlとなるように添加した検体4〜6を用意し、これらを試験群1とした。また、RNaseHを添加していない混合液(検体1〜3)も用意し、これを比較群1とした。試験群1及び比較群1における核酸増幅反応は、LAMP法で行った。核酸増幅反応の反応条件及び増幅核酸鎖の検出方法は、実験例5と同様である。
本実験例の結果を表6に示す。表6に示すように、比較群1では核酸の増幅が見られなかったのに対し、試験群1では核酸の増幅が見られた。本実験例の結果から、逆転写反応を伴う核酸増幅反応では、RNaseHが添加されている方が好ましいことが示された。
10.逆転写反応を伴う核酸増幅反応におけるRNaseH濃度の検討
本実験例では、逆転写反応を伴う核酸増幅反応におけるRNaseH濃度を検討した。
本実験例では、RNaseH 活性を有する逆転写酵素として、Cloned AMV Reverse Transcriptase(Life technologies)を用いた。DNAポリメラーゼとRNaseHについては、実験例9と同じものを用いた。RNaseHを0.16U/25μl、0.31U/25μl、0.63U/25μlとなるように添加し、各々試験群1〜3とした。また、RNaseHを添加していない混合液も用意し、これを比較群1とした。試験群1〜3及び比較群1における核酸増幅反応は、LAMP法で行った。核酸増幅反応の反応条件及び増幅核酸鎖の検出方法は、実験例5と同様である。
本実験例の結果を図8に示す。図8は、試験群1〜3と比較群1の各々のTt値を示す。図8に示すように、比較群1ではTt値がばらついたのに対し、試験群1ではそのばらつきが抑えられた。また、そのばらつきは、試験群2、試験群3とRNaseHの添加量が増すごとに、より抑えられていた。本実験例の結果から、RNaseHは、RNaseH活性を有する逆転写酵素を用いる場合には、0.16U/25μl以上の濃度で含まれていることが好ましいことが示された。また、RNaseH活性を有する逆転写酵素を用いた場合でも、RNaseHを添加しないもの(比較群1)より、RNaseH酵素を添加した方(試験群1〜3)が、Tt値のばらつきが抑えられ、かつTt値が小さくなり、より効率的に核酸増幅反応が行われていることが確認された。
11.RNaseA阻害剤の存在下でのRNaseHによる核酸増幅反応への影響
本実験例では、RNaseA阻害剤が添加された試料においても実験例9で確認された核酸増幅反応への効果が発揮されるか検証した。
本実験例では、RNaseA阻害剤として、Ribonuclease inhibitor(タカラ)を用いた。その他の試薬や鋳型核酸鎖は、実験例9と同様である。RNaseHについては、0.63 U/25μLの濃度で用いた。また、RNaseA阻害剤を添加していないもの(検体4〜6)を試験群1とし、RNaseA阻害剤を25U/25μLとなるように添加したもの(検体7〜9)を試験群2とした。さらに、RNaseHもRNaseA阻害剤も添加されていないもの(検体1〜3)を、比較群1とした。試験群1〜2及び比較群1における核酸増幅反応は、LAMP法で行った。核酸増幅反応の反応条件及び増幅核酸鎖の検出方法は、実験例5と同様である。
本実験例の結果を表7に示す。表7に示すように、RNaseHが添加された試験群1及び試験群2では、核酸の増幅を確認することができた。一方、RNaseHが添加されていない比較群1では、核酸の増幅を確認することができなかった。以上より、RNaseA阻害剤を添加してもRNaseH活性は阻害されず、RNaseHの働きにより、RNAを鋳型とする核酸増幅反応がより効率的となることが確認された。
R:固相状試薬
11,12,13:基板層
21,22,23,24,25:反応場(ウェル)
31,32,33,34,35:流路
4:導入部
Claims (8)
- 核酸を含む液体をイオン性界面活性剤を含む溶液で希釈する手順と、
DNAポリメラーゼとシクロデキストリンとバインダーとを少なくとも含有する固相状
の試薬を、前記液体の希釈液に溶解させる手順と、を含み、
前記シクロデキストリンが、前記イオン性界面活性剤の濃度の8倍以上の濃度で含まれている
核酸増幅反応用試料の調製方法。 - 前記イオン性界面活性剤は、陰イオン性界面活性剤である
請求項1記載の核酸増幅反応用試料の調製方法。 - 前記陰イオン性界面活性剤は、ドデシル硫酸ナトリウムである
請求項2記載の核酸増幅反応用試料の調製方法。 - 前記溶解させる手順の前に、前記液体の希釈液を超音波処理する手順を含む
請求項1記載の核酸増幅反応用試料の調製方法。 - 前記溶解させる手順の前に、前記液体の希釈液を加熱する手順を含む
請求項1記載の核酸増幅反応用試料の調製方法。 - 核酸を含む液体をイオン性界面活性剤を含む溶液で希釈する手順と、
DNAポリメラーゼとシクロデキストリンとバインダーとを少なくとも含有し、前記シクロデキストリンが、前記イオン性界面活性剤の濃度の8倍以上の濃度で含まれている固相状の試薬を、前記液体の希釈液に溶解させる手順と、
前記核酸を増幅する手順と、
を含む核酸増幅方法。 - 前記核酸の増幅を等温で行う
請求項6記載の核酸増幅方法。 - 前記核酸がリボ核酸であり、前記増幅する手順の前に前記リボ核酸を鋳型として逆転写
反応を行う手順と、
を含む請求項6記載の核酸増幅方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013075428A JP5904153B2 (ja) | 2013-03-29 | 2013-03-29 | 核酸増幅反応用試料の調製方法、核酸増幅方法、固相状核酸増幅反応用試薬及びマイクロチップ |
| US14/190,865 US20140322761A1 (en) | 2013-03-29 | 2014-02-26 | Method of preparing sample for nucleic acid amplification reaction, nucleic acid amplification method, and reagent and microchip for solid phase nucleic acid amplification reaction |
| CN201410108292.0A CN104073485A (zh) | 2013-03-29 | 2014-03-21 | 制备用于核酸扩增反应的样品的方法、核酸扩增方法及固相核酸扩增反应用试剂和微芯片 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013075428A JP5904153B2 (ja) | 2013-03-29 | 2013-03-29 | 核酸増幅反応用試料の調製方法、核酸増幅方法、固相状核酸増幅反応用試薬及びマイクロチップ |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2014198029A JP2014198029A (ja) | 2014-10-23 |
| JP2014198029A5 JP2014198029A5 (ja) | 2015-03-19 |
| JP5904153B2 true JP5904153B2 (ja) | 2016-04-13 |
Family
ID=51595091
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2013075428A Expired - Fee Related JP5904153B2 (ja) | 2013-03-29 | 2013-03-29 | 核酸増幅反応用試料の調製方法、核酸増幅方法、固相状核酸増幅反応用試薬及びマイクロチップ |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US20140322761A1 (ja) |
| JP (1) | JP5904153B2 (ja) |
| CN (1) | CN104073485A (ja) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2016065192A1 (en) | 2014-10-22 | 2016-04-28 | Roka Bioscience, Inc. | Compositions and methods for the detection of nucleic acids |
| JP2016182112A (ja) * | 2015-03-25 | 2016-10-20 | 東ソー株式会社 | ウイルスからの核酸抽出試薬 |
| US11299777B2 (en) | 2016-04-04 | 2022-04-12 | Nat Diagnostics, Inc. | Isothermal amplification components and processes |
| US9617587B1 (en) | 2016-04-04 | 2017-04-11 | Nat Diagnostics, Inc. | Isothermal amplification components and processes |
| JP6801237B2 (ja) * | 2016-04-21 | 2020-12-16 | 東ソー株式会社 | ウイルスからの核酸抽出および増幅試薬 |
| US20190127783A1 (en) * | 2016-04-27 | 2019-05-02 | Prominex, Inc. | Compositions and methods for the detection of nucleic acids |
| JP7143596B2 (ja) | 2017-03-13 | 2022-09-29 | 東ソー株式会社 | 核酸抽出および増幅試薬 |
| CN108884488A (zh) * | 2017-03-15 | 2018-11-23 | 东洋纺株式会社 | 基因检测方法及基因检测试剂盒 |
| JP2018201414A (ja) * | 2017-06-05 | 2018-12-27 | 東ソー株式会社 | 保存安定性が増した核酸増幅試薬 |
| CN118591622A (zh) * | 2022-01-30 | 2024-09-03 | 牛津大学(苏州)科技有限公司 | 基于引物和酶一体化小球的目标核酸检测方法 |
| WO2023142129A1 (zh) * | 2022-01-30 | 2023-08-03 | 皮乐迪有限公司 | 改进的酶小球及其制备方法和用途 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1240870B (it) * | 1990-02-14 | 1993-12-17 | Talent | Procedimento per l'estrazione e la purificazione di dna genomico umano |
| US5705345A (en) * | 1991-01-10 | 1998-01-06 | Amersham International Plc | Methods and kits for preparing nucleic acids using cyclodextrin |
| US5550040A (en) * | 1993-06-23 | 1996-08-27 | Hoffman-La Roche Inc. | Method, reagents and kits for the detection of Neisseria gonorrhoeae |
| US6153412A (en) * | 1998-12-07 | 2000-11-28 | Bioneer Corporation | Lyophilized reagent for polymerase chain reaction |
| WO2005118853A2 (en) * | 2004-06-01 | 2005-12-15 | Asm Scientific, Inc. | Recombinase polymerase amplification |
| US20050227275A1 (en) * | 2004-04-07 | 2005-10-13 | Access Bio, Inc. | Nucleic acid detection system |
| WO2007052765A1 (ja) * | 2005-11-02 | 2007-05-10 | Shimadzu Corporation | Rnaの抽出方法及びrnaの検出方法 |
| US20080175836A1 (en) * | 2005-12-09 | 2008-07-24 | Karp Nelson M | Immunogenic composition based on conditionally live virion and method for producing the same |
| JP2007325581A (ja) * | 2006-05-12 | 2007-12-20 | Takeda Chem Ind Ltd | 性ホルモン依存疾患の予防・治療剤 |
| NZ576003A (en) * | 2006-10-06 | 2012-03-30 | Dna Genotek Inc | Stabilizing compositions and methods for extraction of ribonucleic acid |
| JP5034438B2 (ja) * | 2006-10-20 | 2012-09-26 | ソニー株式会社 | 流路系、及びハイブリダイゼーション検出装置 |
| WO2010066908A1 (en) * | 2008-12-12 | 2010-06-17 | Eurogentec S.A. | Use of cyclodextrins to improve the specificity, sensitivity and yield of nucleic acid amplification reactions |
| CA2688174C (en) * | 2008-12-19 | 2018-08-07 | F. Hoffmann-La Roche Ag | Dry composition of reaction compounds with stabilized polymerase |
| CA2810316A1 (en) * | 2010-10-04 | 2012-04-12 | F. Hoffmann-La Roche Ag | Method for cell lysis and pcr within the same reaction vessel |
| SG10201601638QA (en) * | 2011-03-04 | 2016-04-28 | Kaneka Corp | Nucleic acid detection method, and device and kit for use in same |
| GB201219137D0 (en) * | 2012-10-24 | 2012-12-05 | Ge Healthcare Uk Ltd | Direct nucleic acid amplification kit, reagent and method |
-
2013
- 2013-03-29 JP JP2013075428A patent/JP5904153B2/ja not_active Expired - Fee Related
-
2014
- 2014-02-26 US US14/190,865 patent/US20140322761A1/en not_active Abandoned
- 2014-03-21 CN CN201410108292.0A patent/CN104073485A/zh active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2014198029A (ja) | 2014-10-23 |
| US20140322761A1 (en) | 2014-10-30 |
| CN104073485A (zh) | 2014-10-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5904153B2 (ja) | 核酸増幅反応用試料の調製方法、核酸増幅方法、固相状核酸増幅反応用試薬及びマイクロチップ | |
| JP2018183156A (ja) | 直接核酸増幅キット、試薬及び方法 | |
| JP2020150948A (ja) | 等温増幅の成分およびプロセス | |
| JP2013240357A (ja) | 室温で安定な分子診断用キット | |
| JP2009545317A (ja) | 分析物および核酸の検出 | |
| WO2022000152A1 (en) | Rapid pcr-based virus detection method, and kits therefor | |
| JP2014198029A5 (ja) | ||
| US9273303B2 (en) | Dried and stabilized ready-to-use composition containing nucleic acid polymerization enzymes for molecular biology applications | |
| JP2024510270A (ja) | 病原体の等温増幅 | |
| JP2014027934A (ja) | イオン性液体を使って生物学的試料から核酸増幅の増幅効率及び感度を高める方法 | |
| US10982253B2 (en) | Nucleic acid catenane with a linking duplex biosensor for detection of a microorganism target | |
| CN118632934A (zh) | 非不透明裂解性缓冲液组合物制剂 | |
| JP2018000124A (ja) | ウイルスからの核酸抽出増幅キット及びそれを用いた抽出増幅方法 | |
| CN117321221A (zh) | 病原体的等温扩增 | |
| JP6801237B2 (ja) | ウイルスからの核酸抽出および増幅試薬 | |
| EP3597745B1 (en) | Reagent for extracting and amplifying nucleic acid | |
| WO2024054823A1 (en) | Hairpin internal control for isothermal nucleic acid amplification | |
| WO2024054867A1 (en) | Modified molecular beacons for improved detection specificity |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150203 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20150203 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150707 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150813 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20151208 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20160125 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20160216 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20160229 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 5904153 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |
|
| LAPS | Cancellation because of no payment of annual fees |