JP5847710B2 - 低酸素模倣体としての化合物、およびその組成物、およびその使用 - Google Patents
低酸素模倣体としての化合物、およびその組成物、およびその使用 Download PDFInfo
- Publication number
- JP5847710B2 JP5847710B2 JP2012519871A JP2012519871A JP5847710B2 JP 5847710 B2 JP5847710 B2 JP 5847710B2 JP 2012519871 A JP2012519871 A JP 2012519871A JP 2012519871 A JP2012519871 A JP 2012519871A JP 5847710 B2 JP5847710 B2 JP 5847710B2
- Authority
- JP
- Japan
- Prior art keywords
- haloalkyl
- compound
- oxo
- hydroxy
- halogen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 COC(C*C(C(C(C1)=O)=C(*=C)c(cc2)c1cc2-c1cc(*)c([*+])cc1)=O)=O Chemical compound COC(C*C(C(C(C1)=O)=C(*=C)c(cc2)c1cc2-c1cc(*)c([*+])cc1)=O)=O 0.000 description 3
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
- A61K31/366—Lactones having six-membered rings, e.g. delta-lactones
- A61K31/37—Coumarins, e.g. psoralen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/22—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms directly attached in position 4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/06—Antianaemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/42—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms in positions 2 and 4
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/04—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring
- C07D311/42—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms in positions 2 and 4
- C07D311/56—Benzo[b]pyrans, not hydrogenated in the carbocyclic ring with oxygen or sulfur atoms in positions 2 and 4 without hydrogen atoms in position 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/04—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
Description
式中
nは1〜6であり、
R1は、OH、SH、NR3R4、NHC(O)R2、NHSO2R2およびスルホニルから選択され、
R2は、H、低級アルキルおよび置換低級アルキルから選択され、
R3およびR4は、独立に、H、低級アルキル、置換低級アルキル、低級ハロアルキル、置換低級ハロアルキルから選択されるか、またはR3およびR4は結合して、3〜6員環もしくは置換3〜6員環を形成することができ、
R5は、OH、SH、NH2、低級アルキル、置換低級アルキル、低級アルコキシ、置換低級アルコキシ、およびスルファニルから選択され、
R6、R7、R8およびR9の各々は、独立に、H、アルキル、置換アルキル、アルケニル、置換アルケニル、アルキニル、置換アルキニル、アルコキシ、置換アルコキシ、NR3R4、C(O)OH、OR12、SR12、SO2R12、CN、NO2、ハロゲン、アリール、置換アリール、ヘテロアリール、置換ヘテロアリール、アリールアルキル、置換アリールアルキル、ヘテロアリールアルキル、置換ヘテロアリールアルキル、ヘテロシクロアルキル、置換ヘテロシクロアルキル、アルキルシリル、置換アルキルシリル、アルケニルシリル、置換アルケニルシリル、アルキニルシリル、置換アルキニルシリル、アルコキシカルボニル、置換アルコキシカルボニル、および−X−R11から選択されるか、
または隣接対のR1およびR6、R6およびR7、R7およびR8、ならびにR8およびR9のうちの少なくとも1つは、結合して、4〜7員環または置換4〜7員環を形成することができ、
Xは、−N(R10)−Y−および−Y−N(R10)−から選択され、
Yは、C(O)、SO2、アルキレン、置換アルキレン、アルケニレン、置換アルケニレン、アルキニレン、および置換アルキニレンから選択され、
R10は、H、低級アルキル、および置換低級アルキルから選択され、
R11は、H、シクロアルキル、置換シクロアルキル、ヘテロシクロアルキル、置換ヘテロシクロアルキル、アリール、置換アリール、ヘテロアリール、および置換ヘテロアリールから選択され、かつ
R12は、H、アルキル、置換アルキル、アルケニル、置換アルケニル、アルキニル、置換アルキニルおよびNR3R4から選択される。
または薬学的に許容されるその塩であり、
式中、
R21は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
R22は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
Z1はNまたはCR23であり、かつ
R23は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
ただし、R21およびR22および(存在する場合)R23のうちの少なくとも1つは、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択される。
式中、
R21は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、かつ
R22は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
ただし、R21およびR22のうちの少なくとも1つは、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択される。
式中、
R24は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
R25は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
Z2はNまたはCR26であり、かつ
R26は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
ただし、R24およびR25および(存在する場合)R26のうちの少なくとも1つは、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択される。
式中、
R24は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、かつ
R25は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択され、
ただし、R24およびR25のうちの少なくとも1つは、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、および低級ハロアルコキシから選択される。
式中
nは1〜6であり、
R1は、OH、SH、NR3R4、NHC(O)R2、NHSO2R2およびスルホニルから選択され、
R2は、H、低級アルキルおよび置換低級アルキルから選択され、
R3およびR4は、独立に、H、低級アルキル、置換低級アルキル、低級ハロアルキル、置換低級ハロアルキルから選択されるか、またはR3およびR4は結合して、3〜6員環もしくは置換3〜6員環を形成することができ、
R5は、OH、SH、NH2、低級アルキル、置換低級アルキル、低級アルコキシ、置換低級アルコキシ、およびスルファニルから選択され、
R6、R7、R8およびR9の各々は、独立に、H、アルキル、置換アルキル、アルケニル、置換アルケニル、アルキニル、置換アルキニル、アルコキシ、置換アルコキシ、NR3R4、C(O)OH、OR12、SR12、SO2R12、CN、NO2、ハロゲン、アリール、置換アリール、ヘテロアリール、置換ヘテロアリール、アリールアルキル、置換アリールアルキル、ヘテロアリールアルキル、置換ヘテロアリールアルキル、ヘテロシクロアルキル、置換ヘテロシクロアルキル、アルキルシリル、置換アルキルシリル、アルケニルシリル、置換アルケニルシリル、アルキニルシリル、置換アルキニルシリル、アルコキシカルボニル、置換アルコキシカルボニル、および−X−R11から選択されるか、
または隣接対のR1およびR6、R6およびR7、R7およびR8、ならびにR8およびR9のうちの少なくとも1つは、結合して、4〜7員環または置換4〜7員環を形成することができ、
Xは、−N(R10)−Y−および−Y−N(R10)−から選択され、
Yは、C(O)、SO2、アルキレン、置換アルキレン、アルケニレン、置換アルケニレン、アルキニレン、および置換アルキニレンから選択され、
R10は、H、低級アルキル、および置換低級アルキルから選択され、
R11は、H、シクロアルキル、置換シクロアルキル、ヘテロシクロアルキル、置換ヘテロシクロアルキル、アリール、置換アリール、ヘテロアリール、および置換ヘテロアリールから選択され、かつ
R12は、H、アルキル、置換アルキル、アルケニル、置換アルケニル、アルキニル、置換アルキニルおよびNR3R4から選択される。
本発明の化合物(その塩を含む)は、既知の有機合成技術を用いて調製することができ、かつ多くの可能な合成経路のいずれかによって合成することができる。
N−[(4−ヒドロキシ−2−オキソ−7−フェニル−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(2−クロロ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3−クロロ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(4−クロロ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3−トリフルオロメチル−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(4−トリフルオロメチル−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3−トリフルオロメトキシ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(4−トリフルオロメトキシ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3,4−ジクロロ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3,4−ジフルオロ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3,4,5−トリフルオロ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3−メトキシ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(4−メトキシ−フェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(3−メチルフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(4−メチルフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−フェニル−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(2−クロロフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3−クロロフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(4−クロロフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3−トリフルオロメチルフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(4−トリフルオロメチルフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3−トリフルオロメトキシフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(4−トリフルオロメトキシフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3,4−ジクロロフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3,4−ジフルオロフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3,4,5−トリフルオロフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3−メトキシフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(4−メトキシフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3−メチルフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(4−メチルフェニル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(6−メトキシピリジン−3−イル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(ピリジン−4−イル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−(ピリジン−3−イル)−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−フェノキシ−2H−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−7−ブロモ−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−ブロモ−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−6−ブロモ−3−クロメニル)カルボニル]グリシンの合成
N−[(4−ヒドロキシ−2−オキソ−8−(3−トリフルオロメチルフェニル)−2H−3−クロメニル)カルボニル]アラニンの合成
ホモジニアスなTR−FRET技術を用いてHIF−PHD2活性を測定した(米国特許第2008/004817号(特許文献1);Dao JHら,Anal Biochem.2009,384:213−23(非特許文献3)も参照されたい)。1/2面積の96ウェルプレートの各ウェルに、DMSO中の試験化合物2μLと、600nMの全長PHD2を含むアッセイ緩衝液(50mMのTris(PH7.4)/0.01%のTween−20/0.1mg/mlのBSA/1mMのアスコルビン酸ナトリウム/20μg/mlのカタラーゼ/10μMのFeSO4)40μLとを添加した。室温で30分間のプレインキュベーションの後、8μLの基質(最終濃度0.2μMの2−オキソグルタラートおよび0.5μMのHIF−1αペプチドビオチニル−DLDLEMLAPYIPMDDDFQL)を添加して酵素反応を開始させた。室温で2時間の後、反応を停止させ、最終濃度1mMのオルト−フェナントロリン、0.1mMのEDTA、0.5nMの抗(His)6LANCE試薬、100nMのAF647標識ストレプトアビジン、および30nMの(His)6−VHL−エロンギンB−エロンギンC複合体となるよう、50μLのクエンチ/検出混合物を添加して、シグナルを発生させた。665nmでの時間分解蛍光シグナルと620nmでの時間分解蛍光シグナルの比を測定し、同時に行なった阻害されていない対照試料と比べて阻害率を算出した。
8週齢の雄のC57BL/6マウスに、20、60および100mg/kgの試験化合物を経口投与した。投与6時間後、眼窩静脈叢から血液試料を採取し、血清を回収した(Robinson Aら,Gastroenterology.2008,134:145−55(非特許文献4);Hsieh MM,ら,Blood.2007,110:2140−7(非特許文献5)も参照されたい)。製造元の指示書に従って、電気化学発光に基づくイムノアッセイ(MSD)により、試料をEPOについて解析した。
8週齢の雄のC57BL/6マウスに、1週間の間、1日1回、60mg/kgの試験化合物を経口投与した。投与1、3および5日後を含む時点で、眼窩静脈叢から血液試料を採取した。自動化血液学分析装置MEK−6318Kを用いて、赤血球数(RBC)、ヘモグロビン濃度(HGB)、ヘマトクリット値(HCT)などの血液学的パラメータを測定した。
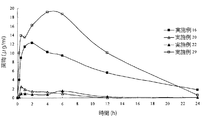
試験化合物を、絶食させた雄のCD(SD)IGSラット(n=6/群)に、50mg/kgで単回経口投与として溶液に含めて投与した。投与後15分、30分、1時間、2時間、4時間、6時間、12時間および24時間で、各々の個々の動物の眼窩静脈叢から血漿試料を採取した。血漿試料中の化合物血液濃度をHPLCで測定した。
Claims (58)
- 式Iの化合物:
式中、
nは1であり、
R1はOHであり、
R2は、H、低級アルキルまたは置換低級アルキルであり、
R3およびR4は、各々独立に、H、低級アルキル、置換低級アルキル、低級ハロアルキル、置換低級ハロアルキルであるか、またはR3およびR4の少なくとも1つの対は、それらが結合している同じ炭素原子とともに、結合して、3〜6員環もしくは置換3〜6員環を形成することができ、
R5は、OHまたは低級アルコキシであり、
R6およびR7はHであり、
R8は、ヘテロアリール、置換ヘテロアリール、フェニル、又は次のいずれか{ハロゲン、アルキル、アルコキシ、ハロアルキル、もしくはハロアルコキシ}によって置換されたフェニルであり、かつR9はHであり、またはR8はHでありかつR9は置換フェニルである、化合物または薬学的に許容されるその塩、溶媒和物。 - R3およびR4が、各々独立に、H、低級アルキル、または低級ハロアルキルである、請求項1に記載の化合物。
- R3およびR4が、各々独立に、Hまたは低級アルキルである、請求項1記載の化合物。
- R3およびR4が各々Hである、請求項1に記載の化合物。
- R5がOHである、請求項1〜4のいずれか一項に記載の化合物。
- R8およびR9のうちの少なくとも1つが、少なくとも1つのハロゲンと置換された部分である、請求項1〜5のいずれか一項に記載の化合物。
- R8が{アルコキシまたはハロアルコキシ}によって置換されたフェニル
である、請求項1〜5のいずれか一項に記載の化合物。 - R8およびR9のうちの少なくとも1つが、フェニル、置換フェニル、ヘテロアリール、または置換ヘテロアリールである、請求項1〜5のいずれか一項に記載の化合物。
- R8およびR9のうちの少なくとも1つが、フェニルまたは置換ヘテロアリールである、請求項1〜8のいずれか一項に記載の化合物。
- R8およびR9のうちの少なくとも1つが、置換フェニルまたは置換ピリジルである、請求項1〜9のいずれか一項に記載の化合物。
- R8およびR9のうちの少なくとも1つがフェニルであり、かつパラ位および/またはメタ位でハロゲン、アルキル、ハロアルキル、アルコキシ、またはハロアルコキシと置換されている、請求項1〜9のいずれか一項に記載の化合物。
- R 8 がピリジルであり、かつパラ位および/またはメタ位でハロゲン、アルキル、ハロアルキル、アルコキシ、またはハロアルコキシと置換されている、請求項1〜9のいずれか一項に記載の化合物。
- R21が、H、Cl、F、メチル、エチル、トリフルオロメチル、メトキシ、エトキシ、またはトリフルオロメトキシである、請求項13に記載の化合物。
- R22が、H、Cl、F、メチル、エチル、トリフルオロメチル、メトキシ、エトキシ、またはトリフルオロメトキシである、請求項13に記載の化合物。
- R23が、H、Cl、F、メチル、エチル、トリフルオロメチル、メトキシ、エトキシ、またはトリフルオロメトキシである、請求項13に記載の化合物。
- R21、R22、およびR23のうちの1つが、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR21、R22、およびR23のうちのあと2つが各々Hである、請求項13に記載の化合物。
- R21およびR23のうちの1つが、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR21およびR23のうちのもう1つがHである、請求項13に記載の化合物。
- R22がHである、請求項18に記載の化合物。
- R21、R22、およびR23のうちの2つが、各々独立に、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR21、R22、およびR23のうちのあと1つがHである、請求項13に記載の化合物。
- R22がHである、請求項20に記載の化合物。
- R21、R22、およびR23が、各々独立に、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項13に記載の化合物。
- R21およびR22のうちの1つが、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR21およびR22のうちのもう1つがHである、請求項13に記載の化合物。
- R21がHであり、かつR22が、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項24に記載の化合物。
- R21がHであり、かつR22が低級アルキルまたは低級ハロアルキルである、請求項24に記載の化合物。
- R21がメチルまたはC1−2ハロアルキルである、請求項26に記載の化合物。
- R22がメチルまたはエチルである、請求項26に記載の化合物。
- R22がHであり、かつR21が、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項24に記載の化合物。
- R22がHであり、かつR21が低級アルキルまたは低級ハロアルキルである、請求項24に記載の化合物。
- R21がメチルまたはC1−2ハロアルキルである、請求項30に記載の化合物。
- R21がメチルまたはエチルである、請求項30に記載の化合物。
- R21およびR22が、各々独立に、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項24に記載の化合物。
- R21およびR22が、各々独立に、C1−2アルキルまたはC1−2ハロアルキルである、請求項24に記載の化合物。
- 前記化合物が、式IIIの化合物:
式中、
R24は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、
R25は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、
Z2はNまたはCR26であり、かつR26は、H、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、
ただし、R24およびR25および(存在する場合)R26のうちの少なくとも1つは、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、
請求項1に記載の化合物。 - Z2がCR26である、請求項35に記載の化合物。
- R24が、H、Cl、F、メチル、エチル、トリフルオロメチル、メトキシ、エトキシ、またはトリフルオロメトキシである、請求項35又は36に記載の化合物。
- R25が、H、Cl、F、メチル、エチル、トリフルオロメチル、メトキシ、エトキシ、またはトリフルオロメトキシである、請求項35〜37のいずれか一項に記載の化合物。
- Z2がCR26であり、R26が、H、Cl、F、メチル、エチル、トリフルオロメチル、メトキシ、エトキシ、またはトリフルオロメトキシである、請求項35〜38のいずれか一項に記載の化合物。
- Z2がCR26であり、R24、R25、およびR26のうちの1つが、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR24、R25、およびR26のうちのあと2つが各々Hである、請求項35に記載の化合物。
- Z2がCR26であり、R24およびR26のうちの1つが、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR24およびR26のうちのもう1つがHである、請求項35に記載の化合物。
- Z 2 がCR26であり、R24、R25、およびR26のうちの2つが、各々独立に、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR24、R25、およびR26のうちのあと1つがHである、請求項35に記載の化合物。
- Z2がCR26であり、R24、R25、およびR26が、各々独立に、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項35に記載の化合物。
- Z2がNである、請求項35に記載の化合物。
- R24およびR25のうちの1つが、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシであり、かつR24およびR25のうちのもう1つがHである、請求項44に記載の化合物。
- R24がHであり、かつR25が、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項46に記載の化合物。
- R25がメチルおよびC1−2ハロアルキルである、請求項47に記載の化合物。
- R25がHであり、かつR24が、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項46に記載の化合物。
- R24がメチルまたはC1−2ハロアルキルである、請求項49に記載の化合物。
- R24およびR25が、各々独立に、ハロゲン、低級アルキル、低級ハロアルキル、低級アルコキシ、または低級ハロアルコキシである、請求項46に記載の化合物。
- 前記化合物が、
2−(4−ヒドロキシ−2−オキソ−7−フェニル−2H−クロメン−3−カルボキサミド)酢酸;
2−(7−(2−クロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(7−(3−クロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(7−(4−クロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−(3−(トリフルオロメチル)フェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−(4−(トリフルオロメチル)フェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−(3−(トリフルオロメトキシ)フェニル)−
2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−(4−(トリフルオロメトキシ)フェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(7−(3,4−ジクロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(7−(3,4−ジフルオロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−(3,4,5−トリフルオロフェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−7−(3−メトキシフェニル)−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−7−(4−メトキシフェニル)−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−m−トリル−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−p−トリル−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−フェニル−2H−クロメン−3−カルボキサミド)酢酸;
2−(8−(2−クロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(8−(3−クロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(8−(4−クロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−(3−(トリフルオロメチル)フェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−(4−(トリフルオロメチル)フェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−(3−(トリフルオロメトキシ)フェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−(4−(トリフルオロメトキシ)フェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(8−(3,4−ジクロロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(8−(3,4−ジフルオロフェニル)−4−ヒドロキシ−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−(3,4,5−トリフルオロフェニル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−8−(3−メトキシフェニル)−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−8−(4−メトキシフェニル)−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−m−トリル−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−8−p−トリル−2H−クロメン−3−カルボキサ
ミド)酢酸;
2−(4−ヒドロキシ−7−(6−メトキシピリジン−3−イル)−2−オキソ−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−(ピリジン−4−イル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−(ピリジン−3−イル)−2H−クロメン−3−カルボキサミド)酢酸;
2−(4−ヒドロキシ−2−オキソ−7−フェノキシ−2H−クロメン−3−カルボキサミド)酢酸;または
2−(4−ヒドロキシ−2−オキソ−8−(3−(トリフルオロメチル)フェニル)−2H−クロメン−3−カルボキサミド)酢酸
である、請求項1に記載の化合物。 - 薬学的に許容される賦形剤、補助剤または担体、および治療有効量の請求項1〜52のいずれか一項に記載の化合物を含む医薬組成物。
- 赤血球生成促進剤または化学療法剤をさらに含む、請求項53に記載の医薬組成物。
- 請求項1〜52のいずれか一項に記載の化合物が、虚血、貧血、創傷治癒、自己移植、異物移植、異種移植、全身性高血圧、サラセミア、糖尿病、癌、炎症性障害、またはそれらの組合せの治療に有効な量で存在する、請求項53に記載の医薬組成物。
- 請求項1〜52のいずれか一項に記載の化合物が、HIFレベルまたはHIF活性と関連する疾患、障害、または状態の治療に有効な量で存在する、請求項53に記載の医薬組成物。
- HIFレベルまたはHIF活性と関連する疾患、障害、または状態の治療のための医薬品の製造における、請求項1〜52のいずれか一項に記載の化合物の使用。
- 虚血、貧血、創傷治癒、自己移植、異物移植、異種移植、全身性高血圧、サラセミア、糖尿病、癌、炎症性障害、またはそれらの組合せである疾患、障害、または状態の治療のための医薬品の製造における、請求項1〜52のいずれか一項に記載の化合物の使用。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN200910089274 | 2009-07-15 | ||
| CN200910089274.1 | 2009-07-15 | ||
| PCT/CN2010/001057 WO2011006355A1 (en) | 2009-07-15 | 2010-07-14 | Compounds as hypoxia mimetics, and compositions, and uses thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012532897A JP2012532897A (ja) | 2012-12-20 |
| JP5847710B2 true JP5847710B2 (ja) | 2016-01-27 |
Family
ID=43448908
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012519871A Expired - Fee Related JP5847710B2 (ja) | 2009-07-15 | 2010-07-14 | 低酸素模倣体としての化合物、およびその組成物、およびその使用 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US8742138B2 (ja) |
| EP (1) | EP2454249B1 (ja) |
| JP (1) | JP5847710B2 (ja) |
| KR (1) | KR20120065311A (ja) |
| CN (1) | CN102164905B (ja) |
| AU (1) | AU2010273101B2 (ja) |
| CA (1) | CA2767911C (ja) |
| ES (1) | ES2702524T3 (ja) |
| HK (1) | HK1161234A1 (ja) |
| IL (1) | IL217531A0 (ja) |
| IN (1) | IN2012DN00549A (ja) |
| SG (1) | SG177598A1 (ja) |
| WO (1) | WO2011006355A1 (ja) |
| ZA (1) | ZA201200293B (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2734504B1 (en) | 2011-07-22 | 2016-09-14 | Beijing Betta Pharmaceuticals Co., Ltd | Polymorphic forms of compounds as prolyl hydroxylase inhibitor, and uses thereof |
| KR20140076549A (ko) * | 2011-07-29 | 2014-06-20 | 베이징 베타 파머수티컬 컴퍼니 리미티드 | 저산소증 유도제로서의 화합물의 안정한 다형체 및 그의 용도 |
| ES2898476T3 (es) | 2014-09-02 | 2022-03-07 | Sunshine Lake Pharma Co Ltd | Compuesto de quinolona y uso del mismo |
| WO2016111523A2 (ko) * | 2015-01-05 | 2016-07-14 | 국립암센터 | HNF4-α 길항제 및 이의 용도 |
| EP3334436A4 (en) | 2015-08-13 | 2019-05-29 | SomaGenics Inc. | PROCESSES AND COMPOSITIONS OF SHORT-SMALL-HAIRPIN-RNAS AND MICRO-RNAS FOR WOUND HEALING |
| WO2018205928A1 (zh) | 2017-05-09 | 2018-11-15 | 杭州安道药业有限公司 | 吲哚嗪衍生物及其在医药上的应用 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2003080649A2 (en) * | 2002-03-20 | 2003-10-02 | Regents Of The University Of Minnesota | Induction of hepatocyte proliferation in vitro by inhibition of cell cycle inhibitors |
| WO2007025169A2 (en) * | 2005-08-25 | 2007-03-01 | Emory University | Hif inhibitors |
| WO2007038571A2 (en) * | 2005-09-26 | 2007-04-05 | Smithkline Beecham Corporation | Prolyl hydroxylase antagonists |
| WO2007070359A2 (en) | 2005-12-09 | 2007-06-21 | Amgen Inc. | Quinolone based compounds exhibiting prolyl hydroxylase inhibitory activity, and compositions, and uses thereof |
| PE20071020A1 (es) * | 2006-03-07 | 2007-12-11 | Smithkline Beecham Corp | Compuestos derivados de glicina n-sustituidos como inhibidores de prolil hidroxilasa |
| AR066691A1 (es) * | 2007-03-29 | 2009-09-09 | Speedel Experimenta Ag | Compuestos espiro heterociclicos derivados de imidazol. composiciones farmaceuticas. |
| WO2009100250A1 (en) * | 2008-02-05 | 2009-08-13 | Fibrogen, Inc. | Chromene derivatives and use thereof as hif hydroxylase activity inhibitors |
| EP2341904A1 (en) * | 2008-08-26 | 2011-07-13 | Fibrogen, Inc. | Methods for treatment of multiple sclerosis |
-
2010
- 2010-07-14 ES ES10799353T patent/ES2702524T3/es active Active
- 2010-07-14 WO PCT/CN2010/001057 patent/WO2011006355A1/en active Application Filing
- 2010-07-14 EP EP10799353.7A patent/EP2454249B1/en not_active Not-in-force
- 2010-07-14 JP JP2012519871A patent/JP5847710B2/ja not_active Expired - Fee Related
- 2010-07-14 SG SG2012001806A patent/SG177598A1/en unknown
- 2010-07-14 AU AU2010273101A patent/AU2010273101B2/en not_active Ceased
- 2010-07-14 CA CA2767911A patent/CA2767911C/en not_active Expired - Fee Related
- 2010-07-14 CN CN201080002367.7A patent/CN102164905B/zh active Active
- 2010-07-14 US US13/384,097 patent/US8742138B2/en active Active
- 2010-07-14 IN IN549DEN2012 patent/IN2012DN00549A/en unknown
- 2010-07-14 KR KR1020127001420A patent/KR20120065311A/ko not_active Application Discontinuation
-
2012
- 2012-01-12 IL IL217531A patent/IL217531A0/en unknown
- 2012-01-13 ZA ZA2012/00293A patent/ZA201200293B/en unknown
- 2012-02-14 HK HK12101426.8A patent/HK1161234A1/xx not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| EP2454249A4 (en) | 2012-12-12 |
| EP2454249A1 (en) | 2012-05-23 |
| CN102164905B (zh) | 2014-04-30 |
| WO2011006355A1 (en) | 2011-01-20 |
| US20120172399A1 (en) | 2012-07-05 |
| US8742138B2 (en) | 2014-06-03 |
| AU2010273101A1 (en) | 2012-02-02 |
| SG177598A1 (en) | 2012-02-28 |
| KR20120065311A (ko) | 2012-06-20 |
| IL217531A0 (en) | 2012-02-29 |
| ES2702524T3 (es) | 2019-03-01 |
| HK1161234A1 (en) | 2012-08-24 |
| AU2010273101B2 (en) | 2016-02-25 |
| IN2012DN00549A (ja) | 2015-06-12 |
| CA2767911A1 (en) | 2011-01-20 |
| ZA201200293B (en) | 2012-09-26 |
| EP2454249B1 (en) | 2018-09-19 |
| CA2767911C (en) | 2016-03-29 |
| AU2010273101A2 (en) | 2012-03-15 |
| JP2012532897A (ja) | 2012-12-20 |
| CN102164905A (zh) | 2011-08-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7569726B2 (en) | Indanone derivatives that inhibit prolyl hydroxylase | |
| JP6099644B2 (ja) | プロリルヒドロキシラーゼ阻害剤としての化合物の多形体、およびその使用 | |
| JP5847710B2 (ja) | 低酸素模倣体としての化合物、およびその組成物、およびその使用 | |
| CA2634168C (en) | Quinolone based compounds exhibiting prolyl hydroxylase inhibitory activity, and compositions, and uses thereof | |
| EP2150251B9 (en) | Thienopyridine and thiazolopyridine derivatives that inhibit prolyl hydroxylase activity | |
| AU781266B2 (en) | Di-aryl acid derivatives as PPAR receptor ligands | |
| ES2442847T3 (es) | Quinolonas y azaquinolonas que inhiben la prolil hidroxilasa | |
| JP2008538777A (ja) | アセチレン誘導体 | |
| WO1997034869A1 (fr) | Derives de l'acide carboxylique a cycles fusionnes | |
| JP2022522334A (ja) | 新規な甲状腺模倣物 | |
| TW202241852A (zh) | 四氫喹啉衍生物及其醫藥用途 | |
| TWI424842B (zh) | 含取代基的雜環化合物、包括其的藥物組合物,以及該化合物的應用 | |
| CN107162913B (zh) | 一类新型氘代苯丙酸衍生物、其制备方法及其作为药物的用途 | |
| WO2020013116A1 (ja) | Ptp-1b阻害剤およびその用途 | |
| JP2014523917A (ja) | 低酸素模倣剤としての化合物の安定な多形体、およびその使用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121130 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140401 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140626 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140703 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140801 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150120 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A711 Effective date: 20150226 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20150303 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150420 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20150707 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20151007 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20151007 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20151104 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20151125 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5847710 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |