JP5773315B2 - 膵癌のバイオマーカーとしてのcxcl4l1 - Google Patents
膵癌のバイオマーカーとしてのcxcl4l1 Download PDFInfo
- Publication number
- JP5773315B2 JP5773315B2 JP2011537960A JP2011537960A JP5773315B2 JP 5773315 B2 JP5773315 B2 JP 5773315B2 JP 2011537960 A JP2011537960 A JP 2011537960A JP 2011537960 A JP2011537960 A JP 2011537960A JP 5773315 B2 JP5773315 B2 JP 5773315B2
- Authority
- JP
- Japan
- Prior art keywords
- cxcl4l1
- cxcl4
- pancreatic
- pancreatic cancer
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 101001126487 Homo sapiens Platelet factor 4 variant Proteins 0.000 title claims description 208
- 102100030582 Platelet factor 4 variant Human genes 0.000 title claims description 191
- 206010061902 Pancreatic neoplasm Diseases 0.000 title claims description 78
- 201000002528 pancreatic cancer Diseases 0.000 title claims description 76
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 title claims description 62
- 208000008443 pancreatic carcinoma Diseases 0.000 title claims description 62
- 239000000090 biomarker Substances 0.000 title claims description 6
- 230000014509 gene expression Effects 0.000 claims description 54
- 238000000034 method Methods 0.000 claims description 52
- 239000000523 sample Substances 0.000 claims description 30
- 239000012472 biological sample Substances 0.000 claims description 25
- 108090000623 proteins and genes Proteins 0.000 claims description 24
- 206010027476 Metastases Diseases 0.000 claims description 20
- 102000004169 proteins and genes Human genes 0.000 claims description 20
- 108020004999 messenger RNA Proteins 0.000 claims description 19
- 206010052747 Adenocarcinoma pancreas Diseases 0.000 claims description 18
- 201000002094 pancreatic adenocarcinoma Diseases 0.000 claims description 18
- 230000009401 metastasis Effects 0.000 claims description 15
- 238000011282 treatment Methods 0.000 claims description 15
- 239000002246 antineoplastic agent Substances 0.000 claims description 11
- 238000001514 detection method Methods 0.000 claims description 9
- 229940127089 cytotoxic agent Drugs 0.000 claims description 8
- 239000003966 growth inhibitor Substances 0.000 claims description 6
- 230000002265 prevention Effects 0.000 claims description 6
- 239000002254 cytotoxic agent Substances 0.000 claims description 5
- 231100000599 cytotoxic agent Toxicity 0.000 claims 1
- 101000582950 Homo sapiens Platelet factor 4 Proteins 0.000 description 86
- 102100030304 Platelet factor 4 Human genes 0.000 description 82
- 210000004027 cell Anatomy 0.000 description 57
- 206010028980 Neoplasm Diseases 0.000 description 50
- 241000282414 Homo sapiens Species 0.000 description 36
- 230000000694 effects Effects 0.000 description 19
- 229940079593 drug Drugs 0.000 description 17
- 239000003814 drug Substances 0.000 description 17
- 150000007523 nucleic acids Chemical class 0.000 description 15
- 230000009870 specific binding Effects 0.000 description 15
- 230000027455 binding Effects 0.000 description 14
- 108020004707 nucleic acids Proteins 0.000 description 14
- 102000039446 nucleic acids Human genes 0.000 description 14
- 239000013615 primer Substances 0.000 description 14
- 239000002987 primer (paints) Substances 0.000 description 14
- 210000001519 tissue Anatomy 0.000 description 14
- 102000004190 Enzymes Human genes 0.000 description 13
- 108090000790 Enzymes Proteins 0.000 description 13
- 229940088598 enzyme Drugs 0.000 description 13
- 210000000496 pancreas Anatomy 0.000 description 13
- 210000004881 tumor cell Anatomy 0.000 description 12
- 230000003321 amplification Effects 0.000 description 11
- 239000012634 fragment Substances 0.000 description 11
- 238000003199 nucleic acid amplification method Methods 0.000 description 11
- 108091023037 Aptamer Proteins 0.000 description 10
- 201000011510 cancer Diseases 0.000 description 10
- 230000004663 cell proliferation Effects 0.000 description 10
- 150000001875 compounds Chemical class 0.000 description 10
- 238000010195 expression analysis Methods 0.000 description 10
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 description 9
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 9
- 210000002889 endothelial cell Anatomy 0.000 description 9
- 230000009545 invasion Effects 0.000 description 9
- -1 mechloretamine Chemical compound 0.000 description 9
- 238000013508 migration Methods 0.000 description 9
- 229940002612 prodrug Drugs 0.000 description 9
- 239000000651 prodrug Substances 0.000 description 9
- 241000271566 Aves Species 0.000 description 8
- 239000003795 chemical substances by application Substances 0.000 description 8
- 201000010099 disease Diseases 0.000 description 8
- 230000002285 radioactive effect Effects 0.000 description 8
- 238000003753 real-time PCR Methods 0.000 description 8
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 7
- 238000011529 RT qPCR Methods 0.000 description 7
- 230000033115 angiogenesis Effects 0.000 description 7
- 230000005012 migration Effects 0.000 description 7
- 108090000765 processed proteins & peptides Proteins 0.000 description 7
- 230000003827 upregulation Effects 0.000 description 7
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 6
- 241000282693 Cercopithecidae Species 0.000 description 6
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 241000699670 Mus sp. Species 0.000 description 6
- 238000003556 assay Methods 0.000 description 6
- 231100000433 cytotoxic Toxicity 0.000 description 6
- 230000001472 cytotoxic effect Effects 0.000 description 6
- 238000002474 experimental method Methods 0.000 description 6
- 238000009396 hybridization Methods 0.000 description 6
- 238000007901 in situ hybridization Methods 0.000 description 6
- 230000002401 inhibitory effect Effects 0.000 description 6
- 239000012528 membrane Substances 0.000 description 6
- 230000000638 stimulation Effects 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 102000019034 Chemokines Human genes 0.000 description 5
- 108010012236 Chemokines Proteins 0.000 description 5
- 230000001772 anti-angiogenic effect Effects 0.000 description 5
- 230000012292 cell migration Effects 0.000 description 5
- 238000003018 immunoassay Methods 0.000 description 5
- 238000000338 in vitro Methods 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 239000002773 nucleotide Substances 0.000 description 5
- 125000003729 nucleotide group Chemical group 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- 208000003098 Ganglion Cysts Diseases 0.000 description 4
- 241000282412 Homo Species 0.000 description 4
- 208000007433 Lymphatic Metastasis Diseases 0.000 description 4
- 206010027458 Metastases to lung Diseases 0.000 description 4
- 241000282577 Pan troglodytes Species 0.000 description 4
- 102000035195 Peptidases Human genes 0.000 description 4
- 108091005804 Peptidases Proteins 0.000 description 4
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 4
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 4
- 208000005400 Synovial Cyst Diseases 0.000 description 4
- 230000002491 angiogenic effect Effects 0.000 description 4
- 230000004709 cell invasion Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 230000012010 growth Effects 0.000 description 4
- 102000052196 human PF4 Human genes 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 230000005764 inhibitory process Effects 0.000 description 4
- 210000004072 lung Anatomy 0.000 description 4
- 238000004519 manufacturing process Methods 0.000 description 4
- 210000004379 membrane Anatomy 0.000 description 4
- 210000004923 pancreatic tissue Anatomy 0.000 description 4
- 230000003389 potentiating effect Effects 0.000 description 4
- 102000004196 processed proteins & peptides Human genes 0.000 description 4
- 238000011002 quantification Methods 0.000 description 4
- 238000003757 reverse transcription PCR Methods 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- 239000012679 serum free medium Substances 0.000 description 4
- 241000894007 species Species 0.000 description 4
- 239000000758 substrate Substances 0.000 description 4
- 108020004414 DNA Proteins 0.000 description 3
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 3
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- ZDZOTLJHXYCWBA-VCVYQWHSSA-N N-debenzoyl-N-(tert-butoxycarbonyl)-10-deacetyltaxol Chemical compound O([C@H]1[C@H]2[C@@](C([C@H](O)C3=C(C)[C@@H](OC(=O)[C@H](O)[C@@H](NC(=O)OC(C)(C)C)C=4C=CC=CC=4)C[C@]1(O)C3(C)C)=O)(C)[C@@H](O)C[C@H]1OC[C@]12OC(=O)C)C(=O)C1=CC=CC=C1 ZDZOTLJHXYCWBA-VCVYQWHSSA-N 0.000 description 3
- 229930012538 Paclitaxel Natural products 0.000 description 3
- 241000282579 Pan Species 0.000 description 3
- 241001494479 Pecora Species 0.000 description 3
- 239000004365 Protease Substances 0.000 description 3
- 210000001744 T-lymphocyte Anatomy 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 210000000577 adipose tissue Anatomy 0.000 description 3
- 239000000427 antigen Substances 0.000 description 3
- 239000011324 bead Substances 0.000 description 3
- 238000001574 biopsy Methods 0.000 description 3
- 230000010261 cell growth Effects 0.000 description 3
- 229960003668 docetaxel Drugs 0.000 description 3
- 239000012091 fetal bovine serum Substances 0.000 description 3
- 210000004408 hybridoma Anatomy 0.000 description 3
- 230000002055 immunohistochemical effect Effects 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 238000002372 labelling Methods 0.000 description 3
- 239000003446 ligand Substances 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 206010061289 metastatic neoplasm Diseases 0.000 description 3
- 230000017095 negative regulation of cell growth Effects 0.000 description 3
- 229960001592 paclitaxel Drugs 0.000 description 3
- 238000002823 phage display Methods 0.000 description 3
- 238000013081 phylogenetic analysis Methods 0.000 description 3
- 210000000952 spleen Anatomy 0.000 description 3
- 238000010561 standard procedure Methods 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 3
- 239000003053 toxin Substances 0.000 description 3
- 231100000765 toxin Toxicity 0.000 description 3
- 108700012359 toxins Proteins 0.000 description 3
- 238000011222 transcriptome analysis Methods 0.000 description 3
- 230000005748 tumor development Effects 0.000 description 3
- STQGQHZAVUOBTE-UHFFFAOYSA-N 7-Cyan-hept-2t-en-4,6-diinsaeure Natural products C1=2C(O)=C3C(=O)C=4C(OC)=CC=CC=4C(=O)C3=C(O)C=2CC(O)(C(C)=O)CC1OC1CC(N)C(O)C(C)O1 STQGQHZAVUOBTE-UHFFFAOYSA-N 0.000 description 2
- 108090001008 Avidin Proteins 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- 108010006303 Carboxypeptidases Proteins 0.000 description 2
- 102000005367 Carboxypeptidases Human genes 0.000 description 2
- 108091026890 Coding region Proteins 0.000 description 2
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- 241000287828 Gallus gallus Species 0.000 description 2
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 description 2
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 description 2
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 description 2
- 230000027311 M phase Effects 0.000 description 2
- 102000029749 Microtubule Human genes 0.000 description 2
- 108091022875 Microtubule Proteins 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- 208000003788 Neoplasm Micrometastasis Diseases 0.000 description 2
- 108010004729 Phycoerythrin Proteins 0.000 description 2
- 241000288906 Primates Species 0.000 description 2
- 108010039491 Ricin Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- NKANXQFJJICGDU-QPLCGJKRSA-N Tamoxifen Chemical compound C=1C=CC=CC=1C(/CC)=C(C=1C=CC(OCCN(C)C)=CC=1)/C1=CC=CC=C1 NKANXQFJJICGDU-QPLCGJKRSA-N 0.000 description 2
- 229940123237 Taxane Drugs 0.000 description 2
- 241001116498 Taxus baccata Species 0.000 description 2
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 208000009956 adenocarcinoma Diseases 0.000 description 2
- 238000000246 agarose gel electrophoresis Methods 0.000 description 2
- 239000003242 anti bacterial agent Substances 0.000 description 2
- 229940088710 antibiotic agent Drugs 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 230000001588 bifunctional effect Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229960002685 biotin Drugs 0.000 description 2
- 235000020958 biotin Nutrition 0.000 description 2
- 239000011616 biotin Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 210000003711 chorioallantoic membrane Anatomy 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 229960000975 daunorubicin Drugs 0.000 description 2
- STQGQHZAVUOBTE-VGBVRHCVSA-N daunorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(C)=O)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 STQGQHZAVUOBTE-VGBVRHCVSA-N 0.000 description 2
- 238000003745 diagnosis Methods 0.000 description 2
- 229960004679 doxorubicin Drugs 0.000 description 2
- 230000000431 effect on proliferation Effects 0.000 description 2
- 230000010595 endothelial cell migration Effects 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 210000002919 epithelial cell Anatomy 0.000 description 2
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 2
- 229960005420 etoposide Drugs 0.000 description 2
- 230000001605 fetal effect Effects 0.000 description 2
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 2
- 229960002949 fluorouracil Drugs 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 102000048725 human PF4V1 Human genes 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- 238000007834 ligase chain reaction Methods 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 201000001441 melanoma Diseases 0.000 description 2
- 229960000485 methotrexate Drugs 0.000 description 2
- 210000004688 microtubule Anatomy 0.000 description 2
- 238000010232 migration assay Methods 0.000 description 2
- 210000001616 monocyte Anatomy 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 239000000101 novel biomarker Substances 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 230000002018 overexpression Effects 0.000 description 2
- 201000008129 pancreatic ductal adenocarcinoma Diseases 0.000 description 2
- 210000002381 plasma Anatomy 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 235000019419 proteases Nutrition 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 238000010839 reverse transcription Methods 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 210000000329 smooth muscle myocyte Anatomy 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 238000007920 subcutaneous administration Methods 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000013518 transcription Methods 0.000 description 2
- 230000035897 transcription Effects 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- 210000003606 umbilical vein Anatomy 0.000 description 2
- 229960003048 vinblastine Drugs 0.000 description 2
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 2
- OGWKCGZFUXNPDA-XQKSVPLYSA-N vincristine Chemical compound C([N@]1C[C@@H](C[C@]2(C(=O)OC)C=3C(=CC4=C([C@]56[C@H]([C@@]([C@H](OC(C)=O)[C@]7(CC)C=CCN([C@H]67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)C[C@@](C1)(O)CC)CC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-XQKSVPLYSA-N 0.000 description 2
- 229960004528 vincristine Drugs 0.000 description 2
- OGWKCGZFUXNPDA-UHFFFAOYSA-N vincristine Natural products C1C(CC)(O)CC(CC2(C(=O)OC)C=3C(=CC4=C(C56C(C(C(OC(C)=O)C7(CC)C=CCN(C67)CC5)(O)C(=O)OC)N4C=O)C=3)OC)CN1CCC1=C2NC2=CC=CC=C12 OGWKCGZFUXNPDA-UHFFFAOYSA-N 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- IEUUDEWWMRQUDS-UHFFFAOYSA-N (6-azaniumylidene-1,6-dimethoxyhexylidene)azanium;dichloride Chemical compound Cl.Cl.COC(=N)CCCCC(=N)OC IEUUDEWWMRQUDS-UHFFFAOYSA-N 0.000 description 1
- FDKXTQMXEQVLRF-ZHACJKMWSA-N (E)-dacarbazine Chemical compound CN(C)\N=N\c1[nH]cnc1C(N)=O FDKXTQMXEQVLRF-ZHACJKMWSA-N 0.000 description 1
- WDCYWAQPCXBPJA-UHFFFAOYSA-N 1,3-dinitrobenzene Chemical compound [O-][N+](=O)C1=CC=CC([N+]([O-])=O)=C1 WDCYWAQPCXBPJA-UHFFFAOYSA-N 0.000 description 1
- FZDFGHZZPBUTGP-UHFFFAOYSA-N 2-[[2-[bis(carboxymethyl)amino]-3-(4-isothiocyanatophenyl)propyl]-[2-[bis(carboxymethyl)amino]propyl]amino]acetic acid Chemical compound OC(=O)CN(CC(O)=O)C(C)CN(CC(O)=O)CC(N(CC(O)=O)CC(O)=O)CC1=CC=C(N=C=S)C=C1 FZDFGHZZPBUTGP-UHFFFAOYSA-N 0.000 description 1
- AOJJSUZBOXZQNB-VTZDEGQISA-N 4'-epidoxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-VTZDEGQISA-N 0.000 description 1
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 1
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 108010006654 Bleomycin Proteins 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 108050006947 CXC Chemokine Proteins 0.000 description 1
- 102000019388 CXC chemokine Human genes 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 102000047934 Caspase-3/7 Human genes 0.000 description 1
- 108700037887 Caspase-3/7 Proteins 0.000 description 1
- 102000004225 Cathepsin B Human genes 0.000 description 1
- 108090000712 Cathepsin B Proteins 0.000 description 1
- 102000004172 Cathepsin L Human genes 0.000 description 1
- 108090000624 Cathepsin L Proteins 0.000 description 1
- 102000005600 Cathepsins Human genes 0.000 description 1
- 108010084457 Cathepsins Proteins 0.000 description 1
- 206010055114 Colon cancer metastatic Diseases 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 201000005171 Cystadenoma Diseases 0.000 description 1
- 102000000311 Cytosine Deaminase Human genes 0.000 description 1
- 108010080611 Cytosine Deaminase Proteins 0.000 description 1
- 125000000030 D-alanine group Chemical group [H]N([H])[C@](C([H])([H])[H])(C(=O)[*])[H] 0.000 description 1
- 150000008574 D-amino acids Chemical group 0.000 description 1
- 229940124087 DNA topoisomerase II inhibitor Drugs 0.000 description 1
- 102000007260 Deoxyribonuclease I Human genes 0.000 description 1
- 108010008532 Deoxyribonuclease I Proteins 0.000 description 1
- 238000009007 Diagnostic Kit Methods 0.000 description 1
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 108010067770 Endopeptidase K Proteins 0.000 description 1
- HTIJFSOGRVMCQR-UHFFFAOYSA-N Epirubicin Natural products COc1cccc2C(=O)c3c(O)c4CC(O)(CC(OC5CC(N)C(=O)C(C)O5)c4c(O)c3C(=O)c12)C(=O)CO HTIJFSOGRVMCQR-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- 241000588724 Escherichia coli Species 0.000 description 1
- 208000000461 Esophageal Neoplasms Diseases 0.000 description 1
- 108700039887 Essential Genes Proteins 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- 230000037057 G1 phase arrest Effects 0.000 description 1
- 108700004714 Gelonium multiflorum GEL Proteins 0.000 description 1
- 208000032612 Glial tumor Diseases 0.000 description 1
- 206010018338 Glioma Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 101001133631 Lysinibacillus sphaericus Penicillin acylase Proteins 0.000 description 1
- 241000282560 Macaca mulatta Species 0.000 description 1
- 101100083539 Mus musculus Pf4 gene Proteins 0.000 description 1
- 102000005348 Neuraminidase Human genes 0.000 description 1
- 108010006232 Neuraminidase Proteins 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 238000000636 Northern blotting Methods 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 206010030155 Oesophageal carcinoma Diseases 0.000 description 1
- 108091034117 Oligonucleotide Proteins 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 208000034038 Pathologic Neovascularization Diseases 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- 108010073038 Penicillin Amidase Proteins 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 101710123388 Penicillin G acylase Proteins 0.000 description 1
- 102000057297 Pepsin A Human genes 0.000 description 1
- 108090000284 Pepsin A Proteins 0.000 description 1
- 108010079855 Peptide Aptamers Proteins 0.000 description 1
- 102000004211 Platelet factor 4 Human genes 0.000 description 1
- 108090000778 Platelet factor 4 Proteins 0.000 description 1
- 241000276498 Pollachius virens Species 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 206010060862 Prostate cancer Diseases 0.000 description 1
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 1
- 108010076504 Protein Sorting Signals Proteins 0.000 description 1
- 238000002123 RNA extraction Methods 0.000 description 1
- 238000011530 RNeasy Mini Kit Methods 0.000 description 1
- 230000018199 S phase Effects 0.000 description 1
- 108010084592 Saporins Proteins 0.000 description 1
- 241000607720 Serratia Species 0.000 description 1
- 108090000787 Subtilisin Proteins 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 108090001109 Thermolysin Proteins 0.000 description 1
- 102000002933 Thioredoxin Human genes 0.000 description 1
- 239000000317 Topoisomerase II Inhibitor Substances 0.000 description 1
- 102000004243 Tubulin Human genes 0.000 description 1
- 108090000704 Tubulin Proteins 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 1
- 241000863480 Vinca Species 0.000 description 1
- 229940122803 Vinca alkaloid Drugs 0.000 description 1
- 238000011481 absorbance measurement Methods 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 229940009456 adriamycin Drugs 0.000 description 1
- 230000004520 agglutination Effects 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 230000000692 anti-sense effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 210000002403 aortic endothelial cell Anatomy 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 238000003149 assay kit Methods 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 229960001561 bleomycin Drugs 0.000 description 1
- OYVAGSVQBOHSSS-UAPAGMARSA-O bleomycin A2 Chemical compound N([C@H](C(=O)N[C@H](C)[C@@H](O)[C@H](C)C(=O)N[C@@H]([C@H](O)C)C(=O)NCCC=1SC=C(N=1)C=1SC=C(N=1)C(=O)NCCC[S+](C)C)[C@@H](O[C@H]1[C@H]([C@@H](O)[C@H](O)[C@H](CO)O1)O[C@@H]1[C@H]([C@@H](OC(N)=O)[C@H](O)[C@@H](CO)O1)O)C=1N=CNC=1)C(=O)C1=NC([C@H](CC(N)=O)NC[C@H](N)C(N)=O)=NC(N)=C1C OYVAGSVQBOHSSS-UAPAGMARSA-O 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- 210000004899 c-terminal region Anatomy 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000006369 cell cycle progression Effects 0.000 description 1
- 238000010822 cell death assay Methods 0.000 description 1
- 238000007806 cell migration and invasion assay Methods 0.000 description 1
- 238000001516 cell proliferation assay Methods 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 239000002738 chelating agent Substances 0.000 description 1
- 239000002975 chemoattractant Substances 0.000 description 1
- JCKYGMPEJWAADB-UHFFFAOYSA-N chlorambucil Chemical compound OC(=O)CCCC1=CC=C(N(CCCl)CCCl)C=C1 JCKYGMPEJWAADB-UHFFFAOYSA-N 0.000 description 1
- 229960004630 chlorambucil Drugs 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 210000001072 colon Anatomy 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 230000002860 competitive effect Effects 0.000 description 1
- 239000002299 complementary DNA Substances 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 230000021615 conjugation Effects 0.000 description 1
- 210000004351 coronary vessel Anatomy 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 238000013211 curve analysis Methods 0.000 description 1
- NZNMSOFKMUBTKW-UHFFFAOYSA-N cyclohexanecarboxylic acid Chemical compound OC(=O)C1CCCCC1 NZNMSOFKMUBTKW-UHFFFAOYSA-N 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 229960003901 dacarbazine Drugs 0.000 description 1
- 230000002498 deadly effect Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 125000005442 diisocyanate group Chemical group 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- ZWIBGKZDAWNIFC-UHFFFAOYSA-N disuccinimidyl suberate Chemical compound O=C1CCC(=O)N1OC(=O)CCCCCCC(=O)ON1C(=O)CCC1=O ZWIBGKZDAWNIFC-UHFFFAOYSA-N 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 235000006694 eating habits Nutrition 0.000 description 1
- 235000013601 eggs Nutrition 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 230000013020 embryo development Effects 0.000 description 1
- 229960001904 epirubicin Drugs 0.000 description 1
- 201000004101 esophageal cancer Diseases 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 125000002573 ethenylidene group Chemical group [*]=C=C([H])[H] 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 208000021045 exocrine pancreatic carcinoma Diseases 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- XRECTZIEBJDKEO-UHFFFAOYSA-N flucytosine Chemical compound NC1=NC(=O)NC=C1F XRECTZIEBJDKEO-UHFFFAOYSA-N 0.000 description 1
- 150000002222 fluorine compounds Chemical class 0.000 description 1
- 230000002538 fungal effect Effects 0.000 description 1
- 229960005277 gemcitabine Drugs 0.000 description 1
- SDUQYLNIPVEERB-QPPQHZFASA-N gemcitabine Chemical compound O=C1N=C(N)C=CN1[C@H]1C(F)(F)[C@H](O)[C@@H](CO)O1 SDUQYLNIPVEERB-QPPQHZFASA-N 0.000 description 1
- 238000009650 gentamicin protection assay Methods 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 239000001046 green dye Substances 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000005802 health problem Effects 0.000 description 1
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 1
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 1
- SYECJBOWSGTPLU-UHFFFAOYSA-N hexane-1,1-diamine Chemical compound CCCCCC(N)N SYECJBOWSGTPLU-UHFFFAOYSA-N 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 238000010562 histological examination Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 238000000760 immunoelectrophoresis Methods 0.000 description 1
- 230000016784 immunoglobulin production Effects 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 239000012133 immunoprecipitate Substances 0.000 description 1
- 230000004957 immunoregulator effect Effects 0.000 description 1
- 230000002637 immunotoxin Effects 0.000 description 1
- 239000002596 immunotoxin Substances 0.000 description 1
- 231100000608 immunotoxin Toxicity 0.000 description 1
- 229940051026 immunotoxin Drugs 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 206010022498 insulinoma Diseases 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 239000000138 intercalating agent Substances 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 201000010985 invasive ductal carcinoma Diseases 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 229960003299 ketamine Drugs 0.000 description 1
- 239000004816 latex Substances 0.000 description 1
- 229920000126 latex Polymers 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- HWYHZTIRURJOHG-UHFFFAOYSA-N luminol Chemical compound O=C1NNC(=O)C2=C1C(N)=CC=C2 HWYHZTIRURJOHG-UHFFFAOYSA-N 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 208000020816 lung neoplasm Diseases 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 230000002101 lytic effect Effects 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 108010082117 matrigel Proteins 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 210000003593 megakaryocyte Anatomy 0.000 description 1
- SGDBTWWWUNNDEQ-LBPRGKRZSA-N melphalan Chemical compound OC(=O)[C@@H](N)CC1=CC=C(N(CCCl)CCCl)C=C1 SGDBTWWWUNNDEQ-LBPRGKRZSA-N 0.000 description 1
- 229960001924 melphalan Drugs 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 238000002493 microarray Methods 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000003068 molecular probe Substances 0.000 description 1
- 239000002808 molecular sieve Substances 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 230000027498 negative regulation of mitosis Effects 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 230000001293 nucleolytic effect Effects 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 208000021010 pancreatic neuroendocrine tumor Diseases 0.000 description 1
- 230000003076 paracrine Effects 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 239000013610 patient sample Substances 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 229940111202 pepsin Drugs 0.000 description 1
- 238000010647 peptide synthesis reaction Methods 0.000 description 1
- 125000001151 peptidyl group Chemical group 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 239000011148 porous material Substances 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- XOFYZVNMUHMLCC-ZPOLXVRWSA-N prednisone Chemical compound O=C1C=C[C@]2(C)[C@H]3C(=O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 XOFYZVNMUHMLCC-ZPOLXVRWSA-N 0.000 description 1
- 229960004618 prednisone Drugs 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000004393 prognosis Methods 0.000 description 1
- 235000019833 protease Nutrition 0.000 description 1
- 239000000941 radioactive substance Substances 0.000 description 1
- 238000003127 radioimmunoassay Methods 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000010188 recombinant method Methods 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 230000009711 regulatory function Effects 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 238000011896 sensitive detection Methods 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 1
- 239000001509 sodium citrate Substances 0.000 description 1
- JUJBNYBVVQSIOU-UHFFFAOYSA-M sodium;4-[2-(4-iodophenyl)-3-(4-nitrophenyl)tetrazol-2-ium-5-yl]benzene-1,3-disulfonate Chemical compound [Na+].C1=CC([N+](=O)[O-])=CC=C1N1[N+](C=2C=CC(I)=CC=2)=NC(C=2C(=CC(=CC=2)S([O-])(=O)=O)S([O-])(=O)=O)=N1 JUJBNYBVVQSIOU-UHFFFAOYSA-M 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 210000004989 spleen cell Anatomy 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 229960001603 tamoxifen Drugs 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- RCINICONZNJXQF-XAZOAEDWSA-N taxol® Chemical compound O([C@@H]1[C@@]2(CC(C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3(C21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-XAZOAEDWSA-N 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- CNHYKKNIIGEXAY-UHFFFAOYSA-N thiolan-2-imine Chemical compound N=C1CCCS1 CNHYKKNIIGEXAY-UHFFFAOYSA-N 0.000 description 1
- 108060008226 thioredoxin Proteins 0.000 description 1
- 229940094937 thioredoxin Drugs 0.000 description 1
- RUELTTOHQODFPA-UHFFFAOYSA-N toluene 2,6-diisocyanate Chemical compound CC1=C(N=C=O)C=CC=C1N=C=O RUELTTOHQODFPA-UHFFFAOYSA-N 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 239000000107 tumor biomarker Substances 0.000 description 1
- 230000002476 tumorcidal effect Effects 0.000 description 1
- 238000010396 two-hybrid screening Methods 0.000 description 1
- 241001515965 unidentified phage Species 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 210000003556 vascular endothelial cell Anatomy 0.000 description 1
- 210000004509 vascular smooth muscle cell Anatomy 0.000 description 1
- 239000013598 vector Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 238000012447 xenograft mouse model Methods 0.000 description 1
- BPICBUSOMSTKRF-UHFFFAOYSA-N xylazine Chemical compound CC1=CC=CC(C)=C1NC1=NCCCS1 BPICBUSOMSTKRF-UHFFFAOYSA-N 0.000 description 1
- 229960001600 xylazine Drugs 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/5005—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells
- G01N33/5008—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics
- G01N33/5044—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving human or animal cells for testing or evaluating the effect of chemical or biological compounds, e.g. drugs, cosmetics involving specific cell types
- G01N33/507—Pancreatic cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/112—Disease subtyping, staging or classification
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/52—Assays involving cytokines
- G01N2333/521—Chemokines
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Pathology (AREA)
- General Health & Medical Sciences (AREA)
- Analytical Chemistry (AREA)
- Cell Biology (AREA)
- Molecular Biology (AREA)
- Microbiology (AREA)
- Urology & Nephrology (AREA)
- Zoology (AREA)
- Medicinal Chemistry (AREA)
- Physics & Mathematics (AREA)
- Hematology (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Oncology (AREA)
- Animal Behavior & Ethology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Hospice & Palliative Care (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Toxicology (AREA)
- Biophysics (AREA)
- General Physics & Mathematics (AREA)
- Food Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Peptides Or Proteins (AREA)
Description
本発明は、患者における膵癌のバイオマーカーとしてのCXCL4L1の使用に関する。本発明はさらに膵癌の処置および/または膵転移の予防のための方法に関する。
膵癌は膵臓の悪性腫瘍である。毎年、アメリカ合衆国で約35000人がこの疾患で診断され、ほぼ同数のヒトがこの疾患のために死亡する。ヨーロッパでは、60000人以上が毎年この癌のため診断される。それ故、膵癌は、すべての癌の中で最も高い致死率のうちの1つを有し(Jemal et al., 2007)、それ故、この致死の病体に対する効果的な処置を緊急に必要とする主要なヒトの健康問題となっている。
本発明は、患者の膵癌および/または膵転移を検出する方法に関し、該方法は、該患者から得られた生物学的サンプル中のCXCL4L1遺伝子の発現レベルを決定する事を含む。
本発明者は、CXCL4L1が、初期の正確な膵癌の検出およびCXCL4L1遺伝子の発現レベルと腫瘍のグレードの重症度との間の関連づけのために使用されうるという所見を有する。
用語「CXCL4L1」は本明細書において使用される時、PF4v1、PF4var1、PF4ALTおよびSCYB4V1を含むがそれらに限定されないすべての同義語を含むことを意図する。この用語はそれ故、天然に生じるCXCL4L1、ならびにその変異体および改変型を含む。用語「成熟CXCL4L1タンパク質」は、より長いプロペプチドのプロセシングにより得ることのできる70アミノ酸の成熟CXCL4L1タンパク質を意味する(アクセッションナンバー NP_002611でGenPeptデータベースに提供される)。CXCL4L1をコードする代表的な天然のヌクレオチド配列はGenBankデータベースにアクセッションナンバーNM_002620で提供される。用語「CXCL4L1」はCXCL4タンパク質の霊長類の天然の変異体も含むことにさらに注意されなければならない。例として、霊長類のCXCL4L1タンパク質は、GenBankアクセッションナンバーXM_001102971.1(アカゲザル)およびXP_001156146.1(チンパンジー)で提供される。
本発明は、患者から得られた生物学的サンプル中のCXCL4L1遺伝子の発現レベルを決定する事を含む、該患者の膵癌および/または膵転移を検出する方法に関する。
(i)該患者から得られた生物学的サンプル中のCXCL4L1の濃度を測定し、
(ii)ステップ(i)で測定されたCXCL4L1の濃度を、膵癌に罹患していない対象からの生物学的サンプル中のCXCL4L1の濃度由来の参照値と比較し、ここで、該患者から得られた生物学的サンプル中のCXCL4L1の、該参照値と比較して増加したレベルは、患者が膵癌に罹患していることを示す
のステップを含む。
本発明の別の面は、膵癌の処置および/または膵転移の予防のための方法および組成物に関する。従って、本発明は、放射性同位体、化学療法剤または他の細胞障害性薬物(つまりTNFα)を膵腫瘍に運搬するための腫瘍標的化剤として使用できるCXCL4L1特異的結合分子に関する。
材料および方法
ヒト膵癌細胞系BxPC3およびウシ大動脈内皮細胞(BAEC)は10%ウシ胎仔血清、抗生物質(ペニシリン/ストレプトマイシン)およびL−グルタミンが追加されたDMEM1g/Lグルコース(Invitrogen, Cergy Pontoise, France)中培養された。ヒト臍帯静脈上皮細胞(HUVEC, Lonza, Levallois-Perret, France)は、2%FBSを含むEGM−2 SingleQuots(Lonza)を追加されたEBM−2(Lonza)中維持された。培養は37℃、5%C02中インキュベーションされた。腫瘍細胞はDr.C.Susini(INSERM U531, Toulouse, France)からの快い贈り物であった。受精鶏卵(Gallus gallus)(EARL Morizeau, Dangers, France)は、かつて記載された通り(Hagedorn et al., 2005)取り扱われた。胎性期10日(E10)において、最終量40μlの無血清培地に希釈された400万のBxPC3細胞は無傷のCAM表面に薄膜として沈着された。
メスのRAG−γ/cマウスはBordeaux 1 Universityの飼養施設(「Animalerie Mutualisee Bordeaux I」)に収容され、処置された。すべての動物の処置は施設のガイドラインに従って実施された。20週令の年老いたマウス(n=26)は、ケタミン(150mg/kg)およびキシラジン(15mg/kg)の腹腔内投与で麻酔され、皮下投与により100μlの無血清培地中の3.106 BxPC3細胞で異種移植された。
細胞または瞬間凍結組織から、全RNAはRNeasy mini kit(Qiagen, Courtaboeuf, France)を用いて抽出された。RNAの質および量はアガロースゲル電気泳動および吸光度測定により評価された。第一鎖cDNAは、Quantitect Reverse Transcription kit(Qiagen)を用いて全RNAの1μgから調製された。
リアルタイムPCRは、SYBRグリーン色素(ABgene, Courtaboeuf, France)を使用しMx3000P thermocycler(Stratagene, La Jolla, CA)で実施された。ヒト特異的プライマーが設計され、Universal Human Reference RNA(Stratagene)を用いて増幅効率が評価された。90〜110%の増幅効率をもつプライマーペアのみが使用された。PCRの特異性は、増幅産物の解離曲線分析およびアガロースゲル電気泳動により検証された。すべてのサンプルは3回の独立した実験の最小値で試験された。
DIG CXCL4およびCXCL4L1ヒトリボプローブは製造業者の説明書に従って合成された(Roche RNA Labeling Kit(SP6/T7)-Roche)。つまり、pCR2.1 TOPO CXCL4_UTRおよびpCR2.1 TOPO CXCL4L1_UTRベクターはXhoI(センスプローブ用)またはBamHI(アンチセンスプローブ用)酵素切断により直鎖化された。転写後、DNAテンプレートは切断され(DNaseI Invitrogen)、その後、リボプローブを塩化リチウムにより沈殿させた。
パラフィン包埋組織は、7μm厚のミクロトーム切片に切断され、組織学的分析、転移の局在および最も代表的な腫瘍領域の選択のためにヘマトキシリン−エオシンで染色された。使用された一次抗体は、ヤギ抗ヒトCXCL4(PF4-AF-795, R&DSystem-Minneapolis)およびCXCL4L1に対するマウスモノクローナル抗体(MabV1, clone 9E11-2D5-2G1)である。この抗体の産生および特徴は他で報告されるであろう(Dubrac et al manuscript in preparation)。対応する二次抗体は、抗ヤギまたは抗マウスHRP結合抗体(Dakocytomation)である。イメージングはNikon DXM Eclipse E600 microscopeを用いて実施された。
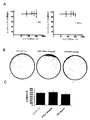
細胞の生存率はWST−1アッセイによって評価された(Roche, Neuilly sur Seine Cedex, France)。アポトーシスの相対的存在量は、製造者の説明書に従って、カスパーゼ3/7活性によって測定される(Apo-one homogeneous assay kit, Promega, Charbonnieres, France)。両方の場合において、細胞は96穴プレートに濃度1×104(HUVEC)または3×103(BxPC3)細胞/ウェルで蒔かれ、一晩接着を可能にした。完全培地は、ゲムシタビン(Laboratoire Lilly, Suresnes, France)および/またはCXCL4L1有りまたは無しの無血清培地で24時間(HUVEC)もしくは48時間(BxPC3)置換された。すべてのアッセイは三つ組みのウェルで実施され、おのおのの実験は3回繰り返された。
細胞遊走および浸潤アッセイは、24穴培養プレートに設置された孔径8μmのTranswell membrane filter(BD Biosciences、Le Pont-de-Claix, France)を用いて実施された。Transwell membraneの上部の表面は、100μg/mlのgrowth factor−reduced Matrigel matrix(BD Biosciences)で被覆され、またはされなかった。その後、無血清培地中の1×105細胞はおのおののTranswellチャンバーに添加され、37℃で、遊走試験のために6時間、浸潤試験のために24時間、化学遊走物質として下部のチャンバーの無血清培地0、5%FBSにより、上部チャンバーの下側に遊走できるようにした。細胞はメタノール30%、酢酸10%で10分間固定され、クマシンブルー0、1%、メタノール30%、酢酸40%で3分間着色された。膜の上部の表面の細胞は、綿棒で拭う事により除去された。
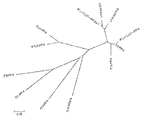
BLASTでタンパク質のRefseqデータベースに対してCXCL4(PF4)とマッチするペプチドがサーチされ、ペプチド目録が引き出された。ハイライトされた配列は、首尾よくヒトに対して戻った相互BLASTの配列を示す。他の配列は対象となるためリストアップされた。ClustalWプログラムは、すべての種においてCXCL4(PF4)およびCXCL4L1(PF4V1)を示すことが見いだされた12配列に対し実施された。
ヒト腺癌サンプルはProf Martin Schilling(Klinik fur Allgemeine Chirurgie, Viszeral-, Gefaeβ-und Kinderchirurgie, Homburg, Germany)によって提供された。新鮮な腫瘍組織は外科手術中に得られ、直接的に液体窒素中瞬間凍結された。患者は診療所のガイドラインに従って組織分析の前に同意した。
CXCL4L1およびCXCL4の系統発生解析
複数のヒト組織のmRNAにおける定量的PCRはCXCL4L1およびCXCL4に関して異なる発現プロファイルを示唆する(図2)。CXCL4L1が単に、胎児肝、結腸およびある程度脾臓に発現する一方、CXCL4は脾臓に高度に発現している。正常なヒト膵臓は、有意にCXCL4L1およびCXCL4を発現しない。
トランスクリプトームのプロファイリングはPDAC−CAMモデルにおいてCXCL4L1は同定するがCXCL4を同定しない:ヒトAffymetrixまたはトリAffymetrixマイクロアレーを用いたデュアルトランスクリプトーム分析は、トリ絨毛尿膜へのBxPC3細胞の移植の腫瘍1日目(T1)および腫瘍6日目(T6)の間(胚発生のE11およびE16に対応する)に実施された。我々は、CXCL4ではなくCXCL4L1がT1と比較してT6に高度にアップレギュレーションされた(14.6倍増加)ことを明確に証明した。CXCL4L1はまたヒトAffymetrixアレイにおいてのみ検出され、トリチップが使用された時、トリのオルソログは存在しなかった。この事は、in vivoで腫瘍発生の間、CXCL4L1が腫瘍細胞において誘導される事を示唆した。
CXCL4L1およびCXCL4の組み換えタンパク質はGST融合タンパク質として相当量精製された。プロテアーゼの切り取りによるGSTの除去は、生物学的活性に対する有意な効果を有さず、切り取りを不必要にする。
CXCL4L1はヒト、サルおよびチンパンジーにのみ発現し、進化の最晩期にCXCL4から分岐する。腸、肝臓および脾臓を含む複数のヒト組織は、CXCL4L1およびCXCL4を発現するが、正常膵臓組織は、このケモカインの弱い発現を示すか全く発現しないことを示す。しかしながらCXCL4ではなくCXCL4L1が膵癌において有意に過発現し、新規のバイオマーカーに相当する。この事は下記の観察に基づく:
(1)qPCRまたはin situ ハイブリダイゼーションとの組み合わせによるトランスクリプトーム分析は、ヒト膵臓腺癌細胞がトリ絨毛尿膜に移植される時、有意なレベルのCXCL4L1 mRNAを発現するが、CXCL4のmRNAは発現しない事を示唆する。
(2)抗ヒトCXCL4L1/CXCL4または特異的なモノクローナル抗CXCL4L1抗体(Mabv1)を用いた免疫局在性は、トリCAMに移植される時、腫瘍細胞において強い免疫反応性を証明する。
(3)マウスに移植後の原発膵腫瘍は、CXCL4L1 mRNAを発現し、原発腫瘍および転移性腫瘍細胞も陽性の免疫反応性を示す。
(4)ヒト患者由来の膵臓腺癌サンプルはCXCL4L1 mRNAのみを発現し、CXCL4 mRNAは発現せず、強い陽性の免疫反応性を示す。
(5)膵臓腺癌細胞ではなく内皮細胞が外来性CXCL4L1に応答することは、膵腫瘍発生においてCXCL4L1の活性のパラクリンモードを示唆する。さらに、我々の結果は、培養液中の膵臓腺癌細胞がCXCL4L1もCXCL4も発現しないので、CXCL4L1発現のアップレギュレーションは特異的な腫瘍−宿主相互作用によるということを示唆する。
Claims (8)
- 患者から得られた生物学的サンプル中のCXCL4L1遺伝子の発現レベルを決定することを含む、該患者における膵癌および/または膵転移の検出を補助する方法。
- 患者から得られた生物学的サンプル中のCXCL4L1遺伝子の発現レベルを決定することを含む、膵癌を有する該患者における膵癌の病期の分類を補助する方法。
- CXCL4L1遺伝子の発現レベルがCXCL4L1 mRNAの量を測定することにより決定され、生物学的サンプルが組織サンプルである、請求項1または2記載の方法。
- 組織サンプルが膵腫瘍サンプルである請求項3記載の方法。
- CXCL4L1遺伝子の発現レベルが患者から得られた生物学的サンプル中のCXCL4L1タンパク質の濃度を測定する事により決定される、請求項1または2記載の方法。
- 膵癌が膵臓腺癌である請求項1〜5のいずれか一項記載の方法。
- CXCL4L1の遺伝子又はタンパク質からなる、患者における膵癌を検出するためのバイオマーカー。
- 膵癌の処置および/または膵転移の予防のための、細胞障害性薬剤または成長阻害剤のような抗癌剤に結合した抗CXCL4L1抗体。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08305853 | 2008-11-27 | ||
| EP08305853.7 | 2008-11-27 | ||
| PCT/EP2009/065805 WO2010060920A1 (en) | 2008-11-27 | 2009-11-25 | Cxcl4l1 as a biomarker of pancreatic cancer |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2012509683A JP2012509683A (ja) | 2012-04-26 |
| JP2012509683A5 JP2012509683A5 (ja) | 2014-08-07 |
| JP5773315B2 true JP5773315B2 (ja) | 2015-09-02 |
Family
ID=40288415
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2011537960A Expired - Fee Related JP5773315B2 (ja) | 2008-11-27 | 2009-11-25 | 膵癌のバイオマーカーとしてのcxcl4l1 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20110318370A1 (ja) |
| EP (1) | EP2361315B1 (ja) |
| JP (1) | JP5773315B2 (ja) |
| ES (1) | ES2465191T3 (ja) |
| WO (1) | WO2010060920A1 (ja) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012072595A1 (en) * | 2010-11-30 | 2012-06-07 | Universiteit Gent | Platelet factor 4 variant for the prognosis of cardiovascular outcome in patients having heart disease |
| PL3141617T3 (pl) * | 2011-01-11 | 2019-04-30 | Assist Publique Hopitaux De Paris | Sposoby przewidywania wyniku w związku z nowotworem u pacjenta przez analizowanie ekspresji genów |
| US9164105B2 (en) | 2011-01-13 | 2015-10-20 | Industry-Academic Cooperation Foundation, Yonsei University | Pancreatic cancer biomarker using the characteristics of pancreatic cancer stem cells, and use thereof |
| WO2012101125A1 (en) * | 2011-01-24 | 2012-08-02 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Specific antibodies against human cxcl4 and uses thereof |
| US20150260721A1 (en) * | 2012-10-12 | 2015-09-17 | Hi-Stem Ggmbh | Novel biomarkers for sub-typing pancreatic ductal adenocarcinoma |
| WO2014177662A1 (en) * | 2013-04-30 | 2014-11-06 | INSERM (Institut National de la Santé et de la Recherche Médicale) | In vitro method for determining if a subject suffering from cancer is responsive to a treatment comprising administering an effective amount of cxcl4l1 or an inhibitor of cxcl4l1 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1981001145A1 (en) | 1979-10-18 | 1981-04-30 | Univ Illinois | Hydrolytic enzyme-activatible pro-drugs |
| US4946778A (en) | 1987-09-21 | 1990-08-07 | Genex Corporation | Single polypeptide chain binding molecules |
| GB8705477D0 (en) | 1987-03-09 | 1987-04-15 | Carlton Med Prod | Drug delivery systems |
| US4975278A (en) | 1988-02-26 | 1990-12-04 | Bristol-Myers Company | Antibody-enzyme conjugates in combination with prodrugs for the delivery of cytotoxic agents to tumor cells |
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| ATE196606T1 (de) | 1992-11-13 | 2000-10-15 | Idec Pharma Corp | Therapeutische verwendung von chimerischen und markierten antikörpern, die gegen ein differenzierung-antigen gerichtet sind, dessen expression auf menschliche b lymphozyt beschränkt ist, für die behandlung von b-zell-lymphoma |
| TW526269B (en) | 1997-11-21 | 2003-04-01 | Dev Center Biotechnology | Monoclonal antibody against morphine derivatives, hybridoma producing the antibody and the use thereof |
| JP2006521562A (ja) * | 2003-03-07 | 2006-09-21 | スレショルド ファーマシューティカルズ インコーポレイティッド | 抗悪性腫瘍剤による治療に対する腫瘍の感受性を決定する方法 |
| EP1812468A2 (en) * | 2004-09-15 | 2007-08-01 | K.U.Leuven Research & Development | Platelet factor 4 variant 1 (pf4var1) related inhibitors of angiogenesis |
| WO2008092002A2 (en) * | 2007-01-24 | 2008-07-31 | The Regents Of The University Of Michigan | Compositions and methods for treating and diagnosing pancreatic cancer |
| WO2009006382A1 (en) * | 2007-07-02 | 2009-01-08 | Purdue Research Foundation | Detection of glycopeptides and glycoproteins for medical diagnostics |
| US8481033B2 (en) * | 2008-10-07 | 2013-07-09 | INSERM (Institute National de la Santé et de la Recherche Médicale) | Neutralizing antibodies and fragments thereof directed against platelet factor-4 variant 1 (PF4V1) |
-
2009
- 2009-11-25 JP JP2011537960A patent/JP5773315B2/ja not_active Expired - Fee Related
- 2009-11-25 US US13/131,084 patent/US20110318370A1/en not_active Abandoned
- 2009-11-25 ES ES09764773.9T patent/ES2465191T3/es active Active
- 2009-11-25 WO PCT/EP2009/065805 patent/WO2010060920A1/en active Application Filing
- 2009-11-25 EP EP09764773.9A patent/EP2361315B1/en not_active Not-in-force
Also Published As
| Publication number | Publication date |
|---|---|
| WO2010060920A1 (en) | 2010-06-03 |
| EP2361315B1 (en) | 2014-03-05 |
| EP2361315A1 (en) | 2011-08-31 |
| JP2012509683A (ja) | 2012-04-26 |
| ES2465191T3 (es) | 2014-06-05 |
| US20110318370A1 (en) | 2011-12-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6430560B2 (ja) | 前立腺癌マーカーとしてのホスホジエステラーゼ4d7 | |
| JP6717428B2 (ja) | カリウムチャネル蛋白質を用いた癌診断用組成物 | |
| JP5773315B2 (ja) | 膵癌のバイオマーカーとしてのcxcl4l1 | |
| KR102054857B1 (ko) | 질환의 진단용 조성물 | |
| KR102210333B1 (ko) | 암의 진단용 조성물 | |
| WO2014185631A1 (ko) | Tgfbi를 이용한 패혈증 진단용 조성물 및 이를 이용한 패혈증 예방 또는 치료용 약학적 조성물과 이의 스크리닝 방법 | |
| KR20090053222A (ko) | 체액 내 대장암 마커로서의 cxcl-16유전자 및 이를이용한 대장암의 진단 및 치료에의 용도 | |
| CN116801788A (zh) | 用于评估肝脏疾病的试剂盒、试剂和方法 | |
| KR101058753B1 (ko) | 대장암 마커로서의 esm-1 유전자 및 이를 이용한대장암의 진단 및 치료에의 용도 | |
| KR100948808B1 (ko) | 간암 마커로서의 lcn2 유전자, 단백질 및 간암 진단키트 | |
| KR102006999B1 (ko) | 대장암 전이 진단 또는 예후 예측용 조성물 및 이의 용도 | |
| US10316319B2 (en) | Composition for diagnosis of liver metastasis of colorectal cancer and the use thereof | |
| KR100861464B1 (ko) | 발암/전이유전자 tip41과 이에 의해 코드되는 단백질 및이를 이용한 발암 및 전이 진단 키트 | |
| US20120156681A1 (en) | Composition for diagnosis of liver metastasis of colorectal cancer and the use thereof | |
| KR101516716B1 (ko) | 간 섬유화 진단용 바이오마커 rorc | |
| KR101515210B1 (ko) | 간 섬유화 진단용 바이오마커 elk3 | |
| KR102325742B1 (ko) | 암의 진단용 조성물 | |
| KR20240109655A (ko) | 담도암 진단용 바이오마커 | |
| Gupta et al. | Oral Sessions | |
| Navaglia et al. | Oral Sessions |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20121017 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20140318 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140618 |
|
| A524 | Written submission of copy of amendment under article 19 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A524 Effective date: 20140618 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141224 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150323 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20150602 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20150619 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5773315 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |